WO2021024906A1 - 短鎖脂肪酸エステルを担持する親水-疎水性共重合体 - Google Patents
短鎖脂肪酸エステルを担持する親水-疎水性共重合体 Download PDFInfo
- Publication number
- WO2021024906A1 WO2021024906A1 PCT/JP2020/029239 JP2020029239W WO2021024906A1 WO 2021024906 A1 WO2021024906 A1 WO 2021024906A1 JP 2020029239 W JP2020029239 W JP 2020029239W WO 2021024906 A1 WO2021024906 A1 WO 2021024906A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- hydrophilic
- formula
- hydrophobic
- prevention
- Prior art date
Links
- 229920001577 copolymer Polymers 0.000 title claims abstract description 43
- 150000003365 short chain fatty acid esters Chemical class 0.000 title description 6
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 36
- 201000011510 cancer Diseases 0.000 claims abstract description 31
- 230000002209 hydrophobic effect Effects 0.000 claims abstract description 22
- 229920001223 polyethylene glycol Polymers 0.000 claims abstract description 11
- 229920000578 graft copolymer Polymers 0.000 claims abstract description 9
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical group OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 claims abstract description 7
- 229920001400 block copolymer Polymers 0.000 claims abstract description 7
- 239000002105 nanoparticle Substances 0.000 claims description 44
- 230000002265 prevention Effects 0.000 claims description 25
- 208000008338 non-alcoholic fatty liver disease Diseases 0.000 claims description 24
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 19
- 210000004369 blood Anatomy 0.000 claims description 18
- 239000008280 blood Substances 0.000 claims description 18
- 230000005855 radiation Effects 0.000 claims description 15
- 206010009900 Colitis ulcerative Diseases 0.000 claims description 13
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 13
- 201000006704 Ulcerative Colitis Diseases 0.000 claims description 13
- 208000019425 cirrhosis of liver Diseases 0.000 claims description 13
- 239000008103 glucose Substances 0.000 claims description 13
- 230000001629 suppression Effects 0.000 claims description 13
- 238000000034 method Methods 0.000 claims description 12
- 229920000642 polymer Polymers 0.000 claims description 12
- 208000008589 Obesity Diseases 0.000 claims description 11
- 206010012601 diabetes mellitus Diseases 0.000 claims description 11
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 11
- 239000000693 micelle Substances 0.000 claims description 11
- 235000020824 obesity Nutrition 0.000 claims description 11
- 125000001424 substituent group Chemical group 0.000 claims description 11
- 238000001959 radiotherapy Methods 0.000 claims description 10
- 206010020575 Hyperammonaemia Diseases 0.000 claims description 9
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 claims description 8
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 8
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 7
- -1 phenethylamino group Chemical group 0.000 claims description 7
- 230000002708 enhancing effect Effects 0.000 claims description 6
- 239000000825 pharmaceutical preparation Substances 0.000 claims description 6
- 125000000217 alkyl group Chemical group 0.000 claims description 5
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 5
- 125000005647 linker group Chemical group 0.000 claims description 5
- 229910052760 oxygen Inorganic materials 0.000 claims description 5
- 229910021529 ammonia Inorganic materials 0.000 claims description 4
- 239000012736 aqueous medium Substances 0.000 claims description 4
- 125000004432 carbon atom Chemical group C* 0.000 claims description 4
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 claims description 4
- 239000004480 active ingredient Substances 0.000 claims description 3
- 125000003545 alkoxy group Chemical group 0.000 claims description 3
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 claims description 3
- 229910052736 halogen Inorganic materials 0.000 claims description 3
- 150000002367 halogens Chemical class 0.000 claims description 3
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 2
- 125000003118 aryl group Chemical group 0.000 claims description 2
- 229910052799 carbon Inorganic materials 0.000 claims description 2
- 150000004666 short chain fatty acids Chemical class 0.000 abstract description 17
- 230000035790 physiological processes and functions Effects 0.000 abstract description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 abstract description 3
- 201000010099 disease Diseases 0.000 abstract description 2
- 108090000371 Esterases Proteins 0.000 abstract 1
- 208000035475 disorder Diseases 0.000 abstract 1
- 238000001727 in vivo Methods 0.000 abstract 1
- 238000012360 testing method Methods 0.000 description 101
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 58
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 44
- 210000004185 liver Anatomy 0.000 description 32
- 238000004519 manufacturing process Methods 0.000 description 32
- 239000000523 sample Substances 0.000 description 25
- 235000019260 propionic acid Nutrition 0.000 description 22
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 22
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 20
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 20
- 241000699666 Mus <mouse, genus> Species 0.000 description 18
- 201000001441 melanoma Diseases 0.000 description 17
- 239000002245 particle Substances 0.000 description 17
- 210000001519 tissue Anatomy 0.000 description 17
- OBKXEAXTFZPCHS-UHFFFAOYSA-N 4-phenylbutyric acid Chemical compound OC(=O)CCCC1=CC=CC=C1 OBKXEAXTFZPCHS-UHFFFAOYSA-N 0.000 description 16
- 239000000243 solution Substances 0.000 description 16
- 210000004027 cell Anatomy 0.000 description 15
- 210000000056 organ Anatomy 0.000 description 15
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 14
- 241000699670 Mus sp. Species 0.000 description 14
- 230000000694 effects Effects 0.000 description 14
- 206010053219 non-alcoholic steatohepatitis Diseases 0.000 description 14
- 239000007787 solid Substances 0.000 description 14
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 13
- 241001465754 Metazoa Species 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 12
- 239000000047 product Substances 0.000 description 12
- 230000002829 reductive effect Effects 0.000 description 12
- 208000029618 autoimmune pulmonary alveolar proteinosis Diseases 0.000 description 11
- 230000037396 body weight Effects 0.000 description 11
- 235000021391 short chain fatty acids Nutrition 0.000 description 11
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 10
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 10
- 238000000692 Student's t-test Methods 0.000 description 10
- 238000010586 diagram Methods 0.000 description 10
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 10
- 210000000952 spleen Anatomy 0.000 description 10
- 238000010186 staining Methods 0.000 description 10
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 10
- 238000002360 preparation method Methods 0.000 description 9
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 8
- 239000012188 paraffin wax Substances 0.000 description 8
- 238000012353 t test Methods 0.000 description 8
- 238000011746 C57BL/6J (JAX™ mouse strain) Methods 0.000 description 7
- 206010027476 Metastases Diseases 0.000 description 7
- 238000010171 animal model Methods 0.000 description 7
- 230000015572 biosynthetic process Effects 0.000 description 7
- 231100000135 cytotoxicity Toxicity 0.000 description 7
- 230000003013 cytotoxicity Effects 0.000 description 7
- 238000002224 dissection Methods 0.000 description 7
- 238000003786 synthesis reaction Methods 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 6
- 206010061218 Inflammation Diseases 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 238000002296 dynamic light scattering Methods 0.000 description 6
- 210000001035 gastrointestinal tract Anatomy 0.000 description 6
- 230000004054 inflammatory process Effects 0.000 description 6
- 230000002401 inhibitory effect Effects 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- TVZRAEYQIKYCPH-UHFFFAOYSA-N 3-(trimethylsilyl)propane-1-sulfonic acid Chemical compound C[Si](C)(C)CCCS(O)(=O)=O TVZRAEYQIKYCPH-UHFFFAOYSA-N 0.000 description 5
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 5
- 108010082126 Alanine transaminase Proteins 0.000 description 5
- 108010003415 Aspartate Aminotransferases Proteins 0.000 description 5
- 102000004625 Aspartate Aminotransferases Human genes 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 230000006378 damage Effects 0.000 description 5
- 210000004072 lung Anatomy 0.000 description 5
- 230000007935 neutral effect Effects 0.000 description 5
- 229910052757 nitrogen Inorganic materials 0.000 description 5
- 229950009215 phenylbutanoic acid Drugs 0.000 description 5
- 239000002244 precipitate Substances 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- 239000008399 tap water Substances 0.000 description 5
- 235000020679 tap water Nutrition 0.000 description 5
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 4
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 4
- 230000005907 cancer growth Effects 0.000 description 4
- 238000007796 conventional method Methods 0.000 description 4
- 238000000502 dialysis Methods 0.000 description 4
- 235000014113 dietary fatty acids Nutrition 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 229930195729 fatty acid Natural products 0.000 description 4
- 239000000194 fatty acid Substances 0.000 description 4
- 150000004665 fatty acids Chemical class 0.000 description 4
- 230000009401 metastasis Effects 0.000 description 4
- 208000037819 metastatic cancer Diseases 0.000 description 4
- 208000011575 metastatic malignant neoplasm Diseases 0.000 description 4
- 229930182817 methionine Natural products 0.000 description 4
- 208000031648 Body Weight Changes Diseases 0.000 description 3
- HTQBXNHDCUEHJF-XWLPCZSASA-N Exenatide Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 HTQBXNHDCUEHJF-XWLPCZSASA-N 0.000 description 3
- 108010011459 Exenatide Proteins 0.000 description 3
- 230000004579 body weight change Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 210000001198 duodenum Anatomy 0.000 description 3
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 3
- 229960001519 exenatide Drugs 0.000 description 3
- 210000003405 ileum Anatomy 0.000 description 3
- 230000000968 intestinal effect Effects 0.000 description 3
- 210000004153 islets of langerhan Anatomy 0.000 description 3
- 210000001630 jejunum Anatomy 0.000 description 3
- 210000003734 kidney Anatomy 0.000 description 3
- 210000002429 large intestine Anatomy 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 239000000178 monomer Substances 0.000 description 3
- 231100000956 nontoxicity Toxicity 0.000 description 3
- 229920005604 random copolymer Polymers 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 210000003462 vein Anatomy 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- KGKAYWMGPDWLQZ-UHFFFAOYSA-N 1,2-bis(bromomethyl)benzene Chemical group BrCC1=CC=CC=C1CBr KGKAYWMGPDWLQZ-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- IMROMDMJAWUWLK-UHFFFAOYSA-N Ethenol Chemical compound OC=C IMROMDMJAWUWLK-UHFFFAOYSA-N 0.000 description 2
- 206010020880 Hypertrophy Diseases 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 206010067125 Liver injury Diseases 0.000 description 2
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 2
- 208000003788 Neoplasm Micrometastasis Diseases 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 2
- 231100000439 acute liver injury Toxicity 0.000 description 2
- 239000003472 antidiabetic agent Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 238000010876 biochemical test Methods 0.000 description 2
- 238000004820 blood count Methods 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 239000012986 chain transfer agent Substances 0.000 description 2
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 2
- 229960001231 choline Drugs 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 238000012790 confirmation Methods 0.000 description 2
- 238000007405 data analysis Methods 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 238000013118 diabetic mouse model Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 230000009266 disease activity Effects 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- MEGHWIAOTJPCHQ-UHFFFAOYSA-N ethenyl butanoate Chemical compound CCCC(=O)OC=C MEGHWIAOTJPCHQ-UHFFFAOYSA-N 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 230000003176 fibrotic effect Effects 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 230000005251 gamma ray Effects 0.000 description 2
- 238000007446 glucose tolerance test Methods 0.000 description 2
- 230000009422 growth inhibiting effect Effects 0.000 description 2
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 2
- 238000007654 immersion Methods 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- KQNPFQTWMSNSAP-UHFFFAOYSA-N isobutyric acid Chemical compound CC(C)C(O)=O KQNPFQTWMSNSAP-UHFFFAOYSA-N 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 230000003908 liver function Effects 0.000 description 2
- 210000005228 liver tissue Anatomy 0.000 description 2
- 201000005202 lung cancer Diseases 0.000 description 2
- 208000020816 lung neoplasm Diseases 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 2
- 238000007726 management method Methods 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 210000004923 pancreatic tissue Anatomy 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 238000004904 shortening Methods 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 230000004614 tumor growth Effects 0.000 description 2
- 210000000689 upper leg Anatomy 0.000 description 2
- 229920001567 vinyl ester resin Polymers 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- SXLHPBDGZHWKSX-UHFFFAOYSA-N 1-(5-amino-2-hydroxyphenyl)ethanone Chemical compound CC(=O)C1=CC(N)=CC=C1O SXLHPBDGZHWKSX-UHFFFAOYSA-N 0.000 description 1
- XYHKNCXZYYTLRG-UHFFFAOYSA-N 1h-imidazole-2-carbaldehyde Chemical compound O=CC1=NC=CN1 XYHKNCXZYYTLRG-UHFFFAOYSA-N 0.000 description 1
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- XXZCIYUJYUESMD-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-3-(morpholin-4-ylmethyl)pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C(=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2)CN1CCOCC1 XXZCIYUJYUESMD-UHFFFAOYSA-N 0.000 description 1
- GWYFCOCPABKNJV-UHFFFAOYSA-M 3-Methylbutanoic acid Natural products CC(C)CC([O-])=O GWYFCOCPABKNJV-UHFFFAOYSA-M 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 238000011814 C57BL/6N mouse Methods 0.000 description 1
- QDHHCQZDFGDHMP-UHFFFAOYSA-N Chloramine Chemical compound ClN QDHHCQZDFGDHMP-UHFFFAOYSA-N 0.000 description 1
- 208000035859 Drug effect increased Diseases 0.000 description 1
- 208000004930 Fatty Liver Diseases 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 206010019708 Hepatic steatosis Diseases 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 206010041660 Splenomegaly Diseases 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- 235000010724 Wisteria floribunda Nutrition 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000008065 acid anhydrides Chemical group 0.000 description 1
- 238000005576 amination reaction Methods 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 229940127003 anti-diabetic drug Drugs 0.000 description 1
- 230000003178 anti-diabetic effect Effects 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- GWYFCOCPABKNJV-UHFFFAOYSA-N beta-methyl-butyric acid Natural products CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 238000010241 blood sampling Methods 0.000 description 1
- 150000005693 branched-chain amino acids Chemical class 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 238000012754 cardiac puncture Methods 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000011258 core-shell material Substances 0.000 description 1
- FYACMHCOSCVNHO-UHFFFAOYSA-N cyanomethyl n-methyl-n-phenylcarbamodithioate Chemical compound N#CCSC(=S)N(C)C1=CC=CC=C1 FYACMHCOSCVNHO-UHFFFAOYSA-N 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 229960000633 dextran sulfate Drugs 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 239000012470 diluted sample Substances 0.000 description 1
- 230000035622 drinking Effects 0.000 description 1
- 235000020188 drinking water Nutrition 0.000 description 1
- 239000003651 drinking water Substances 0.000 description 1
- NNOIBRCUUKQWFO-UHFFFAOYSA-N ethenyl 4-phenylbutanoate Chemical compound C=COC(=O)CCCC1=CC=CC=C1 NNOIBRCUUKQWFO-UHFFFAOYSA-N 0.000 description 1
- UIWXSTHGICQLQT-UHFFFAOYSA-N ethenyl propanoate Chemical compound CCC(=O)OC=C UIWXSTHGICQLQT-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000005313 fatty acid group Chemical group 0.000 description 1
- 208000010706 fatty liver disease Diseases 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- VLKZOEOYAKHREP-UHFFFAOYSA-N hexane Substances CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229960003943 hypromellose Drugs 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 229940057948 magnesium stearate Drugs 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- TZBAVQKIEKDGFH-UHFFFAOYSA-N n-[2-(diethylamino)ethyl]-1-benzothiophene-2-carboxamide;hydrochloride Chemical compound [Cl-].C1=CC=C2SC(C(=O)NCC[NH+](CC)CC)=CC2=C1 TZBAVQKIEKDGFH-UHFFFAOYSA-N 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 239000003002 pH adjusting agent Substances 0.000 description 1
- 230000004203 pancreatic function Effects 0.000 description 1
- 229960005489 paracetamol Drugs 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- JCBJVAJGLKENNC-UHFFFAOYSA-M potassium ethyl xanthate Chemical compound [K+].CCOC([S-])=S JCBJVAJGLKENNC-UHFFFAOYSA-M 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 231100000240 steatosis hepatitis Toxicity 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000004584 weight gain Effects 0.000 description 1
- 235000019786 weight gain Nutrition 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F290/00—Macromolecular compounds obtained by polymerising monomers on to polymers modified by introduction of aliphatic unsaturated end or side groups
- C08F290/02—Macromolecular compounds obtained by polymerising monomers on to polymers modified by introduction of aliphatic unsaturated end or side groups on to polymers modified by introduction of unsaturated end groups
- C08F290/06—Polymers provided for in subclass C08G
- C08F290/062—Polyethers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/337—Polymers modified by chemical after-treatment with organic compounds containing other elements
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/58—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. poly[meth]acrylate, polyacrylamide, polystyrene, polyvinylpyrrolidone, polyvinylalcohol or polystyrene sulfonic acid resin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6927—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores
- A61K47/6929—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle
- A61K47/6931—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle the material constituting the nanoparticle being a polymer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F293/00—Macromolecular compounds obtained by polymerisation on to a macromolecule having groups capable of inducing the formation of new polymer chains bound exclusively at one or both ends of the starting macromolecule
- C08F293/005—Macromolecular compounds obtained by polymerisation on to a macromolecule having groups capable of inducing the formation of new polymer chains bound exclusively at one or both ends of the starting macromolecule using free radical "living" or "controlled" polymerisation, e.g. using a complexing agent
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F8/00—Chemical modification by after-treatment
- C08F8/14—Esterification
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/26—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers and other compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/334—Polymers modified by chemical after-treatment with organic compounds containing sulfur
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/334—Polymers modified by chemical after-treatment with organic compounds containing sulfur
- C08G65/3344—Polymers modified by chemical after-treatment with organic compounds containing sulfur containing oxygen in addition to sulfur
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/334—Polymers modified by chemical after-treatment with organic compounds containing sulfur
- C08G65/3344—Polymers modified by chemical after-treatment with organic compounds containing sulfur containing oxygen in addition to sulfur
- C08G65/3346—Polymers modified by chemical after-treatment with organic compounds containing sulfur containing oxygen in addition to sulfur having sulfur bound to carbon and oxygen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L71/00—Compositions of polyethers obtained by reactions forming an ether link in the main chain; Compositions of derivatives of such polymers
- C08L71/02—Polyalkylene oxides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2438/00—Living radical polymerisation
- C08F2438/03—Use of a di- or tri-thiocarbonylthio compound, e.g. di- or tri-thioester, di- or tri-thiocarbamate, or a xanthate as chain transfer agent, e.g . Reversible Addition Fragmentation chain Transfer [RAFT] or Macromolecular Design via Interchange of Xanthates [MADIX]
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2650/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G2650/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule characterized by the type of post-polymerisation functionalisation
- C08G2650/04—End-capping
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L2201/00—Properties
- C08L2201/54—Aqueous solutions or dispersions
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L2203/00—Applications
- C08L2203/02—Applications for biomedical use
Definitions
- the present invention relates to a block copolymer or graft copolymer containing a hydrophobic portion carrying a short-chain fatty acid ester and a poly (ethylene glycol) chain as a hydrophilic portion, and its use as a nanomedicine material.
- Short-chain fatty acids such as acetic acid, propionic acid, butyric acid (or butyric acid) have various physiological functions such as immunosuppressive ability, liver fibrosis inhibitory ability, obesity inhibitory ability, and anticancer ability depending on the chain length. It has been reported to have (see, for example, Non-Patent Document 1,). Although the short-chain fatty acids having the above-mentioned physiological functions are produced from sugars by the intestinal flora, they are not always sufficient and are expected to be sufficiently supplied.
- short-chain fatty acids are not only limited in administration method due to their solubility and odor, but also metabolized quickly due to their low molecular weight, and their physiological functions are changed by association. Have difficulty. Therefore, although some of them are provided as supplements, it is no exaggeration to say that there is no effective administration method or preparation capable of exerting the physiological functions inherent in short-chain fatty acids.
- An object of the present invention is to provide a means for effectively administering and delivering short-chain fatty acids into a living body.
- the present inventors have conventionally carried a drug to a polymer compound which has an associative property and can self-assemble in an aqueous medium to modify the delivery property of the drug.
- a polymer compound which has an associative property and can self-assemble in an aqueous medium to modify the delivery property of the drug.
- Has been designed and proposed for example, WO 2009/133647, WO 2016/052463.
- the present inventors have conducted repeated studies on the assumption that if any polymerized drug system can be successfully used to achieve the above-mentioned object, it will contribute to the solution of the above-mentioned problems.
- Aspect 1 Hydrophilic-hydrophobic copolymer, (1) Equation I:
- R 1 is an unsubstituted or substituted linear or branched alkyl having 1 to 7 carbon atoms (when substituted).
- Substituents are unsubstituted or substituted phenyls, and the substituents on the substituted phenyls are one or more halogens, hydroxys, methyloxys), where the hydrogen atom is n30, if any. % Or less, preferably 20% or less, more preferably 10% or less, most preferably 0%, and n is an integer of 5 to 1000, preferably 10 to 1000, more preferably 15 to 1000, 30 to 1000.
- Equation IIa Represented by Hydrophobic segments derived from repeating units, and (2) hydrophilic segments containing poly (ethylene glycol) chains. Equation IIa:
- A is an unsubstituted or substituted C 1 -C 12 alkyloxy, substituents when substituted the formyl group, the formula R 'R "CH- group, phenylamino group or phenethylamino group, phenyl, methoxyphenyl group, wherein, R 'and R "C 1 -C 4 alkyloxy or R independently' and R" are -OCH 2 CH 2 O together -, - O ( CH 2 ) 3 O- or —O (CH 2 ) 4 O-, m is an integer of 2 to 500, preferably 10 to 300, more preferably 20 to 200.
- Ra is a hydrogen atom or a carboxy group
- B is A-CH 2 CH 2 , and A and m are as defined above, respectively.
- y is an integer of 1 to 300, preferably 2 to 150, more preferably 5 to 100.
- Aspect 2 Hydrophilic-hydrophobic copolymer of Aspect 1, which forms nanoparticles or nano-sized polymeric micelles by associating in water and self-assembling.
- Aspect 3 A hydrophilic-hydrophobic copolymer of Aspect 1 or 2. The copolymer containing the hydrophobic segment derived from the repeating unit represented by the formula (I) of the formula (1) and the hydrophilic segment of the formula IIa of the formula IIa of the formula (2) (i) is described in the formula BC:
- R, Ra , B, X, m, n, and y are as defined above, respectively. It is a graft copolymer represented by, Hydrophilic-hydrophobic copolymer.
- Aspect 4 Nanoparticles formed in an aqueous medium from the hydrophilic-hydrophobic copolymer of any of aspects 1-3.
- Aspect 5 A pharmaceutical preparation comprising the hydrophilic-sparse copolymer of any one of Aspects 1 to 3 or the nanoparticles of Aspect 4 as an active ingredient.
- Aspect 6 Prevention or treatment of cancer, suppression of obesity, prevention or treatment of ulcerative colitis, non-alcoholic fatty liver (or suppression of liver fibrosis), prevention or treatment of diabetes, enhancement of radiation in radiation therapy, or , A pharmaceutical formulation of embodiment 5 for use in the prevention or treatment of hyperammonemia.
- Aspect 7 Prevention or treatment of cancer, suppression of obesity, prevention or treatment of ulcerative colitis, non-alcoholic fatty liver, prevention or treatment of diabetes, enhancement of radiation in radiation therapy, prevention or prevention of hyperammonemia
- the hydrophilic-hydrophobic copolymer according to any one of aspects 1 to 3 for use in therapy.
- Aspect 8 Prevention or treatment of cancer, suppression of obesity, prevention or treatment of ulcerative colitis, non-alcoholic fatty liver (or suppression of liver fibrosis), prevention or treatment of diabetes, enhancement of radiation in radiation therapy, or , Nanoparticles of embodiment 4 for use in the prevention or treatment of hyperammonemia.
- a hydrophilic-hydrophobic copolymer according to any one of Aspects 1 to 3 is administered to a patient in need thereof to prevent or treat cancer, suppress obesity, ulcerative colitis, non-alcoholic fatty liver.
- a hydrophilic-hydrophobic copolymer according to any one of Aspect 4 is administered to a patient in need thereof to prevent or treat cancer, suppress obesity, prevent ulcerative colitis, and prevent non-alcoholic fatty liver.
- a method for treating, preventing or treating diabetes (or suppressing liver fibrosis), enhancing radiation in radiation therapy, suppressing liver fibrosis, or preventing or treating hyperammonemia is administered to a patient in need thereof to prevent or treat cancer, suppress obesity, prevent ulcerative colitis, and prevent non-alcoholic fatty liver.
- hydrophilic-hydrophobic copolymer of the present invention or its nanoparticles or high molecular weight micelles are administered to mammals including humans, they are delivered locally to the living body, and the short-chain fatty acid ester in the hydrophobic segment is locally delivered.
- the bond can be enzymatically hydrolyzed to release the corresponding short-chain fatty acid, which can eliminate or alleviate the problems associated with the administration of the short-chain fatty acid itself. Therefore, it is possible to provide a copolymer capable of efficiently exerting various physiological functions essentially possessed by short-chain fatty acids locally or systemically in a mammal, and nanoparticles thereof and a pharmaceutical preparation.
- Short-chain fatty acids can be produced from sugars by the intestinal flora of mammals, typically including acetic acid, propionic acid, butyric acid (or butyric acid).
- Branch-chain fatty acids such as isobutyric acid and isovaleric acid, which may be produced by the decomposition of proteins containing certain branched-chain amino acids, and even when they exert functions similar to these fatty acids.
- Examples of 1 include, but are not limited to, methyl, ethyl, propyl, isopropyl, butyl, isobutyl, heptyl, pentyl, 3-methylbutyl and the like. These groups may be substituted, and the substituents when substituted are preferably unsubstituted or substituted phenyls capable of binding to carbon atoms at the unbonded ends, and substituted phenyls. Substituents can be one or more halogens, hydroxys, methyloxys. Also, C x -C alkyl moiety described with xx alkyloxy, etc., it refers to an alkyl carbon atoms x number ⁇ xx number of linear or branched.
- R can be a hydrogen atom, where it is 30% or less, preferably 20% or less, more preferably 10% or less, most preferably 0% (absent) of the total number of repeating units of n.
- the degree of such preference is the degree to which the copolymer more reliably forms a hydrophobic domain or region when associating and self-assembling in water.
- the segment represented by formula IIa for providing a hydrophilic segment provides a hydrophilic block
- the hydrophobic segment represented by formula I can be a member of hydrophilic-hydrophobic block copolymers, which are hydrophobic blocks, or also
- Each repeating unit represented by the formula IIb that provides the hydrophilic segment can be a member of a hydrophilic-hydrophobic random copolymer that can randomly exist with each hydrophobic segment represented by the formula I. ..
- Random may, where appropriate, alternate, for example, when n in formula I and y in formula IIb are approximate numbers, or, for example, n pairs in formula I.
- y of formula IIb is 30 or more: 1
- the hydrophobic segment may be in a form in which a plurality of segments form a block.
- block copolymers and random copolymers contain a hydrophobic segment in the core and a hydrophilic segment in the shell by associating and self-assembling a plurality of copolymers in water.
- Other members can be included as long as they can form so-called core-shell type nanoparticles or polymer micelles.
- typical copolymers disclosed herein include the above-mentioned copolymers of formula BC or formula GC.
- the divalent linking group generally has a maximum of 34, preferably 18, and more preferably a maximum of 10 carbons.
- optionally means a group containing oxygen and nitrogen atoms.
- Specific examples of such a linking group include the following groups:
- nano size refers to nanoparticles or nano-sized polymer micelles, and the mean diameter is in the nanometer range when dynamic light scattering measurement (DLS) of nanoparticles or polymer micelles is performed in water.
- DLS dynamic light scattering measurement
- the average diameter is about 10 nm to about 2000 nm, preferably about 10 nm to about 500 nm, and more preferably about 25 nm to about 200 nm.
- hydrophilic-hydrophobic copolymer can be produced according to a production method known per se, with reference to the defined chemical structure. Conveniently, one of the following methods can be followed.
- copolymer represented by the typical formula BC defined by the above (1) and the above (2) (i) is as follows with reference to the above WO 2009/133647 and WO 2016/052463. It is convenient to manufacture in.
- the substituent is obtained by a reduction amination reaction between the formyl group of the compound corresponding to the formula IIa having a formyl group as the substituent and the corresponding amine. Can be introduced.
- a graft copolymer represented by a typical GC carries a short chain fatty acid ester of vinyl alcohol and a carboxy group or a protected group thereof or a halogen atom (Cl, Br, etc.) corresponding to the repeating unit of the formula I.
- the copolymer according to the present invention is amphipathic, and a water-soluble organic solvent such as N, N-dimethylformamide (DMF) or dimethylsulfoxide (DMSO) -containing aqueous solution is prepared.
- a water-soluble organic solvent such as N, N-dimethylformamide (DMF) or dimethylsulfoxide (DMSO) -containing aqueous solution is prepared.
- the copolymer itself is associated to form micelles by dialyzing water through a dialysis membrane having a constant molecular weight cut-off.
- the micelles or nanoparticles thus formed can be obtained as separated solids by, for example, freeze-drying, centrifugation, or the like.
- nanoparticles and nano-sized polymeric micelles are provided as solubilized or uniformly dispersed solutions or solutions in an aqueous medium (an aqueous solution that may optionally contain saline or a pH adjuster). Therefore, it can be an oral preparation in various forms including a parenteral preparation.
- an aqueous solution that may optionally contain saline or a pH adjuster.
- the nanoparticles of the present invention can also be provided as tablets, pills, or granules by utilizing the excipients and diluents commonly used in the art.
- Excipients or diluents are not limited, but are commonly used in the art, such as sodium chlorocarmellose, crystalline cellulose, hypromellose, sodium lauryl sulfate, magnesium stearate, macrogol 4000, titanium oxide, etc. Can be.
- compositions containing such nanoparticles as an active ingredient have the above-mentioned physiological functions inherent in the short-chain fatty acid itself, which are locally present in the living body of mammals including humans to which the nanoparticles are delivered. Can be demonstrated in. Since the optimum dose of such a pharmaceutical preparation varies depending on the disease and administration method for the purpose of treatment, the dose cannot be uniquely specified, but the dose can be obtained through small-scale clinical trials or the like. A specialist can make a decision based on data and the like.
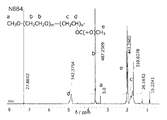
- Production Example 8 Preparation of self-assembled particles 2 Except for using the graft polymer (N741) synthesized in Production Example 6, the operation of Production Example 7 was repeated, and it was confirmed that particles having an average particle size of 153 nm were formed (see FIG. 6).
- Test Example 1 Cytotoxicity 1 In 96-well plates seeded with HepG2 cells for each 1x10 4, and adding each sample of the self-assembled particles prepared in Preparation Example 7, was incubated for 24 hours, it was added WST solution, 450 nm UV absorption after 2 hours was measured and compared with the control, and it was confirmed that there was almost no toxicity under the measured concentration (FIG. 7: Cytotoxicity of each nanoparticles of N684, N731 and N721 is shown).
- Test Example 2 Cytotoxicity 2
- the cytotoxicity of N741 was evaluated by repeating the operation of Test Example 1 except that the self-assembled particles prepared in Production Example 8 were used. The test results are shown in FIG. From FIG. 8, it can be seen that the nanoparticles of N741 do not show cytotoxicity in this test system.
- Test Example 3 Cancer metastasis inhibitory effect 5-7 5-week-old BALB / c mice (male) in Group 1 were allowed to freely ingest each of the samples described in the following GP1 to GP6 administration groups. Two days later, dispensed caudal vein the 1x10 4 of B16F10 / B16F10 melanoma cells (obtained from Riken Cell Bank), was continued the water consumption of sample water.
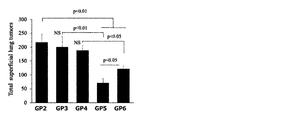
- FIG. 10 shows the result of dissecting on the 11th day and confirming the number of cancers normally attached to the lung by macroscopic observation
- FIG. 9 shows the change in body weight of the experimental animal under test.
- FIG. 10 shows the results of measuring the number of micrometastases that cannot be observed with the naked eye under a microscope. Similar to FIG. 10, it was confirmed that propionic acid nanoparticles (abbreviated as PEG-b-PVPro in the figure) extremely suppressed cancer metastasis.
- PEG-b-PVPro propionic acid nanoparticles
- FIG. 12 shows the H & E staining chart of the lung tissue chart (left) and the number of metastatic cancers obtained from the chart (right). Compared with the control, propionic acid nanoparticles and butyric acid nanoparticles showed a significant reduction in the number of cancers.
- FIG. 13 shows the H & E staining diagram (left) of the lung tissue chart and the area of metastatic cancer determined from the diagram (right). Propionic acid nanoparticles and butyric acid nanoparticles significantly reduced the area of cancer compared to controls and low molecular weight fatty acids.
- FIG. 14 shows the levels of ALT, AST, LDH and ALB in blood. In each case, it was confirmed that there was almost no damage to the liver or organs.
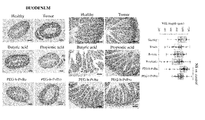
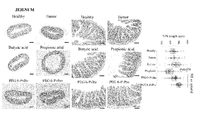
- FIGS. 15-18 show H & E staining diagrams of the small and large intestine tissues. Villi shortening was observed in the low molecular weight fatty acid group depending on the location, and it was confirmed that there was damage.
- Sample administration group GP1: Healthy group (n 5)
- GP2: Melanoma administration group (n 7)
- GP3: Melanoma administration group / 30 mM propionic acid free intake group (n 7)
- Test Example 4 Diet effect Five 4-week-old C57BL / 6J mice (male) in one group were fed solid feed D12492 (60% Fat, ultra-high fat feed) purchased from EPS Masshin Co., Ltd., and the following GP1 to Each sample described in each administration group of GP3 was given, and the body weight was measured. The results are shown in FIG.
- Test Example 5 Effect on ulcerative colitis Seven 7-week-old ICR mice (male) in one group were allowed to freely ingest 4% sodium dextran sulfate (DSS), and the following sample was orally administered once a day by sonde. After 10 days, the disease activity index (DAI) was measured and blood was evaluated. As shown in FIG. 20, butyric acid nanoparticles (denoted as BNP in the figure) were significantly reduced in the ulcerative colitis model, and a therapeutic effect was observed. In addition, as shown in FIG. 21, the white blood cell count was significantly increased in the ulcerative colitis model, whereas it was significantly suppressed in BNP.
- DAS disease activity index
- Sample administration group GP1 Free intake of tap water + tap water (0.65 mL) GP2: 4% DSS intake + tap water (0.65 mL) GP3: 4% DSS intake + butyric acid (2.32 mg / mL, 0.65 mL) GP4: 4% DSS intake + CNP (PEG-b-polystyrene) (10 mg / mL, 0.65 mL) GP5: 4% DSS intake + BNP (PEG-b-Poly (vinyl butyrate) (10 mg / mL, 0.65 mL)
- Test Example 6 Effect on non-alcoholic steatohepatitis (NASH) 49 5-week-old C57BL / 6J mice (male) were fed with solid feed A06071302 (choline-deficient high-fat feed, methionine weight loss, 0) purchased from EPS Masushin Co., Ltd. (Addition of 1% methionine) was given by free intake, and after 4 weeks, the animals were randomly divided into 7 animals per group, and each sample described in each of the following GP1 to GP7 administration groups was administered by free intake. Data analysis was performed after 8 weeks.
- FIG. 22 shows the weight of the liver and spleen.
- Sample administration group GP1 Normal solid feed (Oriental yeast MF)
- GP2 Solid feed A06071302
- GP3 Solid feed A06071302 + butyric acid (65 mM)
- GP4 Solid feed A06071302 + propionic acid (50 mM)
- GP5 Solid feed A06071302 + butyric acid nanoparticles (10 mg / mL, polymer concentration 1 mM butyric acid equivalent 65 mM)
- GP6 Solid feed A06071302 + propionic acid nanoparticles (10 mg / mL, polymer concentration 1 mM propionic acid equivalent 50 mM)
- GP7 Solid feed A06071302 + polystyrene nanoparticles (10 mg / mL)
- Test Example 7 Cancer metastasis inhibitory effect # 2 5-7 7-8 week old C57BL / 6J mice (male) per group were obtained from Charles River Japan, Inc., Yokohama. These mice were bred under pathogenic conditions in a 12 hour dark / light cycle at controlled temperature (23 ⁇ 1 ° C.) and humidity (50 ⁇ 5%) with free feeding of standard solid feed. .. Mice were randomly divided into the following GP1 to GP6 administration groups, and each of the described samples was freely ingested. After one day, was injected caudal vein with 200 [mu] L B16F10 / B16F10 melanoma cells (physiological saline) per 2.5 ⁇ 10 5 (obtained from Riken Cell Bank). From 1 day before this tail injection to 11th, the end of the test, each sample was continuously fed to mice as a free drinking form. Plasma and other organs were harvested on day 11 and stored appropriately for each further analysis below.
- Test Example 8 Effect on anti-diabetic test Animal management and use in this test and tests using all experimental animals disclosed in the present specification were carried out in strict accordance with the guidelines of the University of Tsukuba regarding the management and the like. Seven 7-8 week old C57BL / 6J mice (male) in one group were obtained from Charles River Japan, Inc. (Yokohama). These mice were bred under pathogenic conditions in a 12 hour dark / light cycle at controlled temperature (23 ⁇ 1 ° C.) and humidity (50 ⁇ 5%) with free feeding of standard solid feed. .. Mice were randomly divided into the following GP1 to GP6 administration groups, and each of the listed samples was fed freely for up to 36 days. One day later, a glucose tolerance test was performed.
- Sample administration group GP1 Exenatide (traditional antidiabetic drug), 1 ⁇ g (day 1-4), 2 ⁇ g (day 5-36) daily subcutaneous injection group GP2: 60 mM BNP (particles derived from N721: Production example) 7) Free intake group GP3: 60 mM PNP (particles derived from N721: see Production Example 7) Free intake group GP4: 30 mM Buty acid free intake group GP5: 30 mM Propionic acid free intake group. GP6: Control group (free water intake)
- the amount of sample consumed in the test is shown as the amount per mouse (mL), and the body weight of the mouse is shown as the average ⁇ SD value in FIG. 24, respectively.
- the size of islets of Langerhans decreased in the diabetic model mice and the propionic acid-administered group, butyric acid-administered group, and PNP-administered group, but the islets of Langerhans were not atrophic in the BNP-administered group and the exenatide-administered group. It is shown to be maintained.
- Test Example 9 Effect as a radiation enhancer Part 1
- mice Five 5-7 week old C57BL / 6J mice in a group obtained in the same manner as in the above test were bred under the same conditions. 100 [mu] L (serum free DMEM) per 0.076 ⁇ 10 6 melanoma B16F10 cells were injected subcutaneously into the right thigh outer side of the mouse (day 7 before irradiation). After 1 week of cancer growth, mice were randomly divided into the following treatment groups. BNP 500 mg / kg was administered intraperitoneally (ip) of mice 1 day before irradiation and immediately after irradiation, and the radiation enhancing effect was confirmed (GP3 and GP4, respectively).
- Irradiation conditions were set at 10 Gy, 150 kV, 20 mA, Al filtration, and 330 mm intervals.
- Sample administration group GP1 Cancer symmetric group GP2: Cancer + irradiation (IR: 10 Gy) group GP3: BNP 500 mg / kg (1 day before irradiation) group GP4: BNP 500 mg / kg (0 day after irradiation) group
- Plasma and other organs were collected at the end of the study and stored appropriately for further analysis.
- the 10 Gy irradiation group has a tumor growth inhibitory effect, and even if BNP is administered before and after X-ray irradiation, the tumor size after 8 days is significantly smaller than that in the BNP non-administration group, confirming the radiation enhancing effect.
- Test Example 10 Effect as a radiation enhancer Part 2
- 100 [mu] L (serum free DMEM) per 0.076 ⁇ 10 6 melanoma B16F10 cells were injected subcutaneously into the right thigh outer side of the mouse (day 9 before irradiation).
- mice were randomly divided into the following treatment groups. Irradiation conditions were set at 10 Gy, 150 kV, 20 mA, Al + Cu (0.5 mm + 0.1 mm) filtration, and 330 mm intervals.
- FIG. 33 The data of the cancer growth profile by irradiation with 5 Gy after administration of butyric acid and NP in the melanoma xenograft model is shown in FIG. 33.
- Butyric acid and BNP were administered prior to irradiation.
- Weight loss was observed in the butyric acid administration group, and toxicity was observed. On the other hand, the BNP-administered group showed no weight loss and was not toxic.
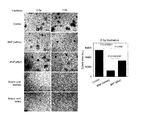
- Mouse melanoma B16F10 cells were purchased from Cell Bank (RIKEN, Japan). These cell lines were supplemented with 10% fetal bovine serum and an antibiotic mixture of 100 ng / mL penicillin-streptomycin-neomycin in Dalveco's modified Eagle's medium (DMEM; L-glutamine, 1 g / L glucose, sodium bicarbonate, Sigma- Aldrich, St Louis, MO, USA) was maintained at 37 ° C. under a humid atmosphere of 5% CO 2 . The results are shown in FIG. The growth inhibitory effect of spheroid cancer cells is clearly confirmed in the BNP-administered group.
- DMEM Dalveco's modified Eagle's medium
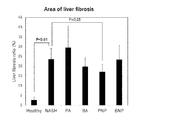
- Test Example 12 Effect on non-alcoholic steatohepatitis (NASH) Part 2 Forty-two 5-week-old C57BL / 6J mice (male) were fed a solid feed A06071302 (choline-deficient high-fat feed, methionine reduction, 0.1% methionine addition) purchased from EPS Masushin Co., Ltd. by free intake. After 4 weeks, the animals were randomly divided into 7 animals per group, and were divided into the following healthy groups (Healthy) (no solid feed A06071302), NASH, butyric acid (BA), propionic acid (PA), PNP, and BNP 6 groups. Each sample described in the above was administered by free ingestion (prepared to a concentration of 65 mM for PA in the PA and PNP groups and 50 mM for BA in the BA and BNP groups). Data analysis was performed after 8 weeks.
- NASH non-alcoholic steatohepatitis
- the liver weight (left figure) is significantly heavier in the NASH group than in the healthy group, causing inflammation.
- the PNP-administered group has a significantly lighter liver weight than the NASH group and suppresses inflammation.
- the spleen weight (left figure) was significantly increased in the NASH group and significantly decreased in the PNP-administered group compared to the healthy group.
- the graph shows the error bars based on the mean value and standard deviation of the oil droplet structure area of each group.
- the t-test is performed to check for statistically significant differences between the mean values, and there is a statistically significant difference at P ⁇ 0.05.
- the amount of oil droplets in the liver increased significantly in the NASH group compared to the healthy group (fatty liver condition).
- the amount of oil droplets in the PNP-administered group was significantly smaller than that in the NASH group.
- the graph shows error bars based on the mean value and standard deviation of the fibrotic tissue area of each group.
- the T-test is performed to check for statistically significant differences between the mean values, and there is a statistically significant difference at p ⁇ 0.05.
- the amount of liver fibrosis is significantly higher in the NASH group than in the healthy group.
- the amount of liver fibrosis in the PNP-administered group was significantly smaller than that in the NASH group.
- Test Example 13 Anti-ammonemia effect Twenty-four 6-week-old C57BL / 6N mice (male) were randomly divided into 4 groups, and samples were orally administered by sonde over 4 days (1.22 mmol once a day). -4 PBA / kg). In the administration group 2GP-4GP, acetaminophen (acetyl-p-aminophenol; APAP; 300 mg / kg) was intraperitoneally administered on the 4th day to cause acute liver injury and hyperammonemia, and on the 5th day. It was dissected and evaluated.
- acetaminophen acetyl-p-aminophenol
- APAP 300 mg / kg
- Sample administration group 1GP: Saline 2GP: APAP + water 3GP: APAP + 4-phenylbutyric acid (200mg / kg, 1.22 mmol-4PBA / kg) 4GP: APAP + Ph-BNP (200 mg / kg, 1.22 mmol-4PBA / kg)
- Test Example 15 Pharmacokinetic test According to the method of Production Examples 1 to 8 described above, the corresponding modification is carried out according to a conventional method, and PEG-b-poly (vinyl butyric acid) having a benzene ring at the ⁇ terminal of PEG (the following formula left). (See.) And PEG-b-poly (vinyl4-phenylbutyric acid) (see the formula on the right), 125 I was introduced by the chloramine method, purified twice on a PD-10 column, and unreacted iodine was added. Sorted.
- mice in which N932 was freely ingested from a water bottle were collected from blood, liver and gastrointestinal tract, and their gamma ray intensities were measured by a scintillation detector. The results are shown in FIG. 42 (left). From the figure, it was confirmed that N932 was almost completely localized in the gastrointestinal tract.
- N930 was orally administered by force with a sonde, and the gamma ray intensity of major organs was measured 24 hours later.
- the results are shown in FIG. 42 (right). From this figure, it can be confirmed that 4-phenylbutyric acid is widely distributed in the digestive tract, blood, liver, kidney, etc., and is hydrolyzed in the digestive tract and taken up in the circulatory system.
- Sample administration group 1GP: Saline (control, 3 animals)
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Polymers & Plastics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Nanotechnology (AREA)
- Child & Adolescent Psychology (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Medicinal Preparation (AREA)
Abstract
Description
態様1:親水-疎水性共重合体であって、
(1)式I:
で表される、
反復単位に由来する疎水性セグメント、と
(2)ポリ(エチレングリコール)鎖を含む親水性セグメントであって、
(i)式IIa:
で表される、親水性セグメント、又は
(ii)式IIb:
XはRaがカルボキシ基であるとき、C(=O)O若しくはC(=O)NHであり、又はRaが水素原子であるとき、O若しくはNHであり、
Bは、A-CH2CH2であって、A及びmはそれぞれ、上記定義のとおりであり、
yは1~300、好ましくは2~150、より好ましくは5~100、の整数である、
で表される反復単位に由来する親水性セグメントを含み、
前記(1)の疎水性セグメントと、(2)(i)の親水性セグメントは、それぞれブロックとして存在し、
前記(1)の疎水性セグメントと、(2)(ii)の親水性セグメントを含むそれぞれの反復単位の各構成員は、相互にランダムに存在する、
親水-疎水性共重合体。
態様2:水中で会合して自己組織化することによりナノ粒子又はナノサイズの高分子ミセルを形成する、態様1の親水-疎水性共重合体。
態様3: 態様1又は2の親水-疎水性共重合体であって、
前記(1)の式(I)で表される反復単位に由来する疎水性セグメントと前記(2)(i)の式IIaの親水性セグメントを含む共重合体は、式BC:
で表されるブロック共重合体であり、
前記(1)の式(I)で表される反復単位に由来する疎水性セグメントと前記(2)(ii)の式IIbの親水性セグメントを含む共重合体は、式GC:
で表されるグラフト共重合体である、
親水-疎水性共重合体。
態様4;態様1~3のいずれかの親水-疎水性共重合体から水性媒体中で形成された、ナノ粒子。
態様5:態様1~3のいずれかの親水-疎性共重合体又は態様4のナノ粒子を有効成分として含んでなる、製薬学的製剤。
態様6:がんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療(若しくは肝線維化の抑制)、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療に使用するための態様5の製薬学的製剤。
態様7:がんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療に使用するための態様1~3のいずれかの親水-疎水性共重合体。
態様8:がんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療(若しくは肝線維化の抑制)、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療に使用するための態様4のナノ粒子。
態様9:態様1~3のいずれかの親水-疎水性共重合体を、それらを必要とする患者に投与してがんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療(若しくは肝線維化の抑制)、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療するための方法。
態様10:態様4のいずれかの親水-疎水性共重合体を、それらを必要とする患者に投与してがんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療、糖尿病の予防若しくは治療(若しくは肝線維化の抑制)、放射線療法における放射線の増強、肝線維化の抑制、又は、高アンモニア血症の予防若しくは治療するための方法。
親水性セグメントを提供する式IIbで表される各反復単位は、式Iで表される各疎水性セグメントと相互にランダムに存在できる親水-疎水性ランダム共重合体の構成員となることができる。相互にランダムと称するのは、適する場合には、例えば、式Iのnと式IIbのyが近似する数値であるときは、交互に存在してもよく、また、例えば、式Iのn対式IIbのyが、30以上:1であるときは、実質的に、疎水性セグメントは複数のセグメントがブロックを形成するような形態にあってもよい。
式A-1:
式A-2:
で表されるPEG誘導体を用意し、次いで、式Iの反復単位に対応するビニルアルコールの短鎖脂肪酸エステルを用意し、可逆的な交換連鎖移動を介するリビング的なラジカル重合反応により、前者の単位に後者を付加する方法を利用することができる。このとき、A-1における、L-S(C=S)Phは、後述する、L-S(C=S)OCH2CH3であると、より効率よく目的の共重合体を得ることができる。なお、Aが置換基としてフェニルアミノ基、フェネチルアミノ基を有する場合には、置換基としてホルミル基を有する式IIaに対応する化合物のホルミル基と対応するアミンとの還元アミノ化反応により当該置換基を導入することができる。
市販のCH3O-(CH2CH2O)m-H(MW=5,000,100g,20mmol)にテトラヒドロフラン(THF)(200mL)及びブチルリチウム14.4mL(23mmol,1.6M-ヘキサン)を加えたのち、α,α‘-ジブロモキシレン(25g,95mmol)を加え50°C、2日間反応させた。2-プロパノール(IPA)に沈殿させた後沈殿物を減圧乾燥した。得られた淡黄色ポリマーをメタノールに溶解し、遠心分離してα,α‘-ジブロモキシレンを沈殿として除いた。メタノール溶液をIPAに投入し、得られた白色沈殿を減圧乾燥させ、目的物(N686)を得た。(収量104g)
製造例1で合成したN686(20g)を100mLのエタノールに溶解させ、エチルキサントゲン酸カリウム(CH3CH2OC(=S)SK,7g)を加え、室温で10分間反応させた。沈殿を遠心分別した後エタノールを減圧留去した。残渣をクロロホルムに溶解し、水で洗浄、クロロホルム層を分別し、無水硫酸ナトリウム脱水ろ過後IPAに沈殿させ、遠心分離後減圧乾燥して目的物(N717)を得た(収量15g)。
製造例2で合成したN717(1g)、アゾビスイソブチロニトリル(15mg)、酢酸ビニル(6.6g)をフラスコに加え、5分間窒素バブルしたのち60°C、1日反応させた。得られた目的物をTHFに溶解させ、IPAに沈殿、減圧乾燥し目的物(N684)を得た(2.6g)。N684の1H NMRスペクトルを図1に示す。
製造例2で合成したN717(5g)、アゾビスイソブチロニトリル(75mg)、プロピオン酸ビニル(7g)をフラスコに加え、5分間窒素バブルしたのち60°C、2日反応させた。得られた目的物をTHFに溶解させ、IPAに沈殿、減圧乾燥し目的物を得た(9.3g)。N731の1H NMRスペクトルを図2に示す。
実施例2で合成したN717(5g)、アゾビスイソブチロニトリル(75mg)、酪酸ビニル(10g)をフラスコに加え、5分間窒素バブルしたのち60°C、2日反応させた。得られた目的物をTHFに溶解させ、IPAに沈殿、減圧乾燥し目的物(N721)を得た(12.3g)。N721の1H NMRスペクトルを図3に示す。
*THF(20mL)にCH3O-(CH2CH2O)mOH(MW=5,000,5g)及びブチルリチウム(0.6mL)を加えCH3O-(CH2CH2O)mOLiのTHF溶液を作製した。
上記で合成したポリマー(N684,N731,N721)をそれぞれ50mg採取し、1mLのDMFに溶解させ水を1mL加えて透析膜(MWCO=3.5KDa)に入れて2Lの水に対して透析した。半日ごとに3度透析水を交換した後、動的光散乱測定を行い、平均30-100nmの粒子が形成していることを確認した(図5参照)。
製造例6で合成したグラフトポリマー(N741)を用いたこと以外、製造例7の操作を繰り返し、153nmの平均粒径を有する粒子が形成していることを確認した(図6参照)。
各1x104のHepG2細胞を播種した96穴プレートに、製造例7で作製した自己組織化粒子の各サンプルを添加し、24時間インキュベートした後、WST溶液を添加し、2時間後に450nmのUV吸収を測定しコントロールと比較したところ、いずれも測定の濃度下ではほとんど毒性が出ないことを確認した(図7:N684,N731,N721の各ナノ粒子の細胞毒性を示す。)。
製造例8で作製した自己組織化粒子を使用したこと以外、試験例1の操作を繰り返し、N741の細胞毒性を評価した。試験結果を図8に示す。図8から、N741のナノ粒子は本試験系で細胞毒性を示さないことが判る。
1群5-7匹の5週齢BALB/cマウス(オス)に、下記のGP1乃至GP6の投与群に記載の各サンプルを自由摂取させた。2日後、1x104のB16F10/B16F10メラノーマ細胞(理研細胞バンクから入手)を尾静注し、サンプル水の摂水を継続した。11日目に解剖し、肺に正着しているがんの個数を肉眼観察により確認した結果を図10に示し、また、試験中の実験動物の体重変化を図9に示す。
サンプル投与群
GP1 :健康群(n=5)
GP2 :メラノーマ投与群(n=7)
GP3 :メラノーマ投与群/30mMプロピオン酸自由摂取群(n=7)
GP4 :メラノーマ投与群/30mM酪酸自由摂取群(n=7)
GP5 :メラノーマ投与群/30mM N731自由摂取群(n=7)
GP6 :メラノーマ投与群/30mM N721自由摂取群(n=7)
1群5匹の4週齢C57BL/6Jマウス(オス)にEPS益新株式会社より購入した固形飼料D12492(60% Fat、超高脂肪飼料)を与え、下記のGP1乃至GP3の各投与群に記載の各サンプルを与え、体重測定を行った。結果を図19に示す。
サンプル投与群
GP1:水道水自由摂取
GP2:N731自由摂取(5mg/mL)
GP3:N721自由摂取(5mg/mL)
1群7匹の7週齢ICRマウス(オス)に4%デキストラン硫酸ナトリウム(DSS)を自由摂取させ、下記サンプルをゾンデで一日一度経口投与した。10日後疾患活動性評価指標(disease activity index(DAI))を測定し、血液を評価した。図20に示すように、酪酸ナノ粒子(図中ではBNPと表記)が潰瘍性大腸炎モデルに対して有意に低下しており、治療効果を認めた。また、図21に示すように潰瘍性大腸炎モデルでは白血球数の著しい上昇が見られるのに対し、BNPでは有意に抑制した。
サンプル投与群
GP1:水道水自由摂取+水道水(0.65mL)
GP2:4%DSS摂取+水道水(0.65mL)
GP3:4%DSS摂取+酪酸(2.32mg/mL,0.65mL)
GP4:4%DSS摂取+CNP(PEG-b‐ポリスチレン)(10mg/mL,0.65mL)
GP5:4%DSS摂取+BNP(PEG-b‐Poly(vinyl butyrate)(10mg/mL,0.65mL)
49匹の5週齢C57BL/6Jマウス(オス)にEPS益新株式会社より購入した固形飼料A06071302(コリン欠乏高脂肪飼料、メチオニン減量、0.1%メチオニン添加)を自由摂取にて与え、4週間後に無作為に1群7匹に分け、下記のGP1乃至GP7の各投与群に記載の各サンプルを自由摂取にて投与した。8週間後にデータ解析を行った。図22に肝臓及び脾臓重量を示す。NASH群が炎症により肥大化しているのに対し、プロピオン酸粒子投与群で有意に肥大化が抑制されていることを確認した。
サンプル投与群
GP1:通常固形飼料(オリエンタル酵母MF)
GP2:固形飼料A06071302
GP3:固形飼料A06071302+酪酸(65mM)
GP4:固形飼料A06071302+プロピオン酸(50mM)
GP5:固形飼料A06071302+酪酸ナノ粒子(10mg/mL,ポリマー濃度1mM 酪酸換算65mM)
GP6:固形飼料A06071302+プロピオン酸ナノ粒子(10mg/mL,ポリマー濃度1mM プロピオン酸換算50mM)
GP7:固形飼料A06071302+ポリスチレンナノ粒子(10mg/mL)
1群5-7匹の7-8週齢C57BL/6Jマウス(オス)をチャールズ リバー ジャパン社、横浜より入手した。これらのマウスを、無病原性条件下、12時間の暗/明サイクルで、制御された温度(23±1℃)及び湿度(50±5%)において標準固形飼料を自由摂餌させながら飼育した。マウスは下記のGP1乃至GP6の投与群に無作為に分け、記載の各サンプルを自由摂取させた。1日後、200μL(生理食塩水)当たり2.5x105のB16F10/B16F10メラノーマ細胞(理研細胞バンクから入手)を尾静注した。この尾注射の1日前から試験の終点である11日迄、各サンプルを自由飲水形式として継続してマウスに与えた。11日目に血漿及び他の臓器を採取し、下記のさらなる各分析に備えて適切に貯蔵した。
サンプル投与群
GP1:健康群(n=5)
GP2:メラノーマ投与群(n=7)
GP3:メラノーマ投与群/30mMプロピオン酸自由摂取群(n=7)
GP4:メラノーマ投与群/30mM酪酸自由摂取群(n=7)
GP5:メラノーマ投与群/30mM PNP(N731由来の粒子:製造例7参照)自由摂取群(n=7)
GP6:メラノーマ投与群/30mM BNP(N721由来の粒子:製造例7参照)自由摂取群(n=7)
本試験及び本明細書に開示するすべての実験動物を用いる試験における動物の管理及び使用については当該管理等に関する筑波大学のガイドラインに厳密に従って行った。
1群7匹の7-8週齢C57BL/6Jマウス(オス)をチャールズ リバー ジャパン社(横浜)より入手した。これらのマウスを、無病原性条件下、12時間の暗/明サイクルで、制御された温度(23±1℃)及び湿度(50±5%)において標準固形飼料を自由摂餌させながら飼育した。マウスは下記のGP1乃至GP6の投与群に無作為に分け、記載の各サンプルを36日迄自由に飲めるようにして摂取させた。1日後、グルコース耐性試験を行った。試験では、1日おきに各マウスの体重及びサンプルの消費についてモニターした。その後、試験の終了時点(40日目)まで、サンプルを飲料水で置き換えた。
サンプル投与群
GP1:エキセナチド(伝統的な抗糖尿病薬)、1μg(1-4日目)、2μg(5-36日目)の各毎日皮下注射群
GP2:60mM BNP(N721由来の粒子:製造例7参照)自由摂取群
GP3:60mM PNP(N721由来の粒子:製造例7参照)自由摂取群
GP4:30mM 酪酸自由摂取群
GP5:30mM プロピオン酸自由摂取群。
GP6:対照群(水自由摂取)
最終グルコース濃度(mg/mL)= [グルコース]60分 -[グルコース]0分
スチューデントのt-検定、テール(2)及びタイプ(2)を行い平均値間の統計誤差を決定した(P<0.05は統計的に有意であると考えられた)。
マウスの解剖後,速やかに取り出した脾臓、腎臓、及び肝臓の重量を測定した結果を図26に示す、これらの臓器をさらなる組織学的分析用として10%中性緩衝液中に保存した。スチューデントのt-検定は上記と同じ。
解剖後取り出したマウスの器官を、速やかに10%中性ホルマリン液に入れて1日間浸漬することによって固定した。その後、パラフィン包埋するために70%エタノール溶液に置換した。パラフィン包埋後のすべての器官を厚さ5μmの組織切片に加工し、常法により、ヘマトキシリン・エオシン(H・E)染色した。組織切片を高濃度アルコールで脱水し、キシレンで洗浄した後、顕微鏡検査を行った(biorevo, BZ-9000,Keyence)。絨毛の長さをイメージ ジェイ ソフトウエア(Image J software)(NIH)により測定した。結果を図29に示す。定量データは、最小と最大範囲の値、上限と下限の四分価(quartile)、中央値:十二指腸(n=130-132)、空腸(n=96-185)、回腸(n=109-138)、結腸(n=37-47),をボックス中のプロットとして表示した。t-検定は上記に同じ。
解剖後取り出したマウスの器官を、速やかに10%中性ホルマリン液に入れて1日間浸漬することによって固定した。その後、パラフィン包埋するために70%エタノール溶液に置換した。常法に従い、パラフィン包埋後のすべての臓器を厚さ5μmの組織切片に加工し、常法により、ヘマトキシリン・エオシン(H・E)染色した。組織切片を高濃度アルコールで脱水し、キシレンで洗浄した後、固定して顕微鏡検査に供した(biorevo, BZ-9000,Keyence)。イメージ ジェイ ソフトウエア(Image J software)(NIH)によりランゲルハンス島の領域を決定した。結果を図30に示す。定量データは、最小と最大範囲の値、上限と下限の四分価(quartile)、中央値(n=10-20)をボックス中のプロットとして表示している。t-検定は上記に同じ。
上記試験と同様に入手した、一群5匹の5-7週令のC57BL/6Jマウスを、同様の条件下で飼育した。100μL(血清不含DMEM)当たり0.076×106のメラノーマB16F10細胞をマウスの右腿外側部に皮下注射した(照射前7日目)。がん増殖1週間後、マウスを下記投与群に無作為に分けた。BNP500mg/kgを照射前1日及び照射直後にマウスの腹腔内(i.p.)に投与し、放射線増強効果を確認した(それぞれ、GP3及びGP4)。照射条件は、10Gy、150kV、20mA、Alフィルトレーション、330mm間隔に設定した。
サンプル投与群
GP1:がん対称群
GP2:がん+照射(IR:10Gy)群
GP3:BNP 500mg/kg (照射前1日)群
GP4:BNP 500mg/kg (照射後0日)群
BNP投与群でも非投与群と同様に体重変化がなく、毒性が見られない。
がんの体積=0.52×長さ×幅2
結果を図30に示す。t-検定は、試験8(2)に同じ。
10Gy照射群で腫瘍成長抑制効果があり、X線照射前及び後にBNPを投与しても8日後の腫瘍サイズはBNP非投与群に比較して有意に小さく、放射線増強効果が確認される。
上記試験と同様に入試した、一群5又は7匹の5-7週令のC57BL/6Jマウスを、同様の条件下で飼育した。100μL(血清不含DMEM)当たり0.076×106のメラノーマB16F10細胞をマウスの右腿外側部に皮下注射した(照射前9日目)。がんの体積が350-560mm3になったとき、マウスを下記投与群に無作為に分けた。照射条件は、10Gy、150kV、20mA、Al+Cu(0.5mm+0.1mm)フィルトレ―ション、330mm間隔に設定した。
がん体積は上記と同様に算出した。
サンプル投与群
GP1:健康(生理食塩水)群(n=5)
GP2:がん対照群(n=7)
GP3:がん+照射(IR(5Gy))群(n=7)
GP4:酪酸(i.p.;250mg/kg)(照射前6時間)+IR群(n=7)
GP5:酪酸(i.p.;500mg/kg)(照射前24時間)+IR群(n=7)
GP6:BNP(i.p.:500mg/kg)(照射前6時間)+IR群(n=7)
GP7:BNP(i.p.:500mg/kg)(照射前12時間)+IR群(n=7)
放射線照射前に酪酸及びBNPを投与した。腫瘍増殖抑制効果は 照射群<6時間前酪酸投与群<6時間前BNP投与群=24時間前酪酸投与群<24時間前BNP投与群の順に増加した。
マウスメラノーマB16F10細胞は、Cell Bank(理研、日本)から購入した。これらの細胞株を、10%ウシ胎児血清及び100ng/mLのペニシリン-ストレプトマイシン-ネオマイシンの抗生物質混合物を補充したダルベッコ改変イーグル培地(DMEM;L-グルタミン、1g/L グルコース、重炭酸ナトリウム、Sigma-Aldrich,St Louis, MO, USA)中に5%CO2の加湿雰囲気下に37℃で保持した。結果を図34に示す。
BNP投与群で明らかにスフェロイドがん細胞の成長抑制効果が確認される。
42匹の5週齢C57BL/6Jマウス(オス)にEPS益新(株)より購入した固形飼料A06071302(コリン欠乏高脂肪飼料、メチオニン減量、0.1%メチオニン添加)を自由摂取にて与え、4週間後に無作為に1群7匹に分け、下記の健康群(Healthy)(固形飼料A06071302無投与)、NASH、酪酸投与(BA)、プロピオン酸投与(PA)、PNP投与、BNP投与6群に記載の各サンプルを(PA及びPNP群はPAが65mM、BAおよびBNP群はBAが50mMの濃度に調製)自由摂取にて投与した。8週間後にデータ解析を行った。
ここでは、肝臓に蓄積した脂肪量の違いと肝臓での炎症に呼応した脾臓の腫大の程度を比較するために、マウスの解剖後に取り出した肝臓および脾臓の重量を測定し、各群の平均重量を求めた。(各群n=7)。各群の平均肝臓重量値および平均脾臓重量値のエラーバーは、標準偏差値(各群n=7)を用いた。t-検定は、平均値間の統計的有意差の有無を調べるために行われ、P<0.05で統計的に有意差がある。
解剖後取り出されたマウスの肝臓は、速やかに10%中性緩衝ホルマリン液に入れて1日間浸漬することによって固定した。その後、パラフィン包埋するために70%エタノール溶液に置換した。パラフィン包埋後すべての肝臓は、厚さ5μmの組織切片に加工され、ヘマトキシリン・エオジン(HE)染色された。染色後のすべての組織切片は、顕微鏡(オールインワン蛍光顕微鏡、BZ-X710,Keyence)によって画像データ化された後、ImageJ(NIH)によって肝臓組織面積に対する油滴組織面積の割合が求められた(各群n=7)。結果を図36に示す。グラフは各群の油滴組織面積の平均値及び標準偏差によるエラーバーを示したものである。t-検定は、平均値間の統計的有意差の有無を調べるために行われ、P<0.05で統計的に有意差がある。
肝臓の油滴量は健康群に対してNASH群が大幅に増加している(脂肪肝状態)。一方PNP投与群はNASH群に比較して油滴量が有意に少ない。
解剖後取り出されたマウスの肝臓は、速やかに10%中性緩衝ホルマリン液に入れて1日間浸漬することによって固定した。その後、パラフィン包埋するために70%エタノール溶液に置換した。パラフィン包埋後すべての肝臓は、厚さ5μmの組織切片に加工され、マッソントリクローム(MT)染色された。染色後のすべての組織切片は、顕微鏡(オールインワン蛍光顕微鏡、BZ-X710,Keyence)によって画像データ化された後、Image J(NIH)によって肝臓組織面積に対する線維化組織面積の割合が求められた(各群n=7)。結果を図42に示す。グラフは各群の線維化組織面積の平均値及び標準偏差によるエラーバーを示したものである。T-検定は、平均値間の統計的有意差の有無を調べるために行われ、p<0.05で統計的に有意差がある。
肝線維化量は健康群に対してNASH群が有意に多い。一方PNP投与群はNASH群に比較して肝線維化量が有意に少ない。
製造例2(本願)で合成したN717と同様にして合成したN817(1.5g)、アゾビスイソブチロニトリル(45mg)、4-フェニル酪酸ビニル(2g)をフラスコに加え、5分間窒素バブルしたのち60°C、1日反応させた。得られた目的物をTHFに溶解させ、イソプロピルアルコール(IPA)に沈殿、減圧乾燥し目的物(N821)を得た(2.8g)。N821の1H NMRスペクトルを図38に示す。
製造例9で合成したポリマー(NN821)をそれぞれ50mg採取し、1mLのDMFに溶解させ水を1mL加えて透析膜(MWCO=3.5KDa)に入れて2Lの水に対して透析した。半日ごとに3度透析水を交換した後、動的光散乱測定を行い、平均67nmの粒子が形成していることが確認できた。動的散乱測定の結果である、PEG-b-ポリ(ビニル4-フェニル酪酸)ナノ粒子(Ph-BNP,N832)のサイズ分布を図44に示す。
24匹の6週齢C57BL/6Nマウス(オス)をランダムに4群にわけ、4日間に渡ってゾンデによりサンプルを経口投与(1日1回、1.22mmol-4PBA/kg)した。投与群2GP-4GPにおいては、4日目にアセトアミノフェン(アセチル-p-アミノフェノール;APAP;300mg/kg)を腹腔投与することで急性肝障害及び高アンモニア血症を引き起こし、5日目に解剖し評価した。
サンプル投与群:
1GP: 生理食塩
2GP: APAP+水
3GP: APAP+4-フェニル酪酸(200mg/kg,1.22mmol-4PBA/kg)
4GP: APAP+Ph-BNP(200mg/kg,1.22mmol-4PBA/kg)
試験開始5日目の心採血直後に血中アンモニア濃度、肝機能指標として血漿アスパラギン酸アミノトランスフェラーゼ(AST)、血漿アラニンアミノトランスフェラーゼ(ALT)レベルをそれぞれ、比色法スライドを用いて動物用生化学自動分析装置で測定した。結果(APAP急性肝障害モデルに対するPh-BNPの経口投与効果)を、図40に示す。
図より、4-Ph-BNPが有意に血中アンモニア濃度を下げ、また、AST、ALTレベルも有意に低下し、肝機能が回復に寄与していることが分かる。
解剖後取り出されたマウスの肝臓を、前述した器官又は臓器のHE染色法に従い、染色した。その結果を図41に示す。図より、APAP投与で肝臓に強く障害が現れているものの、Ph-BNPでダメージが抑制されていることが分かる。図中、Healthyは健康群マウス、APAP投与群マウス、APAP+PBAは、APAPと4-フェニル酪酸の投与群、APAP+Ph-BNPは、APAPとPh-BNP(本発明に従うナノ粒子)の投与群に相当する。
上述の製造例1~8の方法に準じ、該当する改変を常法に従い行い、ベンゼン環をPEGのα末端に有するPEG-b-ポリ(ビニル酪酸)(下式左参照。)及びPEG-b-ポリ(ビニル4-フェニル酪酸)(下式右参照。)のフェニル基にクロラミン法で125Iを導入し、PD-10カラムにて2回精製、未反応ヨウ素を分別した。
N932を給水瓶から自由摂取させたマウスを24時間後、血液、肝臓および消化管を採取し、そのガンマ線強度をシンチレーション検出器により測定した。結果を、図42(左)に示す。図より、N932は消化管にほぼ完全に局在化することが確認された。
45匹の7週齢ICRマウス(オス)をランダムに以下の3群にわけ、投与群:2GPと3GPの投与量について、含まれるフェニル酪酸が200mg/kg(1.22mmol-4PBA/kg)となるように決定した。各サンプルをほぼ同時に全マウスに投与後、各エンドポイント(30min,1h,2h,4h,12h,16h,24hの7つのエンドポイント)に従い、心臓穿刺によって血液1mL取り、血漿を分離させる。また、マウスからターゲット臓器の肝臓を取り出し、高速液体クロマトグラフィー/質量分析法(LC/MS)によりフェニル酪酸モノマーの含有量を定量化した。測定結果を図43に示す。これらの図より、PBAは4時間以内に完全に体内から代謝されたのに対して、4-Ph-BNPは血中及び肝臓において持続的にフェニル酪酸モノマーを放出させ、24時間経過時点でもその放出は終わっていなかった。また、濃度時間曲線化面積(AUC)を計算しても、血液においては、4-Ph-BNPはPBAの約3倍、肝臓においては約15倍の増加を見せた。
サンプル投与群:
1GP: 生理食塩 (コントロール、3匹)
2GP: 4-フェニル酪酸 (30min,1h,2h,4h,12h,16h,24hの7つのエンドポイント×3匹)
3GP: Ph-BNP (30min,1h,2h,4h,12h,16h,24hの7つのエンドポイント×3匹)
Claims (10)
- 親水-疎水性共重合体であって、
(1)式I:
式中、
Rは、-(C=O)R1又は水素原子であり、R1は、非置換又は置換された炭素原子数1~7個の直鎖又は分岐のアルキル(置換された場合の置換基は非置換若しくは置換されたフェニルであり、置換されたフェニルの置換基は、1以上のハロゲン、ヒドロキシル、メチルオキシである。)であり、ここで、水素原子は存在するとしてもnの30%以下であり、nは5~1000の整数である、
で表される、反復単位に由来する疎水性セグメント、と
(2)ポリ(エチレングリコール)鎖を含む親水性セグメントであって、
(i)式IIa:
式中、Aは、非置換または置換C1-C12アルキルオキシであり、置換されている場合の置換基は、ホルミル基、式R’R”CH-基、又はフェニルアミノ基若しくはフェネチルアミノ基であり、ここで、R’及びR”は独立してC1-C4アルキルオキシ又はR’とR”は一緒になって-OCH2CH2O-、-O(CH2)3O-もしくは-O(CH2)4O-であり、mは10~500の整数である,で表される、親水性セグメント、又は
(ii)式IIb:
式中、Raは水素原子又はカルボキシ基であり、
XはRaがカルボキシ基であるとき、C(=O)O若しくはC(=O)NHであるか、又はRaが水素原子であるとき、O若しくはNHであり、
Bは、A-CH2CH2であって、A及びmはそれぞれ、上記定義のとおりであり、
yは1~300の整数である、
で表される反復単位に由来する親水性セグメント、
とを含み、前記(1)の疎水性セグメントと、(2)(i)の親水性セグメントは、それぞれブロックとして存在し、
前記(1)の疎水性セグメントと、(2)(ii)の親水性セグメントを含むそれぞれの反復単位の各構成員は、相互にランダムに存在する、
親水-疎水性共重合体。 - 水中で会合して自己組織化することによりナノ粒子又はナノサイズの高分子ミセルを形成する、請求項1に記載の親水-疎水性共重合体。
- 請求項1又は2に記載の親水-疎水性共重合体であって、
前記(1)の式Iで表される反復単位に由来する疎水性セグメントと前記(2)(i)の式IIaの親水性セグメントを含む共重合体は、式BC:
式中、A、R、m、nはそれぞれ、上記定義のとおりであり、L1は直接結合又は二価の連結基を表し、Zは、水素原子、SH、S(C=S)-Ph、S(=S)OCH2CH3、ヒドロキシル基、C1-C6アルキルオキシ基又はアリール-C1-C2アルキルオキシ基である、
で表されるブロック共重合体であり、
前記(1)の式Iで表される反復単位に由来する疎水性セグメントと前記(2)(ii)の式IIbの親水性セグメントを含む共重合体は、式RC:
式中、R、Ra、B、X、m、n、yはそれぞれ、上記定義のとおりである、
で表されるグラフト共重合体である、
親水-疎水性共重合体。 - 請求項1~3のいずれかに記載の親水-疎水性共重合体の水性媒体中で形成されるナノ粒子。
- 請求項1~3のいずれかに記載の親水-疎性共重合体又は請求項4に記載のナノ粒子を有効成分として含んでなる、製薬学的製剤。
- がんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療(若しくは肝線維化の抑制)、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療に使用するための請求項5の製薬学的製剤。
- がんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療に使用するための請求項1~3のいずれかの親水-疎水性共重合体。
- がんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療(若しくは肝線維化の抑制)、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療に使用するための請求項4のナノ粒子。
- 請求項1~3のいずれかの親水-疎水性共重合体を、それらを必要とする患者に投与してがんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療(若しくは肝線維化の抑制)、糖尿病の予防若しくは治療、放射線療法における放射線の増強、又は、高アンモニア血症の予防若しくは治療するための方法。
- 請求項4のナノ粒子を、それらを必要とする患者に投与してがんの予防若しくは治療、肥満抑制、潰瘍性大腸炎、非アルコール性脂肪肝の予防若しくは治療、糖尿病の予防若しくは治療(若しくは肝線維化の抑制)、放射線療法における放射線の増強、肝線維化の抑制、又は、高アンモニア血症の予防若しくは治療するための方法。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2020324649A AU2020324649A1 (en) | 2019-08-05 | 2020-07-30 | Hydrophilic-hydrophobic copolymer carrying short-chain fatty acid ester |
| US17/631,593 US20220332876A1 (en) | 2019-08-05 | 2020-07-30 | Hydrophilic-hydrophobic copolymer carrying short chain fatty acid ester |
| CA3152003A CA3152003A1 (en) | 2019-08-05 | 2020-07-30 | Hydrophilic-hydrophobic copolymer carrying short chain fatty acid ester |
| CN202080069272.0A CN114430756A (zh) | 2019-08-05 | 2020-07-30 | 担载短链脂肪酸酯的亲水-疏水性共聚物 |
| JP2021537269A JP7548586B2 (ja) | 2019-08-05 | 2020-07-30 | 短鎖脂肪酸エステルを担持する親水-疎水性共重合体 |
| EP20848934.4A EP4011444A4 (en) | 2019-08-05 | 2020-07-30 | HYDROPHILIC-HYDROPHOBIC COPOLYMER WITH SHORT-CHAIN FATTY ACID ESTERS |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019-143619 | 2019-08-05 | ||
| JP2019143619 | 2019-08-05 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021024906A1 true WO2021024906A1 (ja) | 2021-02-11 |
Family
ID=74503809
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/029239 WO2021024906A1 (ja) | 2019-08-05 | 2020-07-30 | 短鎖脂肪酸エステルを担持する親水-疎水性共重合体 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20220332876A1 (ja) |
| EP (1) | EP4011444A4 (ja) |
| JP (1) | JP7548586B2 (ja) |
| CN (1) | CN114430756A (ja) |
| AU (1) | AU2020324649A1 (ja) |
| CA (1) | CA3152003A1 (ja) |
| WO (1) | WO2021024906A1 (ja) |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0616747A (ja) * | 1992-06-29 | 1994-01-25 | Kuraray Co Ltd | 分散安定剤および水性分散液 |
| JPH0616752A (ja) * | 1992-04-16 | 1994-01-25 | Huels Ag | 水性プラスチック分散液の製造方法 |
| JP2007185494A (ja) * | 2005-11-29 | 2007-07-26 | Cordis Corp | 両親媒性コポリマー組成物 |
| WO2009133647A1 (ja) | 2008-05-02 | 2009-11-05 | 国立大学法人筑波大学 | 高分子化環状二トロキシドラジカル化合物およびその使用 |
| WO2016052463A1 (ja) | 2014-09-30 | 2016-04-07 | 国立大学法人筑波大学 | ポリ(エチレングリコール)-b-ポリ(ハロメチルスチレン)並びにその誘導体及び製造方法 |
| WO2018135592A1 (ja) * | 2017-01-19 | 2018-07-26 | 国立大学法人筑波大学 | 側鎖に環状ニトロキシドラジカルとトリアルコキシシリルを含む共重合体およびその使用 |
| JP2019001786A (ja) * | 2017-06-19 | 2019-01-10 | 国立大学法人 筑波大学 | 感染症治療薬 |
| WO2019208617A1 (ja) * | 2018-04-27 | 2019-10-31 | 国立大学法人筑波大学 | ソラフェニブの経口デリバリー用組成物及びその使用 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1231905B1 (en) * | 1999-11-15 | 2009-04-08 | BioCure, Inc. | Responsive polymeric hollow particles |
| JP7136807B2 (ja) * | 2017-04-17 | 2022-09-13 | ザ・ユニバーシティ・オブ・シカゴ | ヒトの健康及び疾患の治療用途向けの短鎖脂肪酸の腸への送達用ポリマー材料 |
-
2020
- 2020-07-30 AU AU2020324649A patent/AU2020324649A1/en active Pending
- 2020-07-30 JP JP2021537269A patent/JP7548586B2/ja active Active
- 2020-07-30 US US17/631,593 patent/US20220332876A1/en active Pending
- 2020-07-30 WO PCT/JP2020/029239 patent/WO2021024906A1/ja unknown
- 2020-07-30 EP EP20848934.4A patent/EP4011444A4/en active Pending
- 2020-07-30 CA CA3152003A patent/CA3152003A1/en active Pending
- 2020-07-30 CN CN202080069272.0A patent/CN114430756A/zh active Pending
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0616752A (ja) * | 1992-04-16 | 1994-01-25 | Huels Ag | 水性プラスチック分散液の製造方法 |
| JPH0616747A (ja) * | 1992-06-29 | 1994-01-25 | Kuraray Co Ltd | 分散安定剤および水性分散液 |
| JP2007185494A (ja) * | 2005-11-29 | 2007-07-26 | Cordis Corp | 両親媒性コポリマー組成物 |
| WO2009133647A1 (ja) | 2008-05-02 | 2009-11-05 | 国立大学法人筑波大学 | 高分子化環状二トロキシドラジカル化合物およびその使用 |
| WO2016052463A1 (ja) | 2014-09-30 | 2016-04-07 | 国立大学法人筑波大学 | ポリ(エチレングリコール)-b-ポリ(ハロメチルスチレン)並びにその誘導体及び製造方法 |
| WO2018135592A1 (ja) * | 2017-01-19 | 2018-07-26 | 国立大学法人筑波大学 | 側鎖に環状ニトロキシドラジカルとトリアルコキシシリルを含む共重合体およびその使用 |
| JP2019001786A (ja) * | 2017-06-19 | 2019-01-10 | 国立大学法人 筑波大学 | 感染症治療薬 |
| WO2019208617A1 (ja) * | 2018-04-27 | 2019-10-31 | 国立大学法人筑波大学 | ソラフェニブの経口デリバリー用組成物及びその使用 |
Non-Patent Citations (2)
| Title |
|---|
| See also references of EP4011444A4 |
| TAKASHI SAKATAHIROHUMI ICHIKAWA: "Physiological Actions of Short-Chain Fatty Acids", JOURNAL OF JAPAN OIL CHEMISTS' SOCIETY, vol. 46, 1997, pages 1205 - 1212 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20220332876A1 (en) | 2022-10-20 |
| CN114430756A (zh) | 2022-05-03 |
| EP4011444A1 (en) | 2022-06-15 |
| JP7548586B2 (ja) | 2024-09-10 |
| AU2020324649A1 (en) | 2022-03-17 |
| EP4011444A4 (en) | 2023-10-25 |
| JPWO2021024906A1 (ja) | 2021-02-11 |
| CA3152003A1 (en) | 2021-02-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5525814B2 (ja) | 20(R)−人参サポニン(ジンセノサイド)Rg3薬用組成物水溶液の調製方法 | |
| EP1773450B1 (fr) | Combinaisons therapeutiques | |
| EP3031456A1 (en) | Application of andrographolide in the preparation of a pharmaceutical for treatment of inflammatory bowel disease, andrographolide enteric targeting micropellet, and method for preparation thereof | |
| US20160008385A1 (en) | Adrenomedullin production enhancer | |
| US20070141173A1 (en) | Medicament comprising noble metal fine particles | |
| US20240261349A1 (en) | Pharmaceutical Complex for Radioprotection, Preparation Method, and Applications thereof | |
| JPH10130153A (ja) | 大腸癌、食道癌及び乳癌より選ばれた癌に用いる 抗悪性腫瘍剤 | |
| WO2021024906A1 (ja) | 短鎖脂肪酸エステルを担持する親水-疎水性共重合体 | |
| EP3049074A1 (en) | Prodrugs of monomethyl fumarate (mmf) | |
| ZA200507289B (en) | Medical Drug Containing Fine Particle of Noble Metal | |
| JP5346360B2 (ja) | 塩分の吸収阻害作用をもつ血管保護剤 | |
| JP2009531379A (ja) | 鉄代謝機能障害を治療するためのストロビルリンの使用 | |
| Ahmad et al. | Leveraging thiol-functionalized biomucoadhesive hybrid nanoliposome for local therapy of ulcerative colitis | |
| CH665637A5 (fr) | 5-(3-n-butyloxalylaminophenyl)tetrazole comme agent antiasthmatique, composition le contenant et procede de preparation de la composition. | |
| WO2001010378A2 (en) | Controlled release from copolymers of acrylic or methacrylic acid/l-dopa, acrylic or methacrylic acid/l-$g(a)-methyl dopa, acrylic or methacrylic acid/carbidopa and their combinations | |
| CN116270549B (zh) | 一种靶向结肠炎的氧化苦参碱的纳米粒及其制备方法和应用 | |
| US12128023B2 (en) | Pharmaceutical composition containing B-lapachone as active ingredient for prevention or treatment of cholestatic liver disease | |
| US20230055593A1 (en) | Pharmaceutical composition containing b-lapachone as active ingredient for prevention or treatment of cholestatic liver disease | |
| RU2715679C1 (ru) | Способ снижения прооксидантного действия антиконвульсантов в эксперименте | |
| CN116478430A (zh) | 一种具有过氧化氢敏感性的共价环糊精骨架及其制备方法 | |
| CN108530309B (zh) | 一种富勒烯衍生物及其制备方法和其在化疗保护中的应用 | |
| TWI527828B (zh) | 新穎的三萜化合物及其用途 | |
| CN116407554A (zh) | 降低靶向抗肿瘤药物对肠道损伤的药物及其应用 | |
| WO2013007383A1 (en) | Use of lipoteichoic acid in the treatment of cancer in an inflammatory state |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20848934 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2021537269 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 3152003 Country of ref document: CA |
|
| ENP | Entry into the national phase |
Ref document number: 2020848934 Country of ref document: EP Effective date: 20220307 |
|
| ENP | Entry into the national phase |
Ref document number: 2020324649 Country of ref document: AU Date of ref document: 20200730 Kind code of ref document: A |