WO2017131242A1 - 細胞内物質移送システムおよびその利用 - Google Patents
細胞内物質移送システムおよびその利用 Download PDFInfo
- Publication number
- WO2017131242A1 WO2017131242A1 PCT/JP2017/003880 JP2017003880W WO2017131242A1 WO 2017131242 A1 WO2017131242 A1 WO 2017131242A1 JP 2017003880 W JP2017003880 W JP 2017003880W WO 2017131242 A1 WO2017131242 A1 WO 2017131242A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- nanoparticles
- general formula
- group
- represented
- site
- Prior art date
Links
- 0 *c1ccc(C[Tc])cc1C(F)F Chemical compound *c1ccc(C[Tc])cc1C(F)F 0.000 description 3
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6925—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a microcapsule, nanocapsule, microbubble or nanobubble
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/24—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing atoms other than carbon, hydrogen, oxygen, halogen, nitrogen or sulfur, e.g. cyclomethicone or phospholipids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/34—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyesters, polyamino acids, polysiloxanes, polyphosphazines, copolymers of polyalkylene glycol or poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6923—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being an inorganic particle, e.g. ceramic particles, silica particles, ferrite or synsorb
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/99—Enzyme inactivation by chemical treatment
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
Abstract
Description
関連出願の相互参照
本出願は、2016年1月29日出願の日本特願2016−15760号の優先権を主張し、その全記載は、ここに特に開示として援用される。
さらに本発明は、薬剤を効率良くエンドリソソームに運搬する上記システムを利用して、細胞膜内の酵素、例えば、キナーゼ等に対する活性物質(例えば、阻害剤)を送達するシステムを提供することを目的とする。
加えて本発明は、このようなシステムを利用した抗ガン剤を提供することも目的とする。
[1]
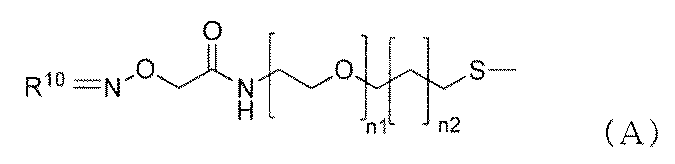
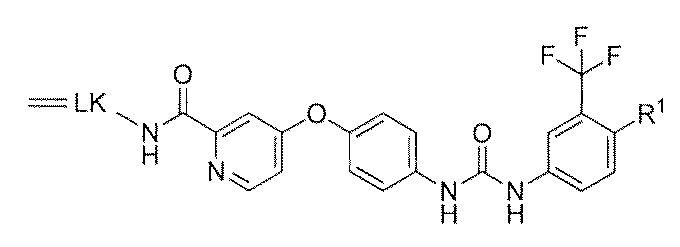
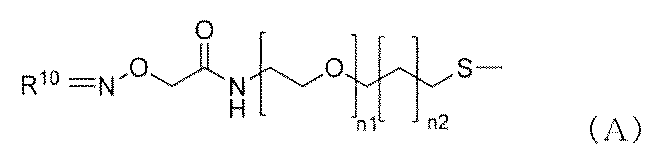
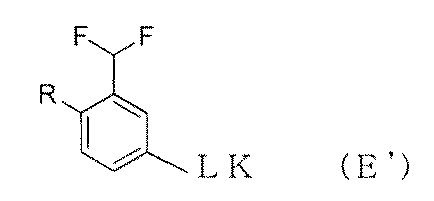
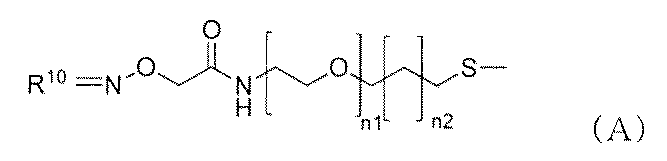
ナノ粒子及び前記ナノ粒子の表面に担持された下記一般式(A)で示されるリソソーム酵素阻害剤又はキナーゼ阻害剤及び下記一般式(B)で示されるリン脂質疑似物質を含む複合体。
[2]
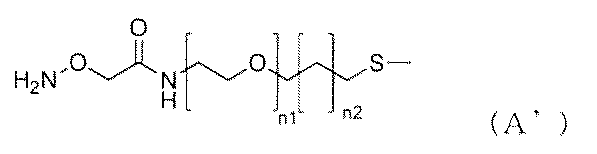
ナノ粒子の表面に下記一般式(A’)で示される物質がさらに担持された[1]に記載の複合体。
[3]
一般式(A)、(B)及び(A’)において、n1とn2の合計はn3以上である、[1]又は[2]に記載の複合体。
[4]
自殺基質部位は、リソソーム酵素の活性中心と反応性を有する基(以下、反応性基)を含む、[1]~[3]のいずれかに記載の複合体。
[5]
自殺基質部位は、
N−アセチル−D−グルコサミン残基、N−アセチル−D−グガラクトサミン残基、ガラクトース残基、グルコース残基、フコース残基、マンノース残基、及びシアル酸残基、から成る群から選ばれる少なくとも1種の糖残基、並びにジフルオメチルアリール基、及びトリフルオメチルアリール基から成る群から選ばれる少なくとも1種の反応性基を有する[4]に記載の複合体。
[6]
自殺基質部位は、下記官能基を含む[4]に記載の複合体。
[7]
自殺基質部位は、下記式で示されるいずれかの官能基を含む[4]~[6]のいずれかに記載の複合体。
キナーゼ阻害部位は、キナーゼと反応性を有する基(以下、細胞膜キナーゼ反応性基)を含む、[1]~[3]のいずれかに記載の複合体。
[9]
キナーゼ阻害部位は、下記式で示されるいずれかの官能基を含む[8]に記載の複合体。
[10]
キナーゼ阻害部位は、下記式で示される官能基を含む[8]又は[9]に記載の複合体。
一般式(A)で示されるリソソーム酵素阻害剤と一般式(B)で示されるリン脂質疑似物質のモル比率が1:100~10:1の範囲である、[1]~[1]0のいずれかに記載の複合体。
[12]
一般式(A)で示されるリソソーム酵素阻害剤と一般式(A’)で示される物質のモル比率が1:100~100:0の範囲である、[2]~[1]1のいずれかに記載の複合体。
[13]
前記ナノ粒子は、金属ナノ粒子又は半導体ナノ粒子である、[1]~[12]のいずれかに記載の複合体。
[14]
金属ナノ粒子は、金ナノ粒子、白金ナノ粒子、銀ナノ粒子、及び鉄磁性ナノ粒子から成る群から選ばれる少なくとも1種の粒子である[13]に記載の複合体。
[15]
半導体ナノ粒子は、量子ドットである[13]に記載の複合体。
[16]
前記ナノ粒子は、粒子径が0.1~100nmの範囲である[1]~[15]のいずれかに記載の複合体。
[17]
[1]~[16]のいずれかに記載の複合体を有効成分として含有する抗ガン剤。
[18]
前記抗ガン剤は、乳癌、前立腺癌、肝細胞癌、膵癌、大腸癌、卵巣癌、腎癌、肺癌、または脳腫瘍に対する抗ガン剤である[17]に記載の抗ガン剤。
[19]
[1]~16のいずれかに記載の複合体の製造方法であって、
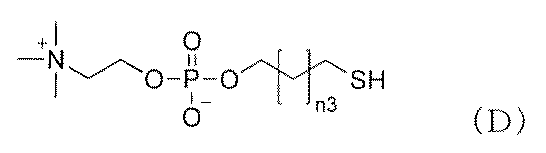
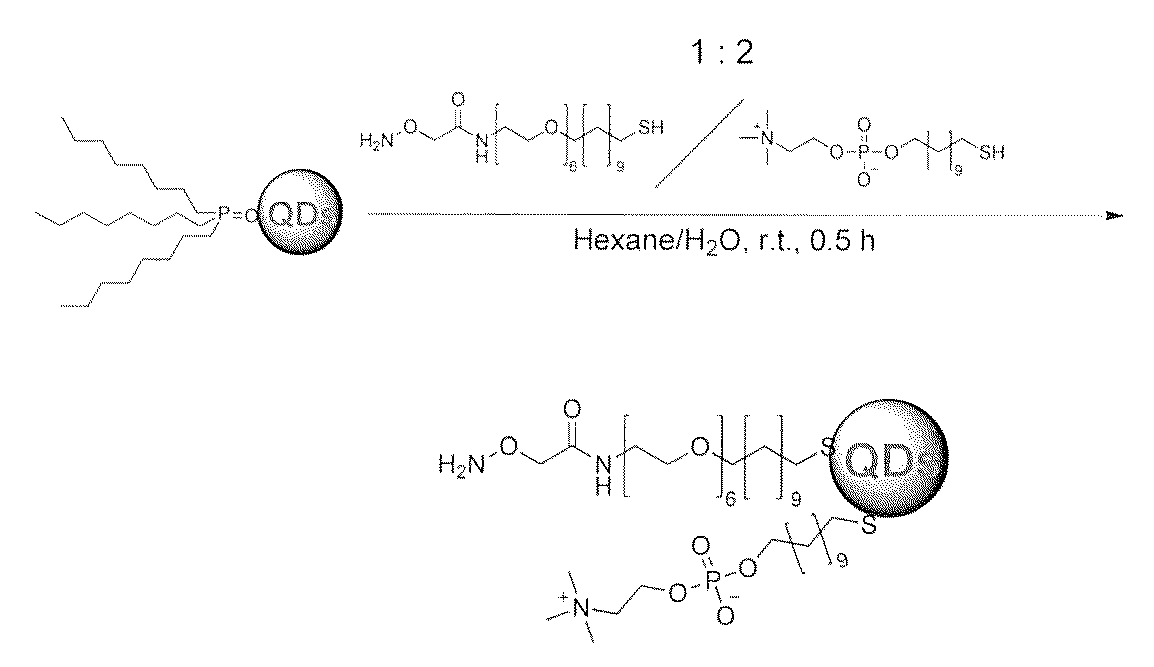
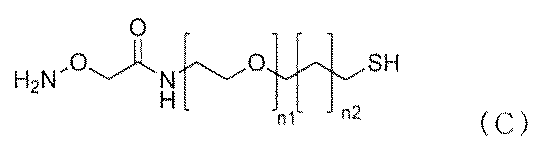
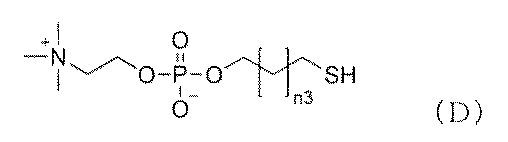
下記一般式(C)で示される阻害剤架橋前駆体X及び下記一般式(D)で示されるリン脂質疑似物質前駆体とコロイド状ナノ粒子とを混合して、ナノ粒子の表面に阻害剤架橋前駆体X及びリン脂質疑似物質を担持した表面修飾ナノ粒子を得る工程(1)、
得られた表面修飾ナノ粒子にリソソーム酵素阻害剤前駆体Y又はキナーゼ阻害剤前駆体Zを混合して、阻害剤架橋前駆体Xと連結させて下記一般式(A)で示されるリソソーム酵素阻害剤又はキナーゼ阻害剤を形成する、
但し、リソソーム酵素阻害剤前駆体Yは、リソソーム酵素の活性中心と反応性を有する基(以下、反応性基)を含む自殺基質部位を含み、
キナーゼ阻害剤前駆体Zはキナーゼと反応性を有する基を含むキナーゼ阻害部位を含む、
[1]~[16]のいずれかに記載の複合体を得る工程(2)、
を含む前記方法。
[20]
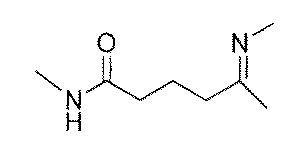
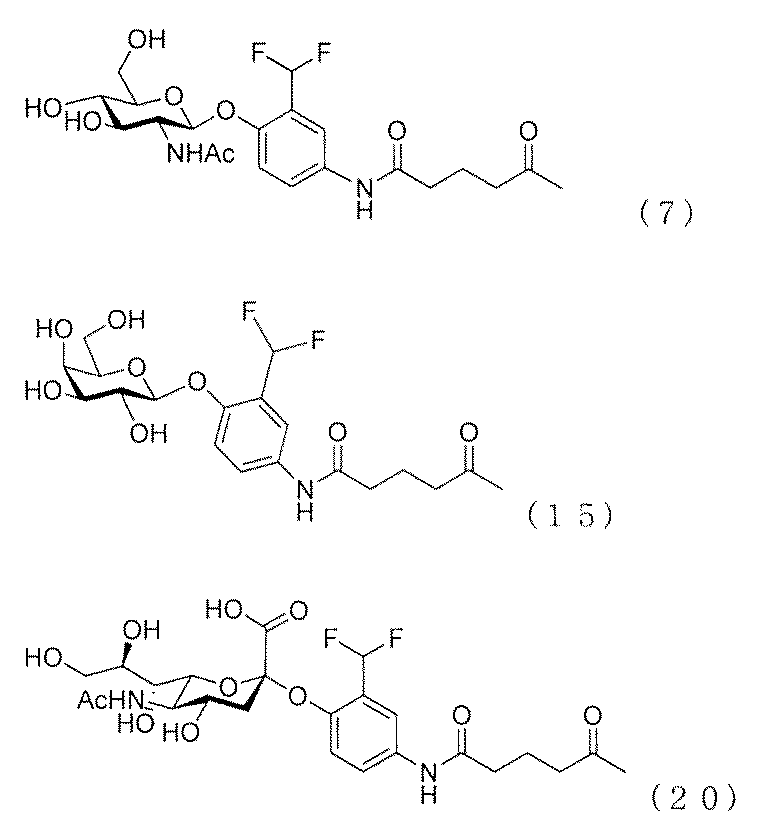
リソソーム酵素阻害剤前駆体Yが、下記式で示されるいずれかの化合物である[19]に記載の製造方法。
キナーゼ阻害剤前駆体Zが、下記式で示されるいずれかの化合物である[19]に記載の製造方法。
本発明は、ナノ粒子及び前記ナノ粒子の表面に担持された下記一般式(A)で示されるリソソーム酵素阻害剤又はキナーゼ阻害剤及び下記一般式(B)で示されるリン脂質疑似物質を含む複合体に関する。
本発明は、上記本発明の複合体の製造方法を包含する。この方法は、
下記一般式(C)で示される阻害剤架橋前駆体X及び下記一般式(D)で示されるリン脂質疑似物質前駆体とコロイド状ナノ粒子とを混合して、ナノ粒子の表面に阻害剤架橋前駆体X及びリン脂質疑似物質を担持して表面修飾ナノ粒子を得る工程(1)、
得られた表面修飾ナノ粒子にリソソーム酵素阻害剤Y又はキナーゼ阻害剤前駆体Zを混合して、阻害剤架橋前駆体Xと連結させて下記一般式(A)で示されるリソソーム酵素阻害剤又はキナーゼ阻害剤を形成する、本発明の複合体を得る工程(2)、
を含む。
一般式(C)で示される阻害剤架橋前駆体X及び一般式(D)で示されるリン脂質疑似物質前駆体とコロイド状ナノ粒子とを混合して、ナノ粒子の表面に阻害剤架橋前駆体X及びリン脂質疑似物質を担持して表面修飾ナノ粒子を得る工程である。
参考文献
A.T.Ohyanagi,et.al.,J.Am.Chem.Soc.2011,133,12507−12517(非特許文献2)
B.R.S.Tan,et.al.,ACS Chem.Biol.2015,10,2073−2086(非特許文献3)
工程(1)で得られた表面修飾ナノ粒子にリソソーム酵素阻害剤前駆体Y又はキナーゼ阻害剤前駆体Zを混合して、阻害剤架橋前駆体Xと連結させて一般式(A)で示されるリソソーム酵素阻害剤又はキナーゼ阻害剤を形成して、本発明の複合体を得る工程である。
本発明は、前記の複合体を有効成分として含有する抗ガン剤を包含する。本発明の抗ガン剤は、前記複合体を有効成分として含有するガン(癌、悪性腫瘍)の予防又は/及び治療用の医薬組成物であり、任意で医薬的に許容される担体をさらに含むことができる。前記ガンとしては、本発明の複合体の取込み効率が、正常細胞より桁違いに高いガン細胞に起因する物であれば、制限はなく、例えば、乳癌、前立腺癌、肝細胞癌、膵癌、大腸癌、卵巣癌、腎癌、肺癌、及び脳腫瘍などを挙げることができる。好ましくは、乳癌、肝細胞癌、膵癌、及び脳腫瘍である。
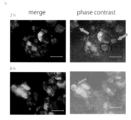
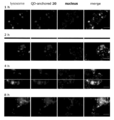
細胞内イメージング:ヒト乳癌細胞(MCF−7,P13,ATCCより入手)を5000cell/200μl/wellで播種し、D−MEM High glucose,10%fetal bovine serum(FBS)中、37℃,5%CO2の条件下で48時間インキュベートをした後に、化合物7を提示した蛍光性ナノ微粒子[10nMの化合物7担持型AO/PC SAM−QDs(AO/PC=1/2)]および比較物質としてのAO/PC SAM−QDs(AO/PC=1/2)を添加してその後の8時間までの細胞生育過程を観察した。細胞は以下の方法で染色した後に蛍光顕微鏡にて観察した。培地を除去した後、細胞をOpti−MEMで3回洗浄後LysoTracker R Green DND−26(200μl,5nM/Opti−MEM)を加えて37℃,5%CO2の条件下で30分インキュベートしてリソソームを染色した。その後Hoechst(2μl,0.1ng/μl/Opti−MEM)を加えて37℃,5%CO2雰囲気下でさらに15分間インキュベートして核を染色した後にOpti−MEMで3回洗浄してイメージングを行った(図2)。
MTAアッセイ法による死細胞の定量:MCF7細胞(5×103/100μl/well)を37℃、5%CO2雰囲気下で24時間インキュベートした後にそれぞれ90μlの培地に対してQD−anchored inhibitor 7(1μM,10μl/milli Q),QD control,(1μM,10μl/milli Q),compound 7(1μM,10μl/milli Q),cisplatin(1mM,10μl/milli Q)を加えて終濃度が100nM(ただしシスプラチンは100μM)となるように調整した。培養開始後96時間で培地成分により3回洗浄を行い、細胞培養液を10μl採取してCell Counting Kit−8 solution(Dojindo,Kumamoto,Japan)を加えて37℃、5%CO2雰囲気下で1.5時間インキュベートし450nmでの吸光度を測定することで細胞の生存率を定量した。
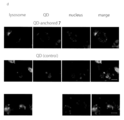
GFP発現細胞を用いたイメージング:ヒト乳癌細胞(MCF−7,P17,ATCCより入手)を5000cell/200μl/wellで播種し、D−MEM High glucose,10%fetal bovine serum(FBS)中、37℃、5%CO2雰囲気化で24時間インキュベートをした後に、CellLightTM Lysosomes−GFP *BacMam 2.0*(1μl 5000Cell/μl/medium)を添加してさらに24時間インキュベートしてリソソーム表面にGFPを発現させた。その後、化合物7を提示した蛍光性ナノ微粒子[10nMの化合物7担持型AO/PC SAM−QDs(AO/PC=1/2)]および比較物質としてのAO/PC SAM−QDs(AO/PC=1/2)を添加してその8時間後の細胞生育過程を観察した。細胞は以下の方法で染色した後に蛍光顕微鏡にて観察した。培地を除去した後、細胞をOpti−MEMで3回洗浄後Hoechest(200μl,0.001ng/μl/Opti−MEM)を加えて37℃,5%CO2雰囲気化で15分間インキュベートして核を染色した後にOpti−MEMで3回洗浄してイメージングを行った(図3d)。
1.M.Ichikawa et al.Bioorg.Med.Chem.Lett.2001,11,1769−1773
2.T.Ohyanagi,et.al.,J.Am.Chem.Soc.2011,133,12507−12517
3.R.S.Tan,et.al.,ACS Chem.Biol.2015,10,2073−2086
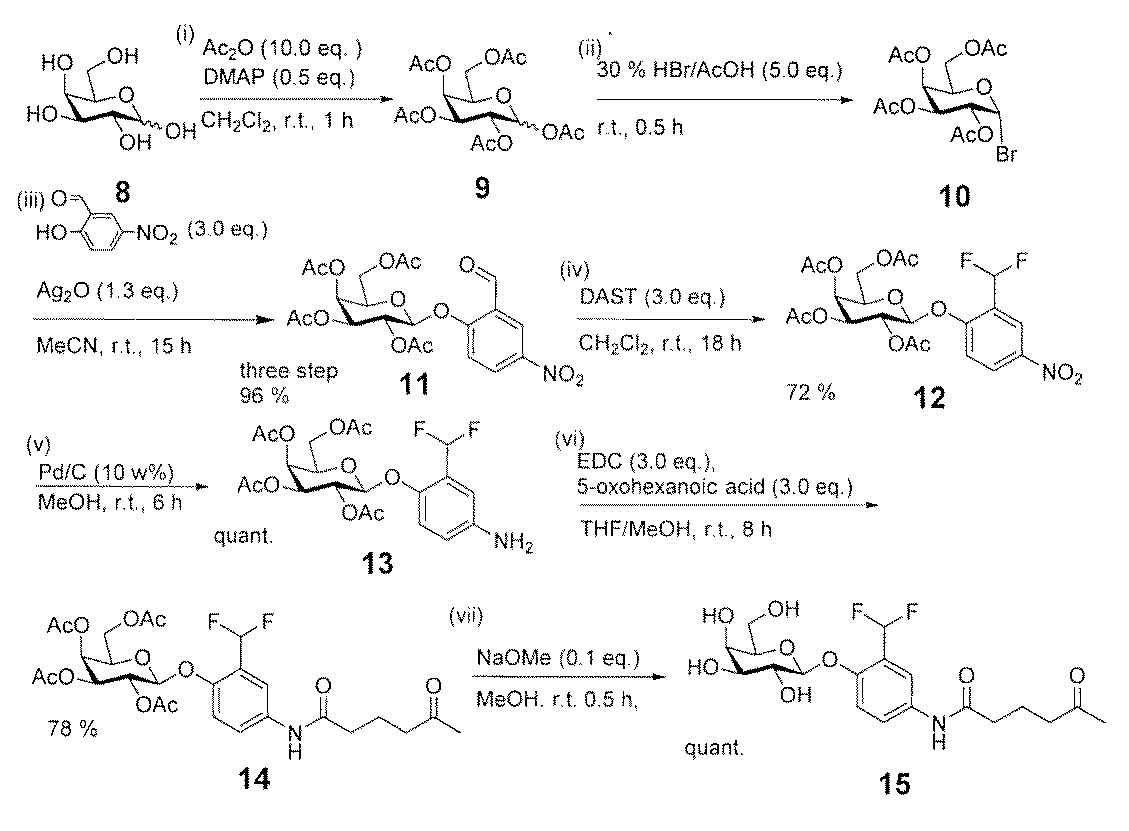
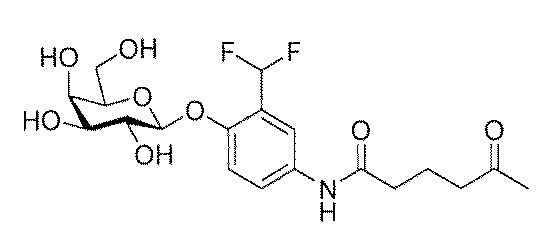
細胞内イメージング:ヒト乳癌細胞(MCF−7,P17,ATCCより入手)を5000cell/200μl/wellで播種し、D−MEM High glucose,10%fetal bovine serum(FBS)中、37℃,5%CO2雰囲気化で48時間インキュベートをした後に、化合物15を提示した蛍光性ナノ微粒子[10nMの化合物15担持型AO/PC SAM−QDs(AO/PC=1/2)]を添加してその後の8時間までの細胞生育過程を観察した。細胞は以下の方法で染色した後に蛍光顕微鏡にて観察した。培地を除去した後、細胞をOpti−MEMで3回洗浄後Lyso Tracker R Green DND−26(200μl,5nM/Opti−MEM)を加えて37℃,5%CO2の条件下で30分インキュベートしてリソソームを染色した。その後Hoechest(2μl,0.1ng/μl/Opti−MEM)を加えて37℃,5%CO2雰囲気化でさらに15分間インキュベートして核を染色した後にOpti−MEMで3回洗浄してイメージングを行った(図5)。図5化合物15を提示した蛍光性ナノ微粒子(10nM)の癌細胞内挙動:蛍光性ナノ微粒子の乳癌細胞(MCF−7)培養開始後(1~8時間)での細胞内動体(Scale bar size=50μm)。図5から、化合物15を提示した蛍光性ナノ微粒子が細胞内に取り込まれることが分かる。
MTTアッセイ法による死細胞の定量:MCF−7細胞(5×104/100ml/well)を37℃、5%CO2雰囲気化で24時間インキュベートした後にそれぞれ90mlの培地に対してQD−anchored inhibitor 15(1μM,10μl/milli Q)を加えて終濃度が100nM(ただしシスプラチンは100μM)となるように調整した。培養開始後96時間で培地成分により3回洗浄を行い、細胞培養液に対し10μlのCell Counting Kit−8(Dojindo,Kumamoto,Japan)を加えて37℃、5%CO2雰囲気化で1.5時間インキュベートし450nmでの吸光度を測定することで細胞の生存率を定量した。
1.M.Kurogochi,et al.,J.Biol.Chem.2004,279,44704−44712
2.T.Ohyanagi,et al.,J.Am.Chem.Soc.2011,133,12057−12517
3.R.S.Tan,et al.,ACS Chem.Biol.2015,10,2073−2086
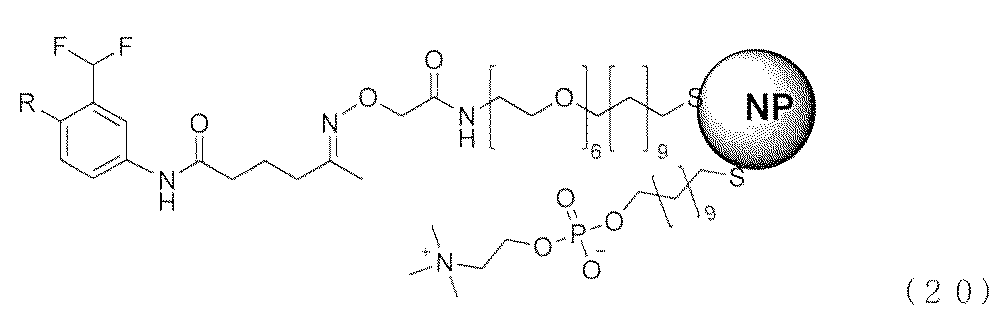
細胞内イメージング:ヒト乳癌細胞(MCF−7,P16,ATCCより入手)を5000cell/200μl/wellで播種し、D−MEM High glucose,10%fetal bovine serum(FBS)中、37℃,5%CO2雰囲気化で48時間インキュベートをした後に、化合物20を提示した蛍光性ナノ微粒子[10nMの化合物20担持型AO/PC SAM−QDs(AO/PC=1/2)]を添加してその後の8時間までの細胞生育過程を観察した。細胞は以下の方法で染色した後に蛍光顕微鏡にて観察した。培地を除去した後、細胞をOpti−MEMで3回洗浄後Lyso Tracker R Green DND−26(200μl,5nM/Opti−MEM)を加えて37℃,5%CO2の条件下で30分インキュベートしてリソソームを染色した。その後Hoechest(2μl,0.1ng/μl/Opti−MEM)を加えて37℃,5%CO2雰囲気化でさらに15分間インキュベートして核を染色した後にOpti−MEMで3回洗浄してイメージングを行った(図8)。図8.化合物20を提示した蛍光性ナノ微粒子(10nM)の癌細胞内挙動:蛍光性ナノ微粒子の乳癌細胞(MCF−7)培養開始後(1~8時間)での細胞内動体(Scale bar size=50μm)。図8から、化合物20を提示した蛍光性ナノ微粒子が細胞内に取り込まれることが分かる。
MTTアッセイ法による死細胞の定量:MCF−7細胞(5×104/100ml/well)を37℃、5%CO2雰囲気化で24時間インキュベートした後にそれぞれ90mlの培地に対してQD−anchored inhibitor 15(1μM,10μl/milli Q)を加えて終濃度が100nM(ただしシスプラチンは100μM)となるように調整した。培養開始後96時間で培地成分により3回洗浄を行い、細胞培養液に対し10μlのCell Counting Kit−8(Dojindo,Kumamoto,Japan)を加えて37℃、5%CO2雰囲気化で1.5時間インキュベートし450nmでの吸光度を測定することで細胞の生存率を定量した。
1.T.Ohyanagi,et al.,J.Am.Chem.Soc.2011,133,12057−12517
2.R.S.Tan,et al.,ACS Chem.Biol.2015,10,2073−2086
A:リソソーム酵素阻害剤を担持した蛍光性ナノ微粒子の細胞内イメージング
ヒト肝臓癌細胞(HepG2,P3,ATCCより入手)を5000cell/200ml/wellで播種し、D−MEM High glucose,10%fetal bovine serum(FBS)中、37℃、5%CO2雰囲気化で48時間インキュベートをした後に、化合物7、15、および20を担持したリン脂質被覆蛍光性ナノ微粒子溶液[10nMの阻害剤担持型AO/PC SAM−QDs(AO/PC=1/2)、既報(T.Ohyanagi,et al.,J.Am.Chem.Soc.2011,133,12057−12517)に従い調製した。]をそれぞれ添加して、共培養後8時間までの癌細胞生育過程を観察した。細胞は以下の方法で染色した後に蛍光顕微鏡によりイメージングした。以下にそのプロトコルの概要を示す。培地を除去した後、細胞をOpti−MEMで3回洗浄後Lyso Tracker R Green DND−26(200ml、5nM/Opti−MEM)を加えて37℃、5%CO2の条件下で30分インキュベートしてリソソームを染色した。その後Hoechest(2ml,0.1ng/ml/Opti−MEM)を加えて37℃、5%CO2雰囲気化でさらに15分間インキュベートして核を染色した後にOpti−MEMで3回洗浄して蛍光顕微鏡によりそれぞれを観察・イメージングした(図10)。
HepG2細胞(5×104/100ml/well)を37℃、5%CO2雰囲気化で24時間インキュベートした後にそれぞれ90mlの培地に対して化合物7、15、および20(milliQに溶解して1mMとした溶液の10ml)を加えて終濃度が100nMとなるように調整した。共培養開始後96時間で培地成分により3回洗浄を行い、細胞培養液に対し10mlのCell Counting Kit−8(Dojindo,Kumamoto,Japan)を加えて37℃、5%CO2雰囲気下で1.5時間インキュベートし450nmでの吸光度を測定することで細胞の生存率を定量した。対照薬として100nM 5−fluorouracil溶液(5−FU)を用いた(図11)。
C:リソソーム酵素阻害剤7および15を担持した蛍光性ナノ微粒子の抗腫瘍効果(IC 50 の決定)
化合物(非可逆的反応機構による糖分解酵素阻害剤)の合成法に関連する文献
1.M.Ichikawa,et al.Bioorg.Med.Chem.Lett.2001,11,1769−1773.
2.M.Kurogochi,et al.,J.Biol.Chem.2004,279,44704−44712.
3.H.Hinou,et al.Biochemistry 2005,44,11669−11675.
リン脂質単分子膜被覆量子ドット(生体膜模倣蛍光性ナノ微粒子)の作製法と性質に関連する文献
4.T.Ohyanagi,et al.,J.Am.Chem.Soc.2011,133,12057−12517.
5.R.S.Tan,et al.,ACS Chem.Biol.2015,10,2073−2086.
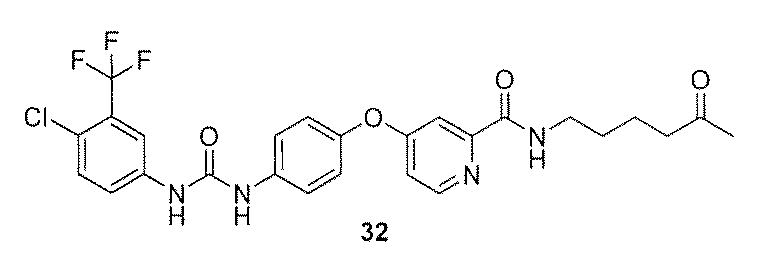
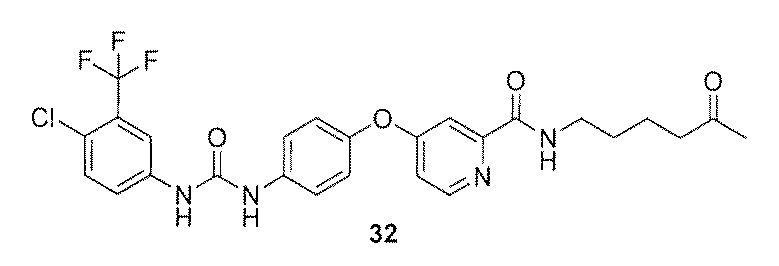
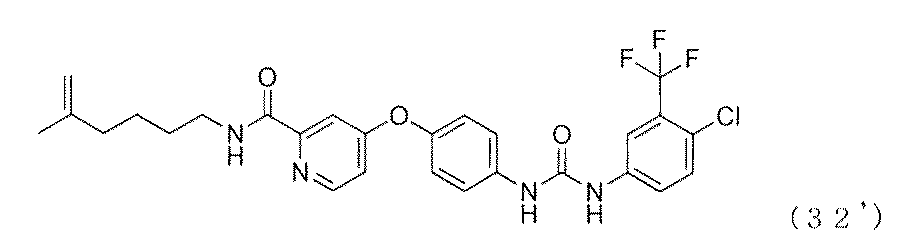
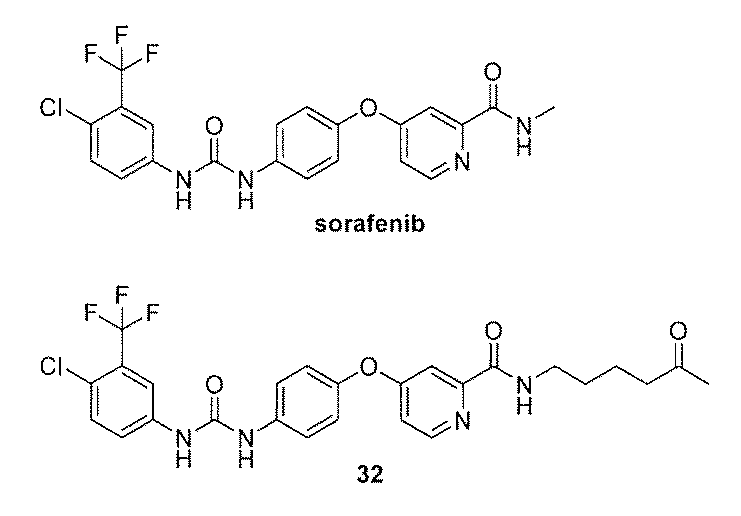
A:新規ソラフェニブ誘導体(32)の合成
肝細胞癌および腎細胞癌の治療薬であるソラフェニブは疎水性構造が原因で癌患者の血液中ではそのほとんどが血清アルブミンやa1−酸性タンパク質と非特異的に吸着するため、癌組織(癌細胞)への取り込み効率が著しく低いことが明らかとなっている。このため標的キナーゼ群を発現する培養癌細胞による実験で見られたようなIC50=4.5mMレベルの有意な抗腫瘍活性が、実際には疾患モデル動物や患者に対するin vivoの実験系においては充分発揮できていない可能性が高いことが最近指摘されている(Smith,M.A.and Hougton,P.Clin.Cancer Res.2013,19,2828−2833)。
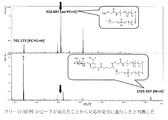
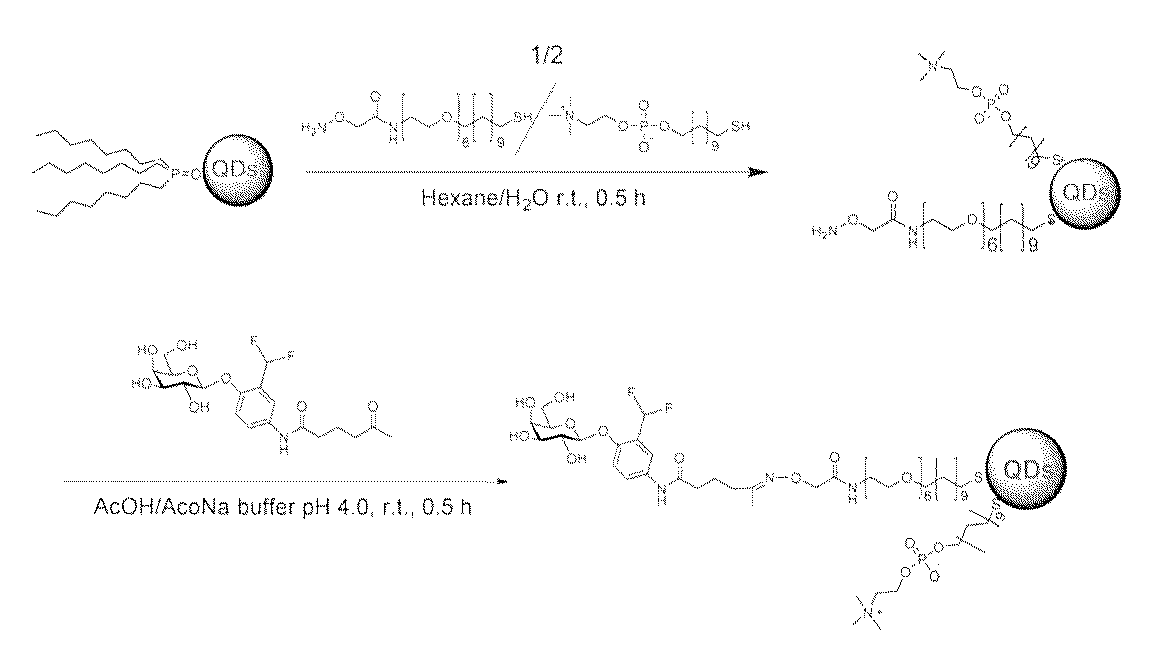
既報(T.Ohyanagi,et al.,J.Am.Chem.Soc.2011,133,12057−12517)に従い、TOPO−QDs(1mM,50ml/octane)に対しMeOH(50ml)、i−PrOH(100ml)を加えて遠心によりナノ微粒子を沈殿させ、溶媒を取り除き再びヘキサン(50ml)を加えて分散させた。その後予め脱保護により活性化済みのアミノオキシリンカー(10mM,5ml/MeOH)、ホスホリルコリンリンカー(100mM,8ml/MeOH)、NaBH4(1ml,12wt % in 14 N NaOH)、およびmilli Q(50ml)を加えて30分間撹拌し配位子交換をして反応性ナノ微粒子前駆体AO/PC SAM−QDs(AO/PC=1/16)とした。限外濾過(YM50)により精製した後、化合物32とのカップリングに供した(下記スキーム参照)。図13のMALDI−TOFMSに示すとおり、反応はスムーズに進行し全てのアミノオキシ基の化合物32との置換反応が確認できた。
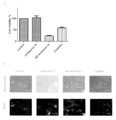
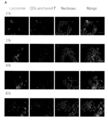
ヒト肝癌細胞(HepG2,P8,ATCCより入手)を5000cell/200ml/wellで播種し、D−MEM High glucose,10%fetal bovine serum(FBS)中、37℃,5%CO2雰囲気化で48時間インキュベートをした後に、10nM蛍光性ナノ微粒子[化合物32担持型AO/PC SAM−QDs(AO/PC=1/16)]を添加、共培養してその後の24時間までの癌細胞生育過程を観察した。細胞は以下の方法で染色した後に蛍光顕微鏡にて観察した。培地を除去した後、細胞をOpti−MEMで3回洗浄後Lyso Tracker R Green DND−26(200ml,5nM/Opti−MEM)を加えて37℃、5%CO2の条件下で30分インキュベートしてリソソームを染色した。その後Hoechest(2ml,0.1ng/ml/Opti−MEM)を加えて37℃、5%CO2雰囲気下でさらに15分間インキュベートして核を染色した後にOpti−MEMで3回洗浄してイメージングを行った(図14)。
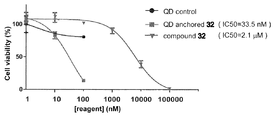
Cell viability assayによる死細胞の定量:HepG2細胞(5×104/100ml/well)を37℃、5%CO2雰囲気化で24時間インキュベートした後にそれぞれ90mlの培地に対してQD(1000~10nM,10ml/milli Q)、QD−anchored 32(1000~10nM,10ml/milli Q)、およびソラフェニブ誘導体32(10×107~10nM,10ml/DMSO)を加えて終濃度が100~1nM(ただし、化合物32はIC50値がmMレベルであることが推察されたので1×106~1nM)となるように調整した。共培養開始後48時間で培地成分により3回洗浄を行い、細胞培養液に対し10mlのCell Counting Kit−8(Dojindo,Kumamoto,Japan)を加えて37℃、5%CO2雰囲気化で1.5時間インキュベートし450nmでの吸光度を測定することで癌細胞の生存率を定量した(図15)。
Claims (21)
- 一般式(A)、(B)及び(A’)において、n1とn2の合計はn3以上である、請求項1又は2に記載の複合体。
- 自殺基質部位は、リソソーム酵素の活性中心と反応性を有する基(以下、反応性基)を含む、請求項1~3のいずれかに記載の複合体。
- 自殺基質部位は、
N−アセチル−D−グルコサミン残基、N−アセチル−D−グガラクトサミン残基、ガラクトース残基、グルコース残基、フコース残基、マンノース残基、及びシアル酸残基、から成る群から選ばれる少なくとも1種の糖残基、並びにジフルオメチルアリール基、及びトリプルオメチルアリール基から成る群から選ばれる少なくとも1種の反応性基を有する請求項4に記載の複合体。 - キナーゼ阻害部位は、キナーゼと反応性を有する基(以下、細胞膜キナーゼ反応性基)を含む、請求項1~3のいずれかに記載の複合体。
- 一般式(A)で示されるリソソーム酵素阻害剤と一般式(B)で示されるリン脂質疑似物質のモル比率が1:100~10:1の範囲である、請求項1~10のいずれかに記載の複合体。
- 一般式(A)で示されるリソソーム酵素阻害剤と一般式(A’)で示される物質のモル比率が1:100~100:0の範囲である、請求項2~11のいずれかに記載の複合体。
- 前記ナノ粒子は、金属ナノ粒子又は半導体ナノ粒子である、請求項1~12のいずれかに記載の複合体。
- 金属ナノ粒子は、金ナノ粒子、白金ナノ粒子、銀ナノ粒子、及び鉄磁性ナノ粒子から成る群から選ばれる少なくとも1種の粒子である請求項13に記載の複合体。
- 半導体ナノ粒子は、量子ドットである請求項13に記載の複合体。
- 前記ナノ粒子は、粒子径が0.1~100nmの範囲である請求項1~15のいずれかに記載の複合体。
- 請求項1~16のいずれかに記載の複合体を有効成分として含有する抗ガン剤。
- 前記抗ガン剤は、乳癌、前立腺癌、肝細胞癌、膵癌、大腸癌、卵巣癌、腎癌、肺癌、または脳腫瘍に対する抗ガン剤である請求項17に記載の抗ガン剤。
- 請求項1~16のいずれかに記載の複合体の製造方法であって、
下記一般式(C)で示される阻害剤架橋前駆体X及び下記一般式(D)で示されるリン脂質疑似物質前駆体とコロイド状ナノ粒子とを混合して、ナノ粒子の表面に阻害剤架橋前駆体X及びリン脂質疑似物質を担持した表面修飾ナノ粒子を得る工程(1)、
得られた表面修飾ナノ粒子にリソソーム酵素阻害剤前駆体Y又はキナーゼ阻害剤前駆体Zを混合して、阻害剤架橋前駆体Xと連結させて下記一般式(A)で示されるリソソーム酵素阻害剤又はキナーゼ阻害剤を形成する、
但し、リソソーム酵素阻害剤前駆体Yは、リソソーム酵素の活性中心と反応性を有する基(以下、反応性基)を含む自殺基質部位を含み、キナーゼ阻害剤前駆体Zはキナーゼと反応性を有する基を含むキナーゼ阻害部位を含む、
請求項1~16のいずれかに記載の複合体を得る工程(2)、
を含む前記方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017563899A JP7018191B2 (ja) | 2016-01-29 | 2017-01-27 | 細胞内物質移送システムおよびその利用 |
| EP17744471.8A EP3409772B1 (en) | 2016-01-29 | 2017-01-27 | Intracellular substance transport system and use thereof |
| US16/073,677 US11007276B2 (en) | 2016-01-29 | 2017-01-27 | Intracellular substance transport system and use thereof |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016-015760 | 2016-01-29 | ||
| JP2016015760 | 2016-01-29 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2017131242A1 true WO2017131242A1 (ja) | 2017-08-03 |
Family
ID=59398225
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2017/003880 WO2017131242A1 (ja) | 2016-01-29 | 2017-01-27 | 細胞内物質移送システムおよびその利用 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US11007276B2 (ja) |
| EP (1) | EP3409772B1 (ja) |
| JP (1) | JP7018191B2 (ja) |
| WO (1) | WO2017131242A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019208820A1 (ja) * | 2018-04-27 | 2019-10-31 | 国立大学法人北海道大学 | 細胞内物質移送システムおよびその利用 |
| WO2021054420A1 (ja) * | 2019-09-20 | 2021-03-25 | 国立大学法人北海道大学 | 糖鎖提示粒子およびその製造方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113230415B (zh) * | 2021-05-18 | 2022-04-12 | 南华大学 | 岩藻糖与环糊精修饰多肽靶向动脉粥样硬化相关巨噬细胞纳米载体系统及其制备方法和应用 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007254452A (ja) * | 2006-03-24 | 2007-10-04 | Kyushu Univ | 有機化合物 |
| JP2009534309A (ja) | 2006-03-31 | 2009-09-24 | マサチューセッツ インスティテュート オブ テクノロジー | 治療剤の標的化送達のためのシステム |
| JP2011528275A (ja) | 2008-07-17 | 2011-11-17 | ミセル テクノロジーズ,インク. | 薬物送達医療デバイス |
| WO2014197937A1 (en) * | 2013-06-13 | 2014-12-18 | University Of South Australia | Methods for detecting prostate cancer |
| JP2015520197A (ja) | 2012-06-20 | 2015-07-16 | フランク・グー | 粘膜付着性ナノ粒子送達系 |
| JP2015520194A (ja) | 2012-06-07 | 2015-07-16 | プレジデント・アンド・フェロウズ・オブ・ハーバード・カレッジ | 薬物標的指向化のためのナノ療法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000042012A1 (en) * | 1999-01-13 | 2000-07-20 | Bayer Corporation | φ-CARBOXYARYL SUBSTITUTED DIPHENYL UREAS AS RAF KINASE INHIBITORS |
| EP2104420A2 (en) | 2006-10-30 | 2009-09-30 | George Mason Intellectual Properties, Inc. | Tissue preservation and fixation method |
| CA2745972C (en) * | 2008-12-16 | 2016-11-01 | Fundacio Privada Institut Catala De Nanotecnologia | Conjugates comprising nanoparticles coated with platinum containing compounds |
| JP2014214139A (ja) | 2013-04-26 | 2014-11-17 | ポーラ化成工業株式会社 | Nadh産生促進剤 |
-
2017
- 2017-01-27 US US16/073,677 patent/US11007276B2/en active Active
- 2017-01-27 WO PCT/JP2017/003880 patent/WO2017131242A1/ja active Application Filing
- 2017-01-27 JP JP2017563899A patent/JP7018191B2/ja active Active
- 2017-01-27 EP EP17744471.8A patent/EP3409772B1/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007254452A (ja) * | 2006-03-24 | 2007-10-04 | Kyushu Univ | 有機化合物 |
| JP2009534309A (ja) | 2006-03-31 | 2009-09-24 | マサチューセッツ インスティテュート オブ テクノロジー | 治療剤の標的化送達のためのシステム |
| JP2011528275A (ja) | 2008-07-17 | 2011-11-17 | ミセル テクノロジーズ,インク. | 薬物送達医療デバイス |
| JP2015520194A (ja) | 2012-06-07 | 2015-07-16 | プレジデント・アンド・フェロウズ・オブ・ハーバード・カレッジ | 薬物標的指向化のためのナノ療法 |
| JP2015520197A (ja) | 2012-06-20 | 2015-07-16 | フランク・グー | 粘膜付着性ナノ粒子送達系 |
| WO2014197937A1 (en) * | 2013-06-13 | 2014-12-18 | University Of South Australia | Methods for detecting prostate cancer |
Non-Patent Citations (20)
| Title |
|---|
| A. T. OHYANAGI, J. AM. CHEM. SOC., vol. 133, 2011, pages 12507 - 12517 |
| B. R. S.TAN, ACS CHEM. BIOL., vol. 10, 2015, pages 2073 - 2086 |
| BIOCHEMISTRY, vol. 44, 2005, pages 11669 - 11675 |
| BIOORG. MED. CHEM. LETT., vol. 11, 2001, pages 1769 - 1773 |
| H. HINOU ET AL., BIOCHEMISTRY, vol. 44, 2005, pages 11669 - 11675 |
| HAMMOCK, B. D., BIOORGANIC & MED. CHEM. LETT., vol. 23, 2013, pages 3732 - 3737 |
| KANIA, R. S. ET AL., PROC. NATL. ACAD. SCI. USA, vol. 109, 2012, pages 18281 - 18289 |
| LIN, L. ET AL., CANCER RES., vol. 66, 2006, pages 11851 - 11858 |
| M. ICHIKAWA ET AL., BIOORG. MED. CHEM. LETT., vol. 11, 2001, pages 1769 - 1773 |
| M. KUROGOCHI ET AL., J. BIOL. CHEM., vol. 279, 2004, pages 44704 - 44712 |
| R. S. TAN ET AL., ACS CHEM. BIOL., vol. 10, 2015, pages 2073 - 2086 |
| R. S.TAN, ACS CHEM. BIOL., vol. 10, 2015, pages 2073 - 2086 |
| See also references of EP3409772A4 |
| SHIN-ICHIRO NISHIMURA ET AL., ANGEW. CHEM. INT. ED., vol. 51, 2012, pages 3386 - 3390 |
| SMITH, M. A.; HOUGTON, P., CLIN. CANCER RES., vol. 19, 2013, pages 2828 - 2833 |
| T. OHYANAGI ET AL., J. AM. CHEM. SOC., vol. 133, 2011, pages 12057 - 12517 |
| T. OHYANAGI ET AL., J. AM. CHEM. SOC., vol. 133, 2011, pages 12507 - 12517 |
| T. OHYANAGI, J. AM. CHEM. SOC., vol. 133, 2011, pages 12507 - 12517 |
| TAN, ROGER S.: "Rapid Endolysosomal Escape and Controlled Intracellular Trafficking of Cell Surface Mimetic Quantum-Dots-Anchored Peptides and Glycopeptides", ACS CHEM. BIOL., vol. 10, 24 June 2015 (2015-06-24), pages 2073 - 2086, XP055538410 * |
| WILHELM, S. M. ET AL., CANCER RES., vol. 64, 2004, pages 2099 - 7109 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019208820A1 (ja) * | 2018-04-27 | 2019-10-31 | 国立大学法人北海道大学 | 細胞内物質移送システムおよびその利用 |
| WO2021054420A1 (ja) * | 2019-09-20 | 2021-03-25 | 国立大学法人北海道大学 | 糖鎖提示粒子およびその製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3409772A1 (en) | 2018-12-05 |
| US11007276B2 (en) | 2021-05-18 |
| JP7018191B2 (ja) | 2022-02-10 |
| EP3409772B1 (en) | 2023-06-28 |
| US20200138973A1 (en) | 2020-05-07 |
| JPWO2017131242A1 (ja) | 2018-11-22 |
| EP3409772A4 (en) | 2019-10-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Sung et al. | Delivery of nitric oxide with a nanocarrier promotes tumour vessel normalization and potentiates anti-cancer therapies | |
| Xiao et al. | Aminopeptidase‐N‐activated theranostic prodrug for NIR tracking of local tumor chemotherapy | |
| Malik et al. | AS1411-conjugated gold nanospheres and their potential for breast cancer therapy | |
| Lin et al. | Targeting the delivery of glycan-based paclitaxel prodrugs to cancer cells via glucose transporters | |
| CN103221070B (zh) | 用于狭窄病变和溶解血栓疗法的切变控制释放 | |
| Chen et al. | Smart hypoxia-responsive transformable and charge-reversible nanoparticles for the deep penetration and tumor microenvironment modulation of pancreatic cancer | |
| Xiang et al. | Restoration and enhancement of immunogenic cell death of cisplatin by coadministration with digoxin and conjugation to HPMA copolymer | |
| WO2017131242A1 (ja) | 細胞内物質移送システムおよびその利用 | |
| KR102053065B1 (ko) | 히알루론산 및 독소루비신을 이용한 pH 감응성 항암 엑소좀 조성물 | |
| Petrov et al. | New small-molecule glycoconjugates of docetaxel and GalNAc for targeted delivery to hepatocellular carcinoma | |
| Li et al. | Metal-phenolic networks with ferroptosis to deliver NIR-responsive CO for synergistic therapy | |
| Tang et al. | Oxaliplatin-based platinum (IV) prodrug bearing toll-like receptor 7 agonist for enhanced immunochemotherapy | |
| Cheng et al. | Carrier‐Free Nanoassembly of Curcumin–Erlotinib Conjugate for Cancer Targeted Therapy | |
| Chen et al. | Penetrating micelle for reversing immunosuppression and drug resistance in pancreatic cancer treatment | |
| Deng et al. | Two-step assembling of near-infrared “OFF–ON” fluorescent nanohybrids for synchronous tumor imaging and microrna modulation-based therapy | |
| Li et al. | Liver‑targeted delivery of liposome‑encapsulated curcumol using galactosylated‑stearate | |
| Jia et al. | Micromixer based preparation of functionalized liposomes and targeting drug delivery | |
| Mehata et al. | Chitosan-g-estrone nanoparticles of palbociclib vanished hypoxic breast tumor after targeted delivery: development and ultrasound/photoacoustic imaging | |
| Xiao et al. | Synthesis of novel tetravalent galactosylated DTPA-DSPE and study on hepatocyte-targeting efficiency in vitro and in vivo | |
| Zeng et al. | A mitochondria-targeting ROS-activated nanoprodrug for self-augmented antitumor oxidation therapy | |
| Huan et al. | In vivo anti-tumor activity of a new doxorubicin conjugate via α-linolenic acid | |
| Dou et al. | Orthogonally engineered albumin with attenuated macrophage phagocytosis for the targeted visualization and phototherapy of liver cancer | |
| Yao et al. | A Self‐Assembly Combined Nano‐Prodrug to Overcome Gemcitabine Chemo‐Resistance of Pancreatic Tumors | |
| Sun et al. | A phenolic based tumor-permeated nano-framework for immunogenic cell death induction combined with PD-L1 immune checkpoint blockade | |
| Chen et al. | Integration of dual targeting and dual therapeutic modules endows self-assembled nanoparticles with anti-tumor growth and metastasis functions |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 17744471 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2017563899 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2017744471 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 2017744471 Country of ref document: EP Effective date: 20180829 |