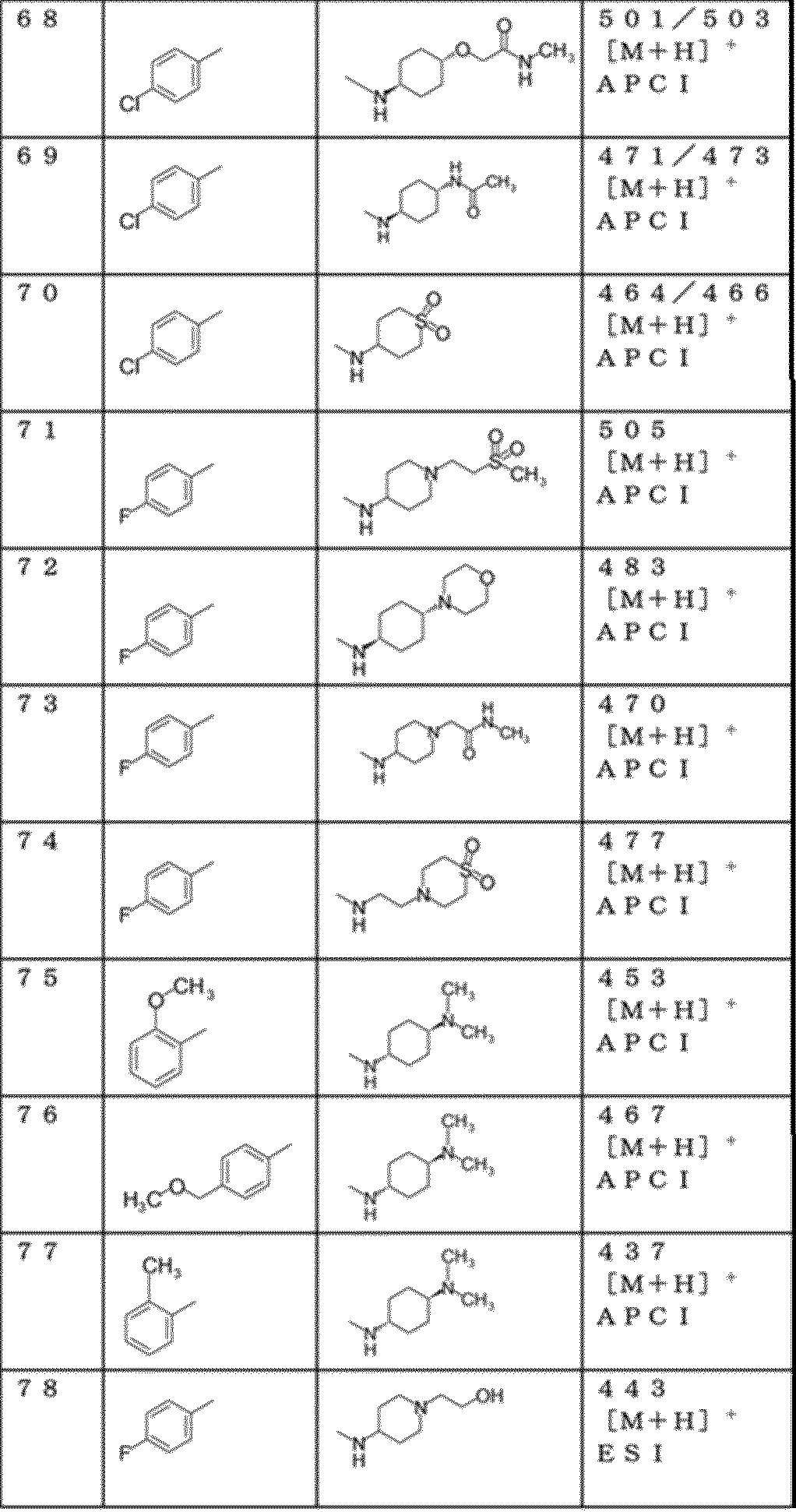WO2017069226A1 - 新規含窒素芳香族複素環化合物 - Google Patents
新規含窒素芳香族複素環化合物 Download PDFInfo
- Publication number
- WO2017069226A1 WO2017069226A1 PCT/JP2016/081214 JP2016081214W WO2017069226A1 WO 2017069226 A1 WO2017069226 A1 WO 2017069226A1 JP 2016081214 W JP2016081214 W JP 2016081214W WO 2017069226 A1 WO2017069226 A1 WO 2017069226A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- optionally substituted
- alkyl
- groups
- independently selected
- Prior art date
Links
- 0 CCC(N(*)*)=O Chemical compound CCC(N(*)*)=O 0.000 description 3
- GYPNJSBBOATUPK-UHFFFAOYSA-N CC(C)NC(CCl)=O Chemical compound CC(C)NC(CCl)=O GYPNJSBBOATUPK-UHFFFAOYSA-N 0.000 description 1
- VDJUVPSLVQYKLD-UHFFFAOYSA-N CC(C)NC(CN(CC1)CCN1C1=CCC(C#N)N=C1)=O Chemical compound CC(C)NC(CN(CC1)CCN1C1=CCC(C#N)N=C1)=O VDJUVPSLVQYKLD-UHFFFAOYSA-N 0.000 description 1
- SLHWAVOXJSXPNV-UHFFFAOYSA-N N#CC1N=CC(N2CCNCC2)=CC1 Chemical compound N#CC1N=CC(N2CCNCC2)=CC1 SLHWAVOXJSXPNV-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D237/00—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings
- C07D237/02—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings
- C07D237/06—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D237/10—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D237/20—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/10—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D241/14—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D241/20—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D451/00—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof
- C07D451/02—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof
- C07D451/04—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof with hetero atoms directly attached in position 3 of the 8-azabicyclo [3.2.1] octane or in position 7 of the 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D453/00—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids
- C07D453/02—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids containing not further condensed quinuclidine ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/08—Bridged systems
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Pyridine Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Description
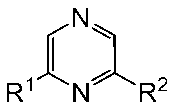
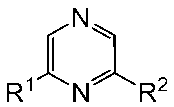
下式[I]:
X及びYは以下の(1)~(3)のいずれかを表し、
(1)XがN、かつYがCH又はC-RY、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RYはアルキル基を表し;
RAは置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、又は部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基を表し;
R1は水素原子、又はアルキル基を表し;
R2は置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよい脂肪族複素環基、又は部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基を表し;
R3は水素原子、又はアルキル基を表す〕で示される化合物又はその薬理的に許容し得る塩に関する。
本発明において、アルキルとは、炭素数1~6(C1~6)の直鎖または分岐鎖状の飽和炭化水素基をいう。とりわけ炭素数1~5(C1~5)の基が好ましい。具体的には、メチル、エチル、n-プロピル、i-プロピル、n-ブチル、i-ブチル、1,2-ジメチルプロピル、t-ブチル、i-アミル、n-ペンチル、n-ヘキシルなどが挙げられる。とりわけ、メチル、エチル、i-プロピル、i-ブチル、1,2-ジメチルプロピル、t-ブチルなどが好ましい。
他の好ましい例としては、前記式[I]中のR2で表される「部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基」における該ヘテロアリール部分として、ピロリル、フラニル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、チアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、ベンゾピラニルなどが挙げられる。とりわけピラゾリル、ピリジル、ベンゾイミダゾリルなどが好ましい。
さらに、他の好ましい例において、置換されていてもよいヘテロアリール基としてピリミジニル基が挙げられる。
X及びYは以下の(1)~(3)のいずれかを表し、
(1)XがN、かつYがCH又はC-RY、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RYはアルキル基を表し;
RAで表される置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立して、ハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分が6~10員単環又は二環式アリールであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分が硫黄原子、酸素原子、及び窒素原子からなる群より独立して選ばれる1~2個の異項原子を含む、6~10員単環又は二環式ヘテロアリールであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
(ii)置換されていてもよいシクロアルキル基、(iii)置換されていてもよい脂肪族複素環基、及び(iv)部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基、水酸基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iv)の各置換基において脂肪族複素環基は独立して、硫黄原子、酸素原子、又は窒素原子から選ばれる1~2個の異項原子を含む4~9員単環又は二環式脂肪族複素環基であり、
上記(i)~(iv)の各置換基においてヘテロアリール基は独立して、硫黄原子、酸素原子、及び窒素原子からなる群より独立して選ばれる1~4個の異項原子を含む、5~10員単環又は二環式ヘテロアリール基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分が硫黄原子、酸素原子、及び窒素原子からなる群より独立して選ばれる1~3個の異項原子を含む4~9員単環又は二環式脂肪族複素環であり;
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分が5~10員単環又は二環式ヘテロアリールであり、
R3が水素原子、又はアルキル基である、化合物又はその薬理的に許容し得る塩を包含する。
X及びYは以下の(1)~(3)のいずれかを表し、
(1)XがN、かつYがCH又はC-RY、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RYはアルキル基を表し;
RAで表される置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立して、ハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分がフェニル、又はナフチルであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分がピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、又はベンゾピラニルであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
R2で表される(ii)置換されていてもよいシクロアルキル基、(iii)置換されていてもよい脂肪族複素環基、及び(iv)部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;水酸基、1~2個のアルキル基で置換されていてもよいカルバモイル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iv)の各置換基において脂肪族複素環基は独立して、アゼチジニル、オキセタニル、ピロリジニル、テトラヒドロチエニル、テトラヒドロフラニル、チアゾリジニル、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、ホモモルホリニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、及び3-オキソ-9-アザビシクロ[3.3.1]ノニルからなる群より選ばれる基であり、
上記(i)~(iv)の各置換基においてヘテロアリール基は独立して、ピロリル、フラニル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、チアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、及びベンゾピラニルからなる群より選ばれる基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分は、アゼチジニル、オキセタニル、ピロリジニル、テトラヒドロエニル、テトラヒドロフラニル、チアゾリジニル、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、ホモモルホリニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分は、ピロリル、フラニル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、チアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、又はベンゾピラニルであり、
R3が水素原子、又はアルキルである化合物又はその薬理的に許容し得る塩を包含する。
R2で表される「部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基」における部分的に水素化されていてもよいヘテロアリール基が、ピロリル基、フラニル基、チエニル基、イミダゾリル基、イミダゾリニル基、ピラゾリル基、オキサゾリル基、チアゾリル基、トリアゾリル基、テトラゾリル基、ピリジル基、ピラジニル基、ピリミジニル基、ピリダジニル基、チアジニル基、トリアジニル基、インドリル基、イソインドリル基、イソインドリニル基、インダゾリル基、ベンゾイミダゾリル基、テトラヒドロベンゾイミダゾリル基、ベンゾチアゾリル基、ベンゾフラニル基、ジヒドロベンゾフラニル基、キノリル基、イソキノリル基、イミダゾピリジル基、テトラヒドロイミダゾピリジル基、ベンゾピラニル基、及びジヒドロベンゾピラニル基からなる群より選ばれる基である、化合物又はその薬理的に許容し得る塩が挙げられる。
X及びYは以下の(1)~(3)のいずれかを表し、
(1)XがN、かつYがCH又はC-RY、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RYはアルキル基を表し;
RAで表される置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立して、ハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分がフェニル、又はナフチルであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル、又はベンゾフラニルであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
R2で表される(ii)置換されていてもよいシクロアルキル基、(iii)置換されていてもよい脂肪族複素環基、及び(iv)部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;水酸基、1~2個のアルキル基で置換されていてもよいカルバモイル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iv)の各置換基において脂肪族複素環基は独立して、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、及びテトラヒドロピラニルから選ばれる基であり、
上記(i)~(iv)の各置換基においてヘテロアリール基は独立して、ピリミジニル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分が、ピロリジニル、ピペリジニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分が、ピラゾリル、ピリジル、又はベンゾイミダゾリルであり、
R3が水素原子、又はアルキル基である、化合物又はその薬理的に許容し得る塩を包含する。
R2で表される「部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基」における部分的に水素化されていてもよいヘテロアリール基が、ピラゾリル基、ピリジル基、及びテトラヒドロベンゾイミダゾリル基からなる群より選ばれる基である、化合物又はその薬理的に許容し得る塩が挙げられる。
X及びYは以下の(1)~(3)のいずれかを表し、
(1)XがN、かつYがCH又はC-RY、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RYはアルキル基を表し;
RAが
(1)アルキル基で置換されていてもよいシクロアルキル基、
(2)アルキル基で置換されていてもよいシクロアルケニル基、
(3)ハロゲン原子、アルキル基、ハロアルキル基、アルコキシアルキル基及びアルコキシ基からなる群より独立して選ばれる1~3個の基で置換されていてもよいフェニル基、
(4)ナフチル基、又は
(5)部分的に水素化されていてもよく、シアノ基、アルキル基、及びハロアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいヘテロアリール基であり、
RAで表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル又はベンゾフラニルであり、
R1が水素原子、又はアルキル基であり、
R2が
(i)水酸基;ハロゲン原子;及び、水酸基、オキソ基、アルキル基、アルコキシカルボニル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はピペリジニル基、ピペラジニル基、モルホリニル基、又はチオモルホリニル基である)からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基、
(ii)水酸基;水酸基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及び、水酸基、及びオキソ基からなる群より独立して選ばれる1~2個の基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はピペリジニル基、モルホリニル基、又はピペラジニル基である)からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基、水酸基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアルキル基;アルコキシ基;アルコキシカルボニル基;テトラヒドロピラニル基;及び、ピリミジニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)部分的に水素化されていてもよく、1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルキル基で置換されていてもよいヘテロアリール基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分がピロリジニル、ピペリジニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピラゾリル、ピリジル、又はベンゾイミダゾリルであり、
R3が水素原子である、化合物又はその薬理的に許容し得る塩を包含する。
R2で表される「部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基」における部分的に水素化されていてもよいヘテロアリール基が、ピラゾリル基、ピリジル基、及びテトラヒドロベンゾイミダゾリル基からなる群より選ばれる基である、化合物又はその薬理的に許容し得る塩が挙げられる。
XがNであり、YがCH又はC-RYであり、
RYがアルキル基であり、
RAが
(1)アルキル基で置換されていてもよいシクロヘキシル基、
(2)アルキル基で置換されていてもよいシクロヘキセニル基、
(3)ハロゲン原子、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~2個の基で置換されていてもよいフェニル基、
(4)ナフチル基、又は
(5)部分的に水素化されていてもよく、シアノ基で置換されていてもよいヘテロアリール基であり、
RAで表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、又はベンゾフラニルであり、
R1が水素原子であり、
R2が
(i)水酸基;及びオキソ基、アルキル基、アルコキシカルボニル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はピペリジニル基、ピペラジニル基、モルホリニル基、又はチオモルホリニル基から選ばれる)からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基、
(ii)1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びモルホリニル基からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基、水酸基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアルキル基;アルコキシカルボニル基;及びアルコキシ基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)ピリジル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分がピペリジニル、テトラヒドロチオピラニル、又はテトラヒドロピラニルであり、
R3が水素原子である、化合物又はその薬理的に許容し得る塩が好ましい。
XがCHであり、YがNであり、
RAが(1)アルキル基で置換されていてもよいシクロヘキシル基、
(2)ハロゲン原子、アルキル基、及びハロアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいフェニル基、又は
(3)部分的に水素化されていてもよく、シアノ基、及びアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいヘテロアリール基であり、
RAで表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル、又はベンゾフラニルであり、
R1が水素原子又はアルキル基であり、
R2が
(i)水酸基;ハロゲン原子;及び、水酸基、及びアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいピペリジニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基、
(ii)水酸基;水酸基で置換されていてもよいアルキル基;アルコキシ基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及び、1~2個のオキソ基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はモルホリニル基、又はピペラジニル基から選ばれる)からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)オキソ基;アルキルスルホニル基で置換されていてもよいアルキル基;テトラヒドロピラニル基;及び、ピリミジニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルキル基で置換されていてもよいピラゾリル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分がピロリジニル、ピペリジニル、テトラヒドロチオピラニル、又は1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)であり、
R3が水素原子である、化合物又はその薬理的に許容し得る塩が挙げられる。
XがCHであり、YがCHであり、
RAが(1)アルキル基で置換されていてもよいシクロヘキシル基、
(2)アルキル基で置換されていてもよいシクロヘキセニル基、
(3)ハロゲン原子、及びアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいフェニル基、又は
(4)部分的に水素化されていてもよく、シアノ基、アルキル基、及びハロアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいヘテロアリール基であり、
RAで表される水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル、又はベンゾフラニルであり、
R1が水素原子であり、
R2が
(i)水酸基で置換されていてもよいアルキル基、
(ii)アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及び水酸基で置換されていてもよいピペリジニル基からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)水酸基;アルキル基;及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)部分的に水素化されていてもよく、1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルキル基で置換されていてもよいヘテロアリール基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分が8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピラゾリル、又はベンゾイミダゾリルであり、
R3が水素原子である、化合物又はその薬理的に許容し得る塩が挙げられる。
X及びYが以下の(1)~(3)のいずれかであり、
(1)XがN、かつYがCH、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RAが置換されていてもよいアリール基、又は部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基であり;
R1が水素原子であり;
R2が置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、又は置換されていてもよい脂肪族複素環基であり;
R3が水素原子である、化合物又はその薬理的に許容し得る塩を包含する。
X及びYが以下の(1)~(3)のいずれかであり、
(1)XがN、かつYがCH、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RAで表される置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立してハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分がフェニル、又はナフチルであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分がピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、又はベンゾピラニルであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
R2で表される(ii)置換されていてもよいシクロアルキル基、及び(iii)置換されていてもよい脂肪族複素環基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;水酸基、1~2個のアルキル基で置換されていてもよいカルバモイル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iii)の各置換基において脂肪族複素環基は独立して、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、及びテトラヒドロピラニルからなる群より選ばれる基であり、
上記(i)~(iii)の各置換基においてヘテロアリール基は独立して、ピリミジニル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分は、ピロリジニル、ピペリジニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R3が水素原子である、化合物又はその薬理的に許容し得る塩を包含する。
X及びYが以下の(1)~(3)のいずれかであり、
(1)XがN、かつYがCH、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RAがハロゲン原子で置換されていてもよいフェニル基、又は部分的に水素化されていてもよくアルキル基で置換されていてもよいインダゾリル基であり、
R2が(1)アルキル基、
(2)1~2個のアルキル基で置換されていてもよいアミノ基で置換されていてもよいシクロヘキシル基、若しくはアルコキシ基で置換されていてもよいシクロヘキシル基、又は
(3)アルキル基で置換されていてもよい8-アザビシクロ[3.2.1]オクチルであり、
R3が水素原子である、化合物又はその薬理的に許容し得る塩を包含する。
3-[4-[(trans-4-メトキシシクロヘキシル)カルバモイルメチル]ピペラジン-1-イル]-5-(1-メチル-1H-インダゾール-6-イル)ピラジン;
3-[4-(イソプロピルカルバモイルメチル)ピペラジン-1-イル]-5-(1-メチル-1H-インダゾール-6-イル)ピラジン;
5-(4-フルオロフェニル)-3-[4-[[trans-4-(N,N-ジメチルアミノ)シクロヘキシル]カルバモイルメチル]ピペラジン-1-イル]ピリダジン;及び
3-(4-クロロフェニル)-5-[4-[(exo-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル)カルバモイルメチル]ピペラジン-1-イル]ピリジン
からなる群より選ばれる化合物又はその薬理的に許容し得る塩が挙げられる。
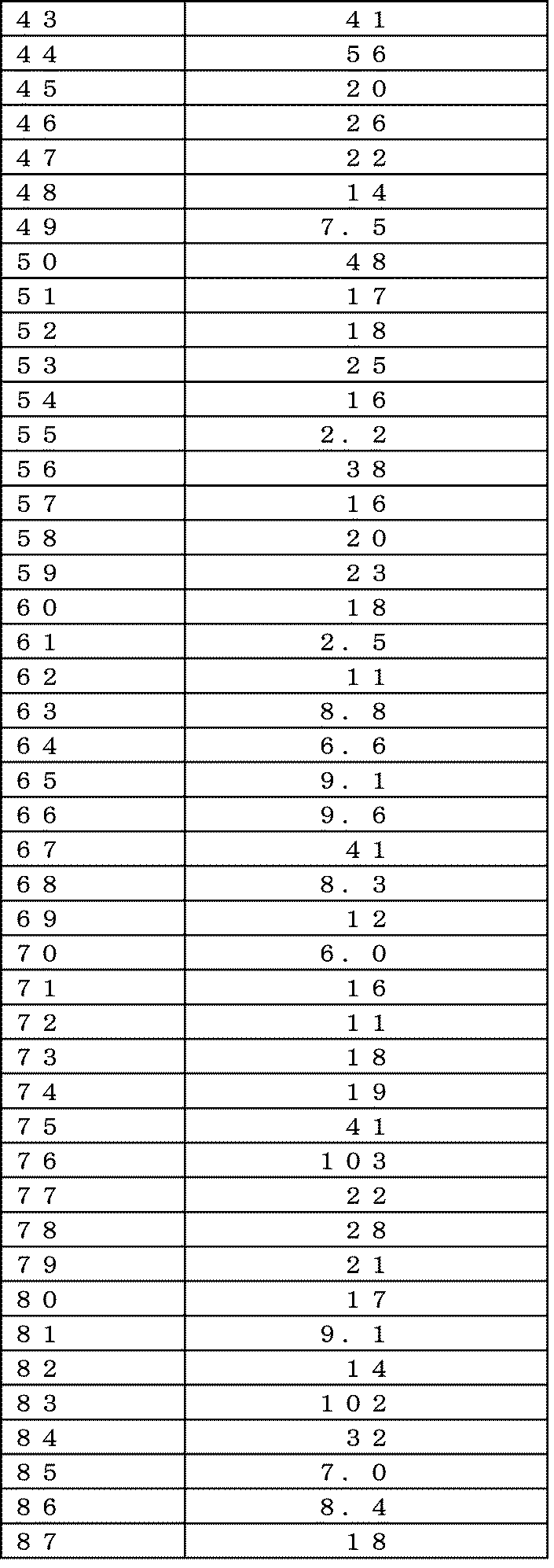
例えば、実施例49に記載された化合物(化学名:3-[4-(イソプロピルカルバモイルメチル)ピペラジン-1-イル]-5-(1-メチル-1H-インダゾール-6-イル)ピラジン)は、類縁酵素であるヒトCyp11B1阻害におけるIC50値(nM)とヒトCyp11B2阻害におけるIC50(nM)の比が100倍以上であり、Cyp11B2に対して高い選択性を示す。
このような医薬組成物の剤形は特に限定されるものではなく、例えば、錠剤、顆粒剤、カプセル剤、散剤、注射剤、吸入剤、坐剤等の慣用の医薬製剤が挙げられる。
合成法A1
(1)XがN、かつYがCH又はC-RY、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RYはアルキル基を表し;
W1、W2、W3はハロゲン原子、Ra、Rbは水素原子、又はアルキル基、Rcはアルキル基を表す。Z1はアミノ基の保護基(例えば、tert-ブトキシカルボニル基の如きアルコキシカルボニル基等)を示す。RAは置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、又は部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基を表す。R1は水素原子、又はアルキル基を表し、R2は置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよい脂肪族複素環基、又は部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基を表し、R3は水素原子、又はアルキル基を表す。〕
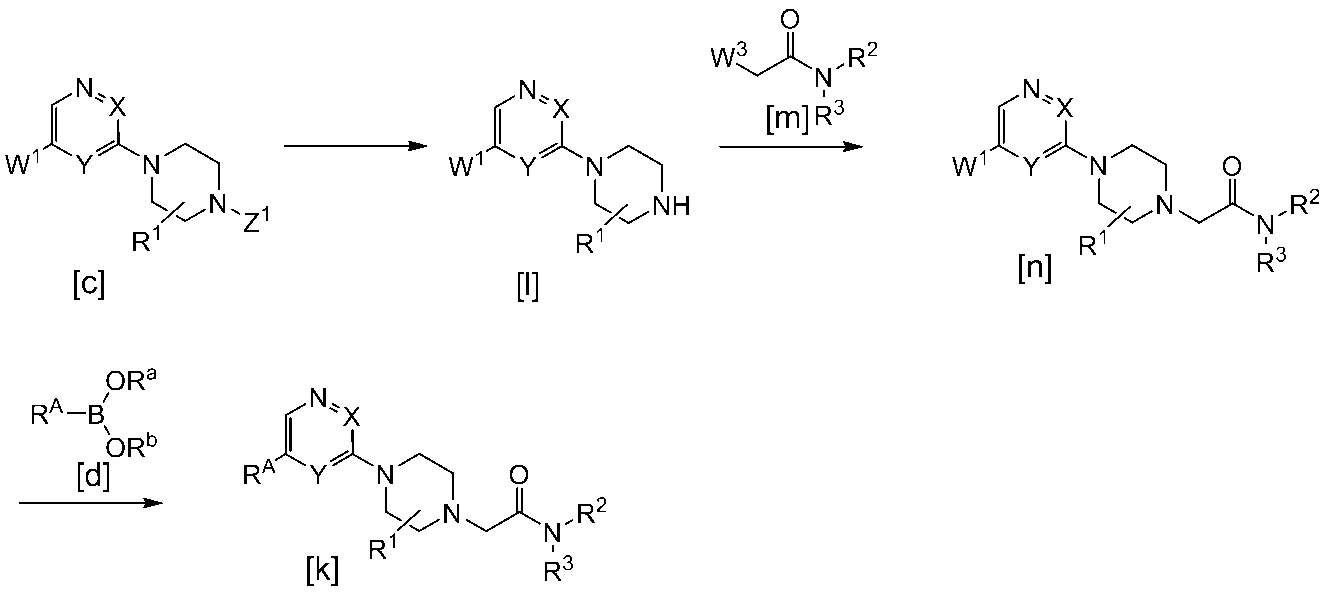
まず、一般式[a]で示される化合物と、一般式[b]で示される化合物との求核置換反応、又はカップリング反応を行うことにより一般式[c]で示される化合物を得る。一般式[e]で示される化合物は、化合物[c]と一般式[d]で示される化合物とのカップリング反応によって得ることができる。得られた一般式[e]で示される化合物を脱保護して一般式[f]で示される化合物を得る。一般式[h]で示される化合物は、化合物[f]と一般式[g]で示される化合物との置換反応によって得ることができる。得られた一般式[h]で示される化合物を加水分解して一般式[i]で示される化合物を得る。得られた化合物[i]と一般式[j]で示される化合物又はその塩を反応させ、所望により生成物を薬理学的に許容し得る塩とすることにより目的化合物[k]またはその薬理的に許容し得る塩を製造することができる。
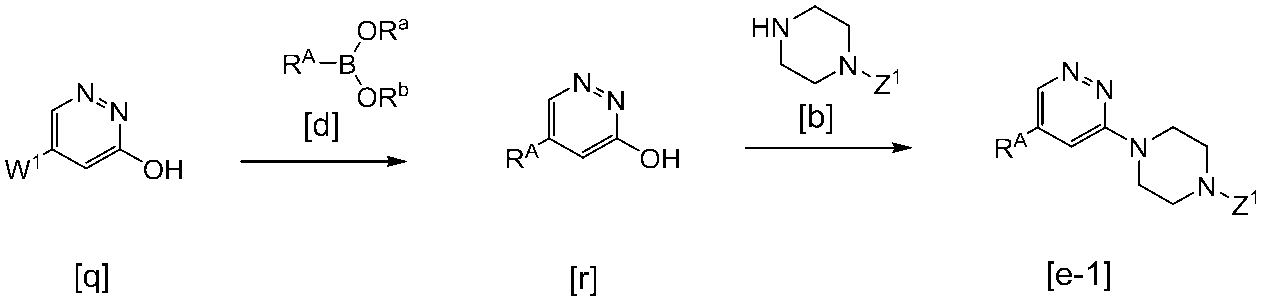
まず、一般式[a-1]で示される化合物とベンジルアルコールとの求核置換反応を行うことにより一般式[u]で示される化合物を得る。一般式[v]で示される化合物は、化合物[u]と一般式[d]で示される化合物とのカップリング反応によって得ることができる。得られた一般式[v]で示される化合物を脱ベンジル化して一般式[r]で示される化合物を得る。得られた化合物[r]と一般式[A]で示される化合物又はその塩を反応させ、所望により生成物を薬理学的に許容し得る塩とすることにより目的化合物[k-1]またはその薬理的に許容し得る塩を製造することができる。
まず、[B]で示される化合物とベンジルハライドとの置換反応を行うことにより[C]で示される化合物を得る。[D]で示される化合物は、化合物[C]のハロゲン交換・還元的脱ハロゲン反応によって得ることができる。得られた[D]で示される化合物と一般式[d]で示される化合物とのカップリング反応によって、一般式[E]で示される化合物を得る。得られた化合物[E]の脱ベンジル反応を行うことにより、一般式[r]で示される化合物を得る。
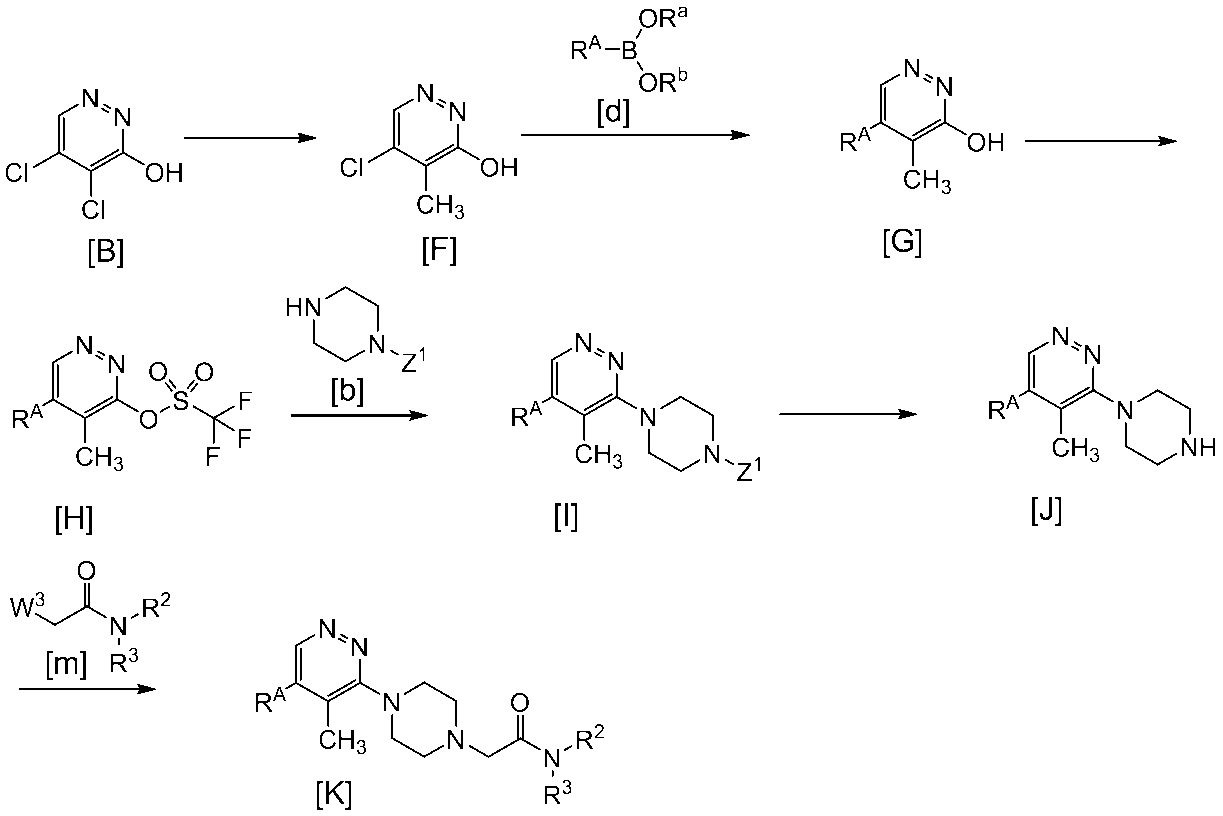
まず、[B]で示される化合物とメチル化剤との反応を行うことにより[F]で示される化合物を得る。得られた[F]で示される化合物と一般式[d]で示される化合物とのカップリング反応によって、一般式[G]で示される化合物を得る。得られた化合物[G]をトリフルオロメタンスルホニル化して、一般式[H]で示される化合物を得る。一般式[H]で示される化合物と一般式[b]で示される化合物との求核置換反応により、一般式[I]で示される化合物を得る。得られた一般式[I]で示される化合物を脱保護して一般式[J]で示される化合物を得る。得られた化合物[J]と一般式[m]で示される化合物又はその塩を反応させ、所望により生成物を薬理学的に許容し得る塩とすることにより目的化合物[K]またはその薬理的に許容し得る塩を製造することができる。
MS(APCI):344[M+H]+
(2)化合物2(4.3g)をエタノール(31mL)に懸濁し、1mol/L水酸化ナトリウム水溶液(12.4mL)を加え、室温にて16時間撹拌した。反応混合物に生じた沈殿をろ取し、ジエチルエーテルにて洗浄することにより、無色固体として化合物3(1.1g)を得た。
MS(ESI):314[M+H]-
(3)化合物3(34mg)と化合物4(16mg)をDMF(1mL)に懸濁し、ジイソプロピルエチルアミン(35μL)とHATU(46mg)を加え、室温にて3時間撹拌した。反応混合物に水と飽和炭酸水素ナトリウム水溶液を加え、クロロホルムにて3回抽出した。有機層を飽和食塩水で洗浄した後、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/メタノール=100/0~90/10 グラジエント)にて精製することにより、無色固体として化合物5(18mg)を得た。
MS(APCI):435[M+H]+
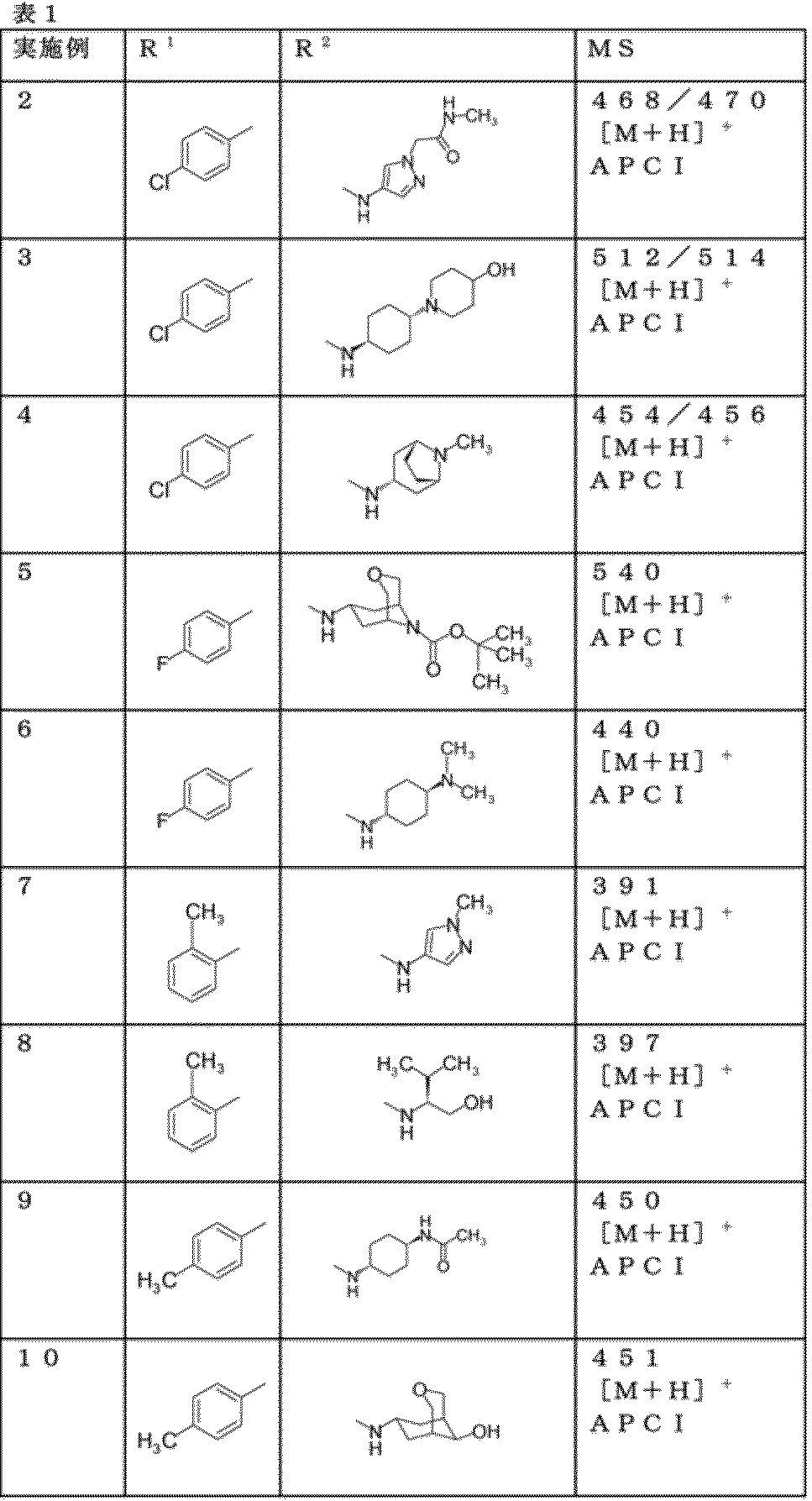
対応原料化合物を、前記の実施例1と同様に処理することにより、下記一般式においてR1およびR2がそれぞれ下記表1に記載の構造を有する各化合物を得た。
MS(APCI):365[M+H]+
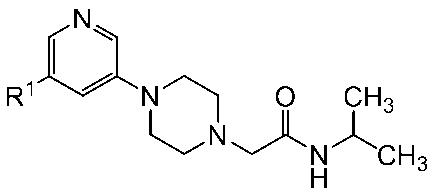
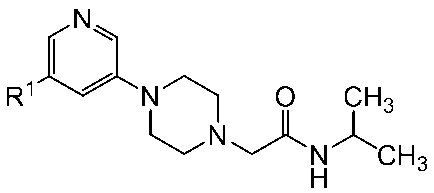
対応原料化合物を、前記の実施例11と同様に処理することにより、下記一般式においてR1が下記表2に記載の構造を有する化合物を得た。
MS(APCI):381[M+H]+
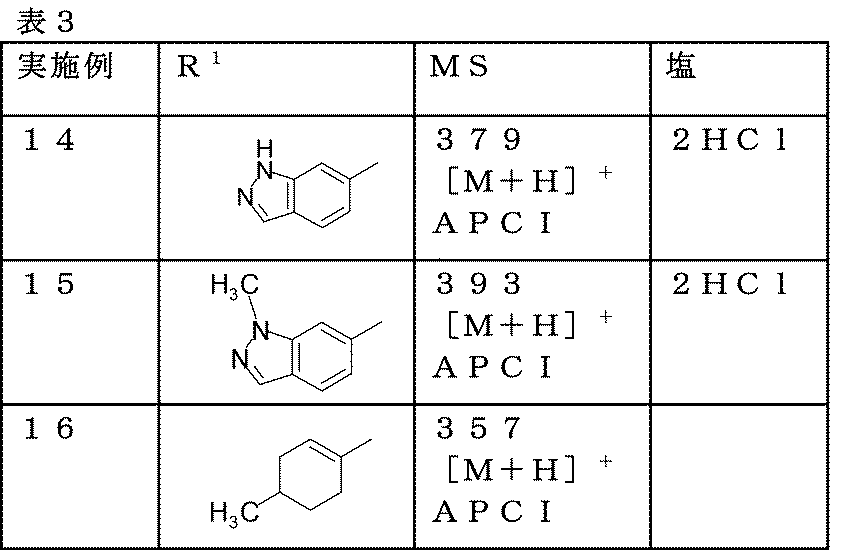
対応原料化合物を、前記の実施例13と同様に処理することにより、下記一般式においてR1がそれぞれ下記表3に記載の構造を有する各化合物を得た。
MS(APCI):359[M+H]+
MS(APCI):381[M+H]+
(2)化合物2(1.9g)をエタノール(10mL)に懸濁し、2mol/L水酸化ナトリウム水溶液(5mL)を加え、室温にて1日間撹拌した。反応混合物を減圧下濃縮し、残渣を水に溶解させたのち、氷冷下2mol/L塩酸水溶液を加え、pH5に調整した。析出物をろ取、水洗、減圧下乾燥することにより、淡黄色固体として化合物3(1.7g)を得た。
MS(APCI):353[M+H]+
(3)化合物3(150mg)と化合物4(96mg)をDMF(2mL)に懸濁し、ジイソプロピルエチルアミン(224μL)とHATU(486mg)を加え、室温下4日間撹拌した。反応混合物を水で希釈し、クロロホルムにて3回抽出した。有機層を無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/メタノール=100/0~95/5 グラジエント)にて精製することにより、淡黄色固体として化合物5(144mg)を得た。
MS(APCI):410[M+H]+
対応原料化合物を、前記の実施例18と同様に処理することにより、下記一般式においてR1およびR2がそれぞれ下記表4に記載の構造を有する各化合物を得た。
MS(APCI):341[M+H]+
(2)化合物2(4.6g)をエタノール(13mL)に懸濁し、2mol/L水酸化ナトリウム水溶液(16mL)を加え、室温にて6時間撹拌した。反応混合物を減圧下濃縮し、黄色アモルファスを得た。ジイソプロピルエーテルを加え、得られた沈殿物をろ取、減圧下乾燥することにより、淡黄色固体として化合物3(4.5g)を得た。
MS(ESI):311[M+H]+
(3)化合物3(33mg)と化合物4(25mg)をDMF(2mL)に懸濁し、ジイソプロピルエチルアミン(35μL)とHATU(46mg)を加え、室温下4日間撹拌した。反応混合物を水で希釈し、クロロホルムにて3回抽出した。有機層を無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/メタノール=100/0~95/5 グラジエント)にて精製することにより、無色固体として化合物5(38mg)を得た。
MS(APCI):501[M+H]+
対応原料化合物を、前記の実施例47と同様に処理することにより、下記一般式においてR1およびR2がそれぞれ下記表5に記載の構造を有する化合物を得た。
MS(APCI):394[M+H]+
対応原料化合物を、前記の実施例49と同様に処理することにより、下記一般式においてR1およびR2がそれぞれ下記表6に記載の構造を有する各化合物を得た。
MS(APCI):367[M+H]+
(2)化合物3(151mg)とチオアニソール(510mg)のジクロロメタン(2mL)溶液中に、トリフルオロ酢酸(1mL)を加え、室温にて1時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮して化合物4の粗生成物を得た。
MS(APCI):267[M+H]+
(3)化合物4(150mg)、化合物5(11mg)、及び炭酸ナトリウム(87mg)のアセトニトリル(5mL)混合液をアルゴン雰囲気下、50℃にて18時間撹拌した。反応混合物を室温まで冷却し、酢酸エチルで希釈後、水にて洗浄し、ケムエルート(登録商標)にて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/メタノール=100/0~95/5 グラジエント)にて精製し、得られた残渣を酢酸エチルで懸濁洗浄することにより、黄色固体として化合物6(77mg)を得た。
MS(APCI):366[M+H]+
対応原料化合物を、前記の実施例53と同様に処理することにより、下記一般式においてR1およびR2がそれぞれ下記表7に記載の構造を有する化合物を得た。
MS(APCI):382[M+H]+
対応原料化合物を、前記の実施例55と同様に処理することにより、下記一般式においてR1およびR2がそれぞれ下記表8に記載の構造を有する化合物を得た。
MS(APCI):479[M+H]+
対応原料化合物を、前記の実施例57と同様に処理することにより、下記一般式においてR1およびR2がそれぞれ下記表9に記載の構造を有する各化合物を得た。
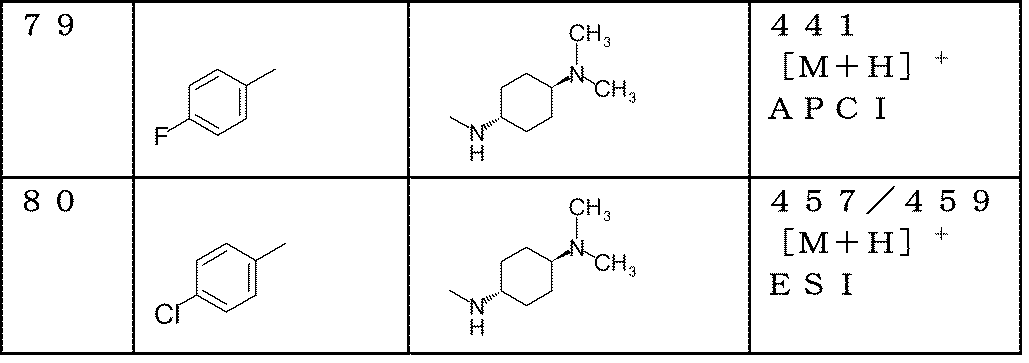
MS(APCI):358[M+H]+
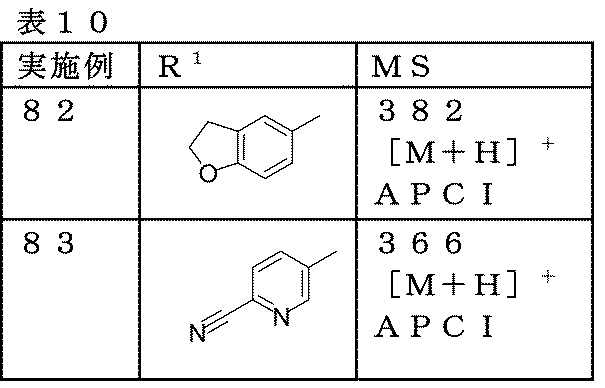
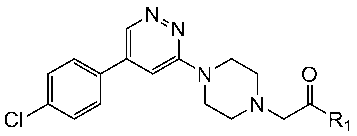
対応原料化合物を、前記の実施例81と同様に処理することにより、下記一般式においてR1がそれぞれ下記表10に記載の構造を有する各化合物を得た。
MS(APCI):360[M+H]+
MS(APCI):358[M+H]+
MS(APCI):255/257[M+H]+
(2)化合物2(6.0g)と57%ヨウ化水素酸(35mL)の混合物を加熱還流下16時間撹拌した。反応混合物を室温まで冷却し、30%チオ硫酸ナトリウム水溶液に注ぎ、酢酸エチルにて抽出した。有機層を無水硫酸マグネシウムにて乾燥、溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=85/15→クロロホルム/メタノール=90/10)にて精製することにより、淡黄色固体として化合物3(5.3g)を得た。
MS(APCI):313[M+H]+
(3)化合物3(500mg)、化合物4(413mg)、及びテトラキス(トリフェニルホスフィン)パラジウム(93mg)のジメトシキエタン(8mL)溶液中に、2mol/L炭酸ナトリウム水溶液(1.6mL)を加えアルゴン置換して、80℃で3時間撹拌した。次いで、化合物4(200mg)を加えて同温度で16時間撹拌した。室温まで冷却した後、水を加えてクロロホルムで抽出した。有機層を飽和食塩水にて洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=85/15~70/30 グラジエント)にて精製することにより、無色固体として化合物5(467mg)を得た。
MS(APCI):313[M+H]+
(4)アルミニウムクロリド(140mg)のトルエン(2.1mL)懸濁液に、化合物5(65mg)をアルゴン雰囲気下室温にて少量ずつ添加したのち加熱還流下1時間撹拌した。反応混合物を室温まで冷却し、1mol/L塩酸を加え、酢酸エチルで抽出した。有機層を無水硫酸ナトリウムにて乾燥し、溶媒を減圧留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/酢酸エチル=67/33 アイソクラティック)にて精製することにより、淡黄色固体として化合物6(34mg)を得た。
MS(APCI):223[M+H]+
(5)化合物6(30mg)をアセトニトリル(1mL)/DMF(5滴)の混合溶媒に溶解し、化合物7(70mg)、ジアザビシクロウンデセン(111μL)、及び1H-ベンゾトリアゾール-1-イルオキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロりん酸塩(BOP、78mg)を加え、室温にて35分間撹拌したのち、更に加熱還流下15時間、マイクロ波反応装置(Initiator、バイオタージ社製)中、120℃で20分間撹拌した。反応混合物を室温まで冷却し、酢酸エチルで希釈後、水にて洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をNHシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/酢酸エチル=90/10~50/50 グラジエント)にて精製することにより、淡黄色固体として化合物8(17mg)を得た。
MS(APCI):390[M+H]+
MS(APCI):221/223[M+H]+
(2)化合物2(100mg)、化合物3(103mg)、及びジクロロビス(トリフェニルホスフィン)パラジウム(16mg)のジオキサン(2mL)溶液中に、2mol/L炭酸ナトリウム水溶液(1.5mL)を加え、マイクロ波反応装置(Initiator、バイオタージ社製)中、150℃で15分間撹拌した。室温に放冷した後、酢酸エチルで希釈して、水と飽和食塩水で洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/酢酸エチル=100/0~90/10 グラジエント)にて精製した後、酢酸エチル/ヘキサンの混合溶媒で懸濁洗浄、ろ取、乾燥することにより無色固体として化合物4(69mg)を得た。
MS(APCI):331[M+H]+
(3)化合物4(53mg)をメタノール(4mL)に溶解し、10%含水パラジウム炭素(27mg)を加え、水素雰囲気下15分間撹拌した。パラジウム炭素をろ過により除去したのち、メタノールで洗浄した。ろ液を減圧下濃縮することにより、無色固体として化合物5(37mg)を得た。
MS(APCI):273[M+H]+
(4)化合物5(36mg)をアセトニトリル(1.5mL)/ジメチルアセトアミド(1.5mL)の混合溶媒に溶解し、化合物6(55mg)、ジアザビシクロウンデセン(33μL)および1H-ベンゾトリアゾール-1-イルオキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロりん酸塩(BOP、86mg)を加え、加熱還流下2時間撹拌した。反応混合物を室温まで冷却し、酢酸エチルで希釈後、水と飽和炭酸水素ナトリウム水溶液にて洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をNHシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/酢酸エチル=90/10~50/50 グラジエント)、次いでNHシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/メタノール=100/0~90/10 グラジエント)にて精製することにより、淡黄色固体として化合物7(18mg)を得た。
MS(APCI):408[M+H]+
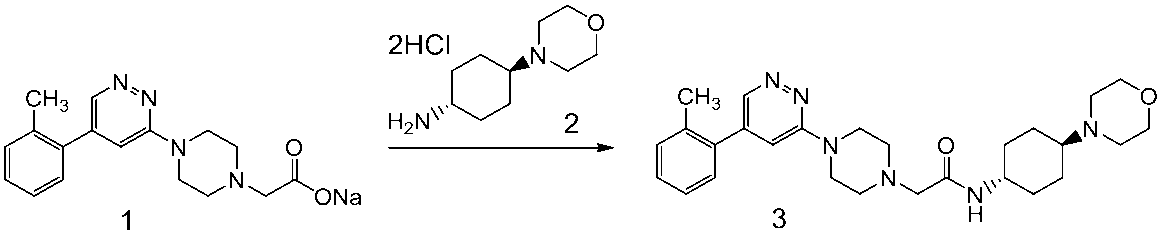
化合物1(300mg)と化合物2(290mg)をDMF(8.8mL)に懸濁し、ジイソプロピルエチルアミン(740μL)とHATU(674mg)を加え、室温下40分間撹拌した。反応混合物を水で希釈したのち、クロロホルムで抽出した。有機層を無水硫酸ナトリウムにて乾燥し、溶媒を減圧留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=30/70~0/100 グラジエント)にて精製することにより、無色固体として化合物3(440mg)を得た。
MS(APCI):517[M+H]+
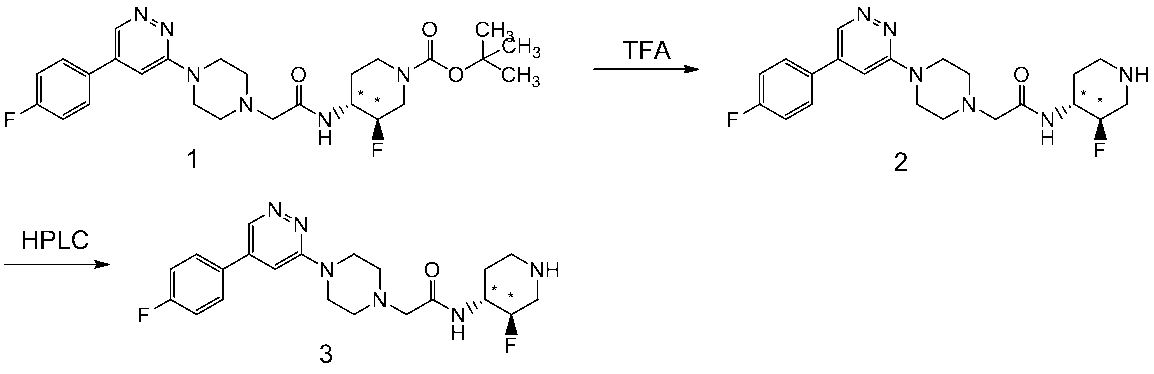
化合物1(430mg)のクロロホルム(4mL)溶液中に、トリフルオロ酢酸(4mL)を加え、室温にて17時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/アンモニア水(10%メタノール溶液)=60/40 アイソクラティック)で精製することにより、無色固体としてラセミの化合物2を得た。このラセミ体をリサイクルHPLC(Chiralpak IC (30×250), メタノール/THF/ジエチルアミン=95/5/0.5、流速20mL/分)にて分画することで、それぞれのエナンチオマー(実施例89a、無色固体、142mg、及び実施例89b、無色固体、69mg)を得た。
実施例89a
保持時間:9.38分 (Chiralpak IC-3(4.6×150)、メタノール/THF/ジエチルアミン=95/5/0.5、流速0.5mL/分)
光学純度:98.3%ee
MS(APCI):417[M+H]+
実施例89b
保持時間:10.3分(Chiralpak IC-3(4.6×150)、メタノール/THF/ジエチルアミン=95/5/0.5、流速0.5mL/分)
光学純度:96.4%ee
MS(APCI):417[M+H]+
対応原料化合物を、前記の実施例89と同様に処理することにより、下記一般式においてR1がそれぞれ下記表11に記載の構造を有する各化合物を得た。ただし、式中、*で標識した炭素原子の置換基の立体表記は相対立体配置(トランス)であることを示すものであって絶対立体配置を示すものではない。
実施例91a
保持時間:6.42分(Chiralpak IC-3(4.6×150)、メタノール/THF/ジエチルアミン=60/40/0.1、流速0.5mL/分)
光学純度:>99.8%ee
MS(APCI):443/445[M+H]+
実施例91b
保持時間:8.90分(Chiralpak IC-3(4.6×150)、メタノール/THF/ジエチルアミン=60/40/0.1、流速0.5mL/分)
光学純度:99.7%ee
MS(APCI):443/445[M+H]+
MS(APCI):145/147[M+H]+
(2)化合物2(1.0g)、化合物3(4.2g)、及び1,1’-ビス(ジフェニルホスフィノ)フェロセンパラジウムジクロリドジクロロメタン錯体(252mg)のジオキサン(35mL)溶液中に、2mol/L炭酸ナトリウム水溶液(14mL)を加え、アルゴン置換した後、80℃で20時間撹拌した。室温に放冷して水で希釈した後、クロロホルムで抽出した。有機層を無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=80/20~30/70 グラジエント)にて精製して化合物4(200mg)を得た。
MS(APCI):205[M+H]+
(3)化合物4(100mg)をピリジン(2.5mL)に懸濁した後、氷冷下トリフルオロメタンスルホン酸無水物(165μL)を加え、同温度で80分間撹拌した。反応混合物を水で希釈した後、クロロホルムで抽出した。有機層を無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=95/5~85/15 グラジエント)にて精製して化合物5(126mg)を得た。化合物5(100mg)をジメチルスルホキシド(3mL)に溶解した後、室温で化合物6(553mg)とジイソプロピルエチルアミン(260μL)を加え、50℃で4時間加熱撹拌した。室温に放冷した後、水を加えて、酢酸エチル/ヘキサンの混合溶媒で抽出した。有機層を硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=70/30~50/50 グラジエント)、次いでNHシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=90/10~0/100 グラジエント)にて精製することにより、化合物7(51mg)を得た。
MS(ESI):373[M+H]+
(4)化合物7(50mg)のクロロホルム(0.5mL)溶液中に、トリフルオロ酢酸(0.5mL)を加え、室温にて1.5時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(Porapak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮した。濃縮残渣をアセトニトリル(1.3mL)に溶解して、炭酸ナトリウム(71mg)と化合物8(55mg)を加え、65℃にて20時間撹拌した。反応混合物を水で希釈後、酢酸エチルで抽出し、有機層を無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をNHシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=50/50~30/70 グラジエント)にて精製することにより、無色固体として化合物9(32mg)を得た。
MS(APCI):372[M+H]+
MS(APCI):342/344[M+H]+
(2)化合物3(8.8g)と化合物4(7.2g)、ジクロロビス(トリフェニルホスフィン)パラジウム(905mg)のジオキサン(130mL)混合液中に、2mol/L炭酸ナトリウム水溶液(52mL)を加え、80℃にて1時間撹拌した。反応混合物を室温まで冷却し、水を加えた後、クロロホルムで3回抽出した。無水硫酸ナトリウムにて乾燥した後、溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/酢酸エチル=10/1~25/1 グラジエント)にて精製し、無色固体として化合物5(8.1g)を得た。
MS(APCI):358[M+H]+
(3)化合物5(8.1g)のジクロロメタン(81mL)溶液中に、トリフルオロ酢酸(81mL)を氷冷下加え、室温にて1時間撹拌した。反応混合物の溶媒を留去し、クロロホルムに溶解させた後1mol/L水酸化ナトリウム水溶液にて中和した。有機層と水層を分離し、水層をクロロホルムにて3回抽出した。有機層を水で抽出した後、無水硫酸ナトリウムにて乾燥させ、溶媒を減圧留去した。得られた結晶性残渣をジエチルエーテル/ヘキサンで懸濁洗浄、ろ取することにより、無色固体として化合物6(1.2g)を得た。
MS(APCI):258[M+H]+
対応原料化合物を、前記の参考例1と同様に処理することにより、下記表12に記載の各化合物を得た。
MS(APCI):366[M+H]+
(2)化合物3(292mg)とチオアニソール(993mg)のジクロロメタン(4mL)溶液中に、トリフルオロ酢酸(2mL)を加え、室温にて3時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(Parapak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/アンモニア水(10%メタノール溶液)=90/10)にて精製し、化合物4を得た。
MS(APCI):266[M+H]+
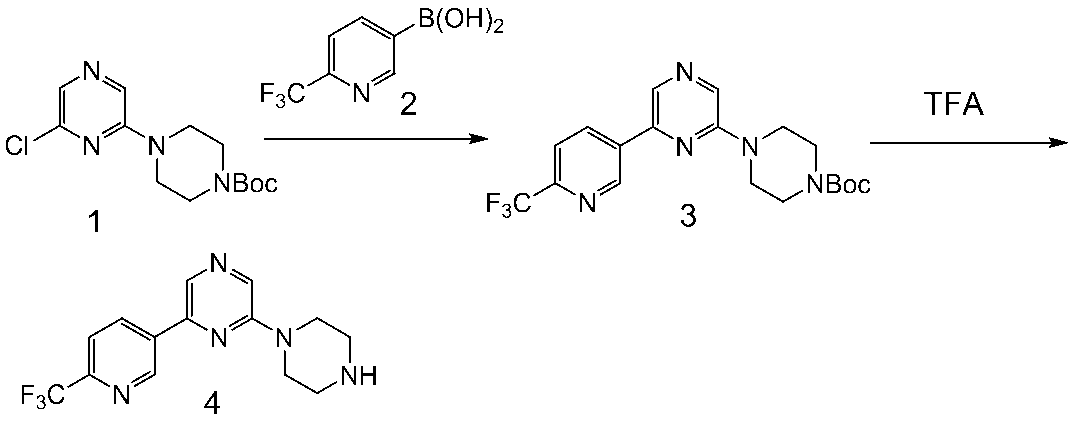
MS(APCI):299/301[M+H]+
(2)化合物3(2.0g)、化合物4(1.1g)、トリス(ジベンジリデンアセトン)ジパラジウム(306mg)、トリ-t-ブチルホスフィン(1mol/Lトルエン溶液、0.67mL)、及び炭酸セシウム(8.7g)のTHF(100mL)混合液をアルゴン雰囲気下21時間加熱還流した。反応混合物を室温まで冷却し、酢酸エチル/水で希釈後、セライトろ過した。ろ液を水、飽和食塩水にて洗浄し、無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=80/20~60/40 グラジエント)にて精製し、得られた結晶性残渣を酢酸エチル/ヘキサンで懸濁洗浄、ろ取、乾燥することにより、黄色固体として化合物5(1.3g)を得た。
MS(APCI):375/377[M+H]+
(3)化合物5(1.3g)のジクロロメタン(10mL)溶液に、トリフルオロ酢酸(5mL)を加え、室温にて18時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮して得られた結晶性残渣をジイソプロピルエーテル/ヘキサンで懸濁洗浄、ろ取、乾燥することにより、黄色固体として化合物6(849mg)を得た。
MS(APCI):275/277[M+H]+
対応原料化合物を、前記の参考例7と同様に処理することにより、下記表13に記載の各化合物を得た。
MS(APCI):410[M+H]+
(2)化合物3(182mg)のジクロロメタン(2mL)溶液に、トリフルオロ酢酸(1mL)を氷冷下加え、室温にて2時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮することにより、黄色固体として化合物4(142mg)を得た。
MS(APCI):310[M+H]+
MS(ESI):359[M+H]+
(2)化合物3(1.78g)とトリエチルアミン(9mL)のメタノール(50mL)溶液に、10%含水パラジウム炭素(530mg)を加え、水素雰囲気下室温にて2時間撹拌した。反応混合物をセライト濾過し溶媒を減圧留去した後、再びメタノール(50mL)溶液とし、トリエチルアミン(9mL)と10%含水パラジウム炭素(530mg)を加え、水素雰囲気下室温にて18時間撹拌した。反応混合物をセライト濾過した後、溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=80/20~60/40 グラジエント)にて精製することにより、淡黄色粘体として化合物4(1.4g)をシス体とトランス体の混合物(3:2、主生成物は未決定)として得た。
MS(APCI):361[M+H]+
(3)化合物4(200mg)のクロロホルム(3mL)溶液に、トリフルオロ酢酸(6mL)を加え、室温にて22時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮することにより、黄色固体として化合物5(121mg)をシス体とトランス体の混合物(3:2、主生成物は未決定)として得た。
MS(APCI):261[M+H]+
MS(APCI):298/300[M+H]+
MS(APCI):187[M+H]+
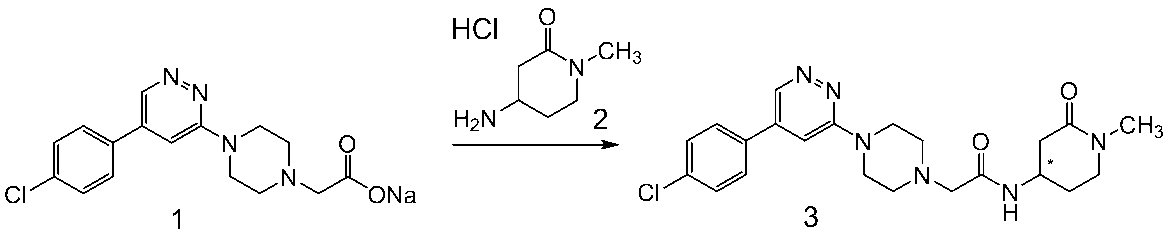
(2)化合物3(4.26g)、化合物4(12.8g)、1H-ベンゾトリアゾール-1-イルオキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロりん酸塩(BOP、15.2g)、及びジアザビシクロウンデセン(10.3mL)をDMF(110mL)に加え、アルゴン置換した後、80℃で18時間撹拌した。室温に放冷した後、反応混合物に水を加えた後、酢酸エチルで抽出した。有機層を飽和炭酸水素ナトリウム水溶液、飽和食塩水で洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/酢酸エチル=100/0~90/10 グラジエント)にて精製することにより、黄色固体として化合物5(5.0g)を得た。
MS(APCI):355[M+H]+
(3)化合物5(5.0g)をクロロホルム(70mL)に溶解し、トリフルオロ酢酸(70mL)を加え、室温で3時間撹拌した。溶媒を減圧留去し、残渣に20%炭酸カリウム水溶液を加え、クロロホルムで抽出した。有機層を水と飽和食塩水で洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をNHシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/酢酸エチル=100/0~50/50 グラジエント)にて精製した後、ジイソプロピルエーテルで懸濁洗浄、ろ取、乾燥することにより、無色固体として化合物6(3.20g)を得た。
MS(APCI):255[M+H]+
(4)化合物6(3.20g)をアセトニトリル(60mL)に溶解し、化合物7(1.70g)と炭酸ナトリウム(2.67g)を加え、65℃で18時間撹拌した。溶媒を減圧留去し、残渣に水を加えて、クロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 酢酸エチル/メタノール=100/0~95/5 グラジエント)にて精製した後、ジイソプロピルエーテルで懸濁洗浄、ろ取、乾燥した。次いで、酢酸エチルに加熱溶解した後、氷冷し生じた固体をろ取、乾燥することで茶色固体として化合物8(2.40g)を得た。
MS(APCI):341[M+H]+
(5)化合物8(2,40g)をエタノール(50mL)に溶解し、1mol/L水酸化ナトリウム水溶液(5.3mL)を加え、室温にて3時間撹拌した。反応混合物を濃縮し、得られた残渣にエタノールを加えて懸濁洗浄、ろ取、乾燥することにより、無色固体として化合物9(2.10g)を得た。
MS(ESI):311[M+Na]―
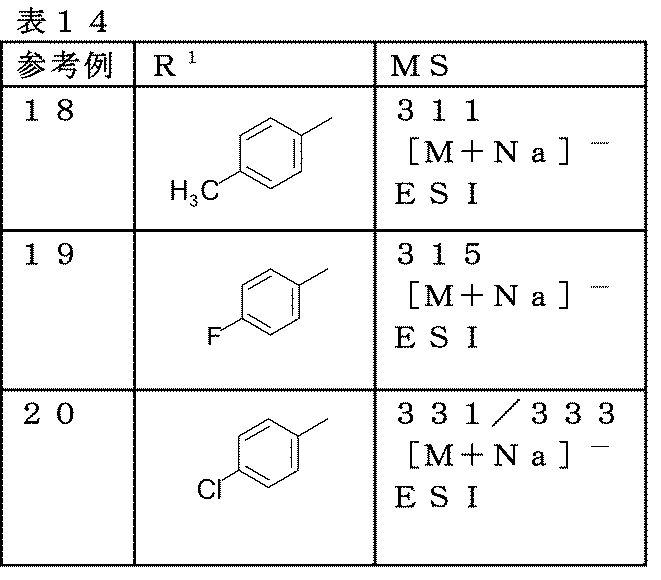
対応原料化合物を、前記の参考例17と同様に処理することにより、下記一般式においてR1がそれぞれ下記表14に記載の構造を有する各化合物を得た。
MS(APCI):299/301[M+H]+
(2)化合物3(600mg)をクロロホルム(6mL)に溶解し、トリフルオロ酢酸(12mL)を加え、室温で23時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮することにより、淡黄色固体として化合物4(315mg)を得た。
MS(APCI):199/201[M+H]+
(3)化合物4(312mg)をアセトニトリル(10mL)に溶解し、化合物5(319mg)と炭酸ナトリウム(333mg)を加え、室温で4日間撹拌した。反応混合物に飽和炭酸ナトリウム水溶液を加えて、クロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水炭酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 酢酸エチル/メタノール=100/0~90/10 グラジエント)にて精製することで無色固体として化合物6(405mg)を得た。
MS(APCI):298/00[M+H]+
MS(APCI):217[M+H]+
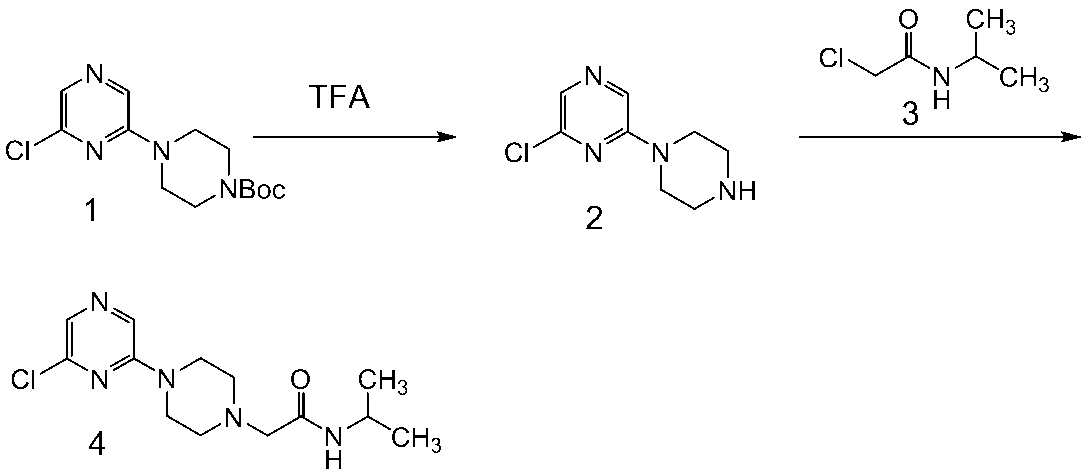
(2)化合物3(4.3g)をオキシ塩化リン(30.5g)に加えて、120℃で25分間撹拌した。反応混合物を減圧濃縮した後、残渣にクロロホルムと飽和炭酸ナトリウム水溶液を加えて、不溶物をろ過した。ろ液の有機層を無水硫酸マグネシウムで乾燥後、溶媒を減圧留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=80/20~50/50 グラジエント)にて精製することにより、淡黄色固体として化合物4(613mg)を得た。
MS(APCI):235/237[M+H]+
(3)化合物4(285mg)と化合物5(1.05g)をジメチルアセトアミド(4mL)に懸濁して、マイクロ波反応装置(Initiator、バイオタージ社製)中、120℃で20分間撹拌した。同様の操作を繰り返し、合わせた反応混合物に炭酸カリウム水溶液を加えて、クロロホルムで抽出した。有機層を無水硫酸ナトリウムにて乾燥した後、溶媒を減圧留去し、得られた残渣を酢酸エチル/ヘキサンの混合溶媒で懸濁洗浄、ろ取した。ろ過物とろ液を合わせて濃縮後、シリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/アンモニア水(10%メタノール溶液)=100/0~90/10 グラジエント)にて精製することにより、淡茶色固体として化合物6(587mg)を得た。
MS(APCI):285[M+H]+
(4)化合物6(578mg)をアセトニトリル(18mL)に溶解し、化合物7(373mg)と炭酸ナトリウム(431mg)を加え、室温で7時間撹拌した。反応混合物を酢酸エチルで希釈して、水で洗浄した。水層は酢酸エチルで抽出して、合わせた有機層を無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/メタノール=100/0~95/5 グラジエント)にて精製することで橙色固体として化合物8(535mg)を得た。
MS(APCI):357[M+H]+
(5)化合物8(527mg)をメタノール(5mL)に溶解し、1mol/L水酸化ナトリウム水溶液(3mL)を加え、室温にて5分間撹拌した。メタノール(5mL)と水(1mL)を加えて同温度で25分間撹拌した。反応混合物を減圧濃縮した後、水に溶解して1mol/L塩酸を加えて、析出物をろ取、乾燥することにより、無色固体として化合物9(441mg)を得た。
MS(APCI):343[M+H]+
MS(APCI):371[M+H]+
(2)化合物3(1.19g)のクロロホルム(6.5mL)溶液に、トリフルオロ酢酸(6.5mL)を加え、室温にて1時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮することにより、無色固体として化合物4(870mg)を得た。
MS(APCI):271[M+H]+
(3)化合物4(867mg)のアセトニトリル(32mL)溶液に、炭酸ナトリウム(680mg)と化合物5(378μL)を加え、65℃にて18時間撹拌した。反応混合物を水で希釈後、酢酸エチルで抽出し、有機層を無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をNHシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル=50/50~20/80 グラジエント)にて精製することにより、無色固体として化合物6(915mg)を得た。
MS(APCI):357[M+H]+
(4)化合物6(915mg)をエタノール(12.5mL)/THF(12.5mL)の混合溶媒に溶解し、1mol/L水酸化ナトリウム水溶液(5.1mL)を加え、室温にて1時間撹拌した。反応混合物を減圧濃縮し、水に溶解して1mol/L塩酸を加えて、析出物をろ取、乾燥することにより、無色固体として化合物7(986mg)を得た。
MS(APCI):329[M+H]+
MS(APCI):209[M+H]+
(2)化合物3(614mg)、化合物4(1.65g)、1H-ベンゾトリアゾール-1-イルオキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロりん酸塩(BOP、2.0g)、及びジアザビシクロウンデセン(1.32mL)をDMF(30mL)に加え、アルゴン置換した後、80℃で13.5時間撹拌した。室温に放冷した後、反応混合物に水と飽和炭酸水素ナトリウム水溶液を加え、クロロホルムで抽出した。有機層を無水硫酸マグネシウムにて乾燥した後、溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 ヘキサン/酢酸エチル65/35~50/50 グラジエント)にて精製することにより、淡黄色固体として化合物5(808mg)を得た。
MS(APCI):377[M+H]+
(3)化合物5(791mg)をクロロホルム(10mL)に溶解し、トリフルオロ酢酸(7.9mL)を加え、室温で1時間撹拌した。反応混合物をメタノールで希釈後、強陽イオン交換充填剤(PoraPak Rxn Cx、溶出液 アンモニア(1mol/Lメタノール溶液))にて処理し、溶出液を減圧下濃縮した。得られた残渣をアセトニトリル(15mL)に溶解し、化合物6(270μL)と炭酸ナトリウム(445mg)を加え、60℃で7.5時間撹拌した。反応混合物を酢酸エチルで希釈して、水と飽和食塩水で洗浄し、無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出液 クロロホルム/メタノール=100/0~95/5 グラジエント)にて精製することで黄色液体として化合物7(614mg)を得た。
MS(APCI):363[M+H]+
(4)化合物7(595mg)をエタノール(6mL)に溶解し、1mol/L水酸化ナトリウム水溶液(3.3mL)を加え、室温にて30分間撹拌した。反応混合物を濃縮し、水に溶解して1mol/L塩酸を加えて、析出物をろ取、乾燥することにより、無色固体として化合物8(434mg)を得た。
MS(APCI):335[M+H]+
<実験方法>
チャイニーズハムスター肺線維芽細胞V79細胞株にpcDNA3.1-ヒトCyp11B2プラスミドをトランスフェクションし、ヒトCyp11B2遺伝子の安定発現株を作製した。
本細胞を10%ウシ胎児血清、1% G418二硫酸塩溶液を添加したダルベッコ修飾イーグルハム培地で、37℃、95%空気、5%CO2環境下で培養および増殖させて細胞を回収した。
次に、Chabre et al. JCE&M 85(11) 4060-68, 2000の方法を参考にミトコンドリアを画分取得した。具体的には250 mmol/L スクロースを含有する5 mmol/L Tris-HCl buffer (pH 7.4) で懸濁した細胞をテフロン(登録商標)ポッターエルベージェムホモジナイザーでホモジナイズしたのちに懸濁液を遠心分離(800×gで15分)した。上清を分取したのちに再び遠心分離(10000×gで15分)し、ペレット(ミトコンドリア画分)を取得した。
96ウェルプレートに10 mmol/L KH2PO4、10 mmol/L Tris、20 mmol/L KCl、25 mmol/L スクロース、5 mmol/L MgCl2、0.05% ウシ血清アルブミンを含むバッファーを用いて希釈したミトコンドリア画分を分注した。0.5μmol/L デオキシコルチコステロン、150μmol/L NADPH、各濃度の化合物を添加し、1.5~2時間室温でインキュベーションしてアルドステロンを産生させた。溶液中のアルドステロン産生量をHTRF(Homogeneous Time Resolved Fluorescense)法を用いて測定した。
各濃度の化合物のアルドステロン産生阻害率(%)からロジスティック曲線による非線形回帰を行ってIC50(nmol/L)を算出した。
Claims (26)
- 下式[I]:
X及びYは以下の(1)~(3)のいずれかを表し、
(1)XがN、かつYがCH又はC-RY、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RYはアルキル基を表し;
RAは置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、又は部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基を表し;
R1は水素原子、又はアルキル基を表し;
R2は置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよい脂肪族複素環基、又は部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基を表し;
R3は水素原子、又はアルキル基を表す〕で示される化合物又はその薬理的に許容し得る塩。 - RAで表される置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立して、ハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分が6~10員単環又は二環式アリールであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分が硫黄原子、酸素原子、及び窒素原子からなる群より独立して選ばれる1~2個の異項原子を含む、6~10員単環又は二環式ヘテロアリールであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
(ii)置換されていてもよいシクロアルキル基、(iii)置換されていてもよい脂肪族複素環基、及び(iv)部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基、水酸基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iv)の各置換基において脂肪族複素環基は独立して、硫黄原子、酸素原子、又は窒素原子から選ばれる1~2個の異項原子を含む4~9員単環又は二環式脂肪族複素環基であり、
上記(i)~(iv)の各置換基においてヘテロアリール基は独立して、硫黄原子、酸素原子、及び窒素原子からなる群より独立して選ばれる1~4個の異項原子を含む、5~10員単環又は二環式ヘテロアリール基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分が硫黄原子、酸素原子、及び窒素原子からなる群より独立して選ばれる1~3個の異項原子を含む4~9員単環又は二環式脂肪族複素環であり;
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分が5~10員単環又は二環式ヘテロアリールである、請求項1に記載の化合物又はその薬理的に許容し得る塩。 - RAで表される置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立して、ハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分がフェニル、又はナフチルであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分がピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、又はベンゾピラニルであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
R2で表される(ii)置換されていてもよいシクロアルキル基、(iii)置換されていてもよい脂肪族複素環基、及び(iv)部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;水酸基、1~2個のアルキル基で置換されていてもよいカルバモイル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iv)の各置換基において脂肪族複素環基は独立して、アゼチジニル、オキセタニル、ピロリジニル、テトラヒドロチエニル、テトラヒドロフラニル、チアゾリジニル、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、ホモモルホリニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、及び3-オキソ-9-アザビシクロ[3.3.1]ノニルからなる群より選ばれる基であり、
上記(i)~(iv)の各置換基においてヘテロアリール基は独立して、ピロリル、フラニル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、チアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、及びベンゾピラニルからなる群より選ばれる基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分は、アゼチジニル、オキセタニル、ピロリジニル、テトラヒドロチエニル、テトラヒドロフラニル、チアゾリジニル、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、ホモモルホリニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分は、ピロリル、フラニル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、チアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、又はベンゾピラニルである、請求項1又は2のいずれかに記載の化合物又はその薬理的に許容し得る塩。 - RAで表される置換されていてもよいシクロアルキル基、置換されていてもよいシクロアルケニル基、置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立して、ハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分がフェニル、又はナフチルであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル、又はベンゾフラニルであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
R2で表される(ii)置換されていてもよいシクロアルキル基、(iii)置換されていてもよい脂肪族複素環基、及び(iv)部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;水酸基、1~2個のアルキル基で置換されていてもよいカルバモイル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iv)の各置換基において脂肪族複素環基は独立して、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、及びテトラヒドロピラニルから選ばれる基であり、
上記(i)~(iv)の各置換基においてヘテロアリール基は独立して、ピリミジニル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分が、ピロリジニル、ピペリジニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分が、ピラゾリル、ピリジル、又はベンゾイミダゾリルである、請求項1~3のいずれかに記載の化合物又はその薬理的に許容し得る塩。 - RAが
(1)アルキル基で置換されていてもよいシクロアルキル基、
(2)アルキル基で置換されていてもよいシクロアルケニル基、
(3)ハロゲン原子、アルキル基、ハロアルキル基、アルコキシアルキル基及びアルコキシ基からなる群より独立して選ばれる1~3個の基で置換されていてもよいフェニル基、
(4)ナフチル基、又は
(5)部分的に水素化されていてもよく、シアノ基、アルキル基、及びハロアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいヘテロアリール基であり、
RAで表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル又はベンゾフラニルであり、
R1が水素原子、又はアルキル基であり、
R2が
(i)水酸基;ハロゲン原子;及び、水酸基、オキソ基、アルキル基、アルコキシカルボニル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はピペリジニル基、ピペラジニル基、モルホリニル基、又はチオモルホリニル基である)からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基、
(ii)水酸基;水酸基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及び、水酸基、及びオキソ基からなる群より独立して選ばれる1~2個の基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はピペリジニル基、モルホリニル基、又はピペラジニル基である)からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基、水酸基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアルキル基;アルコキシ基;アルコキシカルボニル基;テトラヒドロピラニル基;及び、ピリミジニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)部分的に水素化されていてもよく、1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルキル基で置換されていてもよいヘテロアリール基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分がピロリジニル、ピペリジニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピラゾリル、ピリジル、又はベンゾイミダゾリルであり、
R3が水素原子である、請求項4に記載の化合物又はその薬理的に許容し得る塩。 - XがNであり、YがCH又はC-RYであり、
RYがアルキル基であり、
RAが
(1)アルキル基で置換されていてもよいシクロヘキシル基、
(2)アルキル基で置換されていてもよいシクロヘキセニル基、
(3)ハロゲン原子、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~2個の基で置換されていてもよいフェニル基、
(4)ナフチル基、又は
(5)部分的に水素化されていてもよく、シアノ基で置換されていてもよいヘテロアリール基であり、
RAで表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、又はベンゾフラニルであり、
R1が水素原子であり、
R2が
(i)水酸基;及びオキソ基、アルキル基、アルコキシカルボニル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はピペリジニル基、ピペラジニル基、モルホリニル基、又はチオモルホリニル基から選ばれる)からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基、
(ii)1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びモルホリニル基からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基、水酸基、及びアルキルスルホニル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアルキル基;アルコキシカルボニル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)ピリジル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分がピペリジニル、テトラヒドロチオピラニル、又はテトラヒドロピラニルであり、
R3が水素原子である、請求項4に記載の化合物又はその薬理的に許容し得る塩。 - XがCHであり、YがNであり、
RAが
(1)アルキル基で置換されていてもよいシクロヘキシル基、
(2)ハロゲン原子、アルキル基、及びハロアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいフェニル基、又は
(3)部分的に水素化されていてもよく、シアノ基、及びアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいヘテロアリール基であり、
RAで表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル、又はベンゾフラニルであり、
R1が水素原子又はアルキル基であり、
R2が
(i)水酸基;ハロゲン原子;及び、水酸基、及びアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいピペリジニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基、
(ii)水酸基;水酸基で置換されていてもよいアルキル基;アルコキシ基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及び、1~2個のオキソ基で置換されていてもよい脂肪族複素環基(ここにおいて、該脂肪族複素環基はモルホリニル基、又はピペラジニル基から選ばれる)からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)オキソ基;アルキルスルホニル基で置換されていてもよいアルキル基;テトラヒドロピラニル基;及びピリミジニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルキル基で置換されていてもよいピラゾリル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分がピロリジニル、ピペリジニル、テトラヒドロチオピラニル、又は1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)であり、
R3が水素原子である、請求項4に記載の化合物又はその薬理的に許容し得る塩。 - XがCHであり、YがCHであり、
RAが
(1)アルキル基で置換されていてもよいシクロヘキシル基、
(2)アルキル基で置換されていてもよいシクロヘキセニル基、
(3)ハロゲン原子、及びアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいフェニル基、又は
(4)部分的に水素化されていてもよく、シアノ基、アルキル基、及びハロアルキル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいヘテロアリール基であり、
RAで表される水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピリジル、インダゾリル、又はベンゾフラニルであり、
R1が水素原子であり、
R2が
(i)水酸基で置換されていてもよいアルキル基、
(ii)アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及び、水酸基で置換されていてもよいピペリジニル基からなる群から独立して選ばれる1~3個の基で置換されていてもよいシクロアルキル基、
(iii)水酸基;アルキル基;及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基、又は
(iv)部分的に水素化されていてもよく、1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルキル基で置換されていてもよいヘテロアリール基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分が8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルであり、
R2で表される部分的に水素化されていてもよく、置換されていてもよいヘテロアリール基において該ヘテロアリール部分がピラゾリル、又はベンゾイミダゾリルであり、
R3が水素原子である、請求項4に記載の化合物又はその薬理的に許容し得る塩。 - X及びYが以下の(1)~(3)のいずれかであり、
(1)XがN、かつYがCH、
(2)XがCH、かつYがN、又は
(3)XがCH、かつYがCH;
RAが置換されていてもよいアリール基、又は部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基であり;
R1が水素原子であり;
R2が置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、又は置換されていてもよい脂肪族複素環基であり;
R3が水素原子である、請求項1に記載の化合物又はその薬理的に許容し得る塩。 - RAで表される置換されていてもよいアリール基、及び部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基の各置換基が独立して、ハロゲン原子、シアノ基、アルキル基、ハロアルキル基、アルコキシアルキル基、及びアルコキシ基からなる群より独立して選ばれる1~3個の基であり、
RAで表される置換されていてもよいアリール基において該アリール部分がフェニル、又はナフチルであり、
RAで表される部分的に水素化されていてもよく、置換されていてもよい6~10員単環又は二環式ヘテロアリール基において該ヘテロアリール部分がピリジル、ピラジニル、ピリミジニル、ピリダジニル、チアジニル、トリアジニル、インドリル、イソインドリル、インダゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、ベンゾフラニル、キノリル、イソキノリル、イミダゾピリジル、又はベンゾピラニルであり;
R2で表される(i)置換されていてもよいアルキル基の置換基が、ハロゲン原子;水酸基;オキソ基;1~2個のアルキル基で置換されていてもよいカルバモイル基;アルキルスルホニル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基、及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
R2で表される(ii)置換されていてもよいシクロアルキル基、及び(iii)置換されていてもよい脂肪族複素環基の各置換基が独立して、ハロゲン原子;水酸基;オキソ基;水酸基、1~2個のアルキル基で置換されていてもよいカルバモイル基、及びアルキルスルホニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよいアルキル基;1~2個のアルキル基で置換されていてもよいカルバモイル基で置換されていてもよいアルコキシ基;水酸基、オキソ基、アルキル基、アルキルスルホニル基、及びアルコキシカルボニル基からなる群より独立して選ばれる1~3個の基で置換されていてもよい脂肪族複素環基;アルコキシカルボニル基;アルキル基及びアルカノイル基からなる群より独立して選ばれる1~2個の基で置換されていてもよいアミノ基;及びヘテロアリール基からなる群より独立して選ばれる1~3個の基であり、
上記(i)~(iii)の各置換基において脂肪族複素環基は独立して、ピペリジニル、ピペラジニル、モルホリニル、チオモルホリニル、及びテトラヒドロピラニルからなる群より選ばれる基であり、
上記(i)~(iii)の各置換基においてヘテロアリール基は独立して、ピリミジニル基であり、
R2で表される置換されていてもよい脂肪族複素環基において該脂肪族複素環部分は、ピロリジニル、ピペリジニル、テトラヒドロチオピラニル、テトラヒドロピラニル、1-アザビシクロ[2.2.2]オクチル(キヌクリジニル)、8-アザビシクロ[3.2.1]オクチル、3-オキサビシクロ[3.3.1]ノニル、又は3-オキソ-9-アザビシクロ[3.3.1]ノニルである、請求項9に記載の化合物又はその薬理的に許容し得る塩。 - RAがハロゲン原子で置換されていてもよいフェニル基、又は部分的に水素化されていてもよくアルキル基で置換されていてもよいインダゾリル基であり、
R2が
(1)アルキル基、
(2)1~2個のアルキル基で置換されていてもよいアミノ基で置換されていてもよいシクロヘキシル基、若しくはアルコキシ基で置換されていてもよいシクロヘキシル基、又は
(3)アルキル基で置換されていてもよい8-アザビシクロ[3.2.1]オクチルである、請求項9に記載の化合物又はその薬理的に許容し得る塩。 - 3-[4-[(trans-4-メトキシシクロヘキシル)カルバモイルメチル]ピペラジン-1-イル]-5-(1-メチル-1H-インダゾール-6-イル)ピラジン;
3-[4-(イソプロピルカルバモイルメチル)ピペラジン-1-イル]-5-(1-メチル-1H-インダゾール-6-イル)ピラジン;
5-(4-フルオロフェニル)-3-[4-[[trans-4-(N,N-ジメチルアミノ)シクロヘキシル]カルバモイルメチル]ピペラジン-1-イル]ピリダジン;及び
3-(4-クロロフェニル)-5-[4-[(exo-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル)カルバモイルメチル]ピペラジン-1-イル]ピリジン
からなる群より選ばれる化合物又はその薬理的に許容し得る塩。 - 請求項1~12のいずれかに記載の化合物又はその薬理的に許容し得る塩を有効成分として含有する、医薬組成物。
- アルドステロンレベルの増大及び/又はアルドステロンの過剰産生により惹起される各種の疾患及び/又は疾患状態の予防又は治療、或いはこれら疾患の予後改善に使用される、請求項13に記載の医薬組成物。
- 原発性アルドステロン症、二次性アルドステロン症、高血圧、心不全、心筋症、心肥大、心筋梗塞、心筋壊死病変、心筋虚血後障害、冠動脈疾患、心筋又は血管の線維化又はリモデリング、血管再狭窄、血管壁肥厚、動脈硬化、急性腎障害、慢性腎臓病、腎線維化、腎症、低カリウム血症、肥満、メタボリック症候群、睡眠時無呼吸症候群、網膜症、肝疾患、突発性及び/又は周期性浮腫、又は交感神経亢進の予防又は治療剤である、請求項13に記載の医薬組成物。
- 原発性アルドステロン症、二次性アルドステロン症、高血圧、心不全、動脈硬化、腎症、又は網膜症の予防又は治療剤である、請求項13に記載の医薬組成物。
- 原発性アルドステロン症が片側性又は両側性副腎腺腫、片側性又は両側性副腎過形成、アルドステロン産生副腎癌、片側副腎性多発小結節アルドステロン症、糖質コルチコイド反応性アルドステロン症、家族性アルドステロン症、又は異所性アルドステロン産生腫瘍である、請求項15又は16のいずれかに記載の医薬組成物。
- 二次性アルドステロン症がエストロゲン製剤に起因する高血圧、腎血管性高血圧、妊娠高血圧、悪性高血圧、褐色細胞腫、うっ血性心不全、偽性低アルドステロン症、腹水を随伴した慢性肝疾患、下剤及び利尿薬などの薬剤不適切使用、又はネフローゼ症候群、バーター症候群もしくはギッテルマン症候群にともなう高アルドステロン血症である、請求項15又は16のいずれかに記載の医薬組成物。
- 心不全がうっ血性心不全、左室不全、右室不全、収縮機能不全又は拡張機能不全である、請求項15又は16のいずれかに記載の医薬組成物。
- 腎症が糖尿病性腎症である、請求項15又は16のいずれかに記載の医薬組成物。
- 腹水を随伴した慢性肝疾患が肝硬変である、請求項18に記載の医薬組成物。
- 網膜症が糖尿病性網膜症である、請求項15又は16のいずれかに記載の医薬組成物。
- 高血圧が本態性高血圧、二次性高血圧、治療抵抗性高血圧またはミネラルコルチコイド関連高血圧である、請求項15又は16のいずれかに記載の医薬組成物。
- 二次性高血圧が腎血管性高血圧、腎実質性高血圧、原発性アルドステロン症、褐色細胞腫、睡眠時無呼吸症候群、クッシング症候群、薬剤誘発性高血圧、大動脈狭窄症または副甲状腺機能亢進症である、請求項23に記載の医薬組成物。
- 治療上有効な量の、請求項1~12のいずれかに記載の化合物又はその薬理的に許容し得る塩を、患者に投与する工程を含む、アルドステロンレベルの増大及び/又はアルドステロンの過剰産生により惹起される各種の疾患及び/又は疾患状態の予防又は治療方法。
- 疾患及び/又は疾患状態が原発性アルドステロン症、二次性アルドステロン症、高血圧、心不全、心筋症、心肥大、心筋梗塞、心筋壊死病変、心筋虚血後障害、冠動脈疾患、心筋又は血管の線維化又はリモデリング、血管再狭窄、血管壁肥厚、動脈硬化、急性腎障害、慢性腎臓病、腎線維化、腎症、低カリウム血症、肥満、メタボリック症候群、睡眠時無呼吸症候群、網膜症、肝疾患、突発性及び/又は周期性浮腫、又は交感神経亢進である、請求項25に記載の予防又は治療方法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ES16857539T ES2882138T3 (es) | 2015-10-23 | 2016-10-21 | Nuevo compuesto heterocíclico aromático que contiene nitrógeno |
| EP16857539.7A EP3381904B1 (en) | 2015-10-23 | 2016-10-21 | Novel nitrogen-containing aromatic heterocyclic compound |
| US15/769,844 US10717731B2 (en) | 2015-10-23 | 2016-10-21 | Nitrogen-containing aromatic heterocyclic compound |
| JP2017545804A JP6545275B2 (ja) | 2015-10-23 | 2016-10-21 | 新規含窒素芳香族複素環化合物 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015-208888 | 2015-10-23 | ||
| JP2015208888 | 2015-10-23 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2017069226A1 true WO2017069226A1 (ja) | 2017-04-27 |
Family
ID=58557108
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2016/081214 WO2017069226A1 (ja) | 2015-10-23 | 2016-10-21 | 新規含窒素芳香族複素環化合物 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US10717731B2 (ja) |
| EP (1) | EP3381904B1 (ja) |
| JP (1) | JP6545275B2 (ja) |
| ES (1) | ES2882138T3 (ja) |
| WO (1) | WO2017069226A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022059700A1 (ja) * | 2020-09-15 | 2022-03-24 | 田辺三菱製薬株式会社 | トリアジン化合物の塩、その結晶形及び製造方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023172415A1 (en) * | 2022-03-07 | 2023-09-14 | Firmenich Incorporated | Sweetener compositions |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010034838A2 (en) * | 2008-09-29 | 2010-04-01 | Boehringer Ingelheim International Gmbh | New chemical compounds |
| WO2012012478A1 (en) * | 2010-07-21 | 2012-01-26 | Merck Sharp & Dohme Corp. | Aldosterone synthase inhibitors |
| JP2012526774A (ja) * | 2009-05-15 | 2012-11-01 | ノバルティス アーゲー | アルドステロンシンターゼ阻害剤としてのアリールピリジン |
| WO2013079452A1 (en) * | 2011-11-30 | 2013-06-06 | F. Hoffmann-La Roche Ag | New bicyclic dihydroisoquinoline-1-one derivatives |
| WO2014179186A1 (en) * | 2013-04-30 | 2014-11-06 | Boehringer Ingelheim International Gmbh | Aldosterone synthase inhibitors |
| WO2015163427A1 (ja) * | 2014-04-24 | 2015-10-29 | 田辺三菱製薬株式会社 | 新規二置換1,2,4-トリアジン化合物 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1947178A (en) * | 1932-07-11 | 1934-02-13 | Wilson Francis Condry | Interlocking wheel |
| US20130225548A1 (en) * | 2010-10-28 | 2013-08-29 | Nippon Shinyaku Co., Ltd. | Pyridine Derivative and Medicinal Agent |
| AU2012307509B2 (en) * | 2011-09-15 | 2017-06-29 | F. Hoffmann-La Roche Ag | New dihydroquinoline-2-one derivatives |
-
2016
- 2016-10-21 EP EP16857539.7A patent/EP3381904B1/en active Active
- 2016-10-21 JP JP2017545804A patent/JP6545275B2/ja active Active
- 2016-10-21 WO PCT/JP2016/081214 patent/WO2017069226A1/ja active Application Filing
- 2016-10-21 US US15/769,844 patent/US10717731B2/en active Active
- 2016-10-21 ES ES16857539T patent/ES2882138T3/es active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010034838A2 (en) * | 2008-09-29 | 2010-04-01 | Boehringer Ingelheim International Gmbh | New chemical compounds |
| JP2012526774A (ja) * | 2009-05-15 | 2012-11-01 | ノバルティス アーゲー | アルドステロンシンターゼ阻害剤としてのアリールピリジン |
| WO2012012478A1 (en) * | 2010-07-21 | 2012-01-26 | Merck Sharp & Dohme Corp. | Aldosterone synthase inhibitors |
| WO2013079452A1 (en) * | 2011-11-30 | 2013-06-06 | F. Hoffmann-La Roche Ag | New bicyclic dihydroisoquinoline-1-one derivatives |
| WO2014179186A1 (en) * | 2013-04-30 | 2014-11-06 | Boehringer Ingelheim International Gmbh | Aldosterone synthase inhibitors |
| WO2015163427A1 (ja) * | 2014-04-24 | 2015-10-29 | 田辺三菱製薬株式会社 | 新規二置換1,2,4-トリアジン化合物 |
Non-Patent Citations (5)
| Title |
|---|
| DATABASE REGISTRY [o] 13 October 2008 (2008-10-13), "1-Piperazineacetamide, N,N- dimethyl-4-[5-[4-(trifluoromethyl)phenyl]- 1,2,4-triazin-3-yl", XP055530302, retrieved from STN Database accession no. 1060824-77-2 * |
| DATABASE REGISTRY [o] 14 May 2010 (2010-05-14), "1-Piperazineacetamide, N,N- dimethyl-4-[6-(1H-1,2,4-triazol-1-yl)-2- pyrazinyl", XP 055530271, retrieved from STN Database accession no. 1223591-34-1 * |
| DATABASE REGISTRY [o] 2 November 2008 (2008-11-02), "1-Piperazineacetamide, 4- [5-(4-chlorophenyl)-1,2,4-triazin-3-yl]-N,N- dimethyl", XP 055530294, retrieved from STN Database accession no. 1069628-74-5 * |
| DATABASE REGISTRY [o] 3 November 2008 (2008-11-03), "1-Piperazineacetamide, 4- [5-(4-methoxyphenyl)-1,2,4-triazin-3-yl]-N- (1-methylethyl", XP 055530286, retrieved from STN Database accession no. 1070398-58-1 * |
| HU , Q. ET AL.: "Aldosterone Synthase Inhibitors as Promising Treatments for Mineralocorticoid Dependent Cardiovascular and Renal Diseases", JOURNAL OF MEDICINAL CHEMISTRY, vol. 57, no. 12, 2014, pages 5011 - 5022, XP 055228601, ISSN: 0022-2623 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022059700A1 (ja) * | 2020-09-15 | 2022-03-24 | 田辺三菱製薬株式会社 | トリアジン化合物の塩、その結晶形及び製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6545275B2 (ja) | 2019-07-17 |
| EP3381904A1 (en) | 2018-10-03 |
| US10717731B2 (en) | 2020-07-21 |
| EP3381904A4 (en) | 2019-05-22 |
| EP3381904B1 (en) | 2021-07-28 |
| ES2882138T3 (es) | 2021-12-01 |
| US20180312503A1 (en) | 2018-11-01 |
| JPWO2017069226A1 (ja) | 2018-08-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6148402B2 (ja) | 新規二置換1,2,4−トリアジン化合物 | |
| JP5336378B2 (ja) | 2−アリール−6−フェニルイミダゾ[1,2−α]ピリジン誘導体、これらの調製およびこれらの治療的使用 | |
| TWI481604B (zh) | Novel 5-fluorouracil derivatives | |
| TW201835070A (zh) | 芳香烴受體(AhR)調節劑化合物 | |
| JP2012513956A (ja) | ジヒドロインデンアミド化合物の製造方法、それらの化合物を含有する医薬組成物、及びプロテインキナーゼ阻害剤としての使用 | |
| TW201838991A (zh) | 芳基烴受體(AhR)調節劑化合物 | |
| CA3126484A1 (en) | Compound for inhibiting pge2/ep4 signaling transduction inhibiting, preparation method therefor, and medical uses thereof | |
| JP6670906B2 (ja) | 新しい3,4−ジヒドロ−2h−イソキノリン−1−オン及び2,3−ジヒドロ−イソインドール−1−オン化合物 | |
| JP6250862B2 (ja) | アルドステロン合成酵素阻害薬 | |
| JP2007015928A (ja) | 新規オレフィン誘導体 | |
| JP6545275B2 (ja) | 新規含窒素芳香族複素環化合物 | |
| JP2023545552A (ja) | 置換6,7-ジヒドロ-5h-ベンゾ[7]アヌレン化合物およびそれらの誘導体、それらの製造のための方法ならびにそれらの治療的使用 | |
| WO2017170765A1 (ja) | 新規含窒素複素環化合物 | |
| US8895565B2 (en) | Heterocyclic compound and use of the same | |
| IL298966A (en) | A bicyclic compound and its application | |
| JP6314196B2 (ja) | 医薬組成物 | |
| US20120196915A1 (en) | Antitumor 1,2-Diphenylpyrrole Compounds and their Preparation Process | |
| JPWO2009048123A1 (ja) | ビス(トリメチルシリル)フェニル化合物又はその塩、及びその用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 16857539 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2017545804 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15769844 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2016857539 Country of ref document: EP |