WO2012173244A1 - 人獣共通感染性歯周病菌検出用マーカー - Google Patents
人獣共通感染性歯周病菌検出用マーカー Download PDFInfo
- Publication number
- WO2012173244A1 WO2012173244A1 PCT/JP2012/065408 JP2012065408W WO2012173244A1 WO 2012173244 A1 WO2012173244 A1 WO 2012173244A1 JP 2012065408 W JP2012065408 W JP 2012065408W WO 2012173244 A1 WO2012173244 A1 WO 2012173244A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- antibody
- strain
- anone
- marker
- antigen
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/0216—Bacteriodetes, e.g. Bacteroides, Ornithobacter, Porphyromonas
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/569—Immunoassay; Biospecific binding assay; Materials therefor for microorganisms, e.g. protozoa, bacteria, viruses
- G01N33/56911—Bacteria
- G01N33/56955—Bacteria involved in periodontal diseases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/55—Medicinal preparations containing antigens or antibodies characterised by the host/recipient, e.g. newborn with maternal antibodies
- A61K2039/552—Veterinary vaccine
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2469/00—Immunoassays for the detection of microorganisms
- G01N2469/20—Detection of antibodies in sample from host which are directed against antigens from microorganisms
Abstract
従来未知であった、ヒト及び他の哺乳動物、特に愛玩動物に対して共通感染性を有する歯周病菌の感染判定システムを提供することである。 人獣共通感染性歯病菌であるP.ジンジバリス アノン株を新たに同定し、当該菌に特異的な抗原をマーカーとして、被検体の体液から当該マーカーに特異的な抗体を検出することにより、被検体のP.ジンジバリス アノン株の感染歴及び現在の感染状況を判定する。
Description
本発明は、人獣に共通する歯周病原菌を検出するためのマーカー、当該菌による感染を判定する方法及び当該菌を検出する方法に関する。
歯周病は、歯肉、歯根膜、セメント質及び歯槽骨等の歯周組織に発生する炎症であり、全世界の人口の約30%が罹患している極めて一般的な疾患である。歯周病には、歯肉炎、歯周炎及び咬合性外傷等が知られるが、このうち最も多く見られる歯周病は、歯周炎、特に、歯周病菌による慢性歯周炎である(非特許文献1)。慢性歯周炎は、軽度の歯肉炎から年齢と共に徐々に進行していく。5歳以上の人で歯肉に所見が認められる割合は、昭和62年では64.3%(歯科疾患実態調査)、平成5年では68.1%(同調査)、平成11年では72.9%(同調査)と、近年増加傾向にある。慢性歯周炎は、口腔内の炎症のみならず、脳血管疾患、心疾患、早産等の種々の全身疾患の発症リスクを高めることが知られている。したがって、慢性歯周炎が顕在化していない段階で、その原因となる歯周病菌を検出することは、慢性歯周炎の予防及び早期治療をする上で重要である。
しかし、慢性歯周炎は、歯肉の炎症や出血等の症状を伴うため、発症後の視認による診断が比較的容易である。それ故、歯科分野では、これまで被検体から歯周病菌を早期段階で簡便、かつ高い正診率で検出し、その被験者の慢性歯周炎の罹患可能性を予測し、その結果に基づいて慢性歯周炎を予防する方法の開発は、十分に行われていなかった。
歯周病菌検出方法としては、口腔内常在性菌の一つであり、最も一般的な歯周病菌として知られるポルフィロモナス ジンジバリス(Porphyromonas ginigivalis)(以下、「P.ジンジバリス」と略称する)を、抗原抗体反応を用いて検出する方法が知られている。
例えば、特許文献1には、特定のアミノ酸配列を有するP.ジンジバリス由来の抗原に対する抗体を用いて、イムノアッセイにより当該菌を検出する方法、及びその抗体を含む洗口剤又は歯磨き剤を患者に適用することによって、歯周炎を治療する方法が開示されている。
また、特許文献2には、P.ジンジバリスのリポ多糖に結合する抗体を含む口腔洗浄剤、エアロゾル、ペースト又は軟膏を患者に適用することにより歯周炎を治療する方法が開示されている。
さらに、特許文献3には、P.ジンジバリスに対するモノクローナル抗体を用いて、歯肉溝に当該菌が存在するか否かをELISA法によって診断する方法が開示されている。
Haake SK et al., 2006, Periodontal diseases, pp.253-294,In:Oral Micorobiology and Immunology, ASM press, Washington, US
本発明は、ヒト及び他の哺乳動物、特に愛玩動物に対して共通感染性を有する、従来知られていなかった性質を有する歯周病菌の感染判定システムを提供することである。
歯周病は、ヒトに限られず、他の哺乳動物も発症し得る。特に、愛玩動物として飼育されるイヌやネコでは罹患率が高く、5歳以上のイヌの約80%は、歯周病に罹患していると報告されている(Hamp SE et al., 1975.Clinical and roentgengraphical observations, 53rd. Gen. Meet. IARD, London, J. Dent. Res. 54: special issue A, L-5)。本発明者らが日本においてイヌの歯周ポケット内の歯周組織破壊酵素活性を、Periocheck(サンスター、大阪)を用いて調べたところ、1歳未満のイヌは全て陰性だったのに対して、1歳以上のイヌは全て陽性を示し、またその陽性犬の80%以上からポルフィロモナス属が分離された(Isogai H. et al., 1999, J Vet Med B46: 467-473,1999)。このように、ポルフィロモナス属は、ヒト以外の哺乳動物でも主な歯周病菌とされている。
ところで、前述のようにP.ジンジバリスはイヌからも検出されるが、イヌ由来のP.ジンジバリスは、ヒト由来のP.ジンジバリスとはタイプが異なるとされており、現在では、P.ジンジバリスとは別種のP.グラエ(P. gulae)として扱われている(Fournier D., et al., 2001, Int J Syst Evolution Microbiol, 51: 1179-1189)。したがって、歯科分野では、ヒト由来と他の哺乳動物由来の歯周病菌、特にポルフィロモナス属には、共通性がないというのが通説であり、歯周病の診断及び予防においてもヒトと他の哺乳動物は、疫学的に全く無関係のそれぞれ別個の対象として扱われてきた。実際、米国では、歯周病予防として動物用ワクチン(Porphyromonas Denticanis-Gulae-Salivosa BacterinTM(Porphyromonas Vaccine)ファイザー社)が実用化されているが、このワクチンはイヌのみを対象としている。
しかし、仮に未知の人獣共通感染性歯周病菌が存在した場合には、当該歯周病菌がイヌやネコ等の愛玩動物からヒトへと感染し得る。それ故、そのような歯周病菌を愛玩動物のような他の哺乳動物から検出し、その感染リスクを予め知ることによって、ヒトへの感染予防及び早期治療が期待できる。
本発明者らは、獣医分野で問題となっていた犬の歯周病の疫学、診断法、口腔細菌叢の解析の研究成果を踏まえ、当該疾患を予防するためのドッグフード開発を行ってきた。その過程で、異なる3匹の個体から分離したP.ジンジバリスが、カタラーゼ陽性のP.ジンジバリス株(P.グラエ)ではなく、カタラーゼ陰性の株であることを見出した(Isogai E, et al. 1995, Microbial Ecol Health Dis 8: 57-61)。当初、これらの分離株は、P.グラエのカタラーゼ欠損型と解釈していたが、分離株を増やし、様々な解析を行った結果、従来の定説を覆す人獣共通の感染性を有するP.ジンジバリス株であることが判明し、P.ジンジバリス アノン(P. ginigivalis ANON)株と命名した。さらに、本発明者らは、P.ジンジバリス アノンの病原性に関与する遺伝子において、他のP.ジンジバリス株では見られない当該株に特有の領域を分離することに成功した。本発明は、上記知見に基づくものであり、以下を提供する。
(1)人獣共通感染性歯周病菌P.ジンジバリス アノンを不活化又は弱毒化したワクチン。
(2)配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチドを用いて、前記ペプチド中に存在するエピトープを認識する抗体/又はその抗原結合性断片を被検体より採取した体液から検出する抗体検出工程、及び抗体検出工程の結果に基づいて、被検体のアノン株に対する感染の有無を判定する判定工程を含む、人獣共通感染性歯周病菌P. ジンジバリス アノンの感染判定方法。
(3)配列番号1~7のいずれか一で示されるアミノ酸配列を含む一以上のポリペプチドを、前記アミノ酸配列からなるペプチド中に存在するエピトープを認識する抗体及び/又はその抗原結合性断片を用いて被検体より採取したプラークから検出するポリペプチド検出工程を含む、人獣共通感染性歯周病菌P. ジンジバリス アノンの検出方法。
(4)配列番号1~7のいずれか一で示されるアミノ酸配列を含むペプチドからなる、人獣共通感染性歯周病菌P. ジンジバリス アノン検出用マーカー。
(5)配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド中に存在するエピトープを認識する人獣共通感染性歯周病菌P. ジンジバリス アノン検出用抗体又はその抗原結合性断片。
(6)配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチドに存在するエピトープを認識する一以上の抗体及び/又はその抗原結合性断片を有効成分として含む、人獣共通感染性歯周病菌P. ジンジバリス アノンの感染抑制又は炎症抑制剤。
(7)(4)に記載の一以上のマーカー、(5)に記載の一以上の抗体及び/又は抗原結合性断片を含む、人獣共通感染性歯周病菌P.ジンジバリス アノン検出用キット。
本明細書は本願の優先権の基礎である日本国特許出願2011-135669号の明細書及び/又は図面に記載される内容を包含する。
本発明によれば、人獣共通感染性を有するP.ジンジバリス アノンを検出することができる。それによって、従来想定されていなかったヒト以外の他の哺乳動物からヒトへの、またその逆の感染リスクを知り、予防又は早期治療を行うことができる。
本発明によれば、簡便に、かつ短時間でP.ジンジバリス アノンの検出が可能になる。
1.人獣共通感染性歯周病菌検出用マーカー
本発明の第1の実施形態は、人獣共通感染性歯周病菌検出用マーカーである。
本発明の第1の実施形態は、人獣共通感染性歯周病菌検出用マーカーである。
「人獣共通感染性歯周病菌検出用マーカー」(以下、単に「マーカー」とも表記する)とは、人獣共通感染性歯周病菌を特異的に検出するためのマーカーをいう。本明細書において「人獣共通感染性歯周病菌」とは、ヒト及び他の哺乳動物の口腔内に共通して存在し、両者のいずれにも歯周病を引き起こし得る病原性感染細菌である。具体的には、P.ジンジバリス アノン(P. ginigivalis ANON)(以下、「アノン株」とする)が該当する。本明細書において「他の哺乳動物」とは、ヒト以外の全ての哺乳動物を意味し、特に制限するものではないが、ヒトへの感染率を考慮すれば、ヒトとの直接的な接触頻度の高い哺乳動物、例えば、イヌ、ネコ、ウサギ、ハムスター、テンジクネズミ、マウス、ラット、フェレット、リス、フクロモモンガ、サル及びハリネズミのような愛玩動物、ウマ、ウシ、ヒツジ、ヤギ、ブタ、トナカイ、ラクダ及びラマのような家畜、又は実験動物が該当する。特に、ヒトが日常的に接触することの多い愛玩動物、一般的にはイヌ及びネコは、本明細書における他の哺乳動物として好適である。
本マーカーは、配列番号1~7のいずれか一で示されるアミノ酸配列を含むペプチドで構成される。これらのアミノ酸配列は、いずれもP.ジンジバリスの病原性及び感染性に関与するタンパク質の部分配列に相当する。具体的には、以下の通りである。
配列番号1で示されるアミノ酸配列は、P.ジンジバリスW83株の遺伝子記号PG1972にコードされるヘマグルチニン(HagB)の331位~350位(開始メチオニン残基を1位とする。以下、同様とする。)に相当するアノン株のアミノ酸配列である。本明細書では、配列番号1で示されるアミノ酸配列からなるペプチドを、便宜的に「Hem331」とする。
配列番号2で示されるアミノ酸配列は、P.ジンジバリスW83株の前記HagBの190位~210位に相当するアノン株のアミノ酸配列である。本明細書では、配列番号2で示されるアミノ酸配列からなるペプチドを、便宜的に「Hem190」とする。
配列番号3で示されるアミノ酸配列は、P.ジンジバリスW83株の遺伝子記号PG1043にコードされる第一鉄輸送タンパク質B(FeoB-1)の55位~74位に相当するアノン株のアミノ酸配列である。本明細書では、配列番号3で示されるアミノ酸配列からなるペプチドを、便宜的に「Fe55」とする。
配列番号4で示されるアミノ酸配列は、P.ジンジバリスW83株の遺伝子記号PG2132にコードされるフィンブリリン(fimbrilin)(fimA)の141位~160位に相当するアノン株のアミノ酸配列である。本明細書では、配列番号4で示されるアミノ酸配列からなるペプチドを、便宜的に「Fim141」とする。
配列番号5で示されるアミノ酸配列は、P.ジンジバリスW83株の前記fimAの353位~370位に相当するアノン株のアミノ酸配列である。本明細書では、配列番号5で示されるアミノ酸配列からなるペプチドを、便宜的に「Fim353」とする。
配列番号6で示されるアミノ酸配列は、P.ジンジバリスW83株の遺伝子記号PG0383にコードされるメタロプロテアーゼの85位~106位に相当するアノン株のアミノ酸配列である。本明細書では、配列番号6で示されるアミノ酸配列からなるペプチドを、便宜的に「Me85」とする。
配列番号7で示されるアミノ酸配列は、P.ジンジバリスW83株の前記メタロプロテアーゼの48位~65位に相当するアノン株のアミノ酸配列である。本明細書では、配列番号7で示されるアミノ酸配列からなるペプチドを、便宜的に「Me48」とする。
これらのタンパク質において、配列番号1~7で示されるアミノ酸配列は、アノン株でのみ特異的に認められる配列である。したがって、これらのアミノ酸配列を含むペプチドは、アノン株、すなわち、人獣共通感染性歯周病菌を検出する上で有用なマーカーとなり得る。
本実施形態のマーカーは、配列番号1~7で示すアミノ酸配列を含むペプチドであれば、そのペプチドのアミノ酸数は特に限定はしない。好ましくは40アミノ酸以下、より好ましくは30アミノ酸以下、もっとも好ましくは配列番号1~7で示されるアミノ酸配列のみからなるペプチド、すなわち、Hem331、Hem190、Fe55、Fim141、Me85又はMe48である。
本実施形態のマーカーは、例えば、検出を容易にするタグ配列と融合させることもできる。タグ酸配列としては、例えば、ヒスチジン「His」タグ(Gentz et al., 1989, Proc. Natl. Acad. Sci. USA, 86:821-824)、ヘマグルチニン「HA」タグ(Wilson et al., 1984, Cell, 37:767)、及び「Flag」タグ(Knappik et al., Biotechniques, 1994, 17(4):754-761)が挙げられる。
本実施形態のマーカーは、その検出用に標識子で標識されていてもよい。標識子には、例えば、蛍光色素(フルオレセイン、FITC、ローダミン、ウンベリフェロン、テキサスレッド、Cy3、Cy5)、蛍光タンパク質(例えば、PE、APC、GFP)、酵素(例えば、西洋ワサビペルオキシダーゼ、アルカリフォスファターゼ、グルコースオキシダーゼ、β-ガラクトシダーゼ)、ビオチン若しくは(ストレプト)アビジン、又は放射線同位元素(例えば、32P、33P、35S、90Y、111In、112In)等を利用することができる。本実施形態のマーカーの標識方法は、当該分野で公知の技術によって行えばよい。
本実施形態のマーカーの製造は、生合成又は化学合成によって、公知の技術にしたがって製造すればよい。
生合成する場合には、例えば、本実施形態のマーカーをコードするポリヌクレオチド断片を化学合成によって、又はアノン株のゲノムDNA若しくはcDNAライブラリーからPCR等の核酸増幅法で目的とするDNA領域を増幅させることによって入手した後、その断片を適当な発現ベクターに挿入し、大腸菌等の宿主細胞に導入後、その細胞内で発現させることによって得ることができる。このとき、本実施形態のマーカーに上述したタグ配列を融合させておけば、宿主細胞から目的のマーカーを分離、精製する上で便利である。このような組換タンパク質技術は、当該分野で公知であり、本実施形態のマーカーを生合成する際にも、公知の技術に従って行えばよい。例えば、生物工学実験書(社団法人 日本生物工学会編、培風館、1996)に記載の組換タンパク質技術を参考にすることができる。
化学合成を行う場合には、公知のペプチド合成技術を用いて合成すればよい。ペプチド合成は、例えば、神戸天然物化学株式会社、タカラバイオ社及びEZBiolab (US)社等の各メーカーが受託合成を行っており、それらを利用することもできる。
アノン株に感染歴のある個体、又は現在アノン株を口腔内に保菌する個体は、原則、血清中にP.ジンジバリス由来の各タンパク質に対する抗体を有している。したがって、アノン株特異的なペプチド抗原である本実施形態のマーカーを用いれば、被検体の血清中のアノン株に対して特異的な抗体を検出することが可能となり、また、その結果によって被検体にアノン株感染歴があるか、又は現在アノン株に感染していることを判定できる。
2.抗人獣共通感染性歯周病菌検出用マーカー抗体又はその抗原結合性断片
本発明の第2の実施形態は、抗人獣共通感染性歯周病菌検出用マーカー抗体又はその抗原結合性断片である。
本発明の第2の実施形態は、抗人獣共通感染性歯周病菌検出用マーカー抗体又はその抗原結合性断片である。
2-1.抗人獣共通感染性歯周病菌検出用マーカー抗体
「抗人獣共通感染性歯周病菌検出用マーカー抗体」(以下、「抗マーカー抗体」とする)とは、前記第1実施形態の人獣共通感染性歯周病菌検出用マーカーを抗原とする抗体である。具体的には、配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド、すなわち、Hem331、Hem190、Fe55、Fim141、Me85又はMe48中に存在するエピトープを特異的に認識する抗体をいう。「エピトープ」は、抗原性又は免疫原性を有するポリペプチド断片であって、約7~12アミノ酸、好ましくは8~11アミノ酸からなる。
「抗人獣共通感染性歯周病菌検出用マーカー抗体」(以下、「抗マーカー抗体」とする)とは、前記第1実施形態の人獣共通感染性歯周病菌検出用マーカーを抗原とする抗体である。具体的には、配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド、すなわち、Hem331、Hem190、Fe55、Fim141、Me85又はMe48中に存在するエピトープを特異的に認識する抗体をいう。「エピトープ」は、抗原性又は免疫原性を有するポリペプチド断片であって、約7~12アミノ酸、好ましくは8~11アミノ酸からなる。
上記ペプチド中に複数のエピトープが存在する場合、本実施形態の抗マーカー抗体は、いずれのエピトープを認識してもよい。「エピトープを特異的に認識」とは、標的エピトープのみを特異的に認識して結合し、それ以外のエピトープを認識せず、また実質的に結合しない、すなわち交差反応性を有さないことを意味する。
本実施形態の抗マーカー抗体は、抗原結合性を保持し得る限り、いかなる種類の抗体であってもよい。例えば、ポリクローナル抗体、モノクローナル抗体、組換え抗体が挙げられる。
本実施形態の抗マーカー抗体がポリクローナル抗体(抗マーカーポリクローナル抗体)又はモノクローナル抗体(抗マーカーモノクローナル抗体)の場合、免疫グロブリン分子の任意のクラス、例えば、IgG、IgE、IgM、IgA、IgD及びIgY、又は任意のサブクラス、例えば、IgG1、IgG2、IgG3、IgG4、IgA1、IgA2が該当する。また、モノクローナル抗体には、ヒトモノクローナル抗体、非ヒト動物モノクローナル抗体(例えばマウスモノクローナル抗体)、キメラ型モノクローナル抗体が含まれる。
本発明の抗マーカーポリクローナル抗体及び抗マーカーモノクローナル抗体は、公知の方法によって作製することができる。例えば、抗マーカーポリクローナル抗体は、Hem331、Hem190、Fe55、Fim141、Me85又はMe48を抗原として、適当な動物に免疫して得ることができる。また、抗マーカーモノクローナル抗体は、Hem331、Hem190、Fe55、Fim141、Me85又はMe48を抗原として免疫した非ヒト哺乳動物(例えば、マウス、ヒト抗体産生マウス、ニワトリ、ウサギ等)からの脾細胞とミエローマ細胞との融合によって得られたハイブリドーマを培養することによって作製することができる。これらの抗体作製技術は、当該分野で公知の技術であり、例えば、Harlow et al., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2nd ed. 1988)、The Immunoassay Handbook (D. Wild編, Stockton Press NY, 1994); Bioconjugate Techniques (Greg T. Hermanson編, Academic Press, 1996)、Hammerling et al., in: Monoclonal Antibodies and T-Cell Hybridomas, pp. 563-681 (Elsevier, N.Y., 1981)、又はMethods of Immunological Analysis (R. Masseyeff, W. H. Albert, and N. A. Staines編, Weinheim: VCH Verlags gesellschaft mbH, 1993)に記載の方法を参照して作製すればよい。
本明細書において上記「組換え抗体」とは、例えば、キメラ抗体、ヒト化抗体及び多重特異性抗体をいう。
「キメラ抗体」とは、異なる動物由来の抗体のアミノ酸配列を組み合わせて作製される抗体で、ある抗体の定常領域(C領域)を他の抗体のC領域で置換した抗体である。例えば、Hem331を認識するマウスモノクローナル抗体のC領域をヒト抗体のC領域と置き換えた抗体が該当する。これによりヒト体内における当該抗体に対する免疫反応を軽減し得る。キメラ抗体の作製は、公知の方法を用いて行うことができる。例えば、可変領域(V領域)をコードするDNAとヒト抗体のC領域をコードするDNAとを連結し、これを発現ベクターに組み込んで宿主に導入し産生させればよい。
「ヒト化抗体」とは、ヒト以外の哺乳動物、例えば、マウス抗体のV領域における相補性決定領域(CDR)とヒト抗体のCDRとを置換したモザイク抗体である。抗体の抗原結合特異性は、主としてV領域中のCDR群が担っている。したがって、ある特定の抗体と同様の結合特性を有する組換え抗体を作製する際には、その抗体の全アミノ酸配列を得る必要はなく、既存の組換えDNA技術を用いて、その抗体由来の各CDR領域をコードするDNA配列を、それぞれヒト抗体由来の対応するCDRをコードするDNA配列と置き換えたモザイク抗体を調製し、それを発現させることにより、その特定の抗体の性質を模倣した組換え抗体を得ることができる。ヒト化抗体は、例えば、上記抗マーカーモノクローナル抗体を用いて、その抗体のCDR群をコードする塩基配列に基づき、当該分野で知られる様々な技術を用いて作製することができる。例えば、CDRグラフト法(Jones et al., Nature(1986) Vol.321:522-525)、ベニアリング法(veneering)又はリサーフェイシング法(resurfacing)(Padlan, 1991, Molecular Immunology 28(4/5):489 498;Studnicka et al., 1994, Protein Engineering 7(6):805 814;及び Roguska et al, 1994, Proc Natl Acad Sci USA 91:969 973)、チェーンシャッフリング法(chain shuffling)(米国特許第5,565,332号)、並びに、例えば、Tan et al,2002, J. Immunol. 169:1119 25、Caldas et al,2000, Protein Eng. 13:353 60、で開示された技術等を利用して作製すればよい。
「多重特異性抗体」とは、多価抗体、すなわち抗原結合部位を一分子内に複数有する抗体において、それぞれの抗原結合部位が異なるエピトープと結合する抗体をいう。例えば、IgGのように2つの抗原結合部位を有する抗体で、それぞれの抗原結合部位が異なるエピトープと結合する二重特異性抗体(Bispecific抗体)が挙げられる。本発明においては、この多重特異性抗体は、それぞれの抗原結合部位がHem331、Hem190、Fe55、Fim141、Me85又はMe48中に存在する異なるエピトープと結合できることが好ましい。これらの抗体は、組換えDNA技術を用いて、公知方法によりIgG等を人工的に改変することによって得ることができる。
キメラ抗体、ヒト化抗体及び多重特異性抗体等の組換え抗体を作製する場合、得られる抗体が機能的に同等である限りにおいて、可変領域のフレームワーク領域(FR)やC領域中の、例えば4以下、3以下、又は2以下のアミノ酸、好ましくは1~5アミノ酸、より好ましくは1又は2アミノ酸を他のアミノ酸で置換等してもよい。ここでいう「機能的に同等」とは、アミノ酸置換変異導入前の抗体と同様の生物学的あるいは生化学的活性、具体的には抗原である本発明のマーカーを特異的に認識する機能を有することをいう。この場合、置換するアミノ酸は、電荷、側鎖、極性、芳香族性等の性質の類似するアミノ酸間の置換(保存的アミノ酸置換)であることが望ましい。例えば、塩基性アミノ酸群(アルギニン、リジン、ヒスチジン)、酸性アミノ酸群(アスパラギン酸、グルタミン酸)、無電荷極性アミノ酸群(グリシン、アスパラギン、グルタミン、セリン、トレオニン、システイン、チロシン)、無極性アミノ酸群(ロイシン、イソロイシン、アラニン、バリン、プロリン、フェニルアラニン、トリプトファン、メチオニン)、分枝鎖アミノ酸群(トレオニン、バリン、イソロイシン)、芳香族アミノ酸群(フェニルアラニン、チロシン、トリプトファン、ヒスチジン)の各群内でのアミノ酸置換が該当する。
本実施形態の抗マーカー抗体及び後述するその抗原結合性断片は、修飾されていてもよい。修飾には、標識子による修飾の他、グリコシル化、アセチル化、ホルミル化、アミド化、リン酸化、又はPEG化が含まれる。
標識子には、前記第1実施形態に記載した標識子と同じ標識子を利用することができる。標識子による修飾は、本実施形態の抗マーカー抗体及び後述するその抗原結合性断片を検出する上で有用である。
グリコシル化に関する修飾は、内在性の抗体分子が有する天然型のグリコシル化であってもよいし、例えば、組換えDNA技術により又は化学的処理によって、天然型グリコシル化部位を改変した改変型グリコシル化部位であってもよい。改変型グリコシル化部位は、標的抗原に対する抗体の親和性を調整するため等、抗体の機能を所望の状態に改変する上で有用である。グリコシル化部位の改変は、当業者に公知のあらゆる方法で行うことができる。例えば、上述のような遺伝子操作による方法、グリコシル化変異型の変異株を用いる方法、1以上の酵素、例えばDI N-アセチルグルコサミントランスフェラーゼIII (GnTIII)との共発現による方法、各種生物若しくは各種生物由来の細胞株で本発明の抗原結合断片を発現させて精製した後に糖鎖を修飾することによる方法が挙げられる。遺伝子操作による改変型グリコシル化部位を作製する方法については、例えば、Umana et al., 1999, Nat. Biotechnol 17:176-180;Davies et al., 2001, Biotechnol Bioeng 74:288-294;Shields et al., 2002, J Biol Chem 277:26733-26740;Shinkawa et al., 2003, J Biol Chem 278:3466-3473を参照することができる。糖鎖を改変する方法については、例えば、米国特許第6,218,149号;欧州特許第0,359,096B1号;米国特許公開第2002/0028486号;国際公開WO 03/035835号;米国特許公開第2003/0115614号;米国特許第6,218,149号;米国特許第6,472,511号を参照することができる。
PEG化による修飾は、ポリエチレングリコール(PEG)等の水溶性ポリマー分子を本実施形態の抗マーカー抗体及び後述するその抗原結合性断片に結合させたものである。PEG化は、抗体等のN末端アミノ基、C末端カルボキシル基、又はリシン(Lys)残基のε-アミノ基などにPEGを化学的に結合することによって達成することができる。PEG化による修飾は、修飾したポリペプチドのin vivo半減期を高めることができる。
2-2.抗人獣共通感染性歯周病菌検出用マーカー抗体の抗原結合性断片
「抗人獣共通感染性歯周病菌検出用マーカー抗体の抗原結合性断片」(以下、単に「抗原結合性断片」とする)とは、上記2-1に記載の抗マーカー抗体の部分断片であって、該抗体が有する抗原特異的結合活性と実質的に同等の活性を有するポリペプチド鎖又はその複合体をいう。例えば、前述の抗原結合部位を少なくとも1つ包含する抗体部分、すなわち、少なくとも1組の軽鎖可変領域(VL)と重鎖可変領域(VH)を有するポリペプチド鎖又はその複合体が該当する。具体的には、例えば、免疫グロブリンを様々なペプチダーゼで切断することによって生じる多数の十分に特徴付けられた抗体断片等が挙げられる。より具体的には、例えば、Fab、F(ab’)2、Fab’等が挙げられる。
「抗人獣共通感染性歯周病菌検出用マーカー抗体の抗原結合性断片」(以下、単に「抗原結合性断片」とする)とは、上記2-1に記載の抗マーカー抗体の部分断片であって、該抗体が有する抗原特異的結合活性と実質的に同等の活性を有するポリペプチド鎖又はその複合体をいう。例えば、前述の抗原結合部位を少なくとも1つ包含する抗体部分、すなわち、少なくとも1組の軽鎖可変領域(VL)と重鎖可変領域(VH)を有するポリペプチド鎖又はその複合体が該当する。具体的には、例えば、免疫グロブリンを様々なペプチダーゼで切断することによって生じる多数の十分に特徴付けられた抗体断片等が挙げられる。より具体的には、例えば、Fab、F(ab’)2、Fab’等が挙げられる。
Fabは、パパインによりIgG分子がヒンジ部のジスルフィド結合よりもN末端側で切断されることによって生じる断片であって、VH及び重鎖定常領域(CH)を構成する3つのドメイン(CH1、CH2、CH3)のうちVHに隣接するCH1からなるポリペプチドと、軽鎖から構成される。F(ab’)2は、ペプシンによりIgG分子がヒンジ部のジスルフィド結合よりもC末端側で切断されることによって生じるFab’の二量体である。Fab’は、Fabよりもヒンジ部を含む分だけH鎖が若干長いものの、実質的にはFabと同等の構造を有する。
Fab、F(ab’)2及びFab'は、当該分野で公知の方法で作製することができる。例えば、Fabであれば、パパイン処理によって、F(ab’)2であれば、ペプシン処理によって、それぞれ得ることができる。また、Fab'であれば、前記ペプシン処理で得られたF(ab’)2をマイルドな条件下で還元処理して、ヒンジ領域のジスルフィド連結を切断することによって得ることができる。
これらの抗原結合性断片は、いずれも抗マーカー抗体の抗原結合部位を包含しており、抗マーカー抗体と同様に、前記第1実施形態のマーカーを特異的に認識し、結合する能力を有している。
本実施形態の抗原結合性断片は、さらに、化学的に、又は組換えDNA法を用いることによって合成した合成抗体断片であってもよい。例えば、組換えDNA法を用いて新たに合成された抗体断片が挙げられる。具体的には、例えば、本発明の抗マーカーモノクローナル抗体のVL及びVHを、適当な長さと配列を有するリンカーペプチド等で人工的に連結させた一量体ポリペプチド、又はその多量体ポリペプチドが該当する。このような構成抗体断片の例としては、例えば、一本鎖Fv(scFv:single chain Fragment of variable region)(Pierce catalog and Handbook、1994-1995、Pierce Chemical co.、Rockford、ILを参照されたい)、ダイアボディ(diabody)、トリアボディ(triabody)又はテトラボディ(tetrabody)等が挙げられる。
一本鎖Fvは、それをコードする組換えDNAを、公知技術を用いてファージゲノムに組み込み、発現させることで得ることができる。ダイアボディは、一本鎖Fvの二量体構造を基礎とした構造を有する分子である(Holliger et al., 1993, Proc. Natl. Acad. Sci. USA 90:6444-6448)。例えば、上記リンカーの長さが約12アミノ酸残基よりも短い場合、一本鎖Fvでは自身の2つの可変部位は自己集合できないが、ダイアボディを形成させ、2つの一本鎖Fvを相互作用させることにより、一方のFv鎖のVLが他方のFv鎖のVHと集合可能となり、2つの機能的な抗原結合部位を形成することができる(Marvin et al., 2005, Acta Pharmacol. Sin. 26:649-658)。さらに、一本鎖FvのC末端にシステイン残基を付加させることにより、2本のFv鎖同士のジスルフィド結合が可能となり、安定的なダイアボディを形成させることもできる(Olafsen et al., 2004, Prot. Engr. Des. Sel. 17:21-27)。このようにダイアボディは、二価の抗体断片であるが、それぞれの抗原結合部位は、同一エピトープと結合する必要はなく、それぞれが異なるエピトープを認識し、特異的に結合する二重特異性を有していてもよい。トリアボディ及びテトラボディは、ダイアボディと同様に一本鎖Fv構造を基本としたその三量体、及び四量体構造を有する、それぞれ三価及び四価の抗体断片であり、ダイアボディと同様に多重特異性抗体であってもよい。
なお、前記抗マーカー抗体及びその抗原結合性断片は、アノン株の宿主への感染やそれによる炎症を抑制する活性を有する、いわゆる中和抗体であってもよい。本実施形態の抗マーカー抗体及びその抗原結合性断片は、第1実施形態のマーカー中に存在するエピトープを特異的に認識し、結合する。前述のように、第1実施形態のマーカーを構成するペプチドは、いずれもP.ジンジバリスの病原性及び感染性に関与するタンパク質の一部を構成する。したがって、本実施形態の抗マーカー抗体及び/又はその抗原結合性断片は、アノン株において標的エピトープを有するタンパク質に結合することにより、そのタンパク質の本来の機能を阻害、又は抑制する活性を有し得る。その結果、アノン株は、宿主口腔内でその感染力を失うこととなる。ここでいう「宿主」とは、アノン株が感染し得るヒト及び前述の他の哺乳動物が該当する。
2-3.効果
本実施形態の抗マーカー抗体又はその抗原結合性断片によれば、アノン株を特異的に認識することができる。したがって、後述する第5実施形態における被検体から得られるプラークよりアノン株を検出する上で有用である。
本実施形態の抗マーカー抗体又はその抗原結合性断片によれば、アノン株を特異的に認識することができる。したがって、後述する第5実施形態における被検体から得られるプラークよりアノン株を検出する上で有用である。
3.人獣共通感染性歯周病菌感染又は炎症抑制剤
3-1.人獣共通感染性歯周病菌感染又は炎症抑制剤の構成
本発明の第3の実施形態は、人獣共通感染性歯周病菌感染又は炎症抑制剤である。
3-1.人獣共通感染性歯周病菌感染又は炎症抑制剤の構成
本発明の第3の実施形態は、人獣共通感染性歯周病菌感染又は炎症抑制剤である。
本実施形態の「人獣共通感染性歯周病菌感染又は炎症抑制剤」(以下、単に「感染又は炎症抑制剤」とする)は、第2実施形態に記載の一以上の抗体及び/又は一以上の抗原結合性断片を有効成分として含み、アノン株の歯周組織や歯(歯根部)への付着等を特異的に抑制することによりその宿主感染を抑制し、またアノン株由来のタンパク質等を抑制することによって、該タンパク質等により誘導されるサイトカインを介した炎症を抑制することのできる医薬組成物である。
本実施形態の感染又は炎症抑制剤の有効成分である前記抗体及び抗原結合性断片は、いずれも前述したアノン株の宿主への感染を抑制する活性を有する。また、その抗体は、感染又は炎症抑制剤を投与する被検体と同じ生物種由来であるか、組換え抗体であることが好ましい。例えば、投与する被検体がヒトである場合、有効成分である抗体(モノクローナル抗体又はポリクローナル抗体)は、ヒト抗体、C領域がヒト抗体由来であるキメラ抗体、又はヒト化抗体であることが好ましい。
本実施形態の感染又は炎症抑制剤は、前記有効成分に加えて、医薬的に許容可能な担体を含有することができる。
「医薬的に許容可能な担体」とは、製剤技術分野において通常使用し得る添加剤をいう。添加剤には、コラーゲン、ポリビニルアルコール、ポリビニルピロリドン、カルボキシビニルポリマー、カルボキシメチルセルロースナトリウム、ポリアクリル酸ナトリウム、アルギン酸ナトリウム、水溶性デキストラン、カルボキシメチルスターチナトリウム、ペクチン、メチルセルロース、エチルセルロース、キサンタンガム、アラビアゴム、カゼイン、寒天、ポリエチレングリコール、ジグリセリン、グリセリン、プロピレングリコール、ワセリン、パラフィン、ステアリルアルコール、ステアリン酸、ヒト血清アルブミン(HSA)、マンニトール、ソルビトール、ラクトース、医薬添加物として許容される界面活性剤等が挙げられる。
この他、必要に応じて、賦形剤、結合剤、崩壊剤、充填剤、乳化剤、流動添加調節剤、滑沢剤、矯味矯臭剤、溶解補助剤(可溶化剤)、懸濁剤、希釈剤、界面活性剤、安定剤、吸収促進、増量剤、付湿剤、保湿剤(例えば、グリセリン及び澱粉)、吸着剤、崩壊抑制剤、コーティング剤、着色剤、保存剤、抗酸化剤、香料、風味剤、甘味剤、緩衝剤等を含むこともできる。
上記担体は、本実施形態の感染又は炎症抑制剤の剤形に応じて単独で又は適宜組み合わせて使用することができる。例えば、感染又は炎症抑制剤を注射用製剤として使用する場合、精製された抗マーカー抗体を、医薬的に許容可能な溶媒に溶解し、これに吸着防止剤(例えば、Tween80、Tween20、ゼラチン及びヒト血清アルブミン)を添加したものを使用することができる。ここでいう「医薬的に許容可能な溶媒」とは、例えば、水、生理食塩水、緩衝液、ブドウ糖溶液、医薬的に許容される有機溶剤(例えば、エタノール、プロピレングリコール、エトキシ化イソステアリルアルコール、ポリオキシ化イソステアリルアルコール、ポリオキシエチレンソルビタン脂肪酸エステル類)が挙げられる。これらは、殺菌されていることが望ましく、必要に応じて血液と等張に調整されていることが好ましい。
あるいは、本実施形態の感染又は炎症抑制剤は、使用前に溶解再構成する剤形とするために、凍結乾燥したものであってもよい。例えば、凍結乾燥のために賦形剤(例えば、マンニトール、ブドウ糖等の糖アルコールや糖類)を使用することができる。
本発明の医薬組成物は、常法に従って製剤化することができる。製剤化については、例えば、Remington’s Pharmaceutical Science,latest edition,Mark Publishing Company,Easton,U.S.A.を参照されたい。
3-2.感染又は炎症抑制剤の投与方法
本実施形態の感染又は炎症抑制剤は、経口投与、又は組織内投与(例えば、口腔粘膜内投与、筋肉内投与及び静脈内投与)、局所投与(例えば、経粘膜投与)で投与することができる。それ故、感染又は炎症抑制剤の剤形は、投与方法に適する形態であることが好ましい。例えば、組織内投与の場合、血流を介した注射が好ましく、それ故、剤形は液体である。
本実施形態の感染又は炎症抑制剤は、経口投与、又は組織内投与(例えば、口腔粘膜内投与、筋肉内投与及び静脈内投与)、局所投与(例えば、経粘膜投与)で投与することができる。それ故、感染又は炎症抑制剤の剤形は、投与方法に適する形態であることが好ましい。例えば、組織内投与の場合、血流を介した注射が好ましく、それ故、剤形は液体である。
注射の場合、注入部位は特に限定しないが、アノン株の感染部位が口腔内の歯周組織であることを鑑みれば、例えば、静脈内若しくは動脈内等の血管内、又は口腔粘膜内(歯周組織内)であることが好ましい。血管内注射の場合、血流を介して本発明の感染又は炎症抑制剤を直ちに全身に行き渡らせることが可能であり、また侵襲性が比較的低く、被験者に与える負担が小さいからである。また、口腔粘膜内、特に歯周組織内注射の場合、アノン株に直接的に有効成分を作用させることができるからである。
上記の感染又は炎症抑制剤を投与する場合、一投与単位中には、その感染又は炎症抑制活性が発揮され得る有効量が含有されていることが好ましい。ここでいう「有効量」とは、有効成分である抗マーカー抗体やその抗原結合性断片がその機能を発揮する上で必要な量、すなわち、感染又は炎症抑制剤がアノン株の歯周組織への感染及びそれによる炎症の発生を抑制する上で必要な量であって、かつ投与する被験体であるヒト又は他の哺乳動物に対して有害な副作用をほとんど又は全く付与しない量をいう。この有効量は、被験体の情報、剤型及び投与経路等の様々な条件によって変化し得る。「被験体の情報」とは、生物種、歯周病の進行度若しくは重症度、全身の健康状態、年齢(月齢、週齢)、体重、性別、食生活、薬剤感受性、併用医薬の有無及び治療に対する耐性等を含む。上記の感染又は炎症抑制剤の最終的な投与量及び有効量は、個々の被験体の情報等に応じて、医師又は獣医師の判断によって決定される。感染又は炎症抑制効果を得る上で、上記の感染又は炎症抑制剤の大量投与が必要な場合、被験体に対する負担軽減のために数回に分割して投与することもできる。
具体的な投与量の一例として、例えば、アノン株による歯周病感染初期であって、他の薬剤の併用を必要としないヒト成人に投与する場合、感染又は炎症抑制剤の有効量は、一回につき体重1kgあたり0.01mg~100mgの範囲で選択されるが、この投与量に制限されるものではない。
本発明の感染又は炎症抑制剤は、アノン株に対して特異的にその感染性を抑制することによって、該菌によって引き起こされる炎症を抑え、アノン株による歯周病を予防又は治療すると共に、ヒト及び他の哺乳動物間の感染を阻止することが可能となる。
4.人獣共通感染性歯周病菌検出用キット
本発明の第4の実施形態は、人獣共通感染性歯周病菌検出用キットである。本実施形態のキットは、前記第1実施形態に記載の一以上のマーカー、及び/又は第2実施形態の一以上の抗マーカー抗体及び/又は一以上の抗原結合性断片を含む。この他、本キットは、必要に応じて、標識二次抗体、標識の検出に必要な基質、陽性対照や陰性対照、試料の希釈や洗浄に用いる緩衝液及び/又は使用説明書等を加えることもできる。
本発明の第4の実施形態は、人獣共通感染性歯周病菌検出用キットである。本実施形態のキットは、前記第1実施形態に記載の一以上のマーカー、及び/又は第2実施形態の一以上の抗マーカー抗体及び/又は一以上の抗原結合性断片を含む。この他、本キットは、必要に応じて、標識二次抗体、標識の検出に必要な基質、陽性対照や陰性対照、試料の希釈や洗浄に用いる緩衝液及び/又は使用説明書等を加えることもできる。
本実施形態のキットによれば、第2実施形態の抗マーカー抗体又はその抗原結合性断片を用いて、プラーク等の適当な試料中に含まれるアノン株由来の第1実施形態のマーカーを免疫学的測定方法により容易かつ簡便に測定することができる。また、その結果に基づき、試料を提供した被検体のアノン株の保菌の有無を迅速に判定することも可能となる。
さらに、本実施形態のキットによれば、第1実施形態のマーカー用いて、体液等の適当な試料中に含まれる抗アノン株抗体を免疫学的測定方法により容易かつ簡便に測定することができる。また、その結果に基づき、試料を提供した被検体のアノン株の感染歴又はその抗体価の値から現在の感染の有無を迅速に判定することも可能となる。
5.人獣共通感染性歯周病菌感染判定方法
本発明の第5の実施形態は、人獣共通感染性歯周病菌の感染を判定方法である。本実施形態の方法は、被検体におけるアノン株の既往歴及び/又は現在の感染状況を判定することができる。
本発明の第5の実施形態は、人獣共通感染性歯周病菌の感染を判定方法である。本実施形態の方法は、被検体におけるアノン株の既往歴及び/又は現在の感染状況を判定することができる。
本実施形態の判定方法は、抗体検出工程及び判定工程を含む。以下、各工程について具体的に説明をする。
5-1.抗体検出工程
「抗体検出工程」とは、被検体より採取した体液に含まれる配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド中に存在するエピトープを認識する抗体を、実施形態1のマーカーを用いて検出する工程である。
「抗体検出工程」とは、被検体より採取した体液に含まれる配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド中に存在するエピトープを認識する抗体を、実施形態1のマーカーを用いて検出する工程である。
「被検体」とは、本実施形態の判定方法の検査に供される個体であって、アノン株に感染され得る哺乳動物をいう。例えば、ヒトや他の哺乳動物をいう。ここでいう「他の哺乳動物」とは、前述したヒト以外の全ての哺乳動物を意味するが、愛玩動物、特にイヌ及びネコが該当する。
「体液」とは、生体由来の液体物質をいう。例えば、血液(血清、血漿、間質液を含む)、リンパ液、髄液、唾液、尿、汗、涙、精液、膣液、鼻汁、又は細胞若しくは組織抽出液が該当する。本実施形態において、体液は、抗体を含み得るものであれば、特に制限はしない。好ましくは、血液、髄液、リンパ液である。特に、血清は好ましい。
本実施形態でいう「抗体」は、被検体自身の免疫生産システムによって産生され、上記体液中に含まれる抗体をいう。したがって、被検体からの免疫グロブリン分子の任意のクラス、例えば、IgG、IgE、IgM、IgA、IgD及びIgY、又は任意のサブクラス、例えば、IgG1、IgG2、IgG3、IgG4、IgA1、IgA2が該当し、第2実施形態に記載の組換え抗体や抗原結合性断片等の人工的に改変、合成した抗体やその断片は、ここでいう抗体には、該当しない。
本実施形態の「抗体」は、配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド、Hem331、Hem190、Fe55、Fim141、Me85又はMe48を抗原として、その抗原中に存在するエピトープとして認識し、結合する。すなわち、本実施形態の抗体は、アノン株を特異的に認識して結合する抗アノン株抗体(以下、単に「抗アノン株抗体」という)である。それ故、体液中に当該抗体を有する被検体は、アノン株に対する感染歴を有し、体液中に含まれるその抗体価が高い場合には、現在もアノン株を保菌している可能性が高いと推定することができる。
被検体からの体液の採取は、当該分野で公知の技術に準じて行えばよい。例えば、血液であれば、その採取方法は、公知の採血方法に従えばよい。具体的には、末梢血の場合には、末梢部の静脈等に注射をして採取すればよく、骨髄液の場合には、骨髄穿刺(マルク)によって採取すればよく、また、臍帯血の場合には、分娩後胎盤の娩出前の臍帯に針を刺して採取すればよい。被検体から採取した体液は、直ちに本実施形態の判定方法に供してもよいし、ヘパリン等の血液凝固阻害剤を添加する等の適当な処理を行った後に低温下で一旦保存した後に、必要時に、冷凍又は冷蔵血液を公知の方法によって解凍及び加温処理して判定検査に使用すればよい。
本実施形態の判定方法に供する体液は、被検体の種類、その体液の種類又は抗体検出方法によって変動するが、例えば、血液であれば、通常、20μL~200μLの範囲であれば足り、血清であれば、10μL~100μLの範囲であれば足りる。
体液中に含まれる前記抗体を検出する方法は、第1実施形態のマーカーを用いたあらゆる免疫学的検出方法を使用することができる。例えば、第1実施形態のマーカーを用いたELISA法、蛍光免疫測定法、放射免疫測定法若しくは発光免疫測定法により実施することができる。
ELISA法、蛍光免疫測定法、放射免疫測定法及び発光免疫測定法は、いずれも標識した抗体によって抗原であるマーカーと標的抗体との抗原抗体複合体を検出する点において共通する。しかし、その複合体検出のための標識子がそれぞれ異なり、ELISA法では酵素標識、蛍光免疫測定法では蛍光物質、放射免疫測定法では放射性物質、そして発光免疫測定法では発光物質が用いられる。より具体的には、酵素としては、例えば、ペルオキシダーゼ(POD)、アルカリフォスファターゼ、β-ガラクトシダーゼ、ウレアーゼ、カタラーゼ、グルコースオキシダーゼ、乳酸脱水素酵素、アミラーゼ又はビオチン-アビジン複合体等を、蛍光物質としては、蛍光色素(フルオレセイン、FITC、ローダミン、ウンベリフェロン、テキサスレッド、Cy3、Cy5)又は蛍光タンパク質(例えば、PE、APC、GFP)等を、放射性物質としては、例えば、3H、125I若しくは131I等を、そして発光物質としては、NADH-FMNH2-ルシフェラーゼ系、ルミノール-過酸化水素-POD系、アクリジニウムエステル系又はジオキセタン化合物系等を、用いることができる。以下、ELISA法を例に挙げて説明する。
ELISA(Enzyme-Linked Immuno Sorbent Assay)法では、体液中の標的分子である抗アノン株抗体を、固相担体に固定した抗原及び酵素標識抗体等を用いて、当該酵素の作用を利用して抗原抗体反応を発色濃度や蛍光強度として検出し、抗アノン株抗体を定量する方法である。
固相担体に固定する抗原は、第1実施形態に記載のマーカーのいずれか一以上を使用することができる。固相担体には、ポリスチレン、ポリカーボネート、ポリビニルトルエン、ポリプロピレン、ポリエチレン、ポリ塩化ビニル、ナイロン、ポリメタクリレート、ラテックス、ゼラチン、アガロース、セルロース、セファロース、ガラス、金属、セラミックス又は磁性体等の材質よりなるビーズ、マイクロプレート、試験管、スティック又は試験片等の形状の不溶性担体を用いることができる。抗原の固相担体への固定は、物理的吸着法、化学的結合法又はこれらの併用する方法等、公知の方法に従って結合させることにより達成できる。
酵素標識抗体は、被検体の免疫グロブリン分子を抗原とし、特に、その定常領域に存在するエピトープを認識する抗体に適当な検出用酵素で標識したものである。免疫グロブリン分子のクラスは、特に限定はしないが、好ましくはIgGである。標識物質と抗体との結合法は、グルタルアルデヒド法、マレイミド法、ピリジルジスルフィド法又は過ヨウ素酸法等の公知の方法を用いればよい。酵素標識抗体は、ヒトを被検体とする場合には抗ヒトIgG抗体等を、またイヌを被検体とする場合には抗イヌIgG抗体等を使用する点に留意する。
ELISA法の測定方法については、公知である。したがって、具体的な検出方法については、例えば、日本臨床病理学会編「臨床病理臨時増刊特集第53号臨床検査のためのイムノアッセイ-技術と応用-」、臨床病理刊行会、1983年、石川榮治ら編「酵素免疫測定法」、第3版、医学書院、1987年、北川常廣ら編「タンパク質核酸酵素別冊No.31酵素免疫測定法」、共立出版、1987年、入江實編「ラジオイムノアッセイ」、講談社サイエンティフィク、1974年、入江實編「続ラジオイムノアッセイ」、講談社サイエンティフィク、1979年を参照すればよい。
以下でELISA法を用いた本実施形態の抗体検出について、一例を挙げて説明をする。まず、第1実施形態に記載のマーカーの一つ、例えば、Fe55を抗原として担体に固相化する。なお、固相化するマーカーは、Fe55の1種類のみならず、複種類であってもよい。次に、固相化したFe55に、抗アノン株IgG抗体を含み得るヒト血清を作用させ、Fe55と抗アノン株抗体の複合体を担体の表面上に形成させる。その後、洗浄液を用いて十分に洗浄することで、試料中に存在していた抗アノン株抗体以外の未結合の抗体が除去される。さらに、標識化したヒトIgGを特異的に認識する抗ヒトIgG抗体を作製し、この標識抗体を前記複合体が形成された担体に作用させる。洗浄液を用いて十分に洗浄した後、標識を利用して複合体を検出することで試料中に存在する抗アノン株抗体を検出することができる。抗アノン株抗体を含み得る体液と前記標識抗体とを先に混合し、抗体複合体を形成させた後に、前記固相化マーカーに作用させてもよい。あるいは、固相化するマーカーを、例えば、ビオチンで標識しておき、ビオチン化マーカー、抗アノン株抗体、ビオチン以外の標識抗体を、予め全て混合して抗原抗体複合体を形成させた後、アビジンを固相化した担体に作用させることで、前記抗原抗体複合体を検出することもできる。
また、免疫学的検出方法として、免疫クロマト用テストストリップを用いることもできる。「免疫クロマト用テストストリップ」とは、例えば、試料を吸収しやすい材料からなる試料受容部、本発明の診断薬を含有する試薬部、試料と診断薬との反応物が移動する展開部、展開してきた反応物を呈色する標識部、呈色された反応物が展開してくる提示部等から構成される。例えば、市販の妊娠診断薬等がこれと同様の形態を有する。本実施形態の場合、まず、試料受容部に体液を供することで、試料受容部は、体液を吸収して試薬部にまで到達させる。続いて、試薬部において体液中の抗アノン株抗体とマーカーが抗原抗体反応し、一次複合体が形成される。続いて、その一次複合体が展開部を移動して標識部に到達する。標識部では、一次複合体と標識抗体との反応により二次複合体が生じ、その二次複合体が提示部にまで展開すると、呈色が認められることになる。上記免疫クロマト用テストストリップは、侵襲性が低く、使用者に対し苦痛や試薬使用による危険性を一切与えないものであるため、家庭におけるモニターに使用することができ、その結果を各医療機関レベルで精査・治療(外科的切除等)し、転移・再発予防に結びつけることが可能となる。また、このようなテストストリップは、例えば、特開平10-54830号に記載の製造方法等により安価に大量生産できる点でも便利である。
この他、免疫学的検出方法として、免疫比濁法、ラテックス凝集反応、ラテックス比濁法のような赤血球凝集反応又は粒子凝集反応等の免疫複合体凝集物の生成を、その透過光や散乱光を光学的方法によって測定するか、目視的に測る方法が挙げられる。その場合には、溶媒としてリン酸緩衝液、グリシン緩衝液、トリス緩衝液又はグッド緩衝液等を用いることができ、さらにPEG等の反応促進剤や非特異的反応抑制剤を含ませてもよい。これらは、いずれも公知の方法であるので、公知の技術に基づいて検出すればよい。
また、免疫学的検出方法として、表面プラズモン共鳴法(SPR法)を用いることもできる。表面プラズモン共鳴現象とは、金属薄膜に特定の入射角度(共鳴角)でレーザー光を照射すると反射光強度が著しく減衰する現象をいう。SPR現象の原理を利用したSPRセンサは、金属薄膜表面上の吸着物を高感度に測定することができる。したがって、該金属薄膜表面上に予め抗体及び/又は標的抗原を固定化しておき、その金属薄膜表面上に試料を通過させることにより、抗原抗体反応の結果生じた試料通過前後の金属表面上の吸着物の差を検出することができる。置換法、間接競合法等が知られるが、いずれを用いてもよい。本技術は、当該分野において周知である。例えば、永田和弘、及び半田宏、生体物質相互作用のリアルタイム解析実験法、シュプリンガー・フェアラーク東京、東京、2000を参照されたい。
さらに、本発明の測定方法は、水晶振動子マイクロバランス測定法(QCM法)を用いることもできる。この方法は、晶振動子に取り付けた電極表面に物質が吸着するとその質量に応じて水晶振動子の共振周波数が減少する現象を利用するものである。該方法を用いたQCMセンサは、水共振周波数の変化量によって極微量な吸着物を定量的に捕らえる質量測定センサである。本技術は、当該分野において周知である。例えば、J.Christopher Love, et al., 2005, Chemical Review, 105:1103-1169;森泉豊榮, 中本高道, 1997, センサ工学, 昭晃堂を参照されたい。
5-2.判定工程
「判定工程」は、抗体検出工程の結果に基づいて、被検体のアノン株に対する感染の有無を判定する工程である。
「判定工程」は、抗体検出工程の結果に基づいて、被検体のアノン株に対する感染の有無を判定する工程である。
ここでいう「感染の有無」は、過去に被検体がアノン株に感染したことがあるか否か(感染歴)、及び現在アノン株に感染しているか否か(感染状況)のいずれも含む。
感染歴については、前記抗体検出工程の結果、被検体の体液から抗アノン株抗体が検出された場合には、その被検体が少なくとも過去及び/又は現在アノン株に感染されていた又は感染されていると判定する。一方、抗アノン株抗体が検出されなかった場合には、その被検体は、これまでアノン株の感染歴はない可能性が高いと判定する。
感染状況については、前記抗体検出工程の結果、被検体の体液から抗アノン株抗体が検出された場合であって、その抗体価がカットオフ値(対照での抗体価+3SD(標準偏差))以上のとき、その個体は、現在アノン株に感染している可能性が高いと判定する。一方、抗体価がカットオフ値を下回るときは、その個体は、過去にアノン株への感染歴があるが、現在は感染していない可能性が高いと判定する。なお、カットオフ値は、被検体と同種の生物で、アノン株未感染の個体群の体液、好ましくは血清中の抗アノン株抗体の抗体価に基づいて、定めればよい。例えば、被検体がイヌで、Fe55に対する抗体価のカットオフ値は、未感染個体の抗体価の「平均値+3SD」とすればよい。
抗体価は、前記抗体検出工程に記載の免疫学的検出方法による測定値に基づいて算出すればよい。例えば、ELISA等が該当する。
6.人獣共通感染性歯周病菌検出方法
本発明の第6の実施形態は、人獣共通感染性歯周病菌の検出方法である。本実施形態の方法は、被検体がアノン株を保菌しているか否かを検出することができる。
本発明の第6の実施形態は、人獣共通感染性歯周病菌の検出方法である。本実施形態の方法は、被検体がアノン株を保菌しているか否かを検出することができる。
本実施形態の検出方法は、ポリペプチド検出工程を含む。
「ポリペプチド検出工程」とは、被検体より採取したプラークに含まれる前記第1実施形態に記載のマーカーを含む一以上のポリペプチドを、前記第2実施形態に記載の抗原結合性断片を用いて検出する工程である。
「プラーク」とは、歯垢とも呼ばれ、口腔内の歯周組織や歯(歯根部)に付着した歯周病菌を含む口腔常在菌とその代謝物から構成される。
「第1実施形態に記載のマーカーを含む一以上のポリペプチド」(以下、便宜的に「マーカータンパク質」とする)とは、配列番号1~7で示されるアミノ酸配列を含むアノン株特異的なHagB、FeoB-1、fimA若しくはメタロプロテアーゼ又はそのポリペプチド断片をいう。すなわち、プラークから前記タンパク質又はそのポリペプチド断片のいずれかが一以上検出された場合には、そのプラークを採取した被検体の口腔内にはアノン菌が存在することを意味する。
被検体からのプラークの採取は、当該分野で公知の技術に準じて行えばよい。例えば、綿棒やスクレーパー等を用いて採取する。その後、必要に応じて適当なバッファに懸濁してもよい。
プラーク中に含まれる前記マーカータンパク質は、第2実施形態の抗アノン株抗体及び/又はその抗原結合性断片(以下、「抗アノン抗体」等とする)を用いることを除けば、基本的には第5実施形態の検出工程で用いた免疫学的検出方法によって検出することができる。すなわち、第2実施形態の抗アノン株抗体等を用いて、ELISA法、蛍光免疫測定法、放射免疫測定法若しくは発光免疫測定法、表面プラズモン共鳴法(SPR法)、又は水晶振動子マイクロバランス測定法(QCM法)によってマーカータンパク質を検出することができる。
本実施形態では、抗アノン抗体等を用いて、抗原であるマーカーを包含するマーカータンパク質をプラーク中から検出するため、前記ELISA法も、直接法及び間接法に加えて、サンドイッチ法を使用することができる。特に、本実施形態においては、このサンドイッチ法が好ましく適用される。「サンドイッチ法」は、固相担体に固定した第1抗体(固相化抗体)を、抗原と結合させた後、第1抗体とは異なるエピトープを認識する第2抗体(標識抗体又は一次抗体)を加えて抗原と結合させ、第2抗体が標識抗体の場合にはその標識を、また第2抗体が一次抗体の場合には第3抗体(二次抗体)によって、検出する方法である。以下で、具体例を挙げてサンドイッチELISA法により本実施形態の検出方法を説明する。
まず、例えば、実施形態2の抗アノン株抗体等を、担体に固相化する。固相化する抗アノン株抗体等は、1種類であっても、又は数種類であってもよい。次に、固相化した抗アノン株抗体(以下、「固相化抗体」とする)に、マーカータンパク質を含み得るプラークを懸濁したバッファ等の試料を作用させ、固相化抗体とマーカータンパク質からなる抗原抗体複合体(固相化複合体)を固相担体表面に形成させる。その後、洗浄液を用いて十分に洗浄して、固相化抗体と未結合の物質を除去する。続いて、マーカータンパク質中のマーカーに存在し、前記固相化抗体とは異なるエピトープを特異的に認識する抗体を標識抗体として標識し、固相化複合体が結合した担体に作用させる。すなわち、ここで使用する固相化抗体と標識抗体は、いずれも第1実施形態に記載した同一のマーカーを認識する第2実施形態の抗アノン株抗体等を使用することができる。これによって、固相担体上に固相化抗体/マーカータンパク質/標識抗体からなる三重複合体が形成される。その後、洗浄液を用いて未結合の標識抗体を十分に洗浄した後、前記三重複合体における標識抗体の標識を利用して検出することで試料中に存在したマーカータンパク質を検出及び定量することができる。標識抗体は、1種類であっても数種類であってもよいが、2種類以上使用することが好ましく、3種類使用することがより好ましい。また、固相化抗体と標識抗体の由来する動物種が異なる場合には、標識抗体を標識しなくても、一次抗体として固相化抗体/マーカータンパク質に作用させて、その一次抗体を認識する標識二次抗体を使用して、検出することもできる。なお、固相化に用いた抗体と標識に用いた抗体は、それぞれ逆に用いることも可能である。
また、標識抗体とマーカータンパク質を含む試料を予め混合して抗原抗体複合体を形成させた後、固相化抗体に作用させることもできる。固相化抗体をビオチン標識しておけば、ビオチン化固相化抗体、マーカータンパク質を含む試料、ビオチン以外の標識抗体を混合して抗原抗体複合体を形成させた後、アビジンを固相化した担体に作用させることで、ビオチン化以外の標識を利用して抗原抗体複合体を検出することができる。
7.人獣共通感染性歯周病菌治療用ワクチン
本発明の第7の実施形態は、人獣共通感染性歯周病菌治療用ワクチンである。本実施形態のワクチンは、アノン株を不活化又は弱毒化処理することによって得ることができる。
本発明の第7の実施形態は、人獣共通感染性歯周病菌治療用ワクチンである。本実施形態のワクチンは、アノン株を不活化又は弱毒化処理することによって得ることができる。
アノン株の培養は、P.ジンジバリスに公知の培養方法を用いればよい。例えば、BHI培地(精製水1Lあたり脳抽出物、心臓抽出物及びペプトンの混合物27.5g、D-グルコース2.0g、塩化ナトリウム5.0g、リン酸水素2ナトリウム2.5g;Merk社)又はGAM培地(精製水1Lあたりペプトン10.0g、大豆ペプトン3.0g、プロテアーゼペプトン10.0g、血清末13.5g、酵母エキス5.0g、肉エキス1.2g、ブドウ糖3.0g、リン酸2水素カリウム2.5g、塩化ナトリウム3.0g、可溶性でんぷん5.0g、L-システイン塩酸塩0.3g、チオグリコール酸ナトリウム0.3g;ニッスイ社)にて37℃で、48時間嫌気条件下で培養する方法が挙げられる。嫌気条件は、嫌気性グローブボックス(N2 70%、CO215%、H215%)、又は嫌気ジャー内で行えばよい。
ワクチンとして使用するためのアノン株の不活化又は弱毒化処理は、公知の方法で行えばよい。例えば、ホルマリン、β-プロピオラクトン、グルタルジアルデヒド等の不活化剤を、感染性アノン株を含む培養液に添加して、十分に混合することにより達成できる(Appaiahgari et al., 2004, Vaccine, 22:3669-3675)。また、感染性アノン株に紫外線を照射することにより感染性を迅速に失わせることもできる。紫外線照射による不活性化方法は、アノン株を構成するタンパク質等への影響が少ない点で好ましい。紫外線の線源には、一般に市販されている殺菌灯、特に15W殺菌灯を用いることができるが、それに限るものではない。
なお、本発明のアノン株を不活化又は弱毒化した人獣共通感染性歯周病菌治療用ワクチンは、二種以上の他のワクチンと共に混合ワクチンとして使用することができる。混合するワクチンの種類は特に限定しないが、好ましくはアノン株以外の歯周病菌を不活化又は弱毒化したワクチンである。例えば、ポルフィロモナス属に属する菌を上記と同様の公知の方法により不活化又は弱毒化したワクチンが挙げられる。具体的には、例えば、アノン株以外のP.ジンジバリス菌又はP.グラエを不活化又は弱毒化したワクチンである。
[実施例1]
<人獣共通感染性歯周病菌検出用マーカーの分離>
従来予想されていなかった人獣に共通の感染性歯周病菌として同定されたP. ジンジバリス アノン株からアノン株特異的な検出用マーカーを分離する。
<人獣共通感染性歯周病菌検出用マーカーの分離>
従来予想されていなかった人獣に共通の感染性歯周病菌として同定されたP. ジンジバリス アノン株からアノン株特異的な検出用マーカーを分離する。
(方法)
アレイCGDによるゲノム解析を用いて、Mutation Mappingで解読の完了した遺伝子情報からヒト及び他の哺乳動物間で共通の領域及び動物株特異な領域を決定した。具体的には、Mutation Mapping及びリシークエンス解析を行い、ヒト由来W83株と動物(イヌ)由来アノン株の共通領域、すなわち、4抗原×3領域からなる計12種のアミノ酸配列を有するペプチド(Hem331、Hem301、Hem190、Fe297、Fe259、Fe55、Fim331、Fim141、Fim353、Me85、Me48、Me191)をマーカー候補として合成した。ここで、Hem301は、P.ジンジバリスW83株におけるHagBの301位~320位に相当するアミノ酸配列からなるペプチドであることを示す。Fe297及びFe259は、それぞれP.ジンジバリスW83株におけるFeoB-1の297位~315位に相当するアミノ酸配列からなるペプチド及び259位~278位に相当するアミノ酸配列からなるペプチドであることを示す。Fim331及びFim141は、それぞれP.ジンジバリスW83株におけるfimAの331位~350位に相当するアミノ酸配列からなるペプチド及び141位~160位に相当するアミノ酸配列からなるペプチドであることを示す。また、Me191は、P.ジンジバリスW83株におけるメタロプロテアーゼの191位~210位に相当するアミノ酸配列からなるペプチドであることを示す。他のペプチドについては、上述した通りである。ペプチドの合成は、神戸天然物化学株式会社KNCバイオリサーチセンターに委託した。
アレイCGDによるゲノム解析を用いて、Mutation Mappingで解読の完了した遺伝子情報からヒト及び他の哺乳動物間で共通の領域及び動物株特異な領域を決定した。具体的には、Mutation Mapping及びリシークエンス解析を行い、ヒト由来W83株と動物(イヌ)由来アノン株の共通領域、すなわち、4抗原×3領域からなる計12種のアミノ酸配列を有するペプチド(Hem331、Hem301、Hem190、Fe297、Fe259、Fe55、Fim331、Fim141、Fim353、Me85、Me48、Me191)をマーカー候補として合成した。ここで、Hem301は、P.ジンジバリスW83株におけるHagBの301位~320位に相当するアミノ酸配列からなるペプチドであることを示す。Fe297及びFe259は、それぞれP.ジンジバリスW83株におけるFeoB-1の297位~315位に相当するアミノ酸配列からなるペプチド及び259位~278位に相当するアミノ酸配列からなるペプチドであることを示す。Fim331及びFim141は、それぞれP.ジンジバリスW83株におけるfimAの331位~350位に相当するアミノ酸配列からなるペプチド及び141位~160位に相当するアミノ酸配列からなるペプチドであることを示す。また、Me191は、P.ジンジバリスW83株におけるメタロプロテアーゼの191位~210位に相当するアミノ酸配列からなるペプチドであることを示す。他のペプチドについては、上述した通りである。ペプチドの合成は、神戸天然物化学株式会社KNCバイオリサーチセンターに委託した。
続いて、合成した12種のペプチドを用いて、ELISA法によりアノン株の免疫学的検出方法に効率的なペプチドをスクリーニングした。スクリーニングの概略を以下に記載する。96ウェルマイクロプレート上へのペプチドの固相化は、ペプチドコーティングキット(タカラバイオ社)を用いた。具体的には、ペプチド100μgを25mLのリアクションバッファー(キット添付試薬)に溶解し、96ウェルマイクロプレートに50μL/ウェルとなるように分注した。次に、カップリング試薬(エチル酸ジメチルアミノプロピルカルボジイミドハイドロクロライド:キット添付試薬)を蒸留水で溶解し、96ウェルマイクロプレートに10μL/ウェルを分注した。十分に混合した後、2時間、室温で反応させて、フリーのカルボキシル基にカップリングを行った。続いて、マイクロプレートの底面に表出しているアミノ基との間で架橋させて固相化した。各ウェルを3回洗浄し、ブロッキング後サンプル中の抗体の検出を行った。抗体の検出には1:100に希釈した血清を用いた。血清は、生後2~8ヶ月のP.ジンジバリス分離陰性ラブラドールレトリーバ5匹、並びにアノン株が分離されたP.ジンジバリス分離陽性ラブラドールレトリーバ1匹及びアノン株と同様の性状を示す6匹のイヌ(すなわち、ジャーマンシェパード雄1匹(5歳)、雌3匹(4歳及び9歳)、ゴールデンレトリーバ雌1匹(8歳)、ラブラドールレトリーバ雌2匹(1歳及び3歳))の計7匹から採取した。室温で1時間希釈した血清と反応後、10回洗浄、室温1時間ペルオキシダーゼ標識プロテインA(Abcam,Co.)と反応させ、10回洗浄した後、発色基質TMB(K-blue,Neogen.Co. Lexington KY)で発色、1N硫酸で反応停止し、ELISAリーダー(ELNX96, TFB社)でOD値を求めた。
なお、本明細書で「分離陰性」とは、P.ジンジバリス培養陰性で、口腔内に炎症がなく、仮に口腔内にP.ジンジバリスが存在したとしても非常に少ない菌数であり、また炎症がないことから体内への当該菌の侵入はなく、したがって抗体も産生されない状態をいう。
(結果)
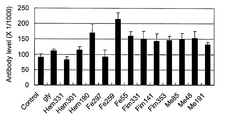
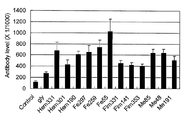
結果を図1及び2に示す。図1は、P.ジンジバリス分離陰性のイヌの血清の平均抗体価を示す。また、図2は、P.ジンジバリス分離陽性のイヌ及びアノン株と同様の性状を示すイヌの血清の平均抗体値を示す。
結果を図1及び2に示す。図1は、P.ジンジバリス分離陰性のイヌの血清の平均抗体価を示す。また、図2は、P.ジンジバリス分離陽性のイヌ及びアノン株と同様の性状を示すイヌの血清の平均抗体値を示す。
図1で示すように、抗体陰性のイヌ血清は、牛胎児血清を用いたバックグラウンド(Control)の抗体価及びグリシンをコートした96ウェルマイクロプレートを用いた対照(gly)の抗体価との間で、Hem331、Hem301、Fe297については、有意差は見られなかった。また、それ以外のペプチドについては、平均値において有意な差が認められたものの、たとえ有意差があっても偽陽性となる可能性が高いほどにOD値が低かった。
一方、図2で示すように、P.ジンジバリス分離陽性のイヌ及びアノン株と同様の性状を示すイヌの血清は、いずれのペプチドも図1のP.ジンジバリス分離陰性のイヌの血清と比較して平均抗体値が4~5倍に上昇した。図1と図2における平均抗体値の差の検定を行った結果、用いたペプチド抗原12種のうち7種類(Hem331、Hem190、Fe55、Fim141、Fim353、Me85、Me48)が有意に高かった。この結果から、配列番号1~7で示す前記7種類のペプチドを人獣共通感染性歯周病菌アノン株検出用マーカー(以降、本明細書の実施例において、しばしば「検出用マーカー」と表記する)として分離した。
[実施例2]
<イヌにおける抗体価と臨床所見との相関(1)>
実施例1で得られた7種の人獣共通感染性歯周病菌アノン株検出用マーカーが、実際にアノン菌感染判定に利用できるか否かを、ビーグル犬10匹を用いて検証した。
<イヌにおける抗体価と臨床所見との相関(1)>
実施例1で得られた7種の人獣共通感染性歯周病菌アノン株検出用マーカーが、実際にアノン菌感染判定に利用できるか否かを、ビーグル犬10匹を用いて検証した。
(方法)
まず、対照用として、分離陰性で、かつ曝露期間の短い生後8ヶ月の個体5匹(No.1~5)から末梢血2mLを、シリンジを用いて採取した。これらの個体については、引き続き飼育し、2歳時の歯周病未発症段階に、再び同量の末梢血を採取した。
まず、対照用として、分離陰性で、かつ曝露期間の短い生後8ヶ月の個体5匹(No.1~5)から末梢血2mLを、シリンジを用いて採取した。これらの個体については、引き続き飼育し、2歳時の歯周病未発症段階に、再び同量の末梢血を採取した。
次に、歯周病を発症し、アノン株が検出された歯周病菌分離陽性である5~6歳の雌個体5匹(No.6~10)のそれぞれから同様に末梢血2mLを、シリンジを用いて採取した。
各個体から採取した末梢血を室温で凝固させ、3000rpm/10分間遠心した後、血清を分離した。
続いて、得られた血清のうち10μLを用いて、血清中の抗アノン株抗体を実施例1で分離した検出用マーカーによるELISA法で検出した。検出用マーカーの96ウェルマイクロプレートへの固相化は、ペプチドコーティングキット(タカラバイオ社)を用いた。具体的には、検出用マーカー100μgを25mLのリアクションバッファー(上述)に溶解し、96ウェルマイクロプレートに50μL/ウェルとなるように分注した。カップリング試薬を蒸留水で溶解し、10μL/ウェルを分注した。十分に混合した後、2時間室温でカップリングを行い、固相化した。各ウェルを3回洗浄し、ブロッキングを行った。また、各血清は、リン酸緩衝食塩水(pH7.4、ブロッキング液-ブロックエース1%含有)で1:100に希釈したものを用いた。室温で1時間血清と反応させた後、洗浄液(リン酸緩衝食塩水(pH7.4);0.05% Tween 20及び0.1% ブロッキング液-ブロックエース含有)で10回洗浄し、室温で1時間ペルオキシダーゼ標識プロテインA(Abcam,Co.)と反応させた。前記洗浄液で10回洗浄した後、発色基質TMB(K-blue,Neogen.Co. Lexington KY)で発色させ、1N硫酸で反応停止し、ELISAリーダー(ELNX96, TFB社)でOD値(492nm)を測定した。
(結果)
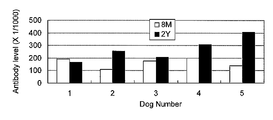
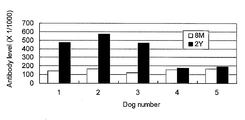
結果を図3及び4に示す。抗体価は、ELISAにおける抗体レベルを示すOD値で示した。
結果を図3及び4に示す。抗体価は、ELISAにおける抗体レベルを示すOD値で示した。
図3Aは、対照用グリシンに対する生後8ヶ月時(8M)と2歳時(2Y)の抗体価を示す。この図に示すように、NO.1~5の各個体において、生後8ヶ月時(8M)と2歳時(2Y)の抗体価はいずれも低かった。
そこで、このグリシンにおける平均抗体価(n=5×2=10)と式(対照の平均抗体価+3SD)に基づき、「陽性」と判断するカットオフ値を0.153+(3×0.030)と定めた。
図3B、3C、3D、3E、3F、3G及び3Hは、それぞれHem331、Hem190、Fe55、Fim141、Fim353、Me85及びMe48の7種の人獣共通感染性歯周病菌アノン株検出用マーカーに対する生後8ヶ月時(8M)と2歳時(2Y)の抗体価を示す。これらの図で示すように、生後8ヶ月時では、いずれの検出用マーカーを用いた場合も抗体価は0.2以下と低かった。一方、2歳時における歯周病未発症時は、個体により異なってはいたが、いくつかの検出用マーカーで抗体価の上昇が見られ、抗体陽性率は、Fim141、Fim353、Me85及びMe48で60%であった。つまり、アノン株分離陰性であっても、本発明の検出用マーカーを用いて体液中の抗アノン株抗体等を検出することによって、アノン株の既往歴、すなわち過去感染していたか又は現在保菌していると推定できることが立証された。
図4は、アノン株分離陽性である5~6歳の5個体(No.6~10)における、グリシン及び7種の検出用マーカーに対する抗体価を示す。この図で示すように、アノン株分離陽性個体では、7種の検出用マーカー全てにおいて高い抗体価が得られ、抗体陽性率は100%を示した。本発明の検出用マーカーを用いることで、その個体のアノン株の既往歴を推定できることが立証された。
[実施例3]
<イヌにおける抗体価と臨床所見との相関(2)>
抗体価と臨床所見としての歯肉炎指数GIとの関連性をビーグル犬で検証した。
<イヌにおける抗体価と臨床所見との相関(2)>
抗体価と臨床所見としての歯肉炎指数GIとの関連性をビーグル犬で検証した。
(方法)
ビーグル犬は、実施例2と同様に、分離陰性の5匹(8ヶ月時及び2歳時の2回)及び分離陽性の5匹(5~6歳)を使用した。用いた歯肉炎指数GI(Jpn. J. Vet. Sci., 51:1151-1162, 1989)は、Loe &Silnessの方法をイヌ用に改変したものであり、診査は、頬側からのみで行った。全歯牙に対応する歯肉の炎症を4段階で評価し、各個体の平均値として表わした。なお、抗体価測定法は、実施例1、2と同様ELISA法により測定した。
ビーグル犬は、実施例2と同様に、分離陰性の5匹(8ヶ月時及び2歳時の2回)及び分離陽性の5匹(5~6歳)を使用した。用いた歯肉炎指数GI(Jpn. J. Vet. Sci., 51:1151-1162, 1989)は、Loe &Silnessの方法をイヌ用に改変したものであり、診査は、頬側からのみで行った。全歯牙に対応する歯肉の炎症を4段階で評価し、各個体の平均値として表わした。なお、抗体価測定法は、実施例1、2と同様ELISA法により測定した。
(結果)
8ヶ月時及び2歳時の5匹では、いずれもG1=0であり、歯肉の炎症は見られなかった。一方、分離陽性の5匹では、GIは、2、2.1、1.3、2.8、及び2.1であった。スピルマン順位相関で抗体価とGIとの相関係数及び有意差があるかどうかを検討した。結果を表1に示す。それぞれ7種のペプチドに対する抗体価は、GIと相関し、またいずれも有意差が見られることが明らかとなった。
8ヶ月時及び2歳時の5匹では、いずれもG1=0であり、歯肉の炎症は見られなかった。一方、分離陽性の5匹では、GIは、2、2.1、1.3、2.8、及び2.1であった。スピルマン順位相関で抗体価とGIとの相関係数及び有意差があるかどうかを検討した。結果を表1に示す。それぞれ7種のペプチドに対する抗体価は、GIと相関し、またいずれも有意差が見られることが明らかとなった。
[実施例4]
<ヒトにおける抗体価と臨床所見の相関>
実施例1で得られた人獣共通感染性歯周病菌アノン株検出用マーカーが、ヒトに対しても使用可能であることを示すため、ヒト血清中の抗アノン株抗体の検出を行った。
<ヒトにおける抗体価と臨床所見の相関>
実施例1で得られた人獣共通感染性歯周病菌アノン株検出用マーカーが、ヒトに対しても使用可能であることを示すため、ヒト血清中の抗アノン株抗体の検出を行った。
(方法)
抗体価の基本的な測定方法は、実施例2の方法に準じた。なお、ヒトのIgG1、2及び4は、イヌIgGと同様にプロテインAと強い結合性を示すことが知られている。
抗体価の基本的な測定方法は、実施例2の方法に準じた。なお、ヒトのIgG1、2及び4は、イヌIgGと同様にプロテインAと強い結合性を示すことが知られている。
(結果)
図5に結果を示す。ヒトの歯周疾患は、年齢依存性に患者数が増加し、症状が進行することが知られている。選択したペプチド領域について、ヒトでも年齢依存性に抗アノン株抗体の保有率及び抗体価の上昇が見られた。この結果から、本発明の検出用マーカーは、動物だけでなく、ヒトのアノン株既往歴の診断用にも使えることが立証された。
図5に結果を示す。ヒトの歯周疾患は、年齢依存性に患者数が増加し、症状が進行することが知られている。選択したペプチド領域について、ヒトでも年齢依存性に抗アノン株抗体の保有率及び抗体価の上昇が見られた。この結果から、本発明の検出用マーカーは、動物だけでなく、ヒトのアノン株既往歴の診断用にも使えることが立証された。
[実施例5]
<イヌ特異的ペプチドの合成>
上記検出用マーカーのように、ヒト由来株W83と共通する領域を抗原ペプチドとして用いた場合、感染菌がイヌを自然宿主とする動物由来株タイプなのか、又はヒトを自然宿主としているヒト由来株タイプなのかの判断ができない。そこで、歯周病未発症犬と歯周病発症犬でのそれぞれの抗原ペプチドに対する抗体価を検証し、動物由来株タイプに対して特異的に反応するペプチド抗原(獣特異的感染マーカー)の作成を試みた。
<イヌ特異的ペプチドの合成>
上記検出用マーカーのように、ヒト由来株W83と共通する領域を抗原ペプチドとして用いた場合、感染菌がイヌを自然宿主とする動物由来株タイプなのか、又はヒトを自然宿主としているヒト由来株タイプなのかの判断ができない。そこで、歯周病未発症犬と歯周病発症犬でのそれぞれの抗原ペプチドに対する抗体価を検証し、動物由来株タイプに対して特異的に反応するペプチド抗原(獣特異的感染マーカー)の作成を試みた。
歯周病発症犬は、いずれもアノン株タイプを保有している。このアノン株タイプが単なる一過性の保菌であるならば、抗体応答を起こさないことになる。逆に、発症に伴う高い抗体価が認められれば、感染関連の抗原領域を示すペプチドといえる。
(方法)
ANON-hexosaminidase(配列番号8)、ANON-ASCP(配列番号9)、ANON-HagE (配列番号10)のペプチド合成を行った。これらの合成ペプチドは、ヒトタイプのP.ジンジバリス菌とは異なるアノン株特有のアミノ酸配列を有している。抗原は、ペプチドコーティングキットを用いて固相化した。抗体価についてELISAを用いた。イヌは、ラブラドールレトリーバ、ゴールデンレトリーバ、ジャーマンシェパードの3犬種を使用した。それぞれの犬種を歯周病未発症犬と歯周病発症犬とにグループ分けして、後者は、アノン株タイプを保有していることを確認した。
ANON-hexosaminidase(配列番号8)、ANON-ASCP(配列番号9)、ANON-HagE (配列番号10)のペプチド合成を行った。これらの合成ペプチドは、ヒトタイプのP.ジンジバリス菌とは異なるアノン株特有のアミノ酸配列を有している。抗原は、ペプチドコーティングキットを用いて固相化した。抗体価についてELISAを用いた。イヌは、ラブラドールレトリーバ、ゴールデンレトリーバ、ジャーマンシェパードの3犬種を使用した。それぞれの犬種を歯周病未発症犬と歯周病発症犬とにグループ分けして、後者は、アノン株タイプを保有していることを確認した。
(結果)
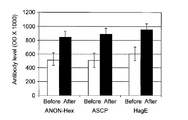
図6に結果を示す。図6AはANON-hexosaminidaseの、図6BはANON-ASCPの、そして図6CはANON-HagEの結果を示している。いずれの合成ペプチドを用いた場合にも、歯周疾患未発症犬10匹(No.1~10)では、全て抗体陰性であり、また歯周疾患発症犬(菌分離陽性 5匹、No.11~15)では全て抗体陽性であった。抗体価は、未発症犬で0.032~0.116と低かった。一方、発症犬では0.586~1.214と高い値を示した。したがって、ANON-hexosaminidase、ANON-ASCP、及びANON-HagEは、いずれも獣特異的感染マーカーとなり得ることが示された。
図6に結果を示す。図6AはANON-hexosaminidaseの、図6BはANON-ASCPの、そして図6CはANON-HagEの結果を示している。いずれの合成ペプチドを用いた場合にも、歯周疾患未発症犬10匹(No.1~10)では、全て抗体陰性であり、また歯周疾患発症犬(菌分離陽性 5匹、No.11~15)では全て抗体陽性であった。抗体価は、未発症犬で0.032~0.116と低かった。一方、発症犬では0.586~1.214と高い値を示した。したがって、ANON-hexosaminidase、ANON-ASCP、及びANON-HagEは、いずれも獣特異的感染マーカーとなり得ることが示された。
[実施例6]
<アノン株を用いた歯周病予防ワクチン>
不活化したアノン株ワクチンと、ワクチン接種後の歯周病の炎症改善について検証した。
<アノン株を用いた歯周病予防ワクチン>
不活化したアノン株ワクチンと、ワクチン接種後の歯周病の炎症改善について検証した。
(方法)
ラブラドールレトリーバ由来のアノン株を遠心し、PBSで洗浄した後、再びPBSに懸濁した。5×108/MLに調整したアノン菌液を最終濃度0.4%のホルマリンで4℃にて一晩固定し、菌を不活化した。PBSで洗浄し、一部について生残菌の有無を確認したがあるかどうかを調べた。すなわち、不活化5×108/MLの細菌浮遊液0.1MLを7%馬血液加BHI寒天培地に接種し、嫌気性培養装置(混合ガス:N2 70%, CO2 15%, H2 15% 環境下)内で37℃72時間培養し、増殖する細菌のないことを確認した。不活化の確認後、軽度~中等度の歯周疾患を発症しているビーグル犬にそのワクチンの接種を行った。ワクチン接種による歯周病の炎症の改善は、抗体価の上昇について検証した。炎症の指標にはGIを用いた。GIは、Isogaiらの方法(Isogai H., et al., 1989, Jpn. J. Vet. Sci. 51, 1151-1162)に従った。すなわち、診査は上顎右の頬側から順番に、大臼歯(M2及びM1)、小臼歯(P4,P3,P2,P1)、犬歯(C)、前歯(I3,I2,I1)と続き、次いで上顎左頬側に移動し、左上顎前歯(I1,I2,I3)、犬歯(C)、小臼歯(P1,P2,P3,P4)、大臼歯(M1,M2)と続き、その後、下顎に移り、左側の大臼歯(M3,M2,M1)、小臼歯(P4,P3,P2,P1)、犬歯(C)、前歯(I3,I2,I1)を確認後、下顎左側に移動して前歯(I1,I2,I3)、犬歯(C)、小臼歯(P1,P2,P3,P4)、大臼歯(M1,M2,M3)を確認した。それぞれの歯の歯肉部分の炎症の程度を、炎症なし:0、軽度炎症:1、中等度炎症:2、重度炎症:3とスコアリングした。前記スコアの中間段階の炎症については、0.5、1.5、2.5とした。それぞれの歯の歯肉部分の炎症の程度の平均値を各イヌの平均GIとして表した。
ラブラドールレトリーバ由来のアノン株を遠心し、PBSで洗浄した後、再びPBSに懸濁した。5×108/MLに調整したアノン菌液を最終濃度0.4%のホルマリンで4℃にて一晩固定し、菌を不活化した。PBSで洗浄し、一部について生残菌の有無を確認したがあるかどうかを調べた。すなわち、不活化5×108/MLの細菌浮遊液0.1MLを7%馬血液加BHI寒天培地に接種し、嫌気性培養装置(混合ガス:N2 70%, CO2 15%, H2 15% 環境下)内で37℃72時間培養し、増殖する細菌のないことを確認した。不活化の確認後、軽度~中等度の歯周疾患を発症しているビーグル犬にそのワクチンの接種を行った。ワクチン接種による歯周病の炎症の改善は、抗体価の上昇について検証した。炎症の指標にはGIを用いた。GIは、Isogaiらの方法(Isogai H., et al., 1989, Jpn. J. Vet. Sci. 51, 1151-1162)に従った。すなわち、診査は上顎右の頬側から順番に、大臼歯(M2及びM1)、小臼歯(P4,P3,P2,P1)、犬歯(C)、前歯(I3,I2,I1)と続き、次いで上顎左頬側に移動し、左上顎前歯(I1,I2,I3)、犬歯(C)、小臼歯(P1,P2,P3,P4)、大臼歯(M1,M2)と続き、その後、下顎に移り、左側の大臼歯(M3,M2,M1)、小臼歯(P4,P3,P2,P1)、犬歯(C)、前歯(I3,I2,I1)を確認後、下顎左側に移動して前歯(I1,I2,I3)、犬歯(C)、小臼歯(P1,P2,P3,P4)、大臼歯(M1,M2,M3)を確認した。それぞれの歯の歯肉部分の炎症の程度を、炎症なし:0、軽度炎症:1、中等度炎症:2、重度炎症:3とスコアリングした。前記スコアの中間段階の炎症については、0.5、1.5、2.5とした。それぞれの歯の歯肉部分の炎症の程度の平均値を各イヌの平均GIとして表した。
(結果)
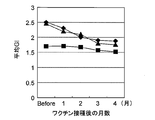
図7~9に結果を示す。図7からも明らかなように、1ヶ月後にはアノン株に特異的なANON- hexosaminidase、ANON-ASCP、及びANON-HagEに対する抗体上昇が認められた。また、アノン株に特異的なペプチドに対する抗体価だけでなく、ヒト由来W83株とほぼ同じアミノ酸配列を有する線毛の一部を反映しているFim331,Fim141,Fim353に対する抗体価としても上昇した。歯肉の炎症軽減は、ワクチン接種後から4か月後においても認められた(歯肉炎指数GIの変化)。HagEやFimペプチドを含む抗原は、菌体表層に存在する付着関連タンパク質として重要な病原因子となっている。実際、P. ジンジバリス 381株の線毛タンパク質に対して特異的なモノクローナル抗体が、該株の歯周組織や歯根部への付着を抑制することが知られている(Isogai, H., et al., 1988, Archs. oral Biol. 33、 479-485)。P. ジンジバリス 381株とアノン株は、いずれも強いプロテアーゼ活性を有するが、Porphyromonas菌属間においてジンジパインのうちrgpAはシークエンスバリエーションがほとんどないがrgpBには5つの異なったバリエーションが存在することが報告されている(Beikler T. et al., 2005, J.Peridontal Res. 40, 193-198)。また、rgp1やrgp2にはよく保存された領域が存在している(Mikolajczyk-Pawlinska J et al., 1998, Biol Chem 379, 205-211)。P. ジンジバリス381株と同一と考えられているP. ジンジバリス ATCC33277(PubMed)、W83(PubMed)及びアレイ解析から得られたアノン株のRgpBのシークエンスは、ほぼ一致(約99%)している(未発表)。アノン菌株や同様に人獣感染性を有するP.gingivalisに感染した後、抗体が産生されたとしてもIgGプロテアーゼ(Vincents B et al, FAseB J, 2011, 25: 3741-3750)によって抗体が分解される場合には病原体を駆逐することができずに炎症が持続することになる。さらに、P.ジンジバリスは、歯肉ポケットに存在するため、
抗原刺激が不十分となる可能性が高い。したがって、皮下ワクチン投与によって免疫応答を強化すれば炎症の軽減が起こると考えられる。本実施例では、その効果を実証している。イヌの永久歯列は上顎前歯I1-3、犬歯C、小臼歯P1-4、大臼歯M1-2、下顎では前歯I1-3、犬歯C、小臼歯P1-4、大臼歯M1-3の合計42歯からなる。それぞれの歯に該当する部分の歯肉の炎症レベルを4段階で診査した。全合計GI値を42で割って平均GIとした。ワクチン接種後平均GIは3匹のビーグル犬で低下した(図8)。特に歯石付着の少ないI1-3及びCまでの平均GIでは顕著であった(図9)。歯肉溝には血清中の抗体とほぼ同レベルの抗体が検出されることがすでに報告されている。効果的に抗体を誘導することで、炎症の軽減をもたらすことができたと考えた。歯石付着部分で炎症の軽減が少ないことは歯石そのものの炎症誘導能や歯垢が付着しやすくなるなどの影響によるものと考えられる。また、アノン株はリシークエンスで固有の機能不明遺伝子領域を多数含んでおり、これらのうちいくつかは感染防御抗原としてより有力な候補となり得る。
図7~9に結果を示す。図7からも明らかなように、1ヶ月後にはアノン株に特異的なANON- hexosaminidase、ANON-ASCP、及びANON-HagEに対する抗体上昇が認められた。また、アノン株に特異的なペプチドに対する抗体価だけでなく、ヒト由来W83株とほぼ同じアミノ酸配列を有する線毛の一部を反映しているFim331,Fim141,Fim353に対する抗体価としても上昇した。歯肉の炎症軽減は、ワクチン接種後から4か月後においても認められた(歯肉炎指数GIの変化)。HagEやFimペプチドを含む抗原は、菌体表層に存在する付着関連タンパク質として重要な病原因子となっている。実際、P. ジンジバリス 381株の線毛タンパク質に対して特異的なモノクローナル抗体が、該株の歯周組織や歯根部への付着を抑制することが知られている(Isogai, H., et al., 1988, Archs. oral Biol. 33、 479-485)。P. ジンジバリス 381株とアノン株は、いずれも強いプロテアーゼ活性を有するが、Porphyromonas菌属間においてジンジパインのうちrgpAはシークエンスバリエーションがほとんどないがrgpBには5つの異なったバリエーションが存在することが報告されている(Beikler T. et al., 2005, J.Peridontal Res. 40, 193-198)。また、rgp1やrgp2にはよく保存された領域が存在している(Mikolajczyk-Pawlinska J et al., 1998, Biol Chem 379, 205-211)。P. ジンジバリス381株と同一と考えられているP. ジンジバリス ATCC33277(PubMed)、W83(PubMed)及びアレイ解析から得られたアノン株のRgpBのシークエンスは、ほぼ一致(約99%)している(未発表)。アノン菌株や同様に人獣感染性を有するP.gingivalisに感染した後、抗体が産生されたとしてもIgGプロテアーゼ(Vincents B et al, FAseB J, 2011, 25: 3741-3750)によって抗体が分解される場合には病原体を駆逐することができずに炎症が持続することになる。さらに、P.ジンジバリスは、歯肉ポケットに存在するため、
抗原刺激が不十分となる可能性が高い。したがって、皮下ワクチン投与によって免疫応答を強化すれば炎症の軽減が起こると考えられる。本実施例では、その効果を実証している。イヌの永久歯列は上顎前歯I1-3、犬歯C、小臼歯P1-4、大臼歯M1-2、下顎では前歯I1-3、犬歯C、小臼歯P1-4、大臼歯M1-3の合計42歯からなる。それぞれの歯に該当する部分の歯肉の炎症レベルを4段階で診査した。全合計GI値を42で割って平均GIとした。ワクチン接種後平均GIは3匹のビーグル犬で低下した(図8)。特に歯石付着の少ないI1-3及びCまでの平均GIでは顕著であった(図9)。歯肉溝には血清中の抗体とほぼ同レベルの抗体が検出されることがすでに報告されている。効果的に抗体を誘導することで、炎症の軽減をもたらすことができたと考えた。歯石付着部分で炎症の軽減が少ないことは歯石そのものの炎症誘導能や歯垢が付着しやすくなるなどの影響によるものと考えられる。また、アノン株はリシークエンスで固有の機能不明遺伝子領域を多数含んでおり、これらのうちいくつかは感染防御抗原としてより有力な候補となり得る。
本明細書で引用した全ての刊行物、特許及び特許出願をそのまま参考として本明細書にとり入れるものとする。
Claims (7)
- 人獣共通感染性歯周病菌ポルフィロモナス ジンジバリス アノン(Porphyromonas gingivalis ANON)を不活化又は弱毒化した人獣共通感染性歯周病治療用ワクチン。
- 配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチドを用いて、被検体より採取した体液から前記ペプチド中に存在するエピトープを認識する抗体及び/又はその抗原結合性断片を検出する抗体検出工程、及び
抗体検出工程の結果に基づいて、被検体のアノン株に対する感染の有無を判定する判定工程を含む、人獣共通感染性歯周病菌P. ジンジバリス アノンの感染判定方法。 - 配列番号1~7のいずれか一で示されるアミノ酸配列を含む一以上のポリペプチドを、前記アミノ酸配列からなるペプチド中に存在するエピトープを認識する抗体及び/又はその抗原結合性断片を用いて被検体より採取したプラークから検出するポリペプチド検出工程を含む、人獣共通感染性歯周病菌P. ジンジバリス アノンの検出方法。
- 配列番号1~7のいずれか一で示されるアミノ酸配列を含むペプチドからなる、P. ジンジバリス アノン検出用マーカー。
- 配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド中に存在するエピトープを認識する人獣共通感染性歯周病菌P. ジンジバリス アノン検出用抗体又はその抗原結合性断片。
- 配列番号1~7のいずれか一で示されるアミノ酸配列からなるペプチド中に存在するエピトープを認識する一以上の抗体及び/又はその抗原結合性断片を有効成分として含む、人獣共通感染性歯周病菌P. ジンジバリス アノンの感染又は炎症抑制剤。
- 請求項4に記載の一以上のマーカー、請求項5に記載の一以上の抗体及び/又は抗原結合性断片を含む、人獣共通感染性歯周病菌P. ジンジバリス アノン検出用キット。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011135669 | 2011-06-17 | ||
| JP2011-135669 | 2011-06-17 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012173244A1 true WO2012173244A1 (ja) | 2012-12-20 |
Family
ID=47357221
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2012/065408 WO2012173244A1 (ja) | 2011-06-17 | 2012-06-15 | 人獣共通感染性歯周病菌検出用マーカー |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2012173244A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018154574A (ja) * | 2017-03-16 | 2018-10-04 | 合同会社チューモス | 点眼ワクチン及び免疫誘導方法 |
| JP2021521421A (ja) * | 2018-04-12 | 2021-08-26 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 歯肉炎の診断方法、使用、キット |
| JP2021521423A (ja) * | 2018-04-12 | 2021-08-26 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 歯肉炎の診断方法、使用、キット |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995010612A1 (fr) * | 1993-10-08 | 1995-04-20 | Lion Corporation | PROTEINE FIMBRILLINE DE $i(PORPHYROMONAS GINGIVALIS) |
| JP2000511041A (ja) * | 1994-12-09 | 2000-08-29 | ユニバーシティ オブ フロリダ | クローン化したポルフィロモナス・ジンジバリス(Porphiromonas gingivalis)の遺伝子、および歯周病の検出のためのプローブ |
| JP2007529195A (ja) * | 2003-08-15 | 2007-10-25 | ユニバーシティ オブ フロリダ リサーチ ファウンデーション,インク. | 歯周病の診断,治療,およびモニタリングのためのPorphyromonasgingivalis毒性ポリヌクレオチドの同定 |
| JP2009544279A (ja) * | 2006-06-27 | 2009-12-17 | オーラル ヘルス オーストラリア ピーティーワイ リミテッド | 歯周病の予防に有用なポルフィロモナス・ジンジバリスポリペプチド |
-
2012
- 2012-06-15 WO PCT/JP2012/065408 patent/WO2012173244A1/ja active Application Filing
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995010612A1 (fr) * | 1993-10-08 | 1995-04-20 | Lion Corporation | PROTEINE FIMBRILLINE DE $i(PORPHYROMONAS GINGIVALIS) |
| JP2000511041A (ja) * | 1994-12-09 | 2000-08-29 | ユニバーシティ オブ フロリダ | クローン化したポルフィロモナス・ジンジバリス(Porphiromonas gingivalis)の遺伝子、および歯周病の検出のためのプローブ |
| JP2007529195A (ja) * | 2003-08-15 | 2007-10-25 | ユニバーシティ オブ フロリダ リサーチ ファウンデーション,インク. | 歯周病の診断,治療,およびモニタリングのためのPorphyromonasgingivalis毒性ポリヌクレオチドの同定 |
| JP2009544279A (ja) * | 2006-06-27 | 2009-12-17 | オーラル ヘルス オーストラリア ピーティーワイ リミテッド | 歯周病の予防に有用なポルフィロモナス・ジンジバリスポリペプチド |
Non-Patent Citations (7)
| Title |
|---|
| DASHPER,S.G. ET AL.: "A novel Porphyromonas gingivalis FeoB plays a role in manganese accumulation", J BIOL CHEM, vol. 280, no. 30, 2005, pages 28095 - 102 * |
| DESHPANDE,R.G. ET AL.: "Purification and characterization of hemolysin from Porphyromonas gingivalis A7436", FEMS MICROBIOL LETT, vol. 176, no. 2, 1999, pages 387 - 94 * |
| FUJIWARA,T. ET AL.: "Molecular cloning and sequencing of the fimbrilin gene of Porphyromonas gingivalis strains and characterization of recombinant proteins", BIOCHEM BIOPHYS RES COMMUN, vol. 197, no. 1, 1993, pages 241 - 7 * |
| ISOGAI, E ET AL.: "Effect of Japanese Green Tea Extract on Canine Periodontal Diseases", MICROBIAL ECOLOGY IN HEALTH AND DISEASE, vol. 8, no. 2, 1995, pages 57 - 61 * |
| NELSON,K.E. ET AL.: "Complete genome sequence of the oral pathogenic Bacterium porphyromonas gingivalis strain W83", J BACTERIOL, vol. 185, no. 18, 2003, pages 5591 - 5601 * |
| NOBUSHIRO HAMADA ET AL.: "Kokushoku Shikiso Sansei Gram Insei Kankin Porphyromonas gulae no Bunpu to Watage no Seijo", J ORAL BIOSCI, vol. 46, no. 5, 2004, pages 483 * |
| YASUATSU TAKEDA: "Cloning and Sequencing of Antigenically Different Fimbrial Protein Gene from Porphyromonas ginigivalis", KANAGAWA SHIGAKU, vol. 29, no. 4, 1995, pages 355 - 370 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018154574A (ja) * | 2017-03-16 | 2018-10-04 | 合同会社チューモス | 点眼ワクチン及び免疫誘導方法 |
| JP2021521421A (ja) * | 2018-04-12 | 2021-08-26 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 歯肉炎の診断方法、使用、キット |
| JP2021521423A (ja) * | 2018-04-12 | 2021-08-26 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 歯肉炎の診断方法、使用、キット |
| JP7379368B2 (ja) | 2018-04-12 | 2023-11-14 | コーニンクレッカ フィリップス エヌ ヴェ | 歯肉炎の診断方法、使用、キット |
| JP7431747B2 (ja) | 2018-04-12 | 2024-02-15 | コーニンクレッカ フィリップス エヌ ヴェ | 歯肉炎の診断方法、使用、キット |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Porter et al. | Q Fever: current state of knowledge and perspectives of research of a neglected zoonosis | |
| JP5597128B2 (ja) | H5トリインフルエンザの診断および監視に有用なh5亜型特異的結合タンパク質 | |
| BR112014006376B1 (pt) | Anticorpo isolado que se liga a um ou mais epítopos tau, ácido nucleico, vetor, composição farmacêutica, artigo de fabricação, dispositivo médico, método in vitro para diagnosticar ou triar um indivíduo quanto à presença de doença de alzheimer ou de uma tauopatia relacionada e usos do referido anticorpo | |
| KR20220158053A (ko) | 중증 급성 호흡기 증후군 코로나바이러스 2(SARS-CoV-2)에 대한 인간 단클론 항체 | |
| JP2019142921A (ja) | 黄色ブドウ球菌のLukGH(LukAB)毒素を中和する、非常に強力な抗体の生成 | |
| WO2012173244A1 (ja) | 人獣共通感染性歯周病菌検出用マーカー | |
| JP2023099009A (ja) | 新規な重症熱性血小板減少症候群ウイルス | |
| JP7431450B2 (ja) | ヘリコバクター・スイス感染の診断法 | |
| US20230122364A1 (en) | HUMAN MONOCLONAL ANTIBODIES TO SEVERE ACUTE RESPIRATORY SYNDROME CORONAVIRUS 2 (SARS-CoV-2) | |
| WO2022036337A1 (en) | Compositions and methods for recombinant polypeptide mimicking sars-cov-2 nucleocapsid protein (np) | |
| KR101647159B1 (ko) | 조성물, 방법 및 키트 | |
| US20200115439A1 (en) | HUMAN IgE ANTIBODIES BINDING TO ASPERGILLUS ALLERGENS | |
| Tzang et al. | Induction of antiphospholipid antibodies and antiphospholipid syndrome-like autoimmunity in naive mice with antibody against human parvovirus B19 VP1 unique region protein | |
| WO2021218947A1 (zh) | 一种抗新型冠状病毒的单克隆抗体及其应用 | |
| EP1791967B1 (en) | Methods and compositions relating to mannuronic acid specific binding peptides | |
| KR102097989B1 (ko) | 신규한 중증열성혈소판감소증후군 바이러스 | |
| US20220280618A1 (en) | Antibodies to candida and uses thereof | |
| US20220221455A1 (en) | Antigen binding proteins and assays | |
| Lee et al. | Flagellin-adjuvanted trivalent mucosal vaccine targeting key periodontopathic bacteria | |
| Bowe et al. | Immunogenicity and efficacy of a subcutaneously administered, adjuvanted vaccine containing modified S1 spike protein of SARS-CoV-2 variant C. 1.2 | |
| Nara et al. | An octavalent dendrimer of multiple antigenic peptide with a property of pan-coronavirus IgM induction improved clinical signs of feline infectious peritonitis in cats | |
| WO2021252722A1 (en) | Sars-cov-2 polypeptides, ant-sars-cov-2 antibodies and uses thereof | |
| WO2023288204A1 (en) | Diagnostics for porphyromonas gingivalis | |
| WO2023079442A2 (en) | Antigen-binding molecules that bind to porphyromonas gingivalis | |
| WO2023235666A2 (en) | Human antibodies to bordetella pertussis and uses therefor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 12800921 Country of ref document: EP Kind code of ref document: A1 |
|
| DPE1 | Request for preliminary examination filed after expiration of 19th month from priority date (pct application filed from 20040101) | ||
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 12800921 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: JP |