WO2012140856A1 - 酸化還元反応を利用した熱電変換方法および熱電変換素子 - Google Patents
酸化還元反応を利用した熱電変換方法および熱電変換素子 Download PDFInfo
- Publication number
- WO2012140856A1 WO2012140856A1 PCT/JP2012/002391 JP2012002391W WO2012140856A1 WO 2012140856 A1 WO2012140856 A1 WO 2012140856A1 JP 2012002391 W JP2012002391 W JP 2012002391W WO 2012140856 A1 WO2012140856 A1 WO 2012140856A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- electrode
- thermoelectric conversion
- oxidation
- reduction reaction
- electrolyte
- Prior art date
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M14/00—Electrochemical current or voltage generators not provided for in groups H01M6/00 - H01M12/00; Manufacture thereof
Abstract
アルカリ金属イオンを含む電解質(2)に対して、活物質を含む第1の電極(6)と、前記第1の電極(6)と同一の活物質を含む第2の電極(7)と、を接触させて、前記第1の電極(6)および第2の電極(7)のいずれか一方を加熱または冷却することで、前記第1の電極(6)と前記第2の電極(7)との間に温度差を発生させて、各電極(6,7)における酸化還元反応による熱起電力を発生させることを特徴とする酸化還元反応を利用した熱電変換方法により、小型で低コストで高効率の熱電変換技術を提供する。
Description
本発明は、熱エネルギーを電気エネルギーに変換する熱電変換方法および熱電変換素子に関し、特に、酸化還元反応を利用した熱電変換方法および熱電変換素子に関する。
一般に、熱電変換技術は、熱エネルギーと電気的なエネルギーとを変換する技術であり、様々な日常生活や生産活動で発生する廃熱を電力に変換したり、電圧を印加して温度差を発生させたりすることが可能である。
このような熱電変換技術に関し、以下の特許文献1~3記載の技術が従来公知である。
特許文献1(特開平5-144483号公報)には、フェロシアン化カリウム(K4FeII(CN)6)およびフェリシアン化カリウム(K3FeIII(CN)6)の水溶液中に黒鉛シートを入れて煮沸することにより、フェロシアン化カリウムおよびフェリシアン化カリウムが層間に挿入された黒鉛層間化合物を作成し、一対の黒鉛層間化合物を電極(E1,E2)として、フェロシアン化カリウムおよびフェリシアン化カリウムの水溶液に浸して、一方の電極(E1)を高温熱源(2)に接触させ、他方の電極(E2)を低温浴(3)に接触させることで、電極間に熱起電力を発生させる電気化学的温度差電池が記載されている。
このような熱電変換技術に関し、以下の特許文献1~3記載の技術が従来公知である。
特許文献1(特開平5-144483号公報)には、フェロシアン化カリウム(K4FeII(CN)6)およびフェリシアン化カリウム(K3FeIII(CN)6)の水溶液中に黒鉛シートを入れて煮沸することにより、フェロシアン化カリウムおよびフェリシアン化カリウムが層間に挿入された黒鉛層間化合物を作成し、一対の黒鉛層間化合物を電極(E1,E2)として、フェロシアン化カリウムおよびフェリシアン化カリウムの水溶液に浸して、一方の電極(E1)を高温熱源(2)に接触させ、他方の電極(E2)を低温浴(3)に接触させることで、電極間に熱起電力を発生させる電気化学的温度差電池が記載されている。
特許文献2(特開平5-166554号公報)には、一対の白金(Pt)電極をフェロシアン化カリウムおよびフェリシアン化カリウムの水溶液に浸して、白金電極の温度が10℃および70℃となるように温度制御をすることで熱起電力を発生させる技術が記載されている。また、特許文献2には、一対の白金電極の間をガラスフィルターまたはイオン交換樹脂の隔膜で仕切り、温度差が消失した後に、濃度差に基づいて起電力を発生させる濃度差電池として機能させる技術と組み合わせることも記載されている。
特許文献3(特開平6-140082号公報)には、同一材料からなる一対の電極(1,3)をフェロシアンイオンとフェリシアンイオンの容積中に浸した状態で温度差を発生させることで熱起電力を発生させる温度差電池が記載されている。また、特許文献3には、一対の電極(1,3)をイオン交換膜(6)で仕切ると共に、イオン交換膜(6)を挟んで一対の白金電極(7,8)を配置して濃度差による起電力を発生可能な技術と組み合わせることも記載されている。
(従来技術の問題点)
引用文献1~3記載の技術では、電解質であるフェロシアンイオンやフェリシアンイオンの移動により起電力を発生させているが、分子量が大きいため、比較的移動速度が低速であり、熱起電力の発生速度や応答性が低い問題がある。
また、電極として黒鉛シートや白金電極を使用する場合、薄膜化、極薄化に限界があり、小型化に限界がある問題があると共に、電極の表面近傍でしか反応が発生しにくく、電極全体が均一に使用されず、効率が悪い問題がある。
さらに、電極として白金電極を使用する場合、貴金属である白金(Pt)が高価であり、コストが高くなる問題もある。
引用文献1~3記載の技術では、電解質であるフェロシアンイオンやフェリシアンイオンの移動により起電力を発生させているが、分子量が大きいため、比較的移動速度が低速であり、熱起電力の発生速度や応答性が低い問題がある。
また、電極として黒鉛シートや白金電極を使用する場合、薄膜化、極薄化に限界があり、小型化に限界がある問題があると共に、電極の表面近傍でしか反応が発生しにくく、電極全体が均一に使用されず、効率が悪い問題がある。
さらに、電極として白金電極を使用する場合、貴金属である白金(Pt)が高価であり、コストが高くなる問題もある。
特に、引用文献1~3記載の技術では、電池として機能する際に、電子の受け渡しを行う活物質であるフェロシアンイオンやフェリシアンイオンが、電解質(溶媒)中に溶けた状態となっている。よって、溶液に溶けない活物質を使用することが困難である問題がある。また、溶ける量に限界があるため、活物質の密度を高くすることに限界があり、効率を向上させにくいと共に、所定量の活物質を確保するにはある程度の量の溶液が必要となり、電池全体の小型化が困難である問題もある。
本発明は、小型で低コストで高効率の熱電変換技術を提供することを技術的課題とする。
前記技術的課題を解決するために、請求項1に記載の発明の酸化還元反応を利用した熱電変換方法は、
アルカリ金属イオンを含む電解質に対して、電子の受け渡しを行う活物質を含む第1の電極と、前記第1の電極と同一の活物質を含む第2の電極と、を接触させて、前記第1の電極および第2の電極の少なくとも一方を加熱または冷却することで、前記第1の電極と前記第2の電極との間に温度差を発生させて、各電極における酸化還元反応および電解質中のアルカリ金属イオンの移動による熱起電力を発生させることを特徴とする。
アルカリ金属イオンを含む電解質に対して、電子の受け渡しを行う活物質を含む第1の電極と、前記第1の電極と同一の活物質を含む第2の電極と、を接触させて、前記第1の電極および第2の電極の少なくとも一方を加熱または冷却することで、前記第1の電極と前記第2の電極との間に温度差を発生させて、各電極における酸化還元反応および電解質中のアルカリ金属イオンの移動による熱起電力を発生させることを特徴とする。
請求項2に記載の発明は、請求項1に記載の酸化還元反応を利用した熱電変換方法において、
導電性の基板の表面に、前記活物質としてのシアノ架橋金属錯体が、成膜されて作成された前記第1の電極及び第2の電極を使用する
ことを特徴とする。
導電性の基板の表面に、前記活物質としてのシアノ架橋金属錯体が、成膜されて作成された前記第1の電極及び第2の電極を使用する
ことを特徴とする。
請求項3に記載の発明は、請求項2に記載の酸化還元反応を利用した熱電変換方法において、
前記第1の電極および第2の電極は、インジウムスズ酸化物の基板表面にシアノ架橋金属錯体が成膜されて作成された
ことを特徴とする。
前記第1の電極および第2の電極は、インジウムスズ酸化物の基板表面にシアノ架橋金属錯体が成膜されて作成された
ことを特徴とする。
請求項4に記載の発明は、請求項1に記載の酸化還元反応を利用した熱電変換方法において、
前記活物質としてのコバルト酸リチウムにより構成された前記第1の電極及び第2の電極を使用する
ことを特徴とする。
前記活物質としてのコバルト酸リチウムにより構成された前記第1の電極及び第2の電極を使用する
ことを特徴とする。
請求項5に記載の発明は、請求項4に記載の酸化還元反応を利用した熱電変換方法において、
リチウム欠損を引き起こした前記第1の電極及び第2の電極を使用する
ことを特徴とする。
リチウム欠損を引き起こした前記第1の電極及び第2の電極を使用する
ことを特徴とする。
請求項6に記載の発明は、請求項1に記載の酸化還元反応を利用した熱電変換方法において、
前記活物質としての炭素により構成された前記第1の電極及び第2の電極を使用する
ことを特徴とする。
前記活物質としての炭素により構成された前記第1の電極及び第2の電極を使用する
ことを特徴とする。
請求項7に記載の発明は、請求項6に記載の酸化還元反応を利用した熱電変換方法において、
リチウム導入した前記第1の電極及び第2の電極を使用する
ことを特徴とする。
リチウム導入した前記第1の電極及び第2の電極を使用する
ことを特徴とする。
請求項8に記載の発明は、請求項1に記載の酸化還元反応を利用した熱電変換方法において、
前記第1の電極および第2の電極のいずれか一方を、太陽熱により加熱する
ことを特徴とする。
前記第1の電極および第2の電極のいずれか一方を、太陽熱により加熱する
ことを特徴とする。
請求項9に記載の発明は、請求項1に記載の酸化還元反応を利用した熱電変換方法において、
前記第1の電極、第2の電極および前記電解質とを有する層状の構成を、一方の層状の構成の第1の電極と、他方の層状の構成の第2の電極とが隣り合うように積層し、積層された最も外側の第1の電極と、最も外側の第2の電極との間に温度差を発生させることを特徴とする。
前記第1の電極、第2の電極および前記電解質とを有する層状の構成を、一方の層状の構成の第1の電極と、他方の層状の構成の第2の電極とが隣り合うように積層し、積層された最も外側の第1の電極と、最も外側の第2の電極との間に温度差を発生させることを特徴とする。
請求項10に記載の発明は、請求項1に記載の酸化還元反応を利用した熱電変換方法において、
前記第1の電極、第2の電極および前記電解質とを有する構成を、複数有し、一方の第1の電極を、他方の第2の電極に直列に接続したことを特徴とする。
前記第1の電極、第2の電極および前記電解質とを有する構成を、複数有し、一方の第1の電極を、他方の第2の電極に直列に接続したことを特徴とする。
前記技術的課題を解決するために、請求項11に記載の発明の酸化還元反応を利用した熱電変換素子は、
アルカリ金属イオンを含む電解質と、
電子の受け渡しを行う活物質を含む第1の電極であって、前記電解質に接触する前記第1の電極と、
前記第1の電極と同一の活物質を含み且つ前記電解質に接触する第2の電極と、
前記第1の電極および前記第2の電極の少なくとも一方に設けられ、加熱または冷却される被温冷部と、
を備え、
前記第1の電極と前記第2の電極との間に発生した温度差に応じて、各電極における酸化還元反応および電解質中のアルカリ金属イオンの移動により熱起電力を発生させる
ことを特徴とする。
アルカリ金属イオンを含む電解質と、
電子の受け渡しを行う活物質を含む第1の電極であって、前記電解質に接触する前記第1の電極と、
前記第1の電極と同一の活物質を含み且つ前記電解質に接触する第2の電極と、
前記第1の電極および前記第2の電極の少なくとも一方に設けられ、加熱または冷却される被温冷部と、
を備え、
前記第1の電極と前記第2の電極との間に発生した温度差に応じて、各電極における酸化還元反応および電解質中のアルカリ金属イオンの移動により熱起電力を発生させる
ことを特徴とする。
請求項12に記載の発明は、請求項11に記載の酸化還元反応を利用した熱電変換素子において、
導電性の基板の表面に、前記活物質としてのシアノ架橋金属錯体が、成膜されて作成された前記第1の電極および第2の電極、
を備えたことを特徴とする。
導電性の基板の表面に、前記活物質としてのシアノ架橋金属錯体が、成膜されて作成された前記第1の電極および第2の電極、
を備えたことを特徴とする。
請求項13に記載の発明は、請求項12に記載の酸化還元反応を利用した熱電変換素子において、
インジウムスズ酸化物により構成された前記基板を有する前記第1の電極および第2の電極、
を備えたことを特徴とする。
インジウムスズ酸化物により構成された前記基板を有する前記第1の電極および第2の電極、
を備えたことを特徴とする。
請求項14に記載の発明は、請求項11に記載の酸化還元反応を利用した熱電変換素子において、
前記活物質としてのコバルト酸リチウムにより構成された前記第1の電極及び第2の電極、
を備えたことを特徴とする。
前記活物質としてのコバルト酸リチウムにより構成された前記第1の電極及び第2の電極、
を備えたことを特徴とする。
請求項15に記載の発明は、請求項14に記載の酸化還元反応を利用した熱電変換素子において、
リチウム欠損を引き起こした前記第1の電極及び第2の電極、
を備えたことを特徴とする。
リチウム欠損を引き起こした前記第1の電極及び第2の電極、
を備えたことを特徴とする。
請求項16に記載の発明は、請求項11に記載の酸化還元反応を利用した熱電変換素子において、
前記活物質としての炭素により構成された前記第1の電極及び第2の電極、
を備えたことを特徴とする。
前記活物質としての炭素により構成された前記第1の電極及び第2の電極、
を備えたことを特徴とする。
請求項17に記載の発明は、請求項16に記載の酸化還元反応を利用した熱電変換素子において、
リチウム導入した前記第1の電極及び第2の電極、
を備えたことを特徴とする。
リチウム導入した前記第1の電極及び第2の電極、
を備えたことを特徴とする。
請求項18に記載の発明は、請求項11に記載の酸化還元反応を利用した熱電変換素子において、
太陽熱により加熱される前記被温冷部、
を備えたことを特徴とする。
太陽熱により加熱される前記被温冷部、
を備えたことを特徴とする。
請求項19に記載の発明は、請求項11に記載の酸化還元反応を利用した熱電変換素子において、
前記第1の電極、第2の電極および前記電解質とを有する層状の構成を、一方の層状の構成の第1の電極と、他方の層状の構成の第2の電極とが隣り合うように積層され、
前記被温冷部が、積層された最も外側の第1の電極および最も外側の第2の電極の少なくとも一方に設けられた
ことを特徴とする。
前記第1の電極、第2の電極および前記電解質とを有する層状の構成を、一方の層状の構成の第1の電極と、他方の層状の構成の第2の電極とが隣り合うように積層され、
前記被温冷部が、積層された最も外側の第1の電極および最も外側の第2の電極の少なくとも一方に設けられた
ことを特徴とする。
請求項20に記載の発明は、請求項11に記載の酸化還元反応を利用した熱電変換素子において、
前記第1の電極、第2の電極および前記電解質とを有する構成を、複数有し、
一方の第1の電極が、他方の第2の電極に直列に接続された
ことを特徴とする。
前記第1の電極、第2の電極および前記電解質とを有する構成を、複数有し、
一方の第1の電極が、他方の第2の電極に直列に接続された
ことを特徴とする。
請求項1、11に記載の発明によれば、同一の活物質を含む一対の電極をアルカリ金属イオンを含む電解質に接触させているため、小型で低コストで高効率の熱電変換技術を提供することができる。
請求項2、12に記載の発明によれば、活物質としてシアノ架橋金属錯体を使用されているため、低コスト化と、薄膜化を容易に行うことができる。
請求項3,13に記載の発明によれば、ITO基板を使用しない場合に比べて、低コスト化することができる。
請求項2、12に記載の発明によれば、活物質としてシアノ架橋金属錯体を使用されているため、低コスト化と、薄膜化を容易に行うことができる。
請求項3,13に記載の発明によれば、ITO基板を使用しない場合に比べて、低コスト化することができる。
請求項4,14に記載の発明によれば、コバルト酸リチウムにより構成された電極が使用されているため、既存のリチウムイオン電池を生産する施設や材料を利用することができ、低コスト化が可能である。
請求項5,15に記載の発明によれば、リチウム欠損をしない場合に比べて、効率を高めることができる。
請求項6,16に記載の発明によれば、炭素により構成された電極が使用されているため、既存の電池を生産する施設や材料を利用することができ、低コスト化が可能である。
請求項5,15に記載の発明によれば、リチウム欠損をしない場合に比べて、効率を高めることができる。
請求項6,16に記載の発明によれば、炭素により構成された電極が使用されているため、既存の電池を生産する施設や材料を利用することができ、低コスト化が可能である。
請求項7,17に記載の発明によれば、リチウム導入をしない場合に比べて、効率を高めることができる。
請求項8,18に記載の発明によれば、太陽熱を利用しているため、化石燃料や原子力等を使用する場合に比べて、クリーンな構成とすることができる。
請求項9,19に記載の発明によれば、層状の構成を積層しない場合に比べて、熱抵抗を大きくすることができ、熱電変換効率を向上させることができる。
請求項10,20に記載の発明によれば、直列に接続しない場合に比べて、全体の電圧を高めることができる。
請求項8,18に記載の発明によれば、太陽熱を利用しているため、化石燃料や原子力等を使用する場合に比べて、クリーンな構成とすることができる。
請求項9,19に記載の発明によれば、層状の構成を積層しない場合に比べて、熱抵抗を大きくすることができ、熱電変換効率を向上させることができる。
請求項10,20に記載の発明によれば、直列に接続しない場合に比べて、全体の電圧を高めることができる。
次に図面を参照しながら、本発明の実施の形態の具体例である実施例を説明するが、本発明は以下の実施例に限定されるものではない。
なお、以下の図面を使用した説明において、理解の容易のために説明に必要な部材以外の図示は適宜省略されている。
なお、以下の図面を使用した説明において、理解の容易のために説明に必要な部材以外の図示は適宜省略されている。
図1は本発明の実施例1の熱電変換素子の説明図である。
図1において、本発明の実施例1の熱電変換素子の一例としての電池1は、液体状の電解質2が収容される電解質槽3を有する。実施例1の電解質槽3は、被温冷部の一例としての第1槽3aと、第2槽3bと、第1槽3aおよび第2槽3bを接続する接続部3cと、を有する。実施例1の電解質槽3には、アルカリ金属イオンの一例としてのナトリウムイオン(Na+)を含む塩化ナトリウム(NaCl)水溶液が電解質2として収容されている。
図1において、本発明の実施例1の熱電変換素子の一例としての電池1は、液体状の電解質2が収容される電解質槽3を有する。実施例1の電解質槽3は、被温冷部の一例としての第1槽3aと、第2槽3bと、第1槽3aおよび第2槽3bを接続する接続部3cと、を有する。実施例1の電解質槽3には、アルカリ金属イオンの一例としてのナトリウムイオン(Na+)を含む塩化ナトリウム(NaCl)水溶液が電解質2として収容されている。
前記電解質槽3には、第1の電極の一例として、第1槽3aに浸漬されて電解質2と接触する負極6と、第2の電極の一例として、第2槽3bに浸漬されて電解質2と接触する正極7とが配置されている。実施例1の電極6,7は、同一の構成となっており、基板6a,7aの表面に、シアノ架橋金属錯体により構成された表面層6b,7bが支持されている。実施例1では、前記基板6a、7aは、導電性のITO(Indium Tin Oxide、インジウム錫酸化物)電極板を使用したが、これに限定されず、例えば、シリコン基板の表面に導電性の金属(金や銅等)が被覆された構成とすることも可能である。
また、表面層6b,7bは、シアノ架橋金属錯体の一例としてのNa0.21Ni[Fe(CN)6]0.68・5.1H2Oが使用されている。前記シアノ架橋金属錯体は、電解析出法によりITO基板6a,7aの表面に成膜されているが、これに限定されず、スピンコート法等、従来公知の種々の作製方法を採用可能である。なお、以下、Na0.21Ni[Fe(CN)6]0.68・5.1H2Oを、Naの「N」、Niの「N」、Feの「F」、0.68の「68」をとって、「NNF68」と表記し、シアノ架橋金属錯体に関しては、同様の表記法で表記をする。
実施例1の第1槽3aには、加熱体の一例としての熱源8が設置されており、第1槽3aに収容された電解質2や正極6が加熱可能に構成されている。
実施例1の第1槽3aには、加熱体の一例としての熱源8が設置されており、第1槽3aに収容された電解質2や正極6が加熱可能に構成されている。
(実施例1の作用)
前記構成を備えた実施例1の電池1では、熱源8により加熱されていない状態では、第1槽3a内の電解質2と第2槽3b内の電解質2との間で温度差が発生せず、電極6,7で温度差が発生しない。このとき、各電極6,7において、表面層6b,7bでは、下記の式(1)の酸化反応と、式(2)の還元反応とが、反応速度が同一(平衡)となり、電流が流れない。
[Fe2+(CN)6]4- → [Fe3+(CN)6]3- + e- …式(1)
[Fe3+(CN)6]3- + e- → [Fe2+(CN)6]4- …式(2)
そして、熱源8により加熱が開始されると、第1槽3a内の電解質2や負極6が加熱され、第2槽3b内の電解質2や正極7との間に温度差が発生する。温度が上昇すると、NNF68の薄膜では酸化反応の速度が還元反応の速度に比べて相対的に速くなる。したがって、第1槽3a側の電極が負極6となり、第2槽3b側の電極が正極7となる。この電極6,7での反応に伴って、電解質2内でアルカリ金属イオンであるナトリウムイオンNa+が移動する。
したがって、電極間6,7に温度差が発生すると、シアノ架橋金属錯体が活物質となって電子の受け渡しが行われ、電極6,7間には電流が流れる。すなわち、実施例1の電池1では、電解質2と電極6,7との酸化還元反応に起因して熱起電力が発生する。
前記構成を備えた実施例1の電池1では、熱源8により加熱されていない状態では、第1槽3a内の電解質2と第2槽3b内の電解質2との間で温度差が発生せず、電極6,7で温度差が発生しない。このとき、各電極6,7において、表面層6b,7bでは、下記の式(1)の酸化反応と、式(2)の還元反応とが、反応速度が同一(平衡)となり、電流が流れない。
[Fe2+(CN)6]4- → [Fe3+(CN)6]3- + e- …式(1)
[Fe3+(CN)6]3- + e- → [Fe2+(CN)6]4- …式(2)
そして、熱源8により加熱が開始されると、第1槽3a内の電解質2や負極6が加熱され、第2槽3b内の電解質2や正極7との間に温度差が発生する。温度が上昇すると、NNF68の薄膜では酸化反応の速度が還元反応の速度に比べて相対的に速くなる。したがって、第1槽3a側の電極が負極6となり、第2槽3b側の電極が正極7となる。この電極6,7での反応に伴って、電解質2内でアルカリ金属イオンであるナトリウムイオンNa+が移動する。
したがって、電極間6,7に温度差が発生すると、シアノ架橋金属錯体が活物質となって電子の受け渡しが行われ、電極6,7間には電流が流れる。すなわち、実施例1の電池1では、電解質2と電極6,7との酸化還元反応に起因して熱起電力が発生する。
したがって、実施例1の電池1では、引用文献1~3記載の技術のように電解質として分子量の大きなフェロシアンイオン等を使用する場合に比べて、原子量の小さいナトリウムイオンが使用されており、電解質2において高速でのイオンの移動が期待できる。よって、熱起電力の発生速度や応答性が向上することが期待できる。
また、実施例1の電極6,7の表面層6b,7bでは、低コスト且つ電解析出等で厚さを1μm程度まで薄膜化が容易なシアノ架橋金属錯体が使用されており、引用文献1~3のバルク状の電極に比べて、小型化ができる。また、薄膜化することで、酸化還元反応が薄膜の内部まで高速且つ均一に発生し、バルク状の電極を使用する場合に比べて、使用されない部分が少なく、効率よく電極6,7が使用される。
また、実施例1の電極6,7の表面層6b,7bでは、低コスト且つ電解析出等で厚さを1μm程度まで薄膜化が容易なシアノ架橋金属錯体が使用されており、引用文献1~3のバルク状の電極に比べて、小型化ができる。また、薄膜化することで、酸化還元反応が薄膜の内部まで高速且つ均一に発生し、バルク状の電極を使用する場合に比べて、使用されない部分が少なく、効率よく電極6,7が使用される。
さらに、実施例1の電極6,7では、基板6a,7aとして、白金電極に比べて低コストなITO電極を使用しており、コストを削減することが可能である。
特に、実施例1では、電極6,7として、同一の構成の電極を使用しており、構成の異なる電極の組を使用する場合に比べて、部品点数を削減でき、コストを低減することも可能である。
また、実施例1では、電解質として、低コスト且つ容易に入手可能な塩化ナトリウムの水溶液を使用しており、さらに低コスト化することができる。
特に、実施例1では、電極6,7として、同一の構成の電極を使用しており、構成の異なる電極の組を使用する場合に比べて、部品点数を削減でき、コストを低減することも可能である。
また、実施例1では、電解質として、低コスト且つ容易に入手可能な塩化ナトリウムの水溶液を使用しており、さらに低コスト化することができる。
(実験例)
次に、実施例1の効果を確認するための実験を行った。
(実験例1)
実験例1では、ITO基板の表面に電解析出法により、膜厚1600[nm]のNa0.72Ni[Fe(CN)6]0.68・5.1H2Oの膜を製膜する。そして、1[M(=mol/L)]のNaCl水溶液中で酸化を行い、Na0.21Ni[Fe(CN)6]0.68・5.1H2Oの薄膜、すなわち、NNF68の薄膜を得た。
次に、実施例1の効果を確認するための実験を行った。
(実験例1)
実験例1では、ITO基板の表面に電解析出法により、膜厚1600[nm]のNa0.72Ni[Fe(CN)6]0.68・5.1H2Oの膜を製膜する。そして、1[M(=mol/L)]のNaCl水溶液中で酸化を行い、Na0.21Ni[Fe(CN)6]0.68・5.1H2Oの薄膜、すなわち、NNF68の薄膜を得た。
(実験例1-1)
図2は実験例1-1の実験結果の説明図であり、横軸に温度を取り、縦軸に自然電位を取ったグラフである。
実験例1-1では、得られたNNF68の薄膜を1[M]のNaCl水溶液に浸し、自然電位の温度依存性を測定した。測定は、ITO基板を市販のポテンショスタットに接続して、参照電極に対する電位を自然電位として測定した。なお、自然電位とは、前記式(1)の酸化反応と、式(2)の還元反応の反応速度が同一となり、電流が流れなくなる電圧である。
実験例1-1の実験結果を図2に示す。
図2において、自然電位は、温度上昇に伴って、-1.1[mV/度]の割合で低下することが確認された。したがって、NNF68の薄膜では、前述のように酸化反応の速度が還元反応の速度に比べて相対的に速くなり、この酸化反応の速度上昇に伴って電極に電子が発生し、自然電位が相対的に低下する。
図2は実験例1-1の実験結果の説明図であり、横軸に温度を取り、縦軸に自然電位を取ったグラフである。
実験例1-1では、得られたNNF68の薄膜を1[M]のNaCl水溶液に浸し、自然電位の温度依存性を測定した。測定は、ITO基板を市販のポテンショスタットに接続して、参照電極に対する電位を自然電位として測定した。なお、自然電位とは、前記式(1)の酸化反応と、式(2)の還元反応の反応速度が同一となり、電流が流れなくなる電圧である。
実験例1-1の実験結果を図2に示す。
図2において、自然電位は、温度上昇に伴って、-1.1[mV/度]の割合で低下することが確認された。したがって、NNF68の薄膜では、前述のように酸化反応の速度が還元反応の速度に比べて相対的に速くなり、この酸化反応の速度上昇に伴って電極に電子が発生し、自然電位が相対的に低下する。
(実験例1-2)
図3は実験例1-2の実験結果の説明図であり、横軸に温度を取り、縦軸に熱起電力を取ったグラフである。
次に、実験例1のNNF68の薄膜が成膜されたITO基板を2つに分割して、それぞれを、実施例1の構成の電解質槽3に収容された1[M]のNaCl水溶液に浸した。室温は23度であった。次に、熱源8を作動させて、2つのNNF68の薄膜間の起電力を測定した。
実験結果を図3に示す。
図3において、グラフの横軸に取った第1槽3a内の水溶液の温度上昇に伴って、薄膜の起電力が、-0.55[mV/度]の割合で低下していった(熱起電力の絶対値は大きくなっている)。すなわち、両電極間に温度差を発生させると、両極間で自然電位に差が発生し、熱起電力は、温度上昇に伴う自然電位の変化に起因するものであると考えられる。
図3は実験例1-2の実験結果の説明図であり、横軸に温度を取り、縦軸に熱起電力を取ったグラフである。
次に、実験例1のNNF68の薄膜が成膜されたITO基板を2つに分割して、それぞれを、実施例1の構成の電解質槽3に収容された1[M]のNaCl水溶液に浸した。室温は23度であった。次に、熱源8を作動させて、2つのNNF68の薄膜間の起電力を測定した。
実験結果を図3に示す。
図3において、グラフの横軸に取った第1槽3a内の水溶液の温度上昇に伴って、薄膜の起電力が、-0.55[mV/度]の割合で低下していった(熱起電力の絶対値は大きくなっている)。すなわち、両電極間に温度差を発生させると、両極間で自然電位に差が発生し、熱起電力は、温度上昇に伴う自然電位の変化に起因するものであると考えられる。
(実験例2)
実験例2では、ITO基板の表面に電解析出法により成膜した、膜厚1400[nm]、1370[nm]のNa1.60Co[Fe(CN)6]0.90・2.9H2Oの薄膜、すなわち、NCF90の薄膜を使用した。
(実験例2-1)
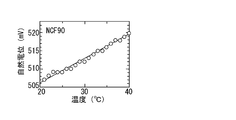
図4は実験例2-1の実験結果の説明図であり、横軸に温度を取り、縦軸に自然電位を取ったグラフである。
実験例2-1では、実験例1-1と同様にして、自然電位の温度依存性を測定した。実験結果を図4に示す。
図4において、自然電位は、温度上昇に伴って、+0.7[mV/度]で増大することが確認された。
実験例2では、ITO基板の表面に電解析出法により成膜した、膜厚1400[nm]、1370[nm]のNa1.60Co[Fe(CN)6]0.90・2.9H2Oの薄膜、すなわち、NCF90の薄膜を使用した。
(実験例2-1)
図4は実験例2-1の実験結果の説明図であり、横軸に温度を取り、縦軸に自然電位を取ったグラフである。
実験例2-1では、実験例1-1と同様にして、自然電位の温度依存性を測定した。実験結果を図4に示す。
図4において、自然電位は、温度上昇に伴って、+0.7[mV/度]で増大することが確認された。
(実験例2-2)
図5は実験例2-2の実験結果の説明図であり、横軸に温度を取り、縦軸に熱起電力を取ったグラフである。
次に、実験例1-2と同様にして、NCF90の薄膜をそれぞれ、1[M]のNaCl水溶液に浸して起電力を測定した。このときの室温は20度であった。
実験結果を図5に示す。
図5において、グラフの横軸に取った第1槽3a内の水溶液の温度上昇に伴って、薄膜の起電力が、+0.85[mV/度]の割合で増大した。
図5は実験例2-2の実験結果の説明図であり、横軸に温度を取り、縦軸に熱起電力を取ったグラフである。
次に、実験例1-2と同様にして、NCF90の薄膜をそれぞれ、1[M]のNaCl水溶液に浸して起電力を測定した。このときの室温は20度であった。
実験結果を図5に示す。
図5において、グラフの横軸に取った第1槽3a内の水溶液の温度上昇に伴って、薄膜の起電力が、+0.85[mV/度]の割合で増大した。
(実験例3)
実験例3では、ITO基板の表面に電解析出法により成膜した、膜厚950[nm]、1000[nm]のNa0.84Co[Fe(CN)6]0.71・3.8H2Oの薄膜、すなわち、NCF71の薄膜を使用した。
(実験例3-1)
図6は実験例3-1の実験結果の説明図であり、横軸に温度を取り、縦軸に自然電位を取ったグラフである。
実験例3-1では、実験例1-1、1-2と同様にして、自然電位の温度依存性を測定した。実験結果を図6に示す。
図6において、自然電位は、温度上昇に伴って、-0.85[mV/度]で低下することが確認された。
実験例3では、ITO基板の表面に電解析出法により成膜した、膜厚950[nm]、1000[nm]のNa0.84Co[Fe(CN)6]0.71・3.8H2Oの薄膜、すなわち、NCF71の薄膜を使用した。
(実験例3-1)
図6は実験例3-1の実験結果の説明図であり、横軸に温度を取り、縦軸に自然電位を取ったグラフである。
実験例3-1では、実験例1-1、1-2と同様にして、自然電位の温度依存性を測定した。実験結果を図6に示す。
図6において、自然電位は、温度上昇に伴って、-0.85[mV/度]で低下することが確認された。
(実験例3-2)
図7は実験例3-2の実験結果の説明図であり、横軸に温度を取り、縦軸に熱起電力を取ったグラフである。
次に、実験例1-2、2-2と同様にして、NCF71の薄膜をそれぞれ、1[M]のNaCl水溶液に浸して起電力を測定した。このときの室温は20度であった。
実験結果を図7に示す。
図7において、グラフの横軸に取った第1槽3a内の水溶液の温度上昇に伴って、薄膜の起電力が、-0.7[mV/度]の割合で増大した。
図7は実験例3-2の実験結果の説明図であり、横軸に温度を取り、縦軸に熱起電力を取ったグラフである。
次に、実験例1-2、2-2と同様にして、NCF71の薄膜をそれぞれ、1[M]のNaCl水溶液に浸して起電力を測定した。このときの室温は20度であった。
実験結果を図7に示す。
図7において、グラフの横軸に取った第1槽3a内の水溶液の温度上昇に伴って、薄膜の起電力が、-0.7[mV/度]の割合で増大した。
したがって、前記実験例1~3から、実施例1の電池1では、室温付近で、1[mV/度]程度の比較的大きな熱起電力が得られている。よって、例えば、負極6の数を増やしたり、電極6,7の組を多くし、且つ、直列に接続することで、比較的大きな起電力を、室温近くで発生させることが可能になっている。
図8は実施例2の熱電変換素子の説明図であり、実施例1の図1に対応する図である。
なお、この実施例2の説明において、前記実施例1の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例2は、下記の点で前記実施例1と相違しているが、他の点では前記実施例1と同様に構成されている。
なお、この実施例2の説明において、前記実施例1の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例2は、下記の点で前記実施例1と相違しているが、他の点では前記実施例1と同様に構成されている。
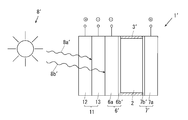
図8において、実施例2の熱電変換素子の一例としての複合型電池1′では、電解質2が収容された電解質槽3′の左右両側に対向して、一対の電極6′,7′が配置されている。各電極6′,7′の電解質槽3′側の表面に実施例1と同様に構成された表面層6b′,7b′が配置されており、表面層6b′,7b′が電解質2に接触している。被温冷部の一例としての実施例2の負極6′には、電解質槽3′とは逆側の面に、発電素子の一例としての太陽電池11が支持されている。太陽電池11は、従来公知の発電素子であり、p型半導体により構成された陽極12と、n型半導体により構成された陰極13と、を有する。そして、実施例2では、実施例1の熱源8に替えて、熱源の一例としての太陽8′を使用する。
(実施例2の作用)
前記構成を備えた実施例2の複合型電池1′では、太陽光に含まれる紫外線8a′により太陽電池11で発電を行うと共に、太陽光に含まれる赤外線8b′により負極6が加熱される。したがって、赤外線8b′の加熱に伴って、電極6′,7′間に温度差が発生し、実施例1の電池1と同様に、熱起電力が発生する。よって、実施例2の複合型電池1′では、熱源の一例としての太陽8′からの太陽光を利用し、発電を行うことができる。特に、実施例2では、電極6′,7′間に温度差を発生させる際に、太陽電池11で使用される紫外線8aとは波長が異なる赤外線8bが主として利用されており、太陽光を効率よく利用することが可能となっている。なお、電池1′の電極6′,7′と、太陽電池11の電極12,13とは、直列でも並列でも任意の接続方法が可能である。
前記構成を備えた実施例2の複合型電池1′では、太陽光に含まれる紫外線8a′により太陽電池11で発電を行うと共に、太陽光に含まれる赤外線8b′により負極6が加熱される。したがって、赤外線8b′の加熱に伴って、電極6′,7′間に温度差が発生し、実施例1の電池1と同様に、熱起電力が発生する。よって、実施例2の複合型電池1′では、熱源の一例としての太陽8′からの太陽光を利用し、発電を行うことができる。特に、実施例2では、電極6′,7′間に温度差を発生させる際に、太陽電池11で使用される紫外線8aとは波長が異なる赤外線8bが主として利用されており、太陽光を効率よく利用することが可能となっている。なお、電池1′の電極6′,7′と、太陽電池11の電極12,13とは、直列でも並列でも任意の接続方法が可能である。
図9は本発明の実施例3の熱電変換素子の説明図であり、実施例1の図1に対応する図である。
なお、この実施例3の説明において、前記実施例1、2の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例3は、下記の点で前記実施例1、2と相違しているが、他の点では前記実施例1、2と同様に構成されている。
なお、この実施例3の説明において、前記実施例1、2の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例3は、下記の点で前記実施例1、2と相違しているが、他の点では前記実施例1、2と同様に構成されている。
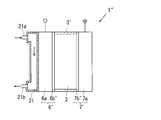
図9において、実施例3の熱電変換素子の一例としての電池1″では、実施例2と同様に構成された電解質槽3′や電極6′,7′を有し、実施例2の太陽電池11に替えて、熱流路21が支持されている。前記熱流路21には、外部に接続された図示しない熱発生部からの流体が上端の導入部21aから導入され、下端の排出部21bから排出される。
電池1″を、例えば、自動車に搭載した場合には、熱発生部は自動車のエンジンを使用可能であり、自動車のエンジンで発生した廃熱で加熱された流体を、熱流路21に導入可能である。また、熱発生部としての温泉や銭湯等から排出される湯を、加熱された流体として熱流路21に導入することも可能である。この他にも、地熱や、商業施設やオフィスビル等からの廃熱等を利用することも可能である。
電池1″を、例えば、自動車に搭載した場合には、熱発生部は自動車のエンジンを使用可能であり、自動車のエンジンで発生した廃熱で加熱された流体を、熱流路21に導入可能である。また、熱発生部としての温泉や銭湯等から排出される湯を、加熱された流体として熱流路21に導入することも可能である。この他にも、地熱や、商業施設やオフィスビル等からの廃熱等を利用することも可能である。
(実施例3の作用)
前記構成を備えた実施例3の電池1″では、廃熱等を利用して、電極6′,7′間に温度差を発生させて、熱起電力を発生させ、発電を行うことができる。特に、実施例3の電池1″では、本来は廃棄されるだけの廃熱等を有効利用することも可能である。なお、負極6′側を加熱するのに並行して、正極7′側を外気に接触させたり、送風する等して冷却することも可能であり、温度差を大きくすることで、熱起電力を大きくして発電効率を高めることも可能である。
前記構成を備えた実施例3の電池1″では、廃熱等を利用して、電極6′,7′間に温度差を発生させて、熱起電力を発生させ、発電を行うことができる。特に、実施例3の電池1″では、本来は廃棄されるだけの廃熱等を有効利用することも可能である。なお、負極6′側を加熱するのに並行して、正極7′側を外気に接触させたり、送風する等して冷却することも可能であり、温度差を大きくすることで、熱起電力を大きくして発電効率を高めることも可能である。
図10は本発明の実施例4の熱電変換素子の説明図であり、実施例1の図1に対応する図である。
なお、この実施例4の説明において、前記実施例1~3の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例4は、下記の点で前記実施例1~3と相違しているが、他の点では前記実施例1~3と同様に構成されている。
図10において、実施例4の熱電変換素子31は、活物質の一例としてのコバルト酸リチウム(LiCoO2)からなる一対の第1の電極32および第2の電極33を有する。電極32,33どうしは、間隔をあけて配置されており、電極32,33の間は、一対の壁部材34で仕切られている。したがって、前記電極32,33および壁部材34により囲まれた空間には、電解質溶液36が収容されている。
そして、実施例4では、第1の電極32に、熱源の一例としてのヒータ37が接触しており、第1の電極32が被温冷部となっている。
なお、この実施例4の説明において、前記実施例1~3の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例4は、下記の点で前記実施例1~3と相違しているが、他の点では前記実施例1~3と同様に構成されている。
図10において、実施例4の熱電変換素子31は、活物質の一例としてのコバルト酸リチウム(LiCoO2)からなる一対の第1の電極32および第2の電極33を有する。電極32,33どうしは、間隔をあけて配置されており、電極32,33の間は、一対の壁部材34で仕切られている。したがって、前記電極32,33および壁部材34により囲まれた空間には、電解質溶液36が収容されている。
そして、実施例4では、第1の電極32に、熱源の一例としてのヒータ37が接触しており、第1の電極32が被温冷部となっている。
実施例4の電極32,33は、LiCoO2の粉末をバインダーとカーボンブラックと共に混ぜ合わせ、スラリーを作製し、このスラリーをアルミニウム箔上に塗布して、120℃で2時間乾燥させ電極とした。なお、以下、この電極32,33を「LCO電極」と記載する。
また、実施例4の壁部材34は、ポリテトラフルオロエチレン(PTFE)により構成したが、材料はこれに限定されず、使用可能な任意の材料に変更可能である。
さらに、実施例4では、炭酸エチレンと炭酸ジエチルとを体積比で1対1で混合した溶媒(EC+DEC溶液)中に、アルカリ金属イオンの一例としてのリチウムイオン(Li+)を含む過塩素酸リチウム(LiClO4)を1モル溶かした溶液を、電解質溶液36の一例として使用した。
また、実施例4の壁部材34は、ポリテトラフルオロエチレン(PTFE)により構成したが、材料はこれに限定されず、使用可能な任意の材料に変更可能である。
さらに、実施例4では、炭酸エチレンと炭酸ジエチルとを体積比で1対1で混合した溶媒(EC+DEC溶液)中に、アルカリ金属イオンの一例としてのリチウムイオン(Li+)を含む過塩素酸リチウム(LiClO4)を1モル溶かした溶液を、電解質溶液36の一例として使用した。
なお、実施例4の電極32,33では、作製されたLCO電極に対して、リチウム欠損を引き起こしたものを使用した。すなわち、1モルの過塩素酸リチウムが溶かされたEC+DEC溶液に、LCO電極と、リチウム金属の電極とを浸し、LCO電極が正極、リチウム金属が負極となるように電圧を印加した。このとき、LCO電極では、以下の式(3)の反応が発生し、リチウムイオンが流出して、LCO電極にリチウムの欠損が発生する。
LiCoO2 → Li1-xCoO2+ xLi+ + xe- …式(3)
なお、式(3)において、xは0より大きく1未満の数値である。
すなわち、この電圧印加により、LCO電極は、いわば、充電がされた状態となる。
LiCoO2 → Li1-xCoO2+ xLi+ + xe- …式(3)
なお、式(3)において、xは0より大きく1未満の数値である。
すなわち、この電圧印加により、LCO電極は、いわば、充電がされた状態となる。
(実施例4の作用)
前記構成を備えた実施例4の熱電変換素子31では、ヒータ37により第1の電極32が加熱されていない状態では、以下の式(4)に示す酸化反応と、式(5)に示す還元反応とが平衡して電流が流れない。
LiCo3+O2 → LiCo4+O2 + e- …式(4)
LiCo4+O2 + e- → LiCo3+O2 …式(5)
そして、ヒータ37により第1の電極32が加熱されると、電極32,33間に温度差が発生し、平衡状態が崩れる。LCO電極では、温度が高くなると、酸化反応の速度が上昇し、第1の電極32が負極となり、第2の電極33が正極となる。この電極32,33での反応に伴って、収容空間36の電解質において、分子量が非常に小さく移動速度の速いアルカリ金属イオンであるリチウムイオンLi+が移動する。したがって、実施例4の熱電変換素子31でも、実施例1~3と同様に、電極32,33における酸化還元反応に起因して熱起電力が発生する。
前記構成を備えた実施例4の熱電変換素子31では、ヒータ37により第1の電極32が加熱されていない状態では、以下の式(4)に示す酸化反応と、式(5)に示す還元反応とが平衡して電流が流れない。
LiCo3+O2 → LiCo4+O2 + e- …式(4)
LiCo4+O2 + e- → LiCo3+O2 …式(5)
そして、ヒータ37により第1の電極32が加熱されると、電極32,33間に温度差が発生し、平衡状態が崩れる。LCO電極では、温度が高くなると、酸化反応の速度が上昇し、第1の電極32が負極となり、第2の電極33が正極となる。この電極32,33での反応に伴って、収容空間36の電解質において、分子量が非常に小さく移動速度の速いアルカリ金属イオンであるリチウムイオンLi+が移動する。したがって、実施例4の熱電変換素子31でも、実施例1~3と同様に、電極32,33における酸化還元反応に起因して熱起電力が発生する。
特に、実施例4では、従来公知のリチウムイオン電池において正極として使用されているコバルト酸リチウムの電極を使用することが可能であり、既存の生産設備を使用することができ、コスト上昇を抑制することができる。また、従来技術のように、白金(Pt)電極のような高価な電極を使用する必要がなく、コストを削減することができる。
また、実施例4の熱電変換素子31では、実施例1~3と同様に、活物質が固体である電極32,33中に存在しており、従来のように活物質が液体である溶液中に存在する構成に比べて、活物質の密度が高くなる。したがって、実施例4の熱電変換素子31では、活物質の密度が低い従来の構成に比べて、熱電変換の効率も向上すると共に、低密度の溶液を使用せず、高密度の活物質を使用しており、薄型で小型化しても、同様の出力を得ることが可能になっている。
また、実施例4の熱電変換素子31では、活物質として、溶液に溶けない材料も使用することができ、材料選択の幅を広げることができる。
また、実施例4の熱電変換素子31では、実施例1~3と同様に、活物質が固体である電極32,33中に存在しており、従来のように活物質が液体である溶液中に存在する構成に比べて、活物質の密度が高くなる。したがって、実施例4の熱電変換素子31では、活物質の密度が低い従来の構成に比べて、熱電変換の効率も向上すると共に、低密度の溶液を使用せず、高密度の活物質を使用しており、薄型で小型化しても、同様の出力を得ることが可能になっている。
また、実施例4の熱電変換素子31では、活物質として、溶液に溶けない材料も使用することができ、材料選択の幅を広げることができる。
(実験例)
次に、実施例4の効果を確かめるための実験を行った。
(実験例4)
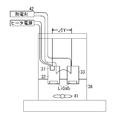
図11は実験例4の測定装置の説明図である。
図11において、実験例4では、実施例4の電極32,33や電解質溶液36を使用した。実験例4では、電界質溶液36中に、電界質溶液36を撹拌する回転子41を配置した。また、電極32,33の間に、電圧計を接続して電位差△Vを測定すると共に、電極32,33の間に熱電対42を接続して、電極32,33間の温度差△Tも測定した。
次に、実施例4の効果を確かめるための実験を行った。
(実験例4)
図11は実験例4の測定装置の説明図である。
図11において、実験例4では、実施例4の電極32,33や電解質溶液36を使用した。実験例4では、電界質溶液36中に、電界質溶液36を撹拌する回転子41を配置した。また、電極32,33の間に、電圧計を接続して電位差△Vを測定すると共に、電極32,33の間に熱電対42を接続して、電極32,33間の温度差△Tも測定した。
(実験例4-1、4-2)
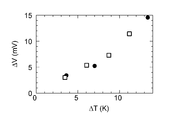
図12は実験例4の実験結果の説明図であり、横軸に温度差を取り、縦軸に電位差を取ったグラフである。
実験例4-1では、回転子41を停止させた状態で、ヒータ37に電流を供給することで、温度差△Tを発生させ、最大で13.5[K]の温度差が発生した。なお、電位差△Vの測定は、温度差△Tが、4.5[K]、7[K]、13.5[K]の場合に行った。実験結果を図12の黒丸(●)で示す。
また、実験例4-2では、回転子41を回転させた状態で、ヒータ37に電流を供給して、温度差△Tを発生させ、最大で12[K]の温度差が発生した。なお、電位差△Vの測定は、温度差△Tが、4.5[K]、6[K]、9[K]、12[K]の場合に行った。実験結果を図12の四角(□)で示す。
図12は実験例4の実験結果の説明図であり、横軸に温度差を取り、縦軸に電位差を取ったグラフである。
実験例4-1では、回転子41を停止させた状態で、ヒータ37に電流を供給することで、温度差△Tを発生させ、最大で13.5[K]の温度差が発生した。なお、電位差△Vの測定は、温度差△Tが、4.5[K]、7[K]、13.5[K]の場合に行った。実験結果を図12の黒丸(●)で示す。
また、実験例4-2では、回転子41を回転させた状態で、ヒータ37に電流を供給して、温度差△Tを発生させ、最大で12[K]の温度差が発生した。なお、電位差△Vの測定は、温度差△Tが、4.5[K]、6[K]、9[K]、12[K]の場合に行った。実験結果を図12の四角(□)で示す。
図12において、実験例4-1,4-2のいずれにおいても、温度差△Tが大きくなるに連れて、電位差△Vが大きくなる結果が得られた。この実験結果から、ゼーベック係数を演算すると、実験例4-1,4-2は、それぞれ、1.08[mV/K]、0.99[mV/K]であった。なお、これは、現在実用化されている熱電変換素子の一例としてのペルティエ素子で使用されているビスマステルル(Bi2Te3)の5倍程度であった。したがって、実施例4の熱電変換素子31は、従来公知のペルティエ素子に比べて、高効率の熱電変換素子を作製できることが期待できる。
(実験例4-3)
次に、実験例4-3として、リチウム欠損を引き起こしていないLCO電極を使用して、同様に実験を行った。
実験例4-3では、測定を2回行った結果、電極間に最大で18.5[K]、17.9[K]の温度差△Tが発生し、このときの電位差△Vが2.6[mV]、1.9[mV]であった。これらのゼーベック係数を演算すると、それぞれ、0.14[mV/K]、0.11[mV/K]であった。これらは、実験例4-1,4-2に比べて、1桁小さいが、従来のビスマス-テルル(Bi2Te3)系に比べて、1/2程度の効率は有していることが確認された。
実験例4-3でゼーベック係数が小さくなった原因は、リチウム欠損がないLCO電極、すなわち、充電していないLCO電極では、酸化還元反応が引き起こされにくいが、LCO電極に自然に発生している少量のリチウム欠損や、LCO電極が電解質溶液中に浸された時にリチウムイオンの導入が自然に発生したことに起因していると考えられる。
次に、実験例4-3として、リチウム欠損を引き起こしていないLCO電極を使用して、同様に実験を行った。
実験例4-3では、測定を2回行った結果、電極間に最大で18.5[K]、17.9[K]の温度差△Tが発生し、このときの電位差△Vが2.6[mV]、1.9[mV]であった。これらのゼーベック係数を演算すると、それぞれ、0.14[mV/K]、0.11[mV/K]であった。これらは、実験例4-1,4-2に比べて、1桁小さいが、従来のビスマス-テルル(Bi2Te3)系に比べて、1/2程度の効率は有していることが確認された。
実験例4-3でゼーベック係数が小さくなった原因は、リチウム欠損がないLCO電極、すなわち、充電していないLCO電極では、酸化還元反応が引き起こされにくいが、LCO電極に自然に発生している少量のリチウム欠損や、LCO電極が電解質溶液中に浸された時にリチウムイオンの導入が自然に発生したことに起因していると考えられる。
図13は本発明の実施例5の熱電変換素子の説明図であり、実施例1の図1に対応する図である。
なお、この実施例5の説明において、前記実施例1~4の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例5は、下記の点で前記実施例1~4と相違しているが、他の点では前記実施例1~4と同様に構成されている。
図13において、実施例5の熱電変換素子の一例としての電池51では、合計で10層分の電極52-1,52-2,52-3,…,52-10が、間隔をあけて平行に配置されている。
実施例5の電極52-1~電極52-10は、実施例4の電極32,33と同様に、アルミ箔の表面にコバルト酸リチウム(LiCoO2)が塗布された構成が採用されている。そして、第1層の電極52-1および第10層の電極52-10では、アルミ箔53の片面にコバルト酸リチウムが塗布された活物質層54が形成されており、第2層の電極52-2~第9層の電極52-9では、アルミ箔53の両面にコバルト酸リチウムが塗布された活物質層54が形成されている。なお、第1層および第10層の電極52-1,52-10でも、第2層~第9層の電極52-2~52-9と同様に構成されている。
なお、この実施例5の説明において、前記実施例1~4の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例5は、下記の点で前記実施例1~4と相違しているが、他の点では前記実施例1~4と同様に構成されている。
図13において、実施例5の熱電変換素子の一例としての電池51では、合計で10層分の電極52-1,52-2,52-3,…,52-10が、間隔をあけて平行に配置されている。
実施例5の電極52-1~電極52-10は、実施例4の電極32,33と同様に、アルミ箔の表面にコバルト酸リチウム(LiCoO2)が塗布された構成が採用されている。そして、第1層の電極52-1および第10層の電極52-10では、アルミ箔53の片面にコバルト酸リチウムが塗布された活物質層54が形成されており、第2層の電極52-2~第9層の電極52-9では、アルミ箔53の両面にコバルト酸リチウムが塗布された活物質層54が形成されている。なお、第1層および第10層の電極52-1,52-10でも、第2層~第9層の電極52-2~52-9と同様に構成されている。
各電極52-1~52-10の間には、保持部材の一例としてのセパレータ56が配置されている。前記セパレータ56は、従来公知の電池で使用されているセパレータが使用されている、セパレータ56には、電界質溶液が保持されている。なお、図13では、理解を容易にするために、模式的に、セパレータ56とその両側を挟む電極52-1~52-10との間に電界質溶液57,58の層を記載している。
実施例5の電界質溶液57,58は、EC+DEC溶液中に過塩素酸リチウム(LiClO4)を1モル溶かした溶液が使用されている。
実施例5の電界質溶液57,58は、EC+DEC溶液中に過塩素酸リチウム(LiClO4)を1モル溶かした溶液が使用されている。
図13において、実施例5では、各電極52-1~52-10およびセパレータ56の外側は、外装部材の一例としてのフィルム59で被覆されると共に、1層の電極52-1と10層目の電極52-10には、導線61が接続されている。
そして、実施例5では、被温冷部の一例としての第1層の電極52-1の外側に、予め設定された温度THの高温熱浴62が接触して配置されている。また、被温冷部の一例としての第10層の電極52-10の外側に、高温熱浴62の温度THよりも低温の予め設定された温度TLの低温熱浴63が接触して配置されている。したがって、実施例5の各電極52-1,52-2,…,52-10の温度T1,T2,…,T10は、各熱浴62,63の温度TH,TLの温度差により、自然に、TH=T1>T2>…>T10=TLとなる。
よって、実施例5では、対向する電極52-1~52-10の各組において、高温側の電極52-1~52-9が第1の電極となり、低温側の電極52-2~52-10が第2の電極となっている。
そして、実施例5では、被温冷部の一例としての第1層の電極52-1の外側に、予め設定された温度THの高温熱浴62が接触して配置されている。また、被温冷部の一例としての第10層の電極52-10の外側に、高温熱浴62の温度THよりも低温の予め設定された温度TLの低温熱浴63が接触して配置されている。したがって、実施例5の各電極52-1,52-2,…,52-10の温度T1,T2,…,T10は、各熱浴62,63の温度TH,TLの温度差により、自然に、TH=T1>T2>…>T10=TLとなる。
よって、実施例5では、対向する電極52-1~52-10の各組において、高温側の電極52-1~52-9が第1の電極となり、低温側の電極52-2~52-10が第2の電極となっている。
図14は実施例5の熱電変換素子が直列に接続されたモジュールの説明図である。
図14において、実施例5の電池モジュール71では、3つの電池51が、電気的に直列に接続されている。すなわち、図14に示すように、第2の電池51Bの第1層の電極52-1の導線61が第3の電池51Cの第10層の電極52-10に接続され、且つ、第2の電池51Bの第10層の電極52-10の導線61が第1の電池51Aの第1層の電極52-1に接続されている。
そして、各電池51A~51Cは、共通の高温熱浴62および低温熱浴63に接触している。
図14において、実施例5の電池モジュール71では、3つの電池51が、電気的に直列に接続されている。すなわち、図14に示すように、第2の電池51Bの第1層の電極52-1の導線61が第3の電池51Cの第10層の電極52-10に接続され、且つ、第2の電池51Bの第10層の電極52-10の導線61が第1の電池51Aの第1層の電極52-1に接続されている。
そして、各電池51A~51Cは、共通の高温熱浴62および低温熱浴63に接触している。
(実施例5の作用)
前記構成を備えた実施例5の電池51では、各電極52-1~52-10の活物質層54がセパレータ56に保持された電界質溶液57,58を挟んで対向して配置されており、各電極52-1~52-10の間には、それぞれ温度差△T1=T1-T2、△T2=T2-T3,…,△T9=T9-T10が発生している。したがって、各電極52-1~52-10の間で熱起電力が発生し、電流が流れ、第1層の電極52-1と第10層の電極52-10と間で電位差△Vが発生する。このときの電位差△Vは、各電極52-1~52-10の間で発生する電位差△V1=S(T1-T2),△V2=S(T2-T3),…,△V9=S(T9-T10)の和となる。なお、Sは、ゼーベック係数である。
すなわち、△V=△V1+△V2+…+△V9=S(T1-T10)=S(TH-TL)となる。
前記構成を備えた実施例5の電池51では、各電極52-1~52-10の活物質層54がセパレータ56に保持された電界質溶液57,58を挟んで対向して配置されており、各電極52-1~52-10の間には、それぞれ温度差△T1=T1-T2、△T2=T2-T3,…,△T9=T9-T10が発生している。したがって、各電極52-1~52-10の間で熱起電力が発生し、電流が流れ、第1層の電極52-1と第10層の電極52-10と間で電位差△Vが発生する。このときの電位差△Vは、各電極52-1~52-10の間で発生する電位差△V1=S(T1-T2),△V2=S(T2-T3),…,△V9=S(T9-T10)の和となる。なお、Sは、ゼーベック係数である。
すなわち、△V=△V1+△V2+…+△V9=S(T1-T10)=S(TH-TL)となる。
実施例4のように1層の薄型素子の場合、電極間につく温度差は、理想的には(TH-TL)であるが、実際の温度差は、熱抵抗等により、熱浴間の温度差(TH-TL)よりも小さくなる。これに対応して、実施例5のような多層型の電池51では、多層化することで、熱抵抗を大きくすることができ、第1層の電極52-1と第10層の電極52-10との間に発生する温度差△Tは、TH-TLに近づく。すなわち、温度差が理想値に近づき、発生する電位差△Vを大きくすることができ、効率を高めることができる。
また、実施例5の電池モジュール71では、電池51を直列に接続することで、発生する電圧を高めることができ、電池51の数を増やすことで、mVオーダーではなく、Vオーダーの電圧を発生させることも可能である。
また、実施例5の電池モジュール71では、電池51を直列に接続することで、発生する電圧を高めることができ、電池51の数を増やすことで、mVオーダーではなく、Vオーダーの電圧を発生させることも可能である。
次に実施例6の説明をするが、この実施例6の説明において、前記実施例1~5の構成要素に対応する構成要素には同一の符号を付して、その詳細な説明を省略する。
この実施例6は、下記の点で前記実施例1~5と相違しているが、他の点では前記実施例1~5と同様に構成されている。
実施例6の熱電変換素子の一例としての電池は、実施例4のコバルト酸リチウムが使用された電極に代えて、活物質の一例としての炭素(グラファイト、C6)が使用された電極が採用されており、電極以外は同様に構成されているため、詳細な説明は省略する。すなわち、実施例6では、実施例4と同様の電界質溶液やヒータ等が使用されている。
この実施例6は、下記の点で前記実施例1~5と相違しているが、他の点では前記実施例1~5と同様に構成されている。
実施例6の熱電変換素子の一例としての電池は、実施例4のコバルト酸リチウムが使用された電極に代えて、活物質の一例としての炭素(グラファイト、C6)が使用された電極が採用されており、電極以外は同様に構成されているため、詳細な説明は省略する。すなわち、実施例6では、実施例4と同様の電界質溶液やヒータ等が使用されている。
実施例6の電極は、炭素粉末を、実施例4と同様に、バインダーとともに混ぜ合わせて、スラリーを作製して、スラリーをアルミニウム箔上に塗布して、120℃で2時間乾燥させて電極とした。なお、この電極を、以下、「C電極」と表記する。
なお、実施例6の電極では、実施例4のリチウム欠損とは逆に、C電極に対して、以下の式(6)に示すように、リチウムの導入を引き起こしたものを使用した。すなわち、実施例4と同様に、1モルの過塩素酸リチウムが溶かされたEC+DEC溶液に、C電極と、リチウム金属の電極とを浸し、C電極が正極、リチウム金属が負極となるように電圧を印加した。このとき、C電極では、以下の式(6)の反応が発生し、リチウムイオンが流入して、C電極にリチウムの導入が発生する。
xLi++ xe- +C6 → LixC6 …式(6)
これにより、C電極は、いわば放電された状態となる。
なお、実施例6の電極では、実施例4のリチウム欠損とは逆に、C電極に対して、以下の式(6)に示すように、リチウムの導入を引き起こしたものを使用した。すなわち、実施例4と同様に、1モルの過塩素酸リチウムが溶かされたEC+DEC溶液に、C電極と、リチウム金属の電極とを浸し、C電極が正極、リチウム金属が負極となるように電圧を印加した。このとき、C電極では、以下の式(6)の反応が発生し、リチウムイオンが流入して、C電極にリチウムの導入が発生する。
xLi++ xe- +C6 → LixC6 …式(6)
これにより、C電極は、いわば放電された状態となる。
(実施例6の作用)
前記構成を備えた実施例6の電池では、ヒータにより第1の電極が加熱されていない状態では、以下の式(7)に示す酸化反応と、式(8)に示す還元反応とが平衡して電流が流れない。
LixC6 → xLi++ xe- +C6 …式(7)
xLi++ xe- +C6 → LixC6 …式(8)
そして、実施例4と同様に、ヒータにより第1の電極が加熱されると、電極間に温度差が発生し、平衡状態が崩れる。C電極では、温度が高くなると、還元反応の速度が上昇し、第1の電極(32)が正極となり、第2の電極(33)が負極となる。この電極(32,33)での反応に伴って、電解質溶液(36)において、分子量が非常に小さく移動速度の速いアルカリ金属イオンであるリチウムイオンLi+が移動する。したがって、実施例6の電池でも、実施例1~5と同様に、電極(32,33)における酸化還元反応に起因して熱起電力が発生する。
前記構成を備えた実施例6の電池では、ヒータにより第1の電極が加熱されていない状態では、以下の式(7)に示す酸化反応と、式(8)に示す還元反応とが平衡して電流が流れない。
LixC6 → xLi++ xe- +C6 …式(7)
xLi++ xe- +C6 → LixC6 …式(8)
そして、実施例4と同様に、ヒータにより第1の電極が加熱されると、電極間に温度差が発生し、平衡状態が崩れる。C電極では、温度が高くなると、還元反応の速度が上昇し、第1の電極(32)が正極となり、第2の電極(33)が負極となる。この電極(32,33)での反応に伴って、電解質溶液(36)において、分子量が非常に小さく移動速度の速いアルカリ金属イオンであるリチウムイオンLi+が移動する。したがって、実施例6の電池でも、実施例1~5と同様に、電極(32,33)における酸化還元反応に起因して熱起電力が発生する。
(実験例)
次に、実施例6の効果を確かめるための実験を行った。
(実験例6)
実験例6では、実施例4と同様の実験装置を使用して、電極の間の電位差△Vを測定すると共に、電極間の温度差△Tも測定した。
次に、実施例6の効果を確かめるための実験を行った。
(実験例6)
実験例6では、実施例4と同様の実験装置を使用して、電極の間の電位差△Vを測定すると共に、電極間の温度差△Tも測定した。
(実験例6-1)
図15は実験例6の実験結果の説明図であり、横軸に温度差を取り、縦軸に電位差を取ったグラフである。
実験例6-1では、実験例4-1と同様に、回転子41を停止させた状態で、ヒータ37に電流を供給することで、温度差△Tを発生させ、最大で20[K]程度の温度差を発生させた。なお、測定は2つの異なる試料について行い、電位差△Vの測定は、温度差△Tが、5[K]、10[K]、12.5[K]、16[K]、20[K]、21[K]、の場合に行った。実験結果を図15に示す。
図15は実験例6の実験結果の説明図であり、横軸に温度差を取り、縦軸に電位差を取ったグラフである。
実験例6-1では、実験例4-1と同様に、回転子41を停止させた状態で、ヒータ37に電流を供給することで、温度差△Tを発生させ、最大で20[K]程度の温度差を発生させた。なお、測定は2つの異なる試料について行い、電位差△Vの測定は、温度差△Tが、5[K]、10[K]、12.5[K]、16[K]、20[K]、21[K]、の場合に行った。実験結果を図15に示す。
図15において、実験例6-1において、温度差△Tが大きくなるに連れて、電位差△Vの絶対値が大きくなる結果が得られた。この実験結果から、ゼーベック係数を演算すると、実験例6-1では、2回の測定が-1.65[mV/K]、-1.70[mV/K]であった。なお、これは、現在実用化されている熱電変換素子の一例としてのペルティエ素子で使用されているビスマステルル(Bi2Te3)の8倍程度であった。したがって、実施例6の熱電変換素子は、従来公知のペルティエ素子に比べて、高効率の熱電変換素子を作製できることが期待できる。
(実験例6-2)
実験例6-2では、実験例4-3と同様に、放電を行わないC電極(すなわち、リチウム導入のない電極)を使用して、ゼーベック係数の測定を2回行った。各測定では、電極間に、12.5[K]、17.8[K]の温度差を発生させると、-13.2[mV]、-12.8[mV]、が測定された。これより、ゼーベック係数は、-1.06[mV/K]、-0.72[mV/K]と見積もられた。これは、実験例6-1に比べて半分程度になっているが、従来のビスマステルル系に比べて、4倍程度高くなっている。なお、実験例6-1に比べて小さなゼーベック係数は放電しないC電極において酸化還元反応が引き起こされにくいことに起因している。
したがって、実験例6-1,6-2から、リチウム導入をしなくても、従来よりも高効率の素子が作成可能であるが、リチウム導入をした方が、さらに高効率の素子を作成可能であることが確認された。
実験例6-2では、実験例4-3と同様に、放電を行わないC電極(すなわち、リチウム導入のない電極)を使用して、ゼーベック係数の測定を2回行った。各測定では、電極間に、12.5[K]、17.8[K]の温度差を発生させると、-13.2[mV]、-12.8[mV]、が測定された。これより、ゼーベック係数は、-1.06[mV/K]、-0.72[mV/K]と見積もられた。これは、実験例6-1に比べて半分程度になっているが、従来のビスマステルル系に比べて、4倍程度高くなっている。なお、実験例6-1に比べて小さなゼーベック係数は放電しないC電極において酸化還元反応が引き起こされにくいことに起因している。
したがって、実験例6-1,6-2から、リチウム導入をしなくても、従来よりも高効率の素子が作成可能であるが、リチウム導入をした方が、さらに高効率の素子を作成可能であることが確認された。
(変更例)
以上、本発明の実施例を詳述したが、本発明は、前記実施例に限定されるものではなく、特許請求の範囲に記載された本発明の要旨の範囲内で、種々の変更を行うことが可能である。本発明の変更例(H01)~(H07)を下記に例示する。
(H01)前記実施例において、基板の一例としてのITO電極にシアノ架橋金属錯体を析出させる場合について説明し、コスト面からはITO電極を使用することが望ましいが、これに限定されず、白金、金、アルミニウム等の導電体表面に製膜することも可能である。
以上、本発明の実施例を詳述したが、本発明は、前記実施例に限定されるものではなく、特許請求の範囲に記載された本発明の要旨の範囲内で、種々の変更を行うことが可能である。本発明の変更例(H01)~(H07)を下記に例示する。
(H01)前記実施例において、基板の一例としてのITO電極にシアノ架橋金属錯体を析出させる場合について説明し、コスト面からはITO電極を使用することが望ましいが、これに限定されず、白金、金、アルミニウム等の導電体表面に製膜することも可能である。
(H02)前記実験例において例示した電解質については、例示したものに限定されず、任意のアルカリ金属イオンを含む電解質を使用可能である。特に、アルカリ金属イオンの一例としてのLi+イオンを使用する場合には、従来公知のリチウムイオン電池の構成を利用して、セパレータを固体電解質として使用することも可能となり、更なる小型化、薄膜化が可能となり、正極と負極を多層、多段に並べて、小型で大容量化や高電圧化することも可能となる。特に、リチウムイオン電池の構成を使用する場合には、公知の技術を利用して、低コストな素子開発が十分に可能であり、室温付近での熱発電や太陽熱発電が期待できる。
(H03)前記実施例において、シアノ架橋金属錯体は、実験例で例示した構成に限定されず、製法や用途等に応じて、Aをアルカリ金属の少なくとも一種、Mを遷移金属の少なくとも一種、Lを遷移金属の少なくとも一種、xを0より大きく2以下の数、yを0より大きく1以下の数、zを0より大きく14以下の数とした場合に、化学式AxM[L(CN)6]y・nH2Oで表されるシアノ架橋金属錯体を使用可能である。なお、前記Aのアルカリ金属としては、例えば、Li、Na、K、Rb、Csが挙げられる。また、前記Mの遷移金属としては、Fe、Mn、Ni、Co、Cr、V、Cu、Znが挙げられる。また、Lの遷移金属としては、Fe、Cr、V、Mn、Tiが挙げられる。また、x、y、zは、それぞれ、遷移金属Mの1モルに対するアルカリ金属A、L(CN)6、結晶水H2Oの割合(モル)を示し、シアノ架橋金属錯体では、製法や構造により、xが0~2、yが0~1、zが0~14の値を取りうる。なお、本願明細書および特許請求の範囲において、「異なる組成の錯体」とは、アルカリ金属A、遷移金属M,Lおよび数x、yの少なくとも1つが異なるものを指している。
(H04)前記実施例において、熱源として、電極6,6′を加熱する構成を例示したが、これに限定されず、電極6,6′側を加熱せず、電極7,7′側を冷却することで温度差を発生させる構成とすることも可能であり、電極6,6′側を加熱し且つ電極7,7′側を冷却することで更に大きな温度差を発生させる構成とすることも可能である。他にも、熱電変換素子を衣服に装着して、人体の体温と外気温との温度差を利用して、熱発電を行うことも可能である。
(H05)前記実験例において、特許文献2,3に記載されているような濃度差を利用して発電を行う構成も組み合わせることも可能である。
(H05)前記実験例において、特許文献2,3に記載されているような濃度差を利用して発電を行う構成も組み合わせることも可能である。
(H06)前記実施例における熱電変換素子では、外部に電流を取り出すと、ナトリウムイオンやリチウムイオンが移動し、内部では、いわば、充電が発生するため、無限に電流を取り出すことができず、熱発電効率が経時的に低下する。したがって、起電力や電極間の温度差をモニタリングして、内部を放電させるプロセス、例えば、逆に電流を流したり、逆の電極を加熱したりするプロセスを、定期的、自動的に実行することが望ましく、このようにすることで、電池としての性能を持続させることができる。なお、蓄電素子と接続して、電力発生時には、蓄電素子を充電すると共に、起電力が低下すると蓄電素子から電流を受けて電池1、1′、1″、31、51の内部の放電を行うことも可能である。
また、熱発電効率が低下した状態では、温度勾配による起電力をリチウムイオンやナトリウムイオンの濃度差による起電力が打ち消した状態となり、正味の起電力がなくなった状態であるので、熱発電効率が低下した場合に、温度勾配を取り除く、すなわち、太陽熱や熱浴を取り除くことで、濃度差による起電力を取り出すことができる。なお、濃度差による起電力が取り出されると、電極の放電が発生するため、濃度差による起電力が取り出された後に、温度勾配をつけると、再度、熱発電を行うことが期待できる。
また、熱発電効率が低下した状態では、温度勾配による起電力をリチウムイオンやナトリウムイオンの濃度差による起電力が打ち消した状態となり、正味の起電力がなくなった状態であるので、熱発電効率が低下した場合に、温度勾配を取り除く、すなわち、太陽熱や熱浴を取り除くことで、濃度差による起電力を取り出すことができる。なお、濃度差による起電力が取り出されると、電極の放電が発生するため、濃度差による起電力が取り出された後に、温度勾配をつけると、再度、熱発電を行うことが期待できる。
(H07)前記実施例4~6において、リチウム欠損やリチウム導入を行うことが望ましいが、省略することも可能である。
前述の本発明の熱電変換素子は、電圧印加で温度差を誘起するペルティエ素子や、熱発電素子、太陽熱発電素子、蓄電素子と一体化した電力システムとして使用することが可能である。
また、本発明の熱電変換素子は、安価で薄型の熱電変換素子が実現可能であり、ポータブル(携帯性、可搬性)、または、ウェアブル(着用性、身につけられる)な熱発電素子として使用することが可能である。さらに、ポータブルまたはウェアブルな熱充電素子としても使用することが可能である。
また、本発明の熱電変換素子は、安価で薄型の熱電変換素子が実現可能であり、ポータブル(携帯性、可搬性)、または、ウェアブル(着用性、身につけられる)な熱発電素子として使用することが可能である。さらに、ポータブルまたはウェアブルな熱充電素子としても使用することが可能である。
1,1′,1″,31,51…熱電変換素子、
2,36,57,58…電解質、
3a,6′,32,52-1,52-10…被温冷部、
6,6′,32,52-1~52-9…第1の電極、
6a,7a…基板、
6b,7b,6b′,7b′…シアノ架橋金属錯体、
7,7′,52-2~52-10…第2の電極。
2,36,57,58…電解質、
3a,6′,32,52-1,52-10…被温冷部、
6,6′,32,52-1~52-9…第1の電極、
6a,7a…基板、
6b,7b,6b′,7b′…シアノ架橋金属錯体、
7,7′,52-2~52-10…第2の電極。
Claims (20)
- アルカリ金属イオンを含む電解質に対して、電子の受け渡しを行う活物質を含む第1の電極と、前記第1の電極と同一の活物質を含む第2の電極と、を接触させて、前記第1の電極および第2の電極の少なくとも一方を加熱または冷却することで、前記第1の電極と前記第2の電極との間に温度差を発生させて、各電極における酸化還元反応および電解質中のアルカリ金属イオンの移動による熱起電力を発生させることを特徴とする酸化還元反応を利用した熱電変換方法。
- 導電性の基板の表面に、前記活物質としてのシアノ架橋金属錯体が、成膜されて作成された前記第1の電極及び第2の電極を使用する
ことを特徴とする請求項1に記載の酸化還元反応を利用した熱電変換方法。 - 前記第1の電極および第2の電極は、インジウムスズ酸化物の基板表面にシアノ架橋金属錯体が成膜されて作成された
ことを特徴とする請求項2に記載の酸化還元反応を利用した熱電変換方法。 - 前記活物質としてのコバルト酸リチウムにより構成された前記第1の電極及び第2の電極を使用する
ことを特徴とする請求項1に記載の酸化還元反応を利用した熱電変換方法。 - リチウム欠損を引き起こした前記第1の電極及び第2の電極を使用する
ことを特徴とする請求項4に記載の酸化還元反応を利用した熱電変換方法。 - 前記活物質としての炭素により構成された前記第1の電極及び第2の電極を使用する
ことを特徴とする請求項1に記載の酸化還元反応を利用した熱電変換方法。 - リチウム導入した前記第1の電極及び第2の電極を使用する
ことを特徴とする請求項6に記載の酸化還元反応を利用した熱電変換方法。 - 前記第1の電極および第2の電極のいずれか一方を、太陽熱により加熱する
ことを特徴とする請求項1に記載の酸化還元反応を利用した熱電変換方法。 - 前記第1の電極、第2の電極および前記電解質とを有する層状の構成を、一方の層状の構成の第1の電極と、他方の層状の構成の第2の電極とが隣り合うように積層し、積層された最も外側の第1の電極と、最も外側の第2の電極との間に温度差を発生させることを特徴とする請求項1に記載の酸化還元反応を利用した熱電変換方法。
- 前記第1の電極、第2の電極および前記電解質とを有する構成を、複数有し、一方の第1の電極を、他方の第2の電極に直列に接続したことを特徴とする請求項1に記載の酸化還元反応を利用した熱電変換方法。
- アルカリ金属イオンを含む電解質と、
電子の受け渡しを行う活物質を含む第1の電極であって、前記電解質に接触する前記第1の電極と、
前記第1の電極と同一の活物質を含み且つ前記電解質に接触する第2の電極と、
前記第1の電極および前記第2の電極の少なくとも一方に設けられ、加熱または冷却される被温冷部と、
を備え、
前記第1の電極と前記第2の電極との間に発生した温度差に応じて、各電極における酸化還元反応および電解質中のアルカリ金属イオンの移動により熱起電力を発生させる
ことを特徴とする酸化還元反応を利用した熱電変換素子。 - 導電性の基板の表面に、前記活物質としてのシアノ架橋金属錯体が、成膜されて作成された前記第1の電極および第2の電極、
を備えたことを特徴とする請求項11に記載の酸化還元反応を利用した熱電変換素子。 - インジウムスズ酸化物により構成された前記基板を有する前記第1の電極および第2の電極、
を備えたことを特徴とする請求項12に記載の酸化還元反応を利用した熱電変換素子。 - 前記活物質としてのコバルト酸リチウムにより構成された前記第1の電極及び第2の電極、
を備えたことを特徴とする請求項11に記載の酸化還元反応を利用した熱電変換素子。 - リチウム欠損を引き起こした前記第1の電極及び第2の電極、
を備えたことを特徴とする請求項14に記載の酸化還元反応を利用した熱電変換素子。 - 前記活物質としての炭素により構成された前記第1の電極及び第2の電極、
を備えたことを特徴とする請求項11に記載の酸化還元反応を利用した熱電変換素子。 - リチウム導入した前記第1の電極及び第2の電極、
を備えたことを特徴とする請求項16に記載の酸化還元反応を利用した熱電変換素子。 - 太陽熱により加熱される前記被温冷部、
を備えたことを特徴とする請求項11に記載の酸化還元反応を利用した熱電変換素子。 - 前記第1の電極、第2の電極および前記電解質とを有する層状の構成を、一方の層状の構成の第1の電極と、他方の層状の構成の第2の電極とが隣り合うように積層され、
前記被温冷部が、積層された最も外側の第1の電極および最も外側の第2の電極の少なくとも一方に設けられた
ことを特徴とする請求項11に記載の酸化還元反応を利用した熱電変換素子。 - 前記第1の電極、第2の電極および前記電解質とを有する構成を、複数有し、
一方の第1の電極が、他方の第2の電極に直列に接続された
ことを特徴とする請求項11に記載の酸化還元反応を利用した熱電変換素子。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013509779A JP5988172B2 (ja) | 2011-04-12 | 2012-04-05 | 酸化還元反応を利用した熱電変換方法および熱電変換素子 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011088683 | 2011-04-12 | ||
| JP2011-088683 | 2011-04-12 | ||
| JP2011220060 | 2011-10-04 | ||
| JP2011-220060 | 2011-10-04 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012140856A1 true WO2012140856A1 (ja) | 2012-10-18 |
Family
ID=47009051
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2012/002391 WO2012140856A1 (ja) | 2011-04-12 | 2012-04-05 | 酸化還元反応を利用した熱電変換方法および熱電変換素子 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP5988172B2 (ja) |
| WO (1) | WO2012140856A1 (ja) |
Cited By (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015160151A1 (ko) * | 2014-04-17 | 2015-10-22 | 부산대학교 산학협력단 | 열전 장치 및 이를 포함하는 열전 시스템 |
| WO2015160150A1 (ko) * | 2014-04-17 | 2015-10-22 | 부산대학교 산학협력단 | 열전 장치용 전해질 용액 및 이를 포함하는 열전 장치 |
| KR20150120284A (ko) * | 2014-04-17 | 2015-10-27 | 부산대학교 산학협력단 | 열전 장치용 전해질 용액 및 이를 포함하는 열전 장치 |
| WO2017038988A1 (ja) * | 2015-09-04 | 2017-03-09 | 国立大学法人東京工業大学 | 熱電発電素子及びそれを含む熱電発電モジュール、並びにそれを用いた熱電発電方法 |
| KR101747165B1 (ko) * | 2015-10-12 | 2017-06-14 | 부산대학교 산학협력단 | 열전기화학 전지 시스템 |
| KR101755228B1 (ko) * | 2015-09-11 | 2017-07-07 | 부산대학교 산학협력단 | 열전기화학 전지 시스템 |
| JP2018073596A (ja) * | 2016-10-28 | 2018-05-10 | 国立大学法人 筑波大学 | 熱発電素子 |
| WO2020031992A1 (ja) * | 2018-08-06 | 2020-02-13 | 国立大学法人東京工業大学 | 熱利用発電池、及びそれを用いた熱利用発電方法 |
| WO2020262171A1 (ja) * | 2019-06-26 | 2020-12-30 | 三桜工業株式会社 | 熱利用発電モジュール |
| WO2020262165A1 (ja) * | 2019-06-26 | 2020-12-30 | 三桜工業株式会社 | 熱利用発電モジュール |
| WO2020262164A1 (ja) * | 2019-06-26 | 2020-12-30 | 三桜工業株式会社 | 熱利用発電モジュール及びそれを備える熱発電装置 |
| CN112713233A (zh) * | 2019-10-25 | 2021-04-27 | 南方科技大学 | 准固态离子型热电转换材料、热电转换器件及其应用 |
| CN113388845A (zh) * | 2021-06-11 | 2021-09-14 | 四川大学 | 微生物-光电化学-热电化学耦合产氢系统 |
| EP3818585A4 (en) * | 2018-07-06 | 2022-03-30 | The Government of the United States of America, as represented by the Secretary of the Navy | INTERNAL BATTERY SHORT CIRCUIT TRIGGER AND METHOD FOR ENHANCED PERFORMANCE |
| US11346103B2 (en) * | 2018-10-18 | 2022-05-31 | Arizona Board Of Regents On Behalf Of Arizona State University | Systems and methods for a power-generating thermogalvanic brick |
| WO2022191101A1 (ja) * | 2021-03-08 | 2022-09-15 | 国立大学法人東京工業大学 | 熱電発電素子、熱電発電池、及び発電の安定化方法 |
| WO2022239856A1 (ja) * | 2021-05-14 | 2022-11-17 | 国立大学法人東京工業大学 | 熱電変換装置及びコバルト金属錯体 |
| EP3993255A4 (en) * | 2019-06-26 | 2023-08-23 | Sanoh Industrial Co., Ltd. | METHOD OF THERMOELECTRIC GENERATION |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20230004984A (ko) * | 2021-06-30 | 2023-01-09 | 포항공과대학교 산학협력단 | 열전기화학 전지 시스템 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS60243979A (ja) * | 1984-05-18 | 1985-12-03 | Toho Rayon Co Ltd | 温度差電池 |
| JPH05144483A (ja) * | 1991-11-19 | 1993-06-11 | Nippon Telegr & Teleph Corp <Ntt> | 温度差電池 |
| JPH09259944A (ja) * | 1996-03-22 | 1997-10-03 | Nippon Telegr & Teleph Corp <Ntt> | 温度差電池 |
| WO2001071821A1 (en) * | 2000-03-24 | 2001-09-27 | Shin-Etsu Chemical Co., Ltd. | Thermoelectric power generator |
| JP2010114349A (ja) * | 2008-11-10 | 2010-05-20 | Konica Minolta Holdings Inc | 複合発電装置 |
-
2012
- 2012-04-05 WO PCT/JP2012/002391 patent/WO2012140856A1/ja active Application Filing
- 2012-04-05 JP JP2013509779A patent/JP5988172B2/ja active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS60243979A (ja) * | 1984-05-18 | 1985-12-03 | Toho Rayon Co Ltd | 温度差電池 |
| JPH05144483A (ja) * | 1991-11-19 | 1993-06-11 | Nippon Telegr & Teleph Corp <Ntt> | 温度差電池 |
| JPH09259944A (ja) * | 1996-03-22 | 1997-10-03 | Nippon Telegr & Teleph Corp <Ntt> | 温度差電池 |
| WO2001071821A1 (en) * | 2000-03-24 | 2001-09-27 | Shin-Etsu Chemical Co., Ltd. | Thermoelectric power generator |
| JP2010114349A (ja) * | 2008-11-10 | 2010-05-20 | Konica Minolta Holdings Inc | 複合発電装置 |
Non-Patent Citations (1)
| Title |
|---|
| TERUKI MOTOHASHI ET AL.: "Sojo Cobalt Sankabutsu LixCo02(4): Netsuden Henkan Tokusei to Denshi Kozo", DAI 57 KAI EXTENDED ABSTRACTS, March 2010 (2010-03-01), pages 09 - 075 * |
Cited By (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015160150A1 (ko) * | 2014-04-17 | 2015-10-22 | 부산대학교 산학협력단 | 열전 장치용 전해질 용액 및 이를 포함하는 열전 장치 |
| KR20150120284A (ko) * | 2014-04-17 | 2015-10-27 | 부산대학교 산학협력단 | 열전 장치용 전해질 용액 및 이를 포함하는 열전 장치 |
| KR101574012B1 (ko) | 2014-04-17 | 2015-12-02 | 부산대학교 산학협력단 | 열전 장치 및 이를 포함하는 열전 시스템 |
| KR101691946B1 (ko) * | 2014-04-17 | 2017-01-02 | 부산대학교 산학협력단 | 열전 장치용 전해질 용액 및 이를 포함하는 열전 장치 |
| US20170062689A1 (en) * | 2014-04-17 | 2017-03-02 | Pusan National University Industry-University Cooperration Foundation | Thermoelectric device and thermoelectric system including the device |
| WO2015160151A1 (ko) * | 2014-04-17 | 2015-10-22 | 부산대학교 산학협력단 | 열전 장치 및 이를 포함하는 열전 시스템 |
| US10305013B2 (en) | 2014-04-17 | 2019-05-28 | Pusan National University Industry University Cooperation Foundation Of Pusan | Electrolyte solution for thermoelectric device and thermoelectric device including the electrolyte solution |
| JPWO2017038988A1 (ja) * | 2015-09-04 | 2018-06-21 | 国立大学法人東京工業大学 | 熱電発電素子及びそれを含む熱電発電モジュール、並びにそれを用いた熱電発電方法 |
| WO2017038988A1 (ja) * | 2015-09-04 | 2017-03-09 | 国立大学法人東京工業大学 | 熱電発電素子及びそれを含む熱電発電モジュール、並びにそれを用いた熱電発電方法 |
| KR101755228B1 (ko) * | 2015-09-11 | 2017-07-07 | 부산대학교 산학협력단 | 열전기화학 전지 시스템 |
| KR101747165B1 (ko) * | 2015-10-12 | 2017-06-14 | 부산대학교 산학협력단 | 열전기화학 전지 시스템 |
| JP2018073596A (ja) * | 2016-10-28 | 2018-05-10 | 国立大学法人 筑波大学 | 熱発電素子 |
| EP3818585A4 (en) * | 2018-07-06 | 2022-03-30 | The Government of the United States of America, as represented by the Secretary of the Navy | INTERNAL BATTERY SHORT CIRCUIT TRIGGER AND METHOD FOR ENHANCED PERFORMANCE |
| JPWO2020031992A1 (ja) * | 2018-08-06 | 2021-08-12 | 国立大学法人東京工業大学 | 熱利用発電池、及びそれを用いた熱利用発電方法 |
| WO2020031992A1 (ja) * | 2018-08-06 | 2020-02-13 | 国立大学法人東京工業大学 | 熱利用発電池、及びそれを用いた熱利用発電方法 |
| US11758814B2 (en) | 2018-08-06 | 2023-09-12 | Tokyo Institute Of Technology | Heat-utilizing power generation battery and heat-utilizing power generation method using same |
| JP7329517B2 (ja) | 2018-08-06 | 2023-08-18 | 国立大学法人東京工業大学 | 熱利用発電池、及びそれを用いた熱利用発電方法 |
| TWI803679B (zh) * | 2018-08-06 | 2023-06-01 | 國立大學法人東京工業大學 | 熱力發電電池,及使用此之熱力發電方法 |
| US11346103B2 (en) * | 2018-10-18 | 2022-05-31 | Arizona Board Of Regents On Behalf Of Arizona State University | Systems and methods for a power-generating thermogalvanic brick |
| JP2021005650A (ja) * | 2019-06-26 | 2021-01-14 | 三桜工業株式会社 | 熱利用発電モジュール |
| WO2020262165A1 (ja) * | 2019-06-26 | 2020-12-30 | 三桜工業株式会社 | 熱利用発電モジュール |
| WO2020262171A1 (ja) * | 2019-06-26 | 2020-12-30 | 三桜工業株式会社 | 熱利用発電モジュール |
| JP2021005651A (ja) * | 2019-06-26 | 2021-01-14 | 三桜工業株式会社 | 熱利用発電モジュール |
| JP2021005649A (ja) * | 2019-06-26 | 2021-01-14 | 三桜工業株式会社 | 熱利用発電モジュール及びそれを備える熱発電装置 |
| EP3993255A4 (en) * | 2019-06-26 | 2023-08-23 | Sanoh Industrial Co., Ltd. | METHOD OF THERMOELECTRIC GENERATION |
| US20220359805A1 (en) * | 2019-06-26 | 2022-11-10 | Sanoh Industrial Co., Ltd. | Heat-utilizing power generation module and thermal power generation device equipped with same |
| EP3968392A4 (en) * | 2019-06-26 | 2023-07-12 | Sanoh Industrial Co., Ltd. | HEAT-USED POWER GENERATION MODULE AND THERMAL ENERGY GENERATION DEVICE EQUIPPED THEREOF |
| WO2020262164A1 (ja) * | 2019-06-26 | 2020-12-30 | 三桜工業株式会社 | 熱利用発電モジュール及びそれを備える熱発電装置 |
| CN112713233A (zh) * | 2019-10-25 | 2021-04-27 | 南方科技大学 | 准固态离子型热电转换材料、热电转换器件及其应用 |
| CN112713233B (zh) * | 2019-10-25 | 2023-09-26 | 南方科技大学 | 准固态离子型热电转换材料、热电转换器件及其应用 |
| WO2022191101A1 (ja) * | 2021-03-08 | 2022-09-15 | 国立大学法人東京工業大学 | 熱電発電素子、熱電発電池、及び発電の安定化方法 |
| WO2022239856A1 (ja) * | 2021-05-14 | 2022-11-17 | 国立大学法人東京工業大学 | 熱電変換装置及びコバルト金属錯体 |
| CN113388845A (zh) * | 2021-06-11 | 2021-09-14 | 四川大学 | 微生物-光电化学-热电化学耦合产氢系统 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2012140856A1 (ja) | 2014-07-28 |
| JP5988172B2 (ja) | 2016-09-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5988172B2 (ja) | 酸化還元反応を利用した熱電変換方法および熱電変換素子 | |
| Gao et al. | Thermally regenerative electrochemical cycle for low-grade heat harvesting | |
| Ding et al. | Simultaneous energy harvesting and storage via solar-driven regenerative electrochemical cycles | |
| Dupont et al. | Thermo-electrochemical cells for waste heat harvesting–progress and perspectives | |
| Reed et al. | Performance of Nafion® N115, Nafion® NR-212, and Nafion® NR-211 in a 1 kW class all vanadium mixed acid redox flow battery | |
| JP6803076B2 (ja) | 熱電発電素子及びそれを含む熱電発電モジュール、並びにそれを用いた熱電発電方法 | |
| Poletayev et al. | Continuous electrochemical heat engines | |
| Li et al. | 3D Hierarchical Electrodes Boosting Ultrahigh Power Output for Gelatin‐KCl‐FeCN4−/3− Ionic Thermoelectric Cells | |
| Cheng et al. | Insights into the thermopower of thermally regenerative electrochemical cycle for low grade heat harvesting | |
| Zhang et al. | Copper foam electrodes for increased power generation in thermally regenerative ammonia-based batteries for low-grade waste heat recovery | |
| Li et al. | Design principles and developments of integrated solar flow batteries | |
| Cheng et al. | Review of liquid-based systems to recover low-grade waste heat for electrical energy generation | |
| Kazim et al. | Thermo-electrochemical generator: energy harvesting & thermoregulation for liquid cooling applications | |
| Feng et al. | Advances and challenges in photoelectrochemical redox batteries for solar energy conversion and storage | |
| Li et al. | Thermocells-enabled low-grade heat harvesting: challenge, progress, and prospects | |
| Li et al. | Continuous thermally regenerative electrochemical systems for directly converting low-grade heat to electricity | |
| Zhang et al. | Efficient Low‐Grade Heat Conversion and Storage with an Activity‐Regulated Redox Flow Cell via a Thermally Regenerative Electrochemical Cycle | |
| Heo et al. | Performance of an intermediate-temperature fuel cell using a proton-conducting Sn0. 9In0. 1P2O7 electrolyte | |
| Mu et al. | Direct thermal charging cell using nickel hexacyanoferrate (ΙΙ) anode for green recycling of low-grade heat | |
| Vassel et al. | Electrochemical way of converting low-grade heat energy into electricity based on crystalline hydrate melting and crystallization | |
| Zhang et al. | Continuous electricity generation from solar heat and darkness | |
| Ye et al. | Micro-tubular solid oxide fuel cells and their stacks running on direct ethanol fuels | |
| WO2020121799A1 (ja) | 熱電池 | |
| JP6908256B2 (ja) | 熱発電素子 | |
| JP2014216059A (ja) | 酸化グラフェンを固体電解質とする二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 12772018 Country of ref document: EP Kind code of ref document: A1 |
|
| DPE1 | Request for preliminary examination filed after expiration of 19th month from priority date (pct application filed from 20040101) | ||
| ENP | Entry into the national phase |
Ref document number: 2013509779 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 12772018 Country of ref document: EP Kind code of ref document: A1 |