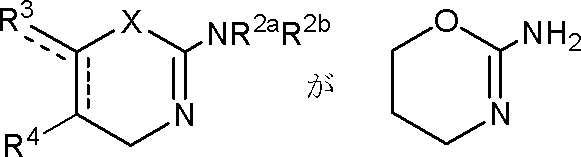WO2011058763A1 - アミノリンカーを有するアミノチアジンまたはアミノオキサジン誘導体 - Google Patents
アミノリンカーを有するアミノチアジンまたはアミノオキサジン誘導体 Download PDFInfo
- Publication number
- WO2011058763A1 WO2011058763A1 PCT/JP2010/006680 JP2010006680W WO2011058763A1 WO 2011058763 A1 WO2011058763 A1 WO 2011058763A1 JP 2010006680 W JP2010006680 W JP 2010006680W WO 2011058763 A1 WO2011058763 A1 WO 2011058763A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- substituted
- unsubstituted
- group
- carbocyclic
- ring
- Prior art date
Links
- 0 *N(*)IC1=CC=CC=CC=CC=C1 Chemical compound *N(*)IC1=CC=CC=CC=CC=C1 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
- A61K9/1623—Sugars or sugar alcohols, e.g. lactose; Derivatives thereof; Homeopathic globules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D279/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one sulfur atom as the only ring hetero atoms
- C07D279/04—1,3-Thiazines; Hydrogenated 1,3-thiazines
- C07D279/06—1,3-Thiazines; Hydrogenated 1,3-thiazines not condensed with other rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Definitions
- the present invention relates to a compound having an inhibitory effect on amyloid ⁇ production and useful as a therapeutic agent for diseases induced by production, secretion and / or deposition of amyloid ⁇ protein.
- Alzheimer's disease In the brain of Alzheimer's disease patients, insoluble spots (senile plaques) in which a peptide consisting of about 40 amino acids called amyloid ⁇ protein accumulates outside the nerve cells are widely observed. It is thought that Alzheimer's disease develops when this senile plaque kills nerve cells, and amyloid ⁇ protein degradation accelerators, amyloid ⁇ vaccines, and the like have been studied as therapeutic agents for Alzheimer's disease.
- Secretase is an enzyme that cleaves a protein called amyloid ⁇ precursor protein (APP) in cells to produce amyloid ⁇ protein.
- the enzyme responsible for the N-terminal generation of amyloid ⁇ protein is called ⁇ -site APP-cleaving enzyme 1, BACE1, and inhibiting this enzyme suppresses amyloid ⁇ protein production and treats Alzheimer's disease It can be considered as an agent.
- Patent Document 5 describes a compound having a structure similar to that of the present invention, but describes that it is useful as a dye.
- Patent Documents 1 to 4, 6, 7 and the like are known as BACE1 inhibitors, all of which have a skeleton different from the compound of the present invention.
- amyloid ⁇ production inhibitory action particularly a BACE1 inhibitory action
- R 1 is substituted or unsubstituted alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, substituted or unsubstituted acyl, cyano, carboxy, substituted or unsubstituted alkoxycarbonyl, substituted or unsubstituted Substituted alkenyloxycarbonyl, substituted or unsubstituted alkynyloxycarbonyl, substituted or unsubstituted carbamoyl, substituted or unsubstituted thiocarbamoyl, substituted or unsubstituted carbocyclic group or substituted or unsubstituted heterocyclic group Yes, R 2a and R 2b are each independently hydrogen, substituted or unsubstituted alkyl, substituted or unsubstituted acyl, substituted or unsubstituted alk
- R 1 is substituted or unsubstituted alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, cyano, substituted or unsubstituted carbocyclic group or substituted or unsubstituted heterocyclic group.
- R 2a and R 2b are each independently hydrogen, substituted or unsubstituted alkyl or substituted or unsubstituted acyl;
- X is S or O; When X is S,
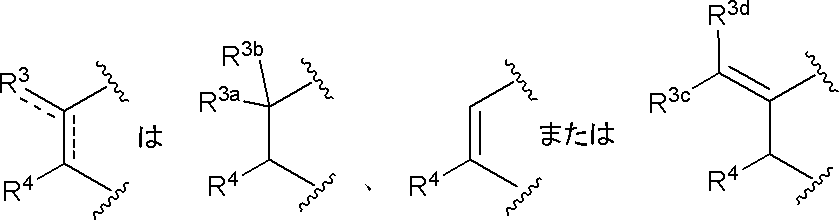
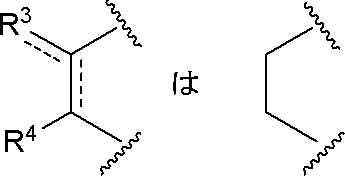
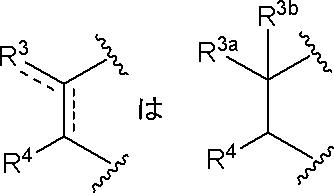
- R 3a and R 3b are each independently hydrogen, halogen, hydroxy, substituted or unsubstituted alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, substituted or unsubstituted acyl, substituted or unsubstituted alkoxy Substituted or unsubstituted arylalkyl, substituted or unsubstituted heteroarylalkyl, substituted or unsubstituted arylalkoxy, substituted or unsubstituted heteroarylalkoxy, substituted or unsubstituted alkylthio, carboxy, cyano, substituted or unsubstituted Alkoxycarbonyl, substituted or unsubstituted amino, substituted or unsubstituted carbamoyl, substituted or unsubstituted carbocyclic group or substituted or unsubstituted heterocyclic group, R 3c and R 3d are
- Ring B is a substituted or unsubstituted carbocycle, substituted or unsubstituted pyridine, substituted or unsubstituted pyrimidine or substituted or unsubstituted 5-membered heterocyclic ring; 2) L 3 is a single bond,
- Ring B is a substituted or unsubstituted carbocyclic ring or a substituted or unsubstituted heterocyclic ring, 3)
- L 3 is substituted or unsubstituted alkylene, substituted or unsubstituted alkenylene or substituted or unsubstituted alkynylene, Ring B is a substituted nitrogen-containing aromatic monocycle) Or a pharmaceutically acceptable salt thereof or a solvate thereof.
- R 3a is hydrogen, substituted or unsubstituted alkyl, cyano, substituted or unsubstituted alkoxycarbonyl, substituted or unsubstituted carbamoyl, substituted or unsubstituted carbocyclic group, or substituted or unsubstituted heterocyclic Or a pharmaceutically acceptable salt thereof according to any one of items (1), (1 ′) and (2) to (4), wherein R 3b , R 4a and R 4b are hydrogen Or a solvate thereof.
- composition according to item (10) or (11) which is a medicament for the treatment of a disease induced by production, secretion or deposition of amyloid ⁇ protein.
- a compound or a pharmaceutically acceptable salt thereof or a solvate thereof according to any one of items (1), (1 ′) and (2) to (9) is administered. , How to treat Alzheimer's disease.
- a pharmaceutical composition comprising the compound according to any one of items (1), (1 ′) and (2) to (9), a pharmaceutically acceptable salt thereof, or a solvate thereof. Preparation methods, systems, devices, kits, etc.
- the compound of the present invention is useful as a therapeutic agent for diseases (such as Alzheimer's disease) induced by production, secretion or deposition of amyloid ⁇ protein.
- halogen includes fluorine, chlorine, bromine and iodine.
- alkyl refers to a linear or branched alkyl having 1 to 15 carbon atoms, such as 1 to 10 carbon atoms, such as 1 to 6 carbon atoms, such as 1 to 3 carbon atoms.
- alkoxy “halogenoalkyl”, “hydroxyalkyl”, “halogenoalkoxy”, “hydroxyalkoxy”, “alkoxycarbonyl”, “halogenoalkoxycarbonyl”, “alkoxycarbonylalkyl”, “alkylamino” , “Alkoxyalkyl”, “hydroxyiminoalkyl”, “alkoxyiminoalkyl”, “aminoalkyl”, “alkoxyalkoxy”, “alkoxyalkenyl”, “alkoxyalkenyloxy”, “alkoxycarbonylalkenyl”, “alkoxyalkynyl”, “Alkoxycarbonylalkynyl”, “alkylcarbamoyl”, “hydroxyalkylcarbamoyl”, “alkoxyimino”, “alkylthio”, “alkylsulfonyl”, “alkylsulfuryl” Nyloxy, alkylsulfonylamino, alkyl
- substituted or unsubstituted alkyl may be substituted with one or more groups selected from the substituent group ⁇ .
- the substituent group ⁇ is halogen, hydroxy, alkoxy, halogenoalkoxy, hydroxyalkoxy, alkoxyalkoxy, acyl, acyloxy, carboxy, alkoxycarbonyl, amino, acylamino, alkylamino, imino, hydroxyimino, alkoxyimino, alkylthio, Carbamoyl, alkylcarbamoyl, hydroxyalkylcarbamoyl, sulfamoyl, alkylsulfamoyl, alkylsulfinyl, alkylsulfonylamino, alkylsulfonylalkylamino, alkylsulfonylimino, alkylsulfinylamino, alkylsulfinylalkylamino, alkylsulfinylimino, cyano, nitro, carbon Cyclic and heterocyclic groups (where each carbo,
- substituted or unsubstituted alkoxy “substituted or unsubstituted alkoxycarbonyl”, “substituted or unsubstituted alkylthio”, “substituted or unsubstituted alkylsulfinyl”, and “substituted or unsubstituted”
- substituent of “alkylsulfonyl” include one or more groups selected from the above substituent group ⁇ .
- halogenoalkyl examples include trifluoromethyl, fluoromethyl, trichloromethyl and the like.
- alkylidene includes the above-mentioned divalent group of “alkyl” and includes, for example, methylidene, ethylidene, propylidene, isopropylidene, butylidene, pentylidene, hexylidene and the like.
- alkenyl means 2 to 15 carbon atoms having one or more double bonds at any position, for example, 2 to 10 carbon atoms, for example, 2 to 6 carbon atoms, for example, 2 carbon atoms. Includes up to 4 linear or branched alkenyl.
- alkynyl is a straight chain or branched chain having 2 to 10 carbon atoms, for example, 2 to 8 carbon atoms, for example 3 to 6 carbon atoms, having one or more triple bonds at any position.
- alkynyl Specifically, ethynyl, propynyl, butynyl, pentynyl, hexynyl, heptynyl, octynyl, nonynyl, decynyl and the like are included. These may further have a double bond at an arbitrary position.
- hydroxyalkenyl “alkoxyalkenyl”, “alkoxycarbonylalkenyl”, “carbocyclic alkenyl”, “alkenyloxy”, “alkenyloxycarbonyl”, “alkoxyalkenyloxy”, “alkenylthio”, “ The alkenyl part of “alkenylsulfinyl”, “alkenylsulfonyl” and “alkenylamino” is the same as the above “alkenyl”.
- alkynyl In the present specification, “hydroxyalkynyl”, “alkoxyalkynyl”, “alkoxycarbonylalkynyl”, “carbocyclic alkynyl”, “alkynyloxy”, “alkynyloxycarbonyl”, “alkoxyalkynyloxy”, “alkynylthio”, “ The alkynyl moiety of “alkynylsulfinyl”, “alkynylsulfonyl” and “alkynylamino” is the same as the above “alkynyl”.
- substituents of “substituted or unsubstituted amino”, “substituted or unsubstituted carbamoyl”, “substituted or unsubstituted thiocarbamoyl” and “substituted or unsubstituted sulfamoyl” include alkyl, acyl 1 to 2 groups selected from hydroxy, alkoxy, alkoxycarbonyl, carbocyclic group, heterocyclic group and the like.
- acyl includes aliphatic acyl having 1 to 10 carbon atoms, carbocyclic carbonyl and heterocyclic carbonyl. Specifically, formyl, acetyl, propionyl, butyryl, isobutyryl, valeryl, pivaloyl, hexanoyl, acryloyl, propioroyl, methacryloyl, crotonoyl, benzoyl, cyclohexanecarbonyl, pyridinecarbonyl, furancarbonyl, thiophenecarbonyl, benzothiazolecarbonyl, pyrazinecarbonyl, Examples include piperidine carbonyl and thiomorpholino.
- acyl part of “acyloxy” is the same as the above “acyl”.
- examples of the substituent of “substituted or unsubstituted acyl” and “substituted or unsubstituted acyloxy” include one or more groups selected from the substituent group ⁇ .
- the ring portion of carbocyclic carbonyl and heterocyclic carbonyl is substituted with one or more groups selected from alkyl, substituent group ⁇ , and alkyl substituted with one or more groups selected from substituent group ⁇ . It may be.
- “carbocyclic group” includes cycloalkyl, cycloalkenyl, aryl, non-aromatic fused carbocyclic group and the like.
- cycloalkyl is a carbocyclic group having 3 to 10, for example, 3 to 8, for example, 4 to 8 carbon atoms, such as cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, Includes cycloheptyl, cyclooctyl, cyclononyl, cyclodecyl and the like.
- cycloalkylalkyl In the present specification, “cycloalkylalkyl”, “cycloalkyloxy”, “cycloalkylalkoxy”, “cycloalkylthio”, “cycloalkylamino”, “cycloalkylalkylamino”, “cycloalkylsulfamoyl”, “ The cycloalkyl part of “cycloalkylsulfonyl”, “cycloalkylcarbamoyl”, “cycloalkylalkylcarbamoyl”, “cycloalkylalkoxycarbonyl” and “cycloalkyloxycarbonyl” is the same as the above “cycloalkyl”.
- cycloalkenyl includes those having one or more double bonds at any position in the ring of the cycloalkyl, specifically, cyclopropenyl, cyclobutenyl, cyclopentenyl. , Cyclohexenyl, cycloheptynyl, cyclooctynyl, cyclohexadienyl and the like.
- aryl includes phenyl, naphthyl, anthryl, phenanthryl and the like, and particularly includes phenyl.
- non-aromatic fused carbocyclic group means a non-aromatic group in which two or more cyclic groups selected from the above “cycloalkyl”, “cycloalkenyl” and “aryl” are condensed. Specific examples include indanyl, indenyl, tetrahydronaphthyl and fluorenyl.
- to form a substituted or unsubstituted carbocycle together with carbon atoms to be bonded means that two substituents together form the above “carbocycle”.
- to form a substituted or unsubstituted non-aromatic carbocycle together with a carbon atom to be bonded means that two substituents together form the above “cycloalkyl” or “cycloalkenyl”. Is formed.
- the carbocyclic part of “carbocyclic oxycarbonyl” is the same as “carbocyclic group”.
- arylalkyl In the present specification, “arylalkyl”, “aryloxy”, “aryloxycarbonyl”, “arylalkoxycarbonyl”, “arylthio”, “arylamino”, “arylalkoxy”, “arylalkylamino”, “arylsulfonyl”
- aryl part of “arylsulfamoyl”, “arylcarbamoyl” and “arylalkylcarbamoyl” is the same as the above “aryl”.
- the “heterocyclic group” includes a heterocyclic group having one or more hetero atoms arbitrarily selected from O, S and N in the ring, specifically, pyrrolyl, imidazolyl, 5- to 6-membered heteroaryl such as pyrazolyl, pyridyl, pyridazinyl, pyrimidinyl, pyrazinyl, triazolyl, triazinyl, tetrazolyl, furyl, thienyl, isoxazolyl, oxazolyl, oxadiazolyl, isothiazolyl, thiazolyl, thiadiazolyl; , Azetidinyl, thianyl, thiazolidinyl, pyrrolidinyl, pyrrolinyl, imidazolidinyl, imidazolinyl, pyrazolidinyl, pyrazolinyl, piperidyl, piperazinyl
- heterocycle “heterocycle alkyl”, “heterocycle oxy”, “heterocycle thio”, “heterocycle carbonyl”, “heterocycle alkoxy”, “heterocycle amino”, “heterocycle sulfamoyl” , “Heterocyclic sulfinyl”, “heterocyclic sulfonyl”, “heterocyclic carbamoyl”, “heterocyclic oxycarbonyl”, “heterocyclic alkylamino", “heterocyclic alkoxycarbonyl” and “heterocyclic alkylcarbamoyl”
- the moiety is also the same as the above “heterocyclic group”.
- the bond of the above “heterocyclic group” may be located on any ring.
- heteroaryl includes those of the above “heterocyclic group” which are aromatic cyclic groups. The same applies to the heteroaryl part of “heteroarylalkyl” and “heteroarylalkoxy”.
- non-aromatic heterocycle includes non-aromatic heterocycles among the above “heterocyclic groups”.
- “to form a substituted or unsubstituted heterocycle together with carbon atoms to be bonded” means that two substituents together form the above “heterocycle”.
- “to form a substituted or unsubstituted non-aromatic heterocycle together with a carbon atom to be bonded” means that two substituents together form the above “non-aromatic heterocycle”. It means forming.
- heterocyclic heterocycle includes those in which the heterocyclic moiety is a 5-membered ring among the above-mentioned “heterocyclic groups”.
- heterocyclic groups include pyrrole, imidazole, pyrazole, tetrazole, furan, thiophene, isoxazole, oxazole, oxadiazole, isothiazole, thiazole, thiadiazole, thiazolidine, pyrrolidine, pyrroline, imidazolidine, imidazoline, pyrazolidine, pyrazoline, tetrahydrofuran, dihydrothiazole, tetrahydro Thiazole, tetrahydroisothiazole and the like.
- the “nitrogen-containing aromatic monocycle” includes those in which the heterocyclic moiety is a monocyclic heterocycle containing at least one nitrogen among the above “heterocyclic groups”.
- the heterocyclic moiety is a monocyclic heterocycle containing at least one nitrogen among the above “heterocyclic groups”.
- substituents of “substituted or unsubstituted pyrimidine”, “substituted or unsubstituted 5-membered heterocycle” and “substituted nitrogen-containing aromatic monocycle” A group selected from the substituent group ⁇ (for example, halogen, hydroxy, acyl, acyloxy, carboxy, alkoxycarbonyl, carbamoyl, amino, cyano, alkylamino and / or alkylthio, etc.); Alkyl substituted with one or more groups selected from the group consisting of the substituent group ⁇ , hydroxyimino and alkoxyimino (wherein the substituent is, for example, halogen, hydroxy,
- substituent of “substituted or unsubstituted pyrimidine”, “substituted or unsubstituted 5-membered heterocycle” and “substituted nitrogen-containing aromatic monocycle” include, for example, halogen, cyano, hydroxy, nitro, carboxy, Alkyl substituted with one or more groups selected from substituent group ⁇ , unsubstituted alkyl, alkoxy substituted with one or more groups selected from substituent group ⁇ , unsubstituted alkoxy, selected from substituent group ⁇ Selected from carbamoyl, unsubstituted carbamoyl, and substituent group ⁇ substituted
- substituents include one or more groups selected from the group consisting of alkyl substituted with one or more groups selected from substituent group ⁇ , unsubstituted alkyl, and substituent group ⁇ .
- alkylene includes a linear or branched divalent carbon chain having 1 to 10, for example, 1 to 6, for example, 1 to 3 carbon atoms. Specific examples include methylene, dimethylene, trimethylene, tetramethylene, methyltrimethylene and the like.
- alkylene part of “alkylenedioxy” is the same as the above “alkylene”.
- alkenylene means a linear or branched carbon having 2 to 10 carbon atoms having a double bond at an arbitrary position, for example, 2 to 6 carbon atoms, such as 2 having 2 to 4 carbon atoms. Includes a valent carbon chain. Specific examples include vinylene, propenylene, butenylene, butadienylene, methylpropenylene, pentenylene and hexenylene.
- alkynylene means a linear or branched carbon number of 2 to 10, for example, carbon number, which has a triple bond at an arbitrary position and may further have a double bond. It includes 2 to 6, for example, a divalent carbon chain having 2 to 4 carbon atoms. Specific examples include ethynylene, propynylene, butynylene, pentynylene and hexynylene.
- examples of the substituent of “substituted or unsubstituted alkylene”, “substituted or unsubstituted alkenylene”, and “substituted or unsubstituted alkynylene” include halogen, alkoxy, halogenoalkoxy, hydroxyalkoxy, alkoxyalkoxy, Acyl, acyloxy, carboxy, alkoxycarbonyl, amino, acylamino, alkylamino, imino, hydroxyimino, alkoxyimino, alkylthio, carbamoyl, alkylcarbamoyl, hydroxyalkylcarbamoyl, sulfamoyl, alkylsulfamoyl, alkylsulfamoyl, alkylsulfinyl, alkylsulfonylamino, alkyl Sulfonylalkylamino, alkylsulfonylimino
- the “solvate” includes, for example, solvates and hydrates with an organic solvent, and can be converted into solvates and hydrates by a known method.
- Suitable solvates include solvates with acetone, 2-butanol, 2-propanol, ethanol, ethyl acetate, tetrahydrofuran, diethyl ether and the like.
- non-toxic and water-soluble hydrates or solvates for example, ethanol and the like
- it may be coordinated with any number of solvent molecules or water molecules.
- the compounds represented by formula (I) and formula (I ′) include pharmaceutically acceptable salts.
- alkali metals such as lithium, sodium or potassium
- alkaline earth metals such as calcium
- magnesium transition metals (zinc, iron), ammonium
- salts with organic bases and amino acids or inorganic acids (hydrochloric acid, sulfuric acid, Nitric acid, hydrobromic acid, phosphoric acid or hydroiodic acid) and organic acids (acetic acid, trifluoroacetic acid, citric acid, lactic acid, tartaric acid, oxalic acid, maleic acid, fumaric acid, mandelic acid, glutaric acid, apple Acid, benzoic acid, phthalic acid, benzenesulfonic acid, p-toluenesulfonic acid, methanesulfonic acid or ethanesulfonic acid).
- hydrochloric acid, phosphoric acid, tartaric acid, methanesulfonic acid and the like can be mentioned.
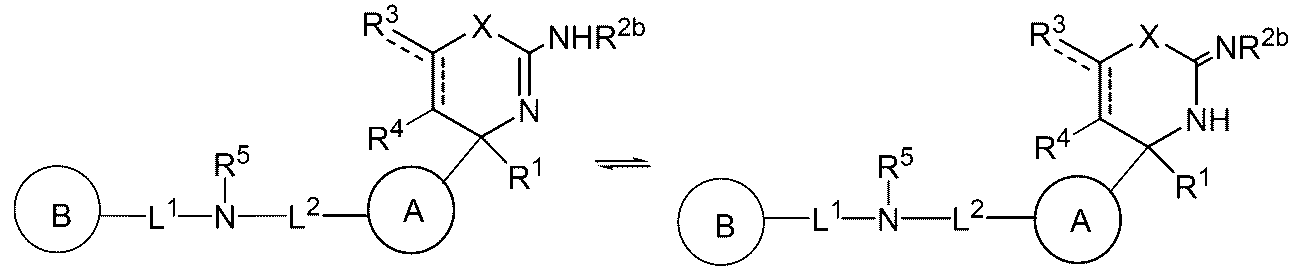
- the compounds represented by the formula (I) and the formula (I ′) are not limited to specific isomers, but all possible isomers (keto-enol isomer, imine-enamine isomer, diastereoisomer) Isomers, optical isomers, rotational isomers, etc.) and racemates.
- the compound represented by the formula (I) in which R 2a is hydrogen includes the following tautomers.
- the compounds represented by formula (I) and formula (I ′) have an asymmetric carbon atom and include any of the following optical isomers. Preferably It is.
- one or more hydrogen, carbon or other atoms of the compounds of formulas (I) and (I ') may be replaced with isotopes of hydrogen, carbon or other atoms.
- Compounds of formula (I) and (I ') include all radiolabeled compounds of compounds of formula (I) and (I'). Such “radiolabeled”, “radiolabeled” and the like of the compounds of formulas (I) and (I ′) are each encompassed by the present invention and are studied and / or diagnosed in metabolic pharmacokinetic studies and binding assays. Useful as a tool. It is also useful as a pharmaceutical product.
- isotopes that can be incorporated into the compounds of formula (I) and (I ′) of the present invention include 2 H, 3 H, 11 C, 13 C, 14 C, 15 N, 18 O, 17 O, Hydrogen, carbon, nitrogen, oxygen, phosphorus, sulfur, fluorine, iodine and chlorine are included, such as 31 P, 32 P, 35 S, 18 F, 123 I and 36 Cl.
- the radiolabeled compound of the present invention can be prepared by methods well known in the art.
- a tritium labeled compound of formula (I) can be prepared by introducing tritium into a specific compound of formula (I) by, for example, catalytic dehalogenation reaction using tritium.
- This method involves reacting a compound of formula (I) with a suitably halogen-substituted precursor and tritium gas in the presence of a suitable catalyst, for example Pd / C, in the presence or absence of a base. It may be included.
- a suitable catalyst for example Pd / C
- the 14C-labeled compound can be prepared by using a raw material having 14C carbon.
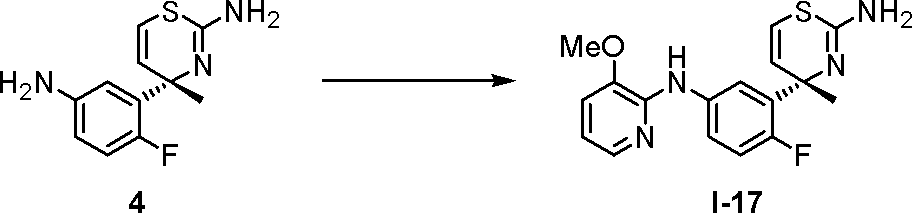
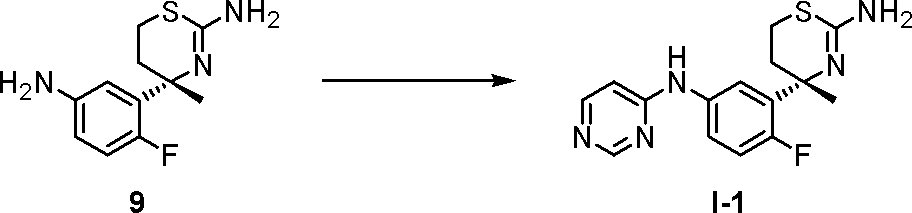
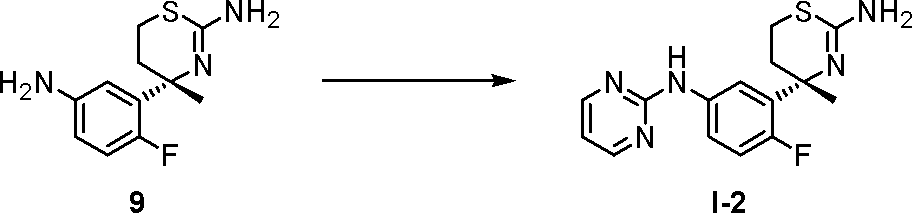
- the compounds of the present invention represented by the formulas (I) and (I ′) are, for example, Patent Document 1 or Journal of Heterocyclic Chemistry, Vol. 14, 717-723 (1977). Or according to the method described below.
- the compound represented by the general formula (a) is a commercially available product, or can be synthesized by a known method (Tetrahedron, 2009, Vol. 65, pages 757 to 764) or a method analogous thereto.
- the compound represented by the general formula (b) is, for example, according to the method described in Patent Document 1 (WO2007 / 049532), Patent Document 2 (WO2008 / 133274), Patent Document 3 (WO2008 / 133273), or described later. Can be produced by a general preparation method.
- Method A Condensation under acidic conditions Compound (a) and Compound (b) are mixed in a solvent such as methanol, ethanol, isopropyl alcohol, butanol, isobutanol, sec-butanol, acetic acid, water, or a mixed solvent thereof. Acids such as hydrochloric acid, sulfuric acid, trifluoroacetic acid, methanesulfonic acid, trifluoromethanesulfonic acid, perchloric acid are added, and the temperature is 0 to 180 ° C, preferably 20 to 140 ° C, preferably 0.1 to 120 hours, preferably Can be reacted for 0.5 to 72 hours to obtain a compound represented by the general formula (I).
- a solvent such as methanol, ethanol, isopropyl alcohol, butanol, isobutanol, sec-butanol, acetic acid, water, or a mixed solvent thereof.
- Acids such as hydrochloric acid, sulfuric acid, triflu
- Method B Condensation under basic conditions Compound (a) and Compound (b) are mixed in a solvent such as toluene, tetrahydrofuran, dimethylformamide, 1,2-dimethoxyethane, 1,4-dioxane, methanol, triethylamine, sodium carbonate.
- a base such as potassium carbonate, cesium carbonate, sodium methoxide, potassium tert-butoxide, n-butyllithium, lithium hexamethyldisilazide, sodium hexamethyldisilazide, potassium hexamethyldisilazide, etc.
- trisdibenzylideneacetone dipalladium, palladium acetate, palladium (0) etc. prepared in the system and triphenylphosphine, tritert-butylphosphine, dicyclohexylbiphenylphosphine, 9,9-dimethyl-4,6-bis (Diphenylphosphino) xanthene, 2-dicyclohexylphosphino-2 ′, 4 ′, 6′-triisopropylbiphenyl (X-Phos), 2-dicyclohexylphosphino-2 ′, 6′-diisopropoxy1
- the reaction may be carried out by adding a phosphine ligand such as 1,1'-biphenyl (Ruphos).
- reaction is carried out at 0 ° C. to 150 ° C., preferably 10 ° C. to 100 ° C. for 0.5 hours to 72 hours, preferably 1 hour to 24 hours under microwave irradiation or non-irradiation.
- a compound represented by (I) can be obtained.
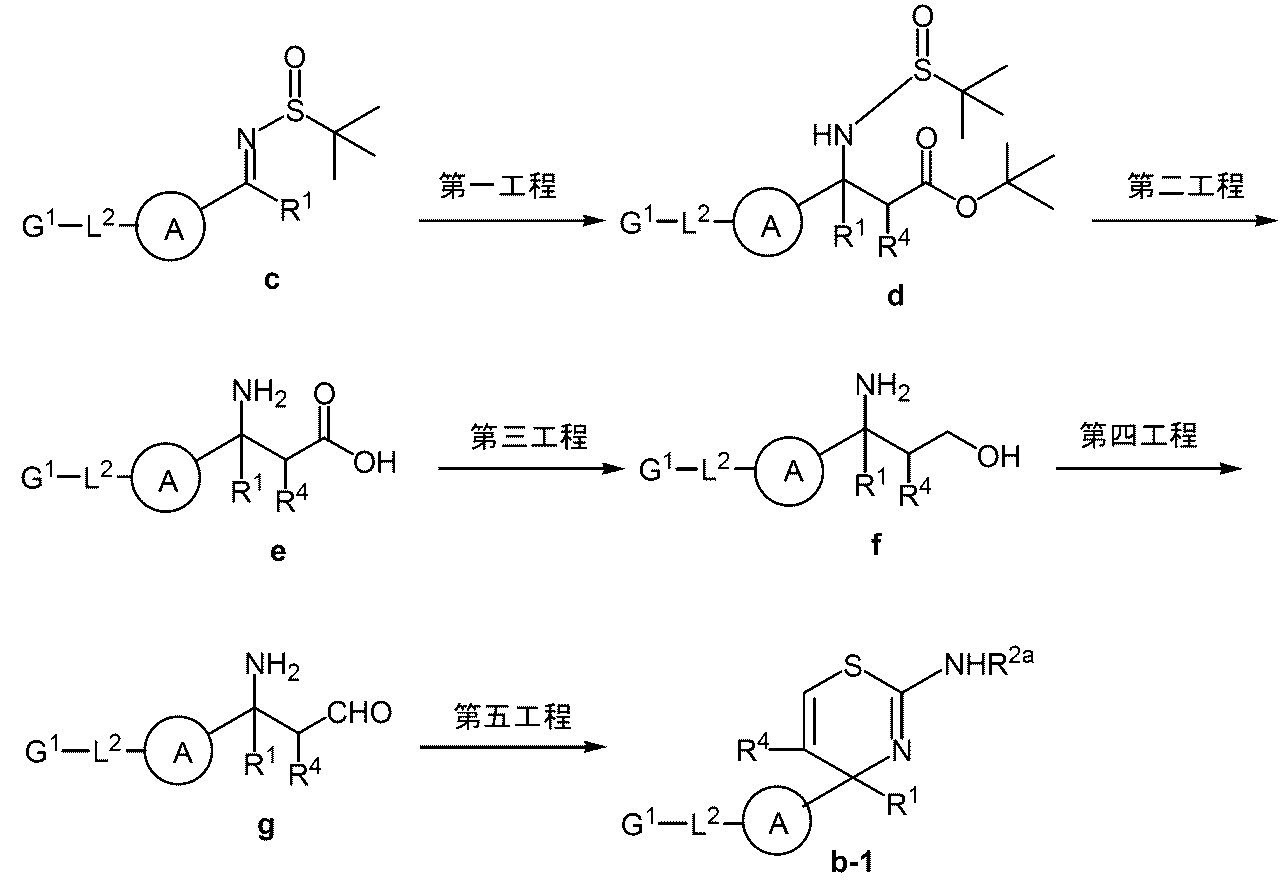
- First step Enolate obtained by reacting with a target ester such as t-butyl propionate in the presence of a base such as lithium diisopropylamide in a solvent such as toluene, dichloromethane or tetrahydrofuran, or in a mixed solvent thereof.
- a titanium reagent such as chlorotitanium triisopropoxide is added, and compound c which can be prepared by a known method is added, and the temperature is ⁇ 80 ° C. to 30 ° C., preferably ⁇ 80 ° C. to 0 ° C., for 0.1 hour to 24
- Compound d can be obtained by reacting for a period of time, preferably 0.1 to 12 hours.
- Second Step Compound d is dissolved in a solvent such as dioxane, methanol, dichloromethane, or a mixed solvent thereof in the presence of an acid such as hydrochloric acid, hydrobromic acid, sulfuric acid, trifluoroacetic acid, preferably 0 ° C. to 80 ° C.
- an acid such as hydrochloric acid, hydrobromic acid, sulfuric acid, trifluoroacetic acid, preferably 0 ° C. to 80 ° C.
- Compound e is added with a reducing agent such as borane, sodium hydride, lithium aluminum hydride or the like in a solvent such as dioxane, tetrahydrofuran, toluene or the like, or a mixed solvent thereof.
- a reducing agent such as borane, sodium hydride, lithium aluminum hydride or the like
- a solvent such as dioxane, tetrahydrofuran, toluene or the like, or a mixed solvent thereof.
- Compound f can be obtained by reacting at ⁇ 20 ° C. to 30 ° C. for 0.5 to 48 hours, preferably for 1 to 12 hours.
- Compound f is added with an oxidizing agent such as 2-iodoxybenzoic acid in a solvent such as dimethyl sulfoxide or dichloromethane, and 0 ° C. to 80 ° C., preferably 10 ° C. to 40 ° C., for 0.5 hour to 48 hours.
- compound g can be obtained by reacting for 1 to 12 hours.
- the amine and / or aldehyde group of compound f and compound g are protected by the method described in Protective Groups in Organic Synthesis, Theodora W Greene (John Wiley & Sons), etc., as necessary. And can be appropriately deprotected.
- a thiocyanate having a protecting group for example, benzoyl isothiocyanate
- a solvent such as dioxane, tetrahydrofuran, toluene, acetone, or a mixed solvent thereof
- Reaction is performed at 30 ° C. to 50 ° C., preferably ⁇ 10 ° C. to 25 ° C. for 0.1 hour to 12 hours, preferably 0.1 hour to 3 hours, followed by addition of concentrated sulfuric acid, concentrated nitric acid, etc.
- Compound b-1 can be obtained by reacting at 0 ° C. to 100 ° C., preferably 0 ° C. to 60 ° C., for 0.5 to 24 hours, preferably for 1 to 12 hours.
- Second Step To the compound h obtained in the first step, hydrochloric acid, hydrobromic acid, trifluoroacetic acid and the like are added, and 0 ° C. to 60 ° C., preferably 0 ° C. to 30 ° C., for 0.1 hour to 24 hours, Preferably, compound i can be obtained by reacting for 0.5 to 12 hours.
- Third step Compound i is added with a thiocyanate having a protecting group (for example, benzoyl isothiocyanate) prepared in a solvent such as dioxane, tetrahydrofuran, toluene, acetone or the like, or a mixed solvent thereof by a commercially available or known method, and- The reaction is carried out at 30 ° C. to 70 ° C., preferably ⁇ 20 ° C. to 50 ° C. for 0.1 hour to 12 hours, preferably 0.1 hour to 6 hours. Subsequently, after distilling off the solvent, concentrated sulfuric acid, Compound b-2 can be obtained by adding nitric acid or the like and reacting at ⁇ 30 ° C. to 70 ° C., preferably ⁇ 20 ° C. to 50 ° C. for 1 hour to 12 hours, preferably 1 hour to 6 hours.
- a protecting group for example, benzoyl isothiocyanate
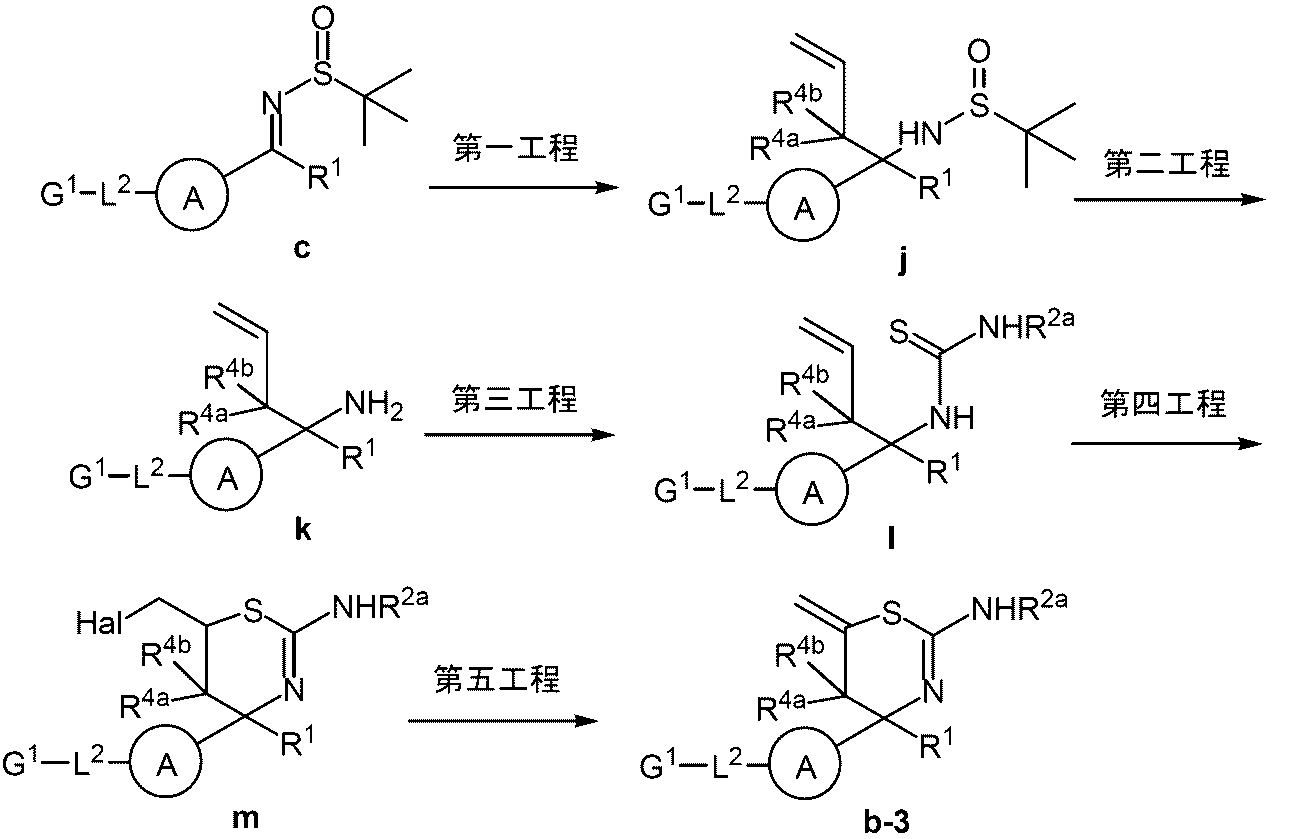
- a compound c that can be prepared by a known method is added to a Grignard reagent such as allylmagnesium bromide, and -80 ° C to 30 ° C, preferably Can be obtained by reacting at ⁇ 80 ° C. to 0 ° C. for 0.1 to 24 hours, preferably 0.1 to 12 hours.
- a Grignard reagent such as allylmagnesium bromide, and -80 ° C to 30 ° C, preferably Can be obtained by reacting at ⁇ 80 ° C. to 0 ° C. for 0.1 to 24 hours, preferably 0.1 to 12 hours.
- Second Step To the compound j obtained in the first step, a hydrochloric acid solution is added in a solvent such as methanol, ethanol, water, or a mixed solvent thereof, and the temperature is ⁇ 20 ° C. to 80 ° C., preferably 0 ° C. to 30 ° C.
- the compound k can be obtained by reacting for 0.1 to 24 hours, preferably 0.1 to 12 hours.
- Compound k is added with an isothiocyanate having a protecting group (for example, benzoyl isothiocyanate) prepared by a commercially available or known method in a solvent such as dichloromethane, dioxane, tetrahydrofuran, toluene, acetone, or a mixed solvent thereof.
- Compound 1 can be obtained by reacting at ⁇ 30 ° C. to 70 ° C., preferably ⁇ 20 ° C. to 50 ° C. for 0.1 hour to 12 hours, preferably 0.1 hour to 6 hours.
- Compound l is added to a halogenium cation source such as iodine, bromine, N-bromosuccinimide (NBS) in a solvent such as dichloromethane, and the temperature is set to ⁇ 20 ° C. to 40 ° C., preferably 0 ° C. to 20 ° C.
- Compound m can be obtained by reacting for 1 to 12 hours, preferably 0.1 to 6 hours.
- the compound b-3 is added to a base such as pyrrolidine, piperidine, piperazine, morpholine, etc. in a solvent such as dioxane, tetrahydrofuran, toluene or a mixed solvent thereof, and 20 ° C. to 100 ° C., preferably 40 ° C. to 80 ° C.
- the compound b-3 can be obtained by reacting for 0.1 to 24 hours, preferably 1 to 12 hours.
- Step 1 Compound n is prepared by adding ethyl acrylate and a Grubbs reagent to compound k in which an amino group is appropriately protected with a protecting group in a solvent such as toluene, dichloromethane, tetrahydrofuran, or a mixed solvent thereof, and subjecting it to an olefin metathesis reaction. Can be obtained.
- the reaction temperature is ⁇ 20 ° C. to 60 ° C., preferably 0 ° C. to 30 ° C.
- the reaction time is 0.5 hour to 24 hours, preferably 1 hour to 12 hours.
- Second Step Compound n is added with an isothiocyanate having a protecting group (for example, benzoyl isothiocyanate) prepared in a solvent such as dichloromethane, dioxane, tetrahydrofuran, toluene, acetone or the like, or a mixed solvent thereof, commercially or by a known method.
- Compound o can be obtained by reacting at ⁇ 30 ° C. to 70 ° C., preferably ⁇ 20 ° C. to 50 ° C. for 0.1 hour to 12 hours, preferably 0.1 hour to 6 hours.
- Compound o is subjected to a reduction reaction by adding diisobutylaluminum hydride, lithium aluminum hydride, sodium borohydride, etc. in a solvent such as dioxane, tetrahydrofuran, toluene, or a mixed solvent thereof, at ⁇ 80 ° C.
- Compound b-4 can be obtained by reacting at ⁇ 0 ° C., preferably -80 ° C. to -20 ° C. for 0.1 hour to 12 hours, preferably 0.1 hour to 3 hours.
- Compound b-4 can further convert the alcohol group by subjecting it to an appropriate reaction.
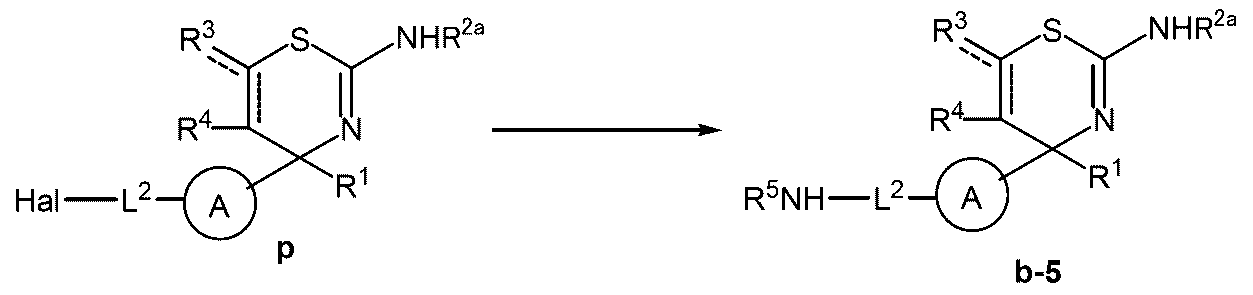
- a reagent having a substituent corresponding to the target compound such as lithium hexamethyldisilazide and benzophenone imine is added at ⁇ 10 ° C. to 30 ° C., and 30 ° C. to 120 ° C., preferably 50 ° C. to 100 ° C.
- Compound b-5 can be obtained by reacting at a temperature of 0.5 to 48 hours, preferably 3 to 20 hours.
- the amino protecting group may be any substituent that can be deprotected by the method described in Protective Groups in Organic Synthesis, Theodora W Greene (John Wiley & Sons), etc., for example, lower alkoxycarbonyl, lower alkenyloxycarbonyl, trialkylsilyl. , Acyl, methanesulfonyl, trifluoroethanesulfonyl, toluenesulfonyl and the like.
- Compound is obtained by adding iron to compound q in a mixed solvent of acetic acid and water and reacting at 20 ° C. to 120 ° C., preferably 50 ° C. to 80 ° C. for 0.5 hour to 48 hours, preferably 6 hours to 20 hours.
- b-6 can be obtained.
- a catalytic reduction catalyst such as 10% palladium / carbon or the like is added to compound q in a solvent such as tetrahydrofuran, ethyl acetate, methanol, etc., and 30 ° C. to 5 atmospheres under a hydrogen atmosphere of normal pressure to 5 atmospheres, preferably normal pressure to 2 atmospheres.
- Compound b can also be reacted at 120 ° C., preferably 50 ° C. to 80 ° C. for 0.5 to 48 hours, preferably 6 to 20 hours, or by the method described in Comprehensive Organic Transformations, Richard C. Larock (Mcgraw-Hill). -6 can be obtained.
- First Step Compound r which is commercially available or can be prepared by a known method, is vinylmagnesium chloride in a solvent such as ether, tetrahydrofuran or a mixed solvent such as ether-tetrahydrofuran at ⁇ 100 ° C. to 50 ° C., preferably ⁇ 80 ° C. to 0 ° C.
- a Grignard reagent having a substituent corresponding to the target compound, such as vinyl magnesium bromide, propenyl magnesium bromide, and reacting for 0.2 to 24 hours, preferably 0.5 to 5 hours, compound s Can be obtained.
- an acid such as acetic acid, trifluoroacetic acid, hydrochloric acid, sulfuric acid or a mixture thereof in the presence or absence of a solvent such as toluene, thiourea or N-methylthiourea, N, N′-dimethylthio
- a solvent such as toluene, thiourea or N-methylthiourea, N, N′-dimethylthio
- a substituted thiourea having a substituent corresponding to the target compound such as urea is added, and the reaction is carried out at ⁇ 20 ° C. to 100 ° C., preferably 0 ° C. to 50 ° C. for 0.5 hour to 120 hours, preferably 1 hour to 72 hours.
- Third Step An acid such as trifluoroacetic acid, methanesulfonic acid, trifluoromethanesulfonic acid or a mixture thereof is added to compound t in the presence or absence of a solvent such as toluene, and -20 ° C to 100 ° C, preferably 0 ° C.
- a solvent such as toluene
- b-7 By reacting at -50 ° C. for 0.5 to 120 hours, preferably 1 to 72 hours, b-7 can be obtained.
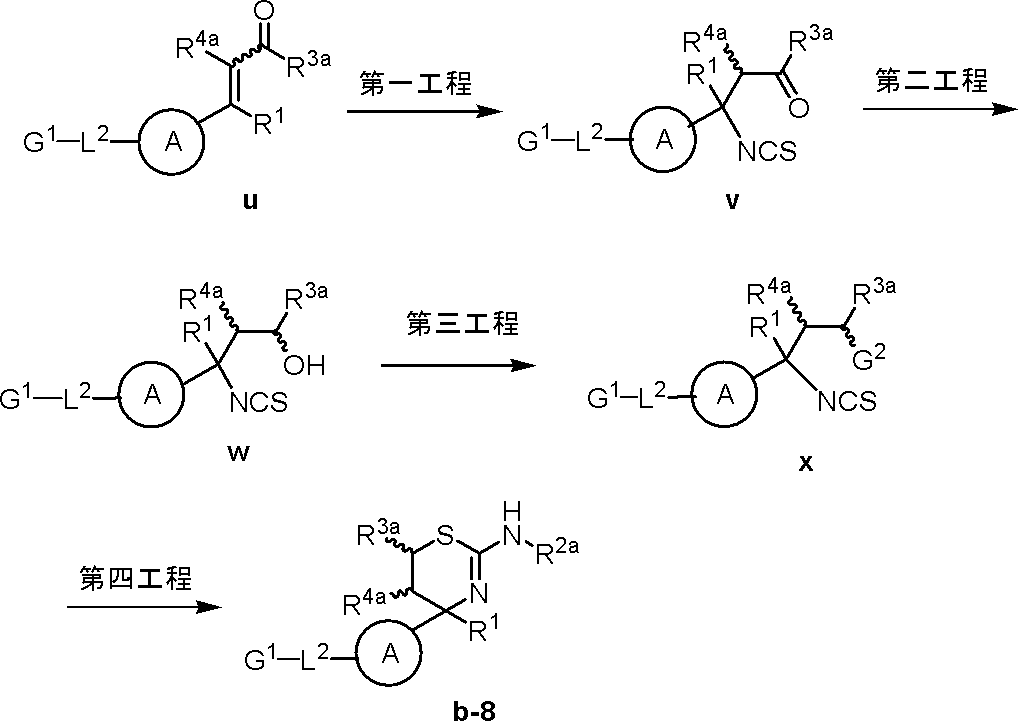
- G 1 is a leaving group such as halogen or a sulfonyloxy group, and other symbols are as defined above.
- First step Compound u, which can be prepared commercially or by a known method, is dissolved in thiocyanate such as sodium thiocyanate and ammonium thiocyanate in a solvent such as toluene, chloroform and tetrahydrofuran in the presence of water and an acid such as hydrochloric acid and sulfuric acid.
- Compound v can be obtained by reacting at a temperature of from 150 ° C. to 150 ° C., preferably from 20 ° C. to 100 ° C., for 0.5 to 24 hours, preferably 1 to 12 hours.
- Compound w can be obtained by adding an agent and reacting at ⁇ 80 ° C. to 50 ° C., preferably ⁇ 20 ° C. to 20 ° C. for 0.1 hour to 24 hours, preferably 0.5 hour to 12 hours.
- Third Step Compound w is -80 ° C to 50 ° C, preferably with a halogenating agent such as thionyl chloride, phosphorus oxychloride, carbon tetrabromide-triphenylphosphine in the presence or absence of a solvent such as toluene or dichloromethane. Is reacted at ⁇ 20 ° C. to 20 ° C. for 0.1 hours to 24 hours, preferably 0.5 hours to 12 hours, or methanesulfonyl in the presence of a base such as triethylamine in a solvent such as toluene or dichloromethane.
- a halogenating agent such as thionyl chloride, phosphorus oxychloride, carbon tetrabromide-triphenylphosphine in the presence or absence of a solvent such as toluene or dichloromethane.
- Compound x is mixed with a primary amine such as ammonia or methylamine in a solvent such as methanol, ethanol, water or a mixed solvent such as methanol-water at ⁇ 20 ° C. to 80 ° C., preferably 0 ° C. to 40 ° C.
- Compound b-8 can be obtained by reacting for 0.5 to 48 hours, preferably 1 to 24 hours.
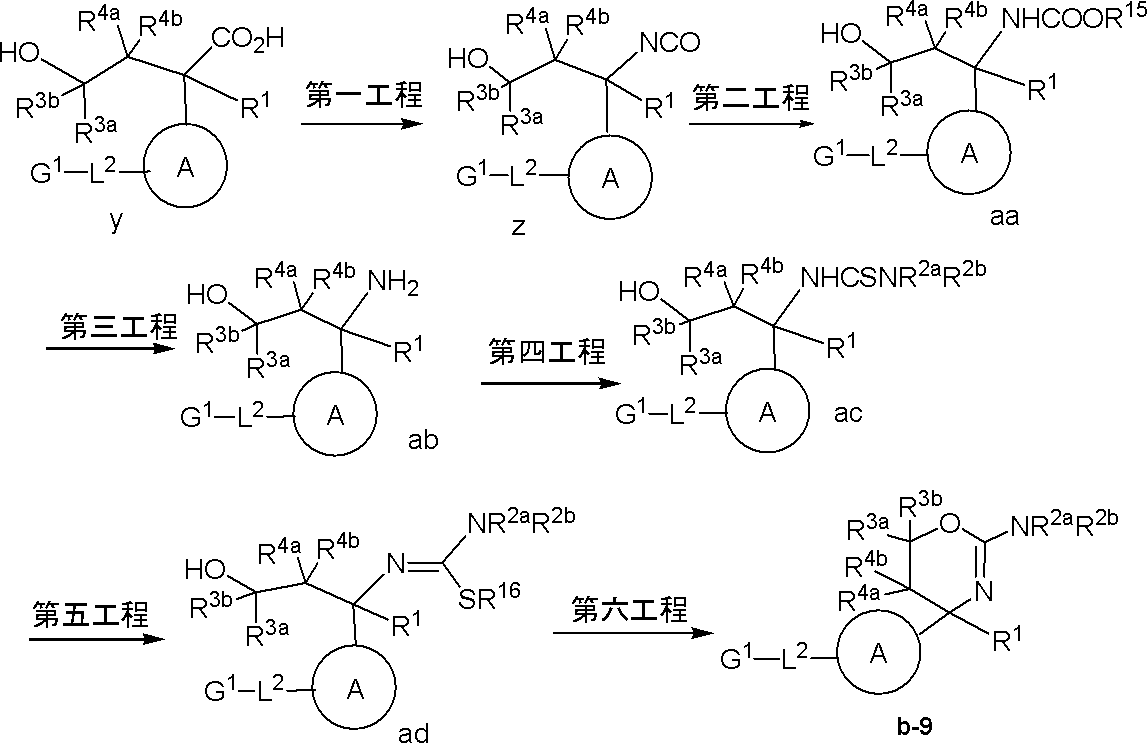
- First step Compound y which is commercially available or can be prepared by a known method, is added with an azidating agent such as diphenylphosphoryl azide in the presence of a base such as diisopropylethylamine, triethylamine or pyridine in a solvent such as toluene, t-butyl alcohol or tetrahydrofuran.
- the compound z can be obtained by reacting at 0 ° C. to 200 ° C., preferably 40 ° C. to 150 ° C. for 1 hour to 48 hours, preferably 0.5 hour to 24 hours.
- an alcohol such as t-butyl alcohol, 3,4-dimethoxybenzyl alcohol, 4-methoxybenzyl alcohol or the like in a solvent such as toluene, xylene, dimethylformamide, tetrahydrofuran or the like, preferably at 0 ° C. to 300 ° C.
- a solvent such as toluene, xylene, dimethylformamide, tetrahydrofuran or the like, preferably at 0 ° C. to 300 ° C.
- a solvent such as toluene, xylene, dimethylformamide, tetrahydrofuran or the like
- Compound aa is added with hydrochloric acid, sulfuric acid, hydrobromic acid, trifluoroacetic acid or the like in the presence or absence of a solvent such as water, toluene, dichloromethane, methanol, 1,4-dioxane, acetic acid or ethyl acetate.
- Compound ab can be obtained by reacting in the presence of an acid at 0 ° C. to 200 ° C., preferably 25 ° C. to 150 ° C. for 0.1 hour to 48 hours, preferably 0.5 hour to 24 hours.
- the compound ad is 0 ° C.-200 ° C., preferably 10 ° C.- Compound b-9 can be obtained by reacting at 150 ° C. for 1 hour to 120 hours, preferably 0.5 hour to 100 hours.
- a base such as diisopropylethylamine, triethylamine, pyridine, sodium hydroxide, etc.
- a solvent such as acetone, acetonitrile, dimethylformamide, tetrahydrofuran, dichloromethane, etc.
- R 17 is a substituted or unsubstituted lower alkyl, substituted or unsubstituted lower alkenyl, a substituted or unsubstituted carbocyclic group, a substituted or unsubstituted heterocyclic group or the like, or ⁇ -methyl Benzyl and the like
- LG is a leaving group such as halogen or a lower alkylsulfonyloxy group, and other symbols are as defined above.
- the above compounds ae and af are, for example, (1) T. Fujisawa et al., Tetrahedron Lett ., 37, 3881-3884 (1996), (2) DH Hua et al, Sulfur Reports, vol. 21, pp.
- First Step Compound r which is commercially available or can be prepared by a known method, in a solvent such as ether, tetrahydrofuran, toluene, benzene or a mixed solvent such as ether-tetrahydrofuran at 60 ° C. to 120 ° C., preferably 80 ° C. to 100 ° C.
- a solvent such as ether, tetrahydrofuran, toluene, benzene or a mixed solvent such as ether-tetrahydrofuran at 60 ° C. to 120 ° C., preferably 80 ° C. to 100 ° C.
- Compound ae can be obtained by adding a reagent having a substituent corresponding to the target compound such as amide and reacting for 0.5 to 24 hours, preferably 0.5 to 5 hours.
- Second Step Reagents having substituents corresponding to the target compound such as acetate ester commercially available or prepared by known methods, enolates such as lithium, aluminum, zinc and titanium, or target compounds such as acetate ester Presence of Lewis acids such as titanium tetrachloride and boron trifluoride ether complex in ketene silyl acetate prepared from reagents having substituents such as ether, tetrahydrofuran, toluene, methylene chloride, etc. or mixed solvents such as ether-tetrahydrofuran Reaction with compound ae for 0.5 to 24 hours, preferably 0.5 to 5 hours at ⁇ 100 ° C. to 50 ° C., preferably ⁇ 80 ° C. to ⁇ 30 ° C.
- Compound af can be obtained according to the methods described in documents (1) and (3).
- compound af is subjected to the purpose of methylmagnesium chloride, ethylmagnesium bromide, etc. at ⁇ 100 ° C. to 50 ° C., preferably ⁇ 80 ° C. to 30 ° C.
- a Grignard reagent having a substituent corresponding to the compound to be added is added, or the compound af has a substituent corresponding to the target compound such as R 3a MgBr, R 3b MgBr via Weinreb Amide.
- the compound ag can be obtained by sequentially reacting a Grignard reagent and reacting for 0.2 to 24 hours, preferably 0.2 to 5 hours.
- Compound ah in a solvent such as methanol, ethanol, ether, tetrahydrofuran, 1,4-dioxane, methylene chloride, ethyl acetate containing hydrogen chloride, trifluoroacetic acid or the like, or without solvent, in trifluoroacetic acid, Compound ah can be obtained by reacting at ⁇ 30 ° C. to 100 ° C., preferably ⁇ 10 ° C. to 90 ° C., for 0.5 to 12 hours, preferably 0.5 to 5 hours.
- a solvent such as methanol, ethanol, ether, tetrahydrofuran, 1,4-dioxane, methylene chloride, ethyl acetate containing hydrogen chloride, trifluoroacetic acid or the like, or without solvent, in trifluoroacetic acid
- a solvent such as methylene chloride and toluene of compound ah or in a mixed solvent such as methylene chloride-water, calcium carbonate, potassium carbonate and the like are added, and -30 ° C to 50 ° C, preferably -10 ° C to 25 ° C.
- the compound ai can be obtained by adding thiophosgene and reacting for 0.5 to 12 hours, preferably 0.5 to 5 hours.
- the compounds b-1, b-2, b-3, b-4, b-5, b-6, b-7, b-8, b-9, b-10, b-11, (I) and (I ') is, for example, (1) T. Fujisawa et al., Tetrahedron Lett., 37,3881-3884 (1996), (2) DH Hua et al, Sulfur Reports, vol.21, pp.211-239 ( (1999), (3) Y. Koriyama et al., Tetrahedron, 58, 9621-9628 (2002) or (4) T. Vilavan et al, Current Organic Chemistry, 9, 1315-1392 (2005), Patent Document 1, It can be produced according to the methods described in Patent Document 2, Patent Document 3, and the like.
- the optically active compound (I) is an optically active starting material, an asymmetric synthesis is carried out at an appropriate stage to obtain an optically active intermediate, or an intermediate or final product of a racemate at an appropriate stage. It can be manufactured by optical division.
- Optical resolution methods include separation of optical isomers using an optically active column, kinetic optical resolution using enzymatic reactions, etc., diastereomers by salt formation using chiral acids and chiral bases. There are crystallization division, preferential crystallization method and the like.
- optically active (I) and (I ′) can be synthesized by using optically active sulfinylimine c as a raw material in the above production method.
- R 1 includes substituted or unsubstituted alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, cyano, substituted or unsubstituted carbocyclic group, or substituted or unsubstituted heterocyclic group.
- R 1 is, for example, unsubstituted alkyl having 1 to 3 carbon atoms.
- R 2a and R 2b each independently include hydrogen, substituted or unsubstituted alkyl, or substituted or unsubstituted acyl.
- R 2a and R 2b are, for example, both hydrogen.
- X includes S or O.
- X is, for example, S.
- X is, for example, O.
- R 3a and R 3b are each independently hydrogen, halogen, hydroxy, substituted or unsubstituted alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, substituted or unsubstituted acyl, substituted or unsubstituted Substituted alkoxy, substituted or unsubstituted carbocyclic alkyl, substituted or unsubstituted heterocyclic alkyl, substituted or unsubstituted carbocyclic alkoxy, substituted or unsubstituted heterocyclic alkoxy, substituted or unsubstituted alkylthio, carboxy, cyano Substituted or unsubstituted alkoxycarbonyl, substituted or unsubstituted amino, substituted or unsubstituted carbamoyl, substituted or unsubstituted carbocyclic group or substituted or unsubstituted heterocyclic group.
- R 3a and R 3b are each independently, for example, hydrogen, substituted or unsubstituted alkyl, cyano, substituted or unsubstituted alkoxycarbonyl, substituted or unsubstituted carbamoyl, substituted or unsubstituted carbocyclic group, or A substituted or unsubstituted heterocyclic group.
- R 3a and R 3b are, for example, hydrogen.
- R 3c and R 3d are each independently hydrogen, halogen, substituted or unsubstituted alkyl, or R 3c and R 3d together with the carbon atom to which they are attached are substituted or unsubstituted non-aromatic Form a group carbocycle.
- R 3c and R 3d are each independently, for example, hydrogen, halogen, substituted or unsubstituted alkyl.
- R 4a and R 4b each independently include hydrogen or substituted or unsubstituted alkyl.
- R 4a and R 4b are, for example, hydrogen.
- R 5 is hydrogen, substituted or unsubstituted alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, or substituted or unsubstituted acyl.
- R 5 is, for example, hydrogen or substituted or unsubstituted alkyl.
- L 1 and L 2 are each independently a single bond, substituted or unsubstituted alkylene (excluding oxo and thioxo as substituents), substituted or unsubstituted alkenylene (excluding oxo and thioxo as substituents) or substituted Alternatively, unsubstituted alkynylene (except oxo and thioxo as substituents).
- L 1 and L 2 are each independently a single bond, substituted or unsubstituted alkylene (wherein the substituents are halogen, alkoxy, halogenoalkoxy, hydroxyalkoxy, alkoxyalkoxy, acyl, acyloxy, carboxy, alkoxycarbonyl, amino, acylamino, Alkylamino, imino, hydroxyimino, alkoxyimino, alkylthio, carbamoyl, alkylcarbamoyl, hydroxyalkylcarbamoyl, sulfamoyl, alkylsulfamoyl, alkylsulfamoyl, alkylsulfinyl, alkylsulfonylamino, alkylsulfonylalkylamino, alkylsulfonylimino, alkylsulfinylamino, alkyl Sulfinylalkylamino, al
- L 1 and L 2 are, for example, a single bond.
- Ring A is a substituted or unsubstituted carbocyclic ring or a substituted or unsubstituted heterocyclic ring.
- Ring A is, for example, substituted or unsubstituted benzene.
- Ring B is a substituted or unsubstituted carbocycle, substituted or unsubstituted pyridine, substituted or unsubstituted pyrimidine, or substituted or unsubstituted 5-membered heterocycle.
- Ring B is, for example, substituted or unsubstituted benzene, substituted or unsubstituted pyridine, or substituted or unsubstituted pyrimidine.
- Ring B is a substituted or unsubstituted carbocyclic ring or a substituted or unsubstituted heterocyclic ring.
- Ring B is, for example, a substituted or unsubstituted carbocycle, a substituted or unsubstituted pyridine, a substituted or unsubstituted pyrimidine, or a substituted or unsubstituted 5-membered heterocyclic ring.
- Ring B is, for example, substituted or unsubstituted pyridine or substituted or unsubstituted pyrimidine.
- Ring B is a substituted nitrogen-containing aromatic monocycle.
- Ring B is, for example, substituted pyridine or substituted pyrimidine.
- R 1 is substituted or unsubstituted alkyl
- R 2a and R 2b are both hydrogen
- X is S, Or X is O
- And R 5 is hydrogen
- L 1 and L 2 are a single bond
- Ring A is a substituted or unsubstituted carbocycle
- Ring B is a substituted or unsubstituted carbocycle, a substituted or unsubstituted pyridine or a substituted or unsubstituted pyrimidine, or a pharmaceutically acceptable salt thereof, or a solvate thereof.
- R 1 is unsubstituted alkyl having 1 to 3 carbon atoms; R 2a and R 2b are both hydrogen, X is S, Or X is O, And R 5 is hydrogen; L 1 and L 2 are a single bond, Ring A is a benzene ring optionally substituted with halogen, Ring B is a substituted or unsubstituted carbocycle, substituted or unsubstituted pyridine or substituted or unsubstituted pyrimidine (where each substituent is halogen, hydroxy, alkyl, halogenoalkyl, hydroxyalkyl, alkoxyalkyl, alkoxy, alkoxy A compound selected from the group consisting of alkoxy, alkoxycarbonyl, amino, alkylamino, carbamoyl, cyano and nitro), or a pharmaceutically acceptable salt thereof, or a solvate thereof.
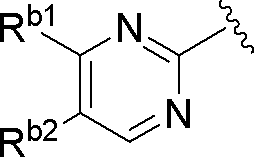
- ring B is B1
- Ring B is (Wherein R b1 and R b2 are as defined above)
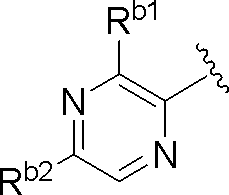
- a compound hereinafter, ring B is B2)
- Ring B is (Wherein R b1 and R b2 are as defined above)
- a compound in which the combination of ring X, R 1 , ring A, L and ring B is as follows.
- Ring B is Wherein R b1 is hydrogen, chloro, methoxy, hydroxymethyl, cyano, amino or carbamoyl. (Hereinafter, ring B is B5).
- a compound in which the combination of ring B, R b1 and R b2 (B, R b1 , R b2 ) is as follows.
- a compound in which the combination of ring B and R b1 (B, R b1 ) is as follows.
- (B4, hydrogen) (hereinafter, ring B is b81), (B4, chloro) (hereinafter, ring B is b82), (B4, methoxy) (hereinafter, ring B is b83), (B4, hydroxymethyl) (hereinafter, ring B is b84), (B4, cyano) (hereinafter, ring B is b85), (B4, amino) (hereinafter, ring B is b86), (B4, carbamoyl) (hereinafter, ring B is b87), (B5, hydrogen) (hereinafter, ring B is b88), (B5, chloro) (hereinafter, ring B is b89), (B5, methoxy) (hereinafter, ring B is b90), (B5, hydroxymethyl) (hereinafter, ring B is b91), (B5, cyano) (herein
- a compound in which the combination of ring X, R 1 , ring A and ring B is as follows, and L is L 1.
- the compound of the present invention is useful for diseases induced by production, secretion or deposition of amyloid ⁇ protein.
- diseases induced by production, secretion or deposition of amyloid ⁇ protein For example, Alzheimer type dementia (Alzheimer's disease, Alzheimer type senile dementia etc.), Down's syndrome, memory disorder, prion disease (Kreuz's disease) Felt-Jakob disease, etc.), mild cognitive impairment (MCI), Dutch hereditary amyloid cerebral hemorrhage, cerebral amyloid angiopathy, other degenerative dementia, mixed vascular dementia, dementia associated with Parkinson's disease, progression Treatment and / or prevention of dementia associated with supranuclear paralysis, dementia associated with corticobasal degeneration, diffuse Lewy body Alzheimer's disease, age-related macular degeneration, Parkinson's disease, amyloid angiopathy, etc. It is effective for improvement.
- Alzheimer type dementia Alzheimer's disease, Alzheimer type senile dementia etc.
- the compound of the present invention has high inhibitory activity against BACE1 and / or high selectivity to other enzymes, and therefore can be a pharmaceutical with reduced side effects. Furthermore, since it has a high inhibitory effect on amyloid ⁇ production in cell systems, and particularly has a high inhibitory effect on amyloid ⁇ production in the brain, it can be an excellent pharmaceutical product. Moreover, it can become a pharmaceutical with a wider safety margin with respect to a side effect by setting it as the optically active substance which has appropriate stereochemistry.
- the compound of the present invention has high metabolic stability, high solubility, high oral absorption, good bioavailability, good clearance, high brain transferability, long half-life, non-protein binding rate It has advantages such as high HERG channel inhibition, low CYP inhibition, low CYP MBI (Mechanism-based inhibition), and / or negative Ames test.
- the compound of the present invention When administering the compound of the present invention, it may be used in combination with other drugs (for example, other Alzheimer's disease therapeutic agents such as acetylcholinesterase).
- other drugs for example, other Alzheimer's disease therapeutic agents such as acetylcholinesterase.
- antidementia drugs such as donepezil hydrochloride, tacrine, galantamine, rivastigmine, zanapezil, memantine, and vinpocetine.
- the compound of the present invention When the compound of the present invention is administered to humans, it can be administered orally as powders, granules, tablets, capsules, pills, liquids, etc. or parenterally as injections, suppositories, transdermal absorption agents, inhalants, etc. Can be administered.
- excipients, binders, wetting agents, disintegrants, lubricants and other pharmaceutical additives suitable for the dosage form may be mixed with an effective amount of the present compound as necessary to obtain a pharmaceutical preparation. it can.
- the dose varies depending on the disease state, administration route, patient age, or body weight, but when administered orally to an adult, it is usually 0.1 ⁇ g to 1 g / day, preferably 0.01 to 200 mg / day. In the case of parenteral administration, it is usually 1 ⁇ g to 10 g / day, preferably 0.1 to 2 g / day.
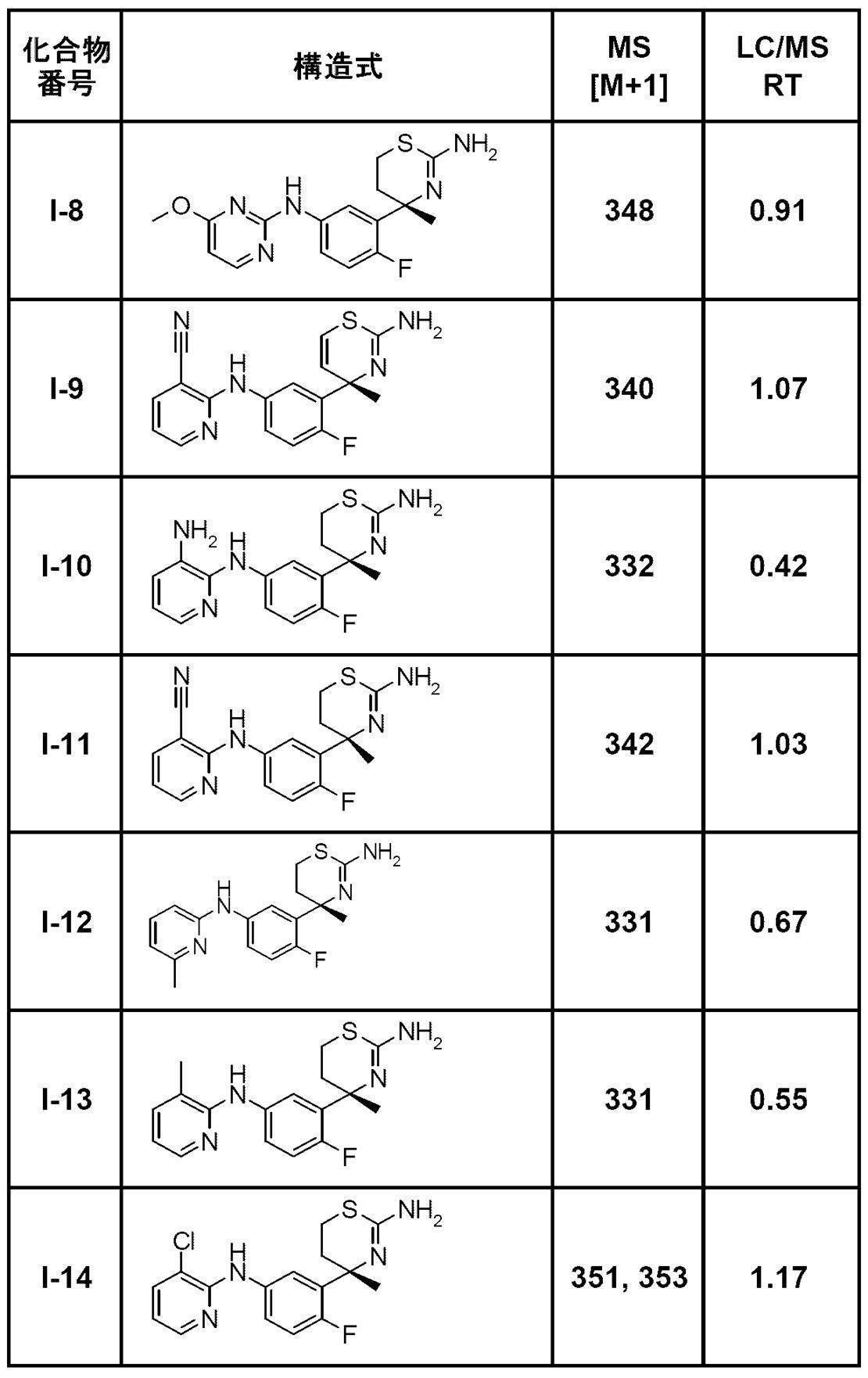
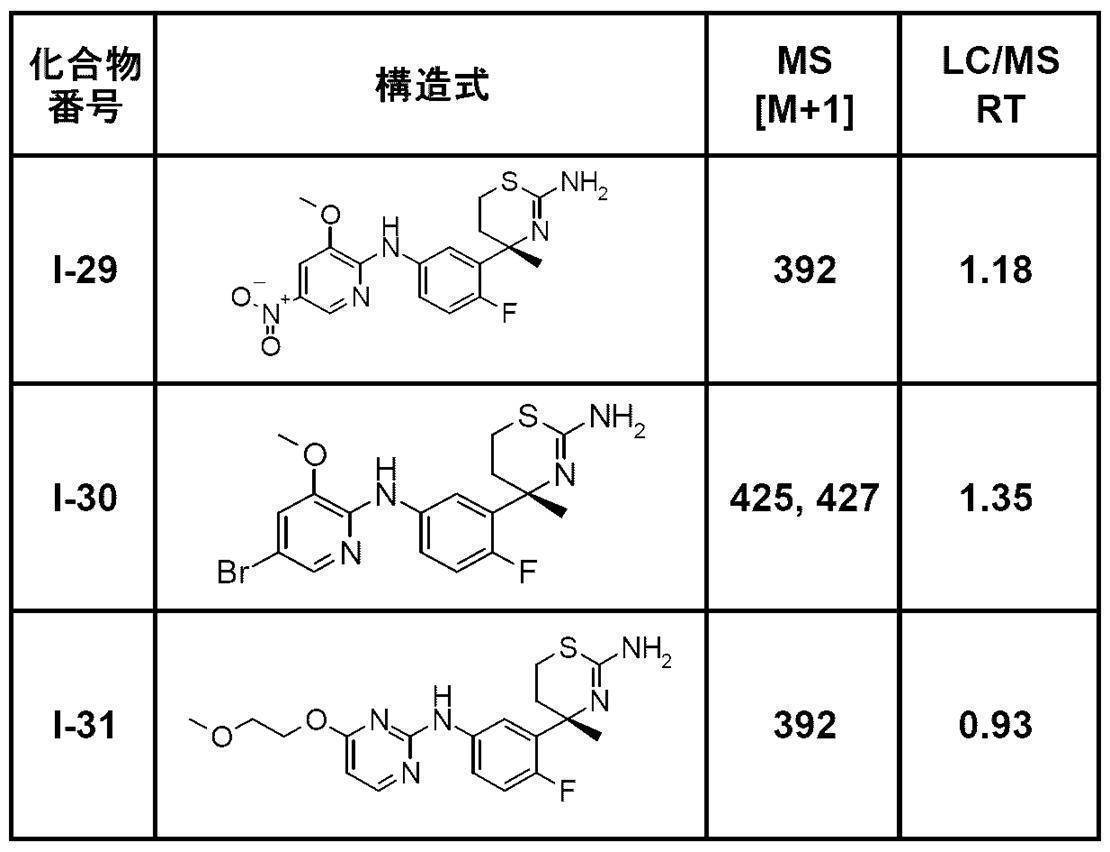
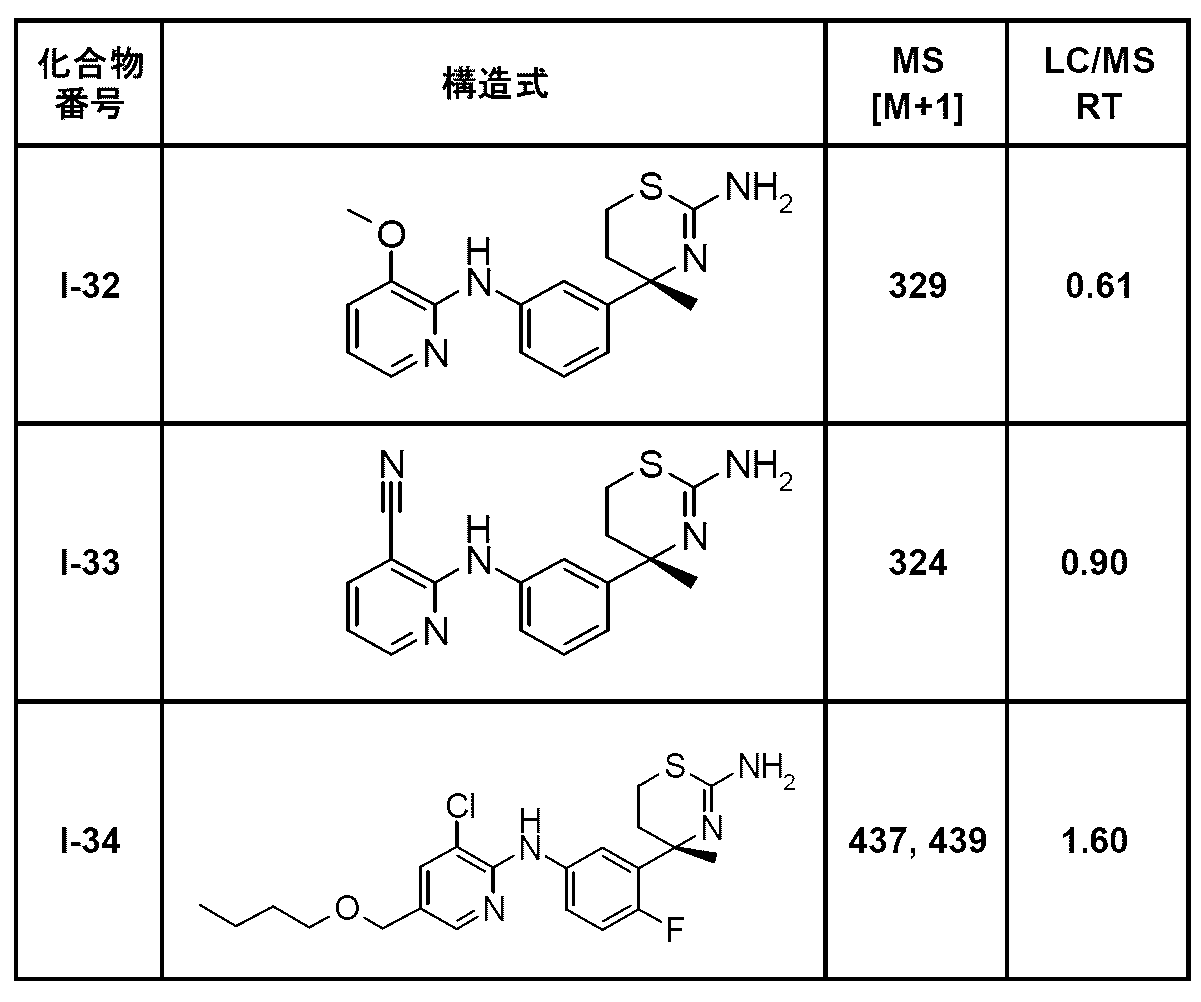
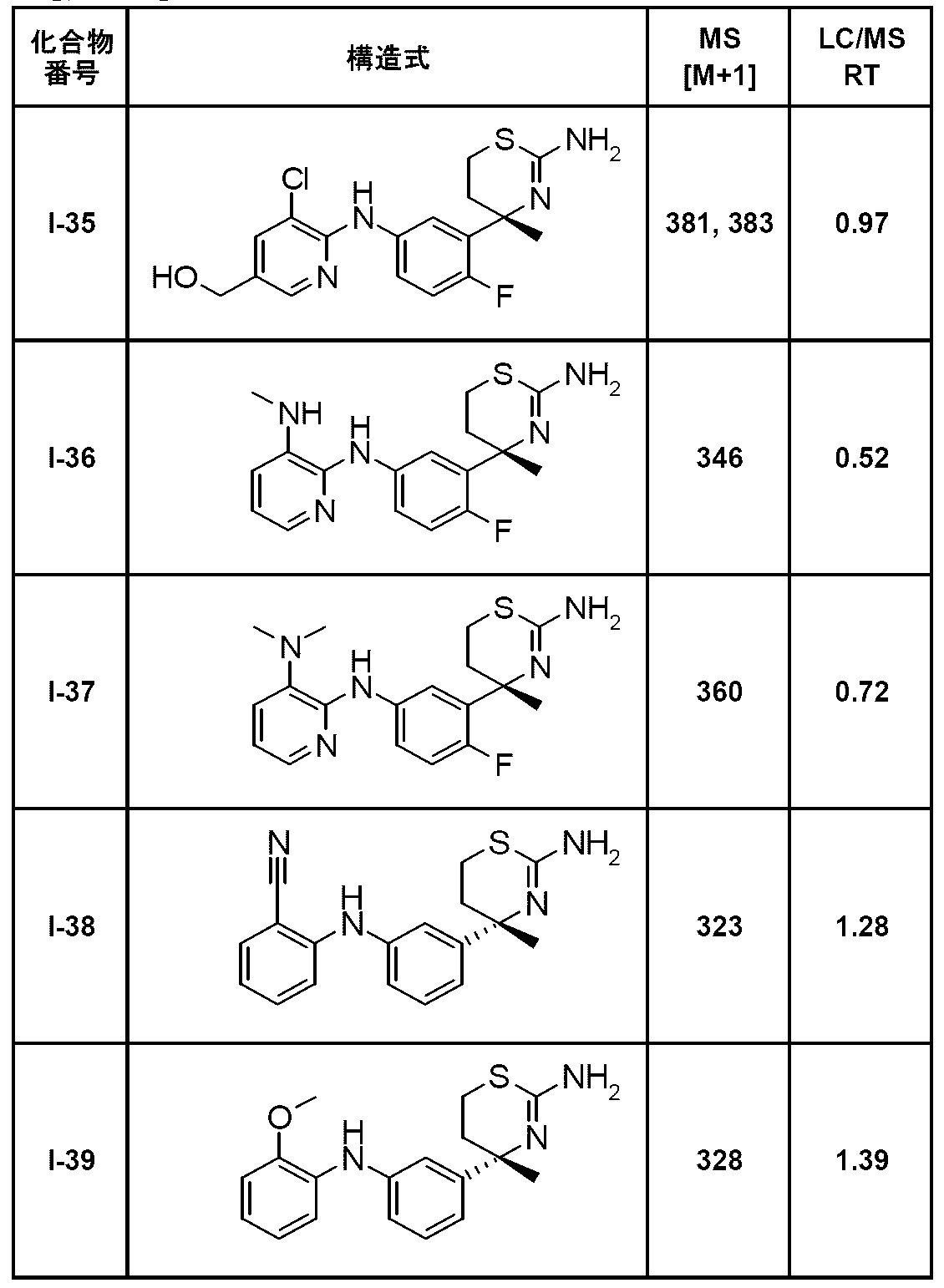
- RT represents the retention time (minutes).
- the substrate peptide was synthesized by reacting biotin-XSEVNLDAEFRHDSGC (Peptide Institute) with cryptate TBPCOOH mono SMP (CIS bio international).
- the final concentration of substrate peptide is 18 nmol / L
- the final concentration of recombinant human BACE1 is 7.4 nmol / L
- the reaction buffer is sodium acetate buffer (50 mmol / L sodium acetate pH 5.0, 0.008% Triton X-100). Using.
- the enzyme activity was determined from the count rate at each measurement wavelength (10000 ⁇ count 665 / count 620), and the dose (IC 50 ) that inhibits the enzyme activity by 50% was calculated.
- Table 2 shows the IC 50 values of the test substances. In the table, “ ⁇ M” represents “ ⁇ mol / L”.
- Neuroblastoma SH-SY5Y cells (SH / APPwt) overexpressing human wild-type ⁇ APP were adjusted to 8 ⁇ 105 cells / mL and plated on 96-well culture plates (Falcon) at 150 ⁇ l per well. The cells were cultured at 37 ° C. in a 5% carbon dioxide incubator for 2 hours. Thereafter, a solution in which a test compound (DMSO: dimethyl sulfoxide solution) was added and suspended in advance to form a 2 ⁇ l / 50 ⁇ l medium was added to the cell solution. That is, the final DMSO concentration was 1% and the cell culture solution was 200 ⁇ l. After 24 hours of incubation after addition of the test compound, 100 ⁇ l of the culture supernatant was collected, and the amount of A ⁇ contained therein was measured.
- DMSO dimethyl sulfoxide solution
- the amount of A ⁇ was measured using a 384-well half area plate (black plate; manufactured by Coaster), 10 ⁇ l of homogeneous time-resolved fluorescence (HTRF) measurement reagent (Amyloid ⁇ 1-40 peptide; IBA Molecular Holding, SA) 10 ⁇ l of clean water was added and mixed, and the mixture was allowed to stand overnight at 4 ° C. protected from light. Thereafter, fluorescence intensity (excitation wavelength: 337 nm, measurement wavelengths: 620 nm and 665 nm) was measured using a Wallac 1420 multilabel counter (Perkin Elmer life sciences).
- HTRF time-resolved fluorescence
- the amount of A ⁇ was determined from the count rate of each measurement wavelength (10000 ⁇ count 665 / count 620), and the dose that inhibits A ⁇ production by 50% (IC50) was calculated from at least 6 different doses.
- Table 3 shows the IC 50 values of the test substances.
- compounds I-1, I-10, I-12, I-16, I-19, I-20, I-23, I-24, I-25 and I-26 have an IC 50 of 3 ⁇ M or less. It was.
- Test Example 3 Rat brain ⁇ -amyloid reducing action
- the test compound is suspended in 0.5% methylcellulose, prepared to a final concentration of 2 mg / mL, and orally administered to male Crj: SD rats (7-9 weeks old) to 10 mg / kg. .
- the base control group is administered with 0.5% methylcellulose alone, and 3 to 8 animals are administered in each group.
- the brain is removed, the cerebral hemisphere is isolated, weighed, and then immediately frozen in liquid nitrogen and stored at ⁇ 80 ° C. until the date of extraction.
- the frozen cerebral hemisphere was transferred to a Teflon (registered trademark) homogenizer under ice-cooling, and an extraction buffer (1% CHAPS ( ⁇ 3-[(3-chloroamidopropyl) dimethylammonio] -1-propane) having a volume 5 times its weight was used. Sulfonate ⁇ ), 20 mmol / L Tris-HCl (pH 8.0), 150 mmol / L NaCl and Complete (Roche) protease inhibitor) are added, and the mixture is repeatedly homogenized for 2 minutes to solubilize. The suspension is transferred to a centrifuge tube and left on ice for 3 hours or more, and then centrifuged at 100,000 ⁇ g, 4 ° C.
- ⁇ -amyloid 40 manufactured by Wako Pure Chemical Industries, Ltd., product number 294-62501.
- the ELISA measurement is performed according to the attached instructions.
- the decreasing effect is calculated as the ratio of the base control group of each test to ⁇ -amyloid 40 in the brain.
- the CYP3A4 fluorescent MBI test is a test for examining the enhancement of CYP3A4 inhibition of a compound by metabolic reaction, and 7-benzyloxytrifluoromethylcoumarin (7-BFC) is debenzylated by CYP3A4 enzyme using E. coli-expressed CYP3A4 as an enzyme.
- the reaction for producing a fluorescent metabolite 7-hydroxytrifluoromethylcoumarin (HFC) was performed as an index.
- reaction conditions are as follows: substrate, 5.6 ⁇ mol / L 7-BFC; pre-reaction time, 0 or 30 minutes; reaction time, 15 minutes; reaction temperature, 25 ° C. (room temperature); CYP3A4 content (E. coli expression enzyme), Pre-reaction 62.5 pmol / mL, reaction 6.25 pmol / mL (10-fold dilution); test drug concentration, 0.625, 1.25, 2.5, 5, 10, 20 ⁇ mol / L (6 points) ).
- NADPH is also added to the remaining pre-reaction solution to start the pre-reaction (pre-reaction is present), and after pre-reaction for a predetermined time, one plate is diluted to 1/10 with the substrate and K-Pi buffer.
- the control (100%) was obtained by adding DMSO, which is a solvent in which the drug was dissolved, to the reaction system, and the residual activity (%) at each concentration with the test drug solution added was calculated.
- the IC 50 was calculated by inverse estimation using a logistic model. The case where the difference in IC 50 values was 5 ⁇ M or more was designated as (+), and the case where it was 3 ⁇ M or less was designated as ( ⁇ ). (result) Compound I-3: ( ⁇ ).
- Test Example 5 CYP inhibition test
- CYP1A2 O-deethylation of 7-ethoxyresorufin
- methyl tolbutamide as a typical substrate metabolic reaction of the major human CYP5 species (CYP1A2, 2C9, 2C19, 2D6, 3A4) -Index of hydroxylation (CYP2C9), mephenytoin 4'-hydroxylation (CYP2C19), dextromethorphan O-demethylation (CYP2D6), and terfenadine hydroxylation (CYP3A4).
- the degree of inhibition by the test compound was evaluated.
- reaction conditions are as follows: substrate, 0.5 ⁇ mol / L ethoxyresorufin (CYP1A2), 100 ⁇ mol / L tolbutamide (CYP2C9), 50 ⁇ mol / L S-mephenytoin (CYP2C19), 5 ⁇ mol / L dextromethorphan (CYP2D6), 1 ⁇ mol / L terfenadine (CYP3A4); reaction time, 15 minutes; reaction temperature, 37 ° C .; enzyme, pooled human liver microsomes 0.2 mg protein / mL; test drug concentration 1, 5, 10, 20 ⁇ mol / L (4 points) ).
- resorufin CYP1A2 metabolite
- CYP1A2 metabolite resorufin in the supernatant of the centrifugation was collected with a fluorescent multilabel counter
- tolbutamide hydroxide CYP2C9 metabolite
- mephenytoin 4 ′ hydroxide CYP2C19 metabolite
- Dextrorphan CYP2D6 metabolite
- terfenadine alcohol CYP3A4 metabolite
- the control (100%) was obtained by adding only DMSO, which is a solvent in which the drug was dissolved, to the reaction system, and the residual activity (%) at each concentration of the test drug solution was calculated.
- the IC 50 was calculated by inverse estimation using a logistic model. (result) Compound I-10: 5 species> 21 ⁇ M.
- Test Example 6 FAT test Inoculate 20 ⁇ L of Salmonella typhimurium TA98 strain, TA100 strain in a cryopreserved 10 mL liquid nutrient medium (2.5% Oxoid nutrient broth No. 2) and incubate at 37 ° C for 10 hours before shaking.
- TA98 strain 9 mL of the bacterial solution is centrifuged (2000 ⁇ g, 10 minutes) to remove the culture solution, and 9 mL of Micro F buffer solution (K 2 HPO 4 : 3.5 g / L, KH 2 PO 4 : 1 g /) L, (NH 4 ) 2 SO 4 : 1 g / L, trisodium citrate dihydrate: 0.25 g / L, MgSO 4 ⁇ 7H 2 0: 0.1 g / L), and 110 mL of Exposure Add to medium (BioF: 8 ⁇ g / mL, histidine: 0.2 ⁇ g / mL, glucose: MicroF buffer solution containing 8 mg / mL), TA100 strain to 3.16 mL bacterial solution added to 120 mL of Exposure medium and test bacterial solution To prepare.
- Micro F buffer solution K 2 HPO 4 : 3.5 g / L, KH 2 PO 4 : 1 g /) L, (NH
- Test substance DMSO solution (maximum dose 50 mg / mL to 8-fold dilution at 2-fold common ratio), DMSO as negative control, 50 ⁇ g / mL 4-nitroquinoline for TA98 strain under non-metabolic activation conditions as positive control -1-oxide DMSO solution, for TA100 strain, 0.25 ⁇ g / mL 2- (2-furyl) -3- (5-nitro-2-furyl) acrylamide DMSO solution, for metabolic activation conditions, for TA98 strain 40 ⁇ g / mL 2-aminoanthracene DMSO solution and 20 ⁇ g / mL 2-aminoanthracene DMSO solution for the TA100 strain, respectively, and test bacterial solution 588 ⁇ L (under metabolic activation conditions, test bacterial solution 498 ⁇ L and S9 mix 90 ⁇ L) and incubate at 37 ° C for 90 minutes with shaking.
- Test Example 7 Solubility test
- Three-level evaluation was performed (High;> 40 ⁇ M, Medium; 3 to 40 ⁇ M, Low; ⁇ 3 ⁇ M).
- Compound I-9 High.
- Test Example 8 Metabolic stability test
- the target compound was allowed to react for a certain period of time, and the residual rate was calculated by comparing the reaction sample with the unreacted sample to evaluate the degree of metabolism in the liver.
- Human liver microsomes 0.5 mg protein / mL in 0.2 mL buffer (50 mmol / L tris-HCl pH 7.4, 150 mmol / L potassium chloride, 10 mmol / L magnesium chloride) in the presence of 1 mmol / L NADPH
- the reaction was carried out at 0 ° C. for 0 minutes or 30 minutes (oxidative reaction).
- test compound in the centrifugal supernatant was quantified by LC / MS / MS, and the remaining amount of the test compound after the reaction was calculated with the amount of the compound at 0 minute reaction as 100%.
- the absolute value of the maximum tail current was measured from the obtained I Kr using the analysis software (DataXpress ver. 1, Molecular Devices Corporation) based on the current value at the holding membrane potential. Furthermore, the inhibition rate with respect to the maximum tail current before application of the test substance was calculated, and compared with the medium application group (0.1% dimethyl sulfoxide solution), the influence of the test substance on I Kr was evaluated. (result) Compound I-1: 3.2%.
- Test Example 10 Powder solubility test
- JP-1 solution 2.0 g sodium chloride, 7.0 mL hydrochloric acid to add 1000 mL
- JP-2 solution 500 mL pH 6.8 phosphate buffer, 500 mL water
- TCA sodium taurocholate
- JP-2 solution water was added to TCA 1.08 g to make 100 mL
- 200 ⁇ L each was added.
- When dissolving after adding the test solution add bulk powder as appropriate. Seal and shake at 37 ° C for 1 hour. Filter, add 100 ⁇ L of methanol to 100 ⁇ L of each filtrate and dilute 2 times. Change the dilution factor as necessary. Check for bubbles and precipitates, seal and shake. Quantify using HPLC with the absolute calibration curve method.
- Intravenous administration is performed from the tail vein using a syringe with an injection needle.
- Evaluation items Blood is collected over time, and the drug concentration in plasma is measured using LC / MS / MS.
- Rats are intravenously administered at a dose of 0.5 mg / mL / kg, and 30 minutes later, they are exsanguinated by whole blood collection from the lower aorta under isoflurane anesthesia. Thereafter, the brain was removed and 20-25% homogenate was prepared with distilled water. On the other hand, the obtained blood is made into plasma after centrifugation. Thereafter, control plasma was added to the brain sample, and control brain was added to the plasma sample at a ratio of 1: 1, and each sample was measured using LC / MS / MS. The obtained area ratio (brain / plasma) at the time of measurement was defined as the brain Kp value. (result) Compound I-11: 2.2.
- Formulation Example 1 A granule containing the following ingredients is produced.
- Formulation Example 2 A capsule filling granule containing the following ingredients is produced.
- Formulation Example 3 A tablet containing the following ingredients is produced.
- Formulation Example 4 The following ingredients are heated and mixed and then sterilized to give an injection.
- the compound of the present invention can be a useful drug as a therapeutic agent for diseases induced by production, secretion and / or deposition of amyloid ⁇ protein.
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Dermatology (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen- Or Sulfur-Containing Heterocyclic Ring Compounds With Rings Of Six Or More Members (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
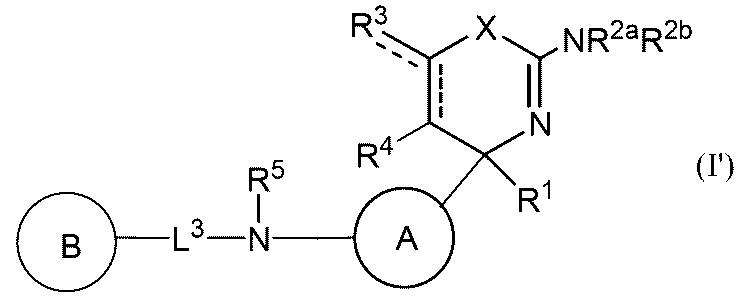
(1)式(I):
(式中、R1は置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアシル、シアノ、カルボキシ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアルケニルオキシカルボニル、置換もしくは非置換のアルキニルオキシカルボニル、置換もしくは非置換のカルバモイル、置換もしくは非置換のチオカルバモイル、置換もしくは非置換の炭素環式基または置換もしくは非置換の複素環式基であり、
R2aおよびR2bは各々独立して水素、置換もしくは非置換のアルキル、置換もしくは非置換のアシル、置換もしくは非置換のアルコキシカルボニルまたは置換もしくは非置換のカルバモイルであり、
XはSまたはOであり、
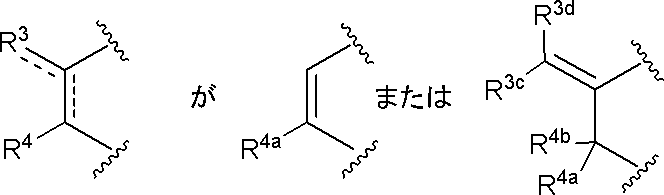
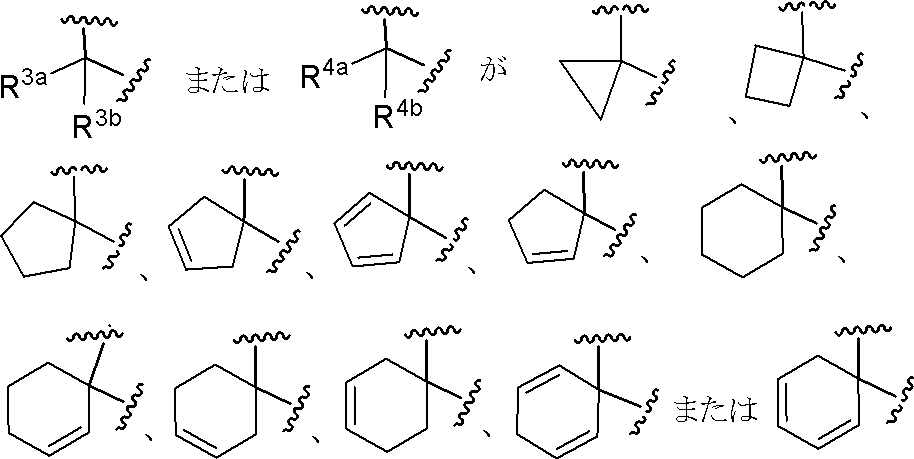
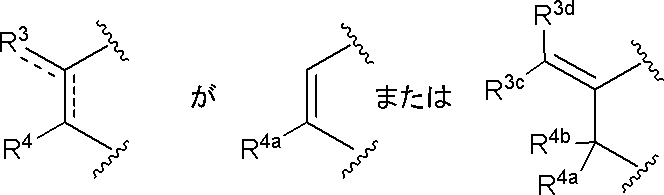
XがSのとき、
であり、
XがOのとき、
であり、
R3a、R3b、R4aおよびR4bは各々独立して、
水素、ハロゲン、ヒドロキシ、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアシル、置換もしくは非置換のアシルオキシ、置換もしくは非置換のアルコキシ、置換もしくは非置換のアルケニルオキシ、置換もしくは非置換のアルキニルオキシ、置換もしくは非置換のアルキルチオ、置換もしくは非置換のアルケニルチオ、置換もしくは非置換のアルキニルチオ、カルボキシ、シアノ、ニトロ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアルケニルオキシカルボニル、置換もしくは非置換のアルキニルオキシカルボニル、置換もしくは非置換のアミノ、置換もしくは非置換のカルバモイル、置換もしくは非置換のチオカルバモイル、置換もしくは非置換のスルファモイル、置換もしくは非置換のアルキルスルフィニル、置換もしくは非置換のアルケニルスルフィニル、置換もしくは非置換のアルキニルスルフィニル、置換もしくは非置換のアルキルスルホニル、置換もしくは非置換のアルケニルスルホニル、置換もしくは非置換のアルキニルスルホニル、置換もしくは非置換の炭素環式基、置換もしくは非置換の炭素環オキシ、置換もしくは非置換の炭素環チオ、置換もしくは非置換の炭素環アルキル、置換もしくは非置換の炭素環アルコキシ、置換もしくは非置換の炭素環オキシカルボニル、置換もしくは非置換の炭素環スルフィニル、置換もしくは非置換の炭素環スルホニル、置換もしくは非置換の複素環式基、置換もしくは非置換の複素環オキシ、置換もしくは非置換の複素環チオ、置換もしくは非置換の複素環アルキル、置換もしくは非置換の複素環アルコキシ、置換もしくは非置換の複素環オキシカルボニル、置換もしくは非置換の複素環スルフィニルまたは置換もしくは非置換の複素環スルホニルであり、
R3aおよびR3bが、それらが結合する炭素原子と一緒になって置換もしくは非置換の炭素環または置換もしくは非置換の複素環を形成してもよく、
R4aおよびR4bが、それらが結合する炭素原子と一緒になって置換もしくは非置換の炭素環または置換もしくは非置換の複素環を形成してもよく、
R3cおよびR3dは各々独立して水素、ハロゲン、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシ、置換もしくは非置換のアルケニルオキシ、置換もしくは非置換のアルキニルオキシ、置換もしくは非置換のアルキルチオ、置換もしくは非置換のアルケニルチオ、置換もしくは非置換のアルキニルチオ、置換もしくは非置換のアシル、カルボキシ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアルケニルオキシカルボニル、置換もしくは非置換のアルキニルオキシカルボニル、置換もしくは非置換のアミノ、置換もしくは非置換のカルバモイル、置換もしくは非置換のチオカルバモイル、置換もしくは非置換の炭素環式基、置換もしくは非置換の炭素環オキシ、置換もしくは非置換の炭素環チオ、置換もしくは非置換の炭素環アルキル、置換もしくは非置換の炭素環アルコキシ、置換もしくは非置換の炭素環オキシカルボニル、置換もしくは非置換の複素環式基、置換もしくは非置換の複素環オキシ、置換もしくは非置換の複素環チオ、置換もしくは非置換の複素環アルキル、置換もしくは非置換の複素環アルコキシまたは置換もしくは非置換の複素環オキシカルボニルであるか、またはR3cおよびR3dが、それらが結合する炭素原子と一緒になって置換もしくは非置換の非芳香族炭素環または置換もしくは非置換の非芳香族複素環を形成し、
R5は水素、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニルまたは置換もしくは非置換のアシルであり、
L1およびL2は各々独立して単結合、置換もしくは非置換のアルキレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)、置換もしくは非置換のアルケニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)または置換もしくは非置換のアルキニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)であり、
環Aは置換もしくは非置換の炭素環または置換もしくは非置換の複素環であり、
1)L1およびL2が単結合であり、
であるとき、
環Bは置換もしくは非置換の炭素環、置換もしくは非置換のピリジン、置換もしくは非置換のピリミジンまたは置換もしくは非置換の5員複素環であり、
2)L1およびL2が単結合であり、
であるとき、
環Bは置換もしくは非置換の炭素環または置換もしくは非置換の複素環であり、
3)L1およびL2の少なくとも一方が置換もしくは非置換のアルキレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)、置換もしくは非置換のアルケニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)または置換もしくは非置換のアルキニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)であるとき、
環Bは置換された含窒素芳香族単環である。ただし、以下の化合物を除く。
)
で示される化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
R2aおよびR2bは各々独立して水素、置換もしくは非置換のアルキルまたは置換もしくは非置換のアシルであり、
XはSまたはOであり、
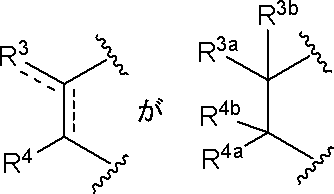
XがSのとき、
XがOのとき、
R3aおよびR3bは各々独立して
水素、ハロゲン、ヒドロキシ、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアシル、置換もしくは非置換のアルコキシ、置換もしくは非置換のアリールアルキル、置換もしくは非置換のヘテロアリールアルキル、置換もしくは非置換のアリールアルコキシ、置換もしくは非置換のヘテロアリールアルコキシ、置換もしくは非置換のアルキルチオ、カルボキシ、シアノ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアミノ、置換もしくは非置換のカルバモイル、置換もしくは非置換の炭素環式基または置換もしくは非置換の複素環式基であり、
R3cおよびR3dは各々独立して
水素、ハロゲン、置換もしくは非置換のアルキルであるか、R3cおよびR3dが、それらが結合する炭素原子と一緒になって置換もしくは非置換の非芳香族炭素環を形成し、
R4aおよびR4bは各々独立して水素または置換もしくは非置換のアルキルであり、
R5は水素、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニルまたは置換もしくは非置換のアシルであり、
L3は単結合、置換もしくは非置換のアルキレン(ただし置換基としてオキソおよびチオキソは除く)、置換もしくは非置換のアルケニレン(ただし置換基としてオキソおよびチオキソは除く)または置換もしくは非置換のアルキニレン(ただし置換基としてオキソおよびチオキソは除く)であり、
環Aは置換もしくは非置換の炭素環または置換もしくは非置換の複素環であり、
1)L3が単結合であり、
環Bは置換もしくは非置換の炭素環、置換もしくは非置換のピリジン、置換もしくは非置換のピリミジンまたは置換もしくは非置換の5員複素環であり、
2)L3が単結合であり、
環Bは置換もしくは非置換の炭素環または置換もしくは非置換の複素環であり、
3)L3が置換もしくは非置換のアルキレン、置換もしくは非置換のアルケニレンまたは置換もしくは非置換のアルキニレンであるとき、
環Bは置換された含窒素芳香族単環である)
で示される化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
本明細書中、「結合する炭素原子と一緒になって置換もしくは非置換の非芳香族炭素環を形成」するとは、2個の置換基が一緒になって上記「シクロアルキル」または「シクロアルケニル」を形成することをいう。
である場合等を包含する。これらは、置換基群αから選択される1以上の基で置換されたアルキル、非置換アルキルおよび置換基群αからなる群から選択される1以上の基で任意の位置が置換されていてもよい。
インドリル、イソインドリル、インダゾリル、インドリジニル、インドリニル、イソインドリニル、キノリル、イソキノリル、シンノリニル、フタラジニル、キナゾリニル、ナフチリジニル、キノキサリニル、プリニル、プテリジニル、ベンゾピラニル、ベンズイミダゾリル、ベンゾトリアゾリル、ベンズイソオキサゾリル、ベンズオキサゾリル、ベンズオキサジアゾリル、ベンゾイソチアゾリル、ベンゾチアゾリル、ベンゾチアジアゾリル、ベンゾフリル、イソベンゾフリル、ベンゾチエニル、ベンゾトリアゾリル、チエノピリジル、チエノピロリル、チエノピラゾリル、チエノピラジニル、フロピロリル、チエノチエニル、イミダゾピリジル、イミダゾピラゾリル、ピラゾロピリジル、ピラゾロピラジニル、チアゾロピリジル、ピラゾロピリミジニル、ピラゾロトリアニジル、ピリダゾロピリジル、トリアゾロピリジル、イミダゾチアゾリル、ピラジノピリダジニル、ジヒドロチアゾロピリミジニル、テトラヒドロキノリル、テトラヒドロイソキノリル、ジヒドロベンゾフリル、ジヒドロベンズオキサジニル、ジヒドロベンズイミダゾリル、テトラヒドロベンゾチエニル、テトラヒドロベンゾフリル、ベンゾジオキソリル、ベンゾジオキソニル、クロマニル、クロメニル、オクタヒドロクロメニル、ジヒドロベンゾジオキシニル、ジヒドロベンゾオキセジニル、ジヒドロベンゾジオキセピニル、ジヒドロチエノジオキシニル、等の2環の縮合複素環式基;
カルバゾリル、アクリジニル、キサンテニル、フェノチアジニル、フェノキサチイニル、フェノキサジニル、ジベンゾフリル、イミダゾキノリル、テトラヒドロカルバゾリル、等の3環の縮合複素環式基等を包含する。例えば、5~6員のヘテロアリールまたは非芳香族複素環式基である。
本明細書中、「結合する炭素原子と一緒になって置換もしくは非置換の非芳香族複素環を形成」するとは、2個の置換基が一緒になって上記「非芳香族複素環」を形成することをいう。
である場合等を包含する。これらは、置換基群αから選択される1以上の基で置換されたアルキル、非置換アルキルおよび置換基群αからなる群から選択される1以上の基で任意の位置が置換されていてもよい。
置換基群αから選択される基(例えば、ハロゲン、ヒドロキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、カルバモイル、アミノ、シアノ、アルキルアミノおよび/またはアルキルチオ等);
置換基群α、ヒドロキシイミノおよびアルコキシイミノからなる群から選択される1以上の基で置換されたアルキル(ここで置換基としては、例えば、ハロゲン、ヒドロキシ、アルコキシおよび/またはアルコキシカルボニル等)、もしくは非置換アルキル;
置換基群αから選択される1以上の基で置換されたアミノアルキル(ここで置換基としては、例えば、アシル、アルキルおよび/またはアルコキシ等);
置換基群αから選択される1以上の基で置換されたアルケニル(ここで置換基としては、例えば、アルコキシカルボニル、ハロゲンおよび/またはハロゲノアルコキシカルボニル等)、もしくは非置換アルケニル;
置換基群αから選択される1以上の基で置換されたアルキニル(ここで置換基としては、例えば、アルコキシカルボニル等)、もしくは非置換アルキニル;
置換基群αから選択される1以上の基で置換されたアルコキシ(ここで置換基としては、例えば、ハロゲン、カルバモイル、アルキルカルバモイルおよび/またはヒドロキシアルキルカルバモイル等)、もしくは非置換アルコキシ;
置換基群αから選択される1以上の基で置換されたアルコキシアルコキシ;
置換基群αから選択される1以上の基で置換されたアルケニルオキシ(ここで置換基として、例えば、ハロゲン、ヒドロキシ、アミノおよび/またはアルキルアミノ等)、もしくは非置換アルケニルオキシ;
置換基群αから選択される1以上の基で置換されたアルコキシアルケニルオキシ、もしくは非置換アルコキシアルケニルオキシ;
置換基群αから選択される1以上の基で置換されたアルキニルオキシ(ここで置換基として、例えば、ハロゲンおよび/またはヒドロキシ等)、もしくは非置換アルキニルオキシ;
置換基群αから選択される1以上の基で置換されたアルコキシアルキニルオキシ;
置換基群αから選択される1以上の基で置換されたアルキルチオ、もしくは非置換アルキルチオ;
置換基群αから選択される1以上の基で置換されたアルケニルチオ、もしくは非置換アルケニルチオ;
置換基群αから選択される1以上の基で置換されたアルキニルチオ、もしくは非置換アルキニルチオ;
置換基群αから選択される1以上の基で置換されたアルキルアミノ;
置換基群αから選択される1以上の基で置換されたアルケニルアミノ;
置換基群αから選択される1以上の基で置換されたアルキニルアミノ;
置換基群αおよびアルキリデンから選択される1以上の基で置換されたアミノオキシ、もしくは非置換アミノオキシ;
置換基群αから選択される1以上の基で置換されたアシル;
置換基群αから選択される1以上の基で置換されたアルキルスルホニル、もしくは非置換アルキルスルホニル;
置換基群αから選択される1以上の基で置換されたアルキルスルフィニル、もしくは非置換アルキルスルフィニル;
置換基群αから選択される1以上の基で置換されたアルキルスルファモイル、もしくは非置換アルキルスルファモイル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環式基(例えばシクロアルキル、アリール等)、もしくは非置換炭素環式基(例えばシクロアルキル、アリール等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環式基、もしくは非置換複素環式基;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環アルキル(例えばシクロアルキルアルキル、アリールアルキル等)、もしくは非置換炭素環アルキル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環アルキル、もしくは非置換複素環アルキル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環オキシ(例えばシクロアルキルオキシ、アリールオキシ等)、もしくは非置換炭素環オキシ(例えばシクロアルキルオキシ、アリールオキシ等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環オキシ、もしくは非置換複素環オキシ;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環アルコキシ(例えばシクロアルキルアルコキシ、アリールアルコキシ等)、もしくは非置換炭素環アルコキシ(例えばシクロアルキルアルコキシ、アリールアルコキシ等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環アルコキシ、もしくは非置換複素環アルコキシ;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環アルコキシカルボニル(例えばシクロアルキルアルコキシカルボニル、アリールアルコキシカルボニル等)、もしくは非置換炭素環アルコキシカルボニル(例えばシクロアルキルアルコキシカルボニル、アリールアルコキシカルボニル等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環アルコキシカルボニル、もしくは非置換複素環アルコキシカルボニル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環チオ(例えばシクロアルキルチオ、アリールチオ等)、もしくは非置換炭素環チオ(例えばシクロアルキルチオ、アリールチオ等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環チオ、もしくは非置換複素環チオ;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環アミノ(例えばシクロアルキルアミノ、アリールアミノ等)、もしくは非置換炭素環アミノ(例えばシクロアルキルアミノ、アリールアミノ等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環アミノ、もしくは非置換複素環アミノ;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環アルキルアミノ(例えばシクロアルキルアルキルアミノ、アリールアルキルアミノ等)、もしくは非置換炭素環アルキルアミノ(例えばシクロアルキルアルキルアミノ、アリールアルキルアミノ等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環アルキルアミノ、もしくは非置換複素環アルキルアミノ;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環スルファモイル(例えばシクロアルキルスルファモイル、アリールスルファモイル等)、もしくは非置換炭素環スルファモイル(例えばシクロアルキルスルファモイル、アリールスルファモイル等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環スルファモイル、もしくは非置換複素環スルファモイル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環スルホニル(例えばシクロアルキルスルホニル、アリールスルホニル等)、もしくは非置換炭素環スルホニル(例えばシクロアルキルスルホニル、アリールスルホニル等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環スルホニル、もしくは非置換複素環スルホニル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環カルバモイル(例えばシクロアルキルカルバモイル、アリールカルバモイル等)、もしくは非置換炭素環カルバモイル(例えばシクロアルキルカルバモイル、アリールカルバモイル等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環カルバモイル、もしくは非置換複素環カルバモイル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環アルキルカルバモイル(例えばシクロアルキルアルキルカルバモイル、アリールアルキルカルバモイル)、もしくは非置換炭素環アルキルカルバモイル(例えばシクロアルキルアルキルカルバモイル、アリールアルキルカルバモイル);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環アルキルカルバモイル、もしくは非置換複素環アルキルカルバモイル;
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された炭素環オキシカルボニル(例えばシクロアルキルオキシカルボニル、アリールオキシカルボニル等)、もしくは非置換炭素環オキシカルボニル(例えばシクロアルキルオキシカルボニル、アリールオキシカルボニル等);
置換基群α、アジド、アルキルおよびハロゲノアルキルからなる群から選択される1以上の基で置換された複素環オキシカルボニル、もしくは非置換複素環オキシカルボニル;
ハロゲンで置換されたアルキレンジオキシもしくは非置換アルキレンジオキシ;
オキソ;
アジド等が挙げられる。これらから選択される1以上の基で置換されていてもよい。
A.式(I)で示される化合物の製造
一般式(a)で示される化合物は、市販品であるか、あるいは公知(Tetrahedron、2009年、第65巻、757~764頁)の方法ならびにそれらに準ずる方法で合成することができる。また、一般式(b)に示される化合物は、例えば特許文献1(WO2007/049532)、特許文献2(WO2008/133274)、特許文献3(WO2008/133273)に記載の方法に準じて、あるいは後述する一般調製法により製造することができる。
化合物(a)と化合物(b)をメタノール、エタノール、イソプロピルアルコール、ブタノール、イソブタノール、sec-ブタノール、酢酸、水などの溶媒中、またはそれらの混合溶媒中、塩酸、硫酸、トリフルオロ酢酸、メタンスルホン酸、トリフルオロメタンスルホン酸、過塩素酸などの酸を加え、0℃~180℃、好ましくは20℃~140℃で、0.1時間~120時間、好ましくは、0.5時間~72時間反応させることにより、一般式(I)で示される化合物を得ることができる。
化合物(a)と化合物(b)をトルエン、テトラヒドロフラン、ジメチルホルムアミド、1,2-ジメトキシエタン、1,4-ジオキサン、メタノール等の溶媒中、トリエチルアミン、炭酸ナトリウム、炭酸カリウム、炭酸セシウム、ナトリウムメトキシド、カリウムtert-ブトキシド、n-ブチルリチウム、リチウムヘキサメチルジシラジド、ナトリウムヘキサメチルジシラジド、カリウムヘキサメチルジシラジド等の塩基存在下、0℃~180℃、好ましくは20℃~140℃で、0.5時間~100時間、好ましくは、0.5時間~72時間反応させることにより一般式(I)で示される化合物を得ることができる。
式(b)で示される化合物は、例えば以下に示す化合物b-1、b-2、b-3、b-4、b-5またはb-6の合成法に従って、製造することができる。
第一工程
トルエン、ジクロロメタン、テトラヒドロフラン等の溶媒中、またはそれらの混合溶媒中、リチウムジイソプロピルアミド等の塩基の存在下で、プロピオン酸t-ブチル等の目的とするエステルとを反応させて得たエノラートに、クロロチタニウムトリイソプロポキシド等のチタニウム試薬を加え、公知の方法により調製できる化合物cを加えて、-80℃~30℃、好ましくは-80℃~0℃で、0.1時間~24時間、好ましくは、0.1時間~12時間反応させることにより化合物dを得ることができる。
化合物dを、ジオキサン、メタノール、ジクロロメタン等の溶媒中、またはそれらの混合溶媒中、塩酸、臭化水素酸、硫酸、トリフルオロ酢酸等の酸の存在下、0℃~80℃、好ましくは0℃~30℃で、0.5時間~48時間、好ましくは、1時間~24時間反応させることにより化合物eを得ることができる。
化合物eを、ジオキサン、テトラヒドロフラン、トルエン等の溶媒中、またはそれらの混合溶媒中、ボラン、水素化ナトリウム、水素化リチウムアルミニウム等の還元剤を加え、-80℃~80℃、好ましくは-20℃~30℃で、0.5時間~48時間、好ましくは、1時間~12時間反応させることにより化合物fを得ることができる。
化合物fを、ジメチルスルホキシド、ジクロロメタン等の溶媒中、2-ヨードキシ安息香酸等の酸化剤を加え、0℃~80℃、好ましくは10℃~40℃で、0.5時間~48時間、好ましくは、1時間~12時間反応させることにより化合物gを得ることができる。
化合物gをジオキサン、テトラヒドロフラン、トルエン、アセトン等の溶媒中、またはそれらの混合溶媒中、市販または公知の方法により調製した保護基を有するイソチオシアネート(例えば、ベンゾイルイソチオシアネート)を加え、-30℃~50℃、好ましくは-10℃~25℃で、0.1時間~12時間、好ましくは、0.1時間~3時間反応させ、続いて、濃硫酸、濃硝酸等を加えて、0℃~100℃、好ましくは0℃~60℃で、0.5時間~24時間、好ましくは、1時間~12時間反応させることにより化合物b-1を得ることができる。
第一工程
トルエン、ジクロロメタン、テトラヒドロフラン等の溶媒中、またはそれらの混合溶媒中、リチウムジイソプロピルアミド、カリウムヘキサメチルジシラジド等の塩基の存在下で、対応するアルキルケトン(例えば、3-メチル-2-ブタノン等)を反応させて得たエノラートに、公知の方法により調製できる化合物cを加えて、-80℃~30℃、好ましくは-80℃~0℃で、0.1時間~24時間、好ましくは、0.1時間~12時間反応させることにより化合物hを得ることができる。
第一工程で得られた化合物hに塩酸、臭化水素酸、トリフルオロ酢酸等を加え、0℃~60℃、好ましくは0℃~30℃で、0.1時間~24時間、好ましくは、0.5時間~12時間反応させることにより化合物iを得ることができる。
化合物iをジオキサン、テトラヒドロフラン、トルエン、アセトン等の溶媒中、またはそれらの混合溶媒中、市販または公知の方法により調製した保護基を有するイソチオシアネート(例えば、ベンゾイルイソチオシアネート)を加え、-30℃~70℃、好ましくは-20℃~50℃で、0.1時間~12時間、好ましくは、0.1時間~6時間反応させ、続いて、溶媒を留去した後に濃硫酸、濃硝酸等を加え-30℃~70℃、好ましくは-20℃~50℃で、1時間~12時間、好ましくは、1時間~6時間反応させることにより化合物b-2を得ることができる。
第一工程
トルエン、ジクロロメタン、テトラヒドロフラン等の溶媒中、またはそれらの混合溶媒中、臭化アリルマグネシウムなどのグリニヤール試薬に、公知の方法により調製できる化合物cを加えて、-80℃~30℃、好ましくは-80℃~0℃で、0.1時間~24時間、好ましくは、0.1時間~12時間反応させることにより化合物jを得ることができる。
第一工程で得られた化合物jにメタノール、エタノール、水等の溶媒中、またはそれらの混合溶媒中、塩酸溶液を加え、-20℃~80℃、好ましくは0℃~30℃で、0.1時間~24時間、好ましくは、0.1時間~12時間反応させることにより化合物kを得ることができる。
化合物kをジクロロメタン、ジオキサン、テトラヒドロフラン、トルエン、アセトン等の溶媒中、またはそれらの混合溶媒中、市販または公知の方法により調製した保護基を有するイソチオシアネート(例えば、ベンゾイルイソチオシアネート)を加え、-30℃~70℃、好ましくは-20℃~50℃で、0.1時間~12時間、好ましくは、0.1時間~6時間反応させることにより、化合物lを得ることができる。
化合物lをジクロロメタンなどの溶媒中、ヨウ素、臭素、N-ブロモスクシンイミド(NBS)等のハロゲニウム陽イオン源を加え、-20℃~40℃、好ましくは0℃~20℃で、0.1時間~12時間、好ましくは、0.1時間~6時間反応させることにより化合物mを得ることができる。
化合物mをジオキサン、テトラヒドロフラン、トルエンなどの溶媒中、またはそれらの混合溶媒中、ピロリジン、ピペリジン、ピペラジン、モルホリンなどの塩基を加え、20℃~100℃、好ましくは40℃~80℃で、0.1時間~24時間、好ましくは、1時間~12時間反応させることにより化合物b-3を得ることができる。
第一工程
トルエン、ジクロロメタン、テトラヒドロフラン等の溶媒中、またはそれらの混合溶媒中、アミノ基を適宜保護基で保護した化合物kをアクリル酸エチルとグラブス試薬を加え、オレフィンメタセシス反応に付すことにより化合物nを得ることができる。反応温度は-20℃~60℃、好ましくは0℃~30℃であり、反応時間は0.5時間~24時間、好ましくは、1時間~12時間である。
化合物nをジクロロメタン、ジオキサン、テトラヒドロフラン、トルエン、アセトン等の溶媒中、またはそれらの混合溶媒中、市販または公知の方法により調製した保護基を有するイソチオシアネート(例えば、ベンゾイルイソチオシアネート)を加え、-30℃~70℃、好ましくは-20℃~50℃で、0.1時間~12時間、好ましくは、0.1時間~6時間反応させることにより、化合物oを得ることができる。
化合物oをジオキサン、テトラヒドロフラン、トルエンなどの溶媒中、またはそれらの混合溶媒中、水素化ジイソブチルアルミニウム、水素化リチウムアルミニウム、水素化ホウ素ナトリウムなどを加えて還元反応に付し、-80℃~0℃、好ましくは-80℃~-20℃で、0.1時間~12時間、好ましくは、0.1時間~3時間反応させることにより化合物b-4を得ることができる。
である。
酢酸および水の混合溶媒中、化合物qに鉄を加え、20℃~120℃、好ましくは50℃~80℃で0.5時間~48時間、好ましくは6時間~20時間反応させることにより、化合物b-6を得ることが出来る。
第一工程
市販または公知の方法により調製できる化合物rをエーテル、テトラヒドロフラン等の溶媒またはエーテル-テトラヒドロフラン等の混合溶媒中、-100℃~50℃、好ましくは-80℃~0℃にてビニルマグネシウムクロリド、ビニルマグネシウムブロミド、プロペニルマグネシウムブロミド等の目的とする化合物に対応する置換基を有するグリニヤール試薬を加えて0.2時間~24時間、好ましくは0.5時間~5時間反応させることにより、化合物sを得ることができる。
化合物sにトルエン等の溶媒の存在下または非存在下に酢酸、トリフルオロ酢酸、塩酸、硫酸等の酸またはそれらの混合物中、チオ尿素またはN-メチルチオ尿素、N,N’-ジメチルチオ尿素等の目的とする化合物に対応する置換基を有する置換チオ尿素を加え、-20℃~100℃好ましくは0℃~50℃で0.5時間~120時間、好ましくは1時間~72時間反応させることにより、化合物tを得ることができる。
化合物tにトルエン等の溶媒の存在下または非存在下にトリフルオロ酢酸、メタンスルホン酸、トリフルオロメタンスルホン酸等の酸またはそれらの混合物を加え、-20℃~100℃好ましくは0℃~50℃で0.5~120時間好ましくは1時間~72時間反応させることにより、b-7を得ることができる。
第一工程
市販または公知の方法により調製できる化合物uをトルエン、クロロホルム、テトラヒドロフラン等の溶媒中、水および塩酸、硫酸等の酸の存在下にチオシアン酸ナトリウム、チオシアン酸アンモニウム等のチオシアン酸塩を0℃~150℃好ましくは20℃~100℃で0.5時間~24時間、好ましくは1時間~12時間反応させることにより、化合物vを得ることができる。
化合物vにテトラヒドロフラン、メタノール、エタノール、水などの溶媒中またはエタノール-水等の混合溶媒中、リン酸二水素ナトリウム等の緩衝剤存在下または非存在下、水素化ホウ素ナトリウム等の還元剤を加え、-80℃~50℃、好ましくは-20℃~20℃で0.1時間~24時間、好ましくは0.5時間~12時間反応させることにより、化合物wを得ることができる。
化合物wをトルエン、ジクロロメタン等の溶媒の存在下または非存在下に、塩化チオニル、オキシ塩化リン、四臭化炭素-トリフェニルホスフィン等のハロゲン化剤と-80℃~50℃、好ましくは-20℃~20℃で0.1時間~24時間、好ましくは0.5時間~12時間反応させるか、化合物wにトルエン、ジクロロメタン等の溶媒中、トリエチルアミン等の塩基の存在下にメタンスルホニルクロリド、p-トルエンスルホニルクロリド等のスルホン化剤を-80℃~50℃、好ましくは-20℃~20℃で0.1時間~24時間、好ましくは0.5時間~12時間反応させることにより化合物xを得ることができる。
化合物xにメタノール、エタノール、水等の溶媒中またはメタノール-水等の混合溶媒中アンモニアまたはメチルアミン等の第一アミンを、-20℃~80℃、好ましくは0℃~40℃で0.5時間~48時間、好ましくは1時間~24時間反応させることにより、化合物b-8を得ることができる。
第一工程
市販または公知の方法により調製できる化合物yにトルエン、t-ブチルアルコール、テトラヒドロフラン等の溶媒中、ジイソプロピルエチルアミン、トリエチルアミン、ピリジンなどの塩基の存在下、アジ化ジフェニルホスホリル等のアジド化剤を、0℃~200℃、好ましくは40℃~150℃で1時間~48時間、好ましくは0.5時間~24時間反応させることにより、化合物zを得ることができる。
化合物zに、トルエン、キシレン、ジメチルホルムアミド、テトラヒドロフラン等の溶媒中、t-ブチルアルコール、3,4-ジメトキシベンジルアルコール、4-メトキシベンジルアルコール等のアルコールを、0℃~300℃、好ましくは50℃~200℃で1時間~800時間、好ましくは5時間~500時間反応させることにより、化合物aaを得ることができる。
化合物aaを水、トルエン、ジクロロメタン、メタノール、1,4-ジオキサン、酢酸、酢酸エチル等の溶媒の存在下または非存在下に、塩酸、硫酸、臭化水素酸、トリフルオロ酢酸等の酸の存在下で0℃~200℃、好ましくは25℃~150℃で0.1時間~48時間、好ましくは0.5時間~24時間反応させることにより化合物abを得ることができる。
化合物abにアセトン、トルエン、クロロホルム、テトラヒドロフラン、水等の溶媒中、またはそれらの混合溶媒中、ジイソプロピルエチルアミン、トリエチルアミン、ピリジン等の塩基の存在下、メチルイソチオシアナート、エチルイソチオシアナート等の目的とする化合物に対応するイソチオシアナートあるいは、N,N-ジメチルチオカルバモイルクロリド、N,N-ジエチルチオカルバモイルクロリド等の目的とする化合物に対応するチオカルバモイルハライドを0℃~150℃好ましくは20℃~100℃で0.5時間~120時間、好ましくは1時間~72時間反応させることにより、化合物acを得ることができる。
化合物acに、アセトン、アセトニトリル、ジメチルホルムアミド、テトラヒドロフラン等の溶媒中、ジイソプロピルエチルアミン、トリエチルアミン、ピリジン、水酸化ナトリウム等の塩基の存在下または非存在下、ヨウ化メチル、ジエチル硫酸、ベンジルブロミド等のアルキル化剤を、0℃~200℃、好ましくは40℃~150℃で1時間~48時間、好ましくは0.5時間~24時間反応させることにより、化合物adを得ることができる。
化合物adに、アセトン、アセトニトリル、ジメチルホルムアミド、テトラヒドロフラン、ジクロロメタン等の溶媒中、ジイソプロピルエチルアミン、トリエチルアミン、ピリジン、水酸化ナトリウム等の塩基の存在下、0℃~200℃、好ましくは10℃~150℃で1時間~120時間、好ましくは0.5時間~100時間反応させることにより、化合物b-9を得ることができる。
市販または公知の方法により調製できる化合物rをエーテル、テトラヒドロフラン、トルエン、ベンゼン等の溶媒またはエーテル-テトラヒドロフラン等の混合溶媒中、60℃~120℃、好ましくは80℃~100℃にて、モレキュラーシーブスまたは硫酸マグネシウム等の存在下、またはディーンスタークを用いて連続的に脱水を行いながら、または上記文献に記載の方法に準じてα-メチルベンジルアミン、p-トルエンスルフィンアミドまたはtert-ブチルスルフィンアミド等の目的とする化合物に対応する置換基を有する試薬を加えて0.5時間~24時間、好ましくは0.5時間~5時間反応させることにより、化合物aeを得ることができる。
市販または公知の方法により調製できる酢酸エステル等の目的とする化合物に対応する置換基を有する試薬のリチウム、アルミニウム、亜鉛、チタン等のエノラート、または酢酸エステル等の目的とする化合物に対応する置換基を有する試薬から調整されるケテンシリルアセテートをエーテル、テトラヒドロフラン、トルエン、塩化メチレン等の溶媒またはエーテル-テトラヒドロフラン等の混合溶媒中、四塩化チタン、三フッ化ホウ素エーテル錯体等のルイス酸存在化または非存在下、-100℃~50℃、好ましくは-80℃~-30℃にて化合物aeと0.5時間~24時間、好ましくは0.5時間~5時間反応させる、または、上記文献(1),(3)に記載の方法に準じて、化合物afを得ることができる。
エーテル、テトラヒドロフラン等の溶媒またはエーテル-テトラヒドロフラン等の混合溶媒中、化合物afに-100℃~50℃、好ましくは-80℃~30℃にてメチルマグネシウムクロリド、エチルマグネシウムブロミド等の目的とする化合物に対応する置換基を有するグリニヤール試薬を加える、または化合物afからワインレブアミド(Weinreb Amide)を経由して、R3aMgBr、R3bMgBr等の目的とする化合物に対応する置換基を有するグリニヤール試薬を順次作用させて、0.2時間~24時間、好ましくは0.2時間~5時間反応させることにより、化合物agを得ることができる。
化合物agを塩化水素、トリフルオロ酢酸等を含むメタノール、エタノール、エーテル、テトラヒドロフラン、1,4-ジオキサン、塩化メチレン、酢酸エチル等の溶媒中、または、無溶媒下、トリフルオロ酢酸中、-30℃~100℃、好ましくは-10℃~90℃にて、0.5時間~12時間、好ましくは0.5時間~5時間反応させることにより、化合物ahを得ることができる。
化合物ahの塩化メチレン、トルエン等の溶媒中、または塩化メチレン-水等の混合溶媒中、炭酸カルシウム、炭酸カリウム等を加え、-30℃~50℃、好ましくは-10℃~25℃にて、チオホスゲンを加え、0.5時間~12時間、好ましくは0.5時間~5時間反応させることにより、化合物aiを得ることができる。
化合物aiの塩化メチレン、テトラヒドロフラン、トルエン等の溶媒中、-30℃~50℃、好ましくは-10℃~20℃にてオキサリルクロライド、チオニルクロライド等と触媒量のN,N-ジメチルホルムアミドを加え、0℃~100℃、好ましくは20℃~90℃にて、0.5時間~12時間、好ましくは0.5時間~5時間反応させることにより、またはComprehensive Organic Transformations, Richard C Larock(Mcgraw-Hill)記載の方法で化合物ajを得ることができる。
化合物ajの酢酸エチル、塩化メチレン、テトラヒドロフラン、トルエン等の溶媒中、-30℃~50℃、好ましくは-10℃~30℃にて15~30%アンモニア水またはtert-ブチルアミン等の目的とする化合物に対応する置換基を有する試薬を加え、-10℃~30℃にて0℃~30℃にて、0.5時間~72時間、反応させることにより、化合物b-10または化合物b-11を得ることができる。
R1としては、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、シアノ、置換もしくは非置換の炭素環式基または置換もしくは非置換の複素環式基が挙げられる。
L1およびL2は各々独立して単結合、置換もしくは非置換のアルキレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)、置換もしくは非置換のアルケニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)または置換もしくは非置換のアルキニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)である。
環Bは置換もしくは非置換の炭素環、置換もしくは非置換のピリジン、置換もしくは非置換のピリミジンまたは置換もしくは非置換の5員複素環である。
環Bは置換もしくは非置換の炭素環または置換もしくは非置換の複素環である。
環Bは置換された含窒素芳香族単環である。
R1が置換もしくは非置換のアルキルであり、
R2aおよびR2bが、共に水素であり、
XがSであり、
であるか、
XがOであり、
であり、
R5が水素であり、
L1およびL2が単結合であり、
環Aは置換もしくは非置換の炭素環であり、
環Bは置換もしくは非置換の炭素環、置換もしくは非置換のピリジンまたは置換もしくは非置換のピリミジンである化合物、もしくはその製薬上許容される塩またはそれらの溶媒和物。
R2aおよびR2bが、共に水素であり、
XがSであり、
であるか、
XがOであり、
であり、
R5が水素であり、
L1およびL2が単結合であり、
環Aはハロゲンで置換されていてもよいベンゼン環であり、
環Bは置換もしくは非置換の炭素環、置換もしくは非置換のピリジンまたは置換もしくは非置換のピリミジン(ここで各置換基は、ハロゲン、ヒドロキシ、アルキル、ハロゲノアルキル、ヒドロキシアルキル、アルコキシアルキル、アルコキシ、アルコキシアルコキシ、アルコキシカルボニル、アミノ、アルキルアミノ、カルバモイル、シアノおよびニトロからなる群から選択される1以上の基)である化合物、もしくはその製薬上許容される塩またはそれらの溶媒和物。
式(I)において、
である化合物(以下、環XがX1であるとする)、
である化合物(以下、環XがX2であるとする)、
である化合物(以下、環XがX3であるとする)、
である化合物(以下、環XがX4であるとする)、
R1がメチルである化合物(以下、R1がR11であるとする)
R1がトリフルオロメチルである化合物(以下、R1がR12であるとする)、
環Aが
である化合物(以下、環AがA1であるとする)、
環Aが
である化合物(以下、環AがA2であるとする)、
環Aが
である化合物(以下、環AがA3であるとする)、
である化合物(以下、LがL1であるとする)、
である化合物(以下、LがL2であるとする)、
である化合物(以下、LがL3であるとする)、
環Bが
(式中、Rb1およびRb2は各々独立して水素、クロロ、メトキシ、ヒドロキシメチル、シアノ、アミノまたはカルバモイルである)
である化合物(以下、環BがB1であるとする)、
環Bが
(式中、Rb1およびRb2は上記と同義である)
である化合物(以下、環BがB2であるとする)、
環Bが
(式中、Rb1およびRb2は上記と同義である)
である化合物(以下、環BがB3であるとする)、または
環Bが
(式中、Rb1は上記と同義である)
である化合物(以下、環BがB4であるとする)。
(X1,R11,A1,L1,B1),(X1,R11,A1,L1,B2),(X1,R11,A1,L1,B3),(X1,R11,A1,L1,B4),(X1,R11,A1,L2,B1),(X1,R11,A1,L2,B2),(X1,R11,A1,L2,B3),(X1,R11,A1,L2,B4),(X1,R11,A1,L3,B1),(X1,R11,A1,L3,B2),(X1,R11,A1,L3,B3),(X1,R11,A1,L3,B4),(X1,R11,A2,L1,B1),(X1,R11,A2,L1,B2),(X1,R11,A2,L1,B3),(X1,R11,A2,L1,B4),(X1,R11,A2,L2,B1),(X1,R11,A2,L2,B2),(X1,R11,A2,L2,B3),(X1,R11,A2,L2,B4),(X1,R11,A2,L3,B1),(X1,R11,A2,L3,B2),(X1,R11,A2,L3,B3),(X1,R11,A2,L3,B4),(X1,R11,A3,L1,B1),(X1,R11,A3,L1,B2),(X1,R11,A3,L1,B3),(X1,R11,A3,L1,B4),(X1,R11,A3,L2,B1),(X1,R11,A3,L2,B2),(X1,R11,A3,L2,B3),(X1,R11,A3,L2,B4),(X1,R11,A3,L3,B1),(X1,R11,A3,L3,B2),(X1,R11,A3,L3,B3),(X1,R11,A3,L3,B4),(X1,R12,A1,L1,B1),(X1,R12,A1,L1,B2),(X1,R12,A1,L1,B3),(X1,R12,A1,L1,B4),(X1,R12,A1,L2,B1),(X1,R12,A1,L2,B2),(X1,R12,A1,L2,B3),(X1,R12,A1,L2,B4),(X1,R12,A1,L3,B1),(X1,R12,A1,L3,B2),(X1,R12,A1,L3,B3),(X1,R12,A1,L3,B4),(X1,R12,A2,L1,B1),(X1,R12,A2,L1,B2),(X1,R12,A2,L1,B3),(X1,R12,A2,L1,B4),(X1,R12,A2,L2,B1),(X1,R12,A2,L2,B2),(X1,R12,A2,L2,B3),(X1,R12,A2,L2,B4),(X1,R12,A2,L3,B1),(X1,R12,A2,L3,B2),(X1,R12,A2,L3,B3),(X1,R12,A2,L3,B4),(X1,R12,A3,L1,B1),(X1,R12,A3,L1,B2),(X1,R12,A3,L1,B3),(X1,R12,A3,L1,B4),(X1,R12,A3,L2,B1),(X1,R12,A3,L2,B2),(X1,R12,A3,L2,B3),(X1,R12,A3,L2,B4),(X1,R12,A3,L3,B1),(X1,R12,A3,L3,B2),(X1,R12,A3,L3,B3),(X1,R12,A3,L3,B4),(X2,R11,A1,L1,B1),(X2,R11,A1,L1,B2),(X2,R11,A1,L1,B3),(X2,R11,A1,L1,B4),(X2,R11,A1,L2,B1),(X2,R11,A1,L2,B2),(X2,R11,A1,L2,B3),(X2,R11,A1,L2,B4),(X2,R11,A1,L3,B1),(X2,R11,A1,L3,B2),(X2,R11,A1,L3,B3),(X2,R11,A1,L3,B4),(X2,R11,A2,L1,B1),(X2,R11,A2,L1,B2),(X2,R11,A2,L1,B3),(X2,R11,A2,L1,B4),(X2,R11,A2,L2,B1),(X2,R11,A2,L2,B2),(X2,R11,A2,L2,B3),(X2,R11,A2,L2,B4),(X2,R11,A2,L3,B1),(X2,R11,A2,L3,B2),(X2,R11,A2,L3,B3),(X2,R11,A2,L3,B4),(X2,R11,A3,L1,B1),(X2,R11,A3,L1,B2),(X2,R11,A3,L1,B3),(X2,R11,A3,L1,B4),(X2,R11,A3,L2,B1),(X2,R11,A3,L2,B2),(X2,R11,A3,L2,B3),(X2,R11,A3,L2,B4),(X2,R11,A3,L3,B1),(X2,R11,A3,L3,B2),(X2,R11,A3,L3,B3),(X2,R11,A3,L3,B4),
(X2,R12,A1,L1,B1),(X2,R12,A1,L1,B2),(X2,R12,A1,L1,B3),(X2,R12,A1,L1,B4),(X2,R12,A1,L2,B1),(X2,R12,A1,L2,B2),(X2,R12,A1,L2,B3),(X2,R12,A1,L2,B4),(X2,R12,A1,L3,B1),(X2,R12,A1,L3,B2),(X2,R12,A1,L3,B3),(X2,R12,A1,L3,B4),(X2,R12,A2,L1,B1),(X2,R12,A2,L1,B2),(X2,R12,A2,L1,B3),(X2,R12,A2,L1,B4),(X2,R12,A2,L2,B1),(X2,R12,A2,L2,B2),(X2,R12,A2,L2,B3),(X2,R12,A2,L2,B4),(X2,R12,A2,L3,B1),(X2,R12,A2,L3,B2),(X2,R12,A2,L3,B3),(X2,R12,A2,L3,B4),(X2,R12,A3,L1,B1),(X2,R12,A3,L1,B2),(X2,R12,A3,L1,B3),(X2,R12,A3,L1,B4),(X2,R12,A3,L2,B1),(X2,R12,A3,L2,B2),(X2,R12,A3,L2,B3),(X2,R12,A3,L2,B4),(X2,R12,A3,L3,B1),(X2,R12,A3,L3,B2),(X2,R12,A3,L3,B3),(X2,R12,A3,L3,B4),(X3,R11,A1,L1,B1),(X3,R11,A1,L1,B2),(X3,R11,A1,L1,B3),(X3,R11,A1,L1,B4),(X3,R11,A1,L2,B1),(X3,R11,A1,L2,B2),(X3,R11,A1,L2,B3),(X3,R11,A1,L2,B4),(X3,R11,A1,L3,B1),(X3,R11,A1,L3,B2),(X3,R11,A1,L3,B3),(X3,R11,A1,L3,B4),(X3,R11,A2,L1,B1),(X3,R11,A2,L1,B2),(X3,R11,A2,L1,B3),(X3,R11,A2,L1,B4),(X3,R11,A2,L2,B1),(X3,R11,A2,L2,B2),(X3,R11,A2,L2,B3),(X3,R11,A2,L2,B4),(X3,R11,A2,L3,B1),(X3,R11,A2,L3,B2),(X3,R11,A2,L3,B3),(X3,R11,A2,L3,B4),(X3,R11,A3,L1,B1),(X3,R11,A3,L1,B2),(X3,R11,A3,L1,B3),(X3,R11,A3,L1,B4),(X3,R11,A3,L2,B1),(X3,R11,A3,L2,B2),(X3,R11,A3,L2,B3),(X3,R11,A3,L2,B4),(X3,R11,A3,L3,B1),(X3,R11,A3,L3,B2),(X3,R11,A3,L3,B3),(X3,R11,A3,L3,B4),(X3,R12,A1,L1,B1),(X3,R12,A1,L1,B2),(X3,R12,A1,L1,B3),(X3,R12,A1,L1,B4),(X3,R12,A1,L2,B1),(X3,R12,A1,L2,B2),(X3,R12,A1,L2,B3),(X3,R12,A1,L2,B4),(X3,R12,A1,L3,B1),(X3,R12,A1,L3,B2),(X3,R12,A1,L3,B3),(X3,R12,A1,L3,B4),(X3,R12,A2,L1,B1),(X3,R12,A2,L1,B2),(X3,R12,A2,L1,B3),(X3,R12,A2,L1,B4),(X3,R12,A2,L2,B1),(X3,R12,A2,L2,B2),(X3,R12,A2,L2,B3),(X3,R12,A2,L2,B4),(X3,R12,A2,L3,B1),(X3,R12,A2,L3,B2),(X3,R12,A2,L3,B3),(X3,R12,A2,L3,B4),(X3,R12,A3,L1,B1),(X3,R12,A3,L1,B2),(X3,R12,A3,L1,B3),(X3,R12,A3,L1,B4),(X3,R12,A3,L2,B1),(X3,R12,A3,L2,B2),(X3,R12,A3,L2,B3),(X3,R12,A3,L2,B4),
(X3,R12,A3,L3,B1),(X3,R12,A3,L3,B2),(X3,R12,A3,L3,B3),(X3,R12,A3,L3,B4),(X4,R11,A1,L1,B1),(X4,R11,A1,L1,B2),(X4,R11,A1,L1,B3),(X4,R11,A1,L1,B4),(X4,R11,A1,L2,B1),(X4,R11,A1,L2,B2),(X4,R11,A1,L2,B3),(X4,R11,A1,L2,B4),(X4,R11,A1,L3,B1),(X4,R11,A1,L3,B2),(X4,R11,A1,L3,B3),(X4,R11,A1,L3,B4),(X4,R11,A2,L1,B1),(X4,R11,A2,L1,B2),(X4,R11,A2,L1,B3),(X4,R11,A2,L1,B4),(X4,R11,A2,L2,B1),(X4,R11,A2,L2,B2),(X4,R11,A2,L2,B3),(X4,R11,A2,L2,B4),(X4,R11,A2,L3,B1),(X4,R11,A2,L3,B2),(X4,R11,A2,L3,B3),(X4,R11,A2,L3,B4),(X4,R11,A3,L1,B1),(X4,R11,A3,L1,B2),(X4,R11,A3,L1,B3),(X4,R11,A3,L1,B4),(X4,R11,A3,L2,B1),(X4,R11,A3,L2,B2),(X4,R11,A3,L2,B3),(X4,R11,A3,L2,B4),(X4,R11,A3,L3,B1),(X4,R11,A3,L3,B2),(X4,R11,A3,L3,B3),(X4,R11,A3,L3,B4),(X4,R12,A1,L1,B1),(X4,R12,A1,L1,B2),(X4,R12,A1,L1,B3),(X4,R12,A1,L1,B4),(X4,R12,A1,L2,B1),(X4,R12,A1,L2,B2),(X4,R12,A1,L2,B3),(X4,R12,A1,L2,B4),(X4,R12,A1,L3,B1),(X4,R12,A1,L3,B2),(X4,R12,A1,L3,B3),(X4,R12,A1,L3,B4),(X4,R12,A2,L1,B1),(X4,R12,A2,L1,B2),(X4,R12,A2,L1,B3),(X4,R12,A2,L1,B4),(X4,R12,A2,L2,B1),(X4,R12,A2,L2,B2),(X4,R12,A2,L2,B3),(X4,R12,A2,L2,B4),(X4,R12,A2,L3,B1),(X4,R12,A2,L3,B2),(X4,R12,A2,L3,B3),(X4,R12,A2,L3,B4),(X4,R12,A3,L1,B1),(X4,R12,A3,L1,B2),(X4,R12,A3,L1,B3),(X4,R12,A3,L1,B4),(X4,R12,A3,L2,B1),(X4,R12,A3,L2,B2),(X4,R12,A3,L2,B3),(X4,R12,A3,L2,B4),(X4,R12,A3,L3,B1),(X4,R12,A3,L3,B2),(X4,R12,A3,L3,B3)または(X4,R12,A3,L3,B4)。
(B1、水素、水素)(以下、環Bがb1であるとする)、
(B1、水素、クロロ)(以下、環Bがb2であるとする)、
(B1、水素、メトキシ)(以下、環Bがb3であるとする)、
(B1、水素、ヒドロキシメチル)(以下、環Bがb4であるとする)、
(B1、水素、シアノ)(以下、環Bがb5であるとする)、
(B1、水素、アミノ)(以下、環Bがb6であるとする)、
(B1、水素、カルバモイル)(以下、環Bがb7であるとする)、
(B1、クロロ、水素)(以下、環Bがb8であるとする)、
(B1、クロロ、クロロ)(以下、環Bがb9であるとする)、
(B1、クロロ、メトキシ)(以下、環Bがb10であるとする)、
(B1、クロロ、ヒドロキシメチル)(以下、環Bがb11であるとする)、
(B1、クロロ、シアノ)(以下、環Bがb12であるとする)、
(B1、クロロ、アミノ)(以下、環Bがb13であるとする)、
(B1、クロロ、カルバモイル)(以下、環Bがb14であるとする)、
(B1、メトキシ、水素)(以下、環Bがb15であるとする)、
(B1、メトキシ、クロロ)(以下、環Bがb16であるとする)、
(B1、メトキシ、メトキシ)(以下、環Bがb17であるとする)、
(B1、メトキシ、ヒドロキシメチル)(以下、環Bがb18であるとする)、
(B1、メトキシ、シアノ)(以下、環Bがb19であるとする)、
(B1、メトキシ、アミノ)(以下、環Bがb20であるとする)、
(B1、メトキシ、カルバモイル)(以下、環Bがb21であるとする)、
(B1、シアノ、水素)(以下、環Bがb22であるとする)、
(B1、シアノ、クロロ)(以下、環Bがb23であるとする)、
(B1、シアノ、メトキシ)(以下、環Bがb24であるとする)、
(B1、シアノ、ヒドロキシメチル)(以下、環Bがb25であるとする)、
(B1、シアノ、シアノ)(以下、環Bがb26であるとする)、
(B1、シアノ、アミノ)(以下、環Bがb27であるとする)、
(B1、シアノ、カルバモイル)(以下、環Bがb28であるとする)、
(B1、ヒドロキシメチル、水素)(以下、環Bがb29であるとする)、
(B1、ヒドロキシメチル、クロロ)(以下、環Bがb30であるとする)、
(B1、ヒドロキシメチル、メトキシ)(以下、環Bがb31であるとする)、
(B1、ヒドロキシメチル、シアノ)(以下、環Bがb32であるとする)、
(B1、アミノ、水素)(以下、環Bがb33であるとする)、
(B1、アミノ、クロロ)(以下、環Bがb34であるとする)、
(B1、アミノ、メトキシ)(以下、環Bがb35であるとする)、
(B1、アミノ、シアノ)(以下、環Bがb36であるとする)、
(B1、カルバモイル、水素)(以下、環Bがb37であるとする)、
(B1、カルバモイル、クロロ)(以下、環Bがb38であるとする)、
(B1、カルバモイル、メトキシ)(以下、環Bがb39であるとする)、
(B1、カルバモイル、シアノ)(以下、環Bがb40であるとする)、
(B3、水素、クロロ)(以下、環Bがb42であるとする)、
(B3、水素、メトキシ)(以下、環Bがb43であるとする)、
(B3、水素、ヒドロキシメチル)(以下、環Bがb44であるとする)、
(B3、水素、シアノ)(以下、環Bがb45であるとする)、
(B3、水素、アミノ)(以下、環Bがb46であるとする)、
(B3、水素、カルバモイル)(以下、環Bがb47であるとする)、
(B3、クロロ、水素)(以下、環Bがb48であるとする)、
(B3、クロロ、クロロ)(以下、環Bがb49であるとする)、
(B3、クロロ、メトキシ)(以下、環Bがb50であるとする)、
(B3、クロロ、ヒドロキシメチル)(以下、環Bがb51であるとする)、
(B3、クロロ、シアノ)(以下、環Bがb52であるとする)、
(B3、クロロ、アミノ)(以下、環Bがb53であるとする)、
(B3、クロロ、カルバモイル)(以下、環Bがb54であるとする)、
(B3、メトキシ、水素)(以下、環Bがb55であるとする)、
(B3、メトキシ、クロロ)(以下、環Bがb56であるとする)、
(B3、メトキシ、メトキシ)(以下、環Bがb57であるとする)、
(B3、メトキシ、ヒドロキシメチル)(以下、環Bがb58であるとする)、
(B3、メトキシ、シアノ)(以下、環Bがb59であるとする)、
(B3、メトキシ、アミノ)(以下、環Bがb60であるとする)、
(B3、メトキシ、カルバモイル)(以下、環Bがb61であるとする)、
(B3、シアノ、水素)(以下、環Bがb62であるとする)、
(B3、シアノ、クロロ)(以下、環Bがb63であるとする)、
(B3、シアノ、メトキシ)(以下、環Bがb64であるとする)、
(B3、シアノ、ヒドロキシメチル)(以下、環Bがb65であるとする)、
(B3、シアノ、シアノ)(以下、環Bがb66であるとする)、
(B3、シアノ、アミノ)(以下、環Bがb67であるとする)、
(B3、シアノ、カルバモイル)(以下、環Bがb68であるとする)、
(B3、ヒドロキシメチル、水素)(以下、環Bがb69であるとする)、
(B3、ヒドロキシメチル、クロロ)(以下、環Bがb70であるとする)、
(B3、ヒドロキシメチル、メトキシ)(以下、環Bがb71であるとする)、
(B3、ヒドロキシメチル、シアノ)(以下、環Bがb72であるとする)、
(B3、アミノ、水素)(以下、環Bがb73であるとする)、
(B3、アミノ、クロロ)(以下、環Bがb74であるとする)、
(B3、アミノ、メトキシ)(以下、環Bがb75であるとする)、
(B3、アミノ、シアノ)(以下、環Bがb76であるとする)、
(B3、カルバモイル、水素)(以下、環Bがb77であるとする)、
(B3、カルバモイル、クロロ)(以下、環Bがb78であるとする)、
(B3、カルバモイル、メトキシ)(以下、環Bがb79であるとする)または
(B3、カルバモイル、シアノ)(以下、環Bがb80であるとする)。
(B4、水素)(以下、環Bがb81であるとする)、
(B4、クロロ)(以下、環Bがb82であるとする)、
(B4、メトキシ)(以下、環Bがb83であるとする)、
(B4、ヒドロキシメチル)(以下、環Bがb84であるとする)、
(B4、シアノ)(以下、環Bがb85であるとする)、
(B4、アミノ)(以下、環Bがb86であるとする)、
(B4、カルバモイル)(以下、環Bがb87であるとする)、
(B5、水素)(以下、環Bがb88であるとする)、
(B5、クロロ)(以下、環Bがb89であるとする)、
(B5、メトキシ)(以下、環Bがb90であるとする)、
(B5、ヒドロキシメチル)(以下、環Bがb91であるとする)、
(B5、シアノ)(以下、環Bがb92であるとする)、
(B5、アミノ)(以下、環Bがb93であるとする)または
(B5、カルバモイル)(以下、環Bがb94であるとする)。
(X1,R11,A1,b1),(X1,R11,A1,b2),(X1,R11,A1,b3),(X1,R11,A1,b4),(X1,R11,A1,b5),(X1,R11,A1,b6),(X1,R11,A1,b7),(X1,R11,A1,b8),(X1,R11,A1,b9),(X1,R11,A1,b10),(X1,R11,A1,b11),(X1,R11,A1,b12),(X1,R11,A1,b13),(X1,R11,A1,b14),(X1,R11,A1,b15),(X1,R11,A1,b16),(X1,R11,A1,b17),(X1,R11,A1,b18),(X1,R11,A1,b19),(X1,R11,A1,b20),(X1,R11,A1,b21),(X1,R11,A1,b22),(X1,R11,A1,b23),(X1,R11,A1,b24),(X1,R11,A1,b25),(X1,R11,A1,b26),(X1,R11,A1,b27),(X1,R11,A1,b28),(X1,R11,A1,b29),(X1,R11,A1,b30),(X1,R11,A1,b31),(X1,R11,A1,b32),(X1,R11,A1,b33),(X1,R11,A1,b34),(X1,R11,A1,b35),(X1,R11,A1,b36),(X1,R11,A1,b37),(X1,R11,A1,b38),(X1,R11,A1,b39),(X1,R11,A1,b40),(X1,R11,A1,b41),(X1,R11,A1,b42),(X1,R11,A1,b43),(X1,R11,A1,b44),
(X1,R11,A1,b45),(X1,R11,A1,b46),(X1,R11,A1,b47),(X1,R11,A1,b48),(X1,R11,A1,b49),(X1,R11,A1,b50),(X1,R11,A1,b51),(X1,R11,A1,b52),(X1,R11,A1,b53),(X1,R11,A1,b54),(X1,R11,A1,b55),(X1,R11,A1,b56),(X1,R11,A1,b57),(X1,R11,A1,b58),(X1,R11,A1,b59),(X1,R11,A1,b60),(X1,R11,A1,b61),(X1,R11,A1,b62),(X1,R11,A1,b63),(X1,R11,A1,b64),(X1,R11,A1,b65),(X1,R11,A1,b66),(X1,R11,A1,b67),(X1,R11,A1,b68),(X1,R11,A1,b69),(X1,R11,A1,b70),(X1,R11,A1,b71),(X1,R11,A1,b72),(X1,R11,A1,b73),(X1,R11,A1,b74),(X1,R11,A1,b75),(X1,R11,A1,b76),(X1,R11,A1,b77),(X1,R11,A1,b78),(X1,R11,A1,b79),(X1,R11,A1,b80),(X1,R11,A1,b81),(X1,R11,A1,b82),(X1,R11,A1,b83),(X1,R11,A1,b84),(X1,R11,A1,b85),(X1,R11,A1,b86),(X1,R11,A1,b87),(X1,R11,A1,b88),(X1,R11,A1,b89),(X1,R11,A1,b90),(X1,R11,A1,b91),(X1,R11,A1,b92),(X1,R11,A1,b93),(X1,R11,A1,b94),(X1,R11,A2,b1),(X1,R11,A2,b2),(X1,R11,A2,b3),(X1,R11,A2,b4),(X1,R11,A2,b5),(X1,R11,A2,b6),(X1,R11,A2,b7),(X1,R11,A2,b8),(X1,R11,A2,b9),(X1,R11,A2,b10),(X1,R11,A2,b11),(X1,R11,A2,b12),(X1,R11,A2,b13),(X1,R11,A2,b14),(X1,R11,A2,b15),(X1,R11,A2,b16),(X1,R11,A2,b17),(X1,R11,A2,b18),(X1,R11,A2,b19),(X1,R11,A2,b20),(X1,R11,A2,b21),(X1,R11,A2,b22),(X1,R11,A2,b23),(X1,R11,A2,b24),(X1,R11,A2,b25),(X1,R11,A2,b26),(X1,R11,A2,b27),(X1,R11,A2,b28),(X1,R11,A2,b29),(X1,R11,A2,b30),(X1,R11,A2,b31),(X1,R11,A2,b32),(X1,R11,A2,b33),(X1,R11,A2,b34),(X1,R11,A2,b35),(X1,R11,A2,b36),(X1,R11,A2,b37),(X1,R11,A2,b38),(X1,R11,A2,b39),(X1,R11,A2,b40),(X1,R11,A2,b41),(X1,R11,A2,b42),(X1,R11,A2,b43),(X1,R11,A2,b44),(X1,R11,A2,b45),(X1,R11,A2,b46),(X1,R11,A2,b47),(X1,R11,A2,b48),(X1,R11,A2,b49),(X1,R11,A2,b50),(X1,R11,A2,b51),(X1,R11,A2,b52),(X1,R11,A2,b53),(X1,R11,A2,b54),(X1,R11,A2,b55),(X1,R11,A2,b56),(X1,R11,A2,b57),(X1,R11,A2,b58),
(X1,R11,A2,b59),(X1,R11,A2,b60),(X1,R11,A2,b61),(X1,R11,A2,b62),(X1,R11,A2,b63),(X1,R11,A2,b64),(X1,R11,A2,b65),(X1,R11,A2,b66),(X1,R11,A2,b67),(X1,R11,A2,b68),(X1,R11,A2,b69),(X1,R11,A2,b70),(X1,R11,A2,b71),(X1,R11,A2,b72),(X1,R11,A2,b73),(X1,R11,A2,b74),(X1,R11,A2,b75),(X1,R11,A2,b76),(X1,R11,A2,b77),(X1,R11,A2,b78),(X1,R11,A2,b79),(X1,R11,A2,b80),(X1,R11,A2,b81),(X1,R11,A2,b82),(X1,R11,A2,b83),(X1,R11,A2,b84),(X1,R11,A2,b85),(X1,R11,A2,b86),(X1,R11,A2,b87),(X1,R11,A2,b88),(X1,R11,A2,b89),(X1,R11,A2,b90),(X1,R11,A2,b91),(X1,R11,A2,b92),(X1,R11,A2,b93),(X1,R11,A2,b94),(X1,R11,A3,b1),(X1,R11,A3,b2),(X1,R11,A3,b3),(X1,R11,A3,b4),(X1,R11,A3,b5),(X1,R11,A3,b6),(X1,R11,A3,b7),(X1,R11,A3,b8),(X1,R11,A3,b9),(X1,R11,A3,b10),(X1,R11,A3,b11),(X1,R11,A3,b12),(X1,R11,A3,b13),(X1,R11,A3,b14),(X1,R11,A3,b15),(X1,R11,A3,b16),(X1,R11,A3,b17),(X1,R11,A3,b18),(X1,R11,A3,b19),(X1,R11,A3,b20),(X1,R11,A3,b21),(X1,R11,A3,b22),(X1,R11,A3,b23),(X1,R11,A3,b24),(X1,R11,A3,b25),(X1,R11,A3,b26),(X1,R11,A3,b27),(X1,R11,A3,b28),(X1,R11,A3,b29),(X1,R11,A3,b30),(X1,R11,A3,b31),(X1,R11,A3,b32),(X1,R11,A3,b33),(X1,R11,A3,b34),(X1,R11,A3,b35),(X1,R11,A3,b36),(X1,R11,A3,b37),(X1,R11,A3,b38),(X1,R11,A3,b39),(X1,R11,A3,b40),(X1,R11,A3,b41),(X1,R11,A3,b42),(X1,R11,A3,b43),(X1,R11,A3,b44),(X1,R11,A3,b45),(X1,R11,A3,b46),(X1,R11,A3,b47),(X1,R11,A3,b48),(X1,R11,A3,b49),(X1,R11,A3,b50),(X1,R11,A3,b51),(X1,R11,A3,b52),(X1,R11,A3,b53),(X1,R11,A3,b54),(X1,R11,A3,b55),(X1,R11,A3,b56),(X1,R11,A3,b57),(X1,R11,A3,b58),(X1,R11,A3,b59),(X1,R11,A3,b60),(X1,R11,A3,b61),(X1,R11,A3,b62),(X1,R11,A3,b63),(X1,R11,A3,b64),(X1,R11,A3,b65),(X1,R11,A3,b66),(X1,R11,A3,b67),(X1,R11,A3,b68),(X1,R11,A3,b69),(X1,R11,A3,b70),(X1,R11,A3,b71),(X1,R11,A3,b72),(X1,R11,A3,b73),(X1,R11,A3,b74),(X1,R11,A3,b75),(X1,R11,A3,b76),(X1,R11,A3,b77),(X1,R11,A3,b78),(X1,R11,A3,b79),(X1,R11,A3,b80),(X1,R11,A3,b81),(X1,R11,A3,b82),(X1,R11,A3,b83),(X1,R11,A3,b84),(X1,R11,A3,b85),(X1,R11,A3,b86),(X1,R11,A3,b87),(X1,R11,A3,b88),(X1,R11,A3,b89),(X1,R11,A3,b90),(X1,R11,A3,b91),(X1,R11,A3,b92),(X1,R11,A3,b93),(X1,R11,A3,b94),(X1,R12,A1,b1),(X1,R12,A1,b2),(X1,R12,A1,b3),(X1,R12,A1,b4),(X1,R12,A1,b5),(X1,R12,A1,b6),(X1,R12,A1,b7),(X1,R12,A1,b8),(X1,R12,A1,b9),(X1,R12,A1,b10),(X1,R12,A1,b11),(X1,R12,A1,b12),(X1,R12,A1,b13),(X1,R12,A1,b14),(X1,R12,A1,b15),(X1,R12,A1,b16),(X1,R12,A1,b17),(X1,R12,A1,b18),(X1,R12,A1,b19),(X1,R12,A1,b20),(X1,R12,A1,b21),(X1,R12,A1,b22),
(X1,R12,A1,b23),(X1,R12,A1,b24),(X1,R12,A1,b25),(X1,R12,A1,b26),(X1,R12,A1,b27),(X1,R12,A1,b28),(X1,R12,A1,b29),(X1,R12,A1,b30),(X1,R12,A1,b31),(X1,R12,A1,b32),(X1,R12,A1,b33),(X1,R12,A1,b34),(X1,R12,A1,b35),(X1,R12,A1,b36),(X1,R12,A1,b37),(X1,R12,A1,b38),(X1,R12,A1,b39),(X1,R12,A1,b40),(X1,R12,A1,b41),(X1,R12,A1,b42),(X1,R12,A1,b43),(X1,R12,A1,b44),(X1,R12,A1,b45),(X1,R12,A1,b46),(X1,R12,A1,b47),(X1,R12,A1,b48),(X1,R12,A1,b49),(X1,R12,A1,b50),(X1,R12,A1,b51),(X1,R12,A1,b52),(X1,R12,A1,b53),(X1,R12,A1,b54),(X1,R12,A1,b55),(X1,R12,A1,b56),(X1,R12,A1,b57),(X1,R12,A1,b58),(X1,R12,A1,b59),(X1,R12,A1,b60),(X1,R12,A1,b61),(X1,R12,A1,b62),(X1,R12,A1,b63),(X1,R12,A1,b64),(X1,R12,A1,b65),(X1,R12,A1,b66),(X1,R12,A1,b67),(X1,R12,A1,b68),(X1,R12,A1,b69),(X1,R12,A1,b70),(X1,R12,A1,b71),(X1,R12,A1,b72),(X1,R12,A1,b73),(X1,R12,A1,b74),(X1,R12,A1,b75),(X1,R12,A1,b76),(X1,R12,A1,b77),(X1,R12,A1,b78),(X1,R12,A1,b79),(X1,R12,A1,b80),(X1,R12,A1,b81),(X1,R12,A1,b82),(X1,R12,A1,b83),(X1,R12,A1,b84),(X1,R12,A1,b85),(X1,R12,A1,b86),(X1,R12,A1,b87),(X1,R12,A1,b88),(X1,R12,A1,b89),(X1,R12,A1,b90),(X1,R12,A1,b91),(X1,R12,A1,b92),(X1,R12,A1,b93),(X1,R12,A1,b94),
(X1,R12,A2,b1),(X1,R12,A2,b2),(X1,R12,A2,b3),(X1,R12,A2,b4),(X1,R12,A2,b5),(X1,R12,A2,b6),(X1,R12,A2,b7),(X1,R12,A2,b8),(X1,R12,A2,b9),(X1,R12,A2,b10),(X1,R12,A2,b11),(X1,R12,A2,b12),(X1,R12,A2,b13),(X1,R12,A2,b14),(X1,R12,A2,b15),(X1,R12,A2,b16),(X1,R12,A2,b17),(X1,R12,A2,b18),(X1,R12,A2,b19),(X1,R12,A2,b20),(X1,R12,A2,b21),(X1,R12,A2,b22),(X1,R12,A2,b23),(X1,R12,A2,b24),(X1,R12,A2,b25),(X1,R12,A2,b26),(X1,R12,A2,b27),(X1,R12,A2,b28),(X1,R12,A2,b29),(X1,R12,A2,b30),(X1,R12,A2,b31),(X1,R12,A2,b32),(X1,R12,A2,b33),(X1,R12,A2,b34),(X1,R12,A2,b35),(X1,R12,A2,b36),(X1,R12,A2,b37),(X1,R12,A2,b38),(X1,R12,A2,b39),(X1,R12,A2,b40),(X1,R12,A2,b41),(X1,R12,A2,b42),(X1,R12,A2,b43),(X1,R12,A2,b44),(X1,R12,A2,b45),(X1,R12,A2,b46),(X1,R12,A2,b47),(X1,R12,A2,b48),(X1,R12,A2,b49),(X1,R12,A2,b50),(X1,R12,A2,b51),(X1,R12,A2,b52),(X1,R12,A2,b53),(X1,R12,A2,b54),(X1,R12,A2,b55),(X1,R12,A2,b56),(X1,R12,A2,b57),(X1,R12,A2,b58),(X1,R12,A2,b59),(X1,R12,A2,b60),(X1,R12,A2,b61),(X1,R12,A2,b62),(X1,R12,A2,b63),(X1,R12,A2,b64),(X1,R12,A2,b65),(X1,R12,A2,b66),(X1,R12,A2,b67),(X1,R12,A2,b68),(X1,R12,A2,b69),(X1,R12,A2,b70),(X1,R12,A2,b71),(X1,R12,A2,b72),(X1,R12,A2,b73),(X1,R12,A2,b74),(X1,R12,A2,b75),(X1,R12,A2,b76),(X1,R12,A2,b77),(X1,R12,A2,b78),(X1,R12,A2,b79),(X1,R12,A2,b80),(X1,R12,A2,b81),(X1,R12,A2,b82),(X1,R12,A2,b83),(X1,R12,A2,b84),(X1,R12,A2,b85),(X1,R12,A2,b86),(X1,R12,A2,b87),(X1,R12,A2,b88),(X1,R12,A2,b89),(X1,R12,A2,b90),(X1,R12,A2,b91),(X1,R12,A2,b92),(X1,R12,A2,b93),(X1,R12,A2,b94),(X1,R12,A3,b1),(X1,R12,A3,b2),(X1,R12,A3,b3),(X1,R12,A3,b4),(X1,R12,A3,b5),(X1,R12,A3,b6),(X1,R12,A3,b7),(X1,R12,A3,b8),(X1,R12,A3,b9),(X1,R12,A3,b10),(X1,R12,A3,b11),(X1,R12,A3,b12),(X1,R12,A3,b13),(X1,R12,A3,b14),(X1,R12,A3,b15),(X1,R12,A3,b16),(X1,R12,A3,b17),(X1,R12,A3,b18),(X1,R12,A3,b19),(X1,R12,A3,b20),(X1,R12,A3,b21),(X1,R12,A3,b22),(X1,R12,A3,b23),(X1,R12,A3,b24),(X1,R12,A3,b25),(X1,R12,A3,b26),(X1,R12,A3,b27),(X1,R12,A3,b28),(X1,R12,A3,b29),(X1,R12,A3,b30),(X1,R12,A3,b31),(X1,R12,A3,b32),(X1,R12,A3,b33),(X1,R12,A3,b34),(X1,R12,A3,b35),(X1,R12,A3,b36),(X1,R12,A3,b37),(X1,R12,A3,b38),(X1,R12,A3,b39),(X1,R12,A3,b40),(X1,R12,A3,b41),(X1,R12,A3,b42),(X1,R12,A3,b43),(X1,R12,A3,b44),(X1,R12,A3,b45),(X1,R12,A3,b46),(X1,R12,A3,b47),(X1,R12,A3,b48),(X1,R12,A3,b49),(X1,R12,A3,b50),(X1,R12,A3,b51),(X1,R12,A3,b52),(X1,R12,A3,b53),(X1,R12,A3,b54),(X1,R12,A3,b55),(X1,R12,A3,b56),(X1,R12,A3,b57),(X1,R12,A3,b58),
(X1,R12,A3,b59),(X1,R12,A3,b60),(X1,R12,A3,b61),(X1,R12,A3,b62),(X1,R12,A3,b63),(X1,R12,A3,b64),(X1,R12,A3,b65),(X1,R12,A3,b66),(X1,R12,A3,b67),(X1,R12,A3,b68),(X1,R12,A3,b69),(X1,R12,A3,b70),(X1,R12,A3,b71),(X1,R12,A3,b72),(X1,R12,A3,b73),(X1,R12,A3,b74),(X1,R12,A3,b75),(X1,R12,A3,b76),(X1,R12,A3,b77),(X1,R12,A3,b78),(X1,R12,A3,b79),(X1,R12,A3,b80),(X1,R12,A3,b81),(X1,R12,A3,b82),(X1,R12,A3,b83),(X1,R12,A3,b84),(X1,R12,A3,b85),(X1,R12,A3,b86),(X1,R12,A3,b87),(X1,R12,A3,b88),(X1,R12,A3,b89),(X1,R12,A3,b90),(X1,R12,A3,b91),(X1,R12,A3,b92),(X1,R12,A3,b93),(X1,R12,A3,b94),(X2,R11,A1,b1),(X2,R11,A1,b2),(X2,R11,A1,b3),(X2,R11,A1,b4),(X2,R11,A1,b5),(X2,R11,A1,b6),(X2,R11,A1,b7),(X2,R11,A1,b8),(X2,R11,A1,b9),(X2,R11,A1,b10),(X2,R11,A1,b11),(X2,R11,A1,b12),(X2,R11,A1,b13),(X2,R11,A1,b14),(X2,R11,A1,b15),(X2,R11,A1,b16),(X2,R11,A1,b17),(X2,R11,A1,b18),(X2,R11,A1,b19),(X2,R11,A1,b20),(X2,R11,A1,b21),(X2,R11,A1,b22),(X2,R11,A1,b23),(X2,R11,A1,b24),(X2,R11,A1,b25),(X2,R11,A1,b26),(X2,R11,A1,b27),(X2,R11,A1,b28),(X2,R11,A1,b29),(X2,R11,A1,b30),(X2,R11,A1,b31),(X2,R11,A1,b32),(X2,R11,A1,b33),(X2,R11,A1,b34),(X2,R11,A1,b35),(X2,R11,A1,b36),(X2,R11,A1,b37),(X2,R11,A1,b38),(X2,R11,A1,b39),(X2,R11,A1,b40),(X2,R11,A1,b41),(X2,R11,A1,b42),(X2,R11,A1,b43),(X2,R11,A1,b44),(X2,R11,A1,b45),(X2,R11,A1,b46),(X2,R11,A1,b47),(X2,R11,A1,b48),(X2,R11,A1,b49),(X2,R11,A1,b50),(X2,R11,A1,b51),(X2,R11,A1,b52),(X2,R11,A1,b53),(X2,R11,A1,b54),(X2,R11,A1,b55),(X2,R11,A1,b56),(X2,R11,A1,b57),(X2,R11,A1,b58),(X2,R11,A1,b59),(X2,R11,A1,b60),(X2,R11,A1,b61),(X2,R11,A1,b62),(X2,R11,A1,b63),(X2,R11,A1,b64),(X2,R11,A1,b65),(X2,R11,A1,b66),(X2,R11,A1,b67),(X2,R11,A1,b68),(X2,R11,A1,b69),(X2,R11,A1,b70),(X2,R11,A1,b71),(X2,R11,A1,b72),(X2,R11,A1,b73),(X2,R11,A1,b74),(X2,R11,A1,b75),(X2,R11,A1,b76),
(X2,R11,A1,b77),(X2,R11,A1,b78),(X2,R11,A1,b79),(X2,R11,A1,b80),(X2,R11,A1,b81),(X2,R11,A1,b82),(X2,R11,A1,b83),(X2,R11,A1,b84),(X2,R11,A1,b85),(X2,R11,A1,b86),(X2,R11,A1,b87),(X2,R11,A1,b88),(X2,R11,A1,b89),(X2,R11,A1,b90),(X2,R11,A1,b91),(X2,R11,A1,b92),(X2,R11,A1,b93),(X2,R11,A1,b94),(X2,R11,A2,b1),(X2,R11,A2,b2),(X2,R11,A2,b3),(X2,R11,A2,b4),(X2,R11,A2,b5),(X2,R11,A2,b6),(X2,R11,A2,b7),(X2,R11,A2,b8),(X2,R11,A2,b9),(X2,R11,A2,b10),(X2,R11,A2,b11),(X2,R11,A2,b12),(X2,R11,A2,b13),(X2,R11,A2,b14),(X2,R11,A2,b15),(X2,R11,A2,b16),(X2,R11,A2,b17),(X2,R11,A2,b18),(X2,R11,A2,b19),(X2,R11,A2,b20),(X2,R11,A2,b21),(X2,R11,A2,b22),(X2,R11,A2,b23),(X2,R11,A2,b24),(X2,R11,A2,b25),(X2,R11,A2,b26),(X2,R11,A2,b27),(X2,R11,A2,b28),(X2,R11,A2,b29),(X2,R11,A2,b30),(X2,R11,A2,b31),(X2,R11,A2,b32),(X2,R11,A2,b33),(X2,R11,A2,b34),(X2,R11,A2,b35),(X2,R11,A2,b36),(X2,R11,A2,b37),(X2,R11,A2,b38),(X2,R11,A2,b39),(X2,R11,A2,b40),(X2,R11,A2,b41),(X2,R11,A2,b42),(X2,R11,A2,b43),(X2,R11,A2,b44),(X2,R11,A2,b45),(X2,R11,A2,b46),(X2,R11,A2,b47),(X2,R11,A2,b48),(X2,R11,A2,b49),(X2,R11,A2,b50),(X2,R11,A2,b51),(X2,R11,A2,b52),(X2,R11,A2,b53),(X2,R11,A2,b54),(X2,R11,A2,b55),(X2,R11,A2,b56),(X2,R11,A2,b57),(X2,R11,A2,b58),(X2,R11,A2,b59),(X2,R11,A2,b60),(X2,R11,A2,b61),(X2,R11,A2,b62),(X2,R11,A2,b63),(X2,R11,A2,b64),(X2,R11,A2,b65),(X2,R11,A2,b66),(X2,R11,A2,b67),(X2,R11,A2,b68),(X2,R11,A2,b69),(X2,R11,A2,b70),(X2,R11,A2,b71),(X2,R11,A2,b72),(X2,R11,A2,b73),(X2,R11,A2,b74),(X2,R11,A2,b75),(X2,R11,A2,b76),(X2,R11,A2,b77),(X2,R11,A2,b78),(X2,R11,A2,b79),(X2,R11,A2,b80),(X2,R11,A2,b81),(X2,R11,A2,b82),(X2,R11,A2,b83),(X2,R11,A2,b84),(X2,R11,A2,b85),(X2,R11,A2,b86),(X2,R11,A2,b87),(X2,R11,A2,b88),(X2,R11,A2,b89),(X2,R11,A2,b90),
(X2,R11,A2,b91),(X2,R11,A2,b92),(X2,R11,A2,b93),(X2,R11,A2,b94),(X2,R11,A3,b1),(X2,R11,A3,b2),(X2,R11,A3,b3),(X2,R11,A3,b4),(X2,R11,A3,b5),(X2,R11,A3,b6),(X2,R11,A3,b7),(X2,R11,A3,b8),(X2,R11,A3,b9),(X2,R11,A3,b10),(X2,R11,A3,b11),(X2,R11,A3,b12),(X2,R11,A3,b13),(X2,R11,A3,b14),(X2,R11,A3,b15),(X2,R11,A3,b16),(X2,R11,A3,b17),(X2,R11,A3,b18),(X2,R11,A3,b19),(X2,R11,A3,b20),(X2,R11,A3,b21),(X2,R11,A3,b22),(X2,R11,A3,b23),(X2,R11,A3,b24),(X2,R11,A3,b25),(X2,R11,A3,b26),(X2,R11,A3,b27),(X2,R11,A3,b28),(X2,R11,A3,b29),(X2,R11,A3,b30),(X2,R11,A3,b31),(X2,R11,A3,b32),(X2,R11,A3,b33),(X2,R11,A3,b34),(X2,R11,A3,b35),(X2,R11,A3,b36),(X2,R11,A3,b37),(X2,R11,A3,b38),(X2,R11,A3,b39),(X2,R11,A3,b40),(X2,R11,A3,b41),(X2,R11,A3,b42),(X2,R11,A3,b43),(X2,R11,A3,b44),(X2,R11,A3,b45),(X2,R11,A3,b46),(X2,R11,A3,b47),(X2,R11,A3,b48),(X2,R11,A3,b49),(X2,R11,A3,b50),(X2,R11,A3,b51),(X2,R11,A3,b52),(X2,R11,A3,b53),(X2,R11,A3,b54),(X2,R11,A3,b55),(X2,R11,A3,b56),(X2,R11,A3,b57),(X2,R11,A3,b58),(X2,R11,A3,b59),(X2,R11,A3,b60),(X2,R11,A3,b61),(X2,R11,A3,b62),(X2,R11,A3,b63),(X2,R11,A3,b64),(X2,R11,A3,b65),(X2,R11,A3,b66),(X2,R11,A3,b67),(X2,R11,A3,b68),(X2,R11,A3,b69),(X2,R11,A3,b70),(X2,R11,A3,b71),(X2,R11,A3,b72),(X2,R11,A3,b73),(X2,R11,A3,b74),(X2,R11,A3,b75),(X2,R11,A3,b76),(X2,R11,A3,b77),(X2,R11,A3,b78),(X2,R11,A3,b79),(X2,R11,A3,b80),(X2,R11,A3,b81),(X2,R11,A3,b82),(X2,R11,A3,b83),(X2,R11,A3,b84),(X2,R11,A3,b85),(X2,R11,A3,b86),(X2,R11,A3,b87),(X2,R11,A3,b88),(X2,R11,A3,b89),(X2,R11,A3,b90),(X2,R11,A3,b91),(X2,R11,A3,b92),(X2,R11,A3,b93),(X2,R11,A3,b94),(X2,R12,A1,b1),(X2,R12,A1,b2),(X2,R12,A1,b3),(X2,R12,A1,b4),(X2,R12,A1,b5),(X2,R12,A1,b6),(X2,R12,A1,b7),(X2,R12,A1,b8),(X2,R12,A1,b9),(X2,R12,A1,b10),(X2,R12,A1,b11),(X2,R12,A1,b12),(X2,R12,A1,b13),(X2,R12,A1,b14),(X2,R12,A1,b15),(X2,R12,A1,b16),(X2,R12,A1,b17),(X2,R12,A1,b18),(X2,R12,A1,b19),(X2,R12,A1,b20),(X2,R12,A1,b21),(X2,R12,A1,b22),(X2,R12,A1,b23),(X2,R12,A1,b24),(X2,R12,A1,b25),(X2,R12,A1,b26),(X2,R12,A1,b27),(X2,R12,A1,b28),(X2,R12,A1,b29),(X2,R12,A1,b30),(X2,R12,A1,b31),(X2,R12,A1,b32),(X2,R12,A1,b33),(X2,R12,A1,b34),(X2,R12,A1,b35),(X2,R12,A1,b36),(X2,R12,A1,b37),(X2,R12,A1,b38),(X2,R12,A1,b39),(X2,R12,A1,b40),(X2,R12,A1,b41),(X2,R12,A1,b42),(X2,R12,A1,b43),(X2,R12,A1,b44),(X2,R12,A1,b45),(X2,R12,A1,b46),
(X2,R12,A1,b47),(X2,R12,A1,b48),(X2,R12,A1,b49),(X2,R12,A1,b50),(X2,R12,A1,b51),(X2,R12,A1,b52),(X2,R12,A1,b53),(X2,R12,A1,b54),(X2,R12,A1,b55),(X2,R12,A1,b56),(X2,R12,A1,b57),(X2,R12,A1,b58),(X2,R12,A1,b59),(X2,R12,A1,b60),(X2,R12,A1,b61),(X2,R12,A1,b62),(X2,R12,A1,b63),(X2,R12,A1,b64),(X2,R12,A1,b65),(X2,R12,A1,b66),(X2,R12,A1,b67),(X2,R12,A1,b68),(X2,R12,A1,b69),(X2,R12,A1,b70),(X2,R12,A1,b71),(X2,R12,A1,b72),(X2,R12,A1,b73),(X2,R12,A1,b74),(X2,R12,A1,b75),(X2,R12,A1,b76),(X2,R12,A1,b77),(X2,R12,A1,b78),(X2,R12,A1,b79),(X2,R12,A1,b80),(X2,R12,A1,b81),(X2,R12,A1,b82),(X2,R12,A1,b83),(X2,R12,A1,b84),(X2,R12,A1,b85),(X2,R12,A1,b86),(X2,R12,A1,b87),(X2,R12,A1,b88),(X2,R12,A1,b89),(X2,R12,A1,b90),(X2,R12,A1,b91),(X2,R12,A1,b92),(X2,R12,A1,b93),(X2,R12,A1,b94),(X2,R12,A2,b1),(X2,R12,A2,b2),(X2,R12,A2,b3),(X2,R12,A2,b4),(X2,R12,A2,b5),(X2,R12,A2,b6),(X2,R12,A2,b7),(X2,R12,A2,b8),(X2,R12,A2,b9),(X2,R12,A2,b10),(X2,R12,A2,b11),(X2,R12,A2,b12),(X2,R12,A2,b13),(X2,R12,A2,b14),(X2,R12,A2,b15),(X2,R12,A2,b16),(X2,R12,A2,b17),(X2,R12,A2,b18),(X2,R12,A2,b19),(X2,R12,A2,b20),(X2,R12,A2,b21),(X2,R12,A2,b22),(X2,R12,A2,b23),(X2,R12,A2,b24),(X2,R12,A2,b25),(X2,R12,A2,b26),(X2,R12,A2,b27),(X2,R12,A2,b28),(X2,R12,A2,b29),(X2,R12,A2,b30),(X2,R12,A2,b31),(X2,R12,A2,b32),(X2,R12,A2,b33),(X2,R12,A2,b34),(X2,R12,A2,b35),(X2,R12,A2,b36),(X2,R12,A2,b37),(X2,R12,A2,b38),(X2,R12,A2,b39),(X2,R12,A2,b40),(X2,R12,A2,b41),(X2,R12,A2,b42),(X2,R12,A2,b43),(X2,R12,A2,b44),(X2,R12,A2,b45),(X2,R12,A2,b46),(X2,R12,A2,b47),(X2,R12,A2,b48),(X2,R12,A2,b49),(X2,R12,A2,b50),(X2,R12,A2,b51),(X2,R12,A2,b52),(X2,R12,A2,b53),(X2,R12,A2,b54),(X2,R12,A2,b55),(X2,R12,A2,b56),(X2,R12,A2,b57),(X2,R12,A2,b58),(X2,R12,A2,b59),(X2,R12,A2,b60),(X2,R12,A2,b61),(X2,R12,A2,b62),(X2,R12,A2,b63),(X2,R12,A2,b64),(X2,R12,A2,b65),(X2,R12,A2,b66),(X2,R12,A2,b67),(X2,R12,A2,b68),(X2,R12,A2,b69),(X2,R12,A2,b70),(X2,R12,A2,b71),(X2,R12,A2,b72),
(X2,R12,A2,b73),(X2,R12,A2,b74),(X2,R12,A2,b75),(X2,R12,A2,b76),(X2,R12,A2,b77),(X2,R12,A2,b78),(X2,R12,A2,b79),(X2,R12,A2,b80),(X2,R12,A2,b81),(X2,R12,A2,b82),(X2,R12,A2,b83),(X2,R12,A2,b84),(X2,R12,A2,b85),(X2,R12,A2,b86),(X2,R12,A2,b87),(X2,R12,A2,b88),(X2,R12,A2,b89),(X2,R12,A2,b90),(X2,R12,A2,b91),(X2,R12,A2,b92),(X2,R12,A2,b93),(X2,R12,A2,b94),(X2,R12,A3,b1),(X2,R12,A3,b2),(X2,R12,A3,b3),(X2,R12,A3,b4),(X2,R12,A3,b5),(X2,R12,A3,b6),(X2,R12,A3,b7),(X2,R12,A3,b8),(X2,R12,A3,b9),(X2,R12,A3,b10),(X2,R12,A3,b11),(X2,R12,A3,b12),(X2,R12,A3,b13),(X2,R12,A3,b14),(X2,R12,A3,b15),(X2,R12,A3,b16),(X2,R12,A3,b17),(X2,R12,A3,b18),(X2,R12,A3,b19),(X2,R12,A3,b20),(X2,R12,A3,b21),(X2,R12,A3,b22),(X2,R12,A3,b23),(X2,R12,A3,b24),(X2,R12,A3,b25),(X2,R12,A3,b26),(X2,R12,A3,b27),(X2,R12,A3,b28),(X2,R12,A3,b29),(X2,R12,A3,b30),(X2,R12,A3,b31),(X2,R12,A3,b32),(X2,R12,A3,b33),(X2,R12,A3,b34),(X2,R12,A3,b35),(X2,R12,A3,b36),(X2,R12,A3,b37),(X2,R12,A3,b38),(X2,R12,A3,b39),(X2,R12,A3,b40),(X2,R12,A3,b41),(X2,R12,A3,b42),(X2,R12,A3,b43),(X2,R12,A3,b44),(X2,R12,A3,b45),(X2,R12,A3,b46),(X2,R12,A3,b47),(X2,R12,A3,b48),(X2,R12,A3,b49),(X2,R12,A3,b50),(X2,R12,A3,b51),(X2,R12,A3,b52),(X2,R12,A3,b53),(X2,R12,A3,b54),(X2,R12,A3,b55),(X2,R12,A3,b56),(X2,R12,A3,b57),(X2,R12,A3,b58),(X2,R12,A3,b59),(X2,R12,A3,b60),(X2,R12,A3,b61),(X2,R12,A3,b62),(X2,R12,A3,b63),(X2,R12,A3,b64),(X2,R12,A3,b65),(X2,R12,A3,b66),(X2,R12,A3,b67),(X2,R12,A3,b68),(X2,R12,A3,b69),(X2,R12,A3,b70),(X2,R12,A3,b71),(X2,R12,A3,b72),(X2,R12,A3,b73),(X2,R12,A3,b74),(X2,R12,A3,b75),(X2,R12,A3,b76),(X2,R12,A3,b77),(X2,R12,A3,b78),(X2,R12,A3,b79),(X2,R12,A3,b80),(X2,R12,A3,b81),(X2,R12,A3,b82),(X2,R12,A3,b83),(X2,R12,A3,b84),(X2,R12,A3,b85),(X2,R12,A3,b86),(X2,R12,A3,b87),(X2,R12,A3,b88),(X2,R12,A3,b89),(X2,R12,A3,b90),
(X2,R12,A3,b91),(X2,R12,A3,b92),(X2,R12,A3,b93),(X2,R12,A3,b94),(X3,R11,A1,b1),(X3,R11,A1,b2),(X3,R11,A1,b3),(X3,R11,A1,b4),(X3,R11,A1,b5),(X3,R11,A1,b6),(X3,R11,A1,b7),(X3,R11,A1,b8),(X3,R11,A1,b9),(X3,R11,A1,b10),(X3,R11,A1,b11),(X3,R11,A1,b12),(X3,R11,A1,b13),(X3,R11,A1,b14),(X3,R11,A1,b15),(X3,R11,A1,b16),(X3,R11,A1,b17),(X3,R11,A1,b18),(X3,R11,A1,b19),(X3,R11,A1,b20),(X3,R11,A1,b21),(X3,R11,A1,b22),(X3,R11,A1,b23),(X3,R11,A1,b24),(X3,R11,A1,b25),(X3,R11,A1,b26),(X3,R11,A1,b27),(X3,R11,A1,b28),(X3,R11,A1,b29),(X3,R11,A1,b30),(X3,R11,A1,b31),(X3,R11,A1,b32),(X3,R11,A1,b33),(X3,R11,A1,b34),(X3,R11,A1,b35),(X3,R11,A1,b36),
(X3,R11,A1,b37),(X3,R11,A1,b38),(X3,R11,A1,b39),(X3,R11,A1,b40),(X3,R11,A1,b41),(X3,R11,A1,b42),(X3,R11,A1,b43),(X3,R11,A1,b44),(X3,R11,A1,b45),(X3,R11,A1,b46),(X3,R11,A1,b47),(X3,R11,A1,b48),(X3,R11,A1,b49),(X3,R11,A1,b50),(X3,R11,A1,b51),(X3,R11,A1,b52),(X3,R11,A1,b53),(X3,R11,A1,b54),(X3,R11,A1,b55),(X3,R11,A1,b56),(X3,R11,A1,b57),(X3,R11,A1,b58),(X3,R11,A1,b59),(X3,R11,A1,b60),(X3,R11,A1,b61),(X3,R11,A1,b62),(X3,R11,A1,b63),(X3,R11,A1,b64),(X3,R11,A1,b65),(X3,R11,A1,b66),(X3,R11,A1,b67),(X3,R11,A1,b68),(X3,R11,A1,b69),(X3,R11,A1,b70),(X3,R11,A1,b71),(X3,R11,A1,b72),(X3,R11,A1,b73),(X3,R11,A1,b74),(X3,R11,A1,b75),(X3,R11,A1,b76),(X3,R11,A1,b77),(X3,R11,A1,b78),(X3,R11,A1,b79),(X3,R11,A1,b80),(X3,R11,A1,b81),(X3,R11,A1,b82),(X3,R11,A1,b83),(X3,R11,A1,b84),(X3,R11,A1,b85),(X3,R11,A1,b86),(X3,R11,A1,b87),(X3,R11,A1,b88),(X3,R11,A1,b89),(X3,R11,A1,b90),(X3,R11,A1,b91),(X3,R11,A1,b92),(X3,R11,A1,b93),(X3,R11,A1,b94),(X3,R11,A2,b1),(X3,R11,A2,b2),(X3,R11,A2,b3),(X3,R11,A2,b4),(X3,R11,A2,b5),(X3,R11,A2,b6),(X3,R11,A2,b7),(X3,R11,A2,b8),(X3,R11,A2,b9),(X3,R11,A2,b10),(X3,R11,A2,b11),(X3,R11,A2,b12),(X3,R11,A2,b13),(X3,R11,A2,b14),(X3,R11,A2,b15),(X3,R11,A2,b16),(X3,R11,A2,b17),(X3,R11,A2,b18),(X3,R11,A2,b19),(X3,R11,A2,b20),(X3,R11,A2,b21),(X3,R11,A2,b22),(X3,R11,A2,b23),(X3,R11,A2,b24),(X3,R11,A2,b25),(X3,R11,A2,b26),(X3,R11,A2,b27),(X3,R11,A2,b28),(X3,R11,A2,b29),(X3,R11,A2,b30),(X3,R11,A2,b31),(X3,R11,A2,b32),(X3,R11,A2,b33),(X3,R11,A2,b34),(X3,R11,A2,b35),(X3,R11,A2,b36),(X3,R11,A2,b37),(X3,R11,A2,b38),(X3,R11,A2,b39),(X3,R11,A2,b40),(X3,R11,A2,b41),(X3,R11,A2,b42),(X3,R11,A2,b43),(X3,R11,A2,b44),(X3,R11,A2,b45),(X3,R11,A2,b46),(X3,R11,A2,b47),(X3,R11,A2,b48),(X3,R11,A2,b49),(X3,R11,A2,b50),(X3,R11,A2,b51),(X3,R11,A2,b52),(X3,R11,A2,b53),(X3,R11,A2,b54),
(X3,R11,A2,b55),(X3,R11,A2,b56),(X3,R11,A2,b57),(X3,R11,A2,b58),(X3,R11,A2,b59),(X3,R11,A2,b60),(X3,R11,A2,b61),(X3,R11,A2,b62),(X3,R11,A2,b63),(X3,R11,A2,b64),(X3,R11,A2,b65),(X3,R11,A2,b66),(X3,R11,A2,b67),(X3,R11,A2,b68),(X3,R11,A2,b69),(X3,R11,A2,b70),(X3,R11,A2,b71),(X3,R11,A2,b72),(X3,R11,A2,b73),(X3,R11,A2,b74),(X3,R11,A2,b75),(X3,R11,A2,b76),(X3,R11,A2,b77),(X3,R11,A2,b78),(X3,R11,A2,b79),(X3,R11,A2,b80),(X3,R11,A2,b81),(X3,R11,A2,b82),(X3,R11,A2,b83),(X3,R11,A2,b84),(X3,R11,A2,b85),(X3,R11,A2,b86),(X3,R11,A2,b87),(X3,R11,A2,b88),(X3,R11,A2,b89),(X3,R11,A2,b90),(X3,R11,A2,b91),(X3,R11,A2,b92),(X3,R11,A2,b93),(X3,R11,A2,b94),(X3,R11,A3,b1),(X3,R11,A3,b2),(X3,R11,A3,b3),(X3,R11,A3,b4),(X3,R11,A3,b5),(X3,R11,A3,b6),(X3,R11,A3,b7),(X3,R11,A3,b8),(X3,R11,A3,b9),(X3,R11,A3,b10),(X3,R11,A3,b11),(X3,R11,A3,b12),(X3,R11,A3,b13),(X3,R11,A3,b14),(X3,R11,A3,b15),(X3,R11,A3,b16),(X3,R11,A3,b17),(X3,R11,A3,b18),(X3,R11,A3,b19),(X3,R11,A3,b20),(X3,R11,A3,b21),(X3,R11,A3,b22),(X3,R11,A3,b23),(X3,R11,A3,b24),(X3,R11,A3,b25),(X3,R11,A3,b26),(X3,R11,A3,b27),(X3,R11,A3,b28),(X3,R11,A3,b29),(X3,R11,A3,b30),(X3,R11,A3,b31),(X3,R11,A3,b32),(X3,R11,A3,b33),(X3,R11,A3,b34),(X3,R11,A3,b35),(X3,R11,A3,b36),(X3,R11,A3,b37),(X3,R11,A3,b38),(X3,R11,A3,b39),(X3,R11,A3,b40),(X3,R11,A3,b41),(X3,R11,A3,b42),(X3,R11,A3,b43),(X3,R11,A3,b44),(X3,R11,A3,b45),(X3,R11,A3,b46),(X3,R11,A3,b47),(X3,R11,A3,b48),(X3,R11,A3,b49),(X3,R11,A3,b50),(X3,R11,A3,b51),(X3,R11,A3,b52),(X3,R11,A3,b53),(X3,R11,A3,b54),(X3,R11,A3,b55),(X3,R11,A3,b56),(X3,R11,A3,b57),(X3,R11,A3,b58),(X3,R11,A3,b59),(X3,R11,A3,b60),(X3,R11,A3,b61),(X3,R11,A3,b62),(X3,R11,A3,b63),(X3,R11,A3,b64),(X3,R11,A3,b65),(X3,R11,A3,b66),(X3,R11,A3,b67),(X3,R11,A3,b68),(X3,R11,A3,b69),(X3,R11,A3,b70),(X3,R11,A3,b71),(X3,R11,A3,b72),
(X3,R11,A3,b73),(X3,R11,A3,b74),(X3,R11,A3,b75),(X3,R11,A3,b76),(X3,R11,A3,b77),(X3,R11,A3,b78),(X3,R11,A3,b79),(X3,R11,A3,b80),(X3,R11,A3,b81),(X3,R11,A3,b82),(X3,R11,A3,b83),(X3,R11,A3,b84),(X3,R11,A3,b85),(X3,R11,A3,b86),(X3,R11,A3,b87),(X3,R11,A3,b88),(X3,R11,A3,b89),(X3,R11,A3,b90),(X3,R11,A3,b91),(X3,R11,A3,b92),(X3,R11,A3,b93),(X3,R11,A3,b94),(X3,R12,A1,b1),(X3,R12,A1,b2),(X3,R12,A1,b3),(X3,R12,A1,b4),(X3,R12,A1,b5),(X3,R12,A1,b6),(X3,R12,A1,b7),(X3,R12,A1,b8),(X3,R12,A1,b9),(X3,R12,A1,b10),(X3,R12,A1,b11),(X3,R12,A1,b12),(X3,R12,A1,b13),(X3,R12,A1,b14),(X3,R12,A1,b15),(X3,R12,A1,b16),(X3,R12,A1,b17),(X3,R12,A1,b18),(X3,R12,A1,b19),(X3,R12,A1,b20),(X3,R12,A1,b21),(X3,R12,A1,b22),(X3,R12,A1,b23),(X3,R12,A1,b24),(X3,R12,A1,b25),(X3,R12,A1,b26),(X3,R12,A1,b27),(X3,R12,A1,b28),(X3,R12,A1,b29),(X3,R12,A1,b30),(X3,R12,A1,b31),(X3,R12,A1,b32),(X3,R12,A1,b33),(X3,R12,A1,b34),(X3,R12,A1,b35),(X3,R12,A1,b36),(X3,R12,A1,b37),(X3,R12,A1,b38),(X3,R12,A1,b39),(X3,R12,A1,b40),(X3,R12,A1,b41),(X3,R12,A1,b42),(X3,R12,A1,b43),(X3,R12,A1,b44),(X3,R12,A1,b45),(X3,R12,A1,b46),(X3,R12,A1,b47),(X3,R12,A1,b48),(X3,R12,A1,b49),(X3,R12,A1,b50),(X3,R12,A1,b51),(X3,R12,A1,b52),(X3,R12,A1,b53),(X3,R12,A1,b54),(X3,R12,A1,b55),(X3,R12,A1,b56),(X3,R12,A1,b57),(X3,R12,A1,b58),(X3,R12,A1,b59),(X3,R12,A1,b60),(X3,R12,A1,b61),(X3,R12,A1,b62),(X3,R12,A1,b63),(X3,R12,A1,b64),(X3,R12,A1,b65),(X3,R12,A1,b66),(X3,R12,A1,b67),(X3,R12,A1,b68),(X3,R12,A1,b69),(X3,R12,A1,b70),(X3,R12,A1,b71),(X3,R12,A1,b72),(X3,R12,A1,b73),(X3,R12,A1,b74),(X3,R12,A1,b75),(X3,R12,A1,b76),(X3,R12,A1,b77),(X3,R12,A1,b78),(X3,R12,A1,b79),(X3,R12,A1,b80),(X3,R12,A1,b81),(X3,R12,A1,b82),(X3,R12,A1,b83),(X3,R12,A1,b84),(X3,R12,A1,b85),(X3,R12,A1,b86),
(X3,R12,A1,b87),(X3,R12,A1,b88),(X3,R12,A1,b89),(X3,R12,A1,b90),(X3,R12,A1,b91),(X3,R12,A1,b92),(X3,R12,A1,b93),(X3,R12,A1,b94),(X3,R12,A2,b1),(X3,R12,A2,b2),(X3,R12,A2,b3),(X3,R12,A2,b4),(X3,R12,A2,b5),(X3,R12,A2,b6),(X3,R12,A2,b7),(X3,R12,A2,b8),(X3,R12,A2,b9),(X3,R12,A2,b10),(X3,R12,A2,b11),(X3,R12,A2,b12),(X3,R12,A2,b13),(X3,R12,A2,b14),(X3,R12,A2,b15),(X3,R12,A2,b16),(X3,R12,A2,b17),(X3,R12,A2,b18),(X3,R12,A2,b19),(X3,R12,A2,b20),(X3,R12,A2,b21),(X3,R12,A2,b22),(X3,R12,A2,b23),(X3,R12,A2,b24),(X3,R12,A2,b25),(X3,R12,A2,b26),(X3,R12,A2,b27),(X3,R12,A2,b28),(X3,R12,A2,b29),(X3,R12,A2,b30),(X3,R12,A2,b31),(X3,R12,A2,b32),(X3,R12,A2,b33),(X3,R12,A2,b34),(X3,R12,A2,b35),(X3,R12,A2,b36),
(X3,R12,A2,b37),(X3,R12,A2,b38),(X3,R12,A2,b39),(X3,R12,A2,b40),(X3,R12,A2,b41),(X3,R12,A2,b42),(X3,R12,A2,b43),(X3,R12,A2,b44),(X3,R12,A2,b45),(X3,R12,A2,b46),(X3,R12,A2,b47),(X3,R12,A2,b48),(X3,R12,A2,b49),(X3,R12,A2,b50),(X3,R12,A2,b51),(X3,R12,A2,b52),(X3,R12,A2,b53),(X3,R12,A2,b54),(X3,R12,A2,b55),(X3,R12,A2,b56),(X3,R12,A2,b57),(X3,R12,A2,b58),(X3,R12,A2,b59),(X3,R12,A2,b60),(X3,R12,A2,b61),(X3,R12,A2,b62),(X3,R12,A2,b63),(X3,R12,A2,b64),(X3,R12,A2,b65),(X3,R12,A2,b66),(X3,R12,A2,b67),(X3,R12,A2,b68),(X3,R12,A2,b69),(X3,R12,A2,b70),(X3,R12,A2,b71),(X3,R12,A2,b72),(X3,R12,A2,b73),(X3,R12,A2,b74),(X3,R12,A2,b75),(X3,R12,A2,b76),(X3,R12,A2,b77),(X3,R12,A2,b78),(X3,R12,A2,b79),(X3,R12,A2,b80),(X3,R12,A2,b81),(X3,R12,A2,b82),(X3,R12,A2,b83),(X3,R12,A2,b84),(X3,R12,A2,b85),(X3,R12,A2,b86),(X3,R12,A2,b87),(X3,R12,A2,b88),(X3,R12,A2,b89),(X3,R12,A2,b90),(X3,R12,A2,b91),(X3,R12,A2,b92),(X3,R12,A2,b93),(X3,R12,A2,b94),(X3,R12,A3,b1),(X3,R12,A3,b2),(X3,R12,A3,b3),(X3,R12,A3,b4),(X3,R12,A3,b5),(X3,R12,A3,b6),(X3,R12,A3,b7),(X3,R12,A3,b8),(X3,R12,A3,b9),(X3,R12,A3,b10),(X3,R12,A3,b11),(X3,R12,A3,b12),(X3,R12,A3,b13),(X3,R12,A3,b14),(X3,R12,A3,b15),(X3,R12,A3,b16),(X3,R12,A3,b17),(X3,R12,A3,b18),(X3,R12,A3,b19),(X3,R12,A3,b20),(X3,R12,A3,b21),(X3,R12,A3,b22),(X3,R12,A3,b23),(X3,R12,A3,b24),(X3,R12,A3,b25),(X3,R12,A3,b26),(X3,R12,A3,b27),(X3,R12,A3,b28),(X3,R12,A3,b29),(X3,R12,A3,b30),(X3,R12,A3,b31),(X3,R12,A3,b32),(X3,R12,A3,b33),(X3,R12,A3,b34),(X3,R12,A3,b35),(X3,R12,A3,b36),(X3,R12,A3,b37),(X3,R12,A3,b38),(X3,R12,A3,b39),(X3,R12,A3,b40),(X3,R12,A3,b41),(X3,R12,A3,b42),(X3,R12,A3,b43),(X3,R12,A3,b44),(X3,R12,A3,b45),(X3,R12,A3,b46),(X3,R12,A3,b47),(X3,R12,A3,b48),(X3,R12,A3,b49),(X3,R12,A3,b50),
(X3,R12,A3,b51),(X3,R12,A3,b52),(X3,R12,A3,b53),(X3,R12,A3,b54),(X3,R12,A3,b55),(X3,R12,A3,b56),(X3,R12,A3,b57),(X3,R12,A3,b58),(X3,R12,A3,b59),(X3,R12,A3,b60),(X3,R12,A3,b61),(X3,R12,A3,b62),(X3,R12,A3,b63),(X3,R12,A3,b64),(X3,R12,A3,b65),(X3,R12,A3,b66),(X3,R12,A3,b67),(X3,R12,A3,b68),(X3,R12,A3,b69),(X3,R12,A3,b70),(X3,R12,A3,b71),(X3,R12,A3,b72),(X3,R12,A3,b73),(X3,R12,A3,b74),(X3,R12,A3,b75),(X3,R12,A3,b76),(X3,R12,A3,b77),(X3,R12,A3,b78),(X3,R12,A3,b79),(X3,R12,A3,b80),(X3,R12,A3,b81),(X3,R12,A3,b82),(X3,R12,A3,b83),(X3,R12,A3,b84),(X3,R12,A3,b85),(X3,R12,A3,b86),(X3,R12,A3,b87),(X3,R12,A3,b88),(X3,R12,A3,b89),(X3,R12,A3,b90),(X3,R12,A3,b91),(X3,R12,A3,b92),(X3,R12,A3,b93)または(X3,R12,A3,b94)。
Me メチル
Et エチル
Bz ベンゾイル
THF テトラヒドロフラン。
カラム:Shim-pack XR-ODS (2.2μm、i.d.50x3.0mm) (Shimadzu)
流速:1.6 mL/分
カラムオーブン:50℃
UV検出波長:254nm
移動相:[A]は0.1%ギ酸含有水溶液、[B]は0.1%ギ酸含有アセトニトリル溶液グラジェント:3分間で10%-100%溶媒[B]のリニアグラジエントを行い、1分間、100%溶媒[B]を維持した。
化合物4の合成
特許文献2(WO2008/133274)に記載の方法により調製されるアミノアルコールを常法に従い塩酸塩とした化合物1(6.1 g)のテトラヒドロフラン(60 ml)溶液に、水(30 ml)、炭酸水素ナトリウム(3.9 g)およびN-((9-フルオレニル)メトキシカルボニルオキシ)コハク酸イミド(7.8 g)を加え、室温で2時間30分間撹拌した。酢酸エチルで抽出後、無水硫酸マグネシウムで乾燥し、減圧下溶媒を留去し、残渣をジメチルスルホキシド(30 ml)に溶解し、2-ヨードキシ安息香酸(6.5 g)を加え、室温で一晩撹拌した。水を加え、酢酸エチルで抽出後、無水硫酸マグネシウムで乾燥し、減圧下溶媒を留去した、残渣をメタノール(100 ml)に溶解し、Amberlite15(2.0 g)を加え、2時間30分加熱還流した。ろ過後、減圧下溶媒を留去し、残渣をジメチルホルムアミドに溶解後、ピペリジン(2.8 ml)を加え、室温で1時間撹拌した。水を加え、酢酸エチルで抽出後、水で洗浄し、無水硫酸マグネシウムで乾燥した。減圧化溶媒を留去し、残渣をカラムクロマトグラフィーで精製し、化合物2(3.4 g)を得た。
1H-NMR (CDCl3) δ:1.56(3H,d,J=0.9Hz),2.10(1H,ddd,J=14.4,6.9,0.9Hz),2.39(1H,ddd,J=14.4,4.2,2.1Hz),3.18(3H,s),3.19(3H,s),4.13(1H,dd,J=6.9,4.2Hz),7.16(1H,dd,J=10.8,8.9Hz),8.16(1H,ddd,J=8.9,4.0,3.0Hz),8.62(1H,dd,J=6.9,3.0Hz)。
第一工程で得られた化合物2(3.4 g)のアセトン(12 ml)溶液に、0℃でベンゾイルイソチオシアナート(1.7 ml)を加え、30分間撹拌した。減圧下溶媒留去し、残渣に濃硫酸 (13 ml)を加え、40℃で一晩撹拌した。氷(40 g)およびテトラヒドロフラン(10 ml)を加え、28%アンモニア水でアルカリ性にした後、酢酸エチルで抽出し、無水硫酸マグネシウムで乾燥した。減圧下溶媒を留去し、残渣をカラムクロマトグラフィーで精製し、化合物 3 (2.6 g)を得た。
1H-NMR(CDCl3)δ:1.72(3H,d,J=0.9Hz),6.26(1H,dd,J=9.5,4.6Hz),6.35(1H,d,J=9.5Hz),7.16(1H,dd,J=10.5,8.9Hz),8.13(1H,ddd,J=8.9,4.1,3.0Hz),8.41(1H,dd,J=6.9,3.0Hz)。
第二工程で得られた化合物3(2.6 g)の酢酸(13 ml)及び水(1.3 ml)溶液に50℃で鉄(2.2 g)を加え、1時間撹拌した。28%アンモニア水でアルカリ性にした後、酢酸エチルを加え、不溶物をろ過で除いた後、酢酸エチルで抽出し、無水硫酸マグネシウムで乾燥した。減圧下溶媒を留去し化合物4(2.1 g)を得た。
1H-NMR(CDCl3)δ:1.67(3H,s),3.53(2H,br),6.20-6.29(2H,m),6.48(1H,ddd,J=8.4,4.0,3.0Hz),6.75(1H,dd,J=6.6,3.0Hz),6.81(1H,dd,J=11.1,8.4Hz)。
化合物8の合成
化合物1(1.20 g)にアセトン(70 ml)-水(40 ml)溶液にベンゾイルイソチオシアナート(0.82 g)のアセトン(10 ml)溶液を0℃で加え、室温で2時間撹拌した。減圧下溶媒を留去した後、残渣をカラムクロマトグラフィーで精製し、化合物5(1.35 g)を得た。
1H-NMR (CDCl3) δ:1.69(1H,t,J=4.7Hz),2.14(3H,s),2.21-2.31(1H,m),2.73-2.83(1H,m),3.78-3.98(2H,m),7.15(1H,dd,J=11.1,9.1Hz),7.48-7.55(2H,m),7.60-7.67(1H,m),7.85(2H,d,7.2Hz),8.14-8.20(1H,m),8.30-8.34(1H,m),8.81(1H,s),11.56(1H,s)。
第一工程で得られた化合物5(1.26 g)のアセトニトリル(5 ml)溶液に、ヨウ化メチル(0.30 ml)およびジイソプロピルエチルアミン(0.84 ml)を加え、室温で32時間、40℃で2時間撹拌した。水を加え、酢酸エチルで抽出した。水、飽和食塩水で順次洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下溶媒留去し、残渣をカラムクロマトグラフィーで精製し、化合物6(1.11 g)を得た。
1H-NMR (CDCl3) δ:1.88(3H,s),2.30-2.40(1H,m),2.66-2.74(1H,m),4.01-4.10(1H,m),4.42-4.49(1H,m),7.25-7.32(1H,m),7.39-7.54(3H,m),8.21-8.29(3H,m),8.37(1H,dd,J=7.1,2.9Hz),11.90(1H,br)。
第二工程で得られた化合物6(1.10 g)に濃硫酸(3.28 ml)を加え、80℃で1.5時間撹拌した。氷冷下、反応液を飽和重曹水に加え、酢酸エチルで抽出した。水、飽和食塩水で順次洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下溶媒留去し、残渣をカラムクロマトグラフィーで精製し、化合物7(0.615 g)を得た。
1H-NMR (CDCl3) δ:1.58(3H,s),2.22(2H,t,J=5.4Hz),3.86-3.94(1H,m),4.15-4.25(3H,m),7.14(1H,dd,J=10.7,8.9Hz),8.09-8.15(1H,m),8.62(1H,dd,J=7.0,3.0Hz)。
第三工程で得られた化合物7(614 mg)のTHF(5 ml)溶液に10%パラジウム-炭素(120 mg)を加え、水素雰囲気下20時間撹拌した。反応液をセライトを用いてろ過し、ろ液を減圧濃縮した。得られた残渣をカラムクロマトグラフィーで精製し、さらに酢酸エチル-ヘキサンで再結晶して、化合物4(400 mg)を得た。
1H-NMR (CDCl3) δ:1.54(3H,s),1.97-2.07(1H,m),2.30-2.38(1H,m),3.54(2H,brs),3.83(1H,dt,J=3.2,10.6Hz),4.10(1H,ddd,10.6,4.7,4.2Hz),6.48(1H,ddd,8.4,3.7,3.2Hz),6.78(1H,dd,J=11.8,8.4Hz),6.86(1H,dd,J=6.9,3.0Hz)。
化合物I-17の合成
1H-NMR(CDCl3)δ:1.70(3H,s),3.88(3H,s),4.65(2H,br),6.23-6.33(2H,m),6.66(1H,dd,J=10.2,5.2Hz),6.91-7.02(3H,m),7.43(1H,dd,J=7.1,2.9Hz),7.78(1H,dd,J=5.0,1.3Hz),7.84-7.91(1H,m)。
化合物I-6の合成
1H-NMR (CDCl3) δ:1.58(3H,s),2.02-2.12(1H,m),2.33-2.42(1H,m),3.82-4.00(3H,m),3.89(3H,s),4.09-4.17(1H,m),6.67(1H,dd,J=7.9,5.0Hz),6.93-6.99(2H,m),7.01(1H,brs),7.34(1H,dd,J=7.9,3.0Hz),7.79(1H,dd,J=5.0,1.3Hz),8.02-8.08(1H,m)。
化合物 I-5の合成
1H-NMR (CDCl3) δ:1.61(3H,s),1.81-1.91(1H,m),2.43-2.52(1H,m),2.67-2.76(1H,m),2.89-2.97(1H,m),3.95(2H,br),6.66-6.71(1H,m),6.73(1H,d,J=8.6Hz),6.83(1H,brs),6.98(1H,dd,J=11.8,8.7Hz),7.17-7.21(1H,m),7.30-7.36(1H,m),7.41-7.48(1H,m),8.15(1H,dd,J=5.0,1.0Hz)。
化合物I-1の合成
1H-NMR (CDCl3) δ:1.55(3H,s),1.80-1.90(1H,m),2.43-2.52(1H,m),2.60-2.70(1H,m),2.89-2.97(1H,m),5.00(2H,br),6.41(1H,d,J=6.0Hz),6.98(1H,dd,J=10.9,9.2Hz),7.17-7.23
(2H,m),8.17(1H,d,J=6.0Hz),8.58(1H,s),9.07(1H,br)。
化合物I-2の合成
1H-NMR (CDCl3) δ:1.62(3H,s),1.81-1.91(1H,m),2.44-2.52(1H,m),2.67-2.76(1H,m),2.88-2.96(1H,m),4.52(2H,br),6.68(1H,t,J=4.7Hz),7.01(1H,dd,J=11.7,8.7Hz),7.25-7.29(1H,m),7.43(1H,brs),7.75-7.81(1H,m),8.38(2H,d,J=4.7Hz)。
I-32:
1H-NMR (CDCl3) δ:1.57(s,3H),1.80-1.90(m,1H),2.15-2.24(m,1H),2.72-2.90(m,2H),3.89(s,3H),4.35(br,2H),6.68(dd,J=7.9,5.0Hz,1H),6.90-6.98(m,1H),7.06(brs,1H),7.29(t,J=7.9Hz,1H),7.41(s,1H),7.80-7.87(m,2H).
I-33:
1H-NMR (CDCl3) δ:1.57(s,3H),1.81-1.92(m,1H),2.10-2.20(m,1H),2.73-2.83(m,1H),2.86-2.95(m,1H),4.36(br,2H),6.78(dd,J=7.7,5.0Hz,1H),7.04(br,1H),7.07-7.11(m,1H),7.30-7.40(m,2H),7.63-7.67(m,1H),7.77(dd,J=7.7,2.0Hz,1H),8.37(dd,J=5.0,2.0Hz,1H).
I-34:
1H-NMR (CDCl3) δ:0.92(t,J=7.2Hz,3H),1.38(sext,J=7.2Hz,2H),1.53-1.64(m,2H),1.62(d,J=1.2Hz,3H),1.86-1.96(m,1H),2.40-2.50(m,1H),2.71-2.81(m,1H),2.91-3.00(m,1H),3.45(t,J=6.5Hz,2H),4.37(s,2H),4.40(br,2H),6.93(brs,1H),7.01(dd,J=11.7,8.7Hz,1H),7.24-7.30(m,1H),7.59(d,J=2.0Hz,1H),7.77-7.83(m,1H),8.03(d,J=2.0Hz,1H).
I-35:
1H-NMR (CDCl3) δ:1.62(d,J=1.3Hz,3H),1.85-1.96(m,1H),2.42-2.52(m,1H),2.70-2.80(m,1H),2.90-3.00(m,1H),3.70(br,2H),4.56(s,2H),6.92(brs,1H),7.00(dd,J=11.8,8.9Hz,1H),7.33(dd,J=7.2,2.9Hz,1H),7.60(d,J=2.2Hz,1H),7.70-7.76(m,1H),8.02(d,J=2.2Hz,1H).
I-36:
1H-NMR (CDCl3) δ:1.59(s,3H),1.79-1.90(m,1H),2.44-2.53(m,1H),2.74(dt,J=3.5,11.9Hz,1H),2.81(d,J=4.9Hz,3H),2.87-2.96(m,1H),3.48(br,1H),4.30(br,2H),6.11(brs,1H),6.79-7.03(m,4H),7.26-7.34(m,1H),7.70(d,J=4.7Hz,1H).
I-37:
1H-NMR (CDCl3) δ:1.62(d,J=1.3Hz,3H),1.85-1.95(m,1H),2.42-2.52(m,1H),2.67(s,6H),2.72-2.82(m,1H),2.90-2.99(m,1H),4.40(br,2H),6.69(dd,J=7.6,5.0Hz,1H),6.99(dd,J=11.9,8.7Hz,1H),7.22(dd,J=7.2,2.9Hz,1H),7.26(dd,J=7.6,1.7Hz,1H),7.45(brs,1H),7.91-7.97(m,2H).
I-38:
1H-NMR (CDCl3) δ:7.49(1H,dd,J=7.60,1.52Hz),7.38-7.30(2H,m),7.20(1H,d,J=8.62Hz),7.15(1H,t,J=1.77Hz),7.10-7.06(2H,m),6.83(1H,dd,J=11.15,4.06Hz),6.34(1H,s),4.35(1H,brs),2.96-2.90(1H,m),2.79-2.72(1H,m),2.15-2.09(1H,m),1.90-1.83(1H,m),1.56(3H,s).
I-39:
1H-NMR (CDCl3) δ:7.29(1H,dd,J=7.35,1.77Hz),7.23(1H,t,J=7.86Hz),7.08(1H,t,J=1.77Hz),7.04(1H,dd,J=8.11,1.52Hz),6.90-6.81(4H,m),6.18(1H,s),4.38(2H,brs),3.89(3H,s),2.91-2.85(1H,m),2.80-2.74(1H,m),2.18-2.12(1H,m),1.86-1.79(1H,m),1.56(3H,s).
96穴ハーフエリアプレート(黒色プレート;コースター社製)の各ウェルに48.5μlの基質ペプチド(ビオチン-XSEVNLDAEFRHDSGC-Eu:X=ε-アミノ-n-カプロン酸、Eu=ユーロピウムクリプテート)溶液を入れ、0.5μlの被検化合物(N,N'-ジメチルホルムアルデヒド溶液)および1μlの組み替えヒトBACE1(R&D systems社製)をそれぞれ添加した後30℃にて3時間反応した。基質ペプチドはビオチン-XSEVNLDAEFRHDSGC(ペプチド研究所製)にクリプテート TBPCOOH mono SMP(CIS bio international社製)を反応させることにより合成した。基質ペプチドの最終濃度は18 nmol/L、組み替えヒトBACE1の最終濃度は7.4 nmol/Lとし、反応バッファーには酢酸ナトリウム緩衝液(50 mmol/L 酢酸ナトリウムpH 5.0、0.008% Triton X-100)を用いた。反応終了後、リン酸緩衝液(150 mmol/L K2HPO4-KH2PO4 pH 7.0、0.008 % Triton X-100、0.8 mol/L KF)に溶解した8.0 μg/ml のストレプトアビジン-XL665(CIS bio international社製)を各ウェルに50μlずつ添加し、30℃にて1時間静置した。その後、蛍光強度(励起波長 320nm、測定波長 620nmおよび665nm)をワラック1420マルチラベルカウンター(Perkin Elmer life sciences社製)を用いて測定した。酵素活性は各測定波長のカウント率(10000 x カウント 665/カウント 620)から求め、酵素活性を50%阻害する用量(IC50)を算出した。被検物質のIC50値を表2に示す。表中、「μM」は「μmol/L」を表す。
ヒト野生型βAPPを過剰発現させた神経芽細胞腫SH-SY5Y細胞(SH/APPwt)を8×105 セル/mLに調整し、1ウェルあたり150 μlずつ96ウェル培養プレート(Falcon社製)に蒔き、37℃、5%炭酸ガスインキュベータ内で2時間培養した。その後、被検化合物(DMSO:ジメチルスルホキシド溶液)を2μl/50μl培地となるようにあらかじめ添加・懸濁した溶液を細胞液に添加した。すなわち、最終DMSO濃度が1%、細胞培養液は200μlとなった。被検化合物添加から24時間インキュベートした後、培養上清を100μlずつ回収し、その中に含まれるAβ量を測定した。
被験化合物を0.5%メチルセルロースに懸濁させ、最終濃度2mg/mLとなるように調製し、雄性Crj:SDラット(7~9週齢)に対し、10mg/kgとなるように経口投与する。基剤対照群は0.5%メチルセルロースのみを投与し、各群3~8匹で投与試験を実施する。投与3時間後に脳を摘出し、大脳半球を単離し、重量を測定した後、速やかに液体窒素中にて凍結させ、抽出日まで-80℃にて保存する。凍結した大脳半球を氷冷下テフロン(登録商標)製ホモゲナイザーに移し、重量の5倍容量の抽出バッファー(1%CHAPS({3-〔(3-クロルアミドプロピル)ジメチルアンモニオ〕-1-プロパンスルホネート})、20mmol/L Tris-HCl(pH8.0)、150 mmol/L NaCl、Complete(Roche社製)プロテアーゼ阻害剤含有)を加え、上下動を繰り返し2分間ホモゲナイズし可溶化する。懸濁液を遠心用のチューブに移し、3時間以上氷上にて放置し、その後、100,000xg、4℃、20分遠心する。遠心後、上清をβアミロイド40測定用のELISAプレート(和光純薬工業製:製品番号294-62501)に移す。ELISA測定は添付の説明書に従い行う。減少作用は各試験の基剤対照群の脳内βアミロイド40に対する割合として算出する。
CYP3A4蛍光MBI試験は、代謝反応による化合物のCYP3A4阻害の増強を調べる試験であり、酵素に大腸菌発現CYP3A4を用いて、7-ベンジルオキシトリフルオロメチルクマリン(7-BFC)がCYP3A4酵素により脱ベンジル化し、蛍光を発する代謝物7-ハイドロキシトリフルオロメチルクマリン(HFC)を生成する反応を指標として行った。
(結果)
化合物I-3:(-)。
市販のプールドヒト肝ミクロソームを用いて、ヒト主要CYP5分子種(CYP1A2、2C9、2C19、2D6、3A4)の典型的基質代謝反応として7-エトキシレゾルフィンのO-脱エチル化(CYP1A2)、トルブタミドのメチル-水酸化(CYP2C9)、メフェニトインの4’-水酸化(CYP2C19)、デキストロメトルファンのO脱メチル化(CYP2D6)、テルフェナジンの水酸化(CYP3A4)を指標とし、それぞれの代謝物生成量が被検化合物によって阻害される程度を評価した。
(結果)
化合物I-10:5種>21μM。
凍結保存しているネズミチフス菌(Salmonella typhimurium TA98株、TA100株)20 μLを10 mL液体栄養培地(2.5% Oxoid nutrient broth No.2)に接種し37℃にて10 時間、振盪前培養する。TA98株は9mLの菌液を遠心(2000×g、10 分間)して培養液を除去し、9mLのMicro F緩衝液(K2HPO4:3.5 g/L、KH2PO4:1 g/L、(NH4)2SO4:1g/L、クエン酸三ナトリウム二水和物:0.25 g/L、MgSO4・7H20:0.1g/L)に菌を懸濁し、110 mLのExposure培地(ビオチン:8 μg/mL、ヒスチジン:0.2 μg/mL、グルコース:8 mg/mLを含むMicroF緩衝液)に添加し、TA100株は3.16mL菌液に対しExposure培地120mLに添加し試験菌液を調製する。被験物質DMSO溶液(最高用量50mg/mLから2倍公比で8段階希釈)、陰性対照としてDMSO、陽性対照として非代謝活性化条件ではTA98株に対しては50 μg/mLの4-ニトロキノリン-1-オキシドDMSO溶液、TA100株に対しては0.25 μg/mLの2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド DMSO溶液、代謝活性化条件ではTA98株に対して40μg/mLの2-アミノアントラセンDMSO溶液、TA100株に対しては20 μg/mLの2-アミノアントラセンDMSO溶液それぞれ12 μLと試験菌液588μL(代謝活性化条件では試験菌液498 μLとS9 mix 90 μLの混合液)を混和し、37℃にて90分間、振盪培養する。被験物質を暴露した菌液460 μLを、Indicator培地(ビオチン:8 μg/mL、ヒスチジン:0.2 μg/mL、グルコース:8 mg/mL、ブロモクレゾールパープル:37.5 μg/mLを含むMicroF緩衝液)2300μLに混和し50 μLずつマイクロプレート48ウェル/用量に分注し、37℃にて 3日間、静置培養する。アミノ酸(ヒスチジン)合成酵素遺伝子の突然変異によって増殖能を獲得した菌を含むウェルは、pH変化により紫色から黄色に変色するため、1用量あたり48ウェル中の黄色に変色した菌増殖ウェルを計数し、陰性対照群と比較して評価する。変異原性が陰性のものを(-)、陽性のものを(+)として示す。
被験化合物の10mM DMSO溶液の2倍希釈系列(12 points)を媒体(JP-I,JP-II)に添加(2%)し、4時間後の濁度(晶析情報)から、溶解性を3段階評価(High;>40μM,Medium;3~40μM,Low;<3μM)した。
(結果)
化合物I-9:High。
市販のプールドヒト肝ミクロソームを用いて、対象化合物を一定時間反応させ、反応サンプルと未反応サンプルの比較により残存率を算出し、肝で代謝される程度を評価した。
(結果)
化合物I-33:95%。
心電図QT間隔延長のリスク評価を目的として、human ether-a-go-go related gene (hERG) チャンネルを発現させたHEK293細胞を用いて、心室再分極過程に重要な役割を果たす遅延整流K+電流(IKr)への作用を検討した。
(結果)
化合物I-1:3.2%。
適当な容器に検体を適量入れ、JP-1液(塩化ナトリウム2.0g、塩酸7.0mLに水を加えて1000mLとした)、JP-2液(pH6.8のリン酸塩緩衝液500mLに水500mLを加えた)、20mmol/L TCA(タウロコール酸ナトリウム)/JP-2液(TCA 1.08gに水を加え100mLとした)を200μLずつ添加する。試験液添加後に溶解する場合には、適宜原末を追加する。密閉し37℃で1時間振とうする。濾過し、各濾液100μLにメタノール100μLを添加して2倍希釈を行う。希釈倍率は、必要に応じて変更する。気泡および析出物がないかを確認し、密閉して振とうする。絶対検量線法によりHPLCを用いて定量を行う。
経口吸収性の検討実験材料と方法
(1)使用動物:マウスまたはラットを使用する。
(2)飼育条件:マウスまたはラットは、固形飼料および滅菌水道水を自由摂取させる。
(3)投与量、群分けの設定:経口投与、静脈内投与を所定の投与量により投与する。以下のように群を設定する(化合物ごとで投与量は変更有)。
経口投与 1~30mg/kg(n=2~3)
静脈内投与 0.5~10mg/kg(n=2~3)
(4)投与液の調製:経口投与は溶液または懸濁液として投与する。静脈内投与は可溶化して投与する。
(5)投与方法:経口投与は、経口ゾンデにより強制的に胃内に投与する。静脈内投与は、注射針を付けたシリンジにより尾静脈から投与する。
(6)評価項目:経時的に採血し、血漿中薬物濃度をLC/MS/MSを用いて測定する。
(7)統計解析:血漿中濃度推移について、非線形最小二乗法プログラムWinNonlin(登録商標)を用いて血漿中濃度‐時間曲線下面積(AUC)を算出し、経口投与群と静脈内投与群のAUCからバイオアベイラビリティ(BA)を算出する。
ラットに0.5mg/mL/kgの用量で静脈内投与し、30分後にイソフルラン麻酔下で下大動脈より全採血により放血死させる。その後、脳を摘出し、蒸留水で20-25%のホモジネートを調製した。一方、得られた血液は遠心処理後、血漿にする。その後、脳サンプルにはコントロール血漿を、血漿サンプルにはコントロール脳を1:1で添加し、それぞれのサンプルをLC/MS/MSを用いて測定した。得られた測定時のエリア比(脳/血漿)を脳Kp値とした。
(結果)
化合物I-11:2.2。
以下の成分を含有する顆粒剤を製造する。
乳糖 700 mg
コーンスターチ 274 mg
HPC-L 16 mg
1000 mg
式(I)で示される化合物と乳糖を60メッシュのふるいに通す。コーンスターチを120メッシュのふるいに通す。これらをV型混合機にて混合する。混合末にHPC-L(低粘度ヒドロキシプロピルセルロース)水溶液を添加し、練合、造粒(押し出し造粒 孔径0.5~1mm)、乾燥工程する。得られた乾燥顆粒を振動ふるい(12/60メッシュ)で櫛過し顆粒剤を得る。
以下の成分を含有するカプセル充填用顆粒剤を製造する。
乳糖 90 mg
コーンスターチ 42 mg
HPC-L 3 mg
150 mg
式(I)で示される化合物、乳糖を60メッシュのふるいに通す。コーンスターチを120メッシュのふるいに通す。これらを混合し、混合末にHPC-L溶液を添加して練合、造粒、乾燥する。得られた乾燥顆粒を整粒後、その150mgを4号硬ゼラチンカプセルに充填する。
以下の成分を含有する錠剤を製造する。
乳糖 90 mg
微結晶セルロース 30 mg
CMC-Na 15 mg
ステアリン酸マグネシウム 5 mg
150 mg
式(I)で示される化合物、乳糖、微結晶セルロース、CMC-Na(カルボキシメチルセルロース ナトリウム塩)を60メッシュのふるいに通し、混合する。混合末にステアリン酸マグネシウム混合し、製錠用混合末を得る。本混合末を直打し、150mgの錠剤を得る。
以下の成分を加温混合後、滅菌して注射剤とする。
非イオン界面活性剤 15 mg
注射用精製水 1 ml
Claims (19)
- 式(I):
(式中、R1は置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアシル、シアノ、カルボキシ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアルケニルオキシカルボニル、置換もしくは非置換のアルキニルオキシカルボニル、置換もしくは非置換のカルバモイル、置換もしくは非置換のチオカルバモイル、置換もしくは非置換の炭素環式基または置換もしくは非置換の複素環式基であり、
R2aおよびR2bは各々独立して水素、置換もしくは非置換のアルキル、置換もしくは非置換のアシル、置換もしくは非置換のアルコキシカルボニルまたは置換もしくは非置換のカルバモイルであり、
XはSまたはOであり、
XがSのとき、
であり、
XがOのとき、
であり、
R3a、R3b、R4aおよびR4bは各々独立して
水素、ハロゲン、ヒドロキシ、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアシル、置換もしくは非置換のアシルオキシ、置換もしくは非置換のアルコキシ、置換もしくは非置換のアルケニルオキシ、置換もしくは非置換のアルキニルオキシ、置換もしくは非置換のアルキルチオ、置換もしくは非置換のアルケニルチオ、置換もしくは非置換のアルキニルチオ、カルボキシ、シアノ、ニトロ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアルケニルオキシカルボニル、置換もしくは非置換のアルキニルオキシカルボニル、置換もしくは非置換のアミノ、置換もしくは非置換のカルバモイル、置換もしくは非置換のチオカルバモイル、置換もしくは非置換のスルファモイル、置換もしくは非置換のアルキルスルフィニル、置換もしくは非置換のアルケニルスルフィニル、置換もしくは非置換のアルキニルスルフィニル、置換もしくは非置換のアルキルスルホニル、置換もしくは非置換のアルケニルスルホニル、置換もしくは非置換のアルキニルスルホニル、置換もしくは非置換の炭素環式基、置換もしくは非置換の炭素環オキシ、置換もしくは非置換の炭素環チオ、置換もしくは非置換の炭素環アルキル、置換もしくは非置換の炭素環アルコキシ、置換もしくは非置換の炭素環オキシカルボニル、置換もしくは非置換の炭素環スルフィニル、置換もしくは非置換の炭素環スルホニル、置換もしくは非置換の複素環式基、置換もしくは非置換の複素環オキシ、置換もしくは非置換の複素環チオ、置換もしくは非置換の複素環アルキル、置換もしくは非置換の複素環アルコキシ、置換もしくは非置換の複素環オキシカルボニル、置換もしくは非置換の複素環スルフィニルまたは置換もしくは非置換の複素環スルホニルであり、
R3aおよびR3bが、それらが結合する炭素原子と一緒になって置換もしくは非置換の炭素環または置換もしくは非置換の複素環を形成してもよく、
R4aおよびR4bが、それらが結合する炭素原子と一緒になって置換もしくは非置換の炭素環または置換もしくは非置換の複素環を形成してもよく、
R3cおよびR3dは各々独立して水素、ハロゲン、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシ、置換もしくは非置換のアルケニルオキシ、置換もしくは非置換のアルキニルオキシ、置換もしくは非置換のアルキルチオ、置換もしくは非置換のアルケニルチオ、置換もしくは非置換のアルキニルチオ、置換もしくは非置換のアシル、カルボキシ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアルケニルオキシカルボニル、置換もしくは非置換のアルキニルオキシカルボニル、置換もしくは非置換のアミノ、置換もしくは非置換のカルバモイル、置換もしくは非置換のチオカルバモイル、置換もしくは非置換の炭素環式基、置換もしくは非置換の炭素環オキシ、置換もしくは非置換の炭素環チオ、置換もしくは非置換の炭素環アルキル、置換もしくは非置換の炭素環アルコキシ、置換もしくは非置換の炭素環オキシカルボニル、置換もしくは非置換の複素環式基、置換もしくは非置換の複素環オキシ、置換もしくは非置換の複素環チオ、置換もしくは非置換の複素環アルキル、置換もしくは非置換の複素環アルコキシまたは置換もしくは非置換の複素環オキシカルボニルであるか、またはR3cおよびR3dが、それらが結合する炭素原子と一緒になって置換もしくは非置換の非芳香族炭素環または置換もしくは非置換の非芳香族複素環を形成し、
R5は水素、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニルまたは置換もしくは非置換のアシルであり、
L1およびL2は各々独立して単結合、置換もしくは非置換のアルキレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)、置換もしくは非置換のアルケニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)または置換もしくは非置換のアルキニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)であり、
環Aは置換もしくは非置換の炭素環または置換もしくは非置換の複素環であり、
1)L1およびL2が単結合であり、
であるとき、
環Bは置換もしくは非置換の炭素環、置換もしくは非置換のピリジン、置換もしくは非置換のピリミジンまたは置換もしくは非置換の5員複素環であり、
2)L1およびL2が単結合であり、
であるとき、
環Bは置換もしくは非置換の炭素環または置換もしくは非置換の複素環であり、
3)L1およびL2の少なくとも一方が置換もしくは非置換のアルキレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)、置換もしくは非置換のアルケニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)または置換もしくは非置換のアルキニレン(ただし置換基はハロゲン、アルコキシ、ハロゲノアルコキシ、ヒドロキシアルコキシ、アルコキシアルコキシ、アシル、アシルオキシ、カルボキシ、アルコキシカルボニル、アミノ、アシルアミノ、アルキルアミノ、イミノ、ヒドロキシイミノ、アルコキシイミノ、アルキルチオ、カルバモイル、アルキルカルバモイル、ヒドロキシアルキルカルバモイル、スルファモイル、アルキルスルファモイル、アルキルスルフィニル、アルキルスルホニルアミノ、アルキルスルホニルアルキルアミノ、アルキルスルホニルイミノ、アルキルスルフィニルアミノ、アルキルスルフィニルアルキルアミノ、アルキルスルフィニルイミノ、シアノ、ニトロ、炭素環式基および複素環式基(それぞれの炭素環および複素環はハロゲン、アルキル、ヒドロキシおよびアルコキシからなる群から選択される1以上の基で置換されていてもよい)からなる群から選択される1以上の基)であるとき、
環Bは置換された含窒素芳香族単環である。ただし、以下の化合物を除く。
)
で示される化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。 - L1およびL2が単結合である、請求項1記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- 環Aが置換もしくは非置換のベンゼンであり、環Bが置換もしくは非置換のピリジンまたは置換もしくは非置換のピリミジンである、請求項1または2記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- R3aが水素、置換もしくは非置換のアルキル、シアノ、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のカルバモイル、置換もしくは非置換の炭素環式基または置換もしくは非置換の複素環式基であり、R3b、R4aおよびR4bが水素である、請求項4記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- XがSである、請求項4または5記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- R1が炭素数1~3の非置換アルキルである、請求項1~7のいずれかに記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- R2aおよびR2bが共に水素である、請求項1~8のいずれかに記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- 請求項1~9のいずれかに記載の化合物、もしくはその製薬上許容される塩またはそれらの溶媒和物を有効成分とすることを特徴とする、医薬組成物。
- 請求項1~9のいずれかに記載の化合物、もしくはその製薬上許容される塩またはそれらの溶媒和物を有効成分とすることを特徴とする、BACE1阻害活性を有する医薬組成物。
- アミロイドβタンパク質の産生、分泌または沈着により誘発される疾患の治療のための医薬である請求項10または11記載の医薬組成物。
- アルツハイマー症の治療のための医薬である請求項10または11記載の医薬組成物。
- 請求項1~9のいずれかに記載の化合物、もしくはその製薬上許容される塩またはそれらの溶媒和物を投与することを特徴とする、BACE1活性を阻害する方法。
- BACE1活性を阻害するために使用する請求項1~9のいずれかに記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- 請求項1~9のいずれかに記載の化合物、もしくはその製薬上許容される塩またはそれらの溶媒和物を投与することを特徴とする、アミロイドβタンパク質の産生、分泌または沈着により誘発される疾患の治療方法。
- アミロイドβタンパク質の産生、分泌または沈着により誘発される疾患の治療のために使用する請求項1~9のいずれかに記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
- 請求項1~9のいずれかに記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物を投与することを特徴とする、アルツハイマー症の治療方法。
- アルツハイマー症の治療のために使用する、請求項1~9のいずれかに記載の化合物もしくはその製薬上許容される塩またはそれらの溶媒和物。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201080061302XA CN102686584A (zh) | 2009-11-13 | 2010-11-12 | 具有氨基连接基的氨基噻嗪或氨基噁嗪衍生物 |
| EP10829723.5A EP2500344A4 (en) | 2009-11-13 | 2010-11-12 | AMINOTHIAZIN OR AMINOOXAZINE DERIVATIVES WITH AN AMINO TERMINATION |
| JP2011540420A JPWO2011058763A1 (ja) | 2009-11-13 | 2010-11-12 | アミノリンカーを有するアミノチアジンまたはアミノオキサジン誘導体 |
| US13/508,899 US20120238557A1 (en) | 2009-11-13 | 2010-11-12 | Aminothiazine or aminooxazine derivative having amino linker |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009-260514 | 2009-11-13 | ||
| JP2009260514 | 2009-11-13 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2011058763A1 true WO2011058763A1 (ja) | 2011-05-19 |
Family
ID=43991429
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2010/006680 WO2011058763A1 (ja) | 2009-11-13 | 2010-11-12 | アミノリンカーを有するアミノチアジンまたはアミノオキサジン誘導体 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20120238557A1 (ja) |
| EP (1) | EP2500344A4 (ja) |
| JP (1) | JPWO2011058763A1 (ja) |
| CN (1) | CN102686584A (ja) |
| WO (1) | WO2011058763A1 (ja) |
Cited By (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8168630B2 (en) | 2007-04-24 | 2012-05-01 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives substituted with a cyclic group |
| WO2012057248A1 (ja) | 2010-10-29 | 2012-05-03 | 塩野義製薬株式会社 | ナフチリジン誘導体 |
| WO2012057247A1 (ja) | 2010-10-29 | 2012-05-03 | 塩野義製薬株式会社 | 縮合アミノジヒドロピリミジン誘導体 |
| US8173642B2 (en) | 2005-10-25 | 2012-05-08 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives |
| US8207164B2 (en) | 2009-07-24 | 2012-06-26 | Novartis Ag | Oxazine derivatives and their use in the treatment of neurological disorders |
| WO2012147763A1 (ja) | 2011-04-26 | 2012-11-01 | 塩野義製薬株式会社 | オキサジン誘導体およびそれを含有するbace1阻害剤 |
| WO2012147762A1 (ja) | 2011-04-26 | 2012-11-01 | 塩野義製薬株式会社 | ピリジン誘導体およびそれを含有するbace1阻害剤 |
| WO2012156284A1 (en) * | 2011-05-16 | 2012-11-22 | F. Hoffmann-La Roche Ag | 1,3-oxazines as bace1 and/or bace2 inhibitors |
| US8338413B1 (en) | 2012-03-07 | 2012-12-25 | Novartis Ag | Oxazine derivatives and their use in the treatment of neurological disorders |
| US8524897B2 (en) | 2011-01-12 | 2013-09-03 | Novartis Ag | Crystalline oxazine derivative |
| US8557826B2 (en) | 2009-10-08 | 2013-10-15 | Merck Sharp & Dohme Corp. | Pentafluorosulfur imino heterocyclic compounds as BACE-1 inhibitors, compositions, and their use |
| US8563543B2 (en) | 2009-10-08 | 2013-10-22 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as bace inhibitors, compositions, and their use |
| US8569310B2 (en) | 2009-10-08 | 2013-10-29 | Merck Sharp & Dohme Corp. | Pentafluorosulfur imino heterocyclic compounds as BACE-1 inhibitors, compositions and their use |
| US8637504B2 (en) | 2008-06-13 | 2014-01-28 | Shionogi & Co., Ltd. | Sulfur-containing heterocyclic derivative having beta secretase inhibitory activity |
| US8637508B2 (en) | 2011-01-13 | 2014-01-28 | Novartis Ag | Heterocyclic derivatives and their use in the treatment of neurological disorders |
| US8653067B2 (en) | 2007-04-24 | 2014-02-18 | Shionogi & Co., Ltd. | Pharmaceutical composition for treating Alzheimer's disease |
| WO2014059185A1 (en) | 2012-10-12 | 2014-04-17 | Amgen Inc. | Amino - dihydrothiazine and amino - dioxido dihydrothiazine compounds as beta-secretase antagonists and methods of use |
| US8703785B2 (en) | 2008-10-22 | 2014-04-22 | Shionogi & Co., Ltd. | 2-aminopyrimidin-4-one and 2-aminopyridine derivatives both having BACE1-inhibiting activity |
| US8729071B2 (en) | 2009-10-08 | 2014-05-20 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as BACE inhibitors, compositions and their use |
| WO2014078314A1 (en) | 2012-11-15 | 2014-05-22 | Amgen Inc. | Amino-oxazine and amino-dihydrothiazine compounds as beta-secretase modulators and methods of use |
| JP2014515382A (ja) * | 2011-05-27 | 2014-06-30 | エフ.ホフマン−ラ ロシュ アーゲー | Bace1及び/又はbace2阻害剤としてのスピロ−[1,3]−オキサジン及びスピロ−[1,4]−オキサゼピン誘導体 |
| JP5554346B2 (ja) * | 2009-12-09 | 2014-07-23 | 塩野義製薬株式会社 | 含硫黄複素環誘導体を含有するアルツハイマー症の治療用または予防用医薬組成物 |
| CN103974940A (zh) * | 2011-12-06 | 2014-08-06 | 詹森药业有限公司 | 5-(3-氨基苯基)-5-烷基-5,6-二氢-2h-[1,4]噁嗪-3-胺衍生物 |
| WO2014134341A1 (en) | 2013-03-01 | 2014-09-04 | Amgen Inc. | Perfluorinated 5,6-dihydro-4h-1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| WO2014138484A1 (en) | 2013-03-08 | 2014-09-12 | Amgen Inc. | Perfluorinated cyclopropyl fused 1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| JP2014532066A (ja) * | 2011-10-13 | 2014-12-04 | ノバルティス アーゲー | オキサジン誘導体および神経障害の処置におけるその使用 |
| JP2015504906A (ja) * | 2012-01-26 | 2015-02-16 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | フルオロメチル−5,6−ジヒドロ−4h−[1,3]オキサジン |
| US8999980B2 (en) | 2009-12-11 | 2015-04-07 | Shionogi & Co., Ltd. | Oxazine derivatives |
| US9145426B2 (en) | 2011-04-07 | 2015-09-29 | Merck Sharp & Dohme Corp. | Pyrrolidine-fused thiadiazine dioxide compounds as BACE inhibitors, compositions, and their use |
| WO2015156421A1 (en) | 2014-04-11 | 2015-10-15 | Shionogi & Co., Ltd. | Dihydrothiazine and dihydrooxazine derivatives having bace1 inhibitory activity |
| US9181236B2 (en) | 2011-08-22 | 2015-11-10 | Merck Sharp & Dohme Corp. | 2-spiro-substituted iminothiazines and their mono-and dioxides as bace inhibitors, compositions and their use |
| US9221839B2 (en) | 2011-04-07 | 2015-12-29 | Merck Sharp & Dohme Corp. | C5-C6 oxacyclic-fused thiadiazine dioxide compounds as BACE inhibitors, compositions, and their use |
| WO2016012384A1 (en) | 2014-07-22 | 2016-01-28 | F. Hoffmann-La Roche Ag | Trifluormethyloxazine amidines as bace1 inhibitors |
| US9499502B2 (en) | 2011-04-13 | 2016-11-22 | Merck Sharp & Dohme Corp. | 5-substituted iminothiazines and their mono- and dioxides as BACE inhibitors, compositions, and their use |
| US9540359B2 (en) | 2012-10-24 | 2017-01-10 | Shionogi & Co., Ltd. | Dihydrooxazine or oxazepine derivatives having BACE1 inhibitory activity |
| US9550762B2 (en) | 2014-08-08 | 2017-01-24 | Amgen, Inc. | Cyclopropyl fused thiazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| WO2017061534A1 (en) | 2015-10-08 | 2017-04-13 | Shionogi & Co., Ltd. | Dihydrothiazine derivatives |
| US11629154B2 (en) | 2018-04-27 | 2023-04-18 | Shionogi & Co., Ltd. | Tetrahydropyranooxazine derivatives having selective BACE1 inhibitory activity |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101730937B1 (ko) | 2010-06-09 | 2017-04-27 | 얀센 파마슈티카 엔.브이. | 베타-세크레타아제(bace) 저해제로 유용한 5,6-디하이드로-2h-[1,4]옥사진-3-일-아민 유도체 |
| SG191097A1 (en) | 2010-12-22 | 2013-08-30 | Janssen Pharmaceutica Nv | 5,6-DIHYDRO-IMIDAZO[1,2-a]PYRAZIN-8-YLAMINE DERIVATIVES USEFUL AS INHIBITORS OF BETA-SECRETASE (BACE) |
| KR102012671B1 (ko) | 2011-03-01 | 2019-08-21 | 얀센 파마슈티카 엔.브이. | 베타-세크레타제(BACE)의 억제제로서 유용한 6,7-디하이드로-피라졸로[1,5-a]피라진-4-일아민 유도체 |
| MX340031B (es) | 2011-03-09 | 2016-06-21 | Janssen Pharmaceutica Nv | Derivados de 3,4-dihidropirrolo[1,2-a]pirazin-1-ilamina utiles como inhibidores de beta-secretasa (bace). |
| WO2014120658A1 (en) | 2013-01-29 | 2014-08-07 | Amgen Inc. | Fused multicyclic 3-amino-5,6-dihydro-2h-1,4-thiazine derivatives and their use as beta-secretase inhibitors |
| AU2014280124B2 (en) | 2013-06-12 | 2018-11-01 | Janssen Pharmaceutica Nv | 4-amino-6-phenyl-5,6-dihydroimidazo[1,5-a]pyrazine derivatives as inhibitors of beta-secretase (BACE) |
| EA032662B1 (ru) | 2013-06-12 | 2019-06-28 | Янссен Фармацевтика Нв | ПРОИЗВОДНЫЕ 4-АМИНО-6-ФЕНИЛ-5,6-ДИГИДРОИМИДАЗО[1,5-а]ПИРАЗИН-3(2H)-ОНА В КАЧЕСТВЕ ИНГИБИТОРОВ БЕТА-СЕКРЕТАЗЫ (BACE) |
| CN105324383B (zh) | 2013-06-12 | 2017-10-31 | 詹森药业有限公司 | 作为β‑分泌酶(BACE)抑制剂的4‑氨基‑6‑苯基‑6,7‑二氢[1,2,3]三唑并[1,5‑A]吡嗪衍生物 |
| US9096615B2 (en) | 2013-07-30 | 2015-08-04 | Amgen Inc. | Bridged bicyclic amino thiazine dioxide compounds as inhibitors of beta-secretase and methods of use thereof |
| CA2967164A1 (en) | 2014-12-18 | 2016-06-23 | Janssen Pharmaceutica Nv | 2,3,4,5-tetrahydropyridin-6-amine and 3,4-dihydro-2h-pyrrol-5-amine compound inhibitors of beta-secretase |
| WO2017024180A1 (en) | 2015-08-06 | 2017-02-09 | Amgen Inc. | Vinyl fluoride cyclopropyl fused thiazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| WO2017216726A1 (en) | 2016-06-13 | 2017-12-21 | Glaxosmithkline Intellectual Property Development Limited | Substituted pyridines as inhibitors of dnmt1 |
| MX2019007103A (es) | 2016-12-15 | 2019-11-05 | Amgen Inc | Derivados de tiazina condensados con ciclopropilo como inhibidores de beta-secretasa y metodos de uso. |
| MX2019007104A (es) | 2016-12-15 | 2019-11-05 | Amgen Inc | Derivados de dioxido de 1,4-tiazina y dioxido de 1,2,4-tiadiazina como inhibidores de beta-secretasa y metodos de uso. |
| CA3047285A1 (en) | 2016-12-15 | 2018-06-21 | Amgen Inc. | Bicyclic thiazine and oxazine derivatives as beta-secretase inhibitors and methods of use |
| AU2017376441B2 (en) | 2016-12-15 | 2021-10-14 | Amgen Inc. | Oxazine derivatives as beta-secretase inhibitors and methods of use |
| CA3047288A1 (en) | 2016-12-15 | 2018-06-21 | Amgen Inc. | Thiazine derivatives as beta-secretase inhibitors and methods of use |
| CN107056729A (zh) * | 2017-03-15 | 2017-08-18 | 华东师范大学 | 噻嗪类衍生物及其合成方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DD140144A1 (de) | 1978-11-08 | 1980-02-13 | Horst Hartmann | Verfahren zur herstellung von p-aminophenylsubstituierten 2-amino-1,3-thiaziniumsalzen |
| WO2007049532A1 (ja) | 2005-10-25 | 2007-05-03 | Shionogi & Co., Ltd. | アミノジヒドロチアジン誘導体 |
| WO2008133273A1 (ja) | 2007-04-24 | 2008-11-06 | Shionogi & Co., Ltd. | アルツハイマー症治療用医薬組成物 |
| WO2008133274A1 (ja) | 2007-04-24 | 2008-11-06 | Shionogi & Co., Ltd. | 環式基で置換されたアミノジヒドロチアジン誘導体 |
| WO2009091016A1 (ja) | 2008-01-18 | 2009-07-23 | Eisai R & D Management Co., Ltd. | 縮合アミノジヒドロチアジン誘導体 |
| WO2009151098A1 (ja) * | 2008-06-13 | 2009-12-17 | 塩野義製薬株式会社 | βセクレターゼ阻害作用を有する含硫黄複素環誘導体 |
-
2010
- 2010-11-12 US US13/508,899 patent/US20120238557A1/en not_active Abandoned
- 2010-11-12 CN CN201080061302XA patent/CN102686584A/zh active Pending
- 2010-11-12 JP JP2011540420A patent/JPWO2011058763A1/ja not_active Withdrawn
- 2010-11-12 EP EP10829723.5A patent/EP2500344A4/en not_active Withdrawn
- 2010-11-12 WO PCT/JP2010/006680 patent/WO2011058763A1/ja active Application Filing
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DD140144A1 (de) | 1978-11-08 | 1980-02-13 | Horst Hartmann | Verfahren zur herstellung von p-aminophenylsubstituierten 2-amino-1,3-thiaziniumsalzen |
| WO2007049532A1 (ja) | 2005-10-25 | 2007-05-03 | Shionogi & Co., Ltd. | アミノジヒドロチアジン誘導体 |
| WO2008133273A1 (ja) | 2007-04-24 | 2008-11-06 | Shionogi & Co., Ltd. | アルツハイマー症治療用医薬組成物 |
| WO2008133274A1 (ja) | 2007-04-24 | 2008-11-06 | Shionogi & Co., Ltd. | 環式基で置換されたアミノジヒドロチアジン誘導体 |
| WO2009091016A1 (ja) | 2008-01-18 | 2009-07-23 | Eisai R & D Management Co., Ltd. | 縮合アミノジヒドロチアジン誘導体 |
| WO2009151098A1 (ja) * | 2008-06-13 | 2009-12-17 | 塩野義製薬株式会社 | βセクレターゼ阻害作用を有する含硫黄複素環誘導体 |
Non-Patent Citations (15)
| Title |
|---|
| "Isotopes in the Physical and Biomedical Sciences", vol. 1, 1987 |
| D. H. HUA ET AL., SULFUR REPORTS, vol. 21, 1999, pages 211 - 239 |
| D.H.HUA ET AL., SULFUR REPORTS, vol. 21, 1999, pages 211 - 239 |
| JOURNAL OF HETEROCYCLIC CHEMISTRY, vol. 14, 1977, pages 717 - 723 |
| RICHARD C LAROCK: "Comprehensive Organic Transformations", MCGRAW-HILL |
| See also references of EP2500344A4 * |
| T. FUJISAWA ET AL., TETRAHEDRON LETT., vol. 37, 1996, pages 3881 - 3884 |
| T. VILAVAN ET AL., CURRENT ORGANIC CHEMISTRY, vol. 9, 2005, pages 1315 - 1392 |
| T.FUJISAWA ET AL., TETRAHEDRON LETT., vol. 37, 1996, pages 3881 - 3884 |
| T.VILAVAN ET AL., CURRENT ORGANIC CHEMISTRY, vol. 9, 2005, pages 1315 - 1392 |
| TETRAHEDRON, vol. 65, 2009, pages 757 - 764 |
| THEODORA W GREEN: "Protective Groups in Organic Synthesis", JOHN WILEY & SONS |
| THEODORA W GREENE: "Protective Groups in organic Synthesis", JOHN WILEY & SONS |
| Y KORIYAMA ET AL., TETRAHEDRON, vol. 58, 2002, pages 9621 - 9628 |
| Y.KORIYAMA ET AL., TETRAHEDRON, vol. 58, 2002, pages 9621 - 9628 |
Cited By (71)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8546380B2 (en) | 2005-10-25 | 2013-10-01 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives |
| US9029358B2 (en) | 2005-10-25 | 2015-05-12 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives |
| US8173642B2 (en) | 2005-10-25 | 2012-05-08 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives |
| US8815851B2 (en) | 2005-10-25 | 2014-08-26 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives |
| US8633188B2 (en) | 2005-10-25 | 2014-01-21 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives |
| US8895548B2 (en) | 2007-04-24 | 2014-11-25 | Shionogi & Co., Ltd. | Pharmaceutical composition for treating alzheimer's disease |
| US8884062B2 (en) | 2007-04-24 | 2014-11-11 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives substituted with a cyclic group |
| US8653067B2 (en) | 2007-04-24 | 2014-02-18 | Shionogi & Co., Ltd. | Pharmaceutical composition for treating Alzheimer's disease |
| US8168630B2 (en) | 2007-04-24 | 2012-05-01 | Shionogi & Co., Ltd. | Aminodihydrothiazine derivatives substituted with a cyclic group |
| US8637504B2 (en) | 2008-06-13 | 2014-01-28 | Shionogi & Co., Ltd. | Sulfur-containing heterocyclic derivative having beta secretase inhibitory activity |
| US9650371B2 (en) | 2008-06-13 | 2017-05-16 | Shionogi & Co., Ltd. | Sulfur-containing heterocyclic derivative having beta secretase inhibitory activity |
| US9273053B2 (en) | 2008-06-13 | 2016-03-01 | Shionogi & Co., Ltd. | Sulfur-containing heterocyclic derivative having Beta secretase inhibitory activity |
| US8703785B2 (en) | 2008-10-22 | 2014-04-22 | Shionogi & Co., Ltd. | 2-aminopyrimidin-4-one and 2-aminopyridine derivatives both having BACE1-inhibiting activity |
| US8207164B2 (en) | 2009-07-24 | 2012-06-26 | Novartis Ag | Oxazine derivatives and their use in the treatment of neurological disorders |
| US8846658B2 (en) | 2009-07-24 | 2014-09-30 | Novartis Ag | Oxazine derivatives and their use in the treatment of neurological disorders |
| US9687494B2 (en) | 2009-10-08 | 2017-06-27 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as BACE inhibitors, compositions, and their use |
| US9475785B2 (en) | 2009-10-08 | 2016-10-25 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as BACE inhibitors, compositions and their use |
| US9428475B2 (en) | 2009-10-08 | 2016-08-30 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as BACE inhibitors, compositions, and their use |
| US8569310B2 (en) | 2009-10-08 | 2013-10-29 | Merck Sharp & Dohme Corp. | Pentafluorosulfur imino heterocyclic compounds as BACE-1 inhibitors, compositions and their use |
| US8729071B2 (en) | 2009-10-08 | 2014-05-20 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as BACE inhibitors, compositions and their use |
| US8563543B2 (en) | 2009-10-08 | 2013-10-22 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as bace inhibitors, compositions, and their use |
| US9029362B2 (en) | 2009-10-08 | 2015-05-12 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as brace inhibitors, compositions, and their use |
| US8940748B2 (en) | 2009-10-08 | 2015-01-27 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as BACE inhibitors, compositions, and their use |
| US8557826B2 (en) | 2009-10-08 | 2013-10-15 | Merck Sharp & Dohme Corp. | Pentafluorosulfur imino heterocyclic compounds as BACE-1 inhibitors, compositions, and their use |
| JP5554346B2 (ja) * | 2009-12-09 | 2014-07-23 | 塩野義製薬株式会社 | 含硫黄複素環誘導体を含有するアルツハイマー症の治療用または予防用医薬組成物 |
| US9656974B2 (en) | 2009-12-11 | 2017-05-23 | Shionogi & Co., Ltd. | Oxazine derivatives |
| US9290466B2 (en) | 2009-12-11 | 2016-03-22 | Shionogi & Co., Ltd. | Oxazine derivatives |
| US8999980B2 (en) | 2009-12-11 | 2015-04-07 | Shionogi & Co., Ltd. | Oxazine derivatives |
| US9018219B2 (en) | 2010-10-29 | 2015-04-28 | Shionogi & Co., Ltd. | Fused aminodihydropyrimidine derivative |
| WO2012057247A1 (ja) | 2010-10-29 | 2012-05-03 | 塩野義製薬株式会社 | 縮合アミノジヒドロピリミジン誘導体 |
| WO2012057248A1 (ja) | 2010-10-29 | 2012-05-03 | 塩野義製薬株式会社 | ナフチリジン誘導体 |
| US8927721B2 (en) | 2010-10-29 | 2015-01-06 | Shionogi & Co., Ltd. | Naphthyridine derivative |
| US8524897B2 (en) | 2011-01-12 | 2013-09-03 | Novartis Ag | Crystalline oxazine derivative |
| US10301296B2 (en) | 2011-01-13 | 2019-05-28 | Novartis Ag | Heterocyclic derivatives and their use in the treatment of neurological disorders |
| US10035794B2 (en) | 2011-01-13 | 2018-07-31 | Novartis Ag | Heterocyclic derivatives and their use in the treatment of neurological disorders |
| US9550758B2 (en) | 2011-01-13 | 2017-01-24 | Novartis Ag | Heterocyclic derivatives and their use in the treatment of neurological disorders |
| US8637508B2 (en) | 2011-01-13 | 2014-01-28 | Novartis Ag | Heterocyclic derivatives and their use in the treatment of neurological disorders |
| US8865712B2 (en) | 2011-01-13 | 2014-10-21 | Novartis Ag | Heterocyclic derivatives and their use in the treatment of neurological disorders |
| US10683287B2 (en) | 2011-01-13 | 2020-06-16 | Novartis Ag | Heterocyclic derivatives and their use in the treatment of neurological disorders |
| US9221839B2 (en) | 2011-04-07 | 2015-12-29 | Merck Sharp & Dohme Corp. | C5-C6 oxacyclic-fused thiadiazine dioxide compounds as BACE inhibitors, compositions, and their use |
| US9145426B2 (en) | 2011-04-07 | 2015-09-29 | Merck Sharp & Dohme Corp. | Pyrrolidine-fused thiadiazine dioxide compounds as BACE inhibitors, compositions, and their use |
| US9499502B2 (en) | 2011-04-13 | 2016-11-22 | Merck Sharp & Dohme Corp. | 5-substituted iminothiazines and their mono- and dioxides as BACE inhibitors, compositions, and their use |
| US8883779B2 (en) | 2011-04-26 | 2014-11-11 | Shinogi & Co., Ltd. | Oxazine derivatives and a pharmaceutical composition for inhibiting BACE1 containing them |
| WO2012147762A1 (ja) | 2011-04-26 | 2012-11-01 | 塩野義製薬株式会社 | ピリジン誘導体およびそれを含有するbace1阻害剤 |
| WO2012147763A1 (ja) | 2011-04-26 | 2012-11-01 | 塩野義製薬株式会社 | オキサジン誘導体およびそれを含有するbace1阻害剤 |
| WO2012156284A1 (en) * | 2011-05-16 | 2012-11-22 | F. Hoffmann-La Roche Ag | 1,3-oxazines as bace1 and/or bace2 inhibitors |
| CN103534243A (zh) * | 2011-05-16 | 2014-01-22 | 霍夫曼-拉罗奇有限公司 | 作为bace1和/或bace2抑制剂的1,3-噁嗪类 |
| US8785436B2 (en) | 2011-05-16 | 2014-07-22 | Hoffmann-La Roche Inc. | 1,3-oxazines as BACE 1 and/or BACE2 inhibitors |
| JP2014515382A (ja) * | 2011-05-27 | 2014-06-30 | エフ.ホフマン−ラ ロシュ アーゲー | Bace1及び/又はbace2阻害剤としてのスピロ−[1,3]−オキサジン及びスピロ−[1,4]−オキサゼピン誘導体 |
| US9181236B2 (en) | 2011-08-22 | 2015-11-10 | Merck Sharp & Dohme Corp. | 2-spiro-substituted iminothiazines and their mono-and dioxides as bace inhibitors, compositions and their use |
| JP2014532066A (ja) * | 2011-10-13 | 2014-12-04 | ノバルティス アーゲー | オキサジン誘導体および神経障害の処置におけるその使用 |
| CN103974940B (zh) * | 2011-12-06 | 2016-08-24 | 詹森药业有限公司 | 5-(3-氨基苯基)-5-烷基-5,6-二氢-2h-[1,4]噁嗪-3-胺衍生物 |
| CN103974940A (zh) * | 2011-12-06 | 2014-08-06 | 詹森药业有限公司 | 5-(3-氨基苯基)-5-烷基-5,6-二氢-2h-[1,4]噁嗪-3-胺衍生物 |
| JP2015504906A (ja) * | 2012-01-26 | 2015-02-16 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | フルオロメチル−5,6−ジヒドロ−4h−[1,3]オキサジン |
| US8338413B1 (en) | 2012-03-07 | 2012-12-25 | Novartis Ag | Oxazine derivatives and their use in the treatment of neurological disorders |
| WO2014059185A1 (en) | 2012-10-12 | 2014-04-17 | Amgen Inc. | Amino - dihydrothiazine and amino - dioxido dihydrothiazine compounds as beta-secretase antagonists and methods of use |
| US9540359B2 (en) | 2012-10-24 | 2017-01-10 | Shionogi & Co., Ltd. | Dihydrooxazine or oxazepine derivatives having BACE1 inhibitory activity |
| US9758513B2 (en) | 2012-10-24 | 2017-09-12 | Shionogi & Co., Ltd. | Dihydrooxazine or oxazepine derivatives having BACE1 inhibitory activity |
| WO2014078314A1 (en) | 2012-11-15 | 2014-05-22 | Amgen Inc. | Amino-oxazine and amino-dihydrothiazine compounds as beta-secretase modulators and methods of use |
| JP2016511258A (ja) * | 2013-03-01 | 2016-04-14 | アムジエン・インコーポレーテツド | ベータ−セクレターゼ阻害剤としてのパーフルオロ化5,6−ジヒドロ−4h−1,3−オキサジン−2−アミン化合物および使用方法 |
| US9296734B2 (en) | 2013-03-01 | 2016-03-29 | Amgen Inc. | Perfluorinated 5,6-dihydro-4H-1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| WO2014134341A1 (en) | 2013-03-01 | 2014-09-04 | Amgen Inc. | Perfluorinated 5,6-dihydro-4h-1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| US9611261B2 (en) | 2013-03-08 | 2017-04-04 | Amgen Inc. | Perfluorinated cyclopropyl fused 1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| WO2014138484A1 (en) | 2013-03-08 | 2014-09-12 | Amgen Inc. | Perfluorinated cyclopropyl fused 1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| US9085576B2 (en) | 2013-03-08 | 2015-07-21 | Amgen Inc. | Perfluorinated cyclopropyl fused 1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| KR20160141849A (ko) | 2014-04-11 | 2016-12-09 | 시오노기세이야쿠가부시키가이샤 | Bace1 저해 작용을 갖는 디하이드로티아진 및 디하이드로옥사진 유도체 |
| WO2015156421A1 (en) | 2014-04-11 | 2015-10-15 | Shionogi & Co., Ltd. | Dihydrothiazine and dihydrooxazine derivatives having bace1 inhibitory activity |
| WO2016012384A1 (en) | 2014-07-22 | 2016-01-28 | F. Hoffmann-La Roche Ag | Trifluormethyloxazine amidines as bace1 inhibitors |
| US9550762B2 (en) | 2014-08-08 | 2017-01-24 | Amgen, Inc. | Cyclopropyl fused thiazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| WO2017061534A1 (en) | 2015-10-08 | 2017-04-13 | Shionogi & Co., Ltd. | Dihydrothiazine derivatives |
| US11629154B2 (en) | 2018-04-27 | 2023-04-18 | Shionogi & Co., Ltd. | Tetrahydropyranooxazine derivatives having selective BACE1 inhibitory activity |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2500344A1 (en) | 2012-09-19 |
| EP2500344A4 (en) | 2013-05-01 |
| CN102686584A (zh) | 2012-09-19 |
| US20120238557A1 (en) | 2012-09-20 |
| JPWO2011058763A1 (ja) | 2013-03-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2011058763A1 (ja) | アミノリンカーを有するアミノチアジンまたはアミノオキサジン誘導体 | |
| US9656974B2 (en) | Oxazine derivatives | |
| US20120258961A1 (en) | 4-amino-1,3-thiazine or oxazine derivative | |
| KR101324426B1 (ko) | β 세크레타제 저해 작용을 갖는 황 함유 복소환 유도체 | |
| JP5554346B2 (ja) | 含硫黄複素環誘導体を含有するアルツハイマー症の治療用または予防用医薬組成物 | |
| WO2011070781A1 (ja) | 置換アミノチアジン誘導体 | |
| JP5766198B2 (ja) | 縮合アミノジヒドロピリミジン誘導体 | |
| WO2011071109A1 (ja) | アミノ基を有する縮合ヘテロ環化合物 | |
| JP5816630B2 (ja) | ナフチリジン誘導体 | |
| JP2012250933A (ja) | オキサジン誘導体を含有するアルツハイマー症治療用または予防用医薬組成物 | |
| JPWO2010047372A1 (ja) | Bace1阻害活性を有する2−アミノピリミジン−4−オンおよび2−アミノピリジン誘導体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201080061302.X Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 10829723 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011540420 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13508899 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2010829723 Country of ref document: EP |