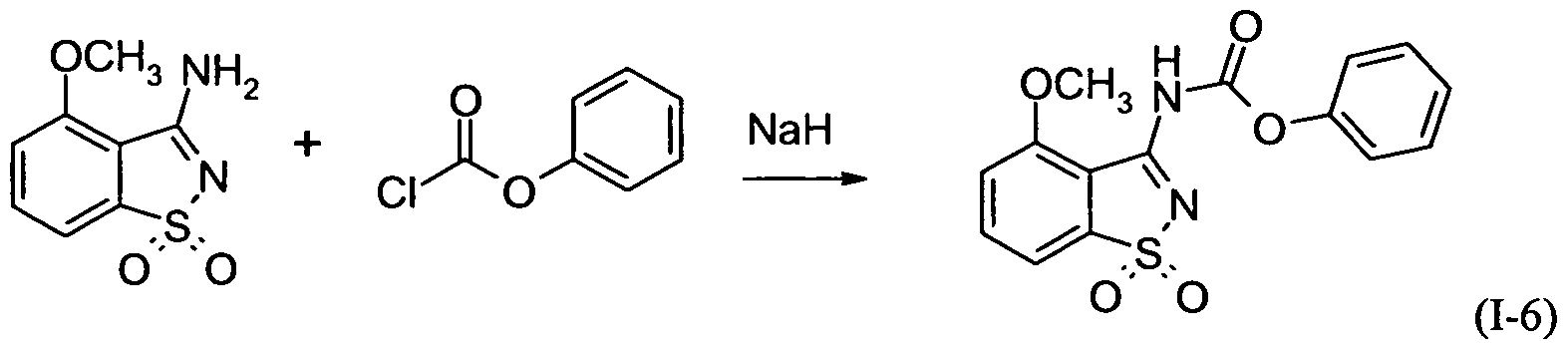
WO2009141065A2 - (1,2-benzisothiazol-3-yl)(thio)carbamate und (1,2-benzisothiazol-3-yl)(thio)oxamate und deren oxidationsformen als pestizide - Google Patents
(1,2-benzisothiazol-3-yl)(thio)carbamate und (1,2-benzisothiazol-3-yl)(thio)oxamate und deren oxidationsformen als pestizide Download PDFInfo
- Publication number
- WO2009141065A2 WO2009141065A2 PCT/EP2009/003304 EP2009003304W WO2009141065A2 WO 2009141065 A2 WO2009141065 A2 WO 2009141065A2 EP 2009003304 W EP2009003304 W EP 2009003304W WO 2009141065 A2 WO2009141065 A2 WO 2009141065A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- spp
- alkyl
- alkoxy
- formula
- compounds
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- NGHXJLFSNFUNBZ-UHFFFAOYSA-N CCOC(NC(c1ccccc11)=NS1(=O)=O)=O Chemical compound CCOC(NC(c1ccccc11)=NS1(=O)=O)=O NGHXJLFSNFUNBZ-UHFFFAOYSA-N 0.000 description 1
- QNOQSOJREDRYBC-UHFFFAOYSA-N NC(c1ccccc11)=NS1(=O)=O Chemical compound NC(c1ccccc11)=NS1(=O)=O QNOQSOJREDRYBC-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/80—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,2
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/08—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having one or more single bonds to nitrogen atoms
- A01N47/10—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof
- A01N47/18—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof containing a —O—CO—N< group, or a thio analogue thereof, directly attached to a heterocyclic or cycloaliphatic ring
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/08—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having one or more single bonds to nitrogen atoms
- A01N47/10—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof
- A01N47/22—O-Aryl or S-Aryl esters thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D275/00—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings
- C07D275/04—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D275/00—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings
- C07D275/04—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings condensed with carbocyclic rings or ring systems
- C07D275/06—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings condensed with carbocyclic rings or ring systems with hetero atoms directly attached to the ring sulfur atom
Definitions
- the present invention relates to a method for controlling animal pests by applying insecticidal and / or acaricidal agents, in particular in combination with agents for increasing the activity, and to novel pesticides and to a plurality of methods for their production.
- EP 133418 are 3-acylamino-l, 2-benzisothiazole as pesticides
- EP 110829 are 3-acylamino-l, 2nd benzothiazole-1, 1-dioxide as insecticides and acaricides
- EP 191734, EP 207891, and in JP 1989/01319467 are 3-acylamino-1,2-benzisothiazol-1,1-dioxides as pesticides
- DE 3544436 3- (diacylamino) -l, 2-benzisothiazol-l, l-dioxide are described as fungicides and insecticides.
- salts of sulfonic acids in which the acids themselves paralyze acting on insects (US 2,842,476).
- An increase in activity, for example, by ammonium sulfate is described, for example, for the herbicides glyphosate and phosphinothricin (US Pat. No. 6,645,914, EP-A2 0 036 106).
- the use of ammonium sulfate as a formulation aid is for certain drugs and applications WO 92/16108), but it serves to stabilize the formulation, not to increase the efficacy.
- the object of the present invention is therefore to provide corresponding benzoisothiazole derivatives which are useful as insecticides and / or acaricides, in particular with a satisfactory insecticidal and / or acaricidal activity against animal pests, with a broad spectrum against animal pests, with a high selectivity and good compatibility in crops, as well as those in combination with other agents to improve the effectiveness especially against difficult to control insects and spider mites, can be used.
- R 1 , R 2 , R 3 and R 4 independently of
- Ci-C 6 alkyl C 2 - C 6 alkenyl, C 2 -C 6 - alkynyl, C 3 -C 6 cycloalkyl, C 3 -C 6 -cycloalkyl-CrC 4 alkyl, C I -C 4 - haloalkyl, C, -C 4 haloalkylthio, C r C 4 alkylthio, Ci-C4-alkylsulfinyl, Ci-C4-haloalkylsulfinyl, Ci-C 4 - alkylsulphonyl, C, -C 4 haloalkylsulfonyl, Ci-Q- alkylcarbonyl, C r C 6 alkoxy, C 1 -C 6 - alkoxycarbonyl, C 3 -C 6 alken
- radicals may be unsubstituted or one, two or more radicals from the group
- A is hydrogen, (C 1 -C 6 -alkyl) carbonyl, (C 1 -C 6 -alkoxy) carbonyl, (C 1 -C 6 -
- radicals may be unsubstituted or one, two or more radicals from the group
- n 0, 1 or 2
- Z is C 1 -C 6 -alkyl, C 2 -C 6 -alkenyl, C 2 -C 6 -alkynyl, C 3 -C 6 -cycloalkyl, QQ-haloalkyl, C 2 -C 6 -
- Haloalkenyl, C 2 -C 6 haloalkynyl, C 3 -C 6 -Halocycloalkyl, aryl, hetaryl, C r C 6 arylalkyl, Q- C 6 -Hetarylalkyl, and in the event that Y is C ( O) also represents C r C 8 -alkoxy, QC 4 -haloalkoxy, aryloxy or hetaryloxy,
- aryl and hetaryl which is optionally mono- or polysubstituted, identically or differently with QC 6 - alkyl, C 2 -C 6 alkenyl, C 2 -C 6 - alkynyl, C 3 -C 6 cycloalkyl, C, -C 6 haloalkyl, C 2 -C 6 haloalkenyl, C 2 - C 6 haloalkynyl, C 3 -C 4 haloalkoxy may be substituted 6 halocycloalkyl, halogen, cyano, nitro, Ci-C 4 alkoxy, Ci-C,
- the compounds of formula (I) may optionally be present in different polymorphic forms or as a mixture of different polymorphic forms. Both the pure polymorphs and the polymorph mixtures are the subject of the invention and can be used according to the invention.
- the compounds of formula (I) optionally comprise diastereomers or enantiomers.
- the (1,2-benzisothiazol-3-yl) (thio) carbamates and (1,2-benzisothiazol-3-yl) (thio) oxamates and their oxidation forms are generally defined by the formula (I).
- Preferred radical definitions of the above and below formulas are given below. These definitions apply equally to the end products of formula (I) as well as to all intermediates.
- R 1 , R 2 , R 3 and R 4 are independently of each other preferably
- radicals may be unsubstituted or one, two or more radicals from the group
- R 1 , R 2 , R 3 and R 4 independently of one another are particularly preferably Hydrogen, halogen, nitro, C r C 3 alkyl, C, -C 3 haloalkyl, C, -C 3 alkylthio, C 1 -C 3 - alkylsulphonyl, C 3 -C 6 alkenyloxy, C 3 - alkoxy, C, -C 2 haloalkoxy, C r C 4 alkoxy-Ci-C4-alkyl, aryloxy, hetaryloxy, C 2 -Arylalkyloxy, C 1 -C 2 -Hetarylalkyloxy, C r C 4 alkoxycarbonyl, O-acetyl stand,
- radicals may be unsubstituted or one, two or more radicals from the group
- Ci-C 4 alkoxy can carry,
- R 1 , R 2 , R 3 and R 4 independently of one another very particularly preferably
- A preferably represents hydrogen, (Ci-C 6 alkyl) carbonyl, (Ci-C 6 alkoxy) carbonyl, (Ci-C 6 - alkylthio) carbonyl, (Ci-C 6 alkoxy) thiocarbonyl, (C r C 6 - alkylthio) thiocarbonyl, C r C 6 alkyl, C 3 -C 6 cycloalkyl, C 2 -C 6 alkenyl, C, -C 4 alkoxy , C 1 - C 4 haloalkyl, aryl, hetaryl, C r C 2 arylalkyl or CRQ-hetarylalkyl,
- A preferably stands for the rest
- Q Y 7 very particularly preferably represents the rest, n is preferably 0, 1 or 2,
- n particularly preferably represents 0 or 2
- n furthermore particularly preferred is 2,
- X is preferred and particularly preferably represents O or S,
- X very particularly preferably represents O
- Y particularly preferably represents O or S
- Y is very particularly preferably O
- Z is preferably C 1 -C 6 -alkyl, C 2 -C 6 -alkenyl, C 2 -C 6 -alkynyl, C 3 -C 6 -cycloalkyl, QC 6 -haloalkyl, C 2 -C 6 -haloalkenyl, C 2 -C 6 -Haloalkynyl, C 3 -C 6 -halocycloalkyl, aryl, hetaryl,
- Ci-C 6 arylalkyl, C r C 6 -Hetarylalkyl, and stands for the case that Y is C ( O), r for C Cg-alkoxy, Ci-C4 haloalkoxy, aryloxy, hetaryloxy,
- Z particularly preferably represents Ci-C4 alkyl, Ci-C 4 haloalkyl, C 2 -C 6 haloalkynyl, aryl and for the
- the present invention preferably also the lithium, sodium, potassium, magnesium, calcium, ammonium, Ci-C 4 -alkyl-ammonium, di- (Ci-C 4 -alkyl) -ammonium, Tn - (C 1 -C 4 -alkyl) -ammonium, tetra (C 1 -C 4 -alkyl) -ammonium, tri- (C 1 -C 4 -alkyl) -sulfonium, C 5 - or C 6 -cycloalkyl-ammonium -, di- (C r C 2 alkyl) benzyl ammonium and Tn- (Q -C 2 alkyl) benzyl ammonium salts of compounds of the formula (I) in which R 1 to R 4 , n , X, Y, Z and A have the above general, preferred, particularly preferred and especially preferred meanings and which can be prepared by generally customary processes.
- these radicals are the lower carbon skeletons, e.g. with 1 to 6 C atoms, in particular 1 to 4 C atoms, or in unsaturated groups having 2 to 6 C atoms, in particular 2 to 4 C atoms, is preferred.
- Alkyl radicals also in the composite meanings such as alkoxy, haloalkyl, etc., mean e.g. Methyl, ethyl, propyls such as n- or i-propyl, butyls such as n-, iso- or tert-butyl, pentyls such as n-pentyl, isopentyl or neo-pentyl, hexyls such as n-hexyl, i-hexyl, 3-methylpentyl, 2,2-dimethylbutyl or 2,3-dimethylbutyl, heptyls such as n-heptyl, 1-methylhexy or 1,4-dimethylpentyl; Alkenyl and alkynyl radicals have the meaning of the possible unsaturated radicals corresponding to the alkyl radicals; wherein at least one double bond or triple bond, preferably a double bond or triple bond is included.
- Alkenyl means e.g. Vinyl, allyl, 1-methylprop-2-en-1-yl, 2-methylprop-2-en-1-yl, but-2-en-1-yl, but-3-en-1-yl, 1-methylbut-3-en-1-yl and 1-methylbut-2-en-1-yl;
- Alkynyl means e.g. Ethynyl, propargyl, but-2-yn-1-yl, but-3-yn-1-yl and 1-methylbut-3-yn-1-yl.
- haloalkyl groups and haloalkyl radicals of haloalkoxy, halothiylthio, haloalkenyl, haloalkynyl, and the like are mentioned. are indicated in these residues, the lower carbon skeletons, z. B. with 1 to 6 carbon atoms or 2 to 6, in particular 1 to 4 carbon atoms or preferably 2 to 4 carbon atoms, and the corresponding unsaturated and / or substituted radicals in the carbon skeleton in each case straight-chain or branched. Examples are difluoromethyl, 2,2,2-trifluoroethyl, trifluoroallyl, 1-chloroprop-1-yl-3-yl.
- sica is used according to the invention synonymously with "halogen".
- Halogen is fluorine, chlorine, bromine or iodine.
- Haloalkoxy is, for example, OCF 3 , OCHF 2 , OCH 2 F, CF 3 CF 2 O, OCH 2 CF 3 and OCH 2 CH 2 Cl; the same applies to haloalkenyl and other halogen-substituted radicals.
- the present compounds of the general formula (I) may optionally have a chiral carbon atom.
- Corresponding chiral carbon atoms can in particular in the
- these substituents may have both an (R) and an (S) configuration.
- the present invention encompasses compounds of the general formula (I) having both (S) and (R) configuration at the respective chiral carbon atoms, that is, that the present invention covers the compounds of the general formula (I), in each of which carbon atoms are independently
- Another object of the present invention are methods for preparing corresponding compounds of general formula (I) and / or salts thereof.
- the compounds of the general formula (I) are prepared by reacting 3-amino-1,2-benzoisothiazoles of the general formula (II)
- R to R, n, X, Y, Z and A are as defined above
- Il and T are halogen and ° ⁇ c ⁇ ⁇ ⁇ z , preferably chlorine and ° ⁇ c ⁇ ⁇ ⁇ z
- the compounds of the general formula (I) are prepared by reacting (thio) carbamates and (thio) oxamates of the formula (Ib)
- the compounds of the general formula (I) are prepared by reacting (thio) carbamates and (thio) oxamates of the formula (Ic)
- inert solvents are solvents which are inert under the particular reaction conditions, ie. in particular do not react with the starting materials, but need not be inert under any reaction conditions.
- toluene particularly preferred are toluene, xylene, dichlorobenzene, chlorobenzene, acetonitrile, acetone, butyronitrile or ethyl acetate.
- the present invention is not limited to the solvents exemplified above.
- the reaction temperature at which the reactions according to the above embodiments can be carried out can vary widely. Corresponding temperatures are in the respective embodiments of the reactions called. In addition, the reactions at a temperature of 0 to 100 0 C, preferably 20 to 70 0 C, are performed.
- the reactions of the present invention are generally carried out under normal pressure. However, it is also possible to work under elevated pressure or reduced pressure, generally between 0, 1 bar and 10 bar.
- the processes for preparing the benzoisothiazoles of the general formula (I) according to the invention are carried out in the presence of a basic or acidic reaction auxiliary or cleavage reagent.
- alkali metal or alkaline earth metal hydrides such as lithium, sodium, potassium or calcium hydride, lithium, sodium or potassium amide, sodium or Potassium methoxide, sodium or potassium ethylate, sodium or potassium propylate, aluminum isopropylate, sodium or potassium tert-butoxide, sodium or potassium hydroxide, ammonium hydroxide, sodium, potassium or calcium acetate, ammonium acetate, sodium, potassium or calcium carbonate, ammonium carbonate, sodium or potassium bicarbonate, and basic organic nitrogen compounds, such as trimethylamine, triethylamine, tripropylamine, tributylamine, ethyl-diisopropylamine, N, N-dimethylcyclohexylamine, dicyclohexylamine, ethyldicy
- Acid reaction auxiliaries are all customary inorganic or organic acids. These include, for example, mineral acids such as sulfuric acid H 2 SO 4 , phosphoric acid H 3 PO 4 or hydrochloric acid HCl or organic acids such as formic acid, acetic acid or trifluoroacetic acid.
- the active compounds according to the invention are suitable for plant tolerance, favorable warm-blood toxicity and good environmental compatibility for protecting plants and plant organs, for increasing crop yields, improving the quality of the crop and for controlling animal pests, in particular insects, arachnids, helminths, nematodes and molluscs which are found in agriculture, horticulture, livestock, forests, gardens and recreational facilities, in the protection of materials and materials and in the hygiene sector. They can preferably be used as crop protection agents. They are against normal sensitive and resistant species as well as effective against all or individual stages of development.
- the above mentioned pests include:
- Anoplura e.g. Damalinia spp., Haematopinus spp., Linognathus spp., Pediculus spp., Trichodectes spp.
- arachnids e.g. Acarus siro, Aceria sheldoni, Aculops spp., Aculus spp., Amblyomma spp., Argas spp., Boophilus spp., Brevipalpus spp., Bryobia praetiosa, Chorioptes spp., Dermanyssus gallinae, Eotetranychus spp., Epitrimerus pyri, Eutetranychus spp.
- Eriophyes spp. Hemitarsonemus spp., Hyalomma spp., Ixodes spp., Latrodectus mactans, Metatetranychus spp., Oligonychus spp., Ornithodoros spp., Panonychus spp., Phyllocoptruta oleivora, Polyphagotarsonemus latus, Psoroptes spp., Rhipicephalus spp. Rhizoglyphus spp., Sarcoptes spp., Scorpio maurus, Stenotarsonemus spp., Tarsonemus spp., Tetranychus spp., Vasates lycopersici.
- Ceuthorhynchus spp. Ceuthorhynchus spp., Cleonus mendicus, Conoderus spp., Cosmopolites spp., Costelytra zealandica, Curculio spp., Cryptorhynchus lapathi, Dermestes spp., Diabrotica spp., Epilachna spp., Faustinus cubae, Gibbium psylloides, Heteronychus arator, Hylamorpha elegans, Hylotrupes bajulus, Hypera postica, Hypothenemus spp., Lachnosterna consanguinea, Leptinotarsa decemlineata, Lissorhoptrus oryzophilus, Lixus spp., Lyctus spp., Meligethes aeneus, Melolontha meiolontha, Migdolus spp., Mon ⁇ u
- Gastropoda e.g. Arion spp., Biomphalaria spp., Bulinus spp., Deroceras spp., Galba spp., Lymnaea spp., Oncomelania spp., Succinea spp.
- helminths e.g. Ancylostoma duodenale, Ancylostoma ceylanicum, Acylostoma braziliensis, Ancylostoma spp., Ascaris lubricoides, Ascaris spp., Brugia malayi, Brugia timori, Bunostomum spp., Chabertia spp., Clonorchis spp., Cooperia spp., Dicrocoelium spp., Dictyocaulus flaria, Diphyllobothrium latum, Dracunculus medinensis, Echinococcus granulosus, Echinococcus multilocularis, Enterobius vermicularis, Faciola spp., Haemonchus spp., Heterakis spp., Hymenolepis nana, Hyostrongulus spp., Loa Loa
- protozoa such as Eimeria
- Eimeria protozoa
- Heliopeltis spp. Horcias nobilellus, Leptocorisa spp., Leptoglossus phyllopus, Lygus spp., Macropes excavatus, Miridae, Nezara spp., Oebalus spp., Pentomidae, Piesma quadrata, Piezodorus spp., Psallus seriatus, Pseudacysta persea, Rhodnius spp. Sahlbergella singularis, Scotinophora spp., Stephanitis nashi, Tibraca spp., Triatoma spp.
- Sogatella furcifera Sogatodes spp., Stictocephala festina, Tenalaphara malayensis, Tinocallis caryaefoliae, Tomaspis spp., Toxoptera spp., Trialeurodes vaporariorum, Trioza spp., Typhlocyba spp., Unaspis spp., Viteus vitifolii.
- Hymenoptera e.g. Diprion spp., Hoplocampa spp., Lasius spp., Monomorium pharaonis, Vespa spp.
- Lepidoptera From the order of Lepidoptera, for example, Acronicta major, Aedia leucomelas, Agrotis spp., Alabama argillacea, Anticarsia spp., Barathra brassicae, Bucculatrix thurberiella, Bupalus piniarius, Cacoecia podana, Capua reticulana, Carpocapsa pomonella, Cheimatobia brumata, Chilo spp., Choristoneura fumiferana , Clysia ambiguella, Cnaphalocerus spp., Earias insulana, Ephestia kuehniella, Euproctis chrysorrhoea, Euxoa spp., Feltia spp., Galleria mellonella, Helicovepha spp., Heliothis spp., Hofmannophila pseudospretella, Homon
- siphonaptera e.g. Ceratophyllus spp., Xenopsylla cheopis.
- Symphyla e.g. Scutigerella immaculata.
- Thysanoptera e.g. Basothrips biformis, Enneothrips flavens, Frankliniella spp., Heliothrips spp., Hercinothrips femoralis, Kakothrips spp., Rhipiphorothrips cruentatus, Scirtothrips spp., Taeniothrips cardamoni, Thrips spp.
- Thysanura e.g. Lepisma saccharina.
- the plant parasitic nematodes include e.g. Anguina spp., Aphelenchoides spp., Belonoaimus spp., Bursaphelenchus spp., Ditylenchus dipsaci, Globodera spp., Heliocotylenchus spp., Heterodera spp., Longidorus spp., Meloidogyne spp., Pratylenchus spp., Radopholus similis, Rotylenchus spp. Trichodorus spp., Tylenchorhynchus spp., Tylenchulus spp., Tylenchulus semipenetrans, Xiphinema spp.
- Anguina spp. Aphelenchoides spp., Belonoaimus spp., Bursaphelenchus spp., Ditylenchus dipsaci, Globodera
- ammonium and phosphonium salts are defined by formula (IV)
- D is nitrogen or phosphorus
- D is preferably nitrogen
- R 5 , R 6 , R 7 , and R 8 are independently hydrogen or in each case optionally substituted Ci-Cg-alkyl or mono- or polyunsaturated, optionally substituted Ci-Cg-alkylene, wherein the substituents selected from halogen, nitro and cyano could be, R 5 , R 6 , R 7 , and R 8 preferably each independently represent hydrogen or in each case optionally substituted C 1 -C 4 -alkyl, where the substituents may be selected from halogen, nitro and cyano,
- R 5 , R 6 , R 7 , and R 8 more preferably independently of one another are hydrogen, methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, s-butyl or t-butyl,
- R 5 , R 6 , R 7 , and R 8 are very particularly preferably hydrogen
- n 1, 2, 3 or 4
- n is preferably 1 or 2
- R 9 is an inorganic or organic anion
- R 9 is preferably hydrogencarbonate, tetraborate, fluoride, bromide, iodide, chloride, monohydrogenphosphate, dihydrogenphosphate, hydrogensulphate, tartrate, sulphate, nitrate, thiosulphate, thiocyanate, formate, lactate, acetate, propionate, butyrate, pentanoate, citrate or oxalate,
- R 9 particularly preferably represents lactate, sulfate, monohydrogen phosphate, dihydrogen phosphate, nitrate, thiosulfate, thiocyanate, citrate, oxalate or formate.
- R 9 very particularly preferably represents sulfate.
- the ammonium and phosphonium salts of the formula (IV) can be used in a wide concentration range for increasing the effect of crop protection agents containing compounds of the formula (I).
- the ammonium or phosphonium salts in the ready-to-use crop protection agent are used in a concentration of 0.5 to 80 mmol / l, preferably 0.75 to 37.5 mmol / l, particularly preferably 1.5 to 25 mmol / l.
- the ammonium and / or phosphonium salt concentration in the formulation is selected to be in the specified general, preferred or more preferred ranges after dilution of the formulation to the desired drug concentration.
- the concentration of the salt in the formulation is usually 1-50 wt .-%.
- the subject of the present invention is therefore also the Use of a combination of Penetrationsforderer and ammonium and / or phosphonium salts to increase the efficacy of pesticides containing acaricidal / insecticidal compounds of the formula (I) as an active ingredient.
- the subject matter of the invention is the use of these agents for controlling harmful insects.
- Penetrationsforderer in the present context, all those substances are considered, which are commonly used to improve the penetration of agrochemical active ingredients in plants.
- Penetration requesters are in this context defined by the fact that they can penetrate from the aqueous spray mixture and / or from the spray coating into the cuticle of the plant and thereby increase the material mobility (mobility) of active ingredients in the cuticle.
- the method described in the literature can be used to determine this property.
- Suitable penetration promoters are, for example, alkanol alkoxylates.
- Inventive Penetrationsforderer are alkanol alkoxylates of the formula
- R is straight-chain or branched alkyl having 4 to 20 carbon atoms
- R 1 is hydrogen, methyl, ethyl, n-propyl, i-propyl, n-butyl, i-butyl, t-butyl, n-pentyl or n-hexyl,
- AO stands for an ethylene oxide radical, a propylene oxide radical, a butylene oxide radical or mixtures of ethylene oxide and propylene oxide radicals or butylene oxide radicals and
- v stands for numbers from 2 to 30.
- a preferred group of penetration enhancers are alkanol alkoxylates of the formula
- EO stands for -CH 2 -CH 2 -O- and n stands for numbers from 2 to 20.
- EO stands for -CH 2 -CH 2 -O-
- q stands for numbers from 1 to 10.
- EO stands for -CH 2 -CH 2 -O-
- s stands for numbers from 1 to 10.
- alkanol alkoxylates of the formula RO - (- EO-) p - (- BO-) q -R '(Vd) in which
- R and R have the meanings given above, EO is CH 2 -CH 2 -O-, BO is --CH-CH-CH-O,
- p stands for numbers from 1 to 10 and q stands for numbers from 1 to 10.
- Another preferred group of penetration enhancers are alkanol alkoxylates of the formula
- R and R have the meanings given above, BO is -CH-CH-TCH-O,
- CH 3 EO is CH 2 -CH 2 -O-, r is a number from 1 to 10 and s is a number from 1 to 10.
- Another preferred group of penetration enhancers are alkanol alkoxylates of the formula CH 3 - (CH 2 ) t -CH 2 -O - (- CH 2 -CH 2 -O-) u -R '(Vf) in which
- R ' has the meaning given above, t represents numbers from 8 to 13 u stands for numbers from 6 to 17.
- R is preferably butyl, isobutyl, n-pentyl, i-pentyl, neopentyl, n-hexyl, i-hexyl, n-octyl, i-octyl, 2-ethylhexyl, nonyl, i-nonyl, decyl, n Dodecyl, i-dodecyl, lauryl, myristyl, i-tridecyl, trimethyl-nonyl, palmityl, stearyl or eicosyl.
- alkanol alkoxylate of the formula (V-c) is 2-ethylhexyl alkoxylate of the formula
- EO stands for -CH 2 -CH 2 -O-
- the numbers 8 and 6 represent average values called.
- EO is CH 2 -CH 2 -O-
- BO stands for - CH-CH- TCH-O
- the numbers 10, 6 and 2 represent average values called.
- Particularly preferred alkanol alkoxylates of the formula (V-f) are compounds of this formula in which
- alkanol alkoxylate of the formula (V-f-1) very particular preference is given to alkanol alkoxylate of the formula (V-f-1)
- u stands for the average 8.4.
- alkanol alkoxylates are generally defined by the above formulas. These substances are mixtures of substances of the specified type with different chain lengths. For the indices, therefore, average values are calculated, which can also differ from whole numbers.
- alkanol alkoxylates of the formulas given are known and are partly available commercially or can be prepared by known methods (compare WO 98/35 553, WO 00/35 278 and EP-A 0 681 865).
- Suitable penetration promoters are substances which promote the solubility of the compounds of the formula (I) in the spray coating. These include, for example, mineral or vegetable oils. Suitable oils are all mineral or vegetable, optionally modified, oils which can usually be used in agrochemical compositions. Examples include sunflower oil, rapeseed oil, olive oil, castor oil, rapeseed oil, corn kernel oil, cottonseed oil and soybean oil or the esters of said oils. Rape oil, sunflower oil and their methyl or ethyl esters are preferred.
- the concentration of penetration promoter can be varied within a wide range. In the case of a formulated crop protection agent, it is generally from 1 to 95% by weight, preferably from 1 to 55% by weight, more preferably from 15 to 40% by weight. In the ready-to-use agents (spray liquors), the concentration is generally between 0.1 and 10 g / l, preferably between 0.5 and 5 g / l.
- the compounds of formula (I) may optionally also in certain concentrations or application rates as herbicides, safeners, growth regulators or agents for improving plant properties, or as microbicides, for example as fungicides, antimycotics, bactericides, viricides (including anti-viral agents) or as Agents against MLO (Mycoplasma-like-organism) and RLO (Rickettsia-like-organism) are used. If appropriate, they can also be used as intermediates or precursors for the synthesis of further active ingredients.
- the active compounds can be converted into the customary formulations, such as solutions, emulsions, wettable powders, water- and oil-based suspensions, powders, dusts, pastes, soluble powders, soluble granules, scattering granules, suspension-emulsion concentrates, active substance-impregnated natural substances, active substance-impregnated synthetic Substances, fertilizers and superfine encapsulations in polymeric substances.
- formulations are prepared in a known manner, e.g. by mixing the active compounds with extenders, ie liquid solvents and / or solid carriers, if appropriate using surface-active agents, ie emulsifiers and / or dispersants and / or foam-forming agents.
- extenders ie liquid solvents and / or solid carriers
- surface-active agents ie emulsifiers and / or dispersants and / or foam-forming agents.
- Excipients which can be used are those which are suitable for imparting special properties to the composition itself and / or preparations derived therefrom (for example spray liquor, seed dressing), such as certain technical properties and / or specific biological properties.
- Typical auxiliaries are: extenders, solvents and carriers.
- polar and non-polar organic chemical liquids e.g. from the classes of aromatic and non-aromatic hydrocarbons (such as paraffins, alkylbenzenes, alkylnaphthalenes, chlorobenzenes), alcohols and polyols (which may also be substituted, etherified and / or esterified), ketones (such as acetone, cyclohexanone), Esters (including fats and oils) and (poly) ethers, simple and substituted amines, amides, lactams (such as N-alkylpyrrolidones) and lactones, sulfones and sulfoxides (such as dimethyl sulfoxide).
- aromatic and non-aromatic hydrocarbons such as paraffins, alkylbenzenes, alkylnaphthalenes, chlorobenzenes
- alcohols and polyols which may also be substituted, etherified and / or esterified
- ketones such
- Suitable liquid solvents are essentially: aromatics, such as xylene, toluene, or alkylnaphthalenes, chlorinated aromatics and chlorinated aliphatic hydrocarbons, such as chlorobenzenes, chloroethylenes or methylene chloride, aliphatic hydrocarbons, such as cyclohexane or paraffins, e.g.
- Petroleum fractions mineral and vegetable oils, alcohols such as butanol or glycol and their ethers and esters, ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone or cyclohexanone, strongly polar solvents such as dimethyl sulfoxide, and water.
- Suitable solid carriers are:
- natural minerals such as kaolins, clays, talc, chalk, quartz, attapulgite, montmorillonite or diatomaceous earth and synthetic minerals such as finely divided Silica, alumina and silicates, as solid carriers for granules are: for example, broken and fractionated natural rocks such as calcite, marble, pumice, sepiolite, dolomite and synthetic granules of inorganic and organic flours and granules of organic material such as paper, sawdust, coconut shells , Corn on the cob and tobacco stalks;
- suitable emulsifiers and / or foam formers are: for example nonionic and anionic emulsifiers, such as polyoxyethylene fatty acid esters, polyoxyethylene fatty alcohol ethers, for example alkylaryl polyglycol ethers, alkylsulfonates, alkyl sulfates, arylsulfonates and protein hydrolysates;
- suitable dispersants are non
- oligo- or polymers for example starting from vinylic monomers, from acrylic acid, from EO and / or PO alone or in combination with, for example, (poly) alcohols or (poly) amines.
- lignin and its sulfonic acid derivatives simple and modified celluloses, aromatic and / or aliphatic sulfonic acids and their adducts with formaldehyde.
- Adhesives such as carboxymethylcellulose, natural and synthetic powdery, granular or latex-type polymers such as gum arabic, polyvinyl alcohol, polyvinyl acetate, and natural phospholipids such as cephalins and lecithins and synthetic phospholipids may be used in the formulations.
- Dyes such as inorganic pigments, e.g. Iron oxide, titanium oxide, ferrocyan blue and organic dyes such as alizarin, azo and metal phthalocyanine dyes and trace nutrients such as salts of iron, manganese, boron, copper, cobalt, molybdenum and zinc.
- inorganic pigments e.g. Iron oxide, titanium oxide, ferrocyan blue and organic dyes such as alizarin, azo and metal phthalocyanine dyes and trace nutrients such as salts of iron, manganese, boron, copper, cobalt, molybdenum and zinc.
- additives may be fragrances, mineral or vegetable optionally modified oils, waxes and nutrients (also trace nutrients), such as salts of iron, manganese, boron, copper, cobalt, molybdenum and zinc.
- Stabilizers such as cold stabilizers, preservatives, antioxidants, light stabilizers or other chemical and / or physical stability-improving agents may also be present.
- the formulations generally contain between 0.01 and 98% by weight of active ingredient, preferably between 0.5 and 90%.
- the active ingredient may be used in its commercial formulations as well as in the formulations prepared from these formulations in admixture with other active ingredients such as insecticides, attractants, sterilants, bactericides, acaricides, nematicides, fungicides, growth regulators, herbicides, safeners, fertilizers, semiochemicals or with agents for Improvement of plant properties are present.
- the active compounds according to the invention can furthermore be present in the form of insecticides in their commercial formulations and in the formulations prepared from these formulations in admixture with synergists.
- Synergists are compounds which increase the effect of the active ingredients without the added synergist itself having to be active.
- the active compounds according to the invention may furthermore, when used as insecticides in their commercial formulations and in the forms of use prepared from these formulations, be present in mixtures with inhibitors which reduce degradation of the active ingredient after application in the environment of the plant, on the surface of plant parts or in plant tissues ,
- the active substance content of the application forms prepared from the commercial formulations can vary within wide ranges.
- the active ingredient concentration of the use forms may be from 0.00000001 up to 95% by weight of active compound, preferably between 0.00001 and 1% by weight.
- the application is done in a custom forms adapted to the application.
- plants and parts of plants can be treated.
- plants are understood as meaning all plants and plant populations, such as desirable and undesired wild plants or crop plants (including naturally occurring plants)
- Crop plants can be plants produced by conventional breeding and
- Plant varieties. Plant parts are to be understood as meaning all aboveground and subterranean parts and organs of the plants, such as shoot, leaf, flower and root.
- Rhizomes are listed.
- the plant parts also include crops and vegetative and generative propagation material, such as cuttings, tubers, rhizomes, offshoots and
- the erf ⁇ ndungshiele treatment of the plants and parts of plants with the active ingredients is carried out directly or by affecting the environment, habitat or storage space after the usual treatment methods, for example by dipping, spraying, vaporizing, atomizing, scattering, brushing, injecting, casting and in propagating material, in particular in seeds, further by single or multi-layer wrapping.
- plants and their parts can be treated.
- wild or obtained by conventional biological breeding methods such as crossing or protoplast fusion
- Plant varieties are understood as meaning plants having new traits which have been bred by conventional breeding, by mutagenesis or by recombinant DNA techniques. These can be varieties, biotypes and genotypes.
- the treatment according to the invention may also give rise to superadditive ("synergistic") effects.
- superadditive for example, reduced application rates and / or extensions of the spectrum of action and / or an increase in the effect of the substances and agents usable in the invention, better plant growth, increased tolerance to high or low temperatures, increased tolerance to drought or to water or soil salt content, increased flowering power facilitated harvest, acceleration of ripeness, higher crop yields, higher quality and / or higher nutritional value of the harvested products, higher shelf life and / or machinability of the harvested products, which exceed the actual expected effects.
- the preferred plants or plant varieties to be treated according to the invention to be treated include all plants which, as a result of the genetic engineering modification, obtained genetic material which gives these plants particularly advantageous valuable properties ("traits").
- traits are better plant growth, increased tolerance to high or low temperatures, increased tolerance to dryness or to bottoms salt, increased flowering, easier harvesting, acceleration of ripeness, higher crop yields, higher quality and / or higher nutritional value of the harvested products , higher shelf life and / or machinability of Harvested products.
- Further and particularly emphasized examples of such properties are an increased defense of the plants against animal and microbial pests, as against insects, mites, phytopathogenic fungi, bacteria and / or viruses as well as an increased tolerance of the plants against certain herbicidal active substances.
- transgenic plants are the important crops such as cereals (wheat, rice), corn, soybeans, potatoes, sugar beets, tomatoes, peas and other vegetables, cotton, tobacco, oilseed rape and fruit plants (with the fruits apples, pears, citrus fruits and Grapes), with special emphasis on maize, soya, potato, cotton, tobacco and oilseed rape.
- Bt plants are the increased defense of the plants against insects, arachnids, nematodes and snails by toxins produced in the plants, in particular those which are produced by the genetic material from Bacillus thuringiensis (eg by the genes Cry ⁇ A (a) , CryIA (b), Cry ⁇ A (c), CryllA, CrylllA, CryIHB2, Cry9c Cry2Ab, Cry3Bb and CrylF, and combinations thereof) in the plants (hereinafter "Bt plants”).
- Bacillus thuringiensis eg by the genes Cry ⁇ A (a) , CryIA (b), Cry ⁇ A (c), CryllA, CrylllA, CryIHB2, Cry9c Cry2Ab, Cry3Bb and CrylF, and combinations thereof
- Traits also highlight the increased resistance of plants to fungi, bacteria and viruses by systemic acquired resistance (SAR), systemin, phytoalexins, elicitors and resistance genes and correspondingly expressed proteins and toxins. Traits which are furthermore particularly emphasized are the increased tolerance of the plants to certain herbicidally active compounds, for example imidazolinones, sulfonylureas, glyphosate or phosphinotricin (eg "PAT" gene). The genes which confer the desired properties (“traits”) can also occur in combinations with one another in the transgenic plants.
- SAR systemic acquired resistance
- PAT phosphinotricin
- Bt plants are maize varieties, cotton varieties, soybean varieties and potato varieties which are sold under the trade names YIELD GARD® (eg corn, cotton, soya), KnockOut® (eg maize), StarLink® (eg maize), Bollgard® ( Cotton), Nucotn® (cotton) and NewLeaf® (potato).
- YIELD GARD® eg corn, cotton, soya
- KnockOut® eg maize
- StarLink® eg maize
- Bollgard® Cotton
- Nucotn® cotton
- NewLeaf® potato
- herbicide-tolerant plants are maize varieties, cotton varieties and soybean varieties, which are sold under the trade names Roundup Ready® (tolerance to glyphosate eg corn, cotton, soy), Liberty Link® (tolerance to phosphinotricin, eg rapeseed), IMI® (tolerance against imidazolinone) and STS® (tolerance to sulfonylureas eg corn).
- Roundup Ready® tolerance to glyphosate eg corn, cotton, soy
- Liberty Link® tolerance to phosphinotricin, eg rapeseed
- IMI® tolerance against imidazolinone
- STS® tolerance to sulfonylureas eg corn
- Clearfield® varieties eg corn
- the active compounds of the invention not only against plant, hygiene and storage pests, but also in the veterinary sector against animal parasites (ecto- and endoparasites) such as ticks, leather ticks, mange mites, running mites, flies (stinging and licking), parasitic fly larvae, lice , Hair pieces, featherlings and fleas.
- animal parasites ecto- and endoparasites
- ticks ecto- and endoparasites
- leather ticks such as ticks, leather ticks, mange mites, running mites, flies (stinging and licking), parasitic fly larvae, lice , Hair pieces, featherlings and fleas.
- flies stinging and licking
- parasitic fly larvae such as ticks, leather ticks, mange mites, running mites, flies (stinging and licking), parasitic fly larvae, lice , Hair pieces, featherlings and fleas.
- Anoplurida e.g. Haematopinus spp., Linognathus spp., Pediculus spp., Phtirus spp., Solenopotes spp.
- Trimenopon spp. Menopon spp., Trinoton spp., Bovicola spp., Werneckiella spp., Lepikentron spp., Damalina spp., Trichodectes spp., Felicola spp.
- Nematocerina and Brachycerina e.g. Aedes spp., Anopheles spp., Culex spp., Simulium spp., Eusimulium spp., Phlebotomus spp., Lutzomyia spp., Culicoides spp., Chrysops spp., Hybomitra spp., Atylotus spp., Tabanus spp., Haematopota spp , Philipomyia spp., Braula spp., Musca spp., Hydrotaea spp., Stomoxys spp., Haematobia spp., Morellia spp., Fannia spp., Glossina spp., Calliphora spp., Glossina spp., Chrysomyia spppp
- siphonaptrida e.g. Pulex spp., Ctenocephalides spp., Xenopsylla spp., Ceratophyllus spp.
- heteropterid e.g. Cimex spp., Triatoma spp., Rhodnius spp., Panstrongylus spp.
- Actinedida Prostigmata
- Acaridida Acaridida
- eg Acarapis spp. Cheyletiella spp., Ornitrocheyletia spp., Myobia spp., Psorergates spp., Demodex spp., Trombicula Spp., Listrophorus spp., Acarus spp., Tyrophagus spp., Caloglyphus spp., Hypodectes spp., Pterolichus spp., Psoroptes spp., Chorioptes spp., Otodectes spp., Sarcoptes spp., Notoedres spp., Knemidocoptes spp. , Cytodites spp., Laminosioptes spp.
- the active compounds of the formula (I) according to the invention are also suitable for controlling arthropods which are farm animals, such as e.g. Cattle, Sheep, Goats, Horses, Pigs,
- Donkeys camels, buffaloes, rabbits, chickens, turkeys, ducks, geese, bees, other pets such as e.g. Dogs, cats, caged birds, aquarium fish and so-called experimental animals, such.
- the use of the active compounds according to the invention takes place in the veterinary sector and in animal husbandry in a known manner by enteral administration in the form of, for example, tablets, capsules, infusions, drenches, granules, pastes, boilies, the feed-through process, suppositories, by parenteral administration, as by injections (intramuscular, subcutaneous, intravenous, intraperitoneal, etc.), implants, by nasal application, by dermal application in the form of, for example, diving or bathing (dipping), spraying, pouring (pour-on and spot-on ), washing, powdering and with the aid of active substance-containing moldings, such as collars, ear tags, tail marks, limb bands, holsters, marking devices, etc.
- enteral administration in the form of, for example, tablets, capsules, infusions, drenches, granules, pastes, boilies, the feed-through process, suppositories
- parenteral administration as by injections (intr
- the active compounds of the formula (I) can be used as formulations (for example powders, emulsions, flowable agents) which contain the active ingredients in an amount of from 1 to 80% by weight, directly or apply after 100 to 10,000 times dilution or use as a chemical bath.
- formulations for example powders, emulsions, flowable agents
- the compounds according to the invention show a high insecticidal activity against insects which destroy industrial materials.
- insects By way of example and preferably without limiting however, the following insects are mentioned:
- Termites such as Kalotermes flavicollis, Cryptotermes brevis, Heterotermes indicola, Reticulitermes flavipes, Reticulitermes santonensis, Reticulitermes lucifigus, Mastotermes darwiniensis, Zootermopsis nevadensis, Coptotermes formosanus;
- Non-living materials such as preferably plastics, adhesives, glues, papers and cardboard, leather, wood, wood processing products and paints.
- the ready-to-use agents may optionally contain further insecticides and, if appropriate, one or more fungicides.
- the compounds according to the invention can be used to protect against fouling of objects, in particular hulls, sieves, nets, structures, quay systems and signal systems, which come into contact with seawater or brackish water.
- the compounds according to the invention can be used alone or in combinations with other active substances as antifouling agents.
- the active compounds are also suitable for controlling animal pests in household, hygiene and storage protection, in particular of insects, arachnids and mites, which are used in closed rooms, such as apartments, factory buildings, offices, vehicle cabins u.a. occurrence. They can be used to control these pests, alone or in combination with other active ingredients and adjuvants in household insecticide products. They are effective against sensitive and resistant species and against all stages of development. These pests include:
- Acarina e.g. Argas persicus, Argas reflexus, Bryobia ssp., Dermanyssus gallinae, Glyciphagus domesticus, Ornithodorus moubat, Rhipicephalus sanguineus, Trombicula alfreddugesi, Neutrombicula autumnalis, Dermatophagoides pteronissimus, Dermatophagoides forinae.
- Opiliones eg Pseudoscorpiones chelifer, Pseudoscorpiones cheiridium, Opiliones phalangium. From the order of the Isopoda eg Oniscus asellus, Porcellio scaber.
- Zygentoma e.g. Ctenolepisma spp., Lepisma saccharina, Lepismodes inquilinus.
- Diptera e.g. Aedes aegypti, Aedes albopictus, Aedes taeniorhynchus, Anopheles spp., Calliphora erythrocephala, Chrysozona pluvialis, Culex quinquefasciatus, Culex pipiens, Culex tarsalis, Drosophila spp., Fannia canicularis, Musca domestica, Phlebotomus spp., Sarcophaga carnaria, Simulium spp., Stomoxys Calcitrans, Tipula paludosa.
- Lepidoptera e.g. Achroia grisella, Galleria mellonella, Plodia interpunctella, Tinea cloacella, Tinea pellionella, Tineola bisselliella.
- Ctenocephalides canis Ctenocephalides felis, Pulex irritans, Tunga penetrans, Xenopsylla cheopis.
- Hymenoptera e.g. Camponotus herculeanus, Lasius fuliginosus, Lasius niger, Lasius umbratus, Monomorium pharaonis, Paravespula spp., Tetramorium caespitum.
- Anoplura eg Pediculus humanus capitis, Pediculus humanus co ⁇ oris, Pemphigus spp., Phylloera vastatrix, Phthirus pubis.
- Heteroptera eg Cimex hemipterus, Cimex lectularius, Rhodinus prolixus, Triatoma infestans.
- Application is in aerosols, non-pressurized sprays, e.g. Pump and atomizer sprays, fog machines, foggers, foams, gels, evaporator products with cellulose or plastic evaporator plates, liquid evaporators, gel and membrane evaporators, propeller driven evaporators, energyless or passive evaporation systems, moth papers, moth cakes and moth gels, as granules or dusts, in litter or bait stations.
- Pump and atomizer sprays e.g. Pump and atomizer sprays, fog machines, foggers, foams, gels, evaporator products with cellulose or plastic evaporator plates, liquid evaporators, gel and membrane evaporators, propeller driven evaporators, energyless or passive evaporation systems, moth papers, moth cakes and moth gels, as granules or dusts, in litter or bait stations.
- 3-Amino-l, 2-Benzisothiazole of formula (II) are known, or can be prepared by general synthesis methods.
- EP 0 138762 describes the synthesis of 3-amino-4-chloro-1,2-benzisothiazole [CAS-RN 25380-80-7].
- the EP 33984 describes the synthesis of 4-chloro-3-amino, 4-fluoro-3-amino and 4-methyl-3-amino-l, 2-benzisothiazol-l, l-dioxide from the corresponding 2-cyano -benzolsulfonklachloriden.
- the preparation of aromatic 2-cyano-benzenesulfonic acid halides is described in DE 860051.
- 3-amino-l, 2-benzisothiazol-l, l-dioxide of the general formula (H) are described as intermediates.
- the 3-amino-l, 2-benzisothiazole of formula (II) are also partially commercially available, for example, 3-amino-l, 2-benzisothiazol [CAS-RN 23031-78-9] or the 3-amino-5-nitro benzisothiazole [CAS RN 84387-89-3].
- EP 105732 describes N-substituted 3-amino-1,2-benzisotbiazole 1,1-dioxides as pharmaceuticals.
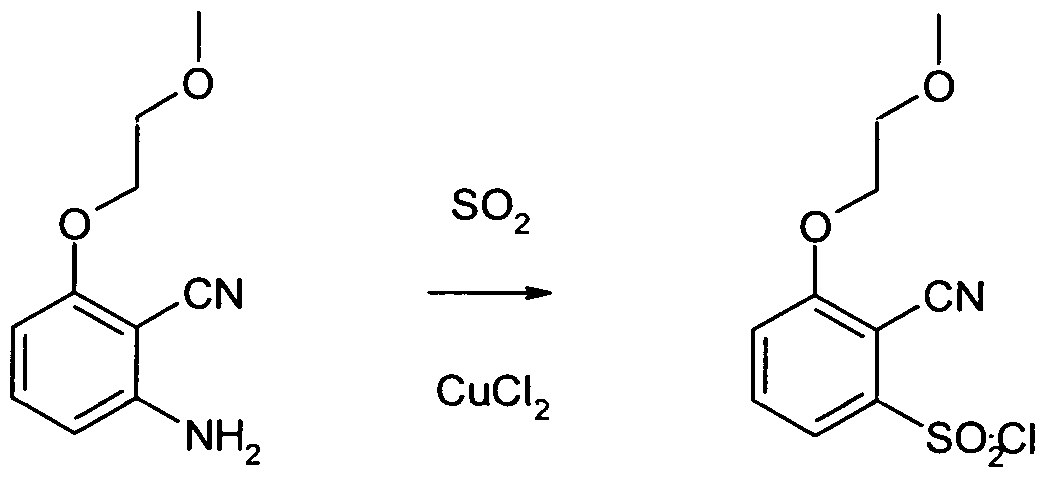
- Step IA Preparation of 2-amino-6- (2-methoxyethoxy) benzonitrile
- Step IC Preparation of 4- (2-methoxyethoxy) -L2-berizisothiazol-3-amine-1-dioxide
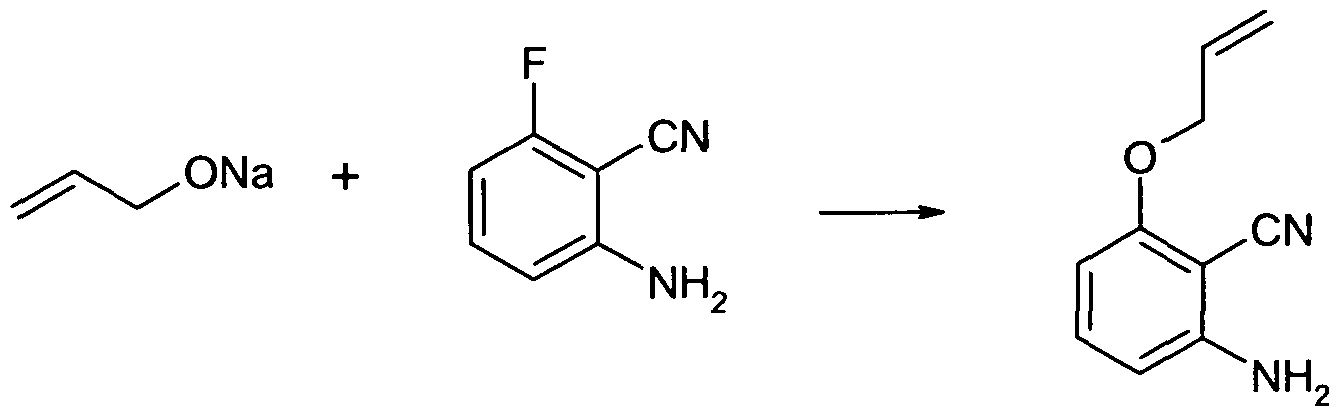
- Step 2A Preparation of 2-amino-6- (prop-2-en-1-yloxy) benzonitrile
- Step 2B Preparation of 2-amino-6- (prop-2-en-1-yloxy) benzenesulfonyl chloride
- Step 2C Preparation of 4-fProp-2-en-1-yloxy) -1,2-benzisothiazol-3-amine-II-dioxide
- Methylchlorothiocarbonat added dropwise in 3 ml of absolute tetrahydrofuran. It is heated under reflux for 16 hours, cooled, treated with 0.5 ml of water and concentrated in vacuo. One takes in
- ⁇ -NMR data is carried out with a Bruker Avance 400, with tetramethylsilane as reference (0.0 ppm) and the solvents CD 3 CN or [D 6 ] -DMSO.
- Emulsifier 0.5 part by weight of alkylaryl polyglycol ether
- active compound 1 part by weight of active compound is mixed with the indicated amounts of solvent and emulsifier, and the concentrate is diluted with emulsifier-containing water to the desired concentration.
- Chinese cabbage leaf discs (Brassica pekinensis) infested with all stages of the green peach aphid (Myzus persicae) are sprayed with an active compound preparation of the desired concentration.
- the effect is determined in%. 100% means that all aphids have been killed; 0% means that no aphids have been killed.
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Dentistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Plant Pathology (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Pest Control & Pesticides (AREA)
- Agronomy & Crop Science (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
Abstract
Die vorliegende Erfindung beinhaltet ein Verfahren zur Bekämpfung von tierischen Schädlingen, wobei (1,2-Benzisothiazol-3-yl)(thio)carbamate und (1,2-Benzisothiazol-3-yl)(thio)oxamate und deren Oxidationsformen der Formel (I) in welcher A, R1, R2, R3, R4, n, X, Y und Z die in der Beschreibung angegebenen Bedeutungen haben- als Pestizide Anwendung finden. Die Erfindung beinhaltet weiterhin spezifische Komponenten der Formel (I), sowie mehrere Verfahren zu ihrer Herstellung.
Description
(l,2-Benzisothiazol-3-vD(thio)carbamate und (l,2-Benzisothiazol-3-vD(thio)oxamate und deren Oxidationsformen als Pestizide
Die vorliegende Erfindung betrifft ein Verfahren zur Bekämpfung tierischer Schädlinge durch Anwendung insektizider und/oder akarizider Wirkstoffe insbesondere in Kombination mit Mitteln zur Wirkungssteigerung, sowie neue Schädlingsbekämpfungsmittel und mehrere Verfahren zu ihrer Herstellung.
In der Literatur sind bereits folgende Verbindungen beschrieben:
Substituierte 2-Cyano-benzolsulfonamide und die isomeren 3-Amino-l,2-benzisothiazol-l,l- dioxide sind beschrieben in der EP 33984. Dabei wird auch eine blattlausabtötende Wirksamkeit beschrieben. 3-Amino-l,2-benzisothiazole und deren Verwendung als Insektizide sind beschrieben in der EP 138762. In der EP 133418 sind 3-Acylamino-l,2-benzisothiazole als Pestizide, in der EP 110829 sind 3-Acylamino-l,2-benzisothiazol-l,l-dioxide als Insektizide und Akarizide in der EP 191734, EP 207891, und in der JP 1989/01319467 sind 3-Acylamino-l,2-benzisothiazol-l,l- dioxide als Pestizide; und in der DE 3544436 sind 3-(Diacylamino)-l,2-benzisothiazol-l,l-dioxide als Fungizide und Insektizide beschrieben. Weitere Derivate der 3-Amino-l,2-benzisothiazol-l,l- dioxide und deren isomerer Formen sind in der EP 86748, JP 1990/006496, WO 2007/057407 und WO 2007/113119 als Insektizide beansprucht. In der WO 2003/087072 wird die Herstellung von 1,2-Benzisothiazolen, in der DE 3112164 wird die Herstellung von 1 ,2-Benzisothiazolyl-oxamaten und deren Verwendung als Arzneimittel beschrieben. Über eine Verwendung als Schädlingsbekämpfungsmittel wird nichts berichtet. Eine antimikrobielle Wirkung der Verbindung Ethyl-(7-nitro-l,2-benzisothiazol-3-yl)carbamat wird erwähnt bei P. Vicini, Farmaca 44, 511-517 (1989).
In der Literatur wurde bereits ebenfalls beschrieben, dass sich die Wirkung verschiedener Wirkstoffe durch Zugabe von Ammoniumsalzcn steigern lässt. Dabei handelt es sich jedoch um als Detergens wirkende Salze (z.B. WO 95/017817) bzw. Salze mit längeren Alkyl- und / oder Arylsubstituenten, die permeabilisierend wirken oder die Löslichkeit des Wirkstoffs erhöhen (z.B. EP-A 0 453 086, EP-A 0 664 081, FR-A 2 600 494, US 4 844 734, US 5 462 912, US 5 538 937, US-A 03/0224939, US-A 05/0009880, US-A 05/0096386). Weiterhin beschreibt der Stand der Technik die Wirkung nur für bestimmte Wirkstoffe und / oder bestimmte Anwendungen der entsprechenden Mittel. In wieder anderen Fällen handelt es sich um Salze von Sulfonsäuren, bei denen die Säuren selber paralysierend auf Insekten wirken (US 2 842 476). Eine Wirkungssteigerung z.B. durch Ammoniumsulfat ist beispielsweise für die Herbizide Glyphosat und Phosphinothricin beschrieben (US 6 645 914, EP-A2 0 036 106). Der Einsatz von Ammoniumsulfat als Formulierhilfs-mittel ist für bestimmte Wirkstoffe und Anwendungen
ebenfalls beschrieben (WO 92/16108), es dient dort aber zur Stabilisierung der Formulierung, nicht zur Wirkungssteigerung.Desweiteren werden Kombinationen von Ammoniumsalzen mit insektiziden Wirkstoffen beschrieben in WO 07/068356, WO 07/068428, WO 07/068355, WO 07/068357, und WO 07/068350. Auf diese Veröffentlichungen wird hiermit ausdrücklich Bezug genommen.
Die gemäß den oben genannten Schriften bereits bekannten Wirkstoffe weisen bei ihrer Anwendung Nachteile auf, sei es,
(a) dass sie keine oder aber eine nur unzureichende insektizide und/oder akarizide Wirkung gegen tierische Schädlinge besitzen oder
(b) dass nur ein zu geringes Spektrum an Schadtieren bekämpft werden kann.
Aufgabe der vorliegenden Erfindung ist es daher, entsprechende Benzoisothiazol-Derivate bereitzustellen, welche als Insektizide und/oder Akarizide, insbesondere mit einer zufrieden stellenden insektiziden und/oder akariziden Wirkung gegen tierische Schädlinge, mit einem breiten Spektrum gegenüber tierischen Schädlingen, mit einer hohen Selektivität und guten Verträglichkeit in Nutzpflanzenkulturen, sowie welche in Kombination mit weiteren Mitteln zur Verbesserung der Wirksamkeit insbesondere gegen schwierig zu bekämpfende Insekten und Spinnmilben, eingesetzt werden können.
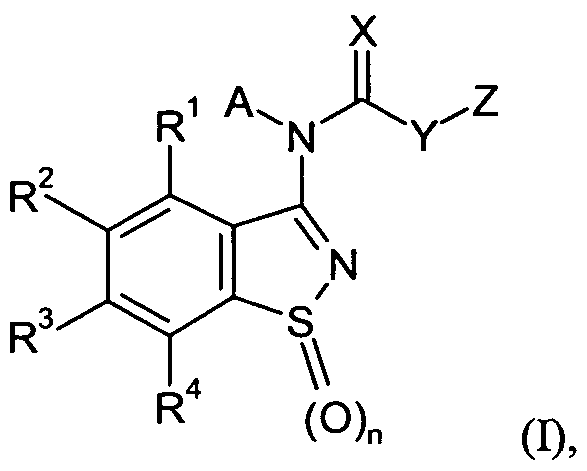
Es wurden nun Benzothiazol-Derivate der allgemeinen Formel (I) gefunden,
R1, R2, R3 und R4 unabhängig voneinander für
Wasserstoff, Halogen, Carbamoyl, Thiocarbamoyl, Nitro, Cyano, Hydroxy, SF5 ; Ci-C6-Alkyl, C2- C6-Alkenyl, C2-C6- Alkinyl, C3-C6-Cycloalkyl, C3-C6-Cycloalkyl-CrC4-Alkyl, CI-C4-Halogenalkyl, C,-C4-Halogenalkylthio, CrC4-Alkylthio, Ci-C4-Alkylsulfinyl, Ci-C4-Halogenalkylsulfinyl, Ci-C4- Alkylsulfonyl, C,-C4-Halogenalkylsulfonyl, Ci-Q-Alkylcarbonyl, CrC6-Alkoxy, C1-C6- Alkoxycarbonyl, C3-C6-Alkenyloxy, C3-C6-Cycloalkyloxy, C3-C6-Cycloalkyloxy-Ci-C4-Alkyl, C1-
C4-Halogenalkoxy, Ci-C4-Alkoxy-Ci-C4-Alkyl, Aryloxy, Hetaryloxy, Aryl-Ci-C4-Alkyloxy, Hetaryl-Ci-C4-Alkyloxy, (CrC4-Alkoxy)carbonyl, O-Acetyl, (Ci-C4-Alkyl)amino, Di-(Ci-C4- alkyl)amino, C3-C6-Trialkylsilyl, Aryl, Hetaryl, Aryl-Ci-C6-Alkyl oder Hetaryl-Ci-C6-Alkyl stehen,
wobei diese Reste unsubstituiert sein können oder einen, zwei oder mehrere Reste aus der Gruppe
Halogen, Cyano, CrC6-Alkyl, C3-C8-Cycloalkyl, C1-C4-AIkOXy, CrC4-Alkylthio, C,-C4- Alkylsulfinyl, Ci-C4-Alkylsulfonyl, CrC4-Halogenalkyl, Ci-C4-Halogenalkoxy, C]-C4- Halogenalkylthio, (Ci-C4-Alkyl)amino, Di-(C 1-C4-alkyl)amino, Aryl und Hetaryl tragen können;
A für Wasserstoff, (C1- C6-Alkyl)carbonyl, (C,- C6-Alkoxy)carbonyl, (Ci-C6-
Alkylthio)carbonyl, (Ci-Cβ-Alkytythiocarbonyl, (Ci-C6- Alkoxy)thiocarbonyl, (Ci-C6- Alkylthio)thiocarbonyl, CrC8-Alkyl, C3-C6-Cycloalkyl, C2-C6- Alkenyl, CrC4-Alkoxy,
CrC4-Alkylthio, Ci-C4-Alkylsulfinyl, CrC4-Alkylsulfonyl, CrC4-Halogenalkyl, Aryl,
Hetaryl, C,-C6-Arylalkyl oder C]-C6-Hetarylalkyl steht,
wobei diese Reste unsubstituiert sein können oder einen, zwei oder mehrere Reste aus der Gruppe
Halogen, Cyano, Ci-C6-Alkyl, C3-C8-Cycloalkyl, CrC4-Alkoxy, C,-C4-Alkylthio, Q-C4- Alkylsulfmyl, Ci-C4-Alkylsulfonyl, C,-C4-Halogenalkyl, C,-C4-Halogenalkoxy, C1-C4- Halogenalkylthio, (Ci-C4-Alkyl)amino, Di-(Ci -C4-alkyl)amino, Aryl und Hetaryl tragen können;
oder
A für den Rest c γ z steht,
n für 0, 1 oder 2 steht,
X für O oder S steht,
Y für O, S, oder C(=O) steht,
Z für Ci-C6-Alkyl, C2-C6-Alkenyl, C2-C6-Alkinyl, C3-C6-Cycloalkyl, Q-Q-Haloalkyl, C2-C6-
Haloalkenyl, C2-C6-Haloalkinyl, C3-C6-Halocycloalkyl, Aryl, Hetaryl, CrC6-Arylalkyl, Q- C6-Hetarylalkyl , und für den Fall, dass Y für C(=O) steht, auch für CrC8-Alkoxy, Q-C4- Haloalkoxy, Aryloxy oder Hetaryloxy steht,
wobei Aryl und Hetaryl gegebenenfalls einfach oder mehrfach, gleich oder verschieden mit Q-C6- Alkyl, C2-C6-Alkenyl, C2-C6- Alkinyl, C3-C6-Cycloalkyl, C,-C6-Haloalkyl, C2-C6-Haloalkenyl, C2-
C6-Haloalkinyl, C3-C6-Halocycloalkyl, Halogen, Cyano, Nitro, Ci-C4-Alkoxy, Ci-C4-Haloalkoxy substituiert sein können,
sowie Salze von Verbindungen der Formel (I), deren Anwendung zur Bekämpfung von tierischen Schädlingen und die Wirkungssteigerung der Verbindungen der Formel (I) durch den Zusatz von Ammonium- oder Phosphoniumsalzen zur Anwendungslösung oder durch den Einbau dieser Salze in eine Formulierung enthaltend Verbindungen der Formel (I).
Die Verbindungen der Formel (I) können gegebenenfalls in verschiedenen polymorphen Formen oder als Mischung verschiedener polymorpher Formen vorliegen. Sowohl die reinen Polymorphe als auch die Polymorphgemische sind Gegenstand der Erfindung und können erfindungsgemäß ver- wendet werden.
Die Verbindungen der Formel (I) umfassen gegebenenfalls Diastereomere oder Enantiomere.
Die (l,2-Benzisothiazol-3-yl)(thio)carbamate und (l,2-Benzisothiazol-3-yl)(thio)oxamate und deren Oxidationsformen sind durch die Formel (I) allgemein definiert. Bevorzugte Restedefinitionen der vorstehenden und nachfolgend genannten Formeln sind im Folgenden angegeben. Diese Definitionen gelten für die Endprodukte der Formel (I) wie für alle Zwischenprodukte gleichermaßen.
Als bevorzugt, besonders bevorzugt und ganz besonders bevorzugt gelten Verbindungen der Formel (I), sowei ein Vefahren zur Bekämpfung von Schädlingen unter Anwendung der Verbindungen der Formel (I), wobei
R1, R2, R3 und R4 unabhängig voneinander bevorzugt für
Wasserstoff, Halogen, Cyano, Nitro, CrC6-Alkyl, C2-C6-Alkenyl, C2-C6-Alkinyl, C3-C6- Cycloaikyi, C3-C6-Cycloalkyl-Ci-C4-Alkyl, CrC4-Halogenalkyl, CrC4-Alkylthio, C]-C4- Alkylsulfonyl, Ci-C4-Alkylcarbonyl, Ci-C6-Alkoxy, CrC6-Alkoxycarbonyl, C3-C6-Alkenyloxy, C3- C6-Cycloalkyloxy, C3-C6-Cycloalkyloxy-CrC4-Alkyl, CrC4-Halogenalkoxy, Ci-C4-Alkoxy-C,-C4- Alkyl, Aryloxy, Hetaryloxy, Aryl-CrC4-Alkyloxy, Hetaryl-CrC4-Alkyloxy, (C1-C4- Alkoxy)carbonyl, O-Acetyl, Aryl, Hetaryl, Aryl-Ci -C6- Alkyl oder Hetaryl-Ci -C6- Alkyl stehen,
wobei diese Reste unsubstituiert sein können oder einen, zwei oder mehrere Reste aus der Gruppe
Halogen, Cyano, Ci-C6-Alkyl, Q-Cg-Cycloalkyl, Ci-C4-Alkoxy tragen können,
R1, R2, R3 und R4 unabhängig voneinander besonders bevorzugt für
Wasserstoff, Halogen, Nitro, CrC3-Alkyl, C,-C3-Halogenalkyl, C,-C3-Alkylthio, C1-C3- Alkylsulfonyl, C3-C6-Alkenyloxy, Ci-C3-Alkoxy, C,-C2-Halogenalkoxy, CrC4-Alkoxy-Ci-C4-Alkyl, Aryloxy, Hetaryloxy, Ci-C2-Arylalkyloxy, C1-C2-Hetarylalkyloxy, CrC4-Alkoxycarbonyl, O-Acetyl stehen,
wobei diese Reste unsubstituiert sein können oder einen, zwei oder mehrere Reste aus der Gruppe
Halogen, Ci-C4-Alkoxy tragen können,
R1, R2, R3 und R4 unabhängig voneinander ganz besonders bevorzugt für
Wasserstoff, Nitro, Methoxy, Ethoxy, Ethoxymethyl, Benzyloxy, Fluor, Chlor, Methyl, Ethyl, Trifluormethyl, OCHF2, OCF3, OCClF2, OCH2CH2-OCH3, SCH3, SO2CH3, -OCH2-CH=CH2, -OCH2-Phenyl stehen,
A bevorzugt für Wasserstoff, , (Ci-C6-Alkyl)carbonyl, (Ci-C6-Alkoxy)carbonyl, (Ci-C6- Alkylthio)carbonyl,
(Ci-C6-Alkoxy)thiocarbonyl, (CrC6- Alkylthio)thiocarbonyl, CrC6-Alkyl, C3-C6-Cycloalkyl, C2-C6-Alkenyl, C,-C4-Alkoxy, C1- C4-Halogenalkyl, Aryl, Hetaryl, CrC2-Arylalkyl oder CrQ-Hetarylalkyl steht,
oder
ö γ 7
A bevorzugt für den Rest steht,
A besonders bevorzugt für Wasserstoff, (Ci-C3-Alkyl)carbonyl, (CrC3-Alkoxy)carbonyl, Q- C2-Alkyl, C1-C4-AIkOXy, C,-C4-Halogenalkyl, CrC4-Halogenalkoxy, CrC2-Arylalkyl oder CrC2-Hetarylalkyl steht,
oder
Q Y 7
A besonders bevorzugt für den Rest steht,
A ganz besonders bevorzugt für Wasserstoff, Acetyl, C1-C2-AIlCyI, Ci-C4-Alkoxy steht,
oder
Q Y 7 ganz besonders bevorzugt für den Rest steht,
n bevorzugt steht für 0, 1 oder 2,
n besonders bevorzugt steht für 0 oder 2,
n weiterhin besonders bevorzugt steht für 2,
X bevorzugt und besonders bevorzugt steht für O oder S,
X ganz besonders bevorzugt steht für O,
Y bevorzugt steht für O, S, oder C(=O),
Y besonders bevorzugt für O oder S steht,
Y ganz besonders bevorzugt für O steht,
Z bevorzugt für d-C6-Alkyl, C2-C6-Alkenyl, C2-C6-Alkinyl, C3-C6-Cycloalkyl, Q-C6- Haloalkyl, C2-C6-Haloalkenyl, C2-C6-Haloalkinyl, C3-C6-Halocycloalkyl, Aryl, Hetaryl,
Ci-C6-Arylalkyl, CrC6-Hetarylalkyl, und für den Fall, dass Y für C(=O) steht, auch für Cr Cg-Alkoxy, Ci-C4-Haloalkoxy, Aryloxy, Hetaryloxy steht,
Z besonders bevorzugt für Ci-C4-Alkyl, Ci-C4-Haloalkyl, C2-C6-Haloalkinyl, Aryl und für den
Fall, dass Y für C(=O) steht, auch für CrC4-Alkoxy steht,
Z ganz besonders bevorzugt für Methyl, Ethyl, Propyl, Isopropyl, tert. Butyl, Phenyl und für den Fall, dass Y für C(=O) steht, auch für Methoxy oder Ethoxy steht.
In einer weiteren Ausführungsform der Erfindung steht A nicht für Phenyl, falls n= 2 ist; bevorzugt stehen A, R1, R2, R3, R4 für Wasserstoff, falls n=2 ist. Ebenfalls in einer weiteren Ausführungsform ist R1 verschieden von Wasserstoff, falls n=0 ist.
Die oben angegebenen einzelnen allgemeinen, bevorzugten, besonders bevorzugten und ganz besonders bevorzugten Bedeutungen für die Substituenten R1 bis R4, n, X, Y, Z und A können beliebig miteinander kombiniert werden. Das heißt, dass Verbindungen der allgemeinen Formel (I) von der vorliegenden Erfindung umfasst sind, in welchen beispielswiese der Substituent R1 eine bevorzugte Bedeutung aufweist und die Substituenten X und Y die allgemeine Bedeutung aufweisen oder aber beispielsweise der Substituent R2 eine bevorzugte Bedeutung aufweist, der Substituent R3 eine besonders bevorzugte Bedeutung, der und die übrigen Substituenten die allgemeine Bedeutung aufweisen.
Gegenstand der vorliegenden Erfindung sind vorzugsweise auch die Lithium-, Natrium-, Kalium-, Magnesium-, Calcium-, Ammonium-, Ci-C4-Alkyl-ammonium, Di-(Ci-C4-alkyl)-ammonium-, Tn- (Ci-C4-alkyl)-ammonium-, Tetra-(Ci-C4-alkyl)-ammonium-, Tri-(Ci-C4-alkyl)-sulfonium, C5- oder C6- Cycloalkyl-ammonium-, Di-(C rC2-alkyl)-benzyl-ammonium und Tn-(Q -C2-alkyl)-benzyl- ammonium-Salze von Verbindungen der Formel (I), in welcher R1 bis R4, n, X, Y, Z und A die oben allgemeinen, bevorzugten, besonders bevorzugten und insbesondere bevorzugten Bedeutungen aufweisen und die nach allgemein üblichen Verfahren hergestellt werden können.
In der allgemeinen Formel (I) und allen übrigen Formern in der vorliegenden Erfindung können die Reste Alkyl, Alkoxy, Haloalkyl, Alkoxyalkyl, Alkenyl, Alkinyl, Haloalkoxy, Alkylamino, Dialkylamino, Alkylthio und Haloalkylthio, sowie die entsprechenden ungesättigten und/oder substituierten Reste im Kohlenstoffgerüst jeweils geradkettig oder verzweigt sein. Wenn nicht speziell angegeben, sind bei diesen Resten die niederen Kohlenstoffgerüste, z.B. mit 1 bis 6 C- Atomen, insbesondere 1 bis 4 C-Atomen, bzw. bei ungesättigten Gruppen mit 2 bis 6 C-Atomen, insbesondere 2 bis 4 C-Atomen, bevorzugt. Alkylreste, auch in den zusammengesetzten Bedeutungen wie Alkoxy, Haloalkyl usw., bedeuten z.B. Methyl, Ethyl, Propyle wie n- oder i- Propyl, Butyle wie n-, iso- oder tert.-Butyl, Pentyle wie n-Pentyl, iso-Pentyl oder neo-Pentyl, Hexyle wie n-Hexyl, i-Hexyl, 3-Methylpentyl, 2,2-Dimethylbutyl oder 2,3-Dimethylbutyl, Heptyle, wie n-Heptyl, 1-Methylhexy oder 1,4-Dimethylpentyl; Alkenyl- und Alkinylreste haben die Bedeutung der den Alkylresten entsprechenden möglichen ungesättigten Reste; wobei mindestens eine Doppelbindung bzw. Dreifachbindung, vorzugsweise eine Doppelbindung bzw. Dreifachbindung enthalten ist. Alkenyl bedeutet z.B. Vinyl, Allyl, l-Methylprop-2-en-l-yl, 2- Methyl-prop-2-en-l-yl, But-2-en-l-yl, But-3-en-l-yl, l-Methyl-but-3-en-l-yl und l-Methyl-but-2- en-l-yl; Alkinyl bedeutet z.B. Ethinyl, Propargyl, But-2-in-l-yl, But-3-in-l-yl und l-Methyl-but-3- in-l-yl.
Wenn Haloalkylgruppen und Haloalkylreste von Haioalkoxy, Halυalkylthio, Haloalkenyl, Haloalkinyl u.a. angegeben sind, sind bei diesen Resten die niederen Kohlenstoffgerüste, z. B. mit 1 bis 6 C-Atomen oder 2 bis 6, insbesondere 1 bis 4 C-Atomen oder bevorzugt 2 bis 4 C-Atomen, sowie die entsprechenden ungesättigten und/oder substituierten Reste im Kohlenstoffgerüst jeweils geradkettig oder verzweigt. Beispiele sind Difluormethyl, 2,2,2-Trifluorethyl, Trifluorallyl, 1- Chlorprop-l-yl-3-yl. Der Begriff , JIaIo" wird erfindungsgemäß synonym zu „Halogen" verwendet.
Halogen bedeutet Fluor, Chlor, Brom oder lod. Haloalkyl, -alkenyl und -alkinyl bedeuten durch Halogen, vorzugsweise durch Fluor, Chlor oder Brom, insbesondere durch Fluor und/oder Chlor, teilweise oder vollständig substituiertes Alkyl, Alkenyl bzw. Alkinyl, z.B. Monohaloalkyl (= Monohalogenalkyl), Perhaloalkyl, CF3, CHF2, CH2F, CF3CF2, CH2FCHCI, CCI3, CHCI2,
CH2CH2CI; Haloalkoxy ist z.B. OCF3, OCHF2, OCH2F, CF3CF2O, OCH2CF3 und OCH2CH2CI; entsprechendes gilt für Haloalkenyl und andere durch Halogen substituierte Reste.
Die vorliegenden Verbindungen der allgemeinen Formel (I) können gegebenenfalls ein chirales Kohlenstoffatom aufweisen. Entsprechende chirale Kohlenstoffatome können insbesondere in dem
X
Il Substituenten A und auftreten
Gemäß den Regeln nach Cahn, Ingold und Prelog (CIP-Regeln) können diese Substituenten sowohl eine (R)- als auch eine (S)-Konfiguration aufweisen.
Von der vorliegenden Erfindung werden Verbindungen der allgemeinen Formel (I) sowohl mit (S)- als auch mit (R)-Konfiguration an den jeweiligen chiralen Kohlenstoffatomen umfasst, d.h., dass die vorliegende Erfindung die Verbindungen der allgemeinen Formel (I) erfasst, in welchen die betreffenden Kohlenstoffatome jeweils unabhängig voneinander
(1) eine (R)-Konfiguration; oder
(2) eine (S)-Konfiguration
aufweisen. Wenn mehrere Chiralitätszentren in den Verbindungen der allgemeinen Formel (I) vorliegen, sind beliebige Kombinationen der Konfigurationen der Chiralitätszentren möglich, d.h. dass
(1) ein Chiralitätszentrum die (R)-Konfiguration und das andere Chiralitätszentrum die (S)- Konfiguration;
(2) ein Chiralitätszentrum die (R)-Konfϊguration und das andere Chiralitätszentrum die (R)- Konfiguration; und
(3) ein Chiralitätszentrum die (S)-Konfiguration und das andere Chiralitätszentrum die (S)- Konfiguration
aufweist.
Erfindungsgemäß umfasst sind daher insbesondere die folgenden Verbindungen der Formeln (1-1), (1-2) und (1-3)
(I- 1) RS -Verbindung
(1-2) RR-Verbindung
(1-3) SS-Verbindung
Weiterer Gegenstand der vorliegenden Erfindung sind Verfahren zur Herstellung entsprechender Verbindungen der allgemeinen Formel (I) und/oder deren Salze.
In einer ersten Ausführungsform (A) der vorliegenden Erfindung erfolgt die Herstellung der Verbindungen der allgemeinen Formel (I) dadurch, dass man 3-Amino-l,2-benzoisothiazole der allgemeinen Formel (II)
X X
Il Il und T für Halogen und °~c~γ~z steht, bevorzugt für Chlor und °~c~γ~z
In einer zweiten Ausführungsform (B) der vorliegenden Erfindung erfolgt die Herstellung der Verbindungen der allgemeinen Formel (I) dadurch, dass man (Thio)carbamate und (Thio)oxamate der Formel (Ib)
in welcher A, X, Y, Z, R1, R2, R3 und R4 die oben angegebenen Bedeutungen haben, mit einem Oxidationsmittel umsetzt.
In einer dritten Ausfuhrungsform (C) der vorliegenden Erfindung erfolgt die Herstellung der Verbindungen der allgemeinen Formel (I) dadurch, dass man (Thio)carbamate und (Thio)oxamate der Formel (Ic)
mit einem basischen oder sauren Spaltungsreagens unsetzt, worin A Wasserstoff bedeutet und R1 bis R4, n, X, Y und Z die vorstehende Bedeutung aufweisen.
Alle dieser Verfahren fuhren zu erfindungsgemäßen Verbindungen der allgemeinen Formel (I).
In den jeweils vorstehend genannten Verfahrensvarianten werden jeweils inerte Lösemittel verwendet. Unter inerte Lösemittel werden im Sinne der vorliegenden Erfindung Lösemittel verstanden, die unter den jeweiligen Reaktionsbedingungen inert sind, d.h. insbesondere nicht mit den Edukten reagieren, jedoch nicht unter beliebigen Reaktionsbedingungen inert sein müssen.
Beispiele organischer Lösemittel, welche im Rahmen der vorliegenden Erfindung verwendet werden können, sind aromatische oder aliphatische Lösemittel, wie Benzol, Toluol, Xylol, Mesitylen, Hexan, Heptan, Octan, Cyclohexan,; aliphatische und aromatische Halogenkohlenwasserstoffe, wie Methylenchlorid, Dichlorethan, Chloroform, Kohlenstofftetrachlorid, Chlorbenzol, Dichlorbenzol, Ether, wie Diethylether, Dibutylether, Diisobutylether, Methyl-tert-butylether, Isopropylethylether, Diisopropylether, Tetrahydrofuran, und Dioxan; weiter auch Dimethylsulfoxid, und Säureamidderivate, wie N,N-Dimethylformamid, N,N-Dimethylacetamid und N-Methyl-2-pyrrolidon, sowie auch Carbonsäureester, wie Ethylacetat, oder aber auch Diglyme, Dimethylglycol; Nitrile wie Acetonitril, Propionitril oder Butyronitril sowie Ketone wie Aceton, Methylethyl-keton oder Cyclohexanon. Besonders bevorzugt sind Toluol, Xylol, Dichlorbenzol, Chlorbenzol, Acetonitril, Aceton, Butyronitril oder Ethylacetat. Allerdings ist die vorliegende Erfindung nicht auf die zuvor beispielhaft genannten Lösemittel beschränkt.
Die Reaktionstemperatur, bei welcher die Umsetzungen gemäß den vorstehenden Ausführungsformen durchgeführt werden können, kann in weiten Bereichen variieren. Entsprechende Temperaturen sind in den jeweiligen Ausführungsformen der Umsetzungen
genannt. Darüber hinaus können die Umsetzungen bei einer Temperatur von 0 bis 100 0C, vorzugsweise 20 bis 70 0C, durchgeführt werden.
Der Umsetzungen der vorliegenden Erfindungen werden im Allgemeinen unter Normaldruck durchgeführt. Es ist jedoch auch möglich, unter erhöhtem Druck oder vermindertem Druck - im Allgemeinen zwischen 0, 1 bar und 10 bar - zu arbeiten.
Die Verfahren zur Herstellung der erfindungsgemäßen Benzoisothiazole der allgemeinen Formel (I) werden gegebenenfalls in Gegenwart eines basischen oder sauren Reaktionshilfsmittels oder Spaltungsreagens durchgeführt.
Als solche kommen alle üblichen anorganischen oder organischen Basen infrage. Hierzu gehören beispielsweise Alkalimetall- oder Erdalkalimetallhydride, -hydroxide,-amide, -alkoholate, -acetate, -carbonate oder -hydrogencarbonate, wie beispielsweise Lithium-, Natrium-, Kalium- oder Calciumhydrid, Lithium-, Natrium- oder Kaliumamid, Natrium- oder Kaliummethylat, Natriumoder Kaliumethylat, Natrium- oder Kaliumpropylat, Aluminiumisopropylat, Natrium- oder Kalium- tert.-butylat, Natrium- oder Kaliumhydroxid, Ammoniumhydroxid, Natrium-, Kalium- oder Calciumacetat, Ammoniumacetat, Natrium-, Kalium- oder Calciumcarbonat, Ammoniumcarbonat, Natrium- oder Kaliumhydrogencarbonat, sowie basische organische Stickstoffverbindungen, wie Trimethylamin, Triethylamin, Tripropylamin, Tributylamin, Ethyl-diisopropylamin, N,N- Dimethylcyclohexylamin, Dicyclohexylamin, Ethyldicyclohexylamin, N,N-Dimethylanilin, N,N- Dimethylbenzylamin, Pyridin, 2-Methyl-, 3-Methyl- und 4-Methylpyridin, 2,4-Dimethyl-, 2,6- Dimethyl-, 3,4-Dimethyl- und 3,5-Dimethylpyridin, 5-Ethyl-2-methyl-pyridin, N-Methylpyridin, 4- (N,N-Dimethylamino)-pyridin, Diazabicyclooctan (DABCO), Diazabicyclononen (DBN) oder Diazabicycloundecen (DBU).
Als saure Reaktionshilfsmittel kommen alle üblichen anorganischen oder organischen Säuren infrage. Hierzu gehören beispielsweise Mineralsäuren wie Schwefelsäure H2SO4, Phosphorsäure H3PO4 oder Salzsäure HCl oder organische Säuren wie Ameisensäure, Essigsäure oder Trifluoressigsäure.
Die erfϊndungsgemäßen Wirkstoffe eignen sich bei guter Pflanzenverträglichkeit, günstiger Warm- blütertoxizität und guter Umweltverträglichkeit zum Schutz von Pflanzen und Pflanzenorganen, zur Steigerung der Ernteerträge, Verbesserung der Qualität des Erntegutes und zur Bekämpfung von tierischen Schädlingen, insbesondere Insekten, Spinnentieren, Helminthen, Nematoden und Mollusken, die in der Landwirtschaft, im Gartenbau, bei der Tierzucht, in Forsten, in Gärten und Freizeiteinrichtungen, im Vorrats- und Materialschutz sowie auf dem Hygienesektor vorkommen. Sie können vorzugsweise als Pflanzenschutzmittel eingesetzt werden. Sie sind gegen normal
sensible und resistente Arten sowie gegen alle oder einzelne Entwicklungsstadien wirksam. Zu den oben erwähnten Schädlingen gehören:
Aus der Ordnung der Anoplura (Phthiraptera) z.B. Damalinia spp., Haematopinus spp., Linognathus spp., Pediculus spp., Trichodectes spp..
Aus der Klasse der Arachnida z.B. Acarus siro, Aceria sheldoni, Aculops spp., Aculus spp., Amblyomma spp., Argas spp., Boophilus spp., Brevipalpus spp., Bryobia praetiosa, Chorioptes spp., Dermanyssus gallinae, Eotetranychus spp., Epitrimerus pyri, Eutetranychus spp., Eriophyes spp., Hemitarsonemus spp., Hyalomma spp., Ixodes spp., Latrodectus mactans, Metatetranychus spp., Oligonychus spp., Ornithodoros spp., Panonychus spp., Phyllocoptruta oleivora, Polyphagotarsonemus latus, Psoroptes spp., Rhipicephalus spp., Rhizoglyphus spp., Sarcoptes spp., Scorpio maurus, Stenotarsonemus spp., Tarsonemus spp., Tetranychus spp., Vasates lycopersici.
Aus der Klasse der Bivalva z.B. Dreissena spp..
Aus der Ordnung der Chilopoda z.B. Geophilus spp., Scutigera spp..
Aus der Ordnung der Coleoptera z.B. Acanthoscelides obtectus, Adoretus spp., Agelastica alni, Agriotes spp., Amphimallon solstitialis, Anobium punctatum, Anoplophora spp., Anthonomus spp., Anthrenus spp., Apogonia spp., Atomaria spp., Attagenus spp., Bruchidius obtectus, Bruchus spp., Ceuthorhynchus spp., Cleonus mendicus, Conoderus spp., Cosmopolites spp., Costelytra zea- landica, Curculio spp., Cryptorhynchus lapathi, Dermestes spp., Diabrotica spp., Epilachna spp., Faustinus cubae, Gibbium psylloides, Heteronychus arator, Hylamorpha elegans, Hylotrupes bajulus, Hypera postica, Hypothenemus spp., Lachnosterna consanguinea, Leptinotarsa decemlineata, Lissorhoptrus oryzophilus, Lixus spp., Lyctus spp., Meligethes aeneus, Melolontha meiolontha, Migdolus spp., Monυuhamus spp., Naupactus xanthographus, Niptus hololeucus, Oryctes rhinoceros, Oryzaephilus surinamensis, Otiorrhynchus sulcatus, Oxycetonia jucunda, Phaedon cochleariae, Phyllophaga spp., Popillia japonica, Premnotrypes spp., Psylliodes chryso- cephala, Ptinus spp., Rhizobius ventralis, Rhizopertha dominica, Sitophilus spp., Sphenophorus spp., Sternechus spp., Symphyletes spp., Tenebrio molitor, Tribolium spp., Trogoderma spp., Tychius spp., Xylotrechus spp., Zabrus spp..
Aus der Ordnung der Collembola z.B. Onychiurus armatus.
Aus der Ordnung der Dermaptera z.B. Forfϊcula auricularia.
Aus der Ordnung der Diplopoda z.B. Blaniulus guttulatus.
Aus der Ordnung der Diptera z.B. Aedes spp., Anopheles spp., Bibio hortulanus, Calliphora erythrocephala, Ceratitis capitata, Chrysomyia spp., Cochliomyia spp., Cordylobia anthropophaga, Culex spp., Cuterebra spp., Dacus oleae, Dermatobia hominis, Drosophila spp., Fannia spp., Gastrophilus spp., Hylemyia spp., Hyppobosca spp., Hypoderma spp., Liriomyza spp.. Lucilia spp., Musca spp., Nezara spp., Oestrus spp., Oscinella frit, Pegomyia hyoscyami, Phorbia spp., Stomoxys spp., Tabanus spp., Tannia spp., Tipula paludosa, Wohlfahrtia spp.
Aus der Klasse der Gastropoda z.B. Arion spp., Biomphalaria spp., Bulinus spp., Deroceras spp., Galba spp., Lymnaea spp., Oncomelania spp., Succinea spp..
Aus der Klasse der Helminthen z.B. Ancylostoma duodenale, Ancylostoma ceylanicum, Acylostoma braziliensis, Ancylostoma spp., Ascaris lubricoides, Ascaris spp., Brugia malayi, Brugia timori, Bunostomum spp., Chabertia spp., Clonorchis spp., Cooperia spp., Dicrocoelium spp., Dictyocaulus fϊlaria, Diphyllobothrium latum, Dracunculus medinensis, Echinococcus granulosus, Echinococcus multilocularis, Enterobius vermicularis, Faciola spp., Haemonchus spp., Heterakis spp., Hymenolepis nana, Hyostrongulus spp., Loa Loa, Nematodirus spp., Oesophagostomum spp., Opisthorchis spp., Onchocerca volvulus, Ostertagia spp., Paragonimus spp., Schistosomen spp, Strongyloides fuelleborni, Strongyloides stercoralis, Stronyloides spp., Taenia saginata, Taenia solium, Trichinella spiralis, Trichinella nativa, Trichinella britovi, Trichinella nelsoni, Trichinella pseudopsiralis, Trichostrongulus spp., Trichuris trichuria, Wuchereria bancrofti.
Weiterhin lassen sich Protozoen, wie Eimeria, bekämpfen.
Aus der Ordnung der Heteroptera z.B. Anasa tristis, Antestiopsis spp., Blissus spp., Calocoris spp., Campylomma livida, Cavelerius spp., Cimex spp., Creontiades dilutus, Dasynus piperis, Dichelops furcatus, Diconocoris hewetti, Dysdercus spp., Euschistus spp., Eurygaster spp., Heliopeltis spp., Horcias nobilellus, Leptocorisa spp., Leptoglossus phyllopus, Lygus spp., Macropes excavatus, Miridae, Nezara spp., Oebalus spp., Pentomidae, Piesma quadrata, Piezodorus spp., Psallus seriatus, Pseudacysta persea, Rhodnius spp., Sahlbergella singularis, Scotinophora spp., Stephanitis nashi, Tibraca spp., Triatoma spp.
Aus der Ordnung der Homoptera z.B. Acyrthosipon spp., Aeneolamia spp., Agonoscena spp., Aleurodes spp., Aleurolobus barodensis, Aleurothrixus spp., Amrasca spp., Anuraphis cardui, Aonidiella spp., Aphanostigma piri, Aphis spp., Arboridia apicalis, Aspidiella spp., Aspidiotus spp., Atanus spp., Aulacorthum solani, Bemisia spp., Brachycaudus helichrysii, Brachycolus spp., Brevicoryne brassicae, Calligypona marginata, Carneocephala fulgida, Ceratovacuna lanigera, Cercopidae, Ceroplastes spp., Chaetosiphon fragaefolii, Chionaspis tegalensis, Chlorita onukii,
Chromaphis juglandicola, Chrysomphalus ficus, Cicadulina mbila, Coccomytilus halli, Coccus spp., Cryptomyzus ribis, Dalbulus spp., Dialeurodes spp., Diaphorina spp., Diaspis spp., Doralis spp., Drosicha spp., Dysaphis spp., Dysmicoccus spp., Empoasca spp., Eriosoma spp., Erythroneura spp., Euscelis bilobatus, Geococcus coffeae, Homalodisca coagulata, Hyalopterus arundinis, Icerya spp., Idiocerus spp., Idioscopus spp., Laodelphax striatellus, Lecanium spp., Lepidosaphes spp., Lipaphis erysimi, Macrosiphum spp., Mahanarva fimbriolata, Melanaphis sacchari, Metcalfiella spp., Metopolophium dirhodum, Monellia costalis, Monelliopsis pecanis, Myzus spp., Nasonovia ribisnigri, Nephotettix spp., Nilaparvata lugens, Oncometopia spp., Orthezia praelonga, Parabemisia myricae, Paratrioza spp., Parlatoria spp., Pemphigus spp., Pere- grinus maidis, Phenacoccus spp., Phloeomyzus passerinii, Phorodon humuli, Phylloxera spp., Pinnaspis aspidistrae, Planococcus spp., Protopulvinaria pyriformis, Pseudaulacaspis pentagona, Pseudococcus spp., Psylla spp., Pteromalus spp., Pyrilla spp., Quadraspidiotus spp., Quesada gigas, Rastrococcus spp., Rhopalosiphum spp., Saissetia spp., Scaphoides titanus, Schizaphis graminum, Selenaspidus articulatus, Sogata spp., Sogatella furcifera, Sogatodes spp., Stictocephala festina, Tenalaphara malayensis, Tinocallis caryaefoliae, Tomaspis spp., Toxoptera spp., Trialeurodes vaporariorum, Trioza spp., Typhlocyba spp., Unaspis spp., Viteus vitifolii.
Aus der Ordnung der Hymenoptera z.B. Diprion spp., Hoplocampa spp., Lasius spp., Monomorium pharaonis, Vespa spp..
Aus der Ordnung der Isopoda z.B. Armadillidium vulgäre, Oniscus asellus, Porcellio scaber.
Aus der Ordnung der Isoptera z.B. Reticulitermes spp., Odontotermes spp..
Aus der Ordnung der Lepidoptera z.B. Acronicta major, Aedia leucomelas, Agrotis spp., Alabama argillacea, Anticarsia spp., Barathra brassicae, Bucculatrix thurberiella, Bupalus piniarius, Cacoecia podana, Capua reticulana, Carpocapsa pomonella, Cheimatobia brumata, Chilo spp., Choristoneura fumiferana, Clysia ambiguella, Cnaphalocerus spp., Earias insulana, Ephestia kuehniella, Euproctis chrysorrhoea, Euxoa spp., Feltia spp., Galleria mellonella, Helicoveφa spp., Heliothis spp., Hofmannophila pseudospretella, Homona magnanima, Hyponomeuta padella, La- phygma spp., Lithocolletis blancardella, Lithophane antennata, Loxagrotis albicosta, Lymantria spp., Malacosoma neustria, Mamestra brassicae, Mocis repanda, Mythimna separata, Oria spp., Oulema oryzae, Panolis flammea, Pectinophora gossypiella, Phyllocnistis citrella, Pieris spp., Plutella xylostella, Prodenia spp., Pseudaletia spp., Pseudoplusia includens, Pyrausta nubilalis, Spodoptera spp., Thermesia gemmatalis, Tinea pellionella, Tineola bisselliella, Tortrix viridana, Trichoplusia spp..
Aus der Ordnung der Orthoptera z.B. Acheta domesticus, Blatta orientalis, Blattella germanica, Gryllotalpa spp., Leucophaea maderae, Locusta spp., Melanoplus spp., Periplaneta americana, Schistocerca gregaria.
Aus der Ordnung der Siphonaptera z.B. Ceratophyllus spp., Xenopsylla cheopis.
Aus der Ordnung der Symphyla z.B. Scutigerella immaculata.
Aus der Ordnung der Thysanoptera z.B. Baliothrips biformis, Enneothrips flavens, Frankliniella spp., Heliothrips spp., Hercinothrips femoralis, Kakothrips spp., Rhipiphorothrips cruentatus, Scirtothrips spp., Taeniothrips cardamoni, Thrips spp..
Aus der Ordnung der Thysanura z.B. Lepisma saccharina.
Zu den pflanzenparasitären Nematoden gehören z.B. Anguina spp., Aphelenchoides spp., Belonoaimus spp., Bursaphelenchus spp., Ditylenchus dipsaci, Globodera spp., Heliocotylenchus spp., Heterodera spp., Longidorus spp., Meloidogyne spp., Pratylenchus spp., Radopholus similis, Rotylenchus spp., Trichodorus spp., Tylenchorhynchus spp., Tylenchulus spp., Tylenchulus semipenetrans, Xiphinema spp..
Die Wirksamkeit der Verbindungen der Formel (I) lässt sich durch die Zugabe von Ammonium- und Phosphoniumsalzen steigern. Die Ammonium- und Phosphoniumsalze werden durch Formel (IV) definiert
in welcher
D für Stickstoff oder Phosphor steht,
D bevorzugt für Stickstoff steht,
R5, R6, R7, and R8 unabhängig voneinander für Wasserstoff oder jeweils gegebenenfalls substituiertes Ci-Cg-Alkyl oder einfach oder mehrfach ungesättigtes, gegebenenfalls substituiertes Ci-Cg-Alkylen stehen, wobei die Substituenten aus Halogen, Nitro und Cyano ausgewählt sein können,
R5, R6, R7, and R8 bevorzugt unabhängig voneinander für Wasserstoff oder jeweils gegebenenfalls substituiertes Ci-C4-Alkyl stehen, wobei die Substituenten aus Halogen, Nitro und Cyano ausgewählt sein können,
R5, R6, R7, and R8 besonders bevorzugt unabhängig voneinander für Wasserstoff, Methyl, Ethyl, n- Propyl, i-Propyl, n-Butyl, i-Butyl, s-Butyl oder t-Butyl stehen,
R5, R6, R7, and R8 ganz besonders bevorzugt für Wasserstoff stehen,
m für 1, 2, 3 oder 4 steht,
m bevorzugt für 1 oder 2 steht,
R9 für ein anorganisches oder organisches Anion steht,
R9 bevorzugt für Hydrogencarbonat, Tetraborat, Fluorid, Bromid, Jodid, Chlorid, Monohydrogenphosphat, Dihydrogenphosphat, Hydrogensulfat, Tartrat, Sulfat, Nitrat, Thiosulfat, Thiocyanat, Formiat, Laktat, Acetat, Propionat, Butyrat, Pentanoat, Citrat oder Oxalat steht,
R9 besonders bevorzugt für Laktat, Sulfat, Monohydrogenphosphat, Dihydrogenphosphat, Nitrat, Thiosulfat, Thiocyanat, Citrat, Oxalat oder Formiat steht.
R9 ganz besonders bevorzugt für Sulfat steht.
Die Ammonium- und Phosphoniumsalze der Formel (IV) können in einem breiten Konzentrationsbereich zur Steigerung der Wirkung von Pflanzenschutzmitteln enthaltend Verbindungen der Formle (I) eingesetzt werden. Im Allgemeinen werden die Ammonium- oder Phosphoniumsalze im anwendungsfertigen Pflanzenschutzmittel in einer Konzentration von 0,5 bis 80 mmol/1, bevorzugt 0,75 bis 37,5 mmol/1, besonders bevorzugt 1,5 bis 25 mmol/1 eingesetzt. Im Fall eines formulierten Produktes wird die Ammonium- und/oder Phosphoniumsalzkonzentration in der Formulierung so gewählt, dass sie nach Verdünnung der Formulierung auf die gewünschte Wirkstoffkonzentration in diesen angegebenen allgemeinen, bevorzugten oder besonders bevorzugten Bereichen liegt. Die Konzentration des Salzes in der Formulierung beträgt dabei üblicherweise 1 - 50 Gew.-%.
In einer bevorzugten Ausführungsform der Erfindung wird den Pflanzenschutzmitteln zur
Wirkungssteigerung nicht nur ein Ammonium- und/oder Phosphoniumsalz, sondern zusätzlich ein
Penetrationsförderer zugegeben. Selbst in diesen Fällen ist eine noch weiter gehende Wirkungssteigerung zu beobachten. Gegenstand der vorliegenden Erfindung ist also ebenfalls die
Verwendung einer Kombination von Penetrationsforderer und Ammonium- und/oder Phosphoniumsalzen zur Wirkungssteigerung von Pflanzenschutzmitteln, die akarizid/insektizid wirksame Verbindungen der Formel (I) als Wirkstoff enthalten. Gegenstand der Erfindung ist schließlich weiterhin die Verwendung dieser Mittel zur Bekämpfung von Schadinsekten.
Als Penetrationsforderer kommen im vorliegenden Zusammenhang alle diejenigen Substanzen in Betracht, die üblicherweise eingesetzt werden, um das Eindringen von agrochemischen Wirkstoffen in Pflanzen zu verbessern. Penetrationsforderer werden in diesem Zusammenhang dadurch definiert, dass sie aus der wässerigen Spritzbrühe und/oder aus dem Spritzbelag in die Kutikula der Pflanze eindringen und dadurch die Stoffbeweglichkeit (Mobilität) von Wirkstoffen in der Kutikula erhöhen können. Die in der Literatur (Baur et al., 1997, Pesticide Science 51, 131- 152) beschriebene Methode kann zur Bestimmung dieser Eigenschaft eingesetzt werden.
Als Penetrationsforderer kommen beispielsweise Alkanol-alkoxylate in Betracht. Erfindungsgemäße Penetrationsforderer sind Alkanol-alkoxylate der Formel
R-O-(-AO)v_R' (V)
in welcher
R für geradkettiges oder verzweigtes Alkyl mit 4 bis 20 Kohlenstoffatomen steht,
R1 für Wasserstoff, Methyl, Ethyl, n-Propyl, i-Propyl, n-Butyl, i-Butyl, t-Butyl, n-Pentyl oder n-Hexyl steht,
AO für einen Ethylenoxid-Rest, einen Propylenoxid-Rest, einen Butylenoxid-Rest oder für Gemische aus Ethylenoxid- und Propylenoxid-Resten oder Butylenoxid-Resten steht und
v für Zahlen von 2 bis 30 steht.
Eine bevorzugte Gruppe von Penetrationsförderern sind Alkanolalkoxylate der Formel
R-O-(-EO-)n-R' (V-a)
in welcher
R die oben angegebene Bedeutung hat,
R' die oben angegebene Bedeutung hat,
EO für -CH2-CH2-O- steht und
n für Zahlen von 2 bis 20 steht.
Eine weitere bevorzugte Gruppe von Penetrationsforderem sind Alkanol-alkoxylate der Formel
R-O-(-EO-)p-(-PO-)q-R' (V-b)
in welcher
R die oben angegebene Bedeutung hat,
R' die oben angegebene Bedeutung hat,
EO für -CH2-CH2-O- steht,
PO für CH- CH-O steht>
CH3
p für Zahlen von 1 bis 10 steht und
q für Zahlen von 1 bis 10 steht.
Eine weitere bevorzugte Gruppe von Penetrationsforderem sind Alkanol-Alkoxylate der Formel
R.O-(-PO-)r-(EO-)s-R' (V-C)
in welcher
R die oben angegebene Bedeutung hat,
R' die oben angegebene Bedeutung hat,
EO für -CH2-CH2-O- steht,
PO für -CH- TCH-O- steht>
CH ",3
r für Zahlen von 1 bis 10 steht und
s für Zahlen von 1 bis 10 steht.
Eine weitere bevorzugte Gruppe von Penetrationsforderem sind Alkanol-alkoxylate der Formel
R-O-(-EO-)p-(-BO-)q-R' (V-d) in welcher
R und R die oben angegebenen Bedeutungen haben, EO für CH2-CH2-O- steht, BO für — CH-CH-CH-O steht,
CH3
p für Zahlen von 1 bis 10 steht und q für Zahlen von 1 bis 10 steht.
Eine weitere bevorzugte Gruppe von Penetrationsförderern sind Alkanol-alkoxylate der Formel
R-O-(-BO-)r-(-EO-)s-R' (V-e) in welcher
R und R die oben angegebenen Bedeutungen haben, BO für — CH-CH- TCH-O steht,
CH3 EO für CH2-CH2-O- steht, r für Zahlen von 1 bis 10 steht und s für Zahlen von 1 bis 10 steht.
Eine weitere bevorzugte Gruppe von Penetrationsförderern sind Alkanol-Alkoxylate der Formel CH3-(CH2)t-CH2-O-(-CH2-CH2-O-)u-R' (V-f) in welcher
R' die oben angegebene Bedeutung hat, t für Zahlen von 8 bis 13 steht
u für Zahlen von 6 bis 17 steht.
In den zuvor angegebenen Formeln steht
R vorzugsweise für Butyl, i-Butyl, n-Pentyl, i-Pentyl, Neopentyl, n-Hexyl, i-Hexyl, n-Octyl, i-Octyl, 2-Ethyl-hexyl, Nonyl, i-Nonyl, Decyl, n-Dodecyl, i-Dodecyl, Lauryl, Myristyl, i-Tridecyl, Trimethyl-nonyl, Palmityl, Stearyl oder Eicosyl.
Als Beispiel für ein Alkanol-Alkoxylat der Formel (V-c) sei 2-Ethyl-hexyl-alkoxylat der Formel
in welcher
EO für -CH2-CH2-O- steht,
PO für CH- CH-O steht und
CH3
die Zahlen 8 und 6 Durchschnittswerte darstellen, genannt.
Als Beispiel für ein Alkanol-Alkoxylat der Formel (V-d) sei die Formel
CH3-(CH2)10-O-(-EO-)6-(-BO-)2-CH3 (V-d-1)
in welcher
EO für CH2-CH2-O- steht,
BO für — CH-CH- TCH-O steht und
CH3
die Zahlen 10, 6 und 2 Durchschnittswerte darstellen, genannt.
Besonders bevorzugte Alkanol-Alkoxylate der Formel (V-f) sind Verbindungen dieser Formel, in denen
t für Zahlen von 9 bis 12 und
u für Zahlen von 7 bis 9
steht.
Ganz besonders bevorzugt genannt sei Alkanol-Alkoxylat der Formel (V-f-1)
CH3-(CH2)t-CH2-O-(-CH2-CH2-O-)u-R' (V-f-1)
in welcher
t für den Durchschnittswert 10,5 steht und
u für den Durchschnittswert 8,4 steht.
Die Alkanol-Alkoxylate sind durch die obigen Formeln allgemein definiert. Bei diesen Substanzen handelt es sich um Gemische von Stoffen des angegebenen Typs mit unterschiedlichen Kettenlängen. Für die Indices errechnen sich deshalb Durchschnittswerte, die auch von ganzen Zahlen abweichen können.
Die Alkanol-Alkoxylate der angegebenen Formeln sind bekannt und sind teilweise kommerziell erhältlich oder lassen sich nach bekannten Methoden herstellen (vgl. WO 98/35 553, WO 00/35 278 und EP-A 0 681 865).
Als Penetrationsförderer kommen beispielsweise auch Substanzen in Betracht, die die Löslichkeit der Verbindungen der Formel (I) im Spritzbelag fördern. Dazu gehören beispielsweise mineralische oder vegetabile Öle. Als Öle kommen alle üblicherweise in agrochemischen Mitteln einsetzbaren mineralischen oder vegetabilen - gegebenenfalls modifizierte - Öle in Frage. Beispielhaft genannt seien Sonnenblumenöl, Rapsöl, Olivenöl, Rizinusöl, Rüböl, Maiskernöl, Baumwollsaatöl und Sojabohnenöl oder die Ester der genannten Öle. Bevorzugt sind Rapsöl, Sonnenblumenöl und deren Methyl- oder Ethylester.
Die Konzentration an Penetrationsförderer kann in einem weiten Bereich variiert werden. Bei einem formulierten Pflanzenschutzmittel liegt sie im allgemeinen bei 1 bis 95 Gew.-%, bevorzugt bei 1 bis 55 Gew.-%, besonders bevorzugt bei 15 - 40 Gew.-%. In den anwendungsfertigen Mitteln (Spritzbrühen) liegen die Konzentration im allgemeinen zwischen 0,1 und 10 g/l, bevorzugt zwischen 0,5 und 5 g/l.
Erfindungsgemäß hervorgehobene Kombinationen von Wirkstoff, Salz und Penetrationsförderer sind in folgender Tabelle aufgeführt."Gemäß Test" bedeutet dabei, dass jede Verbindung geeignet
ist, die in dem Test für die Kutikelpenetration (Baur et al., 1997, Pesticide Science 51, 131-152) als Penetrationsförderer wirkt.
Tabelle 1:
Die Verbindungen der Formel (I) können gegebenenfalls in bestimmten Konzentrationen bzw. Aufwandmengen auch als Herbizide, Safener, Wachstumsregulatoren oder Mittel zur Verbesserung der Pflanzeneigenschaften, oder als Mikrobizide, beispielsweise als Fungizide, Antimykotika, Bakterizide, Virizide (einschließlich Mittel gegen Viroide) oder als Mittel gegen MLO (Mycoplasma-like-organism) und RLO (Rickettsia-like-organism) verwendet werden. Sie lassen sich gegebenenfalls auch als Zwischen- oder Vorprodukte für die Synthese weiterer Wirkstoffe einsetzen.
Die Wirkstoffe können in die üblichen Formulierungen überführt werden, wie Lösungen, Emulsionen, Spritzpulver, wasser- und ölbasierte Suspensionen, Pulver, Stäubemittel, Pasten, lösliche Pulver, lösliche Granulate, Streugranulate, Suspensions-Emulsions-Konzentrate, Wirkstoffimprägnierte Naturstoffe, Wirkstoff-imprägnierte synthetische Stoffe, Düngemittel sowie Feinst- verkapselungen in polymeren Stoffen.
Diese Formulierungen werden in bekannter Weise hergestellt, z.B. durch Vermischen der Wirkstoffe mit Streckmitteln, also flüssigen Lösungsmitteln und/oder festen Trägerstoffen, gegebenenfalls unter Verwendung von oberflächenaktiven Mitteln, also Emulgiermitteln und/oder Dispergiermitteln und/oder schaumerzeugenden Mitteln. Die Herstellung der Formulierungen erfolgt entweder in geeigneten Anlagen oder auch vor oder während der Anwendung.
Als Hilfsstoffe können solche Stoffe Verwendung finden, die geeignet sind, dem Mittel selbst oder und/oder davon abgeleitete Zubereitungen (z.B. Spritzbrühen, Saatgutbeizen) besondere Eigenschaften zu verleihen, wie bestimmte technische Eigenschaften und/oder auch besondere biologische Eigenschaften. Als typische Hilfsmittel kommen in Frage: Streckmittel, Lösemittel und Trägerstoffe.
Als Streckmittel eignen sich z.B. Wasser, polare und unpolare organische chemische Flüssigkeiten z.B. aus den Klassen der aromatischen und nicht-aromatischen Kohlenwasserstoffe (wie Paraffine, Alkylbenzole, Alkylnaphthaline, Chlorbenzole), der Alkohole und Polyole (die ggf. auch substituiert, verethert und/oder verestert sein können), der Ketone (wie Aceton, Cyclohexanon), Ester (auch Fette und Öle) und (poly-)Ether, der einfachen und substituierten Amine, Amide, Lactame (wie N-Alkylpyrrolidone) und Lactone, der Sulfone und Sulfoxide (wie Dimethylsysulfoxid).
Im Falle der Benutzung von Wasser als Streckmittel können z.B. auch organische Lösemittel als Hilfslösungsmittel verwendet werden. Als flüssige Lösemittel kommen im wesentlichen in Frage: Aromaten, wie Xylol, Toluol, oder Alkylnaphthaline, chlorierte Aromaten und chlorierte aliphatische Kohlenwasserstoffe, wie Chlorbenzole, Chlorethylene oder Methylenchlorid, aliphatische Kohlenwasserstoffe, wie Cyclohexan oder Paraffine, z.B. Erdölfraktionen, mineralische und pflanzliche Öle, Alkohole, wie Butanol oder Glykol sowie deren Ether und Ester, Ketone wie Aceton, Methylethylketon, Methylisobutylketon oder Cyclohexanon, stark polare Lösungsmittel, wie Dimethylsulfoxid, sowie Wasser.
Als feste Trägerstoffe kommen in Frage:
z.B. natürliche Gesteinsmehle, wie Kaoline, Tonerden, Talkum, Kreide, Quarz, Attapulgit, Montmorillonit oder Diatomeenerde und synthetische Gesteinsmehle, wie hochdisperse
Kieselsäure, Aluminiumoxid und Silikate, als feste Trägerstoffe für Granulate kommen in Frage: z.B. gebrochene und fraktionierte natürliche Gesteine wie Calcit, Marmor, Bims, Sepiolith, Dolomit sowie synthetische Granulate aus anorganischen und organischen Mehlen sowie Granulate aus organischem Material wie Papier, Sägemehl, Kokosnußschalen, Maiskolben und Tabakstengeln; als Emulgier- und/oder schaumerzeugende Mittel kommen in Frage: z.B. nichtionogene und anionische Emulgatoren, wie Polyoxyethylen-Fettsäure-Ester, Polyoxyethylen-Fettalkohol-Ether, z.B. Alkylaryl-polyglykolether, Alkylsulfonate, Alkylsulfate, Arylsulfonate sowie Eiweiß- hydrolysate; als Dispergiermittel kommen in Frage nicht-ionische und/oder ionische Stoffe, z.B. aus den Klassen der Alkohol-POE- und/oder POP-Ether, Säure- und/oder POP- POE-Ester, Alkyl- Aryl- und/oder POP- POE-Ether, Fett- und/oder POP- POE-Addukte, POE- und/oder POP-Polyol Derivate, POE- und/oder POP-Sorbitan- oder-Zucker-Addukte, Alky- oder Aryl-Sulfate, Sulfonate und Phosphate oder die entsprechenden PO-Ether-Addukte. Ferner geeignete Oligo- oder Polymere, z.B. ausgehend von vinylischen Monomeren, von Acrylsäure, aus EO und/oder PO allein oder in Verbindung mit z.B. (poly-) Alkoholen oder (poly-) Aminen. Ferner können Einsatz finden Lignin und seine Sulfonsäure-Derivate, einfache und modifizierte Cellulosen, aromatische und/oder aliphatische Sulfonsäuren sowie deren Addukte mit Formaldehyd.
Es können in den Formulierungen Haftmittel wie Carboxymethylcellulose, natürliche und synthetische pulvrige, körnige oder latexförmige Polymere verwendet werden, wie Gummi- arabicum, Polyvinylalkohol, Polyvinylacetat, sowie natürliche Phospholipide, wie Kephaline und Lecithine und synthetische Phospholipide.
Es können Farbstoffe wie anorganische Pigmente, z.B. Eisenoxid, Titanoxid, Ferrocyanblau und organische Farbstoffe, wie Alizarin-, Azo- und Metallphthalocyaninfarbstoffe und Spurennährstoffe wie Salze von Eisen, Mangan, Bor, Kupfer, Kobalt, Molybdän und Zink verwendet werden.
Weitere Additive können Duftstoffe, mineralische oder vegetabile gegebenenfalls modifizierte Öle, Wachse und Nährstoffe (auch Spurennährstoffe), wie Salze von Eisen, Mangan, Bor, Kupfer, Kobalt, Molybdän und Zink sein.
Weiterhin enthalten sein können Stabilisatoren wie Kältestabilisatoren, Konservierungsmittel, Oxidationsschutzmittel, Lichtschutzmittel oder andere die chemische und / oder physikalische Stabilität verbessernde Mittel.
Die Formulierungen enthalten im Allgemeinen zwischen 0,01 und 98 Gew.-% Wirkstoff, vorzugsweise zwischen 0,5 und 90 %.
Der Wirkstoff kann in seinen handelsüblichen Formulierungen sowie in den aus diesen Formulierungen bereiteten Anwendungsformen in Mischung mit anderen Wirkstoffen wie Insektiziden, Lockstoffen, Sterilantien, Bakteriziden, Akariziden, Nematiziden, Fungiziden, wachstumsregulierenden Stoffen, Herbiziden, Safenern, Düngemitteln,Semiochemicals oder auch mit Mitteln zur Verbesserung der Pflanzeneigenschaften vorliegen.
Die erfindungsgemäßen Wirkstoffe können ferner beim Einsatz als Insektizide in ihren handelsüblichen Formulierungen sowie in den aus diesen Formulierungen bereiteten Anwendungsformen in Mischung mit Synergisten vorliegen. Synergisten sind Verbindungen, durch die die Wirkung der Wirkstoffe gesteigert wird, ohne daß der zugesetzte Synergist selbst aktiv wirksam sein muß.
Die erfindungsgemäßen Wirkstoffe können ferner beim Einsatz als Insektizide in ihren handelsüblichen Formulierungen sowie in den aus diesen Formulierungen bereiteten Anwendungsformen in Mischungen mit Hemmstoffen vorliegen, die einen Abbau des Wirkstoffes nach Anwendung in der Umgebung der Pflanze, auf der Oberfläche von Pflanzenteilen oder in pflanzlichen Geweben vermindern.
Der Wirkstoffgehalt der aus den handelsüblichen Formulierungen bereiteten Anwendungsformen kann in weiten Bereichen variieren. Die Wirkstoffkonzentration der Anwendungsformen kann von 0,00000001 bis zu 95 Gew.-% Wirkstoff, vorzugsweise zwischen 0,00001 und 1 Gew.-% liegen.
Die Anwendung geschieht in einer den Anwendungsformen angepaßten üblichen Weise.
Erfindungsgemäß können alle Pflanzen und Pflanzenteile behandelt werden. Unter Pflanzen werden hierbei alle Pflanzen und Pflanzenpopulationen verstanden, wie erwünschte und unerwünschte Wildpflanzen oder Kulturpflanzen (einschließlich natürlich vorkommender
Kulturpflanzen). Kulturpflanzen können Pflanzen sein, die durch konventionelle Züchtungs- und
Optimierungsmethoden oder durch biotechnologische und gentechnologischε Methoden oder
Kombinationen dieser Methoden erhalten werden können, einschließlich der transgenen Pflanzen und einschließlich der durch Sortenschutzrechte schützbaren oder nicht schützbaren
Pflanzensorten. Unter Pflanzenteilen sollen alle oberirdischen und unterirdischen Teile und Organe der Pflanzen, wie Sproß, Blatt, Blüte und Wurzel verstanden werden, wobei beispielhaft Blätter,
Nadeln, Stengel, Stämme, Blüten, Fruchtkörper, Früchte und Saatgut sowie Wurzeln, Knollen und
Rhizome aufgeführt werden. Zu den Pflanzenteilen gehört auch Erntegut sowie vegetatives und generatives Vermehrungsmaterial, beispielsweise Stecklinge, Knollen, Rhizome, Ableger und
Saatgut.
Die erfϊndungsgemäße Behandlung der Pflanzen und Pflanzenteile mit den Wirkstoffen erfolgt direkt oder durch Einwirkung auf deren Umgebung, Lebensraum oder Lagerraum nach den
üblichen Behandlungsmethoden, z.B. durch Tauchen, Sprühen, Verdampfen, Vernebeln, Streuen, Aufstreichen, Injizieren, Angießen und bei Vermehrungsmaterial, insbesondere bei Saatgut, weiterhin durch ein- oder mehrschichtiges Umhüllen.
Wie bereits oben erwähnt, können erfindungsgemäß alle Pflanzen und deren Teile behandelt werden. In einer bevorzugten Ausführungsform werden wild vorkommende oder durch konventionelle biologische Zuchtmethoden, wie Kreuzung oder Protoplastenfusion erhaltenen
Pflanzenarten und Pflanzensorten sowie deren Teile behandelt. In einer weiteren bevorzugten
Ausführungsform werden transgene Pflanzen und Pflanzensorten, die durch gentechnologische
Methoden gegebenenfalls in Kombination mit konventionellen Methoden erhalten wurden (Genetically Modified Organisms) und deren Teile behandelt. Die Begriffe "Teile" bzw. "Teile von
Pflanzen" oder "Pflanzenteile" wurden oben erläutert.
Besonders bevorzugt werden erfindungsgemäß Pflanzen der jeweils handelsüblichen oder in Gebrauch befindlichen Pflanzensorten behandelt. Unter Pflanzensorten versteht man Pflanzen mit neuen Eigenschaften ("Traits"), die sowohl durch konventionelle Züchtung, durch Mutagenese oder durch rekombinante DNA-Techniken gezüchtet worden sind. Dies können Sorten, Bio- und Genotypen sein.
Je nach Pflanzenarten bzw. Pflanzensorten, deren Standort und Wachstumsbedingungen (Böden, Klima, Vegetationsperiode, Ernährung) können durch die erfindungsgemäße Behandlung auch überadditive ("synergistische") Effekte auftreten. So sind beispielsweise erniedrigte Aufwandmengen und/oder Erweiterungen des Wirkungsspektrums und/oder eine Verstärkung der Wirkung der erfindungsgemäß verwendbaren Stoffe und Mittel, besseres Pflanzenwachstum, erhöhte Toleranz gegenüber hohen oder niedrigen Temperaturen, erhöhte Toleranz gegen Trockenheit oder gegen Wasser- bzw. Bodensalzgehalt, erhöhte Blühleistung, erleichterte Ernte, Beschleunigung der Reife, höhere Ernteerträge, höhere Qualität und/oder höherer Ernährungswert der Ernteprodukte, höhere Lagerfähigkeit und/oder Bearbeitbarkeit der Ernteprodukte möglich, die über die eigentlich zu erwartenden Effekte hinausgehen.
Zu den bevorzugten erfindungsgemäß zu behandelnden transgenen (gentechnologisch erhaltenen) Pflanzen bzw. Pflanzensorten gehören alle Pflanzen, die durch die gentechnologische Modifikation genetisches Material erhielten, welches diesen Pflanzen besondere vorteilhafte wertvolle Eigenschaften ("Traits") verleiht. Beispiele für solche Eigenschaften sind besseres Pflanzenwachstum, erhöhte Toleranz gegenüber hohen oder niedrigen Temperaturen, erhöhte Toleranz gegen Trockenheit oder gegen Wasser- bzw. Bodensalzgehalt, erhöhte Blühleistung, erleichterte Ernte, Beschleunigung der Reife, höhere Ernteerträge, höhere Qualität und/oder höherer Ernährungswert der Ernteprodukte, höhere Lagerfähigkeit und/oder Bearbeitbarkeit der
Ernteprodukte. Weitere und besonders hervorgehobene Beispiele für solche Eigenschaften sind eine erhöhte Abwehr der Pflanzen gegen tierische und mikrobielle Schädlinge, wie gegenüber Insekten, Milben, pflanzenpathogenen Pilzen, Bakterien und/oder Viren sowie eine erhöhte Toleranz der Pflanzen gegen bestimmte herbizide Wirkstoffe. Als Beispiele transgener Pflanzen werden die wichtigen Kulturpflanzen, wie Getreide (Weizen, Reis), Mais, Soja, Kartoffel, Zuckerrüben, Tomaten, Erbsen und andere Gemüsesorten, Baumwolle, Tabak, Raps, sowie Obstpflanzen (mit den Früchten Äpfel, Birnen, Zitrusfrüchten und Weintrauben) erwähnt, wobei Mais, Soja, Kartoffel, Baumwolle, Tabak und Raps besonders hervorgehoben werden. Als Eigenschaften ("Traits") werden besonders hervorgehoben die erhöhte Abwehr der Pflanzen gegen Insekten, Spinnentiere, Nematoden und Schnecken durch in den Pflanzen entstehende Toxine, insbesondere solche, die durch das genetische Material aus Bacillus Thuringiensis (z.B. durch die Gene CryΙA(a), CryIA(b), CryΙA(c), CryllA, CrylllA, CryIHB2, Cry9c Cry2Ab, Cry3Bb und CrylF sowie deren Kombinationen) in den Pflanzen erzeugt werden (im folgenden "Bt Pflanzen"). Als Eigenschaften ("Traits") werden auch besonders hervorgehoben die erhöhte Abwehr von Pflanzen gegen Pilze, Bakterien und Viren durch Systemische Akquirierte Resistenz (SAR), Systemin, Phytoalexine, Elicitoren sowie Resistenzgene und entsprechend exprimierte Proteine und Toxine. Als Eigenschaften ("Traits") werden weiterhin besonders hervorgehoben die erhöhte Toleranz der Pflanzen gegenüber bestimmten herbiziden Wirkstoffen, beispielsweise Imidazolinonen, Sulfonylharnstoffen, Glyphosate oder Phosphinotricin (z.B. "PAT"-Gen). Die jeweils die gewünschten Eigenschaften ("Traits") verleihenden Gene können auch in Kombinationen miteinander in den transgenen Pflanzen vorkommen. Als Beispiele für "Bt Pflanzen" seien Maissorten, Baumwollsorten, Sojasorten und Kartoffelsorten genannt, die unter den Handelsbezeichnungen YIELD GARD® (z.B. Mais, Baumwolle, Soja), KnockOut® (z.B. Mais), StarLink® (z.B. Mais), Bollgard® (Baumwolle), Nucotn® (Baumwolle) und NewLeaf® (Kartoffel) vertrieben werden. Als Beispiele für Herbizid-tolerante Pflanzen seien Maissorten, Baumwollsorten und Sojasorten genannt, die unter den Handelsbezeichnungen Roundup Ready® (Toleranz gegen Glyphosate z.B. Mais, Baumwolle, Soja), Liberty Link® (Toleranz gegen Phosphinotricin, z.B. Raps), IMI® (Toleranz gegen Imidazolinone) und STS® (Toleranz gegen Sulfonylharnstoffe z.B. Mais) vertrieben werden. Als Herbizid- resistente (konventionell auf Herbizid-Toleranz gezüchtete) Pflanzen seien auch die unter der Bezeichnung Clearfield® vertriebenen Sorten (z.B. Mais) erwähnt. Selbstverständlich gelten diese Aussagen auch für in der Zukunft entwickelte bzw. zukünftig auf den Markt kommende Pflanzensorten mit diesen oder zukünftig entwickelten genetischen Eigenschaften ("Traits").
Die aufgeführten Pflanzen können besonders vorteilhaft erfindungsgemäß mit den Verbindungen der allgemeinen Formel I bzw. den erfindungsgemäßen Wirkstoffmischungen behandelt werden.
Die bei den Wirkstoffen bzw. Mischungen oben angegebenen Vorzugsbereiche gelten auch für die
Behandlung dieser Pflanzen. Besonders hervorgehoben sei die Pflanzenbehandlung mit den im vorliegenden Text speziell aufgeführten Verbindungen bzw. Mischungen.
Die erfindungsgemäßen Wirkstoffe wirken nicht nur gegen Pflanzen-, Hygiene- und Vorratsschädlinge, sondern auch auf dem veterinärmedizinischen Sektor gegen tierische Parasiten (Ekto- und Endoparasiten) wie Schildzecken, Lederzecken, Räudemilben, Laufmilben, Fliegen (stechend und leckend), parasitierende Fliegenlarven, Läuse, Haarlinge, Federlinge und Flöhe. Zu diesen Parasiten gehören:
Aus der Ordnung der Anoplurida z.B. Haematopinus spp., Linognathus spp., Pediculus spp., Phtirus spp., Solenopotes spp..
Aus der Ordnung der Mallophagida und den Unterordnungen Amblycerina sowie Ischnocerina z.B. Trimenopon spp., Menopon spp., Trinoton spp., Bovicola spp., Werneckiella spp., Lepikentron spp., Damalina spp., Trichodectes spp., Felicola spp..
Aus der Ordnung Diptera und den Unterordnungen Nematocerina sowie Brachycerina z.B. Aedes spp., Anopheles spp., Culex spp., Simulium spp., Eusimulium spp., Phlebotomus spp., Lutzomyia spp., Culicoides spp., Chrysops spp., Hybomitra spp., Atylotus spp., Tabanus spp., Haematopota spp., Philipomyia spp., Braula spp., Musca spp., Hydrotaea spp., Stomoxys spp., Haematobia spp., Morellia spp., Fannia spp., Glossina spp., Calliphora spp., Lucilia spp., Chrysomyia spp., Wohlfahrtia spp., Sarcophaga spp., Oestrus spp., Hypoderma spp., Gasterophilus spp., Hippobosca spp., Lipoptena spp., Melophagus spp..
Aus der Ordnung der Siphonapterida z.B. Pulex spp., Ctenocephalides spp., Xenopsylla spp., Ceratophyllus spp..
Aus der Ordnung der Heteropterida z.B. Cimex spp., Triatoma spp., Rhodnius spp., Panstrongylus spp..
Aus der Ordnung der Blattarida z.B. Blatta orientalis, Periplaneta americana, Blattela germanica, Supella spp..
Aus der Unterklasse der Acari (Acarina) und den Ordnungen der Meta- sowie Mesostigmata z.B. Argas spp., Ornithodorus spp., Otobius spp., Ixodes spp., Amblyomma spp., Boophilus spp., Dermacentor spp., Haemophysalis spp., Hyalomma spp., Rhipicephalus spp., Dermanyssus spp., Raillietia spp., Pneumonyssus spp., Sternostoma spp., Varroa spp..
Aus der Ordnung der Actinedida (Prostigmata) und Acaridida (Astigmata) z.B. Acarapis spp., Cheyletiella spp., Ornithocheyletia spp., Myobia spp., Psorergates spp., Demodex spp., Trombicula
spp., Listrophorus spp., Acarus spp., Tyrophagus spp., Caloglyphus spp., Hypodectes spp., Pterolichus spp., Psoroptes spp., Chorioptes spp., Otodectes spp., Sarcoptes spp., Notoedres spp., Knemidocoptes spp., Cytodites spp., Laminosioptes spp..
Die erfindungsgemäßen Wirkstoffe der Formel (I) eignen sich auch zur Bekämpfung von Arthropoden, die landwirtschaftliche Nutztiere, wie z.B. Rinder, Schafe, Ziegen, Pferde, Schweine,
Esel, Kamele, Büffel, Kaninchen, Hühner, Puten, Enten, Gänse, Bienen, sonstige Haustiere wie z.B. Hunde, Katzen, Stubenvögel, Aquarienfische sowie sogenannte Versuchstiere, wie z.B.
Hamster, Meerschweinchen, Ratten und Mäuse befallen. Durch die Bekämpfung dieser
Arthropoden sollen Todesfälle und Leistungsminderungen (bei Fleisch, Milch, Wolle, Häuten, Eiern, Honig usw.) vermindert werden, so daß durch den Einsatz der erfindungsgemäßen
Wirkstoffe eine wirtschaftlichere und einfachere Tierhaltung möglich ist.
Die Anwendung der erfindungsgemäßen Wirkstoffe geschieht im Veterinärsektor und bei der Tierhaltung in bekannter Weise durch enterale Verabreichung in Form von beispielsweise Tabletten, Kapseln, Tränken, Drenchen, Granulaten, Pasten, BoIi, des feed-through- Verfahrens, von Zäpfchen, durch parenterale Verabreichung, wie zum Beispiel durch Injektionen (intramuskulär, subcutan, intravenös, intraperitonal u.a.), Implantate, durch nasale Applikation, durch dermale Anwendung in Form beispielsweise des Tauchens oder Badens (Dippen), Sprühens (Spray), Aufgießens (Pour-on und Spot-on), des Waschens, des Einpuderns sowie mit Hilfe von wirkstoffhaltigen Formkörpern, wie Halsbändern, Ohrmarken, Schwanzmarken, Gliedmaßenbändern, Halftern, Markierungsvorrichtungen usw.
Bei der Anwendung für Vieh, Geflügel, Haustiere etc. kann man die Wirkstoffe der Formel (I) als Formulierungen (beispielsweise Pulver, Emulsionen, fließfähige Mittel), die die Wirkstoffe in einer Menge von 1 bis 80 Gew.-% enthalten, direkt oder nach 100 bis 10 000-facher Verdünnung anwenden oder sie als chemisches Bad verwenden.
Außerdem wurde gefunden, daß die erfindungsgemäßen Verbindungen eine hohe insektizide Wirkung gegen Insekten zeigen, die technische Materialien zerstören.
Beispielhaft und vorzugsweise - ohne jedoch zu limitieren - seien die folgenden Insekten genannt:
Käfer wie Hylotrupes bajulus, Chlorophorus pilosis, Anobium punetatum, Xestobium rufovillosum, Ptilinus pecticornis, Dendrobium pertinex, Ernobius mollis, Priobium carpini, Lyctus brunneus, Lyctus africanus, Lyctus planicollis, Lyctus linearis, Lyctus pubescens, Trogoxylon aequale, Minthes rugicollis, Xyleborus spec. Tryptodendron spec. Apate monachus, Bostrychus capucins, Heterobostrychus brunneus, Sinoxylon spec. Dinoderus minutus;
Hautflügler wie Sirex juvencus, Urocerus gigas, Urocerus gigas taignus, Urocerus augur;
Termiten wie Kalotermes flavicollis, Cryptotermes brevis, Heterotermes indicola, Reticulitermes flavipes, Reticulitermes santonensis, Reticulitermes lucifiigus, Mastotermes darwiniensis, Zootermopsis nevadensis, Coptotermes formosanus;
Borstenschwänze wie Lepisma saccharina.
Unter technischen Materialien sind im vorliegenden Zusammenhang nicht-lebende Materialien zu verstehen, wie vorzugsweise Kunststoffe, Klebstoffe, Leime, Papiere und Kartone, Leder, Holz, Holzverarbeitungsprodukte und Anstrichmittel.
Die anwendungsfertigen Mittel können gegebenenfalls noch weitere Insektizide und ge- gebenenfalls noch ein oder mehrere Fungizide enthalten.
Zugleich können die erfindungsgemäßen Verbindungen zum Schutz vor Bewuchs von Gegenständen, insbesondere von Schiffskörpern, Sieben, Netzen, Bauwerken, Kaianlagen und Signalanlagen, welche mit See- oder Brackwasser in Verbindung kommen, eingesetzt werden.
Weiter können die erfindungsgemäßen Verbindungen allein oder in Kombinationen mit anderen Wirkstoffen als Antifouling-Mittel eingesetzt werden.
Die Wirkstoffe eignen sich auch zur Bekämpfung von tierischen Schädlingen im Haushalts-, Hygiene- und Vorratsschutz, insbesondere von Insekten, Spinnentieren und Milben, die in geschlossenen Räumen, wie beispielsweise Wohnungen, Fabrikhallen, Büros, Fahrzeugkabinen u.a. vorkommen. Sie können zur Bekämpfung dieser Schädlinge allein oder in Kombination mit anderen Wirk- und Hilfsstoffen in Haushaltsinsektizid-Produkten verwendet werden. Sie sind gegen sensible und resistente Arten sowie gegen alle Entwicklungsstadien wirksam. Zu diesen Schädlingen gehören:
Aus der Ordnung der Scorpionidea z.B. Buthus occitanus.
Aus der Ordnung der Acarina z.B. Argas persicus, Argas reflexus, Bryobia ssp., Dermanyssus gallinae, Glyciphagus domesticus, Ornithodorus moubat, Rhipicephalus sanguineus, Trombicula alfreddugesi, Neutrombicula autumnalis, Dermatophagoides pteronissimus, Dermatophagoides forinae.
Aus der Ordnung der Araneae z.B. Aviculariidae, Araneidae.
Aus der Ordnung der Opiliones z.B. Pseudoscorpiones chelifer, Pseudoscorpiones cheiridium, Opiliones phalangium.
Aus der Ordnung der Isopoda z.B. Oniscus asellus, Porcellio scaber.
Aus der Ordnung der Diplopoda z.B. Blaniulus guttulatus, Polydesmus spp..
Aus der Ordnung der Chilopoda z.B. Geophilus spp..
Aus der Ordnung der Zygentoma z.B. Ctenolepisma spp., Lepisma saccharina, Lepismodes inquilinus.
Aus der Ordnung der Blattaria z.B. Blatta orientalies, Blattella germanica, Blattella asahinai, Leucophaea maderae, Panchlora spp., Parcoblatta spp., Periplaneta australasiae, Periplaneta americana, Periplaneta brunnea, Periplaneta fuliginosa, Supella longipalpa.
Aus der Ordnung der Saltatoria z.B. Acheta domesticus.
Aus der Ordnung der Dermaptera z.B. Forficula auricularia.
Aus der Ordnung der Isoptera z.B. Kalotermes spp., Reticulitermes spp.
Aus der Ordnung der Psocoptera z.B. Lepinatus spp., Liposcelis spp.
Aus der Ordnung der Coleoptera z.B. Anthrenus spp., Attagenus spp., Dermestes spp., Latheticus oryzae, Necrobia spp., Ptinus spp., Rhizopertha dominica, Sitophilus granarius, Sitophilus oryzae, Sitophilus zeamais, Stegobium paniceum.
Aus der Ordnung der Diptera z.B. Aedes aegypti, Aedes albopictus, Aedes taeniorhynchus, Anopheles spp., Calliphora erythrocephala, Chrysozona pluvialis, Culex quinquefasciatus, Culex pipiens, Culex tarsalis, Drosophila spp., Fannia canicularis, Musca domestica, Phlebotomus spp., Sarcophaga carnaria, Simulium spp., Stomoxys calcitrans, Tipula paludosa.
Aus der Ordnung der Lepidoptera z.B. Achroia grisella, Galleria mellonella, Plodia interpunctella, Tinea cloacella, Tinea pellionella, Tineola bisselliella.
Aus der Ordnung der Siphonaptera z.B. Ctenocephalides canis, Ctenocephalides felis, Pulex irritans, Tunga penetrans, Xenopsylla cheopis.
Aus der Ordnung der Hymenoptera z.B. Camponotus herculeanus, Lasius fuliginosus, Lasius niger, Lasius umbratus, Monomorium pharaonis, Paravespula spp., Tetramorium caespitum.
Aus der Ordnung der Anoplura z.B. Pediculus humanus capitis, Pediculus humanus coφoris, Pemphigus spp., Phylloera vastatrix, Phthirus pubis.
Aus der Ordnung der Heteroptera z.B. Cimex hemipterus, Cimex lectularius, Rhodinus prolixus, Triatoma infestans.
Die Anwendung im Bereich der Haushaltsinsektizide erfolgt allein oder in Kombination mit anderen geeigneten Wirkstoffen wie Phosphorsäureestern, Carbamaten, Pyrethroiden, Neo- nicotinoiden, Wachstumsregulatoren oder Wirkstoffen aus anderen bekannten Insektizidklassen.
Die Anwendung erfolgt in Aerosolen, drucklosen Sprühmitteln, z.B. Pump- und Zerstäubersprays, Nebelautomaten, Foggern, Schäumen, Gelen, Verdampferprodukten mit Verdampferplättchen aus Cellulose oder Kunststoff, Flüssigverdampfern, Gel- und Membranverdampfern, propellergetriebenen Verdampfern, energielosen bzw. passiven Verdampfungssystemen, Mottenpapieren, Mottensäckchen und Mottengelen, als Granulate oder Stäube, in Streuködern oder Köderstationen.
Erläuterung der Verfahren und Zwischenprodukte
Die folgenden Herstellungs- und Verwendungsbeispiele illustrieren die Erfindung, ohne sie zu beschränken.
Verwendet man beispielsweise 4-Methoxy-l,2-benzisothiazol-3-amino-l,l-dioxid und Chlorameisensaeure-methylester als Ausgangsstoffe, so kann der Verlauf des erfindungsgemäßen Verfahrens der ersten Ausführungsform durch das folgende Formelschema veranschaulicht werden:
3-Amino-l,2-Benzisothiazole der Formel (II) sind bekannt, oder können nach allgemeinen Synthesemethoden hergestellt werden. Die EP0138762 beschreibt beispielsweise die Synthese von 3-Amino-4-chlor-l,2-benzisothiazol [CAS-RN 25380-80-7]. Die EP 33984 beschreibt die Synthese von 4-Chlor-3-amino-, 4-Fluor-3-amino- und 4-Methyl-3-amino-l,2-benzisothiazol-l,l-dioxid aus den entsprechenden 2-Cyano-benzolsulfonsäurechloriden. Die Herstellung aromatischer 2-Cyano- benzolsulfonsäurehalogenide ist in der DE 860051 beschrieben.
In der DE 3015113 werden 3-Amino-l,2-benzisothiazol-l,l-dioxide der allgemeinen Formel (H) als Zwischenprodukte beschrieben.
Die 3-Amino-l,2-benzisothiazole der Formel (II) sind auch teilweise kommerziell erhältlich, z.B. 3- Amino-l,2-benzisothiazol [CAS-RN 23031-78-9] oder das 3-Amino-5-nitro-benzisothiazol [CAS- RN 84387-89-3].
Ein allgemeines Verfahren zur Synthese von N-substituierten 3-Amino-l,2-benzisothiazolen der Formel (II) ist beschrieben in J. Org. Chem. 25, 413-16 (1960).
Die EP 105732 beschreibt N-substituierte 3-Amino-l,2-benzisotbiazol-l,l-dioxide als Arzneimittel.
Verwendet man beispielsweise 4-Methyl-l,2-benzisothiazol-3-amino-l,l-dioxid und Di-tert- butyldicarbonat als Ausgangsstoffe, so kann der Verlauf des erfmdungsgemäßen Verfahrens der ersten Ausführungsform auch durch das folgende Formelschema veranschaulicht werden:
Verwendet man beispielsweise Dimethyl-(l,2-benzisothiazol-3-yl)imidodicarbonat und Wasserstoffperoxid als Ausgangsstoffe, so kann der Verlauf des erfϊndungsgemäßen Verfahrens der zweiten Ausführungsform durch das folgende Formelschema veranschaulicht werden:
In der DE 3544436 wird die Oxidation der 3-Amino-l,2-benzisothiazole der allgemeinen Formel (H) mit 3-Chlor-perbenzoesäure beschrieben.
Verwendet man beispielsweise Dimethyl-(l,l-dioxido-l,2-benzisothiazol-3-yl)imidodicarbonat und ein basisches oder saures Spaltungsreagens, so kann der Verlauf des erfindungsgemäßen Verfahrens der dritten Ausführungsform durch das folgende Formelschema veranschaulicht werden:
Herstellung von Ausgangsverbindungen der Formel I
1. Herstellung von 4-(2-Methoxyethoxy)-l,2-benzisothiazol-3-amin-l,l-dioxid
Stufe IA : Herstellune von 2-Arnino-6-(2-methoxyethoxy)-benzonitril
Zu einer Lösung von 3.2 g (23.5 mmol) 2-Amino-6-fluorbenzonitril in 10 ml trockenem DMF werden 25 g (51 mmol) einer 20 % igen Lösung von Natrium-2-methoxyethanolat in Methoxyethanol gegeben und 16 Stunden unter Rückfluss erhitzt. Nach dem Abkühlen wird mit 0.5 ml Wasser versetzt und im Vakuum eingeengt. Man nimmt in Essigsäureethylester und Wasser auf. Die wässrige Phase wird mit Essigsäureethylester nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Es verbleiben 4 g Produkt mit einem Gehalt (NMR) > 95 %. Theoretische Ausbeute 84.1 %.
δ ([D6J-DMSO) = 3.33 (s, 3H); 3.65-3.67 (t, 2H); 4.12-4.15 (t, 2H); 5.76 (br. s, 2H); 6.22-6.24 (m, IH); 6.36-6.38 (m, IH); 7.15-7.19 (m, IH) ppm.
Stufe IB : Herstellung von 2-Amino-6-(2-methoxyethoxyVbenzolsulfonsäurecrilorid
70 ml Essigsäure werden auf 100C abgekühlt und unter Kühlung mit SO2 gesättigt. Nach weiterem Abkühlen auf 00C erfolgt die Zugabe von 1.4 g (8.2 mmol) Kupfer(II)chlorid-dihydrat, gelöst in 10 ml Wasser. Anschließend wird noch 15 Minuten nachgerührt. Danach wird zu dieser Lösung eine weitere Lösung [Herstellung: 4.0 g (20.8 mmol) 2-Amino-6-(2-methoxyethoxy)-benzonitril und 40 ml Essigsäure und 9 ml konzentrierte Salzsäure bei 0 bis 2°C vorlegen, 1.8 g (26.1 mmol) NaNÜ2,
gelöst in 10 ml Wasser, langsam zutropfen und weitere 30 Minuten bei 00C nachrühren] bei 00C schnell zugetropft. Nach langsamer Erwärmung auf Raumtemperatur wird 18 Stunden bei Raumtemperatur gerührt. Der Ansatz wird auf 500 ml Eiswasser gegeben und der entstandene hellbraune Feststoff wird abgesaugt und mit kaltem Wasser nachgewaschen. Es verbleiben 3.5 g Rohprodukt, das direkt weiter umgesetzt wird. Theoretische Ausbeute 61 %.
Stufe IC : Herstellung von 4-(2-Methoxyethoxy)-L2-berizisothiazol-3-amin-l.l-dioxid
0.55 g (2 mmol) 2-Amino-6-(2-methoxyethoxy)-benzolsulfonsäurechlorid werden in 20 ml 25 % ige Ammoniak-Lösung eingetragen und zunächst 1 Stunde bei Raumtemperatur und dann noch 18 Stunden bei 450C gerührt. Die wässrige Phase wird mit Dichlormethan versetzt, wobei ein beiger Feststoff ausfällt. Dieser wird abgesaugt und getrocknet. Man erhält 150 mg 4-(2- Methoxyethoxy)-l,2-benzisothiazol-3-amin-l,l-dioxid , Reinheitsgehalt (LC/MS) 93.9 %, Ausbeute: 29.4 % d. Theorie.
δ ([D6]-DMSO) = 3.33 (s, 3H); 3.76-3.78 (t, 2H); 4.42-4.44 (m, 2H); 7.46-7.49 (m, 2H); 7.75-7.80 (m, IH); 8.90 (br. s, 2H) ppm.
2. Herstellung von 4-( Prop-2-en-l-yloxy)-l^-benzisothiazol-3-amin-l,l-dioxid
Stufe 2A : Herstellung von 2-Amino-6-(prop-2-en-l-yloxy)-benzonitril
2.3 g Natrium-Späne (100 mmol) werden portionsweise zu 25.0 g (430 mmol) Allylalkohol gegeben und bis zur vollständigen Auflösung gerührt. Diese Lösung wird aus einem Tropftrichter zu einer Lösung von 7.5 g (55.1 mmol) 2-Amino-6-fluorbenzonitril in 20 ml trockenem DMF zugetropft und 16 Stunden unter Rückfluss erhitzt. Nach dem Abkühlen wird mit 0.5 ml Wasser versetzt und im Vakuum eingeengt. Man nimmt in Dichlormethan und Wasser auf. Die wässrige Phase wird mit Dichlormethan nachextrahiert, die vereinigten organischen Phasen werden über Magnesiumsulfat getrocknet und i. Vak. eingeengt. Es verbleiben 8.4 g Produkt mit einem Gehalt von 75 % (GC/MS) das direkt weiter umgesetzt wird. Theoretische Ausbeute 65.6 %.
Stufe 2B : Herstellung von 2-Amino-6-(prop-2-en-l-yloxy)-benzolsulfonsäurechlorid
140 ml Essigsäure werden auf 100C abgekühlt und unter Kühlung mit SO2 gesättigt. Nach weiterem Abkühlen auf 00C erfolgt die Zugabe von 3.32 g (19.5 mmol) Kupfer(II)chlorid-dihydrat, gelöst in 14 ml Wasser. Anschließend wird noch 15 Minuten nachgerührt. Danach wird zu dieser Lösung eine weitere Lösung [Herstellung: 8.9 g (51.1 mmol) 2-Amino-6-(prop-2-en-l-yloxy)- benzonitril und 65 ml Essigsäure und 20 ml konzentrierte Salzsäure bei 0 bis 2°C vorlegen, 4.15 g (60.1 mmol) NaNO2, gelöst in 13 ml Wasser, langsam zutropfen und weitere 30 Minuten bei 00C nachrühren] bei 00C schnell zugetropft. Nach langsamer Erwärmung auf Raumtemperatur wird 18 Stunden bei Raumtemperatur gerührt. Der Ansatz wird auf 750 ml Eiswasser gegeben und der entstandene hellbraune Feststoff wird abgesaugt und mit kaltem Wasser nachgewaschen. Es verbleiben 5.5 g Rohprodukt, das direkt weiter umgesetzt wird. Theoretische Ausbeute 55.7 %.
Stufe 2C : Herstellung von 4-fProp-2-en-l-yloxy)-l,2-benzisothiazol-3-amin-l.l-dioxid
0.5 g (1.94 mmol) 2-Amino-6-(prop-2-en-l-yloxy)sulfonsäurechlorid werden in 40 ml 25 % ige Ammoniak-Lösung eingetragen und zunächst 2 Stunden bei 400C und dann noch 18 Stunden bei Raumtemperatur und nochmals 1 Stunde bei 400C gerührt. Die wässrige Phase wird mit DCM aufgerührt, wobei ein brauner Feststoff ausfällt. Dieser wird abgesaugt. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden über MgSO4 getrocknet und i. Vak. eingeengt. Das Rohprodukt wird durch präparative HPLC gereinigt (Kromasil 100 C 18,Gradient mit Acetonitril [enthält 0.01 % Ameisensäure] / Wasser = 30 : 70. Es verbleiben 0.26 g Feststoff vom Reinheitsgehalt (LC/MS) 100 %, Ausbeute: 56.3 % d. Theorie.
δ ([D6J-DMSO) = 4.90-4.92 (m, 2H); 5.31-5.34 (m, IH); 5.39-5.44 (m, IH); 6.07-6.16 (m, IH); 7.40-7.45 (m, 2H); 7.57 (br. s, IH); 7.73-7.77 (m, IH); 8.97 (br. s, IH) ppm.
Beispiel 1
Herstellung von Ethyl-f4-(2-methoxyethoxy)-l,l-dioxido-l,2-benzisothia2ol-3-yllcarbamat (I- n
150 mg (0.59 mmol) 4-(2-Methoxyethoxy)-l,2-benzisothiazol-3-amin-l,l-dioxid werden in 35 ml absolutem Tetrahydrofuran vorgelegt und mit 60 mg (1.5 mmol) 60 % igem Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 110 mg (1.01 mmol) Ethylchlorocarbonat in 3 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden über MgSO4 getrocknet und i. Vak. eingeengt. Es verbleiben 80 mg Ethyl-[4-(2-methoxyethoxy)-l,l-dioxido-l,2-benzisothiazol-3- yljcarbamat (1-1), Gehalt (LC/MS): 89 %, Ausbeute: 37.1 % der Theorie.
Beispiel 2
Herstellung von Ethyl-(l,l-dioxido-1.2-benzisothiazol-3-yl)carbamat (1-2)
Man legt 300 mg (2.0 mmol) l,2-Benzisothiazol-3-amin-l,l-dioxid in 25 ml trockenem Tetrahydrofuran vor und gibt portionsweise 130 mg (3.25 mmol) 60 % iges Natriumhydrid dazu. Es wird 2 h bei 500C gerührt, auf Raumtemperatur abgekühlt und anschließend langsam 0.24 g (2 mmol) Chlorameisensäureethylester, gelöst in 5 ml trockenem Tetrahydrofliran, dazugegeben. Danach rührt man weitere 18h bei Rückfluss. Nach dem Abkühlen wird das Lösungsmittel i. Vak. entfernt. Das Rohprodukt wird durch präparative HPLC gereinigt (Kromasil 100 C 18,Gradient mit Acetonitril [enthält 0.01 % Ameisensäure] / Wasser = 40 : 60. Es verbleiben 0.06 g Ethyl-(1,1- dioxido-l,2-benzisothiazol-3-yl)carbamat (1-2) als weißer Feststoff vom Reinheitsgehalt (LC/MS) 100 %, Ausbeute: 14.3 % d. Theorie.
Beispiel 3
Methyl-(4-cMor-l,l-dioxido-l,2-benzisothiazol-3-vDcarbamat (1-3)
216.6 mg (1.0 mmol) 4-Chlor-l,2-benzisothiazol-3-amin-l,l-dioxid werden in 20 ml absolutem Tetrahydrofuran vorgelegt und mit 60 mg (1.5 mmol) 60 % igem Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 103.9 mg (1.1 mmol) Methylchlorocarbonat in 3 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Der Rückstand wird mit Diisopropylether verrieben, der ausgefallene Niederschlag abgesaugt (270 mg). Nach Kieselgelchromatographie Dichlormethan /Methanol = 99.5:0.5) erhält man 170 mg Methyl-(4-chlor-l,l-dioxido-l,2-benzisothiazol-3- yl)carbamat vom Reinheitsgehalt (HPLC) 99.9 %, Ausbeute: 61.7 % d. Theorie.
Beispiel 4
l-MethvIethyl-(4-fluor-U-dioxido-1.2-benzisothiazol-3-yl)carbainat (I-4)
200.2 mg (1.0 mmol) 4-Fluor-l,2-benzisothiazol-3-amin-l,l-dioxid werden in 20 ml absolutem Tetrahydrofuran vorgelegt und mit 60 mg (1.5 mmol) Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 134.8 mg (1.1 mmol) 1- Methylethylchlorocarbonat in 3 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Der Rückstand wird mit Diisopropylether verrieben, der ausgefallene Niederschlag abgesaugt (290 mg). Nach Kieselgelchromatographie (Dichlormethan/Methanol = 99.5:0.5) erhält man 190 mg l-Methylethyl-(4-fluor-l,l-dioxido-l,2- benzisothiazol-3-yl)carbamat vom Reinheitsgehalt (HPLC) 97.6 %, Ausbeute: 64.8 % d. Theorie.
Beispiel 5
S-Methyl-(l,l-dioxido-l,2-beiizisothiazol-3-yl)thiocarbamat (1-5)
273.3 mg (1.5 mmol) l,2-Benzisothiazol-3-amin-l,l-dioxid werden in 20 ml absolutem Tetrahydrofuran vorgelegt und mit 123 mg (3.07 mmol) Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 248.8 mg (2.25 mmol) S-
Methylchlorothiocarbonat in 3 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in
Dichlormethan und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Der ausgefallene Niederschlag wird abgesaugt und getrocknet. Man erhält 270 mg S-Methyl-(l,l-dioxido-l,2- benzisothiazol-3-yl)thiocarbamat vom Reinheitsgehalt (HPLC) 100 %, Ausbeute: 70.2 % d.
Theorie.
Beispiel 6
Phenyl-(4-methoxy-l,l-dioxido-l,2-benzisothiazol-3-yl)carbamat (1-6)
212.2 mg (1.0 mmol) 4-Methoxy-l,2-benzisothiazol-3-amin-l,l-dioxid werden in 12 ml absolutem Tetrahydrofuran vorgelegt und mit 82 mg (2.05 mmol) Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 234.8 mg (1.5 mmol) Phenylchlorocarbonat in 2.5 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Die wässrige Phase wird mit Dichlormethan nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Der Rückstand wird mit Cyclohexan/Essigsäureethylester = 3:1 an Kieselgel chromatographiert. Man erhält 60 mg Phenyl-(4-methoxy-l,l-dioxido-l,2- benzisothiazol-3-yl)carbamat vom Reinheitsgehalt (HPLC) 96.9 %, Ausbeute: 17.5 % d. Theorie.
Beispiel 7
Diphenvl-(4-methoxv-l,l-dioxido-1.2-benzisothiazol-3-vlMmidodicarbonat (1-7)
212.2 mg (1.0 mmol) 4-Methoxy-l,2-benzisothiazol-3-amin-l,l-dioxid werden in 12 ml absolutem Tetrahydrofuran vorgelegt und mit 82 mg (2.05 mmol) Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 234.8 mg (1.5 mmol) Phenylchlorocarbonat in 2.5 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Der Rückstand wird mit Cyclohexan/Essigsäureethylester = 3:1 an Kieselgel chromatographiert. Man erhält 60 mg Diphenyl-(4-methoxy-l,l-dioxido-l,2- benzisothiazol-3-yl)imidodicarbonat vom Reinheitsgehalt (HPLC) 91.2 %, Ausbeute: 16.1 % d. Theorie.
Beispiel 8
Methyl (4-chlor-l,2-benzisothiazol-3-yl)carbamat (1-8)
184.6 mg (1.0 mmol) 4-Chlor-l,2-benzisothiazol-3-amin werden in 20 ml absolutem Tetrahydrofuran vorgelegt und mit 60 mg (1.5 mmol) Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 103.9 mg (1.1 mmol) Methylchlorocarbonat in 3 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Der Rückstand wird an Kieselgel chromatographiert, zuerst mit DCM/Methanol = 99.5:0.5, anschließend mit DCM/Essigsäureethylester = 40:1. Man erhält 70 mg Methyl (4-chlor-l,2-benzisothiazol-3-yl)carbamat vom Reinheitsgehalt (HPLC) 97.7 %, Ausbeute: 28.2 % d. Theorie.
Beispiel 9
S-Methyl-(4-chlor-1.2-benzisothiazol-3-vπthiocarbamat (1-9)
184.6 mg (1.0 mmol) 4-Chlor-l,2-benzisothiazol-3-amin werden in 20 ml absolutem Tetrahydrofuran vorgelegt und mit 60 mg (1.5 mmol) Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 121.6 mg (1.1 mmol) S- Methylchlorothiocarbonat in 3 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Der Rückstand wird mit DCM an Kieselgel chromatographiert. Man erhält 70 mg S-Methyl-(4-chlor-l,2-benzisothiazol-3-yl)thiocarbamat vom Reinheitsgehalt (HPLC) 89.7 %, Ausbeute: 24.3 % d. Theorie.
Beispiel 10
Bis(l-methylethylM4-chlor-l,2-benzisothia2θl-3-yl)imidodicarbonat (1-10)
184.6 mg (1.0 mmol) 4-Chlor-l,2-benzisothiazol-3-amin werden in 20 ml absolutem Tetrahydrofuran vorgelegt und mit 60 mg (1.5 mmol) Natriumhydrid versetzt. Nach 2 Stunden bei 50 0C wird auf 20 0C abgekühlt. Unter Rühren wird eine Lösung aus 134.8 mg (1.1 mmol) 1- Methylethylchlorocarbonat in 3 ml absolutem Tetrahydrofuran zugetropft. Man erhitzt 16 Stunden unter Rückfluss, kühlt ab, versetzt mit 0.5 ml Wasser und engt im Vakuum ein. Man nimmt in Dichlormethan (DCM) und Wasser auf und säuert mit halbkonzentrierter Salzsäure an. Die wässrige Phase wird mit DCM nachextrahiert, die vereinigten organischen Phasen werden getrocknet und i. Vak. eingeengt. Der Rückstand wird an Kieselgel chromatographiert, erst DCM/Methanol = 99.5:0.5, anschließend Cyclohexan/Essigsäureethylester = 5:1. Man erhält 150 mg Bis(l-methylethyl)-(4-chlor-l,2-benzisothiazol-3-yl)imidodicarbonat vom Reinheitsgehalt (HPLC) 93.0 %, Ausbeute: 39.1 % d. Theorie.
Beispiel 11
Diethyl-^-chlor-lJ-dioxido-l^-benzisothiazol-S-vOimidodicarbonat (1-11)
100 mg (0.304 mmol) Diethyl-(4-chlor-l,2-benzisothiazol-3-yl)imidodicarbonat werden zusammen mit 149 mg (3.242 mmol) Ameisensäure und 50 mg Ammoniummolybdat in 10 ml Dichlormethan (DCM) vorgelegt. Bei Raumtemperatur werden 443.3 mg (4.562 mmol) 35 %iges Wasserstoffperoxid zugetropft. Nach 4 Tagen Rühren wird auf Eiswasser gegossen, das überschüssige Peroxid durch Na-bisulfit-Lösung zerstört. Die organische Phase wird abgetrennt, getrocknet und i. Vak. eingeengt. Der Rückstand wird an Kieselgel mit Dichlormethan /Methanol = 99:1 chromatographiert. Man erhält 10 mg Diethyl-(4-chlor-l,l-dioxido-l,2-benzisothiazol-3- yl)imidodicarbonat vom Reinheitsgehalt (HPLC) 88.8 %, Ausbeute: 8.1 % d. Theorie.
Die in der Tabelle 1 beschriebenen Verbindungen der allgemeinen Formel (I) erhält man gemäß oder analog zu den oben beschriebenen Synthesebeispielen:
wobei die Reste R1 bis R4, n, A, X,Y und Z die in der Tabelle 1 angegebenen Bedeutungen aufweisen
Tabelle 1 :
M:
δ ([D6J-DMSO) = 1.31 (t, 3H); 3.39 (s, 3H); 3.75-3.77 (m, 2H); 4.27-4.32 (q, 2H); 4.46-4.48 (m, 2H); 7.56-7.58 (m, IH); 7.64-7.66 (m, IH); 7.84-7.88 (m, IH); 9.54 (br. s,l H) ppm.
1-2:
δ ([D6]-DMSO) = 1.33 (t, 3H); 4.27-4.33 (q, 2H); 7.80-8.44 (m, 4H); 8.73 (br. s, IH) ppm.
1-3:
δ (CD3CN) = 3.89 (s, 3H); 7.76-7.83 (m, 2H); 7.93 (dd, IH); 9.1 (br. s, IH) ppm.
1-4:
δ (CD3CN) = 1.35 (d, 6H); 5.08 (m, IH); 7.49-7.54 (m, IH); 7.79-7.80 (d, IH); 7.85-7.90 (m, IH); 8.21 (br. s, IH) ppm.
1-5:
δ ([D6]-DMSO) = 2.38 (s, 3H); 7.83-7.90 (m, 2H); 8.06 (m, IH); 8.43 (m, IH) ppm.
1-6:
δ (CD3CN) = 4.13 (s, 3H); 7.26-7.36 (m, 3H); 7.42-7.49 (m, 3H); 7.55 (dd,lH); 7.84 (dd, IH); 9.53 (br. s, IH) ppm.
1-7:
δ (CD3CN) = 4.06 (s, 3H); 7.17-7.20 (m, 4H); 7.30-7.36 (m, 2H); 7.42-7.49 (m, 5H); 7.63 (dd, IH); 7.90 (dd, IH) ppm.
1-8:
δ (CD3CN) = 3.76 (s, 3H); 7.46-7.53 (m, 2H); 7.94 (dd, IH); 8.2 (br. s, IH) ppm.
1-9:
δ ([Dg]-DMSO) = 2.30 (s, 3H); 7.57-7.63 (m, 2H); 8.21 (dd, IH); 10.76 (s, IH) ppm.
1-10:
δ (CD3CN) =1.10 (d, 6H); 1.13 (d, 6H); 4.99 (m, 2H); 7.51-7.58 (m, 2H); 8.01 (dd, IH) ppm.
Ml:
δ (CD3CN) = 1.17 (t, 6H); 4.28 (q, 4H); 7.84 (d, IH); 7.88 (t, IH); 8.05 (d, IH) ppm.
1-12:
δ ([D6]-DMSO) = 1.31 (t, 3 H); 4.09 (s, 3 H); 4.26-4.32 (q, 2 H); 7.53-7.55 (m, 1 H); 7.61-7.63 (m, 1 H); 7.85-7.89 (m, 1 H); 9.33 (s,l H) ppm.
1-13:
δ ([De]-DMSO) = 1.31 (t, 3 H); 2.68 (s, 3 H); 4.25-4.30 (q, 2 H); 7.77-7.94 (m, 4 H) ppm.
1-14:
δ ([D6I-DMSO) = 1.30 (t, 3 H); 3.60 (s, 3 H); 4.25-4.30 (q, 2 H); 8.11-8.17 (m, 1 H); 8.33-8.47 (m, 3 H) ppm.
1-15:
δ ([D6J-DMSO) = 1.16 (t, 3 H); 4.23-4.28 (q, 2 H); 4.80-4.82 (m, 2 H); 5.33-5.41 (m, 2 H); 5.97 (m, 1 H); 7.54-7.56 (m, 1 H); 7.74-7.76 (m, 1 H); 7.89-7.93 (m, 1 H) ppm.
1-16:
δ ([D6]-DMSO) = 2.59 (s, 3 H); 3.81 (s, 3 H); 7.68-7.82 (m, 3 H); 9.82 (br. s, 1 H) ppm.
1-17:
δ ([D6I-DMSO) = 3.84 (s, 3 H); 4.09 (s, 3 H); 7.53-7.56 (m,l H); 7.62-7.64 (m, 1 H); 7.85-7.89 (m, 1 H); 9.38 (br. s, 1 H) ppm.
1-18:
δ ([D6]-DMSO) = 3.84 (s, 3 H); 7.82-7.90 (m, 2 H); 8.04-8.06 (m, 1 H); 8.42-8.44 (m, 1 H); 11.50 (br. s, 1 H) ppm.
1-19:
δ (CD3CN) = 1.10 (t, 6H); 4.19 (m, 4H); 7.51-7.59 (m, 2H); 8.01 (dd, IH) ppm.
1-20:
δ (CD3CN) = 1.35 (d, 6H); 5.09 (m, IH); 7.75-7.82 (m, 2H); 7.93 (dd, IH); 9.04 (br. s, IK) ppm.
1-21:
δ (CD3CN) = 1.35 (t, 3H); 4.34 (q, 2H); 7.75-7.83 (m, 2H); 7.93 (dd, IH); 9.08 (br. s, IH) ppm.
1-22:
δ (CD3CN) = 1.34 (t, 3H); 4.34 (q, 2H); 7.50-7.55 (m, IH); 7.79-7.81 (m, IH); 7.85-7.91 (m, IH); 8.26 (br. s, IH) ppm.
1-23:
δ (CD3CN) = 3.87 (s, 3H); 7.53-7.58 (m, IH); 7.82-7.84 (m, IH); 7.87-7.93 (m, IH); 8.38 (br. s, IH) ppm.
1-24:
δ ([De]-DMSO) = 2.38 (s, 3H); 7.64-7.69 (m, IH); 7.89-7.96 (m, 2H); 9.05 (br. s, IH) ppm.
1-25:
δ ([D6I-DMSO) = 2.40 (s, 3H); 4.08 (s, 3H); 7.52 (d, IH); 7.61 (d, IH); 7.86 (dd, IH); ~ 10 (br., IH) ppm.
1-26:
δ ([D6]-DMSO) = 2.39 (s, 3H); 7.82-7.88 (m, 2H); 8.02-8.06 (m, IH); 9.25 (br., IH) ppm.
1-27:
δ (CD3CN) = 3.71 (s, 6H); 7.55-7.62 (m, 2H); 8.04-8.06 (m, IH) ppm.
1-28:
δ ([D6J-DMSO) = 1.86 (t, 3H); 4.80 (q, 2H); 8.07-8.14 (m, 2H); 8.55 (dd, IH); 8.85 (br. s, IH) ppm.
1-29:
δ (CD3CN) = 1.28 (d, 6H); 4.98 (m, IH); 7.46-7.53 (m, 2H); 7.94 (dd, IH); 8.11 (br. s, IH) ppm.
1-30:
δ (CD3CN) = 1.38 (t, 3H); 4.40 (q, 2H); 7.51-7.57 (m, 2H); 7.98 (dd, IH); 10.4 (br. s, IH) ppm.
1-31:
δ ([D6]-DMSO) = 2.58 (s, 3H); 3.81 (s, 3H); 7.60-7.71 (m, 2H); 8.16-8.18 (m, IH); 11.50 (br. s,l H) ppm.
1-32:
δ ([D6J-DMSO) = 1.32 (t, 3H); 2.58 (s, 3H); 4.27-4.32 (q, 2H); 7.65-7.73 (m, 2H); 8.23-8.25 (m, IH); 11.31 (br. s,l H) ppm.
1-33:
δ ([D6I-DMSO) = 2.38 (s, 3H); 2.59 (s, 3H); 7.65-7.75 (m, 2H); 8.23-8.25 (m, IH); 11.95 (br. s,l H) ppm.
1-34:
δ ([Ds]-DMSO) = 1.21 (t, 3H); 4.18 (q, 2H); 5.43 (s, 2H); 7.38-7.89 (m, 8H); 9.38 (br. s,l H) ppm.
1-35:
δ ([D6]-DMSO) = 1.33-1.36 (t, 3H); 4.34-4.40 (q, 2H); 8.01-8.04 (m, IH); 8.51-8.54 (m, IH); 8.72 (m,l H); 11.02 (br. s,l H) ppm.
Die Bestimmung der Η-NMR-Daten erfolgt mit einem Bruker Avance 400, mit Tetramethylsilan als Referenz (0.0 ppm) und den Lösungsmitteln CD3CN oder [D6]-DMSO. Die Charakterisierung der Signalaufspaltung erfolgt mit s = Singulett, br. s = breites Singulett, d = Dublett, t = Triplett, q = Quartett, m = Multiplett, dd = doppeltes Dublett.
Anwendungsbeispiele
Myzus-Test (MYZUPE Spritzbehandlung)
Lösungsmittel: 78,0 Gewichtsteile Aceton
1,5 Gewichtsteile Dimethylformamid
Emulgator: 0,5 Gewichtsteile Alkylarylpolyglykolether
Zur Herstellung einer zweckmäßigen Wirkstoffzubereitung vermischt man 1 Gewichtsteil Wirkstoff mit den angegebenen Mengen Lösungsmittel und Emulgator und verdünnt das Konzentrat mit emulgatorhaltigem Wasser auf die gewünschte Konzentration.
Chinakohlblattscheiben (Brassica pekinensis), die von allen Stadien der Grünen Pfirsichblattlaus (Myzus persicae) befallen sind, werden mit einer Wirkstoffzubereitung der gewünschten Konzentration gespritzt.
Nach der gewünschten Zeit wird die Wirkung in % bestimmt. Dabei bedeutet 100 %, dass alle Blattläuse abgetötet wurden; 0 % bedeutet, dass keine Blattläuse abgetötet wurden.
Bei diesem Test zeigen z. B. die folgenden Verbindungen der Herstellungsbeispiele eine Wirkung von > 70 % bei einer Aufwandmenge von 500 g/ha:
Bsp. Nr. 1-2, 1-3, 1-4, 1-5, 1-6, 1-7, 1-8, 1-10, 1-11, 1-12, 1-13, 1-16, 1-17, 1-18, 1-19, 1-20, 1-21, 1-22, I- 23, 1-24, 1-25, 1-26, 1-27, 1-28, 1-29, 1-30, 1-31, 1-32, 1-33
Bei diesem Test zeigen z. B. die folgenden Verbindungen der Herstellungsbeispiele eine Wirkung von > 80 % bei einer Aufwandmenge von 100 g/ha:
Bsp. Nr. 1-9
Claims
1. Verfahren zur Bekämpfung von tierischen Schädlingen, gekennzeichnet dadurch, dass eine Pestizid wirksame Menge mindestens einer Verbindung der Formel (I),
wobei
R1, R2, R3 und R4 unabhängig voneinander für
Wasserstoff, Halogen, Carbamoyl, Thiocarbamoyl, Nitro, Cyano, Hydroxy, SF5 _ C1-C6- Alkyl, C2-C6-Alkenyl, C2-C6-Alkinyl, C3-C6-Cycloalkyl, C3-C6-Cycloalkyl-C,-C4-Alkyl, Q-Q-Halogenalkyl, CrC4-Halogenalkylthio, CrC4-Alkylthio, Ci-C4-Alkylsulfinyl, C1-C4- Halogenalkylsulfinyl, Ci-C4-Alkylsulfonyl, CrC4-Halogenalkylsulfonyl, C1-C4- Alkylcarbonyl, Q-C6- Alkoxy, C]-C6-Alkoxycarbonyl, C3-C6-Alkenyloxy, C3-C6- Cycloalkyloxy, C3-C6-Cycloalkyloxy-Ci-C4-Alkyl, Ci-C4-Halogenalkoxy, Ci-C4-Alkoxy- Ci-C4-Alkyl, Aryloxy, Hetaryloxy, Aryl-CrC4-Alkyloxy, Hetaryl-CrC4-Alkyloxy, (CrC4- Alkoxy)carbonyl, O-Acetyl, (Ci-C4-Alkyl)amino, Di-(C 1-C4-alkyl)amino, C3-C6- Trialkylsilyl, Aryl, Hetaryl, Aryl-CrC6-Alkyl oder Hetaryl-Ci-C6-Alkyl stehen,
wobei diese Reste unsubstituiert sein können oder einen, zwei oder mehrere Reste aus der Gruppe
Halogen, Cyano, Ci-C6-Alkyl, C3-C8-Cycloalkyl, C,-C4-Alkoxy, CrC4-Alkylthio, CrC4- Alkylsulfinyl, CrC4-Alkylsulfonyl, CrC4-Halogenalkyl, Ci-C4-Halogenalkoxy, C1-C4- Halogenalkylthio, (Ci-C4-Alkyl)amino, Di-(Ci -C4-alkyl)amino, Aryl und Hetaryl tragen können;
A für Wasserstoff, (CrC6-Alkyl)carbonyl, (C1- C6-Alkoxy)carbonyl, (C1-C6-
Alkylthio)carbonyl, (CrC6-Alkyl)thiocarbonyl, (C1-C6- Alkoxy)thiocarbonyl, (C1- C6-Alkylthio)thiocarbonyl, CrC8-Alkyl, C3-C6-Cycloalkyl, C2-C6- Alkenyl, C1-C4- Alkoxy, Ci-Q-Alkylthio, Ci-C4-Alkylsulfinyl, C,-C4-Alkylsulfonyl, C1-C4- Halogenalkyl, Aryl, Hetaryl, C1-C6-ATyIaIlCyI oder CrC6-Hetarylalkyl steht,
wobei diese Reste unsubstituiert sein können oder einen, zwei oder mehrere Reste aus der Gruppe
Halogen, Cyano, C1-C6-AIlCyI, C3-C8-Cycloalkyl, CrC4-Alkoxy, CrC4-Alkylthio, CrC4-Alkylsulfinyl, CrC4-Alkylsulfonyl, C,-C4-Halogenalkyl, C1-C4- Halogenalkoxy, Ci-C4-Halogenalkylthio, (Ci-C4-Alkyl)amino, Di-(C1-C4- alkyl)amino, Aryl und Hetaryl tragen können;
oder
A für den Rest c γ z steht,
n für 0, 1 oder 2 steht,
X für O oder S steht,
Y für O, S, oder C(=O) steht,
Z für CrC6-Alkyl, C2-C6-Alkenyl, C2-C6-Alkinyl, C3-C6-Cycloalkyl, C1-C6- Haloalkyl, C2-C6-Haloalkenyl, C2-C6-Haloalkinyl, C3-C6-Halocycloalkyl, Aryl,
Hetaryl, Q-Ce-Arylalkyl, CrC6-Hetarylalkyl, und für den Fall, dass Y für C(=O) steht, auch für C1-Cg-AIkOXy, C1-C4-HaIOaIkOXy, Aryloxy oder Hetaryloxy steht,
wobei Aryl und Hetaryl gegebenenfalls einfach oder mehrfach, gleich oder verschieden mit CrC6-Alkyl, C2-C6-Alkenyl, C2-C6-Alkinyl, C3-C6-Cycloalkyl, CrC6-Haloalkyl, C2- C6-Haloalkenyl, C2-C6-Haloalkinyl, C3-C6-Halocycloalkyl, Halogen, Cyano, Nitro, C1-C4-
Alkoxy, Ci-C4-Haloalkoxy substituiert sein können,
sowie Salze der Verbindungen der Formel (I)
auf tierische Schädlinge und/oder ihre Umgebung aufgebracht werden.
Verfahren zur Bekämpfung von tierischen Schädlingen gemäß Anspruch 1, gekennzeichnet dadurch, dass eine pestizid wirksame Menge mindestens einer Verbindung der Formel (I) mit mindestens einem Salz der Formel (FV)
in welcher
D für Stickstoff oder Phosphor steht,
R5, R6, R7, and R8 unabhängig voneinander für Wasserstoff oder jeweils gegebenenfalls substituiertes Ci-C8-Alkyl oder einfach oder mehrfach ungesättigtes, gegebenenfalls substituiertes Ci-Cg-Alkylen stehen, wobei die Substituenten aus Halogen, Nitro und Cyano ausgewählt sein können,
m für 1,
2, 3 oder 4 steht,
R9 für ein anorganisches oder organisches Anion steht,
auf tierische Schädlinge und/oder ihre Umgebung aufgebracht werden.
3. Verfahren gemäß Anspruch 1 oder 2, dadurch gekennzeichnet, dass mindestens ein PenetrationsfÖrder der Formel (V)
R-O-(-AO)v.R' (V)
in welcher
R für geradkettiges oder verzweigtes Alkyl mit 4 bis 20 Kohlenstoffatomen steht,
R' für Wasserstoff, Methyl, Ethyl, n-Propyl, i-Propyl, n-Butyl, i-Butyl, t-Butyl, n- Pentyl oder n-Hexyl steht,
AO für einen Ethylenoxid-Rest, einen Propylenoxid-Rest, einen Butylenoxid-Rest oder für Gemische aus Ethylenoxid- und Propylenoxid-Resten oder Butylenoxid-
Resten steht und
v für Zahlen von 2 bis 30 steht,
auf tierische Schädlinge und/oder ihre Umgebung aufgebracht wird.
4. Verfahren gemäß Anspruch 1 bis 3, gekennzeichnet dadurch, dass Erntegut und/oder Pflanzenvermehrungsmaterial vor Befall durch tierische Schädlinge geschützt wird, wobei eine pestizid wirksame Menge mindestens einer Verbindung der Formel (I) gemäß Anspruch 1 auf das Erntegut und/oder das Pflanzenvermehrungsmaterial aufgebracht wird.
5. Verbindungen sowie Salze der Verbindungen der Formel (I) gemäß Anspruch 1,
wobei A nicht für Phenyl steht, falls n=2 ist,
und wobei R1 verschieden von Wasserstoff ist, falls n=0 ist.
6. Verbindungen sowie Salze der Verbindungen der Formel (I) gemäß Anspruch 1 oder 5,
wobei
R1 für Halogen, Nitro, CrC3-Alkyl, CrC3-Halogenalkyl, Ci-C3-Alkylthio, Ci-C3-
Alkylsulfonyl, Q-Cö-Alkenyloxy, Ci-C3-Alkoxy, Ci-C2-Halogenalkoxy, Q-C4-
Alkoxy-Ci-C4-Alkyl, Aryloxy, Hetaryloxy, Ci-C2-Arylalkyloxy, CrC2- Hetarylalkyloxy, Ci-C4-Alkoxycarbonyl, O-Acetyl stehen,
wobei diese Reste unsubstituiert sein können oder einen, zwei oder mehrere Reste aus der Gruppe
Halogen, Ci-C4-Alkoxy tragen können,
R2 ? R3 und R4 für Wasserstoff stehen,
A Wasserstoff, (CrC3-Alkyl)carbonyl, (CrC3-Alkoxy)carbonyl, CrC2-Alkyl, C1-C4-
Alkoxy, C]-C4-Halogenalkyl, C]-C4-Halogenalkoxy, Ci-C2-Arylalkyl oder Ci-C2- Hetarylalkyl steht,
oder
X
Il
A für den Rest C~Y Z steht,
n für 0 oder 2 steht, X für O oder S steht,
Y für O, S oder C(=O) steht,
Z für CrC-Alkyl, CrC4-Haloalkyl, C2-C6-Haloalkinyl, Aryl und für den Fall, dass
Y für C(=O) steht, auch für Ci-C4-Alkoxy steht.
7. Verbindungen sowie Salze der Verbindungen der Formel (I) gemäß Anspruch 1 oder 5,
wobei
R1, R2, R3, R4 und A für Wasserstoff stehen,
n für 2 steht,
X für O oder S steht,
Y für O oder S steht,
Z für C,-C4-Alkyl, CrC4-Haloalkyl, C2-C6-Haloalkinyl, Aryl steht.
8. Verfahren zur Herstellung von Verbindungen der Formel (I), dadurch gekennzeichnet daß
(A) 3-Amino-l,2-benzoisothiazole der Formle (II)
X
T Y (EQ) umgesetzt werden,
wobei R bis R , n, X, Y, Z und A die oben angegebenen Bedeutungen aufweisen
Q Q γ ^ und T für Halogen und steht,
oder
(B) (Thio)carbamate und (Thio)oxamate der Formel (Ib)
mit einem Oxidationsmittel umsetzt,
oder
(C) (Thio)carbamate und (Thio)oxamate der Formel (Ic)
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08156621A EP2123159A1 (de) | 2008-05-21 | 2008-05-21 | (1,2-Benzisothiazol-3-yl)(thio)carbamate und (1,2-Benzisothiazol-3-yl)(thio)oxamate und deren Oxidationsformen als Pestizide |
| EP08156621.8 | 2008-05-21 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2009141065A2 true WO2009141065A2 (de) | 2009-11-26 |
| WO2009141065A3 WO2009141065A3 (de) | 2010-10-07 |
Family
ID=39847034
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2009/003304 Ceased WO2009141065A2 (de) | 2008-05-21 | 2009-05-09 | (1,2-benzisothiazol-3-yl)(thio)carbamate und (1,2-benzisothiazol-3-yl)(thio)oxamate und deren oxidationsformen als pestizide |
Country Status (2)
| Country | Link |
|---|---|
| EP (1) | EP2123159A1 (de) |
| WO (1) | WO2009141065A2 (de) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108154100A (zh) * | 2017-12-20 | 2018-06-12 | 中国疾病预防控制中心寄生虫病预防控制所 | 基于生物识别技术的智能投药装置及方法 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3464296B1 (de) * | 2016-06-02 | 2020-10-14 | Bayer CropScience Aktiengesellschaft | Isothiazolopyridone, verfahren zu ihrer herstellung und ihre verwendung als herbizide und/oder pflanzenwachstums-regulatoren |
| WO2017207395A1 (en) | 2016-06-02 | 2017-12-07 | Bayer Cropscience Aktiengesellschaft | Isothiazolopyridones, processes for their preparation and their use as fungicides |
Family Cites Families (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE860051C (de) | 1944-01-27 | 1952-12-18 | Hydrierwerke A G Deutsche | Verfahren zur Herstellung aromatischer o-Cyansulfohalogenide |
| US2842476A (en) | 1953-04-23 | 1958-07-08 | Mclaughlin Gormley King Co | Insecticidal compositions |
| EP0033984B1 (de) | 1980-01-23 | 1984-06-06 | Duphar International Research B.V | Sulphonylverbindungen, Verfahren zu ihrer Herstellung sowie auf diesen Verbindungen basierende Blattlausbekämpfungsmittel |
| DE3008186A1 (de) | 1980-03-04 | 1981-10-15 | Hoechst Ag, 6000 Frankfurt | Synergistische kombinationen von phosphinothricin |
| DE3015113A1 (de) | 1980-04-19 | 1981-10-22 | Dr. Karl Thomae Gmbh, 7950 Biberach | 4-hydroxy-1,2-benzisothiazol-3(2h)-on-1,1-dioxide, ihre salze, ihre herstellung und verwendung |
| DE3112164A1 (de) | 1981-03-27 | 1982-10-14 | Basf Ag, 6700 Ludwigshafen | Benzisothiazolyloxamate, verfahren zu ihrer herstellung und diese enthaltende therapeutische mittel |
| US4492705A (en) | 1982-02-12 | 1985-01-08 | Ciba-Geigy Corporation | 3-Amidino-benzisothiazole-1,1-dioxides and their use for controlling pests |
| EP0105732A3 (de) | 1982-10-01 | 1985-09-04 | Beecham Group Plc | Histamin-H2-rezeptoren-Antagonisten der Benzisothiazolamino- und Benzothiadiazinamino Reihe |
| DE3382093D1 (de) | 1982-11-26 | 1991-02-07 | Ciba Geigy Ag | Schaedlingsbekaempfungsmittel. |
| EP0133418A3 (de) | 1983-08-09 | 1985-04-03 | Ciba-Geigy Ag | Die Verwendung von 3-Acylaminobenzisothiazolen in der Schädlingsbekämpfung |
| EP0138762B1 (de) | 1983-09-14 | 1989-07-19 | Ciba-Geigy Ag | Schädlingsbekämpfungsmittel |
| DE3544436A1 (de) | 1984-12-18 | 1986-06-19 | Ciba-Geigy Ag, Basel | Neue dioxide |
| ZA861026B (en) | 1985-02-13 | 1986-09-24 | Ciba Geigy Ag | Pesticidal compositions |
| EP0207891A1 (de) | 1985-06-14 | 1987-01-07 | Ciba-Geigy Ag | Salze von 3-Acylaminobenzisothiazol-S,S-dioxiden, Verfahren zu ihrer Herstellung und ihre Verwendung in der Schädlingsbekämpfung |
| JPS638302A (ja) | 1986-06-27 | 1988-01-14 | Kao Corp | 殺生剤用効力増強剤 |
| JPH0618761B2 (ja) | 1986-07-14 | 1994-03-16 | 花王株式会社 | 粒状農薬の製造方法 |
| JPH01319467A (ja) | 1988-06-20 | 1989-12-25 | Ishihara Sangyo Kaisha Ltd | ベンゾイソチアゾール系化合物、それらの製造方法及びそれらを含有する殺虫剤 |
| JPH026496A (ja) | 1988-06-27 | 1990-01-10 | Ishihara Sangyo Kaisha Ltd | 有機リン酸アミド系化合物、それらの製造方法及びそれらを含有する有害動物防除剤 |
| JPH0747523B2 (ja) | 1990-04-16 | 1995-05-24 | 花王株式会社 | 殺生剤効力増強剤 |
| US5352674A (en) | 1991-03-25 | 1994-10-04 | Valent U.S.A. | Chemically stable granules containing insecticidal phosphoroamidothioates |
| US5462912A (en) | 1991-10-09 | 1995-10-31 | Kao Corporation | Agricultural chemical composition enhancer comprising quaternary di(polyoxyalkylene) ammonium alkyl sulfates |
| MY111077A (en) | 1992-11-13 | 1999-08-30 | Kao Corp | Agricultural chemical composition |
| BR9406470A (pt) | 1993-12-28 | 1996-01-23 | Kao Corp | Composição e processo para aperfeiçoar produtos quimicos aplicáveis na agricultura e composição quimica aplicável na agricultura |
| DE4401542A1 (de) | 1994-01-20 | 1995-07-27 | Hoechst Schering Agrevo Gmbh | Synergistische Kombinationen von Ammoniumsalzen |
| DE4416303A1 (de) | 1994-05-09 | 1995-11-16 | Bayer Ag | Schaumarmes Netzmittel und seine Verwendung |
| AU699367B2 (en) * | 1995-06-02 | 1998-12-03 | Sanofi-Aventis | Isoindole derivatives, their preparation and their application in therapy |
| GB9703054D0 (en) | 1997-02-14 | 1997-04-02 | Ici Plc | Agrochemical surfactant compositions |
| DE19857963A1 (de) | 1998-12-16 | 2000-06-21 | Bayer Ag | Agrochemische Formulierungen |
| WO2003087072A1 (en) | 2002-03-29 | 2003-10-23 | Mochida Pharmaceutical Co., Ltd. | Therapeutic agent for endothelial disorder |
| US6645914B1 (en) | 2002-05-01 | 2003-11-11 | Ndsu-Research Foundation | Surfactant-ammonium sulfate adjuvant composition for enhancing efficacy of herbicides |
| WO2003101197A1 (en) | 2002-05-31 | 2003-12-11 | Cjb Industries, Inc. | Adjuvant for pesticides |
| US7132448B2 (en) | 2002-09-12 | 2006-11-07 | The Hartz Mountain Corporation | High concentration topical insecticide containing insect growth regulator |
| US6984662B2 (en) | 2003-11-03 | 2006-01-10 | The Hartz Mountain Corporation | High concentration topical insecticide containing insect growth regulator |
| EP1954138A2 (de) | 2005-11-21 | 2008-08-13 | Basf Se | Insektizide verfahren unter verwendung von 3-amino-1,2-benzisothiazolderivaten |
| DE102005059468A1 (de) | 2005-12-13 | 2007-06-14 | Bayer Cropscience Ag | Insektizide Zusammensetzungen mit verbesserter Wirkung |
| DE102005059467A1 (de) | 2005-12-13 | 2007-06-14 | Bayer Cropscience Ag | Insektizide Zusammensetzungen mit verbesserter Wirkung |
| DE102005059470A1 (de) | 2005-12-13 | 2007-06-14 | Bayer Cropscience Ag | Insektizide Zusammensetzungen mit verbesserter Wirkung |
| DE102005059469A1 (de) | 2005-12-13 | 2007-06-14 | Bayer Cropscience Ag | Insektizide Zusammensetzungen mit verbesserter Wirkung |
| DE102005059466A1 (de) | 2005-12-13 | 2007-06-14 | Bayer Cropscience Ag | Insektizide Zusammensetzungen mit verbesserter Wirkung |
| EP2003975B1 (de) | 2006-03-31 | 2009-11-18 | Basf Se | 3-amino-1,2-benzisothiazol-verbindungen zur bekämpfung von tierpest |
| KR20090107070A (ko) * | 2007-01-26 | 2009-10-12 | 바스프 에스이 | 동물 해충 ⅱ의 퇴치를 위한 3-아미노-1,2-벤즈이소티아졸 화합물 |
-
2008
- 2008-05-21 EP EP08156621A patent/EP2123159A1/de not_active Ceased
-
2009
- 2009-05-09 WO PCT/EP2009/003304 patent/WO2009141065A2/de not_active Ceased
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108154100A (zh) * | 2017-12-20 | 2018-06-12 | 中国疾病预防控制中心寄生虫病预防控制所 | 基于生物识别技术的智能投药装置及方法 |
| CN108154100B (zh) * | 2017-12-20 | 2021-12-24 | 中国疾病预防控制中心寄生虫病预防控制所 | 基于生物识别技术的智能投药装置及方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2009141065A3 (de) | 2010-10-07 |
| EP2123159A1 (de) | 2009-11-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2379526B1 (de) | Tetrazolsubstituierte Anthranilsäureamide als Pestizide | |
| EP2309857B1 (de) | Heterocyclische verbindungen als schädlingsbekämpfungsmittel | |
| EP2558458B1 (de) | Neue heterocyclische verbindungen als schädlingsbekämpfungsmittel | |
| EP2582691B1 (de) | Anthranilsäurederivate | |
| EP2582688B1 (de) | Anthranilsäurediamid-derivate | |
| EP2582695B1 (de) | Anthranilsäurediamid-derivate mit zyklischen seitenketten | |
| EP2558460B1 (de) | Triazolsubstituierte anthranilsäureamide als pestizide | |
| EP2262798B1 (de) | Substituierte enaminothiocarbonylverbindungen | |
| US8173641B2 (en) | 4-amino-1,2,3-benzoxathiazine-derivatives as pesticides | |
| WO2009141065A2 (de) | (1,2-benzisothiazol-3-yl)(thio)carbamate und (1,2-benzisothiazol-3-yl)(thio)oxamate und deren oxidationsformen als pestizide | |
| EP2070923A1 (de) | Insektizide Iminoheterocyclen | |
| WO2008155031A1 (de) | Insektizide heterocylische verbindungen | |
| EP1982595A1 (de) | Insektizidderivate von substituierten Aminoheterocyklen | |
| WO2008138499A1 (en) | Insecticidal substituted thiourea derivatives | |
| EP1977646A1 (de) | Insektizide Hydroxyethyl-Thioharnstoff -Derivate | |
| WO2008135181A2 (en) | Insecticidal substituted 2-aminoindanes | |
| WO2009049798A1 (de) | Insektizide iminoheterocyclen | |
| EP2042507A1 (de) | Insektizid wirksame Derivate phosphorylierter Aminoheterocyclen | |
| WO2009040008A1 (en) | Novel iminooxazole and iminothiazole compounds |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09749555 Country of ref document: EP Kind code of ref document: A2 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 09749555 Country of ref document: EP Kind code of ref document: A2 |