WO2009125563A1 - バイオセンサシステム、センサチップおよび血液試料中の分析物濃度の測定方法 - Google Patents
バイオセンサシステム、センサチップおよび血液試料中の分析物濃度の測定方法 Download PDFInfo
- Publication number
- WO2009125563A1 WO2009125563A1 PCT/JP2009/001560 JP2009001560W WO2009125563A1 WO 2009125563 A1 WO2009125563 A1 WO 2009125563A1 JP 2009001560 W JP2009001560 W JP 2009001560W WO 2009125563 A1 WO2009125563 A1 WO 2009125563A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- data
- blood sample
- temperature
- analyte
- measurement
- Prior art date
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/28—Electrolytic cell components
- G01N27/30—Electrodes, e.g. test electrodes; Half-cells
- G01N27/327—Biochemical electrodes, e.g. electrical or mechanical details for in vitro measurements
- G01N27/3271—Amperometric enzyme electrodes for analytes in body fluids, e.g. glucose in blood
- G01N27/3273—Devices therefor, e.g. test element readers, circuitry
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/28—Electrolytic cell components
- G01N27/30—Electrodes, e.g. test electrodes; Half-cells
- G01N27/327—Biochemical electrodes, e.g. electrical or mechanical details for in vitro measurements
- G01N27/3271—Amperometric enzyme electrodes for analytes in body fluids, e.g. glucose in blood
- G01N27/3274—Corrective measures, e.g. error detection, compensation for temperature or hematocrit, calibration
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/26—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving oxidoreductase
Definitions
- the present invention relates to a biosensor system, a sensor chip, and a method for measuring an analyte concentration in a blood sample.
- a portable biosensor system comprising a measuring instrument having a calculation unit and a sensor chip detachably attached to the measuring instrument in order to measure the concentration of an analyte in a blood sample, for example, blood glucose concentration (blood glucose level) Is used.
- the concentration of the analyte is calculated based on the amount of oxidant or reductant generated by the enzyme cycling reaction through the oxidoreductase using the analyte as a substrate.
- the rate of the enzyme cycling reaction depends on the temperature at which the reaction proceeds (reaction temperature). For this reason, it is desirable to correct the concentration of the analyte based on the reaction temperature.
- the reaction temperature is measured by a temperature sensor arranged in a measuring instrument as described in, for example, Japanese Patent Application Laid-Open No. 2003-156469.
- a temperature sensor arranged in a measuring instrument as described in, for example, Japanese Patent Application Laid-Open No. 2003-156469.
- the measured reaction temperature does not accurately reflect the temperature of the blood sample. This may cause errors in the analyte concentration measurement.
- JP 2001-235444 A, JP 2003-42995 A, and International Publication No. 2003/062812 disclose biosensor systems aimed at improving the measurement accuracy of reaction temperature.
- the biosensor system described in Japanese Patent Laid-Open Nos. 2001-235444 and 2003-42995 has a heat conducting member in the vicinity of the blood sample holding portion of the sensor chip, and the heat is transmitted through the heat conducting member.
- the temperature of the blood sample to be detected is detected by a temperature sensor arranged in the measuring instrument.
- a resin plate is disposed between the heat conductive member and the blood sample holding part, so that the heat conductive member is a blood sample. None touch.
- a temperature sensor and a heat conducting member are arranged in a mounting portion of a measuring instrument for attaching a sensor chip, and the temperature of the blood sample is passed through the heat conducting member. Is transmitted to the temperature sensor.
- the temperature of the environment in which the sensor is used changes rapidly. Errors in the analyte concentration measurement are likely to occur.
- the temperature of the blood sample is measured via a resin plate and a heat conducting member. Again, the measured reaction temperature does not accurately reflect the temperature of the blood sample.
- the present invention is a biosensor system comprising a measuring instrument having a calculation unit and a sensor chip that is detachably attached to the measuring instrument and into which a blood sample is introduced, wherein the sensor chip is included in the blood sample.
- a measurement unit A that acquires data a related to the concentration of the analyte based on the amount of current flowing in the blood sample due to a reaction involving an oxidoreductase having an analyte as a substrate, and temperature correction of the data a
- a measurement unit B that acquires data b to be obtained from the blood sample, and the calculation unit is corrected according to the temperature of the blood sample based on the data a and the data b.
- a biosensor system having the function of determining the concentration of the analyte therein is provided.
- the present invention is a sensor chip used in the above biosensor system into which a blood sample is introduced, and a reaction involving an oxidoreductase having an analyte in the blood sample as a substrate.
- Measurement unit A that acquires data a related to the concentration of the analyte based on the amount of current flowing in the blood sample, and measurement that acquires data b for temperature correction of the data a from the blood sample A sensor chip having a portion B is provided.
- the present invention provides data related to the concentration of the analyte based on the amount of current flowing in the blood sample due to a reaction involving an oxidoreductase having the analyte in the blood sample as a substrate.
- a step for obtaining a a step for obtaining data b for correcting the temperature of the data a from the blood sample, and a correction based on the temperature of the blood sample based on the data a and the data b.
- applying a voltage to the electrode of the sample to measure the amount of current flowing in the blood sample as a result of oxidation or reduction of a redox substance other than the analyte.
- FIG. 1 is a diagram showing an example of a biosensor system according to the present invention.
- FIG. 2 is an exploded perspective view of an example of a sensor chip according to the present invention.
- FIG. 3 is a plan view of an example of a sensor chip according to the present invention.
- FIG. 4 is a diagram showing an example of a circuit configuration in the biosensor system according to the present invention.
- FIG. 5 is a diagram illustrating an example of the conversion table.
- FIG. 6 is a diagram illustrating another example of the conversion table.
- the biosensor system acquires data for correcting the concentration of an analyte from a blood sample by a measurement unit arranged on a sensor chip.
- FIG. 1 is a diagram for explaining an example of a biosensor system according to the present invention.
- the biosensor system 100 includes a rectangular parallelepiped measuring device 101 and a sensor chip 200.
- a mounting port 102 that is a rectangular hole is formed on the side wall surface of the measuring instrument 101.
- the sensor chip 200 is detachably attached to the attachment opening 102 and connected to the measuring instrument 101.
- a display unit 103 for displaying a measurement result is disposed at a substantially central portion of one main surface of the measuring instrument 101.
- FIG. 2 is an exploded perspective view of the sensor chip 200
- FIG. 3 is a plan view thereof.
- the sensor chip 200 has a cover 203 on the insulating substrate 201 with a spacer 202 having a rectangular cutout 204 formed therein and leaving one end of the insulating substrate 201 (the right end in the figure). Has been placed.
- the members 201, 202, and 203 are integrated by, for example, adhesion or heat welding.
- the notch portion 204 of the spacer 202 becomes the capillary portion 40 that holds the blood sample after the integration of the members.
- the capillary portion 40 extends along the long side of the chip 200 and communicates with the outside at one end portion (left end portion in the drawing) of the spacer 202. In other words, the capillary section 40 communicates with the blood sample introduction port 16 that opens to the outside of the chip 200.
- the cover 203 has an exhaust port 15 at a portion corresponding to the end of the capillary portion 40 opposite to the end communicating with the outside. Thereby, a blood sample can be easily sucked into the capillary portion 40 from the sample introduction port 16 by capillary action.
- the electrodes 11, 12, 13, 14 are arranged so that each part (portions 31, 32, 33, 34) faces the capillary part 40.
- the portion 31 of the electrode 11 is disposed at a position closer to the blood sample introduction port 16 than the portion 32 of the electrode 12 and the portion 33 of the electrode 13.
- the part 33 of the electrode 13 is a part of the electrode 13 branched in a U-shape, and is disposed at a position sandwiching the part 32 of the electrode 12.
- the reaction reagent layer 20 is formed on the insulating substrate 201 so as to cover the portion 32 of the electrode 12 and the portion 33 of the electrode 13.
- the reaction reagent layer 20 contains an oxidoreductase having an analyte in a blood sample as a substrate.
- the reaction reagent layer 20 is formed at a position away from the portion 31 of the electrode 11.
- the sensor chip 200 is constituted by an electrode system constituted by the part 32 of the electrode 12 and the part 33 of the electrode 13 and a partial space of the capillary part 40 that accommodates the reaction reagent layer 20 and the parts 32 and 33. And a measurement unit 41 (measurement unit A). Furthermore, the sensor chip 200 includes a measurement unit configured by an electrode system constituted by the part 31 of the electrode 11 and the part 32 of the electrode 12 and a partial space of the capillary part 40 that accommodates the part 31 and the part 32. 42 (measurement part B).
- the measurement unit A acquires data a related to the concentration of the analyte in the blood sample based on the amount of current flowing in the blood sample due to the reaction involving the oxidoreductase. Then, as will be described later, the measurement unit B uses the data b for correcting the temperature of the data a, more specifically, a reaction that does not involve the oxidoreductase used to acquire the data a and is not an analyte. Data b relating to the amount of current flowing in the blood sample accompanying the oxidation or reduction of the redox material is obtained from the blood sample.
- the measurement part B may be in the state which acquires the data b using the member which contacts a blood sample, more specifically, the electrode which contacts a blood sample.
- the data related to the amount of current means the amount of the current or a converted value of the current amount.
- the redox substance other than the analyte is at least one selected from ascorbic acid, uric acid, acetaminophen, ferricyanide, p-benzoquinone, p-benzoquinone derivative, oxidized phenazine methosulfate, methylene blue, ferricinium, and ferricinium derivative. Can be illustrated.
- the redox substance other than the analyte may be a solvent, for example water in the case of a blood sample.
- the electrode 12 functions as a working electrode and the electrode 13 functions as a counter electrode.
- the electrode 12 functions as a counter electrode, and the electrode 11 functions as a working electrode.
- the measurement part A and the measurement part B may be in a state where the electrode 12 is shared as shown in the figure, or may be in a state where each has a pair of electrodes.
- the measurement unit B has an electrode for applying a voltage to the blood sample.
- the portion 34 of the electrode 14 is disposed in the vicinity of the end on the back side of the capillary section 40, in other words, in the vicinity of the end opposite to the end communicating with the outside.
- a voltage may be applied between the electrode 12 or the electrode 13 and the electrode 14 instead of the electrode 11.
- the electrodes 11, 12, 13, and 14 are connected to leads (not shown), respectively.
- One end of the lead is exposed to the outside of the chip 200 at the end of the insulating substrate 201 not covered with the spacer 202 and the cover 203 so that a voltage can be applied between the electrodes.
- Analytes in blood samples include substances other than blood cells, such as glucose, albumin, lactic acid, bilirubin, and cholesterol.
- the oxidoreductase one using the target analyte as a substrate is used.
- the oxidoreductase include glucose oxidase, glucose dehydrogenase, lactate oxidase, lactate dehydrogenase, bilirubin oxidase and cholesterol oxidase.
- Examples of the amount of oxidoreductase in the reaction reagent layer include 0.01 to 100 units (U), preferably 0.05 to 10 U, more preferably 0.1 to 5 U.
- the reaction reagent layer 20 includes an electron mediator having a function of transferring electrons generated by the enzyme reaction to the electrode, such as potassium ferricyanide, p-benzoquinone, p-benzoquinone derivative, oxidized phenazine methosulfate, methylene blue, ferricinium, and ferricinium derivative. It is desirable to contain.
- the reaction reagent layer 20 may contain a water-soluble polymer compound in order to improve the moldability of the reaction reagent layer.
- water-soluble polymer compound examples include carboxymethyl cellulose (CMC), hydroxyethyl cellulose, hydroxypropyl cellulose, methyl cellulose, ethyl cellulose, ethyl hydroxyethyl cellulose, carboxyethyl cellulose, polyvinyl alcohol, polyvinyl pyrrolidone and polyzine, polystyrene sulfonic acid, gelatin and its Examples thereof include at least one selected from derivatives, polyacrylic acid and salts thereof, polymethacrylic acid and salts thereof, starch and derivatives thereof, maleic anhydride polymer and salts thereof, agarose gel and derivatives thereof.
- CMC carboxymethyl cellulose
- hydroxypropyl cellulose hydroxypropyl cellulose
- methyl cellulose methyl cellulose
- ethyl cellulose ethyl hydroxyethyl cellulose
- carboxyethyl cellulose examples include at least one selected from derivatives, polyacrylic acid and salts thereof, poly
- resins such as polyethylene terephthalate, polycarbonate, polyimide, polyethylene, polypropylene, polystyrene, polyvinyl chloride, polyoxymethylene, monomer cast nylon, polybutylene terephthalate, methacrylic resin and ABS resin are used. Furthermore, glass can be illustrated.
- the electrodes 11, 12, 13, and 14 can be made of a known conductive material such as palladium, platinum, gold, silver, titanium, copper, nickel, and carbon.
- FIG. 4 is a diagram showing an example of a circuit configuration for measuring an analyte concentration in a blood sample in the biosensor system 100.
- the measuring instrument 101 includes a control circuit 300 that applies a voltage between at least two of the electrodes 11, 12, 13, and 14 in the sensor chip 200, and a liquid crystal display (LCD) 400 that corresponds to a display unit of the measuring instrument. have.
- LCD liquid crystal display
- the control circuit 300 includes four connectors 301a, 301b, 301c, and 301d, a switching circuit 302, a current / voltage conversion circuit 303, an analog / digital (A / D) conversion circuit 304, a reference voltage source 305, and an arithmetic operation. Part 306.
- the control circuit 300 can switch the potential applied to the electrode through the switching circuit 302 so that one electrode can be used as a positive electrode or a negative electrode.
- the calculation unit 306 has a known central processing unit (CPU) and a conversion table for determining the analyte concentration in the blood sample based on the data a and data b.
- the analyte concentration is corrected by referring to a conversion table in which a correction coefficient based on the environmental temperature is described. More specifically, in the conventional biosensor system, the analyte concentration is provisionally calculated with reference to the conversion table for temporary measurement, and then the analyte concentration is corrected with reference to the conversion table for temperature correction. It was.
- the present inventor determines the amount of current flowing in the blood sample due to a reaction involving oxidoreductase, and a reaction not involving the oxidoreductase and a redox substance other than the analyte. It has been found that the amount of current flowing in a blood sample can vary as well as the oxidation or reduction of. And, as will be described later, the blood sample in the measurement of the analyte concentration without measuring the temperature of the blood sample or the like based on the conversion table constructed using this relationship by appropriately designing the biosensor system The influence of temperature can be eliminated.
- the calculation unit 306 is in a state of storing one conversion table constructed in this way, and is not in a state of storing a plurality of conversion tables constructed for each temperature of a blood sample or the like.
- FIG. 5 is a diagram illustrating an example of a conversion table included in the calculation unit 306, and
- FIG. 6 is a diagram illustrating another example thereof.
- the conversion table of the calculation unit 306 has the same voltage application condition as that for acquiring the data a from the reference blood sample in which the analyte concentration is clear and the temperature is fixed to one value.
- the data c related to the amount of current flowing through the reference blood sample and the amount of current flowing through the reference blood sample obtained from the reference blood sample under the same voltage application conditions as the acquisition of data b above.
- the data related to the amount of current means the amount of the current or a converted value of the current amount.
- the conversion table of the calculation unit 306 is not in a state in which the relationship between the blood sample temperature or the environmental temperature and the analyte concentration is described. It is desirable to prepare a conversion table for each biosensor system.
- the temperature of the reference blood sample is preferably in the range of more than 10 ° C. and less than 40 ° C., more preferably in the range of 17 ° C. or more and 33 ° C. or less.
- the measurement of the analyte concentration in the blood sample using the biosensor system 100 is performed, for example, as follows.
- the electrode 13 is connected to the current / voltage conversion circuit 303 via the connector 301c and the electrode 14 is connected to the reference voltage source 305 via the connector 301b in accordance with the CPU command of the arithmetic unit 306. Thereafter, a constant voltage is applied between both electrodes in accordance with a command from the CPU.
- the voltage is, for example, a voltage of 0.01 to 2 V, preferably 0.1 to 1 V, more preferably 0.2 to 0.5 V when the electrode 14 is represented as a positive electrode and the electrode 13 is represented as a negative electrode. is there. This voltage is applied after the sensor chip is inserted into the measurement unit until the blood sample is introduced to the back of the capillary unit 40.
- a current flows between the electrode 14 and the electrode 13.
- the current value is converted into a voltage value by the current / voltage conversion circuit 303, then converted into a digital value by the A / D conversion circuit 304, and input to the CPU.
- the CPU detects that the blood sample has been introduced to the back of the capillary section based on the digital value.
- the analyte in the blood sample is reacted with the oxidoreductase in the range of 0 to 60 seconds, preferably 0 to 30 seconds, more preferably 0 to 15 seconds.
- the data a is acquired as follows. First, in response to a command from the CPU, the switching circuit 302 is activated, the electrode 12 is connected to the current / voltage conversion circuit 303 via the connector 301a, and the electrode 13 is connected to the reference voltage source 305 via the connector 301c. Thereafter, a measurement sequence in the measurement unit A is input according to a command from the CPU.
- the voltage is 0.05 to 1 V, preferably 0.1 to 0.8 V, more preferably 0.2 to 0.6 V, for example, when the electrode 12 is represented as a positive electrode and the electrode 13 is represented as a negative electrode. It is a voltage that becomes a magnitude.
- the voltage application time is in the range of 0.1 to 30 seconds, preferably 0.1 to 15 seconds, more preferably 0.1 to 5 seconds.
- the amount of current flowing between the electrodes due to the application of the voltage is converted into a voltage value by the current / voltage conversion circuit 303 when a signal instructing acquisition of the data a is given from the control circuit to the measurement unit A. After that, it is converted into a digital value by the A / D conversion circuit 304 and input to the CPU, and is stored in the memory of the arithmetic unit 306 as data a.
- the control circuit acquires the data a within a range of 0.5 seconds to less than 2.5 seconds from the time when the blood sample is introduced into the capillary part of the sensor chip. It is preferable to give a signal instructing to the measurement unit A.
- the above data b is acquired as follows. First, in response to a command from the CPU, the switching circuit 303 is activated, the electrode 11 is connected to the current / voltage conversion circuit 303 via the connector 301d, and the electrode 12 is connected to the reference voltage source 305 via the connector 301a. Subsequently, a constant voltage is applied between both electrodes in the measurement unit B according to a command from the CPU.
- the voltage is, for example, a voltage of 0.1 to 5 V, preferably 0.2 to 3 V, more preferably 0.5 to 2.5 V when the electrode 11 is represented as a positive electrode and the electrode 12 is represented as a negative electrode. is there.
- the voltage application time is in the range of 0.1 to 30 seconds, preferably 0.1 to 10 seconds, more preferably 0.1 to 5 seconds.
- the amount of current flowing between the electrodes due to the application of the voltage is converted into a voltage value by the current / voltage conversion circuit 303 when a signal instructing acquisition of the data b is given from the control circuit to the measurement unit B. After that, it is converted into a digital value by the A / D conversion circuit 304 and input to the CPU, and is stored in the memory of the arithmetic unit 306 as data b.
- the data b may be acquired before the data a. In this case, the reduction type mediator is generated on the counter electrode when the data b is acquired.
- the working electrode it is preferable to use the counter electrode when acquiring data a.
- an oxidized mediator is disposed on the counter electrode.
- the oxidation-reduction reaction on the surface of the electrode may be a rate-determining step. From the viewpoint of avoiding such problems,
- the data b is preferably acquired after the data a.
- the current that flows in the blood sample with the oxidation or reduction of the redox substance other than the analyte is a reaction that does not involve the oxidoreductase used to acquire the data a. Can be detected more reliably.
- the calculation unit 306 refers to the conversion table and determines the analyte concentration in the blood sample based on the data a and the data b. Then, the determined analyte concentration is displayed on the LCD 400 as an image.
- the calculation program for the determination may be appropriately designed according to the data structure of the conversion table. When numerical data that completely matches data a and data b is not described in the conversion table, the analyte is obtained by using a known linear interpolation method from data described in the conversion table and approximating data a and data b. What is necessary is just to determine a density
- the value of the data b is obtained from the blood sample X having a temperature of 17 ° C. and the blood sample Y having the same component as the blood sample X and having a temperature of 33 ° C.
- the numerical value (Z) obtained by dividing by the value of a becomes substantially constant, the influence of the temperature of the blood sample in the measurement of the analyte concentration can be eliminated. More specifically, when the numerical values obtained from blood sample X and blood sample Y are respectively indicated as Z X and Z Y , the numerical value indicated by Z X / Z Y may be in the vicinity of 1.0.
- the analyte concentration in blood sample X and blood sample Y may be in the range of greater than 0 mg / dl and less than or equal to 1000 mg / dl, for example, 10 mg / dl or more and 600 mg / dl or less. If it is in the range.
- the biosensor system In order to eliminate the influence of the temperature of the blood sample in the measurement of the analyte concentration to the above extent, it is necessary to design the biosensor system appropriately. More specifically, various parameters such as the composition of the reaction reagent layer, the timing for measuring the amount of current flowing in the blood sample due to the reaction involving the oxidoreductase, and the dimensions of the capillary part are controlled.
- the reaction reagent layer does not contain a water-soluble polymer compound or the amount of the water-soluble polymer compound in the reaction reagent layer is less than 0.2% by mass
- a control circuit that gives the measurement unit A a signal instructing acquisition of the data a within a range of 0.5 seconds or more and less than 2.5 seconds from the time of introduction.
- the measuring instrument is not less than 2.5 seconds after the blood sample is introduced into the sensor chip. It is preferable to have a control circuit that gives the measurement unit A a signal instructing acquisition of the data a.
- the reaction reagent layer contains 0.2% by mass or more of the water-soluble polymer compound
- the dissolution rate of the reagent that contributes to the reaction in the reaction reagent layer elutes into the blood sample is slow, and the diffusion rate is also slow and the reaction is smoothly performed. It takes 2.5 seconds or more to progress.
- the width of the capillary is in the range of 0.8 mm or less, it is desirable to adopt the design.
- the amount of the water-soluble polymer compound in the reaction reagent layer is 0.2% by mass or more
- the upper limit of the content of the water-soluble polymer compound can be exemplified by 2% by mass, and an instruction to obtain data a As an upper limit of the time for, 15 seconds can be exemplified.
- the measuring instrument is a sensor chip
- a control circuit that gives the measurement unit A a signal for instructing the acquisition of the data a within a range of 0.5 seconds or more, further 1.5 seconds or more, particularly 2.0 seconds or more from the time when it was introduced into .
- 15 seconds can be exemplified.
- the capillary portion has a low height when the enzyme amount in the reaction reagent layer is the same, more specifically, 0.3 mm or less, and further 0.15 mm. Is preferably within a range of less than 0.1 mm, particularly 0.1 mm or less. The reason for this is not clear at this time, but the present inventor thinks as follows. If the height of the capillary part is too high, the oxidoreductase eluted from the reaction reagent layer tends to diffuse away from the electrode surface, and the enzyme involved in the enzyme cycling reaction is insufficient in the vicinity of the electrode surface.
- An example of the lower limit of the height of the capillary portion is 0.05 mm.
- the biosensor system according to the present invention can measure the analyte concentration with high accuracy even when the temperature of the environment in which the sensor is used changes rapidly. For this reason, it is not necessary to arrange
- the measuring device may further include an environmental temperature measurement unit that measures the temperature of the environment (measurement environment) in which the biosensor system is used.
- the calculation unit corrects the data c and the data c according to the temperature of the measurement environment (data You may further have the 2nd conversion table in which e) was described. If the temperature of the measurement environment is too high or too low, the analyte concentration measurement accuracy using the first conversion table may decrease. In such a case, the analyte concentration may be corrected by using the second conversion table instead of the first conversion table.
- Examples of the temperature of the measurement environment in which substitution of the second conversion table is preferable include a range of 10 ° C. or lower and a range of 40 ° C. or higher.
- An example of the lower limit of the temperature is 0 ° C.
- an example of the upper limit of the temperature is 50 ° C. If the temperature of the measurement environment is in the range of more than 10 ° C. and less than 40 ° C., it is sufficient to use the first conversion table.
- the first conversion table and the second conversion table are stored in one data table, more specifically, the data c, the data d, and the data e are mutually connected. It is not excluded that they are associated and described in one data table. For example, when the temperature of the measurement environment is in the range of 10 ° C. or lower and the range of 40 ° C. or higher, such a data table shows the analyte concentration calculated by referring to the first conversion table. It may further have data (correction coefficient) to be corrected by.
- the measuring device outputs a signal instructing to perform the first temperature measurement before acquiring the data a and data b, and the second temperature after acquiring the data a and data b.
- the biosensor system according to the present invention displays the temperature measured in the first temperature measurement and the second temperature measurement as the first temperature and the second temperature, respectively, i) When the first temperature and the second temperature satisfy the following relational expression (1), the concentration of the analyte in the blood sample is determined based on the data a and the data b by referring to the first conversion table. And then 2.5 ° C.
- the second temperature measurement may be performed after 5 seconds or more, preferably 15 seconds or more, and more preferably 30 seconds or more have elapsed since the first temperature measurement.
- the biosensor system of the present invention provides a signal for instructing the second temperature measurement after 5 seconds or more, preferably 15 seconds or more, more preferably 30 seconds or more after the first temperature measurement.
- You may have the control circuit given to an environmental temperature measurement part.
- data related to the first temperature and / or the second temperature for example, an average value of the first temperature and the second temperature can be used.
- the data may be temperature or a converted value of temperature.
- the biosensor system according to the present invention has a control circuit that measures the environmental temperature at regular intervals from the first temperature measurement and provides a signal for detecting a temperature transition per unit time to the environmental temperature measurement unit. May be. Thereby, the reliability (presence or absence of failure) of the environmental temperature measurement unit represented by the thermistor can be easily determined.
- the method for measuring the concentration of an analyte according to the present invention applies a voltage to a pair of electrodes in contact with a blood sample, and a current flowing in the blood sample accompanying oxidation or reduction of a redox substance other than the analyte.
- the above data b is obtained by including the step of measuring the amount of.
- the concentration of the analyte in the blood sample based on data a and data b can be determined by referring to the first conversion table.
- the analyte concentration measuring method may further include a step of measuring the ambient temperature around the blood sample.
- the step includes a first temperature measuring step for measuring the environmental temperature before acquiring the data a and data b, and a second temperature measuring step for measuring the environmental temperature after acquiring the data a and data b. May be.
- the analyte concentration measuring method displays the temperatures measured in the first temperature measuring step and the second temperature measuring step as the first temperature and the second temperature, respectively. i) When the first temperature and the second temperature satisfy the following relational expression (1), the concentration of the analyte in the blood sample is determined based on the data a and the data b by referring to the first conversion table. Decide 2.5 ° C. ⁇
- the second temperature measurement may be performed after 5 seconds or more, preferably 15 seconds or more, and more preferably 30 seconds or more have elapsed since the first temperature measurement.
- data related to the first temperature and / or the second temperature for example, an average value of the first temperature and the second temperature can be used.
- the data may be temperature or a converted value of temperature.
- Example 1 The sensor chip shown in FIGS. 2 and 3 was produced.
- the capillary part was designed to have a width of 0.6 mm, a length (depth) of 2.5 mm, and a height of 0.1 mm.
- the reaction reagent layer was formed as follows. Glucose dehydrogenase, potassium ferricyanide (manufactured by Kanto Chemical Co., Inc.), taurine (manufactured by Nacalai Tesque Co., Ltd.) and maltitol (manufactured by Hayashibara Co., Ltd.) were obtained by dissolving them in an aqueous CMC solution (Serogen HE-1500F manufactured by Daiichi Kogyo Seiyaku Co., Ltd.).
- the reagent solution has an enzyme amount of 2.0 U / sensor in the reaction reagent layer, a CMC amount of 0.05 mass%, a potassium ferricyanide amount of 2.5 mass%, a taurine amount of 1.5 mass%, and a maltitol amount.
- a polyethylene terephthalate substrate After coating on a polyethylene terephthalate substrate so as to be 0.1% by mass, it was dried in an atmosphere of 45% humidity and 21 ° C. Each electrode was composed of palladium.
- Blood was collected from 3 subjects. Blood samples were prepared by adding glucose concentrate to each blood such that the glucose concentration was 50 mg / dl, 100 mg / dl, 250 mg / dl, 400 mg / dl, 600 mg / dl.
- a blood sample was introduced into the capillary part of the sensor chip.
- the temperature of the blood sample was 17 ° C, 25 ° C or 33 ° C.
- a voltage of 0.25 V is applied between the working electrode (electrode 12) and the counter electrode (electrode 13) in the measurement unit A, and 1 second after the introduction of the blood sample is completed, the above enzyme and glucose
- the current (glucose response) flowing between the electrodes was measured by an enzyme cycling reaction involving the.
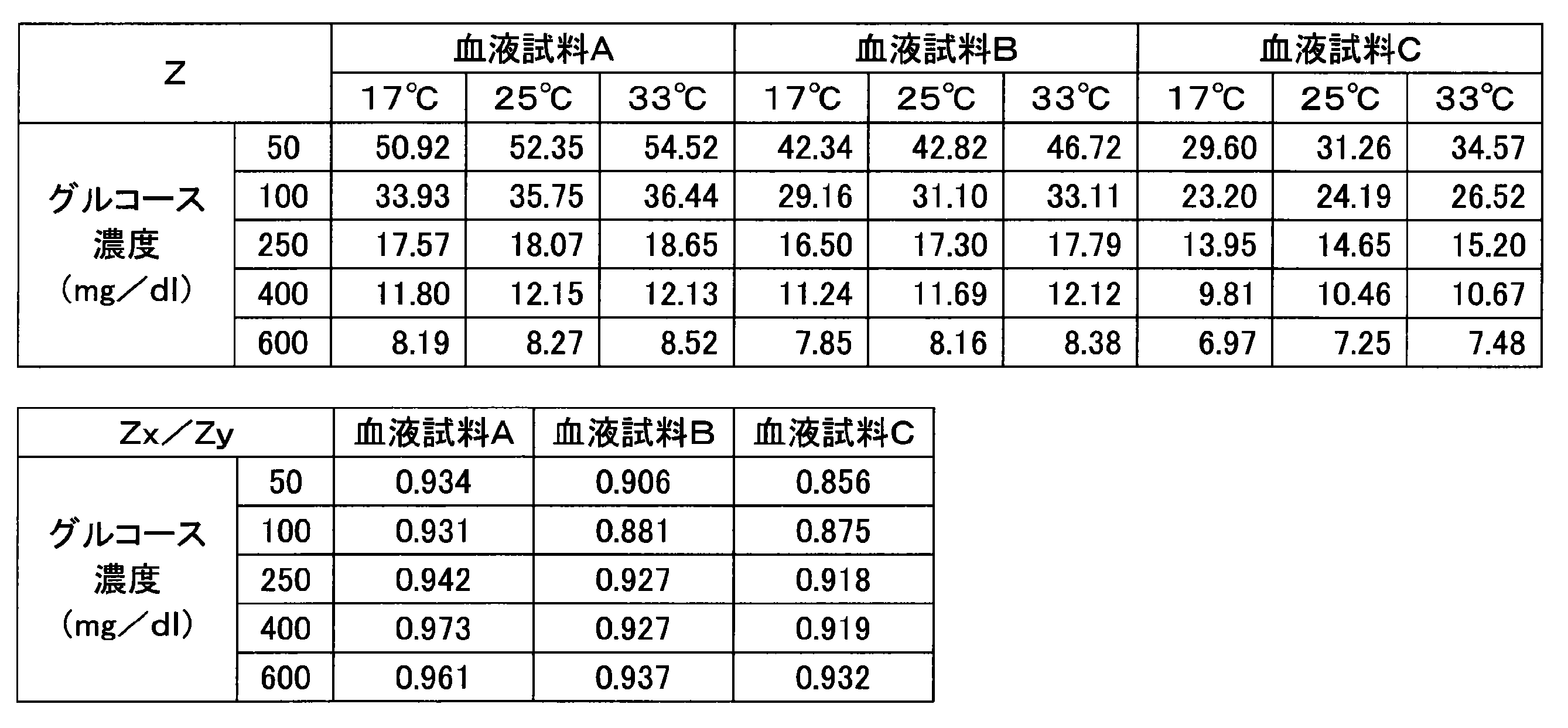
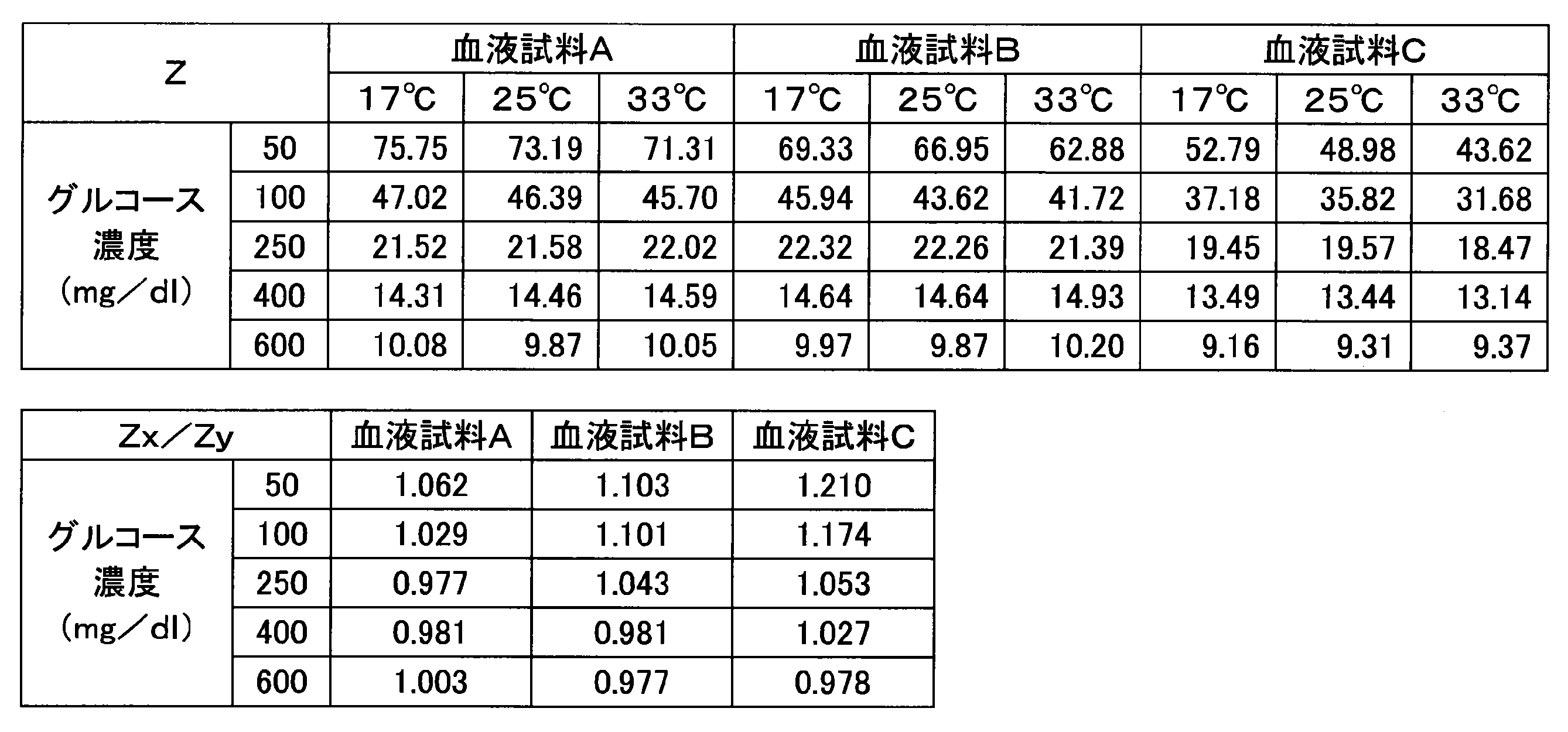
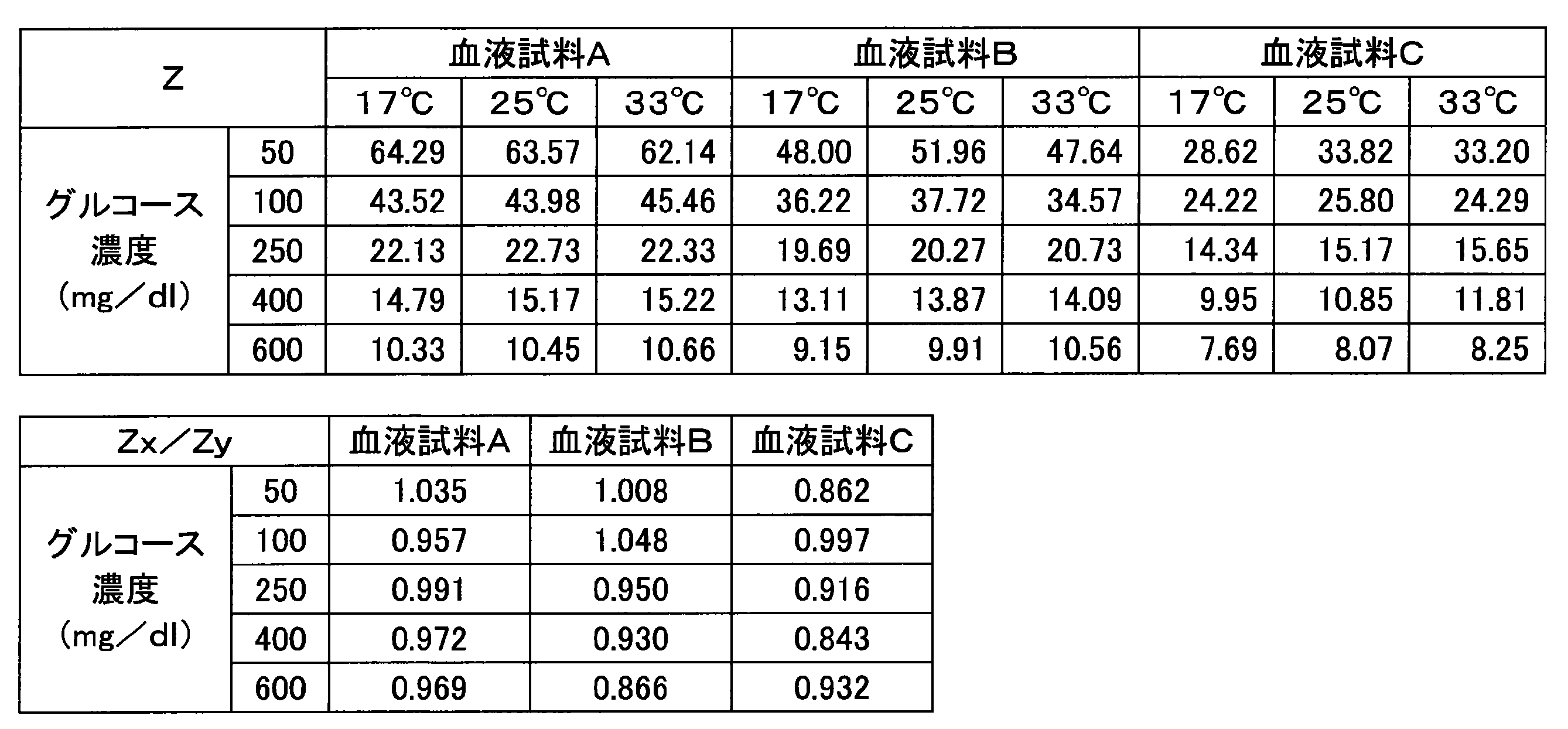
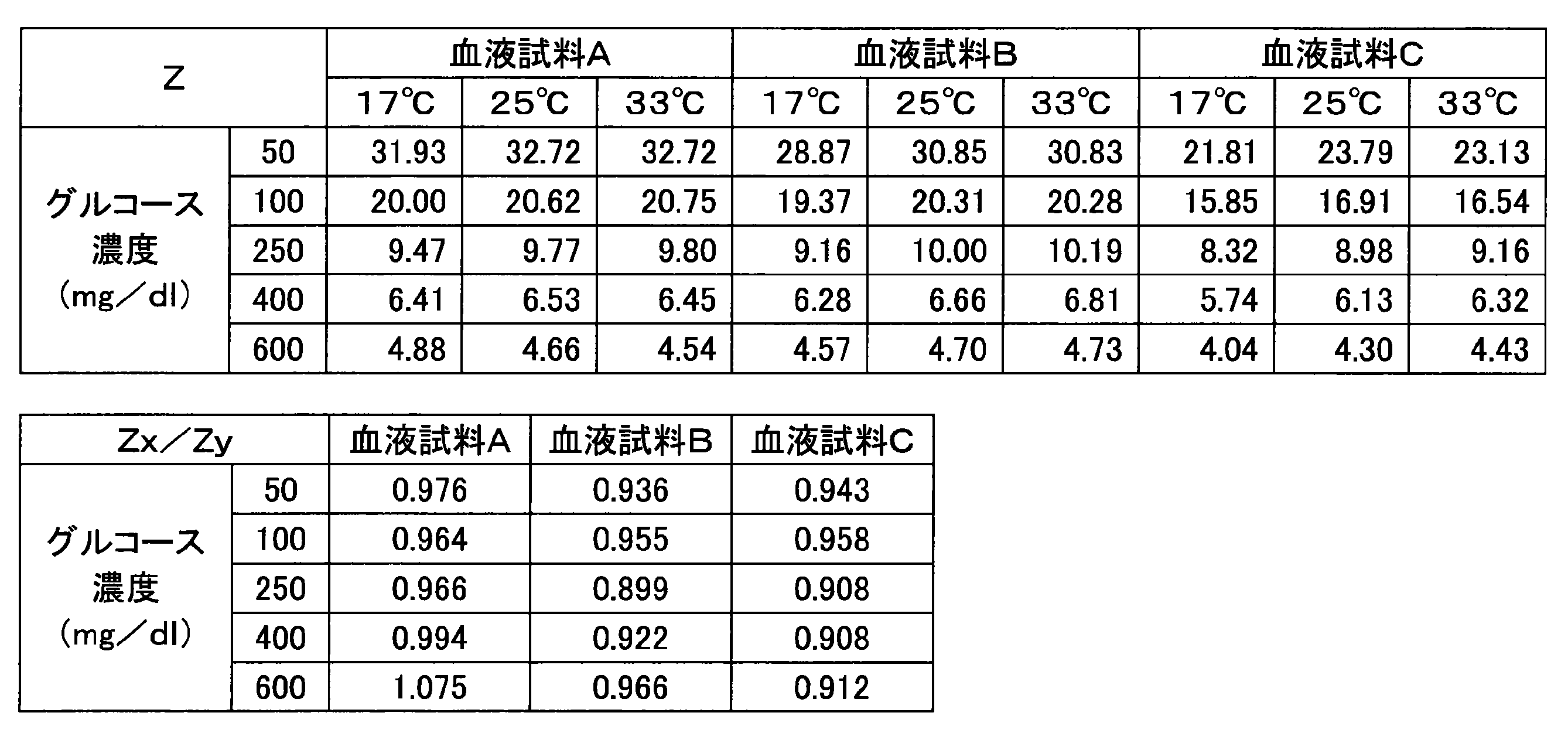
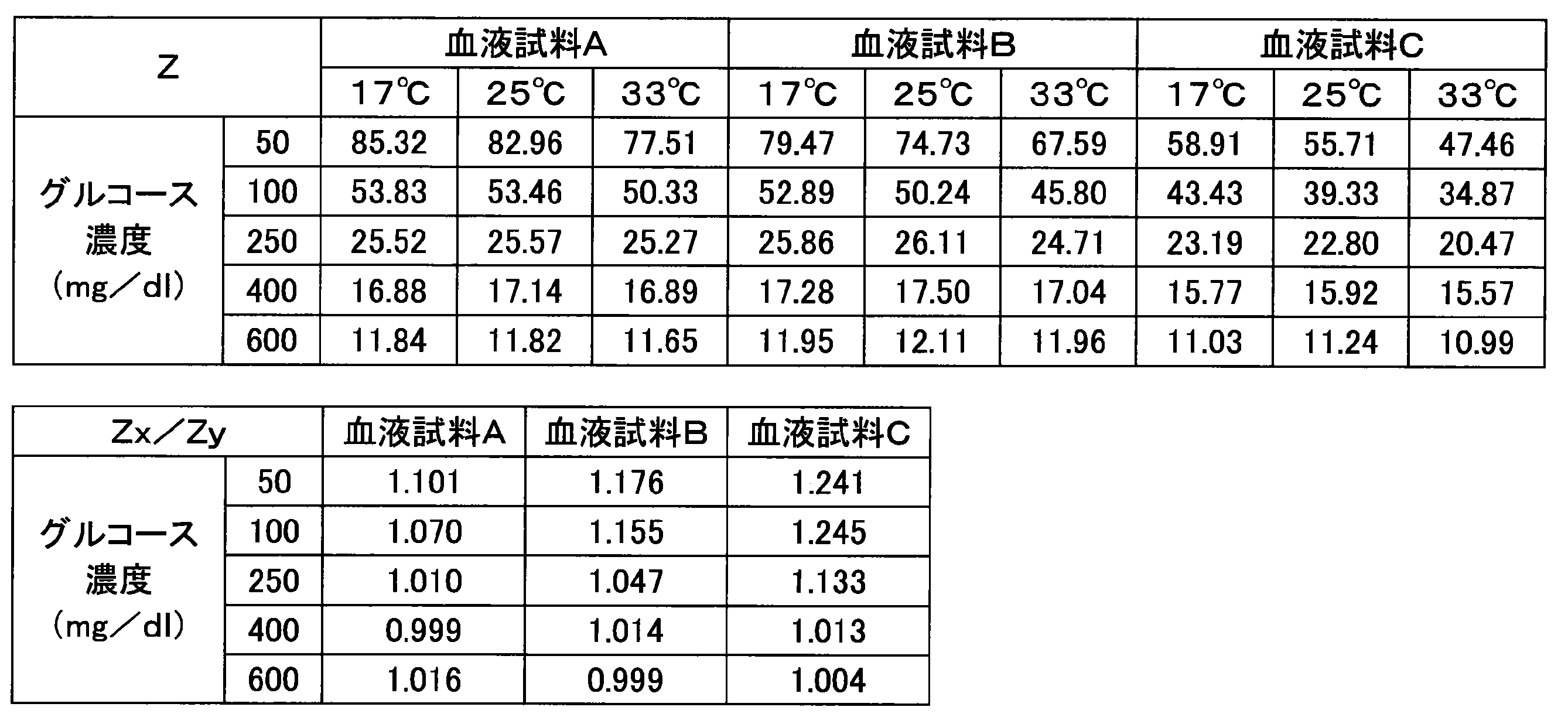
- Table 1 shows the response current value of the glucose response and the response current value of the temperature correction response.
- Table 1 also shows a numerical value (Z) obtained by dividing the response current value of the temperature correction response by the response current value of the glucose response.
- Table 1 shows.
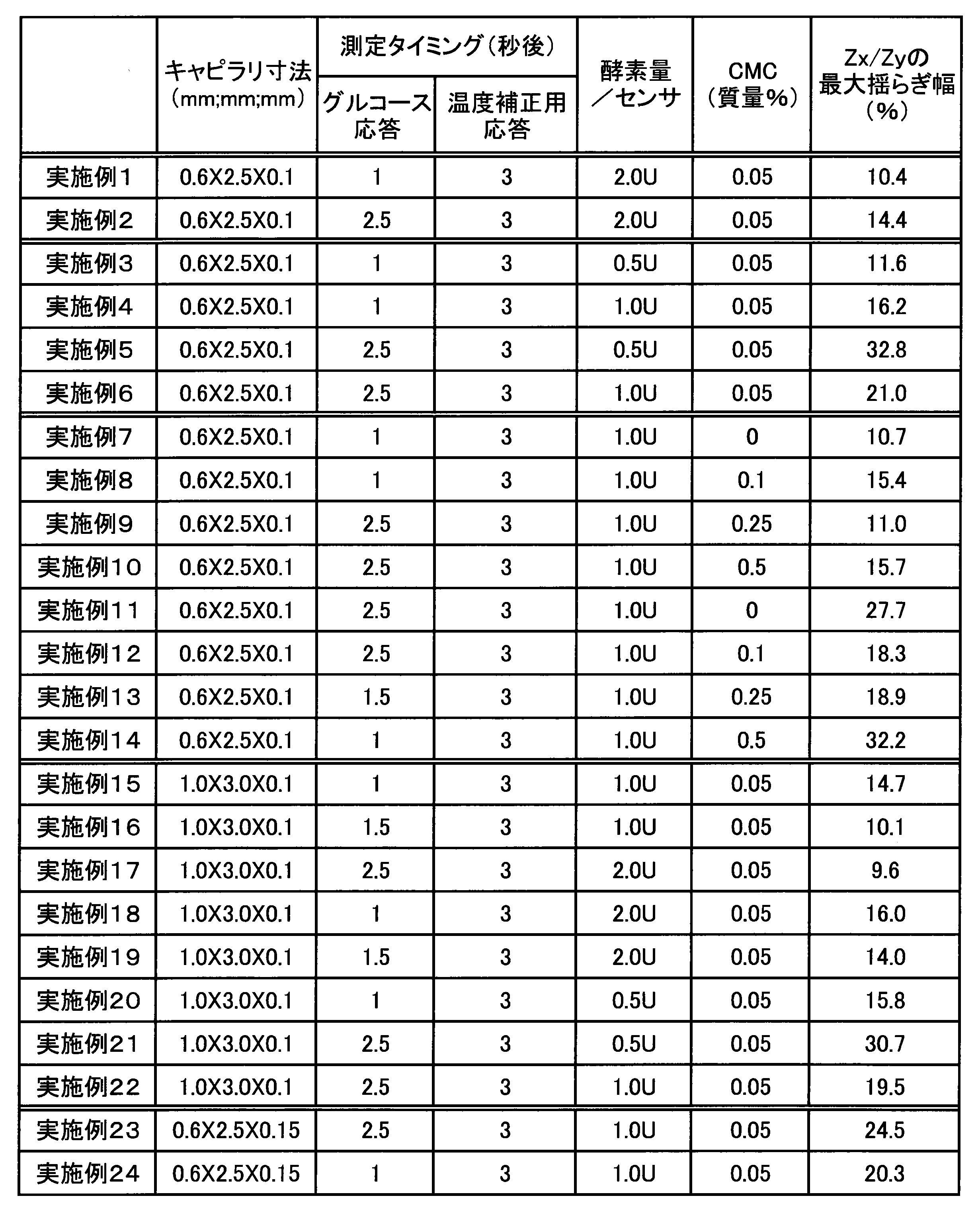
- Table 2 shows the dimensions of the capillary section, the measurement timing of each response, the amount of enzyme, the amount of CMC, and the maximum deviation rate (maximum fluctuation width) from 1.0 of the value of Z x / Z y .
- the maximum fluctuation width of the value of Z x / Z y in Example 1 was in the range of 12% or less.
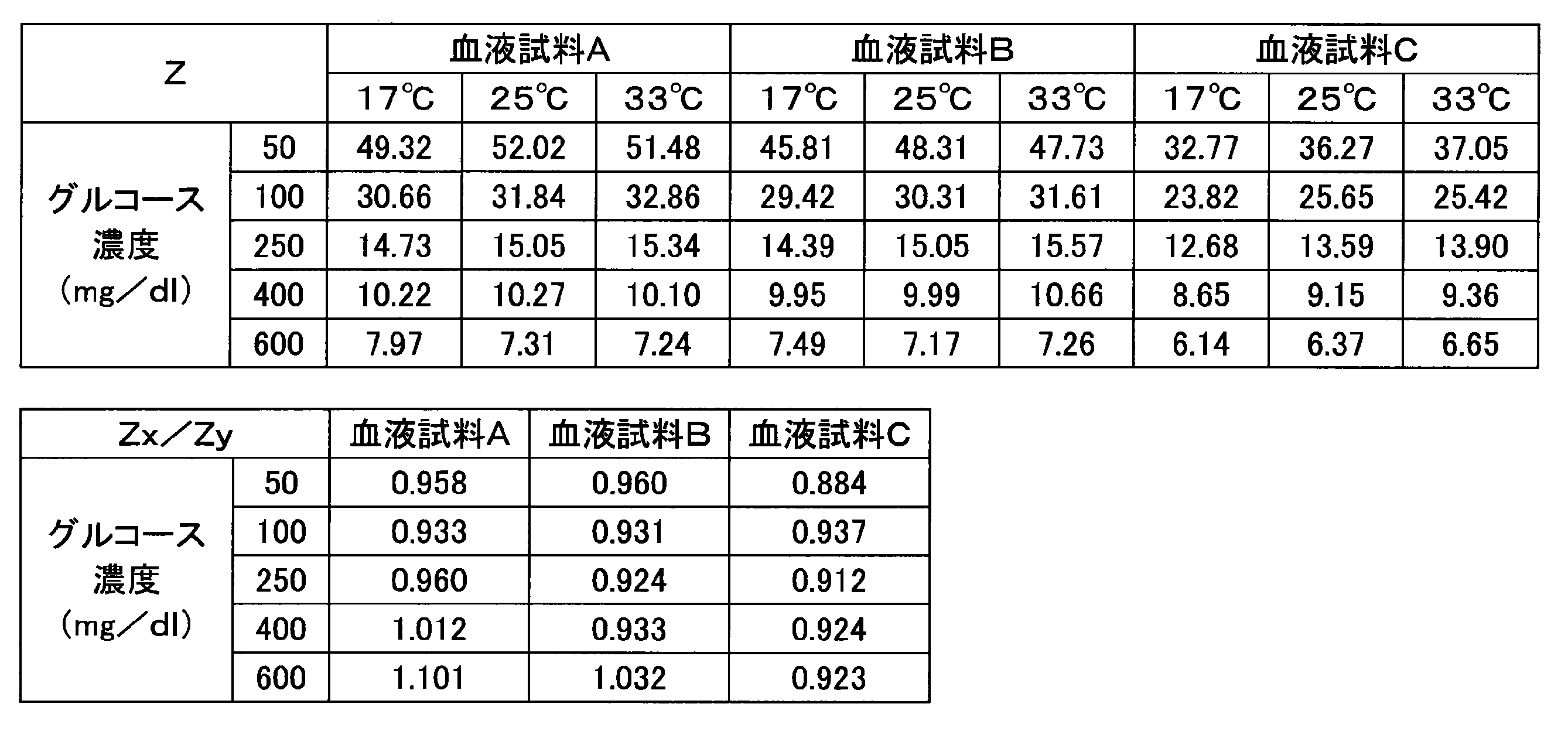
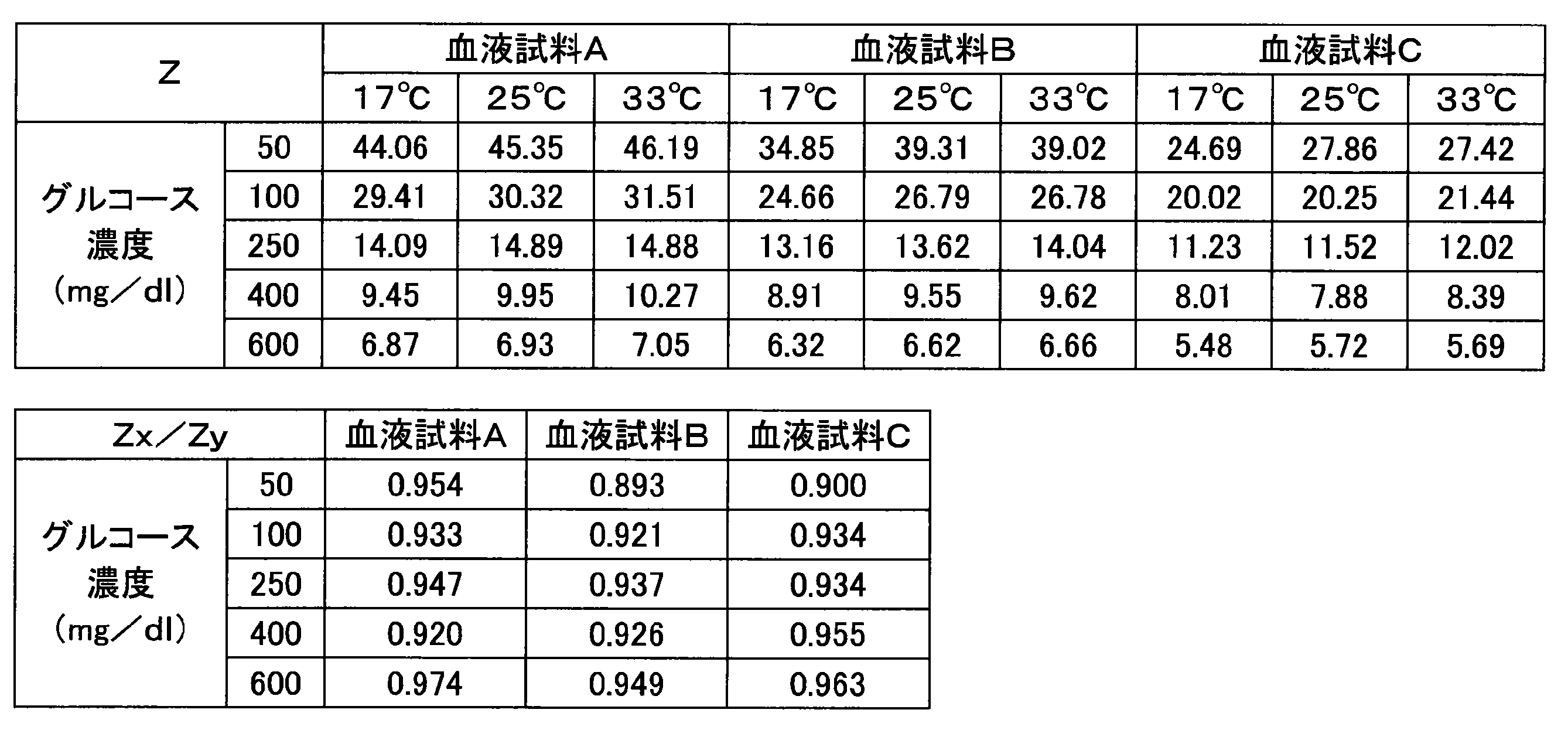
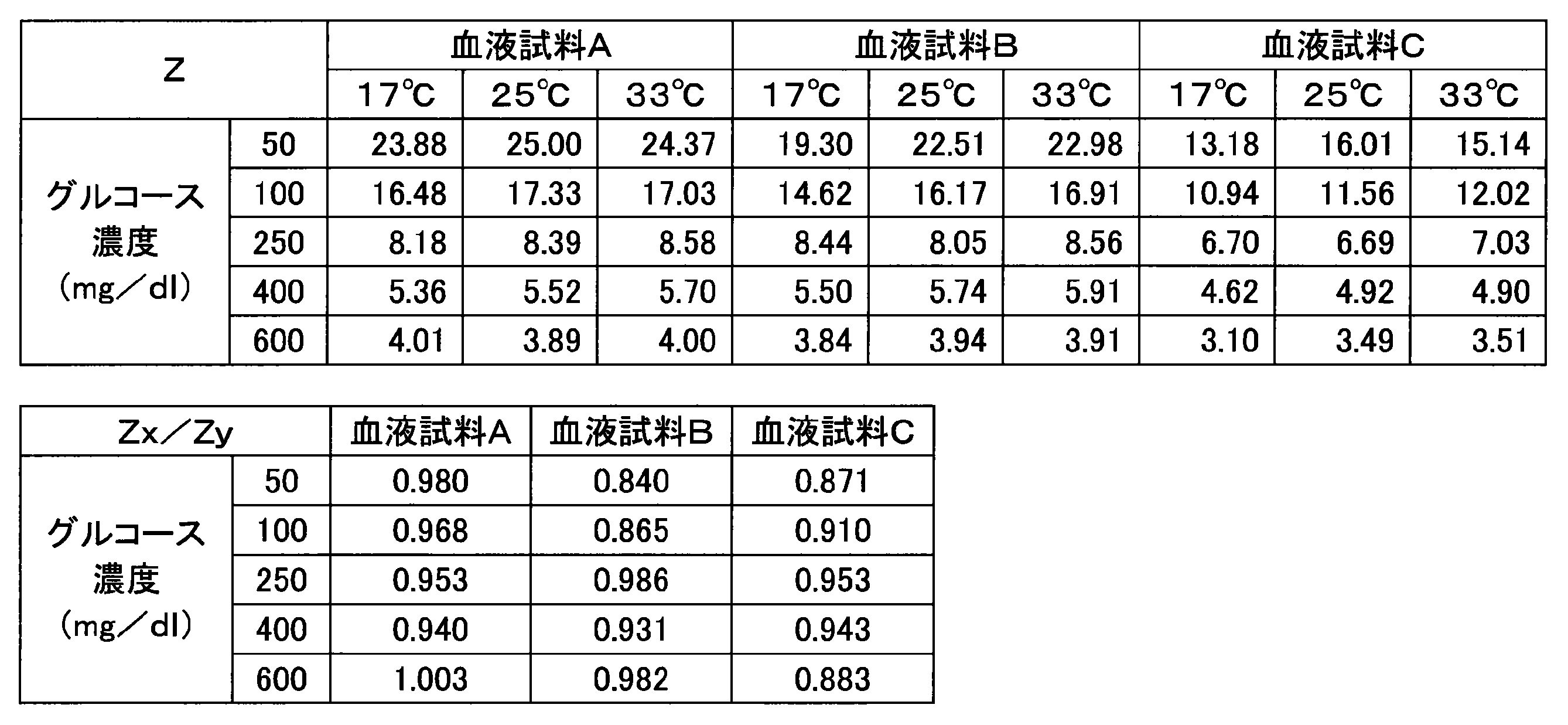
- Example 2 Various current responses were measured in the same manner as in Example 1 except that the glucose response was measured 2.5 seconds after the introduction of the blood sample into the capillary section was completed. Numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 3.
- the maximum fluctuation width of the value of Z x / Z y in Example 2 was in the range of 17% or less.
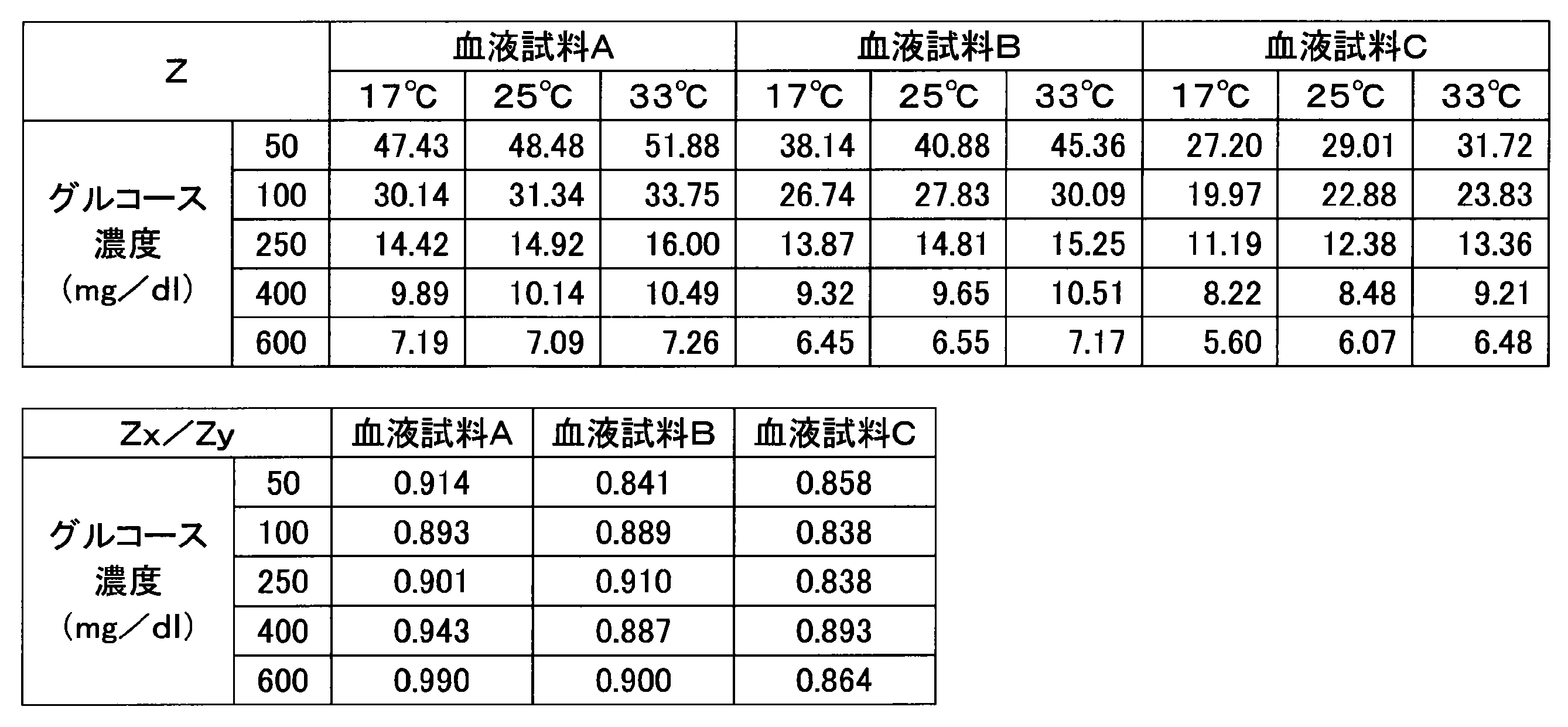
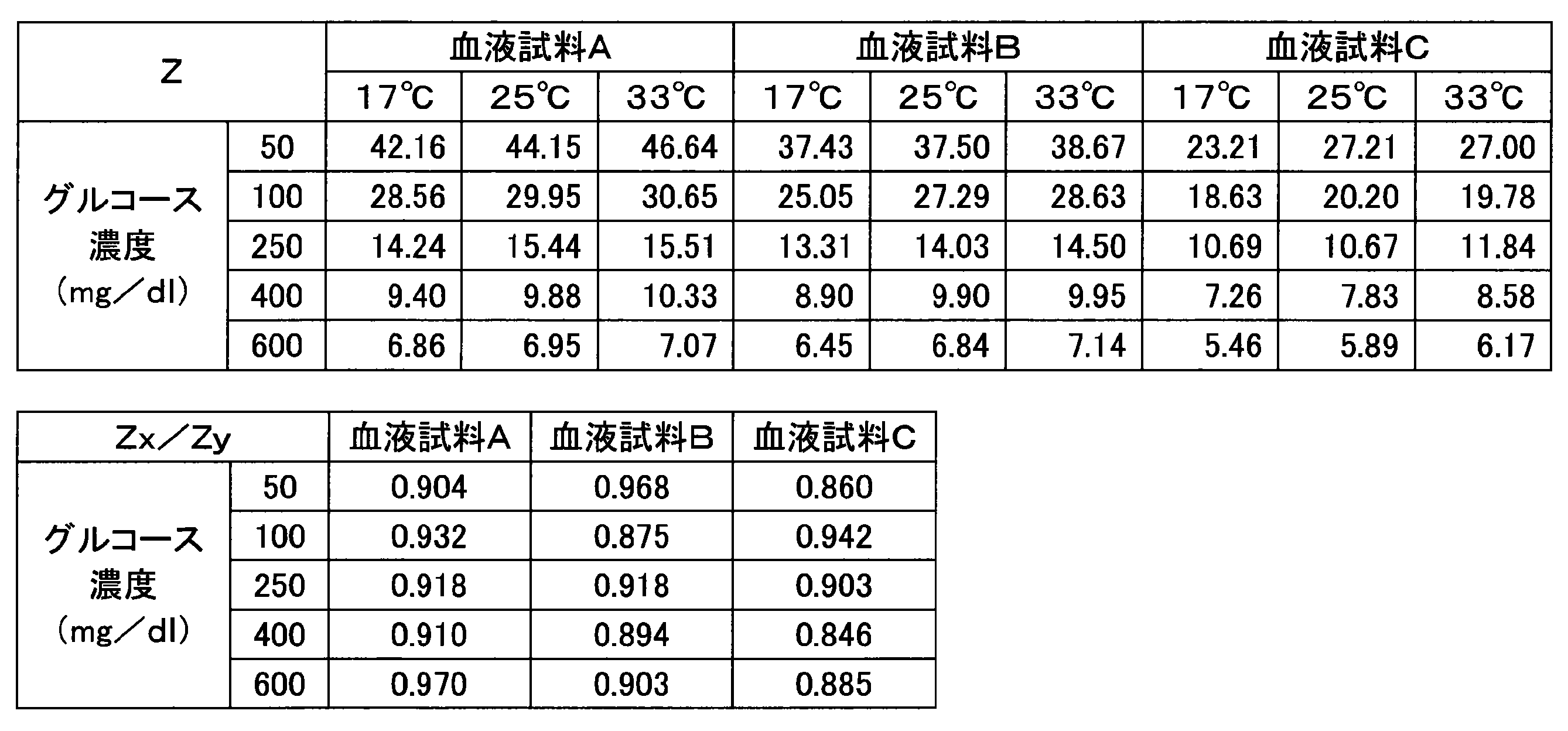
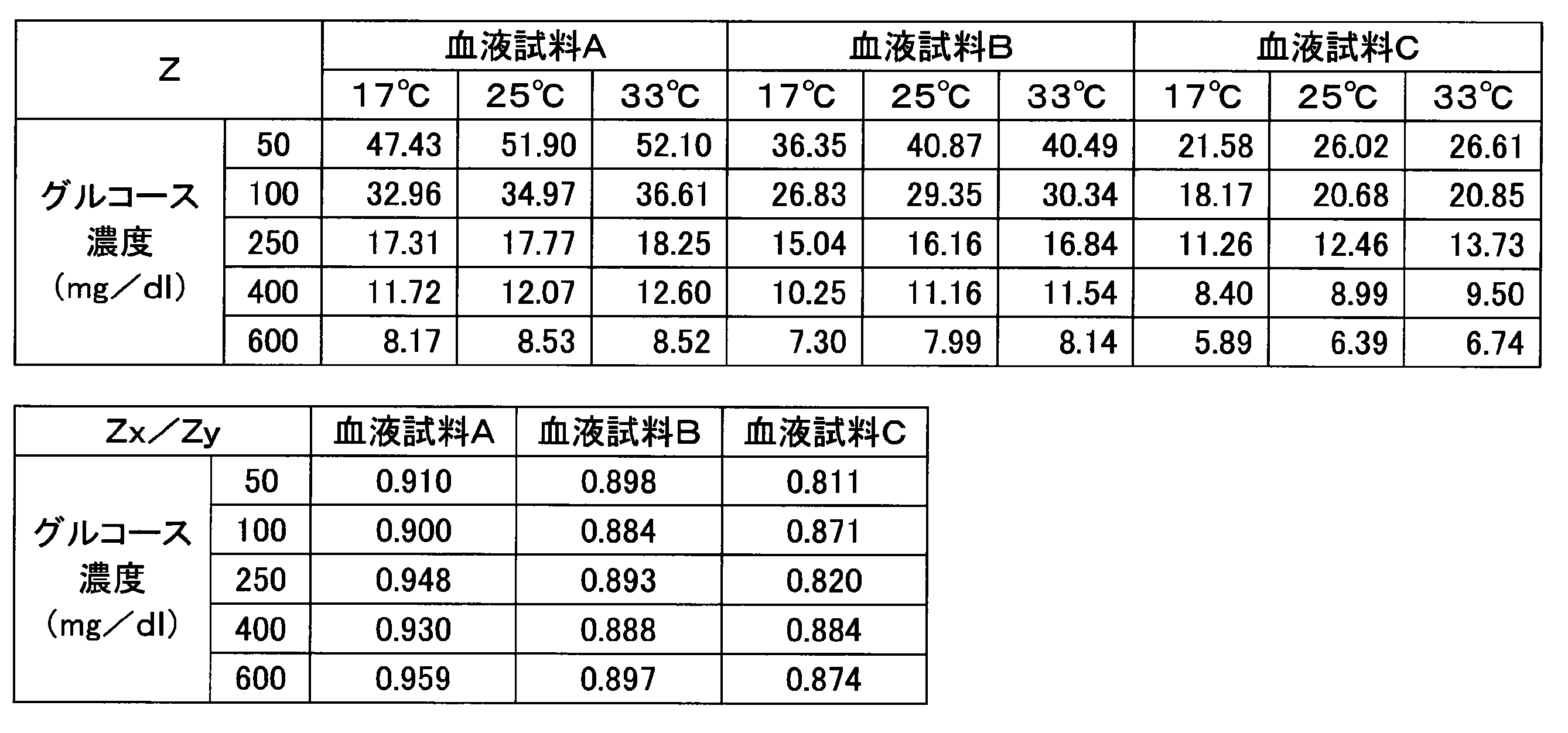
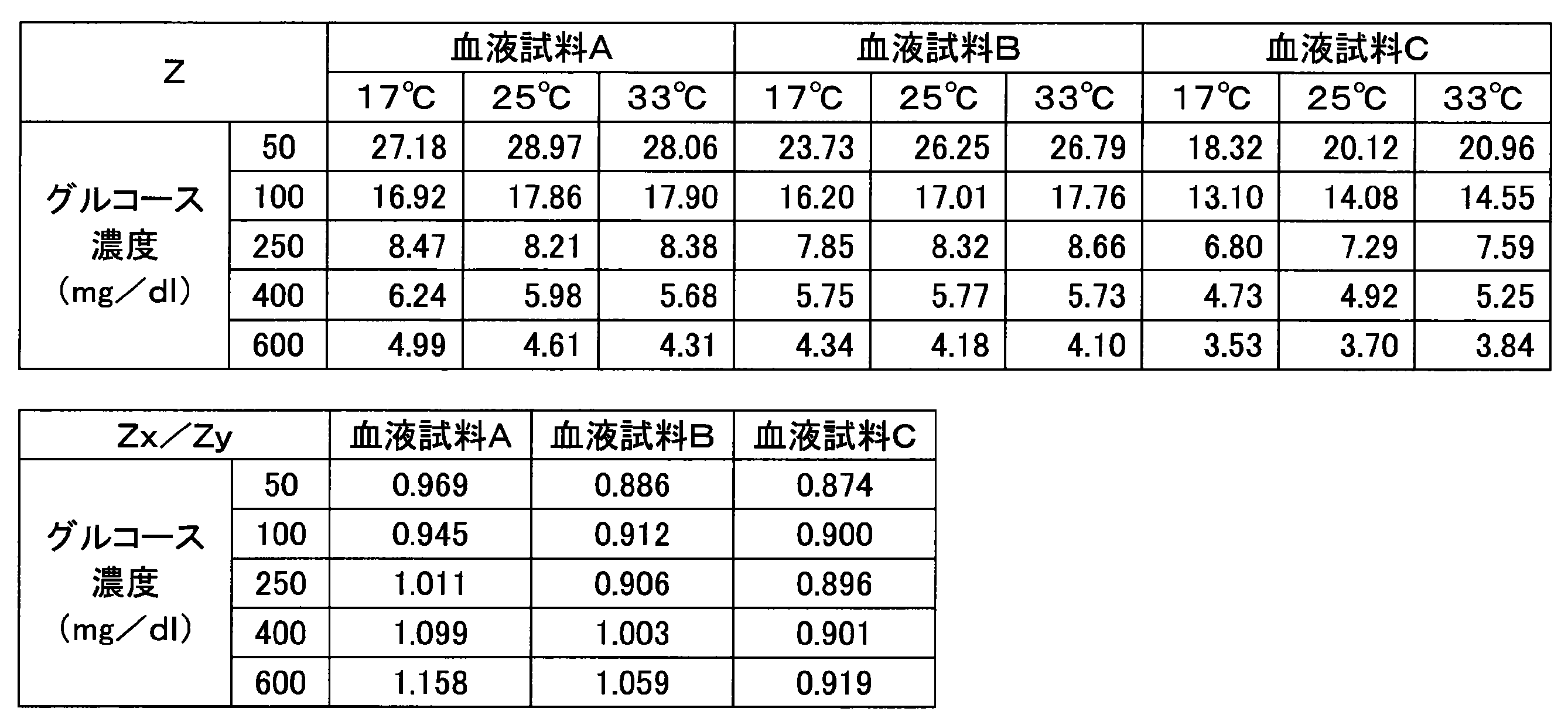
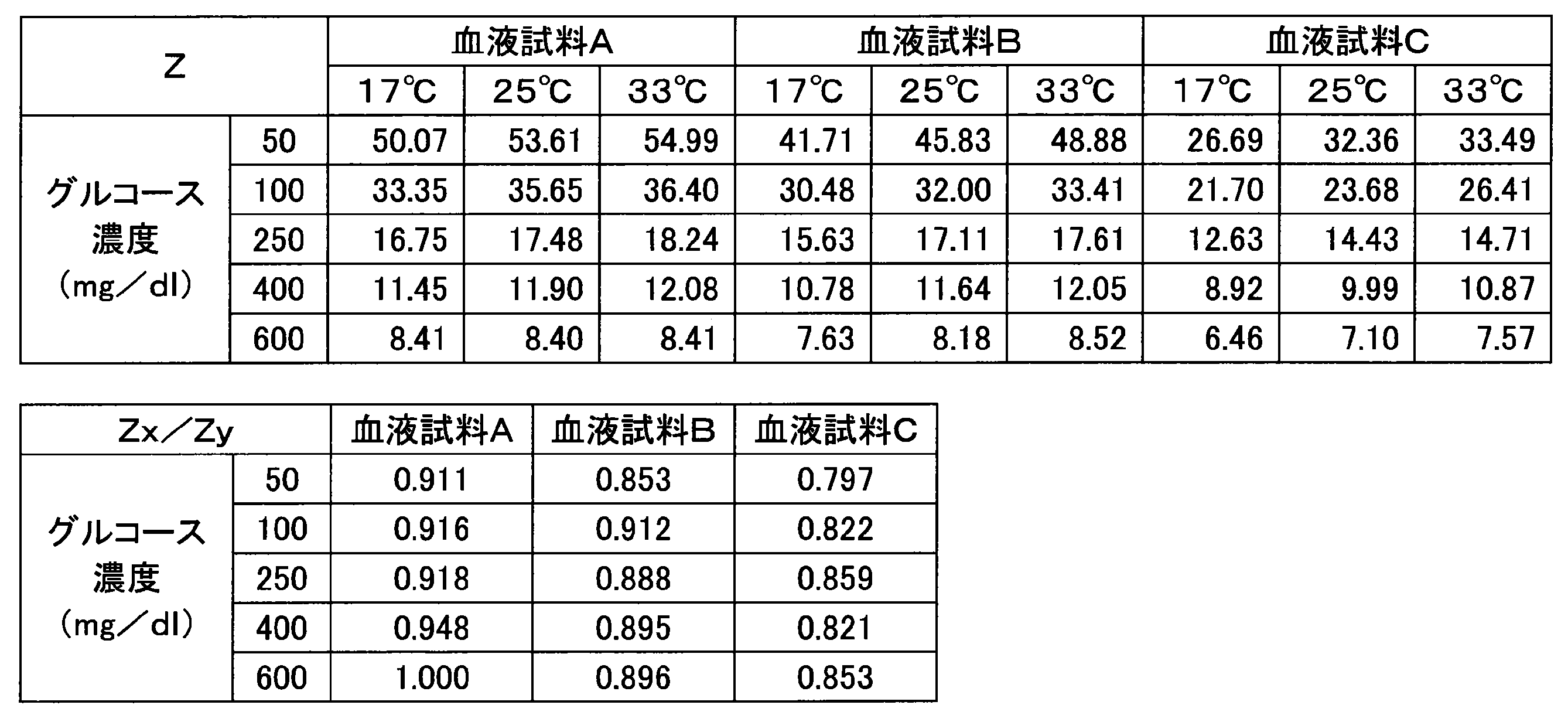
- Example 3 Various current responses were measured in the same manner as in Example 1 except that a sensor chip having an enzyme amount of 0.5 U per sensor was used. Table 4 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 3 was in the range of 12% or less.
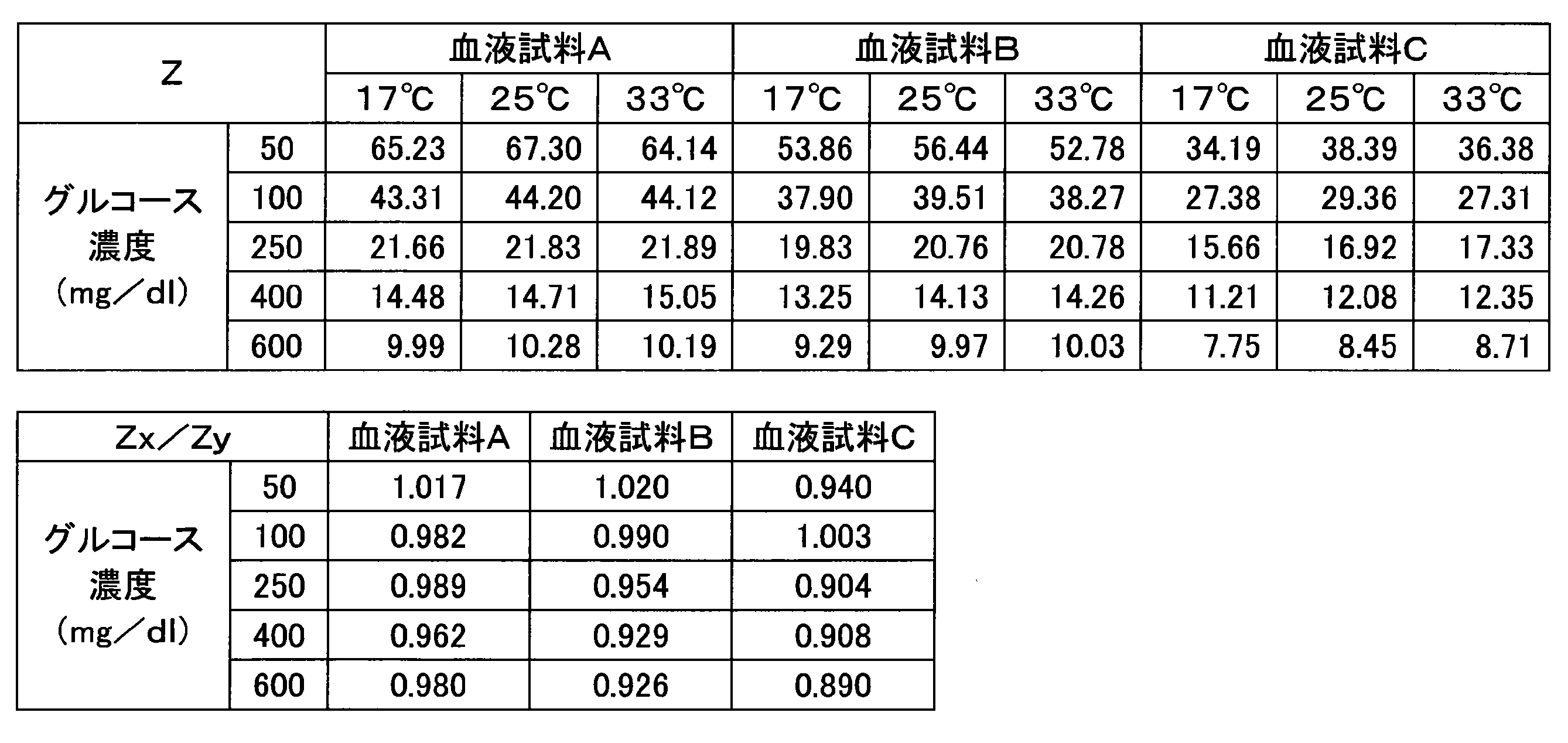
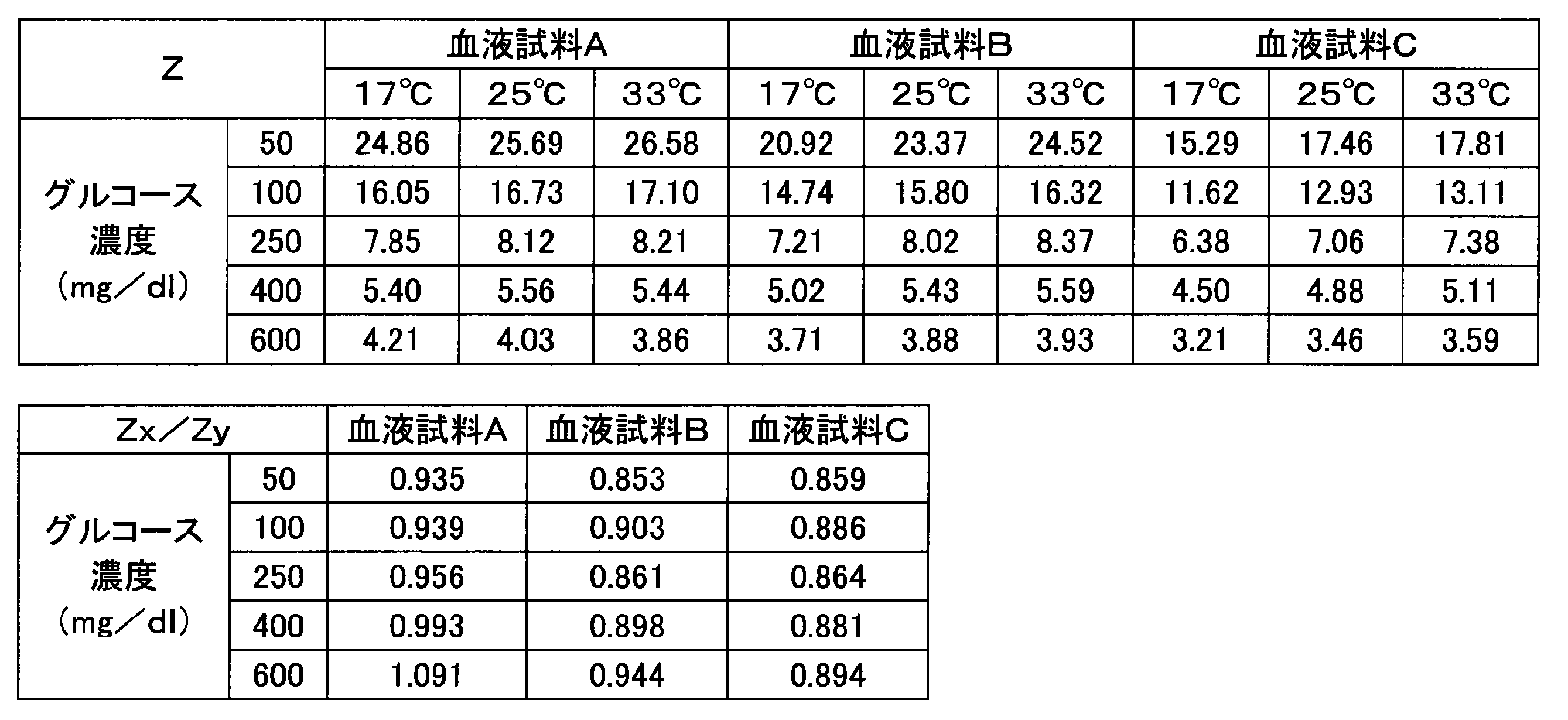
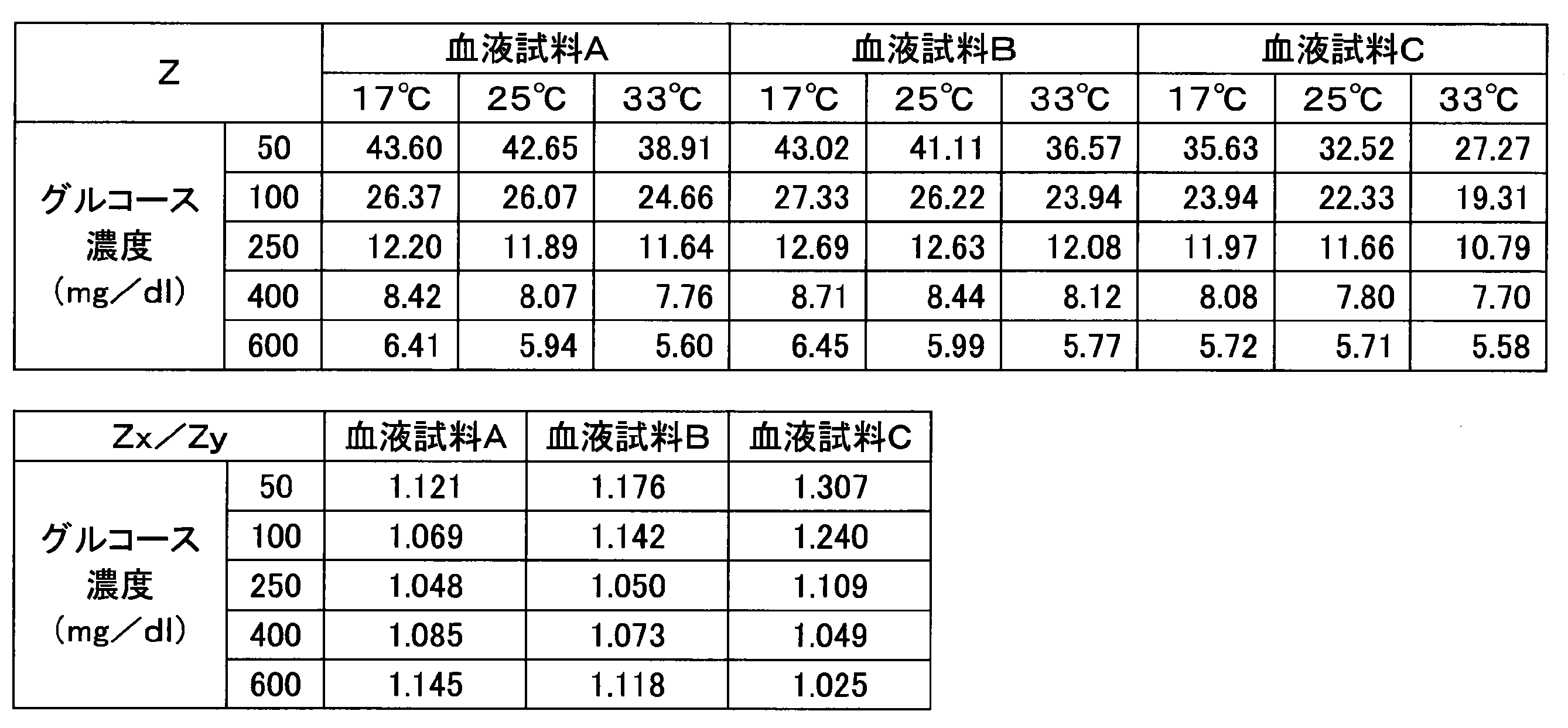
- Example 4 Various current responses were measured in the same manner as in Example 1 except that a sensor chip having an enzyme amount of 1.0 U per sensor was used. Table 5 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 4 was in the range of 17% or less.
- Example 5 Various current responses were measured in the same manner as in Example 3 except that the glucose response was measured 2.5 seconds after the introduction of the blood sample into the capillary part was completed. Numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 6.
- the maximum fluctuation width of the value of Z x / Z y in Example 5 was in a range exceeding 17%.
- Example 6 Various current responses were measured in the same manner as in Example 4 except that the glucose response was measured 2.5 seconds after the introduction of the blood sample into the capillary section was completed.
- the numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 7.
- the maximum fluctuation width of the value of Z x / Z y in Example 6 was in a range exceeding 17%.
- Example 7 Various current responses were measured in the same manner as in Example 4 except that a sensor chip whose reaction reagent layer did not contain CMC was used. The numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 8.
- the maximum fluctuation width of the value of Z x / Z y in Example 7 was in the range of 12% or less.
- Example 8 Various current responses were measured in the same manner as in Example 4 except that a sensor chip having a CMC amount of 0.1% by mass in the reaction reagent layer was used. The numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 9.
- the maximum fluctuation width of the value of Z x / Z y in Example 8 was in the range of 17% or less.
- Example 9 Various current responses were measured in the same manner as in Example 6 except that a sensor chip having a CMC amount of 0.25% by mass in the reaction reagent layer was used. Table 10 shows numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 9 was in the range of 12% or less.
- Example 10 Various current responses were measured in the same manner as in Example 6 except that a sensor chip having a CMC amount of 0.5 mass% in the reaction reagent layer was used. Table 11 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 10 was in the range of 17% or less.
- Example 11 Various current responses were measured in the same manner as in Example 7 except that the glucose response was measured 2.5 seconds after the introduction of the blood sample into the capillary section was completed.
- the numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 12.
- the maximum fluctuation width of the value of Z x / Z y in Example 11 was in a range exceeding 17%.
- Example 12 Various current responses were measured in the same manner as in Example 8 except that the glucose response was measured 2.5 seconds after the introduction of the blood sample into the capillary section was completed.
- the numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 13.
- the maximum fluctuation width of the value of Z x / Z y in Example 12 was in a range exceeding 17%.
- Example 13 Various current responses were measured in the same manner as in Example 9 except that the glucose response was measured 1.5 seconds after the introduction of the blood sample into the capillary section was completed.
- Table 14 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 13 was in a range exceeding 17%.
- Example 14 Various current responses were measured in the same manner as in Example 10 except that the glucose response was measured 1.0 seconds after the introduction of the blood sample into the capillary part was completed.
- the numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 15.
- the maximum fluctuation width of the value of Z x / Z y in Example 14 was in a range exceeding 17%.
- Example 15 Various current responses were measured in the same manner as in Example 4 except that a sensor chip having a capillary part width of 1.0 mm and a length of 3.0 mm was used.
- the numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 16.
- the maximum fluctuation width of the value of Z x / Z y in Example 15 was in the range of 17% or less.
- Example 16 Various current responses were measured in the same manner as in Example 15 except that the glucose response was measured 1.5 seconds after the introduction of the blood sample into the capillary section was completed. Table 17 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 16 was in the range of 12% or less.
- Example 17 Various current responses were measured in the same manner as in Example 2 except that a sensor chip having a capillary part width of 1.0 mm and a length of 3.0 mm was used. Table 18 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 17 was in the range of 12% or less.
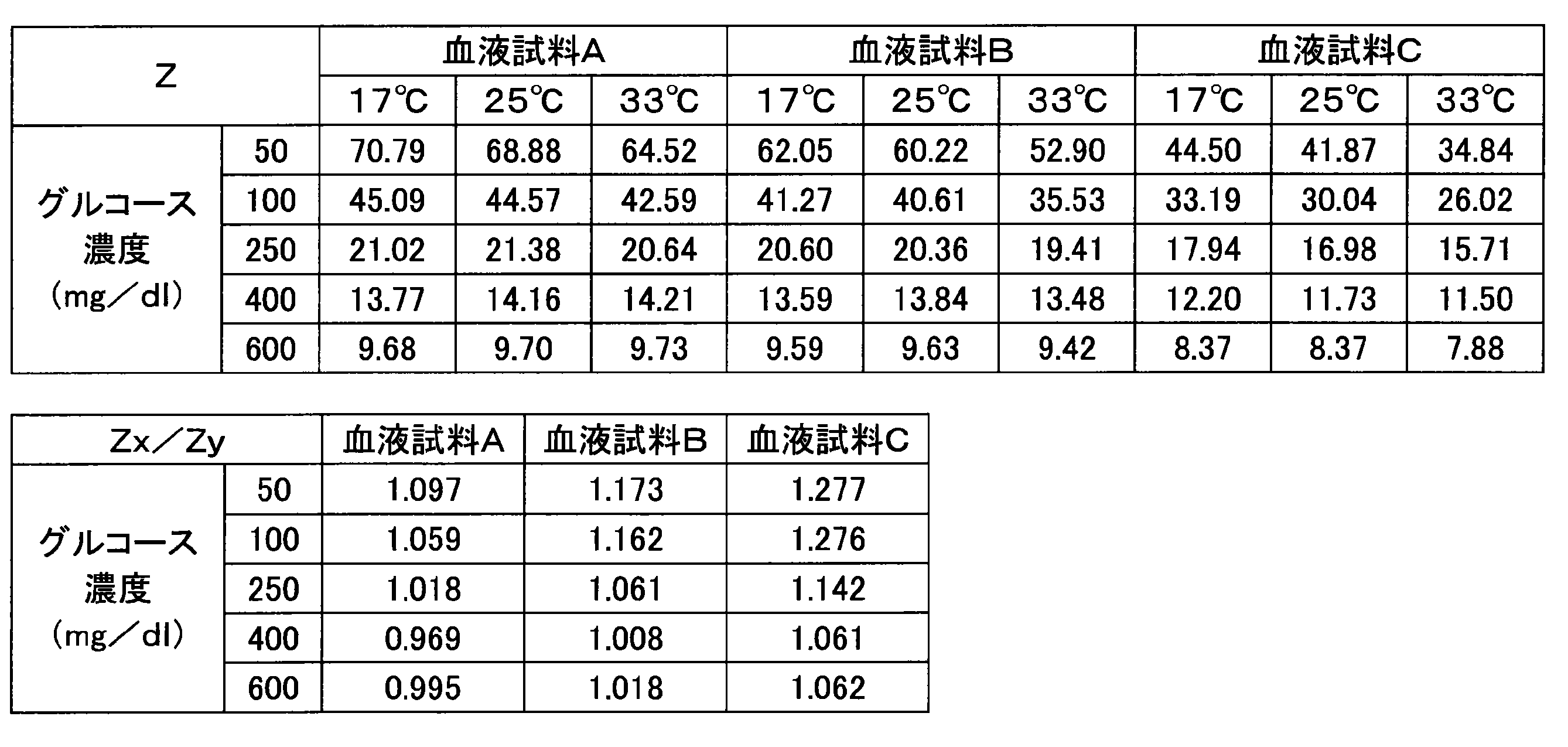
- Example 18 Various current responses were measured in the same manner as in Example 1 except that a sensor chip having a capillary part width of 1.0 mm and a length of 3.0 mm was used. Table 19 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 18 was in the range of 17% or less.
- Example 19 Various current responses were measured in the same manner as in Example 18 except that the glucose response was measured 1.5 seconds after the introduction of the blood sample into the capillary part was completed.
- the numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 20.
- the maximum fluctuation width of the value of Z x / Z y in Example 19 was in the range of 17% or less.
- Example 20 Various current responses were measured in the same manner as in Example 3 except that a sensor chip having a capillary part width of 1.0 mm and a length of 3.0 mm was used. Table 21 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 20 was in the range of 17% or less.
- Example 21 Various current responses were measured in the same manner as in Example 5 except that a sensor chip having a capillary part width of 1.0 mm and a length of 3.0 mm was used.
- the numerical values (Z, Z x / Z y ) obtained from each blood sample are shown in Table 22.
- the maximum fluctuation width of the value of Z x / Z y in Example 21 was in a range exceeding 17%.
- Example 22 Various current responses were measured in the same manner as in Example 6 except that a sensor chip having a capillary part width of 1.0 mm and a length of 3.0 mm was used. Table 23 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 22 was in a range exceeding 17%.
- Example 23 Various current responses were measured in the same manner as in Example 6 except that a sensor chip having a capillary part height of 0.15 mm was used. Table 24 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 23 was in a range exceeding 17%.
- Example 24 Various current responses were measured in the same manner as in Example 4 except that a sensor chip having a capillary part height of 0.15 mm was used. Table 25 shows the numerical values (Z, Z x / Z y ) obtained from each blood sample.
- the maximum fluctuation width of the value of Z x / Z y in Example 24 was in a range exceeding 17%.
- the present invention is very important in various fields where high accuracy of measurement is required to suppress the occurrence of measurement errors due to the temperature of the environment in which the measurement is performed. Has utility value.
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Hematology (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Zoology (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Wood Science & Technology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
本発明は、使用環境の温度に起因する測定誤差の発生を抑制できるバイオセンサシステムを提供する。演算部306を有する測定器101と、測定器101に着脱自在であり、血液試料が導入されるセンサチップ200とを有し、センサチップ200が、血液試料中の分析物を基質とする酸化還元酵素が関与する反応により血液試料中に流れる電流の量に基づいて分析物の濃度に関連するデータaを取得する測定部41(測定部A)と、データaを温度補正するためのデータbを血液試料から取得する測定部42(測定部B)とを有し、演算部306が、データaおよびデータbに基づき、血液試料の温度に応じて補正された、血液試料中の分析物の濃度を決定する機能を有するバイオセンサシステム100とする。
Description
本発明は、バイオセンサシステム、センサチップおよび血液試料中の分析物濃度の測定方法に関する。
血液試料中の分析物の濃度、例えば血中グルコース濃度(血糖値)、を測定するために、演算部を有する測定器と、測定器に着脱自在のセンサチップとを備えた携帯型バイオセンサシステムが用いられている。
分析物の濃度は、分析物を基質とする酸化還元酵素を介した酵素サイクリング反応によって生じる、酸化体または還元体の量に基づいて算出されている。酵素サイクリング反応の速度は、反応が進行している温度(反応温度)に依存する。このため、分析物の濃度は、反応温度に基づいて補正することが望ましい。
反応温度は、例えば、特開2003-156469号公報に記載されるように、測定器に配置された温度センサによって測定される。しかし、特開2003-156469号公報に記載のバイオセンサシステムでは、測定器の内部温度が測定されるので、測定される反応温度は、血液試料の温度を正確に反映しない。このため、分析物濃度の測定に誤差が生じる場合がある。
特開2001-235444号公報、特開2003-42995号公報、国際公開第2003/062812号パンフレットは、反応温度の測定精度の向上を目的とするバイオセンサシステムを開示する。特開2001-235444号公報と特開2003-42995号公報に記載のバイオセンサシステムは、センサチップの血液試料保持部の近傍に熱伝導部材を有しており、この熱伝導部材を介して伝達される血液試料の温度を測定器に配置された温度センサによって検出する。特開2001-235444号公報と特開2003-42995号公報に記載のバイオセンサシステムでは、熱伝導部材と血液試料保持部との間に樹脂板が配置されているため、熱伝導部材が血液試料に接触することはない。国際公開第2003/062812号パンフレットに記載のバイオセンサシステムでは、センサチップを取り付けるための測定器の装着部に温度センサおよび熱伝導部材が配置されており、血液試料の温度が熱伝導部材を介して温度センサに伝達される。
バイオセンサシステムを携帯した使用者が寒暖差の大きな場所を移動(例えば、冬場または夏場に屋外から屋内へ移動)した場合、測定器は、環境温度の急激な変化に追随できず、しばらくの間、移動先の環境よりも高温または低温になる。例えば、特開2003-156469号公報には、40℃または10℃の環境から25℃の環境に測定器を移動させると、測定器の温度が25℃に収束するまでに約30分間もかかることが記載されている。測定器の温度センサによる反応温度の測定において、測定器の温度による影響を完全に排除することは容易でない。このため、特開2001-235444号公報、特開2003-42995号公報、国際公開第2003/062812号パンフレットに記載のバイオセンサシステムにおいても、やはり、センサを使用する環境の温度が急激に変化すると、分析物濃度の測定に誤差が生じやすくなる。また、特開2001-235444号公報、特開2003-42995号公報、国際公開第2003/062812号パンフレットに記載のバイオセンサシステムでは、血液試料の温度が樹脂板および熱伝導部材を介して温度センサに熱伝達されるので、測定される反応温度は、やはり、血液試料の温度を正確に反映しない。
本発明は、使用環境の温度に起因する測定誤差の発生を抑制できるバイオセンサシステム、および当該センサシステムに適したセンサチップの提供を目的とする。また、本発明は、血液試料中の分析物濃度の測定精度を向上できる測定方法の提供を目的とする。
本発明は、演算部を有する測定器と、前記測定器に着脱自在であり、血液試料が導入されるセンサチップと、を有するバイオセンサシステムであって、前記センサチップが、前記血液試料中の分析物を基質とする酸化還元酵素が関与する反応により前記血液試料中に流れる電流の量に基づいて前記分析物の濃度に関連するデータaを取得する測定部Aと、前記データaを温度補正するためのデータbを前記血液試料から取得する測定部Bとを有し、前記演算部が、前記データaおよび前記データbに基づき、前記血液試料の温度に応じて補正された、前記血液試料中の前記分析物の濃度を決定する機能を有する、バイオセンサシステムを提供する。
また、本発明は、別の側面から、上記のバイオセンサシステムにおいて使用され、血液試料が導入されるセンサチップであって、前記血液試料中の分析物を基質とする酸化還元酵素が関与する反応により前記血液試料中に流れる電流の量に基づいて前記分析物の濃度に関連するデータaを取得する測定部Aと、前記データaを温度補正するためのデータbを前記血液試料から取得する測定部Bとを有する、センサチップを提供する。
また、本発明は、別の側面から、血液試料中の分析物を基質とする酸化還元酵素が関与する反応により前記血液試料中に流れる電流の量に基づいて前記分析物の濃度に関連するデータaを取得するステップと、前記データaを温度補正するためのデータbを前記血液試料から取得するステップと、前記データaおよび前記データbに基づき、前記血液試料の温度に応じて補正された、前記血液試料中の前記分析物の濃度を決定するステップとを有する、血液試料中の分析物の濃度の測定方法であって、前記データbを取得するステップが、前記血液試料に接触させた一対の電極に電圧を印加し、前記分析物以外の酸化還元物質の酸化または還元に伴って前記血液試料中に流れる電流の量を測定するステップを含む、血液試料中の分析物の濃度の測定方法を提供する。
分析物濃度を温度補正するためのデータを血液試料から直接取得することによって、血液試料中の分析物濃度の測定において、当該測定を実施する環境の温度に起因した測定誤差の発生をより確実に回避できる。したがって、本発明によれば、血液試料中の分析物濃度の測定精度が高まる。
本発明によるバイオセンサシステムは、センサチップに配置された測定部によって、分析物濃度を温度補正するためのデータを血液試料から取得する。
図1は、本発明によるバイオセンサシステムの一例を説明するための図である。このバイオセンサシステム100は、直方体状の測定器101と、センサチップ200とを有している。測定器101の側壁面には、矩形状の孔である装着口102が形成されている。センサチップ200は、装着口102に着脱自在な状態で装着され測定器101に接続されている。測定器101の一方の主面の略中央部には、測定結果を表示するための表示部103が配置されている。
図2はセンサチップ200の分解斜視図であり、図3はその平面図である。このセンサチップ200は、矩形状の切欠部204が形成されたスペーサー202を介してかつ絶縁基板201の一方の端部(図において右側の端部)を残して、絶縁基板201上にカバー203が配置されている。
各部材201、202、203は、例えば接着または熱溶着によって一体化されている。スペーサー202の切欠部204は、各部材の一体化後には、血液試料を保持するキャピラリ部40となる。キャピラリ部40は、チップ200の長辺に沿って伸長し、スペーサー202の一方の端部(図において左側の端部)において外部に連通している。換言すれば、キャピラリ部40は、チップ200の外部に開口する血液試料導入口16と連通している。そして、カバー203は、キャピラリ部40における外部に連通する端と反対側の端に対応する部分に排気口15を有している。これにより、毛管現象によって血液試料を試料導入口16からキャピラリ部40の内部に容易に吸引できる。
絶縁基板201上には、電極11、12、13、14が、それぞれの一部分(部分31、32、33、34)がキャピラリ部40に面するように配置されている。電極11の部分31は、電極12の部分32および電極13の部分33よりも血液試料導入口16に近接する位置に配置されている。電極13の部分33は、U字状に分岐した電極13の一部であり、電極12の部分32を挟む位置に配置されている。絶縁基板201上には、電極12の部分32および電極13の部分33を覆うように、反応試薬層20が形成されている。反応試薬層20は、血液試料中の分析物を基質とする酸化還元酵素を含有する。反応試薬層20は、電極11の部分31から離れた位置に形成されている。
センサチップ200は、電極12の部分32および電極13の部分33によって構成される電極系と、反応試薬層20ならびに部分32および部分33を収容するキャピラリ部40の一部の空間とによって構成された、測定部41(測定部A)を有する。さらに、センサチップ200は、電極11の部分31および電極12の部分32によって構成される電極系と、部分31および部分32を収容するキャピラリ部40の一部の空間とによって構成された、測定部42(測定部B)を有する。
測定部Aは、後述するように、酸化還元酵素が関与する反応により血液試料中に流れる電流の量に基づいて、血液試料中の分析物の濃度に関連するデータaを取得する。そして、測定部Bは、後述するように、データaを温度補正するためのデータbを、より具体的には、データaの取得に使用する酸化還元酵素が関与しない反応であって分析物以外の酸化還元物質の酸化または還元に伴って血液試料中に流れる電流の量に関連するデータbを、血液試料から取得する。このように、測定部Bは、血液試料に接する部材、より具体的には血液試料に接する電極、を用いてデータbを取得する状態にあってよい。ここで、電流の量に関連するデータとは当該電流の量または当該電流量の換算値を意味する。分析物以外の酸化還元物質としては、アスコルビン酸、尿酸、アセトアミノフェン、フェリシアン化物、p-ベンゾキノン、p-ベンゾキノン誘導体、酸化型フェナジンメトサルフェート、メチレンブルー、フェリシニウムおよびフェリシニウム誘導体から選ばれる少なくとも1種を例示できる。分析物以外の酸化還元物質は溶媒、例えば血液試料の場合は、水であってもよい。
測定部Aでは、電極12は作用極として、電極13は対極として機能する。測定部Bでは、電極12は対極として、電極11は作用極として機能する。測定部Aおよび測定部Bは、図示のように電極12を共有した状態にあってもよいし、一対の電極をそれぞれ有した状態にあってもよい。このように、センサチップ200は、血液試料に電圧を印加する電極を測定部Bが有する。
電極14の部分34は、キャピラリ部40の奥側の端部近傍に、換言すれば、外部に連通する端と反対側の端の近傍に配置されている。電極14と電極11との間に電圧を印加することにより、血液試料がキャピラリ部40の奥にまで導入されたことを容易に検知できる。なお、電極11に代えて電極12または電極13と、電極14との間に電圧を印加してもよい。
電極11、12、13、14は、それぞれリード(図示せず)と連結している。リードの一端は、各電極間に電圧を印加できるように、スペーサー202およびカバー203で覆われていない絶縁基板201の端部においてチップ200の外部に露出している。
血液試料中の分析物としては、血球を除く物質、例えば、グルコース、アルブミン、乳酸、ビリルビンおよびコレステロールが挙げられる。酸化還元酵素は、対象とする分析物を基質とするものを使用する。酸化還元酵素としては、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、ラクテートオキシダーゼ、ラクテートデヒドロゲナーゼ、ビリルビンオキシダーゼおよびコレステロールオキシダーゼを例示できる。反応試薬層中の酸化還元酵素の量としては、0.01~100ユニット(U)、好ましくは0.05~10U、より好ましくは0.1~5Uの範囲を例示できる。
反応試薬層20は、フェリシアン化カリウム、p-ベンゾキノン、p-ベンゾキノン誘導体、酸化型フェナジンメトサルフェート、メチレンブルー、フェリシニウムおよびフェリシニウム誘導体といった、酵素反応にて生じた電子を電極に受け渡す機能を有する電子メディエータを含有することが望ましい。反応試薬層20は、反応試薬層の成形性を高めるために、水溶性高分子化合物を含有してもよい。水溶性高分子化合物としては、カルボキシメチルセルロース(CMC)、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、メチルセルロース、エチルセルロース、エチルヒドロキシエチルセルロース、カルボキシエチルセルロース、ポリビニルアルコール、ポリビニルピロリドンおよびポリジンといったポリアミノ酸、ポリスチレンスルホン酸、ゼラチンおよびその誘導体、ポリアクリル酸およびその塩、ポリメタクリル酸およびその塩、スターチおよびその誘導体、無水マレイン酸重合体およびその塩、アガロースゲルおよびその誘導体、から選ばれる少なくとも1種を例示できる。
絶縁基板201、スペーサー202およびカバー203の材料としては、ポリエチレンテレフタレート、ポリカーボネート、ポリイミド、ポリエチレン、ポリプロピレン、ポリスチレン、ポリ塩化ビニル、ポリオキシメチレン、モノマーキャストナイロン、ポリブチレンテレフタレート、メタクリル樹脂およびABS樹脂といった樹脂、さらにはガラスを例示できる。
電極11、12、13、14は、パラジウム、白金、金、銀、チタン、銅、ニッケルおよび炭素といった、公知の導電性材料により構成できる。
図4は、バイオセンサシステム100における、血液試料中の分析物濃度を測定するための回路構成の一例を示す図である。測定器101は、センサチップ200における電極11、12、13、14のうち少なくとも2つの電極間に電圧を印加する制御回路300と、測定器の表示部に相当する液晶表示装置(LCD)400とを有している。
制御回路300は、4つのコネクタ301a、301b、301c、301dと、切換回路302と、電流/電圧変換回路303と、アナログ/デジタル(A/D)変換回路304と、基準電圧源305と、演算部306とを有している。制御回路300は、切り替え回路302を介して、1つの電極を正極または負極として使用できるように、当該電極に印加する電位を切り換えることができる。
演算部306は、公知の中央演算装置(CPU)と、上記のデータaおよびデータbに基づき血液試料中の分析物濃度を決定するための換算テーブルとを有する。従来のバイオセンサシステムでは、環境温度に基づく補正係数が記述された換算テーブルを参照することによって、分析物濃度が補正されていた。より具体的には、従来のバイオセンサシステムでは、仮測定用の換算テーブルを参照して分析物濃度が仮算出された後、温度補正用の換算テーブルを参照して分析物濃度が補正されていた。本発明者は、血液試料の温度が変動した場合、酸化還元酵素が関与する反応により血液試料中に流れる電流の量と、当該酸化還元酵素が関与しない反応であって分析物以外の酸化還元物質の酸化または還元に伴って血液試料中に流れる電流の量とが同様に変動し得ることを見出した。そして、後述するように、バイオセンサシステムを適切に設計することによって、この関係を利用して構築した換算テーブルに基づき、血液試料等の温度を測定することなく、分析物濃度の測定における血液試料の温度の影響を排除できる。
演算部306は、こうして構築した1つの換算テーブルを格納した状態にあり、血液試料等の温度ごとに構築された複数の換算テーブルを格納した状態にはない。図5は、演算部306が有する換算テーブルの一例を示す図であり、図6はその別例を示す図である。演算部306が有する換算テーブルには、図5に示すように、分析物濃度が明らかでありかつ温度が1つの値に固定された基準血液試料から上記のデータaの取得と同様の電圧印加条件によって取得した、基準血液試料中を流れる電流の量に関連するデータcと、基準血液試料から上記のデータbの取得と同様の電圧印加条件によって取得した、基準血液試料中を流れる電流の量に関連するデータdと、データcおよびデータdに対応する基準血液試料中の分析物濃度とからなる3種類のデータが記述されていてよい。電流の量に関連するデータとは、上記のとおり、当該電流の量または当該電流量の換算値を意味する。演算部306が有する換算テーブルには、図6に示すように、データcおよびデータdに代えて、データcおよびデータdに基づく1つの換算値が記述されていてもよい。より具体的には、この換算テーブルには、データcおよびデータdに代えてデータcをデータdで除算することによって得たデータと、データcおよびデータdに対応する分析物濃度とからなる2種類のデータが記述されていてもよい。このように、演算部306が有する換算テーブルは、血液試料の温度または環境温度と、分析物濃度との関連性が記述された状態にはない。換算テーブルは、バイオセンサシステムごとに用意することが望ましい。基準血液試料の温度は、後述するように、10℃を超え40℃未満の範囲、さらには17℃以上33℃以下の範囲、にあることが好ましい。
バイオセンサシステム100を用いた血液試料中の分析物濃度の測定は、例えば次のようにして実施する。
まず、演算部306のCPUの指令により、電極13がコネクタ301cを介して電流/電圧変換回路303に接続され、電極14がコネクタ301bを介して基準電圧源305に接続される。その後、CPUの指令により、両電極間に一定の電圧が印加される。当該電圧は、例えば、電極14を正極、電極13を負極と表示したときに0.01~2V、好ましくは0.1~1V、より好ましくは0.2~0.5Vの大きさとなる電圧である。この電圧は、センサチップが測定部に挿入されてから、血液試料がキャピラリ部40の奥まで導入されるまでの間、印加される。センサチップ200の血液試料導入口からキャピラリ部40に血液試料が導入されると、電極14と電極13との間に電流が流れる。そのときの単位時間当たりの電流の増加量を識別することによって、キャピラリ部が血液試料にて満たされたことを検知する。この電流の値は、電流/電圧変換回路303により電圧値に変換された後にA/D変換回路304によりデジタル値に変換されCPUに入力される。CPUは、このデジタル値に基づいて血液試料がキャピラリ部の奥にまで導入されたことを検知する。
血液試料の導入後、例えば、0~60秒、好ましくは0~30秒、より好ましくは0~15秒の範囲で、血液試料中の分析物と酸化還元酵素とを反応させる。
続いて、次のようにして上記のデータaを取得する。まず、CPUの指令により、切換回路302が作動して、電極12がコネクタ301aを介して電流/電圧変換回路303に接続され、電極13がコネクタ301cを介して基準電圧源305に接続される。その後、CPUの指令により、測定部Aにおける測定シーケンスが入力される。その際、当該電圧は、例えば、電極12を正極、電極13を負極と表示したときに0.05~1V、好ましくは0.1~0.8V、より好ましくは0.2~0.6Vの大きさとなる電圧である。電圧の印加時間は0.1~30秒、好ましくは0.1~15秒、より好ましくは0.1~5秒の範囲にある。当該電圧の印加に伴って両電極間に流れた電流量は、データaの取得を指示する信号が制御回路から測定部Aに与えられることによって、電流/電圧変換回路303により電圧値に変換された後にA/D変換回路304によりデジタル値に変換されCPUに入力され、データaとして演算部306のメモリに格納される。分析物濃度の測定を迅速化する観点からは、制御回路は、血液試料がセンサチップのキャピラリ部に導入された時点から0.5秒以上2.5秒未満の範囲内に、データaの取得を指示する信号を測定部Aに与えることが好ましい。
その後、次のようにして上記のデータbを取得する。まず、CPUの指令により、切換回路303が作動して、電極11がコネクタ301dを介して電流/電圧変換回路303に接続され、電極12がコネクタ301aを介して基準電圧源305に接続される。続いて、CPUの指令により、測定部Bにおける両電極間に一定の電圧が印加される。当該電圧は、例えば、電極11を正極、電極12を負極と表示したときに0.1~5V、好ましくは0.2~3V、より好ましくは0.5~2.5Vの大きさとなる電圧である。電圧の印加時間は0.1~30秒、好ましくは0.1~10秒、より好ましくは0.1~5秒の範囲にある。当該電圧の印加に伴って両電極間に流れた電流量は、データbの取得を指示する信号が制御回路から測定部Bに与えられることによって、電流/電圧変換回路303により電圧値に変換された後にA/D変換回路304によりデジタル値に変換されCPUに入力され、データbとして演算部306のメモリに格納される。なお、データbはデータaよりも先に取得してもよく、その際には、データb取得の際の対極上には還元型のメディエータが生成されることを考慮し、データa取得の際の作用極を対極に用いることは好ましくなく、データa取得の際の対極を用いることが好ましい。また、データa取得に用いる電極とは異なる独立した電極を対極として配置しても良い。その際、対極上に酸化型メディエータが配置されていることが好ましい。データaおよびデータbの取得の際に1つの電極を作用極および対極として使用する場合、当該電極の表面における酸化還元反応が律速段階になることがあるので、こうした不具合を回避する観点からは、データbはデータaよりも後に取得することが好ましい。さらに、こうした順序でデータbを取得することによって、データaの取得に使用する酸化還元酵素が関与しない反応であって分析物以外の酸化還元物質の酸化または還元に伴って血液試料中に流れる電流の量をより確実に検出できる。
続いて、演算部306が、換算テーブルを参照し、データaおよびデータbに基づき血液試料中の分析物濃度を決定する。そして、決定された分析物濃度が、LCD400に画像表示される。当該決定のための演算プログラムは、換算テーブルのデータ構造に応じて適宜設計すればよい。データaおよびデータbに完全に一致する数値データが換算テーブルに記述されていない場合、当該換算テーブルに記述されデータaおよびデータbに近似するデータから、公知の線形補間法を用いることによって分析物濃度を決定すればよい。
本発明によるバイオセンサシステムによれば、温度が17℃である血液試料Xと、血液試料Xと同一の成分を有しつつ温度が33℃である血液試料Yとにおいて、データbの値をデータaの値で除算することによって得られる数値(Z)が略一定になる程度にまで、分析物濃度の測定における血液試料の温度の影響を排除し得る。より具体的には、血液試料Xおよび血液試料Yから得られる当該数値をそれぞれZXおよびZYと表示したとき、ZX/ZYで表示される数値が1.0の近傍にあり得る。血液中のグルコース濃度を測定する場合の、血液試料Xおよび血液試料Yにおける分析物濃度は、0mg/dlよりも大きく1000mg/dl以下の範囲にあればよく、例えば10mg/dl以上600mg/dl以下の範囲にあればよい。
分析物濃度の測定における血液試料の温度の影響を上記程度にまで排除するためには、バイオセンサシステムを適切に設計する必要がある。より具体的には、反応試薬層の組成、酸化還元酵素が関与する反応により血液試料中に流れる電流の量を測定するタイミング、およびキャピラリ部の寸法といった種々のパラメータを制御する。
例えば、反応試薬層が水溶性高分子化合物を含有しない、または反応試薬層中の水溶性高分子化合物の量が0.2質量%未満である場合は、測定器が、血液試料がセンサチップに導入された時から0.5秒以上2.5秒未満の範囲内にデータaの取得を指示する信号を測定部Aに与える制御回路を有することが好ましい。また例えば、反応試薬層中の水溶性高分子化合物の量が0.2質量%以上である場合は、測定器が、血液試料がセンサチップに導入された時から2.5秒以上経過した後にデータaの取得を指示する信号を測定部Aに与える制御回路を有することが好ましい。この理由は現時点では定かではないが、本発明者は次のように考えている。反応試薬層が水溶性高分子化合物を0.2質量%以上含有すると、反応試薬層中の反応に寄与する試薬が血液試料に溶出する溶解速度が遅く、またその拡散速度も遅く円滑に反応が進行するに至るまでに2.5秒以上かかる。後述する実施例に示すように、キャピラリの幅が0.8mm以下の範囲にある場合、当該設計を採用することが望ましい。なお、反応試薬層中の水溶性高分子化合物の量が0.2質量%以上である場合、水溶性高分子化合物の含有量の上限としては2質量%を例示でき、データaの取得の指示のための時間の上限としては、15秒を例示できる。
また例えば、反応試薬層中の酵素量が1.8U以上でありキャピラリ部の幅が0.8mmを超える範囲にある場合、後述する実施例に示すように、測定器が、血液試料がセンサチップに導入された時点から0.5秒以上、さらに1.5秒以上、特に2.0秒以上の範囲内にデータaの取得を指示する信号を測定部Aに与える制御回路を有することが好ましい。当該指示のための時間の上限としては、15秒を例示できる。
また例えば、キャピラリ部は、後述する実施例に示すように、反応試薬層中の酵素量が同一である場合、高さが低い状態、より具体的には、0.3mm以下、さらに0.15mm未満、特に0.1mm以下の範囲、にあることが好ましい。この理由は現時点では定かではないが、本発明者は次のように考えている。キャピラリ部の高さが高すぎると、反応試薬層から溶出した酸化還元酵素が電極の表面から離れた方向に拡散しやすく、電極の表面付近において酵素サイクリング反応に関与する酵素が不足する。キャピラリ部の高さの下限としては、0.05mmを例示できる。
本発明によるバイオセンサシステムは、センサを使用する環境の温度が急激に変化した場合であっても、分析物濃度を高精度に測定できる。このため、サーミスタに代表される環境温度測定部を測定器に配置する必要はない。しかし、これは、本発明によるバイオセンサシステムにおいて環境温度測定部が設置されることを排除する意図ではない。
すなわち、本発明によるバイオセンサシステムは、測定器が、バイオセンサシステムを使用する環境(測定環境)の温度を測定する環境温度測定部をさらに有していてもよい。そして、本発明によるバイオセンサシステムは、演算部が、上記の換算テーブル(第1の換算テーブル)に加えて、上記のデータcと当該データcを測定環境の温度によって補正するためのデータ(データe)とが記述された、第2の換算テーブルをさらに有していてもよい。測定環境の温度が高すぎたり低すぎたりすると、第1の換算テーブルを用いた分析物濃度の測定精度が低下する場合がある。こうした場合、第1の換算テーブルに代えて第2の換算テーブルを使用することによって、分析物濃度を補正するとよい。第2の換算テーブルの代用が好ましい測定環境の温度としては、10℃以下の範囲および40℃以上の範囲を例示できる。当該温度の下限としては0℃が例示でき、当該温度の上限としては50℃が例示できる。測定環境の温度が10℃を超え40℃未満の範囲にある場合は、第1の換算テーブルを使用すれば足りる。
本発明によるバイオセンサシステムは、第1の換算テーブルと第2の換算テーブルとが1つのデータテーブル内に格納されている状態、より具体的には、データc、データdおよびデータeが、互いに関連づけられて1つのデータテーブルに記述されている状態にあることを排除しない。こうしたデータテーブルは、例えば、測定環境の温度が10℃以下の範囲および40℃以上の範囲にある場合に、敢えて第1の換算テーブルを参照することによって算出される分析物濃度を測定環境の温度によって補正するためのデータ(補正係数)をさらに有していてもよい。
本発明によるバイオセンサシステムは、測定器が、上記のデータaおよびデータbを取得する前に第1の温度測定の実施を指示する信号を、そしてデータaおよびデータbの取得後に第2の温度測定の実施を指示する信号を、環境温度測定部に与える、制御回路をさらに有していてもよい。本発明によるバイオセンサシステムは、第1の温度測定および第2の温度測定において測定された温度をそれぞれ第1温度および第2温度と表示したとき、演算部が、
i)第1温度および第2温度が下記の関係式(1)を満たす場合、第1の換算テーブルを参照することによって、データaおよびデータbに基づき血液試料中の分析物の濃度を決定するように、そして、
2.5℃ ≦ |(第2温度)-(第1温度)| ・・・(1)
ii)第1温度および第2温度が下記の関係式(2)を満たす場合、第2の換算テーブルを参照することによって、データbに代えて第1温度および/または第2温度に関連するデータと、データaと、に基づき血液試料中の分析物の濃度を決定するように、
|(第2温度)-(第1温度)| < 2.5℃ ・・・(2)
構成することもできる。
i)第1温度および第2温度が下記の関係式(1)を満たす場合、第1の換算テーブルを参照することによって、データaおよびデータbに基づき血液試料中の分析物の濃度を決定するように、そして、
2.5℃ ≦ |(第2温度)-(第1温度)| ・・・(1)
ii)第1温度および第2温度が下記の関係式(2)を満たす場合、第2の換算テーブルを参照することによって、データbに代えて第1温度および/または第2温度に関連するデータと、データaと、に基づき血液試料中の分析物の濃度を決定するように、
|(第2温度)-(第1温度)| < 2.5℃ ・・・(2)
構成することもできる。
環境温度の変化をより確実に検出する観点からは、第2の温度測定は、第1の温度測定から5秒以上、好ましくは15秒以上、さらに好ましくは30秒以上経過した後に実施するとよい。このように、本発明のバイオセンサシステムは、第1の温度測定から5秒以上、好ましくは15秒以上、さらに好ましくは30秒以上経過した後に、第2の温度測定の実施を指示する信号を環境温度測定部に与える制御回路を有していてもよい。第1温度および/または第2温度に関連するデータとしては、例えば、第1温度と第2温度との平均値を使用できる。また、当該データは、温度であっても温度の換算値であってもよい。
本発明によるバイオセンサシステムは、第1の温度測定から一定間隔毎に環境温度を測定し、その単位時間当たりの温度推移を検出するための信号を環境温度測定部に与える制御回路を有していてもよい。これにより、サーミスタに代表される環境温度測定部の信頼性(故障の有無)を容易に判断できる。
本発明による分析物濃度の測定方法は、上記のとおり、血液試料に接触させた一対の電極に電圧を印加し、分析物以外の酸化還元物質の酸化または還元に伴って血液試料中に流れる電流の量を測定するステップを含むことによって上記のデータbを取得する。データaおよびデータbに基づく血液試料中の分析物の濃度は、上記の第1の換算テーブルを参照することによって決定できる。
本発明による分析物濃度の測定方法は、血液試料の周囲の環境温度を測定するステップをさらに有していてもよい。当該ステップは、データaおよびデータbを取得する前に環境温度を測定する第1の温度測定ステップと、データaおよびデータbの取得後に環境温度を測定する第2の温度測定ステップとを含んでいてよい。
本発明による分析物濃度の測定方法は、第1の温度測定ステップおよび第2の温度測定ステップにおいて測定された温度をそれぞれ第1温度および第2温度と表示したとき、
i)第1温度および第2温度が下記の関係式(1)を満たす場合、上記の第1の換算テーブルを参照することによって、データaおよびデータbに基づき血液試料中の分析物の濃度を決定し、
2.5℃ ≦ |(第2温度)-(第1温度)| ・・・(1)
ii)第1温度および第2温度が下記の関係式(2)を満たす場合、上記の第2の換算テーブルを参照することによって、データbに代えて第1温度および/または第2温度に関連するデータと、データaと、に基づき血液試料中の分析物の濃度を決定する、
|(第2温度)-(第1温度)| < 2.5℃ ・・・(2)
ように構成してもよい。環境温度の変化をより確実に検出する観点からは、第2の温度測定は、第1の温度測定から5秒以上、好ましくは15秒以上、さらに好ましくは30秒以上経過した後に実施するとよい。第1温度および/または第2温度に関連するデータとしては、例えば、第1温度と第2温度との平均値を使用できる。また、当該データは、温度であっても温度の換算値であってもよい。
i)第1温度および第2温度が下記の関係式(1)を満たす場合、上記の第1の換算テーブルを参照することによって、データaおよびデータbに基づき血液試料中の分析物の濃度を決定し、
2.5℃ ≦ |(第2温度)-(第1温度)| ・・・(1)
ii)第1温度および第2温度が下記の関係式(2)を満たす場合、上記の第2の換算テーブルを参照することによって、データbに代えて第1温度および/または第2温度に関連するデータと、データaと、に基づき血液試料中の分析物の濃度を決定する、
|(第2温度)-(第1温度)| < 2.5℃ ・・・(2)
ように構成してもよい。環境温度の変化をより確実に検出する観点からは、第2の温度測定は、第1の温度測定から5秒以上、好ましくは15秒以上、さらに好ましくは30秒以上経過した後に実施するとよい。第1温度および/または第2温度に関連するデータとしては、例えば、第1温度と第2温度との平均値を使用できる。また、当該データは、温度であっても温度の換算値であってもよい。
以下、実施例により、本発明をさらに詳細に説明する。
(実施例1)
図2および図3に示すセンサチップを作製した。キャピラリ部は、幅0.6mm、長さ(奥行き)2.5mm、高さ0.1mmになるように設計した。反応試薬層は、次のようにして形成した。グルコースデヒドロゲナーゼ、フェリシアン化カリウム(関東化学社製)、タウリン(ナカライテスク社製)およびマルチトール(林原社製)を、CMC水溶液(第一工業製薬社製セロゲンHE-1500F)に溶解することによって得た試薬液を、反応試薬層中の酵素量が2.0U/センサ、CMC量が0.05質量%、フェリシアン化カリウム量が2.5質量%、タウリン量が1.5質量%、マルチトール量が0.1質量%になるように、ポリエチレンテレフタレート基板上に塗布した後、湿度45%温度21℃の雰囲気下で乾燥させた。各電極はパラジウムによって構成した。
図2および図3に示すセンサチップを作製した。キャピラリ部は、幅0.6mm、長さ(奥行き)2.5mm、高さ0.1mmになるように設計した。反応試薬層は、次のようにして形成した。グルコースデヒドロゲナーゼ、フェリシアン化カリウム(関東化学社製)、タウリン(ナカライテスク社製)およびマルチトール(林原社製)を、CMC水溶液(第一工業製薬社製セロゲンHE-1500F)に溶解することによって得た試薬液を、反応試薬層中の酵素量が2.0U/センサ、CMC量が0.05質量%、フェリシアン化カリウム量が2.5質量%、タウリン量が1.5質量%、マルチトール量が0.1質量%になるように、ポリエチレンテレフタレート基板上に塗布した後、湿度45%温度21℃の雰囲気下で乾燥させた。各電極はパラジウムによって構成した。
3名の被験者から血液を採取した。グルコース濃度が50mg/dl、100mg/dl、250mg/dl、400mg/dl、600mg/dlになるように、グルコース濃縮液を各血液に添加することによって、血液試料を調製した。
血液試料をセンサチップのキャピラリ部に導入した。血液試料の温度は、17℃、25℃または33℃とした。次に、測定部Aにおける作用極(電極12)と対極(電極13)との間に0.25Vの大きさの電圧を印加し、血液試料の導入完了から1秒後に、上記の酵素およびグルコースが関与する酵素サイクリング反応により当該電極間に流れる電流(グルコース応答)を測定した。
その後、測定部Bにおける作用極(電極11)と対極(電極12)との間に2.5Vの大きさの電圧を印加し、血液試料の導入完了から3秒後に、当該電極間に流れる電流(温度補正用応答)を測定した。
グルコース応答の応答電流値と、温度補正用応答の応答電流値とを表1に示す。また、温度補正用応答の応答電流値を、グルコース応答の応答電流値で除算することによって得た数値(Z)も、表1に示す。温度17℃の血液試料から得た上記の数値(Zx)を、温度33℃の血液試料から得た上記の数値(Zy)で除算することによって得た数値(Zx/Zy)も、表1に示す。さらに、キャピラリ部の寸法、各応答の測定タイミング、酵素の量、CMCの量、Zx/Zyの値の1.0からの最大の乖離率(最大の揺らぎ幅)を表2に示す。以降の実施例および参照例についてのこれらの値も表2に示す。
実施例1におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、12%以下の範囲にあった。
(実施例2)
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表3に示す。
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表3に示す。
実施例2におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例3)
センサ当たりの酵素量が0.5Uであるセンサチップを使用したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表4に示す。
センサ当たりの酵素量が0.5Uであるセンサチップを使用したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表4に示す。
実施例3におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、12%以下の範囲にあった。
(実施例4)
センサ当たりの酵素量が1.0Uであるセンサチップを使用したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表5に示す。
センサ当たりの酵素量が1.0Uであるセンサチップを使用したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表5に示す。
実施例4におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例5)
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例3と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表6に示す。
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例3と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表6に示す。
実施例5におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例6)
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表7に示す。
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表7に示す。
実施例6におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例7)
反応試薬層がCMCを含有しないセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表8に示す。
反応試薬層がCMCを含有しないセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表8に示す。
実施例7におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、12%以下の範囲にあった。
(実施例8)
反応試薬層中のCMC量が0.1質量%であるセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表9に示す。
反応試薬層中のCMC量が0.1質量%であるセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表9に示す。
実施例8におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例9)
反応試薬層中のCMC量が0.25質量%であるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表10に示す。
反応試薬層中のCMC量が0.25質量%であるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表10に示す。
実施例9におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、12%以下の範囲にあった。
(実施例10)
反応試薬層中のCMC量が0.5質量%であるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表11に示す。
反応試薬層中のCMC量が0.5質量%であるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表11に示す。
実施例10におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例11)
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例7と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表12に示す。
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例7と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表12に示す。
実施例11におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例12)
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例8と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表13に示す。
キャピラリ部への血液試料の導入完了から2.5秒後にグルコース応答を測定したこと以外は、実施例8と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表13に示す。
実施例12におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例13)
キャピラリ部への血液試料の導入完了から1.5秒後にグルコース応答を測定したこと以外は、実施例9と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表14に示す。
キャピラリ部への血液試料の導入完了から1.5秒後にグルコース応答を測定したこと以外は、実施例9と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表14に示す。
実施例13におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例14)
キャピラリ部への血液試料の導入完了から1.0秒後にグルコース応答を測定したこと以外は、実施例10と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表15に示す。
キャピラリ部への血液試料の導入完了から1.0秒後にグルコース応答を測定したこと以外は、実施例10と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表15に示す。
実施例14におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例15)
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表16に示す。
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表16に示す。
実施例15におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例16)
キャピラリ部への血液試料の導入完了から1.5秒後にグルコース応答を測定したこと以外は、実施例15と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表17に示す。
キャピラリ部への血液試料の導入完了から1.5秒後にグルコース応答を測定したこと以外は、実施例15と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表17に示す。
実施例16におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、12%以下の範囲にあった。
(実施例17)
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例2と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表18に示す。
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例2と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表18に示す。
実施例17におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、12%以下の範囲にあった。
(実施例18)
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表19に示す。
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例1と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表19に示す。
実施例18におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例19)
キャピラリ部への血液試料の導入完了から1.5秒後にグルコース応答を測定したこと以外は、実施例18と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表20に示す。
キャピラリ部への血液試料の導入完了から1.5秒後にグルコース応答を測定したこと以外は、実施例18と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表20に示す。
実施例19におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例20)
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例3と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表21に示す。
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例3と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表21に示す。
実施例20におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%以下の範囲にあった。
(実施例21)
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例5と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表22に示す。
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例5と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表22に示す。
実施例21におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例22)
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表23に示す。
キャピラリ部の幅が1.0mmであり長さが3.0mmであるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表23に示す。
実施例22におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例23)
キャピラリ部の高さが0.15mmであるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表24に示す。
キャピラリ部の高さが0.15mmであるセンサチップを使用したこと以外は、実施例6と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表24に示す。
実施例23におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
(実施例24)
キャピラリ部の高さが0.15mmであるセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表25に示す。
キャピラリ部の高さが0.15mmであるセンサチップを使用したこと以外は、実施例4と同様にして種々の電流応答を測定した。各血液試料から得た数値(Z、Zx/Zy)を表25に示す。
実施例24におけるZx/Zyの値の最大の揺らぎ幅は、表2に示すように、17%を超える範囲にあった。
本発明は、血液試料中の分析物濃度の測定において、当該測定を実施する環境の温度に起因した測定誤差の発生を抑制するものとして、測定の高精度化が要求される各分野において多大な利用価値を有する。
Claims (19)
- 演算部を有する測定器と、
前記測定器に着脱自在であり、血液試料が導入されるセンサチップと、
を有するバイオセンサシステムであって、
前記センサチップが、前記血液試料中の分析物を基質とする酸化還元酵素が関与する反応により前記血液試料中に流れる電流の量に基づいて前記分析物の濃度に関連するデータaを取得する測定部Aと、前記データaを温度補正するためのデータbを前記血液試料から取得する測定部Bとを有し、
前記演算部が、前記データaおよび前記データbに基づき、前記血液試料の温度に応じて補正された、前記血液試料中の前記分析物の濃度を決定する機能を有する、
バイオセンサシステム。 - 前記測定部Bが、前記血液試料に電圧を印加する電極を有する、請求項1に記載のバイオセンサシステム。
- 前記データbが、前記分析物以外の酸化還元物質の酸化または還元に伴って前記血液試料中に流れる電流の量に関連するデータである、請求項2に記載のバイオセンサシステム。
- 前記測定器が、前記血液試料が前記センサチップに導入された時点から0.5秒以上2.5秒未満の範囲内に、前記データaの取得を指示する信号を前記測定部Aに与える制御回路を有する、請求項1に記載のバイオセンサシステム。
- 前記センサチップが前記酸化還元酵素を含有する反応試薬層を有しており、
前記反応試薬層が水溶性高分子化合物を含有しない、または前記反応試薬層中の水溶性高分子化合物の量が0.2質量%未満であり、
前記測定器が、前記血液試料が前記センサチップに導入された時から0.5秒以上2.5秒未満の範囲内に前記データaの取得を指示する信号を前記測定部Aに与える制御回路を有する、請求項1に記載のバイオセンサシステム。 - 前記センサチップが前記酸化還元酵素を含有する反応試薬層を有しており、
前記反応試薬層中の水溶性高分子化合物の量が0.2質量%以上であり、
前記測定器が、前記血液試料が前記センサチップに導入された時から2.5秒以上経過した後に前記データaの取得を指示する信号を前記測定部Aに与える制御回路を有する、請求項1に記載のバイオセンサシステム。 - 前記演算部が、血液試料中の分析物を基質とする酸化還元酵素が関与する反応により当該血液試料中を流れる電流の量に関連するデータcと、当該分析物以外の酸化還元物質の酸化または還元に伴って当該血液試料中に流れる電流の量に関連するデータdと、前記データcおよび前記データdに対応する当該分析物の濃度とが記述された換算テーブルを有し、当該換算テーブルを参照することによって前記データaおよび前記データbに基づき前記血液試料中の前記分析物の濃度を決定する、請求項3に記載のバイオセンサシステム。
- 前記換算テーブルにおいて、前記データcおよび前記データdに代えて、前記データcおよび前記データdに基づく1つの換算値が記述されている、請求項7に記載のバイオセンサシステム。
- 前記測定器が、測定環境の温度を測定する環境温度測定部をさらに有する、請求項3に記載のバイオセンサシステム。
- 前記演算部が、第1の換算テーブルおよび第2の換算テーブルを有し、前記第1の換算テーブルが、血液試料中の分析物を基質とする酸化還元酵素が関与する反応により当該血液試料中を流れる電流の量に関連するデータcと、当該分析物以外の酸化還元物質の酸化または還元に伴って当該血液試料中に流れる電流の量に関連するデータdと、前記データcおよび前記データdに対応する当該分析物の濃度とが記述された換算テーブルであり、前記第2の換算テーブルが、前記データcと、前記データcを測定環境の温度によって補正するためのデータeとを有する、請求項3に記載のバイオセンサシステム。
- 前記測定器が、測定環境の温度を測定する環境温度測定部と、前記データaおよび前記データbを取得する前に第1の温度測定の実施を指示する信号と前記データaおよび前記データbの取得後に第2の温度測定の実施を指示する信号とを前記環境温度測定部に与える制御回路と、をさらに有し、
前記第1の温度測定および前記第2の温度測定において測定された温度をそれぞれ第1温度および第2温度と表示したとき、前記演算部が、
i)前記第1温度および前記第2温度が下記の関係式(1)を満たす場合、前記第1の換算テーブルを参照することによって、前記データaおよび前記データbに基づき前記血液試料中の前記分析物の濃度を決定し、
2.5℃ ≦ |(第2温度)-(第1温度)| ・・・(1)
ii)前記第1温度および前記第2温度が下記の関係式(2)を満たす場合、前記第2の換算テーブルを参照することによって、前記データbに代えて前記第1温度および/または前記第2温度に関連するデータと、前記データaと、に基づき前記血液試料中の前記分析物の濃度を決定する、
|(第2温度)-(第1温度)| < 2.5℃ ・・・(2)
請求項10に記載のバイオセンサシステム。 - 前記制御回路が、前記第1の温度測定から5秒以上経過した後に、前記第2の温度測定の実施を指示する信号を前記環境温度測定部に与える、請求項11に記載のバイオセンサシステム。
- 請求項1に記載のバイオセンサシステムにおいて使用され、血液試料が導入されるセンサチップであって、前記血液試料中の分析物を基質とする酸化還元酵素が関与する反応により前記血液試料中に流れる電流の量に基づいて前記分析物の濃度に関連するデータaを取得する測定部Aと、前記データaを温度補正するためのデータbを前記血液試料から取得する測定部Bとを有する、センサチップ。
- 前記測定部Bが、前記血液試料に電圧を印加する電極を有する、請求項13に記載のバイオセンサシステム。
- 血液試料中の分析物を基質とする酸化還元酵素が関与する反応により前記血液試料中に流れる電流の量に基づいて前記分析物の濃度に関連するデータaを取得するステップと、前記データaを温度補正するためのデータbを前記血液試料から取得するステップと、前記データaおよび前記データbに基づき、前記血液試料の温度に応じて補正された、前記血液試料中の前記分析物の濃度を決定するステップとを有する、血液試料中の分析物の濃度の測定方法であって、
前記データbを取得するステップが、前記血液試料に接触させた一対の電極に電圧を印加し、前記分析物以外の酸化還元物質の酸化または還元に伴って前記血液試料中に流れる電流の量を測定するステップを含む、血液試料中の分析物の濃度の測定方法。 - 血液試料中の分析物を基質とする酸化還元酵素が関与する反応により当該血液試料中を流れる電流の量に関連するデータcと、当該分析物以外の酸化還元物質の酸化または還元に伴って当該血液試料中に流れる電流の量に関連するデータdと、前記データcおよび前記データdに対応する当該分析物の濃度とが記述された換算テーブルを参照することによって、前記データaおよび前記データbに基づき前記血液試料中の前記分析物の濃度を決定する、請求項15に記載の測定方法。
- 前記換算テーブルにおいて、前記データcおよび前記データdに代えて、前記データcおよび前記データdに基づく1つの換算値が記述されている、請求項16に記載の測定方法。
- 前記血液試料の周囲の環境温度を測定するステップをさらに有し、当該ステップが、前記データaおよび前記データbを取得する前に前記環境温度を測定する第1の温度測定ステップと、前記データaおよび前記データbの取得後に前記環境温度を測定する第2の温度測定ステップとを含み、
前記第1の温度測定ステップおよび前記第2の温度測定ステップにおいて測定された温度をそれぞれ第1温度および第2温度と表示したとき、
i)前記第1温度および前記第2温度が下記の関係式(1)を満たす場合、血液試料中の分析物を基質とする酸化還元酵素が関与する反応により当該血液試料中を流れる電流の量に関連するデータcと、当該分析物以外の酸化還元物質の酸化または還元に伴って当該血液試料中に流れる電流の量に関連するデータdと、前記データcおよび前記データdに対応する当該分析物の濃度とが記述された第1の換算テーブルを参照することによって、前記データaおよび前記データbに基づき前記血液試料中の前記分析物の濃度を決定し、
2.5℃ ≦ |(第2温度)-(第1温度)| ・・・(1)
ii)前記第1温度および前記第2温度が下記の関係式(2)を満たす場合、前記データcと、前記データcを測定環境の温度によって補正するためのデータeとを有する第2の換算テーブルを参照することによって、前記データbに代えて前記第1温度および/または前記第2温度に関連するデータと、前記データaと、に基づき前記血液試料中の前記分析物の濃度を決定する、
|(第2温度)-(第1温度)| < 2.5℃ ・・・(2)
請求項15に記載の測定方法。 - 前記第2の温度測定ステップを、前記第1の温度測定ステップから5秒以上経過した後に実施する請求項18に記載の測定方法。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP09730495.0A EP2284526B1 (en) | 2008-04-07 | 2009-04-02 | Biosensor system and method of measuring analyte concentration in blood sample |
| CN200980112167.4A CN101983333B (zh) | 2008-04-07 | 2009-04-02 | 生物传感器系统、传感器芯片及血液试样中的分析物浓度的测定方法 |
| US12/935,803 US8940138B2 (en) | 2008-04-07 | 2009-04-02 | Biosensor system, sensor chip, and method of measuring analyte concentration in blood sample |
| US14/568,889 US9829460B2 (en) | 2008-04-07 | 2014-12-12 | Biosensor system, sensor chip, and method of measuring analyte concentration in blood sample |
| US15/797,765 US10352890B2 (en) | 2008-04-07 | 2017-10-30 | Biosensor system, sensor chip, and method of measuring analyte concentration in blood sample |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008-099692 | 2008-04-07 | ||
| JP2008099692A JP2009250806A (ja) | 2008-04-07 | 2008-04-07 | バイオセンサシステム、センサチップおよび血液試料中の分析物濃度の測定方法 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US12/935,803 A-371-Of-International US8940138B2 (en) | 2008-04-07 | 2009-04-02 | Biosensor system, sensor chip, and method of measuring analyte concentration in blood sample |
| US14/568,889 Continuation US9829460B2 (en) | 2008-04-07 | 2014-12-12 | Biosensor system, sensor chip, and method of measuring analyte concentration in blood sample |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009125563A1 true WO2009125563A1 (ja) | 2009-10-15 |
Family
ID=41161700
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2009/001560 WO2009125563A1 (ja) | 2008-04-07 | 2009-04-02 | バイオセンサシステム、センサチップおよび血液試料中の分析物濃度の測定方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (3) | US8940138B2 (ja) |
| EP (1) | EP2284526B1 (ja) |
| JP (1) | JP2009250806A (ja) |
| CN (1) | CN101983333B (ja) |
| WO (1) | WO2009125563A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019168363A (ja) * | 2018-03-23 | 2019-10-03 | アークレイ株式会社 | 測定方法、及び測定装置 |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100981222B1 (ko) * | 2006-01-31 | 2010-09-10 | 파나소닉 주식회사 | 혈액 센서와 그것을 구비하는 혈액 검사 장치 |
| US8859292B2 (en) * | 2009-01-30 | 2014-10-14 | Panasonic Healthcare Co., Ltd. | Method for measuring temperature of biological sample, method for measuring concentration of biological sample, sensor chip and biosensor system |
| JP5738838B2 (ja) * | 2010-02-26 | 2015-06-24 | アークレイ株式会社 | 分析装置、分析方法及び分析システム |
| CN101900704A (zh) * | 2010-07-26 | 2010-12-01 | 北京软测科技有限公司 | 利用插入算法提高血液测量准确度的方法 |
| EP2679992B1 (en) * | 2011-02-23 | 2019-10-23 | PHC Holdings Corporation | Biological sample measuring system |
| DE102012205171B3 (de) * | 2012-03-29 | 2013-09-12 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Integriertes Einweg-Chipkartuschensystem für mobile Multiparameteranalysen chemischer und/oder biologischer Substanzen |
| CN103412012B (zh) * | 2013-03-28 | 2015-09-09 | 利多(香港)有限公司 | 生物传感器 |
| WO2014174815A1 (ja) * | 2013-04-26 | 2014-10-30 | パナソニックヘルスケア株式会社 | 液体試料測定装置、液体試料測定方法、及び、バイオセンサ |
| CN105136251A (zh) * | 2014-06-09 | 2015-12-09 | 浙江海洋学院 | 空气质量流量计的检测方法 |
| US10088447B2 (en) * | 2016-09-30 | 2018-10-02 | Seung Ik Jun | Biosensor |
| US10297872B2 (en) * | 2017-09-18 | 2019-05-21 | StoreDot Ltd. | Regulation of metal ion levels in lithium ion batteries |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08503304A (ja) * | 1993-06-08 | 1996-04-09 | ベーリンガー マンハイム コーポレーション | 周囲温度の評価方法を備えたバイオセンシングメータ及びシステム |
| JP2001235444A (ja) | 1999-12-23 | 2001-08-31 | Roche Diagnostics Corp | 熱伝導性センサー |
| JP2003156469A (ja) | 2001-11-22 | 2003-05-30 | Matsushita Electric Ind Co Ltd | バイオセンサ、バイオセンサ用測定装置及び基質の定量方法 |
| WO2003062812A1 (en) | 2002-01-18 | 2003-07-31 | Arkray, Inc. | Analyzer having temperature sensor |
| JP2007524826A (ja) * | 2003-06-20 | 2007-08-30 | エフ ホフマン−ラ ロッシュ アクチェン ゲゼルシャフト | 用量充足電極を使用する検体測定のためのシステムおよび方法 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4655456A (en) * | 1983-01-13 | 1987-04-07 | Chen Dai Yin Chiao | Budo complex weapon |
| FR2776071B1 (fr) * | 1998-03-13 | 2000-05-26 | Eastman Kodak Co | Dispositif de mesure automatique de la concentration d'un agent developpateur |
| WO2002044705A1 (en) * | 2000-11-30 | 2002-06-06 | Matsushita Electric Industrial Co., Ltd. | Biosensor, measuring instrument for biosensor, and method of quantifying substrate |
| US8187457B2 (en) * | 2003-03-27 | 2012-05-29 | Terumo Kabushiki Kaisha | Test paper and porous membrane |
| ES2657627T3 (es) * | 2003-06-20 | 2018-03-06 | F. Hoffmann-La Roche Ag | Biosensores electroquímicos |
| JP4619359B2 (ja) * | 2003-06-20 | 2011-01-26 | エフ ホフマン−ラ ロッシュ アクチェン ゲゼルシャフト | フレア状に形成された試料受入チャンバーを持つ試験片 |
| JP3612324B1 (ja) * | 2003-09-29 | 2005-01-19 | 株式会社日立製作所 | 血糖値表示方法及び装置 |
| JP4458802B2 (ja) * | 2003-10-02 | 2010-04-28 | パナソニック株式会社 | 血液中のグルコースの測定方法およびそれに用いるセンサ |
| CN100472210C (zh) * | 2003-12-04 | 2009-03-25 | 松下电器产业株式会社 | 血液成分的测定方法及该方法中使用的传感器和测定装置 |
| EP1991112A1 (en) | 2006-02-27 | 2008-11-19 | Bayer Healthcare, LLC | Temperature-adjusted analyte determination for biosensor systems |
| US20070205114A1 (en) * | 2006-03-01 | 2007-09-06 | Mathur Vijaywanth P | Method of detecting biosensor filling |
| US20080118984A1 (en) * | 2006-11-22 | 2008-05-22 | Eps Bio Technology Corp. | Biosensing system and related biosensing method |
-
2008
- 2008-04-07 JP JP2008099692A patent/JP2009250806A/ja active Pending
-
2009
- 2009-04-02 CN CN200980112167.4A patent/CN101983333B/zh active Active
- 2009-04-02 US US12/935,803 patent/US8940138B2/en active Active
- 2009-04-02 WO PCT/JP2009/001560 patent/WO2009125563A1/ja active Application Filing
- 2009-04-02 EP EP09730495.0A patent/EP2284526B1/en active Active
-
2014
- 2014-12-12 US US14/568,889 patent/US9829460B2/en active Active
-
2017
- 2017-10-30 US US15/797,765 patent/US10352890B2/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08503304A (ja) * | 1993-06-08 | 1996-04-09 | ベーリンガー マンハイム コーポレーション | 周囲温度の評価方法を備えたバイオセンシングメータ及びシステム |
| JP2001235444A (ja) | 1999-12-23 | 2001-08-31 | Roche Diagnostics Corp | 熱伝導性センサー |
| JP2003042995A (ja) | 1999-12-23 | 2003-02-13 | Roche Diagnostics Corp | 熱伝導性センサー |
| JP2003156469A (ja) | 2001-11-22 | 2003-05-30 | Matsushita Electric Ind Co Ltd | バイオセンサ、バイオセンサ用測定装置及び基質の定量方法 |
| WO2003062812A1 (en) | 2002-01-18 | 2003-07-31 | Arkray, Inc. | Analyzer having temperature sensor |
| JP2007524826A (ja) * | 2003-06-20 | 2007-08-30 | エフ ホフマン−ラ ロッシュ アクチェン ゲゼルシャフト | 用量充足電極を使用する検体測定のためのシステムおよび方法 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019168363A (ja) * | 2018-03-23 | 2019-10-03 | アークレイ株式会社 | 測定方法、及び測定装置 |
| JP6997659B2 (ja) | 2018-03-23 | 2022-01-17 | アークレイ株式会社 | 測定方法、及び測定装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2284526B1 (en) | 2020-12-09 |
| US8940138B2 (en) | 2015-01-27 |
| US20180045670A1 (en) | 2018-02-15 |
| JP2009250806A (ja) | 2009-10-29 |
| US9829460B2 (en) | 2017-11-28 |
| US10352890B2 (en) | 2019-07-16 |
| US20110027816A1 (en) | 2011-02-03 |
| US20150168340A1 (en) | 2015-06-18 |
| CN101983333B (zh) | 2015-01-21 |
| EP2284526A1 (en) | 2011-02-16 |
| EP2284526A4 (en) | 2014-11-26 |
| CN101983333A (zh) | 2011-03-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2009125563A1 (ja) | バイオセンサシステム、センサチップおよび血液試料中の分析物濃度の測定方法 | |
| JP5358014B2 (ja) | センサチップ、バイオセンサシステム、生体試料の温度測定方法、血液試料の温度測定方法、血液試料中の分析物の濃度測定方法 | |
| JP4814952B2 (ja) | 血液試料のヘマトクリット値の測定方法、血液試料中の分析物の濃度の測定方法、センサチップおよびセンサユニット | |
| ES2800977T3 (es) | Método para análisis electroquímico rápido | |
| JP4814953B2 (ja) | 血液試料のヘマトクリット値の測定方法、血液試料中の分析物の濃度の測定方法、センサチップおよびセンサユニット | |
| JP5179641B2 (ja) | 生体試料の温度測定方法、生体試料の濃度測定方法、およびバイオセンサシステム | |
| RU2453843C2 (ru) | Окисляемые виды соединений в качестве внутреннего стандарта в контрольных растворах для биосенсоров | |
| JP4891821B2 (ja) | 生理学的サンプルから対照溶液を判別するシステム及び方法 | |
| JP5203620B2 (ja) | 干渉物質の存在下でサンプルを分析する方法及び装置 | |
| KR101950615B1 (ko) | 간섭을 보상하는 두 개의 전극들의 테스트 스트립 | |
| US20130098775A1 (en) | Glucose biosensor with improved shelf life | |
| EP2821497A2 (en) | Reagent composition for biosensor and biosensor having the same | |
| JP2009503452A (ja) | ゲート化電流測定器 | |
| AU2010224341A1 (en) | Multi-analyte test strip with inline working electrodes and shared opposing counter/reference electrode | |
| JP5702457B2 (ja) | バイオセンサシステム、センサチップおよび血液試料中の分析物濃度の測定方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200980112167.4 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09730495 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12935803 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009730495 Country of ref document: EP |