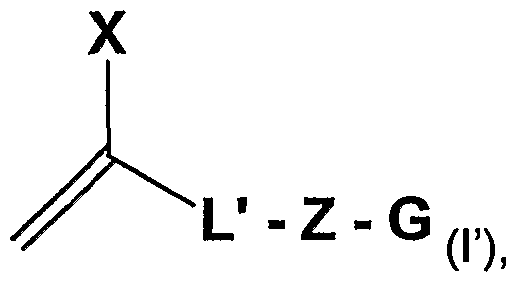Nouveaux glycopolymères, leurs utilisations, et monomères utiles pour leur préparation
La présente invention a pour objet de nouveaux glycopolymères, leurs utilisations, ainsi que de nouveaux monomères, utiles pour leur préparation. L'invention concerne également des procédés pour la préparation des nouveaux monomères et glycopolymères.
Les glycopolymères sont des polymères comprenant des unités comprenant un motif glycoside. Ils peuvent être obtenus par polymérisation de monomères comprenant un glycoside, par copolymérisation en présence d'autres monomères, ou par greffage sur un polymère fonctionnalisé à cet effet.
De nombreux composés comprenant un groupe glycoside, le plus souvent monoglycoside, et un groupe polymérisable, par exemple une double liaison, ont été décrits. La polymérisation de tels composés a également été décrite.
Par exemple, Ie document WO 90/10023 décrit des glycopolymères, comprenant des unités dérivant d'acrylamide, et des unités dérivant de monomères de formule R2- NH-CO-CX=CH2 ou X est H ou un groupe méthyle, et R2 est un glycoside. Ces monomères sont obtenus à partir de composés de formule R2-NH2 dans lesquels le groupe R2 est lié au groupe -NH2 par un carbone anomère réducteur.
La présente invention propose d'autres glycopolymères, et d'autres monomères comprenant un glycoside. Ces nouveaux glycopolymères et monomères peuvent être utiles pour moduler les propriétés des glycopolymères, et ainsi permettre, lors de leur utilisation, de fournir de nouveaux produits. On peut ainsi moduler les propriétés de polymères utilisés par exemple dans des compositions cosmétiques.
Par ailleurs, les glycopolymères suscitent un intérêt croissant dans les domaines de l'industrie et/ou des produits de consommation car il s'agit de produits dérivés de produits naturels, bénéficiant d'une image positive en terme de protection de l'environnement et/ou de nocivité et/ou plus simplement de marketing. Il existe un besoin pour de tels produits.
Ainsi l'invention propose un polymère comprenant des unités comprenant un glycoside, caractérisé en ce qu'il comprend:
- des unités A0 cationiques ou potentiellement cationiques, dérivant de préférence d'un monomère mono-alpha-ethylèniquement insaturé cationique ou potentiellement cationique, et
- des unités dérivant d'un monomère de formule (I) suivante:
dans laquelle:
- X est un atome d'hydrogène ou un groupe méthyle
- L est un groupe de liaison divalent - Z est un atome d'oxygène ou de soufre, ou un groupe comprenant un atome d'azote et
- G est un glycoside.
L'invention concerne également des utilisations du polymère dans des compositions. L'invention concerne également des compositions comprenant le polymère.
L'invention concerne également un monomère particulièrement adapté pour préparation du polymère selon l'invention. Ainsi l'invention propose également un monomère de formule (I1) suivante
- X est un atome d'hydrogène ou un groupe méthyle
- Z est un atome d'oxygène, ou un groupe comprenant un atome d'azote et - G est un glycoside, caractérisé en ce que:
- le groupe -L'-Z-G présente la formule (H') suivante:
-COY-L1 -S-L2-Z-G (H') dans laquelle: - Y est un groupe de liaison divalent ou un atome de liaison,
- L1 est un groupe de liaison divalent, de préférence un groupe hydrocarboné divalent, de préférence un groupe alkyle divalent en C1-C6,
- L2 est un groupe de liaison divalent, de préférence un groupe hydrocarboné divalent, de préférence un groupe alkyle divalent en C1-C6, et - G est lié à Z par un carbone anomère du glycoside.
Le monomère selon l'invention peut être utilisé pour la préparation des polymères selon l'invention. Il peut également être utilisé pour la préparation d'autres polymères, par exemple des homopolymères dudit monomère, ou pour la préparation de copolymères ne comprenant pas d'unités cationiques ou potentiellement cationiques, mais comprenant d'autres unités. Il peut s'agir par exemple de copolymères comprenant des unités dérivant du monomère de formule (I1) et ; au titre des autres unités, des unités neutres, anioniques, et/ou potentiellement anioniques, hydrophobes et/ou hydrophiles. De telles unités sont décrites par la suite.
Définitions
On entend par «polymère» tout composé macromoléculaire comprenant des unités récurrentes. Les polymères, incluent notamment les homopolymères, les copolymères, les oligomères, les co-oligomères, les télomères, les co-télomères.
On entend par copolvmère, tout polymère comprenant au moins deux unités récurrentes différentes. Les copolymères incluent notamment les copolymères statistiques, les copolymères de structure contrôlée, les co-oligomères (copolymères de relativement faible masse moléculaire), les co-telomères.
On entend par (co)polymère à structure contrôlée tout (co)polymère dont l'enchaînement des motifs est contrôlé (par exemple des co-polymères di-blocs, tri- blocs, mais également polymères à gradients de concentration) et/ou dont la polydispersité est contrôlée (par exemple des (co)polymères statistiques ayant un indice de polydispersité de 1 à 1 ,5), par opposition aux (co)polymères obtenus par des procédés de polymérisation standard, qui ne permettent pas un tel contrôle de l'agencement des motifs unitaires ni des indices de polydispersité si faibles. Il peut s'agir d'un copolymère comprenant au moins deux parties A et B de compositions distinctes en unités récurrentes. Les parties d'un copolymère à structure contrôlée peuvent être notamment des blocs, des squelettes linéaires, des chaînes latérales, des greffons, des «cheveux» ou branches de microgels ou d'étoiles, des cœurs d'étoiles ou de microgels, ou bien encore des parties de chaînes polymériques présentant différentes concentrations en différentes unités. Ainsi la structure contrôlée, que peut présenter un copolymère, peut être choisie parmi les structures suivantes: - copolymère à blocs, comprenant au moins deux blocs, la partie A correspondant à un bloc, la partie B correspondant à un autre. La partie A est le plus souvent constituée de plusieurs unités différentes, présentant le cas échéant un gradient de composition. La partie A peut également présenter une structure de copolymère statistique. Ainsi la
partie A peut présenter une structure homopolymère (si elle comprend des unités Az), copolymère statistique ou copolymère à gradient de composition. Il peut par exemple s'agit d'un copolymère à blocs (bloc A)-(bloc B)-(bloc A), ou (bloc B)-(bloc A)-(bloc B), ou (bloc A)-(bloc B). - copolymère peigne ou greffé, comprenant un squelette et des chaînes latérales, avec la partie A correspondant au squelette et la partie B correspondant à des chaînes latérales, ou avec la partie B correspondant au squelette et la partie A correspondant à des chaînes latérales.
- copolymère étoile ou microgel, comprenant un cœur polymère ou non polymère, et des chaînes polymériques périphériques, une partie correspondant au cœur, l'autre correspondant aux chaînes périphériques. La partie A peut correspondre au cœur et la partie B peut correspondre aux chaînes périphériques. Inversement, la partie B peut correspondre au cœur et la partie A peut correspondre aux chaînes périphériques.
On entend par monomères des composés pouvant être utilisés pour la préparation de polymères, homopolymères ou copolymères (on peut parler aussi de comonomères). Les unités récurrentes des polymères dérivent de ces monomères.
Dans la présente demande, on désigne par unité dérivant d'un monomère une unité qui peut être obtenue directement à partir dudit monomère par polymérisation. Ainsi, par exemple, une unité dérivant d'un ester d'acide acrylique ou méthacrylique ne couvre pas une unité de formule -CH2-CH(COOH)-, -CH2-C(CH3)(COOH)-, -CH2- CH(OH)-, respectivement, obtenue par exemple en polymérisant un ester d'acide acrylique ou méthacrylique, ou de l'acétate de vinyle, respectivement, puis en hydrolysant. Une unité dérivant d'acide acrylique ou méthacrylique couvre par exemple une unité obtenue en polymérisant un monomère (par exemple un ester d'acide acrylique ou méthacrylique), puis en faisant réagir (par exemple par hydrolyse) le polymère obtenu de manière à obtenir des unités de formule -CH2-CH(COOH)-, ou - CH2-C(CH3)(COOH)-. Une unité dérivant d'un alcool vinylique couvre par exemple une unité obtenue en polymérisant un monomère (par exemple un ester vinylique), puis en faisant réagir (par exemple par hydrolyse) le polymère obtenue de manière à obtenir des unités de formule -CH2-CH(OH)-.
Dans la présente demande, sauf mention contraire, les masses molaires moyennes sont des masses molaires moyennes en poids, absolues, pouvant être mesurées par chromatographie d'exclusion dans un solvant approprié stérique (par exemple de l'eau Millipore dé ionisée si approprié), couplée à réfractomètre, à un
conductimètre et à un détecteur de diffusion de lumière multi-angle, avec extrapolation à angle zéro (GPC-MALS).
Dans la présente demande «Ac» représente un groupe acétyl de formule -COCH3.
Dans la présente demande, le terme glvcoside se réfère à tout groupe comprenant un ou plusieurs motifs glycoside, et aux dérivés de ces groupes. Dans le cas où le glycoside comprend plusieurs motifs glycosides, on parle également de polyglycosides. Par polyglycoside, on entend un glycoside comprenant au moins deux motifs glycoside.
Les motifs glycoside, les glycosides, les polyglycosides, leurs dérivés, leurs structures et formules, sont connus de l'homme du métier. On précise pour les motifs glycoside qu'il peut notamment s'agir d'aldoses, de cétoses, ou de dérivés, en cycles à
5 atomes (pentoses) ou 6 atomes (hexoses). Il est en outre connu de l'homme du métier que les glycosides, les polyglycosides, et leurs dérivés présentent un «carbone anomère» réducteur à une extrémité, la droite selon des conventions d'écriture. Il est également connu que les motifs glycoside, les glycosides, les polyglycosides, et leurs dérivés présentent des groupes hydroxyle (-OH), acide carboxylique, ou aminés, éventuellement protégés.
Les glycosides incluent notamment:
- les O-, S-, N-, C-alkyl ou aryl- glycosides comprenant éventuellement au moins un groupe -COOH,
- les monoglycosides et les polyglycosides.
A titre d'exemples de glycosides monosaccharides, on cite les glycosides suivants: Glucose (par exemple D-glucose), fructose, sorbose, mannose, galactose, talose, allose, gulose, idose, glucosamine, mannoamine, galactosamine, acide glucuronique, rhamnose, arabinose , acide galacturonique, fucose, xylose, lyxose, ribose, de manière générale les isomères du saccharose comme le palatinose.
A titre d'exemples de glycosides di- ou oligo- saccharides, on cite les glycosides suivants:
- di-saccharides: maltose, gentiobiose, lactose, cellobiose, isomaltose, melibiose, laminaribiose, chitobiose, xylobiose, maηnobiose, sophorose,
- oligo-sacchacaride:
- les maltodextrines notamment, maltotriose, isomaltotriose, maltotetraose, maltopentaose, maltoheptaose
- de manière générales les oligo-saccharides branchés comme le xyloglucane, et ses dérivés, - mannotriose, mannotriose,
- chitotriose, chitotétraose, chitopentaose,
- cellotétraoses, cellodextrines
- de manière générale les di- ou oligo- saccharides présentant des liaisons α- ou β-12, -3, -4,-5 ou -6 .
On cite également à titre d'exemples de glycosides:
- les dérivés de l'amidon, notamment le maltose, les maltodextrines,
- les dérivés de la cellulose,
- les pectines et leurs dérivés, - la chitine, le chitosane et leurs dérivés,
- les glucoaminoglucanes et leurs dérivés,
- les dérivés du xyloglucanes (notamment les dérivés obtenus par hydrolyse, par exemple par hydrolyse enzymatique)
- les galactomannanes et leurs dérivés, par exemple les polymères guars et leurs dérivés, obtenus à par hydrolyse de guar naturel, et éventuellement modification chimique (dérivatisation). Le guar naturel est extrait de l'albumen de certaines graines de plantes, par exemple Cyamopsis Tetragonalobus. La macromolécule de guar est constituée par une chaîne principale linéaire construite à partir de sucres monomères β- D-mannoses liés entre eux par des liaisons (1-4), et des unités latérales α-D-galactoses liées aux β-D-mannoses par des liaisons (1-6).
Les polyglycosides, comprenant plusieurs motifs glycoside, peuvent être décrits comme des enchaînements de glycosides (mono- et/ou polyglycosides). Dans la présente demande, on décrit un enchaînement de glycosides par la formule Ga-Gb-, dans laquelle Ga est un glycoside ou un polyglycoside, et Gb est un glycoside ou un polyglycoside. Dans le cas où Ga ou Gb est un polyglycoside, ce dernier peut également être décrit par une formule Ga'-Gb-, dans laquelle Ga' est un glycoside ou un polyglycoside, et Gb est un glycoside ou un polyglycoside, et ainsi de suite... Des glycosides ou polyglycosides pouvant constituer des groupes Ga, Gb, Ga>, Gb , etc., ont été mentionnés ci-dessus.
Monomères de formule (I) ou (D
Le polymère comprend des unités dérivant d'un monomère de formule (I) suivante:
dans laquelle: - X est un atome d'hydrogène ou un groupe méthyle
- L est un groupe de liaison divalent
- Z est un atome d'oxygène ou de soufre, ou un groupe comprenant un atome d'azote, et
- G est un glycoside.
G peut être lié à -Z- par un atome de carbone anomère ou par un autre atome de carbone.
G peut notamment être lié par:
- le carbone anomère via O, S, N, CH2-O, CH2-S, CH2-N (on obtient des glycosides).
- le carbone anomère oxydé, ouvrant la lactone formée par une aminé en formant une liaison amide.
On peut également greffer G par amination réductrice.
Si G comporte une fonction acide ou aminé sur d'autres positions, on peut greffer par cette fonction.
De préférence:
- Z est un atome d'oxygène, un groupe -NH-, ou -N[COCH3]-, et
- G est lié à -Z- par un carbone anomère du glycoside.
Selon un mode de réalisation, le groupe -L-Z-G est un groupe de formule -O- CH2CH2-O-G. Des monomères présentant un tel groupe sont par exemple commercialisés par la société Nippon Seika, sous la dénomination Sucrograph.
Selon un autre mode de réalisation, le groupe -L-Z-G peut être un groupe de formule -CO-NH-G, ou -CO-aryl-NH-G.
Selon un mode de réalisation particulier de l'invention, le monomère de formule (I) est un monomère de formule (I1) tel que décrit ci-dessous.
Monomère de formule (V)
Un monomère particulièrement adapté à la mise en œuvre de l'invention présente la formule (I1) suivante
- X est un atome d'hydrogène ou un groupe méthyle
- Z est un atome d'oxygène, ou un groupe comprenant un atome d'azote et
- G est un glycoside, caractérisé en ce que:
- le groupe -L'-Z-G présente la formule (H') suivante:
-COY-L1-S-L2-Z-G (II1) dans laquelle:
- Y est un groupe de liaison divalent ou un atome de liaison, - L1 est un groupe de liaison divalent, de préférence un groupe hydrocarboné divalent, de préférence un groupe alkyle divalent en Ci-C6,
- L2 est un groupe de liaison divalent, de préférence un groupe hydrocarboné divalent, de préférence un groupe alkyle divalent en C1-C6, et
- G est lié à Z par un carbone anomère du glycoside.
Ainsi, le composé de formule (I1) présente la formule suivante (I"):
De préférence: - Y est -O- ou -NH-, et
- L1 et L2, identiques ou différents, sont des groupes alkyles en C1-C4.
Selon un mode particulier, le monomère de formule (I) ou (I
1) ou (I") présente la formule (III
1) suivante:
Dans cette formule:
- le groupe -Z- de la formule (I) ou (I1) ou (I") est le groupe -N(COCH3)-,
- le groupe -L- ou -L'- de la formule (I) ou (I1) est le groupe -CONH-(CH2)2-S-(CH2)3-,
- le groupe -COY- de la formule (H') est Ie groupe -CONH-,
- le groupe L1 de la formule (H') est le groupe -(CH2V, et
- le groupe L2 de la formule (II1) est le groupe -(CH2)3-.
En particulier, le monomère de formule (I), (I1), (I") ou (III1) peut présenter l'une des formules suivantes:
dans laquelle: m et n, identiques ou différents, sont des nombres de O à 10, de préférence O ou 1.
Procédé de préparation du monomère de formule (V)
Le monomère de formule (I1) peut être préparé par un procédé comprenant les étapes suivantes:
- étape a): Fonctionnalisation d'un carbone anomère d'un glycoside de formule HO-G où le groupe -OH considéré est porté par le carbone anomère, par un réactif de fonctionnalisation comprenant un groupe aminé, de préférence un groupe aminé primaire, ou alcool, et un groupe comprenant une insaturation (par exemple type alcène ou alcyne). Le réactif de fonctionnalisation est de préférence l'allylamine. On obtient
ainsi un produit de formule CH2=CH2-L'2-Z-G où Z a la définition ci-dessus, dans lequel le groupe CH2=CH2-L'2- constituera le groupe -L2- après l'étape b).
Un mode de réalisation de cette étape peut être représenté par le schéma réactionnel suivant:
La réaction peut être réalisée en absence de solvant, à température ambiante, mais d'autres modalités de réaction ne sont pas exclues.
Ainsi l'étape a) peut comprendre les étapes suivantes: ai) réaction du carbone anomère d'un glycoside de formule G-OH, comprenant des groupes -OH libres avec de l'allylamine en excès, a2) élimination de l'allylamine en excès, a3) réaction avec de l'anhydride acétique, de manière à protéger l'atome d'azote, et éventuellement des groupes -OH primaires du glycoside.
L'étape a3) de réaction avec l'anhydride acétique, peut être réalisée dans des conditions telles qu'au moins une partie des groupes -OH du glycoside sont acétylés, en plus de l'atome d'azote. On peut favoriser cette acétylation de groupes -OH, ou la conserver, ou la supprimer lors d'une étape subséquente, par exemple par un traitement légèrement basique hydrolysant les groupes O-acétates.
- étape b): Réaction avec un composé comprenant un groupe H2S- et un groupe -OH ou -NH2, par exemple la cistéamine, de manière à obtenir un produit de formule Y'-L1-S-L2- Z-G1 dans laquelle Y' est un groupe -OH ou -NH2.
L'addition du composé peut être réalisée par réaction radicalaire, soit en présence d'un amorceur de radicaux (initiateur) soit par réaction photochimique. Dans les deux cas, la réaction a de préférence lieu dans un minimum de solvant, par exemple l'eau, si besoin en chauffant. Selon un mode avantageux, on opère en milieu aqueux. Selon un mode particulièrement avantageux, on opère en milieu aqueux, à l'aide d'un amorceur de radicaux hydrosoluble. Ce mode de réalisation peut permettre notamment de mettre en œuvre de plus faibles quantités de solvant, d'augmenter la cinétique de réaction, d'améliorer le rendement final obtenu. Des amorceurs pouvant être utilisés sont connus de l'homme du métier. On cite à titre d'exemples, le V50 (dihydrochlorure de alpha.alpha'-azodiisobutyramidine dihydrochloride), le VA-041 (dihydrochlorure de 2,2'- Azobis[2-(5-methyl-2-imidazolin-2-yl)propane] ), le VA-060 (dihydrochlorure de 2,2'-
Azobis{2-[1-(2-hydroxyethyl)-2-imidazolin-2-yl]propane} ). Un mode de réalisation de présenté par le schéma réactionnel suivant:
- Cistéamine
- étape c): Réaction avec un composé de formule CH2=CXCOY" dans lequel Y" est un groupe -OH, -NH2, ou -Cl, par exemple de l'acide (meth)acrylique, de l'acrylamide, ou du chlorure d'acryloyle, de manière à obtenir le produit de formule (I1). On précise que l'étape c) est de préférence une réaction de type chimique, non enzymatique. La réaction peut avoir lieu à température ambiante et plus avantageusement à froid, en milieu solvant par exemple dans l'eau ou un mélange eau / alcool. Le mélange solvant est de préférence adapté afin d'avoir la bonne solubilité des composé en présence. L'alcool peut être par exemple le méthanol, l'alcool isopropyle ou l'alcool tertiobutyl. Afin de piéger l'acide chlorhydrique libérée, on peut introduire dans le milieu une base : carbonate de sodium, acétate de sodium, aminé tertiaire etc.. La réaction est généralement rapide. Un mode de réalisation de cette étape peut être représenté par le schéma réactionnel suivant:
Pour tous les modes de réalisation, le glycoside G est de préférence un polyglycoside. Des glycosides pouvant constituer des groupes G de monomères de formule (I), (!'), (I"), ou (IH') ont été décrits ci-dessus dans la section «définitions».
Monomères ou unités cationiques ou potentiellement cationiques
Le polymère selon l'invention comprend des unités A0 cationiques ou potentiellement cationiques, pouvant dériver de monomères cationiques ou potentiellement cationiques. Par unités Ac cationiques ou potentiellement cationiques, on entend des unités qui comprennent un groupe cationique ou potentiellement cationique. Les unités ou groupes cationiques sont des unités ou groupes qui présentent au moins une charge positive (généralement associée à un ou plusieurs anions comme l'ion chlorure, l'ion bromure, un groupe sulfate, un groupe méthylesulfate), quel que soit le pH du milieu où est présent le copolymère. Les unités ou groupes potentiellement cationiques sont des unités ou groupes qui peuvent être neutres ou présenter au moins une charge positive selon le pH du milieu où est présent le copolymère. Dans ce cas on parlera d'unités potentiellement cationiques A0 sous forme neutre ou sous forme cationique. Par extension on peut parler de monomères cationiques ou potentiellement cationiques.
A titre d'exemples de monomères hydrophiles potentiellement cationiques (dont peuvent dériver des unités A0), on peut mentionner : « les N,N(dialky!aminoωalkyl)amides d'acides carboxyliques α-β monoéthyléniquement insaturés comme le 2(N,N-diméthylamino)éthyl-acrylamide ou -méthacrylamide, le 3(N,N-diméthylamino)propyl-acrylamide ou
-méthacrylamide, le 4(N,N-diméthylamino)butyl-acrylamide ou
-méthacrylamide, l'éthylène urée éthyl méthacrylamide (Sipomer WAM II, commercialisé par Rhodia)
• les aminoesters α-β mono-éthyléniquement insaturés comme le 2(diméthyl amino)éthyl acrylate (ADAM), 2(diméthyl amino)éthyl méthacrylate (DMAM), le 3(diméthyl amino)propyl méthacrylate, le 2(tertiobutylamino)éthyl méthacrylate, le 2(dipentylamino)éthyl méthacrylate, le 2(diéthylamino)éthyl méthacrylate, l'éthylène urée éthyl méthacrylate,
• les vinylpyridines, la vinylpyrrolidone, le vinyl caprolactame,
• la vinyl aminé
• les vinylimidazolines
• des monomères précurseurs de fonctions aminés tels que le N-vinyl formamide, le N-vinyl acétamide, ... qui engendrent des fonctions aminés primaires par simple hydrolyse acide ou basique.
A titre d'exemples de monomères hydrophiles cationiques, dont peuvent dériver des unités Ac, on peut mentionner :
• les monomères ammoniumacryloyles ou acryloyloxy comme le chlorure de triméthylammoniumpropylméthacrylate, le chlorure ou le bromure de triméthylammoniuméthylacrylamide ou méthacrylamide, le méthylsulfate de
triméthylammoniumbutylacrylamide ou méthacrylamide, le méthylsulfate de triméthylammoniumpropylméthacrylamide (MES), le chlorure de (3- méthacrylamidopropyl)triméthylammonium (MAPTAC), le chlorure de (3- acrylamidopropyl)triméthylammonium (APTAC), le chlorure ou le méthylsulfate de méthacryloyloxyéthyl triméthylammonium, le chlorure d'acryloyloxyéthyl triméthylammonium, le chlorure d'acryloyléthyl benzyl-dimethylammonium ethyl (ADAMQUAT BZ);
• le bromure, chlorure ou méthylsulfate de 1-éthyl 2-vinylpyridinium, de 1-éthyl 4- vinylpyridinium ; « les monomères N,N-dialkyldiallylamines comme le chlorure de N1N- diméthyldiallylammonium (DADMAC) ;
• les monomères polyquatemaires comme le chlorure de diméthylaminopropylméthacrylamide,N-(3-chloro-2-hydroxypropyl) triméthylammonium (DIQUAT) ...
Autres monomères ou unités
Le polymère peut également comprendre d'autres unités, par exemple des unités neutres AN, hydrophiles ou hydrophobes, et/ou des unités anioniques AA, anioniques ou potentiellement anioniques. Par unités AA anioniques ou potentiellement anioniques, on entend des unités qui comprennent un groupe anionique ou potentiellement anionique. Les unités ou groupes anioniques sont des unités ou groupes qui présentent au moins une charge négative (généralement associée à un ou plusieurs cations comme des cations de composés alcalins ou alcalino-terreux, par exemple le sodium, ou groupes cationiques comme l'ammonium), quel que soit le pH du milieu où est présent le copolymère. Les unités ou groupes potentiellement anioniques sont des unités ou groupes qui peuvent être neutres ou présenter au moins une charge négative selon le pH du milieu où est présent le copolymère. Dans ce cas on parlera d'unités potentiellement anioniques AA sous forme neutre ou sous forme anionique. Par extension, on peut parler de monomères anioniques ou potentiellement anioniques.
Par unités AN neutres, on entend des unités qui ne présentent pas de charge, quel que soit le pH du milieu où est présent le copolymère.
A titre d'exemples de monomères anioniques ou potentiellement anioniques, dont peuvent dériver des unités AA, on peut mentionner : • des monomères possédant au moins une fonction carboxylique, comme les acides carboxyliques α-β éthyléniquement insaturés ou les anhydrides correspondants, tels
que les acides ou anhydrides acrylique, méthacrylique, maleique, l'acide fumarique, l'acide itaconique, le N-méthacroyl alanine, le N-acryloylglycine et leurs sels hydrosolubles
• des monomères précurseurs de fonctions carboxylates, comme l'acrylate de tertiobutyle, qui engendrent, après polymérisation, des fonctions carboxyliques par hydrolyse.
• des monomères possédant au moins une fonction sulfate ou sulfonate, comme le 2- sulfooxyethyl méthacrylate, l'acide vinylbenzène sulfonique, l'acide allyl sulfonique, le 2-acrylamido-2méthylpropane sulfonique, l'acrylate ou le méthacrylate de sulfoethyle , l'acrylate ou le méthacrylate de sulfopropyle et leurs sels hydrosolubles
• des monomères possédant au moins une fonction phosphonate ou phosphate, comme l'acide vinylphosphonique,... les esters de phosphates éthyléniquement insaturés tels que les phosphates dérivés du méthacrylate d'hydroxyéthyle (Empicryl 6835 de RHODIA) et ceux dérivés des méthacrylates de polyoxyalkylènes et leurs sels hydrosolubles
A titre d'exemples de monomères neutres non-ioniques hydophobes, dont peuvent des unités AN, on peut mentionner :
• les monomères vinylaromatiques tels que styrène, alpha-méthylstyrène, vinyltoluène...
• les halogénures de vinyle ou de vinylidène, comme le chlorure de vinyle, chlorure de vinylidène
• les C1-C12 alkylesters d'acides α-β monoéthyléniquement insaturés tels que les acrylates et méthacrylates de méthyle, éthyle, butyle, acrylate de 2-éthylhexyle ... • les esters de vinyle ou d'allyle d'acides carboxyliques saturés tels que les acétates, propionates, versatates, stéarates ... de vinyle ou d'allyle
• les nitriles α-β monoéthyléniquement insaturés contenant de 3 à 12 atomes de carbone, comme l'acrylonitrile, le methacrylonitrile ...
• les α-oléfines comme l'éthylène ... • les diènes conjugués, comme le butadiène, l'isoprène, le chloroprène,
• les monomères susceptibles de générer des chaînes polydiméthylsiloxane (PDMS). Ainsi la partie B peut être un silicone, par exemple une chaîne polydiméthylsiloxane ou un copolymère comprenant des unités diméthylsiloxy.
A titre d'exemples de monomères neutres hydrophiles non-ioniques, dont peuvent dériver des unités AN on peut mentionner :
• les hydroxyalkylesters d'acides α-β éthyléniquement insaturés comme les acrylates et méthacrylates d'hydroxyéthyle, d'hydroxypropyle, le glycérol monométhacrylate...
• les amides α-β éthyléniquement insaturés comme l'acrylamide, le N,N-diméthyl méthacrylamide, le N-méthylolacrylamide ... • les monomères α-β éthyléniquement insaturés portant un segment polyoxyalkyléné hydrosoluble du type polyoxyde d'éthylène, comme les polyoxyde d'éthylène α- méthacrylates (BISOMER S20W, S10W, ... de LAPORTE) ou α,ω-diméthacrylates, le SIPOMER BEM de RHODIA (méthacrylate de polyoxyéthylène ω-béhényle), le SIPOMER SEM-25 de RHODIA (méthacrylate de polyoxyéthylène ω- tristyrylphényle) ...
• les monomères α-β éthyléniquement insaturés précurseurs d'unités ou de segments hydrophiles tels que l'acétate de vinyle qui, une fois polymérisés, peuvent être hydrolyses pour engendrer des unités alcool vinylique ou des segments alcool polyvinylique.
Polymère
Le polymère selon l'invention peut être un copolymère statistique, un copolymère à blocs, un copolymère à gradient de concentration, un copolymère étoile, un co- oligomère ou d'un co-télomère. Il s'agit de préférence d'un copolymère statistique. Selon un mode de réalisation intéressant, le polymère est hydrosoluble ou hydrodispersable. Cela signifie que ledit polymère ne forme pas dans l'eau, sur au moins dans un certain domaine de pH et de concentration, une composition diphasique dans les conditions de mise en œuvre.
Le polymère selon l'invention peut être présenté notamment sous forme de poudre, sous forme de dispersion dans un liquide ou sous forme de solution dans un solvant (eau ou autre). La forme dépend généralement des exigences liées à l'utilisation du polymère. Elle peut être aussi liée au procédé de préparation du polymère.
Le polymère peut comprendre de 0,1% à 99,9 % en nombre (molaire) d'unités dérivant du monomère de formule (I) ou (I'), par rapport au nombre total d'unité dans le polymère. Il comprend de préférence de 0,1% à 15% en nombre (molaire).
Le polymère peut comprendre de 0,1% à 99,9 % en nombre (molaire) d'unités cationiques ou potentiellement cationiques, par rapport au nombre total d'unité dans le polymère. Il comprend de préférence de 0,1% à 15% en nombre (molaire).
La masse molaire moyenne en poids, absolue, peut être de préférence comprise entre 1000 g/mol et 5 00 000 g/mol. Elle est de préférence comprise entre 50 000 g/mol et 1 000 000 g/mol.
Procédé de préparation de polymères selon l'invention
Les polymères selon l'invention peuvent être obtenus par toute méthode connue, que ce soit par polymérisation radicalaire, contrôlée ou non, par polymérisation par ouverture de cycle (notamment anionique ou cationique, avec des monomères appropriés), par polymérisation anionique ou cationique, ou encore par modification chimique d'un polymère.
La polymérisation radicalaire est de préférence conduite dans un environnement exempt d'oxygène, par exemple en présence d'un gaz inerte (hélium, argon, azote, etc). La réaction est effectuée dans un solvant inerte, de préférence le méthanol ou l'éthanol, et de façon plus préférée dans l'eau.
La polymérisation est initiée par addition d'un amorceur de polymérisation. Les amorceurs utilisés sont les générateurs de radicaux libres habituellement utilisés dans la technique. Des exemples comprennent les peresters organiques; des composés organiques de type azo, par exemple le chlorhydrate d'azo-bis-amidino-propane, l'azo- bis-isobutyronitrile, Pazo-bis-2,4-diméthylvaléronitrile, etc) ; les peroxydes inorganiques et organiques, par exemple le peroxyde d'ammonium, de sodium, de potassium, peroxyde d'hydrogène, le peroxyde de benzyle et le peroxyde de butyle, etc ; des systèmes d'initiateurs redox, par exemple ceux comprenant des agents oxydants, tels que les persulfates (notamment les persulfates d'ammonium ou de métaux alcalins, etc), les chlorates et les bramâtes (y compris les chlorates et/ou les bramâtes inorganiques ou organiques), et les agents réducteurs tels que les sulfites et bisulfites (y compris les sulfites ou bisulfites inorganiques et/ou organiques) l'acide oxalique et l'acide ascorbique ainsi que les mélanges de deux ou plusieurs de ces composés. Les amorceurs préférés sont des amorceurs solubles dans l'eau. On préfère en particulier le persulfate de sodium et le chlorhydate d'azo-bis-amidinopropane.
En variante, la polymérisation peut être initiée par irradiation à l'aide de lumière ultra-violette. La quantité d'amorceur utilisée est en général, une quantité suffisante pour réaliser l'amorçage de la polymérisation. De préférence, les amorceurs sont présents en une quantité allant de 0,001 à environ 10 % en poids par rapport au poids total des monomères, et de préférence sont compris en une quantité inférieure à 2 % en poids par rapport au poids total des monomères, une quantité préférée étant située dans la plage de 0,05 à 1 % en poids par rapport au poids total des monomères. L'amorceur est ajouté au mélange de polymérisation, soit de manière continue soit de manière discontinue.
Lorsque l'on veut obtenir des copolymères de masse moléculaire élevée, il est souhaitable de rajouter de l'amorceur pendant la réaction de polymérisation. L'addition
peut être graduelle ou discontinue. La polymérisation est réalisée dans des conditions réactionnelles efficaces pour polymériser les monomères (c) et les monomères (a) en atmosphère exempte d'oxygène. De préférence, la réaction est conduite à une température allant d'environ 30° à environ 100° et de préférence entre 60° et 900C. L'atmosphère exempte d'oxygène est maintenue pendant toute la durée de la réaction, par exemple par maintien d'un balayage d'azote tout au long de la réaction.
On peut notamment utiliser des méthodes de polymérisation radicalaire dite vivante ou contrôlée. Ces méthodes sont particulièrement utiles pour la préparation de copolymères à structure contrôlée.
A titre d'exemple de procédés de polymérisation dite vivante ou contrôlée, on peut notamment se référer à :
- les procédés des demandes WO 98/58974, WO 00/75207 et WO 01/42312 qui mettent en œuvre une polymérisation radicalaire contrôlée par des agents de contrôle de type xanthates,
- le procédé de polymérisation radicalaire contrôlée par des agents de contrôles de type dithioesters de la demande WO 98/01478, le procédé décrit dans la demande WO 02/08307, notamment pour l'obtention de copolymères comprenant des bloc polyorganosiloxane, - le procédé de polymérisation radicalaire contrôlée par des agents de contrôle de type dithiocarbamates de la demande WO 99/31144,
- le procédé de polymérisation radicalaire contrôlée par des agents de contrôle de type dithiocarbazates de la demande WO 02/26836, le procédé de polymérisation radicalaire contrôlée par des agents de contrôle de type dithiophosphoroesters de la demande WO 02/10223,
(éventuellement les copolymères à blocs obtenus comme ci-dessus par polymérisation radicalaire contrôlée, peuvent subir une réaction de purification de leur extrémité de chaîne soufrée, par exemple par des procédés de type hydrolyse, oxydation, réduction, pyrolyse ou substitution) - le procédé de la demande WO 99/03894 qui met en œuvre une polymérisation en présence de précurseurs nitroxydes,
- le procédé de la demande WO 96/30421 qui utilise une polymérisation radicalaire par transfert d'atome (ATRP), le procédé de polymérisation radicalaire contrôlée par des agents de contrôle de type iniferters selon l'enseignement de Otu et al., Makromol. Chem. Rapid.
Commun., 3, 127 (1982),
- le procédé de polymérisation radicalaire contrôlée par transfert dégénératif d'iode selon l'enseignement de Tatemoto et al., Jap. 50, 127, 991 (1975), Daikin Kogyo Co Itd Japan et Matyjaszewski et al., Macromolecules, 28, 2093 (1995),
- le procédé de polymérisation radicalaire contrôlée par les dérivés du tetraphényléthane, divulgué par D. Braun et al. Dans Macromol. Symp. 111 ,63
(1996), ou encore,
- le procédé de polymérisation radicalaire contrôlée par des complexes organocobalt décrit par Wayland et al. Dans J.Am.Chem.Soc. 116,7973 (1994)
- le procédé de polymérisation radicalaire contrôlée par du diphénylethylène (WO 00/39169 ou WO 00/37507).
Lorsqu'il s'agit de copolymères à architecture contrôlée greffés ou peignes, ceux- ci peuvent être obtenus par des méthodes dites de greffage direct et copolymérisation. Le greffage direct consiste à polymériser le(s) monomère(s) choisi(s) par voie radicalaire, en présence du polymère sélectionné pour former le squelette du produit final. Si le couple monomère / squelette ainsi que les conditions opératoires, sont judicieusement choisis, alors il peut y avoir réaction de transfert entre le macroradical en croissance et le squelette. Cette réaction génère un radical sur le squelette et c'est à partir de ce radical que croît le greffon. Le radical primaire issu de l'amorceur peut également contribuer aux réactions de transfert. Pour ce qui a trait à la copolymérisation, elle met en œuvre dans un premier temps le greffage à l'extrémité du futur segment pendant, d'une fonction polymérisable par voie radicalaire. Ce greffage peut être réalisé par des méthodes usuelles de chimie organique. Puis, dans un second temps, le macromonomère ainsi obtenu est polymérisé avec le monomère choisi pour former le squelette et on obtient un polymère dit "peigne". Le greffage peut être réalisé avantageusement en présence d'un agent de contrôle de la polymérisation tel que cité dans les références ci-dessus.
Les procédés de préparation de polymères en forme d'étoile peuvent être essentiellement classés en deux groupes. Le premier correspond à la formation des bras des polymères à partir d'un composé plurifonctionnel constituant le centre (technique "core-first") (Kennedy, J.P. and coll. Macromolecules, 29, 8631 (1996), Deffieux, A. and coll. Ibid, 25, 6744, (1992), Gnanou, Y. and coll. Ibid, 31, 6748 (1998)) et le second correspond à une méthode où les molécules de polymères qui vont constituer les bras sont d'abord synthétisées et ensuite liées ensemble sur un cœur pour former un polymère en forme d'étoile (technique "arm-first"). A titre d'exemple de synthèse de ce type de polymère, on pourra se référer au brevet WO 00/02939. On peut citer également les procédés de polymérisation à partir d'un
cœur comprenant plusieurs groupes de transfert, et les procédés de réticulation de micelles.
Utilisations Le polymère selon l'invention peut notamment être utilisé en tant qu'agent émulsifiant ou co-émulsifiant pour préparer ou stabiliser des émulsions. Il peut par exemple être utilisé dans des émulsions dont une phase est une huile silicone. Il peut être utilisé également pour compatibiliser plusieurs composés au sein d'une formulation. Il peut également être utilisé comme agent d'aide au dépôt d'un autre composé, ou comme déclencheur du dépôt d'un autre composé. Il peut trouver une utilité pour vectoriser un composé, par exemple silicone, sur une surface.
Le polymère peut notamment être utilisé dans des compositions cosmétiques, dans des compositions détergentes pour les soins ménagers, dans des compositions pour le soin du linge, ou en tant qu'agent de reconnaissance moléculaire, ou en tant qu'agent de passage transmembranaire, ou comme additif pour pâte à papier, composition de couchage pour papier, peinture, par exemple peinture pour bois. A titre de compositions cosmétiques on peut citer les shampoings, les après-shampoing, les gel-douche ou les crèmes pour le soin de la peau. Ces compositions peuvent en outre comprendre au moins un tensioactif anionique et/ou amphotère, et éventuellement des agents tels que des huiles silicones, des huiles non silicones, des polysaccharides éventuellement modifiés. Dans ces compositions, le polymère peut apporter des effets de conditionnement, d'aide au conditionnement, des effets sensoriels ou «cosmétiques», des effets de toucher, de la douceur, de la souplesse, une aide au démêlage, de la brillance, de l'aptitude au coiffage sur cheveux secs ou mouillés.
D'autres détails ou avantages de l'invention apparaîtront au vu des exemples ci- dessous, sans caractère limitatif.
EXEMPLES
Exemple 1: Synthèse d'un monomère Λ/-acétyl-Λ/-r(Λ/-2-thioéthvD-2- propenamideipropyn-β-D-qlucopyranosyl-d ->4)-β-D-glucopyranosylamine (Produit 4).
Etape 1: Synthèse de Λ/-acétyl- Λ/-allyl-β-D-glucopyranosyl-(1->4)-β -D- glucopyranosylamine (Produit 2)
(Produit 2)
Du cellobiose (Fluka) (5g, 14.6 mmol) est mis en solution dans de l'allylamine (Aldrich) (150 ml).
Le mélange réactionnel est maintenu sous agitation magnétique pendant 72h à température ambiante. Une chromatographie sur couche mince («CCM», acétate d'éthyle/ éther de pétrole 1/1) est effectuée sur un aliquot acétylé selon une méthode classique (pyridine/ anhydride acétique 1/1). Après évaporation à sec, le produit obtenu est une poudre blanche.
Le brut de réaction est Λ/-acétylé sélectivement dans une solution méthanol/anhydride acétique (10OmL, 5/1 ,v/v). La conversion est suivie par chromatographie sur couche mince (acétonitrile/eau 7/3). La solution est laissée sous agitation pendant 4h puis évaporée à sec après ajout de méthanol (3 fois). Une CCM montre la formation d'un deuxième composé probablement O-acétylé. Pour l'éliminer le brut est repris dans du méthanol (10OmL), et une solution de MeONa 1 M est ajoutée goutte à goutte jusqu'à l'obtention d'un pH de 10. Ce pH est déterminé par dépôt d'une goutte de mélange réactionnel sur une bandelette de papier pH humidifiée. Un contrôle par CCM montre la disparition du composé O-acétylé. La solution est ensuite neutralisée sur Résine Amberiite IR 120 H+, filtrée, évaporée à sec, et lyophilisée. Le produit 2 est obtenu avec un rendement quantitatif (6.18g).
RMN 1H (300 MHz, D2O, 353K)
5=5.86-5.98 (dddd-oct,1H, CH=CH2), 5.32 (d,1 H, J1|2 = 8.04 Hz, H1 13), 5.32-5.15 (m, 2H, -CH=CH2), 4.54 (d, H1"), 4.05-3.91 (m,2H,-CH2-CH=CH2), 3.83-3.77 (m, 2H, H- 6"), 3.75-3.71 (m, H-6), 3.75-3.67 (m, 4H, H-2, H-3, H-4, H-5), 3.56-3.31 (m, 4H, H-3", H-5", H-4", H-2"), 2.23 (s, 3H, -CH3(Ac)). RMN 13C (75 MHz, D2O, 300K)
8=178.41 (-C=O), 135.4 (CH=CH2), 117.76 (CH=CH2), 103.44 (C-111), 83.42 (C- 1 ), 79.45 (C-2), 77.88 (C-3), 77.07 (C-3π), 76.75 (C-5), 76.34 (C-5π), 74.30 (C-2n), 70.71 et 68.91 (C-4 et C-4 "), 61.85 (C-6"), 61.41 (C6), 42.49 (CH2-CH=CH2), 24.33 (-CH3(Ac)). MS (FAB+): m/z = 424 [M + H]+ m/z = 446 [M + Na]+.
Etape 2 : synthèse de Λ/-acétyl-Λ/-[(/V-2-thioaminoéthyl)propyl]-(β-D-glucopyranosyl)- (1→4)-β-D-glucopyranosylamine (produit 3) - par réaction photochimique
Dans une cellule photochimique, au produit 2 (5g, 11.8 mmol), repris dans un minimum d'eau (25mL), est ajoutée de la cystéamine (chlorhydrate de 2- aminoéthanethiol 98 %, Acros Organics) (9.36g, 82.6 mmol, 7 eq). Le tout est irradié (254 nm) sous argon et maintenu sous agitation magnétique à température ambiante pendant 24h. Une chromatographie sur couche mince révèle la présence du produit 3. Celui-ci est purifié sur colonne de résine échangeuse d'ions (DOWEX X 50 WX4) de forme ionique H+ et élue successivement par H2O et NH4OH 0,1 M. Le produit 3 est ensuite lyophilisé et est obtenu avec un rendement de 65% (3.8g, 7.68 mmol).
RMN 1H (300 MHz, D2O, 353K) δ=5.02 (d, 1 H, J1|2 = 8.04 Hz, H/), 4.56 (d,1 H, H1"), 4.01-3.36 (m, 16H), 2.75- 2.63 (m, 4H, S-CH2et CH2-S), 2.27 (s, 3H, CH3(Ac)), 1.94 (m, 2H, -CH2). RMN 13C (75 MHz, D2O, 303K) δ=176.6 et 175.74 (-C=O), 102.86 (C-111), 87.22 (C-1), 78.47 et 77.39 (C-2 et C-
3), 77.17 (C-3 "), 76.39 (C-5 "), 75.75 (C-5), 73.52 (C-2 "), 70.31 (C-4), 69.84 (C-4 "), 60.99 (C-6 "), 60.46 (C-6), 40.65 (-CH2), 29.72 (-CH2), 29.50-28.62-28.23 (3*-CH2), 21.90-21.73 (-CH3(Ac)). MS (FAB+): m/z= 501 [M + H]+
Etape 3: synthèse de Λ/-acétyl-W-[(Λ/-2-thioéthyl)-2-propenamide]propyl]-β-D- glucopyranosyl-(1-»4)-β-D-glucopyranosylamine (Produit 4)
Le produit 3 (5g, 10 mmol) est solubilisé dans un mélange eau/méthanol (75 mL ; 1/1, v/v) en présence de carbonate de sodium (7.7g). Le milieu est maintenu à 00C sous agitation magnétique pendant qu'une solution de chlorure d'acryloyle (4,6 mL, 56.9 mmol, Fluka) et THF (35 mL) est ajouté progressivement pendant 5 min. Une chromatographie sur couche mince (CH3CN / H2O : 6-4) montre une conversion totale du produit 3 en un composé ayant un Rf = 0.6. Le mélange est repris dans 300 mL d'eau puis reconcentré et repris une nouvelle fois dans 200 mL d'eau en présence d'inhibiteur de radicaux (2,6-di-tert-butyl-4-methylphenol) (7.7mL d'une solution de THF à 0.5% d'inhibiteur). Le produit 4 est concentré puis purifié sur colonne de gel de silice
C18 et lyophilisé (5.5g, 100%)
RMN 1H (300 MHz, D2O, 353K) δ= 6.249(m, 2H, CH=CH2), 5.799(dd, 1H1 CH=CH2), 4.95(d, 1H, J1|2 = 7.68 Hz, H1 13), 4.55(d, 1H, H1"), 4.17-3.31 (m, 16H), 2.79(m, 2H1 NCH2CH2CH2S), 2.65(m, 2H, NCH2CH2CH2S), 2.24(s, 3H, CH3 (Ac)), 1.94(m, 2H, NCH2CH2CH2S). RMN 13C (75 MHz, D2O, 303K) δ=175.89 et 168.95(-C=O) 130.35 (CH=CH2) et 127.80 (CH=CH2), 102.90 (C-111), 87.27 (C-1), 78.57 et 77.46(C-2 et C-3), 77.24 (C-3π), 76.41 (C-5π), 75.87 (C-5), 73.57(C-2"), 70.33 (C-4), 69.87 (C-4π), 60.99 (C-6π), 60.58(C-6), 39.16 (-CH2), 30.92, 30.70, 28.99, 28.37, (4*-CH2), 21.76 (-CH3(Ac)). MS (FAB+): m/z≈ 577 [M + Na]+. Spectre de masse haute résolution (ESI+): C22H38N2O12S
Valeur calculée : m/z = 577,20432 [M + Na]+ Valeur mesurée : m/z = 577,2043 [M + Na]+
Exemple 2: Synthèse d'un copolvmère comprenant des unités dérivant de MAPTAC et des unités dérivant du produit 4
Rapport molaire: 95% MAPTAC, 5% du produit 4
Méthode: introduction MAPTAC et produit 4 en réacteur agité fermé
Amorceur: V50
NH
C-NH2 Me NH
I II
Me-C-N=N-C-C- -NH2
Me Me (V50)
Le produit 4 (0.376g) et le MAPTAC (6g, Aldrich) sont dilués dans un minimum d'eau (3g) à 800C sous courant d'azote. Le V50 est injecté toutes les heures pendant trois heures. La polymérisation suit le protocole suivant: t° : injection d'amorceur à 0.4% molaire par rapport à la somme des monomères (13.8 mg dans 250 μL H2O) t1 : injection d'amorceur à 0.4% molaire par rapport à la somme des monomères (13.8 mg dans 250 μL H2O) t2 : injection d'amorceur à 0.2% molaire par rapport à la somme des monomères (6.9 mg dans 250 μL H2O) t3 : injection d'amorceur à 0.2% molaire par rapport à la somme des monomères
(6.9 mg dans 250 μL H2O) cuisson d'une heure à 850C t4 : on laisse revenir la solution à température ambiante Conversion totale: 99% Après ultrafiltration sur membrane 10KDa, le polymère est obtenu avec un rendement massique de 83%.
Les masses molaires moyennes en nombre (Mn) et en poids (Mw) sont mesurées par GPC couplée MALS et conductimétrie dans les conditions suivantes :
Colonnes : Précolonne + 3 colonnes Aquagel Mixte de Polymer - Laboratories (30cm, 8μm)
- Température : T0 ambiante (22°C) Détecteurs :
- Réfractomètre : Rl Waters 410, sensibilité 8 T° 40°C RP03484
- DDL : diffusion de lumière MALLS Wyatt, laser He 633nm RP 03810 - Conductimètre Waters R432 (10μS/V)
- Eluant : eau Millipore 18 MΩ, BrNBu4 0.065M, N3 Na 1/10 000, HCOOH 1 ml/5] vecteur, Polydiallyldimethylammnium chloride (PDAMAC) de haute masse 10ppm sec
- Débit : 1 ml/ mn - Concentration : 40mg /20ml
- Volume injecté : 100μl, filtration 0.45μm
Mw : 1 244 000 g/mol Mn : 360 000 g/mol
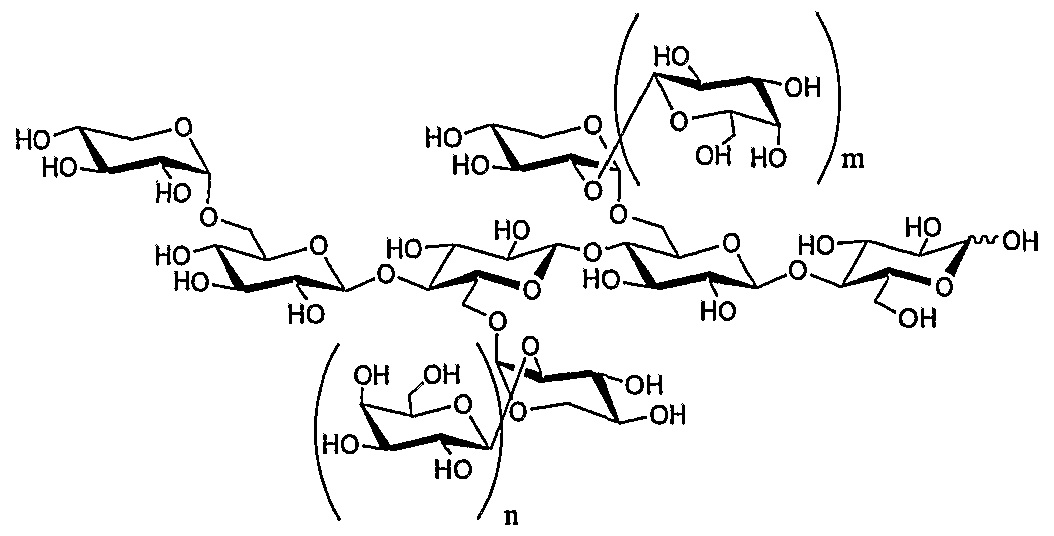
Exemple 3: Synthèse d'oligomères dérivés de xylogucanes
Etape 1 : Hydrolyse de xyloglucanes. Obtention des oligomères XXXG, XXLG (ou XLXG) et XLLG (produits 5,6,7) par la cellulase 3042A
On travaille sur un mélange comprenant les DP 7, 8, 9 respectivement le XXXG, le XXLG (et XLXG) et le XLLG dans un rapport molaire 15%, 35% et 50%.
Produit 5 (DP 7): m=0, n=0 Produit 6 (DP 8): m=0, n=1 (ou m=1 , n=0) Produit 7 (DP 9): m=1 , n=1
13g de xyloglucane de graine de tamarin (3A, Dainippon Pharmaceutical) sont mis en suspension dans de l'eau (1 L) distillée à 37°C sous agitation. Après solubilisation, la cellulase 3042A (2,7mL) est ajoutée alors dans le milieu. Le mélange est agité pendant quatre heures. Une chromatographie sur couche mince (CH3CN/H20 : 7/3) montre la formation des produits 5, 6, 7.
La solution est ensuite portée à ébullition pour dénaturer l'enzyme, filtrée et lyophilisée. Deux ultrafiltrations successives sont effectuées avec des membranes de 500 Da et 10000 Da. Après ces ultrafiltrations on obtient le mélange de produits 5, 6 et 7 avec un rendement massique de 80%. MS (MALDI-TOF) : (5) m/z = 1085 [M+Na]+
(6) m/z = 1247 [M+Na]+ (7) m/z = 1409 [M+Na]+
Etape 2: synthèse de N-acétyl-N-allyl-glycosylamines (produits 8,9,10)
Le mélange 5, 6 et 7 (5g) est mis en solution dans l'allylamine (100 ml_, Aldrich).
Le mélange réactionnel est maintenu sous agitation magnétique pendant 4 jours à température ambiante. Après évaporation à sec (co-évaporation avec le toluène) le mélange obtenu est un solide blanc Λ/-acétylé sélectivement pendant une nuit dans 1 L d'une solution MeOH/Ac2O (20/1, v/v). La conversion est suivie par chromatographie sur couche mince (CH3CN/H2O : 6/4). Les produits 8, 9 et 10 sont ensuite concentrés et lyophilisés (4.9g, 94%) MS (MALDI-TOF) : (8) m/z = 1166 [M+H]+ (9) m/z = 1328 [M+H]+ (10) m/z = 1490 [M+H]+ RMN 1H (300 MHz, D2O, 353K) δ= 5.96(dddd, 1 H1 CH=CH2), 5.29(m, 1 H, CH=CH2,), 5.18 et 4.98(d, 1 H, H1xy,), 4.58(dd, 1 H, H1gluc etgai), 4.10-3.41(m, H), 2.27(s, 3H, CH3 (Ac)).
Etape 3: synthèse de N-acétyl-N-[(N-2-thioaminoéthyl)propyl]-β-D-glucosylamine (produits 11 ,12,13)
Au mélange 8, 9 et 10 (20g, 15 mmol), repris jusqu'à solubilité dans un minimum d'eau distillée (250 mL), est ajoutée de la cystéamine (chlorhydrate 2-aminoéthanethiol 98%, Acros Organics) (8.69g, 5eq).
La solution est irradiée à 254 nm dans une cellule photochimique en quartz maintenue sous argon. Le mélange réactionnel, sous agitation magnétique, est laissé pendant 48h. Une chromatographie sur couche mince (CH3CN / H2O : 1-1 ) montre une conversion presque totale du mélange. Les produits 11 , 12 et 13 sont lavés au méthanol pour enlever l'excédent de cystéamine, filtrés sur bϋchner et purifiés sur résine échangeuse d'ions (DOWEX 50WX4) de forme ionique H+ activée par HCI 0,5M et éluée successivement par H2O et NH4OH 0,1 M. 11 , 12 et 13 sont lyophilisés (17 g, 81 %) MS (MALDI-TOF) : (11) m/z = 1221 [M+H]+
(12) m/z = 1383 [M+H]+ (13) m/z = 1545 [M+H]+
RMN 1H (300 MHz, D2O, 353K) δ= 5.19 et 4.98 (d, 1H, H1xy,), 4.61 (dd, H, H1gluc et gai), 4.06-3.41 (m, H), 2.80(m, 2H, NCH2CH2CH2S), 2.68(m, 2H1 NCH2CH2CH2S), 2.28(s, 3H, CH3 (Ac)), 1.96(m, 2H, NCH2CH2CH2S).
Etape 4 : synthèse de macromonomères 3-(2-N-[(N-2-thioéthyl)-2-propenamide]propyl]- β-D-glucosylamine (produits 14, 15, 16)
Produit 14 (DP 7): m=0, n=0 Produit 15 (DP 8): m=0, n=1 (ou m=1 , n=0) Produit 16 (DP 9): m=1 , n=1
Les produits 11 , 12 et 13 (7.8g, 5.43 mmol) sont solubilisés dans un mélange eau/méthanol (40 mL ; 1-1) en présence de carbonate de sodium (4g). Le milieu est maintenu à O0C sous agitation magnétique pendant qu'une solution de chlorure d'acryloyle (2.4 mL, 29.6 10"3 mol, Fluka) et THF (2OmL) est ajouté progressivement pendant 5 min. La réaction est suivie par chromatographie sur couche mince (CH3CN/H2O : 6/4). Le mélange est repris dans 120 mL d'eau puis reconcentré et repris une nouvelle fois dans 80 mL d'eau en présence d'inhibiteur de radicaux (2,6-di-tert-
butyl-4-methylphenol) (100μL d'une solution de THF à 0,5%). Le mélange 14, 15 et 16 est concentré puis purifié sur colonne de gel de silice C18 et lyophilisé (8 g, 100%) MS (MALDI-TOF) : (14) m/z = 1297 [M+Na]+
(15) m/z = 1459 [M+Na]+
(16) m/z = 1621 [M+Na]+ RMN 1H (300 MHz, D2O, 353K) δ= 6.32-6.20(m, 2H, CH=CW2), 5.80(dd, 1H, CH=CH2), 5.18 et 4.98(d, 2H, H1xy,), 4.61 (d, H, H1glc et gai), 4.09-3.40(m, H), 2.84(m, 2H, NCH2CH2CH2S), 2.68(m, 2H, NCH2CH2CH2S), 2.26(s, 3H, CH3 (Ac)), 1.95(m, 2H, NCH2CH2CH2S).
Exemple 4: Synthèse d'un copolymère comprenant des unités dérivant de MAPTAC et des unités dérivant des produits 14. 15, 16
Rapport molaire: 95% MAPTAC, 5% du mélange 14, 15 et 16
Méthode: introduction MAPTAC et le mélange en réacteur agité fermé
Amorceur: V50
Les produits 14, 15 et 16 (0.976g) et le MAPTAC (6g, Aldrich) sont dilués dans un minimum d'eau (7g) à 8O0C sous courant d'azote. Le V50 est injecté toutes les heures pendant trois heures. La polymérisation suit le protocole :
t° : injection d'amorceur à 0.4% molaire par rapport à la somme des monomères (13.8 mg dans 250 μL H2O) t1 : injection d'amorceur à 0.4% molaire par rapport à la somme des monomères (13.8 mg dans 250 μL H2O) t2 : injection d'amorceur à 0.2% molaire par rapport à la somme des monomères
(6.9 mg dans 250 μL H2O) t3 : injection d'amorceur à 0.2% molaire par rapport à la somme des monomères (6.9 mg dans 250 μL H2O) cuisson d'une heure à 85°C t4 : on laisse revenir la solution à température ambiante
Des prélèvements de 250μL sont effectués toutes les heures pour des études cinétiques et de l'hydroquinone (inhibiteur de réaction) est ajouté dans chaque prélèvement.
Conversion : 96% MAPTAC
95% produits 14, 15 et 16
Après ultrafiltration sur membrane 10KDa, le polymère est obtenu avec un rendement massique de 83%. Mw : 3 047 000 g/mol Mn : 795 000 g/mol
Exemple 5: Synthèse d'un monomère Λ/-acétyl-Λ/-r(Λ/-2-thioéthyl)-2- propenamidelpropyl1-β-D-qlucopyranosyl-(1->4)-β-D-glucopyranosylarnine (Produit 4bis).
Etape 1 : Synthèse de Λ/-acétyl- Λ/-allyl-β-D-glucopyranosyl-(1→4)-β -D- glucopyranosylamine (Produit 2bis)
(Produit 2bis) Du cellobiose (Fluka) (5g, 14.6 mmol) est mis en solution dans de l'allylamine
(Aldrich) (150 ml).
Le mélange réactionnel est maintenu sous agitation magnétique pendant 72h à température ambiante. Une chromatographie sur couche mince («CCM», acétate d'éthyle/ éther de pétrole 1/1) est effectuée sur un aliquot acétylé selon une méthode
classique (pyridine/ anhydride acétique 1/1). Après évaporation à sec, le produit obtenu est une poudre blanche.
Le brut de réaction est Λ/-acétylé sélectivement dans une solution méthanol/anhydride acétique (10OmL, 5/1 ,v/v). La conversion est suivie par chromatographie sur couche mince (acétonitrile/eau 7/3). La solution est laissée sous agitation pendant 4h puis évaporée à sec après ajout de méthanol (3 fois). Une CCM montre la formation d'un deuxième composé probablement O-acétylé. Pour l'éliminer le brut est repris dans du méthanol (10OmL), et une solution de MeONa 1 M est ajoutée goutte à goutte jusqu'à l'obtention d'un pH de 10. Ce pH est déterminé par dépôt d'une goutte de mélange réactionnel sur une bandelette de papier pH humidifiée. Un contrôle par CCM montre la disparition du composé O-acétylé. La solution est ensuite neutralisée sur Résine Amberlite IR 120 H+, filtrée, évaporée à sec, et lyophilisée. Le produit 2bis est obtenu avec un rendement quantitatif (6.18g).
RMN 1H (300 MHz, D2O, 353K) δ=5.86-5.98 (dddd-oct,1H, CH=CH2), 5.32 (d,1 H, J1i2 = 8.04 Hz, H1 13), 5.32-5.15 (m, 2H, -CH=CH2), 4.54 (d, H1"), 4.05-3.91 (m,2H,-CH2-CH=CH2), 3.83-3.77 (m, 2H1 H- 6"), 3.75-3.71 (m, H-6), 3.75-3.67 (m, 4H, H-2, H-3, H-4, H-5), 3.56-3.31 (m, 4H, H-3", H-5", H-4", H-2"), 2.23 (s, 3H, -CH3(Ac)). RMN 13C (75 MHz, D2O, 300K) δ=178.41 (-C=O), 135.4 (CH=CH2), 117.76 (CH=CH2), 103.44 (C-111), 83.42 (C- 1), 79.45 (C-2), 77.88 (C-3), 77.07 (C-3"), 76.75 (C-5), 76.34 (C-5π), 74.30 (C-2n), 70.71 et 68.91 (C-4 et C-4"), 61.85 (C-6"), 61.41 (C6), 42.49 (CH2-CH=CH2), 24.33 (-CH3(Ac)). MS (FAB+): m/z = 424 [M + H]+ m/z = 446 [M + Na]+.
Etape 2 : synthèse de Λ/-acétyl-Λ/-[(Λ/-2-thioaminoéthyl)propyl]-(β-D-glucopyranosyl)- (1→4)-β-D-glucopyranosylamine (produit 3bis) - à l'aide d'initiateurs hydrosolubles
A une solution de produit 2bis (25g, 59 mmol) dans l'eau (40OmL) est ajoutée de la cystéamine (chlorhydrate de 2-aminoéthanethiol 98 %, Acros Organics) (25g, 0,22 mol, 3,7 eq) et du V-50 (dihydrochlorire de alpha.alpha'-azodiisobutyramidine dihydrochloride, 98%, Fluka) (16g, 59 mmol, 1 eq). Le mélange réactionnel est agité à 6O
0C, sous atmosphère d'argon, pendant 2h. La réaction est suivie par chromatographie sur couche mince (AcOEt/AcOH/H
2O 3/3/2 v/v/v). La solution est ensuite purifiée sur
colonne de résine échangeuse d'ions (DOWEX X 50 WX4) de forme ionique H
+ et éluée successivement par H
2O et NH
4OH 0.05M puis 0,1 M. Le produit 3bis est ensuite lyophilisé et est obtenu avec un rendement de 95% (28g, 56 mol).
Etape 3: synthèse de A/-acétyl-Λ/-[(Λ/-2-thioéthyl)-2-propenamide]propyl]-β-D- glucopyranosyl-(1-»4)-β-D-glucopyranosylamine (Produit 4bis)
Le produit 3bis (5g, 10 mmol) est solubilisé dans un mélange eau/méthanol (75 mL ; 1/1 , v/v) en présence de carbonate de sodium (7.7g). Le milieu est maintenu à O0C sous agitation magnétique pendant qu'une solution de chlorure d'acryloyle (4,6 mL, 56.9 mmol, Fluka) et THF (35 mL) est ajouté progressivement pendant 5 min. Une chromatographie sur couche mince (CH3CN / H2O : 6-4) montre une conversion totale du produit 3 en un composé ayant un Rf = 0.6. Le mélange est repris dans 300 mL d'eau puis reconcentré et repris une nouvelle fois dans 200 mL d'eau en présence d'inhibiteur de radicaux (2,6-di-tert-butyl-4-methylphenol) (7.7mL d'une solution de THF à 0.5% d'inhibiteur). Le produit 4bis est concentré puis purifié sur colonne de gel de silice C18 et lyophilisé (5.5g, 100%) RMN 1H (300 MHz, D2O, 353K) δ= 6.249(m, 2H, CH=CH2), 5.799(dd, 1 H, CH=CH2), 4.95(d, 1H, J1i2 = 7.68 Hz, H/),
4.55(d, 1 H, H1"), 4.17-3.31 (m, 16H), 2.79(m, 2H, NCH2CH2CH2S), 2.65(m, 2H, NCH2CH2CH2S), 2.24(S1 3H, CH3 (Ac)), 1.94(m, 2H, NCH2CH2CH2S). RMN 13C (75 MHz, D2O, 303K) δ=175.89 et 168.95(-C=O) 130.35 (CH=CH2) et 127.80 (CH=CH2), 102.90 (C-111), 87.27 (C-1), 78.57 et 77.46(C-2 et C-3), 77.24 (C-3n), 76.41 (C-5M), 75.87 (C-5), 73.57(C-2"), 70.33 (C-4), 69.87 (C-4π), 60.99 (C-6n), 60.58(C-6), 39.16 (-CH2), 30.92, 30.70, 28.99, 28.37, (4*-CH2), 21.76 (-CH3(Ac)). MS (FAB+): m/z= 577 [M + Na]+. Spectre de masse haute résolution (ESI+): C22H38N2O12S Valeur calculée : m/z = 577,20432 [M + Na]+
Valeur mesurée : m/z = 577,2043 [M + Na]+