RU2786591C2 - Способ определения показателей коагуляции плазмы крови - активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину - Google Patents
Способ определения показателей коагуляции плазмы крови - активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину Download PDFInfo
- Publication number
- RU2786591C2 RU2786591C2 RU2020132717A RU2020132717A RU2786591C2 RU 2786591 C2 RU2786591 C2 RU 2786591C2 RU 2020132717 A RU2020132717 A RU 2020132717A RU 2020132717 A RU2020132717 A RU 2020132717A RU 2786591 C2 RU2786591 C2 RU 2786591C2
- Authority
- RU
- Russia
- Prior art keywords
- plasma
- coagulation
- curve
- heparin
- time
- Prior art date
Links
- 210000002381 plasma Anatomy 0.000 title claims abstract description 71
- 230000015271 coagulation Effects 0.000 title claims abstract description 53
- 238000005345 coagulation Methods 0.000 title claims abstract description 53
- 238000000034 method Methods 0.000 title claims abstract description 41
- 108090000190 Thrombin Proteins 0.000 title claims abstract description 40
- 229960004072 thrombin Drugs 0.000 title claims abstract description 40
- 230000000694 effects Effects 0.000 title claims abstract description 32
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 title claims abstract description 22
- 229960002897 heparin Drugs 0.000 title claims abstract description 22
- 229920000669 heparin Polymers 0.000 title claims abstract description 22
- 229950003499 fibrin Drugs 0.000 claims abstract description 26
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 claims abstract description 25
- 108010073385 Fibrin Proteins 0.000 claims abstract description 24
- 102000009123 Fibrin Human genes 0.000 claims abstract description 24
- 108010049003 Fibrinogen Proteins 0.000 claims abstract description 10
- 102000008946 Fibrinogen Human genes 0.000 claims abstract description 10
- 150000001875 compounds Chemical class 0.000 claims abstract description 10
- 229940012952 fibrinogen Drugs 0.000 claims abstract description 10
- 230000006641 stabilisation Effects 0.000 claims abstract description 5
- 238000011105 stabilization Methods 0.000 claims abstract description 5
- 230000008859 change Effects 0.000 claims abstract description 4
- 230000005855 radiation Effects 0.000 claims description 4
- 230000008569 process Effects 0.000 abstract description 15
- 230000023597 hemostasis Effects 0.000 abstract description 12
- 230000035945 sensitivity Effects 0.000 abstract description 8
- 239000003814 drug Substances 0.000 abstract description 3
- 238000011005 laboratory method Methods 0.000 abstract description 2
- 239000000126 substance Substances 0.000 abstract description 2
- 238000002795 fluorescence method Methods 0.000 abstract 1
- 230000015572 biosynthetic process Effects 0.000 description 7
- 208000007536 Thrombosis Diseases 0.000 description 6
- 230000004913 activation Effects 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 238000003745 diagnosis Methods 0.000 description 6
- 108010014806 prothrombinase complex Proteins 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 5
- 102000004190 Enzymes Human genes 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 229940088598 enzyme Drugs 0.000 description 5
- 208000024172 Cardiovascular disease Diseases 0.000 description 4
- 108060008539 Transglutaminase Proteins 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 230000003287 optical effect Effects 0.000 description 4
- 102000003601 transglutaminase Human genes 0.000 description 4
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 238000009825 accumulation Methods 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 239000003146 anticoagulant agent Substances 0.000 description 3
- 229940127219 anticoagulant drug Drugs 0.000 description 3
- 230000035602 clotting Effects 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 208000004476 Acute Coronary Syndrome Diseases 0.000 description 2
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 2
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 2
- 102000004506 Blood Proteins Human genes 0.000 description 2
- 108010017384 Blood Proteins Proteins 0.000 description 2
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 2
- 108010071289 Factor XIII Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 108010000499 Thromboplastin Proteins 0.000 description 2
- 102000002262 Thromboplastin Human genes 0.000 description 2
- 239000012190 activator Substances 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000003114 blood coagulation factor Substances 0.000 description 2
- 229910001424 calcium ion Inorganic materials 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 230000003301 hydrolyzing effect Effects 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 238000006116 polymerization reaction Methods 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 230000001953 sensory effect Effects 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 230000003595 spectral effect Effects 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 239000004475 Arginine Substances 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 206010053567 Coagulopathies Diseases 0.000 description 1
- 102000013566 Plasminogen Human genes 0.000 description 1
- 108010051456 Plasminogen Proteins 0.000 description 1
- 101800004937 Protein C Proteins 0.000 description 1
- 102000017975 Protein C Human genes 0.000 description 1
- 108010094028 Prothrombin Proteins 0.000 description 1
- 101800001700 Saposin-D Proteins 0.000 description 1
- 108090000083 Serine Endopeptidases Proteins 0.000 description 1
- 102000003667 Serine Endopeptidases Human genes 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 230000000035 biogenic effect Effects 0.000 description 1
- -1 biogenic molecules Chemical class 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 230000023555 blood coagulation Effects 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 210000000748 cardiovascular system Anatomy 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003593 chromogenic compound Substances 0.000 description 1
- 229940105784 coagulation factor xiii Drugs 0.000 description 1
- AGVAZMGAQJOSFJ-WZHZPDAFSA-M cobalt(2+);[(2r,3s,4r,5s)-5-(5,6-dimethylbenzimidazol-1-yl)-4-hydroxy-2-(hydroxymethyl)oxolan-3-yl] [(2r)-1-[3-[(1r,2r,3r,4z,7s,9z,12s,13s,14z,17s,18s,19r)-2,13,18-tris(2-amino-2-oxoethyl)-7,12,17-tris(3-amino-3-oxopropyl)-3,5,8,8,13,15,18,19-octamethyl-2 Chemical compound [Co+2].N#[C-].[N-]([C@@H]1[C@H](CC(N)=O)[C@@]2(C)CCC(=O)NC[C@@H](C)OP(O)(=O)O[C@H]3[C@H]([C@H](O[C@@H]3CO)N3C4=CC(C)=C(C)C=C4N=C3)O)\C2=C(C)/C([C@H](C\2(C)C)CCC(N)=O)=N/C/2=C\C([C@H]([C@@]/2(CC(N)=O)C)CCC(N)=O)=N\C\2=C(C)/C2=N[C@]1(C)[C@@](C)(CC(N)=O)[C@@H]2CCC(N)=O AGVAZMGAQJOSFJ-WZHZPDAFSA-M 0.000 description 1
- 238000010668 complexation reaction Methods 0.000 description 1
- GLNDAGDHSLMOKX-UHFFFAOYSA-N coumarin 120 Chemical compound C1=C(N)C=CC2=C1OC(=O)C=C2C GLNDAGDHSLMOKX-UHFFFAOYSA-N 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000013213 extrapolation Methods 0.000 description 1
- 229940012444 factor xiii Drugs 0.000 description 1
- 108010073651 fibrinmonomer Proteins 0.000 description 1
- 230000020764 fibrinolysis Effects 0.000 description 1
- 238000001506 fluorescence spectroscopy Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 229940106780 human fibrinogen Drugs 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000009878 intermolecular interaction Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 238000009533 lab test Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000010297 mechanical methods and process Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- UPSFMJHZUCSEHU-JYGUBCOQSA-N n-[(2s,3r,4r,5s,6r)-2-[(2r,3s,4r,5r,6s)-5-acetamido-4-hydroxy-2-(hydroxymethyl)-6-(4-methyl-2-oxochromen-7-yl)oxyoxan-3-yl]oxy-4,5-dihydroxy-6-(hydroxymethyl)oxan-3-yl]acetamide Chemical compound CC(=O)N[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@H]1[C@H](O)[C@@H](NC(C)=O)[C@H](OC=2C=C3OC(=O)C=C(C)C3=CC=2)O[C@@H]1CO UPSFMJHZUCSEHU-JYGUBCOQSA-N 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 229960000856 protein c Drugs 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 208000010110 spontaneous platelet aggregation Diseases 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229960003766 thrombin (human) Drugs 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 238000004804 winding Methods 0.000 description 1
Images
Abstract
Изобретение относится к области медицины, а именно к лабораторным способам исследования гемостаза, и касается определения показателей коагуляции плазмы крови – активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину. Используют флуоресцентный метод в видимом диапазоне излучения 420-600 нм в присутствии соединений бордипиринового ряда (BODIPY), таких как 4,4-дифторо-8-фенил-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3а,4а-диаза-s-индацен; 4,4-дифторо-8-(пара-диметиламинофенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3а,4а-диаза-8-индацен; 4,4-дифторо-8-(ди-ортометилфенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3а,4а-диаза-s-индацен, флуоресценция которых зависит от присутствия биомолекул фибриногена. Регистрируют зависимость интенсивности флуоресценции на максимуме испускания BODIPY, затем получают кривую коагуляции образца плазмы. При этом исследование прекращают при достижении устойчивого плато на кривой изменения флуоресценции. Далее анализируют кривую коагуляции, при этом на кривой коагуляции наблюдают и анализируют три участка: верхнее плато, ниспадающий участок и нижнее плато. При этом на основании длины верхнего плато (tlag) определяют толерантность плазмы к гепарину. Затем проводят касательную к ниспадающему участку кривой коагуляции, которая образует угол наклона φ к оси ординат: tg φ, который пропорционален активности тромбина. Время рекальцификации плазмы получают путем экстраполяции касательной к ниспадающему участку кривой коагуляции на ось абсцисс (время), отсекая стадию стабилизации фибринового сгустка. Изобретение обеспечивает расширение технических возможностей за счет определения трех указанных показателей коагуляции плазмы крови и повышение чувствительности и точности процесса их определения. 1 ил., 4 табл.
Description
Изобретение относится к области медицины, а именно к лабораторным способам исследования гемостаза.
Тромбин – IIa фактор свертывания крови, сериновая эндопептидаза, катализирующая ключевую реакцию гемостаза – гидролитическое расщепление фибриногена до фибрин-мономеров, которые самопроизвольно полимеризуются в фибрин — основу тромба. Кроме того, тромбин является одним из сильнейших индукторов агрегации тромбоцитов, активатором ключевого фермента фибринолиза плазминогена и системы протеина С как важнейшего физиологического антикоагулянта. Таким образом, тромбин является связующим звеном между всеми компонентами гемостаза: и сосудисто-тромбоцитарного и коагуляционного и физиологических антикоагулянтов. Определение его активности при различных заболеваниях может использоваться в качестве интегрального показателя гемостаза.
В настоящее время еще одним из показателей коагуляции крови является время рекальцификации плазмы (время коагуляции), определяемое после добавления ионов кальция к цитратной плазме. В клинической лабораторной практике этот показатель сопоставляется с активированным временем рекальцификации цельной крови (АВР).
Кроме того, важным показателем гемостаза является толерантность плазмы к гепарину.
По величинам перечисленных показателей судят о состоянии гемостаза.
Определить ферментативную активность тромбина возможно двумя путями: как скорость расходования его субстрата или как скорость накопления продукта реакции.
Путь определения ферментативной активности тромбина по измерению количества его субстрата за определенный промежуток времени нашел отражение в способе, основанном на добавлении к цитратной бестромбоцитратной плазме или цельной крови флуорогенного субстрата (например, пептида, меченного 7-амино-4-метилкумарином) и рекомбинантного человеческого тканевого тромбопластина для запуска коагуляционного каскада по внешнему механизму с последующим измерением интенсивности флуоресценции образующегося при гидролизе флуорофора (Hemiker H.C., Giesen P., Al Dieri R et al. Calibrated automated trombin generation measurement in clotting plasma.// Pathophysiol. Haemost. Thromb. – 2003 - № 33 – р. 4-15).
Этот метод не пригоден для определения других показателей процесса коагуляции.
Измерение активности тромбина по накоплению продукта реакции (фибрина) затруднительно в связи с тем, что фибрин, по мере своего образования, формирует нерастворимый сгусток, в стабилизации которого принимает участие другой фермент трансглутаминаза (фактор XIII a). (Биохимия: Учебник / Под ред. Е. С. Северина. - 2 изд-е, испр. – М.: Гэотар-мед 2004. - 784 с.: ил.).
Существует способ определения активности тромбина, основанный на скорости образования фибриновых нитей оптико-механическим методом (Спиридонова В.А., Рог Е.В., Дугина Т.Н., Струкова С.М., Копылов А.М. // Биоорган. химия. 2003. T. 29, с.495-498). Сущность этого метода состоит в перемешивании магнитной мешалкой бестромбоцитарной плазмы в присутствии ионов кальция, что приводит к наматыванию на нее фибриновых нитей, которые тормозят вращение мешалки вплоть до полной остановки. Время остановки мешалки фиксируется как время коагуляции плазмы. Если время коагуляции плазмы составляет 1,5 – 3 мин, активность тромбина считают нормальной. Повышение или понижение этого показателя говорит об отклонениях в гемостазе. Стандартизация реагентов и условий реакции делает время коагуляции хорошо воспроизводимым параметром.
Однако с помощью этого метода невозможно разграничить реакции образования полимер-фибрина из фибрин-мономера и полимер-фибрина, стабилизированного с участием трансглутаминазы, а также оценить время активации протромбиназного комплекса, характеризующего толерантность плазмы к гепарину.
Известен способ определения активности тромбина [патент 2429488 RU, МПК G01N 33/86/ Способ определения активности тромбина / Головин Андрей Викторович (RU), Копылов Алексей Михайлович (RU), Завьялова Елена Геннадьевна (RU), Павлова Галина Валериевна (RU), Мудрик Николай Николаевич (RU), Бабий Владимир Евстахиевич (RU); заявитель и патентообладатель Общество с ограниченной ответственностью "АПТО-ФАРМ" (RU). - № 2010119575/15; заявл. 18.05.2010; опубл. 20.09.2011, Бюл. № 26], основанный на методе турбидиметрического наблюдения за образованием фибринового сгустка. Регистрацию светопропускания инкубационной среды в методе проводят с помощью ультрафиолетового диапазона излучения от 230 до 320 нм посредством УФ-спектрофотометра в качестве детектора фибрин-полимера. Для получения фибринового сгустка при температуре 27°С используется 0,1±0,005% человеческий фибриноген; буфер с pH 7,4±0,1, 1,4±0,05 М NaCl, 50±5 мМ KCl, 10±1 мМ MgCl2, 10±1 мМ CaCl2) и тромбин человеческий (0,2-50 мкМ).
Момент добавления раствора тромбина фиксируют секундомером и проводят измерения оптической плотности образца при рабочей длине волны 200-300 нм (в работе обычно использовалось излучение 230 нм). Измерения прекращают при достижении плато кривой оптической плотности. Этот период времени является временем коагуляции. В описываемом методе активность тромбина рассчитывали как тангенс угла наклона касательной в точке перегиба полученной кривой изменения оптической плотности. Авторы патента считают, что этот параметр можно интерпретировать как максимальную скорость накопления фибрин-полимера.
Однако этот способ используется в области медицинских исследований, фармацевтической промышленности и биотехнологии с целью определения удельной активности тромбина, полученного в процессе его биохимического синтеза. Не фиксируется стадийность процесса и параметры отдельных стадий.
Известен способ определения активности тромбина плазмы крови, представленный в работе (Stief T.W. Specific determination of plasmatic thrombin activity Clinical and Applied Thrombosis/Haemostasis, -2006, -12(3): 324-329). Для наблюдения за процессом коагуляции авторы использовали хромогенный субстрат в концентрации менее 0,4 мМоль/л, аргинин, при концентрации выше 0,8 Моль/л, и фактор II-истощенную плазму. Коагуляцию, инициировали либо тканевым фактором, либо активатором контактной фазы. Авторами были рассчитаны активности циркулирующего тромбина 0,35 мкМ/мин.
Основным недостатком данного метода является то, что он не пригоден для определения других показателей процесса коагуляции.
Флуоресцентная спектроскопия – один из наиболее чувствительных и информативных методов молекулярной сенсорики, которые позволяют раскрыть механизмы биологических реакций. Большое многообразие флуоресцентных сенсоров в совокупности с возможностями их тонкой спектральной настройки и регуляции механизмов оптического отклика позволяет добиться высокой селективности определения содержания молекул, ионов и параметров состояния системы в условиях нативных биологических систем. Поэтому использование различных флуоресцентных сенсоров является актуальной задачей современной медицинской диагностики (Escobedo J.O., Rusin O., Lim S., Strongin R.M. NIR dyes for bioimaging applications//Current opinion in chemical biology. 2010 - №14- р.64-70).
В настоящее время описано множество флуоресцентных сенсоров. Отдельный класс органических флуорофоров представляют соединения бордипирринового ряда, так называемые BODIPY–флуорофоры. Структурные модификации BODIPY позволяют реализовать разные механизмы спектрально-флуоресцентного отклика молекул на присутствие/концентрацию в системе различных соединений, в том числе биогенных молекул. Изменения флуоресцентных характеристик BODIPY в присутствии биомолекул были интерпретированы с использованием теории динамического/статического тушения Штерна-Фольмера и свидетельствуют о возможности использования данных соединений для анализа полярности, гидрофобности/гидрофильности отдельных сайтов белковых молекул для наблюдения за процессом коагуляции плазмы крови.
Наибольший интерес среди существующих BODIPY–флуорофоров представляют соединения с объемными ароматическими заместителями в мезо-положении дипирринового фрагмента. Обладающие достаточной селективностью к белкам плазмы крови при молекулярном комплексообразовании и других межмолекулярных взаимодействий они повышают свои флуоресцентные свойства за счет резонансного переноса энергии (Мarfin Yu S., Aleksakhina E.L., Merkushev D.A., Rumyantsev E.V., Tomilova I.K., Interaction of BODIPY Dyes with the Blood Plasma Proteins// Journal of Fluorescence – 2016 - №1 – p. 255-261).
Эти свойства BODIPY–флуорофоров позволяют использовать их в качестве сенсоров, отражающих изменение концентрации фибриногена, регистрировать ступенчатый процесс его преобразования в фибрин, определять активность тромбина.
Ни один из известных в литературе способов определения показателей коагуляции плазмы крови не предполагает использование флуоресцентных молекул соединений бордипирринового ряда в качестве сенсоров преобразований молекулярного состояния биомолекул плазмы крови.
Техническим результатом заявляемого изобретения является расширение технических возможностей за счет одновременного определения трех показателей коагуляции плазмы крови - активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину, и повышение чувствительности и точности процесса их определения.
Указанный результат достигается тем, что способ одновременного определения показателей коагуляции плазмы крови - активности тромбина (фактор коагуляции IIa), времени рекальцификации плазмы и толерантности плазмы к гепарину, характеризуется, согласно изобретению, тем, что используют флуоресцентный метод в видимом диапазоне излучения 420 – 600 нм с участием соединений бордипиринового ряда (BODIPY), флуоресцентные характеристики которых зависят от присутствия биомолекул (в частности, фибриногена), наблюдают за образованием фибринового сгустка, получают и анализируют кривую коагуляции при регистрации изменения интенсивности флуоресценции на спектрофлуориметре за промежуток времени от стадии формирования полимерного фибрина до стадии стабилизации кровяного сгустка.
Доказательство достижения технического результата: расширение технических возможностей происходит за счет одновременного определения трех показателей коагуляции плазмы крови - активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину по кривой коагуляции, а повышение чувствительности и точности процесса определения показателей коагуляции плазмы в настоящем способе обусловлена высокой чувствительностью бордипириновых флуорофоров к изменению полярности, гидрофобности/гидрофильности отдельных сайтов фибриногена (субстрата тромбина) и продукта его полимеризации – фибрина. Именно высокая чувствительность BODYPI позволяет регистрировать и наблюдать многоступенчатый процесс коагуляции плазмы, разграничить действие двух различных ферментов, рассчитать активность тромбина, используя для этого кривую коагуляции.
Изобретение поясняется чертежом, на котором приводится кривая коагуляции бестромбоцитарной плазмы»: 1 – в отсутствии гепарина; 2 – в присутствии гепарина.
Пример осуществления способа.
Для исследования использовалась свежая цитратная бестромбоцитарная плазма крови, взятая из локтевой вены. Концентрацию фибриногена в образцах определяли модифицированным методом Клаусса. Плазма, разведенная дистиллированной водой (к 0,4 мл плазмы прибавляли 2,45 мл воды) и 0,15 мл раствора BODIPY–флуорофора в ДМСО (с = 1⋅10-5 моль/л) смешивались в термостатируемой (37°С) спектрофотометрической кювете.
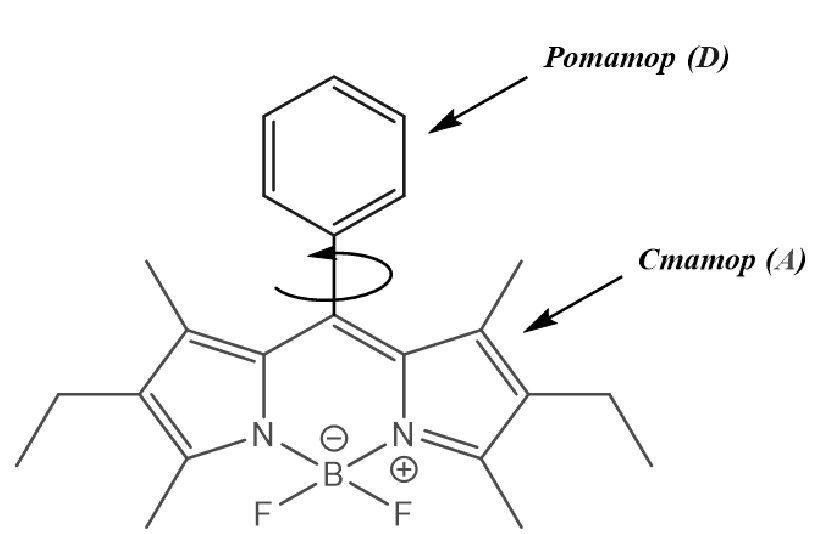
Запуск коагуляции осуществляли добавлением в кювету 0,04 мл 1% хлорида кальция. С момента добавления через равные промежутки времени автоматически с помощью спектрофлуориметра производили измерение интенсивности флуоресценции образца в интервале длин волн 420–600 нм, при этом были использованы такие соединения бордипирринового ряда, как: 4,4-дифторо-8-фенил-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3a,4a-диаза-s-индацен; 4,4-дифторо-8-(пара-диметиламинофенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3a,4a-диаза-s-индацен; 4,4-дифторо-8-(ди-ортометилфенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3a,4a-диаза-s-индацен, имеющие общую структурную формулу:
Таким образом, регистрировали зависимость интенсивности флуоресценции на максимуме испускания BODIPY–флуорофора от времени – кривую коагуляции образца плазмы. Исследование прекращали при достижении устойчивого плато на кривой изменения флуоресценции. Далее проводили анализ кривой коагуляции (чертеж).
На стандартной кривой коагуляции (чертеж - кривые 1 и 2) можно наблюдать три участка: верхнее плато, ниспадающий участок и нижнее плато.
Длина верхнего плато (tlag) соответствует периоду времени активации протромбиназного комплекса и очень чувствительна к наличию или отсутствию антикоагулянтов в плазме. Присутствие гепарина в крови человека (Яковлев А.Н. Медицинский совет, 2010, №5-6, 64 – 67), из которой получена плазма, значительно удлиняет этот период (кривая 2 на чертеже). Промежуток времени tlag является лимитирующим показателем, определяющим толерантность плазмы к гепарину, т.к. является характеристикой, отражающей время начала формирования сгустка фибрина после добавления в исследуемый материал гепарина (табл.1). Ранее доказано, что толерантность плазмы к гепарину в норме составляет 7-15 минут. Если же этот показатель составляет менее 7 мин, то диагностируется заболевание сердечно-сосудистой системы (Кишкун А.А. Руководство по лабораторным методам диагностики. Учебно-практическое издание. ГЭОТАР-Медиа, 2009 - 800 с. Общая врачебная практика: диагностическое значение лабораторных исследований: учебн.пособ./под ред. Вялова С.С., Чорбинской С.А., 4-е изд. , М.: МЕДпресс-информ, 2010).
Ниспадающий участок кривой коагуляции соответствует ключевой реакции плазменного гемостаза – гидролитическому расщеплению фибриногена при каталитическом действии имеющегося в плазме тромбина до фибрин-мономеров, которые самопроизвольно полимеризуются в фибрин — основу тромба. Касательная, проведенная к ниспадающему участку кривой коагуляции, образует угол наклона φ к оси ординат: tg φ пропорционален скорости образования полимерного фибрина из фибриногена, т.е. активности тромбина. Активность тромбина прямо пропорциональна произведению tg φ и концентрации фибриногена в плазме (мкМоль/л) с учетом разведения в спектрофотометрической кювете (табл.2). Как показывают данные этой таблицы, усредненная активность тромбина крови у группы пожилых людей (45-65 лет), определенная по предлагаемому методу, соответствует литературным данным (Stief T.W. Specific determination of plasmatic thrombin activity Clinical and Applied Thrombosis/Haemostasis, -2006. -12(3): 324-329).
При выходе на нижнее плато кривой коагуляции над процессом латеральной полимеризации фибрин-полимеров в фибриновом сгустке начинают преобладать процессы их стабилизации под действием другого фермента – трансглютаминазы. Это наглядно видно на участке ав кривой коагуляции 1: тангенс угла наклона касательной к этому участку кривой коагуляции изменяется. Время выхода на нижнее плато, полученное экстраполяцией касательной, тангенс угла наклона которой характеризует активность тромбина, следует считать временем окончания коагуляции (в клинической практике - время рекальцификации плазмы, референсные значения 100-180 мин) (табл.3).
Время задержки (tlag) формирования фибринового сгустка (время активации протромбиназного комплекса) показаны в таблице 1.
Таблица 1.
| № примеров | Время активации протромбиназного комплекса, мин | |
| Цитратная плазма без гепарина (добровольцы в возрасте 45-65 лет без установленного диагноза сердечно-сосудистого заболевания) |
Цитратная плазма с гепарином (пациенты в возрасте 45-65 лет с диагнозом острый коронарный синдром) |
|
| 1 | 1.67 | 4,33 |
| 2 | 1,33 | 4,33 |
| 3 | 2 | 4,67 |
| 4 | 1,67 | 4,67 |
| 5 | 1,67 | 5,00 |
| 6 | 1,33 | 4,67 |
| 7 | 2 | 4,67 |
| 8 | 1,67 | 5,67 |
| 9 | 1,67 | 4,33 |
| 10 | 1,33 | 5,00 |
| 11 | 2 | 4,67 |
| 12 | 2 | 5,00 |
| 13 | 1,67 | 4,67 |
| 14 | 1,67 | 4,67 |
| 15 | 1,33 | 5,00 |
| 16 | 1,67 | 5,67 |
| 17 | 2 | 5,00 |
| 18 | 2 | 4,33 |
| 19 | 1,67 | 5,00 |
| 20 | 1,67 | 5,33 |
| 1,70±0,30 | 4,60±0,37 | |
Данные таблицы 1 иллюстрируют, что анализ кривой коагуляции, полученной по предлагаемому способу, позволяет оценить время активации (tlag) протромбиназного комплекса, являющееся лимитирующим фактором процесса коагуляции и обуславливающим толерантность плазмы к гепарину, тем самым оценить вклад tlag в величину показателя толерантности и во временя рекальцификации плазмы, повышая чувствительность и точность процесса определения показателей коагуляции плазмы крови.
Активность тромбина крови у группы добровольцев в возрасте 45-65 лет без установленного диагноза сердечно-сосудистого заболевания показана в таблице 2.
Таблица 2
| № примеров | tg φ | Atr, mkM/ мин |
| 1 | 0,26 | 0,33 |
| 2 | 0,18 | 0,23 |
| 3 | 0,38 | 0,48 |
| 4 | 0,23 | 0,29 |
| 5 | 0,20 | 0,25 |
| 6 | 0,22 | 0,28 |
| 7 | 0,24 | 0,30 |
| 8 | 0,27 | 0,34 |
| 9 | 0,26 | 0,33 |
| 10 | 0,49 | 0,61 |
| 11 | 0,41 | 0,51 |
| 12 | 0,33 | 0,42 |
| 13 | 0,23 | 0,29 |
| 14 | 0,29 | 0,37 |
| 15 | 0,21 | 0,26 |
| 16 | 0,17 | 0,22 |
| 17 | 0,35 | 0,45 |
| 18 | 0,29 | 0,37 |
| 19 | 0,18 | 0,23 |
| 20 | 0,41 | 0,51 |
| 0,35±0,11 |
Данные таблицы 2 показывают, что усредненная активность тромбина крови у группы пожилых людей (45-65 лет) соответствует литературным данным (Stief T.W. Specific determination of plasmatic thrombin activity Clinical and Applied Thrombosis/Haemostasis, -2006. -12(3): 324-329) и получена при одновременном определении других заявленных показателей, которые также соответствуют референсным значениям.
Время рекальцификации плазмы у группы добровольцев в возрасте 45-65 лет без установленного диагноза сердечно-сосудистого заболевания показано в таблице 3.
Таблица 3.
| № примеров | Время рекальцификации плазмы, мин |
| 1 | 3,33 |
| 2 | 4,00 |
| 3 | 2,67 |
| 4 | 2,67 |
| 5 | 3,33 |
| 6 | 2,33 |
| 7 | 3,00 |
| 8 | 2,67 |
| 9 | 2,33 |
| 10 | 2,33 |
| 11 | 1,67 |
| 12 | 3,00 |
| 13 | 2,67 |
| 14 | 2,33 |
| 15 | 3,00 |
| 16 | 2,67 |
| 17 | 2,67 |
| 18 | 2,33 |
| 19 | 2,33 |
| 20 | 1,67 |
| 2,65 ±0,98 |
Данные таблицы 3, отражающие время рекальцификации плазмы, получены путем экстраполяции касательной к ниспадающему участку кривой коагуляции на ось абсцисс (время), отсекая стадию стабилизации фибринового сгустка. Такой подход позволяет повысить точность и чувствительность анализа, т.к. учитывает действие только тромбина и не учитывает стабилизирующее действие другого фермента - трансглютаминазы (фактор коагуляции XIII).
Основные контролируемые показатели коагуляции плазмы крови, полученные на разных соединениях бордипирринового ряда, представлены в таблице №4.
Таблица 4
| Название BODIPY | Время рекальцификации плазмы, мин | Актив-ность тромбина Atr, mkM/ мин |
Время активации протромбиназного комплекса, мин | Длина волны макси-мума флуорес-ценции образца BODIPY, нм | |
| Цитратная плазма без гепарина (добровольцы в возрасте 45-65 лет без установленного диагноза сердечно-сосудистого заболевания) |
Цитратная плазма с гепарином (пациенты в возрасте 45-65 лет с диагнозом острый коронарный синдром) |
||||
| 4,4-дифтор-8-фенил-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3а,4а-диаза-s-индацен | 2,65 ±0,98 | 0,35±0,11 | 1,70±0,30 | 4,60±0,37 | 580 |
| 4,4-дифторо-8-(пара-диметиламинофенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3a,4a-диаза-s-индацен | 2,65 ±0,97 | 0,35±0,14 | 1,70±0,31 | 4,60±0,36 | 537 |
| 4,4-дифторо-8-(ди-ортометилфенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3a,4a-диаза-s-индацен | 2,65 ±0,97 | 0,35±0,10 | 1,70±0,29 | 4,60±0,37 | 537 |
Таким образом, данный способ позволяет, используя сенсорные возможности BODIPY–флуорофоров, регистрировать, выделять и одновременно численно характеризовать стадии процесса коагуляции плазмы, т.е. повысить точность и чувствительность определения показателей коагуляции, таких, как активность тромбина, время рекальцификации плазмы и толерантность плазмы к гепарину.
Claims (4)
- Способ определения показателей коагуляции плазмы крови – активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину, характеризующийся тем, что используют флуоресцентный метод в видимом диапазоне излучения 420-600 нм в присутствии соединений бордипиринового ряда (BODIPY), таких, как 4,4-дифтор-8-фенил-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3а,4а-диаза-s-индацен;4,4-дифторо-8-(пара-диметиламинофенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3а,4а-диаза-8-индацен; 4,4-дифторо-8-(ди-ортометилфенил)-1,3,5,7-тетраметил-2,6-диэтил-4-бор-3а,4а-диаза-s-индацен, флуоресценция которых зависит от присутствия биомолекул фибриногена, регистрируют зависимость интенсивности флуоресценции на максимуме испускания BODIPY, получают кривую коагуляции образца плазмы, при этом исследование прекращают при достижении устойчивого плато на кривой изменения флуоресценции, далее анализируют кривую коагуляции, при этом на кривой коагуляции наблюдают и анализируют три участка: верхнее плато, ниспадающий участок и нижнее плато;
- при этом на основании длины верхнего плато (tlag) определяют толерантность плазмы к гепарину;
- затем проводят касательную к ниспадающему участку кривой коагуляции, которая образует угол наклона φ к оси ординат: tg φ, которой пропорционален активности тромбина;
- время рекальцификации плазмы, получают путем экстраполяции касательной к ниспадающему участку кривой коагуляции на ось абсцисс (время), отсекая стадию стабилизации фибринового сгустка.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020132717A RU2786591C2 (ru) | 2020-10-05 | Способ определения показателей коагуляции плазмы крови - активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020132717A RU2786591C2 (ru) | 2020-10-05 | Способ определения показателей коагуляции плазмы крови - активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2020132717A RU2020132717A (ru) | 2022-04-06 |
| RU2020132717A3 RU2020132717A3 (ru) | 2022-04-06 |
| RU2786591C2 true RU2786591C2 (ru) | 2022-12-22 |
Family
ID=
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2429488C1 (ru) * | 2010-05-18 | 2011-09-20 | Общество С Ограниченной Ответственностью "Апто-Фарм" | Способ определения активности тромбина |
| RU2669796C1 (ru) * | 2017-10-30 | 2018-10-16 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр гематологии" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ гематологии" Минздрава России) | Способ определения функционального фибриногена |
| RU2699798C1 (ru) * | 2019-05-22 | 2019-09-11 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр гематологии" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ гематологии" Минздрава России) | Способ выявления дефицитов факторов свертывания крови методом тромбоэластометрии |
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2429488C1 (ru) * | 2010-05-18 | 2011-09-20 | Общество С Ограниченной Ответственностью "Апто-Фарм" | Способ определения активности тромбина |
| RU2669796C1 (ru) * | 2017-10-30 | 2018-10-16 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр гематологии" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ гематологии" Минздрава России) | Способ определения функционального фибриногена |
| RU2699798C1 (ru) * | 2019-05-22 | 2019-09-11 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр гематологии" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ гематологии" Минздрава России) | Способ выявления дефицитов факторов свертывания крови методом тромбоэластометрии |
Non-Patent Citations (1)
| Title |
|---|
| Атауллаханов Ф.И., Гурия Г.Т., Сафрошкина А.Ю. Пространственные аспекты динамики свертывания крови. II. Феноменологическая модель // Биофизика. 1994. Т. 39, JSfe l. с. 97-106. Малая медицинская энциклопедия. - М.: Медицинская энциклопедия. 1991-1996 гг.. Е.Л. Алексахина и др. ИЗУЧЕНИЕ ПРОЦЕССА СВЁРТЫВАНИЯ КРОВИ В ПРИСУТСТВИИ БОРДИПИРРИНОВЫХ ФЛЮОРЕСЦЕНТНЫХ КРАСИТЕЛЕЙ. Казанский медицинский журнал, 2015 г., том 96, N5, с. 792-798. Н.А. Подоплелова и др. Свертывание крови в XXI веке: новые знания, методы и перспективы для терапии. Вопросы гематологии/онкологии и иммунопатологии в педиатрии. 2020, Том 19, N 1, с. 139-157. Renáta Hudák et al. Laboratory characterization of leukemic cell procoagulants. Clin Chem Lab Med, 2017 Jul 26; 55(8): 1215-1223. PMID: 28593927. Hemker Н.С., Giesen P., Al Dieri R., Regnault V., de Smedt E., Wagenvoord R., Lecompte Т., Beguin S. Calibrated automated thrombin generation measurement in clotting plasma //Pathophysiol. Haemost. Thromb. 2003. V.33. P. 4-15. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2032561C (en) | Method of determining levels of extrinsic and intrinsic clotting factors and protein c | |
| JP6461125B2 (ja) | 抗第Xa因子試験のユニバーサル較正のための手段および方法 | |
| JP6300793B2 (ja) | 血漿及び全血中のトロンビン産生と血餅強度との同時測定 | |
| US4234682A (en) | Method and reagent for determining biologically active heparin in plasma | |
| US20090087870A1 (en) | Hematological assay and kit | |
| Mijovski | Advances in monitoring anticoagulant therapy | |
| WO2011057143A1 (en) | Compositions, methods and uses for simultaneous assay of thrombin and plasmin generation | |
| CN1368886A (zh) | 用于测定全血中的凝固因子活性的方法 | |
| JP3248621B2 (ja) | 血栓症リスクのテスト | |
| KR20090085666A (ko) | 세포를 포함한 복합 생체물질에서 단백용해 활성도를 측정하는 방법 | |
| Kitchen et al. | Laboratory tests of hemostasis | |
| Hoffmann et al. | Automated nephelometry of fibrinogen: analytical performance and observations during thrombolytic therapy. | |
| Chantarangkul et al. | Evaluation of a fully automated centrifugal analyzer for performance of hemostasis tests. | |
| RU2786591C2 (ru) | Способ определения показателей коагуляции плазмы крови - активности тромбина, времени рекальцификации плазмы и толерантности плазмы к гепарину | |
| Luo et al. | Drop-of-blood acoustic tweezing technique for integrative turbidimetric and elastometric measurement of blood coagulation | |
| de Freitas Saito et al. | Anticoagulant activity of nucleic acid nanoparticles (NANPs) assessed by thrombin generation dynamics on a fully automated system | |
| JP3713901B2 (ja) | 破骨細胞由来酸性ホスファターゼの測定方法 | |
| EP3649253A1 (en) | Improved detection of anticoagulants in body fluids | |
| RU2660706C1 (ru) | Скрининг-тест определения контактного пути коагуляции (СТОКПК) | |
| CN110133304B (zh) | 组合物、含有该组合物的试剂及其应用 | |
| RU2835822C9 (ru) | Способ определения антикоагулянтного потенциала плазмы крови для диагностики предтромботических состояний | |
| RU2772195C1 (ru) | Способ определения функциональной активности антитромбина iii в плазме крови | |
| RU2429488C1 (ru) | Способ определения активности тромбина | |
| US20220252624A1 (en) | Method for determining the risk of a thromboembolic event | |
| CN117723533A (zh) | 激活试剂、显色试剂、纤溶酶原活性检测试剂和/或试剂盒及其应用 |