RU2777082C1 - Способ получения оксида магния из природных рассолов и попутно добываемых вод нефтяных месторождений - Google Patents
Способ получения оксида магния из природных рассолов и попутно добываемых вод нефтяных месторождений Download PDFInfo
- Publication number
- RU2777082C1 RU2777082C1 RU2021134950A RU2021134950A RU2777082C1 RU 2777082 C1 RU2777082 C1 RU 2777082C1 RU 2021134950 A RU2021134950 A RU 2021134950A RU 2021134950 A RU2021134950 A RU 2021134950A RU 2777082 C1 RU2777082 C1 RU 2777082C1
- Authority
- RU
- Russia
- Prior art keywords
- magnesium
- brine
- waters
- magnesium hydroxide
- value
- Prior art date
Links
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 title claims abstract description 69
- 239000000395 magnesium oxide Substances 0.000 title claims abstract description 48
- 239000003643 water by type Substances 0.000 title claims abstract description 37
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 title claims abstract description 25
- 238000000034 method Methods 0.000 title abstract description 29
- 239000012267 brine Substances 0.000 claims abstract description 62
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 claims abstract description 61
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 claims abstract description 60
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 claims abstract description 46
- 239000000347 magnesium hydroxide Substances 0.000 claims abstract description 44
- 229910001862 magnesium hydroxide Inorganic materials 0.000 claims abstract description 44
- 239000002244 precipitate Substances 0.000 claims abstract description 31
- 239000000243 solution Substances 0.000 claims abstract description 31
- 239000001569 carbon dioxide Substances 0.000 claims abstract description 30
- 229910002092 carbon dioxide Inorganic materials 0.000 claims abstract description 30
- 238000003763 carbonization Methods 0.000 claims abstract description 26
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 claims abstract description 20
- 238000001354 calcination Methods 0.000 claims abstract description 18
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims abstract description 17
- QWDJLDTYWNBUKE-UHFFFAOYSA-L magnesium bicarbonate Chemical compound [Mg+2].OC([O-])=O.OC([O-])=O QWDJLDTYWNBUKE-UHFFFAOYSA-L 0.000 claims abstract description 16
- 229910000022 magnesium bicarbonate Inorganic materials 0.000 claims abstract description 16
- 239000002370 magnesium bicarbonate Substances 0.000 claims abstract description 16
- 235000014824 magnesium bicarbonate Nutrition 0.000 claims abstract description 16
- 239000007789 gas Substances 0.000 claims abstract description 15
- 238000004519 manufacturing process Methods 0.000 claims abstract description 15
- 239000003546 flue gas Substances 0.000 claims abstract description 14
- 238000000926 separation method Methods 0.000 claims abstract description 12
- 239000000446 fuel Substances 0.000 claims abstract description 11
- 238000002485 combustion reaction Methods 0.000 claims abstract description 10
- 238000001914 filtration Methods 0.000 claims abstract description 10
- 229910052742 iron Inorganic materials 0.000 claims abstract description 10
- 238000002347 injection Methods 0.000 claims abstract description 9
- 239000007924 injection Substances 0.000 claims abstract description 9
- -1 iron ions Chemical class 0.000 claims abstract description 8
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 claims abstract description 7
- 239000001095 magnesium carbonate Substances 0.000 claims abstract description 7
- 229910000021 magnesium carbonate Inorganic materials 0.000 claims abstract description 7
- 239000000725 suspension Substances 0.000 claims abstract description 7
- 239000007787 solid Substances 0.000 claims abstract description 6
- 235000012245 magnesium oxide Nutrition 0.000 claims description 43
- 230000015572 biosynthetic process Effects 0.000 claims description 25
- 239000011777 magnesium Substances 0.000 claims description 20
- 238000001556 precipitation Methods 0.000 claims description 18
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 claims description 17
- 229910052749 magnesium Inorganic materials 0.000 claims description 17
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 claims description 10
- 239000000920 calcium hydroxide Substances 0.000 claims description 10
- 235000011116 calcium hydroxide Nutrition 0.000 claims description 10
- 229910000019 calcium carbonate Inorganic materials 0.000 claims description 9
- 238000009835 boiling Methods 0.000 claims description 5
- 238000010438 heat treatment Methods 0.000 claims description 5
- 238000005406 washing Methods 0.000 claims description 4
- 238000000746 purification Methods 0.000 claims description 3
- 235000008733 Citrus aurantifolia Nutrition 0.000 abstract description 22
- 235000011941 Tilia x europaea Nutrition 0.000 abstract description 22
- 239000004571 lime Substances 0.000 abstract description 22
- 239000008267 milk Substances 0.000 abstract description 6
- 210000004080 milk Anatomy 0.000 abstract description 6
- 235000013336 milk Nutrition 0.000 abstract description 6
- 239000000126 substance Substances 0.000 abstract description 4
- 229940088417 precipitated calcium carbonate Drugs 0.000 abstract description 2
- ODINCKMPIJJUCX-UHFFFAOYSA-N Calcium oxide Chemical compound [Ca]=O ODINCKMPIJJUCX-UHFFFAOYSA-N 0.000 description 29
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 18
- 239000000292 calcium oxide Substances 0.000 description 15
- 235000012255 calcium oxide Nutrition 0.000 description 15
- 239000011575 calcium Substances 0.000 description 10
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 8
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 8
- 239000001110 calcium chloride Substances 0.000 description 8
- 229910001628 calcium chloride Inorganic materials 0.000 description 8
- 235000011148 calcium chloride Nutrition 0.000 description 8
- 239000013078 crystal Substances 0.000 description 8
- 239000000203 mixture Substances 0.000 description 8
- 239000012535 impurity Substances 0.000 description 7
- 239000002994 raw material Substances 0.000 description 7
- 230000018109 developmental process Effects 0.000 description 6
- 238000004062 sedimentation Methods 0.000 description 6
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 5
- 238000010276 construction Methods 0.000 description 5
- 229910001629 magnesium chloride Inorganic materials 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 239000013049 sediment Substances 0.000 description 5
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 4
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 4
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 4
- 229910052794 bromium Inorganic materials 0.000 description 4
- 229910052791 calcium Inorganic materials 0.000 description 4
- 229910052500 inorganic mineral Inorganic materials 0.000 description 4
- 239000011707 mineral Substances 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 3
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 3
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 3
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 3
- 239000000460 chlorine Substances 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 239000011630 iodine Substances 0.000 description 3
- 229910052744 lithium Inorganic materials 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 239000012452 mother liquor Substances 0.000 description 3
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 2
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 238000003795 desorption Methods 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 239000008398 formation water Substances 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 2
- 238000009776 industrial production Methods 0.000 description 2
- 235000014413 iron hydroxide Nutrition 0.000 description 2
- NCNCGGDMXMBVIA-UHFFFAOYSA-L iron(ii) hydroxide Chemical compound [OH-].[OH-].[Fe+2] NCNCGGDMXMBVIA-UHFFFAOYSA-L 0.000 description 2
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 description 2
- 229910052808 lithium carbonate Inorganic materials 0.000 description 2
- 150000002681 magnesium compounds Chemical class 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 235000010755 mineral Nutrition 0.000 description 2
- 238000004537 pulping Methods 0.000 description 2
- 239000011819 refractory material Substances 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000002689 soil Substances 0.000 description 2
- 230000008719 thickening Effects 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- CWYNVVGOOAEACU-UHFFFAOYSA-N Fe2+ Chemical compound [Fe+2] CWYNVVGOOAEACU-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 235000019738 Limestone Nutrition 0.000 description 1
- 238000005273 aeration Methods 0.000 description 1
- 230000033558 biomineral tissue development Effects 0.000 description 1
- BRPQOXSCLDDYGP-UHFFFAOYSA-N calcium oxide Chemical compound [O-2].[Ca+2] BRPQOXSCLDDYGP-UHFFFAOYSA-N 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 238000010000 carbonizing Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 239000013065 commercial product Substances 0.000 description 1
- 238000005056 compaction Methods 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000010459 dolomite Substances 0.000 description 1
- 229910000514 dolomite Inorganic materials 0.000 description 1
- 238000005553 drilling Methods 0.000 description 1
- 238000005868 electrolysis reaction Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 239000003673 groundwater Substances 0.000 description 1
- XLYOFNOQVPJJNP-ZSJDYOACSA-N heavy water Substances [2H]O[2H] XLYOFNOQVPJJNP-ZSJDYOACSA-N 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000006028 limestone Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- DHRRIBDTHFBPNG-UHFFFAOYSA-L magnesium dichloride hexahydrate Chemical compound O.O.O.O.O.O.[Mg+2].[Cl-].[Cl-] DHRRIBDTHFBPNG-UHFFFAOYSA-L 0.000 description 1
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000003345 natural gas Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000013535 sea water Substances 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
Images
Abstract
Изобретение относится получению оксида магния из природных рассолов и попутно добываемых пластовых вод нефтяных месторождений с целью их последующей закачки в пласты нефтяных месторождений для поддержания пластового давления. Рассол и попутно добываемые пластовые воды очищают от нефти и ионов железа, после чего обрабатывают известковым молоком с образованием гидроксида магния. Проводят карбонизацию суспензии гидроксида магния с получением раствора бикарбоната магния и твердого осадка. Отделенный раствор бикарбоната магния нагревают до кипения с образованием магнезии углекислой, которую отделяют и прокаливают с получением оксида магния. Причем предварительно определяют значение рН упомянутых исходных рассолов и вод, а также их значение рН после фильтрации гидроксида магния. После отделения гидроксида магния упомянутые рассолы и воды повторно карбонизируют углекислым газом, содержащимся в газах после прокаливания магнезии углекислой, или дымовыми газами, которые образуются при сжигании топлива. Карбонизацию продолжают до тех пор, пока значение рН рассола и попутно добываемых пластовых вод не достигнет значения рН исходного природного рассола. Полученный рассол фильтруют от выпавшего осадка карбоната кальция и направляют на закачку в пласты нефтяных месторождений для поддержания пластового давления. Способ позволяет получать оксид магния с чистотой не менее 98% с использованием извести любого качества на базе попутно добываемых вод нефтяных месторождений, а также природных рассолов при минимальных выбросах диоксида углерода в атмосферу. 2 табл., 1 пр., 2 ил.
Description
Изобретение относится к химической промышленности, а именно к способам получения оксида магния из природных рассолов и попутно добываемых пластовых вод нефтяных месторождений с целью их последующей закачки в пласты нефтяных месторождений для поддержания пластового давления.
Выделение соединений магния из гидроминерального сырья хорошо освоено и используется в промышленном масштабе. В настоящее время больше половины всего мирового производства магниевой продукции производится из гидроминерального сырья, главным образом, из морской воды и подземных рассолов. В частности, крупнейшие промышленные предприятия по производству оксида магния и других его соединений расположены в Китае, США, Японии, Израиле и др.
Главными потребителями соединений магния являются производство огнеупоров, строительная и металлургическая промышленность.
Попутно добываемая с нефтью пластовая вода составляет основной объем вовлеченных в промышленный оборот природных рассолов. Ежегодный объем добываемых пластовых вод на нефтяных месторождениях только в России составляет 2,5 млрд. м3. По мере разработки нефтяных месторождений объем добываемых пластовых вод продолжает увеличиваться и на конечной стадии разработки достигает 95-98%.
Пластовые воды нефтяных месторождений представляют собой рассол с минерализацией от 100 до 300 кг/м3 и традиционно используются только для технологических нужд в системах поддержания пластового давления.
Учитывая, что пластовые воды нефтяных месторождений содержат в себе концентрации магния от 1,5 до 40 кг/м3, являются относительно неисчерпаемым источником гидроминерального сырья и не требуют дополнительных затрат на добычу, то они способны в ряде случаев заменить традиционные виды магнийсодержащего сырья.
Все известные промышленные способы получения оксида магния из гидроминерального сырья основаны на осаждении малорастворимого гидроксида с помощью щелочных реагентов и последующем обжиге полученного продукта до оксида магния. В качестве основного и наиболее дешевого реагента в промышленных способах используется гидроксид кальция [Позин М.Е., Технология минеральных солей. Л., "Химия", 1974, с. 236-310]. Трудность осаждения гидроксида магния и отделения его от маточного раствора заключается в том, что без соблюдения специальных условий осадок получается в коллоидно-дисперсной форме. Другая проблема, связанная с использованием гидроксида кальция, заключается в сложности получения чистого продукта, не содержащего примеси железа, марганца, цветных металлов, бора и других соединений [Сенявин М.М., Хамизов Р.Х., Океанская вода - источник минерального сырья. Природа, 1990, №7, с. 25-33].
Известен способ комплексной переработки попутных вод нефтяных месторождений (патент RU №2189362, МПК C02F 1/58, опубл. 20.09.2002), включающий предварительную очистку воды от механических примесей и нефти с последующим последовательным извлечением магния, лития, йода и брома, при этом литий и йод извлекают методом селективной сорбции, магний - осаждением, бром - воздушной десорбцией, с последующим использованием попутно добываемой воды в системе поддержания пластового давления нефтяных месторождений. Перед извлечением магния, лития, йода и брома экстрагируют бор.
Недостатком способа является необходимость использования извести высочайшего качества с максимально высоким содержанием активного СаО для получения чистого оксида магния, поскольку промышленно выпускаемые извести содержат в себе от 5 до 20% примесей (так называемый «недожог»), которые будут снижать качество товарного магниевого продукта. К недостаткам способа следует отнести и загрязнение атмосферы содержащими СО2 промышленными газами, образующими при прокаливании гидроксида магния и сжигании топлива.
Также известен способ комплексной переработки рассолов хлоридного кальциевого и хлоридного магниевого типов (патент RU №2436732, МПК C01F 5/10, 5/30, опубл. 20.12.2011), включающий получение оксида и хлорида магния, а также брома и карбоната лития, по способу из рассола сначала проводят совместное осаждение карбоната кальция и гидроксида магния с одновременным получением маточного раствора, содержащего хлорид натрия, который подвергают упариванию до выделения кристаллов хлорида натрия, кристаллы отделяют, растворяют в воде с получением концентрированного раствора хлорида натрия, который подвергают электролизу для получения газообразного хлора и католита-раствора гидроксида натрия; газообразный хлор используют для окисления бромид-ионов, содержащихся в упаренном растворе, с последующей десорбцией элементарного брома; католит после карбонизации углекислым газом и получения раствора карбоната и гидроксида натрия используют для осаждения карбоната кальция и гидроксида магния; осадок репульпируют в растворе хлорида кальция и подвергают карбонизации для получения карбоната кальция и раствора хлорида магния, осадок отделяют, из части раствора хлорида магния раствором карбоната и гидроксида натрия осаждают магнезию углекислую, которую затем прокаливают для получения оксида магния и углекислого газа; другую часть раствора хлорида магния упаривают для кристаллизации бишофита; из раствора после отделения кристаллов хлорида натрия осаждают карбонат лития раствором после карбонизации католита.
Недостатками способа являются высокие энергетические затраты, связанные с необходимостью упаривать значительные объемы жидкости (так для 1 м3 перерабатываемой воды требуется упарить более 4 м3 маточного раствора) и повышенной потребностью в природном газе. В конечном счете, вышеуказанные недостатки повышают себестоимость производимых химических соединений. Другим недостатком способа являются ограниченность его применения, в частности для попутно добываемых вод нефтяных месторождений, используемых далее после переработки для поддержания пластового давления, поскольку исходный рассол перерабатывается нацело.
Наиболее близким к заявленному изобретению является способ получения оксида магния из природных рассолов (патент RU №2211803, МПК C01F 5/06, опубл. 10.09.2003), включающий аэрирование и отделение выпавшего осадка гидроксида железа, осаждение гидроксида магния обработкой рассола известковым молоком, полученным после обжига доломита, известняка, сгущение пульпы в присутствии полиакриламида с образованием раствора хлорида кальция и осадка гидроксида магния, фильтрацию и промывку осадка гидроксида магния, карбонизацию пульпы с получением раствора бикарбоната магния и твердого осадка, отделение последнего, нагревание до кипения раствора бикарбоната магния с выпадением в осадок магнезии углекислой, ее прокаливание с получением оксида магния. По способу используют высокоминерализованный рассол с содержанием хлорида кальция 60-350 г/л, который охлаждают до +18÷-25°С, после отделения кристаллов CaCl2⋅6Н2О его разбавляют, аэрируют и отделяют выпавший осадок гидроксида железа, а образующийся при осаждении гидроксида магния раствор хлорида кальция направляют на растворение кристаллов CaCl2⋅6Н2О с получением тяжелых солевых растворов.
Недостатком способа является ограниченность его применения объемами потребления буровых растворов в регионе, вокруг которого разрабатывается рассол, а также невозможность применения для переработки попутно добываемых вод нефтяных месторождений, используемых далее для поддержания пластового давления, поскольку переработанный рассол, из которого извлечен магний, имеет высокое значение рН на уровне 10-11, закачка которого в скважину и смешение с пластовой водой приведет к интенсивному осадкобразованию и кольматации призабойной зоны скважины и соответственно быстрому выходу ее из строя.
Технической задачей изобретения является создание способа получения оксида магния из природных рассолов или попутно добываемых вод нефтяных месторождений, позволяющего получить качественный оксид магния с одновременным сохранением качества рассолов или попутно добываемых вод с целью их последующей закачки в пласты нефтяных месторождений для поддержания пластового давления, позволяющего снизить экологическую нагрузку в виде загрязнения атмосферы промышленными газами, содержащими углекислый газ, за счет использования газов после прокаливания магнезии углекислой и дымовых газов при сжигании топлива в технологическом процессе карбонизации загрязненного осадка гидроксида магния и самого рассола после отделения гидроксида магния, достигнув при этом высокой степени освоения диоксида углерода, а также расширение технологических возможностей способа за счет возможности применения извести любого качества.
Техническая задача решается способом получения оксида магния из природных рассолов и попутно добываемых пластовых вод нефтяных месторождений, включающим предварительную очистку рассола и попутно добываемых пластовых вод от нефти и ионов железа, осаждение магния обработкой рассола и попутно добываемых пластовых вод известковым молоком с образованием гидроксида магния, фильтрацию и промывку осадка гидроксида магния, карбонизацию суспензии гидроксида магния с получением раствора бикарбоната магния и твердого осадка, отделение последнего от раствора бикарбоната магния, нагревание до кипения раствора бикарбоната магния с выпадением в осадок магнезии углекислой, отделение магнезии углекислой и прокаливание с получением оксида магния.
Новым является то, что предварительно определяют значение рН исходных природного рассола и попутно добываемых пластовых вод, а также значение рН природного рассола и попутно добываемых пластовых вод после фильтрации гидроксида магния, после отделения гидроксида магния природный рассол и попутно добываемые пластовые воды повторно карбонизируют углекислым газом, содержащимся в газах после прокаливания магнезии углекислой, или дымовыми газами, которые образуются при сжигании топлива, при этом карбонизацию рассола и попутно добываемых пластовых вод продолжают до тех пор, пока значение рН рассола и попутно добываемых пластовых вод не достигнет значения рН исходного природного рассола, после чего полученный рассол фильтруют от выпавшего осадка карбоната кальция и направляют на закачку в пласты нефтяных месторождений для поддержания пластового давления.
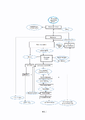
На фиг.1 представлена технологическая схема реализации способа.
На фиг.2 - кривые осаждения гидроксида магния в зависимости от содержания активного СаО в используемых образцах негашеной извести.
Сущность способа заключается в следующем.
В качестве сырья используют природные рассолы и попутно добываемые пластовые воды нефтяных месторождений, которые в своем большинстве по химическому составу относятся к хлоркальциевому типу (по классификации подземных вод В.А. Сулина) с общей минерализацией 100 до 300 кг/м3 и исходным значением рН в диапазоне от 5,5 до 7,0.
Предварительно определяют значение рН исходных природного рассола и попутно добываемых пластовых вод (далее - рассолы). Далее проводят предварительную очистку рассолов от нефти и ионов железа любым из известных способов, при этом попутно удаляются сульфат- и гидрокарбонат-ионы путем подачи в рассол щелочного продукта (например, известкового молока) до получения рН=8 и пропускания через рассол воздуха. В результате протекают процессы в соответствии с химическими реакциями:
Fe2++ Са(ОН)2 → Fe(ОН)2↓ + Са2+
4Fe(ОН)2 + 2Н2О + О2 → 4Fe(ОН)3
Са2+ + НСО3 - → СаСО3↓ + Н+
Са2+ + SO4 2- → CaSO4↓
Образовавшаяся суспензия (суммарный осадок) отфильтровывается на механических фильтрах, благодаря чему рассол очищается как от ионов железа, так и от сульфат- и гидрокарбонат-ионов, которые впоследствии бы загрязнили товарный продукт оксида магния.
Проводят осаждение магния обработкой рассола известковым молоком с образованием гидроксида магния. Известковое молоко для осаждения магния получают путем гашения извести водой в течение часа и доведения концентрации активного СаО в известковом молоке до 10%. Для приготовления известкового молока используют известь привозную или получаемую на месте, причем возможно использование извести любого качества: как высокого, так и более низкого с содержанием активного СаО не менее 74%, при этом содержащиеся примеси в приготовленном известковом молоке будут выступать в качестве затравочных кристаллов при осаждении магния, позволят улучшить седиментационные свойства осадка гидроксида магния, что, в конечном счете, приведет к уменьшению объема отстойного и фильтрационного оборудования.
Известковое молоко подают в очищенный от нефти и ионов железа рассол при постоянном его перемешивании. Образовавшуюся суспензию гидроксида магния отфильтровывают от рассола, промывают путем распульповки в воде с промежуточным отжимом на фильтре. Определяют значение рН отфильтрованного рассола.
Далее проводят карбонизацию суспензии гидроксида магния с получением раствора бикарбоната магния и твердого осадка.
Карбонизацию (первичную) проводят углекислым газом, содержащимся в дымовых газах печей подогрева нефти установок подготовки нефти.
В последующем при реализации предлагаемого способа для карбонизации возможно применение углекислого газа с чистотой до 98%, который образуется после прокаливания магнезии углекислой или дымовыми газами, которые образуются при сжигании топлива, содержащими в своем составе до 16% углекислого газа.
Твердый осадок после карбонизации, представленный в основном карбонатом кальция, отделяют от раствора бикарбоната магния и направляют на производство извести, в последующем его используют в строительной промышленности в качестве наполнителя или в сельском хозяйстве для раскисления кислых почв.
Раствор бикарбоната магния нагревают до кипения с выпадением в осадок магнезии углекислой, который отделяют и прокаливают с получением оксида магния. В процессе прокаливания выделяются газы, содержащие в своем составе углекислый газ.
При прокаливании осадка магнезии углекислой при 500-600°С получают жженую магнезию - оксид магния MgO с насыпной плотностью 0,55 г/см3, при прокаливании при 1650-1800°С - оксид магния (периклаз) для огнеупоров с насыпной плотностью 1,9 г/см3.
После отделения гидроксида магния рассол повторно карбонизируют углекислым газом (например, с чистотой до 98%), содержащимся в газах после прокаливания магнезии углекислой, или дымовыми газами, которые образуются при сжигании топлива (содержащими в своем составе до 16% углекислого газа). При этом карбонизацию рассола продолжают до тех пор, пока значение рН рассола не достигнет значения рН исходного природного рассола.
После чего полученный рассол фильтруют от выпавшего осадка карбоната кальция и направляют на закачку в пласты нефтяных месторождений для поддержания пластового давления.
Предлагаемый способ позволяет создать промышленное производство оксида магния на базе природных рассолов и попутно добываемых вод нефтяных месторождений, получить качественный оксид магния с содержанием основного вещества не менее 98%, позволяет расширить возможности осуществления способа путем применения извести любого качества. Так, возможно использовать сравнительно дешевую низкокачественную известь с содержанием активного СаО от 80% и выше. Также предлагаемый способ позволяет сохранить качество рассола или попутно добываемых вод для последующей закачки в пласт с целью поддержания пластового давления, снизить экологическую нагрузку в виде загрязнения атмосферы промышленными газами, содержащими СО2, так как предполагает их использование.
Пример практического применения.
В качестве сырья использовали попутно добываемую воду с исходным рН=5,8 и имеющую следующий ионный состав, г/дм3: натрий Na+ - 57,11; кальций Ca2+ - 17,62; магний Mg2+ - 3,72; железо общее - 0,115; хлорид-ион Cl- - 129,49; гидрокарбонат-ион HCO3- - 0,082; сульфат-ион SO4 2- - 0,057.
Рассол фильтровали от остаточной нефти. После чего в него подавали известковое молоко до получения рН=8 и пропускали через него воздух в течение 1 часа, в результате содержащееся в рассоле двухвалентное железо Fe2+ окислилось до трехвалентного Fe3+ и осаждалось в виде гидроксида. После отделения осадка концентрация железа общего в рассоле уменьшилась до 0,001 г/дм3; гидрокарбонат-иона HCO3- - до 0,002 г/дм3; сульфат-ион SO4 2- - до 0,003 г/дм3.
Далее для осаждения магния из рассола и построения кривых осаждения гидроксида магния были проверены три образца негашеной извести с содержанием активного оксида кальция 74, 82 и 96,2%. Состав используемых образцов негашеной извести представлен в таблице 1.
Таблица 1 - Состав используемых образцов негашеной извести
| Наименование показателя |
Образец №1 | Образец №2 | Образец №3 |
| Известь строительная кальциевая, 3 сорт по ГОСТ 9179-77 |
Известь строительная кальциевая, 2 сорт по ГОСТ 9179-77 |
Известь строительная кальциевая после дополнительного прокаливания в муфельной печи при температуре 900°С | |
| Содержание активного СаО, % |
74 | 82 | 96,2 |
| Содержание активного MgO, % |
4 | 3 | 2,1 |
Полученную суспензию гидроксида магния сгущали в радиальном отстойнике. Кривые осаждения гидроксида магния приведены на фиг. 2, из которой видно, что уплотнение суспензии гидроксида магния составило в течение первого часа от 20 до 35% от исходного объема рассола, от 17 до 27% - в течение второго часа, причем было отмечено, что, чем выше содержание примесей в извести, тем лучше достигаются условия для осаждения и сгущения гидроксида магния, что свидетельствует о том, что заявленный способ позволяет использовать в производственном процессе известь любого качества: как высокого, так и низкого с содержанием активного СаО не менее 74%, а содержащиеся примеси в приготовленном известковом молоке при осаждении магния будут выступать в качестве затравочных кристаллов и позволят улучшить седиментационные свойства осадка гидроксида магния.
Далее образовавшийся осадок гидроксида магния отфильтровывают от рассола гидроксида магния, промывают путем распульповки в воде в соотношении влага осадка: промывная вода = 1:7 с промежуточным отжимом на фильтре. Определяют значение рН рассола после фильтрования гидроксида магния - 10,8.
После чего осадок гидроксида магния распульповывали в воде в соотношении гидроксид магния / вода = 1/20 и подвергали карбонизации моделью дымовых газов с 12%-ным содержанием CO2 (углекислым газом, содержащимся в дымовых газах печей подогрева нефти установок подготовки нефти) или углекислым газом после процесса прокаливания.
Полученный раствор бикарбоната магния с концентрацией Mg2+ равной 20,7 г/л фильтровали от осадка, который содержал в своем составе 91,7% карбоната кальция.
Раствор бикарбоната магния нагревали до кипения, в результате чего образовывался осадок магнезии углекислой, который отделяли от раствора, высушивали и прокаливали при 600°С. Прокаленный осадок имел следующий состав (%): MgO - 98,2; СаО - 0,6, что отвечает требованию к качеству на магнезию жженую техническую (ГОСТ-844-79).
Раствор после отделения осадка магнезии углекислой, содержащий Ca2+ - 0,45 г/л и Mg2+ - 0,28 г/л, использовали для распульпации следующей порции влажного осадка гидроксида магния.
Рассол после отделения гидроксида магния подвергали карбонизации, которую проводили двумя различными вариантами: углекислым газом из баллона с содержанием углекислого газа 98 %, представляющим модель газа после прокаливания магнезии углекислой, а также смесью газов с содержанием углекислого газа 12 %, представляющей модель дымовых газов после сжигания топлива. Объемная скорость подачи газов карбонизации 20 л/ч на 1 литр рассола. Значения рН рассола в зависимости от продолжительности карбонизации представлены в таблице 2.
Таблица 2 - Значения рН рассола в зависимости от времени карбонизации
| Продолжительность карбонизации, мин. | ||||||||||||
| 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 | 55 | 60 | |
| Углекислый газ из баллона чистотой 99,8 % | 6,7 | 5,8 | 4,3 | 4,2 | 4,1 | 4,1 | 4,1 | 4,1 | 4,1 | 4,1 | 4,1 | 4,1 |
| Модель дымовых газов с содержанием углекислого газа 12 % | 9,7 | 9,0 | 8,1 | 7,6 | 7,2 | 6,8 | 6,5 | 6,0 | 5,8 | 5,6 | 5,3 | 5,0 |
Представленные в таблице 2 результаты показывают, что во время проведения карбонизации при подаче газа после прокаливания магнезии углекислой значение рН рассола снизилось до значения исходного рН=5,8 через 10 мин карбонизации, при подаче модели дымовых газов после сжигания топлива - в течение 45 минут карбонизации. Степень освоения углекислого газа при этом составила 97,6% при подаче газа после прокаливания магнезии углекислой, 95,4 % - при подаче дымовых газов после сжигания топлива.
Рассол после карбонизации фильтровали от выпавшего осадка карбоната кальция, который смешивался с осадком, образованным после фильтрования раствора бикарбоната магния. Смешанный осадок, представленный на 92% карбонатом кальция, как отмечалось ранее, может быть использован в производстве негашеной извести при его обжиге, в строительной промышленности в качестве наполнителя или в сельском хозяйстве для раскисления кислых почв.
После карбонизации рассол полностью отвечал показателям и нормам качества воды при заводнении нефтяных пластов с целью поддержания пластового давления, обозначенных в ОСТ 39-225-88 «Вода для заводнения нефтяных пластов», поскольку из него удалены частицы, приводящие к интенсивному осадкобразованию и кольматации призабойной зоны скважины, такие как нефть, сульфат- и гидрокарбонат-ионы, ионы железа, а рН рассола доведен до рН исходного рассола и находится в пределах от 4,5 до 8,5.
Таким образом, предлагаемый способ позволяет:
- создать промышленное производство оксида магния на базе попутно добываемых вод нефтяных месторождений (а также природных рассолов), составляющих основной объем вовлеченных в промышленный оборот природных рассолов;
- получить оксид магния с чистотой не менее 98%, что отвечает требованию к качеству на магнезию жженую, техническую согласно ГОСТ-844-79;
- использовать в производственном процессе известь любого качества: как высокого, так и низкого с содержанием активного СаО не менее 74%, а содержащиеся примеси в приготовленном известковом молоке при осаждении магния будут выступать в качестве затравочных кристаллов и позволят улучшить седиментационные свойства осадка гидроксида магния и уменьшить количество отстойного и фильтрационного оборудования;
- сохранить качество природного рассола или попутно добываемой воды в соответствии с показателями и нормами качества воды согласно ОСТ 39-225-88 «Вода для заводнения нефтяных пластов», что позволяет использовать их в системе поддержания пластового давления при разработке нефтяных месторождений;
- свести к минимуму выбросы диоксида углерода СО2 в атмосферу за счет использования газов после прокаливания магнезии углекислой и дымовых газов при сжигании топлива в технологическом процессе карбонизации загрязненного осадка гидроксида магния и самого рассола после отделения гидроксида магния, достигнув при этом степени освоения диоксида углерода не менее 95%, что выше, чем у наиболее близкого к заявленному изобретению способу.
Claims (1)
- Способ получения оксида магния из природных рассолов и попутно добываемых пластовых вод нефтяных месторождений, включающий предварительную очистку рассола и попутно добываемых пластовых вод от нефти и ионов железа, осаждение магния обработкой рассола и попутно добываемых пластовых вод известковым молоком с образованием гидроксида магния, фильтрацию и промывку осадка гидроксида магния, карбонизацию суспензии гидроксида магния с получением раствора бикарбоната магния и твердого осадка, отделение последнего от раствора бикарбоната магния, нагревание до кипения раствора бикарбоната магния с выпадением в осадок магнезии углекислой, отделение магнезии углекислой и прокаливание с получением оксида магния, отличающийся тем, что предварительно определяют значение рН исходных природного рассола и попутно добываемых пластовых вод, а также значение рН природного рассола и попутно добываемых пластовых вод после фильтрации гидроксида магния, после отделения гидроксида магния природный рассол и попутно добываемые пластовые воды карбонизируют углекислым газом, содержащимся в газах после прокаливания магнезии углекислой, или дымовыми газами, которые образуются при сжигании топлива, при этом карбонизацию рассола и попутно добываемых пластовых вод продолжают до тех пор, пока значение рН рассола и попутно добываемых пластовых вод не достигнет значения рН исходного природного рассола, после чего полученный рассол фильтруют от выпавшего осадка карбоната кальция и направляют на закачку в пласты нефтяных месторождений для поддержания пластового давления.
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2777082C1 true RU2777082C1 (ru) | 2022-08-01 |
Family
ID=
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115814752A (zh) * | 2023-01-31 | 2023-03-21 | 成都理工大学 | 一种碳酸钙和纳米氧化镁复合材料及其制备与应用方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4634533A (en) * | 1985-04-26 | 1987-01-06 | Somerville Robert L | Method of converting brines to useful products |
| RU2211803C2 (ru) * | 2001-06-26 | 2003-09-10 | Закрытое акционерное общество "Экостар-Наутех" | Способ получения оксида магния из природных рассолов |
| RU2281248C1 (ru) * | 2005-03-10 | 2006-08-10 | Ордена Ленина и ордена Октябрьской Революции Институт геохимии и аналитической химии им. В.И. Вернадского Российской академии наук (ГЕОХИ РАН) | Способ получения оксида магния из высокоминерализованных рассолов |
| WO2007088407A1 (en) * | 2006-01-31 | 2007-08-09 | Council Of Scientific And Industrial Research | An improved process for preparation of magnesium oxide |
| RU2543214C2 (ru) * | 2013-04-11 | 2015-02-27 | Закрытое акционерное общество (ЗАО) "Экостар-Наутех" | Способ комплексной переработки природных рассолов хлоридного кальциево-магниевого типа |
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4634533A (en) * | 1985-04-26 | 1987-01-06 | Somerville Robert L | Method of converting brines to useful products |
| RU2211803C2 (ru) * | 2001-06-26 | 2003-09-10 | Закрытое акционерное общество "Экостар-Наутех" | Способ получения оксида магния из природных рассолов |
| RU2281248C1 (ru) * | 2005-03-10 | 2006-08-10 | Ордена Ленина и ордена Октябрьской Революции Институт геохимии и аналитической химии им. В.И. Вернадского Российской академии наук (ГЕОХИ РАН) | Способ получения оксида магния из высокоминерализованных рассолов |
| WO2007088407A1 (en) * | 2006-01-31 | 2007-08-09 | Council Of Scientific And Industrial Research | An improved process for preparation of magnesium oxide |
| RU2543214C2 (ru) * | 2013-04-11 | 2015-02-27 | Закрытое акционерное общество (ЗАО) "Экостар-Наутех" | Способ комплексной переработки природных рассолов хлоридного кальциево-магниевого типа |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115814752A (zh) * | 2023-01-31 | 2023-03-21 | 成都理工大学 | 一种碳酸钙和纳米氧化镁复合材料及其制备与应用方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA3059899C (en) | PROCESS FOR PREPARING LITHIUM CONCENTRATE FROM NATURAL BRINES CHARGED WITH LITHIUM AND ITS TRANSFORMATION INTO LITHIUM CHLORIDE OR LITHIUM CARBONATE | |
| KR102093004B1 (ko) | 마그네슘 함유 제련 폐수를 종합 회수하는 방법 | |
| US3525675A (en) | Desalination distillation using barium carbonate as descaling agent | |
| KR101936809B1 (ko) | 알칼리 산업부산물과 해수의 간접탄산화를 이용한 고순도 탄산칼슘의 제조방법 | |
| CN105129822B (zh) | 一种处理氯碱生产副产盐泥的系统和方法 | |
| CN103011203A (zh) | 一种处理生产TiCl4过程中产生的氯化废熔盐的方法 | |
| US20100233767A1 (en) | Process for the recovery of magnesium from a solution and pretreatment | |
| US20160244348A1 (en) | A method for treating alkaline brines | |
| CN100594245C (zh) | 利用氯化物型盐湖提钾副产的氯化镁制备合成煅白的方法 | |
| CN107032384B (zh) | 一种从钙镁矿物中分离回收钙镁的方法 | |
| RU2777082C1 (ru) | Способ получения оксида магния из природных рассолов и попутно добываемых вод нефтяных месторождений | |
| CN112546529B (zh) | 一种利用工业废渣及废气实现高碱性赤泥脱碱的工艺 | |
| CN102795701A (zh) | 硫酸法制取钛白粉的酸性废水治理的方法 | |
| RU2211803C2 (ru) | Способ получения оксида магния из природных рассолов | |
| KR20190028937A (ko) | 해수 담수화 농축수의 친환경 처리방법 | |
| KR20130073500A (ko) | 농축해수를 이용한 해수마그네시아 제조방법 | |
| RU2082826C1 (ru) | Способ производства магния | |
| RU2189362C2 (ru) | Способ комплексной переработки попутных вод нефтяных месторождений | |
| WO2014168599A1 (ru) | Способ переработки твердых отходов химической очистки соляных рассолов | |
| RU2036838C1 (ru) | Способ очистки раствора хлорида натрия | |
| Seil et al. | Study of literature on separation of magnesia from lime in dolomite and similar materials | |
| CN101823738B (zh) | 一种用氯碱盐泥生产轻质碳酸镁联产微细碳酸钙和水玻璃的方法 | |
| RU2737659C1 (ru) | Способ получения хлорида магния шестиводного | |
| RU2646008C1 (ru) | Способ очистки и минерализации природных вод | |
| RU2006476C1 (ru) | Способ получения минеральных веществ из морской воды |