RU2707070C2 - Композиции, содержащие комплексы металлов ряда лантаноидов - Google Patents
Композиции, содержащие комплексы металлов ряда лантаноидов Download PDFInfo
- Publication number
- RU2707070C2 RU2707070C2 RU2017116220A RU2017116220A RU2707070C2 RU 2707070 C2 RU2707070 C2 RU 2707070C2 RU 2017116220 A RU2017116220 A RU 2017116220A RU 2017116220 A RU2017116220 A RU 2017116220A RU 2707070 C2 RU2707070 C2 RU 2707070C2
- Authority
- RU
- Russia
- Prior art keywords
- metal
- chelator
- solution
- resin
- lanthanide
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/08—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier
- A61K49/10—Organic compounds
- A61K49/101—Organic compounds the carrier being a complex-forming compound able to form MRI-active complexes with paramagnetic metals
- A61K49/106—Organic compounds the carrier being a complex-forming compound able to form MRI-active complexes with paramagnetic metals the complex-forming compound being cyclic, e.g. DOTA
- A61K49/108—Organic compounds the carrier being a complex-forming compound able to form MRI-active complexes with paramagnetic metals the complex-forming compound being cyclic, e.g. DOTA the metal complex being Gd-DOTA
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/08—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier
- A61K49/10—Organic compounds
- A61K49/101—Organic compounds the carrier being a complex-forming compound able to form MRI-active complexes with paramagnetic metals
- A61K49/106—Organic compounds the carrier being a complex-forming compound able to form MRI-active complexes with paramagnetic metals the complex-forming compound being cyclic, e.g. DOTA
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Radiology & Medical Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Dermatology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Изобретение относится к способу очистки для удаления примесей ионов металлов из комплекса металла ряда лантаноидов, состоящего из металла ряда лантаноидов с макроциклическим хелатором из класса аминокарбоновых кислот. Способ включает следующие стадии: (i) комплексообразование указанного хелатора, содержащего указанную примесь металла M, с избытком указанного металла ряда лантаноидов в подходящем растворителе с образованием первого раствора указанного комплекса металла ряда лантаноидов, содержащего избыток ионов лантаноида и M; (ii) удаление избытка ионов лантаноида и M из первого раствора со стадии (i) путем приведения указанного раствора один или более раз в контакт с поглотительной смолой в форме фармацевтически приемлемой катионной органической соли, при этом избыток лантаноида и M связываются в комплексы на указанной смоле; (iii) отделение твердофазной смолы от первого раствора со стадии (ii) с получением второго раствора, который содержит указанный комплекс металла ряда лантаноидов, свободный от избытка лантаноида и M. M представляет ион металла, выбранный из кальция, магния и цинка или их смесей. Указанный второй раствор содержит менее 10 млн долей (ppm) M. Также предложены способ получения жидкой фармацевтической композиции, способ получения контрастного агента для МРТ, поглотительная смола и ее применение. Предложенное изобретение обеспечивает получение жидкой фармацевтической композиции с низким уровнем примесей ионов металлов. 5 н. и 13 з.п. ф-лы, 2 ил., 3 табл., 9 пр.
Description
Область изобретения
Настоящее изобретение относится к способу удаления примесей ионов металлов, таких как кальций, из комплексов металлов ряда лантаноидов с макроциклическими хелаторами. В способе применяют поглотительную смолу для удаления ионов металла, вытесняемых из хелатора с помощью избытка ионов лантаноида. Также предложен способ получения контрастных агентов для магнитно-резонансной томографии (МРТ) из очищенного комплекса металла ряда лантаноидов путем добавления заданного избытка хелатора.
Уровень техники
Комплексы металлов с металлами ряда лантаноидов, особенно гадолиния, представляют интерес в качестве контрастных агентов для МРТ в области in vivo получения изображений для медицинской диагностики. Контрастные агенты для МРТ на основе металлических комплексов гадолиния подробно рассмотрены (см., например, Zhang et al, Curr.Med.Chem., 12, 751-778 (2005) и Aime et al, Adv.Inorg.Chem., 57, 173-237 (2005)).
Однако свободные ионы гадолиния действительно проявляют значительную in vivo токсичность. US 5876695 решает эту проблему путем включения в композицию с комплексом металла гадолиния добавки, которая является «слабым хелатным комплексом металла», например, с кальцием. Идея состоит в том, что «слабый хелатный комплекс металла» будет эффективно связывать в комплекс любые ионы гадолиния, которые могут быть случайно высвобождены или уже присутствовать, и таким образом улучшать безопасность композиции контрастного вещества для МРТ.
В ЕР 2513043 В1 раскрыт способ получения металлических комплексов гадолиния, в которых гадолиний сначала образует комплекс с катионообменной смолой, возможно функционализированной группой, координирующей металл. Связанный с твердой фазой гадолиний затем реагирует с хелатирующим агентом - аминокарбоновой кислотой, для высвобождения целевого комплекса гадолиния. Любой избыток гадолиния остается связанным с твердой фазой.
В ЕР 2242515 В9 раскрыт способ получения жидкой фармацевтической композиции, содержащей комплекс макроциклического хелата с лантаноидом, где количество свободного макроциклического хелата составляет от 0,002 мол. % до 0,4 мол. %, причем указанный способ включает следующие последовательные стадии:
b) получение жидкой фармацевтической композиции, содержащей комплекс макроциклического хелата с лантаноидом и свободный макроциклический хелат, который не находится в виде эксципиента X[X',L], в котором L представляет собой макроциклический хелат, а X и X' представляют собой ион металла, в частности независимо выбранный из кальция, натрия, цинка и магния, а также свободный лантаноид, путем смешивания раствора свободного макроциклического хелата и свободного лантаноида так, чтобы получить образование комплекса лантаноида с помощью макроциклического хелата, причем количества свободного макроциклического хелата и свободного лантаноида такие, что не весь лантаноид образует комплекс;
c) определение в фармацевтической композиции, полученной на стадии b), концентрации свободного лантаноида ; причем концентрация свободного макроциклического хелата равна 0;
d) регулирование и путем добавления в композицию, полученную на стадии b), количества свободного макроциклического хелата, необходимого, во-первых, для завершения образования комплекса свободного лантаноида для получения , и,
во-вторых, с получением , где является целевой концентрацией свободного макроциклического хелата в конечной жидкой фармацевтической композиции и выбрана в интервале от 0,002 мол. % до 0,4 мол. %,
при этом количество свободного макроциклического хелата в конечной жидкой фармацевтической композиции соответствует доле свободного макроциклического хелата относительно количества образовавшего комплекс макроциклического хелата в конечной жидкой фармацевтической композиции.
В ЕР 2242515 В9 указано, что способ предпочтительно дополнительно включает предварительную стадию а) определения теоретической целевой концентрации свободного макроциклического хелата в конечной жидкой фармацевтической композиции.
В ЕР 2242515 В9 указано, что композиция должна содержать менее 50 млн долей (ppm) кальция, и поэтому необходимо тщательно регулировать содержание кальция во всех реагентах и растворителях. Однако, в ЕР 2242515 указано, что содержание кальция в макроциклическом хелаторе должно быть менее 250 млн долей (ppm), во-первых, из-за того, что свободный хелатор (например, DOTA) прекрасно подходит для кальций-содержащих DOTA частиц по кинетике in vivo захвата любых свободных ионов гадолиния. Во-вторых, в ЕР 2242515 В9 предполагается, что более высокие уровни кальция будут связывать в комплекс макроциклический хелатор, и поэтому стадия (d) регулирования будет недостаточно удовлетворительной. В ЕР 2242515 В9 указано, что предпочтительно измерять содержание кальция в композиции и, если нужно, удалять из нее кальций. В ЕР 2242515 В9, однако, не указано, ни как достичь удаления кальция, ни как минимизировать содержание кальция в реагентах.
В US 2012/0082624 А1 раскрыт способ, аналогичный раскрытому в ЕР 2242515 В9, за исключением того, что фармацевтическую композицию получают в виде порошка.
В ЕР 2242515 В9 и в US 2012/0082624 А1 подчеркивают, что в способах производства фармацевтического вещества в промышленном масштабе добавление 0,1 мол. % свободного макроциклического хелатора с требуемой степенью точности собственно взвешивания является трудноосуществимым. Это было отнесено за счет 1000-кратной разницы в количествах, связанных с гигроскопичностью хелатора. Заявленное решение, описанное выше, состоит, во-первых, в осуществлении образования комплекса металла с избытком иона лантаноидного металла, затем в точном определении концентрации необразовавшего комплекс, находящегося в избытке лантаноида. Это определение впоследствии используют для точного вычисления, сколько дополнительного хелатора должно быть добавлено как для связывания в комплекс избытка лантаноида, так и достижения необходимого 0,1 мол. % избытка макроциклического хелата.
Сравнительный пример 3 из ЕР 2242515 В9 включает получение в лабораторном масштабе, в результате которого получают Gd-DOTA путем реакции DOTA (10 г, 25 ммоль) со стехиометрическим количеством оксида гадолиния (Gd2O3, 12,5 ммоль) при 80°С в воде при рН от 6 до 7. Величину рН затем регулируют до 5, и остаток свободного гадолиния удаляют путем перемешивания со смолой Chelex в течение 2 часов с последующей фильтрацией. В ЕР 2242515 В9 указано, что комплекс Gd-DOTA затем осаждают из водного этанола с выделением белого порошка с выходом 80%. В ЕР 2242515 В9 не указано, как способ из сравнительного примера 3 можно адаптировать для получения жидкой фармацевтической композиции, имеющей избыток макроциклического хелатора в интервале от 0,002 мол. % до 0,4 мол. %, в частности в промышленном масштабе. Кроме того, применение смолы Chelex, как указано в примере 3 из ЕР 2242515 В9, высвобождает ионы натрия, которые загрязняют продукт, если не проводить дополнительные стадии очистки. В Пример 3 из ЕР 2242515 В9 также описывают получение специфического комплекса гадолиния, который требует стадий очистки и выделения, не приемлемых для способа промышленного производства жидкой фармацевтической композиции.
В WO 2014/114664 представлен способ получения комплекса Gd-DOTA с меглумином (гадотерат меглумина), который сначала включает синтез DOTA из циклена (1,4,7,10-тетраазациклододекана), с последующей многостадийной очисткой путем перекристаллизации, а также катионообменной и анионообменной хроматографии. Очищенная DOTA затем реагирует с Gd2O3 с образованием комплекса Gd-DOTA, с последующим добавлением меглумина с образованием целевого продукта. В WO 2014/114664, однако, не указано, ни как достичь в промышленном масштабе получения 0,1%-ного избытка DOTA, ни как удалить примеси ионов металлов.
В WO 2014/161925 указано, что, когда получают комплекс Gd-DOTA и аналогичные комплексы в промышленном масштабе, перед применением необходимо проводить количественное определение содержания влаги в хелаторе и соответственно корректировать используемые молярные количества. В WO 2014/161925 отмечают, что содержание влаги в DOTA меняется в зависимости от условий относительной влажности. В WO 2014/161925, однако, не указано, как получить такие комплексы Gd-DOTA свободными от ионов кальция.
Таким образом, хотя в уровне техники предлагают различные подходы к промышленному получению фармацевтических композиций, содержащих комплекс Gd-DOTA с меглумином, все они не содержат информации по тому, как удалять примеси ионов металлов. Кроме того, ЕР 2242515 В9, в частности, указывает, что для получения фармацевтической композиции, содержащей комплекс Gd-DOTA с меглумином, необходимы сырьевые материалы, не содержащие примесей ионов металлов.
Следовательно, все еще существует потребность в альтернативных способах получения композиций комплексов металлов ряда лантаноидов с макроциклическими хелаторами, содержащих избыток таких хелаторов и низкие уровни примесей ионов металлов. Такие способы предпочтительно должны подходить для фармацевтического производства в промышленном масштабе, а также для обеспечения контрастных агентов для МРТ, содержащих такие композиции.
Настоящее изобретение
Настоящее изобретение относится к способу удаления примесей ионов металлов, таких как кальций, из комплексов металлов ряда лантаноидов с макроциклическими хелаторами. В способе используют избыток ионов лантаноида для вытеснения ионов металла из хелатора и поглотительную смолу для удаления вытесненных ионов металла. Способ обеспечивает получение жидкой фармацевтической композиции, где указанная композиция содержит комплекс металла с металлом ряда лантаноидов и макроциклическим хелатором, а также указанный хелатор в не связанной в комплекс форме в количестве в интервале от 0,002 до 0,4 мол. % указанного металла, и имеет низкие уровни примесей ионов металлов, в частности, кальция. Такие композиции применяют для обеспечения контрастных агентов для МРТ.
В настоящем изобретении предложен способ, в котором небольшой избыток ионов лантаноида добавляют в раствор, содержащий макроциклический хелатор, чтобы, во-первых, связать в комплекс весь не связанный в комплекс макроциклический хелатор и, во-вторых, переметаллировать все комплексы металлов с макроциклическим хелатором, тем самым сделав координирующие примеси ионов металлов (М), таких как кальций, доступными для удаления с помощью смолы, захватывающей ионы металлов. Следовательно, макроциклический хелатор не должен, как указано в уровне техники, подвергаться перед использованием интенсивной очистке для удаления кальция.
Настоящее изобретение решает проблему удаления загрязнений ионов металлов с помощью поглотительной смолы, без дополнительного введения в готовую композицию ионов натрия. Таким образом, предложена новая поглотительная смола, способная осуществлять обмен примесей ионов металлов на ионы меглуминия. Обычно такие смолы действуют по принципу осуществления обмена захваченных ионов металлов на противоион, который предварительно введен в смолу. Коммерчески доступные смолы Chelex® содержат предварительно введенный натрий, и такой тип этой смолы (chelex) не подходит для данного способа, так как фармацевтическая композиция будет загрязнена ионами натрия.
Способ по настоящему изобретению обеспечивает также способ, с помощью которого получают комплекс металла ряда лантаноидов с хелатором в отсутствие избытка ионов лантаноида, так как связывающая на твердой фазе поглотительная смола удаляет и примеси ионов металлов (М), и ионы лантаноида. Кроме того, комплекс лантаноида с хелатором хранят в водном растворе, поэтому поправка на содержание влаги в комплексе не является необходимой. Так как способ обеспечивает промежуточный раствор комплекса металла ряда лантаноидов без свободных ионов лантаноида, можно легко рассчитать количество избытка макроциклического хелатора, которое нужно добавить для получения целевой композиции, имеющей определенный избыток свободного хелатора.
В способе по настоящему изобретению также не требуется проведения стадий определения и регулирования, предусмотренных в уровне техники, что является полезным упрощением сточки зрения времени и усилий.
Способ по настоящему изобретению обладает дополнительными преимуществами, состоящими в том, что способ можно проводить в промышленном масштабе, а связывающую поглотительную смолу можно при необходимости регенерировать после использования для регенерации материала, подходящего для производства следующих партий фармацевтической композиции.
Подробное описание настоящего изобретения
В первом аспекте настоящего изобретения предложен способ очистки для удаления примесей ионов металлов из комплекса металла ряда лантаноидов с металлом ряда лантаноидов и макроциклическим хелатором, где указанный способ включает следующие стадии:
(i) комплексообразование указанного хелатора, содержащего указанную металлическую примесь М, с избытком указанного металла ряда лантаноидов в подходящем растворителе с получением первого раствора указанного комплекса металла ряда лантаноидов, содержащего избыток ионов лантаноида и М;
(ii) удаление избытка ионов лантаноида и М из первого раствора со стадии (i) путем приведения указанного раствора один или более раз в контакт с поглотительной смолой в форме фармацевтически приемлемой катионной органической соли, при этом избыток лантаноида и М связываются в комплекс на указанной смоле;
(iii) отделение твердофазной смолы от первого раствора со стадии (ii) с получением второго раствора, который содержит указанный комплекс металла ряда лантаноидов, свободный от избытка лантаноида и М;
где М - ион металла, выбранный из кальция, магния и цинка, или их смесей;
при этом указанный второй раствор содержит менее 10 млн долей (ppm) М.
Термины «хелатор» или «хелатирующий агент» имеют общепринятое значение и относятся к лигандам, которые образуют координационные комплексы металлов, которые содержат атомы мультикоординирующих металлов-доноров, расположенных так, что в процессе образования координационного соединения (при том, что некоординирующий скелет состоит из атомов углерода или некоординирующих гетероатомов, связанных с атомами металлов-доноров) обычно получают 5-, 6- или 7- членные хелатные кольца (предпочтительно 5- или 6- членные кольца). Термин "макроциклический" употребляется в своем общепринятом значении в области координационной химии и относится к хелатору, где по меньшей мере часть атомов металла-донора указанного хелатора ковалентно связаны в виде части кольцевой системы.
Выражение "содержащий указанную металлическую примесь М" относится к ионам М, координационно связанным с макроциклическим хелатором. Таким образом, способ по настоящему изобретению позволяет использовать такие хелаторы без проведения указанных в уровне техники стадий интенсивной предварительной обработки для удаления кальция.
Выражение "поглотительная смола" относится к катионообменному агенту, ковалентно связанному с твердофазным материалом или смолой, нерастворимым в растворителе, используемом для связывания лантаноида в комплекс. Поглотительная смола связывает ионы свободного металла в растворе и, таким образом, способна удалять или «поглощать» любые такие ионы металла из раствора. Подходящие поглотительные смолы являются стандартными катионообменными смолами, такими как, например, Puropack (Purolite), Applexion ХА 2033, (Novasep) и Amberlite IRP69 (DOW) или «поглотительным хелатором», указанным ниже.
Поглотительная смола предпочтительно содержит поглотительный хелатор. «Поглотительный хелатор» - это хелатирующий агент, ковалентно сопряженный с твердофазным материалом или смолой, который выбирают так, чтобы он отличался от «макроциклического хелатора», и, следовательно, имел соответственно меньшую константу комплексообразования с металлом ряда лантаноидов, чем «макроциклический хелатор». Таким образом, «поглотительный хелатор» выбирают соответственно так, что он не может вытеснять ион металла ряда лантаноидов из комплекса металла ряда лантаноидов с макроциклическим хелатором по настоящему изобретению. Поглотительный хелатор предпочтительно выбирают так, что кинетика захвата свободного иона металла в растворе является быстрой. По этой причине, линейные (т.е. немакроциклические) поглотительные хелаторы являются предпочтительными. Будучи связанным с твердой фазой, поглотительный хелатор легко отделяется от раствора, с которым он находится в контакте, путем фильтрации, при необходимости промывания. Подходящие твердофазные материалы включают синтетические полимеры и сополимеры.
Под выражением "в форме фармацевтически приемлемой катионной органической соли" понимают, что поглотительная смола соответствующим образом модифицирована перед использованием в способе по настоящему изобретению. Поглотительные смолы действуют по принципу осуществления обмена поглощенных ионов металла на противоион, который предварительно внесен в смолу. Например, в коммерчески доступную Chelex® предварительно внесен натрий. Такой натриевый тип смолы (chelex) не подходит для способа по настоящему изобретению, так как полученная фармацевтическая композиция будет загрязнена ионами натрия. Существенный аспект настоящего изобретения состоит в способе предварительной обработки смолы, на котором происходит обмен неподходящего противоиона (натрия) на ион, совместимый с фармацевтической композицией. Такого рода подходящие фармацевтически приемлемые катионные органические соли известны в уровне техники и включают: меглумин, гидроксоний, деанол, диэтаноламин, диэтилэтаноламин, глюкозамин, этаноламин, 2-морфолинэтанол, 1-(2-гидроксиэтил)пирролидин, триэтаноламин, трометамин, пиперазин, пиперидин, пирролидин, триэтиламин, триметиламин, трипропиламин и этилпиперидин. Предпочтительно, соль выбирают так, чтобы она была такой же, как соль фармацевтической композиции, содержащей комплекс металла ряда лантаноидов, и контрастного агента для МРТ, получаемого по второму и третьему аспектам изобретения, соответственно (см. ниже).
Такими солями предпочтительно являются соли меглуминия, трометамолия или гидроксония, причем наиболее предпочтительными являются соли меглуминия. С помощью способа с поглотительной смолой по настоящему изобретению можно осуществить обмен примесей ионов металлов и избытка ионов лантаноида на ионы, совместимые с фармацевтической композицией. Примерами таких совместимых ионов являются меглуминий, трометамолий и гидроксоний.
Выражение "содержащий менее 10 млн долей (ppm) М" относится к ионам М, координированным с макроциклическим хелатором. Предпочтительно, второй раствор содержит менее 5 млн долей (ppm) М, более предпочтительно менее 1 млн доли (ppm) М.
Способ из Примера 3 в ЕР 2242515 В9 имеет проблему высвобождения ионов натрия. Эти ионы натрия будут увеличивать осмоляльность жидкой фармацевтической композиции. Это нежелательно для промежуточных растворов или композиций, используемых при производстве контрастных агентов, так как с контрастными агентами с высокой осмоляльностью связывают отек мягких тканей, воспаление и повреждение тканей [Cohan et al, Radiology, 200(3), 593-604. doi:10.1148/radiology.200.3.8756899 (1996)]. Следовательно, способ производства контрастных агентов не должен вводить ионные частицы, которые будут влиять на осмоляльность продукта.
В случае DOTA, известно, что соль натрия гадотеровой кислоты склонна к кристаллизации [Chang et al, Inorg.Chem., 32(16), 3501-3508 (1993)], следовательно, важно поддерживать уровни натрия на минимально возможном уровне для минимизации риска осаждения GdDOTA-меглумин в виде NaGdDOTA.
Термины "содержащий" или "содержит" имеют свое общепринятое значение в контексте всей заявки и предполагают, что агент или композиция должны иметь перечисленные существенные признаки или компоненты, но, помимо этого, дополнительно могут присутствовать другие. Термин «содержащий» заключает в себе предпочтительный подтекст "состоящий по существу из", который означает, что композиция содержит перечисленные компоненты, без присутствия других признаков или компонентов.
Походящие растворители для комплексообразования на стадии (i) известны в уровне техники [The Chemistry о f Contrast Agents in M edical Magnetic Resonance Imaging, 2nd Edition, A.Merbach, L.Helm & E.Toth (Eds), Wiley (2013)], и предпочтительно являются водными. Комплексообразование лантаноидов с макроциклическими хелаторами (например, DOTA) является многостадийным процессом, который включает до некоторой степени стабильный исходный комплекс, который медленно видоизменяется с образованием конечного, термодинамически устойчивого, комплекса металла. На стадии (i) предпочтительно обеспечить, чтобы перед переходом к стадии (ii) был образован устойчивый комплекс лантаноида, как известно из уровня техники [Moreau et al, Chem.Eur.J., 10(20), 5218-32 (2004)] - например, путем нагревания, увеличенного времени реакций, повышения рН или путем сочетания этих факторов.
Избыток металла ряда лантаноидов на стадии (i) получают путем вычисления молярных соотношений с учетом стехиометрии комплекса металла ряда лантаноидов с макроциклическим хелатором. Обычно это комплекс 1:1. Такая информация приводится в he Chemistry о f Contrast Agents in Medical Magnetic Resonance Imaging, 2nd Edition, A.Merbach, L.Helm & E.Toth (Eds), Wiley (2013); для комплексов гадолиния в Port et al [Biometals, 21, 469-490 (2008)]; и для DOTA комплексов в Viola-Villegas et al [Coord.Chem.Rev., 253, 1906-1925 (2009)]. Принимают во внимание также процент химической чистоты применяемого лантаноида и рассматриваемого хелатора.
Приведение в контакт на стадии (ii) проводят, соответственно, так, что весь "первый раствор" подвергают воздействию поглотительной смолы. Это можно проводить двумя основными способами или путем их комбинаций. Первая возможность состоит в смешивании поглотительной смолы с "первым раствором". Альтернативно, смолу можно обеспечить в виде колонки и элюировать "первый раствор" через колонку. Это не является собственно хроматографическим способом, но является удобным способом взаимодействия "первого раствора" с поглотительной смолой. Разделения на стадии (iii) достигают путем фильтрования раствора для удаления связывающей лантаноид смолы или, соответственно, путем сбора элюата из элюирующей колонки. В любом варианте, "первый раствор" можно подвергнуть воздействию поглотительной смолы несколько раз. Предпочтительно, отфильтрованную смолу или колонку можно промывать подходящим растворителем для обеспечения более полного извлечения "второго раствора".
Способ по первому аспекту подходит для проведения в лабораторном масштабе, масштабе пилотной установки или в масштабе промышленного производства. Способ подходит, в частности, для производства в килограммовом масштабе от 1 кг до 800 кг, предпочтительно в масштабе от 100 кг до 650 кг.
Способ по первому аспекту имеет ограничение, состоящее в том, что только примеси металлов, имеющие более низкую константу комплексообразования с указанным макроциклическим хелатором по сравнению с лантаноидом, можно переметаллировать и одновременно удалить с помощью поглотительной смолы. Это потому, что, как описано выше, образование комплекса с лантаноидом проводят в «термодинамических условиях» так, что получают термодинамический продукт -комплекс металла ряда лантаноидов. Кроме того, реакцию комплексообразования первоначально проводят в кислой среде, в которой быстро устанавливается кинетическое равновесие, так что достигается термодинамическое равновесие [Port et al, Biometals, 21(4), 469-490 (2008)].
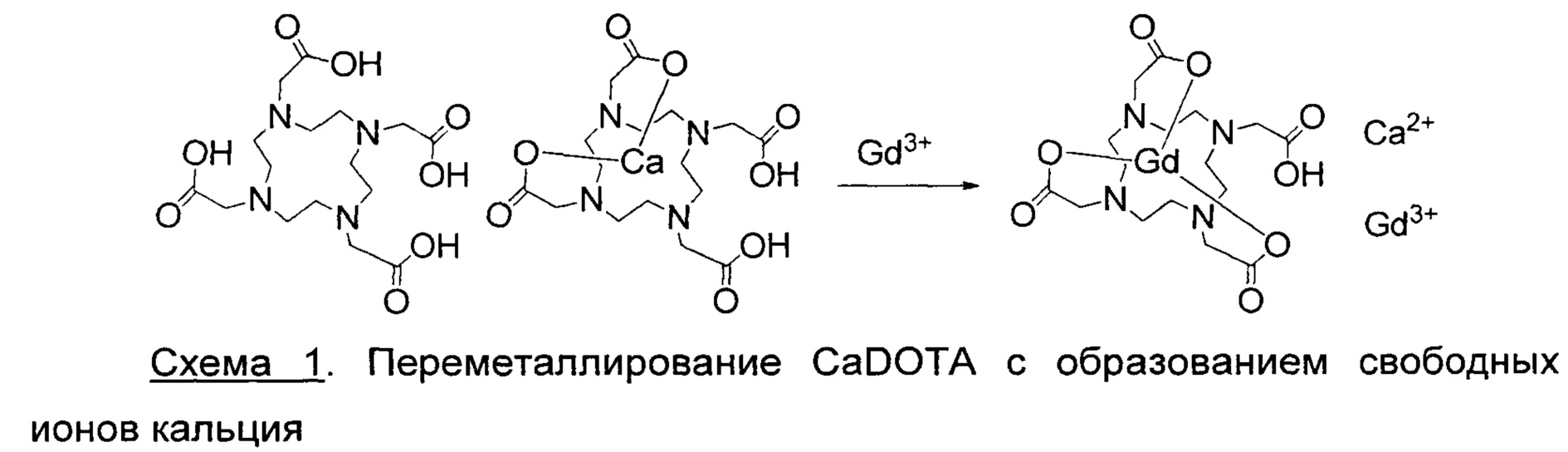
Избыток лантаноида инициирует реакцию переметаллирования, как показано на Схеме 1 для Ca-DOTA и ионов гадолиния:
Небольшой избыток гадолиния обеспечивает полное связывание DOTA в комплексы с образованием Gd-DOTA, а DOTA-координированные ионы примеси металла (такого как кальций) можно эффективно переметаллировать в раствор в виде свободных ионов вследствие их менее удовлетворительной термодинамической устойчивости.
В Таблице 1 приведен список различных комплексов ионов металлов с DOTA и их термодинамическая стабильность:
*Данные из:
Popov, K. Felcman, J. Delgado, R. Arnaud-Neu, F. Anderegg, G. Pure Appl. Chem. 77, 8, 2005;
Cacheris, W.P, Nickle, S.K. Sherry, A.D; Inorg. Chem. 2646, 1986;
Toth, E. Brucher, E; Inorganica Chimica Acta, 221(1-2), 1994, pp. 165-167.
Следовательно, любые координированные ионы металлов, имеющие более низкую константу устойчивости, чем Gd-DOTA (такие как, натрий, кальций, марганец, цинк, медь или магний), будут высвобождаться при переметаллировании Gd и затем удаляться с помощью поглотительного хелатора на стадиях (ii) и (iii). Теоретически комплексы металлов с большей термодинамической устойчивостью, чем Gd-DOTA, можно было бы переметаллировать путем добавления большего избытка ионов гадолиния для сдвига равновесия, однако, это может иметь ограничения на практике в отношении количества поглощающей смолы, необходимой для удаления свободных ионов металлов. Если ионы лантаноида не могут переметаллировать загрязняющий ион металла (М) в комплексе с макроциклическим хелатором из-за более высокой константы устойчивости или из-за недостаточного количества лантаноида в растворе для достижения стехиометрического соотношения, поглотительная смола не сможет удалить загрязняющий ион металла, так как он находится в связанной в комплекс форме. Связанный в комплекс ион металла не будет иметь того суммарного катионного заряда, как в свободной не связанной в комплекс форме, что приведет к меньшей склонности иона металла к обмену на поглотительной смоле.
Предпочтительные воплощения
В способе по первому аспекту М предпочтительно представляет собой кальций.
В способе по первому аспекту избыток металла ряда лантаноидов на стадии (i) предпочтительно составляет от 0,01 до 5, более предпочтительно от 0,01 до 1, наиболее предпочтительно от 0,05 до 0,5 мол. %.
Когда используют поглотительную смолу Chelex-100, смола Chelex имеет более высокую склонность к взаимодействию с гадолинием, чем с кальцием. Это означает, что применение большого избытка гадолиния в реакции комплексообразования на стадии (i) приведет к менее экономически эффективному процессу поглощения, так как потребуется добавлять большой избыток поглотительной смолы - во-первых, для удаления свободного гадолиния и, во-вторых, для удаления свободного кальция (или ионов аналогичных металлов). Следовательно, предпочтительно использовать очень небольшой избыток гадолиния в реакции комплексообразования на стадии (i).
Если считают, что макроциклический хелатор содержит координированные ионы кальция или аналогичного металла, как описано выше, то предпочтительным является очень небольшой избыток гадолиния в интервале примерно от 0,01 до 0,1 мол. % или 10-100 млн долей (ppm) в 0,5 М-ном растворе GdDOTA. Такой интервал является достаточно небольшим для обеспечения достаточной поглотительной активности для удаления кальция (металла), но достаточно высоким для обеспечения полного переметаллирования любого комплекса Ca-DOTA (или родственных молекул).
Самых низких уровней избытка металла ряда лантаноидов в пределах указанного интервала (примерно от 0,01 до 0,1 мол. %) можно достичь путем определения количества избытка лантаноида и, если необходимо, регулирования добавки лантаноида или свободного хелатирующего агента (аналогично указанному в ЕР 2242515 В9, несмотря на то, что в результате есть избыток лантаноида и нет избытка лиганда).
Альтернативно, самых низких уровней избытка металла ряда лантаноидов в пределах указанного интервала (примерно от 0,01 до 0,1 мол. %) можно достичь путем постепенного добавления аликвот такого лантаноида до появления положительной пробы на присутствие свободных ионов металла. Походящий размер аликвоты будет находиться в интервале 0,01-0,1% от общего количества лантаноида, используемого в реакции комплексообразования. Такие "капельные анализы" дают ответ да/нет в отношении присутствия/отсутствия, но не предоставляют информации о концентрации свободных ионов металла. Капельные анализы можно проводить можно проводить с помощью видимого окрашивания с помощью ксиленолового оранжевого, как известно в уровне техники [Barge et al, Contrast Med.Mol. Imaging, 1, 184-188 (2006)]. Barge et al указывают, что визуальное обнаружение оранжевой окраски, характерной для свободного Gd3+, является эффективным для определения Gd3+ при концентрации до 10 мкМ или меньше. Альтернативно, избыток ионов металла можно определить с помощью количественного анализа с ксиленоловым оранжевым или количественного анализа с Арсеназо III, как известно в уровне техники [Barge et al, Contrast Med.Mol. Imaging, 1, 184-188 (2006) и Clogston et al, Molec.Biol., 697, 101-108 (2011), соответственно]. Ксиленлоовый оранжевый и Арсеназо III являются коммерчески доступными, например, от Sigma-Aldrich. Более высоких уровней (более 0,1 мол. % до 5 мол. %) избытка лантаноида можно добиться только взвешиванием.
Колориметрические тесты, описанные выше, могут иметь трудности в различении разных ионов металлов и могут, следовательно, давать информацию по общему количеству свободных ионов металлов, которые координированы в молекулу красителя. Если слишком небольшое количество лантаноида добавляют в раствор, содержащий слишком большое количество ионов металлов-загрязнителей, возможно, что избыток ионов металлов, определяемых путем количественного колориметрического анализа, исключительно состоит из ионов загрязняющих металлов, а не ионов лантаноида, и что ионы загрязняющего металла остаются в связанной в комплекс форме, не доступной для удаления с помощью ионообменной смолы. Для гарантии того, что избыток ионов металла, определяемый путем количественного колориметрического анализа, также содержит металл ряда лантаноидов, а не только ионы загрязняющего металла, предусматривают, что реакцию комплексообразования характеризуют методом элементного анализа, например, ИСП-МС (ионо-связанная плазма с масс-спектрометрией). Метод ИСП-МС анализа не будет отличать свободные ионы металла от связанных в комплекс, а только даст информацию по общему количеству различных элементов. Эту информацию можно использовать для расчета, насколько большим должен быть избыток лантаноида для успешного переметаллирования всех примесных ионов металлов, и гарантирует, что избыток ионов металла, определяемого методом количественного колориметрического анализа, также включает ионы лантаноида.
В способе по первому аспекту, металл ряда лантаноидов предпочтительно представляет собой гадолиний, празеодим, диспрозий, европий или тулий, и наиболее предпочтительно представляет собой гадолиний.
Макроциклический хелатор предпочтительно представляет собой гептадентат или октадентат, и более предпочтительно содержит атомы-доноры N и/или О. Атомы-доноры предпочтительно обеспечивают карбоксилатная, амино, спиртовая или фосфонатная донорные группы. Макроциклический хелатор более предпочтительно относится к классу аминокарбоновой кислоты. Если макроциклический хелатор относится к классу аминокарбоновых кислот, такие хелаторы предпочтительно содержат: DOTA, NOTA, DO3A, BT-DO3A, НР-DO3A или РСТА. Макроциклический хелатор наиболее предпочтительно содержит DOTA или ее соль:
DOTA и комплексы металлов с нею в применении к получению биомедицинских изображений описаны Stasiuk и Long [Chem.Comm., 49, 2732-2746 (2013)].
В способе по первому аспекту, предпочтительно, чтобы металл ряда лантаноидов представлял собой гадолиний и макроциклический хелатор содержал DOTA. Наиболее предпочтительно, комплекс гадолиний-DOTA содержит меглуминовую соль гадолиния-DOTA.
Когда поглотительная смола содержит «поглотительный хелатор», поглотительный хелатор предпочтительно содержит иминодиуксусную кислоту (ИДА), ЭДТА (этилендиаминтетраацетат) или DTPA (диэтилентриаминпентауксусная кислота), более предпочтительно ИДА. Предпочтительным поглотительным хелатором является Chelex® 100, который представляет собой сополимер стирола-дивинилбензола, имеющий сопряженный с ним хелатор ИДА. Chelex® 100 является коммерчески доступным в виде соли натрия или аммония от Bio-Rad Laboratories. Поставщик обеспечивает информацию о количествах смолы, которую необходимо использовать для удаления заданного количества металла. В нейтральной рН Chelex действует в качестве катионообменной смолы, то есть не имеет склонности к взаимодействию с комплексами металлов лантаноидов, которые заряжены отрицательно, например, с Gd(DOTA)-. Это имеет преимущество, состоящее в том, что неспецифическое связывание таких комплексов с твердой фазой является минимальным, и, следовательно, влияние на выход является минимальным.
Способ комплексообразования лантаноида на стадии (i) обычно по существу является многостадийным. В случае гадолиния, во-первых, требуется низкое значение рН (рН примерно 2) для растворения всего Gd2O3 с образованием свободных ионов гадолиния в растворе. При таком низком рН карбоксилатные группы аминокарбоксилатных хелаторов (например, DOTA) не могут полностью связать в комплекс все ионы гадолиния, так как карбоксилатные группы являются частично протонированными. Затем рН повышают (примерно до рН 4-5) путем добавления основания (предпочтительно меглумина) для предпочтительного образования карбоксилатного аниона, который, в свою очередь, способствует комплексообразованию металла. Первоначально образующийся комплекс Gd-DOTA в действительности является bis-протонированным, затем медленно претерпевает превращения с образованием конечного комплекса Gd-DOTA в высокой термодинамической (и кинетической) устойчивостью [Moreau et al, Chem.Eur.J., 10(20), 5218-32 (2004)]. Процесс превращения ускоряется при более высоком рН и нагревании (обычно в течение нескольких часов при рН 5 с доводящим реакцию до конца нагреванием). Предпочтительно, не допускают превышения рН выше 7, так как это вызывает риск протекания гидролиза любых ионов гадолиния с последующим повторным образованием Gd2O3.
Если комплекс металла ряда лантаноидов по первому аспекту нужно получить в виде соли меглумина, комплексообразование на стадии (i) предпочтительно завершают путем регулирования рН до 4,5-5,5 с помощью меглумина.
Удаление на стадии (ii) предпочтительно проводят при рН 4,0-6, более предпочтительно 4,5-5,5, причем величина рН около 5 является идеальной.
Для гарантии того, что процесс удаления завершен, можно использовать колориметрический капельный анализ для подтверждения того, что все ионы металла были удалены поглотительной смолой. Такие "капельные анализы" дают ответ да/нет в отношении присутствия/отсутствия, но не обеспечивают информации о концентрации свободных ионов металла. Капельные анализы можно проводить путем видимого окрашивания с помощью ксиленолового оранжевого, как известно в уровне техники [Barge et al, Contrast Med.Mol.Imaging, 1, 184-188 (2006)]. Barge et al указывают, что визуальное обнаружение оранжевой окраски, являющейся индикатором на присутствие свободного Gd3+, является эффективным для определения Gd3+ в концентрациях ниже 10 мкМ или менее.
Макроциклические хелаторы по изобретению коммерчески доступны у широкого ряда поставщиков. DOTA также можно синтезировать способом Десро (Desreux) [Inorg.Chem., 19, 1319-1324 (1980)]. Дополнительные подробности по синтезу макроциклических хелаторов приведены Kotel et al [Chapter 3 pages 83-155 в The Chemistry of Contrast Agents in Medical Magnetic Resonance Imaging, 2nd Edition, A.Merbach, L.Helm & E.Toth (Eds), Wiley (2013)].
Меглумин (N-метилглюкамин) и другие фармацевтически приемлемые соли коммерчески доступны от ряда поставщиков. Предпочтительно, использовать материал фармацевтической чистоты.
Во втором аспекте настоящего изобретения предложен способ получения жидкой фармацевтической композиции, которая содержит комплекс металла с металлом ряда лантаноидов и макроциклическим хелатором вместе с указанным хелатором в не связанной в комплекс форме в количестве, находящемся в интервале от 0,002 до 0,4 мол. % от указанного комплекса металла, причем указанный способ включает следующие стадии:
(A) проведение способа по первому аспекту с получением второго раствора, указанного в заявке;
(B) добавление макроциклического хелатора, указанного в первом аспекте, в не связанной в комплекс форме в количестве, находящемся в интервале от 0,002 до 0,4 мол. %, к указанному второму раствору со стадии (А) с получением указанной жидкой фармацевтической композиции;
причем указанная композиция содержит менее 10 млн долей (ppm) М, где М такой же, как указан в первом аспекте.
Предпочтительные особенности лантаноида, М, макроциклического хелатора и поглотительной смолы во втором аспекте описаны в первом аспекте (выше).
Выражение "хелатор в в не связанной в комплекс форме" относится к «свободному хелатору», т.е. свободному от любых координированных ионов металла. Следовательно, хелатор в не связанной в комплекс форме не содержит любых ионов координированного лантаноида или другого металла, и, таким образом, полностью доступен для последующего образования комплекса металла. «Хелатор в в не связанной в комплекс форме» может содержать ионы металла в ионной форме, например, когда присутствует в виде группы металлов-доноров, например, карбоновой кислоты.
Добавление на стадии (В) предпочтительно проводят путем первого добавления избытка хелатора, затем нейтрализации до нейтрального рН (примерно рН 6,5-8,0). Когда целевой макроциклический комплекс с лантаноидом представляет собой меглуминовую соль, нейтрализацию предпочтительно проводят с помощью меглумина. Добавление макроциклического хелатора на стадии (В) можно проводить без предварительного, в процессе производства, количественного определения концентрации/количества свободного лантаноида в первом или во втором растворах. Это потому что такая стадия является ненужной для способа по настоящему изобретению - удаление и разделение на стадиях (ii) и (iii) по первому аспекту дает "второй раствор" с известной (т.е. предпочтительно нулевой) концентрацией свободного лантаноида. Следовательно, добавление хелатора проводят на основе вычисленного количества «хелатора в не связанной в комплекс форме», на основании предположительно 100% конверсии в реакции комплексообразования на стадии (i), в пересчете на исходное молярное количество макроциклического хелатора на стадии (i) по первому аспекту. Такая 100% конверсия согласуется с тем, что известно в уровне техники об эффективности таких реакций. Количество хелатного комплекса с металлом ряда лантаноидов, присутствующего в растворе, известно из количества макроциклического хелатора, которое добавляли перед добавлением лантаноида и процессом очистки с помощью поглотительной смолы. Известно, что эти две операции, комплексообразования и очистки, проходят с высокими выходами, и в целях установления базиса для расчета количества не связанного в комплекс хелатора, которое нужно добавить, их считают проходящими количественно.
Альтернативно, можно определить количество хелатного комплекса с металлом ряда лантаноидов и добавить, соответственно, количество избытка хелатора.
Свободный хелатор можно добавлять в виде твердого вещества или в виде раствора, и предпочтительно в виде раствора. Когда раствор макроциклического хелатора приготовлен для проведения стадии (i) по первому аспекту, тогда наиболее предпочтительным способом является извлечение из данного раствора соответствующей объемной фракции перед добавлением лантаноида (например, извлечение примерно 1 л из объема реакции 1000 л или эквивалентного). Эту объемную фракцию затем удобно использовать для добавления на стадии (В) по второму аспекту. Такой подход исключает необходимость приготовления множества растворов и/или проведения множества вычислений для корректировки чистоты или содержания воды.
В способе по второму аспекту, хелатор в не связанной в комплекс форме предпочтительно находится в количестве в интервале от 0,025 до 0,25, более предпочтительно от 0,05 до 0,20, наиболее предпочтительно от 0,10 до 0,15 мол. % относительно макроциклического комплекса лантаноида. Хелатор в не связанной в комплекс форме является соответственно свободным от ионов металла ряда лантаноидов, и предпочтительно также является свободным от координированных ионов кальция, цинка и магния.
В третьем аспекте настоящего изобретения предложен способ получения контрастного агента для МРТ, который включает:
(a) проведение способа по второму аспекту с получением жидкой фармацевтической композиции по настоящему изобретению;
(b) необязательно разбавление жидкой фармацевтической композиции со стадии (а) биосовместимым носителем;
(c) дозирование композиции со стадии (b) в фармацевтически приемлемые контейнеры или шприцы с получением дозированных контейнеров или шприцев;
(d) проведение стадий (а)-(с) в асептических условиях производства или терминальную стерилизацию дозированных контейнеров или шприцев со стадии (с) с получением контрастного агента для МРТ в указанных фармацевтически приемлемых контейнерах или шприцах в форме, приемлемой для введения млекопитающему;
причем указанный контрастный агент содержит менее 10 млн долей (ppm) М.
Предпочтительные воплощения жидкой фармацевтической композиции по третьему аспекту указаны во втором аспекте (выше). Предпочтительные воплощения лантаноида, макроциклического хелатора и способа на стадии (а) в третьем аспекте описаны в первом аспекте (выше).
Термин "контрастный агент" имеет свое общепринятое значение в области in vivo получения изображений для медицинской диагностики и относится к агенту в форме, приемлемой для введения млекопитающему, который помогает в обеспечении более четких изображений в представляющих интерес области или органе, чем можно было бы получить путем получения изображения собственно исследуемого объекта. "Контрастный агент для МРТ" обычно является парамагнитным или ферромагнитным веществом, приемлемым для введения млекопитающему, которое укорачивает время Т1 и/или Т2 релаксации соответствующего ядра (например, 1Н для ЯМР 1Н) во внутренней области субъекта, представляющей интерес для получения изображения.
Под термином "субъект" понимают млекопитающее в состоянии in vivo, предпочтительно in vivo интактное тело млекопитающего, и более предпочтительно живого субъекта-человека. Под выражением "в форме, приемлемой для введения млекопитающему" понимают композицию, которая стерильна, апирогенна, не содержит веществ, которые производят токсическое или неблагоприятное воздействие, и составлена в условиях биосовместимого рН (примерно рН от 4,0 до 10,5). Такие композиции не содержат частиц, которые могут вызвать риск возникновения эмболии in vivo, и составлены так, что не происходит осаждения при контакте с биологическими жидкостями (например, кровью). Такие композиции также содержат только биологически совместимые эксципиенты и предпочтительно являются изотоничными.
Что касается других агентов для in vivo получения изображений, контрастный агент разработан так, чтобы иметь минимальное фармацевтическое воздействие на исследуемого субъекта-млекопитающего. Предпочтительно, контрастный агент можно вводить в тело млекопитающего минимально инвазивным способом, т.е. без существенного риска для здоровья субъекта при проведении профессиональных медицинских исследований. Такие виды минимального инвазивного введения предпочтительно представляют собой внутривенное введение в периферическую вену указанного субъекта, без необходимости в местной или общей анестезии.
Под термином "биосовместимый носитель" понимают текучую среду, особенно жидкость, такую, что композиция является физиологически приемлемой, т.е. может вводиться в тело млекопитающего без токсического или дополнительного дискомфорта. Биосовместимый носитель, соответственно, представляет собой инъекционную жидкость-носитель, например, стерильную апирогенную воду для инъекций; водный раствор, например, солевой раствор (который предпочтительно можно сбалансировать так, что конечный продукт для инъекции является изотоничным); водный буферный раствор, содержащий биосовместимый буферный агент (например, фосфатный буфер); водный раствор одного или более регулирующих тоничность веществ (например, солей катионов плазмы с биосовместимыми противоионами), Сахаров (например, глюкозы или сахарозы), сахароспиртов (например, сорбитола или маннитола), гликолей (например, глицерина) или других неионных многоатомных спиртов (например, полиэтиленгликолей, пропиленгликолей и т.п.). Предпочтительно, биосовместимый носитель представляет собой апирогенную воду для инъекций (WFI), изотонический солевой раствор или фосфатный буфер.
Выражение "асептическое производство" относится к проведению соответствующих стадий способа в условиях асептического производства, т.е. апирогенных условиях, например, в чистых помещениях. Термины "стерилизование" или "стерилизация" употребляются в своем общепринятом смысле и относятся к способу уничтожения микроорганизмов с получением стерильной апирогенной композиции. Выражение "терминальная стерилизация" употребляется в своем общепринятом смысле и относится к проведению стадий в соответствии с практикой GMP (Надлежащей производственной практики), но к проведению стадий стерилизации на как можно более поздней стадии процесса в целом. Компоненты и реагенты можно стерилизовать способами, известными в уровне техники, включая стерильное фильтрование, терминальную стерилизацию, с помощью, например, гамма-излучения, автоклавирования, сухого тепла или химической обработки (например, этиленоксидом) или их комбинаций. Термин "автоклавирование" имеет свой общепринятый смысл и относится к частному способу стерилизации, в котором для стерилизации используют перегретый пар. Автоклавирование и другие способы стерилизации описаны в Achieving Sterility in Medical and Pharmaceutical Products, N.Halls (CRC Press, 1994). В способе по второму аспекту теминальная стерилизация является предпочтительной. Предпочтительным способом терминальной стерилизации является автоклавирование.
Термин "дозированный контейнер или шприц" относится к наполненному контейнеру, т.е. контейнеру, в который внесли аликвоту композиции, т.е. к дозированному сосуду.
Подходящие контейнеры, флаконы с крышками и шприцы для применения в способе по второму аспекту имеют степень фармацевтической чистоты и широко доступны коммерчески.
Контрастный агент по второму аспекту предпочтительно содержит менее 5 млн долей (ppm) М, более предпочтительно менее 1 млн доли (ppm) М.
В четвертом аспекте настоящего изобретения предложена поглотительная смола, которая содержит катионообменную смолу, где анионная функциональная группа указанной смолы присутствует в виде фармацевтически приемлемой катионной органической соли указанной функциональной группы.
Предпочтительные воплощения поглотительной смолы по четвертому аспекту описаны в третьем аспекте (выше).
Когда поглотительную смолу используют в виде, например, меглуминовой соли, такие материалы можно получить с помощью обычных методик ионообменной хроматографии, для замены противоиона (например, натрия или солей аммония на Chelex®-100), путем промывания концентрированной кислотой с последующим удерживанием или элюированием избытком раствора меглумина. Тогда твердая фаза необязательно имеет содержание влаги, уменьшенное перед использованием, но может применяться и во влажном состоянии.
Альтернативно, меглуминиевую поглотительную смолу можно генерировать in situ путем добавления протонированной формы смолы (полученной промыванием, например, коммерческой Chelex сильной кислотой по методике, аналогичной описанной в Примере 1). Гидроксониевая смола Chelex затем образует соответствующую меглуминиевую форму in situ в комплексообразующей реакционной смеси, содержащей меглумин. В соответствии с этим способом, раствор нужно тщательно контролировать для гарантии, что рН не становится слишком кислым, как в том случае, когда гидроксониевая поглотительная смола первоначально приводится в контакт с содержащим меглумин раствором. Срок хранения смолы chelex, однако, значительно ниже и любую гидроксониевую смолу chelex нужно получать непосредственно перед применением. Меглуминиевая форма смолы chelex является устойчивой и может храниться в течение длительного периода времени.
Такие меглуминовые смолы обладают особым преимуществом при получении меглуминовых солей комплекса металла ряда лантаноидов, состоящим в том, что содержание иона/соли натрия в продукте понижается. Так, противоион поглотительного хелата (ИДА) в коммерческой смоле Chelex® представляет собой натрий, и, следовательно, на каждый захваченный ион гадолиния в реакционную смесь высвобождаются три иона натрия. Чтобы избежать загрязнения натрием, смолу Chelex® можно получить так, чтобы все ионы натрия обменялись на ионы меглуминия. Следовательно, когда ион гадолиния захватывается поглотительной смолой, высвобождаются три иона меглуминия.
После использования, поглотительную смолу, содержащую связанные ионы металла, можно при необходимости регенерировать для последующего повторного использования путем обработки избытком меглумина или другого противоиона. В случае Chelex, стандартные способы регенерации описаны в инструкциях, предоставляемых коммерческими поставщиками. Полное удаление гадолиния следует определять методом ИСП-ОЭС (спектроскопия ионизационно связанной плазмы в тандеме с оптической электронной спектроскопией, ICP-AES) или ИСП-МС (спектроскопия ионизационно связанной плазмы в тандеме с масс-спектроскопией, ICP-MS) элюата со смолы после промываний водным раствором кислоты или методом «капельных анализов», описанным выше.
В пятом аспекте настоящего изобретения предложено применение поглотительной смолы по четвертому аспекту в способе очистки по первому аспекту, в способе получения фармацевтической композиции по второму аспекту или в способе получения контрастного агента для МРТ по третьему аспекту.
Предпочтительные воплощения поглотительной смолы в пятом аспекте описаны в первом аспекте (выше).
Описание чертежей
На Фиг. 1 показано, что ионы гадолиния замещены ионами натрия (Na-Chelex) или ионами меглуминия (Meg-Chelex), а содержание хлорид-ионов не затрагивается в процессе обработки стандартного раствора хлорида гадолиния на смолах Chelex.
На Фиг. 2 показано, что такая же методика удаления гадолиния по изобретению является эффективной в случае смеси Gd-DOTA/избыток гадолиния. На Фиг. 2 также показано, что chelex не способна удалять гадолиний из Gd-DOTA, так как не образуется свободной DOTA.
Изобретение проиллюстрировано с помощью неограничивающих примеров, подробно представленных ниже. Пример 1 обеспечивает получение меглуминовой поглотительной хелаторной смолы по изобретению. Пример 2 демонстрирует, что две разные смолы Chelex успешно удаляют ионы гадолиния из стандартного раствора GdCl3. Показано, что натриевая форма смолы увеличивает содержание натрия в растворе, а меглуминиевая форма смолы увеличивает содержание меглуминия в растворе.
Пример 3 показывает, что две разные Chelex смолы из Примера 2 успешно удаляют ионы гадолиния из композиции, содержащей комплекс Gd-DOTA и избыток свободного гадолиния. Пример 3 также демонстрирует, что смола Chelex не способна удалять Gd3+ из комплекса Gd-DOTA, так как на хроматограмме отсутствует свободная DOTA (Фиг. 2). Zn-DOTA элюируется в момент времени 28,1 минут.
В Примере 4 представлен способ ВЭЖХ-CAD (высокоэффективной жидкостной хроматографии с детектором заряженного аэрозоля (англ. -charged aerosol detector)) способный анализировать Gd-DOTA, свободную DOTA и меглумин в смеси этих компонентов.
В Примере 5 представлен пример получения раствора Gd-DOTA с помощью настоящего изобретения.
Пример 6 демонстрирует, как поглотительная смола может удалять кальций в присутствии DOTA.
Пример 7 демонстрирует добавление DOTA к раствору GdDOTA-меглумин.
В Примере 8 представлено получение меглуминовой поглотительной смолы по изобретению в промышленном масштабе.
Пример 9 демонстрирует способ очистки кальция в промышленном масштабе с помощью меглуминовой поглотительной смолы по изобретению.
Сокращения
BT-DO3A: 10-(2,3-дигидрокси-1-гидроксиметилпропил)-1,4,7,10-тетраазациклододекан-1,4,7-триуксусная кислота;
Циклен: 1,4,7,10-тетраазациклододекан;
DO3A: 1,4,7,10-тетраазациклододекан-1,4,7-триуксусная кислота;
DOTA: 1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусная кислота;
DTPA: диэтилентриаминпентауксусная кислота;
ЭДТА: этилендиаминтетрауксусная кислота;
GMP: Надлежащая производственная практика;
HP-DO3A: 1,4,7,10-тетраазациклододекан-1,4,7-триуксусная кислота-10-(2-гидроксипропил);
ВЗЖХ: высокоэффективная жидкостная хроматография;
ВЭЖХ-CAD: ВЭЖХ - детектор заряженного аэрозоля;
ICP-AES: индуктивно связанная плазма - атомноэмиссионная спектроскопия
ICP-MS: индуктивно связанная плазма - масс-спектрометрия;
MeCN: Ацетонитрил;
min: минуты;
МРТ: магнитно-резонансная томография;
NOTA: 1,4,7-триазациклононан-1,4,7-триуксусная кислота;
РСТА: 3,6,9,15-тетраазабицикло[9.3.1]пентадека-1,11,13-триен-3,6,9,-триуксусная кислота;
ppm: млн долей (м.д.);
WFI: вода для инъекций.
Пример 1: Получение меглуминовой смолы Chelex® ("Meg-Chelex")
Смолу Chelex-100 (Sigma-Aldrich; 100 г) на фильтре из пористого стекла обрабатывали 4 порциями 1М-ной HCl (1 л) в течение 4 ч. Затем смолу промывали водой до рН элюата 6,5 и приводили раствор меглумина (10 г) в воде (400 мл) в равновесие со смолой в течение периода 1 ч. Смолу снова промывали водой до рН 8 и затем отфильтровывали и сушили в вакууме в течение минуты с получением влажной смолы, которую использовали в такой форме ("Meg-Chelex").
Пример 2: Удаление ионов гадолиния с помощью смолы Chelex®
Стандартный раствор хлорида гадолиния обрабатывали стандартной Chelex (с ионами натрия; "Na-Chelex") или меглуминовой Chelex (Пример 1; "Meg-Chelex"):
К каждой влажной Chelex (Na или меглуминовой) смоле (0,5 г) добавляли 5 мл стандартного раствора GdCl3 (1 мг/мл). Суспензии затем оставляли на вибрационном столике в течение ночи при 30°С. ВЭЖХ-CAD анализ (с помощью способа из Примера 4) суспензий показал, что загрязнения натрием не наблюдали для раствора гадолиния, обработанного Meg-Chelex, а раствор, обработанный Na-Chelex, содержал значительно большую концентрацию иона натрия. Колориметрический количественный анализ с Арсеназо III показал отсутствие в любом растворе свободного гадолиния. Результаты показаны на Фиг. 1.
Пример 3: Удаление ионов гадолиния из композиции Gd-DOTA с помощью смолы Chelex®
Реакционную смесь Gd-DOTA-меглумин (концентрация ~380 мг/мл), содержащую известный избыток свободного гадолиния (160 мкг/мл), обрабатывали стандартной (Na-Chelex) или меглуминовой (Meg-Chelex) Chelex:
К 0,5 г влажной Chelex смолы (Na-Chelex или Meg-Chelex; Пример 1) добавляли аликвоту 5 мл указанной выше смеси Gd-DOTA-меглумин/свободный Gd. Суспензии оставляли на вибрационном столике на ночь при 30°С.
ВЭЖХ-CAD анализ (с помощью способа из Примера 4) полученных суспензий показал отсутствие загрязнения натрием (использовали DOTA, содержащую некоторое количество ионов натрия) в обработанном Meg-Chelex растворе гадолиния, а обработанный Na-Chelex раствор имел увеличенное количество натрия. Колориметрический количественный анализ с Арсеназо III показал отсутствие в любом растворе свободного гадолиния. Концентрация меглумина в обработанной Meg-Chelex реакционной смеси была немного повышена, что является указанием на обмен гадолиния. Результаты показаны на Фиг. 2.
Пример 4: Способ ВЭЖХ-CAD: определение DOTA в растворе GdDOTA-Меглумин
Детектор: ESA Corona, детектор заряженного аэрозоля;
Колонка: SeQuant ZIC-pHILIC (5 мкмоль, 150*4,6 мм).
Приготовление образца: к 20 мкл (примерно 0,5М) реакционной смеси добавляли Zn(OAc)2 (10 мкл, 10 мг/мл), затем воду (270 мкл), а за ней MeCN (700 мкл)*.
Вводимый объем: 20 мкл;
Подвижная фаза: 100 мкмоль ацетата аммония (А), ацетонитрил (В).
Колонку кондиционировали с исходным составом элюента (соотношение А:В 15:85) при скорости потока 1 мл/мин в течение по меньшей мере пяти минут перед введением образца.
Градиент:
При этом кривизна 6 соответствует линейному градиенту.
Наблюдали следующие времена удерживания:
Времена удерживания (мин)
Меглумин 21,3
GdDOTA 23,2
ZnDOTA* 28,1.
* DOTA анализировали опосредованно в виде Zn-DOTA комплекса.
Пример 5: Промышленное получение Gd-DOTA-меглумин
DOTA (211 кг) растворяли в кипящей воде (1600 кг) и добавляли Gd2O3 (94,8 кг). Температуру устанавливали до 70°С и перемешивали суспензию в течение ночи. Присутствие свободных ионов гадолиния (1390 мкг/г) в растворе определяли методом колориметрического титрования.
Температуру регулировали до 50°С и добавляли меглумин до достижения в растворе рН 5,5. Сначала добавляли 94,8 кг меглумина, а потом регулировали рН путем добавления водного раствора меглумина (1,5 М).
Puropack С150 (50 л, предварительно кондиционированного в соответствии с примером 8) засыпали в колонку. Раствор Gd-DOTA прокачивали через колонку со скоростью потока, достаточной для прохождения всего объема раствора в течение 2 часов. Концентрацию свободного гадолиния (45 мкг/мл) определяли методом колориметрического титрования. Ионный обмен в растворе Gd-DOTA продолжали путем осуществления еще одного прохода через колонку для установления уровня свободного гадолиния ниже предела обнаружения для колориметрического титрования (4 мкг/г) с получением раствора Gd-DOTA-меглумин.
Пример 6: Удаление ионов металла с помощью поглотительной смолы, влияние DOTA на эффективность поглощения К 30 мл 0,1М-ного ацетата аммония добавляли глюконат кальция, хлорид гадолиния и хелатирующий агент DOTA в количествах, указанных в таблице ниже. Растворы нагревали при 50°С в течение 24 ч и затем перемешивали с 1 г меглуминированной Chelex (полученной в соответствии с примером 1) при комнатной температуре. Концентрацию кальция и гадолиния определяли методом ИСП-МС до и через 1 ч после добавления меглуминированной chelex.
Результаты показывают, что chelex не способна удалять кальций в присутствии DOTA (опыты 1 и 2) из-за образования устойчивого Ca-DOTA комплекса. Результаты также показывают, что добавление гадолиния (опыты 2-4) способствует удалению кальция из-за переметаллирования Ca-DOTA и последующего образования Gd-DOTA комплекса и ионов свободного кальция. Смола chelex будет поглощать все полученные в результате переметаллирования ионы кальция и оставлять все ионы, связанные в комплекс с DOTA, в растворе (добавляли стехиометрическое количество гадолиния и оставшаяся DOTA будет связывать в комплекс кальций: 11-7,5 = 3,5 мкмоль; 3,5/7,5*10 = 5 млн долей (ppm)).
Пример 7: добавление DOTA в раствор Gd-DOTA-меглумин Концентрацию GdDOTA (полученную, как в примере 5) определяли методом ИК спектроскопии и при одновременном определении массы раствора определяли общее количество GdDOTA - 269,8 кг. Затем добавляли свободную DOTA (2,79 литра раствора с концентрацией 101,1 г/мл; всего 307,6 г).
Затем небольшими порциями добавляли раствор меглумина (1 М) до получения рН 7,2. Массу уменьшали до 630 кг путем отгонки in vacuo (140°С). Раствор выдерживали при 40°С в течение 10 ч. Концентрацию GdDOTA определяли до 1,06М, и количество свободной DOTA определяли до 537 мкг/мл.
Пример 8: Получение меглуминированной смолы Puropack С150® ("Meg-PPC").
Смолу Puropack С150 кондиционировали с получением протонной формы в соответствии со стандартной методикой. Смолу промывали водой до появления нейтрального элюата со слоя смолы.
Раствор меглумина (400 г/кг смолы) циклически пропускали через слой смолы в течение 10 ч и смолу снова промывали водой до нейтрального рН.
Пример 9: способ удаления кальция
Кальций-содержащую DOTA (1,6 мкг Са/г DOTA по данным ИСП-МС анализа) использовали при производстве раствора Gd-DOTA-меглумин (как описано в примере 5). К раствору Gd-DOTA-меглумин затем добавляли DOTA (как описано в примере 7) с получением фармацевтической композиции. Проводили определение концентрации кальция с помощью ИСП-МС и устанавливали, что она ниже предела обнаружения (<0,1 млн долей (ppm)). Предполагаемая концентрация кальция (при условии, что в процессе производства не применяли способ очистки) составляла 0,6 млн долей (ppm).
Claims (31)
1. Способ очистки для удаления примесей ионов металлов из комплекса металла ряда лантаноидов, состоящего из металла ряда лантаноидов с макроциклическим хелатором из класса аминокарбоновых кислот, где указанный способ включает следующие стадии:
(i) комплексообразование указанного хелатора, содержащего указанную примесь металла M, с избытком указанного металла ряда лантаноидов в подходящем растворителе с образованием первого раствора указанного комплекса металла ряда лантаноидов, содержащего избыток ионов лантаноида и M;
(ii) удаление избытка ионов лантаноида и M из первого раствора со стадии (i) путем приведения указанного раствора один или более раз в контакт с поглотительной смолой в форме фармацевтически приемлемой катионной органической соли, при этом избыток лантаноида и M связываются в комплексы на указанной смоле;
(iii) отделение твердофазной смолы от первого раствора со стадии (ii) с получением второго раствора, который содержит указанный комплекс металла ряда лантаноидов, свободный от избытка лантаноида и M;
где M - ион металла, выбранный из кальция, магния и цинка или их смесей;
причем указанный второй раствор содержит менее 10 млн долей (ppm) M.
2. Способ по п. 1, в котором избыток металла ряда лантаноидов на стадии (i) составляет от 0,001 до 5 мол. %.
3. Способ по п. 1 или 2, в котором металл ряда лантаноидов представляет собой гадолиний.
4. Способ по любому из пп. 1-3, в котором макроциклический хелатор включает DOTA, NOTA, DO3A, BT-DO3A, HP-DO3A и PCTA.
5. Способ по п. 4, в котором макроциклический хелатор включает DOTA.
6. Способ по любому из пп. 1-5, в котором поглотительная смола содержит поглотительный хелатор.
7. Способ по п. 6, в котором поглотительный хелатор включает ЭДТА, DTPA или ИДА.
8. Способ по любому из пп. 1-7, в котором металл ряда лантаноидов представляет собой гадолиний, а макроциклический хелатор включает DOTA.
9. Способ по п. 8, в котором комплекс гадолиний-DOTA включает меглуминовую соль гадолиния-DOTA.
10. Способ по п. 9, в котором фармацевтически приемлемая катионная органическая соль представляет собой меглуминовую соль.
11. Способ по любому из пп. 1-10, в котором комплексообразование на стадии (i) завершается путем доведения pH до 4,5-5,5 с помощью меглумина.
12. Способ получения жидкой фармацевтической композиции, содержащей комплекс металла, состоящего из металла ряда лантаноидов с макроциклическим хелатором, вместе с указанным хелатором в не связанной в комплекс форме в количестве, находящемся в интервале от 0,002 до 0,4 мол. % от указанного комплекса металла, где указанный способ включает следующие стадии:
(A) проведение способа по любому из пп. 1-11 с получением указанного в них второго раствора;
(B) добавление макроциклического хелатора, указанного в п. 1, в не связанной в комплекс форме в количестве, составляющем от 0,002 до 0,4 мол. %, в указанный второй раствор со стадии (A) с получением указанной жидкой фармацевтической композиции;
где указанная композиция содержит менее 10 млн долей (ppm) M, где M, поглотительная смола и макроциклический хелатор такие же, как указано в п. 1.
13. Способ по п. 12, в котором хелатор в не связанной в комплекс форме находится в количестве, составляющем от 0,025 до 0,25 мол. %.
14. Способ по п. 12 или 13, в котором хелатор в не связанной в комплекс форме свободен от ионов координированного металла ряда лантаноидов и содержит менее 50 млн долей (ppm) M.
15. Способ получения контрастного агента для МРТ, включающий следующие стадии:
(a) проведение способа по любому из пп. 12-14 с получением указанной в них жидкой фармацевтической композиции;
(b) необязательно разбавление жидкой фармацевтической композиции со стадии (a) биосовместимым носителем;
(c) дозирование композиции со стадии (b) в фармацевтически приемлемые контейнеры или шприцы с получением дозированных контейнеров или шприцев;
(d) проведение стадий (a)-(c) в условиях асептического производства или терминальная стерилизация дозированных контейнеров или шприцев со стадии (c) с получением контрастного агента для МРТ в указанных фармацевтически приемлемых контейнерах или шприцах в форме, приемлемой для введения млекопитающему;
где указанный контрастный агент содержит менее 10 млн долей (ppm) M, где M, поглотительная смола и макроциклический хелатор такие же, как указано в п. 1.
16. Способ по п. 15, в котором применяют терминальную стерилизацию.
17. Поглотительная смола для применения в способе по п. 1, которая содержит катионообменную смолу, в которой анионная функциональная группа указанной смолы присутствует в виде фармацевтически приемлемой катионной органической соли указанной функциональной группы и в которой поглотительная смола содержит поглотительный хелатор, где поглотительный хелатор включает ЭДТА, DTPA или ИДА.
18. Применение поглотительной смолы по п. 17 в способе очистки по любому из пп. 1-11, в способе получения фармацевтической композиции по любому из пп. 12-14 или в способе получения контрастного агента для МРТ по п. 15 или 16.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1421162.7A GB201421162D0 (en) | 2014-11-28 | 2014-11-28 | Lanthanide complex formulations |
| GB1421162.7 | 2014-11-28 | ||
| PCT/EP2015/077970 WO2016083605A1 (en) | 2014-11-28 | 2015-11-27 | Lanthanide complex formulations |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2017116220A RU2017116220A (ru) | 2018-12-28 |
| RU2017116220A3 RU2017116220A3 (ru) | 2019-02-25 |
| RU2707070C2 true RU2707070C2 (ru) | 2019-11-22 |
Family
ID=52349617
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2017116220A RU2707070C2 (ru) | 2014-11-28 | 2015-11-27 | Композиции, содержащие комплексы металлов ряда лантаноидов |
Country Status (12)
| Country | Link |
|---|---|
| US (4) | US10576169B2 (ru) |
| EP (1) | EP3224250A1 (ru) |
| JP (1) | JP6846347B2 (ru) |
| KR (2) | KR102608019B1 (ru) |
| CN (1) | CN107001293B (ru) |
| AU (1) | AU2015352426B2 (ru) |
| BR (1) | BR112017010889B1 (ru) |
| CA (1) | CA2967877A1 (ru) |
| GB (1) | GB201421162D0 (ru) |
| MX (1) | MX2017006800A (ru) |
| RU (1) | RU2707070C2 (ru) |
| WO (1) | WO2016083605A1 (ru) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201421162D0 (en) | 2014-11-28 | 2015-01-14 | Ge Healthcare As | Lanthanide complex formulations |
| EP3562517A1 (en) * | 2016-12-29 | 2019-11-06 | Inventure, LLC | Solvent-free gadolinium contrast agents |
| US20190269805A1 (en) | 2016-12-29 | 2019-09-05 | Inventure, LLC | Solvent-free gadolinium contrast agents |
| US11654424B1 (en) * | 2019-06-10 | 2023-05-23 | Triad National Security, Llc | Method embodiments for making lanthanide metal complexes from lanthanide metal oxides and separating the same from heavy lanthanide metal oxides, actinide oxides, and non-lanthanide rare earth element oxides |
| GB201919073D0 (en) * | 2019-12-20 | 2020-02-05 | Ge Healthcare As | Novel manufacturing process |
| CN113527222B (zh) * | 2020-04-21 | 2023-06-13 | 威智医药股份有限公司 | 一种钆特酸葡甲胺的制备方法 |
| CN113801071B (zh) * | 2021-09-14 | 2023-04-07 | 安徽普利药业有限公司 | 一种钆特酸葡甲胺的精制方法 |
| WO2024129747A1 (en) * | 2022-12-12 | 2024-06-20 | Inventure Llc | Metastable-free lanthanide based contrast agents and method |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4028234A (en) * | 1974-06-06 | 1977-06-07 | Aerojet-General Corporation | Buffering agents |
| US4647447A (en) * | 1981-07-24 | 1987-03-03 | Schering Aktiengesellschaft | Diagnostic media |
| US5435990A (en) * | 1988-06-24 | 1995-07-25 | The Dow Chemical Company | Macrocyclic congugates and their use as diagnostic and therapeutic agents |
| WO1995032741A1 (en) * | 1994-05-26 | 1995-12-07 | Bracco S.P.A. | Bile acid conjugates, derivatives thereof with metal complexes and related uses |
| WO1997026065A1 (en) * | 1996-01-16 | 1997-07-24 | Culligan International Company | Processes for deionization and demineralization of fluids |
| EA001387B1 (ru) * | 1997-12-10 | 2001-02-26 | Гербе | Хелатные соединения металлов с макроциклическими полиаминокарбоновыми соединениями и их использование для диагностических исследований |
| WO2008144728A1 (en) * | 2007-05-21 | 2008-11-27 | Bracco Imaging S.P.A. | Conjugates which bind a blood protein such as human serum albumin and methods of using the same in diagnostic and therapeutic applications |
| WO2009103744A2 (en) * | 2008-02-19 | 2009-08-27 | Guerbet | Process for preparing a pharmaceutical formulation of contrast agents |
| RU2533833C2 (ru) * | 2009-12-16 | 2014-11-20 | Бракко Имэджинг Спа | Способ получения хелатных соединений |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3640708C2 (de) | 1986-11-28 | 1995-05-18 | Schering Ag | Verbesserte metallhaltige Pharmazeutika |
| IT1292128B1 (it) | 1997-06-11 | 1999-01-25 | Bracco Spa | Processo per la preparazione di chelanti macrociclici e loro chelati con ioni metallici paramagnetici |
| US20040167330A1 (en) | 2001-07-17 | 2004-08-26 | Ivan Lukes | Novel chelating agents and conjugates thereof, their synthesis and use as diagnois and therapeutic agents |
| FR2945448B1 (fr) | 2009-05-13 | 2012-08-31 | Guerbet Sa | Procede de preparation d'une formulation pharmaceutique de chelate de lanthanide sous forme de poudre. |
| CN104955822B (zh) | 2013-01-28 | 2018-03-13 | T2医药有限责任公司 | 制备1,4,7,10‑四氮杂环十二烷‑1,4,7,10‑四乙酸及其络合物的方法 |
| EP2786768A1 (en) | 2013-04-04 | 2014-10-08 | Agfa Healthcare | Process for preparing a material comprising a macrocyclic ligand and for producing a pharmaceutical formulation comprising said ligand with a lanthanide |
| GB201421162D0 (en) | 2014-11-28 | 2015-01-14 | Ge Healthcare As | Lanthanide complex formulations |
-
2014
- 2014-11-28 GB GBGB1421162.7A patent/GB201421162D0/en not_active Ceased
-
2015
- 2015-11-27 MX MX2017006800A patent/MX2017006800A/es unknown
- 2015-11-27 WO PCT/EP2015/077970 patent/WO2016083605A1/en active Application Filing
- 2015-11-27 AU AU2015352426A patent/AU2015352426B2/en active Active
- 2015-11-27 CN CN201580064643.5A patent/CN107001293B/zh active Active
- 2015-11-27 BR BR112017010889-5A patent/BR112017010889B1/pt active IP Right Grant
- 2015-11-27 US US15/531,431 patent/US10576169B2/en active Active
- 2015-11-27 JP JP2017526514A patent/JP6846347B2/ja active Active
- 2015-11-27 RU RU2017116220A patent/RU2707070C2/ru active
- 2015-11-27 EP EP15804098.0A patent/EP3224250A1/en active Pending
- 2015-11-27 KR KR1020237028434A patent/KR102608019B1/ko active IP Right Grant
- 2015-11-27 KR KR1020177014038A patent/KR20170092546A/ko not_active IP Right Cessation
- 2015-11-27 CA CA2967877A patent/CA2967877A1/en active Pending
-
2020
- 2020-01-24 US US16/752,307 patent/US11400172B2/en active Active
-
2022
- 2022-06-28 US US17/851,454 patent/US12070511B2/en active Active
-
2024
- 2024-07-11 US US18/770,289 patent/US20240358864A1/en active Pending
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4028234A (en) * | 1974-06-06 | 1977-06-07 | Aerojet-General Corporation | Buffering agents |
| US4647447A (en) * | 1981-07-24 | 1987-03-03 | Schering Aktiengesellschaft | Diagnostic media |
| US5435990A (en) * | 1988-06-24 | 1995-07-25 | The Dow Chemical Company | Macrocyclic congugates and their use as diagnostic and therapeutic agents |
| WO1995032741A1 (en) * | 1994-05-26 | 1995-12-07 | Bracco S.P.A. | Bile acid conjugates, derivatives thereof with metal complexes and related uses |
| WO1997026065A1 (en) * | 1996-01-16 | 1997-07-24 | Culligan International Company | Processes for deionization and demineralization of fluids |
| EA001387B1 (ru) * | 1997-12-10 | 2001-02-26 | Гербе | Хелатные соединения металлов с макроциклическими полиаминокарбоновыми соединениями и их использование для диагностических исследований |
| WO2008144728A1 (en) * | 2007-05-21 | 2008-11-27 | Bracco Imaging S.P.A. | Conjugates which bind a blood protein such as human serum albumin and methods of using the same in diagnostic and therapeutic applications |
| WO2009103744A2 (en) * | 2008-02-19 | 2009-08-27 | Guerbet | Process for preparing a pharmaceutical formulation of contrast agents |
| RU2533833C2 (ru) * | 2009-12-16 | 2014-11-20 | Бракко Имэджинг Спа | Способ получения хелатных соединений |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20230125860A (ko) | 2023-08-29 |
| KR20170092546A (ko) | 2017-08-11 |
| US12070511B2 (en) | 2024-08-27 |
| CN107001293B (zh) | 2023-09-19 |
| WO2016083605A1 (en) | 2016-06-02 |
| US10576169B2 (en) | 2020-03-03 |
| US11400172B2 (en) | 2022-08-02 |
| US20220354971A1 (en) | 2022-11-10 |
| US20170258945A1 (en) | 2017-09-14 |
| BR112017010889A2 (pt) | 2018-02-14 |
| BR112017010889B1 (pt) | 2022-02-22 |
| CA2967877A1 (en) | 2016-06-02 |
| CN107001293A (zh) | 2017-08-01 |
| US20200155712A1 (en) | 2020-05-21 |
| RU2017116220A (ru) | 2018-12-28 |
| AU2015352426A1 (en) | 2017-05-25 |
| RU2017116220A3 (ru) | 2019-02-25 |
| US20240358864A1 (en) | 2024-10-31 |
| EP3224250A1 (en) | 2017-10-04 |
| JP6846347B2 (ja) | 2021-03-24 |
| KR102608019B1 (ko) | 2023-11-30 |
| MX2017006800A (es) | 2017-09-08 |
| AU2015352426B2 (en) | 2020-03-05 |
| JP2017535553A (ja) | 2017-11-30 |
| GB201421162D0 (en) | 2015-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2707070C2 (ru) | Композиции, содержащие комплексы металлов ряда лантаноидов | |
| RU2710360C2 (ru) | Составы металлических комплексов | |
| JP6655617B2 (ja) | Gd−DOTA金属錯体のメグルミン塩を含む製剤 | |
| US20240366803A1 (en) | Lanthanide complex formulations |