RU2497549C2 - Полимерный материал - Google Patents
Полимерный материал Download PDFInfo
- Publication number
- RU2497549C2 RU2497549C2 RU2011113666/15A RU2011113666A RU2497549C2 RU 2497549 C2 RU2497549 C2 RU 2497549C2 RU 2011113666/15 A RU2011113666/15 A RU 2011113666/15A RU 2011113666 A RU2011113666 A RU 2011113666A RU 2497549 C2 RU2497549 C2 RU 2497549C2
- Authority
- RU
- Russia
- Prior art keywords
- sensitive layer
- sensitive
- solubility
- polymer
- layer
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L29/00—Materials for catheters, medical tubing, cannulae, or endoscopes or for coating catheters
- A61L29/08—Materials for coatings
- A61L29/085—Macromolecular materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L29/00—Materials for catheters, medical tubing, cannulae, or endoscopes or for coating catheters
- A61L29/14—Materials characterised by their function or physical properties, e.g. lubricating compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/08—Materials for coatings
- A61L31/10—Macromolecular materials
Landscapes
- Health & Medical Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Surgery (AREA)
- Heart & Thoracic Surgery (AREA)
- Vascular Medicine (AREA)
- Materials For Medical Uses (AREA)
- Medicinal Preparation (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Dental Preparations (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Polymers With Sulfur, Phosphorus Or Metals In The Main Chain (AREA)
Abstract
Изобретение относится к медицине. Описано устройство, содержащее корпусную структуру, имеющую одну или более поверхностей, где, по меньшей мере, одна из поверхностей включает чувствительный к pH слой, содержащий линейный полимер, где растворимость линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH. Описан также способ формирования устройства и способ профилактики или облегчения инфекции. Устройство устойчиво к инфекциям и позволяет модулировать эффективность чувствительного к pH слоя, при этом можно снижать степень растворимости или эрозии чувствительного к pH слоя в зависимости от состояния пациента. 5 н. и 25 з.п. ф-лы, 20 ил., 8 пр.
Description
Область, к которой относится изобретение
Изобретение относится прежде всего к области медицинских устройств. Конкретнее, изобретение относится к медицинским устройствам, включающим чувствительные к pH разлагаемые слои, к способам изготовления медицинских устройств, содержащих чувствительные к pH разлагаемые слои, и к способам применения медицинских устройств, содержащих чувствительные к pH разлагаемые слои.
Предпосылки изобретения
Применение медицинских устройств, вводимых в тело пациента, в настоящее время представляет собой повседневное явление в практике здравоохранения в условиях стационаров и пансионатов. Хотя с применением вводимых в тело медицинских устройств, таких как, например, катетеры и стенты, связаны существенные благоприятные эффекты, имеется ряд очень беспокоящих опасных осложнений, которые могут привести к увеличению времени, в течение которого пациенты остаются в стационаре, и, что важнее, к увеличению числа случаев смерти пациентов, связанных с применением указанных устройств. Эти осложнения возникают главным образом вследствие типа реакции организма пациента на введение медицинского устройства, которое воспринимается организмом как инородный объект. Следовательно, у пациентов часто развивается инфекция, связанная с введением медицинского устройства, и это рассматривается как одно из самых решающих недостатков в остальном высокоэффективного и благоприятного медицинского лечения. Существует настоятельная потребность в снижении частоты инфекции, которая часто указывается как связанная с устройством.
Обычно связанная с устройством инфекция начинается с бактериальной адгезии, развивающейся с образованием биологической пленки. Бактерии и возбудители, обычно заселяющие катетеры, продуцируют уреазу, которая разлагает мочевину в моче с образованием диоксида углерода и аммиака. При увеличении pH, связанном с таким разложением, минералы в моче осаждаются, приводя к покрытию осаждаемым налетом.
Покрытие катетеров осаждаемым налетом может вызвать блокаду катетера, ведущую к увеличению частоты, с которой катетер должен удаляться и замещаться. Образование осаждаемого налета также приводит к увеличению боли при удалении катетера. Также гораздо вероятнее инфицирование ткани, окружающей катетер. Это особенно проблематично для пациентов, требующих длительной катетеризации. Тяжелые последствия включают септицемию, пиелонефрит и шок.
Кроме того, ассоциированные патогены внутри биомассы могут сократить период использования медицинского устройства посредством экспрессии активных изоферментов уреазы, которые действуют с ощелачиванием мочи через превращение мочевины в аммиак и диоксид углерода.
Предыдущие подходы для преодоления указанной проблемы составляют включение антибиотиков в устройство для борьбы с инфекцией. После введения терапевтические средства могут высвобождаться диффузией и, в конечном счете, находиться местно в биологической жидкости, прилегающей к устройству, таким образом предотвращая бактериальную адгезию. Кроме того, предпринимались попытки модифицировать поверхности устройств для снижения восприимчивости к инфекции.
Несмотря на попытки облегчения осложнений, которые препятствуют применению устройств, вводимых в мочевыводящую систему, все еще остается множество проблем. Поэтому, хотя обработки антибиотиками и новые покрытия поверхности могут обеспечить временное решение, единственным реальным окончательным решением проблем, связанных с катетеризацией мочевыводящих путей и стентированием мочевыводящих путей, является удаление устройства.
Известны медицинские устройства, такие как катетеры, покрытые смазывающими агентами. Также известны смазывающие агенты, содержащие поперечно-сшитые гидрогели, включающие функциональные группы карбоновых кислот.
В патенте США № 6306422 описано устройство, в частности мочевой катетер, покрытый поперечно-сшитым полимерным гидрогелем. При пусковом значении pH полимер набухает посредством абсорбции воды. Эта абсорбция воды увеличивает размер пор гидрогеля, усиливая высвобождение активного вещества в режиме длительного высвобождения. Полимерный гидрогель по патенту США № 6306422 остается нерастворимым в воде и остается в виде покрытия на устройстве. Активное вещество обычно представляет собой один или более из антибиотика и ингибитора уреазы. Высвобождение этих активных веществ может регулировать рост бактерий на поверхности и соответственно регулировать образование осаждаемого налета. Однако высвобождение ингибитора уреазы не устраняет какой-либо осаждаемый налет, который уже образовался в катетере. Кроме того, активные вещества, высвобождаемые из устройств, описанных в патенте США № 6306422, не смогли бы проникнуть через биологическую пленку, образованную бактериями, для устранения существующей бактериальной колонизации.
Краткое описание сущности изобретения
Заявители разработали устройство, которому присуща устойчивость к инфекции посредством использования щадящих реакций in vivo и, предпочтительно, импрегнацией антибиотиками. В частности, поверхность устройства содержит отделяемые биологические материалы, которые могут выделяться в ответ на изменения pH, в качестве альтернативы материалам, используемым в настоящее время.
В соответствии с первым аспектом настоящего изобретения предоставляется устройство, содержащее корпусную структуру, имеющую одну или более поверхностей, содержащих, по меньшей мере, один чувствительный к pH биологически разлагаемый слой, где указанный, по меньшей мере, один чувствительный к pH биологически разлагаемый слой содержит чувствительный к pH полимер, где чувствительный к pH биологически разлагаемый слой способен контролировать разложение при определенном pH. В определенных вариантах осуществления устройство может содержать множество разлагаемых слоев.
В соответствии с настоящим изобретением предоставляется устройство, содержащее корпусную структуру, имеющую одну или более поверхностей, где, по меньшей мере, одна из поверхностей содержит чувствительный к pH слой, содержащий линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
В вариантах осуществления устройство может подходящим образом представлять собой устройство, где pH жидкости, например биологической жидкости, окружающей устройство, увеличивается или уменьшается относительно определенной величины, например, где pH может увеличиваться или уменьшаться относительно физиологического pH в ответ на инфекцию.
При пусковом значении pH линейный полимер ионизируется, и это вызывает увеличение растворимости полимера в воде. Затем ионизированный линейный полимер растворяется в водную среду, окружающую устройство, и выявляется новая поверхность устройства. Новая поверхность не имеет никаких бактерий, расселяющихся по ней, и не подвергается образованию осаждаемого налета. Таким образом, устройство по настоящему изобретению может оставаться имплантированным в течение продолжительных периодов времени, по сравнению с предшествующими устройствами. Риск инфекции и образования осаждаемого налета также снижается, поскольку поверхность устройства по настоящему изобретению отслаивается после колонизации бактериями до какой-либо значимой степени, и обнажается новая поверхность.
Устройство по настоящему изобретению может обычно представлять собой катетер мочевыводящих путей или стент мочевыводящих путей. Бактерии, которые обычно колонизируют такие устройства, высвобождают уреазу. Моча разлагается на аммиак и диоксид углерода после контакта с уреазой, существенно увеличивая pH области, окружающей катетер. Это увеличение pH вызывает осаждение минералов из мочи, вызывая образование осаждаемого налета на катетере. Увеличение pH, генерируемое посредством продукции аммиака, запускает ионизацию линейного полимера по настоящему изобретению, и, соответственно, увеличивается растворимость полимера в воде. Линейный полимер растворяется в окружающей водной среде, и любой осаждаемый налет на наружной поверхности устройства удаляется линейным полимером. Обнажается новая поверхность устройства. Новая поверхность лишена бактерий и осаждаемого налета.
Альтернативно, устройство по настоящему изобретению может быть представлено в форме зубных шин или зубных протезов. После бактериальной колонизации таких устройств pH окружающей среды уменьшается до уровня, ниже физиологического pH. Поскольку бактерии в ротовой полости продуцируют кислоту, то чем больше степень бактериальной колонизации, тем больше количество продуцируемой кислоты, снижающей pH окружающей среды.
Линейный полимер по настоящему изобретению может быть способен к изменению от обеспечения устойчивого слоя в слой, который подвергается контролируемой эрозии или растворению по мере того, как pH окружающей среды сдвигается от физиологического уровня pH, где физиологическиое значение pH составляет обычно 6,2. Подходящим образом, такая эрозия или растворение происходит в направлении конечных точек в диапазоне от pH 5,5 до pH 7. В вариантах осуществления чувствительный к pH полимер может быть способен контролировать разложение или эрозию при pH, указывающем на инфекцию, причем уровень pH сдвигается от физиологического значения pH, например, pH 7,0.
Пусковое значение pH зависит от предполагаемой среды, окружающей устройство по настоящему изобретению. Когда устройство предназначено для имплантации в нейтральную или щелочную среду, такую как мочевой пузырь, то пусковое значение pH составляет обычно выше 6,5; подходящим образом, выше 7; еще более подходяще 7,2. Когда устройство предназначено для имплантации в кислотную среду, такую как желудок, то пусковое значение pH обычно составляет менее чем 6,0; подходящим образом, менее чем 5,5.
Когда pH области, окружающей устройство по настоящему изобретению, сдвигается в сторону от пускового значения pH и в направлении к физиологическому значению pH, то растворимость в воде чувствительного к pH слоя может соответственно уменьшаться и сдвигаться в сторону первого уровня растворимости в воде. По существу, скорость растворения или эрозии чувствительного к pH слоя может уменьшаться. В соответствии с одним вариантом осуществления чувствительный к pH слой растворяется или эродирует, только когда устройство колонизируется бактериями. Растворение или эрозия чувствительного к pH слоя может начинаться и останавливаться в зависимости от колонизации устройства.
Подходящим образом, такой чувствительный к pH слой может обеспечить первую скорость высвобождения функциональных эксципиентов при физиологическом значении pH (например, pH 6,2) и вторую скорость при нефизиологическом значении pH (например, pH 7,0). В целом, первая скорость ниже, чем вторая скорость. В вариантах осуществления, где отслаивание чувствительного к pH слоя минимально при физиологическом значении pH и увеличивается при pH, удаляющемся от физиологического значения pH, элюирование функциональных эксципиентов может коррелироваться с эрозией или растворением чувствительного к pH слоя. Это может иметь преимущества, поскольку инфекция может сдвигать pH в сторону от физиологических величин и, таким образом, высвобождение функциональных эксципиентов может коррелироваться с инфекцией.
Подходящим образом, в предпочтительных вариантах осуществления линейный полимер является биологически совместимым. «Биологически совместимый» материал представляет собой материал, который совместим с живой тканью или живой системой, являясь нетоксичным или не повреждающим. В определенных вариантах осуществления устройство может содержать материал, который образует биологически устойчивые слои. «Биологически не рассасываемый» или «биологически устойчивый» материал относится к материалу, такому как полимер или сополимер, который остается в теле без существенной биологической абсорбции. Такие слои могут быть включены в устройство по настоящему изобретению с получением структурной подложки для устройства.
Соответственно, в вариантах осуществления линейный полимер подвергается структурным изменениям в отношении изменений pH, в частности, линейный полимер может стать ионизированным при изменениях pH, вызывая увеличение растворимости в воде линейного полимера.
Полимеры для использования в устройстве пои настоящему изобретению являются в целом линейными, а не поперечно-сшитыми. Линейный полимер по настоящему изобретению становится ионизированным при пусковом значении pH, вызывая значительное увеличение растворимости в воде линейного полимера. Напротив, поперечно-сшитые полимеры ионизируются при пусковом значении pH, вызывая абсорбцию воды и набухание полимеров. Растворимость в воде поперечно-сшитого полимера не изменяется посредством ионизации, и даже после ионизации поперечно-сшитый полимер удерживается на устройствах, таких как устройства, описанные в патенте США № 6306422. Такие поперечно-сшитые полимеры в целом представлены в форме гидрогелей. Линейные полимеры устройства по настоящему изобретению являются в целом способными подвергаться экструзии.
Обычно чувствительный к pH слой абсорбирует менее чем 30% масс. воды перед ионизацией; в целом, менее чем 20% масс., возможно, менее чем 10% масс. Напротив, поперечно-сшитые гидрогели предшествующего уровня техники для использования в связи с устройствами, такими как устройства, описанные в патенте США № 6306422, абсорбируют воду, масса которой до нескольких тысяч раз превышает их массу в воде перед ионизацией. На растворимость в воде гидрогелей воздействие не оказывается, и эти гидрогели сохраняют свою форму и не растворяются в окружающую водную среду. Хотя полимеры для использования в устройстве по настоящему изобретению могут набухать при абсорбции воды перед ионизацией, это предшествует ионизации, приводя к увеличению растворимости в воде и к растворению.
Когда структурные изменения в линейном полимере предназначены для запуска при pH, по меньшей мере, 6,5, то линейный полимер обычно содержит связи SO и/или одну или более карбоксильных групп и сульфатных групп. Обычно линейный полимер может представлять собой чувствительные к pH полимеры целлюлозы, например, сложные эфиры целлюлозы или простые эфиры целлюлозы. В одном варианте осуществления линейный полимер может представлять собой метакрилатный полимер или полимер, содержащий метакрилат. В соответствии с одним вариантом осуществления полимер имеет следующую структуру:
R=-H
=-CH3
=-COCH3
=-CHCH2CH2COOH
=-CH2CH(OH)CH3
=-CH2CH(OCOCH3)CH3
=-CH2CH(OCOCH2CH2COOH)CH3
В вариантах осуществления по изобретению линейный полимер может быть выбран из метакрилатных полимеров и полимеров целлюлозы. В вариантах осуществления линейный полимер может быть выбран из группы, включающей, например, Eudragit® L100, S100, HPMC-AS, HTMAC-P, и могут использоваться комбинации указанных полимеров. Полимеры, которые могут подходящим образом использоваться для образования чувствительного к pH слоя, могут быть получены, например, от Shin-Etsu, например, Shin-Etsu AQOAT, Degussa или тому подобных.
В вариантах осуществления линейный полимер может представлять собой полимер Eudragit®. Полимеры Eudragit® могут быть предоставлены в виде одной системы или смесей двух различных типов. В вариантах осуществления могут использоваться Eudragit® L100, S100 и комбинации указанных полимеров.
В вариантах осуществления может использоваться Eudragit® L100 для обеспечения слоя, который способен эродироваться при величинах pH, более чем 6.
В вариантах осуществления может использоваться Eudragit® S100 для обеспечения слоя, который способен эродироваться при величинах pH, превышающих 7,0.
Следует понимать, что чувствительные к pH слои могут быть изготовлены с использованием комбинации и L100, и S100 для создания систем, которые медленно эродируются в нормальных условиях мочевой среды, но быстро отслаиваются при более высоких значениях pH. Слои различных чувствительных к pH полимеров, например, слои Eudragit® L100, S100 и комбинации указанных полимеров могут использоваться для образования устройства с тем, чтобы различные слои в устройстве эродировались при различных уровнях pH.
Когда структурные изменения в линейном полимере предназначены для запуска при pH менее чем 6,0, то линейный полимер обычно содержит первичные, вторичные и третичные амины, обычно группы NH2; соответственно, полимер содержит диэтиламиноакрилат, диметиламиноэтилакрилат и/или другие акрилатные мономеры. Подходящим образом, полимер представляет собой полимер, продаваемый под торговой маркой Eudragit® E100.
Как отмечено выше, растворимость в воде линейного полимера устройства по настоящему изобретению увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
Обычно, при pH pKa полимера, ионизируется 50% полимера или более.
В соответствии с одним аспектом настоящего изобретения вторая величина растворимости линейного полимера, по меньшей мере, на 200% больше, чем первая растворимость в воде линейного полимера, в целом, по меньшей мере, на 400% больше, обычно, по меньшей мере, на 600% больше.
Преимущественно, после растворения или эрозии полимерная цепь линейного полимера остается интактной, содержащей такие же мономерные единицы как перед растворением или эрозией.
Устройство по настоящему изобретению может представлять собой любое устройство, в котором изменение pH связано с колонизацией устройства бактериями. В вариантах осуществления настоящего изобретения устройство представляет собой медицинское устройство, например интракорпоральное или экстракорпоральное устройство, включая катетеры, временные или постоянные имплантаты, стенты, трансплантаты, восстановительные устройства и имплантируемые устройства.
Обычно устройство представляет собой катетер, возможно мочевой катетер, уретральный стент, назогастральную трубку, трубку CAPD (для постоянного амбулаторного брюшинного диализа), стент желчных протоков, зубные шины или зубные протезы.
Преимущественно, устройство по настоящему изобретению представляет собой мочевой катетер или стент мочевыводящих путей.
Чувствительный к pH слой может содержать функциональные эксципиенты, подлежащие высвобождению при растворении или эрозии чувствительного к pH слоя. Функциональные эксципиенты могут соответственно представлять собой буферные группы, такие как лимонная кислота, винная кислота, янтарная кислота и фумаровая кислота, противомикробные соединения, левофлоксацин и Налидиксовая кислота, противомикробные соединения, хлоргексидин, повидон-йод, тридосан, ингибиторы уреазы, ЭДТА и пластифицирующие агенты, например, триэтилцитрат и трибутилцитрат или другие стандартные эксципиенты, используемые для облегчения изготовления или усиления их действия.
Обычно функциональные эксципиенты высвобождаются в режиме длительного высвобождения после имплантации устройства. В соответствии с одним вариантом осуществления скорость высвобождения функциональных эксципиентов может резко увеличиваться после эрозии или растворения чувствительного к pH слоя.
Функциональные эксципиенты могут адсорбироваться непосредственно в линейный полимер или могут располагаться внутри устройства или быть иным образом ассоциированы с ним посредством использования одной или нескольких линкерных молекул или других средств присоединения, включая ковалентные, ионные связи и связи ван дер Ваальса. Чувствительный к pH слой и/или поверхность могут быть сконфигурированы так, чтобы происходило контролируемое высвобождение функционального эксципиента, например, функциональный эксципиент элюируется медленно в течение периода времени. Под «контролируемым высвобождением» подразумевается изменение скорости высвобождения терапевтического средства или функционального эксципиента из покрытия медицинского устройства в данной среде. Это может осуществляться с использованием, например, покрытий, обеспечивающих высвобождение в течение времени. В вариантах осуществления устройства по изобретению, обеспечиваются слои, которые приспособлены для одновременного высвобождения терапевтического средства (средств) с двумя или более различными скоростями из различных частей слоя или с двумя различными скоростями, в зависимости от pH среды, окружающей устройство.
В вариантах осуществления устройство может включать слои, которые могут включать слои чувствительного к pH полимера, которые нагружены функциональным эксципиентом, в частности лекарственного средства, например, антибиотика. Альтернативно, в вариантах осуществления медицинское устройство или покрытие медицинского устройства, содержащее чувствительный к pH слой, разлагается контролируемым образом относительно pH, и лекарственное средство может быть связано с линейным полимером. Путем включения лекарственного средства внутрь материала медицинского устройства или материала, покрывающего медицинское устройство, лекарственное средство подается в постепенном режиме, по мере того как разлагается чувствительный к pH полимер.
Соответственно, в вариантах осуществления растворение чувствительного к pH слоя запускает высвобождение антибиотика.
В вариантах осуществления устройство по настоящему изобретению может содержать лекарственное средство, которое минимизирует адгезию к устройству или рост патогена на устройстве, например, антибиотик. Преимущество устройства по настоящему изобретению состоит в том, что оно обеспечивает достижение гораздо более высоких концентраций лекарственного средства в участке инфекции, по сравнению с обычными путями медикаментозной терапии, такими как принимаемые внутрь таблетки.
Высвобождение антибиотика регулирует рост бактерий на поверхности устройства. Однако биологическая пленка в целом образуется после того, как бактерии осуществили колонизацию устройства. Соединения антибиотиков в целом не могут проникнуть через такие биологические пленки и поэтому не очень эффективны при удалении таких бактериальных биологических пленок. Высвобождение ингибитора уреазы действует для регулирования роста осаждаемого налета, но не удаляет уже образовавшийся осевший налет. Поверхность устройства по настоящему изобретению начинает растворяться или эродироваться при пусковом значении pH, и бактериальная колонизация и осевший налет удаляется с поверхностью. Выявляется новая поверхность, лишенная всей бактериальной колонизации и образовавшегося налета.
В сущности, устройство по настоящему изобретению может осуществлять самоочищение после инфекции бактериями, т.е., иными словами, если элюирование лекарственного средства окажется несостоятельным в ингибировании бактериальной адгезии и в последующем приведет к увеличению pH мочи под действием уреазы на мочевину, то слой устройства способен распознавать образование микробной биологической пленки и инициировать контролируемую эрозию (регулируемую включением органических кислот, таких как лимонная кислота) и, таким образом, удалять любые прилипшие массы. При этом поверхность устройства будет очищаться и функциональные агенты (ЭДТА и лимонная кислота), включенные в пленку, будут высвобождаться на поверхность раздела устройство/флюид. Это регулирует pH мочи действием лимонной кислоты и, что очень важно, акцептора ионов металлов Ca2+ и Mg2+. Этот процесс обновит поверхность устройства, возвратит pH к нормальным величинам и «сотрет» ионы металлов. которые склонны к образованию кристаллических отложений на поверхности устройства.
Это обеспечивает возможность устройствам и, в конечном счете, пациентам оставаться лишенными инфекции в течение всего периода предполагаемого использования устройства.
После высвобождения функциональных эксципиентов бактериальная колонизация устройства может быть снижена и pH области, окружающей устройство, может сдвигаться в сторону от пускового значения pH и в направлении к физиологическому значению pH. Растворимость в воде чувствительного к pH слоя может соответственно снижаться по направлению к первой величине растворимости в воде.
Линейный полимер абсорбирует воду при пусковом значении pH, вызывая ионизацию. Скорость ионизации может быть подобрана регулированием скорости абсорбции воды, обычно регулированием плотности чувствительного к pH полимерного слоя. Сниженная плотность линейного полимера в чувствительном к pH слое ведет к сниженной скорости ионизации.
Скорость ионизации зависит от композиции чувствительного к pH слоя, а также от pH области, окружающей устройство.
В соответствии с одним вариантом осуществления чувствительный к pH слой содержит второй или третий гидрофильный полимер. Подходящие гидрофильные полимеры включают полиэтиленоксид, полиакриловые кислоты и/или производные целлюлозы (в частности, линейные производные целлюлозы), такие как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза и поливинилпирролидон. Добавление одного или более гидрофильных полимеров в чувствительный к pH слой обеспечивает физические взаимодействия, такие как взаимодействия ван дер Ваальса.
Альтернативно, чувствительный к pH слой может содержать гидрофобный полимер, в частности, гидрофобный полимер с низкой молекулярной массой. Подходящие гидрофобные полимеры включают полимолочную кислоту, полигликолевую кислоту, полилактид-ко-гликолид и поликапролактон. В целом, гидрофобный полимер по существу равномерно диспергирован в чувствительном к pH слое.
Скорость растворения или эрозии чувствительного к pH слоя зависит от его композиции. Буферные группы могут быть включены в чувствительный к pH слой для снижения скорости растворения или эрозии. Подходящие буферные группы включают лимонную кислоту, винную кислоту, янтарную кислоту, фумаровую кислоту и родственные соединения. Когда степень бактериальной колонизации низкая, то число высвободившихся ионов является низким. Некоторые из этих ионов будут захвачены буферной группой, что приведет к более низкой скорости разложения и увеличению срока службы устройства по настоящему изобретению. Число высвобождаемых ионов будет увеличиваться с увеличением бактериальной колонизации, ведущей к эрозии или растворению чувствительного к pH слоя, независимо от включения буферной группы.
В соответствии с одним аспектом устройство по настоящему изобретению может содержать более чем один чувствительный к pH слой; обычно более чем три чувствительных к pH слоя; более подходяще, пять чувствительных к pH слоев.
Каждый чувствительный к pH слой может иметь одинаковое пусковое значение pH или различное пусковое значение pH.
Каждый чувствительный к pH слой может иметь другую вторую растворимость в воде. Альтернативно, каждый чувствительный к pH слой может иметь одинаковую вторую растворимость в воде.
Каждый чувствительный к pH слой может иметь одинаковую скорость ионизации и одинаковую скорость растворения или эрозии. Альтернативно, различные чувствительные к pH слои могут иметь одинаковые или различные скорости ионизации и/или скорости растворения или эрозии.
В соответствии с одним вариантом осуществления прилегающие чувствительные к pH слои могут иметь одинаковое пусковое значение pH, но различные величины второй растворимости в воде.
Альтернативно, прилегающие чувствительные к pH слои могут иметь различные величины пускового значения pH, но одинаковые величины второй растворимости в воде.
Обычно прилегающие чувствительные к pH слои имеют различные скорости ионизации или различные скорости растворения или эрозии.
В соответствии с одним вариантом осуществления различные чувствительные к pH слои содержат различные функциональные эксципиенты, подлежащие высвобождению после растворения или эрозии чувствительного к pH слоя.
В соответствии с одним вариантом осуществления устройство может содержать смазывающий слой для увеличения легкости его введения и удаления. Обычно смазывающий слой может содержать один или более поперечно-сшитых полимеров.
В целом, устройство включает внутреннюю поверхность и наружную поверхность, причем внутренняя поверхность ограничивает просвет.
Обычно наружная поверхность устройства содержит смазывающий слой. В целом, внутренняя поверхность устройства содержит чувствительный к pH слой.
В целом, устройство содержит, по меньшей мере, один структурный слой, который является по существу не разлагаемым или эродируемым в теле и обеспечивает устройству структурную устойчивость, независимо от pH окружающей среды.
Обычно растворимость в воде структурного слоя остается по существу постоянной при значениях pH от 2 до 10. В целом, растворимость в воде структурного слоя остается по существу постоянной, независимо от pH окружающей среды.
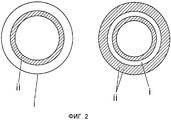
В определенных вариантах осуществления устройство может содержать двухслойную систему, где чувствительный к pH слой, например, слой Eudragit®, обеспечен на внутренней поверхности двухслойной системы. В такой системе жидкость, например биологическая жидкость, такая как моча, может течь через внутренний просвет устройства (Фиг.2а).
В альтернативных вариантах осуществления устройство может содержать трехслойную систему, в которой два чувствительных к pH слоя, например слоя Eudragit®, образуют внутренний и наружный слои устройства. В таких трехслойных системах жидкость, например биологическая жидкость, такая как моча, может течь через внутренний просвет и по наружной поверхности устройства (Фиг.2b).
В еще одних альтернативных вариантах осуществления могут быть предоставлены устройства, содержащие множество чувствительных к pH слоев. В определенных вариантах осуществления может быть предоставлен первый чувствительный к pH слой, прилегающий ко второму чувствительному к pH слою, с тем, чтобы после эрозии первого слоя обнажался второй слой. В вариантах осуществления чувствительные к pH слои могут быть способны к эрозии при различных величинах pH.
Соответственно, в вариантах осуществления внутренний и наружный слои устройства могут быть получены экструзией расплава.
Соответственно, в вариантах осуществления разлагаемый слой может содействовать введению и удалению устройства из тела пациента. В вариантах осуществления, при необходимости, структурный слой, содержащий подходящие полимеры, может быть предоставлен в комбинации с разлагаемым слоем в устройстве.
В соответствии с еще одним аспектом настоящего изобретения предоставляется покрытие для нанесения на устройство, причем устройство содержит корпусную структуру, имеющую одну или более поверхностей, и покрытие приспособлено для нанесения, по меньшей мере, на одну поверхность устройства с тем, чтобы когда поверхность устройства обеспечена, по меньшей мере, одним покрытием, чувствительный к pH слой был предоставлен на устройстве, причем указанный чувствительный к pH слой содержит линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
В определенных вариантах осуществления устройство может содержать покрытие, содержащее множество чувствительных к pH слоев.
Пока нет других указаний, используемый в настоящем описании термин «покрытие» относится в целом к материалу, прикрепленному к устройству. Покрытие может включать материал, покрывающий любую часть медицинского устройства, и он может быть сконфигурирован в виде одного или более слоев покрытия. Покрытие может иметь по существу постоянную или варьирующуюся толщину и композицию. Покрытия могут быть прикреплены к любой части поверхности устройства, например медицинского устройства, включая поверхность просвета, аблюминальную поверхность или любые их части или комбинации.
В целом, под чувствительным к pH слоем подразумевается слой, который может растворяться или эродироваться при определенном pH, например, где полимер может ионизироваться при более высоких уровнях pH с тем, чтобы увеличилась растворимость полимера в воде. Соответственно, после достаточного растворения или эрозии весь слой может быть удален с тем, чтобы обнажился новый слой в устройстве. В целом, после растворения или эрозии чувствительного к pH слоя, полимерная цепь остается интактной с одинаковыми мономерными единицами.
В вариантах осуществления чувствительный к pH слой включает функциональные эксципиенты, такие как лимонная кислота или другие мелкие органические молекулы, и такие функциональные эксципиенты будут высвобождаться после растворения или эрозии чувствительного к pH слоя, в целом, в режиме контролируемого высвобождения.
В соответствии с еще одним аспектом настоящего изобретения, предоставляется способ формирования устройства, включающий стадии обеспечения структурного слоя и нанесения на него, по меньшей мере, одного чувствительного к pH слоя, причем указанный чувствительный к pH слой содержит линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
Обычно структурный слой имеет внутреннюю поверхность и наружную поверхность, причем указанная внутренняя поверхность ограничивает просвет. В целом, чувствительный к pH слой наносится на внутреннюю поверхность структурного слоя. Способ может включать стадию нанесения более чем одного чувствительного к pH слоя.
В целом, устройство представляет собой медицинское устройство, подходящее для введения или имплантации в тело человека или животного.
В определенных вариантах осуществления второго аспекта изобретения способ включает многослойную экструзию.
Соответственно, описанное выше устройство формируется в соответствии со способом по настоящему изобретению.
В соответствии с еще одним аспектом по настоящему изобретению предоставляется способ предотвращения или смягчения инфекции, связанной с устройством, имплантированным или введенным в тело человека или животного, включающий стадию имплантации или введения устройства в тело человека или животного, причем указанное устройство содержит чувствительный к pH слой, содержащий линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
В целом, способ приводит к устранению любой инфекции, которая уже сформировалась.
В целом, способ включает стадию предотвращения или ослабления формирования наслоившегося осажденного налета в устройстве. Обычно способ также включает стадию удаления уже сформировавшегося наслоившегося осажденного налета.
Обычно время, на которое устройство имплантируется или вводится в тело человека или животного без связанной с этим инфекции, составляет, по меньшей мере, 1 день, в целом, по меньшей мере, 3 дня, возможно 7 дней или более.
В соответствии с одним вариантом осуществления время имплантации или введения может быть увеличено, по меньшей мере, на 100%, по сравнению с эквивалентными устройствами, которые не включают, по меньшей мере, один чувствительный к pH слой. В целом, время введения или имплантации может быть увеличено, по меньшей мере, на 150%, обычно, по меньшей мере, на 200%.
В соответствии с одним вариантом осуществления имплантированное устройство представляет собой описанное выше.
Обычно способ по настоящему изобретению предотвращает или облегчает инфекцию, связанную с введением или имплантацией катетера, в частности мочевого катетера, стента, в частности уретрального стента или стента желчных протоков, имплантируемой или вводимой трубки, в частности, назогастральной трубки или трубки CAPD, зубных шин или зубных протезов.
В соответствии с еще одним аспектом настоящего изобретения предоставляется способ предотвращения или облегчения инфекции, связанной с устройством, имплантированным или введенным в тело человека или животного, включающий стадии нанесения, по меньшей мере, одного чувствительного к pH слоя на устройство, причем указанный чувствительный к pH слой содержит линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
Обычно устройство, содержащее чувствительный к pH слой, представляет собой описанное выше.
В соответствии с еще одним аспектом настоящего изобретения предоставляется устройство для применения при лечении, причем указанное устройство содержит, по меньшей мере, один чувствительный к pH слой, содержащий линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
Обычно устройство представляет собой описанное выше.
В целом, лечение предотвращает или облегчает инфекцию, связанную с введением или имплантацией устройства в тело человека или животного.
В соответствии с еще одним аспектом настоящего изобретения предоставляется устройство для применения при лечении, причем указанное устройство содержит чувствительный к pH слой, содержащий линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
Устройство представляет собой в целом описанное выше.
В соответствии с еще одним аспектом настоящего изобретения предоставляется применение устройства для профилактики или облегчения инфекции, причем указанное устройство содержит, по меньшей мере, один чувствительный к pH слой, содержащий линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
Устройство представляет собой в целом описанное выше.
В соответствии с еще одним аспектом настоящего изобретения предоставляется применение устройства при получении лекарственного средства для профилактики или облегчения инфекции, причем указанное устройство содержит, по меньшей мере, один чувствительный к pH слой, содержащий линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
Устройство представляет собой в целом описанное выше.
В соответствии с еще одним аспектом настоящего изобретения предоставляется чувствительный к pH полимер, где указанный полимер проявляет вариабельный профиль элюирования лекарственного средства в диапазоне pH от pH 5 до pH 7,8, предпочтительнее, в диапазоне pH от pH 6 до pH 7,2, или, альтернативно, в диапазоне pH от 5 до 6, предпочтительно, от 5,5 до 6. Чувствительный к pH полимер является в целом линейным.
Под вариабельным профилем элирования лекарственного средства подразумевается, что лекарственное средство элюируется из полимера с первой скоростью на первом конце данного диапазона pH и второй другой скоростью на втором противоположном конце данного диапазона pH. Поскольку чувствительный к pH полимер подвергается разложению, например становится более растворимым при данном pH, например при pH, удаленном от физиологического pH, может произойти высвобождение лекарственного средства. Чем больше разложение, например при более крайних величинах pH, удаленных от физиологического pH, тем больше высвобождение лекарственного средства.
В соответствии с еще одним аспектом настоящего изобретения предоставляется чувствительный к pH полимер, где указанный полимер имеет изменение структурной целостности в диапазоне pH от pH 5 до pH 7,8, предпочтительнее, в диапазоне pH от pH 6 до pH 7,2, или, альтернативно, в диапазоне pH от 5 до 6, предпочтительно, от 5,5 до 6. Чувствительный к pH полимер является в целом линейным.
Под изменением структурной целостности подразумевается, что полимер способен образовывать листки или слои полимера примерно на одном конце диапазона pH, но разлагается и не способен образовывать листки или слои полимера на противоположном конце диапазона pH.
В соответствии с еще одним аспектом настоящего изобретения предоставляются способы применения для лечения пациентов одним или более медицинскими устройствами, описанными в настоящей заявке, которые включают, например, способ терапевтического лечения пациента, включающий обеспечение контакта тела пациента с медицинским устройством, содержащим корпусную структуру, имеющую одну или более поверхностей, содержащих один чувствительный к pH слой, где, по меньшей мере, один чувствительный к pH слой содержит линейный полимер, где растворимость в воде линейного полимера от первой растворимости в воде до второй растворимости в воде при пусковом значении pH. Описаны способы введения лекарственного соединения в тело пациента, которые включают, например, предоставление элюирующего лекарственное средство устройства по настоящему изобретению.
В другом родственном варианте осуществления раскрыт способ введения пациенту композиции, который включает предоставление элюирующего композицию устройства и введение элюирующего композицию устройства в тело пациента, где элюирующее композицию устройство содержит корпусную структуру, имеющую одну или более поверхностей, содержащих, по меньшей мере, один чувствительный к pH слой, где, по меньшей мере, один чувствительный к pH слой содержит линейный полимер, где растворимость в воде линейного полимера увеличивается от первой растворимости в воде до второй растворимости в воде при пусковом значении pH.
По всему описанию, пока контекст не требует иного, термины «содержать» или такие варианты как «содержит» или «содержащий», «включает» или «включающий» следует понимать как подразумевающие включение указанного целого числа или группы целых чисел, но не исключение любого другого целого числа или группы целых чисел.
Предпочтительные признаки и варианты осуществления каждого аспекта изобретения представлены как для каждого из других аспектов, пока контекст не требует изменения того, что подлежит изменению.
Теперь варианты осуществления настоящего изобретения будут описаны только в качестве примера со ссылкой на сопровождающие чертежи, на которых
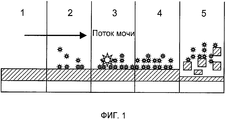
Фиг.1 иллюстрирует стадии бактериальной колонизации катетера по настоящему изобретению, где колонизирующие бактерии, иллюстрируемые обозначением *, начинают колонизировать устройство после введения (1), так что поверхность становится колонизированной (2), и образуется микробная биологическая пленка (3), pH мочи увеличивается расщепляющими мочевину бактериями (4), и эрозия Eudragit® происходит при повышенном pH, приводя к удалению биологической пленки и нерастворимых отложений (5);
Фиг.2 иллюстрирует элюирующий лекарственное средство/самоочищающийся слой (i) и функциональный слой, придающий структурную целостность устройству (ii) двухслойной системы (a) и трехслойной системы (b);
Фиг.3 иллюстрирует крутящий момент червяка экструдера для полимера, который растворяется при pH 7 при загрузке 5, 10 и 20% хинолинового антибиотика Налидиксовой кислоты;
Фиг.4 иллюстрирует механические свойства композиций, которые могут исследоваться с использованием DMTA: или динамического механического термического анализа в режиме натяжения;
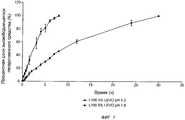
Фиг.5 иллюстрирует профиль высвобождения 10% Налидиксовой кислоты из устройства, имеющего чувствительный к pH слой при pH 6 и pH 7, pH 6, взятом для представления неинфицированной мочи здорового человека; и
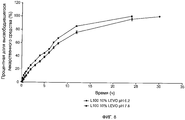
Фиг.6 иллюстрирует профиль высвобождения 10% Налидиксовой кислоты из устройства, имеющего чувствительный к pH слой при pH 6 и pH 7.
Фиг.7 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из устройства, имеющего чувствительный к pH слой из Eudragit® L100, содержащий 5% левофлоксацин, при pH 6,2 и pH 7,8;
Фиг.8 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из устройства, имеющего чувствительный к pH слой из Eudragit® L100, содержащий 10% левофлоксацин, при pH 6,2 и pH 7,8;
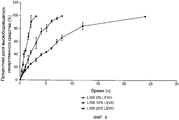
Фиг.9 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из устройств, имеющих чувствительный к pH слой из Eudragit® L100, содержащий соответственно 5%, 10% и 20% левофлоксацин;
Фиг.10 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из устройств, имеющих чувствительный к pH слой из Eudragit® 4155F, содержащий соответственно 5%, 10% и 20% левофлоксацин;
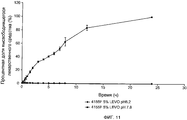
Фиг.11 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из устройства, имеющего чувствительный к pH слой из Eudragit® 4155F, содержащий 5% левофлоксацин при pH 6,2 и pH 7,8;
Фиг.12 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из устройства, имеющего чувствительный к pH слой из Eudragit® 4155F, содержащий 10% левофлоксацин при pH 6,2 и pH 7,8;
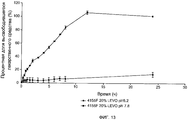
Фиг.13 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из устройства, имеющего чувствительный к pH слой из Eudragit® 4155F, содержащий 20% левофлоксацин при pH 6,2 и pH 7,8;
Фиг.14 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из первого устройства, имеющего чувствительный к pH слой из Eudragit® 4155F, и второго устройства, имеющего чувствительный к pH слой из Eudragit® L100, при pH 6,2 в течение 2 часов, pH 7,8 в течение 2 часов и pH 6,2 в течение 2 часов;
Фиг.15 иллюстрирует профиль высвобождения противомикробного средства левофлоксацина из первого устройства, имеющего чувствительный к pH слой из Eudragit® 4155F, и второго устройства, имеющего чувствительный к pH слой из Eudragit® L100, при pH 7,8 в течение 2 часов, pH 6,2 в течение 2 часов и pH 7,8 в течение 2 часов;
Фиг.16 иллюстрирует динамику во времени средней процентной доли массы при pH 6,2 для первого устройства, имеющего чувствительный к pH слой Eudragit® 4155F, содержащий 10% CA, и второго устройства, имеющего чувствительный к pH слой Eudragit® 4155F, содержащий 10% CA, и 10% Налидиксовую кислоту;
Фиг.17 иллюстрирует динамику во времени средней процентной доли массы при pH 6,2 для первого устройства, имеющего чувствительный к pH слой Eudragit® L100, второго устройства, имеющего чувствительный к pH слой Eudragit® L100, содержащий 10% Налидиксовую кислоту, и третьего устройства, имеющего чувствительный к pH слой Eudragit® L100, содержащий 10% левофлоксацин;
Фиг.18 иллюстрирует динамику во времени средней процентной доли массы при pH 6,2 для первого устройства, имеющего чувствительный к pH слой Eudragit® L100, второго устройства, имеющего чувствительный к pH слой Eudragit® L100, содержащий 10% Налидиксовую кислоту, и третьего устройства, имеющего чувствительный к pH слой Eudragit® L100, содержащий 10% левофлоксацин;
Фиг.19 иллюстрирует динамику во времени средней процентной доли массы при pH 6,2 для первого устройства, имеющего чувствительный к pH слой Eudragit® 4155F, второго устройства, имеющего чувствительный к pH слой Eudragit® 4155F, содержащий 10% Налидиксовую кислоту, и третьего устройства, имеющего чувствительный к pH слой Eudragit® 4155F, содержащий 10% левофлоксацин;
Фиг.20 иллюстрирует увеличенную бактериальную адгезию PMIR к первому устройству, изготовленному из PVC, после 4 часов погружения в искусственную мочу, по сравнению со вторым устройством, имеющим чувствительный к pH слой из Eudragit® 4155F. После 4 часов погружения в искусственную мочу.
Подробное описание
Полимеры смешивали с подходящими пластификаторами для обеспечения возможности переработки двухчервячным экструдером. Затем различные лекарственные загрузки противобактериальных средств смешивали с составами полимера/пластификатора. Композиции хранили в сушилке в течение 24 часов перед переработкой. Затем композиции подвергали экструзии с варьирующимися концентрациями противобактериальных средств. Образцы суспендировали в среде высвобождения, соответствующей условиям in vivo. Затем образцы фильтровали, используя шприцевые фильтры 0,45 мкм, и анализировали с использованием УФ спектроскопии для определения их свойств высвобождения лекарственных средств.
Ожидается, что загруженные одним лекарственным средством пленки Eudragit® будут изготавливаться с использованием устройства двухчервячного экструдера, которое способно подавать противомикробное средство, ЭДТА и лимонную кислоту в четыре различных канала вдоль цилиндра экструдера. Эта соединенная с модулярной конструкция червяка обеспечивает возможность получения продуктов с крайне однородной плотностью и однородностью без разложения функциональных эксципиентов.
После изготовления пленки в последующем будут характеризоваться, и будет предпринят выбор оптимизированных пленочных слоев для коэкструзии с PVC. Многослойная экструзия PVC и оптимизированных реагирующих на pH слоев будет выполняться на современных установках для многослойной листовой экструзии. Хотя типичные устройства для применения в мочевыводящих путях имеют тенденцию быть трубчатыми, для обеспечения возможности тестирования будет проведена экструзия многослойных листков.
Перед коэкструзией нагруженные лекарственным средством гранулы Eudragit® получают с использованием оборудованного охлаждаемой воздухом поверхности головки экструдера гранулятора, соединенного с двухчервячным смесителем. Эти гранулы используются для исследования воздействий типа пластификатора, содержания пластификатора и воздействий включения других функциональных эксципиентов (ЭДТА, лимонной кислоты, хлоргексидина и его солей, Налидиксовой кислоты) на реологические свойства полимеров Eudragit®; которые должны тщательно контролироваться для оптимизации рабочих температур процесса коэкструзии и конечных свойств пленки.
После определения оптимизированных условий переработки с использованием информации, полученной из mDSC и термореологических экспериментов, изготавливаются системы, содержащие многослойные пленки варьирующейся толщины.
ПРИМЕР 1
Как иллюстрируется на Фиг.3, на червяке можно измерить крутящий момент, который обеспечивает достоверное показание вязкости и текучести материала внутри экструдера и дает аппроксимацию того, как различные добавки и функциональные агенты будут воздействовать на легкость продукции материала. Это также оказывает влияние на конечные механические свойства материала. На данном графике показан полимер, который растворяется при pH 7 при добавлении 5, 10 и 20% хинолонового антибиотика Налидиксовой кислоты. Увеличение содержания Налидиксовой кислоты оказывало небольшое влияние на крутящий момент. Однако один из других агентов, левофлоксацин, проявил увеличение наблюдавшегося крутящего момента, указывая на затруднение переработки.
Когда возрастающие уровни Налидиксовой кислоты добавлялись к полимеру, растворяющемуся при pH 6, происходило уменьшение крутящего момента на червяке, указывающее на то, что с этим полимером лекарственное средство способствовало переработке.
ПРИМЕР 2
Механические свойства композиций можно исследовать с использованием DMTA, или динамического механического термического анализа в режиме натяжения. Это включает нагревание продукта по температурному градиенту при постоянном колебании температуры вокруг установленной точки. По этим данным можно определить температуру стеклования, которая представляет собой температуру, ниже которой материал существует в стекловидном состоянии, а выше которой он существует в более гибком, каучукообразном состоянии. Это обеспечивает понимание свойств релаксации полимера, что повлияет на гибкость конечного продукта.
Фиг.4 иллюстрирует величины, которые отражают величины, наблюдаемые во время переработки, причем Налидиксовая кислота вызывает уменьшение температуры стеклования полимера, чувствительного к pH 6. Как и ранее, агент, который увеличивал крутящий момент во время переработки, также увеличивал температуру стеклования.
Используя полоски полученных экструзией композиций, и исследуя их с использованием DMTA в режиме натяжения, и учитывая величины крутящего момента, наблюдали, что левофлоксацин увеличивал определяемую температуру стеклования, возможно, оказывая эффект против пластификации.
ПРИМЕР 3
Один вариант осуществления определенной композиции по изобретению, которая может использоваться для образования определенного слоя устройства по настоящему изобретению, тестировали для определения характеристик элюирования лекарственного средства при pH 6,2. При использовании композиции может быть обеспечено получение слоя, который постоянно элюирует лекарственное средство на низком уровне, когда устройство находится в участке размещения, но в качестве устойчивого к отказам устройства оно должно быть способно переключиться на более быструю реакцию при выявлении инфекции, когда возрастает pH. Обычно pH 6,2 представляет pH неинфицированной мочи здорового человека, тогда как pH 7,8 представляет pH инфицированной мочи. Как иллюстрируется на Фиг.5, исследования высвобождения 10% Налидиксовой кислоты выполняли, используя аппарат растворения раствором PBS при pH 6,2, для представления мочи здорового человека и pH 7,8 для представления инфицированной мочи.
Композиции, использованные в данном тестировании, включали первую композицию, содержащую Eudragit® S100 и 10% PEG 8000, и вторую композицию, содержащую Eudragit® L100 и глицерин 20 и 20% PEG 8000.
ПРИМЕР 4
Варианты осуществления определенной композиции по изобретению, которые могли бы использоваться для образования определенного слоя устройства по настоящему изобретению, тестировали в среде при pH 7,8 представляющей инфицированную мочу. Композиции, использованные в данном тестировании, включали первую композицию, содержащую Eudragit® S100 и 10% PEG 8000, и вторую композицию, содержащую Eudragit® L100 и глицерин 20 и 20% PEG 8000.
В сравнении с растворяющейся при pH 6 полимерной композицией, обсужденной в примере 3, полимер, растворяющийся при pH 7, высвобождает свое лекарственное средство в течение более длительного периода времени.
Полимер, растворяющийся при pH 6, проявляет профиль высвобождения, значительно отличающийся от полимера, растворяющегося при pH 7, обеспечивая возможность быстрой реакции на присутствие инфекции, в то время как полимер, растворяющийся при pH 7, создает защитный барьер при низких величинах pH.
Хотя изобретение было конкретно показано и описано со ссылкой на конкретные примеры, специалистам в данной области будет понятно, что в его форму и детали могут быть внесены различные изменения без отхода от объема настоящего изобретения.
ПРИМЕР 5
Были сформированы первое устройство, содержащее чувствительный к pH слой, включающий Eudragit® L100, и второе устройство, содержащее чувствительный к pH слой, включающий Eudragit® 4155F. Указанные устройства обеспечивали возможность контролируемого высвобождения противомикробных средств левофлоксацина и Налидиксовой кислоты при физиологическом pH (приблизительно 6,2) и увеличенную скорость высвобождения этих активных средств при повышенных уровнях pH, в целом связанных с мочевой инфекцией (приблизительно 7,8).
В дополнение к выбросу противомикробного средства многослойные пленки также обеспечивают новую/чистую поверхность, которая будет свободна от прикрепленных бактерий.
Фиг.7 и 8 свидетельствуют о том, что высвобождение противомикробных средств из устройств может модифицироваться изменением pH среды высвобождения и, кроме того, посредством изменения загрузки противомикробными средствами.
Полимерная матрица, состоящая из 4155F и левофлоксацина, имеет гораздо более контролируемое высвобождение противомикробных средств при pH 6,2, чем L100. Это вызвано тем, что этот полимер не становится растворимым до тех пор, пока pH не превысит 7. Это представляет большой интерес, так как обеспечит возможность непрерывного элюирования противомикробных средств в ‛нормальных' условиях. Это должно предотвратить адгезию бактерий, однако, если продуцируется уреаза (осуществляемая P. mirabilis) и в последующем мочевина разрушается до аммиака, то увеличенное повышение pH приведет к эрозии поверхности и увеличению скорости высвобождения лекарственного средства. Это иллюстрируется на Фиг.9-12.
ПРИМЕР 6
Получали устройства примера 5. Условия pH среды, окружающей устройства, поддерживали на уровне pH 6,2 в течение 2 часов и затем доводили до pH 7,8 в течение 2 часов перед возвратом pH вновь до pH 6,2 в течение 2 часов. Фиг.13 и 14 иллюстрируют профиль высвобождения «стоп,старт» устройств по настоящему изобретению в ответ на изменяющиеся условия pH.
ПРИМЕР 7
Получали устройства примера 5.
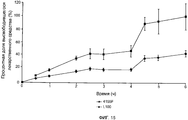
Данные исследования проводили при pH 6,2 и pH 7,8 для оценки эрозии (используя изменение массы в качестве индикатора) чувствительных к pH слоев как функции времени, а также для определения воздействий включения противомикробных средств на этот процесс. Ясно, что при pH 6,2 устройство, содержащее Eudragit® L100, сохраняет массу. Имеется незначительное увеличение массы вследствие захвата воды во время исследования. Eudragit® L100, который начинает эродироваться при величинах pH, превышающих 6, проявляет полную потерю через 24 часа.
Разложение чувствительного к pH слоя, содержащего Eudragit® L100, крайне быстрое при pH 7,8, и это ожидалось. Чувствительный к pH слой, содержащий Eudragit® 4155F, сохраняет массу при pH 7,8, но дополнительно увеличивает массу вследствие захвата воды.
Эрозия чувствительных к pH слоев при pH 6,2 и 7,8 иллюстрируется на Фиг.15 и 16.
ПРИМЕР 8
Первое устройство было изготовлено из PVC и не содержало чувствительный к pH слой. Второе устройство было изготовлено из PVC, содержащего чувствительный к pH слой из Eudragit® 4155F. Эти два устройства погружали в искусственную мочу на 4 часа. Затем два устройства тестировали на наличие адгезии бактерий. Бактериальная адгезия к первому устройству была больше, чем бактериальная адгезия ко второму устройству. Бактериальная адгезия была, по меньшей мере, в 8 раз больше к первому устройству. Это иллюстрируется на Фиг.20.
Claims (30)
1. Устройство, имплантируемое или помещаемое в организм человека или животного, содержащее корпусную структуру, имеющую одну или более поверхностей, где, по меньшей мере, одна из поверхностей содержит чувствительный к pH слой, содержащий линейный полимер, чувствительный к pH, где растворимость в воде чувствительного к pH слоя является более высокой при втором пусковом значении pH, чем при первом физиологическом значении pH, где линейный полимер, чувствительный к pH, подвергается растворению или эрозии в водной среде при втором пусковом значении pH, отличающееся тем, что чувствительный к pH слой содержит буферные группы для снижения степени растворимости или эрозии.
2. Устройство по п.1, где буферные группы выбраны из лимонной кислоты, винной кислоты, янтарной кислоты и фумаровой кислоты.
3. Устройство по п.1, где каждый чувствительный к pH слой имеет одно и то же пусковое значение pH.
4. Устройство по п.1, где каждый чувствительный к pH слой имеет разное пусковое значение pH.
5. Устройство по любому из пп.1-4, где каждый чувствительный к pH слой имеет одинаковую растворимость в воде при втором значении pH.
6. Устройство по любому из пп.1-4, где каждый чувствительный к pH слой имеет разную растворимость в воде при втором значении pH.
7. Устройство по любому из пп.1-4, где соседние чувствительные к pH слои имеют различные уровни ионизации, или различные показатели растворения или разрушения.
8. Устройство по п.1, где различные чувствительные к pH слои содержат различные функциональные соединения, которые выделяются при растворении или разрушении чувствительного к pH слоя.
9. Устройство по п.8, где функциональные соединения либо адсорбированы непосредственно линейным полимером, либо расположены внутри устройства или иным образом присоединены к нему через использование одной или нескольких линкерных молекул или других средств для присоединения, включающих ковалентные, ионные и ван-дер-ваальсовы связи.
10. Устройство по п.8 или 9, где функциональные соединения выбраны из противомикробных соединений, антибиотических соединений, ингибиторов уреазы, EDTA и пластификаторов.
11. Устройство по п.10, где противомикробные или антибиотические соединения выбраны из левофлоксацина, налидиксовой кислоты, антибиотиков, хлоргексидина, повидон-йода, тридосана и ингибиторов уреазы.
12. Устройство по п.1, где линейный полимер выбран из метакрилатных полимеров или полимеров целлюлозы, таких как сложные эфиры целлюлозы или простые эфиры целлюлозы.
13. Устройство по п.1, где второе пусковое значение pH составляет или 7 или выше или 5,5 или ниже.
14. Устройство по п.1, где устройство содержит три слоя, в которых два pH-чувствительных слоя формируют внутренний и внешний слои устройства.
15. Устройство по п.1, содержащее более чем три чувствительных к pH слоя.
16. Устройство по п.1, в форме катетера, стента, имплантируемой или вводимой трубки, зубных шин или зубных протезов.
17. Устройство по п.16 в форме катетера мочевыводящих путей, стента мочевыводящих путей, стента желчных протоков, назо-гастральной трубки, трубки CAPD.
18. Способ формирования устройства, включающий стадии обеспечения структурного слоя и нанесения на него, по меньшей мере, одного чувствительного к pH слоя, причем указанный чувствительный к pH слой содержит линейный полимер, чувствительный к pH, где растворимость в воде чувствительного к pH слоя является более высокой при втором пусковом значении pH, чем при первом физиологическом значении pH, где линейный полимер, чувствительный к pH, подвергается растворению или эрозии в водной среде при втором пусковом значении pH, где чувствительный к pH слой содержит буферные группы для снижения растворимости или эрозии.
19. Способ по п.18, где структурный слой имеет внутреннюю поверхность и наружную поверхность, ограничивающую просвет, и чувствительный к pH слой наносится на внутреннюю поверхность структурного слоя.
20. Способ по любому из пп.18 и 19, включающий стадию нанесения более чем одного чувствительного к pH слоя.
21. Способ по любому из пп.18 и 19, включающий, по меньшей мере, одну стадию мультиэкструзии.
22. Способ по любому из пп.18 и 19, где формируют устройство по любому из пп.1-17.
23. Способ профилактики или облегчения инфекции, связанной с устройством, имплантированным или введенным в тело человека или животного, включающий стадию имплантации или введения в тело человека или животного указанного устройства по любому из пп.1-17.
24. Способ по п.23, где устраняют уже сформированную инфекцию.
25. Способ по любому из пп.23 и 24, где предотвращают или уменьшают образование осаждаемого налета.
26. Способ по любому из пп.23 и 24, где устройство свободно от инфекции или образования осаждаемого налета в течение, по меньшей мере, 5 дней после имплантации или введения.
27. Способ по любому из пп.23 и 24, где время свободной от инфекции имплантации или введения увеличивается, по меньшей мере, на 100%, по сравнению с эквивалентными устройствами, которые не содержат, по меньшей мере, один чувствительный к pH слой.
28. Устройство по п.1 для применения при лечении.
29. Применение устройства по любому из пп.1-17 для профилактики или облегчения инфекции.
30. Применение устройства по любому из пп.1-17 при получении лекарственного средства для профилактики или облегчения инфекции.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0816365.1A GB0816365D0 (en) | 2008-09-08 | 2008-09-08 | Polymeric material |
| GB0816365.1 | 2008-09-08 | ||
| PCT/GB2009/051134 WO2010026433A2 (en) | 2008-09-08 | 2009-09-08 | Polymeric material |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2011113666A RU2011113666A (ru) | 2012-10-20 |
| RU2497549C2 true RU2497549C2 (ru) | 2013-11-10 |
Family
ID=39888966
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2011113666/15A RU2497549C2 (ru) | 2008-09-08 | 2009-09-08 | Полимерный материал |
Country Status (21)
| Country | Link |
|---|---|
| US (2) | US20110238163A1 (ru) |
| EP (1) | EP2341954B1 (ru) |
| JP (1) | JP5702285B2 (ru) |
| CN (1) | CN102202700B (ru) |
| AU (1) | AU2009289024B2 (ru) |
| BR (1) | BRPI0918734A2 (ru) |
| CA (1) | CA2736334C (ru) |
| CY (1) | CY1116528T1 (ru) |
| DK (1) | DK2341954T3 (ru) |
| ES (1) | ES2543002T3 (ru) |
| GB (1) | GB0816365D0 (ru) |
| HR (1) | HRP20150734T1 (ru) |
| HU (1) | HUE025773T2 (ru) |
| MX (1) | MX338190B (ru) |
| PL (1) | PL2341954T3 (ru) |
| PT (1) | PT2341954E (ru) |
| RU (1) | RU2497549C2 (ru) |
| SI (1) | SI2341954T1 (ru) |
| SM (1) | SMT201500180B (ru) |
| WO (1) | WO2010026433A2 (ru) |
| ZA (1) | ZA201102548B (ru) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2485713B1 (en) | 2009-10-05 | 2018-09-26 | Yissum Research Development Company of the Hebrew University of Jerusalem | Liquid precursor compositions and uses thereof for a ph-dependant sustained release treatment of oral disorders |
| US20140328895A1 (en) | 2011-03-29 | 2014-11-06 | Yissum Research Development Company Of The Hebrew University Of Jerusalem, Ltd. | Film-forming composition for a ph-dependant sustained release of the active agent |
| CN102846386B (zh) * | 2012-09-19 | 2015-02-25 | 四川大学 | 智能可控释放抗菌成分的牙种植体及制备方法 |
| US20140127270A1 (en) * | 2012-11-06 | 2014-05-08 | Tina Amarnani | Compositions and Methods for Preventing and Ameliorating Fouling on Medical Surfaces |
| HUE050969T2 (hu) | 2012-11-12 | 2021-01-28 | Hollister Inc | Idõszakos katéter összeállítás |
| ES2705558T3 (es) * | 2012-11-14 | 2019-03-25 | Hollister Inc | Sonda desechable con núcleo interno selectivamente degradable |
| EP2777723B1 (de) * | 2013-03-14 | 2017-12-20 | Biotronik AG | Implantierbarer Gegenstand umfassend gezielt degradierbare Co-Polymere zur verbesserten Explantierbarkeit |
| FI127262B (fi) * | 2013-09-04 | 2018-02-15 | Yrkeshoegskolan Arcada Ab | Mikrobiologisesti puhtaana pysyvät pinnat |
| CA2928646C (en) | 2013-11-08 | 2020-05-05 | Hollister Incorporated | Oleophilic lubricated catheters |
| EP3079750B1 (en) | 2013-12-12 | 2020-05-27 | Hollister Incorporated | Flushable catheters |
| CA2933518C (en) | 2013-12-12 | 2020-12-08 | Hollister Incorporated | Flushable catheters |
| WO2015089181A2 (en) * | 2013-12-12 | 2015-06-18 | Hollister Incorporated | Water disintegrable flushable catheter with a hydrophilic coating |
| LT3079749T (lt) | 2013-12-12 | 2019-12-27 | Hollister Incorporated | Srove nuplaunami kateteriai |
| LT3079748T (lt) | 2013-12-12 | 2020-07-27 | Hollister Incorporated | Srove nuplaunamas suyrantis kateteris |
| EP3310404B1 (en) | 2015-06-17 | 2024-03-13 | Hollister Incorporated | Selectively water disintegrable materials and catheters made of such materials |
| US12064567B2 (en) | 2015-07-20 | 2024-08-20 | Roivios Limited | Percutaneous urinary catheter |
| CA3152431A1 (en) | 2015-07-20 | 2017-01-26 | Roivios Limited | Ureteral and bladder catheters and methods for inducing negative pressure to increase renal perfusion |
| US10918827B2 (en) | 2015-07-20 | 2021-02-16 | Strataca Systems Limited | Catheter device and method for inducing negative pressure in a patient's bladder |
| US10493232B2 (en) | 2015-07-20 | 2019-12-03 | Strataca Systems Limited | Ureteral catheters, bladder catheters, systems, kits and methods for inducing negative pressure to increase renal function |
| US10926062B2 (en) | 2015-07-20 | 2021-02-23 | Strataca Systems Limited | Ureteral and bladder catheters and methods of inducing negative pressure to increase renal perfusion |
| US11541205B2 (en) | 2015-07-20 | 2023-01-03 | Roivios Limited | Coated urinary catheter or ureteral stent and method |
| US11040172B2 (en) | 2015-07-20 | 2021-06-22 | Strataca Systems Limited | Ureteral and bladder catheters and methods of inducing negative pressure to increase renal perfusion |
| US10512713B2 (en) | 2015-07-20 | 2019-12-24 | Strataca Systems Limited | Method of removing excess fluid from a patient with hemodilution |
| CA3014457A1 (en) * | 2016-02-24 | 2017-08-31 | Innovative Surface Technologies, Inc. | Crystallization inhibitor compositions for implantable urological devices |
| CN115120791A (zh) | 2017-08-25 | 2022-09-30 | 罗维奥斯有限公司 | 促进从尿道除尿的排尿泵 |
| DE102017130893A1 (de) | 2017-12-21 | 2019-06-27 | Paul Hartmann Ag | pH regulierende Wundauflage |
| US12115288B2 (en) * | 2018-07-12 | 2024-10-15 | Cook Medical Technologies Llc | Coated medical device and method of coating such a device |
| JP2022515321A (ja) * | 2018-11-30 | 2022-02-18 | ロイヴィオス リミテッド | コーティングおよび/または含浸された尿管カテーテルまたはステントならびに方法 |
| IL295007A (en) | 2020-01-31 | 2022-09-01 | Nanocopoeia Llc | Amorphous nilotinib microparticles and uses thereof |
| CA3181361A1 (en) | 2020-04-30 | 2021-11-04 | Nanocopoeia, Llc | Orally disintegrating tablet comprising amorphous solid dispersion of nilotinib |
| WO2022072930A1 (en) * | 2020-10-02 | 2022-04-07 | Petrychenko Dmitri | Extended release devices and therapeutics for long term treatment of urinary tract infection in-vivo |
| CN112472359A (zh) * | 2020-12-15 | 2021-03-12 | 上海市东方医院(同济大学附属东方医院) | 胆管狭窄自动扩张型胆管支架 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2327486C1 (ru) * | 2007-07-04 | 2008-06-27 | Валентина Васильевна Малиновская | Лекарственное средство для лечения инфекционно-воспалительных заболеваний, обладающее иммуномодулирующим, антивирусным, антибактериальным, антиоксидантным, мембраностабилизирующим, противовоспалительным, антитоксическим свойствами |
Family Cites Families (45)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2237218A (en) * | 1938-09-29 | 1941-04-01 | Wardlyn Corp | Application of cellulose derivatives |
| US3566874A (en) * | 1968-08-13 | 1971-03-02 | Nat Patent Dev Corp | Catheter |
| US3663288A (en) * | 1969-09-04 | 1972-05-16 | American Cyanamid Co | Physiologically acceptible elastomeric article |
| US3580983A (en) * | 1969-12-03 | 1971-05-25 | Nat Catheter Corp | Conductive line tube |
| US3695921A (en) * | 1970-09-09 | 1972-10-03 | Nat Patent Dev Corp | Method of coating a catheter |
| US3861396A (en) * | 1973-08-08 | 1975-01-21 | Hydro Med Sciences Inc | Drainage tube |
| CS173836B1 (ru) * | 1974-03-19 | 1977-03-31 | ||
| US4220153A (en) * | 1978-05-08 | 1980-09-02 | Pfizer Inc. | Controlled release delivery system |
| US4392848A (en) * | 1979-06-25 | 1983-07-12 | The Procter & Gamble Company | Catheterization |
| US4557724A (en) * | 1981-02-17 | 1985-12-10 | University Of Utah Research Foundation | Apparatus and methods for minimizing cellular adhesion on peritoneal injection catheters |
| US4539234A (en) * | 1981-05-27 | 1985-09-03 | Unitika Ltd. | Urethral catheter capable of preventing urinary tract infection and process for producing the same |
| US4515593A (en) * | 1981-12-31 | 1985-05-07 | C. R. Bard, Inc. | Medical tubing having exterior hydrophilic coating for microbiocide absorption therein and method for using same |
| US4773901A (en) * | 1981-12-31 | 1988-09-27 | C. R. Bard, Inc. | Catheter with selectively rigidified portion |
| US4526579A (en) * | 1983-06-17 | 1985-07-02 | Pfizer Inc. | Method for graft copolymerization to natural rubber articles |
| SE8504501D0 (sv) * | 1985-09-30 | 1985-09-30 | Astra Meditec Ab | Method of forming an improved hydrophilic coating on a polymer surface |
| US4708765A (en) * | 1986-10-06 | 1987-11-24 | The Johns Hopkins University | Regulation of the exposure of active surfaces |
| GB8729977D0 (en) * | 1987-12-23 | 1988-02-03 | Bard Ltd | Catheter |
| US5091205A (en) * | 1989-01-17 | 1992-02-25 | Union Carbide Chemicals & Plastics Technology Corporation | Hydrophilic lubricious coatings |
| US5041100A (en) * | 1989-04-28 | 1991-08-20 | Cordis Corporation | Catheter and hydrophilic, friction-reducing coating thereon |
| JPH02299663A (ja) * | 1989-05-15 | 1990-12-11 | Unitika Ltd | 抗感染性カテーテル |
| US5843089A (en) * | 1990-12-28 | 1998-12-01 | Boston Scientific Corporation | Stent lining |
| US5599352A (en) * | 1992-03-19 | 1997-02-04 | Medtronic, Inc. | Method of making a drug eluting stent |
| US5464650A (en) * | 1993-04-26 | 1995-11-07 | Medtronic, Inc. | Intravascular stent and method |
| US5531716A (en) * | 1993-09-29 | 1996-07-02 | Hercules Incorporated | Medical devices subject to triggered disintegration |
| US5554147A (en) * | 1994-02-01 | 1996-09-10 | Caphco, Inc. | Compositions and devices for controlled release of active ingredients |
| US5788687A (en) | 1994-02-01 | 1998-08-04 | Caphco, Inc | Compositions and devices for controlled release of active ingredients |
| US6558798B2 (en) * | 1995-02-22 | 2003-05-06 | Scimed Life Systems, Inc. | Hydrophilic coating and substrates coated therewith having enhanced durability and lubricity |
| US5554174A (en) * | 1995-10-18 | 1996-09-10 | Pacesetter, Inc. | System and method for automatically adjusting cardioverter and defibrillator shock energy as a function of time-to-therapy |
| US6273913B1 (en) * | 1997-04-18 | 2001-08-14 | Cordis Corporation | Modified stent useful for delivery of drugs along stent strut |
| US5877243A (en) * | 1997-05-05 | 1999-03-02 | Icet, Inc. | Encrustation and bacterial resistant coatings for medical applications |
| US20030040790A1 (en) * | 1998-04-15 | 2003-02-27 | Furst Joseph G. | Stent coating |
| AU771367B2 (en) * | 1998-08-20 | 2004-03-18 | Cook Medical Technologies Llc | Coated implantable medical device |
| US20020065546A1 (en) * | 1998-12-31 | 2002-05-30 | Machan Lindsay S. | Stent grafts with bioactive coatings |
| US6368315B1 (en) * | 1999-06-23 | 2002-04-09 | Durect Corporation | Composite drug delivery catheter |
| WO2003056280A1 (de) * | 2001-12-31 | 2003-07-10 | Asm Automation Sensorik Messtechnik Gmbh | Magnetostriktives sensor-element |
| US20040062778A1 (en) | 2002-09-26 | 2004-04-01 | Adi Shefer | Surface dissolution and/or bulk erosion controlled release compositions and devices |
| WO2005044142A2 (en) * | 2003-11-10 | 2005-05-19 | Angiotech International Ag | Intravascular devices and fibrosis-inducing agents |
| JP2007516740A (ja) * | 2003-11-10 | 2007-06-28 | アンジオテック インターナショナル アーゲー | 医療移植片(implants)および瘢痕化抑制剤 |
| US7758892B1 (en) * | 2004-05-20 | 2010-07-20 | Boston Scientific Scimed, Inc. | Medical devices having multiple layers |
| US20050266042A1 (en) * | 2004-05-27 | 2005-12-01 | Medtronic Vascular, Inc. | Methods and apparatus for treatment of aneurysmal tissue |
| GB0417350D0 (en) | 2004-08-04 | 2004-09-08 | Incobar Ltd | Urinary products |
| US7588642B1 (en) * | 2004-11-29 | 2009-09-15 | Advanced Cardiovascular Systems, Inc. | Abluminal stent coating apparatus and method using a brush assembly |
| US8137735B2 (en) * | 2005-11-10 | 2012-03-20 | Allegiance Corporation | Elastomeric article with antimicrobial coating |
| US20070161949A1 (en) * | 2006-01-06 | 2007-07-12 | Knox Susan J | Catheter system for minimizing retrograde bacterial transmission from a catheter tubing |
| EP1938756A1 (en) * | 2006-12-29 | 2008-07-02 | Qiagen GmbH | Method and materials for triggered release of a biological sample |
-
2008
- 2008-09-08 GB GBGB0816365.1A patent/GB0816365D0/en not_active Ceased
-
2009
- 2009-09-08 DK DK09785593.6T patent/DK2341954T3/en active
- 2009-09-08 PT PT97855936T patent/PT2341954E/pt unknown
- 2009-09-08 SI SI200931231T patent/SI2341954T1/sl unknown
- 2009-09-08 WO PCT/GB2009/051134 patent/WO2010026433A2/en active Application Filing
- 2009-09-08 CA CA2736334A patent/CA2736334C/en not_active Expired - Fee Related
- 2009-09-08 AU AU2009289024A patent/AU2009289024B2/en not_active Ceased
- 2009-09-08 JP JP2011525629A patent/JP5702285B2/ja not_active Expired - Fee Related
- 2009-09-08 ES ES09785593.6T patent/ES2543002T3/es active Active
- 2009-09-08 PL PL09785593T patent/PL2341954T3/pl unknown
- 2009-09-08 BR BRPI0918734A patent/BRPI0918734A2/pt not_active IP Right Cessation
- 2009-09-08 HU HUE09785593A patent/HUE025773T2/en unknown
- 2009-09-08 CN CN200980144318.4A patent/CN102202700B/zh not_active Expired - Fee Related
- 2009-09-08 MX MX2011002495A patent/MX338190B/es active IP Right Grant
- 2009-09-08 EP EP09785593.6A patent/EP2341954B1/en active Active
- 2009-09-08 RU RU2011113666/15A patent/RU2497549C2/ru not_active IP Right Cessation
-
2011
- 2011-03-08 US US13/043,021 patent/US20110238163A1/en not_active Abandoned
- 2011-04-06 ZA ZA2011/02548A patent/ZA201102548B/en unknown
-
2015
- 2015-07-06 HR HRP20150734TT patent/HRP20150734T1/hr unknown
- 2015-07-13 CY CY20151100607T patent/CY1116528T1/el unknown
- 2015-07-27 SM SM201500180T patent/SMT201500180B/xx unknown
-
2019
- 2019-03-25 US US16/362,931 patent/US20190343991A1/en not_active Abandoned
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2327486C1 (ru) * | 2007-07-04 | 2008-06-27 | Валентина Васильевна Малиновская | Лекарственное средство для лечения инфекционно-воспалительных заболеваний, обладающее иммуномодулирующим, антивирусным, антибактериальным, антиоксидантным, мембраностабилизирующим, противовоспалительным, антитоксическим свойствами |
Also Published As
| Publication number | Publication date |
|---|---|
| MX2011002495A (es) | 2011-06-16 |
| WO2010026433A2 (en) | 2010-03-11 |
| GB0816365D0 (en) | 2008-10-15 |
| BRPI0918734A2 (pt) | 2015-12-01 |
| JP5702285B2 (ja) | 2015-04-15 |
| EP2341954A2 (en) | 2011-07-13 |
| SI2341954T1 (sl) | 2015-08-31 |
| PT2341954E (pt) | 2015-09-10 |
| WO2010026433A3 (en) | 2010-11-04 |
| CY1116528T1 (el) | 2017-03-15 |
| CA2736334C (en) | 2018-11-13 |
| ES2543002T3 (es) | 2015-08-13 |
| SMT201500180B (it) | 2015-09-07 |
| RU2011113666A (ru) | 2012-10-20 |
| ZA201102548B (en) | 2011-12-28 |
| HUE025773T2 (en) | 2016-04-28 |
| HRP20150734T1 (hr) | 2015-08-14 |
| EP2341954B1 (en) | 2015-05-27 |
| US20110238163A1 (en) | 2011-09-29 |
| PL2341954T3 (pl) | 2015-10-30 |
| JP2012501712A (ja) | 2012-01-26 |
| AU2009289024B2 (en) | 2015-05-21 |
| CN102202700A (zh) | 2011-09-28 |
| AU2009289024A1 (en) | 2010-03-11 |
| CA2736334A1 (en) | 2010-03-11 |
| MX338190B (es) | 2016-04-06 |
| US20190343991A1 (en) | 2019-11-14 |
| DK2341954T3 (en) | 2015-07-20 |
| CN102202700B (zh) | 2015-06-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2497549C2 (ru) | Полимерный материал | |
| US5788687A (en) | Compositions and devices for controlled release of active ingredients | |
| US5554147A (en) | Compositions and devices for controlled release of active ingredients | |
| JP6016805B2 (ja) | 泌尿器科医療デバイス | |
| JP4918222B2 (ja) | 薬物の制御放出用の植え込み可能な若しくは挿入可能な医療装置 | |
| CN106075698B (zh) | 药物释放医用导管、管和装置 | |
| US20050064038A1 (en) | Active agent delivery systems including a single layer of a miscible polymer blend, medical devices, and methods | |
| WO2005096990A2 (en) | Novel modification of medical prostheses | |
| EP1684820A2 (en) | Active agent delivery systems including a miscible polymer blend, medical devices, and methods | |
| JPH11500330A (ja) | 抗菌性医療装置及び方法 | |
| Chew et al. | Technology insight: Novel ureteral stent materials and designs | |
| US20150335794A1 (en) | Smart coating for implantable devices | |
| Hu et al. | Recent development and future application of biodegradable ureteral stents | |
| BRPI0918734B1 (pt) | Dispositivo, método de formação e uso do mesmo | |
| US20220105326A1 (en) | Extended release devices and therapeutics for long term treatment of urinary tract infection in-vivo | |
| Kallidonis et al. | Drug Eluting Devices in the Urinary Tract | |
| Tailly et al. | Coated and Drug‐Eluting Stents |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20200909 |