RU2473557C2 - Вакцины на основе пептида foxp3 - Google Patents
Вакцины на основе пептида foxp3 Download PDFInfo
- Publication number
- RU2473557C2 RU2473557C2 RU2009129531/10A RU2009129531A RU2473557C2 RU 2473557 C2 RU2473557 C2 RU 2473557C2 RU 2009129531/10 A RU2009129531/10 A RU 2009129531/10A RU 2009129531 A RU2009129531 A RU 2009129531A RU 2473557 C2 RU2473557 C2 RU 2473557C2
- Authority
- RU
- Russia
- Prior art keywords
- cells
- foxp3
- peptide
- seq
- peptides
- Prior art date
Links
- 229940023041 peptide vaccine Drugs 0.000 title 1
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 442
- 102000004196 processed proteins & peptides Human genes 0.000 claims abstract description 233
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 claims abstract description 200
- 210000004027 cell Anatomy 0.000 claims abstract description 186
- 210000000612 antigen-presenting cell Anatomy 0.000 claims abstract description 78
- 238000000034 method Methods 0.000 claims abstract description 70
- 102000040430 polynucleotide Human genes 0.000 claims abstract description 60
- 108091033319 polynucleotide Proteins 0.000 claims abstract description 60
- 239000002157 polynucleotide Substances 0.000 claims abstract description 60
- 229960005486 vaccine Drugs 0.000 claims abstract description 29
- 230000001939 inductive effect Effects 0.000 claims abstract description 21
- 239000008177 pharmaceutical agent Substances 0.000 claims abstract description 18
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 claims abstract description 5
- 150000001413 amino acids Chemical group 0.000 claims description 56
- 206010028980 Neoplasm Diseases 0.000 claims description 51
- 229940024606 amino acid Drugs 0.000 claims description 50
- 239000000427 antigen Substances 0.000 claims description 49
- 108091007433 antigens Proteins 0.000 claims description 49
- 102000036639 antigens Human genes 0.000 claims description 49
- 201000011510 cancer Diseases 0.000 claims description 41
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 31
- 230000001105 regulatory effect Effects 0.000 claims description 18
- 108010013476 HLA-A24 Antigen Proteins 0.000 claims description 17
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims description 13
- 229930182817 methionine Natural products 0.000 claims description 13
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims description 10
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 claims description 10
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 claims description 8
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 claims description 8
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 claims description 7
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 claims description 7
- 125000001433 C-terminal amino-acid group Chemical group 0.000 claims description 5
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 claims description 4
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 claims description 4
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims description 4
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims description 4
- 238000012258 culturing Methods 0.000 claims description 4
- 229960000310 isoleucine Drugs 0.000 claims description 4
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 claims description 4
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 claims description 4
- 239000004474 valine Substances 0.000 claims description 4
- 238000002156 mixing Methods 0.000 claims description 3
- 230000003915 cell function Effects 0.000 claims description 2
- 230000004663 cell proliferation Effects 0.000 claims 1
- 125000003275 alpha amino acid group Chemical group 0.000 abstract description 43
- 230000000694 effects Effects 0.000 abstract description 38
- 239000003814 drug Substances 0.000 abstract description 19
- 230000033228 biological regulation Effects 0.000 abstract description 10
- 239000000126 substance Substances 0.000 abstract description 10
- 230000001472 cytotoxic effect Effects 0.000 abstract description 9
- 231100000433 cytotoxic Toxicity 0.000 abstract description 3
- 235000001014 amino acid Nutrition 0.000 description 54
- 108090000623 proteins and genes Proteins 0.000 description 40
- 230000027455 binding Effects 0.000 description 37
- 102100037850 Interferon gamma Human genes 0.000 description 36
- 108010074328 Interferon-gamma Proteins 0.000 description 36
- 238000004519 manufacturing process Methods 0.000 description 30
- 230000006698 induction Effects 0.000 description 28
- 210000004443 dendritic cell Anatomy 0.000 description 26
- 241000699670 Mus sp. Species 0.000 description 25
- 239000000203 mixture Substances 0.000 description 25
- 235000018102 proteins Nutrition 0.000 description 25
- 102000004169 proteins and genes Human genes 0.000 description 25
- 206010062016 Immunosuppression Diseases 0.000 description 24
- 102000011786 HLA-A Antigens Human genes 0.000 description 22
- 108010075704 HLA-A Antigens Proteins 0.000 description 22
- 230000001506 immunosuppresive effect Effects 0.000 description 21
- 230000006870 function Effects 0.000 description 20
- 229920001184 polypeptide Polymers 0.000 description 20
- 238000001727 in vivo Methods 0.000 description 19
- 238000006467 substitution reaction Methods 0.000 description 19
- 238000002255 vaccination Methods 0.000 description 18
- 239000013598 vector Substances 0.000 description 18
- 230000000638 stimulation Effects 0.000 description 17
- 230000028993 immune response Effects 0.000 description 16
- 239000007787 solid Substances 0.000 description 16
- 210000001808 exosome Anatomy 0.000 description 15
- 238000000338 in vitro Methods 0.000 description 15
- 150000007523 nucleic acids Chemical class 0.000 description 14
- 230000004936 stimulating effect Effects 0.000 description 13
- 238000009169 immunotherapy Methods 0.000 description 12
- 239000000463 material Substances 0.000 description 12
- 102000039446 nucleic acids Human genes 0.000 description 12
- 108020004707 nucleic acids Proteins 0.000 description 12
- 108010074032 HLA-A2 Antigen Proteins 0.000 description 11
- 102000025850 HLA-A2 Antigen Human genes 0.000 description 11
- 238000012986 modification Methods 0.000 description 11
- 230000004048 modification Effects 0.000 description 11
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 10
- 241000282414 Homo sapiens Species 0.000 description 10
- 201000010099 disease Diseases 0.000 description 10
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 10
- 238000003114 enzyme-linked immunosorbent spot assay Methods 0.000 description 10
- 238000011282 treatment Methods 0.000 description 10
- 108091008874 T cell receptors Proteins 0.000 description 9
- 125000000539 amino acid group Chemical group 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 9
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 8
- 230000000259 anti-tumor effect Effects 0.000 description 8
- 229940079593 drug Drugs 0.000 description 8
- 210000004881 tumor cell Anatomy 0.000 description 8
- 108020004705 Codon Proteins 0.000 description 7
- 239000004480 active ingredient Substances 0.000 description 7
- 239000002671 adjuvant Substances 0.000 description 7
- 230000004044 response Effects 0.000 description 7
- 238000002965 ELISA Methods 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 6
- 230000014509 gene expression Effects 0.000 description 6
- 230000003053 immunization Effects 0.000 description 6
- 238000002649 immunization Methods 0.000 description 6
- 238000010647 peptide synthesis reaction Methods 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 230000004614 tumor growth Effects 0.000 description 6
- 241000699666 Mus <mouse, genus> Species 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 229910003460 diamond Inorganic materials 0.000 description 5
- 239000010432 diamond Substances 0.000 description 5
- 230000001900 immune effect Effects 0.000 description 5
- 210000000987 immune system Anatomy 0.000 description 5
- 230000002163 immunogen Effects 0.000 description 5
- 230000005847 immunogenicity Effects 0.000 description 5
- 125000003729 nucleotide group Chemical group 0.000 description 5
- 210000005259 peripheral blood Anatomy 0.000 description 5
- 239000011886 peripheral blood Substances 0.000 description 5
- 230000002265 prevention Effects 0.000 description 5
- 230000001629 suppression Effects 0.000 description 5
- 238000013519 translation Methods 0.000 description 5
- 108020004414 DNA Proteins 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- 230000005809 anti-tumor immunity Effects 0.000 description 4
- 230000036755 cellular response Effects 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000001747 exhibiting effect Effects 0.000 description 4
- 239000012634 fragment Substances 0.000 description 4
- 229910052739 hydrogen Inorganic materials 0.000 description 4
- 150000002632 lipids Chemical class 0.000 description 4
- 108091005601 modified peptides Proteins 0.000 description 4
- 210000001616 monocyte Anatomy 0.000 description 4
- 239000008194 pharmaceutical composition Substances 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 230000035755 proliferation Effects 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- 206010006187 Breast cancer Diseases 0.000 description 3
- 208000026310 Breast neoplasm Diseases 0.000 description 3
- 238000011510 Elispot assay Methods 0.000 description 3
- 108010088729 HLA-A*02:01 antigen Proteins 0.000 description 3
- 108010002350 Interleukin-2 Proteins 0.000 description 3
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 description 3
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 235000004279 alanine Nutrition 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 210000003719 b-lymphocyte Anatomy 0.000 description 3
- 238000004422 calculation algorithm Methods 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 239000012636 effector Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 230000036039 immunity Effects 0.000 description 3
- 238000003780 insertion Methods 0.000 description 3
- 230000037431 insertion Effects 0.000 description 3
- 210000004698 lymphocyte Anatomy 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 229960004857 mitomycin Drugs 0.000 description 3
- 210000002433 mononuclear leukocyte Anatomy 0.000 description 3
- 239000002773 nucleotide Substances 0.000 description 3
- 239000002831 pharmacologic agent Substances 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 210000003289 regulatory T cell Anatomy 0.000 description 3
- 210000004988 splenocyte Anatomy 0.000 description 3
- 239000000021 stimulant Substances 0.000 description 3
- 230000008685 targeting Effects 0.000 description 3
- 230000003612 virological effect Effects 0.000 description 3
- 108700028369 Alleles Proteins 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 description 2
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 2
- 108090000978 Interleukin-4 Proteins 0.000 description 2
- 108010002586 Interleukin-7 Proteins 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 108020004511 Recombinant DNA Proteins 0.000 description 2
- 241000700618 Vaccinia virus Species 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 238000011224 anti-cancer immunotherapy Methods 0.000 description 2
- 230000000890 antigenic effect Effects 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 238000002619 cancer immunotherapy Methods 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 238000001415 gene therapy Methods 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 230000013632 homeostatic process Effects 0.000 description 2
- 230000005917 in vivo anti-tumor Effects 0.000 description 2
- 238000010253 intravenous injection Methods 0.000 description 2
- 230000002147 killing effect Effects 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 210000000822 natural killer cell Anatomy 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 210000005105 peripheral blood lymphocyte Anatomy 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 230000001177 retroviral effect Effects 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 238000010532 solid phase synthesis reaction Methods 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- 238000007910 systemic administration Methods 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 239000003053 toxin Substances 0.000 description 2
- 231100000765 toxin Toxicity 0.000 description 2
- LEBVLXFERQHONN-UHFFFAOYSA-N 1-butyl-N-(2,6-dimethylphenyl)piperidine-2-carboxamide Chemical compound CCCCN1CCCCC1C(=O)NC1=C(C)C=CC=C1C LEBVLXFERQHONN-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- 241000193738 Bacillus anthracis Species 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108010077333 CAP1-6D Proteins 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 241000700199 Cavia porcellus Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- 241001227713 Chiron Species 0.000 description 1
- 102000009016 Cholera Toxin Human genes 0.000 description 1
- 108010049048 Cholera Toxin Proteins 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 150000008574 D-amino acids Chemical class 0.000 description 1
- 206010011968 Decreased immune responsiveness Diseases 0.000 description 1
- 101710088194 Dehydrogenase Proteins 0.000 description 1
- 201000009273 Endometriosis Diseases 0.000 description 1
- 102000004533 Endonucleases Human genes 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 102100027581 Forkhead box protein P3 Human genes 0.000 description 1
- 101710088098 Forkhead box protein P3 Proteins 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 102000008949 Histocompatibility Antigens Class I Human genes 0.000 description 1
- 108010088652 Histocompatibility Antigens Class I Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 1
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 1
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 102100026878 Interleukin-2 receptor subunit alpha Human genes 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- QEFRNWWLZKMPFJ-ZXPFJRLXSA-N L-methionine (R)-S-oxide Chemical compound C[S@@](=O)CC[C@H]([NH3+])C([O-])=O QEFRNWWLZKMPFJ-ZXPFJRLXSA-N 0.000 description 1
- QEFRNWWLZKMPFJ-UHFFFAOYSA-N L-methionine sulphoxide Natural products CS(=O)CCC(N)C(O)=O QEFRNWWLZKMPFJ-UHFFFAOYSA-N 0.000 description 1
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical compound CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 102000043129 MHC class I family Human genes 0.000 description 1
- 108091054437 MHC class I family Proteins 0.000 description 1
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 1
- 238000000585 Mann–Whitney U test Methods 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- 108010046117 N-palmitoyl-5,6-dipalmitoyl-S-glycerylcysteinyl-seryl-serine Proteins 0.000 description 1
- 108091061960 Naked DNA Proteins 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 241000282577 Pan troglodytes Species 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 241001504519 Papio ursinus Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 241000009328 Perro Species 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 101100221606 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) COS7 gene Proteins 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 241000293871 Salmonella enterica subsp. enterica serovar Typhi Species 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 206010041067 Small cell lung cancer Diseases 0.000 description 1
- 206010068771 Soft tissue neoplasm Diseases 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- 230000006044 T cell activation Effects 0.000 description 1
- 230000006052 T cell proliferation Effects 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 229910052770 Uranium Inorganic materials 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 206010046865 Vaccinia virus infection Diseases 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229940037003 alum Drugs 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- ILRRQNADMUWWFW-UHFFFAOYSA-K aluminium phosphate Chemical compound O1[Al]2OP1(=O)O2 ILRRQNADMUWWFW-UHFFFAOYSA-K 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 230000002788 anti-peptide Effects 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 230000005975 antitumor immune response Effects 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 230000005784 autoimmunity Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 102000015736 beta 2-Microglobulin Human genes 0.000 description 1
- 108010081355 beta 2-Microglobulin Proteins 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 238000001815 biotherapy Methods 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 229960003150 bupivacaine Drugs 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 229940022399 cancer vaccine Drugs 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- UHBYWPGGCSDKFX-UHFFFAOYSA-N carboxyglutamic acid Chemical compound OC(=O)C(N)CC(C(O)=O)C(O)=O UHBYWPGGCSDKFX-UHFFFAOYSA-N 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- -1 cationic lipid Chemical class 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 230000022534 cell killing Effects 0.000 description 1
- 230000007969 cellular immunity Effects 0.000 description 1
- 230000009956 central mechanism Effects 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 208000006990 cholangiocarcinoma Diseases 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 238000003501 co-culture Methods 0.000 description 1
- 230000004186 co-expression Effects 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 230000000536 complexating effect Effects 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000012531 culture fluid Substances 0.000 description 1
- 238000012136 culture method Methods 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 208000024334 diffuse gastric cancer Diseases 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 201000004101 esophageal cancer Diseases 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 108060003552 hemocyanin Proteins 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- UKAUYVFTDYCKQA-UHFFFAOYSA-N homoserine Chemical compound OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 229960002591 hydroxyproline Drugs 0.000 description 1
- 230000002998 immunogenetic effect Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 201000007270 liver cancer Diseases 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 210000002751 lymph Anatomy 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- LSDPWZHWYPCBBB-UHFFFAOYSA-O methylsulfide anion Chemical compound [SH2+]C LSDPWZHWYPCBBB-UHFFFAOYSA-O 0.000 description 1
- 239000000693 micelle Substances 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 230000004001 molecular interaction Effects 0.000 description 1
- 208000025113 myeloid leukemia Diseases 0.000 description 1
- 229920005615 natural polymer Polymers 0.000 description 1
- 208000025189 neoplasm of testis Diseases 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 201000008968 osteosarcoma Diseases 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-N palmitic acid group Chemical group C(CCCCCCCCCCCCCCC)(=O)O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 230000009955 peripheral mechanism Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- BZQFBWGGLXLEPQ-REOHCLBHSA-N phosphoserine Chemical compound OC(=O)[C@@H](N)COP(O)(O)=O BZQFBWGGLXLEPQ-REOHCLBHSA-N 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 235000019833 protease Nutrition 0.000 description 1
- 238000010188 recombinant method Methods 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 201000010174 renal carcinoma Diseases 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 208000000587 small cell lung carcinoma Diseases 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- 210000001541 thymus gland Anatomy 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 230000009258 tissue cross reactivity Effects 0.000 description 1
- FGMPLJWBKKVCDB-UHFFFAOYSA-N trans-L-hydroxy-proline Natural products ON1CCCC1C(O)=O FGMPLJWBKKVCDB-UHFFFAOYSA-N 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- XVQKZSLOGHBCET-INVHGPFASA-N tripalmitoyl-S-glyceryl-cysteinyl-seryl-serine Chemical compound CCCCCCCCCCCCCCCC(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O)CSCC(OC(=O)CCCCCCCCCCCCCCC)COC(=O)CCCCCCCCCCCCCCC XVQKZSLOGHBCET-INVHGPFASA-N 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 208000007089 vaccinia Diseases 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 230000003313 weakening effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Liposomes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- C07K14/4701—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals not used
- C07K14/4713—Autoimmune diseases, e.g. Insulin-dependent diabetes mellitus, multiple sclerosis, rheumathoid arthritis, systemic lupus erythematosus; Autoantigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55566—Emulsions, e.g. Freund's adjuvant, MF59
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Immunology (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Mycology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- Oncology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Rheumatology (AREA)
- Diabetes (AREA)
- Rehabilitation Therapy (AREA)
- Toxicology (AREA)
- Hematology (AREA)
- Zoology (AREA)
- Dispersion Chemistry (AREA)
- Biotechnology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Изобретение относится к области биохимии. Представлен пептид, обладающий способностью индуцировать цитотоксические Т-клетки, где пептид состоит из аминокислотных последовательностей SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, а также представлен пептид, обладающий способностью индуцировать цитотоксические Т-клетки, где пептид состоит из аминокислотной последовательности SEQ ID NO:3-5, 7-9, 12, 17, 67 или 74, в которой заменены или добавлены 1 или 2 аминокислоты. Представлен пептид, обладающий способностью индуцировать цитотоксические Т-клетки, где пептид состоит из аминокислотных последовательностей SEQ ID NO:15-19, 22, 24, 27-30 и 37, в которой заменены или добавлены 1 или 2 аминокислоты. Представлено фармацевтическое средство, использующееся для регуляции клеток T-reg, содержащее 1 или несколько типов заявленных пептидов. Раскрыт способ индукции антиген-презентирующих клеток. Представлены выделенная цитотоксическая клетка и антиген-презентирующая клетка. Раскрыт способ регуляции клеток T-reg, а также раскрыто применение указанных пептидов для получения вакцины. Представлены полинуклеотиды, кодирующие заявленные пептиды. Изобретение позволяет получить пептиды, использующиеся в составе фармацевтического средства, предназначенного для регуляции T-reg клеток. 12 н. и 9 з.п. ф-лы, 10 ил., 4 табл., 1 пр.
Description
Область техники, к которой относится изобретение
Перекрестная ссылка на родственные заявки
По настоящей заявке испрашивается приоритет предварительной заявки США 60/878615, поданной 3 января 2007, и предварительной заявки США 60/896472, поданной 22 марта 2007, содержание каждой из которых включено в настоящее описание посредством ссылки.
Настоящее изобретение относится к области биологии, более конкретно к терапии рака. Конкретно, настоящее изобретение относится к пептидам Foxp3, которые необычайно эффективны в качестве противораковых вакцин, и к лекарственным средствам для лечения и профилактики опухолей.
Предшествующий уровень техники
Было показано, что CD8+ цитотоксические Т-лимфоциты (CTL) распознают пептидные эпитопы, выделенные из связанных с опухолями антигенов (TAA), присутствующих на молекуле MHC класса I, и затем уничтожают опухолевые клетки. С момента обнаружения MAGE-семейства, первого примера антигенов TAA, было обнаружено много других антигенов TAA с использованием иммунологических способов (Boon T, Int J Cancer 54: 177-80, 1993; Boon T et al., J Exp Med 183: 725-9, 1996; van der Bruggen P et al., Science 254: 1643-7, 1991; Brichard V et al., J Exp Med 178: 489-95, 1993; Kawakami Y et al., J Exp Med 180: 347-52, 1994), и некоторые из них находятся в настоящее время в процессе клинического исследования в качестве мишеней иммунотерапии.
Идентификация новых антигенов TAA, которые индуцируют сильный и специфичный противоопухолевый иммунный ответ, стала основанием для дальнейшей разработки клинического применения стратегий пептидной вакцинации для различных типов рака (Harris CC, J Natl Cancer Inst 88: 1442-5, 1996; Butterfield LH et al., Cancer Res 59: 3134-42, 1999; Vissers JLM et al., Cancer Res 59: 5554-9, 1999; Van der Burg SH et al., J Immunol 156: 3308-14, 1996; Tanaka F et al., Cancer Res 57: 4465-8, 1997; Fujie T et al., Int J Cancer 80: 169-72, 1999; Kikuchi M et al., Int J Cancer 81: 459-66, 1999; Oiso M et al., Int J Cancer 81: 387-94, 1999).
Были выполнены различные типы антиген-специфичной иммунотерапии, однако до сих пор получали низкую клиническую эффективность из-за очевидной опухолевой регрессии (Rosenberg SA et al., Nat Med 10:909-15, 2004). Одной из главных причин является слабый иммунный ответ противоопухолевых эффекторных лимфоцитов (TIL) и лимфоцитов периферической крови (PBL) у пациентов с поздней стадией рака (Miescher S et al., J Immunol 136: 1899-907, 1986). Такая иммуносупрессия, индуцированная опухолью, является причиной слабого ответа на опухолевые антигены (Young RC et al., Am J Med 52: 63-8, 1972), слабой пролиферации Т-клеток (Alexander JP et al., Cancer Res 53: 1380-7, 1993), причиной ослабления продукции цитокинов (Horiguchi S et al., Cancer Res 59: 2950-6, 1999) и дефектной сигнальной трансдукции Т-клеток и природных клеток-киллеров (Kono K et al., Clin Cancer Res 11: 1825-8, 1996, Kiessling R et al., Cancer Immunol Immunother 48: 353-62, 1999).
Для улучшения клинической эффективности иммунотерапии важным является преодоление эффекта иммуносупрессивных факторов, индуцированных опухолями. Иммунологическую толерантность и защиту от аутоиммунности обеспечивают центральный и периферический механизмы, включая клональную делецию самоактивирующихся T-клеток в тимусе и индукцию анэргии при встрече с аутоантигенами на периферии. Недавно стало ясно, что регуляторные Т-клетки (T-reg), характеризующиеся ко-экспрессией маркеров CD4 и CD25, представляют собой функционально уникальную популяцию Т-клеток и функционируют для поддержания иммунного гомеостаза (Sakaguchi S et al., J Immunol. 155: 1151-64, 1995, Dieckmann D et al., J Exp Med 193: 1303-10, 2001). Клетки T-reg являются одним из главных участников подавления различных типов иммунного ответа (Miescher S et al., J Immunol 136: 1899-907, 1986; Young RC et al., Am J Med 52: 63-72, 1972; Alexander JP et al., Cancer Res 53: 1380-7, 1997; Horiguchi S et al., Cancer Res 59: 2950-6, 1999; Kono K et al., Clin Cancer Res 11: 1825-8, 1996; Kiessling R et al., Cancer Immunol Immunother 48: 353-62, 1999).
Хотя молекулярные взаимодействия и сигнальные пути, которые являются важными для создания и функционирования клеток T-reg, еще до конца не ясны, клетки T-reg требуют наличия транскрипционного фактора скурфин (scurfin) семейства Forkhead (Foxp3; SEQ ID NO:2), кодируемого геном Foxp3 (GenBank Accession No. NM_014009; SEQ ID NO:1), который контролирует их развитие и регуляторные свойства (Fontenot JD et al., Nat Immunol 4: 330-6, 2003, Hori S et al., Science 299: 1057-61, 2003, Khattri R et al., Nat Immunol 4: 304-6, 2003). Кроме того, вакцинация мышей дендритными клетками, трансфецированными мРНК Foxp3, вызывает Foxp3-специфичный ответ клеток CTL (Smita N et al., Cancer Res. Jan 1; 67(l):371-80, 2007).
Таким образом, Foxp3 служит мишенью для противораковой иммунотерапии и, более того, неполные пептиды белка, кодируемого геном Foxp3, служат в качестве антигенов, распознаваемых клетками CTL.
Сущность изобретения
Для повышения клинической эффективности иммунотерапии важно подавить иммуносупрессивные факторы, индуцированные опухолью. Было обнаружено, что клетка T-reg является одним из главных участников подавления различных типов иммунного ответа. Таким образом, необходимо разработать вакцины, направленные на клетки T-reg, экспрессирующие Foxp3, чтобы подавить T-reg-индуцированную иммуносупрессию.
Настоящее изобретение основано, по крайне мере отчасти, на идентификации пептидов эпитопа генного продукта Foxp3, которые вызывают ответ цитотоксических Т-лимфоцитов (CTL), специфичных к соответствующим пептидам Foxp3 или эпитопам. Мононуклеарные клетки периферической крови (PBMC) здорового донора стимулировали, используя HLA-A*24- и HLA-A*02-связывающие кандидатные пептиды Foxp3. Было показано, что эти пептиды являются пептидами с эпитопами, ограниченными HLA-A24- или HLA-A02, которые могут индуцировать эффективный и специфичный иммунный ответ в отношении клеток T-reg, экспрессирующих Foxp3.
Соответственно, настоящее изобретение относится к способам регуляции иммуносупрессии, включающим стадию введения полипептидов Foxp3 по изобретению. Антииммуносупрессия (т.е. реверсия или противодействие иммуносупрессии), например, цитотоксических T-лимфоцитов индуцируется с помощью введения полипептидов Foxp3. Таким образом, настоящее изобретение относится к способам индукции антииммуносупрессии, включающим стадию введения полипептидов Foxp3, а также к фармацевтическим средствам для регуляции иммуносупрессии, включающим полипептиды Foxp3.
В одном аспекте изобретение относится к пептидам, содержащим или состоящим из аминокислотной последовательности, выбранной из группы, состоящей из последовательностей SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74.
В другом аспекте изобретение относится к пептидам, обладающим способностью индуцировать цитотоксические Т-клетки, содержащим или состоящим из аминокислотной последовательности, выбранной из группы:
(a) SEQ ID NO:3-5, 7-9, 12, 17, 67 или 74; и
(b) SEQ ID NO:3-5, 7-9, 12, 17, 67 или 74, в которых заменены или введены 1, 2 или несколько аминокислот.
В следующем аспекте изобретение относится к пептидам, обладающим способностью индуцировать цитотоксические Т-клетки, содержащим или состоящим из аминокислотной последовательности, выбранной из группы:
(a) SEQ ID NO:15-19, 22, 24, 27-30 или 37, и
(b) SEQ ID NO:15-19, 22, 24, 27-30 или 37, в которых заменены или введены 1, 2 или несколько аминокислот.
Что касается вариантов осуществления, в некоторых вариантах осуществления второй аминокислотой с N-конца является фенилаланин, тирозин, метионин или триптофан. В некоторых вариантах осуществления C-концевой аминокислотой является фенилаланин, лейцин, изолейцин, триптофан или метионин. В некоторых вариантах осуществления второй аминокислотой с N-конца является лейцин или метионин. В некоторых вариантах осуществления C-концевой аминокислотой является валин или лейцин. Например, пептид, содержащий замены, содержит аминокислотную последовательность SEQ ID NO:95, 97 или 98.
Изобретение дополнительно относится к композициям, содержащим пептиды Foxp3 по изобретению или полинуклеотиды, кодирующие пептиды Foxp3 по изобретению, и фармацевтически приемлемый носитель или эксципиент. В некоторых вариантах осуществления композиции приготовлены для введения в виде вакцины.
Композиции могут содержать один пептид или множество различных пептидов Foxp3 по изобретению. Композиции могут применяться для ингибирования клеток T-reg, например для ингибирования пролиферации или подавления функции клетки T-reg.
В некоторых вариантах осуществления композиции содержат один или несколько пептидов Foxp3, которые вызывают иммунный ответ, который ингибирует клетки T-reg у индивида, антиген HLA которого представляет собой HLA-A24. В некоторых вариантах осуществления композиции содержат один или несколько пептидов Foxp3, которые вызывают иммунный ответ, который ингибирует клетки T-reg у индивида, антиген HLA которого представляет собой HLA-A02.
В другом аспекте изобретение относится к композициям, содержащим полинуклеотид, кодирующий пептид Foxp3 по изобретению. В некоторых вариантах осуществления композиции содержат множество (т.е. два или несколько) полинуклеотидов, кодирующих множество пептидов Foxp3 по изобретению. В некоторых вариантах осуществления композиции содержат полинуклеотид, который кодирует множество пептидов Foxp3 по изобретению.
В некоторых вариантах осуществления композиции содержат другой пептид, который обладает способностью индуцировать цитотоксические Т-клетки против раковых клеток, или содержат другой полинуклеотид, кодирующий этот другой пептид.
В следующем аспекте изобретение относится к экзосоме, которая презентирует на своей поверхности комплекс, содержащий антиген HLA и пептид Foxp3 по изобретению. В некоторых вариантах осуществления антиген HLA выбран из группы, состоящей из антигенов HLA-A24, HLA-A2402, HLA-A02 и HLA-A0201.
В подобном аспекте изобретение относится к способам лечения рака (например, уменьшения роста опухолевых клеток, стимулирования смерти опухолевых клеток) путем введения индивиду пептида Foxp3 или полинуклеотида, кодирующего этот пептид Foxp3.
В другом аспекте изобретение относится к способам индукции антиген-презентирующих клеток, обладающих высокой способностью индуцировать цитотоксические Т-клетки, путем введения пептида Foxp3 по изобретению или полинуклеотида, кодирующего этот пептид Foxp3.
В другом аспекте изобретение относится к способам индукции цитотоксических Т-клеток путем введения пептида Foxp3 по изобретению или полинуклеотида, кодирующего этот пептид Foxp3.
В подобном аспекте изобретение относится к выделенной цитотоксической Т-клетке, индуцируемой пептидом Foxp3 по изобретению.
В другом аспекте изобретение относится к антиген-презентирующей клетке, которая содержит комплекс, образованный антигеном HLA и пептидом Foxp3 по изобретению. В некоторых вариантах осуществления антиген-презентирующая клетка является выделенной.
В следующем аспекте изобретение относится к способам регуляции клеток T-reg у индивида, включающим введение индивиду вакцины, содержащей пептид Foxp3 по изобретению или иммунологически активный фрагмент пептида или полинуклеотид, кодирующий этот пептид.
При применении способов лечения индивидуумом или пациентом может являться человек.
Следует понимать, что и описанная выше сущность изобретения, и следующее подробное описание представляют собой конкретные варианты осуществления и не ограничивают изобретение или другие альтернативные варианты осуществления изобретения.
Краткое описание фигур
Фиг.1. На фиг.1 изображены фотографии, показывающие результаты анализа IFN-γ-ELISPOT на клетках CTL, которые индуцировали пептидами, полученными из Foxp3. На фиг.1A клетки CTL в лунках с номерами #2 и 7, стимулированные Foxp3-A24-9-363 (SEQ ID NO:3), #1 и #6, стимулированные Foxp3-A24-9-366 (SEQ ID NO:7), #5, стимулированные Foxp3-A24-9-190 (SEQ ID NO:9) и #7, стимулированные Foxp3-A24-10-87 (SEQ ID NO:67) и Foxp3-A24-10-60 (SEQ ID NO:74), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.1B клетки CTL в лунке под номером #4, стимулированные Foxp3-A24-9-207 (SEQ ID NO:4), #6, стимулированные Foxp3-A24-9-332 (SEQ ID NO:5), #6, стимулированные Foxp3-A24-9-337 (SEQ ID NO:8), и #1, стимулированные Foxp3-A24-10-l14 (SEQ ID NO:12), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем.
Фиг.2A-B. На фиг.2 изображены фотографии, показывающие результаты анализа IFN-γ-ELISPOT на клетках CTL, которые индуцировали пептидами, полученных из Foxp3. На фиг.2A, клетки CTL в лунке под номером #2, стимулированные Foxp3-A2-9-390 (SEQ ID NO:15), #2, стимулированные Foxp3-A2-9-69 (SEQ ID NO:16), #6, стимулированные Foxp3-A2-9-252 (SEQ ID NO:17), #4, стимулированные Foxp3-A2-10-359 (SEQ ID NO:22), #7, стимулированные Foxp3-A2-263 (SEQ ID NO:24), и #2 и #5, стимулированные Foxp3-A2-10-94 (SEQ ID NO:27), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.2B, клетки CTL во всех лунках, стимулированные Foxp3-A2-10-233 (SEQ ID NO:28), в лунках с номерами #6 и #7, стимулированные Foxp3-A2-10-152 (SEQ ID NO:29), #5, стимулированные Foxp3-A2-10-77 (SEQ ID NO:30), и #l, стимулированные Foxp3-A2-10-246 (SEQ ID NO:37) и Foxp3-A2-10-94 (SEQ ID NO:27), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем.
Фиг.2C. На фиг.2C, клетки CTL в лунках с номерами #1, #2, #4, #5, #7, #9, #11 и #12, стимулированные Foxp3-A2-9-390 (SEQ ID NO:15), #5 и #11, стимулированные Foxp3-A2-9-304 (SEQ ID NO:19), #7, стимулированные Foxp3-A2-9-68 (SEQ ID NO:7), и #12, стимулированные Foxp3-A2-9-252 (SEQ ID NO:17), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем.
Фиг.3A-D. На фиг.3 показано, что клетки в положительных лунках были размножены и был осуществлен анализ IFN-γ-ELISA. На фиг.3A, B и C, клеточные линии CTL, стимулированные Foxp3-A02-9-390 (SEQ ID NO:15) (сплошной ромб), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем (сплошной квадрат). На фиг.3D, клеточные линии CTL, стимулированные Foxp3-A02-9-252 (SEQ ID NO:17) (сплошной ромб), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем (сплошной квадрат).
Фиг.3E-G. На фиг.3E, клеточные линии CTL, стимулированные Foxp3-A24-10-60 (SEQ ID NO:74) (сплошной ромб), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем (сплошной квадрат). На фиг.3F клеточные линии CTL, стимулированные Foxp3-A02-10-94 (SEQ ID NO:27) (сплошной ромб), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем (сплошной квадрат). На фиг.3G клеточные линии CTL, стимулированные Foxp3-A24-10-87 (SEQ ID NO:67) (сплошной ромб), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем (сплошной квадрат).
Фиг.4. На фиг.4 показана специфичная активность клеток CTL в отношении клеток-мишеней, эндогенно экспрессирующих Foxp3 и HLA-A* 02 или 24. На фиг.4A и B, клеточные линии CTL, выращенные в присутствии Foxp3-A02-9-390 (SEQ ID NO:15) и Foxp3-A02-9-252 (SEQ ID NO:17), продемонстрировали высокоспецифичную активность клеток CTL в отношении клеток 293T, которые были трансфецированы с помощью обоих генов Foxp3 и HLA-A02. С другой стороны, не было продемонстрировано существенной специфичной активности клеток CTL в отношении контролей. На фиг.4C, клеточные линии CTL, выращенные в присутствии Foxp3-A02-9-252 (SEQ ID NO:17) продемонстрировали высокоспецифичную активность клеток CTL в отношении клеток 293T, которые были трансфецированы с помощью обоих генов Foxp3 и HLA-A24. С другой стороны, не было продемонстрировано существенной специфичной активности клеток CTL в отношении контролей.
Фиг.5. На фиг.5 показан in vivo анализ иммуногенности пептида Foxp3-252_h и пептида Foxp3-252_m. IFA-конъюгированный пептид или индивидуально IFA вводили подкожно мышам BALB/c в дни 0 и 7. На 14 день спленоциты вакцинированных мышей собирали и использовали в качестве клеток-респондеров. 1×104 RLmalel клеток, стимулированных соответствующим пептидом (сплошной квадрат) или в отсутствие пептида (не закрашенный квадрат), использовали для анализа IFN-γ-ELISPOT. Вакцинацию с использованием Foxp3-252_h (A) и Foxp3-252_m (B) осуществляли пяти мышам (M1-M5) и в качестве контроля в каждом анализе осуществляли инъекцию IFA в отсутствие какого-либо пептида трем мышам (N1-N3).
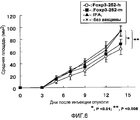
Фиг.6. На фиг.6 показаны in vivo противоопухолевые эффекты вакцинации с использованием пептида эпитопа Foxp3. 1×105 клеток клеточной линии 4Tl рака груди вводили мышам BALB/c в день 0. IFA-конъюгированный пептид Foxp3-252_h (-не закрашенный круг-), IFA-конъюгированный пептид Foxp3-252_m (-сплошной квадрат-), индивидуально IFA в отсутствие пептида (-сплошной треугольник-) вводили в дни 3 и 10. В качестве контроля нормального роста опухоли в этом анализе также получали невакцинированных мышей (-x-). Наблюдали существенное отличие в подавлении роста опухоли при вакцинации с помощью пептида эпитопа Foxp3. *, P<0,01; **, P<0,005.
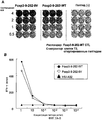
Фиг.7A-B. На фиг.7 показан анализ аффинности пептида Foxp3-9-252, содержащего замены, в отношении молекулы HLA. На фиг.7A клетки CTL, индуцированные Foxp3-9-252-WT, распознают клетки, презентирующие пептид Foxp3-9-252-9V на молекуле HLA-A2. Осуществляли IFN-γ-ELISPOT анализ с использованием клеточной линии CTL, индуцированной пептидом Foxp3-9-252-WT, в качестве клеток-респондеров, и клеток T2, стимулированных пептидом Foxp3-9-252-WT или пептидом Foxp3-9-252-9V, в качестве стимулирующих клеток соответственно. Клетки T2 без стимулирования пептидом получали в качестве контроля. На фиг.7B Foxp3-9-252-9V и Foxp3-9-252-WT продемонстрировали сходную аффинность в отношении молекулы HLA-A2. Осуществляли анализ IFN-γ-ELISA с использованием клеточной линии CTL, индуцированной пептидом Foxp3-9-252-WT, в качестве клеток-респондеров (1×105 клеток/лунка), и клеток T2, стимулированных пептидом Foxp3-9-252-WT (-сплошной круг-), пептидом Foxp3-9-252-9V (-не закрашенный круг-) или HIV-A02 (-сплошной треугольник-), в качестве стимулирующих клеток (1×104 клеток/лунка). Пептидное стимулирование стимулирующих клеток проводили при 37 градусах по Цельсию в течение 2 часов с каждым типом пептида и с каждой концентрацией пептида.
Фиг.7C-D. На фиг.7C клетки CTL могли быть индуцированы с помощью стимулирования пептидом Foxp3-9-252, содержащим замены, нацеленного на молекулу HLA-A2. Клетки CTL для всех пептидов, содержащих замены, нацеленных на молекулу HLA-A2, получали таким способом, как описано в разделе "Материалы и способы". Клетки в лунках с номерами 3 и 7, стимулированные Foxp3-9-252-3M, в лунке под номером 7, стимулированные Foxp3-9-252-3L, и в лунке под номером 8, стимулированные Foxp3-9-252-9V, продемонстрировали продуцирование IFN-γ по сравнению с контролем. На фиг.7D клетки CTL, полученные с помощью Foxp3-9-252-9V, распознают стимулирующие клетки, покрытые пептидом Foxp3-9-252-WT. Клеточную линию CTL, индуцированную с помощью Foxp3-9-252-9V-пептида, использовали в качестве клеток-респондеров. Клетки T2, инкубированные в присутствии пептида Foxp3-9-252-9V (-сплошной круг-), или в присутствии пептида Foxp3-9-252-WT (-не закрашенный круг-), или в отсутствие пептида (-не закрашенный квадрат-), использовали в данном анализе в качестве стимулирующих клеток (1×104 клеток/лунка).
Подробное описание изобретения
I. Определения
Термины "полипептид", "пептид" и "белок" используются в описании взаимозаменяемо и означают полимер, состоящий из аминокислотных остатков. Термины применяют к аминокислотным полимерам, в которых один или несколько аминокислотных остатков являются модифицированными остатками или синтетическими остатками, например, к искусственному химическому миметику соответствующей природной аминокислоты, кроме того, термины применяют к природным аминокислотным полимерам.
Как используется в настоящем описании, термин "аминокислота" означает природные и синтетические аминокислоты, а также аналоги аминокислот и миметики аминокислот, которые функционируют подобно природным аминокислотам. Природные аминокислоты представляют собой аминокислоты, которые кодируются генетическим кодом, а также аминокислоты, модифицированные после трансляции в клетках (например, гидроксипролин, γ-карбоксиглутамат и O-фосфосерин). Термин "аналог аминокислоты" означает соединения, которые имеют такую же основную химическую структуру (атом альфа-углерода, связанный с водородом, карбоксигруппа, аминогруппа и R-группа), как и природная аминокислота, но имеют модифицированную R-группу или модифицированные остовы (например, гомосерин, норлейцин, метионин сульфоксид, метионин метилсульфоний). Термин "миметик аминокислоты" означает химические соединения, которые имеют отличную структуру, но функцию, сходную с функцией основных аминокислот.
Аминокислоты обозначаются в данном случае с помощью общеизвестных трехбуквенных символов или однобуквенных символов, рекомендованных Комиссией Биохимической Номенклатуры IUPAC-IUB.
Термины "ген", "полинуклеотиды", "нуклеотиды" и "нуклеиновые кислоты" используются взаимозаменяемо, если не указано иное, и аналогично аминокислотам обозначаются с помощью общепринятых однобуквенных кодов.
Если не указано иного, все технические и научные термины, используемые в описании, имеют значение, общепринятое в кругу специалистов в данной области, к которой относится настоящее изобретение. В случае возникновения разночтения настоящее описание, в том числе определения, следует истолковывать как руководство.
II. Пептиды
Для того чтобы продемонстрировать, что пептиды, полученные из Foxp3, функционируют как антигены, распознаваемые цитотоксическими Т-клетками (CTL), в настоящем изобретении были проанализированы пептиды, которые являются подпоследовательностями Foxp3, на предмет того, являются ли они антигенными эпитопами, ограниченными HLA-A24 или HLA-A02, которые являются широко распространенными на земле HLA-аллелями (Date Y et al., Tissue Antigens 47: 93-101, 1996; Kondo A et al., J Immunol 155: 4307-12, 1995; Kubo RT et al., J Immunol 152: 3913-24, 1994). Возможные HLA-A24- и HLA-A02-связывающие пептиды, которые являются подпоследовательностями Foxp3, идентифицировали на основе информации об аффинности связывания с HLA-A24 и HLA-A02. После in vitro стимуляции T-клеток дендритными клетками (DC), инкубированными с этими пептидами, успешно получали клетки CTL, используя последовательности:
Foxp3-A24-9-363 (SEQ ID NO:3),
Foxp3-A24-9-366 (SEQ ID NO:7),
Foxp3-A24-9-190 (SEQ ID NO:9),
Foxp3-A24-9-207 (SEQ ID NO:4),
Foxp3-A24-9-332 (SEQ ID NO:5),
Foxp3-A24-9-337 (SEQ ID NO:8),
Foxp3-A24-10-114 (SEQ ID NO:12),
Foxp3-A2-9-390 (SEQ ID NO:15),
Foxp3-A2-9-69 (SEQ ID NO:16),
Foxp3-A2-9-252 (SEQ ID NO:17),
Foxp3-A2-10-359 (SEQ ID NO:22),
Foxp3-A2-10-263 (SEQ ID NO:24),
Foxp3-A2-10-94 (SEQ ID NO:27),
Foxp3-A2-10-233 (SEQ ID NO:28),
Foxp3-A2-10-152 (SEQ ID NO:29),
Foxp3-A2-10-77 (SEQ ID NO:30),
Foxp3-A2-10-246 (SEQ ID NO:37),
Foxp3-A2-9-68 (SEQ ID NO:18),
Foxp3-A2-9-304 (SEQ ID NO:19),
Foxp3-A24-10-87 (SEQ ID NO:67) и
Foxp3-A24-10-60 (SEQ ID NO:74).
Полученные клетки CTL показали эффективную специфичную CTL-активность в отношении клеток-мишеней, стимулированных пептидом. Эти результаты согласуются с выводом о том, что Foxp3 является антигеном, распознаваемым клетками CTL, и что последовательности
Foxp3-A24-9-363 (SEQ ID NO:3),
Foxp3-A24-9-366 (SEQ ID NO:7),
Foxp3-A24-9-190 (SEQ ID NO:9),
Foxp3-A24-9-207 (SEQ ID NO:4),
Foxp3-A24-9-332 (SEQ ID NO:5),
Foxp3-A24-9-337 (SEQ ID NO:8),
Foxp3-A24-10-114 (SEQ ID NO:12),
Foxp3-A2-9-390 (SEQ ID NO:15),
Foxp3-A2-9-69 (SEQ ID NO:16),
Foxp3-A2-9-252 (SEQ ID NO:17),
Foxp3-A2-10-359 (SEQ ID NO:22),
Foxp3-A2-10-263 (SEQ ID NO:24),
Foxp3-A2-10-94 (SEQ ID NO:27),
Foxp3-A2-10-233 (SEQ ID NO:28),
Foxp3-A2-10-152 (SEQ ID NO:29),
Foxp3-A2-10-77 (SEQ ID NO:30),
Foxp3-A2-10-246 (SEQ ID NO:37),
Foxp3-A2-9-68 (SEQ ID NO:18),
Foxp3-A2-9-304 (SEQ ID NO:19),
Foxp3-A24-10-87 (SEQ ID NO:67) и
Foxp3-A24-10-60 (SEQ ID NO:74) представляют собой пептиды эпитопов, ограниченных HLA-A24 и HLA-A2. Так как Foxp3 экспрессируется в клетках большинства пациентов, больных раком, и связан с иммуносупрессией, индуцированной иммуносупрессивными факторами опухолями, то Foxp3 представляет собой приемлемую мишень для иммунотерапии с целью стимулирования клинической эффективности антиген-специфичной противораковой иммунотерапии.
Таким образом, настоящее изобретение относится к нонапептидам (пептидам, состоящим из девяти аминокислотных остатков) и декапептидам (пептидам, состоящим из десяти аминокислотных остатков). Пептиды Foxp3 по изобретению связываются с молекулой HLA и индуцируют цитотоксическую активность цитотоксических Т-лимфоцитов (CTL). Более конкретно, настоящее изобретение относится к пептидам, состоящим из аминокислотной последовательности, выбранной из группы последовательностей SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74.
Как правило, для компьютерного расчета аффинности связывания различных пептидов и антигенов HLA и может использоваться программное обеспечение, доступное в настоящий момент из сети Интернет, например программы, описанные у Parker KC. et al, в J Immunol. 1994 Jan 1; 152(1): 163-75. Аффинность связывания с антигенами HLA может измеряться in vitro, как описано, например, у Parker KC. et al, в J Immunol. 1994 Jan l;152(l):163-75.; Nukaya I. et al, Int J Cancer. 1999 Jan 5;80(l):92-7.; Kuzushima K, et al.( (2001) Blood.;98(6):1872-81.; Journal of Immunological Methods, 1995, 185: 181-190.; Protein Science, 2000, 9: 1838-1846).
Кроме того, пептиды Foxp3 по настоящему изобретению могут фланкироваться дополнительными аминокислотными остатками при условии сохранения пептидами Foxp3 способности индуцировать клетки CTL. Такие пептиды, обладающие способностью индуцировать клетки CTL, могут содержать менее чем примерно 40 аминокислот, например менее чем примерно 20 аминокислот, например менее чем примерно 15 аминокислот. Аминокислотная последовательность, фланкирующая пептиды, состоящие из аминокислотной последовательности, выбранной из группы последовательностей SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 и 74, не ограничена и может содержать аминокислоты любого типа, если они не ингибируют способность пептида индуцировать клетки CTL. Таким образом, настоящее изобретение также относится к пептидам, обладающим способностью индуцировать клетки CTL, причем пептиды включают аминокислотную последовательность, выбранную из группы последовательностей SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 и 74.
По существу, известно, что модификация одной или нескольких аминокислот в белке не влияет на функцию белка или в некоторых случаях даже усиливает желаемую функцию исходного белка. Фактически известно, что модифицированные пептиды (т.е. пептиды, содержащие аминокислотную последовательность, модифицированную заменой или вставкой одной, двух или нескольких аминокислотных остатков в исходную указанную последовательность) сохраняют биологическую активность исходного пептида (Mark et al., Proc Natl Acad Sci USA 81: 5662-6, 1984; Zoller and Smith, Nucleic Acids Res 10: 6487-500, 1982; Dalbadie-McFarland et al., Proc Natl Acad Sci USA 79: 6409-13, 1982. Таким образом, в соответствии с одним из вариантов осуществления изобретения пептид, обладающий способностью индуцировать клетки CTL, по настоящему изобретению может содержать аминокислоты, включающие аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, где одна или несколько аминокислот вставлены и/или заменены.
Специалисту в данной области будет понятно, что индивидуальные вставки или замены в аминокислотной последовательности, которые изменяют одну аминокислоту или небольшой процент аминокислот, приводят в результате к сохранению свойств аминокислотной боковой цепи; их, таким образом, обозначают как "консервативная замена" или "консервативная модификация", при этом изменение белка приводит в результате к получению белка с подобными функциями. Таблицы консервативных замен, на которых представлены функционально подобные аминокислоты, хорошо известны в данной области. Примеры свойств аминокислотных боковых цепей представляют собой гидрофобные аминокислоты (A, I, L, M, F, P, W, Y, V), гидрофильные аминокислоты (R, D, N, C, E, Q, G, H, K, S, T) и боковые цепи, содержащие совокупно следующие функциональные группы или характеристики: алифатическую боковую цепь (G, A, V, L, I, P); боковую цепь, содержащую гидроксильную группу (S, T, Y); боковую цепь, содержащую атом серы (C, M); боковую цепь, содержащую карбоновую кислоту и амид (D, N, E, Q); боковую цепь, содержащую основание (R, K, H); и боковую цепь, содержащую ароматическую группу (H, F, Y, W). Кроме того, каждая из следующих восьми групп содержит аминокислоты, которые представляют собой консервативные замены друг другу:
1) аланин (A), глицин (G);
2) аспарагиновая кислота (D), глутаминовая кислота (E);
3) аспарагин (N), глутамин (Q);
4) аргинин (R), лизин (K);
5) изолейцин (I), лейцин (L), метионин (M), валин (V);
6) фенилаланин (F), тирозин (Y), триптофан (W);
7) серин (S), треонин (T) и
8) цистеин (C), метионин (M) (см., например, Creighton, Proteins (1984)).
Такие консервативно модифицированные пептиды также рассматриваются как пептиды по настоящему изобретению. Однако пептид по настоящему изобретению не ограничен ими и может включать неконсервативные модификации, при условии, что пептид сохраняет способность индуцировать клетки CTL. Кроме того, модифицированные пептиды не исключают CTL-индуцируемые пептиды полиморфных вариантов, межвидовых гомологов и аллелей Foxp3.
Специалист может модифицировать (вставить или заменить) только небольшое количество (например, 1, 2 или несколько) или небольшой процент аминокислотных остатков, сохраняя требуемую способность индуцировать клетки CTL (т.е. активировать CTL). В данном случае термин "несколько" означает 5 или менее или, например, 3 или менее. Процент модифицированных аминокислотных остатков может составлять 20% или менее, например 15% или 10% или менее, например 1-5% всех аминокислот последовательностей SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 и 74. В настоящем изобретении рассматриваются пептиды Foxp3, обладающие по меньшей мере 95%, 96%, 97%, 98%, 99% аминокислотной идентичностью последовательности со всеми идентифицированными последовательностями. Идентичность последовательности может быть измерена с использованием любого алгоритма, известного в данной области, например BLAST, доступного через Национальный Центр Биотехнологической Информации (по адресу ncbi.nlm.nih.gov/blast/Blast.cgi).
Анализ гомологии (т.е. идентичности последовательности) представленных пептидов
Foxp3-A24-9-363 (SEQ ID NO:3),
Foxp3-A24-9-366 (SEQ ID NO:7),
Foxp3-A24-9-190 (SEQ ID NO:9),
Foxp3-A24-9-207 (SEQ ID NO:4),
Foxp3-A24-9-332 (SEQ ID NO:5),
Foxp3-A24-9-337 (SEQ ID NO:8),
Foxp3-A24-10-114 (SEQ ID NO:12),
Foxp3-A2-9-390 (SEQ ID NO:15),
Foxp3-A2-9-69 (SEQ ID NO:16),
Foxp3-A2-9-252 (SEQ ID NO:17),
Foxp3-A2-10-359 (SEQ ID NO:22),
Foxp3-A2-10-263 (SEQ ID NO:24),
Foxp3-A2-10-94 (SEQ ID NO:27),
Foxp3-A2-10-233 (SEQ ID NO:28),
Foxp3-A2-10-152 (SEQ ID NO:29),
Foxp3-A2-10-77 (SEQ ID NO:30),
Foxp3-A2-10-246 (SEQ ID NO:37),
Foxp3-A2-9-68 (SEQ ID NO:18),
Foxp3-A2-9-304 (SEQ ID NO:19),
Foxp3-A24-10-87 (SEQ ID NO:67) и
Foxp3-A24-10-60 (SEQ ID NO:74) показал, что они не имеют существенной гомологии с пептидами, полученными из любых других известных генных продуктов. Это снижает возможность неизвестных или нежелательных иммунных ответов при использовании для иммунотерапии.
Как используется в иммунотерапии, пептиды по настоящему изобретению будут представлены на поверхности клетки или экзосомы в виде комплекса с антигеном HLA. Таким образом, выбирают пептиды, обладающие высокой аффинностью связывания с антигеном HLA кроме их способности индуцировать клетки CTL. Более того, пептиды могут быть модифицированы заменой, вставкой и подобными модификациями аминокислотных остатков с достижением более высокой аффинности связывания. Кроме пептидов, которые обнаруживаются естественным образом, так как известна закономерность (т.е. соответствие) последовательностей пептидов, обнаруживающихся при связывании с антигенами HLA (J Immunol 152: 3913, 1994; Immunogenetics 41: 178, 1995; J Immunol 155: 4307, 1994), могут быть осуществлены модификации иммуногенных пептидов по изобретению на основе такой закономерности. Например, пептиды, проявляющие высокую аффинность связывания HLA-A24, могут содержать замену второй аминокислоты с N-конца на фенилаланин, тирозин, метионин или триптофан, а также пептиды, аминокислота которых с С-конца заменена на фенилаланин, лейцин, изолейцин, триптофан или метионин. С другой стороны, пептиды, у которых вторая аминокислота с N-конца заменена на лейцин или метионин и у которых С-концевая аминокислота заменена на валин или лейцин, могут использоваться в качестве пептидов, обладающих высокой аффинностью связывания HLA-A02. Замену осуществляют не только концевых аминокислот, но также в положении возможного сайта TCR-распознавания пептидов. В статье Zaremba et al. показано, что аминокислотные замены в пептиде CAP1 могут быть эквивалентны или лучше, чем у исходного пептида (Cancer Res. 57, 4570-4577, 1997). Например, пептид, содержащий замены, содержит аминокислотную последовательность SEQ ID NO:95, 97 или 98. Кроме того, на N- и/или C-конце пептидов также могут быть добавлены одна или две аминокислоты. Такие модифицированные пептиды с высокой аффинностью связывания антигена HLA также включены в настоящее изобретение.
Однако, если последовательность пептида идентична части аминокислотной последовательности эндогенного или экзогенного белка, с отличной функцией, то могут возникать побочные эффекты, такие как аутоиммунные нарушения или аллергические реакции в отношении определенных веществ. Таким образом, поиск гомологии может осуществляться с использованием доступных баз данных, чтобы избежать, уменьшить или минимизировать ситуации, при которых последовательность пептида имеет гомологичную аминокислотную последовательность с другим белком. Если при поиске гомологии становится ясно, что не существует пептида, имеющего 1 или 2 отличия по аминокислотам по сравнению с заданным пептидом, то заданный пептид может быть модифицирован для увеличения аффинности связывания с антигенами HLA и/или увеличения способности индуцировать клетки CTL без какой-либо опасности побочных эффектов.
Пептиды, обладающие аффинностью связывания с антигенами HLA, как описано выше, являются высокоэффективными. Возможные пептиды, которые выбирают по наличию высокой аффинности связывания, также могу быть проанализированы на фактическое присутствие способности индуцировать клетки CTL. В данном случае фраза "способность индуцировать клетки CTL" указывает на способность пептида индуцировать клетки CTL, если он представлен на антиген-презентирующих клетках. Кроме того, "способность индуцировать клетки CTL" включает способность пептида индуцировать активацию клеток CTL, пролиферацию клеток CTL и включает способность пептида повышать продукцию IFN-γ.
Подтверждение способности индуцировать клетки CTL может быть осуществлено путем индукции антиген-презентирующих клеток, несущих антигены MHC человека (например, B-лимфоцитов, макрофагов и дендритных клеток), или, более конкретно, дендритных клеток, полученных из мононуклеарных лейкоцитов периферической крови человека, и после стимулирования пептидами путем смешивания с CD8-положительными клетками и последующего измерения IFN-γ, продуцированного и высвобожденного клетками CTL против клеток-мишеней. В качестве реакционной системы может использоваться трансгенное животное, которое получено для экспрессии антигена HLA человека (например, описанные BenMohamed L, Krishnan R, Longmate J, Auge C, Low L, Primus J, Diamond DJ, в Hum Immunol 61(8): 764-79, 2000, август, связанные статьи, книги, Link out Induction of CTL response by a minimal epitope vaccine in HLA A*0201/DRl transgenic mice: dependence on HLA class II restricted T(H) response). Например, клетки-мишени могут быть радиоактивно меченными 51Cr и тому подобное, и цитотоксическая активность может быть рассчитана исходя из радиоактивности, высвобожденной из клеток-мишеней. Альтернативно, активность может быть определена путем измерения IFN-γ, полученного и выделенного клетками CTL в присутствии антиген-презентирующих клеток, которые несут иммобилизованные пептиды, и с помощью визуализации в среде зоны ингибирования с использованием моноклональных антител против IFN-γ.
В результате определения у пептидов способности индуцировать клетки CTL, как описано выше, было установлено, что пептиды, обладающие высокой аффинностью связывания в отношении антигена HLA, необязательно обладают высокой способностью индуцировать клетки. Кроме того, нонапептиды или декапептиды, выбранные из пептидов, содержащих аминокислотные последовательности, обозначенные последовательностями SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, показали особенно высокую способность индуцировать клетки CTL, а также высокую аффинность связывания с антигеном HLA.
Кроме вышеуказанной модификации пептидов по настоящему изобретению, пептиды по настоящему изобретению могут быть дополнительно связаны с другими веществами, при условии сохранения способности индуцировать клетки CTL. Используемые вещества включают: пептиды, липиды, сахара и цепи сахаров, ацетильные группы, природные и синтетические полимеры и т.д. Пептиды могут содержать модификации, такие как гликозилирование, окисление боковой цепи или фосфорилирование; при условии, что модификации не нарушают биологической активности пептидов, как описано выше. Такие типы модификаций могут осуществляться для придания дополнительных функций (например, направляющей функции и функции доставки) или для стабилизации полипептида.
Например, как известно в данной области, для увеличения in vivo стабильности полипептида вводят подходящие разнообразные D-аминокислоты, аминокислотные миметики или неприродные аминокислоты; данная концепция также может быть адоптирована для полипептидов по настоящему изобретению. Стабильность полипептида может оцениваться рядом способов. Например, для определения стабильности использовали пептидазы и разнообразные биологические среды, такие как плазма и сыворотка человека (см., например, публикацию Verhoef et al., Eur J Drug Metab Pharmacokin 11: 291-302, 1986).
III. Получение пептидов
Пептиды по изобретению могут быть получены с использованием хорошо известных методов. Например, пептиды могут быть получены синтетически, технологиями рекомбинантной ДНК или химическим синтезом. Пептиды по изобретению могут быть синтезированы независимо или в виде более длинных полипептидов, включая два или несколько пептида (например, два или несколько пептидов Foxp3 или пептид Foxp3 и пептид, отличный от пептида Foxp3). Пептиды могут быть выделены, т.е. очищены, и являются, по существу, свободными от других природных белков клетки-хозяина и их фрагментов, например, могут быть очищены по меньшей мере примерно на 70%, 80% или 90%.
Пептид по настоящему изобретению может быть получен химическим синтезом на основе выбранной аминокислотной последовательности. Например, подходящие способы пептидного синтеза, которые могут быть использованы для синтеза, включают:
(i) Peptide Synthesis, Interscience, New York, 1966;
(ii) The Proteins, Vol. 2, Academic Press, New York, 1976;
(iii) Peptide Synthesis (in Japanese), Maruzen Co., 1975;
(iv) Basics and Experiment of Peptide Synthesis (in Japanese), Maruzen Co., 1985;
(v) Development of Pharmaceuticals (second volume) (in Japanese), Vol. 14 (peptide synthesis), Hirokawa, 1991;
(vi) WO99/67288; и
(vii) Barany G. & Merrifield R.B., Peptides Vol. 2, "Solid Phase Peptide Synthesis", Academic Press, New York, 1980, 100-118.
Альтернативно, пептиды по настоящему изобретению могут быть получены, используя любые известные способы генной инженерии, предназначенные для получения пептидов (например, Morrison J. (1977) J. Bacteriology 132: 349-51; Clark-Curtiss & Curtiss (1983) Methods in Enzymology (eds. Wu et al.) 101: 347-62). Например, сначала получают подходящий вектор, несущий полинуклеотид, кодирующий мишеневый пептид, в экспрессируемой форме (например, расположенной ниже регуляторной последовательности, соответствующей промоторной последовательности) и трансформируют в подходящую клетку-хозяин. Затем клетку-хозяина культивируют с получением представляющего интерес пептида. Пептиды также могут быть получены с использованием in vitro-систем трансляции.
IV. Полинуклеотиды
Настоящее изобретение относится к полинуклеотидам, которые кодируют любой из вышеуказанных пептидов по настоящему изобретению. К ним относятся полинуклеотиды, выделенные из природного гена Foxp3, и полинуклеотиды, содержащие консервативно модифицированную нуклеотидную последовательность. В данном случае фраза "консервативно модифицированная нуклеотидная последовательность" означает последовательность, которая кодирует, по существу, идентичные аминокислотные последовательности. Из-за вырожденности генетического кода большое количество функционально идентичных нуклеиновых кислот кодирует любой заданный белок. Например, все перечисленные кодоны GCA, GCC, GCG и GCU кодируют аминокислоту аланин. Таким образом, в каждом положении, в котором аланин определяется кодоном, кодон может быть изменен на любой соответствующий кодон без изменения кодируемого полипептида. Такие изменения в нуклеиновой кислоте являются "молчащими вариантами" и представляют собой один из видов консервативно модифицированных вариантов. Каждая последовательность нуклеиновой кислоты, представленная в настоящем описании, которая кодирует пептид, также описывает любой возможный «молчащий вариант» нуклеиновой кислоты. Специалисту будет понятно, что каждый кодон нуклеиновой кислоты (за исключением AUG, который обычно является единственным кодоном для метионина, и TGG, который обычно является единственным кодоном для триптофана) может быть модифицирован с получением функционально идентичной молекулы. Соответственно, каждый «молчащий вариант» нуклеиновой кислоты, который кодирует пептид, описан в неявном виде для каждой описанной последовательности.
Полинуклеотид по настоящему изобретению может состоять из ДНК, РНК и их производных. ДНК обычно состоит из оснований, таких как A, T, C и G. T заменяется на U в РНК.
Полинуклеотиды Foxp3 по настоящему изобретению могут кодировать множество пептидов Foxp3 по настоящему изобретению со вставками или без вставок аминокислотных последовательностей между ними. Например, вставленная аминокислотная последовательность может представлять собой сайт расщепления (например, последовательность, распознаваемая ферментом) полинуклеотида или транслированных пептидов. Кроме того, полинуклеотиды могут содержать любые дополнительные последовательности кроме кодирующей последовательности пептида по настоящему изобретению. Например, полинуклеотиды могут представлять собой рекомбинантные полинуклеотиды, которые содержат регуляторные последовательности, необходимые для экспрессии пептида. Как правило, такие рекомбинантные полинуклеотиды могут быть получены путем манипуляций с полинуклеотидами посредством подходящих рекомбинантных методов с использованием, например, полимераз и эндонуклеаз.
Оба способа синтеза, рекомбинантный и химический, могут использоваться для получения полинуклеотидов по настоящему изобретению. Например, полинуклеотиды могут быть получены вставкой в подходящий вектор, который может экспрессироваться при трансфекции в компетентную клетку. Альтернативно, полинуклеотиды могут быть амплифицированы с использованием методов ПЦР или с помощью экспрессии в подходящих организмах-хозяевах (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 1989). Альтернативно, полинуклеотиды могут быть синтезированы с использованием твердофазных методов, описанных у Beaucage S.L. & Iyer R.P., в Tetrahedron 48: 2223-311, 1992; Matthes et al., EMBO J 3: 801-5, 1984.
V. Фармацевтические средства
Так как Foxp3 был идентифицирован как молекула регуляторных T-клеток (T-reg), функция которых состоит в поддержании иммунного гомеостаза, то пептиды Foxp3 или полинуклеотиды, кодирующие пептиды Foxp3, по настоящему изобретению могут использоваться для регуляции клеток T-reg. Таким образом, настоящее изобретение относится к фармацевтическому средству для регуляции клеток T-reg, которое содержит в качестве активного ингредиента один или несколько пептидов по настоящему изобретению или полинуклеотидов, кодирующих эти пептиды.
В данном случае под "регуляцией" клеток T-reg понимают модификацию состояния клеток T-reg in vivo, например, путем ингибирования пролиферации или подавления функции клеток T-reg. Считается, что клетка T-reg является одним из главных участников, задействованных в подавлении разнообразных типов иммунного ответа, и под "подавлением функции клеток T-reg" в данном случае понимают уменьшение способности клеток T-reg подавлять иммунный ответ. В частности, функция клеток T-reg в периферической крови представляет собой так называемую периферическую толерантность (Miescher S et al., J Immunol 136: 1899-907, 1986; Young RC et al., Am J Med 52: 63-72, 1972; Alexander JP et al., Cancer Res 53: 1380-7, 1997; Horiguchi S et al., Cancer Res 59: 2950-6, 1999; Kono K et al., Clin Cancer Res 11: 1825-8, 1996; Kiessling R et al., Cancer Immunol Immunother 48: 353-62, 1999; Fontenot JD et al., Nat Immunol 4: 330-6, 2003, Hori S et al., Science 299: 1057-61, 2003; Khattri R et al., Nat Immunol 4: 304-6, 2003). Клетки T-reg обеспечивают иммуносупрессивный эффект, например, у пациентов, больных раком. Таким образом, пептиды Foxp3 по настоящему изобретению, сверх-экспрессирующиеся в клетках T-reg, или полинуклеотиды, кодирующие пептиды Foxp3, могут использоваться в качестве фармацевтического средства (например, вакцины) для лечения рака.
В настоящем изобретении фраза "вакцина" (также означающая иммуногенную композицию) означает вещество, функция которого заключается в индукции противоопухолевого иммунитета или иммунитета для регуляции клеток T-reg при инокуляции животным.
Фармацевтические средства по настоящему изобретению могут использоваться для лечения и/или профилактики рака у индивидов, таких как человек или любое другое млекопитающее, включая, но, не ограничиваясь ими, мышь, крысу, морскую свинку, кролика, кошку, собаку, овцу, козу, свинью, крупный рогатый скот, лошадь, обезьяну, павиана и шимпанзе, в частности коммерчески важное животное или одомашненное животное.
Согласно настоящему изобретению полипептиды, содержащие аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, представляют собой пептиды эпитопов, ограниченных HLA-A24- или HLA-A02, которые могут индуцировать эффективный и специфичный иммунный ответ в отношении клеток T-reg, экспрессирующих Foxp3. Таким образом, фармацевтические средства предназначены для введения индивидам, антиген HLA которых представляет собой или HLA-A24, или HLA-A02.
Рак, на который может быть направлено лечение с помощью фармацевтических средств по настоящему изобретению, не ограничен и включает все типы рака, при которых у индивида экспрессируется Foxp3. Характерные типы рака включают рак груди, миелобластный лейкоз (AML), рак мочевого пузыря, рак шейки матки, холангиоцеллюлярную карциному, хронический миелолейкоз (CML), рак толстой кишки и рак прямой кишки, эндометриоз, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, рак легкого, лимфому, нейробластому, остеосаркому, рак яичника, рак поджелудочной железы, рак простаты, карциному почек, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичек.
При необходимости фармацевтические средства по настоящему изобретению, состоящие или из пептида Foxp3, или из полинуклеотида, кодирующего этот пептид Foxp3, необязательно могут включать другие терапевтические средства в качестве активного ингредиента, при условии, что средство не ингибирует регулирующий эффект представляющего интерес пептида на клетку T-reg. Например, композиции могут содержать противовоспалительные средства, болеутоляющие средства, хемотерапевтические средства и тому подобное. Кроме включения в композицию других терапевтических средств, лекарственные средства по настоящему изобретению также могут вводиться последовательно или одновременно с одним или несколькими другими фармакологическими средствами. Количество лекарственного средства и фармакологического средства зависит, например, от типа используемого фармакологического средства(в), от заболевания, на которое направлено лечение, и от схемы и пути введения.
Следует учитывать, что кроме ингредиентов, конкретно указанных в описании, фармацевтические средства по настоящему изобретению могут включать другие подходящие средства, известные в данной области, относящиеся к типу рассматриваемой композиции.
В одном из вариантов осуществления настоящего изобретения фармацевтические средства настоящего изобретения могут быть включены в состав изделия и в наборы, содержащие материалы, используемые для лечения патологических состояний, на которые направлено лечение, например рака. Изделие может включать контейнер с любым из указанных фармацевтических средств с этикеткой. Подходящие контейнеры включают флаконы, ампулы и пробирки. Контейнеры могут быть сделаны из разнообразных материалов, таких как стекло или пластик. На этикетке контейнера следует указать средство, используемое для лечения или профилактики одного или несколько состояний. На этикетке также могут быть указаны руководства по применению и тому подобное.
Кроме контейнера, описанного выше, набор реагентов, содержащих фармацевтическое средство по настоящему изобретению, необязательно, может дополнительно включать второй контейнер, содержащий фармацевтически приемлемый разбавитель. Он может дополнительно включать другие материалы, необходимые как с коммерческой, так и с пользовательской точки зрения, включающие другие буферы, разбавители, фильтры, иглы, шприцы и вкладыш в упаковку с инструкциями по применению.
Фармацевтические композиции, если необходимо, могут быть представлены в упаковке или в распределительном устройстве, которые могут содержать одну или несколько единичных дозированных форм, содержащих активный ингредиент. Упаковка, например, может включать металлическую или пластиковую фольгу, такую как блистерная упаковка. Упаковка или распределительное устройство могут сопровождаться инструкциями для введения.
(1) Фармацевтические средства, содержащие пептиды в качестве активного ингредиента
Пептиды по настоящему изобретению могут вводиться непосредственно в качестве фармацевтического средства, если необходимо, которое составлено в композицию общепринятыми способами получения лекарственных средств. В таких случаях кроме пептидов по настоящему изобретению при необходимости и без конкретных ограничений могут быть включены носители, эксципиенты и вещества, которые обычно используются для лекарственных средств. Примерами таких носителей являются стерилизованная вода, физиологический солевой раствор, фосфатный буфер, культуральная жидкость и тому подобное. Кроме того, фармацевтические средства могут содержать при необходимости стабилизаторы, суспендирующие средства, консерванты, поверхностно-активные вещества и тому подобное. Фармацевтические средства по настоящему изобретению могут использоваться для лечения и/или профилактики рака, в частности для регуляции клеток T-reg.
Пептиды по настоящему изобретению могут быть получены в сочетании, которое содержит два или несколько пептидов Foxp3 по изобретению, для индукции клеток CTL in vivo. Пептиды Foxp3 могут быть представлены в виде смеси или могут быть конъюгированы друг с другом стандартными методами. Например, пептиды Foxp3 могут экспрессироваться в виде одной полипептидной последовательности. Пептиды в указанной комбинации могут быть одинаковыми или различными. Путем введения пептидов Foxp3 по настоящему изобретению пептиды презентируются на антигенах HLA антиген-презентирующих клеток с высокой плотностью, затем индуцируются клетки CTL, которые специфично взаимодействуют по отношению к комплексу, образованному обнаруженным пептидом и антигеном HLA. Альтернативно, получают антиген-презентирующие клетки, которые содержат на своей клеточной поверхности иммобилизованные пептиды Foxp3 по настоящему изобретению, с помощью удаления у индивидов дендритных клеток, стимулированных пептидами по изобретению, клетки CTL индуцируются у индивидов при повторном введении индивидам несущих пептиды Foxp3 дендритных клеток, и в результате может увеличиваться агрессивность в отношении клеток-мишеней.
Фармацевтические средства для регуляции клеток T-reg, которые включают в качестве активного ингредиента пептид Foxp3 по настоящему изобретению, необязательно, могут включать адъювант, для эффективной адаптации клеточного иммунитета, или они могут быть введены с другими активными ингредиентами, и при этом они могут быть введены с помощью полученных лекарственных форм в гранулах. Адъювант означает соединение, которое усиливает иммунный ответ в отношении белка, при введении совместно (или последовательно) с белком, обладающим иммунологической активностью. Адъювант, который может использоваться, включает адъюванты, описанные в литературе (Clin Microbiol Rev 7: 277-89, 1994). Примеры адъювантов включают, но не ограничиваются ими, фосфат алюминия, гидроксид алюминия, квасцы, холерный экзотоксин, токсин сальмонеллы и тому подобное.
Кроме того, могут подходящим образом использоваться липосомные композиции, гранулярные композиции, в которых пептид Foxp3 связан с гранулами диаметром в несколько мкм, и композиции, в которых липид связан с пептидом.
В некоторых вариантах осуществления фармацевтическое средство по изобретению содержит компонент, который индуцирует цитотоксические Т-лимфоциты. Липиды были идентифицированы в качестве средств, способных индуцировать клетки CTL in vivo против вирусных антигенов. Например, остатки пальмитиновой кислоты могут присоединяться к эпсилон- и альфа-аминогруппам остатка лизина и затем связываться с пептидом по изобретению. Липидированный пептид может затем вводиться или непосредственно в мицелле или частице, будучи инкорпорированным в липосому или эмульгированным в адъювант. В качестве другого примера липида, индуцирующего ответы клеток CTL, для индукции клеток CTL могут использоваться липопротеины E. coli, такие как трипальмитоил-S-глицерилцистеинлизерил-серин (P3CSS), при ковалентном присоединении к подходящему пептиду (см., например, Deres et al., Nature 342: 561, 1989).
Способ введения может представлять собой пероральное введение, чрескожное, подкожное, внутривенную инъекцию или тому подобное и находят применение системное введение или местное применение в окружении сайтов-мишеней. Введение может осуществляться путем единственного введения или может повторяться путем множественных введений. Доза пептидов по настоящему изобретению может регулироваться подходящим образом в зависимости от заболевания, на которое необходимо направить лечение, возраста пациента, массы, способа введения и тому подобное и обычно составляет 0,001 мг-1000 мг, например 0,001 мг-1000 мг, например 0,1 мг-10 мг, и может вводиться от одного раза в каждые несколько дней до одного раза в каждые несколько месяцев. Специалист в данной области сможет подходящим образом выбрать подходящую дозу.
(2) Фармацевтические средства, содержащие полинуклеотиды в качестве активного ингредиента
Фармацевтические средства по изобретению могут также содержать нуклеиновые кислоты в экспрессируемой форме, кодирующие описанные в настоящем описании пептиды Foxp3. В данном случае фраза "в экспрессируемой форме" означает, что полинуклеотид при введении в клетку будет экспрессироваться in vivo в виде полипептида, который индуцирует противоопухолевый иммунитет. В одном из вариантов осуществления последовательность нуклеиновой кислоты представляющего интерес полинуклеотида включает регуляторные элементы, необходимые для экспрессии полинуклеотида в клетке-мишени. Полинуклеотид(ы) может быть адаптирован для стабильного интегрирования в геном клетки-мишени (см., например, Thomas KR & Capecchi MR, Cell 51: 503-12, 1987 для описания векторов с кассетой для гомологичной рекомбинации). См., например, Wolff et al., Science 247: 1465-8, 1990; патенты США 5580859; 5589466; 5804566; 5739118; 5736524; 5679647; и WO 98/04720. Примеры технологий доставки на основе ДНК включают доставку с применением "голой" ДНК, облегченную доставку (опосредованную бупивакаином, полимерами, пептидами), доставку с применением катионно-липидных комплексов и опосредованную частицами ("генная пушка") или опосредованную давлением доставку (см., например, патент США 5922687).
Пептиды по изобретению также могут экспрессироваться с помощью вирусных или бактериальных векторов. Примеры экспрессирующих векторов включают ослабленных вирусных хозяев, таких как коровья оспа или оспа птиц. Этот способ включает использование вируса коровьей оспы, например, в качестве вектора для экспрессии нуклеотидных последовательностей, которые кодируют пептид. При введении в организм-хозяин рекомбинантный вирус коровьей оспы экспрессирует иммуногенный пептид, посредством чего вызывает иммунный ответ. Векторы на основе вируса коровьей оспы и способы, использующиеся в протоколах иммунизации, описаны, например в патенте США 4722848. Другой вектор представляет собой BCG (Bacille Calmette Guerin). BCG-векторы описаны Stover et al., в Nature 351: 456-60, 1991. Является очевидным широкое разнообразие других векторов, использующихся для терапевтического введения или иммунизации, например адено и адено-ассоциированные вирусные векторы, ретровирусные векторы, векторы Salmonella typhi, векторы на основе детоксифицированного токсина сибирской язвы и тому подобное. См., например, публикации Shata et al., Mol Med Today 6: 66-71, 2000; Shedlock et al. J Leukoc Biol 68: 793-806, 2000; Hipp et al., In Vivo 14: 571-85, 2000.
Доставка полинуклеотида пациенту может быть или непосредственной, в случае которой пациент подвергается непосредственному воздействию вектора, несущего полинуклеотид, или может быть косвенной, в случае которой клетки сначала трансформируют in vitro с помощью представляющего интерес полинуклеотида и затем трансплантируют пациенту. Эти два способа известны соответственно как in vivo или ex vivo генная терапия.
В качестве общих обзоров методов генной терапии, см. Goldspiel et al., Clinical Pharmacy 12: 488-505, 1993; Wu and Wu, Biotherapy 3: 87-95, 1991; Tolstoshev, Ann Rev Pharmacol Toxicol 33: 573-96, 1993; Mulligan, Science 260: 926-32, 1993; Morgan & Anderson, Ann Rev Biochem 62: 191-217, 1993; Trends in Biotechnology 11(5): 155-215, 1993). Широко известные в данной области способы технологии рекомбинантной ДНК, которые могут использоваться, описаны Ausubel et al., в Current Protocols in Molecular Biology, John Wiley & Sons, NY, 1993; и Krieger, Gene Transfer и Expression, A Laboratory Manual, Stockton Press, NY, 1990.
Способ введения может представлять собой пероральное введение, чрескожное, подкожное, внутривенную инъекцию или тому подобное, и могут использоваться системное введение или местное применение в окружении сайтов-мишеней. Введение может осуществляться путем единственного введения или может повторяться путем множественных введений. Доза полинуклеотидов в подходящем носителе или доза клеток, трансформированных полинуклеотидом, кодирующим полипептиды по настоящему изобретению, может регулироваться подходящим образом в зависимости от заболевания, на которое необходимо направить лечение, возраста пациента, массы, способа введения и тому подобное, и обычно составляет 0,001 мг-1000 мг, например 0,001 мг-1000 мг, например 0,1 мг-10 мг, и может вводиться от одного раза в каждые несколько дней до одного раза в каждые несколько месяцев. Специалист в данной области сможет подходящим образом выбрать подходящую дозу.
(3) Экзосомы
Альтернативно, настоящее изобретение относится к внутриклеточным везикулам, называемым экзосомами, которые презентируют на своей поверхности комплексы, образованные пептидами по настоящему изобретению и антигенами HLA. Например, экзосомы могут быть получены с использованием способов, подробно описанных в опубликованном японском переводе международной заявки Hei 11-510507 и 2000-512161, и могут быть получены с использованием антиген-презентирующих клеток, полученных у индивидов, являющихся мишенями для лечения и/или профилактики заболевания. Экзосомы по настоящему изобретению могут инокулироваться в виде вакцин подобно пептидам по настоящему изобретению.
Тип используемых антигенов HLA должен соответствовать антигенам индивида, которому требуется лечение и/или профилактика заболевания. Например, для японцев наиболее подходящим является HLA-A24, конкретно HLA-A2402.
Что касается антигенов HLA, то использование типа A-24 или A-02, которые высоко экспрессируются у японцев и европейцев, является предпочтительным для получения эффективных результатов, и находят применение субтипы, включающие A-2402 и A-0201. В медицинской практике является характерным, что тип антигена HLA пациента, для которого требуется лечение, исследуется заранее, что дает возможность подходящего выбора пептидов, имеющих высокий уровень аффинности связывания с этим антигеном или обладающих способностью индуцировать цитотоксические Т-клетки (CTL) презентирующим антигеном. Кроме того, для того чтобы получить пептиды, проявляющие высокую аффинность связывания и способность индуцировать клетки CTL, можно осуществлять замену или введение 1, 2 или нескольких аминокислот на основе аминокислотной последовательности природного неполного пептида Foxp3.
(4) Антиген-презентирующие клетки
Настоящее изобретение также относится к антиген-презентирующим клеткам (APC), которые презентируют на своей поверхности комплексы, образованные антигенами HLA и пептидами по настоящему изобретению. APC, которые получают путем контактирования пептидов по настоящему изобретению или нуклеотидов, кодирующих эти пептиды по настоящему изобретению, могут быть получены у индивидов, являющихся мишенями для лечения и/или профилактики заболевания, и могут вводиться как вакцины индивидуально или в комбинации с другими лекарственными средствами, включая пептиды по настоящему изобретению, экзосомы или цитотоксические Т-клетки.
APC не ограничиваются каким-либо типом клеток и включают дендритные клетки (DC), клетки Лангеранса, макрофаги, В-клетки и активированные Т-клетки, причем о каждых из них известно, что они презентируют на своей клеточной поверхности белково-подобные антигены, чтобы быть распознанными лимфоцитами. Так как DC представляют собой репрезентативные клетки APC, обладающие сильнейшим CTL-индуцирующим воздействием среди клеток APC, то DC нашли конкретное применение в качестве клеток APC по настоящему изобретению.
Например, клетки APC могут быть получены путем индукции дендритных клеток из моноцитов периферической крови и последующего контактирования (стимулирования) их с пептидами по настоящему изобретению in vitro, ex vivo или in vivo. Если пептиды по настоящему изобретению вводят индивидам, клетки APC, которые содержат на своей поверхности иммобилизованные пептиды по настоящему изобретению, индуцируются в организме индивида, причем "индукция клеток APC" включает контактирование (стимулирование) клетки с пептидами по настоящему изобретению или нуклеотидами, кодирующими эти пептиды по настоящему изобретению, для презентации на клеточной поверхности комплексов, образованных антигенами HLA и пептидами. Альтернативно, после иммобилизации пептидов по настоящему изобретению с клетками APC клетки APC могут вводиться индивиду в виде вакцины. Например, введение ex vivo может включать стадии: a) забора клеток APC у индивида и b) контактирование клеток APC стадии a) с пептидом. Клетки APC, полученные на стадии b), могут вводиться индивиду в виде вакцины.
Согласно одному из аспектов настоящего изобретения клетки APC способны к индукции клеток CTL на высоком уровне. Такие клетки APC, способные к индукции цитотоксических Т-клеток на высоком уровне, могут быть получены способом, который включает стадию переноса генов, включающих полинуклеотиды, которые кодируют пептиды по настоящему изобретению, к клеткам APC in vitro. Введенные гены могут быть представлены в форме ДНК или РНК. В качестве методов введения без конкретных ограничений могут использоваться разнообразные способы, обычно осуществляемые в данной области, такие как липофекция, электропорация и кальций-фосфатный метод. Более конкретно, это может быть осуществлено, как описано в публикациях Cancer Res 56: 5672-7, 1996; J Immunol 161: 5607-13, 1998; J Exp Med 184: 465-72, 1996; опубликованном Японском переводе международной заявки 2000-509281. При переносе гена в клетки APC ген подвергается транскрипции, трансляции и другим процессам в клетке, и затем полученный белок процессируется MHC класса I или класса II, проходит через путь презентации и презентирует неполные пептиды.
(5) Цитотоксические T-клетки
Предполагается, что цитотоксическая T-клетка, индуцированная против любого пептида Foxp3 по настоящему изобретению, укрепляет иммунную систему, регулируя клетки T-reg in vivo, и, таким образом, может использоваться в качестве вакцин подобно пептидам. Таким образом, настоящее изобретение относится к выделенным цитотоксическим Т-клеткам, которые индуцируются с помощью любого пептида по настоящему изобретению.
Такие цитотоксические Т-клетки могут быть получены путем (1) введения индивиду или (2) контактирования (стимулирования) полученных от индивида клеток APC, CD8-положительных клеток или мононуклеарных лейкоцитов периферической крови in vitro с пептидом по настоящему изобретению.
Цитотоксические Т-клетки, которые были индуцированы путем стимулирования из клеток APC, которые презентируют на своей поверхности пептиды по настоящему изобретению, могут быть получены от индивидов, являющихся мишенями для лечения и/или профилактики заболевания, и могут вводиться индивидуально или в сочетании с другими лекарственными средствами, включающими пептиды по настоящему изобретению или экзосомы, с целью получения эффектов регуляции. Полученные цитотоксические Т-клетки действуют специфично против клеток-мишеней, презентирующих пептиды по настоящему изобретению, например такие же пептиды, которые используются для индукции. Клетки-мишени могут представлять собой клетки, которые эндогенно экспрессируют Foxp3, или клетки, которые трансфецированы генами Foxp3, и клетки, которые презентируют на своей поверхности пептиды по настоящему изобретению и благодаря стимулированию этими пептидами могут также становиться мишенями для атаки.
(6) TCR
Настоящее изобретение также относится к композиции, содержащей нуклеиновые кислоты, кодирующие полипептиды, которые способны к формированию субъединицы Т-клеточного рецептора (TCR), и к способам ее применения. Субъединицы TCR обладают способностью образовывать TCR, которые придают специфичность в отношении Т-клеток для клеток, презентирующих пептид по настоящему изобретению. Нуклеиновые кислоты альфа- и бета-цепи в качестве субъединиц TCR клеток CTL, индуцированных с помощью одного или нескольких пептидов по настоящему изобретению, могут быть идентифицированы способом, известным в данной области (WO2007/032255 и Morgan et al., J Immunol, 171, 3288 (2003)). Производные TCR предпочтительно связываются с клетками-мишенями, презентирующими пептид Foxp3 с высокой авидностью, и необязательно опосредуют эффективное уничтожение клеток-мишеней, презентирующих пептид Foxp3 in vivo и in vitro.
Нуклеиновые кислоты, кодирующие субъединицы TCR, могут быть введены в подходящие векторы, например ретровирусные векторы. Эти векторы хорошо известны в данной области. Нуклеиновые кислоты или векторы, включающие их, могут эффективно переноситься в Т-клетку, которая предпочтительно представляет собой Т-клетку пациента. Преимущественно изобретение относится к готовой композиции, позволяющей быструю модификацию собственных Т-клеток пациента (или Т-клеток другого млекопитающего) для быстрого и легкого получения модифицированных Т-клеток, обладающих превосходными свойствами уничтожения клеток T-reg.
Также настоящее изобретение относится к клеткам CTL, которые получают путем трансдукции с помощью нуклеиновых кислот, кодирующих полипептидные субъединицы TCR, связывающиеся с пептидом Foxp3 по настоящему изобретению. Трансдуцированные клетки CTL способны к образованию комплекса с клетками T-reg in vivo и культивируются с помощью хорошо известного метода культивирования in vitro (например, Kawakami et al., J Immunol., 142, 3452-3461 (1989)). T-клетки по изобретению могут использоваться для образования иммуногенной композиции, используемой для лечения или профилактики рака у пациента, нуждающегося в терапии или в повышении иммунитета (WO2006/031221).
VI. Способы применения пептидов Foxp3
Пептиды Foxp3 по настоящему изобретению и полинуклеотиды, кодирующие пептиды Foxp3, могут использоваться для индукции клеток APC и CTL. Пептиды Foxp3 и полинуклеотиды могут использоваться в сочетании с любыми другими соединениями, при условии, что соединения не ингибируют их способность индуцировать клетки CTL. Таким образом, любые из вышеуказанных фармацевтических средств по настоящему изобретению могут использоваться в способах по настоящему изобретению, указанных ниже.
(1) Способы индукции антиген-презентирующих клеток (APC)
Таким образом, настоящее изобретение относится к способам индукции клеток APC с использованием пептидов по настоящему изобретению или полинуклеотидов, кодирующих эти пептиды. Индукция клеток APC может осуществляться, как описано выше, в параграфе "V-(4) Антиген-презентирующие клетки". Настоящее изобретение также относится к способу индукции клеток APC, способных на высоком уровне к индукции цитотоксических Т-клеток, индукция которых описана выше в параграфе "V-(4) Антиген-презентирующие клетки". Альтернативно, настоящее изобретение относится к применению пептидов Foxp3, выбранных из пептидов, содержащих аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, или полинуклеотидов, кодирующих пептиды Foxp3, для получения фармацевтической композиции, содержащей антиген-презентирующие клетки. Кроме того, настоящее изобретение относится к пептидам Foxp3, выбранным из пептидов, содержащих аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, или полинуклеотидам, кодирующим пептиды Foxp3, для индукции антиген-презентирующих клеток.
(2) Способы индукции цитотоксических Т-клеток
Кроме того, настоящее изобретение относится к способам индукции клеток CTL с использованием пептидов Foxp3 по настоящему изобретению или полинуклеотидов, кодирующих пептиды Foxp3. Когда пептиды Foxp3 по настоящему изобретению вводят индивиду, клетки CTL индуцируются в организме индивида и повышается сила иммунной системы, регулирующей клетки T-reg. Альтернативно, способы индукции могут использоваться для ex vivo-терапевтического способа, в котором полученные у индивида APC и CD8-положительные клетки или мононуклеарные лейкоциты периферической крови контактируют (стимулируются) in vitro с пептидами по настоящему изобретению, и после индукции клеток CTL клетки возвращают индивиду. Например, способ может включать стадии: a) забора клеток APC у индивида; b) контактирования клеток APC стадии a) с пептидом; c) смешивания клеток APC стадии b) с CD8+ T-клетками и совместного культивирования для индукции цитотоксических Т-клеток и d) забора CD8+ T-клеток из совместной культуры стадии c).
CD8+ T-клетки клетки, обладающие цитотоксической активностью, полученные на стадии d), могут вводиться индивиду в качестве вакцины. Клетки APC, которые следует смешивать с CD8+ T-клетками на описанной выше стадии c), также могут быть получены путем переноса генов, кодирующих пептиды по настоящему изобретению, в клетки APC, как подробно описано выше в параграфе "V-(4) Антиген-презентирующие клетки"; но ими не ограничены, и любые клетки APC или экзосома, которые эффективно презентируют пептиды по настоящему изобретению Т-клеткам, могут использоваться в соответствии с настоящим способом. Альтернативно, настоящее изобретение относится к использованию пептидов Foxp3, выбранных из пептидов, содержащих аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, или полинуклеотидов, кодирующих пептиды Foxp3, для получения фармацевтической композиции, содержащей клетки CTL. Кроме того, настоящее изобретение также относится к пептидам Foxp3, выбранным из пептидов, содержащих аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, или полинуклеотидам, кодирующим пептиды Foxp3, для индукции клеток CTL.
(3) Регуляция иммуносупрессии
Как обсуждалось выше, пептиды, полинуклеотиды, экзосомы, APC и CTL по настоящему изобретению могут использоваться в качестве вакцин для регуляции (т.е. подавления) клеток T-reg. На основании предположения о том, что клетки T-reg являются одним из главных игроков, участвующих в подавлении разнообразных типов иммунного ответа, конкретно цитотоксической активности клеток CTL, способность пептидов, полинуклеотидов, экзосом, клеток APC и CTL по настоящему изобретению указывает на то, что они также могут использоваться для противодействия иммуносупрессии, конкретно, цитотоксической активности клеток CTL. Соответственно, настоящее изобретение относится к способу регуляции клеток T-reg, а также к способу регуляции (т.е. противодействия) иммуносупрессии, включающим стадии введения нуждающемуся в этом индивиду пептидов, полинуклеотидов, экзосом, клеток APC или CTL по настоящему изобретению. Кроме того, настоящее изобретение также относится к применение пептидов Foxp3, выбранных из пептидов, содержащих аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, или полинуклеотидов, кодирующих пептиды Foxp3, для получения иммуногенной композиции, предназначенной для регуляции иммуносупрессии. Альтернативно, настоящее изобретение также относится к пептидам Foxp3, выбранным из пептидов, содержащих аминокислотную последовательность SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74, или к полинуклеотидам, кодирующим пептиды Foxp3, предназначенным для регуляции иммуносупрессии.
В данном случае регуляция иммуносупрессии означает, что введение пептидов, полинуклеотидов, экзосом, клеток APC или CTL по настоящему изобретению вызывает любой тип изменения in vivo. В некоторых вариантах осуществления изменение, вызванное введением пептидов, полинуклеотидов, экзосом, клеток APC или CTL по настоящему изобретению, представляет собой уменьшение уровня иммуносупрессивного состояния (подавление или противодействие иммуносупрессии), а именно индукцию антииммуносупрессии. Таким образом, настоящее изобретение также относится к способу индукции антииммуносупрессии, причем указанный способ включает стадии введения нуждающемуся в этом индивиду пептидов, полинуклеотидов, экзосом, клеток APC или CTL по настоящему изобретению. В целом, антииммуносупрессия включает иммунные ответы, такие как:
- индукция цитотоксических Т-лимфоцитов против клеток T-reg, экспрессирующих Foxp3,
- индукция антител, которые распознают клетки T-reg, экспрессирующие Foxp3, и
- индукция продукции анти-T reg цитокинов.
Таким образом, если определенный белок индуцирует любой иммунный ответ при инокуляции животному, то считается, что белок обладает эффектом индукции антииммуносупрессии. Индукция белком антииммуносупрессии может определяться с помощью наблюдения in vivo или in vitro ответа иммунной системы организма-хозяина против белка.
Например, хорошо известен способ определения индукции (т.е. активации) цитотоксических Т-лимфоцитов. Конкретно, известно, что чужеродное вещество, которое попадает в живой организм, презентируется Т- или В-клеткам с помощью антиген-презентирующих клеток (APC). T-клетки, которые отвечают за антиген, презентируемых APC, дифференцируются в цитотоксические Т-клетки антиген-специфичным образом (или цитотоксические Т-лимфоциты; CTL) благодаря стимулированию антигеном, и затем пролиферируют (этим обозначается активация Т-клеток). Таким образом, индукция клеток CTL с помощью определенного пептида может оцениваться путем презентации пептида Т-клетке с помощью APC и с помощью детекции индукции (т.е. пролиферации, продукции IFN-γ и цитотоксической активности) клеток CTL. Кроме того, клетки APC обладают эффектом активации CD4+ T-клеток, CD8+ T-клеток, макрофагов, эозинофилов и NK-клеток. Так как CD4+ T-клетки также являются важными в процессе противоопухолевого иммунитета, функция пептида как индуктора противоопухолевого иммунитета может оцениваться с использованием в качестве показателя эффекта активации этих клеток.
Способ оценки функции, определяющей способность индуцировать клетки CTL с использованием дендритных клеток (DC) в качестве APC, хорошо известен в данной области. Согласно этому способу тестируемый пептид сначала контактирует с DC и затем DC контактирует с T-клетками. Обнаружение T-клеток, обладающих цитотоксическими эффектами в отношении клеток, экспрессирующих (т.е. презентированными на HLA-молекуле) представляющий интерес пептид, после контактирования с клетками DC, демонстрирует, что тестируемый пептид обладает активностью индуцировать цитотоксические Т-клетки. Активность клеток CTL в отношении клеток T-reg может обнаруживаться, например, с использованием в качестве показателя лизиса опухолевых клеток, меченных 51Cr. Альтернативно, также хорошо известен и может использоваться в настоящем изобретении способ оценки степени разрушения клеток T-reg с использованием в качестве показателя активности поглощения 3H-тимидина или высвобождения LDH (лактозодегидрогеназы).
Кроме клеток DC, в качестве APC также могут использоваться мононуклеарные клетки периферической крови. Сообщалось, что индукция клеток CTL повышается при культивировании PBMC в присутствии GM-CSF и IL-4. Подобным образом, было показано, что клетки CTL индуцируются при культивировании PBMC в присутствии гемоцианина лимфы улитки (KLH) и IL-7.
С помощью этих способов было подтверждено, что тестируемые пептиды, обладающие активностью индуцировать клетки CTL, представляют собой пептиды, обладающие эффектом активации клеток DC и последующей активностью индукции клеток CTL. Таким образом, пептиды Foxp3, которые индуцируют клетки CTL в отношении опухолевых клеток, могут быть использованы в качестве вакцин против клеток T-reg. Кроме того, клетки APC, которые приобретают способность индуцировать клетки CTL против клеток T-reg при контактировании с пептидами Foxp3, также могут использоваться в качестве вакцин против клеток T-reg. Кроме того, клетки CTL, которые приобретают цитотоксичность благодаря презентации пептидных антигенов клетками APC, также могут использоваться в качестве вакцин против клеток T-reg. Такие способы регуляции клеток T-reg с использованием иммунитета, вызванного клетками APC и CTL, обозначаются как клеточная иммунотерапия и охватываются настоящим изобретением.
Как правило, известно, что при использовании полипептида для клеточной иммунотерапии эффективность индукции клеток CTL увеличивается при комбинировании множества пептидов, имеющих различные структуры, и их контактировании с клетками DC. Таким образом, при стимулировании клеток DC фрагментами белка, преимущественно используется смесь фрагментов множества типов белков.
Альтернативно, индукция антииммуносупрессии с помощью пептида может быть подтверждена с помощью наблюдения индукции процесса продукции антител против клеток T-reg. Например, когда у индивида, например пациента-человека, лабораторного животного, иммунизированного с помощью пептида, индуцируются антитела против пептида и когда клетки T-reg подавляются с помощью этих антител, то пептид может определяться по его способности индуцировать антииммуносупрессию.
Антииммуносупрессия индуцируется путем введения вакцины по настоящему изобретению, и индукция обеспечивает подавление иммуносупрессии. Такие эффекты могут быть статистически значимыми. Например, из наблюдения, при уровне значимости, составляющем 5% или менее, эффект регуляции вакцины против клеток T-reg сравним с контролем, где отсутствовало введение вакцины. Например, для статистического анализа могут использоваться тест Стюдента, U-критерий Манна Уитни или ANOVA.
При использовании в качестве вакцины клеток APC или CTL по настоящему изобретению могут регулироваться клетки T-reg (т.е. подавляться), например, методом ex vivo. Более конкретно, клетки PBMC индивида, получающего лечение или которому необходима профилактика заболевания, собирают, приводят клетки ex vivo в контакт с полипептидом, и после индукции клеток APC или CTL могут вводиться индивиду. Клетки APC также могут индуцироваться введением вектора, кодирующего полипептид, в клетки PBMC ex vivo. Клетки APC или CTL, индуцированные in vitro, могут быть клонированы перед введением. С помощью клонирования и роста клеток, обладающих активностью разрушать клетки-мишени, клеточная иммунотерапия может осуществляться более эффективно. Кроме того, клетки APC и CTL, выделенные таким способом, могут использоваться для клеточной иммунотерапии не только против заболеваний индивидов, от которых клетки были получены, но также против подобных типов заболеваний у других индивидов.
Если не указано иначе, все технические и научные термины, используемые в настоящем описании, имеют такое же значение, как общепринято для любого специалиста в данной области, к которой относится настоящее изобретение. Хотя материалы и способы, подобные или эквивалентные описанным в настоящем описании, могут использоваться при практическом применении или при тестировании настоящего изобретения, подходящие материалы и способы описаны ниже. Все публикации, патентные заявки, патенты и другая литература, приведенная в настоящем описании, включена в настоящее описание посредством ссылки во всей своей полноте. В случае разночтения настоящее описание, в том числе определения, следует рассматривать как приоритетное. Кроме того, материалы, способы и примеры являются исключительно иллюстративными и не предназначены для ограничения изобретения.
Приведенные ниже примеры представлены для иллюстрации настоящего изобретения и оказания помощи любому специалисту в получении и использовании таких же результатов. Примеры никоим образом не предназначены для ограничения объема изобретения.
Примеры
Материалы и способы
Клеточные линии
Клетки A24LCL (HLA-A24/24), клетки T2 (HLA-A02/02), B-лимфобластные клетки человека, 293T и COS7 были получены из ATCC.
Селекция возможных пептидов, полученных из Foxp3
Структура 9-мерного и 10-мерного пептидов, полученных из Foxp3, которые связываются с молекулами HLA-A*2402 и HLA-A*0201, были спрогнозированы с использованием программного обеспечения для прогноза связывания "BIMAS" (http://bimas.dcrt.nih.gov/cgi-bin/molbio/ken_parker_comboform), алгоритмы которого описаны Parker KC, et al.((1994) J Immunol.;152(l):163-75) и Kuzushima K, et al. ((2001) Blood.;98(6):1872-81). Эти пептиды синтезировали с помощью Sigma (Sapporo, Japan) согласно стандартному методу твердофазного синтеза и очищали ВЭЖХ с обращенной фазой. Чистоту (>90%) и идентичность пептидов определяли аналитическим анализом ВЭЖХ и анализом масс-спектрометрии соответственно. Пептиды растворяли в диметилсульфоксиде (ДМСО) в концентрации 20 мг/мл и хранили при -80ºC.
In vitro индукция клеток CTL
Выделенные из моноцитов дендритные клетки (DC) получали как антиген-презентирующие клетки (APC) для индукции ответа CTL в отношении пептидов, презентированных на HLA. DC генерировали in vitro, как описано в других источниках (Horiguchi S. et al. Cancer Res. 59:2950-6). Конкретно, мононуклеарные клетки периферической крови (PBMC), взятые у здорового добровольца (HLA-A*2402 и/или HLA-A*0201), с помощью Ficoll-Plaque (Pharmacia) разделяли с помощью адгезии на пластиковую чашку Петри (Becton Dickinson) для обогащения фракцией моноцитов. Обогащенную моноцитами популяцию культивировали в присутствии 1000 Ед/мл GM-CSF (R&D System) и 1000 Ед/мл IL-4 (R&D System) в среде AIM-V (Invitrogen), содержащей 2% инактивированную нагреванием аутологичную сыворотку (AS). Через 7 дней культивирования клетки DC, продуцируемые цитокинами, стимулировали синтезированными пептидами 20 мкг/мл в присутствии 3 мкг/мл бета-2-микроглобулина в течение 4 часов при 20ºC в среде AIM-V. Стимулированные пептидом клетки DC затем инактивировали с помощью митомицина C (MMC) (30 мкг/мл в течение 30 мин) и смешивали в соотношении 1:20 с аутологичными CD8+ T-клетками, полученными положительной селекцией с использованием набора реагентов для выделения CD8-положительных клеток (Dynal). Полученные культуры помещали в 48-луночные планшеты (Corning); каждая лунка содержала 1,5×104 стимулированных пептидом клеток DC, 3×105 CD8+ T-клеток и 10 нг/мл IL-7 (R&D System) в 0,5 мл среды AIM-V/2% AS. Через три дня к культурам добавляли IL-2 (CHIRON) до конечной концентрации 20 МЕ/мл. На 7 и 14 день T-клетки дополнительно повторно стимулировали пептидом аутологичных клеток DC. Клетки DC получали каждый раз по аналогичной методике, как описано выше. Активность CTL тестировали в отношении стимулированных пептидом клеток A24LCL или клеток T2 на 21 день после третьего раунда пептидного стимулирования.
Методика размножения клеток CTL
Количество клеток CTL увеличивали за счет их деления в культуре с применением способа, как описано в публикации Riddell, et al. (Walter et al., N Engl J Med 333(16): 1038-44, 1995; Riddell et al., Nat Med 2(2): 216-23, 1996 Feb). Клетки CTL в количестве 5×104 ресуспендировали в 25 мл AIM-V/5% AS вместе с двумя типами B-лимфобластных клеточных линий человека, инактивированных с помощью MMC, в присутствии 40 нг/мл моноклонального антитела к CD3 (Pharmingen). Через один день после инициирования культур к ним добавляли 120 МЕ/мл IL-2. В культурах меняли среду на свежую AIM-V/5% AS, содержащую 30 МЕ/мл IL-2 на 5, 8 и 11 день.
Специфичная активность клеток CTL
Для определения специфичной активности клеток CTL осуществляли анализ IFN-γ-ELISPOT и анализ IFN-γ-ELISA. Коротко, стимулированные пептидом клетки A24-LCL, T2 (1×104/лунка) или клетки, эндогенно экспрессирующие Foxp3 и молекулу HLA, получали в качестве стимулирующих клеток. Культивированные в 48-луночных планшетах клеточные линии CTL использовали в качестве клеток-респондеров. Анализ IFN-γ-ELISPOT и анализ IFN-γ-ELISA осуществляли согласно рекомендациям производителя.
Иммуногенность пептидов эпитопа у мышей BALB/c
Для индукции пептидо-специфичных клеток CTL иммунизацию проводили с использованием 100 мкл вакцинной смеси, которая содержала 50 мкл рестриктированного пептида HLA-A24 и 50 мкл IFA на мышь. Вакцину вводили подкожно в правый бок мышей для первой иммунизации в день 0 и в левый бок для второй иммунизации на 7 день. На 14 день спленоциты вакцинированных мышей использовали в качестве клеток-респондеров и клетки RLmalel, стимулированные пептидом или без него, использовали в качестве стимулятора клеток для анализа IFN-γ-ELISPOT.
In vivo противоопухолевые эффекты
Клетки 4T1 (1×105 на мышь) вводили подкожно в правый бок мышей BALB/c в день 0. Вакцинацию проводили на 3 и 10 день с использованием hFoxp3-252 (KLSAMQAHL: SEQ ID NO:17) или mFoxp3-252 (KLGAMQAHL: SEQ ID NO:88) конъюгированных пептидов IFA.
Анализ на аффинность пептида Foxp3-9-252, содержащего замену, в отношении молекулы HLA
Анализ IFN-γ-ELISA осуществляли для определения аффинности пептида, содержащего замену, в отношении молекулы HLA-A2. Клетки CTL, индуцированные с помощью пептида Foxp3-9-252-WT (KLSAMQAHL: SEQ ID NO:17), использовали в качестве клеток-респондеров и клетки T2 получали в качестве стимулятора клеток путем инкубирования в присутствии пептида Foxp3-9-252-WT, Foxp3-9-252-9V (KLSAMQAHV: SEQ ID NO:95) и HIV-A02 (SLYNTYATL) при 37ºС в течение 2 часов. Стимулирование пептидом клеток T2 осуществляли в широком интервале концентраций каждого пептида (10-10-4 мкг/мл).
Результаты
Прогнозирование результатов HLA-A24- и HLA-A2-связывающих пептидов, полученных из Foxp3
В таблицах 1, 2 и 3 показаны HLA-A*2402-связывающие пептиды или HLA-A*0201-связывающие пептиды Foxp3-белка для бальной оценки высокого прогнозирования аффинности связывания. В общем выбирали 60 пептидов с потенциальной активностью связывания HLA-A24 и 26 пептидов с потенциальной активностью связывания HLA-A2.
|
Таблица 1
HLA-A2402-связывающие 9-мерные пептиды, полученные из Foxp3 |
||||
| Стартовое положение | Последовательность | Бальная оценка | SEQ ID NO | |
| Foxp3-A24-9мер | 363 | IYHWFTRMF | 100 | 3 |
| 207 | VFEEPEDFL | 36 | 4 | |
| 332 | KFHNMRPPF | 20 | 5 | |
| 323 | EFLHNMDYF | 15 | 6 | |
| 366 | WFTRMFAFF | 12 | 7 | |
| 337 | RPPFTYATL | 12 | 8 | |
| 190 | SYPLLANGV | 10,8 | 9 | |
| 27 | RAAPKASDL | 9,6 | 39 | |
| 238 | MVQSLEQQL | 8,64 | 40 | |
| 87 | GPLPHLQAL | 8,64 | 41 | |
| 252 | KLSAMQAHL | 8 | 17 | |
| 8 | KPSAPSLAL | 8 | 42 | |
| 352 | EAPEKQRTL | 7,2 | 43 | |
| 240 | QSLEQQLVL | 12 | 44 | |
| 245 | QLVLEKEKL | 6,6 | 45 | |
| 403 | GAVWTVDEL | 6,6 | 46 | |
| 185 | AVPQSSYPL | 6 | 47 | |
| 28 | AAPKASDLL | 6 | 48 | |
| 141 | FSLKARPGL | 6 | 49 | |
| 383 | NAIRHNLSL | 6 | 50 | |
| 186 | VPQSSYPLL | 6 | 51 | |
| 343 | ATLIRWAIL | 6 | 52 | |
| 200 | KWPGCEKVF | 6 | 53 | |
| 68 | QLQLPTLPL | 6 | 54 | |
| 341 | TYATLIRWA | 6 | 55 | |
| 115 | TPVLQVHPL | 6 | 56 | |
| 61 | LNPMPPSQL | 6 | 57 | |
| 159 | EWVSREPAL | 6 | 58 | |
| 175 | SAPRKDSTL | 6 | 59 | |
| 234 | LQREMVQSL | 5,76 | 60 | |
| 304 | SLFAVRRHL | 5,6 | 61 | |
| 359 | TLNEIYHWF | 5,04 | 62 | |
| Стартовое положение означает номер аминокислоты с N-конца Foxp3. Бальную оценку связывания получают с помощью программы "BIMAS", описанной в разделе «Материалы и способы». |
||||
|
Таблица 2
HLA-A2402-связывающие 10-мерные пептиды, полученные из Foxp3 |
||||||||
| Стартовое положение | Последовательность | Бальная оценка | SEQ ID NO | |||||
| Foxp3-A24-10мер | 341 | TYATLIRWAI | 70 | 10 | ||||
| 140 | VFSLKARPGL | 20 | 11 | |||||
| 114 | RTPVLQVHPL | 12 | 12 | |||||
| 27 | RAAPkASDLL | 9,6 | 63 | |||||
| 206 | KVFEePEDFL | 9,6 | 64 | |||||
| 402 | KGAVwTVDEL | 8,8 | 65 | |||||
| 237 | EMVQsLEQQL | 8,64 | 66 | |||||
| 87 | GPLPhLQALL | 8,64 | 67 | |||||
| 303 | DSLFaVRRHL | 8,4 | 68 | |||||
| 358 | RTLNeIYHWF | 8,4 | 69 | |||||
| 5 | RPGKpSAPSL | 8 | 70 | |||||
| 382 | KNAIrHNLSL | 8 | 71 | |||||
| 190 | SYPLIANGVC | 7,5 | 72 | |||||
| 86 | LGPLpHLQAL | 7,2 | 73 | |||||
| 60 | SLNPmPPSQL | 12 | 74 | |||||
| 184 | SAVPqSSYPL | 7,2 | 75 | |||||
| 62 | NPMPpSQLQL | 12 | 76 | |||||
| 233 | LLQReMVQSL | 12 | 77 | |||||
| 244 | QQLVIEKEKL | 6,6 | 78 | |||||
| 185 | AVPQsSYPLL | 6 | 79 | |||||
| 149 | LPPGiNVASL | 6 | 80 | |||||
| 296 | SGPReAPDSL | 6 | 81 | |||||
| 77 | VMVApSGARL | 6 | 82 | |||||
| 159 | EWVSrEPALL | 6 | 83 | |||||
| 67 | SQLQIPTLPL | 6 | 84 | |||||
| 316 | HGNStFPEFL | 6 | 85 | |||||
| 380 | TWKNaIRHNL | 5,6 | 86 | |||||
| 363 | IYHWfTRMFA | 5 | 87 | |||||
| Стартовое положение означает номер аминокислоты с N-конца Foxp3. Бальную оценку связывания получают с помощью программы "BIMAS", описанной в разделе «Материалы и способы». |
||||||||
|
Таблица 3
HLA-A0201-связывающие 10-мерные пептиды, полученные из Foxp3 |
||||
| Стартовое положение | Последовательность | Бальная оценка | SEQ ID NO | |
| Foxp3-A2-9мер | 388 | NLSLHKCFV | 382,536 | 13 |
| 95 | LLQDRPHFM | 190,448 | 14 | |
| 390 | SLHKCFVRV | 132,149 | 15 | |
| 69 | LQLPTLPLV | 102,018 | 16 | |
| 252 | KLSAMQAHL | 74,768 | 17 | |
| 68 | QLQLPTLPL | 21,362 | 18 | |
| 304 | SLFAVRRHL | 15,808 | 19 | |
| 239 | VQSLEQQLV | 11,988 | 20 | |
| 245 | QLVLEKEKL | 10,468 | 21 | |
| Foxp3-A2-10мер | 359 | TLNEIYHWFT | 1260,32 | 22 |
| 206 | KVFEEPEDFL | 267,467 | 23 | |
| 263 | KMALTKASSV | 175,812 | 24 | |
| 70 | QLPTLPLVMV | 159,97 | 25 | |
| 68 | QLQLPTLPLV | 159,97 | 26 | |
| 94 | ALLQDRPHFM | 101,099 | 27 | |
| 233 | LLQREMVQSL | 83,527 | 28 | |
| 152 | GINVASLEWV | 59,279 | 29 | |
| 77 | VMVAPSGARL | 26228 | 30 | |
| 60 | SLNPMPPSQL | 21,362 | 31 | |
| 299 | REAPDSLFAV | 18,041 | 32 | |
| 252 | KLSAMQAHLA | 17,388 | 33 | |
| 102 | FMHQLSTVDA | 16,505 | 34 | |
| 223 | LLDEKGRAQC | 13,851 | 35 | |
| 344 | TLIRWAILEA | 11,426 | 36 | |
| 246 | LVLEKEKLSA | 11,21 | 37 | |
| 238 | MVQSLEQQLV | 10,346 | 38 | |
| Стартовое положение означает номер аминокислоты с N-конца Foxp3. Бальную оценку связывания получают с помощью программы "BIMAS", описанной в разделе «Материалы и способы». |
||||
Стимулирование Т-клеток с использованием пептидов с прогнозируемой структурой, рестриктированных по HLA-A2402
Согласно методу, описанному выше в разделе «Материалы и способы», получали клетки CTL с использованием пептидов, полученных из Foxp3-белка. Полученные в результате клетки CTL, проявляющие с помощью анализа IFN-γ-ELISPOT определяемую специфичную активность CTL, показаны на фиг.IA и фиг.IB. На фиг.IA, клетки в лунке под номером #2 и 7, стимулированные Foxp3-A24-9-363, #1 и #6, стимулированные Foxp3-A24-9-366, #5, стимулированные Foxp3-A24-9-190, #7, стимулированные Foxp3-A24-10-87 и Foxp3-A24-10-60, продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.IB, клетки в лунке под номером #4, стимулированные Foxp3-A24-9-207, #6, стимулированные Foxp3-A24-9-332, #6, стимулированные Foxp3-A24-9-337, и #1, стимулированные Foxp3-A24-10-l14, продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем.
Стимулирование Т-клеток с использованием пептидов с прогнозируемой структурой, рестриктированных по HLA-A0201
Полученные в результате клетки CTL, проявляющие при осуществлении анализа IFN-γ-ELISPOT определяемую специфичную активность CTL, показаны на фиг.2A, фиг.2B и фиг.2C. На фиг.2A, клетки в лунке под номером #2, стимулированные Foxp3-A2-9-390, #2 с помощью Foxp3-A2-9-69, #6, стимулированные Foxp3-A2-9-252, #4, стимулированные Foxp3-A2-10-359, #7, стимулированные Foxp3-A2-263, и #2 и #5, стимулированные Foxp3-A2-10-94, продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.2B, клетки во всех лунках, стимулированные Foxp3-A2-10-233, в лунках с номерами #6 и #7, стимулированные Foxp3-A2-10-152, #5, стимулированные Foxp3-A2-10-77, и #l, стимулированные Foxp3-A2-10-246 и Foxp3-A2-10-94, продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.2C, клетки в лунках с номерами #1, #2, #4, #5, #7, #9, #11 и #12, стимулированные Foxp3-A2-9-390, #5 и #11, стимулированные Foxp3-A2-9-304, #7, стимулированные Foxp3-A2-9-68, и #12, стимулированные Foxp3-A2-9-252, продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем.
Создание клеточных линий CTL из специфичных пептидов Foxp3
Количество клеток в положительных лунках увеличивали за счет их деления и осуществляли анализ IFN-γ-ELISA. На фиг.3A, B и C, клеточные линии CTL, стимулированные Foxp3-A02-9-390 (SEQ ID NO:15), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.3D, клеточные линии CTL, стимулированные Foxp3-A02-9-252 (SEQ ID NO:17), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.3E клеточные линии CTL, стимулированные Foxp3-A24-10-60 (SEQ ID NO:74), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.3F клеточные линии CTL, стимулированные Foxp3-A02-10-94 (SEQ ID NO:27), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем. На фиг.3G клеточные линии CTL, стимулированные Foxp3-A24-10-87 (SEQ ID NO:68), продемонстрировали эффективное продуцирование IFN-γ по сравнению с контролем.
Специфичная активность CTL против клеток-мишеней, эндогенно экспрессирующих Foxp3 и HLA-A*2402 или HLA-A*0201
Созданные клоны CTL, индуцированных против этих пептидов, исследовали на способность распознавать клетки-мишени, эндогенно экспрессирующие Foxp3 и HLA-A*24 или 02. Специфичную активность CTL против клеток 293T, трансфецированных одновременно геном Foxp3 и молекулой HLA-A*24 или 02, которые являются специфичной моделью клеток-мишеней, эндогенно экспрессирующих Foxp3 и HLA-A*24 или 02, тестировали с использованием клеточных линий CTL, индуцированных с помощью Foxp3-A02-9-390 (SEQ ID NO:15) и Foxp3-A02-9-252 (SEQ ID NO:17), в качестве эффекторных клеток. На фиг.4A и на фиг.4B, клеточные линии CTL, индуцированные с помощью Foxp3-A02-9-390 (SEQ ID NO:15) и Foxp3-A02-9-252 (SEQ ID NO:17), продемонстрировали высокую специфичную активность клеток CTL против клеток 293T, которые были трансфецированы одновременно с помощью Foxp3 и HLA-A02. На фиг.4C, клеточные линии CTL, индуцированные с помощью Foxp3-A02-9-252 (SEQ ID NO:17), продемонстрировали высокую специфичную активность клеток CTL против клеток 293T, которые были трансфецированы одновременно с помощью Foxp3 и HLA-A24. С другой стороны, не продемонстрировано значительной специфичной активности клеток CTL в отношении контролей. Ясно продемонстрировано, что Foxp3-A02-9-390 и Foxp3-A02-9-252 естественно экспрессировались на поверхности клетки-мишени вместе с молекулой HLA-A02 и/или 24 и распознавались клетками CTL. Кроме того, эти пептиды представляли собой пептиды эпитопов, которые могут использоваться в качестве вакцины, направленной против клеток T-reg, экспрессирующих Foxp3.
Иммуногенность пептида Foxp3-A24-9-252 у мышей BALB/c
Для оценки иммуногенности пептида Foxp3-9-252 у мышей BALB/c осуществляли иммунизацию пептидом Foxp3-9-252 человека (Foxp3-252_h; KLSAMQAHL) и пептидом Foxp3-9-252 мыши (Foxp3-252_m; KLGAMQAHL) (SEQ ID NO:89) соответственно. После второй инъекции пептида определяли пептидо-специфичную активность клеток CTL с помощью анализа IFN-γ-ELISPOT (фиг.5).
В спленоцитах, собранных от мышей, вакцинированных пептидом, определяли эффективное продуцирование IFN-γ в лунке, где осуществляли совместное культивирование с соответствующими стимулированными пептидом клетками, при этом отсутствовало продуцирование IFN-γ в контрольных лунках. На фиг.5A, у трех из пяти мышей определяли специфичный для пептида Foxp3-252_h ответ клеток CTL (M3, M4 и M5), но не у контрольных мышей (N1-N3), которых вакцинировали только IFA. На фиг.5B, у одной из пяти мышей определяли специфичный для пептида Foxp3-252_m ответ клеток (Ml), но не у контрольных мышей (N1-N3), которых вакцинировали только IFA. Эти данные означают, что пептидная вакцинация каждым из пептидов Foxp3-252_h или Foxp3-252_m может индуцировать клетки CTL против стимулированных пептидом клеток-мишеней in vivo.
Противоопухолевые эффекты вакцинации пептида эпитопа Foxp3
Для определения противоопухолевых эффектов пептидной вакцинации, регулируемой Foxp3, проводили попытку in vivo терапевтической регуляции с использованием опухолевых клеток 4Tl и мышей BALB/c. Клетки рака груди 4Tl вводили подкожно мышам BALB/c в день 0 и затем вакцинацию проводили этим мышам на 3 и 10 день после появления признаков опухоли. В результате рост опухоли видимо уменьшился у мышей BALB/c, вакцинированных пептидами Foxp3-252_h или Foxp3-252_m, по сравнению с контрольными мышами (фиг.6). Что касается статистического анализа, то он показал значительное отличие от подавления опухолевого роста у мышей, вакцинированных с использованием пептидов эпитопа Foxp3.
Аминокислотная замена в пептиде эпитопа Foxp3
В приведенных выше результатах пептид Foxp3-9-252 (SEQ ID NO:17) идентифицируется как пептид эпитопа, рестриктированный одновременно по HLA-A*2402 и HLA-A*0201. Для повышения иммуногенности пептида Foxp3-9-252 выбирали одну или две аминокислотные замены для достижения более высокой аффинности связывания с молекулой HLA-A*2402 или с HLA-A*0201, чем у природного пептида Foxp3-9-252; Foxp3-9-252-WT (KLSAMQAHL)(SEQ ID NO:17). Бальную оценку связывания пептида с аминокислотной заменой Foxp3-9-252 (SEQ ID NO:17) получали с помощью программ BIMAS. В таблице 4 показаны аминокислотные последовательности и бальная оценка связывания с молекулой HLA-A*2402 и 0201 пептида Foxp3-9-252, содержащего аминокислотную замену. Бальную оценку связывания пептида получали с помощью программ BIMAS. Синтезировали, в общем, пятнадцать пептидов, содержащих шесть или девять типов замен, для которых прогнозировали более высокую аффинность связывания с молекулой HLA-A24 или HLA-A2, чем у пептида дикого типа (таблица 4).
|
Таблица 4
Бальная оценка связывания пептида Foxp3-9-252, содержащего аминокислотную замену, (SEQ ID NO:17) с молекулой HLA-A*2402 или 0201 |
||||
| Название пептида | Последовательность | Бальная оценка | SEQ ID NO | |
| A2402 | Foxp3-9-252 | KLSAMQAHL | 8,0 | 17 |
| 2Y | KYSAMQAHL | 400,0 | 89 | |
| 2F | KFSAMQAHL | 40,0 | 90 | |
| 2Y9I | KYSAMQAHI | 100,0 | 91 | |
| 2Y9F | KYSAMQAHF | 200,0 | 92 | |
| 2F9I | KFSAMQAHI | 10,0 | 93 | |
| 2F9F | KFSAMQAHF | 20,0 | 94 | |
| A0201 | WT | KLSAMQAHL | 74,8 | 17 |
| 9V | KLSAMQAHV | 243,4 | 95 | |
| 3Y | KLYAMQAHL | 239,3 | 96 | |
| 3M | KLMAMQAHL | 276,6 | 97 | |
| 3L | KLLAMQAHL | 276,6 | 98 | |
| 3F | KLFAMQAHL | 276,6 | 99 | |
| 3Y9V | KLYAMQAHV | 779,0 | 100 | |
| 3M9V | KLMAMQAHV | 900,7 | 101 | |
| 3L9V | KLLAMQAHV | 900,7 | 102 | |
| 3F9V | KLFAMQAHV | 900,7 | 103 | |
Затем авторы настоящего изобретения определяли, распознаются ли с использованием этих замен клетками CTL, генерированными с помощью пептида Foxp3-9-252-WT, стимуляторы клеток, стимулированных пептидом. Вследствие этого клетки CTL, индуцированные с помощью пептида Foxp3-9-252-WT, продуцировали IFN-γ против клеток T2, стимулированных пептидом Foxp3-9-252-9V (KLSAMQAHV)(SEQ ID NO:95), подобно клеткам Т2, стимулированным пептидом Foxp3-9-252-WT (фиг.7A). Хотя в отсутствие какого-либо пептидного стимулирования не определяли продукции IFN-γ клетками CTL против стимулирующих клеток, это означает, что клетки CTL, генерированные с помощью пептида Foxp3-9-252-WT, могут распознавать презентацию пептида Foxp3-9-252-9V на молекуле HLA-A2, а также пептида Foxp3-9-252-WT.
Кроме того, для оценки, обладает ли пептид Foxp3-9-252-9V более высокой аффинностью в отношении молекулы HLA-A2, чем пептид Foxp3-9-252-WT, активность клеток CTL определяли с использованием стимуляторов клеток, стимулированных этими пептидами, в широком интервале концентраций (10-10-4 мкг/мл). В результате аналогично продуцировался IFN-γ клетками CTL, культивированными совместно со стимуляторами клеток, стимулированных пептидом Foxp3-9-252-WT или Foxp3-9-252-9V соответственно (фиг.7B). На основании этих данных было показано, что презентация пептида Foxp3-9-252-9V на молекуле HLA-A*0201 может распознаваться клетками CTL, созданными с помощью пептида Foxp3-9-252-WT.
С другой стороны, авторы настоящего изобретения осуществили попытку индукции клеток CTL с использованием всех пептидов, содержащих замены, рестриктированных по HLA-A*0201, включающих пептид Foxp3-9-252-9V. В результате клетки CTL индуцировали с помощью стимулирования пептидом Foxp3-9-252-3M (KLMAMQAHL)(SEQ ID NO:97), Foxp3-9-252-3L (KLLAMQAHL)(SEQ ID NO:98) или пептидом Foxp3-9-252-9V (фиг.7C). Клетки в лунке под номером 3 и 7, стимулированные Foxp3-A02-9-252-3M, в лунке под номером 7, стимулированные Foxp3-A02-9-252-3L, и в лунке под номером 8, стимулированные Foxp3-A02-9-252-9V, продемонстрировали по сравнению с контролем пептидозависимую продукцию IFN-γ. После создания in vitro клеточной линии CTL, индуцированной с помощью стимулирования пептидом Foxp3-9-252-9V, определяли активность клеток CTL с использованием стимулятора клеток, стимулированных пептидом Foxp3-9-252-WT или Foxp3-9-252-9V. Следовательно, клетки CTL, индуцированные с помощью стимулирования пептидом Foxp3-9-252-9V, распознавали стимулирующие клетки, стимулированные пептидом Foxp3-9-252-WT, точно так же, как клетки, стимулированные пептидом Foxp3-9-252-9V (фиг.7D). Эти результаты убедительно показали, что пептид Foxp3-9-252-9V может индуцировать Foxp3-специфичные клетки CTL, так же как пептид Foxp3-9-252-WT.
Анализ гомологии антигенных пептидов
Клетки CTL, стимулированные
FOXp3-A24-9-363 (SEQ ID NO:3),
FOXp3-A24-9-366 (SEQ ID NO:7),
FOXp3-A24-9-190 (SEQ ID NO:9),
FOXp3-A24-9-207 (SEQ ID NO:4),
FOXp3-A24-9-332 (SEQ ID NO:5),
FOXp3-A24-9-337 (SEQ ID NO:8),
FOXp3-A24-10-114 (SEQ ID NO:12),
FOXp3-A2-9-390 (SEQ ID NO:15),
FOXp3-A2-9-69 (SEQ ID NO:16),
FOXp3-A2-9-252 (SEQ ID NO:17),
FOXp3-A2-10-359 (SEQ ID NO:22),
FOXp3-A2-10-263 (SEQ ID NO:24),
FOXp3-A2-10-94 (SEQ ID NO:27),
FOXp3-A2-10-233 (SEQ ID NO:28),
FOXp3-A2-10-152 (SEQ ID NO:29),
FOXp3-A2-10-77 (SEQ ID NO:30),
FOXp3-A2-10-246 (SEQ ID NO:37),
FOXp3-A2-9-68 (SEQ ID NO:18),
FOXp3-A2-9-304 (SEQ ID NO:19)
Foxp3-A24-10-87 (SEQ ID NO:67) и
Foxp3-A24-10-60 (SEQ ID NO:74), демонстрировали существенную и специфичную активность CTL.
Это означает, что последовательности
FOXp3-A24-9-363 (SEQ ID NO:3),
FOXp3-A24-9-366 (SEQ ID NO:7),
FOXp3-A24-9-190 (SEQ ID NO:9),
FOXp3-A24-9-207 (SEQ ID NO:4),
FOXp3-A24-9-332 (SEQ ID NO:5),
FOXp3-A24-9-337 (SEQ ID NO:8),
FOXp3-A24-10-114 (SEQ ID NO:12),
FOXp3-A2-9-390 (SEQ ID NO:15),
FOXp3-A2-9-69 (SEQ ID NO:16),
FOXp3-A2-9-252 (SEQ ID NO:17),
FOXp3-A2-10-359 (SEQ ID NO:22),
FOXp3-A2-10-263 (SEQ ID NO:24),
FOXp3-A2-10-94 (SEQ ID NO:27),
FOXp3-A2-10-233 (SEQ ID NO:28),
FOXp3-A2-10-152 (SEQ ID NO:29),
FOXp3-A2-10-77 (SEQ ID NO:30),
FOXp3-A2-10-246 (SEQ ID NO:37),
FOXp3-A2-9-68 (SEQ ID NO:18),
FOXp3-A2-9-304 (SEQ ID NO:19)
Foxp3-A24-10-87 (SEQ ID NO:67) и
Foxp3-A24-10-60 (SEQ ID NO:74) являются гомологичными пептидам, полученным из других молекул, о которых известно, что они синтезируются иммунной системой человека. Для исключения такой возможности осуществляли анализ на гомологию с последовательностями пептидов как запрос с использованием алгоритма BLAST (http://www.ncbi.nlm.nih.gov/blast/blast.cgi) и не обнаружили последовательности, обладающей существенной гомологией с данными последовательностями.
Полученные результаты показывают, что последовательности
FOXp3-A24-9-363 (SEQ ID NO:3),
FOXp3-A24-9-366 (SEQ ID NO:7),
FOXp3-A24-9-190 (SEQ ID NO:9),
FOXp3-A24-9-207 (SEQ ID NO:4),
FOXp3-A24-9-332 (SEQ ID NO:5),
FOXp3-A24-9-337 (SEQ ID NO:8),
FOXp3-A24-10-114 (SEQ ID NO:12),
FOXp3-A2-9-390 (SEQ ID NO:15),
FOXp3-A2-9-69 (SEQ ID NO:16),
FOXp3-A2-9-252 (SEQ ID NO:17),
FOXp3-A2-10-359 (SEQ ID NO:22),
FOXp3-A2-10-263 (SEQ ID NO:24),
FOXp3-A2-10-94 (SEQ ID NO:27),
FOXp3-A2-10-233 (SEQ ID NO:28),
FOXp3-A2-10-152 (SEQ ID NO:29),
FOXp3-A2-10-77 (SEQ ID NO:30),
FOXp3-A2-10-246 (SEQ ID NO:37),
FOXp3-A2-9-68 (SEQ ID NO:18),
FOXp3-A2-9-304 (SEQ ID NO:19)
Foxp3-A24-10-87 (SEQ ID NO:67) и
Foxp3-A24-10-60 (SEQ ID NO:74) являются уникальными и существует малая вероятность того, насколько известно авторам, что может быть получен непредусмотренный иммунологический ответ на любую другую молекулу.
В заключение, Foxp3 представляет собой антиген, который может быть использован для регуляции клеток T-reg, а также вакцины, использующие такие пептиды эпитопов, могут быть использованы для иммунотерапии.
Обсуждение
Из данных фиг.6 следует, что вакцинация каждым из пептидов hFoxp3-252 и mFoxp3-252 может индуцировать эпитоп-специфичный ответ клеток CTL in vivo. Это означает, что оба пептида эпитопов Foxp3 могут индуцировать клетки CTL против клеток-мишеней, экспрессирующих Foxp3, и соответствующую молекулу главного комплекса гистосовместимости. Другими словами, предполагается, что клетки CTL могут распознавать регуляторные T-лимфоциты (T-reg). Для оценки этой гипотезы определяли in vivo противоопухолевые эффекты вакцинации с помощью пептидов эпитопа Foxp3 при использовании мышей BALB/c. Были продемонстрированы очевидные противоопухолевые эффекты у мышей, вакцинированных с помощью пептида hFoxp3-252 и mFoxp3-252 соответственно. Эти результаты убедительно показывают, что опухолевый рост может ингибироваться подавлением клеток T-reg внутри локального микроокружения опухоли даже без вакцинации с использованием любых пептидов эпитопа TAA. Авторы настоящего изобретения считают, что клетки CTL против опухолевых клеток индуцируются, когда опухоль появляется внутри организма, однако клетки T-reg также индуцируются некоторыми иммуносупрессивными факторами опухолевых клеток и ингибируют функцию противоопухолевых эффекторных клеток. Так как вакцинация с использованием пептида эпитопа Foxp3 может остановить развитие иммуносупрессивного процесса посредством уничтожения или подавления клеток T-reg, противоопухолевые эффекты были продемонстрированы в отсутствие вакцинации с помощью пептида эпитопа TAA или стимулирования иммунной системы в целом с использованием сильнодействующего адъюванта.
Между прочим, вакцинация с помощью пептида hFoxp3-252 (KLSAMQAHL) (SEQ ID NO:17) может индуцировать клетки CTL и противоопухолевые эффекты в большей степени, чем вакцинация с помощью пептида mFoxp3-252 (KLGAMQAHL)(SEQ ID NO:88), как показано на фиг.5 и фиг.6. Из этих результатов можно предположить, что с помощью вакцинации с использованием пептида hFoxp3-252 можно эффективно избежать иммунологической толерантности по сравнению с вакцинацией с использованием пептида mFoxp3-252. Другими словами, так как аминокислотная последовательность пептида hFoxp3-252 отличается от аминокислотной последовательности пептида mFoxp3-252 в положении 3, то предполагается, что пептид hFoxp3-252 не является "аутоантигеном" in vivo и может эффективно индуцировать клетки CTL против клеток T-reg.
В заключение, показано, что Foxp3 может служить в качестве новых мишеней для иммунотерапии рака. Кроме того, полученные результаты убедительно поддерживают тот факт, что вакцинация с использованием пептида эпитопа Foxp3 может подавлять функцию клеток T-reg и должна быть доступна для иммунотерапии рака для многих типов раковых клеток.
Claims (21)
1. Пептид, обладающий способностью индуцировать цитотоксические Т-клетки, где пептид состоит из аминокислотных последовательностей SEQ ID NO:3-5, 7-9, 12, 15-19, 22, 24, 27-30, 37, 67 или 74.
2. Пептид, обладающий способностью индуцировать цитотоксические Т-клетки, где пептид состоит из аминокислотной последовательности SEQ ID NO:3-5, 7-9, 12, 17, 67 или 74, в которой заменены или добавлены 1 или 2 аминокислот.
3. Пептид по п.2, в котором вторая аминокислота с N-конца аминокислотной последовательности SEQ ID NO:3-5, 7-9, 12, 17, 67 или 74 заменена фенилаланином, тирозином, метионином или триптофаном.
4. Пептид по п.2 или 3, в котором С-концевая аминокислота аминокислотной последовательности SEQ ID NO:3-5, 7-9, 12,17, 67 или 74 заменена фенилаланином, лейцином, изолейцином, триптофаном или метионином.
5. Пептид, обладающий способностью индуцировать цитотоксические Т-клетки, где пептид состоит из аминокислотной последовательности SEQ ID NO:15-19, 22, 24, 27-30 или 37, в которой заменены или добавлены 1 или 2 аминокислот.
6. Пептид по п.5, в котором вторая аминокислота с N-конца аминокислотной последовательности SEQ ID NO:15-19, 22, 24, 27-30 или 37 заменена лейцином или метионином.
7. Пептид по п.5 или 6, в котором С-концевая аминокислота аминокислотной последовательности SEQ ID NO:15-19, 22, 24, 27-30 или 37 является валином или лейцином.
8. Пептид по п.2 или 5, причем пептид содержит аминокислотную последовательность SEQ ID NO:95, 97 или 98.
9. Фармацевтическое средство, использующееся для регуляции клеток Т-reg, которое содержит 1 или несколько типов пептидов по любому из пп.1-8, которое предназначено для введения индивиду, антиген HLA которого представляет собой HLA-A24 или HLA-A02.
10. Фармацевтическое средство по п.9, использующееся для ингибирования пролиферации клеток T-reg.
11. Фармацевтическое средство по п.9, использующееся для подавления функции клетки T-reg.
12. Фармацевтическое средство по п.9, использующееся для лечения рака.
13. Фармацевтическое средство по п.12, представляющее собой вакцину.
14. Способ индукции антиген-презентирующих клеток, обладающих высокой способностью индуцировать цитотоксические Т-клетки, путем введения пептида по любому из пп.1-8.
15. Способ индукции цитотоксических Т-клеток путем приведения в контакт антиген-презентирующей клетки с пептидом по любому из пп.1-8 и смешивания антиген-презентирующей клетки с CD8+ Т-клетками и совместного культивирования.
16. Выделенная цитотоксическая Т-клетка, индуцируемая пептидом по любому из пп.1-8.
17. Выделенная цитотоксическая Т-клетка, индуцированная способом по п.15.
18. Антиген-презентирующая клетка, индуцируемая способом по п.14.
19. Способ регуляции клеток T-reg у индивида, включающий введение указанному индивиду вакцины, содержащей пептид по любому из пп.1-8.
20. Применение пептида по любому из пп.1-8 для получения вакцины, использующейся для регуляции клеток T-rеg у индивида.
21. Полинуклеотид, кодирующий пептид по любому из пп.1-8.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US87861507P | 2007-01-03 | 2007-01-03 | |
| US60/878,615 | 2007-01-03 | ||
| US89647207P | 2007-03-22 | 2007-03-22 | |
| US60/896,472 | 2007-03-22 | ||
| PCT/JP2007/001466 WO2008081581A1 (en) | 2007-01-03 | 2007-12-26 | Foxp3 peptide vaccine |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2009129531A RU2009129531A (ru) | 2011-02-10 |
| RU2473557C2 true RU2473557C2 (ru) | 2013-01-27 |
Family
ID=39588270
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2009129531/10A RU2473557C2 (ru) | 2007-01-03 | 2007-12-26 | Вакцины на основе пептида foxp3 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US8563516B2 (ru) |
| EP (2) | EP2481748A3 (ru) |
| JP (1) | JP5339375B2 (ru) |
| KR (1) | KR20090099075A (ru) |
| CN (1) | CN101641369B (ru) |
| AU (1) | AU2007340834B2 (ru) |
| BR (1) | BRPI0720794A2 (ru) |
| CA (1) | CA2674365A1 (ru) |
| IL (1) | IL199622A0 (ru) |
| MX (1) | MX2009007261A (ru) |
| RU (1) | RU2473557C2 (ru) |
| SG (1) | SG177199A1 (ru) |
| TW (1) | TWI441648B (ru) |
| WO (1) | WO2008081581A1 (ru) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009050486A2 (en) * | 2007-10-19 | 2009-04-23 | The University Of Surrey | Peptide manipulators of regulatory t cell activity |
| CZ2008565A3 (cs) * | 2008-09-15 | 2009-11-18 | Vysoká škola chemicko technologická v Praze | Príprava monoklonálních protilátek proti FoxP3 proteinu s použitím modifikovaných virum podobných cástic Masonova-Pfizerova opicího viru |
| CN102333867B (zh) * | 2008-12-24 | 2015-01-14 | 肿瘤疗法科学股份有限公司 | C1orf59肽及包含它的疫苗 |
| TWI507204B (zh) * | 2009-05-26 | 2015-11-11 | Oncotherapy Science Inc | Cdc45l胜肽與含此胜肽之疫苗 |
| MX350220B (es) * | 2011-08-12 | 2017-08-30 | Oncotherapy Science Inc | Peptidos de mphosph1 y vacunas que incluyen los mismos. |
| CN102603892B (zh) * | 2012-02-22 | 2013-10-30 | 尉军 | 一种肿瘤标志物foxp3抗原多肽及应用 |
| WO2017124001A2 (en) | 2016-01-14 | 2017-07-20 | Memorial Sloan-Kettering Cancer Center | T cell receptor-like antibodies specific for foxp3-derived peptides |
| CN111375055B (zh) * | 2020-02-20 | 2021-09-03 | 陈宛莎 | 一种2019-nCoV亚单位疫苗组合物及其免疫方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2129439C1 (ru) * | 1991-07-25 | 1999-04-27 | Айдек Фармасьютикалс Корпорейшн | Антигенная композиция для индуцирования ответа цитотоксических т-лимфоцитов, способ индуцирования и способ лечения болезни |
| US20030170648A1 (en) * | 2001-05-08 | 2003-09-11 | Darwin Molecular Corporation | Method for regulating immune function in primates using the Foxp3 protein |
| WO2004024766A1 (ja) * | 2002-09-12 | 2004-03-25 | Oncotherapy Science, Inc. | Kdrペプチド及びこれを含むワクチン |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0417430D0 (en) | 2004-08-05 | 2004-09-08 | Uc3 | A novel HPV vaccine comprising peptides from host cell proteins |
| JP4628208B2 (ja) * | 2004-08-10 | 2011-02-09 | オンコセラピー・サイエンス株式会社 | Cxadrl1またはgcud1タンパク質を発現する胃癌または結腸直腸癌の治療のためのペプチドワクチン |
| JP4840866B2 (ja) * | 2005-01-19 | 2011-12-21 | 学校法人慶應義塾 | 癌ワクチン |
-
2007
- 2007-12-25 TW TW096149888A patent/TWI441648B/zh not_active IP Right Cessation
- 2007-12-26 CN CN200780051977.4A patent/CN101641369B/zh not_active Expired - Fee Related
- 2007-12-26 EP EP12153796A patent/EP2481748A3/en not_active Withdrawn
- 2007-12-26 AU AU2007340834A patent/AU2007340834B2/en not_active Ceased
- 2007-12-26 KR KR1020097015693A patent/KR20090099075A/ko active IP Right Grant
- 2007-12-26 CA CA002674365A patent/CA2674365A1/en not_active Abandoned
- 2007-12-26 SG SG2011091279A patent/SG177199A1/en unknown
- 2007-12-26 EP EP07849885A patent/EP2114987A4/en not_active Withdrawn
- 2007-12-26 BR BRPI0720794-8A patent/BRPI0720794A2/pt not_active IP Right Cessation
- 2007-12-26 MX MX2009007261A patent/MX2009007261A/es active IP Right Grant
- 2007-12-26 US US12/522,066 patent/US8563516B2/en not_active Expired - Fee Related
- 2007-12-26 RU RU2009129531/10A patent/RU2473557C2/ru not_active IP Right Cessation
- 2007-12-26 JP JP2009524039A patent/JP5339375B2/ja not_active Expired - Fee Related
- 2007-12-26 WO PCT/JP2007/001466 patent/WO2008081581A1/en active Application Filing
-
2009
- 2009-06-30 IL IL199622A patent/IL199622A0/en unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2129439C1 (ru) * | 1991-07-25 | 1999-04-27 | Айдек Фармасьютикалс Корпорейшн | Антигенная композиция для индуцирования ответа цитотоксических т-лимфоцитов, способ индуцирования и способ лечения болезни |
| US20030170648A1 (en) * | 2001-05-08 | 2003-09-11 | Darwin Molecular Corporation | Method for regulating immune function in primates using the Foxp3 protein |
| WO2004024766A1 (ja) * | 2002-09-12 | 2004-03-25 | Oncotherapy Science, Inc. | Kdrペプチド及びこれを含むワクチン |
Non-Patent Citations (1)
| Title |
|---|
| NAIR S. et al., Vaccination against the Forkhead Family Transcription Factor Foxp3. Enhances Tumor Immunity, Cancer Res, 2007, n.67 (1), January 1, 2007. * |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2008081581A1 (en) | 2008-07-10 |
| MX2009007261A (es) | 2009-11-11 |
| EP2114987A4 (en) | 2010-07-21 |
| KR20090099075A (ko) | 2009-09-21 |
| JP2010514669A (ja) | 2010-05-06 |
| BRPI0720794A2 (pt) | 2014-03-11 |
| US8563516B2 (en) | 2013-10-22 |
| TWI441648B (zh) | 2014-06-21 |
| CA2674365A1 (en) | 2008-07-10 |
| RU2009129531A (ru) | 2011-02-10 |
| EP2481748A2 (en) | 2012-08-01 |
| IL199622A0 (en) | 2010-04-15 |
| TW200835516A (en) | 2008-09-01 |
| SG177199A1 (en) | 2012-01-30 |
| EP2114987A1 (en) | 2009-11-11 |
| AU2007340834B2 (en) | 2013-02-28 |
| US20100092501A1 (en) | 2010-04-15 |
| AU2007340834A1 (en) | 2008-07-10 |
| JP5339375B2 (ja) | 2013-11-13 |
| CN101641369B (zh) | 2014-10-22 |
| EP2481748A3 (en) | 2012-10-24 |
| CN101641369A (zh) | 2010-02-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10711047B2 (en) | CDCA1 epitope peptides and vaccines containing the same | |
| TWI434853B (zh) | 腫瘤血管內皮標誌8胜肽及包含此胜肽之疫苗 | |
| US20110280898A1 (en) | Inhbb epitope peptides and vaccines containing the same | |
| US8617562B2 (en) | FOXM1 peptides and immunogenic compositions containing them | |
| RU2473557C2 (ru) | Вакцины на основе пептида foxp3 | |
| RU2496787C2 (ru) | Пептиды эпитопов mybl2 и содержащие их вакцины | |
| US9675680B2 (en) | MELK epitope peptides and vaccines containing the same | |
| KR20110074919A (ko) | Rab6kifl/kif20a 에피토프 펩티드 및 이를 포함하는 백신 | |
| US9745343B2 (en) | Method of inducing an immune response by administering WDRPUH epitope peptides |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20151227 |