RU2470907C2 - Терапевтические соединения - Google Patents
Терапевтические соединения Download PDFInfo
- Publication number
- RU2470907C2 RU2470907C2 RU2009145541/04A RU2009145541A RU2470907C2 RU 2470907 C2 RU2470907 C2 RU 2470907C2 RU 2009145541/04 A RU2009145541/04 A RU 2009145541/04A RU 2009145541 A RU2009145541 A RU 2009145541A RU 2470907 C2 RU2470907 C2 RU 2470907C2
- Authority
- RU
- Russia
- Prior art keywords
- formula
- compound
- propofol
- pharmaceutically acceptable
- animal
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C39/00—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring
- C07C39/02—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring monocyclic with no unsaturation outside the aromatic ring
- C07C39/06—Alkylated phenols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/05—Phenols
- A61K31/055—Phenols the aromatic ring being substituted by halogen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/08—Drugs for disorders of the alimentary tract or the digestive system for nausea, cinetosis or vertigo; Antiemetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/02—Muscle relaxants, e.g. for tetanus or cramps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P23/00—Anaesthetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/12—Ophthalmic agents for cataracts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/06—Free radical scavengers or antioxidants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C245/00—Compounds containing chains of at least two nitrogen atoms with at least one nitrogen-to-nitrogen multiple bond
- C07C245/20—Diazonium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C271/00—Derivatives of carbamic acids, i.e. compounds containing any of the groups, the nitrogen atom not being part of nitro or nitroso groups
- C07C271/06—Esters of carbamic acids
- C07C271/40—Esters of carbamic acids having oxygen atoms of carbamate groups bound to carbon atoms of six-membered aromatic rings
- C07C271/42—Esters of carbamic acids having oxygen atoms of carbamate groups bound to carbon atoms of six-membered aromatic rings with the nitrogen atoms of the carbamate groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C271/44—Esters of carbamic acids having oxygen atoms of carbamate groups bound to carbon atoms of six-membered aromatic rings with the nitrogen atoms of the carbamate groups bound to hydrogen atoms or to acyclic carbon atoms to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C37/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring
- C07C37/001—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by modification in a side chain
- C07C37/003—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by modification in a side chain by hydrogenation of an unsaturated part
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C37/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring
- C07C37/01—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by replacing functional groups bound to a six-membered aromatic ring by hydroxy groups, e.g. by hydrolysis
- C07C37/045—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by replacing functional groups bound to a six-membered aromatic ring by hydroxy groups, e.g. by hydrolysis by substitution of a group bound to the ring by nitrogen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C37/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring
- C07C37/01—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by replacing functional groups bound to a six-membered aromatic ring by hydroxy groups, e.g. by hydrolysis
- C07C37/055—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by replacing functional groups bound to a six-membered aromatic ring by hydroxy groups, e.g. by hydrolysis the substituted group being bound to oxygen, e.g. ether group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C37/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring
- C07C37/68—Purification; separation; Use of additives, e.g. for stabilisation
- C07C37/86—Purification; separation; Use of additives, e.g. for stabilisation by treatment giving rise to a chemical modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C39/00—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring
- C07C39/24—Halogenated derivatives
- C07C39/26—Halogenated derivatives monocyclic monohydroxylic containing halogen bound to ring carbon atoms
- C07C39/27—Halogenated derivatives monocyclic monohydroxylic containing halogen bound to ring carbon atoms all halogen atoms being bound to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/07—Optical isomers
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Pain & Pain Management (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- Ophthalmology & Optometry (AREA)
- Hospice & Palliative Care (AREA)
- Anesthesiology (AREA)
- Psychology (AREA)
- Psychiatry (AREA)
- Toxicology (AREA)
- Urology & Nephrology (AREA)
- Immunology (AREA)
- Vascular Medicine (AREA)
- Addiction (AREA)
- Rheumatology (AREA)
- Cardiology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Pulmonology (AREA)
- Heart & Thoracic Surgery (AREA)
- Otolaryngology (AREA)
- Biochemistry (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Настоящее изобретение относится к новому (-)-стереизомеру формулы (I), где Х является Н, или к его фармацевтически приемлемой соли, которые агонизируют рецептор GABA, к фармацевтической композиции на основе предложенного соединения, к способам получения (-)-стереизомера формулы (I) или его фармацевтически приемлемой соли, к способу индуцирования или поддержания общей анастезии, к способу промотирования обезболивания и к способу прототирования антиэметической активности с использованием предложенного (-)-стереоизомера или его фармацевтически приемлемой соли, а также к новому диастереизомеру (-)-2-втор-бутил-6-изопропилфенилового эфира карбаминовой кислоты формулы (II), где R1 представляет хиральную аминогруппу и Х является Н. 10 н. и 6 з.п. ф-лы, 12 пр., 6 табл., 4 ил.
Description
Область техники, к которой относится изобретение
Настоящее изобретение относится к терапевтическим соединениям, пригодным в качестве анестетиков.
Уровень техники
Пропофол (2,6-диизопропилфенол) является внутривенным седативным/снотворным средством, широко используемым для индуцирования и поддержания общей анестезии (общего наркоза), обезболивания серьезно больных пациентов и обезболивания при процедурах (например, эндоскопии). См. Langly, M.S. и Heel, R.C. Drugs, 1988, 35, 334-372. Пропофол только умеренно растворяется в воде и в настоящее время продается в 10% соевом масле на основе липидной эмульсии, подобно композициям для парентерального питания.
Пропофол представляет собой агонист GABAA (гамма-аминомасляной кислоты, ГАМК), активирующий разные подтипы рецепторов GABAA, которые являются ионными каналами, переносящими анионы хлора через клеточные мембраны в центральной нервной системе. Несмотря на то, что пропофол является ахиральным, рацемические смеси ряда диалкилфенолов являются известными агонистами рецептора GABAA (James et al., J. Med. Chem. 23, 1350, 1980; Krasowski et al., J. Pharmacol. & Exp.Therapeutics 297, 338, 2001). James et al. сообщает об открытии факта, что пропофол является преобладающим в общем профиле по отношению к другим оцененным аналогам.
Многие клиницисты предпочитают пропофол из-за его прекрасного фармакокинетического и фармакодинамического профилей, профилей выхода из наркоза и восстановления сознания после наркоза. Однако нежелательные побочные действия (например, угнетение дыхания, синдром ICU, инъекционная боль и гемодинамические эффекты), вызываемые терапевтической дозой или близкой к ней дозой, значительно ограничивают его пользу в разнообразных клинических ситуациях. Это, в частности, относится к гемодинамическим эффектам. Введение пропофола, особенно в болюсной форме, часто вызывает снижение кровяного давления без компенсаторного увеличения частоты сердечных сокращений. Некоторые клинические состояния являются несовместимыми с применением пропофола из-за нежелательных и потенциально вредных гемодинамических последствий. Примеры таких состояний включают сердечно-сосудистую болезнь, такую как болезнь коронарных артерий, кардиомиопатию, ишемическую болезнь сердца, порок клапана сердца и врожденный порок сердца. Хроническая гипертония, цереброваскулярная болезнь, травма головного мозга и пожилой возраст могут сделать применение пропофола затрудненным или проблематичным из-за его гемодинамических свойств. Пациенты с острой потерей крови, обезвоживанием или тяжелой инфекцией, включая пациентов с геморрагическим шоком, гиповолемическим шоком или септическим шоком, могут быть подвергнуты чрезмерному риску при применении пропофола. Гемодинамические свойства пропофола могут ограничивать его использование у пациентов, получающих другие медикаменты или виды лечения, такие как спинальная анестезия, эпидуральная анестезия или вазоактивные медикаменты.
Раскрытие изобретения
Изобретение предоставляет терапевтические соединения, которые демонстрируют сходную или улучшенную фармакологическую активность по сравнению с пропофолом наряду с улучшенным гемодинамическим профилем. Соответственно, в одном варианте осуществления изобретение предоставляет (-)-стереоизомер формулы (I):
в которой X представляет собой H или F, или его соль, или пролекарство.
Изобретение также предоставляет фармацевтическую композицию, содержащую
(-)-стереоизомер формулы (I), или его фармацевтически приемлемую соль, или пролекарство и фармацевтически приемлемый носитель.
Изобретение также предоставляет способ лечения тошноты, рвоты, мигрени, нейродегенеративных состояний нервной системы (например, болезни Фридриха, болезни Паркинсона, болезни Альцгеймера, болезни Хантингтона, бокового амиотрофического склероза (ALS), рассеянного склероза (MS), болезни Пика и т.д.), травм центральной нервной системы (например, перелома черепа и происходящего в результате этого отека, сотрясения, контузии, тяжелого кровоизлияния в мозг, резаных повреждений, субдурального и эпидурального кровоизлияния и повреждения спинного мозга (например, механического повреждения вследствие сжатия или изгибания позвоночника)), конвульсий (например, эпилептических припадков) или болезни, связанной со свободными радикалами (например, ишемического реперфузионного повреждения, воспалительного заболевания, системной красной волчанки, инфаркта миокарда, инсульта, травматической геморрагии, образования катаракты, увеита, эмфиземы, язвы желудка, неоплазии, лучевой болезни и т.д.) у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ индуцирования или поддержания общей анестезии у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ промотирования обезболивания у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ лечения мигрени у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ лечения бессонницы у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ промотирования анксиолитического эффекта у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ лечения синдрома отмены зависимости у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ промотирования антиэметического эффекта у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет способ агонизирования рецептора GABA, включающий соприкосновение рецептора (in vitro или in vivo) с эффективным количеством (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства.
Изобретение также предоставляет способ агонизирования рецептора GABA у животного, включающий введение эффективного количества (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства животному.
Изобретение также предоставляет (-)-стереоизомер формулы (I), или его фармацевтически приемлемую соль, или его пролекарство для применения в лекарственной терапии.
Изобретение также предоставляет применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента для лечения тошноты, рвоты, мигрени, нейродегенеративных состояний нервной системы (например, болезни Фридриха, болезни Паркинсона, болезни Альцгеймера, болезни Хантингтона, бокового амиотрофического склероза (ALS), рассеянного склероза (MS), болезни Пика и т.д.), травм центральной нервной системы (например, перелома черепа и происходящего в результате этого отека, сотрясения, контузии, тяжелого кровоизлияния в мозг, резаных повреждений, субдурального и эпидурального кровоизлияния и повреждения спинного мозга (например, механического повреждения вследствие сжатия или изгибания позвоночника)), конвульсий (например, эпилептических конвульсий) или болезни, связанной со свободными радикалами (например, ишемического реперфузионного повреждения, воспалительного заболевания, системной красной волчанки, инфаркта миокарда, инсульта, травматической геморрагии, образования катаракты, увеита, эмфиземы, язвы желудка, неоплазии, лучевой болезни и т.д.) у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента для индуцирования или поддержания общей анестезии у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента для проведения обезболивания у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента для лечения мигрени у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента для лечения бессонницы у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента промотирования анксиолитического эффекта у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента для лечения синдрома отмены зависимости у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента промотирования антиэметического эффекта у животного.
Изобретение также обеспечивает применение (-)-стереоизомера формулы (I), или его фармацевтически приемлемой соли, или его пролекарства для приготовления медикамента для агонизирования рецептора GABA у животного.
Изобретение также предоставляет способ синтеза и промежуточные соединения, раскрытые в данном описании, которые являются пригодными для получения (-)-стереоизомера формулы (I), или его соли, или его пролекарства.
Краткое описание чертежей
Фигура 1 показывает гемодинамические эффекты (-) стереоизомера формулы (I), в которой X представляет собой Н, применяемого в дозе 3 мг/кг, в исследовании на свиньях.
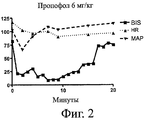
Фигура 2 показывает гемодинамические эффекты пропофола, применяемого в дозе 6 мг/кг, в исследовании на свиньях.
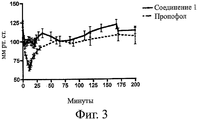
Фигура 3 показывает влияние (-)стереоизомера формулы (I), в которой X представляет собой H, на значение артериального кровяного давления (мм рт.ст.) у свиней после внутривенного (BB) вливания по сравнению с пропофолом.
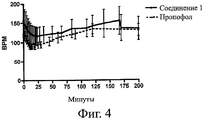
Фигура 4 показывает влияние (-)стереоизомера формулы (I), в которой X представляет собой H, на частоту сердечного ритма (ударов в минуту) у свиней после внутривенного (BB) вливания по сравнению с пропофолом.
Осуществление изобретения
Настоящее изобретение предоставляет (-)стереоизомер формулы (I), или его соль, или его пролекарство, как определено выше.
Абсолютная конфигурация такого стереоизомера определена как (R).
В одном варианте X является H. Когда X является H, стереоизомер также может называться (R)-(-)-2-втор-бутил-6-изопропилфенолом.
Было обнаружено, что, по сравнению с пропофолом, (R)-(-)-2-втор-бутил-6-изопропилфенол демонстрирует неожиданно улучшенный общий профиль активности в качестве анестетика. В частности, было найдено, что соединение оказывает более сильное анестезирующее действие, показывает более высокий терапевтический индекс и сохраняет сравнимый фармакокинетический профиль, например демонстрирует сходную скорость выведения из организма. Также соединение может оказывать менее сильное воздействие на артериальное давление и частоту сердечного ритма. Более того, полагают, что клинические испытания продемонстрируют, что соединение вызывает меньше боли при инъекции, чем пропофол. Боль при инъекции пропофола коррелировала с концентрацией пропофола в его липидном эмульсионном носителе. Было обнаружено, что при включении в состав в идентичной липидной эмульсии концентрация водной фазы (R)-(-)-2-втop-бутил-6-изопропилфенола значительно уменьшается (до более чем 70%) по сравнению с пропофолом.
Также неожиданно было обнаружено, что другой энантиомер 2-втор-бутил-6-изопропилфенола, (S)-(+)-2-втор-бутил-6-изопропилфенол, демонстрирует улучшенный гемодинамический профиль наряду со сходной или улучшенной фармакологической активностью по сравнению с пропофолом.
Соответственно, соединения согласно изобретению являются, в частности, пригодными для индуцирования, или поддержания общей анестезии, или промотирования обезболивания у пациента. Они особенно являются пригодными для анестезирования пациентов, имеющих повышенную чувствительность к гемодинамическим эффектам. Такие пациенты включают пациентов, страдающих от сердечно-сосудистой болезни, такой как болезнь коронарных артерий, кардиомиопатия, ишемическая болезнь сердца, порок клапана сердца и врожденный порок сердца; пациентов, страдающих от хронической гипертонии, цереброваскулярной болезни или травмы головного мозга; пациентов пожилого возраста (например, выше 50-, 60-, 70- или 80-летнего возраста); пациентов с острой потерей крови, обезвоживанием или тяжелой инфекцией, включая пациентов с геморрагическим шоком, гиповолемическим шоком или септическим шоком; и пациентов, получающих спинальную анестезию, эпидуральную анестезию или вазоактивные медикаменты; см., например, Reich DL et al., 2005, Anesth Analg 101, 622. Например, пациентом может быть человек, физическое состояние которого по классификации Американского общества анестезиологов (ASA) составляет, по меньшей мере, 3. Настоящее изобретение также рассматривает введение соединения согласно изобретению пациентам, которые не могут подвергаться предварительному обезболиванию при инъекции.
При использовании здесь термин "фармацевтически приемлемый носитель" включает растворители, адъюванты, эксципиенты или наполнители.
Термин "животное" включает млекопитающих, таких как, например, люди, домашние животные, зоологические животные и крупный рогатый скот.
Термин "лечение" болезни или расстройства включает: 1) улучшение болезни или расстройства (т.е. остановку или уменьшение развития болезни или расстройства или, по меньшей мере, одного из его клинических симптомов), 2) улучшение, по меньшей мере, одного физического параметра, который может быть незаметным для пациента, 3) ингибирование болезни или расстройства, которое может быть выражено или физически (например, стабилизация заметного симптома), или физиологически (например, стабилизация физического параметра), или и тем, и другим, или 4) задержку начала болезни или расстройства.
Стереоизомерная чистота соединений и пролекарств, описанных здесь, может быть установлена с помощью обычных аналитических методов, хорошо известных специалистам в данной области техники. Например, для установления стереохимической чистоты отдельного стереоизомера можно использовать применение хиральных ЯМР шифт-реагентов, газохроматографический анализ на хиральных колонках, высокоэффективную жидкостную хроматографию с использованием хиральных колонок, поляриметрию, изотопное разбавление, калориметрию, ферментные методы, капиллярный электрофорез на хиральных гелях, образование диастереоизомерных производных посредством реакции с хиральными реактивами и стандартный способ анализа с помощью принятых аналитических методов. Альтернативно, для установления стереохимической чистоты описанного здесь соединения можно использовать синтез с использованием исходных материалов известного стереохимического обогащения. В данной области известны другие аналитические способы для демонстрации стереохимической однородности.
Настоящее изобретение предоставляет стереоизомер формулы (I), или его соль, или его пролекарство в нерацемической (т.е. энантиомерно обогащенной) форме в центре, отмеченном "*" в формуле (I). Таким образом, изобретение включает стереоизомер формулы (I) в обогащенной смеси, которая содержит не больше, чем 45%, другого энантиомера того соединения формулы (I), которое показано, или его соли, или пролекарства. (-)-Энантиомер, выделенный в примере 2 ниже, является специфическим соединением изобретения. В некоторых вариантах изобретения обогащенная смесь содержит не больше, чем около 40%, 35%, 30%, 25%, 20%, 15%, 10%, 5%, 4%, 3%, 2% или 1% другого энантиомера соединения формулы (I), или его соли, или его пролекарства. В другом варианте осуществления изобретения обогащенная смесь содержит меньше, чем около 1%, другого энантиомера соединения формулы (I), или его соли, или его пролекарства.
Способы получения соединения формулы (I)
Как правило, соединения формулы (I) можно получить с помощью, по меньшей мере, трех разных подходов. В одном подходе рацемическую смесь получают, используя обычные способы органического синтеза, или приобретают из коммерческих источников, а смесь разделяют с помощью методов, известных специалистам в данной области техники, таких как, например, фракционная кристаллизация, разделение на хиральных колонках, образование и разделение производных или их кинетическое оптическое расщепление и т.д., для того чтобы обеспечить по существу чистый энантиомер формулы (I) или энантиомерно обогащенные смеси соединений формулы (I). Альтернативно, для получения соединения формулы (I) можно использовать асимметричный синтез. Для получения по существу чистых энантиомеров формулы (I) или энантиомерно обогащенных смесей соединений формулы (I) можно использовать известные хиральные предшественники, применяя известные методы. Другие способы включают получение хиральных промежуточных продуктов с использованием, например, асимметричной гидрогенизации, восстановления и/или образования углерод-углеродной связи. Также для получения соединения формулы (I) можно использовать ферментативное расщепление прохиральных ацетатных предшественников и т.д.
Способы получения энантиомерно обогащенного соединения формулы (I) или его соли предоставлены как дополнительные варианты осуществления изобретения и проиллюстрированы нижеперечисленными методиками.
Соединение формулы (I) можно получить из рацемического соединения (I) с помощью хирального «помощника» (chiral auxiliary), кристаллографического и/или хроматографического разделения с последующим гидролизом. В одном способе стереоизомер формулы (I) можно получить, используя хиральный изоцианат для образования смеси карбаматных диастереомеров, которую можно разделить с получением искомого диастереомера формулы (I) после гидролиза остатка карбамата. Конкретно, но не ограничиваясь этим, можно использовать хиральный карбамат, полученный из R-(+)1-фенилэтилизоцианата. В другом способе соединение формулы (I) может быть получено посредством диазотирования хирального анилина. В еще одном способе соединение формулы (I) может быть получено восстановлением хирального алкена.
Следовательно, согласно другому аспекту настоящее изобретение предоставляет способ получения (-)стереоизомера формулы (I), или его соли, или его пролекарства, который включает:
(a) проведение гидролиза диастереоизомера карбаминовой кислоты (-)-2-втор-бутил-6-изопропилфенилового эфира формулы
в которой R1 представляет хиральную аминогруппу;
(b) диазотирование соответствующего (-)-2-втор-бутил-6-изопропил анилина формулы
или
(c) восстановление соответствующего 2-(1-метилаллил)-6-изопропилфенола формулы
с последующим, если необходимо, образованием свободного фенола, или его соли (такой, как фармацевтически приемлемая соль), или его пролекарства.
Гидролиз согласно этапу процесса (a) может быть проведен посредством реакции карбамата с основанием, например гидроксидом щелочного металла, таким как гидрокисид калия или натрия, которая дает соль (-) стереоизомера формулы (I), такую как соль щелочного металла. Свободный фенол можно получить обработкой этой соли кислотой, такой как соляная кислота. Хиральная аминогруппа может быть, например, хиральной 1-арилэтиламиногруппой, например (R)-1-арилэтиламиногруппой, такой как (R)-1-фенилэтиламиногруппа.
Карбаматный исходный материал можно получить путем реагирования рацемической смеси соответствующего 2-втор-бутил-6-изопропилфенола с хиральным изоцианатом с получением смеси диастереоизомеров, содержащей диастереоизомер (-)-2-втор-бутил-6-изопропилфенилового эфира карбаминовой кислоты; и отделения соответствующего диастереоизомера (-)-2-втор-бутил-6-изопропилфенилового эфира карбаминовой кислоты формулы (II).
Хиральный изоцианат может быть, например, хиральным 1-арилэтилизоцианатом, например (R)-1-арилэтилизоцианатом, таким как (R)-(+)-1-фенилэтилизоцианат. Получающийся в результате продукт является смесью соответствующих диастереоизомеров 2-втор-бутил-6-изопропилфенилового эфира 1-арилэтилкарбаминовой кислоты. Искомый диастереоизомер можно отделить с помощью хроматографии с использованием, например, кремния в качестве стационарной фазы или посредством кристаллизации.
Неожиданно было обнаружено, что использование (R)-(+)-1-фенилэтилизоцианата в вышеописанном способе обеспечивает хорошее разделение стереоизомеров (-)-2-втор-бутил-6-изопропилфенола.
Рацемический 2-втор-бутил-6-изопропилфенол можно получить из 2-изопропилфенола, следуя способу, описанному в примере 1.
Этап диазотирования процесса (b) легко осуществляется посредством реагирования анилина с нитритом щелочного металла, таким как нитрит натрия, в присутствии медного катализатора, такого как Cu2O, с солью меди (II), такой как сульфат меди.
Хиральный анилин формулы (III) можно получить, следуя способу, описанному здесь в примере 3.
Этап восстановления процесса (с) легко осуществляется посредством гидрогенизации в присутствии металлического катализатора группы (VIII), такого как палладий на углероде.
Соединения формулы (IV) можно получить из рацемического фенола, получение которого описано здесь в примере 1.
Соли
В случаях, когда соединения являются достаточно кислыми, соль соединения формулы (I) может быть использована как промежуточное соединение для отделения и очистки соединения формулы (I) или его обогащенной смеси. Кроме того, подходящим может быть введение соединения формулы (I) в виде фармацевтически приемлемой соли. Примеры фармацевтически приемлемых солей включают соли, которые получены с помощью обычных методик, хорошо известных в данной области техники, например, посредством реагирования достаточно кислого соединения формулы (I) с подходящим основанием, дающим физиологически приемлемый катион. Например, можно получить соли щелочного металла (например, натрия, калия или лития) или щелочноземельного металла (например, кальция).
Фармацевтические композиции
Фармацевтические композиции, раскрытые здесь, содержат соединение формулы (I), раскрытое здесь, с подходящим количеством фармацевтически приемлемого носителя, для того, чтобы обеспечить форму для надлежащего введения пациенту. Соединения формулы (I) могут быть включены в состав фармацевтических композиций и введены пациенту в целом ряде форм, приспособленных для выбранного способа введения, т.е. орально, парентерально, внутривенно, внутримышечно, местно или подкожно.
Таким образом, соединения формулы (I) могут быть введены системно в комбинации с фармацевтически пригодными носителями, такими как инертные растворители или съедобные носители. Такие композиции и препараты могут содержать, по меньшей мере, 0,1% активного соединения. Несомненно, процентное содержание композиций и препаратов может изменяться и может условно находиться в интервале между от около 0,1% до около 60% от массы данной стандартной лекарственной формы. Количество активного соединения в таких терапевтически пригодных композициях является таким, чтобы получался эффективный уровень дозировки.
Соединения формулы (I), описанные здесь, обычно включают в состав фармацевтических композиций, пригодных для внутривенного введения. Соединения формулы (I) могут быть относительно нерастворимыми в воде. Таким образом, для внутривенного введения соединения формулы (I) обычно включают в состав в водных средах, используя один или больше растворителей, несмешивающихся с водой, и один или больше эмульгаторов или поверхностно-активных веществ. Отдельные композиции могут включать один или больше дополнительных компонентов, таких как стабилизирующие вещества, модификаторы тоничности, основания или кислоты для регулирования pH и солюбилизаторы. Композиции также могут необязательно содержать консерванты, такие как, например, этилендиаминтетрауксусная кислота (ЭДТА) или метабисульфит натрия. Пригодные эмульсии масло-в-воде, содержащие консервант, такой как ЭДТА, который можно использовать вместе с соединениями, описанными здесь, охарактеризованы в Патентах США №5,908,869, 5,714,520, 5,731,356 и 5,731,355.
В описанных здесь фармацевтических композициях можно использовать широкий диапазон несмешивающихся с водой растворителей. Несмешивающийся с водой растворитель может быть растительным маслом, таким как, например, соевое, сафлоровое, хлопковое, кукурузное, подсолнечное, арахисовое, касторовое или оливковое масло. Альтернативно, несмешивающийся с водой растворитель может быть сложным эфиром средне- или длинноцепочечной жирной кислоты, такой как, например, моно-, ди- или триглицерид, сложным эфиром комбинации средне- и длинноцепочечной жирной кислоты или химически модифицированным или синтетическим веществом, таким как этилолеат, изопропилмиристат, изопропилпальмират, сложный эфир глицерина, полиоксил или гидрогенизированное касторовое масло. Несмешивающийся с водой растворитель также может быть маслом морской рыбы, таким как, например, печень трески или другое масло из рыбы. Другие подходящие растворители включают фракционированные масла, такие как, например, фракционированное кокосовое масло или модифицированное масло соевых бобов. Несмешивающийся с водой растворитель может включать "структурированные липиды" (см., например, Lipid Biotechnology, Т.М.Kuo and H.W.Gardner (eds.), Marcel Dekker, Inc. New York, NY). Многие структурированные липиды доступны от частных поставщиков, таких как Danisco A/S, Copenhagen Denmark и S & J Lipids, Ostrander, Огайо.
Фармацевтические составы, описанные здесь, также могут содержать эмульгатор. Подходящие эмульгаторы включают синтетические неионные эмульгаторы, такие как, например, этоксилированные эфиры, полиоксипропилен-полиоксиэтилен блок-сополимеры и фосфолипиды. Также можно использовать природные фосфолипиды, такие как фосфолипиды яиц или сои, и модифицированные или искусственно созданные фосфолипиды или их смеси. В некоторых вариантах осуществления эмульгаторы являются фосфолипидами яиц и фосфолипидами сои. Фосфолипиды яичного желтка включают фосфатидилхолин, лецитин и фосфатидилэтаноламин.
Фармацевтические составы, описанные здесь, могут включать липидную эмульсию, содержащую от около 0,1% до около 5% (масс./масс.) соединения формулы (I), от около 5 до около 25% (масс./масс.) несмешивающегося с водой растворителя и от около 40% до около 90% (масс./масс.) воды. Предпочтительный состав содержит от около 0,5% до около 2% (масс./масс.) соединения формулы (I). В одном варианте осуществления фармацевтический состав содержит от около 0,5% до около 5% (масс./масс.) соединения формулы (I) и от около 0% до около 50% (масс./масс.) несмешивающегося с водой растворителя.
Фармацевтические составы, описанные здесь, также могут включать стабилизирующие вещества. Анионные стабилизаторы включают, например, фосфатидилэтаноламины, конъюгированные с полиэтиленгликолем (PEG-РЕ), и фосфатидилглицерины, отдельным примером которых является димиристоил фосфатидилглицерин (DMPG). Дополнительные стабилизаторы включают, но не ограничиваются этим, олеиновую кислоту и ее натриевую соль, холевую кислоту и дезоксихолевую кислоту и их соответствующие соли, катионные липиды, такие как стеариламин и олеиламин, и 3|3-[N-(N',N'-даметиламиноэтан)карбамоил]холестерин (DC-Chol).
Фармацевтические композиции, описанные здесь, можно сделать изотоническими с кровью включением подходящего модификатора тоничности. Наиболее часто в качестве модификатора тоничности используется глицерин. Альтернативные модифицирующие тоничность агенты включают ксилитол, маннитол и сорбитол. Фармацевтические композиции обычно составляют так, чтобы они имели физиологически нейтральное значение pH, обычно в пределах 6,0-8,5. Значение pH можно отрегулировать добавлением основания, например NaOH или NaHCO3, или в некоторых случаях кислоты, такой как HCl.
Соединения формулы (I) могут быть заключены в состав с фармацевтически безопасными эмульсиями типа масло-вода, содержащими растительное масло, фосфатидный эмульгатор, обычно лецитин яиц или лецитин соевых бобов, и модификатор тоничности, такой как, например, Liposyn® II и Liposyn® III (Abbott Laboratories, Норт-Чикаго, Иллинойс) и Intralipid® (Fresenius Kabi АВ, Упсала, Швеция) или другими подобными эмульсиями типа масло-вода.
Соединения формулы (I) также могут быть включены в состав с триглицеридом, содержащим сложные эфиры, по меньшей мере, одной жирной кислоты со средней длиной цепи (C6-C12). В некоторых вариантах осуществления триглицериды являются сложными эфирами C8-С10 жирной кислоты. Триглицериды, подходящие для включения в состав соединений формулы (I), включают, но не ограничиваются этим, Miglyol® (Condea Chemie GmbH (Witten, Германия). Например, Miglyol® 810 или 812 (каприловый(C10)/каприновый (C8) глицерид) является пригодным для состава соединений формулы (I).
Кроме того, соединения формулы (I), описанные здесь, могут быть включены в состав аналогично фармацевтическим композициям пропофола, описанным, например, в Патентах Соединенных Штатов Америки №4,056,635, 4,452,817 и 4,798,846.
Другие подходящие составы для применения в настоящем изобретении можно найти, например, в Remington's Pharmaceutical Sciences, Philadelphia, Pa., 19th ed. (1995).
Терапевтическое/профилактическое введение и дозы.
Соединение формулы (I) и/или его фармацевтические композиции можно вводить отдельно или в комбинации с другими фармацевтическими средствами, включая соединения, раскрытые здесь, и/или их фармацевтические композиции. Соединения, раскрытые здесь, можно вводить или применять сами по себе или как фармацевтические композиции. Определенная фармацевтическая композиция зависит от желательного способа введения, как хорошо известно специалисту в данной области техники.
Соединения, раскрытые здесь, и/или их фармацевтические композиции могут быть введены субъекту посредством внутривенной болюсной инъекции, непрерывного внутривенного вливания, в виде таблетки для перорального приема, капсулы для перорального приема, раствора для перорального приема, внутримышечной инъекции, подкожной инъекции, посредством трансдермального всасывания, буккального (щечного) всасывания, внутриносового всасывания, ингаляции, подъязычно, интрацеребрально, интравагинально, ректально, местно, в частности в уши, нос, глаза или на кожу, или любым другим удобным способом, известным специалистам в данной области техники. В некоторых вариантах осуществления соединения, раскрытые здесь, и/или их фармацевтические композиции доставляются посредством лекарственных форм с замедленным высвобождением, включая лекарственные формы с замедленным высвобождением для приема внутрь. Введение может быть системным или местным. Известны разные системы доставки (например, инкапсулирование в липосомы, микрочастицы, микрокапсулы, капсулы, системы доставки лекарственного средства "аналгезия, управляемая пациентом", и т.д.), которые можно использовать для доставки соединений, раскрытых здесь, и/или их фармацевтических композиций.
Количество соединений, раскрытых здесь, и/или их фармацевтических композиций, которое будет эффективно, может быть определено с помощью стандартных клинических методик, известных в данной области техники. Введенное количество соединений, раскрытых здесь, и/или их фармацевтических композиций будет, конечно, зависеть, в числе других факторов, от субъекта, которого лечат, веса субъекта, возраста субъекта, состояния субъекта, ожидаемого действия соединения, способа введения и мнения лечащего врача. Например, уровень дозировки (R)-(-) или (-) стереоизомера формулы I для получения общей анестезии может находиться в пределах от около 1 до около 10 мг/кг. Предпочтительные дозы для индуцирования анестезии находятся в пределах от около 1 до около 3 мг/кг. Предпочтительные поддерживающие дозы находятся в пределах от около 1 до около 20 мг/кг/час. Предпочтительные дозы для получения седативного эффекта находятся в пределах от около 0,3 до около 8 мг/кг/час.
Комбинированная терапия
В определенных вариантах осуществления соединения, раскрытые здесь, и/или их фармацевтические композиции можно использовать в комбинированной терапии, по меньшей мере, с одним терапевтическим средством. Соединения, раскрытые здесь, и/или их фармацевтические композиции и терапевтическое средство могут действовать аддитивно или, более предпочтительно, синергично. В некоторых вариантах осуществления соединения, раскрытые здесь, и/или их фармацевтические композиции вводят одновременно с введением другого терапевтического средства, такого как, например, другие седативные снотворные средства (например, этомидат, тиопентал, мидазолам, дексмедетомидин, кетамин), анестетики (например, десфлюран, севофлюран, изофлюран, закись азота), анальгетики (например, опиоид, такой как ремифентанил, морфий, меперидин, гидроморфон, метадон, фентанил, сулфентанил или алфентанил, или неопиоидный анальгетик, такой как кеторолак, гапапентин, лидокаин или кетамин), паралитические средства, такие как рокурониум, цис-атракуриум, векурониум или панкурониум бромид, противорвотные средства (например, ондансетрон, доласетрон, дроперидол), сердечно-сосудистые средства (например, метопролол, пропранолол, эсмолол, клонидин, фенилэфрин, эфедрин, эпинефрин, норэпинефрин, допамин, дилтиазем, атропин, гликопирролат, лизиноприл, нитроглицерин, натрия нитропруссид, дигоксин, милринон), стероиды (например, дексаметазон, гидрокортозон, метилпреднизолон), антисептики (например, цефазолин, ванкомицин), мочегонные средства (например, фуросемид, гидрохлортиазид, спиронолактон), изменяющие настроение средства (например, флуоксетин, арипипразол) или возбуждающие средства, такие как никотин или цитизин.
Например, соединения, раскрытые здесь, и/или их фармацевтические композиции можно вводить вместе с другими терапевтическими средствами. В других вариантах осуществления соединения, раскрытые здесь, и/или их фармацевтические композиции вводят до или после введения других терапевтических средств.
Пролекарства
Термин "пролекарство" при использовании здесь относится к соединению, которое может метаболизироваться или превращаться in vivo для предоставления соединения формулы (I). Обычно, пролекарства включают соединения, которые получаются при модификации фенольной группы в соединении формулы (I) с получением соответствующего соединения, которое может быть метаболизировано или превращено in vivo для того, чтобы предоставить соответствующее соединение формулы (I). О пролекарствах из фенольных соединений, а также способах их получения уже сообщалось. Например, смотри Публикации Патентных Заявок США №20070015716, 20060287525, 20060205969, 20060041011, 20050239725 и 20050107385.
Другие пригодные группы пролекарств обсуждаются в следующих Публикациях Международных Патентных Заявок и Публикациях Патентных Заявок США: WO 2005023204; US 2005107385; US 2005004381; WO 2004092187; WO 2004032971; US 2006100163; WO 2006033911; WO 2004033424; US 2005267169; WO 2003086413; US 2002370213; WO 2003057153; US 2001342755; US 2002099013; WO 2002034237; US 2004127397; WO 2002013810; WO 2000048572; US 2006166903; WO 200008033; US 2001025035; WO 9958555 и US 199875356; и в других последующих публикациях: Krasowski, M.D. Current Opinion in Investigational Drags (Thompson Scientific) (2005) 6(1), 90-98; Fechner, J. et al., Anesthesiology, 2004, 101, 3, 626-639; Altomare C. et al, European Journal of Pharmaceutical Sciences; 2003, 20, 1, 17-26; Sagara, Y. et al., Journal of Neurochemistry; 1999; 73, 6, 2524-2530 и Trapani, G., et al., International Journal of Pharmaceuticals, 1998,175, 2, 195-204.
Как описано выше, было обнаружено, что другой энантиомер 2-втор-бутил-6-изопропилфенола, (S)-(+)-2-втор-бутил-6-изопропилфенол, демонстрирует улучшенный гемодинамический профиль наряду с подобной или улучшенной фармакологической активностью по сравнению с пропофолом. Соответственно, настоящее изобретение также обеспечивает этот изомер, его пара-фтор производное, и их фармацевтически приемлемые соли, и их пролекарства, и их фармацевтические композиции для применения в качестве анестетиков.
Каждый из (S)-(+) или (+) стереоизомеров формулы (I), их соли и их пролекарства могут быть получены, следуя общим способам, описанным для получения соответствующих (-) стереоизомеров. Например, (S)-(+) или (+) стереоизомер 2-втор-бутил-6-изопропилфенола можно получить при реагировании рацемической смеси соответствующих 2-втор-бутил-6-изопропилфенолов с хиральным изоцианатом с получением смеси карбаматных диастереомеров, которые можно разделить с получением искомого диастереомера формулы (I) после гидролиза карбаматного остатка. Для получения (S)-(+) или (+) стереоизомера можно предпочтительно использовать (S)-l-арилэтилизоцианат, такой как (S)-(+)-1-фенилэтилизоцианат. Соответственно, настоящее изобретение также предоставляет диастереоизомер (S)-2-втор-бутил-6-изопропилфенилового эфира карбаминовой кислоты формулы (II), в котором R1 представляет хиральную аминогруппу, такую как (S)-1-арилэтиламиногруппа. Все из этих стереоизомеров можно отделить от рацемического соединения с помощью хиральной фазовой хроматографии, например, как описано в примере 2.
(S)-(+) или (+) стереоизомеры формулы (I) могут существовать, быть включены в состав и введены пациентам, как описано и приведено в пример здесь для (R)-(-) или (-) стереоизомеров. Для (S)-(+) или (+) стереоизомеров уровень дозировки для получения общей анестезии может находиться в пределах от около 1 до около 12 мг/кг. Предпочтительные дозы для индуцирования анестезии находятся в пределах от около 1,2 до около 4 мг/кг. Предпочтительные поддерживающие дозы находятся в пределах от около 1,5 до около 30 мг/кг/час. Предпочтительные дозы для получения седативного эффекта находятся в пределах от около 0,5 до около 12 мг/кг/час.
Изобретение теперь будет проиллюстрировано следующими неограничивающими примерами.
Способность соединения изобретения оказывать седативное или снотворное действие может быть установлена с помощью стандартных фармакологических моделей, которые хорошо известны в данной области техники. Эффективность соединения изобретения как снотворного средства была показана с помощью исследования потери рефлекса выпрямления у крысы (как описано в тесте А, ниже). Потенциальную возможность соединения изобретения сравнили с эффективностью пропофола, используя этот способ исследования.
Тест А. Тест на потерю рефлекса выпрямления
Крыс самцов Sprague Dawley зажимали в штативе и делали инъекцию исследуемого соединения в хвостовую вену (исходя из мг исследуемого соединения/кг веса тела). После введения крыс помещали в положение «на спине с согнутыми лапами» на пластину с подогревом. Отмечали время начала потери рефлекса выпрямления (RR-способность крысы выпрямиться), а также продолжительность потери RR. Было найдено, что соединение формулы (I), полученное в примере 2, является более сильнодействующим, чем пропофол в тесте А. Крысы, которым было введено 7 мг/кг композиции 1% (R)-(-)-2-втор-бутил-6-изопропилфенола, показали продолжительность анестезии 14,9 минут по сравнению с 7,1 минутами у крыс, которым вводили ту же дозу композиции 1% пропофола.
Гемодинамический профиль соединения изобретения можно определить, используя стандартные фармакологические модели, которые хорошо известны в данной области техники. Гемодинамический и анестетический профили соединения изобретения оценивали одновременно, используя модель анестезии на свиньях (как описано в тесте В, ниже). В этом исследовании гемодинамический профиль соединения изобретения сравнивали с профилем пропофола в экви-анестетических дозах.
Тест B. Модель анестезии на свиньях
Индуцирование анестезии выполняли с помощью модификации методики, описанной Ко et al. (Ко et al., Lab Anim Sci 1993; 43: 476-80) для свиньи (телазол, ксилазин и кетамин давали в виде внутримышечной инъекции). Использовали минимальную эффективную дозу и трахеальную интубацию. Когда животное помещено в положение «лежа», кислород подают через маску в количестве 8 мл/мин, а внутривенное введение начинают в ушную вену в текущем физиологическом растворе в количестве 70 мл/час. Трахею свиньи инкубируют и механически вентилируют для сохранения артериального PCO2 на уровне приблизительно 35 мм рт.ст.
Электроды для ЭКГ размещают, используя конфигурацию отведения II, чтобы контролировать сердечную активность. Артериальный катетер помещают в правую бедренную артерию, чтобы контролировать кровяное давление. Легочный артериальный катетер помещают через правую яремную вену для измерения минутного сердечного выброса, давления в концевых легочных капиллярах и центрального венозного давления. Также размещают катетер в брюшной аорте через левую бедренную артерию для забора образцов крови.
Двухполярные отведения электроэнцефалографа размещают, используя электроды с низким сопротивлением поверхности, помещенные над лобной и затылочной областями полушарий головного мозга, приблизительно 50 мм в сторону и 20 мм от средней линии. Заземляющий электрод помещают на средней линии между лобной и затылочной областями. Альтернативно, можно использовать интегральный комплект датчиков-электродов (integrated electrode sensor array) (Aspect Medical), совместимый с электроэнцефалографом (Aspect Medical). Анестезию поддерживают с помощью изофлюрана, регулируя так, чтобы поддерживать среднее артериальное давление на уровне 100 мм рт.ст. в течение периода стабилизации, и при необходимости внутривенно вводят панкурониум для мышечной релаксации.
После того как завершено первоначальное использование приборов на животном (обычно требующее приблизительно 2-3 часа), дополнительные 1 час и 15 минут служат как период стабилизации и сбора базовых данных (и чтобы гарантировать почти полное исчезновение эффектов лекарственных препаратов, вызывающих анестезию). Ингаляция изофлураном может продолжаться на всем протяжении исследования или может быть прекращена, причем изофлурану дают возможность "вымываться (выводиться)" в течение 15 минут перед введением исследуемого соединения.
Вещество или пропофол вводят внутривенно с помощью 20-минутного вливания после периода стабилизации через периферический внутривенный (BB) катетер. Выполняют пилотное исследование по подбору дозы для установления приблизительной дозы вливания для каждого вещества. В этом пилотном исследовании многократные дозы (всего вплоть до 5 вливаний) могли быть введены каждой свинье с интервалом, по меньшей мере, 90 минут между дозами. Образцы крови (по 1 мл каждый) отбирают перед вливанием дозы (пре-доза) и через 2, 4, 6, 8, 10, 12, 15, 20, 22, 22, 25, 35, 50, 65 и 80 минут после начала первого вливания для фармакокинетических исследований; ЭЭГ регистрируют постоянно как первичную фармакодинамическую конечную точку.
Образцы артериальной крови (1 мл каждый) отбирают из брюшной аорты через 2, 4, 6, 8, 10, 11, 12, 13, 14, 15, 17.5, 20, 25, 30, 45, 60, 90, 120 и 180 минут после начала вливания. Также отбирают контрольный образец перед началом вливания.
Сигнал ЭЭГ направляется на BIS анализатор (Aspect Medical), который обеспечивает непрерывный выход обработанных данных ЭЭГ. Результат заключается в числе "BIS", вычисленном по специальному алгоритму, которое находится в пределах между 100 (полное сознание) и 0 (изоэлектрическое) и показывает активность мозга.
Гемодинамические данные регистрируют и наносят на график, чтобы оценить тренды (тенденции) в течение периода обработки лекарственным средством. Данные для каждого вещества сравнивают с действием пропофола на BIS, сердечный ритм (HR), среднее артериальное давление крови (MAP) и минутный сердечный выброс.
Гемодинамические данные для (R)-(-)-2-втор-бутил-6-изопропилфенола (исследуемое соединение), полученного, как описано в примере 2, и для пропофола показаны на фигурах 1 и 2, соответственно. Данные показывают, что это соединение изобретения демонстрирует улучшенный гемодинамический профиль (в частности, в отношении гипотонии) по сравнению с пропофолом в экви-анестетических дозах.
ПРИМЕРЫ
Пример 1. Синтез рацемического 2-втор-бутил-6-изопропилфенола (соединение c).
Синтез аллилового эфира (a): К раствору сухого CH2Cl2 (40 л) в реактор (емкость ~200 л) добавили 2-изопропилфенол (2,5 кг; 18,38 моль). Смесь охлаждали с 0°C до -10°C. Кротоновый спирт (1,9 л; 22 моль) добавили к реакционной смеси, а затем добавили трифенилфосфин (6 кг; 22 моль) по порциям в течение 5 часов. К этому добавили DIAD (4,5 л; 22,1 моль) по каплям в течение 4 часов. Смесь доводили до комнатной температуры и перемешивали в течение ночи. После исчезновения исходного материала, судя по ТСХ, смесь разбавляли дихлорметаном (25 л) и промывали водой (50 л×2) и рассолом (50 л). Органический слой высушивали над безводным Na2SO4 (5 кг), фильтровали и концентрировали до сухости. Затем добавляли петролейный эфир (50 л) и смесь перемешивали при комнатной температуре в течение 1 часа. Осажденное белое твердое вещество (трифенилфосфин оксид) отфильтровывали и промывали петролейным эфиром (10 л×2). Объединенный фильтрат (~80 л) концентрировали до получения желтой вязкой жидкости (~5 кг). Этот сырой материал очищали с помощью колоночной хроматографии на силикагеле (ячейка 60-120; ~30 кг) с использованием 5% этилацетата в петролейном эфире в качестве растворителя для элюирования. Чистые фракции объединяли, а растворители концентрировали с получением 1,5 кг (43%) чистого материала.
Синтез гомостирилфенола (b): Аллиловый эфир (250 г; 1,28 моль) нагревали при 270°C в атмосфере азота в течение примерно 25 часов. Затем реакционную смесь разбавили этилацетатом (2 л) и промыли водой (3 л) и рассолом (1 л). Высушили над безводным Na2SO4 (100 г), профильтровали и выпарили до сухости с получением 240 г продукта.
Синтез 2-втор-бутил-6-изопропи л фенола (c): К раствору соединения b (500 г; 2,57 моль) в обезвоженном MeOH (5 л) при 0°C добавили Pd\C (50 г; 10 моль %). Затем смесь гидрировали в автоклаве под давлением водорода 5 кг в течение ночи. Затем реакционную смесь фильтровали через целит® и выпаривали с получением 400 г сырого продукта, который очищали с помощью колоночной хроматографии на силикагеле с использованием 2% этилацетата в петролейном эфире в качестве растворителя для элюирования. Очищенные фракции объединяли и концентрировали с получением 273 г продукта.
Пример 2. Кристаллографическое разделение рацемического 2-втор-бутил-6-изопропилфенола через образование хирального карбамата с предоставлением стереоизомера формулы (I).
где: (R)-(1-isocyanatoethyl)benzene - (R)-1(изоцианатоэтил)бензол;
racemic 2-sec-butyl-6-isopropylphenol - рацемический 2-втор-бутил-6-изопропилфенол;
(S)-(1-isocyanatoethyl)benzene - (S)-(1-изоцианатоэтил)бензол;
fractional recristallization - фракционная рекристаллизация;
NaOH/dioxane - диоксан;
stereoisomer of Formula (I), (-) 2-sec-butyl-6-isopropylphenol - стереоизомер формулы (I), (-)2-втор-бутил-6-изопропилфенол.
Синтез R-(+)-(1-фенил-этил)карбамата рацемического 2-втор-бутил-6-изопропилфенола (1a): Смесь рацемического 2-втор-бутил-6-изопропилфенола (1,92 г; 10 ммоль), R-(+)-1-фенилэтилизоцианата (1,47 г; 10 ммоль) и 4-(диметиламино)пиридина (0,06 г; 0,5 ммоль) нагревали при 80°C в обезвоженном пиридине (10 мл) в течение ночи. Реакционную смесь концентрировали на роторном испарителе. Затем получающийся осадок разделили между этилацетатом (75 мл) и 1 М HCl aq. (100 мл) в делительной воронке. Органический слой промывали 1 М HCl aq. (2×100 мл), рассолом (100 мл), затем высушивали над безводным MgSO4. Фильтрация и последующее выпаривание растворителя давало карбамат (1) (3,1 г; 90%) в виде твердого вещества.
(-)-2-втор-бутил-6-изопропилфенол (3): R-(+)-(1-фенил)этилкарбамат 2-втор-бутил-6-изопропилфенола (1) (100 г; 294 ммоль) растворяли в ~2,5 л горячих гексанов. Раствор держали при комнатной температуре в течение 24-48 часов, чтобы сделать возможной полную кристаллизацию. Получающиеся кристаллы профильтровали и промыли холодными гексанами (~200 мл). Эту процедуру повторили 7 раз (с происходящим одновременно уменьшением объемов гексанов). Кристаллы высушивали под вакуумом с получением кристаллического диастереоизомерно обогащенного R-(+)-(1-фенил-этил)-карбамата 2-втор-бутил-6-изопропилфенола (17 г; 34%). Получающуюся карбаматную смесь гидролизовали при 100°C в 1:1 смеси диоксан:1 М NaOH aq. в течение 1-2 мин. Затем реакционную смесь разбавляли эфиром, нейтрализовали с разбавленной HCl aq. и промывали рассолом. Затем эфирный слой сушивали над безводным MgSO4, фильтровали и выпаривали с выходом (-)-2-втор-бутил-6-изопропилфенола (9,6 г; ~100%). Выполняли вакуумную перегонку (~1-2 мм). Фракции (105-110°C) собирали с получением (3), (-)-2-втор-бутил-6-изопропилфенола (7,5 г; 78%, отношение энантиомеров 19:1, как определено с помощью хиральной ВЭЖХ). Оптическое вращение: α20 D=-7,16°. 1H ЯМР (250 МГц, хлороформ-dl) δ 0.84-0.90 (t. 3H), δ 1.21-1.26 (m. 11H), δ 2.85-2.89 (m. 1H), δ 3.11-3.16 (m. 1H), δ 4.74 (s, 1H), δ 6.87-6.90 (t, 1H) δ 6.987-7.05 (m 2H).
Анализ оптической чистоты с помощью хиральной хроматографии: Анализы R (+)-(1-фенил)этилкарбамата 2-втор-бутил-6-изопропилфенола (1) выполняли на колонке CHIRALCEL OD-H (4,6×250 мм) в изократическом режиме, мобильная фаза - н-гексаны, содержащие 1% изопропанол, скорость потока 1 мл/мин, 20 мин, обнаружение 270 нм. Образцы растворяли в гексанах.
Синтез S-(-)-1-фенил-этил-карбамата рацемического 2-втор-бутил-6-изопропилфенола (lb): Смесь рацемического 2-втор-бутил-6-изопропилфенола (1,92 г; 10 ммоль), S-(-)-1-фенилэтилизоцианата (1,47 г, 10 ммоль) и 4-(диметиламино)пиридина (0,06 г; 0,5 ммоль) нагревали при 80°C в обезвоженном пиридине (10 мл) в течение ночи. Реакционную смесь концентрировали на роторном испарителе. Полученный осадок затем разделили между этилацетатом (75 мл) и 1 М HCl aq. (100 мл) в делительной колонке. Органический слой промыли 1 М HCl aq. (2×100 мл), рассолом (100 мл), затем высушили над безводным MgSO4. Фильтрование и последующее выпаривание растворителя давало карбамат (1b) в виде твердого вещества.
(+)-2-втор-бутил-6-изопропилфенол (3): S-(-)-(1-фенил)этилкарбамат 2-втор-бутил-6-изопропилфенола (1b) (100 г; 294 ммоль) растворяли в ~2,5 л горячих гексанов. Раствор держали при комнатной температуре в течение 24-48 часов, чтобы сделать возможной полную кристаллизацию. Получающиеся кристаллы отфильтровывали и промывали холодными гексанами (~200 мл). Эту процедуру повторяли 7 раз (с происходящим одновременно уменьшением объемов гексанов). Кристаллы высушивали под вакуумом с получением кристаллического диастереомерно обогащенного S-(-)-1-фенил-этилкарбамата 2-втор-бутил-6-изопропилфенола. Получающуюся карбаматную смесь гидролизовали при 100°C в смеси 1:1 диоксан:1М NaOH aq. в течение 1-2 мин. Затем реакционную смесь разбавляли эфиром, нейтрализовали разбавленной HCl aq. и промывали рассолом. Затем эфирный слой высушивали над безводным MgSO4, фильтровали и выпаривали с получением энантиомерно обогащенного 2-втор-бутил-6-изопропилфенола. Выполняли вакуумную перегонку (~1-2 мм). Фракции (105-110°C) собирали с получением (3), энантиомерно обогащенного 2-втор-бутил-6-изопропилфенола (отношение энантиомеров 19:1, как определено с помощью хиральной ВЭЖХ). Оптическое вращение: α20 D:=+5,95°. 1Н ЯМР (250 МГц, хлороформ-dl) δ 0.84-0.90 (t. 3H), δ 1.21-1.26 (m. 11H), δ 2.85-2.89 (m. 1H), δ 3.11-3.16 (m. 1H), δ 4.74 (s, 1H), δ 6.87-6.90 (t, 1H) δ 6.987-7.05 (m 2H).
Пример 3. (-)-2-втор-бутил-6-изопропилфенол из (-)-2-втор-бутиланилина
racemic 2-sec-butylaniline - рацемический 2-втор-бутиланилин;
(S)-mandelic acid - (S)-миндальная кислота;
fractional recristallization - фракционная рекристаллизация;
1. enatiomerically enriched 2-sec-butylaniline - энантиомерно-обогащенный 2-втор-бутиланилин;
Suzuki/reduction - реакция Судзуки/восстановление;
4. stereoisomer of Formula (I), (-) 2-sec-butyl-6-isopropylphenol - стереоизомер формулы (I), (-)2-втор-бутил-6-изопропилфенол.
Кристаллографический анализ (-)-2-втор-бутиланилина (1): 2-втор-бутиланилин (1,49 г; 10 ммоль) и (S)-(+)-миндальную кислоту (1,52 г; 10 ммоль) растворили в 20 мл эфира при умеренном нагревании. Раствор охлаждали до 4°C и держали при 4°C в течение 2 час. Кристаллический материал отфильтровывали, промывали водой и высушивали (1,5 г; 50%). Соль перекристаллизовывали из этилацетат-гексана (1 г; 33%, 19:1 отношение изомеров). Оптическую чистоту 2-втор-бутиланилина определяли с помощью хиральной хроматографии. (-)-2-втор-бутиланилин (1) извлекали обработкой эфирного раствора соли 1 М NaOH (0,4 г; 26,5%).
Анализ оптической чистоты с помощью хиральной хроматографии: Анализы 2-втор-бутиланилинов были выполнены на колонке CHIRALCEL OD-H (4,6×250 мм) в изократическом режиме, мобильная фаза - n-гексаны, содержащие 1% изопропанола, скорость потока 1 мл/мин, 20 мин, обнаружение 270 нм. Образцы растворяли в гексанах. Соли миндальной кислоты предварительно обрабатывали смесью гексанов и 3 М NaOH aq. Слой гексанов загружали прямо в колонку.
Синтез (-)-2-втор-бутил-6-бромоанилина (2): (-)-2-втор-бутиланилин (1) (6,7 г; 45 ммоль) растворяли в 240 мл бензола, а затем добавляли N-бромосукцинимид (8 г; 45 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем растворитель удаляли при пониженном давлении. Искомый продукт очищали с помощью хроматографии на силикагеле (CombiFlash, колонка 120 г, гексан-DCM). Фракции 1 - 3,1 г (30%, чистый (-)-2-втор-бутил-4-бромоанилин), фракции 2 - 6,2 g (60% смесь (-)-2-втор-бутил-6-бромо- и (-)-2-втор-бутил-4,6-дибромоанилинов). Фракцию 2 отгоняли и (-)-2-втор-бутил-6- бромоанилин собирали 115-127°C, при 5 мм (4,9 г; 48%).
Синтез (-)-2-втор-бутил-6-изопропиланилина (3): (-)-2-втор-бутил-6-бромоанилин (2) (0,684 г; 3 ммоль), изопропенилбороновой кислоты пинаконовый эфир (1 г; 6 ммоль), тетракис(трифенилфосфин)палладий(0) (0,035 г; 0,03 ммоль), MeCN 10 мл и K2CO3 (5 мл; 1 М раствор) нагревали в микроволновой печи при 160°C в течение 400 сек. Реакционную смесь разбавляли водой (75 мл). Продукты извлекали этилацетатом (50 мл). Органический слой промывали 5% NaHCO3, рассолом и высушивали над безводным MgSO4. Растворитель удаляли при пониженном давлении и соединение очищали с помощью хроматографии на силикагеле (CombiFlash, 30 г колонка, гексан-этил ацетат). Затем проводили восстановление в МеОН (40 мл) при 5% Pd/C (~0,3 г), давление водорода 60 psi в течение ночи (0,48 г; 72%).
Синтез (-)-2-втор-бутил-6-изопропилфенола (4): (-)-2-втор-бутил-6-изопропиланилин (3) (1,92 г; 10 ммоль) растворили в 20 мл 15% H2SO4 при 60°C, и затем охладили до 0°C. Раствор NaNO2 (0,76 г; 11 ммоль) в 8 мл воды быстро добавили к реакционной смеси (~30 сек) при энергичном перемешивании, поддерживая температуру ниже 0°C. Раствор перемешивали в течение дополнительных 2 минут и затем добавили по частям к суспензии Cu2O (1,5 г) в водном CuSO4X5H2O (10 г в 220 мл) при энергичном перемешивании при 50°C. Реакционную смесь перемешивали в течение 30 мин и охлаждали до комнатной температуры. Реакцию повторяли пять раз в том же размере (всего было использовано 9,13 г анилина), а все реакционные смеси объединили. Органический материал дважды экстрагировали эфиром (400 мл). Растворитель выпаривали и соединение очищали с помощью хроматографии на силикагеле. Проводили CombiFlash хроматографию (Гексан/этилацетат) и конечный продукт дистиллировали (105-110°С/~3 мм) (4,1 г (45%). Оптическое вращение: α20 D:=-7,58° (с=5, пентан). 1H ЯМР (250 МГц, хлороформ-dl) δ 0.84-0.90 (t. 3H), δ 1.21-1.26 (m. 11H), δ 2.85-2.89 (m.1H), δ 3.11-3.16 (m. 1H), δ 4.74 (s, 1H), δ 6.87-6.90 (t, 1H) δ 6.987-7.05 (m 2H).
Пример 4. Состав
Следующая таблица иллюстрирует репрезентативную лекарственную форму, содержащую соединение формулы (I) для терапевтического применения.
| Ингредиент | Масса порции | Масс./масс.% |
| Соевое масло | 70 г | 11,71 |
| Фосфолипиды соевых бобов (Липид S-75) | 8,4 г | 1,41 |
| Соединение формулы (I) | 3,5 г | 0,59 |
| Глицерин | 15,75 г | 2,64 |
| Динатрия эдетат | 0,035 г | 0,01 |
| Гидроксид натрия (регулирование pH) | ||
| Промежуточный итог | 97,685 | |
| Стерильная вода для инъекции | 500 мл | 83,66 |
| Всего | 597,685 | 100 |
Пример 5. Состав
Следующая таблица иллюстрирует репрезентативную лекарственную форму, содержащую соединение формулы (I) для терапевтического применения.
| Ингредиент | Масса порции | Масс./масс. % |
| Соевое масло | 70 г | 11,66 |
| Фосфолипиды соевых бобов (Липид S-75) | 8,4 г | 1,40 |
| Соединение формулы (I) | 6,0 г | 1,00 |
| Глицерин | 15,75 г | 2,62 |
| Динатрия эдетат | 0,035 г | 0,01 |
| Гидроксид натрия (регулирование pH) | ||
| Промежуточный итог | 100,185 | |
| Стерильная вода для инъекции | 500 мл | 83,31 |
| Всего | 600,185 | 100 |
Пример 6. Состав
Следующая таблица иллюстрирует репрезентативную лекарственную форму, содержащую соединение формулы (I) для терапевтического применения.
| Ингредиент | Масса порции | Масс./масс.% |
| Соевое масло | 70 г | 11,72 |
| Фосфолипиды соевых бобов (Липид S-75) | 8,4 г | 1,41 |
| Соединение формулы (I) | 3,0 г | 0,50 |
| Глицерин | 15,75 г | 2,64 |
| Динатрия эдетат | 0,035 г | 0,01 |
| Гидроксид натрия (регулирование рН) | ||
| Промежуточный итог | 97,185 | |
| Стерильная вода для инъекции | 500 мл | 83,73 |
| Всего | 597,185 | 100 |
Биологические тесты
Фармакологический профиль (R)-(-)-2-втор-бутил-6-изопропилфенола был оценен по сравнению с пропофолом в тестах, описанных в следующих примерах. В этих примерах (R)-(-)-2-втор-бутил-6-изопропилфенол называется соединением 1.
Пример 7. Боль при инъекции - Концентрация водной фазы
Полагают, что боль при инъекции, общая проблема введения пропофола, вызывается пропофолом, присутствующим в водной фазе липидной эмульсии (см., например, Klement W et al., 1991, Br J Anaesth 67, 281). В некоторых исследованиях сообщалось о значительном снижении боли при инъекции, когда концентрацию водной фазы пропофола уменьшали по сравнению с количеством пропофола в водной фазе дипривана (см., например, Doenicke AW et al., 1996, Anesth Analg 82, 472; Ueki R et al., 2007, J Anesth 21,325).
Была определена концентрация соединения 1 в водной фазе (концентрация водной фазы) липидного эмульсионного состава. Эта концентрация водной фазы была сравнима с концентрацией водной фазы пропофола, включенного в состав такой же композиции, и с концентрацией водной фазы дипривана® (AstraZeneca, Wilmington, DE, USA).
Была составлена однопроцентная (1%) композиция соединения 1 в соответствии с примером 5, соединение 1 получили, как описано в примере 2. Композиция 1% пропофола была составлена таким же образом. Использовали диприван (эмульсия для инъекции 1% пропофола) от компании AstraZeneca.
Концентрации водных фаз соединения 1 и пропофола определяли с помощью метода ультрафильтрации, описанного в Teagarden DL at al., 1988, Pharmaceutical Research 5, 482. Коротко, четыре образца композиции (0,4 мл) с 1% соединения 1, четыре образца композиции (0,4 мл) с 1% пропофола и два образца (0,4 мл) дипривана поместили на микроцентрифужные фильтры Ultrafree®-MC (Millipore, Billerica, MA) и отделили водные фазы от жидких фаз с помощью микроцентрифугирования в течение 15 мин при 5000 об/мин. Концентрации соединения 1 и пропофола в соответствующих водных фазах количественно определили с помощью метода жидкостной хроматографии/тандемной масс-спектрометрии (LC/MS/MS) по отношению к стандартным кривым соединения 1 и пропофола с использованием тимола в качестве внутреннего стандарта (анализы были выполнены Alturas Analytics, Inc., Москва, ID).
Концентрация водной фазы соединения 1 в композиции с 1% соединения 1 составляла 1,78±0,17 мкг/мл. Концентрация водной фазы пропофола в композиции с 1% пропофола составляла 6,28±0,41 мкг/мл. Концентрация водной фазы пропофола в диприване составляла 4,1 мкг/мл.
Эти результаты показали уменьшение на 72% в концентрации водной фазы соединения 1 по сравнению с концентрацией водной фазы пропофола в идентичных композициях и уменьшение на 57% в концентрации водной фазы соединения 1 по сравнению с концентрацией водной фазы пропофола в диприване.
Пример 8. Фармакокинетические исследования
Фармакокинетические (РК) исследования проводили на домашних свиньях, чтобы оценить фармакодинамические эффекты соединения 1 и сравнить их с фармакодинамическими эффектами пропофола.
Композицию с 0,5% соединения 1, полученную, как описано в примере 2, и составленную в соответствии с примером 6, вводили 6 свиньям с помощью 20-мин внутривенного (BB) вливания при скорости 0,6 мг/кг/мин (общая доза 12 мг/кг). Концентрации в плазме соединения 1 сравнивали с литературными данными по пропофолу со сходным протоколом, в котором композицию 1% пропофола, составленную таким же образом, как композиция соединения 1, вводили 5 свиньям с помощью 10-мин внутривенного (BB) вливания при скорости 0,750 мг/кг/мин (общая доза 7,5 мг/кг).
По данным этого исследования соединение 1 показало сходный фармакокинетический профиль относительно пропофола на модели на свиньях. Трехчастевая модель лучше всего описала соединение 1 и данные для пропофола. Клиренс соединения 1 превышал предполагаемый печеночный кровоток, подобно пропофолу. Также соединение 1 показало сходный метаболический путь пропофола у свиней и у людей: глюкуронидация в 1-положении вместе с 4-положением подвергается гидроксилированию с последующей конъюгацией глюкуронида и сульфата. Исследование на собаке с повышением дозировки показало сходные концентрации в плазме при выведении соединения 1 и пропофола, также указывая на сходные уровни клиренса в этих видах.
Пример 9. Анестетические эффекты у крыс
Исследовали ответ на анестезирующую дозу болюсной BB инъекции соединения 1 по сравнению с пропофолом у крыс.
Использовали признанную модель общей анестезии на грызунах, для того чтобы определить начало и продолжительность анестезии (см. Hill-Venning С et al., 1996, Neuropharmacology 35, 1209; Lingamaneni R et al., 2001, Anesthesiology 94, 1050), что продемонстрировано с помощью потери рефлекса выпрямления (LORR) и времени восстановления (временной интервал от возвращения рефлекса выпрямления до тех пор, пока крыса не будет способна цепляться и влезать на стальной каркас и нормально переходить с места на место). Также оценивали минимальную дозу для достижения LORR и максимально переносимую дозу (MTD).
Композицию 1% соединения 1, полученную, как описано в примере 2, и составленную в соответствии с примером 5, или диприван вводили посредством болюсной внутривенной (BB) инъекции при скорости 2,5 мл/мин 6 самцам крыс Sprague-Dawley (200-300 г) на дозовую группу за время, необходимое для введения доз, описанных ниже. Относительную активность оценивали путем установления дозы, необходимой для того, чтобы вызвать у 50% крыс потерю рефлекса выпрямления (HD50), и дозы, необходимой для того, чтобы вызвать 7-минутную анестезию (HD7 мин). Были исследованы дозы 2, 3, 4, 7, 14 и 21 мг/кг для соединения 1 и дозы 3,5; 4,0; 7,0 и 14,0 мг/кг для дипривана.
Результаты показали, что болюсное внутривенное (BB) введение соединения вызывало дозозависимую продолжительность анестезии у крыс. Время наступления (начала) LORR составляло меньше, чем 15 сек, когда вводили соответствующие лекарственные средства в дозе, по меньшей мере, 3 мг/кг для соединения 1 и в дозе, по меньшей мере, 7,0 мг/кг для пропофола. Соединение 1 вызывало LORR при всех дозах, по меньшей мере, от 3 мг/кг. Пропофол не вызывал LORR у 4 из 6 крыс, проверенных в дозе 3,5 мг/кг, но вызывал LORR при всех других проверенных дозах. Таблица 1 сравнивает результаты по HD50, HD7 мин, MTD и терапевтический индекс (TI; определенный здесь как отношение MTD к HD7 мин) для соединения 1 и пропофола. Одна крыса погибла при введении 14 мг/кг дипривана. Три крысы погибли при введении 21 мг/кг соединения 1. Время восстановления показало незначительную взаимосвязь с дозой.
| Таблица 1. | ||
| Сравнение результатов по HD50, HD7 мин, MTD и TI для соединения 1 и пропофола, которые вводили крысам с помощью болюсного внутривенного (BB) вливания | ||
| Пропофол | Соединение 1 | |
| HD50 | 3,8 мг/кг | 2,3 мг/кг |
| HD7 мин | 7,0 мг/кг | 3,4 мг/кг |
| MTD | <14 мг/кг | 14 мг/кг |
| TI | <2 | 4.1 |
Итак, соединение 1 показало эффективность при более низких дозах, чем пропофол, и также показало более высокую MTD и улучшенный TI по сравнению с пропофолом.
Также в этих тестах был оценен (S)-(+)-2-втор-бутил-6-изопропилфенол, полученный в соответствии с примером 2, в дозах 4, 5, 6, 7, 14, 21, 28 и 35 мг/кг. Таблица 1a показывает результаты по HD50, HD7 мин, MTD и TI для этого соединения. Одна из шести крыс погибла при введении 28 мг/кг (S)-(+)-2-втор-бутил-6-изопропилфенола.
| Таблица 1a. | |
| Результаты по HD50, HD7 мин, MTD и TI для (S)-(+)-2-втор-бутил-6-изопропилфенола, который вводили крысам с помощью болюсного внутривенного (BB) вливания. | |
| (S)-(+) | |
| HD50 | 5 мг/кг |
| HD7 мин | 6,7 мг/кг |
| MTD | 21 мг/кг |
| TI | 3,1 |
Итак, эффективность (S)-(+)-2-втор-бутил-6-изопропилфенола была сходна с пропофолом. (S)-(+)-2-втор-бутил-6-изопропилфенол показал более высокую MTD и улучшенный TI по сравнению с пропофолом.
Пример 10. Анестетический и гемодинамический эффекты у собак породы бигль
Исследование с повышением дозировки проводили на собаках, чтобы продемонстрировать анестетический и гемодинамический эффекты болюсного BB введения соединения 1 по сравнению с пропофолом.
Конечными точками в этом исследовании была зависимость от дозы индуцирования, продолжительности, глубины и качества анестезии и гемодинамических эффектов болюсного внутривенного (BB) введения соединения 1 или пропофола. Использовали составленную в соответствии с примером 5 композицию 1% соединения 1, полученного, как описано в примере 2, и композицию 1% пропофола, составленного таким же образом.
Электроэнцефалографическое (ЭЭГ) измерение глубины анестезии проводили с помощью биспектрального индекса (BIS), который представляет собой одну из нескольких систем, используемых для измерения эффектов анестетических лекарственных средств на мозг, и для того, чтобы следить за изменениями уровня обезболивания или анестезии. BIS представляет собой математический алгоритм, который анализирует данные от ЭЭГ, и результатом является одно число от 100 (полное сознание) до 0 (изоэлектрическая ЭЭГ). Другие оценки включали шкалу седативного эффекта, клинические наблюдения, кровяное давление, электрокардиограмму (ЭКГ) и насыщение кислородом.
Собакам породы бигль (самцы, 2-4 летнего возраста, 8-10 кг) имплантировали порты для сосудистого доступа. Во время хирургической операции по вживлению портов головы собак брили, размечали для размещения ЭЭГ электродов и вводили BOTOX® (Allergan, Inc., Irvine, СА; очищенный комплекс ботулических токсинов типа A): всего вводили 40 единиц на собаку за 5 внутримышечных (IM) инъекций через бровь. Инъекции предназначались для подавления мышечных движений и электромиографическую (EMG) интерференцию с сигналом BIS.
Исследование было перекрестным. Каждая собака получала от 2 до 4 возрастающих болюсных внутривенных (BB) доз (введенных в течение 60 секунд) соединения 1 или пропофола, отделенных, по меньшей мере, 30 минутами (или временем, пока собака не просыпалась) до тех пор, пока не будет достигнута MTD. MTD была определена как доза, которая уменьшала среднее артериальное давление крови (MAP) на 50% или до значения меньше, чем 50 миллиметров ртутного столба (мм рт.ст.). Все животные получали дополнительно кислород и, если необходимо, вентиляторную поддержку после 4 минут апноэ.
Глубину анестезии определяли посредством оценки наличия или отсутствия lash (махать хвостом) рефлекса, ответа на легкий удар между бровями или слуховой раздражитель, сжатие пальца (toe pinch) и дыхания. Наличие каждого признака считали как 1 и отсутствие каждого как 0. Это давало возможность подсчитать совокупный счет седативного эффекта во множестве временных точек в течение 30 мин между дозами (5 = пробуждение, 0 = апноэ/глубокая анестезия). Качество анестезии оценивали, отмечая плавность вызывания (состояния анестезии), с помощью качественной оценки мышечного тонуса и по наличию непроизвольного движения. Случаи непроизвольных движений (например, во время «выхода») подсчитывали как наличие или отсутствие на всем протяжении наблюдаемого периода для каждой дозы. BIS и гемодинамические эффекты анализировали, с помощью 2-факторного дисперсионного метода анализа ANOVA с последующим t-тестом с поправкой Бонферрони для множественных сравнений эффектов времени и дозы.
А. Анестетические эффекты
Способность соединения 1 и пропофола, введенных с помощью болюсного внутривенного (BB) вливания, вызывать дозозависимую анестезию у самопроизвольно дышащих собак породы бигль без премедикации (5-30 мг/кг/дозу; 3-6 собак на дозу соединения 1; 1-5 собак на дозу пропофола) показана в таблице 2. Две из 3 собак, которым вводили 15 мг/кг пропофола, достигли MTD при 15 мг/кг. Следовательно, только 1 собаке дали дозу 30 мг/кг пропофола.
| Таблица 2. | ||
| Дозированная продолжительность анестезии (время сна) после болюсного BB вливания собакам соединения 1 и пропофола. | ||
| Доза | Пропофол | Соединение 1 |
| 5 мг/кг | 13 мин | 23 мин |
| 10 мг/кг | 28 мин | 33 мин |
| 15 мг/кг | 43 мин | 40 мин |
| 30 мг/кг | 69 мин | 71 мин |
Также данные показали, что анестезия была вызвана в течение 1 минуты при всех дозах соединения 1 и пропофола. Продолжительность анестезии, измеренная временем сна, была сходна при большинстве доз соединения 1 и пропофола. Совокупный счет седативного эффекта показал приблизительно равносильную глубину анестезии обоих препаратов, и пропофола, и соединения 1, в дозе выше 5 мг/кг. Не наблюдалось значительного различия между значениями BIS у собак, которым вводили соединение 1 в дозе 10 мг/кг или пропофол в дозе 10 мг/кг или 15 мг/кг. Соединение 1 вызывало большее действие на BIS в дозах, по меньшей мере, 15 мг/кг, но эти дозы являются очень высокими и потенциально не уместными клинически. Качество анестезии (плавность индуцирования анестезии, качественная оценка мышечного тонуса, наличие непроизвольного движения) соединения 1 было сходно с пропофолом.
Также в этом тесте был оценен (S)-(+)-2-втор-бутил-6-изопропилфенол, полученный в соответствии с примером 2. Таблица 2a показывает дозозависимую продолжительность анестезии (время сна) для этого соединения.
| Таблица 2a. | |
| Дозозависимая продолжительность анестезии (время сна) после болюсного внутривенного (BB) вливания собакам (S)-(+)-2-втор-бутил-6-изопропилфенола и пропофола. | |
| Доза | (S)(+) |
| 5 мг/кг | 12 мин |
| 10 мг/кг | 33 мин |
| 15 мг/кг | 50 мин |
| 30 мг/кг | 56 мин |
Данные показали, что продолжительность анестезии была сходна для соединения 1 и пропофола.
B. Гемодинамические эффекты: Кровяное давление
Гемодинамические данные, такие как среднее артериальное давление (MAP), регистрировали на базовом уровне, через 1, 2, 4, 8, 15, 20 и 30 мин. Соединение 1 вводили в дозах 5, 10, 15 и 30 мг/кг соответственно 6, 4, 3 и 3 собакам. Пропофол вводили в тех же самых дозах 3, 5, 5 и 1 собакам, соответственно. Только 1 собака получила 30 мг/кг пропофола, так как критерий MTD был достигнут при дозе 15 мг/кг у двух животных. Данные анализировали с помощью 2-факторного дисперсионного метода анализа ANOVA с последующим t-тестом с поправкой Бонферрони для множественных сравнений.
Сравнение данных показало, что пропофол вызывал значительно более сильное действие на MAP, чем соединение 1. Таблица 3 представляет пример, в котором процент изменений среднего артериального давления (MAP %) от базового уровня 4 мин после болюсного BB введения 10, 15 или 30 мг/кг соединения 1 сравнивается с изменениями MAP %, вызванными некоторыми дозами пропофола.
| Таблица 3. | ||
| Дозозависимое изменение среднего артериального давления, измереннрого как изменение МАР от базового значения 4 мин, после болюсного внутривенного (BB) введения соединения 1 или пропофола. | ||
| Доза | Пропофол | Соединение 1 |
| 10 мг/кг | -22% | 5% |
| 15 мг/кг | -32% | -19% |
| 30 мг/кг | -66%* | -41% |
| * Только 1 собака прошла испытания при дозе 30 мг/кг пропофола, принимая во внимание 2 собак, достигших критерия MTD при дозе 15 мг/кг пропофола. | ||
Также в этом тесте оценили (S)-(+)-2-втор-бутил-6-изопропилфенол, полученный в соответствии с примером 2. Сравнение данных показало, что пропофол оказывал значительно большее действие на MAP, чем (S)-(+)-2-втор-бутил-6-изопропилфенол. Таблица 3a предоставляет пример, сравнивающий изменения MAP % от базового значения 4 мин.
| Таблица 3a. | |
| Дозозависимое изменение среднего артериального давления, измереннрого как изменение МАР от базового значения 4 мин, после болюсного внутривенного (BB) введения (S)-(+)-2-втор-бутил-6-изопропилфенола. | |
| Доза | (S)-(+) |
| 10 мг/кг | +3% |
| 15 мг/кг | +1% |
| 30 мг/кг | -33% |
Пример 11. Анестетический и гемодинамический эффекты у свиней
Анестетический и гемодинамический эффекты соединения 1 и пропофола сравнивали на анестезированных вентилируемых свиньях, которым внутривенно (BB) вливали композицию с 0,5% соединения 1, полученную, как описано в примере 2, и составленную в соответствии с примером 6, или диприван (эмульсия 1% пропофола для инъекции). Оценки включали ЭЭГ измерения глубины анестезии с использованием BIS, показатели фармакокинетики, кровяное давление, ЭКГ, сердечный ритм, минутный сердечный выброс, температуру тела и насыщение кислородом.
Эксперименты проводили на коммерческих свиньях фермерского разведения и того и другого пола (средний вес 33,6 кг). Анестезию вызывали изофлураном. Внутрисосудистый доступ получали через ушную вену. Каждую свинью инкубировали и механически вентилировали. Насыщение кислородом ткани контролировали с помощью непрерывной пульсовой оксиметрии с размещением на языке. За вентилированием следили с помощью анализатора вдыхаемого/выдыхаемого воздуха, который измерял концентрации кислорода, углекислого газа и сильного ингаляционного анестетика. Установочные параметры вентилирования при необходимости регулировали для поддержания устойчивого состояния.
Непрерывный уровень анестезии достигался с помощью изофлурана и вливания панкурониума (10 мг/час). ЭКГ контролировали на всем протяжении исследования. Артериальное давление крови контролировали через катетер в левой бедренной артерии. MAP, систолическое и диастолическое артериальное давление и сердечный ритм регистрировали каждые 5 секунд. Во внутреннюю яремную вену был помещен легочный артериальный катетер для термодилюционной оценки минутного сердечного выброса и температуры крови. Поддерживали температуру тела 37°С. Для проведения мониторинга ЭЭГ с помощью приборов применяли липкие электроды в лобно-затылочных областях (Aspect Medical, Норвуд, Массачусетс, США).
План эксперимента включал 30-минутный период стабилизации, с последующим BB вливанием соединения 1 (0,6 мг/кг/мин×20 мин) или пропофола (0,750 мг/кг/мин×10 мин). За соответствующим вливанием следовал 180-минутный период вымывания. Образцы крови для гемодинамических измерений и для фармакокинетических исследований отбирали перед вливанием, каждые 2 мин в течение вливания соединения 1 или пропофола и с повторяющимися интервалами в течение периода вымывания. Время и скорости вымывания соединения 1 и пропофола были установлены заранее, чтобы вызвать максимальное снижение BIS (<10) в течение периода вливания. Образцы артериальной крови для определения pH, pO2, pCO2, глюкозы, калия и лактата измеряли на базовом уровне до вливания соединения 1 или пропофола, во время вливания и ежечасно после вливания.
A. Анестетические эффекты
Соединение 1 и пропофол вызывали максимальное подавление BIS (<10) при BB вливаниях 0,6 мг соединения 1 в течение 17,3±1,9 мин (на кг в мин) и 0,750 мг пропофола в течение 9,4±1,9 мин (на кг в мин), соответственно. Действие на ЭЭГ было обратимо, и возвращение к базовому уровню происходило в течение 60 минут.
B. Гемодинамические эффекты
Среднее артериальное давление и сердечный ритм измеряли с интервалами на всем протяжении внутривенного (BB) вливания и «вымывания» соединения 1 (0,6 мг/кг/мин, 6 свиней) и пропофола (0,750 мг/кг/мин, 6 свиней). Результаты показаны на фигурах 3 и 4 соответственно. У свиней, которым вводили соединение 1, брали образцы артериальной крови для анализа крови на газы и кислотность и биохимического анализа крови.
Базовые значения MAP и HR не различались между соединением 1 и пропофолом. Оба соединения уменьшали MAP, но пропофол вызывал значительно большее снижение MAP, чем соединение 1. Самое низкое значение HR, измеренное для пропофола, было значительно ниже, чем самое низкое значение HR, измеренное для соединения 1. Оба значения (HR и MAP) возвращались к базовому значению после прекращения вливания соединения 1 или пропофола.
Значения анализа крови на газы и кислотность и биохимического анализа крови находились в границах нормы. Соединение 1 не вызывало каких-либо значительных метаболических изменений, таких как метаболический ацидоз или повышенный лактат.
Пример 12. Антиэметическая активность
Соединение 1 проверили на антиэметическую активность на хорьках и сравнивали с активностью пропофола.
Самцов descented (без запаха) хорьков весом 1,0-1,5 кг с портами для сосудистого доступа в яремной вене содержали при цикле день/ночь 12 час/12 час при контролируемой температуре с неограниченным доступом к воде и пище (ad libitum). Каждый день на протяжении исследования хорьков кормили за один час до введения дозы вещества. Непосредственно перед введением дозы вещества воду и пищу убирали. Композицию 1% соединения 1, приготовленную, как описано в примере 2, и составленную в соответствии с примером 5, или диприван вводили хорькам с помощью внутривенного (BB) вливания; см. Wynn RL et al., 1993, Eur J Pharmacol 241, 42 re DIPRBBAN administration in ferrets. После введения соединения 1 или дипривана животных помещали в чистые прозрачные клетки (с крышками) и оставляли свободными в течение 45-мин периода наблюдения (наблюдение проводили «вслепую» относительно конкретного примененного воздействия).
Рвота у хорьков отличается ритмичными сокращениями брюшных мышц, которые связаны или с оральным выталкиванием твердого или жидкого вещества из желудочно-кишечного тракта (т.е. рвотой) или с движениями, которые не включают прохождение вещества (т.е. позывы на рвоту). Случаи позывов и/или рвоты рассматривались как отдельные случаи, когда интервал между позывами и/или рвотой достигал 5 сек.
Проэметическую активность соединения 1 или пропофола исследовали на 6 хорьках (на одно лекарственное средство), как указано далее: хорькам давали наркоз посредством ингаляции изофлураном. Соединение 1 или пропофол вводили внутривенным (BB) вливанием в течение 15 мин при скорости 1 мг/кг/мин. После завершения вливания за хорьками наблюдали непрерывно в течение 45 мин и подсчитывали количество случаев рвоты и позывов на рвоту.
Антиэметическую активность соединения 1 или пропофола исследовали на 6 хорьках (на одно лекарственное средство), как указано далее: хорькам давали наркоз изофлураном, вводили соединение 1 или пропофол посредством 15 мин внутривенного (BB) вливания при скорости 1 мг/кг/мин. После завершения вливания подкожно вводили 0,5 мг/кг морфина сульфата, за хорьками наблюдали в течение 45 минут, как описано выше. Еще шести хорькам вводили только 0,5 мг/кг морфина сульфата подкожно.
Один морфин сульфат (0,5 мг/кг) обладал проэметической активностью у хорьков, приводя к 15 случаям рвоты и 157 случаям позывов на рвоту. Соединение 1 не вызывало какого-либо количества случаев рвоты или позывов на рвоту, когда его вводили отдельно. У хорьков, которым вводили соединение 1 в присутствии морфина, наблюдали 1 случай рвоты и 47 случаев позывов на рвоту. У хорьков, получивших пропофол и морфина сульфат, насчитали 3 случая рвоты и 47 случаев позывов на рвоту. Следовательно, и соединение 1, и пропофол уменьшали долю случаев рвоты и позывов в присутствии морфина.
Все публикации, патенты и патентные документы включены в данное описание путем отсылки, как будто включены в данное описание по отдельности. Изобретение описано со ссылкой на различные особые и предпочтительные варианты осуществления и методики. Однако должно быть понятно, что можно сделать много изменений и модификаций, но и оставаться в духе и рамках изобретения.
Claims (16)
2. Фармацевтическая композиция, введение эффективного количества которой агонизирует рецептор GABA, содержащая соединение по п.1 и фармацевтически приемлемый носитель.
3. Фармацевтическая композиция по п.2, которая включена в состав для внутривенного введения.
4. Фармацевтическая композиция по п.3, которая включена в состав, как липидная эмульсия.
7. Соединение по п.1, которое агонизирует рецептор GABA, для применения в лекарственной терапии.
8. Соединение по п.1 для индуцирования или поддержания общей анестезии у животного.
9. Соединение по п.1 для промотирования обезболивания у животного.
10. Способ получения соединения по п.1, который включает:
гидролиз диастереоизомера (-)-2-втор-бутил-6-изопропилфенилового эфира карбаминовой кислоты формулы (II):
где Х является Н и R1 представляет хиральную аминогруппу;
с последующим, если необходимо, образованием свободного фенола или его фармацевтически приемлемой соли.
гидролиз диастереоизомера (-)-2-втор-бутил-6-изопропилфенилового эфира карбаминовой кислоты формулы (II):
где Х является Н и R1 представляет хиральную аминогруппу;
с последующим, если необходимо, образованием свободного фенола или его фармацевтически приемлемой соли.
12. Диастереоизомер по п.11, где R1 представляет (R)-l-арилэтиламиногруппу.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US92841607P | 2007-05-09 | 2007-05-09 | |
| US92834507P | 2007-05-09 | 2007-05-09 | |
| US60/928,345 | 2007-05-09 | ||
| US60/928,416 | 2007-05-09 | ||
| PCT/US2008/063088 WO2008141099A1 (en) | 2007-05-09 | 2008-05-08 | Therapeutic compounds |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2009145541A RU2009145541A (ru) | 2011-06-20 |
| RU2470907C2 true RU2470907C2 (ru) | 2012-12-27 |
Family
ID=39619201
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2009145541/04A RU2470907C2 (ru) | 2007-05-09 | 2008-05-08 | Терапевтические соединения |
Country Status (18)
| Country | Link |
|---|---|
| US (3) | US8173849B2 (ru) |
| EP (2) | EP2152651B1 (ru) |
| JP (1) | JP2010526827A (ru) |
| KR (1) | KR20100017435A (ru) |
| CN (1) | CN101687746A (ru) |
| AT (1) | ATE540010T1 (ru) |
| AU (1) | AU2008251484A1 (ru) |
| BR (1) | BRPI0811284A2 (ru) |
| CA (1) | CA2685813A1 (ru) |
| DK (1) | DK2152651T3 (ru) |
| ES (1) | ES2380824T3 (ru) |
| HK (1) | HK1138830A1 (ru) |
| IL (1) | IL201735A0 (ru) |
| MX (1) | MX2009012125A (ru) |
| MY (1) | MY147215A (ru) |
| RU (1) | RU2470907C2 (ru) |
| WO (1) | WO2008141099A1 (ru) |
| ZA (1) | ZA201007602B (ru) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NZ580752A (en) | 2007-05-09 | 2012-03-30 | Pharmacofore Inc | Stereoisomers propofol therapeutic compounds |
| WO2009140275A1 (en) * | 2008-05-12 | 2009-11-19 | Pharmacofore, Inc. | Analogs of propofol, preparation thereof and use as anesthetics |
| CN102085185B (zh) * | 2010-12-07 | 2013-04-24 | 西安力邦制药有限公司 | 无痛和低注射刺激的新型丙泊酚脂肪乳制剂配方和制备方法 |
| CN102603488B (zh) * | 2012-03-06 | 2017-01-04 | 云南龙海天然植物药业有限公司 | 一种制备高纯度丙泊酚的新方法 |
| CN102731265B (zh) * | 2012-06-12 | 2014-12-10 | 四川百利药业有限责任公司 | 一种高纯度丙泊酚的制备方法 |
| WO2014069611A1 (ja) * | 2012-11-02 | 2014-05-08 | 住友化学株式会社 | 化合物のラセミ体の製造方法 |
| CN104649867B (zh) * | 2013-11-21 | 2017-02-15 | 辽宁药联制药有限公司 | 一种丙泊酚的制备方法 |
| CN105384608B (zh) * | 2014-08-22 | 2019-08-16 | 四川海思科制药有限公司 | 一种异丙基苯酚衍生物及其制备方法 |
| CN105384604B (zh) * | 2014-08-22 | 2019-07-05 | 四川海思科制药有限公司 | 一种异丙基苯酚衍生物及其制备方法 |
| CN105384607B (zh) * | 2014-08-22 | 2019-08-16 | 四川海思科制药有限公司 | 一种异丙基苯酚衍生物及其制备方法 |
| PT3189834T (pt) * | 2014-09-04 | 2024-03-15 | Sichuan Haisco Pharmaceutical Co Ltd | Utilização de agente de reforço do recetor gabaa na preparação de medicamento sedativo e anestésico |
| CN105820040B (zh) * | 2015-01-22 | 2018-07-24 | 四川海思科制药有限公司 | 一种异丙基苯酚衍生物及其制备方法 |
| CN106278947B (zh) * | 2015-05-19 | 2020-03-06 | 四川海思科制药有限公司 | 苯酚衍生物的晶型及其制备方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2747982A (en) * | 1955-05-11 | 1956-05-29 | Dow Chemical Co | Method and composition for the control of the growth of vegetation |
| SU1525139A1 (ru) * | 1987-11-10 | 1989-11-30 | Куйбышевский политехнический институт им.В.В.Куйбышева | Способ получени о-втор-бутилфенола |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4798846A (en) | 1974-03-28 | 1989-01-17 | Imperial Chemical Industries Plc | Pharmaceutical compositions |
| GB1472793A (en) | 1974-03-28 | 1977-05-04 | Ici Ltd | Pharmaceutical compositions |
| ES2087019B1 (es) * | 1994-02-08 | 1997-03-16 | Bobel246 S L | Uso de derivados de fenoles 2,4-disubstituidos como inhibidores de la 5-lipoxigenasa. |
| US5731356A (en) | 1994-03-22 | 1998-03-24 | Zeneca Limited | Pharmaceutical compositions of propofol and edetate |
| GB9405593D0 (en) * | 1994-03-22 | 1994-05-11 | Zeneca Ltd | Pharmaceutical compositions |
| US6254853B1 (en) | 1998-05-08 | 2001-07-03 | Vyrex Corporation | Water soluble pro-drugs of propofol |
| US6204257B1 (en) | 1998-08-07 | 2001-03-20 | Universtiy Of Kansas | Water soluble prodrugs of hindered alcohols |
| US6140374A (en) * | 1998-10-23 | 2000-10-31 | Abbott Laboratories | Propofol composition |
| WO2000048572A1 (en) | 1999-02-18 | 2000-08-24 | Supergen, Inc | Phosphocholine linked prodrug derivatives |
| US6716452B1 (en) | 2000-08-22 | 2004-04-06 | New River Pharmaceuticals Inc. | Active agent delivery systems and methods for protecting and administering active agents |
| US6362234B1 (en) | 2000-08-15 | 2002-03-26 | Vyrex Corporation | Water-soluble prodrugs of propofol for treatment of migrane |
| US20020099013A1 (en) | 2000-11-14 | 2002-07-25 | Thomas Piccariello | Active agent delivery systems and methods for protecting and administering active agents |
| EP1358200A4 (en) | 2000-10-06 | 2005-07-20 | Xenoport Inc | COMPOUNDS DERIVED FROM GALLENIC ACID TO IMPROVE THE ORAL ABSORPTION AND SYSTEMIC BIOVERABILITY OF MEDICAMENTS |
| JP4334229B2 (ja) * | 2001-03-20 | 2009-09-30 | サイデックス・ファーマシューティカルズ・インコーポレイテッド | プロポフォール及びスルホアルキルエーテルシクロデキストリン含有製剤 |
| CA2470500C (en) | 2001-12-28 | 2012-05-15 | Guilford Pharmaceuticals, Inc. | Aqueous based pharmaceutical formulations of water-soluble prodrugs of propofol |
| US7035343B2 (en) | 2002-01-31 | 2006-04-25 | Qualcomm Inc. | Closed loop transmit diversity antenna verification using trellis decoding |
| US6927036B2 (en) | 2002-02-19 | 2005-08-09 | Xero Port, Inc. | Methods for synthesis of prodrugs from 1-acyl-alkyl derivatives and compositions thereof |
| BG65734B1 (bg) | 2002-02-22 | 2009-09-30 | Био Терапютикс - Еоод | Течен мукоадхезивен фармацевтичен състав |
| PL373850A1 (en) | 2002-04-08 | 2005-09-19 | Guilford Pharmaceuticals, Inc. | Pharmaceutical compositions containing water-soluble prodrugs of propofol and methods of administering same |
| ES2314238T3 (es) | 2002-10-08 | 2009-03-16 | Fresenius Kabi Deutschland Gmbh | Conjugados de oligosacaridos farmaceuticamente activos. |
| DE20215415U1 (de) | 2002-10-08 | 2004-02-26 | Biotechnologie Gesellschaft Mittelhessen Mbh | Wasserlösliche Medikamentenvorstufen von Propofol |
| ZA200504940B (en) | 2003-01-28 | 2006-09-27 | Xenoport Inc | Amino acid derived prodrugs of propofol, compositions and uses thereof |
| AU2003901815A0 (en) | 2003-04-15 | 2003-05-01 | Vital Health Sciences Pty Ltd | Phosphate derivatives |
| US7230003B2 (en) | 2003-09-09 | 2007-06-12 | Xenoport, Inc. | Aromatic prodrugs of propofol, compositions and uses thereof |
| WO2005033279A2 (en) * | 2003-09-29 | 2005-04-14 | University Of Virginia Patent Foundation | Discovery of novel soluble crystalline anesthetics |
| WO2006017351A1 (en) | 2004-07-12 | 2006-02-16 | Xenoport, Inc. | Prodrugs of propofol, compositions and uses thereof |
| WO2006033911A2 (en) | 2004-09-17 | 2006-03-30 | Mgi Gp, Inc. | Methods of administering water-soluble prodrugs of propofol |
| JP2008525501A (ja) | 2004-12-23 | 2008-07-17 | ゼノポート,インコーポレイティド | セリンアミノ酸誘導のプロポフォールのプロドラッグ、その使用及び結晶体 |
| DE102005033496A1 (de) * | 2005-07-19 | 2007-01-25 | Bayer Healthcare Ag | Desinfektionsmittel |
| JP5537033B2 (ja) * | 2005-12-19 | 2014-07-02 | ザ ユニヴァーシティー オブ リヴァプール | 無痛覚 |
| US7535698B2 (en) | 2006-03-07 | 2009-05-19 | Panasonic Corporation | Case, portable information equipment using the same and manufacturing method of the case |
| US7731356B1 (en) * | 2006-07-24 | 2010-06-08 | Daniel Ayers Gilbert | Hanging eyeglasses |
-
2008
- 2008-05-08 CA CA002685813A patent/CA2685813A1/en not_active Abandoned
- 2008-05-08 KR KR1020097024778A patent/KR20100017435A/ko not_active Application Discontinuation
- 2008-05-08 AT AT08769340T patent/ATE540010T1/de active
- 2008-05-08 EP EP08769340A patent/EP2152651B1/en active Active
- 2008-05-08 BR BRPI0811284-3A2A patent/BRPI0811284A2/pt not_active IP Right Cessation
- 2008-05-08 RU RU2009145541/04A patent/RU2470907C2/ru not_active IP Right Cessation
- 2008-05-08 DK DK08769340.4T patent/DK2152651T3/da active
- 2008-05-08 MY MYPI20094593A patent/MY147215A/en unknown
- 2008-05-08 MX MX2009012125A patent/MX2009012125A/es active IP Right Grant
- 2008-05-08 US US12/596,711 patent/US8173849B2/en not_active Expired - Fee Related
- 2008-05-08 JP JP2010507667A patent/JP2010526827A/ja active Pending
- 2008-05-08 CN CN200880015398A patent/CN101687746A/zh active Pending
- 2008-05-08 AU AU2008251484A patent/AU2008251484A1/en not_active Abandoned
- 2008-05-08 WO PCT/US2008/063088 patent/WO2008141099A1/en active Application Filing
- 2008-05-08 ES ES08769340T patent/ES2380824T3/es active Active
- 2008-05-08 EP EP11177818A patent/EP2392559A1/en not_active Withdrawn
-
2009
- 2009-10-25 IL IL201735A patent/IL201735A0/en unknown
-
2010
- 2010-06-04 HK HK10105524.2A patent/HK1138830A1/xx not_active IP Right Cessation
- 2010-10-25 ZA ZA2010/07602A patent/ZA201007602B/en unknown
-
2012
- 2012-04-02 US US13/437,802 patent/US8350097B2/en not_active Expired - Fee Related
- 2012-12-03 US US13/692,853 patent/US20130217783A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2747982A (en) * | 1955-05-11 | 1956-05-29 | Dow Chemical Co | Method and composition for the control of the growth of vegetation |
| SU1525139A1 (ru) * | 1987-11-10 | 1989-11-30 | Куйбышевский политехнический институт им.В.В.Куйбышева | Способ получени о-втор-бутилфенола |
Non-Patent Citations (1)
| Title |
|---|
| R.James et al "Synthesis, Biological Evaluation, and Preliminary Structure-Activity Considerations of a Series of Alkylphenols as Intravenous Anesthetic Agents". J. Med. Chem., 1980, 23(12), 1350-135. * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2152651A1 (en) | 2010-02-17 |
| EP2392559A1 (en) | 2011-12-07 |
| BRPI0811284A2 (pt) | 2015-01-20 |
| CN101687746A (zh) | 2010-03-31 |
| IL201735A0 (en) | 2010-06-16 |
| KR20100017435A (ko) | 2010-02-16 |
| RU2009145541A (ru) | 2011-06-20 |
| HK1138830A1 (en) | 2010-09-03 |
| US8350097B2 (en) | 2013-01-08 |
| CA2685813A1 (en) | 2008-11-20 |
| MY147215A (en) | 2012-11-14 |
| MX2009012125A (es) | 2010-02-18 |
| WO2008141099A1 (en) | 2008-11-20 |
| US8173849B2 (en) | 2012-05-08 |
| AU2008251484A1 (en) | 2008-11-20 |
| US20130217783A1 (en) | 2013-08-22 |
| US20100249246A1 (en) | 2010-09-30 |
| DK2152651T3 (da) | 2012-04-10 |
| JP2010526827A (ja) | 2010-08-05 |
| ES2380824T3 (es) | 2012-05-18 |
| US20120196939A1 (en) | 2012-08-02 |
| ATE540010T1 (de) | 2012-01-15 |
| EP2152651B1 (en) | 2012-01-04 |
| ZA201007602B (en) | 2012-08-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2470907C2 (ru) | Терапевтические соединения | |
| US20120283335A1 (en) | Analogs of Propofol, Preparation Thereof and Use as Anesthetics | |
| US8871815B2 (en) | Therapeutic compounds | |
| CH630068A5 (en) | Process for the preparation of 4-hydroxyphenylalkanolamine derivatives | |
| US20130005800A1 (en) | Composition for transdermal or transmucosal administration | |
| ES2354595T3 (es) | (-)-estereoisómero de 2,6-di-sec-butilfenol y análogos del mismo. | |
| NZ580759A (en) | Stereoisomers propofol therapeutic compounds |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20130509 |