KR20230048501A - {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형 및 그의 용도 - Google Patents
{2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형 및 그의 용도 Download PDFInfo
- Publication number
- KR20230048501A KR20230048501A KR1020237000609A KR20237000609A KR20230048501A KR 20230048501 A KR20230048501 A KR 20230048501A KR 1020237000609 A KR1020237000609 A KR 1020237000609A KR 20237000609 A KR20237000609 A KR 20237000609A KR 20230048501 A KR20230048501 A KR 20230048501A
- Authority
- KR
- South Korea
- Prior art keywords
- crystalline form
- xrpd pattern
- peaks
- cyclohexyl
- theta
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/54—Nitrogen and either oxygen or sulfur atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Diabetes (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Epidemiology (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Thiazole And Isothizaole Compounds (AREA)
Abstract
본 발명은 a) {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산("화합물 I")의 결정형; b) 화합물 I의 하나 이상의 결정형, 및 선택적으로, 약학적으로 허용가능한 담체를 포함하는 약학 조성물; c) 화합물 I의 하나 이상의 결정형을 투여함으로써 당뇨병의 유형 또는 다른 장애를 치료하는 방법; 및 d) 화합물 I의 결정형의 제조 방법에 관한 것이다.
Description
본 개시내용은 a) {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산("화합물 I" 또는 "API")의 결정형; b) {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 하나 이상의 결정형, 및 선택적으로 약학적으로 허용가능한 담체를 포함하는 약학 조성물; 및 c) {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 하나 이상의 결정형을 이를 필요로 하는 대상체에게 투여함으로써 당뇨병의 유형 및 다른 장애를 치료하는 방법에 관한 것이다.
글루코키나제("GK")는 글루코스 항상성의 핵심 조절자이며 생리학적 글루코스 센서로서 작용하여, 글루코스 농도의 변화와 동시에 그의 형태, 활성 및/또는 세포내 위치를 변화시킨다. GK는 혈당 제어를 위한 좋은 선택으로 만드는 두 가지 구별되는 특징을 갖는다. 첫째, 그의 발현은 주로 글루코스 감지가 필요한 조직(주로 간 및 췌장 β 세포)으로 제한된다. 둘째, GK는 혈청 글루코스 수준의 변화를 감지하고 간 글루코스 대사의 변화를 조절하여 간 글루코스 생산(HGP)과 글루코스 소비 사이의 균형을 조절할 수 있고, 베타 세포에 의한 인슐린 분비의 변화를 조절할 수 있다. 당뇨병 치료를 위한 GK 활성화의 개념은 매력적인데, 현재 시판 중인 항당뇨 요법의 작용과 완전히 구별되는 메커니즘에 의해 1형 및 2형 당뇨병의 동물 모델에서 혈당증을 정상화하는 데 효과적이고 안전한 것으로 입증되었기 때문이다.
GK의 여러 소분자 활성제가 임상 개발되었지만, 이들의 초기 치료 약속은 저혈당증의 발생, 증가된 트리글리세라이드(TG)의 농도, 및 시간 경과에 따른 효능의 손실에 의해 방해받았다. 이러한 부작용(AE)은 진행 중인 β 세포 활성화와 관련이 있었다. 간 선택제인 화합물 I은 유사한 적대적 효과를 유발하지 않는다. (Vella et al., Science Translational Medicine 16 Jan 2019).
화합물 I은 혈당 제어를 개선하고 저혈당증, 이상지질혈증, 또는 치료적 관련 용량에서 간에서 글리코겐 및 TG의 병리학적 증가를 유도하지 않을 수 있는 경구용 소분자 간 선택적 글루코키나제 활성제이다. (Vella et al., Science Translational Medicine 16 Jan 2019).
GK 활성제인 모든 화합물이 유용한 치료제가 될 최상의 잠재력을 제공하는 특징을 갖는 것은 아니다. 이러한 특징 중 일부는 글루코키나제에서의 높은 친화력, 글루코키나제 활성화의 지속시간, 경구 생체이용률, 조직 분포, 및 안정성(예컨대, 제제화하거나 또는 결정화하는 능력, 저장 수명)을 포함한다. 유리한 특징은 개선된 안전성, 내약성, 효능, 치료 지수, 환자 순응도, 비용 효율성, 제조 용이성 등을 야기할 수 있다.
또한, 허용가능한 고체 상태 특징(화학적 안정성, 열 안정성, 용해도, 흡습성, 및/또는 입자 크기 포함), 화합물 제조가능성(수율, 결정화 동안 불순물 제거, 여과 특성, 건조 특성, 및 밀링 특성 포함), 및 제제 실행가능성(타정 동안 압력 또는 압축력에 대한 안정성 포함)을 갖는 화합물 I의 결정형 및 상응하는 약학적 제제의 단리 및 상업적 규모 제조는 많은 문제를 제시한다.
따라서, 이들 특성들의 허용가능한 균형을 갖고 약학적으로 허용가능한 고체 투여 형태의 제조에 사용될 수 있는 화합물 I의 하나 이상의 결정형이 현재 필요하다.
일 양태에서, 본 개시내용은 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다. 일 양태에서, 결정형은 무수이다. 또 다른 양태에서, 결정형은 용매화된다.
일 양태에서, 본 개시내용은
a) 16.9 ± 0.2, 17.4 ± 0.2, 및 20.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
b) 11.0 ± 0.2, 11.6 ± 0.2, 및 17.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
c) 4.3 ± 0.2, 17.4 ± 0.2, 및 21.6 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
d) 5.3 ± 0.2, 8.7 ± 0.2, 및 26.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
e) 5.8 ± 0.2, 17.9 ± 0.2, 및 18.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
f) 3.8 ± 0.2, 9.5 ± 0.2, 및 16.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
g) 3.4 ± 0.2, 21.2 ± 0.2, 및 21.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
h) 3.8 ± 0.2, 5.3 ± 0.2, 및 8.5 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
i) 5.0 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형; 및
j) 5.9 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형
으로 이루어진 군으로부터 선택되는, 화학식 (I)의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다:
일 양태에서, 본 개시내용은 16.9 ± 0.2, 17.4 ± 0.2, 및 20.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 DSC에 의해 결정된 바와 같이 약 160℃에서 개시되는 흡열 피크를 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 1099.7 ± 2.0, 1158.0 ± 2.0, 및 1313.2 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 실질적으로 도 4에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 단순 단사정계(primitive monoclinic)로 인덱스되는 단위 셀을 갖는다. 또 다른 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 약 10.193 Å의 a 값, 약 12.256 Å의 b 값, 및 약 18.991 Å의 c 값을 갖는 단위 셀을 갖는다. 또 다른 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 약 2370.9Å3의 부피를 갖는 단위 셀을 갖는다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 A이다.
일 양태에서, 본 개시내용은 11.0 ± 0.2, 11.6 ± 0.2, 및 17.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 DSC에 의해 결정된 바와 같이 약 166℃에서 개시되는 흡열 피크를 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 1310.1 ± 2.0, 1514.4 ± 2.0, 및 1661.3 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 실질적으로 도 8에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 단순 단사정계로 인덱스되는 단위 셀을 갖는다. 또 다른 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 약 11.028Å의 a 값, 약 11.933 Å의 b 값, 및 약 18.737Å의 c 값을 갖는 단위 셀을 갖는다. 또 다른 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 약 2449.0 Å3의 부피를 갖는 단위 셀을 갖는다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 B이다.
일 양태에서, 본 개시내용은 4.3 ± 0.2, 17.4 ± 0.2, 및 21.6 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 DSC에 의해 결정된 바와 같이 약 149℃에서 개시되는 흡열 피크를 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 디클로로메탄 용매화물이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 단순 단사정계로 인덱스되는 단위 셀을 갖는다. 또 다른 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 약 5.541 Å의 a 값, 약 13.040 Å의 b 값, 및 약 40.818 Å의 c 값을 갖는 단위 셀을 갖는다. 또 다른 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 약 2947.6 Å3의 부피를 갖는 단위 셀을 갖는다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 C이다.
일 양태에서, 본 개시내용은 5.3 ± 0.2, 8.7 ± 0.2, 및 26.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 DSC에 의해 결정된 바와 같이 약 147℃에서 개시되는 흡열 피크를 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 실질적으로 도 13에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 D이다.
일 양태에서, 본 개시내용은 5.8 ± 0.2, 17.9 ± 0.2, 및 18.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 DSC에 의해 결정된 바와 같이 약 171℃에서 개시되는 흡열 피크를 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 E이다.
일 양태에서, 본 개시내용은 3.8 ± 0.2, 9.5 ± 0.2, 및 16.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 F이다.
일 양태에서, 본 개시내용은 3.4 ± 0.2, 21.2 ± 0.2, 및 21.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 G이다.
일 양태에서, 본 개시내용은 3.8 ± 0.2, 5.3 ± 0.2, 및 8.5 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 H이다.
일 양태에서, 본 개시내용은 5.0 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 I이다.
일 양태에서, 본 개시내용은 5.9 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 DSC에 의해 결정된 바와 같이 약 164℃에서 개시되는 흡열 피크를 특징으로 한다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 J이다.
일부 양태에서, 결정형은 실질적으로 다른 다형 형태가 없다. 일부 양태에서, 결정형은 적어도 약 80%의 다형 순도를 갖는다.
일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형은 형태 A, 형태 B, 형태 C, 형태 D, 형태 E, 형태 F, 형태 G, 형태 H, 형태 I, 및 형태 J로 이루어진 군으로부터 선택된다. 일 양태에서, {2-[3-사이클로헥실-3-(트랜스-4 -프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산은 형태 A이다.
일부 양태에서, 본 개시내용은 상기 논의된 결정형 중 임의의 하나 이상 및 약학적으로 허용가능한 담체, 희석제, 부형제, 또는 이들의 혼합물을 포함하는 약학 조성물에 관한 것이다.
일부 양태에서, 본 개시내용은 당뇨병의 유형 또는 다른 장애를 치료하는 방법에 관한 것으로서, 상기 방법은 상기 논의된 약학 조성물을 이를 필요로 하는 환자에게 투여하는 단계를 포함한다. 일부 양태에서, 당뇨병의 유형은 1형 당뇨병이다. 일부 양태에서, 당뇨병의 유형은 2형 당뇨병이다.
일부 구현예에서, 약학 조성물은 경구 투여된다. 일부 양태에서, 약학 조성물은 정제로서 투여된다. 일부 양태에서, 환자는 최대 약 2000 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 매일 투여받는다.
일부 양태에서, 본 개시내용은 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형을 제조하는 방법으로서, 결정형은 형태 A, 형태 B, 형태 C, 형태 D, 형태 E, 형태 F, 형태 G, 형태 H, 형태 I 및 형태 J로 이루어진 군으로부터 선택되는 것인 방법을 제공한다.
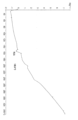
도 1은 결정형 A에 상응하는 분말 X선 회절 패턴("XRPD")이다.
도 2a는 결정형 A에 상응하는 시차 주사 열량측정 온도기록도("DSC")이다.
도 2b는 결정형 A에 상응하는 열중량측정 분석 온도기록도("TGA")이다.
도 3은 결정형 A에 상응하는 적외선("IR") 스펙트럼이다.
도 4는 결정형 A에 상응하는 13C 고체 상태 NMR이다.
도 5는 결정형 B에 상응하는 XRPD이다.
도 6a는 결정형 B에 상응하는 DSC이다.
도 6b는 결정형 B에 상응하는 TGA이다.
도 7은 결정형 B에 상응하는 IR 스펙트럼이다.
도 8은 결정형 B에 상응하는 13C 고체 상태 NMR이다.
도 9는 결정형 C에 상응하는 XRPD이다.
도 10a는 결정형 C에 상응하는 DSC이다.
도 10b는 결정형 C에 상응하는 TGA이다.
도 11은 결정형 D에 상응하는 XRPD이다.
도 12a는 결정형 D에 상응하는 DSC이다.
도 12b는 결정형 D에 상응하는 TGA이다.
도 13은 결정형 D에 상응하는 13C 고체 상태 NMR이다.
도 14는 결정형 E에 상응하는 XRPD이다.
도 15a는 결정형 E에 상응하는 DSC이다.
도 15b는 결정형 E에 상응하는 TGA이다.
도 16은 결정형 F에 상응하는 XRPD이다.
도 17은 결정형 G에 상응하는 XRPD이다.
도 18은 결정형 H에 상응하는 XRPD이다.
도 19는 결정형 I에 상응하는 XRPD이다.
도 20은 결정형 J에 상응하는 XRPD이다.
도 21a는 결정형 J에 상응하는 DSC이다.
도 21b는 결정형 J에 해당하는 TGA이다.
도 2a는 결정형 A에 상응하는 시차 주사 열량측정 온도기록도("DSC")이다.
도 2b는 결정형 A에 상응하는 열중량측정 분석 온도기록도("TGA")이다.
도 3은 결정형 A에 상응하는 적외선("IR") 스펙트럼이다.
도 4는 결정형 A에 상응하는 13C 고체 상태 NMR이다.
도 5는 결정형 B에 상응하는 XRPD이다.
도 6a는 결정형 B에 상응하는 DSC이다.
도 6b는 결정형 B에 상응하는 TGA이다.
도 7은 결정형 B에 상응하는 IR 스펙트럼이다.
도 8은 결정형 B에 상응하는 13C 고체 상태 NMR이다.
도 9는 결정형 C에 상응하는 XRPD이다.
도 10a는 결정형 C에 상응하는 DSC이다.
도 10b는 결정형 C에 상응하는 TGA이다.
도 11은 결정형 D에 상응하는 XRPD이다.
도 12a는 결정형 D에 상응하는 DSC이다.
도 12b는 결정형 D에 상응하는 TGA이다.
도 13은 결정형 D에 상응하는 13C 고체 상태 NMR이다.
도 14는 결정형 E에 상응하는 XRPD이다.
도 15a는 결정형 E에 상응하는 DSC이다.
도 15b는 결정형 E에 상응하는 TGA이다.
도 16은 결정형 F에 상응하는 XRPD이다.
도 17은 결정형 G에 상응하는 XRPD이다.
도 18은 결정형 H에 상응하는 XRPD이다.
도 19는 결정형 I에 상응하는 XRPD이다.
도 20은 결정형 J에 상응하는 XRPD이다.
도 21a는 결정형 J에 상응하는 DSC이다.
도 21b는 결정형 J에 해당하는 TGA이다.
I. 정의
본원에 제시된 개시내용의 이해를 용이하게 하기 위해, 다수의 용어가 하기에 정의된다.
일반적으로, 본원에 사용된 명명법 및 본원에 기술된 유기 화학, 의료 화학, 및 약리학에서의 실험실 절차는 잘 알려져 있고 당업계에서 일반적으로 사용되는 것이다. 달리 정의되지 않는 한, 본원에 사용된 모든 기술적 및 과학적 용어는 본 개시내용이 속하는 기술 분야에서 통상의 지식을 가진 자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다.
본 명세서 및 첨부된 청구범위에서, 단수 형태 "a", "an" 및 "the"는 문맥이 달리 명확하게 지시하지 않는 한 복수의 지시 대상을 포함한다. 용어 "a"(또는 "an") 뿐만 아니라 용어 "하나 이상" 및 "적어도 하나"는 본원에서 상호교환적으로 사용될 수 있다. 특정 양태에서, 용어 "a" 또는 "an"은 "단일"을 의미한다. 다른 양태에서, 용어 "a" 또는 "an"은 "둘 이상" 또는 "다중"을 포함한다.
또한, 본원에서 사용되는 "및/또는"은 다른 것을 갖거나 갖지 않는 2개의 지정된 특징 또는 구성요소 각각의 특정한 개시로서 간주되어야 한다. 따라서, 본원에서 "A 및/또는 B"와 같은 문구에서 사용되는 용어 "및/또는"은 "A 및 B", "A 또는 B", "A"(단독) 및 "B"(단독)을 포함하는 것으로 의도된다. 마찬가지로, "A, B, 및/또는 C"와 같은 문구에서 사용되는 용어 "및/또는"은 하기 양태 각각을 포함하는 것으로 의도된다: A, B, 및 C; A, B, 또는 C; A 또는 C; A 또는 B; B 또는 C; A 및 C; A 및 B; B 및 C; A(단독); B(단독); 및 C(단독).
용어 "화합물 I"은 화학적 화합물 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 지칭한다.
용어 "대상체"는 비제한적으로 영장류(예컨대, 인간), 소, 양, 염소, 말, 개, 고양이, 토끼, 쥐, 또는 마우스를 포함하는 동물을 지칭한다. 용어 "대상체" 및 "환자"는 예를 들어 포유동물 대상체, 예컨대 인간 대상체와 관련하여 본원에서 상호교환적으로 사용된다.
용어 "치료하다", "치료하는" 및 "치료"는 장애, 질환 또는 병태, 또는 장애, 질환 또는 병태와 관련된 하나 이상의 증상을 경감시키거나 없애는 것; 또는 장애, 질환 또는 병태 자체의 원인(들)을 완화시키는 것을 포함하는 것을 의미한다.
용어 "약학적으로 허용가능한 담체", "약학적으로 허용가능한 희석제", 또는 "약학적으로 허용가능한 부형제"는 약학적으로 허용가능한 물질, 조성물 또는 비히클, 예컨대 액체 또는 고체 충전제, 희석제, 부형제, 용매, 또는 캡슐화 물질을 지칭한다. 일 양태에서, 각각의 구성요소는 약학적 제제의 다른 성분과 양립가능하고 합리적인 이익/위험 비율에 상응하는 과도한 독성, 자극, 알레르기 반응, 면역원성, 또는 다른 문제 또는 합병증 없이 인간 및 동물의 조직 또는 기관과 접촉하여 사용하기에 적합하다는 의미에서 "약학적으로 허용가능"하다. 문헌[Remington: The Science and Practice of Pharmacy, 21st Edition, Lippincott Williams & Wilkins: Philadelphia, PA, 2005; Handbook of Pharmaceutical Excipients, 5th Edition, Rowe et al., Eds., The Pharmaceutical Press and the American Pharmaceutical Association: 2005; and Handbook of Pharmaceutical Additives, 3rd Edition, Ash and Ash Eds., Gower Publishing Company: 2007; Pharmaceutical Preformulation and Formulation, Gibson Ed., CRC Press LLC: Boca Raton, FL, 2004 (본원에 참조로 포함됨)]을 참조한다.
용어 "약" 또는 "대략"은 값이 측정되거나 결정되는 방법에 부분적으로 의존하는 당업자에 의해 결정된 특정 값에 대한 허용가능한 오차를 의미한다. 특정 양태에서, 용어 "약" 또는 "대략"은 1, 2, 3, 또는 4 표준 편차 이내를 의미한다. 특정 구현예에서, 용어 "약" 또는 "대략"은 주어진 값 또는 범위의 50%, 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0.5%, 또는 0.05% 이내를 의미한다.
용어 "활성 성분" 및 "활성 물질"은 병태, 장애, 또는 질환의 하나 이상의 증상을 치료하거나, 이의 개시를 지연시키거나, 또는 이를 완화시키기 위해, 단독으로 또는 하나 이상의 약학적으로 허용가능한 부형제와 조합하여 대상체에게 투여되는 화합물을 지칭한다. 본원에 사용된 바와 같이, "활성 성분" 및 "활성 물질"은 본원에 기재된 화합물의 광학적으로 활성인 이성질체일 수 있다.
용어 "용매화물" 또는 "용매화된"은 비공유 분자간 힘에 의해 결합된 화학량론적 또는 비화학량론적 양의 용매를 추가로 포함하는 본원에 제공된 화합물 또는 이의 염을 지칭한다. 용매가 물인 경우, 용매화물은 수화물이다. 용매가 에탄올을 포함하는 경우, 화합물은 에탄올 용매화물일 수 있다.
본원에서 사용되는 용어 "다형(polymorph)"은 특정 결정 패킹 배열에서 화합물 또는 그의 염, 수화물 또는 용매화물의 결정형을 지칭한다. 모든 다형은 동일한 원소 조성을 갖는다. 본원에서 사용되는 용어 "결정질"은 구조 단위의 규칙적인 배열로 구성되는 고체 상태 형태를 지칭한다. 동일한 화합물, 또는 이의 염, 수화물 또는 용매화물의 상이한 결정형들은 고체 상태의 분자의 상이한 패킹으로부터 발생하며, 이는 상이한 결정 대칭 및/또는 단위 셀 파라미터를 초래한다. 상이한 결정형은 일반적으로 상이한 X선 회절 패턴, 적외선 스펙트럼, 녹는점, 밀도, 경도, 결정 모양, 광학적 및 전기적 특성, 안정성, 및 용해도를 갖는다. 예를 들어, 문헌[Remington's Pharmaceutical Sciences, 18 th ed., Mack Publishing, Easton PA, 173 (1990); The United States Pharmacopeia, 23 rd ed., 1843-1844 (1995)(본원에 참조로 포함됨)]을 참조한다.
결정형은 가장 일반적으로 X선 분말 회절(XRPD)을 특징으로 한다. 반사의 XRPD 패턴(전형적으로 도 2-세타로 표현되는 피크)은 일반적으로 특정 결정형의 지문으로 간주된다. XRPD 피크의 상대적 강도는 특히 샘플 제조 기술, 결정 크기 분포, 필터, 샘플 장착 절차, 및 사용된 특정 기기에 따라 크게 달라질 수 있다. 일부 경우에, 기기의 유형이나 설정에 따라 새로운 피크가 관찰될 수 있거나 기존 피크가 사라질 수 있다. 일부 경우에, 기기의 유형이나 설정, 기기의 감도, 측정 조건, 및/또는 결정형의 순도에 따라, XRPD 패턴에서 임의의 특정 피크가 단일항(singlet), 이중항(doublet), 삼중항(triplet), 사중항(quartet), 또는 다중항(multiplet)으로 나타날 수 있다. 일부 경우에, XRPD에서의 임의의 특정 피크는, 예컨대 숄더(shoulder)를 갖는 대칭 모양 또는 비대칭 모양으로 나타날 수 있다. 또한, 기기 변동 및 다른 요인이 2-세타 값에 영향을 미칠 수 있다. 이러한 변동을 이해하는 숙련된 기술자는 XRPD를 사용하는 것뿐만 아니라 다른 공지된 물리화학적 기술을 사용하여 특정 결정형의 정의하는 특징 또는 특성을 구별하거나 확인할 수 있다.
화합물에 적용되는 용어 "무수물" 또는 "무수"는 화합물이 결정 격자 내에 구조적 물을 함유하지 않는 고체 상태를 지칭한다.
문맥상 달리 요구되지 않는 한, 용어 "포함하다" 및 "포함하는"은 이들이 배타적이 아니라 포괄적으로 해석되어야 하며 출원인이 하기 청구범위를 포함하여 이 특허를 해석함에 있어서 이들 단어 각각이 그렇게 해석되는 것을 의도한다는 근거와 명확한 이해에 따라 사용된다.
본원에 개시된 모든 구현예에 대해, 피크 위치 재현성은 도-2θ(XRPD), ppm(13C 고체 상태 NMR), 및 cm-1(IR)의 값과 연관된다. 따라서, 본원에 개시된 모든 피크는 개시된 값 ± 각 분석 기술과 연관된 피크 위치 재현성을 갖는다는 것을 이해할 것이다. XRPD 피크 위치 재현성은 도-2θ로 표현된 ±0.2이다. 13C NMR 피크 위치 재현성은 ±0.2 ppm이다. IR 피크 위치 재현성은 ±2 cm-1이다.
달리 정의되지 않는 한, 본원에 사용되는 모든 기술 및 과학 용어는 본 개시내용이 속하는 기술 분야에서 통상의 지식을 가진 자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다. 상충하는 경우, 정의를 포함한 본 출원이 우선할 것이다. 문맥상 달리 요구되지 않는 한, 단수형 용어는 복수형을 포함하고 복수형 용어는 단수형을 포함한다. 본원에 언급된 모든 간행물, 특허 및 다른 참고문헌은 마치 각각의 개별 간행물 또는 특허 출원이 구체적이고 개별적으로 참조로 포함되는 것으로 표시된 것처럼 모든 목적을 위해 전체가 참조로 포함된다.
II. 결정형
일 양태에서, 본 개시내용은 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다. 일 양태에서, 결정형은 1H NMR에 의해 결정된 바와 같이 무수이다. 또 다른 양태에서, 결정형은 1H NMR에 의해 결정된 바와 같이 용매화된다.
일 양태에서, 본 개시내용은
a) 16.9 ± 0.2, 17.4 ± 0.2, 및 20.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
b) 11.0 ± 0.2, 11.6 ± 0.2, 및 17.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
c) 4.3 ± 0.2, 17.4 ± 0.2, 및 21.6 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
d) 5.3 ± 0.2, 8.7 ± 0.2, 및 26.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
e) 5.8 ± 0.2, 17.9 ± 0.2, 및 18.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
f) 3.8 ± 0.2, 9.5 ± 0.2, 및 16.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
g) 3.4 ± 0.2, 21.2 ± 0.2, 및 21.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
h) 3.8 ± 0.2, 5.3 ± 0.2, 및 8.5 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
i) 5.0 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형; 및
j) 5.9 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형
으로 이루어진 군으로부터 선택되는, 화학식 (I)의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형에 관한 것이다:
A. 결정형 A
일 양태에서, 본 개시내용은 16.9 ± 0.2, 17.4 ± 0.2, 및 20.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 8.7 ± 0.2, 16.9 ± 0.2, 17.4 ± 0.2, 및 20.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 1에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 1에서의 하기 XRPD 패턴을 특징으로 한다:
표 1
일 양태에서, 화합물 I의 결정형은 DSC에 의해 결정된 바와 같이 약 160℃에서 개시되는 흡열 피크를 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 2a에 나타낸 바와 같은 DSC 프로파일을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 2b에 나타낸 바와 같은 TGA 프로파일을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 1099.7 ± 2.0, 1158.0 ± 2.0, 및 1313.2 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 1099.7 ± 2.0, 1158.0 ± 2.0, 1238.7 ± 2.0, 및 1313.2 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 표 2에서의 하기 IR 피크를 특징으로 한다.
표 2
일 양태에서, 화합물 I의 결정형은 실질적으로 도 3에 나타낸 바와 같은 IR 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 4에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 한다.
일 양태에서, 결정형은 1H NMR에 의해 결정되는 바와 같이 무수이다.
일 양태에서, 화합물 I의 결정형은 단순 단사정계로 인덱스되는 단위 셀을 갖는다. 또 다른 양태에서, 화합물 I의 결정형은 약 10.193 Å의 a 값, 약 12.256 Å의 b 값, 및 약 18.991 Å의 c 값을 갖는 단위 셀을 갖는다. 또 다른 양태에서, 화합물 I의 결정형은 약 2370.9 Å3의 부피를 갖는 단위 셀을 갖는다.
일 양태에서, 화합물 I의 결정형은 형태 A이다.
B. 결정형 B
일 양태에서, 본 개시내용은 11.0 ± 0.2, 11.6 ± 0.2, 및 17.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 11.0 ± 0.2, 11.6 ± 0.2, 17.8 ± 0.2, 및 21.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 5에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 3에서의 하기 XRPD 패턴을 특징으로 한다:
표 3
일 양태에서, 화합물 I의 결정형은 DSC에 의해 결정된 바와 같이 약 166℃에서 개시되는 흡열 피크를 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 6a에 나타낸 바와 같은 DSC 프로파일을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 6b에 나타낸 바와 같은 TGA 프로파일을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 1310.1 ± 2.0, 1514.4 ± 2.0, 및 1661.3 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 1097.3 ± 2.0, 1310.1 ± 2.0, 1541.4 ± 2.0, 및 1661.3 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 표 4에서의 하기 IR 피크를 특징으로 한다.
표 4
일 양태에서, 화합물 I의 결정형은 실질적으로 도 7에 나타낸 바와 같은 IR 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 8에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 한다.
일 양태에서, 결정형은 1H NMR에 의해 결정되는 바와 같이 무수이다.
일 양태에서, 화합물 I의 결정형은 단순 단사정계로 인덱스되는 단위 셀을 갖는다. 또 다른 양태에서, 화합물 I의 결정형은 약 11.028 Å의 a 값, 약 11.933 Å의 b 값 및 약 18.737 Å의 c 값을 갖는 단위 셀을 갖는다. 또 다른 양태에서, 화합물 I의 결정형은 약 2449.0 Å3의 부피를 갖는 단위 셀을 갖는다.
일 양태에서, 화합물 I의 결정형은 형태 B이다.
C. 결정형 C
일 양태에서, 본 개시내용은 4.3 ± 0.2, 17.4 ± 0.2, 및 21.6 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 4.3 ± 0.2, 8.0 ± 0.2, 17.4 ± 0.2, 및 약 21.6 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 9에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 5에서의 하기 XRPD 패턴을 특징으로 한다:
표 5
일 양태에서, 화합물 I의 결정형은 DSC에 의해 결정된 바와 같이 약 149℃에서 개시되는 흡열 피크를 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 10a에 나타낸 바와 같은 DSC 프로파일을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 10b에 나타낸 바와 같은 TGA 프로파일을 특징으로 한다.
일 양태에서, 결정형은 1H NMR에 의해 결정되는 바와 같은 용매화물이다. 일 양태에서, 화합물 I의 결정형은 디클로로메탄 용매화물이다.
일 양태에서, 화합물 I의 결정형은 단순 단사정계로 인덱스되는 단위 셀을 갖는다. 또 다른 양태에서, 화합물 I의 결정형은 약 5.541 Å의 a 값, 약 13.040 Å의 b 값, 및 약 40.818 Å의 c 값을 갖는 단위 셀을 갖는다. 또 다른 양태에서, 화합물 I의 결정형은 약 2947.6 Å3의 부피를 갖는 단위 셀을 갖는다.
일 양태에서, 화합물 I의 결정형은 형태 C이다.
D. 결정형 D
일 양태에서, 본 개시내용은 5.3 ± 0.2, 8.7 ± 0.2, 및 26.4 ± 0.2도 2 세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 5.3 ± 0.2, 8.7 ± 0.2, 18.2 ± 0.2, 및 26.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 11에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 6에서의 하기 XRPD 패턴을 특징으로 한다:
표 6
일 양태에서, 화합물 I의 결정형은 DSC에 의해 결정된 바와 같이 약 147℃에서 개시되는 흡열 피크를 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 12a에 나타낸 바와 같은 DSC 프로파일을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 12b에 나타낸 바와 같은 TGA 프로파일을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 13과 실질적으로 유사한 13C 고체 상태 NMR을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 형태 D이다.
E. 결정형 E
일 양태에서, 본 개시내용은 5.8 ± 0.2, 17.9 ± 0.2, 및 18.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 5.8 ± 0.2, 17.9 ± 0.2, 18.9 ± 0.2, 및 20.7 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 14에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 7에서의 하기 XRPD 패턴을 특징으로 한다:
표 7
일 양태에서, 화합물 I의 결정형은 DSC에 의해 결정된 바와 같이 약 171℃에서 개시되는 흡열 피크를 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 15a에 나타낸 바와 같은 DSC 프로파일을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 15b에 나타낸 바와 같은 TGA 프로파일을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 형태 E이다.
F. 결정형 F
일 양태에서, 본 개시내용은 3.8 ± 0.2, 9.5 ± 0.2, 및 16.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 3.8 ± 0.2, 9.5 ± 0.2, 16.8 ± 0.2, 및 17.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 16에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 8에서의 하기 XRPD 패턴을 특징으로 한다:
표 8
일 양태에서, 화합물 I의 결정형은 형태 F이다.
G. 결정형 G
일 양태에서, 본 개시내용은 3.4 ± 0.2, 21.2 ± 0.2, 및 21.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 3.4 ± 0.2, 21.2 ± 0.2, 21.9 ± 0.2, 및 22.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 17에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 9에서의 하기 XRPD 패턴을 특징으로 한다:
표 9
일 양태에서, 화합물 I의 결정형은 형태 G이다.
H. 결정형 H
일 양태에서, 본 개시내용은 3.8 ± 0.2, 5.3 ± 0.2, 및 8.5 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 3.8 ± 0.2, 5.3 ± 0.2, 8.5 ± 0.2, 및 15.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 18에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 10에서의 하기 XRPD 패턴을 특징으로 한다:
표 10
일 양태에서, 화합물 I의 결정형은 형태 H이다.
I. 결정형 I
일 양태에서, 본 개시내용은 5.0 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 5.0 ± 0.2, 15.9 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 19에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 11에서의 하기 XRPD 패턴을 특징으로 한다:
표 11
일 양태에서, 화합물 I의 결정형은 형태 I이다.
J. 결정형 J
일 양태에서, 본 개시내용은 5.9 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다. 일 양태에서, 본 개시내용은 5.9 ± 0.2, 12.7 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는, 화합물 I의 결정형에 관한 것이다.
일 양태에서, 화합물 I의 결정형은 실질적으로 도 20에 나타낸 바와 같은 XRPD 패턴을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 DSC에 의해 결정된 바와 같이 약 164℃에서 개시되는 흡열 피크를 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 21a에 나타낸 바와 같은 DSC 프로파일을 특징으로 한다. 일 양태에서, 화합물 I의 결정형은 실질적으로 도 21b에 나타낸 바와 같은 TGA 프로파일을 특징으로 한다.
일 양태에서, 화합물 I의 결정형은 도 2θ 및 상대적 강도로 표현된 표 12에서의 하기 XRPD 패턴을 특징으로 한다:
표 12
일 양태에서, 화합물 I의 결정형은 형태 J이다.
일부 양태에서, 상기 논의된 결정형 중 임의의 하나는 실질적으로 다른 다형 형태가 없다. 일부 양태에서, 결정형은 적어도 약 80%의 다형 순도를 갖는다. 일부 양태에서, 결정형은 적어도 약 80%, 적어도 약 85%, 적어도 약 86%, 적어도 약 87%, 적어도 약 88%, 적어도 약 89%, 적어도 약 89%, 적어도 약 90%, 적어도 약 91%, 적어도 약 92%, 적어도 약 93%, 적어도 약 94%, 적어도 약 95%, 적어도 약 96%, 적어도 약 97%, 적어도 약 98%, 또는 적어도 약 99%의 다형 순도를 갖는다.
일 양태에서, 화합물 I의 결정형은 형태 A, 형태 B, 형태 C, 형태 D, 형태 E, 형태 F, 형태 G, 형태 H, 형태 I 및 형태 J로 이루어진 군으로부터 선택된다. 일 양태에서, 화합물 I의 결정형은 형태 A이다.
일 양태에서, 화합물 I의 결정형은 형태 A, 형태 B, 형태 C, 형태 D, 형태 E, 형태 F, 형태 G, 형태 H, 형태 I, 및 형태 J로 이루어진 군으로부터 선택되는 둘 이상의 형태의 혼합물이다. 또 다른 양태에서, 화합물 I의 결정형은 형태 A, 형태 B 및 형태 C로 이루어진 군으로부터 선택된 2개 이상의 형태의 혼합물이다. 또 다른 양태에서, 화합물 I의 결정형은 형태 A와 형태 B의 혼합물이며, 여기서 형태 B는 주 형태이고 형태 A는 부 형태이다.
일부 양태에서, 본 개시내용은 화합물 I의 결정형을 제조하는 방법을 제공하며, 여기서 결정형은 형태 A, 형태 B, 형태 C, 형태 D, 형태 E, 형태 F, 형태 G, 형태 H, 형태 I, 및 형태 J로 이루어진 군으로부터 선택된다. 형태 A-J를 제조하는 하나 이상의 방법이 본원의 실험 섹션에 제공된다.
III.
약학 조성물
본 개시내용은 화합물 I의 형태 A-J 중 임의의 하나의 결정형 및 약학적으로 허용가능한 담체, 희석제, 또는 부형제, 또는 이들의 혼합물을 포함하는 약학 조성물에 관한 것이다.
일 양태에서, 약학 조성물은 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다.
화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함하는 약학 조성물은 경구 용도에 적합한 형태, 예를 들어 정제, 트로키, 로젠지, 분산성 분말 또는 과립, 또는 경질 또는 연질 캡슐일 수 있다. 경구 용도를 위한 조성물은 임의의 공지된 방법에 따라 제조될 수 있으며, 이러한 조성물은 약학적으로 우아하고 입맛에 맞는 제제를 제공하기 위해 감미제, 향미제, 착색제, 및 보존제로 이루어진 군으로부터 선택된 하나 이상의 제제를 함유할 수 있다.
일부 양태에서, 약학 조성물은 경구, 비경구(예컨대, 피하, 정맥내, 근육내, 흉골내 및 주입 기술), 직장, 비강내, 국소 또는 경피(예컨대, 패치의 사용을 통한) 경로를 통해 대상체에게 투여될 수 있다.
일 양태에서, 약학 조성물은 약 100 mg 내지 약 1500 mg, 약 100 mg 내지 약 1400 mg, 약 100 mg 내지 약 1300 mg, 약 100 mg 내지 약 1200 mg, 약 100 mg 내지 약 1100 mg, 약 100 mg 내지 약 1000 mg, 약 100 mg 내지 약 900 mg, 약 100 mg 내지 약 800 mg, 약 100 mg 내지 약 700 mg, 약 100 mg 내지 약 600 mg, 약 100 mg 내지 약 500 mg, 약 100 mg 내지 약 400 mg, 약 100 mg 내지 약 300 mg, 약 100 mg 내지 약 200 mg, 또는 약 100 mg 내지 약 150 mg의 본원에 개시된 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일 양태에서, 약학 조성물은 약 100 mg, 약 200 mg, 약 300 mg, 약 400 mg, 약 500 mg, 약 600 mg, 약 700 mg, 약 800 mg, 약 900 mg, 약 1000 mg, 약 1100 mg, 약 1200 mg, 약 1300 mg, 약 1400 mg, 또는 약 1500 mg의 본원에 개시된 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다.
일부 양태에서, 약학 조성물은 경구 정제이다. 일부 양태에서, 경구 정제는 약 0.1 mg 내지 2000 mg의 형태 A-J 2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산 중 임의의 하나의 결정형 을 포함한다. 일부 양태에서, 경구 정제는 약 1 mg 내지 약 2000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 1 mg 내지 약 1000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 100 mg 내지 약 800 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 50 mg 내지 약 400 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 100 mg 내지 약 400 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 100 mg 내지 약 300 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 500 mg 내지 약 1000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 0.1 mg, 약 0.5 mg, 약 1 mg, 약 5 mg, 약 10 mg, 약 20 mg, 약 30 mg, 약 40 mg, 약 50 mg, 약 60 mg, 약 70 mg, 약 80 mg, 약 90 mg, 약 100 mg, 약 125 mg, 약 150 mg, 약 175 mg, 약 200 mg, 약 225 mg, 약 250 mg, 약 275 mg, 약 300 mg, 약 325 mg, 약 350 mg, 약 375 mg, 약 400 mg, 약 425 mg, 약 450 mg, 약 475 mg, 약 500 mg, 약 550 mg, 약 600 mg, 약 650 mg, 약 700 mg, 약 750 mg, 약 800 mg, 약 850 mg, 약 900 mg, 약 1000 mg, 약 1050 mg, 약 1100 mg, 약 1150 mg, 약 1200 mg, 약 1250 mg, 약 1300 mg, 약 1350 mg, 약 1400 mg, 약 1450 mg, 약 1500 mg, 약 1550 mg, 약 1600 mg, 약 1650 mg, 약 1700 mg, 약 1750 mg, 약 1800 mg, 약 1850 mg, 약 1900 mg, 약 1950 mg, 또는 약 2000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 800 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 400 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 300 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다. 일부 양태에서, 경구 정제는 약 200 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 포함한다.
IV. 치료 방법
일부 양태에서, 본 개시내용은 당뇨병의 유형을 치료하는 방법에 관한 것이며, 상기 방법은 상기 논의된 약학 조성물을 이를 필요로 하는 환자에게 투여하는 단계를 포함한다. 방법은 화합물 I의 형태 A-J 중 임의의 하나의 결정형의 치료적 유효량을 포함하는 약학 조성물을 투여하는 단계를 포함할 수 있다. 일부 양태에서, 당뇨병의 유형은 1형 당뇨병이다. 일부 양태에서, 당뇨병의 유형은 2형 당뇨병이다. 일부 양태에서, 당뇨병의 유형은 1형 당뇨병 및 2형 당뇨병의 하나 또는 2개의 유형이다.
일부 양태에서, 환자는 인슐린 요법으로 치료받고 있다. 일부 양태에서, 인슐린 요법은 연속적인 인슐린 주입이다. 일부 양태에서, 인슐린 요법은 연속적인 피하 인슐린 주입이다. 일부 양태에서, 인슐린 요법은 인슐린의 다중 일일 용량이다.
또 다른 양태에서, 본 개시내용은 본 개시내용의 화합물 또는 약학 조성물을 이를 필요로 하는 대상체에게 투여하는 단계를 포함하는, 글루코키나제 결핍 매개 병태 또는 질환, 또는 글루코키나제 활성의 증가로부터 이익을 얻는 병태의 치료 방법을 제공한다.
또 다른 양태에서, 본 개시내용은 본 개시내용의 화합물 또는 약학 조성물을 이러한 치료를 필요로 하는 대상체에게 투여하는 단계를 포함하는, 대사 장애를 치료하기 위한, 혈당 강하를 위한, 고혈당증을 치료하기 위한, 저혈당증을 치료하기 위한, 내당능 손상(IGT)을 치료하기 위한, 증후군 X를 치료하기 위한, 공복 혈당 장애(IFG)를 치료하기 위한, 내당능 장애(IGT)이 2형 당뇨병으로 진행하는 것을 지연시키기 위한, 비인슐린 요구 2형 당뇨병이 인슐린 요구 2형 당뇨병으로 진행하는 것을 지연시키기 위한, 이상지질혈증을 치료하기 위한, 고지혈증을 치료하기 위한, 고혈압을 치료하기 위한, 음식 섭취를 감소시키기 위한, 식욕 조절을 위한, 비만 치료를 위한, 섭식 행동을 조절하기 위한, 또는 엔테로인크레틴(enteroincretin)의 분비를 향상시키기 위한 방법을 제공한다.
또 다른 양태에서, 본 개시내용은 본 개시내용의 화합물 또는 약학 조성물을 이러한 치료를 필요로 하는 대상체에게 투여하는 단계를 포함하는, 베타 세포 질량 및 기능의 보존 방법을 제공한다.
또 다른 양태에서, 본 개시내용은 본 개시내용의 화합물 또는 약학 조성물을 이러한 치료를 필요로 하는 대상체에게 투여하는 단계를 포함하는, 췌도 이식을 받은 대상체에서 베타 세포 질량 및 기능을 보존 및/또는 증가시키는 방법을 제공한다.
또 다른 양태에서, 본 개시내용은 본 개시내용의 화합물 또는 약학 조성물을 이러한 치료를 필요로 하는 대상체에게 투여하는 단계를 포함하는, 간 이식을 받는 대상체에서 간 기능 및/또는 생존을 개선하는 방법을 제공한다. 추가 양태에서, 투여는 이식 전, 동안 또는 후에, 또는 이들의 임의의 조합으로 일어난다.
또 다른 양태에서, 본 개시내용은 본 개시내용의 화합물 또는 약학 조성물을 이러한 치료를 필요로 하는 대상체에게 투여하는 단계를 포함하는, 대상체에서 당뇨병성 케톤산증을 예방하거나 당뇨병성 케톤산증 사건의 발생을 감소시키는 방법을 제공한다.
치료될 병태, 장애, 또는 질환 및 대상체의 상태에 따라, 본원에서 제공되는 약학 조성물은 경구, 비경구(예컨대, 근육내, 복강내, 정맥내 또는 동맥내(예컨대, 카테터를 통해), ICV, 수조내(intracisternal) 주사 또는 주입, 피하 주사, 또는 이식), 흡입, 비강, 질, 직장, 설하, 및/또는 국소(예컨대, 경피 또는 국소) 투여 경로에 의해 투여될 수 있으며, 단독으로 또는 각 투여 경로에 적절한 약학적으로 허용가능한 비히클, 담체, 희석제, 부형제 또는 이들의 혼합물과 함께 적합한 투여 단위로 함께 제제화될 수 있다. 일 양태에서, 약학 조성물은 경구 투여된다.
경구 투여를 위해, 본원에 제공된 약학 조성물은 경구 투여를 위한 고체, 반고체, 또는 액체 투여 형태로 제공될 수 있다. 본원에서 사용되는 바와 같이, 경구 투여는 또한 협측, 설측, 및 설하 투여를 포함한다. 적합한 경구 투여 형태는, 비제한적으로 정제, 캡슐, 환제, 트로키, 로젠지, 패스틸(pastille), 카셰(cachet), 펠렛, 약용 츄잉 검, 과립, 벌크 분말, 발포성 또는 비발포성 분말 또는 과립, 용액, 유화액, 현탁액(예컨대, 수성 또는 오일 현탁액), 웨이퍼, 스프링클, 엘릭시르, 시럽, 볼루스, 연약, 또는 페이스트를 포함한다. 일 양태에서, 약학 조성물은 정제로서 투여된다.
용량은 하루에 적절한 간격으로 투여되는 1, 2, 3, 4, 5, 6, 또는 그 이상의 하위용량의 형태일 수 있다. 용량 또는 하위용량은 투여량 단위당 약 1 mg 내지 약 2000 mg, 약 10 mg 내지 약 2000 mg, 약 100 mg 내지 약 1500 mg, 약 200 mg 내지 약 1500 mg, 약 200 mg 내지 약 1500 mg, 약 300 mg 내지 약 1500 mg, 약 400 mg 내지 약 1500 mg, 약 500 mg 내지 약 1500 mg, 약 500 mg 내지 약 1000 mg, 또는 약 500mg 내지 약 800 mg의 형태 A-J 중 임의의 하나의 결정형을 함유하는 용량 단위의 형태로 투여될 수 있다. 예를 들어, 용량 또는 하위용량은 약 100 mg, 약 200 mg, 약 300 mg, 약 400 mg, 약 500 mg, 약 600 mg, 약 700 mg, 약 800 mg, 약 900 mg, 약 1000 mg, 약 1100 mg, 약 1200 mg, 약 1300 mg, 약 1400 mg, 약 1500 mg, 약 1600 mg, 약 1700 mg, 약 1800 mg, 약 1900 mg, 또는 약 2000 mg의 본원에 개시된 형태 A-J 중 임의의 하나의 결정형을 함유하는 투여량 단위의 형태로 투여될 수 있다.
일부 양태에서, 환자는 약 0.1 mg 내지 약 2000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 매일 투여받는다. 일부 양태에서, 환자는 약 1 mg 내지 약 2000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 매일 투여받는다. 일부 양태에서, 환자는 약 100 mg 내지 약 800 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 매일 투여받는다. 일부 양태에서, 환자는 약 50 mg 내지 약 400 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 매일 투여받는다. 일부 양태에서, 환자는 약 100 mg 내지 약 400 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 매일 투여받는다. 일부 양태에서, 환자는 약 100 mg 내지 약 300 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 매일 투여받는다. 일부 양태에서, 환자는 약 500 mg 내지 약 1000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 매일 투여받는다. 일부 구현예에서, 환자는 약 0.1 mg, 약 0.5 mg, 약 1 mg, 약 5 mg, 약 10 mg, 약 20 mg, 약 30 mg, 약 40 mg, 약 50 mg, 약 60 mg, 약 70 mg, 약 80 mg, 약 90 mg, 약 100 mg, 약 125 mg, 약 150 mg, 약 175 mg, 약 200 mg, 약 225 mg, 약 250 mg, 약 275 mg, 약 300 mg, 약 325 mg, 약 350 mg, 약 375 mg, 약 400 mg, 약 425 mg, 약 450 mg, 약 500 mg, 약 550 mg, 약 1000 mg, 약 1050 mg, 약 1100 mg, 약 1150 mg, 약 1200 mg, 약 1250 mg, 약 1300 mg, 약 1350 mg, 약 1400 mg, 약 1450 mg, 약 1500 mg, 약 1550 mg, 약 1600 mg, 약 1650 mg, 약 1700 mg, 약 1750 mg, 약 1800 mg, 약 1850 mg, 약 1900 mg, 약 1950 mg, 또는 약 2000 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 1일 1회 투여받는다. 일부 양태에서, 환자는 약 800 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 1일 1회 투여받는다. 일부 양태에서, 환자는 약 400 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 1일 1회 투여받는다. 일부 양태에서, 환자는 약 300 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 1일 1회 투여받는다. 일부 양태에서, 환자는 약 200 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 1일 1회 투여받는다. 일부 양태에서, 환자는 약 100 mg의 화합물 I의 형태 A-J 중 임의의 하나의 결정형을 1일 1회 투여받는다.
실시예
A. 약어와 두문자어
B. 실험 방법
실시예 1: 슬러리-연마(Slurry-Trituration) 실험을 통한 안정한 형태 및 수화물 스크린
슬러리 연마 실험은 안정한 용매화물 및 수화물을 포함하는 안정한 형태를 대상으로 한다.
다양한 온도에서 7일(상승된 온도) 또는 14-18일(주변 온도 및 주변 미만 온도) 동안 지정된 용매 및 용매 혼합물에서 화합물 I의 고체를 교반함으로써 슬러리-연마 실험을 수행하였다. 실험 조건 및 결과의 요약이 표 13에 자세히 설명되어 있다.
표 13
실시예 2: 다형 스크린
달리 언급하지 않는 한 화합물 I의 고체를 출발 물질로 사용하였다. 연구에서 생산된 물질을 선택된 실험에 이용하였다.
방법 a: 증발 실험
출발 물질의 용액을 빠른 증발(FE)을 위해 개방된 바이알로부터 또는 느린 증발(SE)을 위해 핀 홀을 갖는 알루미늄 호일로 덮인 바이알로부터 주변 또는 상승된 온도에서 부분적으로 증발시키거나 건조될 때까지 증발시켰다. 증발 전에, 용액을 0.2 μm 나일론 필터를 사용하여 주변 또는 상승된 온도에서 여과하였다.
방법 b: 냉각 실험
출발 물질의 용액을 가열용 핫 플레이트를 사용하여 상승된 온도에서 지정된 용매에서 제조하였다. 이들을 전형적으로 0.2 μm 나일론 필터를 통해 가온 수용 바이알 내로 고온 여과하였다. 바이알을 크래쉬 냉각(CC)을 위해 주변 미만의 온도 배쓰(전형적으로 드라이 아이스/아세톤) 내로 빠르게 옮기거나, 빠른 냉각(FC)을 위해 뜨거운 곳으로부터 꺼내거나, 또는 느린 냉각(SC)을 허용하기 위해 열을 껐다. 고체가 침전되면, 이들을 진공 여과에 의해 차갑게 분리하였다. 용액이 투명한 상태로 남아 있으면, 샘플을 주변 미만 온도에서 유지시키거나 추가 결정화 기술을 적용하였다.
방법 c: 슬러리 실험
고체를 지정된 용매에 현탁시켰다. 그런 다음 현탁액을 주변 온도 또는 설정 온도에서 교반하였다. 주어진 시간 후, 고체를 분리하였다.
방법 d: 용매/반용매(anti-solvent) 침전
시작 물질의 용액을 주변 또는 상승된 온도에서 제조하고 0.2 μm 나일론 필터를 사용하여 여과하였다. 그런 다음 이들을 상승된 온도에서 적절한 반용매와 혼합하였다. 고체가 관찰되지 않으면, 샘플을 주변 온도 또는 주변 미만 온도로 냉각하거나 다른 결정화 기술을 적용하였다.
다형 스크리닝을 증발, 냉각, 슬러리, 용매/반용매 첨가, 및 이러한 기술의 조합을 포함하는 다양한 용매 기반 기술을 사용하여 수행하였다. 자세한 실험 조건, 관찰, 및 XRPD 결과가 표 14에 요약되어 있다.
표 14
실시예 3: 선택된 물질의 제조
표 15는 선택한 물질에 대한 제조 조건을 요약한다.
표 15
표 16은 선택한 물질의 건조 조건을 요약한다.
표 16
실시예 4: 경쟁적 슬러리 실험
형태 A, 형태 D, 형태 B, 및 형태 E 중에서 열역학적으로 가장 안정한 무수 형태를 확인하기 위해, 경쟁적 슬러리를 2-8℃, 주변 온도, 및 45℃에서 아세톤에서 수행하였다.
각 조건에서, 4개의 형태/물질로부터 유사한 양의 고체를 조사된 온도 조건에서 7일 동안 미리 포화된 용액에서 슬러리화한 다음, 고체를 분리하고 XRPD에 의해 습식 분석하였다. 상세한 실험 조건 및 XRPD 결과가 표 17에 요약되어 있다.
표 17
X선 분말 회절(XRPD)
XRPD 패턴을 Optix 긴 미세 초점 광원을 사용하여 생성된 Cu 방사선의 입사 빔을 사용하는 PANalytical X'Pert PRO MPD 또는 Empyrean 회절계로 수집하였다. Cu Kα X선 방사선을 시편을 통과하여 검출기에 집중시키기 위해 타원형(elliptically graded) 다층박막 거울을 사용하였다. 분석에 앞서, 실리콘 시편(NIST SRM 640e)을 분석하여 Si(111) 피크의 관찰된 위치가 NIST 인증 위치와 일치하는지 확인하였다. 샘플의 시편을 3 μm 두께의 필름 사이에 끼우고 전달 기하학에서 분석하였다. 빔 스톱(beam-stop), 짧은 산란방지 연장(short antiscatter extension), 및 산란방지 나이프 에지(antiscatter knife-edge)를 사용하여 공기에 의해 생성된 배경을 최소화하였다. 입사 및 회절 빔에 대한 솔러 슬릿(soller slit)을 사용하여 축방향 분기(axial divergence)로부터의 확장을 최소화하였다. 시편으로부터 240 mm에 위치한 스캐닝 위치 민감성 검출기(X'Celerator) 및 데이터 수집기 소프트웨어 v. 5.5를 사용하여 회절 패턴을 수집하였다.
열중량측정 분석 및 시차 주사 열량계 조합 분석(TGA/DSC)
TGA/DSC 조합 분석을 Mettler Toledo TGA/DSC3+ 분석기를 사용하여 수행하였다. 온도 및 엔탈피 조정을 인듐, 주석, 및 아연을 사용하여 수행한 다음, 인듐으로 검증하였다. 균형을 칼슘 옥살레이트로 검증하였다. 샘플을 알루미늄 팬에 넣었다. 팬을 밀봉하고, 뚜껑을 뚫은 다음, TG 용광로에 삽입하였다. 샘플 팬으로 구성된 계량된 알루미늄 팬을 기준 플랫폼 위에 두었다. 용광로를 질소 하에서 가열하였다.
동적 증기 수착(DVS)
수분 수착/탈착 데이터를 표면 측정 시스템 DVS 인트린직 기기에서 수집하였다. 샘플은 분석 전에 건조되지 않았다. 받은 그대로의 로트에 대해, 수착 및 탈착 데이터를 10% RH 증분으로 5%부터 95% RH까지의 범위에 걸쳐 수집하였다. 분석에 사용된 평형 기준은 5분 내에 0.0100% 미만의 중량 변화 미만이었고, 최대 평형 시간은 3시간이었다. 데이터는 샘플의 초기 수분 함량에 대해 수정되지 않았다.
핫 스테이지 현미경 검사(HSM)
핫 스테이지 현미경 검사를 SPOT Insight™ 컬러 디지털 카메라가 장착된 Leica DM LP 현미경에 장착된 Linkam 핫 스테이지(FTIR 600)를 사용하여 수행하였다. 온도 보정을 USP 융점 표준물질을 사용하여 수행하였다. 샘플을 커버 유리 위에 두고, 두 번째 커버 유리를 샘플 위에 두었다. 스테이지가 가열됨에 따라, 각 샘플을 교차 편광판과 1차 적색 보상기가 있는 20x 대물렌즈, 0.40 NA를 사용하여 시각적으로 관찰하였다. 이미지를 SPOT 소프트웨어(v. 4.5.9)를 사용하여 캡처하였다.
편광 현미경 검사(PLM)
PLM을 Spot Insight 컬러 카메라가 장착된 Leica DM LP 현미경을 사용하여 수행하였다. 교차 편광을 1차 적색 보상기와 함께 사용하였다. 샘플을 보기 위해 다양한 대물렌즈를 사용하였다. 샘플을 방법을 위해 선택된 미네랄 오일 또는 분산제에 현탁시켰다. 이미지를 Spot Advanced 소프트웨어(v.4.5.9)를 사용하여 주변 온도에서 획득하였다. 크기에 대한 참조로서 마이크로미터 막대를 이미지에 삽입하였다. 입자 크기를 NIST 추적가능 스테이지 마이크로미터를 사용하여 보정된 접안 렌즈 레티클 스케일을 사용하여 측정하였다.
양성자 용액 핵 자기 공명 분광법(1H NMR)
용액 NMR 스펙트럼을 DMSO-d 6 를 사용한 Bruker AVANCE 600MHz 분광계로 획득하였다.
탄소-13 고체 상태 핵 자기 공명 분광법(13C 고체 상태 NMR)
Agilent DD2-400 분광계(Larmor 주파수: 13C = 100.549 MHz, 1H = 399.812 MHz)에서 주변 온도에서 13C 고체 상태 교차 편광 매직 각 스피닝(CP/MAS) NMR 스펙트럼을 획득하였다. 샘플을 4 mm PENCIL 유형 지르코니아 로터에 채우고, 매직 각에서 12 kHz로 회전시켰다. 스펙트럼을 2.6 μs(90°)의 1H 펄스 폭, 5 ms의 경사 진폭 교차 편광 접촉 시간, 30 ms 획득 시간, 스캔간 10초 지연, 2678개의 데이터 포인트를 갖는 45 kHz의 스펙트럼 폭, 및 1600개의 공동 추가 스캔을 사용하여 획득 시간 동안 위상 변조된(SPINAL-64) 고출력 1H 디커플링으로 스펙트럼을 획득하였다. 자유 유도 붕괴(free induction decay, FID)를 65536개의 포인트와 10 Hz의 지수 라인 확장 계수를 갖는 Agilent VnmrJ 3.2A 소프트웨어를 사용하여 처리하여 신호 대 잡음비를 개선하였다. FID의 처음 3개의 데이터 포인트를 VNMR 선형 예측 알고리즘을 사용하여 역 예측하여 평평한 기저선을 생성하였다. 스펙트럼 피크의 화학적 이동은 176.5 ppm에서 글리신의 카르보닐 탄소 공명을 외부적으로 참조하였다.
적외선 분광법(IR)
Ever-Glo 중/원적외선 광원, 브롬화칼륨(KBr) 빔분할기, 및 중수소화된 트리글리신 설페이트(DTGS) 검출기가 장착된 Nicolet 6700 푸리에 변환 적외선(FT-IR) 분광광도계(Thermo Nicolet)를 사용하여 IR 스펙트럼을 획득하였다. NIST SRM 1921b(폴리스티렌)를 사용하여 파장 검증을 수행하였다. 게르마늄(Ge) 결정이 장착된 감쇠 전 반사(ATR) 액세서리(Thunderdome™, Thermo Spectra-Tech)를 데이터 수집에 사용하였다. 스펙트럼은 4 cm-1의 스펙트럼 분해능에서 수집된 256개의 공동 추가 스캔을 나타낸다. 깨끗한 Ge 결정으로 배경 데이터 세트를 획득하였다. 서로에 대한 이들 두 데이터 세트의 비율을 취함으로써 로그 1/R( R = 반사율) 스펙트럼을 수득하였다.
XRPD 인덱싱
화합물 I의 고해상도 XRPD 패턴을 이 연구에서 X'Pert High Score Plus 2.2a(2.2.1)를 사용하여 인덱싱하였다. 인덱싱 및 구조 개선은 계산 연구이다. 빨간색 막대로 표시된 허용된 피크 위치와 관찰된 피크 사이의 일치는 일관된 단위 셀 결정을 나타낸다. 패턴의 성공적인 인덱싱은 샘플이 주로 단일 결정상으로 구성되어 있음을 나타낸다. 할당된 소멸 기호, 단위 셀 매개변수, 및 도출된 양과 일치하는 공간 그룹은 잠정적인 인덱싱 솔루션을 보여주는 각 그림 아래 표로 표시된다. 잠정적인 인덱싱 솔루션을 확인하기 위해, 결정학적 단위 셀 내의 분자 패킹 모티프가 결정되어야 한다. 분자 패킹에서 어떠한 시도도 수행되지 않았다.
결론
형태 A-J를 포함하여 화합물 I의 다수의 결정질 물질이 본 연구에서 관찰되었다.
형태 A, B, D 및 E는 화합물 I의 무수 물질이다. 그 중에서, 형태 A는 경쟁적 슬러리로부터의 결과에 기초하여 2-8℃ ~ 45℃ 내에서 가장 안정한 형태일 가능성이 높다.
형태 C는 형태 D로 탈용매화되는 DCM 용매화물일 가능성이 높다. 형태 F도 용매화된 물질이며 건조시 형태 D로 전환된다.
형태 I는 등구조(iso-structural) 용매화물의 계열을 나타낼 수 있다. 그것은 건조시 형태 E 또는 형태 E와 유사한 고체로 전환된다.
형태 G 및 H는 무질서한 결정질 물질이며 용매화물일 수 있다. 이들은 건조시 무질서해진다.
본 발명은 그의 특정 양태과 관련하여 설명되었지만, 본 발명은 추가 변형될 수 있고 본 출원은 일반적으로 원리에 따르고 본 발명이 속하는 기술 분야 내에서 공지된 또는 관례적인 관행 내에 있는 본 개시내용으로부터의 이러한 일탈을 포함하는 임의의 변형, 사용 또는 적응을 포함하는 것으로 의도되며, 전술한 필수적인 특징에 적용될 수 있고 청구범위에서 다음과 같다.
Claims (105)
- a) 16.9 ± 0.2, 17.4 ± 0.2, 및 20.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
b) 11.0 ± 0.2, 11.6 ± 0.2, 및 17.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
c) 4.3 ± 0.2, 17.4 ± 0.2, 및 21.6 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
d) 5.3 ± 0.2, 8.7 ± 0.2, 및 26.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
e) 5.8 ± 0.2, 17.9 ± 0.2, 및 18.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
f) 3.8 ± 0.2, 9.5 ± 0.2, 및 16.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
g) 3.4 ± 0.2, 21.2 ± 0.2, 및 21.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
h) 3.8 ± 0.2, 5.3 ± 0.2, 및 8.5 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형;
i) 5.0 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형; 및
j) 5.9 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형
으로 이루어진 군으로부터 선택되는, 하기 화학식 (I)의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형:
. - 제1항에 있어서, 16.9 ± 0.2, 17.4 ± 0.2, 및 20.1 ± 0.2도 2 세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제2항에 있어서, 8.7±0.2, 16.9±0.2, 17.4±0.2, 20.1±0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제2항 또는 제3항에 있어서, 실질적으로 도 1에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제2항 내지 제4항 중 어느 한 항에 있어서, DSC에 의해 결정된 바와 같이 약 160℃에서 개시되는 흡열 피크를 특징으로 하는 결정형.
- 제2항 내지 제5항 중 어느 한 항에 있어서, 실질적으로 도 2a에 나타낸 바와 같은 DSC 프로파일을 특징으로 하는 결정형.
- 제2항 내지 제6항 중 어느 한 항에 있어서, 실질적으로 도 2b에 나타낸 바와 같은 TGA 프로파일을 특징으로 하는 결정형.
- 제2항 내지 제7항 중 어느 한 항에 있어서, 1099.7 ± 2.0, 1158.0 ± 2.0, 및 1313.2 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 하는 결정형.
- 제2항 내지 제8항 중 어느 한 항에 있어서, 1099.7 ± 2.0, 1158.0 ± 2.0, 1238.7 ± 2.0, 및 1313.2 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 하는 결정형.
- 제2항 내지 제9항 중 어느 한 항에 있어서, 실질적으로 도 3에 나타낸 바와 같은 IR 패턴을 특징으로 하는 결정형.
- 제2항 내지 제10항 중 어느 한 항에 있어서, 실질적으로 도 4에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 하는 결정형.
- 제2항 내지 제11항 중 어느 한 항에 있어서, 무수인 결정형.
- 제2항 내지 제12항 중 어느 한 항에 있어서, 단순 단사정계(primitive monoclinic)로 인덱스되는 단위 셀을 갖는 결정형.
- 제2항 내지 제13항 중 어느 한 항에 있어서, 약 10.193 Å의 a 값, 약 12.256 Å의 b 값, 및 약 18.991 Å의 c 값을 갖는 단위 셀을 갖는 결정형.
- 제2항 내지 제14항 중 어느 한 항에 있어서, 약 2370.9Å3의 부피를 갖는 단위 셀을 갖는 결정형.
- 제2항 내지 제15항 중 어느 한 항에 있어서, 형태 A인 결정형.
- 제1항에 있어서, 11.0 ± 0.2, 11.6 ± 0.2, 및 17.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제17항에 있어서, 11.0 ± 0.2, 11.6 ±0.2, 17.8 ± 0.2, 21.1 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제17항 또는 제18항에 있어서, 실질적으로 도 5에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제17항 내지 제19항 중 어느 한 항에 있어서, DSC에 의해 결정된 바와 같이 약 166℃에서 개시되는 흡열 피크를 특징으로 하는 결정형.
- 제17항 내지 제20항 중 어느 한 항에 있어서, 결정형은 실질적으로 도 6a에 나타낸 바와 같은 DSC 프로파일을 특징으로 하는 결정형.
- 제17항 내지 제21항 중 어느 한 항에 있어서, 실질적으로 도 6b에 나타낸 바와 같은 TGA 프로파일을 특징으로 하는 결정형.
- 제17항 내지 제22항 중 어느 한 항에 있어서, 1310.1 ± 2.0, 1514.4 ± 2.0, 및 1661.3 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 하는 결정형.
- 제17항 내지 제23항 중 어느 한 항에 있어서, 1097.3 ± 2.0, 1310.1 ± 2.0, 1541.4 ± 2.0, 및 1661.3 ± 2.0 cm-1에서 피크를 갖는 IR 패턴을 특징으로 하는 결정형.
- 제17항 내지 제24항 중 어느 한 항에 있어서, 실질적으로 도 7에 나타낸 바와 같은 IR 패턴을 특징으로 하는 결정형.
- 제17항 내지 제25항 중 어느 한 항에 있어서, 실질적으로 도 8에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 하는 결정형.
- 제17항 내지 제26항 중 어느 한 항에 있어서, 무수인 결정형.
- 제17항 내지 제27항 중 어느 한 항에 있어서, 단순 단사정계로 인덱스되는 단위 셀을 갖는 결정형.
- 제17항 내지 제28항 중 어느 한 항에 있어서, 약 11.028Å의 a 값, 약 11.933 Å의 b 값, 및 약 18.737Å의 c 값을 갖는 단위 셀을 갖는 결정형.
- 제17항 내지 제29항 중 어느 한 항에 있어서, 약 2449.0 Å3의 부피를 갖는 단위 셀을 갖는 결정형.
- 제17항 내지 제30항 중 어느 한 항에 있어서, 형태 B인 결정형.
- 제1항에 있어서, 4.3 ± 0.2, 17.4 ± 0.2, 및 21.6 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제32항에 있어서, 4.3 ± 0.2, 8.0 ± 0.2, 17.4 ± 0.2, 및 약 21.6 ± 0.2도 2 세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제32항 또는 제33항에 있어서, 실질적으로 도 9에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제32항 내지 제34항 중 어느 한 항에 있어서, DSC에 의해 결정된 바와 같이 약 149℃에서 개시되는 흡열 피크를 특징으로 하는 결정형.
- 제32항 내지 제35항 중 어느 한 항에 있어서, 실질적으로 도 10a에 나타낸 바와 같은 DSC 프로파일을 특징으로 하는 결정형.
- 제32항 내지 제36항 중 어느 한 항에 있어서, 실질적으로 도 10b에 나타낸 바와 같은 TGA 프로파일을 특징으로 하는 결정형.
- 제32항 내지 제37항 중 어느 한 항에 있어서, 디클로로메탄 용매화물인 결정형.
- 제32항 내지 제38항 중 어느 한 항에 있어서, 단순 단사정계로 인덱스되는 단위 셀을 갖는 결정형.
- 제32항 내지 제39항 중 어느 한 항에 있어서, 약 5.541 Å의 a 값, 약 13.040 Å의 b 값, 및 약 40.818 Å의 c 값을 갖는 단위 셀을 갖는 결정형.
- 제32항 내지 제40항 중 어느 한 항에 있어서, 약 2947.6 Å3의 부피를 갖는 단위 셀을 갖는 결정형.
- 제32항 내지 제41항 중 어느 한 항에 있어서, 형태 C인 결정형.
- 제1항에 있어서, 5.3 ± 0.2, 8.7 ± 0.2, 및 26.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제43항에 있어서, 5.3 ± 0.2, 8.7 ± 0.2, 18.2 ± 0.2, 및 26.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제43항 또는 제44항에 있어서, 실질적으로 도 11에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제43항 내지 제45항 중 어느 한 항에 있어서, DSC에 의해 결정된 바와 같이 약 147℃에서 개시되는 흡열 피크를 특징으로 하는 결정형.
- 제43항 내지 제46항 중 어느 한 항에 있어서, 실질적으로 도 12a에 나타낸 바와 같은 DSC 프로파일을 특징으로 하는 결정형.
- 제43항 내지 제47항 중 어느 한 항에 있어서, 실질적으로 도 12b에 나타낸 바와 같은 TGA 프로파일을 특징으로 하는 결정형.
- 제43항 내지 제48항 중 어느 한 항에 있어서, 실질적으로 도 13에 나타낸 바와 같은 13C 고체 상태 NMR을 특징으로 하는 결정형.
- 제43항 내지 제49항 중 어느 한 항에 있어서, 무수인 결정형.
- 제43항 내지 제50항 중 어느 한 항에 있어서, 형태 D인 결정형.
- 제1항에 있어서, 5.8 ± 0.2, 17.9 ± 0.2, 및 18.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제52항에 있어서, 5.8±0.2, 17.9±0.2, 18.9±0.2, 및 20.7±0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제52항 또는 제53항에 있어서, 실질적으로 도 14에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제52항 내지 제54항 중 어느 한 항에 있어서, DSC에 의해 결정되는 바와 같이 약 171℃에서 개시되는 흡열 피크를 특징으로 하는 결정형.
- 제52항 내지 제55항 중 어느 한 항에 있어서, 실질적으로 도 15a에 나타낸 바와 같은 DSC 프로파일을 특징으로 하는 결정형.
- 제52항 내지 제56항 중 어느 한 항에 있어서, 실질적으로 도 15b에 나타낸 바와 같은 TGA 프로파일을 특징으로 하는 결정형.
- 제52항 내지 제57항 중 어느 한 항에 있어서, 무수인 결정형.
- 제52항 내지 제58항 중 어느 한 항에 있어서, 형태 E인 결정형.
- 제1항에 있어서, 3.8 ± 0.2, 9.5 ± 0.2, 및 16.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제60항에 있어서, 3.8 ± 0.2, 9.5 ± 0.2, 16.8 ± 0.2, 및 17.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제60항 또는 제61항에 있어서, 실질적으로 도 16에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제60항 내지 제62항 중 어느 한 항에 있어서, 용매화물인 결정형.
- 제60항 내지 제63항 중 어느 한 항에 있어서, 형태 F인 결정형.
- 제1항에 있어서, 3.4 ± 0.2, 21.2 ± 0.2, 및 21.9 ± 0.2도 2 세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제65항에 있어서, 3.4 ± 0.2, 21.2 ± 0.2, 21.9 ± 0.2, 및 22.4 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제65항 또는 제66항에 있어서, 실질적으로 도 17에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제65항 내지 제67항 중 어느 한 항에 있어서, 용매화물인 결정형.
- 제65항 내지 제68항 중 어느 한 항에 있어서, 형태 G인 결정형.
- 제1항에 있어서, 3.8 ± 0.2, 5.3 ± 0.2, 및 8.5 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제70항에 있어서, 3.8 ± 0.2, 5.3 ± 0.2, 8.5 ± 0.2, 및 15.9 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제70항 또는 제71항에 있어서, 실질적으로 도 18에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제70항 내지 제72항 중 어느 한 항에 있어서, 용매화물인 결정형.
- 제70항 내지 제73항 중 어느 한 항에 있어서, 형태 H인 결정형.
- 제1항에 있어서, 5.0 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제75항에 있어서, 5.0 ± 0.2, 15.9 ± 0.2, 16.8 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제75항 또는 제76항에 있어서, 실질적으로 도 19에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제75항 내지 제77항 중 어느 한 항에 있어서, 용매화물인 결정형.
- 제75항 내지 제78항 중 어느 한 항에 있어서, 형태 I인 결정형.
- 제1항에 있어서, 5.9 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제80항에 있어서, 5.9 ± 0.2, 12.7 ± 0.2, 17.4 ± 0.2, 및 18.8 ± 0.2도 2세타에서 피크를 갖는 XRPD 패턴을 특징으로 하는 결정형.
- 제80항 또는 제81항에 있어서, 실질적으로 도 20에 나타낸 바와 같은 XRPD 패턴을 특징으로 하는 결정형.
- 제80항 내지 제82항 중 어느 한 항에 있어서, DSC에 의해 결정된 바와 같이 약 164℃에서 개시되는 흡열 피크를 특징으로 하는 결정형.
- 제80항 내지 제83항 중 어느 한 항에 있어서, 실질적으로 도 21a에 나타낸 바와 같은 DSC 프로파일을 특징으로 하는 결정형.
- 제80항 내지 제84항 중 어느 한 항에 있어서, 실질적으로 도 21b에 나타낸 바와 같은 TGA 프로파일을 특징으로 하는 결정형.
- 제80항 내지 제85항 중 어느 한 항에 있어서, 형태 J인 결정형.
- 제1항 내지 제86항 중 어느 한 항에 있어서, 실질적으로 다른 다형 형태를 가 갖지 않는 결정형.
- 제1항 내지 제86항 중 어느 한 항에 있어서, 적어도 약 80%의 다형 순도를 갖는 결정형.
- 제1항 내지 제86항 중 어느 한 항에 있어서, 적어도 약 90%의 다형 순도를 갖는 결정형.
- 제1항 내지 제86항 중 어느 한 항에 있어서, 적어도 약 95%의 다형 순도를 갖는 결정형.
- 제1항 내지 제86항 중 어느 한 항에 있어서, 적어도 약 99%의 다형 순도를 갖는 결정형.
- 제1항 내지 제91항 중 어느 한 항의 결정형 및 약학적으로 허용가능한 담체, 희석제, 부형제, 또는 이들의 혼합물을 포함하는 약학 조성물.
- 당뇨병의 치료를 필요로 하는 환자에게 제92항의 약학 조성물을 투여하는 것을 포함하는, 당뇨병의 유형을 치료하는 방법.
- 제93항에 있어서, 당뇨병의 유형은 1형 당뇨병인 방법.
- 제93항에 있어서, 당뇨병의 유형은 2형 당뇨병인 방법.
- 제93항 내지 제95항 중 어느 한 항에 있어서, 약학 조성물은 경구 투여되는 것인 방법.
- 제93항 내지 제96항 중 어느 한 항에 있어서, 약학 조성물은 정제로서 투여되는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 최대 약 2000 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 약 100 mg 내지 약 1500 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 약 500 mg 내지 약 1000 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 약 800 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 800 mg 미만의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 약 500 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 약 300 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
- 제93항 내지 제97항 중 어느 한 항에 있어서, 환자는 약 100 mg의 {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산을 1일 1회 투여받는 것인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063035994P | 2020-06-08 | 2020-06-08 | |
| US63/035,994 | 2020-06-08 | ||
| PCT/US2021/036082 WO2021252309A1 (en) | 2020-06-08 | 2021-06-07 | Crystalline forms of {2-[3-cyclohexyl-3-(trans-4-propoxy- cyclohexyl)-ureido]-thiazol-5-ylsulfanyl} -acetic acid and and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20230048501A true KR20230048501A (ko) | 2023-04-11 |
Family
ID=78846441
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237000609A KR20230048501A (ko) | 2020-06-08 | 2021-06-07 | {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형 및 그의 용도 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20230219910A1 (ko) |
| EP (1) | EP4161639A4 (ko) |
| JP (1) | JP2023530785A (ko) |
| KR (1) | KR20230048501A (ko) |
| CN (1) | CN116056760A (ko) |
| AU (1) | AU2021289591A1 (ko) |
| CA (1) | CA3181665A1 (ko) |
| MX (1) | MX2022015524A (ko) |
| WO (1) | WO2021252309A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2014226292B2 (en) * | 2013-03-04 | 2018-10-04 | Vtv Therapeutics Llc | Solid compositions comprising a glucokinase activator and methods of making and using the same |
| CA3093025A1 (en) | 2018-06-12 | 2019-12-19 | Vtv Therapeutics Llc | Therapeutic uses of glucokinase activators in combination with insulin or insulin analogs |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005066145A1 (en) * | 2004-01-06 | 2005-07-21 | Novo Nordisk A/S | Heteroaryl-ureas and their use as glucokinase activators |
| PL2576524T3 (pl) * | 2010-05-26 | 2018-03-30 | Vtv Therapeutics Llc | Zastosowanie metforminy w skojarzeniu z aktywatorem glukokinazy i kompozycje zawierające metforminę i aktywator glukokinazy |
| EP2849776B1 (en) * | 2012-05-17 | 2021-04-21 | vTv Therapeutics LLC | Glucokinase activator compositions for the treatment of diabetes |
| JP6441828B2 (ja) * | 2013-03-04 | 2018-12-19 | ブイティーブイ・セラピューティクス・エルエルシー | 安定なグルコキナーゼ活性化剤組成物 |
| AU2014226292B2 (en) * | 2013-03-04 | 2018-10-04 | Vtv Therapeutics Llc | Solid compositions comprising a glucokinase activator and methods of making and using the same |
| CN109674752B (zh) * | 2016-12-15 | 2022-10-11 | 华领医药技术(上海)有限公司 | 葡萄糖激酶激活剂的口服制剂及其制备方法 |
-
2021
- 2021-06-07 WO PCT/US2021/036082 patent/WO2021252309A1/en unknown
- 2021-06-07 CN CN202180056233.1A patent/CN116056760A/zh active Pending
- 2021-06-07 AU AU2021289591A patent/AU2021289591A1/en active Pending
- 2021-06-07 CA CA3181665A patent/CA3181665A1/en active Pending
- 2021-06-07 EP EP21821691.9A patent/EP4161639A4/en active Pending
- 2021-06-07 KR KR1020237000609A patent/KR20230048501A/ko unknown
- 2021-06-07 MX MX2022015524A patent/MX2022015524A/es unknown
- 2021-06-07 JP JP2023519156A patent/JP2023530785A/ja active Pending
- 2021-06-07 US US18/000,908 patent/US20230219910A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CA3181665A1 (en) | 2021-12-16 |
| EP4161639A4 (en) | 2024-01-17 |
| JP2023530785A (ja) | 2023-07-19 |
| EP4161639A1 (en) | 2023-04-12 |
| WO2021252309A1 (en) | 2021-12-16 |
| AU2021289591A1 (en) | 2023-01-19 |
| US20230219910A1 (en) | 2023-07-13 |
| CN116056760A (zh) | 2023-05-02 |
| MX2022015524A (es) | 2023-03-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6114849B2 (ja) | プリン誘導体の結晶性形態 | |
| EP2989084B1 (en) | Crystal modifications of elobixibat | |
| CN110577534B (zh) | 苯甲酰氨基吡啶衍生物的盐及其在药物中的应用 | |
| KR20230048501A (ko) | {2-[3-사이클로헥실-3-(트랜스-4-프로폭시-사이클로헥실)-우레이도]-티아졸-5-일설파닐}-아세트산의 결정형 및 그의 용도 | |
| KR20160118204A (ko) | 2-하이드록시-6-((2-(1-이소프로필-1h-피라졸-5-일)피리딘-3-일)메톡시)벤즈알데하이드의 유리 염기의 결정성 다형체 | |
| EP2961734A1 (en) | Glycopyrrolate salts | |
| CA3150424A1 (en) | Solid state forms of (s)-2-(((s)-6,8-difluoro-1,2,3,4-tetrahydronaphthalen-2-yl)amino)-n-(1-(2-methyl-1-(neopentylamino)propan-2-yl)-1h-imidazol-4-yl)pentanamide and uses thereof | |
| CN116262741A (zh) | 作为突变型egfr抑制剂的化合物 | |
| US20230219909A1 (en) | Salts or co-crystals of {2-[3-cyclohexyl-3-(trans-4-propoxy-cyclohexyl)-ureido]-thiazol-5-ylsulfanyl}-acetic acid and uses thereof | |
| JP2024001167A (ja) | ノボビオシン類似体とプロリンとの共結晶形態 | |
| CN115385894A (zh) | 与吡啶酰基哌啶5-ht1f激动剂相关的组合物和方法 | |
| EP3453712B1 (en) | Diethylamine solvate of sodium-glucose linked transporter inhibitor, and preparation method and application thereof | |
| CN114127074A (zh) | 无定形乌帕拉尼单甲苯磺酸盐 | |
| TW202333676A (zh) | 吡唑並〔3,4-d〕嘧啶化合物之固體形式 | |
| KR20210134065A (ko) | 벤조티아졸 화합물의 약제학적 염, 다형체 및 이들의 제조 방법 | |
| TW202333694A (zh) | 稠環衍生物的晶型、其製備方法及其應用 | |
| TW202016092A (zh) | Otr抑制劑的晶型及其製備方法 |