KR20230027277A - 혈우병을 치료하기 위한 방법 및 조성물 - Google Patents
혈우병을 치료하기 위한 방법 및 조성물 Download PDFInfo
- Publication number
- KR20230027277A KR20230027277A KR1020237002631A KR20237002631A KR20230027277A KR 20230027277 A KR20230027277 A KR 20230027277A KR 1020237002631 A KR1020237002631 A KR 1020237002631A KR 20237002631 A KR20237002631 A KR 20237002631A KR 20230027277 A KR20230027277 A KR 20230027277A
- Authority
- KR
- South Korea
- Prior art keywords
- patient
- hemophilia
- pitusiran
- inhibitor
- qol
- Prior art date
Links
- 208000009292 Hemophilia A Diseases 0.000 title claims abstract description 88
- 208000031220 Hemophilia Diseases 0.000 title claims description 54
- 238000000034 method Methods 0.000 title claims description 51
- 239000000203 mixture Substances 0.000 title description 8
- 102100022641 Coagulation factor IX Human genes 0.000 claims abstract description 36
- 102100026735 Coagulation factor VIII Human genes 0.000 claims abstract description 36
- 101000911390 Homo sapiens Coagulation factor VIII Proteins 0.000 claims abstract description 36
- 208000009429 hemophilia B Diseases 0.000 claims abstract description 34
- 201000003542 Factor VIII deficiency Diseases 0.000 claims abstract description 31
- 230000008407 joint function Effects 0.000 claims abstract description 4
- 239000003112 inhibitor Substances 0.000 claims description 44
- 238000011282 treatment Methods 0.000 claims description 41
- 239000003814 drug Substances 0.000 claims description 19
- 238000004519 manufacturing process Methods 0.000 claims description 19
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 claims description 16
- 239000002953 phosphate buffered saline Substances 0.000 claims description 16
- 108010013773 recombinant FVIIa Proteins 0.000 claims description 11
- 230000006872 improvement Effects 0.000 claims description 10
- 238000003556 assay Methods 0.000 claims description 9
- 208000002193 Pain Diseases 0.000 claims description 7
- 210000004369 blood Anatomy 0.000 claims description 6
- 239000008280 blood Substances 0.000 claims description 6
- 239000003795 chemical substances by application Substances 0.000 claims description 6
- 208000006820 Arthralgia Diseases 0.000 claims description 5
- 108010076282 Factor IX Proteins 0.000 claims description 5
- 108010054218 Factor VIII Proteins 0.000 claims description 5
- 102000001690 Factor VIII Human genes 0.000 claims description 5
- 229960004222 factor ix Drugs 0.000 claims description 5
- 229960000301 factor viii Drugs 0.000 claims description 5
- 229940071643 prefilled syringe Drugs 0.000 claims description 4
- 206010023232 Joint swelling Diseases 0.000 claims description 3
- 208000034819 Mobility Limitation Diseases 0.000 claims description 3
- 208000018934 joint symptom Diseases 0.000 claims description 3
- 229940024790 prothrombin complex concentrate Drugs 0.000 claims description 2
- 102100023804 Coagulation factor VII Human genes 0.000 claims 1
- 108010023321 Factor VII Proteins 0.000 claims 1
- 230000003213 activating effect Effects 0.000 claims 1
- 229940012413 factor vii Drugs 0.000 claims 1
- 238000002560 therapeutic procedure Methods 0.000 abstract description 14
- 108091034117 Oligonucleotide Proteins 0.000 abstract description 5
- 150000001875 compounds Chemical class 0.000 abstract description 2
- 239000004019 antithrombin Substances 0.000 description 33
- 208000032843 Hemorrhage Diseases 0.000 description 29
- 208000034158 bleeding Diseases 0.000 description 28
- 231100000319 bleeding Toxicity 0.000 description 28
- 230000000740 bleeding effect Effects 0.000 description 28
- 230000000694 effects Effects 0.000 description 18
- 108010052295 fibrin fragment D Proteins 0.000 description 15
- 239000003154 D dimer Substances 0.000 description 14
- 108090000190 Thrombin Proteins 0.000 description 14
- 229960004072 thrombin Drugs 0.000 description 14
- 229940079593 drug Drugs 0.000 description 13
- 230000036541 health Effects 0.000 description 13
- 239000008194 pharmaceutical composition Substances 0.000 description 13
- RUPXJRIDSUCQAN-PQNNUJSWSA-N N-[1,3-bis[3-[3-[5-[(2R,3R,4R,5R,6R)-3-acetamido-4,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxypentanoylamino]propylamino]-3-oxopropoxy]-2-[[3-[3-[5-[(2R,3R,4R,5R,6R)-3-acetamido-4,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxypentanoylamino]propylamino]-3-oxopropoxy]methyl]propan-2-yl]-12-[(2R,4R)-4-hydroxy-2-methylpyrrolidin-1-yl]-12-oxododecanamide Chemical compound C[C@@H]1C[C@@H](O)CN1C(=O)CCCCCCCCCCC(=O)NC(COCCC(=O)NCCCNC(=O)CCCCO[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1NC(C)=O)(COCCC(=O)NCCCNC(=O)CCCCO[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1NC(C)=O)COCCC(=O)NCCCNC(=O)CCCCO[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1NC(C)=O RUPXJRIDSUCQAN-PQNNUJSWSA-N 0.000 description 11
- 229950002735 fitusiran Drugs 0.000 description 11
- 210000002381 plasma Anatomy 0.000 description 11
- 239000000243 solution Substances 0.000 description 10
- 230000009467 reduction Effects 0.000 description 9
- 230000008859 change Effects 0.000 description 7
- 230000003285 pharmacodynamic effect Effects 0.000 description 6
- 241000711549 Hepacivirus C Species 0.000 description 5
- 108091081021 Sense strand Proteins 0.000 description 5
- 230000000692 anti-sense effect Effects 0.000 description 5
- 210000004185 liver Anatomy 0.000 description 5
- 238000007726 management method Methods 0.000 description 5
- 239000002773 nucleotide Substances 0.000 description 5
- 125000003729 nucleotide group Chemical group 0.000 description 5
- 238000010254 subcutaneous injection Methods 0.000 description 5
- 239000007929 subcutaneous injection Substances 0.000 description 5
- BPYKTIZUTYGOLE-IFADSCNNSA-N Bilirubin Chemical compound N1C(=O)C(C)=C(C=C)\C1=C\C1=C(C)C(CCC(O)=O)=C(CC2=C(C(C)=C(\C=C/3C(=C(C=C)C(=O)N\3)C)N2)CCC(O)=O)N1 BPYKTIZUTYGOLE-IFADSCNNSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 238000013439 planning Methods 0.000 description 4
- 238000011321 prophylaxis Methods 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 241000282414 Homo sapiens Species 0.000 description 3
- MBLBDJOUHNCFQT-UHFFFAOYSA-N N-acetyl-D-galactosamine Natural products CC(=O)NC(C=O)C(O)C(O)C(O)CO MBLBDJOUHNCFQT-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 208000007536 Thrombosis Diseases 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000015271 coagulation Effects 0.000 description 3
- 238000005345 coagulation Methods 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 230000008451 emotion Effects 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 230000023597 hemostasis Effects 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 150000004713 phosphodiesters Chemical class 0.000 description 3
- 230000036470 plasma concentration Effects 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 230000002335 preservative effect Effects 0.000 description 3
- 238000012216 screening Methods 0.000 description 3
- 159000000000 sodium salts Chemical class 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 3
- 230000001052 transient effect Effects 0.000 description 3
- SXUXMRMBWZCMEN-UHFFFAOYSA-N 2'-O-methyl uridine Natural products COC1C(O)C(CO)OC1N1C(=O)NC(=O)C=C1 SXUXMRMBWZCMEN-UHFFFAOYSA-N 0.000 description 2
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 2
- 108010000437 Deamino Arginine Vasopressin Proteins 0.000 description 2
- 206010016077 Factor IX deficiency Diseases 0.000 description 2
- 108010049003 Fibrinogen Proteins 0.000 description 2
- 102000008946 Fibrinogen Human genes 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- OVRNDRQMDRJTHS-KEWYIRBNSA-N N-acetyl-D-galactosamine Chemical compound CC(=O)N[C@H]1C(O)O[C@H](CO)[C@H](O)[C@@H]1O OVRNDRQMDRJTHS-KEWYIRBNSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 108020004459 Small interfering RNA Proteins 0.000 description 2
- 108010000499 Thromboplastin Proteins 0.000 description 2
- 102000002262 Thromboplastin Human genes 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 230000001567 anti-fibrinolytic effect Effects 0.000 description 2
- 239000003146 anticoagulant agent Substances 0.000 description 2
- 229940127219 anticoagulant drug Drugs 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- FPUGCISOLXNPPC-IOSLPCCCSA-N cordysinin B Chemical group CO[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C2=NC=NC(N)=C2N=C1 FPUGCISOLXNPPC-IOSLPCCCSA-N 0.000 description 2
- 229960004397 cyclophosphamide Drugs 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 229940012952 fibrinogen Drugs 0.000 description 2
- 239000004023 fresh frozen plasma Substances 0.000 description 2
- 208000031169 hemorrhagic disease Diseases 0.000 description 2
- 230000006058 immune tolerance Effects 0.000 description 2
- 230000001506 immunosuppresive effect Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- 230000000306 recurrent effect Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 239000004055 small Interfering RNA Substances 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- PGOHTUIFYSHAQG-LJSDBVFPSA-N (2S)-6-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-4-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-1-[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2R)-2-[[(2S)-2-[[(2S)-2-[[2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-1-[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-amino-4-methylsulfanylbutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]propanoyl]pyrrolidine-2-carbonyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-methylpentanoyl]amino]acetyl]amino]-3-hydroxypropanoyl]amino]-4-methylpentanoyl]amino]-3-sulfanylpropanoyl]amino]-4-methylsulfanylbutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-hydroxybutanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-3-hydroxypropanoyl]amino]-3-hydroxypropanoyl]amino]-3-(1H-imidazol-5-yl)propanoyl]amino]-4-methylpentanoyl]amino]-3-hydroxybutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]-5-oxopentanoyl]amino]-3-hydroxybutanoyl]amino]-3-hydroxypropanoyl]amino]-3-carboxypropanoyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]-5-oxopentanoyl]amino]-3-phenylpropanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-oxobutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-4-carboxybutanoyl]amino]-5-oxopentanoyl]amino]hexanoic acid Chemical compound CSCC[C@H](N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](Cc1cnc[nH]1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](Cc1ccccc1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(O)=O PGOHTUIFYSHAQG-LJSDBVFPSA-N 0.000 description 1
- UUDVSZSQPFXQQM-GIWSHQQXSA-N (2r,3s,4r,5r)-2-(6-aminopurin-9-yl)-3-fluoro-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@]1(O)F UUDVSZSQPFXQQM-GIWSHQQXSA-N 0.000 description 1
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 1
- QPHRQMAYYMYWFW-FJGDRVTGSA-N 1-[(2r,3s,4r,5r)-3-fluoro-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]pyrimidine-2,4-dione Chemical compound O[C@]1(F)[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C=C1 QPHRQMAYYMYWFW-FJGDRVTGSA-N 0.000 description 1
- FPUGCISOLXNPPC-UHFFFAOYSA-N 2'-O-Methyladenosine Natural products COC1C(O)C(CO)OC1N1C2=NC=NC(N)=C2N=C1 FPUGCISOLXNPPC-UHFFFAOYSA-N 0.000 description 1
- RFCQJGFZUQFYRF-UHFFFAOYSA-N 2'-O-Methylcytidine Natural products COC1C(O)C(CO)OC1N1C(=O)N=C(N)C=C1 RFCQJGFZUQFYRF-UHFFFAOYSA-N 0.000 description 1
- OVYNGSFVYRPRCG-UHFFFAOYSA-N 2'-O-Methylguanosine Natural products COC1C(O)C(CO)OC1N1C(NC(N)=NC2=O)=C2N=C1 OVYNGSFVYRPRCG-UHFFFAOYSA-N 0.000 description 1
- RFCQJGFZUQFYRF-ZOQUXTDFSA-N 2'-O-methylcytidine Chemical group CO[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)N=C(N)C=C1 RFCQJGFZUQFYRF-ZOQUXTDFSA-N 0.000 description 1
- OVYNGSFVYRPRCG-KQYNXXCUSA-N 2'-O-methylguanosine Chemical group CO[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=C(N)NC2=O)=C2N=C1 OVYNGSFVYRPRCG-KQYNXXCUSA-N 0.000 description 1
- SXUXMRMBWZCMEN-ZOQUXTDFSA-N 2'-O-methyluridine Chemical group CO[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C=C1 SXUXMRMBWZCMEN-ZOQUXTDFSA-N 0.000 description 1
- BGTXMQUSDNMLDW-AEHJODJJSA-N 2-amino-9-[(2r,3s,4r,5r)-3-fluoro-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]-3h-purin-6-one Chemical compound C1=2NC(N)=NC(=O)C=2N=CN1[C@@H]1O[C@H](CO)[C@@H](O)[C@]1(O)F BGTXMQUSDNMLDW-AEHJODJJSA-N 0.000 description 1
- FIEYHAAMDAPVCH-UHFFFAOYSA-N 2-methyl-1h-quinazolin-4-one Chemical compound C1=CC=C2NC(C)=NC(=O)C2=C1 FIEYHAAMDAPVCH-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- PJWBTAIPBFWVHX-FJGDRVTGSA-N 4-amino-1-[(2r,3s,4r,5r)-3-fluoro-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]pyrimidin-2-one Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@](F)(O)[C@H](O)[C@@H](CO)O1 PJWBTAIPBFWVHX-FJGDRVTGSA-N 0.000 description 1
- SLXKOJJOQWFEFD-UHFFFAOYSA-N 6-aminohexanoic acid Chemical compound NCCCCCC(O)=O SLXKOJJOQWFEFD-UHFFFAOYSA-N 0.000 description 1
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 1
- 108010082126 Alanine transaminase Proteins 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 102100022977 Antithrombin-III Human genes 0.000 description 1
- 108010003415 Aspartate Aminotransferases Proteins 0.000 description 1
- 102000004625 Aspartate Aminotransferases Human genes 0.000 description 1
- 101100422770 Caenorhabditis elegans sup-1 gene Proteins 0.000 description 1
- 206010013839 Duodenal ulcer haemorrhage Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 206010014522 Embolism venous Diseases 0.000 description 1
- 206010014935 Enzyme abnormality Diseases 0.000 description 1
- 206010017577 Gait disturbance Diseases 0.000 description 1
- 208000007882 Gastritis Diseases 0.000 description 1
- 208000002927 Hamartoma Diseases 0.000 description 1
- 208000024659 Hemostatic disease Diseases 0.000 description 1
- 206010019670 Hepatic function abnormal Diseases 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 206010062016 Immunosuppression Diseases 0.000 description 1
- 206010022095 Injection Site reaction Diseases 0.000 description 1
- 206010022061 Injection site erythema Diseases 0.000 description 1
- 206010022086 Injection site pain Diseases 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 208000012659 Joint disease Diseases 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- 206010067125 Liver injury Diseases 0.000 description 1
- 208000033375 Moderate hemophilia A Diseases 0.000 description 1
- 206010028309 Muscle haemorrhage Diseases 0.000 description 1
- OVRNDRQMDRJTHS-CBQIKETKSA-N N-Acetyl-D-Galactosamine Chemical compound CC(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@H](O)[C@@H]1O OVRNDRQMDRJTHS-CBQIKETKSA-N 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000233805 Phoenix Species 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 108010094028 Prothrombin Proteins 0.000 description 1
- 102100027378 Prothrombin Human genes 0.000 description 1
- IWUCXVSUMQZMFG-AFCXAGJDSA-N Ribavirin Chemical compound N1=C(C(=O)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 IWUCXVSUMQZMFG-AFCXAGJDSA-N 0.000 description 1
- 101150026876 SERPINC1 gene Proteins 0.000 description 1
- 208000026552 Severe hemophilia A Diseases 0.000 description 1
- 108090000340 Transaminases Proteins 0.000 description 1
- 102000003929 Transaminases Human genes 0.000 description 1
- 108010074506 Transfer Factor Proteins 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229960002684 aminocaproic acid Drugs 0.000 description 1
- 239000003708 ampul Substances 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 239000000504 antifibrinolytic agent Substances 0.000 description 1
- 229940082620 antifibrinolytics Drugs 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000023555 blood coagulation Effects 0.000 description 1
- 230000001364 causal effect Effects 0.000 description 1
- 210000004970 cd4 cell Anatomy 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- 239000000701 coagulant Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 238000000586 desensitisation Methods 0.000 description 1
- 229960004281 desmopressin Drugs 0.000 description 1
- NFLWUMRGJYTJIN-NXBWRCJVSA-N desmopressin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSCCC(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(N)=O)=O)CCC(=O)N)C1=CC=CC=C1 NFLWUMRGJYTJIN-NXBWRCJVSA-N 0.000 description 1
- 229960002845 desmopressin acetate Drugs 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- PYLIXCKOHOHGKQ-UHFFFAOYSA-L disodium;hydrogen phosphate;heptahydrate Chemical compound O.O.O.O.O.O.O.[Na+].[Na+].OP([O-])([O-])=O PYLIXCKOHOHGKQ-UHFFFAOYSA-L 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002594 fluoroscopy Methods 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000024924 glomerular filtration Effects 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 208000031209 hemophilic arthropathy Diseases 0.000 description 1
- 231100000234 hepatic damage Toxicity 0.000 description 1
- 208000027700 hepatic dysfunction Diseases 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 238000002650 immunosuppressive therapy Methods 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 230000037231 joint health Effects 0.000 description 1
- 208000017169 kidney disease Diseases 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000008818 liver damage Effects 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 238000007449 liver function test Methods 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 125000003835 nucleoside group Chemical group 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 238000002616 plasmapheresis Methods 0.000 description 1
- 210000003240 portal vein Anatomy 0.000 description 1
- 238000013105 post hoc analysis Methods 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- 238000009101 premedication Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 239000003805 procoagulant Substances 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000002250 progressing effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 229940039716 prothrombin Drugs 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000010223 real-time analysis Methods 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000009256 replacement therapy Methods 0.000 description 1
- 229960000329 ribavirin Drugs 0.000 description 1
- HZCAHMRRMINHDJ-DBRKOABJSA-N ribavirin Natural products O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1N=CN=C1 HZCAHMRRMINHDJ-DBRKOABJSA-N 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- BBMHARZCALWXSL-UHFFFAOYSA-M sodium dihydrogenphosphate monohydrate Chemical compound O.[Na+].OP(O)([O-])=O BBMHARZCALWXSL-UHFFFAOYSA-M 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- GYDJEQRTZSCIOI-LJGSYFOKSA-N tranexamic acid Chemical compound NC[C@H]1CC[C@H](C(O)=O)CC1 GYDJEQRTZSCIOI-LJGSYFOKSA-N 0.000 description 1
- 229960000401 tranexamic acid Drugs 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 208000004043 venous thromboembolism Diseases 0.000 description 1
- 108010047303 von Willebrand Factor Proteins 0.000 description 1
- 230000036642 wellbeing Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/713—Double-stranded nucleic acids or oligonucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0021—Intradermal administration, e.g. through microneedle arrays, needleless injectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Rheumatology (AREA)
- Biochemistry (AREA)
- Physical Education & Sports Medicine (AREA)
- Immunology (AREA)
- Dermatology (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
본 개시는 혈우병 A 및 혈우병 B 환자의 삶의 질 및 관절 기능을 개선하기 위한 신규 요법으로서 이중가닥 올리고뉴클레오티드 화합물을 사용하는 것을 제공한다.
Description
관련 출원에 대한 상호 참조
본 출원은 2020년 6월 22일에 출원된 미국 가출원 63/042,390호에 대한 우선권을 주장하며, 그 개시 내용은 전체가 본원에 참조로 포함된다.
서열 목록
본 출원에는 ASCII 형식으로 전자 제출되었고 그 전체가 본원에 참조로 포함되는 서열 목록이 포함된다. 2021년 6월 21일자로 생성된 상기 ASCII 사본의 파일명은 N022548.WO080_SL.txt이고 크기는 774 바이트이다.
정상적인 지혈의 유지는 트롬빈이 중심 역할을 하는, 동시에 발생하는 응고 촉진 및 항응고 과정의 조절 조합에 의존한다. 혈우병 A 및 B는 신체가 혈액 응고를 제어할 수 없는 것을 특징으로 하는 유전성 출혈 장애이다. 이는 각각 VIII 인자 및 IX 인자의 결핍으로 인해 발생한다. 혈우병 A 및 B에서의 출혈은 트롬빈 생성이 불충분하여 발생한다(문헌[Peyvandi et al., Lancet (2016) 388(10040):187-97]). 효과적인 치료 없이는, 혈우병 환자는 재발성 출혈을 경험하며, 이는 만성 혈우병성 관절염 및 상당한 통증으로 인해 주요 장애를 초래하고 생명을 위협할 수 있다(문헌[Pipe et al., Haemophilia (2007) 13 Suppl 4:1-16]).
치료의 발전에도 불구하고 모든 혈우병 인구에 대해 충족되지 않은 상당한 필요성과 관리 문제가 지속적으로 존재한다. VIII 인자 또는 IX 인자를 사용한 대체 요법에 기반한 예방은 혈우병 관리의 초석으로 간주되지만 이에는 상당한 한계점이 있다. 예를 들어, 예방을 위한 인자 대체 주사는 부담스럽고 비실용적이며, 주당 다수의 정맥내 주입을 필요로 하는 경우가 많다(문헌[Peyvandi, supra; Ljung and Andersson, Br J Haematol. (2015) 169(6):777-86; Srivastava et al., Haemophilia (2013) 19(1):e1-47; Bauer, Am J Manag Care (2015) 21(6 Suppl):S112-22; Mannucci and Franchini, Blood Transfus. (2013) 11(Suppl 4):s77-81]). 인자 대체는 또한 정맥 접근의 어려움 및 감염 위험으로 인해 제한적이다(문헌[Balkaransingh and Young, Ther Adv Hematol. (2018) 9(2):49-61; Valentino et al., Blood Rev. (2011) 25(1):11-5]). 전달 인자 대체의 한계로 인해 예방 치료에 대한 최초의 접근 없이 전 세계 혈우병 인구의 상당수가 발생한다(문헌[Hemophilia, W.F.O. Treatment Safety and Supply. 2020]).
또한, 인자 대체 제품으로의 치료는 억제성 동종항체의 발생을 야기하여 인자 치료를 비효과적으로 만들 수 있다(문헌[Morfini et al., Haemophilia (2007) 13(5):606-12]). 일반적으로 아동기에 발생하는 이러한 억제인자는 치료 옵션을 제한하고 혈우병의 예후를 급격히 악화시킨다. 더욱이, 지속적 억제인자를 보유한 환자는 일반적으로 억제인자를 보유하지 않은 환자와 비교할 때 삶의 질이 더 낮고, 관절 질환이 더 심각하며, 수술 위험이 더 크고, 혈우병 관련 출혈 합병증으로 인한 사망 위험이 더 높은 것을 포함하여 사망률이 더 높다(문헌[Morfini, supra; Oladapo et al., Orphanet J Rare Dis. (2018) 13(1):198]). 지속적인 억제인자를 보유한 개체에 대한 현재의 치료 전략에는 면역 관용 유도(ITI), 및 활성화 프로트롬빈 복합 농축물(aPCC) 및 재조합 활성화 인자 VII(rFVIIa)와 같은 우회제(BPA)를 사용한 예방이 포함된다(문헌[Benson et al., Eur J Haematol. (2012) 88(5):371-79; Collins et al., Br J Haematol. (2013) 160(2):153-70; Kempton et al., Blood (2014) 124(23):3365-72; Astermark et al., Haemophilia (2007) 13(1):38-45; Eichinger et al., Eur J Clin Invest. (2009) 39(8):707-13]).
재발성 출혈을 예방하고 혈우병 환자의 전반적인 삶의 질을 향상시키는 치료제 및 치료법을 개발해야 하는 시급하고 충족되지 않은 필요성이 남아 있다.
본 개시는 혈우병 환자를 치료하기 위한 방법 및 조성물을 제공한다. 일 양태에서, 본 개시는 혈우병 환자(예를 들어 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자)의 관절 기능을 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 용량당 40 내지 90 mg으로 투여(예를 들어 피하로 투여)하는 단계를 포함하는 방법을 제공한다. 일부 구현예에서, 치료는 보행의 어려움을 감소시키거나 이동성을 증가시킨다.
일 양태에서, 본 개시는 혈우병 환자(예를 들어 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자)의 관절 증상(예를 들어 관절 부종, 움직임 통증, 및 관절 통증)을 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 용량당 40 내지 90 mg으로 투여(예를 들어 피하로 투여)하는 단계를 포함하는 방법을 제공한다.
일 양태에서, 본 개시는 혈우병 환자(예를 들어 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자)에서 환자자기평가결과(PRO)를 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 용량당 40 내지 90 mg으로 투여(예를 들어 피하로 투여)하는 단계를 포함하는 방법을 제공한다. 일부 구현예에서, PRO는 하나 이상의 삶의 질(QoL) 영역에서 개선된다.
일 양태에서, 본 개시는 혈우병 환자(예를 들어 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자)의 QoL을 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 용량당 40 내지 90 mg으로 투여(예를 들어 피하로 투여)하는 단계를 포함하고, QoL은 하나 이상의 삶의 질(QoL) 영역에서 개선되는, 방법을 제공한다.
일부 구현예에서, 하나 이상의 QoL 영역은 QoL 설문지(예를 들어 성인을 위한 혈우병 삶의 질 설문지(Haem-A-QoL) 내의 영역이다. 추가 구현예에서, 치료받는 환자는 설문지의 점수(예를 들어 총점, 스포츠 및 레저 영역 점수, 신체 건강 영역 점수) 중 하나 이상에서 7단위 이상(예를 들어 8단위 이상, 9단위 이상, 또는 10단위 이상)의 감소로 표시되는 임상적으로 의미 있는 개선을 경험한다.
일부 구현예에서, 환자는 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B(선천성 인자 VIII 또는 인자 IX 결핍)가 있는 성인 또는 12세 이상의 청소년 환자이다.
일부 구현예에서, 환자는 혈우병 A가 있다. 추가 구현예에서, 환자는 인자 VIII 대체물 또는 우회제(BPA; 예를 들어 aPCC 또는 rFVIIa)로 치료받은 적이 있다. 특정 구현예에서, 환자는 억제인자가 있다(예를 들어 억제인자의 수준은 베데스다 억제인자 분석법에 따른 측정시 0.6 BU/mL를 초과함). 다른 구현예에서, 환자는 억제인자가 없다.
일부 구현예에서, 환자는 혈우병 B가 있다. 추가 구현예에서, 환자는 인자 IX 대체물 또는 BPA(예를 들어 aPCC 또는 rFVIIa)로 치료받은 적이 있다. 특정 구현예에서, 환자는 억제인자가 있다(예를 들어 억제인자의 수준은 베데스다 억제인자 분석법에 따른 측정시 0.6 BU/mL를 초과함). 다른 구현예에서, 환자는 억제인자가 없다.
일부 구현예에서, 환자는 용량당 50 mg의 피투시란의 복수 용량 또는 용량당 80 mg의 피투시란의 복수 용량으로 치료받는다. 일부 구현예에서, 피투시란은 4주마다 1회 또는 월 1회 환자에게 투여된다. 일부 구현예에서, 피투시란은 인산염 완충 식염수(pH 7) 중 50 내지 200 mg/mL, 임의로 100 mg/mL로 제공된다.
또한 본 개시는 본 치료 방법에 사용하기 위한 제조 물품을 제공한다. 일부 구현예에서, 제조 물품은 0.8 mL의 인산염 완충 식염수(pH 7)에 80 mg의 피투시란을 함유하는 일회용 바이알이다. 다른 구현예에서, 제조 물품은 0.8 mL의 인산염 완충 식염수(pH 7)에 80 mg의 피투시란을 함유하는 일회용 사전충전형 시린지이다.
본 개시는 또한 본 치료 방법에서 사용하기 위한 피투시란 뿐만 아니라 본 치료 방법에서 혈우병을 치료하기 위한 약제의 제조를 위한 피투시란의 용도를 제공한다.
본 발명의 기타 특징, 목적, 및 이점은 하기 상세한 설명에 명백히 나타나 있다. 그러나, 상세한 설명이 본 발명의 구현예 및 양태를 나타내더라도, 이를 제한하는 것은 아니며 단지 예시로서 제공됨을 인지해야 한다. 본 발명의 범주 내에서의 다양한 변경 및 변형은 상세한 설명으로부터 당업자에게 명백할 것이다.
도 1은 피투시란의 확장된 구조식, 화학식, 및 분자량을 나타낸 것이다.
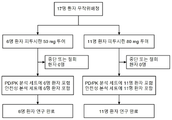
도 2는 본원에 기술된 피투시란 임상 연구의 설계를 보여주는 CONSORT 다이어그램이다.
도 3a 및 3b는 용량군별로 참여자당 시간 경과에 따른 D-dimer(μg/mL) 수준을 나타낸 것이다. A: 50 mg 용량군 B: 80 mg 용량군
도 4a는 매월 피투시란을 투여받는 억제인자가 존재하는 혈우병 A 또는 B 환자에서 기준선 대비 피투시란의 평균(평균[SEM]의 ±표준오차) 항트롬빈(AT) 활성을 나타낸 그래프이다. MDI: 억제인자의 다회 용량.
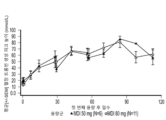
도 4b는 50 mg 및 80 mg 용량군의 환자에서 시간 경과에 따른 혈장 트롬빈 생성 피크 높이(nmol/L)의 평균(±SEM)을 나타낸 그래프이다.
도 5는 억제인자가 존재하는 혈우병 A 또는 B 환자에서 AT 감소와 관련된 트롬빈 생성의 사후 분석을 나타낸 것이다. 모든 환자에 대해 각 시점에서 AT 수준 및 해당 트롬빈 생성 측정값을 기록하였다. 제공가능한 모든 트롬빈 생성값은 기준선 대비 AT 활성 수준과 관련된 것으로 AT 저하 사분위수로 구간화하였다. 박스의 중앙선은 중앙값을 나타내고 박스의 위쪽과 아래쪽은 사분위수 범위를 나타낸다. 최소값과 최대값은 막대(bar)로 표시되어 있다(이상값 제외). 건강한 지원자 데이터(문헌[Pasi et al., N Engl J Med. (2017) 377(9):819-28])를 참조로 사용하였다.
도 2는 본원에 기술된 피투시란 임상 연구의 설계를 보여주는 CONSORT 다이어그램이다.
도 3a 및 3b는 용량군별로 참여자당 시간 경과에 따른 D-dimer(μg/mL) 수준을 나타낸 것이다. A: 50 mg 용량군 B: 80 mg 용량군
도 4a는 매월 피투시란을 투여받는 억제인자가 존재하는 혈우병 A 또는 B 환자에서 기준선 대비 피투시란의 평균(평균[SEM]의 ±표준오차) 항트롬빈(AT) 활성을 나타낸 그래프이다. MDI: 억제인자의 다회 용량.
도 4b는 50 mg 및 80 mg 용량군의 환자에서 시간 경과에 따른 혈장 트롬빈 생성 피크 높이(nmol/L)의 평균(±SEM)을 나타낸 그래프이다.
도 5는 억제인자가 존재하는 혈우병 A 또는 B 환자에서 AT 감소와 관련된 트롬빈 생성의 사후 분석을 나타낸 것이다. 모든 환자에 대해 각 시점에서 AT 수준 및 해당 트롬빈 생성 측정값을 기록하였다. 제공가능한 모든 트롬빈 생성값은 기준선 대비 AT 활성 수준과 관련된 것으로 AT 저하 사분위수로 구간화하였다. 박스의 중앙선은 중앙값을 나타내고 박스의 위쪽과 아래쪽은 사분위수 범위를 나타낸다. 최소값과 최대값은 막대(bar)로 표시되어 있다(이상값 제외). 건강한 지원자 데이터(문헌[Pasi et al., N Engl J Med. (2017) 377(9):819-28])를 참조로 사용하였다.
본 발명은, 억제인자 유무와 관련 없이, 혈우병 A(선천성 인자 VIII 결핍) 또는 혈우병 B(선천성 인자 IX 결핍)와 같은 혈우병이 있는 성인 및 청소년 환자(12세 이상)에서 출혈 에피소드의 빈도를 예방하거나 감소시키는 일상적 예방요법을 위해 피투시란을 사용하는 방법을 특징으로 한다. 이러한 방법은 관절 부종 및/또는 관절 통증을 감소시키고, 관절 기능을 개선하며, 환자의 삶의 질을 향상시킨다. 특정 구현예에서, 본 방법은 신체 건강과 관련된 것과 같은 환자의 삶의 질 점수를 향상시킨다.
억제인자가 존재하는 혈우병 A 또는 B 환자는 이전에 투여받은 인자(예를 들어 혈우병 A 환자의 경우 인자 VIII 또는 혈우병 B 환자의 경우 인자 IX)에 대한 동종항체가 발생한 환자를 지칭한다. 억제인자가 존재하는 혈우병 A 또는 B 환자는 대체 응고인자 요법에 불응성일 수 있다. 억제인자가 존재하지 않는 환자는 이러한 동종항체가 없는 환자를 지칭한다. 본 치료 방법은 억제인자가 존재하거나 존재하지 않는 혈우병 A 환자뿐만 아니라 억제인자가 존재하거나 존재하지 않는 혈우병 B 환자에게도 유익하다.
I.
피투시란 약학적 조성물
피투시란의 구조는 본원에 제공된다. 피투시란은 간에서 AT3 mRNA를 표적으로 하는 트리-안테너리(tri-antennary) N-아세틸-갈락토사민(GalNAc) 리간드에 공유 연결된, 합성, 화학적으로 변형된 이중가닥 소간섭 RNA(siRNA) 올리고뉴클레오티드로, 항트롬빈의 합성을 억제한다. 예를 들어, 문헌[Pasi, supra.] 참조. 항트롬빈은 SERPINC1 유전자에 의해 암호화된다. 피투시란의 각 가닥에 있는 뉴클레오시드는 3'-5' 포스포디에스테르 연결을 통해 연결되어 올리고뉴클레오티드의 당-인산 백본을 형성한다.
센스 가닥 및 안티센스 가닥은 각각 21개 및 23개의 뉴클레오티드를 함유한다. 센스 가닥의 3'-말단은 포스포디에스테르 연결을 통해 GalNAc 함유 모이어티(L96으로 지칭됨)에 접합된다. 센스 가닥은 5' 말단에 두 개의 연속적인 포스포로티오에이트 연결을 함유한다. 안티센스 가닥은 4개의 포스포로티오에이트 연결을 함유하며, 3' 말단에 2개, 5' 말단에 2개가 있다. 센스 가닥의 21개 뉴클레오티드는 안티센스 가닥의 상보적인 21개 뉴클레오티드와 혼성화하여 21개의 뉴클레오티드 염기쌍 및 안티센스 가닥의 3' 말단에 2개의 염기 오버행을 형성한다. 또한 U.S. Pat. 9,127,274, US20170159053, 및 WO 2019/014187 참조.
피투시란의 2개의 뉴클레오티드 가닥은 다음과 같다:
센스 가닥: 5’Gf-ps-Gm-ps-Uf-Um-Af-Am-Cf-Am-Cf-Cf-Af-Um-Uf-Um-Af-Cm-Uf-Um-Cf-Am-Af-L96 3’(서열번호 1), 및
안티센스 가닥: 5’ Um-ps-Uf-ps-Gm-Af-Am-Gf-Um-Af-Am-Af-Um-Gm-Gm-Uf-Gm-Uf-Um-Af-Am-Cf-Cm-ps-Am-ps-Gm 3’(서열번호 2),
여기서,
Af = 2'-플루오로아데노신
Cf = 2'-플루오로시티딘
Gf = 2'-플루오로구아노신
Uf = 2'-플루오로우리딘
Am = 2'-O-메틸아데노신
Cm = 2'-O-메틸시티딘
Gm = 2'-O-메틸구아노신
Um = 2'-O-메틸우리딘
"-"(하이픈) = 3'-5' 포스포디에스테르 연결 나트륨 염
"-ps-" = 3'-5' 포스포로티오에이트 연결 나트륨 염이고,
L96은 다음과 같은 화학식을 갖는다:
[화학식 I]
피투시란의 확장된 구조식, 분자식, 및 분자량을 도 1에 나타내었다.
본 치료 방법에 사용하기 위해, 피투시란은, 피투시란 및 약학적으로 허용가능한 부형제를 포함하는 약학적 조성물로 제공될 수 있다. 특정 구현예에서, dsRNA 화합물은 나트륨 염 형태이다.
일부 구현예에서, 피투시란은 50 내지 200 mg/mL(예를 들어, 50 내지 150 mg/mL, 80 내지 110 mg/mL, 또는 90 내지 110 mg/mL) 농도의 수용액으로 제공된다. 본원에서 사용되는 바와 같이, 인용된 범위 및 값의 중간값도 본 개시의 일부인 것으로 의도된 것이다. 또한, 인용된 값들 중 임의의 조합을 상한치 및/또는 하한치로서 사용하는 값의 범위가 포함되는 것으로 의도된 것이다. 추가 구현예에서, 약학적 조성물은 50, 75, 100, 125, 150, 또는 200 mg/mL 농도의 피투시란을 포함한다.
달리 나타내지 않는 한, 본 개시에 인용된 피투시란 중량은 피투시란 유리산(활성 모이어티)의 중량이다. 예를 들어, 100 mg/mL 피투시란은 mL당 100 mg의 피투시란 유리산(활성 물질인 피투시란 나트륨 106 mg에 해당)을 의미한다.
일부 구현예에서, 약학적 조성물은 인산염 완충 식염수에 피투시란을 포함한다. 용액 중 인산염 농도는 1 내지 10 mM(예를 들어, 2, 3, 4, 5, 6, 7, 8, 또는 9 mM)일 수 있고, pH는 6.0~8.0일 수 있다. 본원의 약학적 조성물은 EDTA와 같은 보존제를 포함할 수 있다. 대안적으로, 약학적 조성물은 보존제를 포함하지 않는다. 특정 구현예에서, 피투시란 약학적 조성물은 보존제가 없고 5 mM 인산 완충 식염수(PBS) 용액의 1 mL당 100 mg의 피투시란을 포함하거나, 이로 구성되거나, 본질적으로 이로 구성된다. PBS 용액은 염화나트륨, 제2인산나트륨(7수화물), 및 제1인산나트륨(1수화물)으로 구성된다. 수산화나트륨 용액 및 희석된 인산을 사용하여 조성물의 pH를 7.0으로 조정할 수 있다.
약학적 조성물은 40 내지 100 mg 피투시란(예를 들어 50 mg 또는 80 mg)을 함유하는 각각의 용기와 함께 일회용 용기(예를 들어, 바이알, 앰플, 시린지, 또는 주사기)로 제공될 수 있다. 피투시란은 용기에 고체 형태로 제공될 수 있고, 사용 전에 수용액(예를 들어 PBS)에서 재구성될 수 있으며, 재구성된 용액은 50 내지 150 mg/mL(예를 들어, 100 mg/mL) 피투시란을 함유한다. 일부 구현예에서, 피투시란은 일회용 유리 바이알 또는 일회용 사전충전형 시린지(예를 들어, 안전 시스템이 있는 것)에 나트륨 형태로 제공된다. 추가 구현예에서, 각각의 바이알 또는 시린지는 0.8 mL의 5 mM 인산염 완충 식염수 용액(pH 7.0)에 80 mg의 피투시란을 함유하고; 용액은 피하 주사를 통해 환자에게 투여된다. 용액은 2℃ 내지 30℃(예를 들어 2℃ 내지 8℃)에서 보관할 수 있다.
특정 구현예에서, 피하 주사용 피투시란 조성물은 pH 7.0에서 0.64 mM NaH2PO4, 4.36 mM Na2HPO4, 및 84 mM NaCl을 갖는 5 mM 인산염 완충 식염수에 피투시란을 함유한다. 특정 구현예에서, 피하 주사용 피투시란 용액의 조성은 하기 표 1에 제공된다:
II.
피투시란의 치료적 용도
피투시란은 항트롬빈(AT)의 간 생성을 억제할 수 있다. 항응고제로서의 역할에서 AT는 트롬빈 생성을 직접적으로 표적화하거나 비복합 FXa를 비활성화하여 결과적으로 트롬빈 생성을 감소시킴으로써 지혈을 조절한다(문헌[Quinsey et al., Int J Biochem Cell Biol. (2004) 36(3):386-9]). 피투시란은 지혈 장애가 있는 환자를 치료하는 데 사용될 수 있다.
예를 들어, 피투시란은 출혈 에피소드의 빈도를 예방하거나 줄이는 일상적 예방요법을 위해 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자를 치료하는 데 사용될 수 있다. 특정 구현예에서, 피투시란은 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B(선천성 인자 VIII 또는 인자 IX 결핍)가 있는 성인 및 청소년 환자(12세 이상)를 치료하는 데 사용된다.
본 방법은 이를 필요로 하는 혈우병 환자(예를 들어, 혈우병 A 또는 혈우병 B 환자)에게 치료적 유효량의 피투시란을 투여하는 단계를 포함한다. "치료적 유효량"은 환자가 목적하는 임상 평가변수를 달성하는 데 도움이 되는 피투시란의 양을 의미한다. 목적하는 임상 평가변수는 예를 들어 연간 출혈률(ABR)의 감소(예를 들어, 10, 20, 30, 40, 50, 60, 70, 80, 90, 또는 100% 초과)일 수 있다. 목적하는 임상 평가변수는 환자의 항트롬빈 수준을 정상 수준(예를 들어 약 64 내지 210 nM)으로 감소시키는 것일 수 있다.
목적하는 임상 평가변수는 또한 하기에서 추가로 설명하는 바와 같이 개선된 환자자기평가결과(PRO)일 수 있다. 일부 구현예에서, 치료 효능은 유효하고 신뢰할 수 있는 혈우병 특이적 PRO 수단, 예를 들어 성인을 위한 혈우병 삶의 질 설문지(문헌[“Haem-A-QoL”; von Mackensen et al., Haematologica (2005) 90(s2):115-6, Abstract 0290; Wyrwich et al., Haemophilia (2015) 21(5):578-84])에 기초하여 환자에 의해 평가되는 질환 중증도의 감소에 의해 측정될 수 있다. 예를 들어, 적절한 척도를 사용하여 측정된 질환 중증도의 감소를 야기하는 임의의 긍정적인 변화는 본원에 기재된 바와 같은 약학적 조성물을 사용한 적절한 치료를 나타낸다.
혈우병은 관련 증상, 기능 제한, 및 치료 부담을 통해 환자의 건강 관련 삶의 질(HRQoL)에 직접적인 영향을 미친다. HRQoL 개선은 혈우병 질환 관리의 중요한 측면이다. 본 방법은 잘 고안된 상세한 설문지에 의해 확인된 바와 같이 환자의 HRQoL을 개선한다. 예를 들어, 성인 환자(17세 이상, 예를 들어, 18세 이상)의 HRQoL은 설문지 Hemofilia-QoL, Haemophila Well-Being Index, HAEMO-QoL-A, Haem-A-QoL, 및 EuroQol 5-Dimensions(EQ-5D)(EuroQol Group, 문헌[Health Policy (1990) 16(3):199-208])을 통해 측정될 수 있다. 청소년 환자(12세 이상 내지 17세)의 HRQoL은 예를 들어 십대를 위한 혈우병 삶의 질 설문지(Haemo-QoL)를 통해 측정될 수 있다. 예를 들어, 문헌[Bullinger et al., Value Health. (2009) 12(5):808-20; 및 Remor, Int J Behav Med. (2013) 20(4):609-17] 참조.
일부 구현예에서, 본 치료는 하나 이상의 QoL 영역(예를 들어, 혈우병 특이적 QoL 영역)에서 환자의 삶의 질을 향상시킨다. 이러한 QoL 영역에는 예를 들어 신체 건강, 감정, 자아관, 스포츠 및 레저, 직장 및 학교, 혈우병 관리, 치료, 미래, 가족 계획, 및/또는 파트너십 및 성에 관련된 영역이 포함된다. 이러한 영역의 개선은 환자자기평가결과(PRO)로 평가할 수 있으며 설문지의 도움을 받을 수 있다. 예를 들어, 이러한 영역의 개선은 환자가 담당 의사에게 전달할 수 있고/있거나 QoL 설문지로 점수를 매길 수 있다.
특정 구현예에서, 성인 환자의 HRQoL은 Haem-A-QoL의 점수에 의해 측정된다. 예를 들어, 문헌[von Mackensen et al., Value in Health. (2005) 8(6):A127; von Mackensen et al., J Thrombosis and Haemostasis. (2005) 3(Sup1):P0813; von Mackensen and Gringeri, “Quality of Life in Hemophilia” In: Handbook of Disease Burdens and Quality of Life Measures. Heidelberg: Springer; 2009, pp.1910-1; 및 Bullinger et al., Value in Health. (2009) 12(5):808-20; Wyrwich, supra.] 참조. Haem-A-QoL 설문지에는 신체 건강(5개 항목), 감정(4개 항목), 자기관(5개 항목), 스포츠 및 레저(5개 항목), 직장 및 학교(4개 항목), 혈우병 관리(3개 항목), 치료(8개 항목), 미래(5개 항목), 가족 계획(4개 항목), 및 파트너십 및 성(3개 항목)을 포함하여 10개 영역에 관여하는 46개 항목을 포함한다.
모든 Haem-A-QoL 항목은 5점 빈도 척도(1 = 전혀 그렇지 않음, 2 = 드물게, 3 = 가끔, 4 = 자주, 및 5 = 항상)에 따라 측정된다. 또한 참여자에게 질문이 적용되지 않는 경우 "스포츠 및 레저", "직장 및 학교" 및 "가족 계획" 영역에 대해 "해당 없음" 응답 선택이 가능하다. 또한 Haem-A-QoL 설문지의 10개 영역 모두의 평균을 나타내는 데에 "총점"이 사용된다. Haem-A-QoL 영역 점수와 총점은 0~100의 척도로 변환되며 점수가 높을수록 장애가 더 크다는 것을 나타낸다. 해당 기준선 점수(치료를 평가하기 전의 점수) 대비 점수가 감소하면 환자의 삶의 질이 향상되었음을 나타낸다. 설문지는 치료 전 및 1회 이상(예를 들어, 2회 이상, 3회 이상, 4회 이상, 5회 이상, 또는 6회 이상) 용량의 피투시란(예를 들어, 80 mg을 4주마다 1회 또는 월 1회 피하 투여) 치료 후에 수행될 수 있다. 예를 들어, 피투시란 치료 개시 후 8주, 12주, 16주, 20주, 24주, 25주, 26주, 또는 27주차에 설문지를 작성할 수 있다.
본 피투시란 요법은 기준선 대비 적어도 하나의 Haem-A-QoL 영역(예를 들어 신체 건강, 감정, 자아관, 스포츠 및 레저, 직장 및 학교, 혈우병 관리, 치료, 미래, 가족 계획, 및/또는 파트너십 및 성)의 점수를 향상시키고/시키거나 기준선 대비 Haem-A-QoL 총점을 향상시킨다. 특히, 본 방법은 신체 건강 점수 및/또는 Haem-A-QoL의 총점에 의해 확인된 바와 같이, 환자자기평가 혈우병 관련 증상(예를 들어 부종 통증 및 관절 통증) 및 신체 기능(예를 들어 움직임 통증 및 장거리 보행 어려움)의 개선(예를 들어 완화 및 사라짐)을 포함하여 혈우병 환자의 삶의 질을 향상시킬 수 있다. 임상적으로 의미 있는 삶의 질 개선에는 예를 들어 총점에서 약 7점 이상 감소, 스포츠 및 레저 영역 점수에서 약 10점 이상 감소, 및/또는 신체 건강 영역 점수에서 약 10점 이상 감소를 포함한다. 문헌[Wyrwich, supra.] 참조. 일부 구현예에서, Haem-A-QoL의 10개 영역 점수(예를 들어, 신체 건강 영역 점수 또는 총점) 중 하나 이상이 1단위 이상(예를 들어 2단위 이상, 3단위 이상, 4단위 이상, 5단위 이상, 6단위 이상, 7단위 이상, 8단위 이상, 9단위 이상, 10단위 이상, 11단위 이상, 12단위 이상, 13단위 이상, 14단위 이상, 15단위 이상, 16단위 이상, 17단위 이상, 18단위 이상, 19단위 이상 또는 20단위 이상) 감소한다.
III.
피투시란 약학적 조성물의 투여
피투시란 약학적 조성물은 복강내, 정맥내, 근육내, 피하, 경피, 또는 간문맥 투여를 포함하지만 이에 한정되지 않는 당업계에 알려진 임의의 수단에 의해 투여될 수 있다. 특정 구현예에서, 약학적 조성물은 예를 들어 용량당 25 내지 100 mg(예를 들어 25 내지 95 mg, 40 내지 90 mg, 50 내지 100 mg, 50 내지 90 mg, 50 내지 85 mg, 또는 50 내지 80 mg)의 용량 강도로 피하 주사에 의해 투여된다. 특정 구현예에서, 피투시란은 상기 기재된 바와 같이 PBS 용액 중 용량당 50 또는 80 mg(활성 모이어티의 중량)으로 피하 투여된다.
복수의 피투시란 용량이 1, 2, 3, 4, 5, 6, 7, 또는 8주, 또는 1, 2, 또는 3개월의 간격으로 대상체에게 투여될 수 있다. 특정 구현예에서, 고정 용량의 피투시란(예를 들어, 50 또는 80 mg 피하 주사)이 혈우병 환자(예를 들어, 12세 이상이고, 발병된 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 혈우병 B 환자)에게 4주마다 1회 또는 월 1회 투여된다.
일부 구현예에서, 본 약학적 조성물은 출혈 장애를 치료하기 위해 현재 사용되는 것과 같은 다른 약제 및/또는 다른 치료 방법과 함께 투여될 수 있다. 예를 들어, 특정 구현예에서, 피투시란은 혈우병 A 및/또는 B 치료에 유용한 제2 제제와 함께 투여된다. 이러한 제2 제제의 예로는 신선-냉동 혈장(FFP); rFVIIa; aPCC; 재조합 또는 혈장 유래 FVIII 또는 FIX; 바이러스-불활성화 vWF-함유 FVIII 농축물; 스테로이드 또는 정맥내 면역글로불린(IVIG) 및 시클로포스파미드와 함께 고용량의 FVIII 또는 FIX를 포함할 수 있는 탈감작 요법; 항섬유소용해 요법의 존재 또는 부재 하의, FVIII 또는 FIX의 주입 및 면역억제와 함께, 혈장분리교환법; 면역억제 요법(예를 들어, 시클로포스파미드, 프레드니손, 및/또는 항-CD20)의 존재 또는 부재 하의 면역 관용 유도(ITI); 데스모프레신 아세테이트(DDAVP); 항섬유소용해제, 예컨대 아미노카프로산 및 트라넥삼산; 혈액응고제; 코르티코스테로이드; 면역억제인자; 및 에스트로겐을 포함한다. 피투시란 조성물 및 추가의 치료제 및/또는 치료는 동시에 및/또는 동일한 조합으로, 예를 들어, 비경구로 투여될 수 있으며, 또는 추가 치료제는 별개의 조성물의 일부로서 또는 별개의 시간에 및/또는 당업계에 알려지거나 본원에 기재된 또 다른 방법에 의해 투여될 수 있다.
본원에서 달리 정의되지 않는 한, 본 발명과 관련하여 사용되는 과학적 용어 및 기술적 용어는 당업자가 일반적으로 이해하는 의미를 가질 것이다. 예시적인 방법 및 물질이 하기에 기술되어 있지만, 본원에 기술되어 있는 것과 유사하거나 동일한 방법 및 물질이 본 개시의 실시 또는 교시에 사용될 수 있다. 상충되는 경우, 정의를 비롯한 본 명세서가 우선할 것이다. 일반적으로, 본원에 기재된 혈액학, 의약, 의약 및 제약 화학, 및 세포 생물학과 관련하여 사용되는 명명법 및 기술은 당업계에 잘 알려져 있고 통상적으로 사용되는 것이다. 효소 반응 및 정제 기법은 당업계에서 보편적으로 달성된 바와 같이 또는 본원에 기재된 바와 같이 제조사의 설명서에 따라 수행된다. 또한, 문맥 상 달리 요구되지 않는 한, 단수의 용어는 복수를 포함할 것이고, 복수의 용어는 단수를 포함할 것이다. 본 명세서 및 구현예 전반에 걸쳐, 단어 "가지다" 및 "포함하다", 또는 "갖다", "가지고 있는", "포함한다", 또는 "포함하는"과 같은 변형은 언급된 정수 또는 정수군을 포함하되, 임의의 기타 정수 또는 정수군을 배제하지 않는다는 것을 의미하는 것으로 이해될 것이다. 본원에 언급된 모든 간행물 및 기타 참고문헌은 그 전체가 본원에 참고로 포함된다. 여러 문헌이 본원에 인용되지만, 상기 인용은 임의의 이들 문헌이 당업계의 통상의 일반 지식을 형성한다는 것을 인정하는 것으로 간주되지 않는다. 본원에서 사용된 바와 같이, 하나 이상의 관심 값에 적용되는 용어 “대략” 또는 “약”은 언급된 기준 값과 유사한 값을 지칭한다. 특정 구현예에서, 이 용어는 달리 명시되거나 문맥에서 달리 명백하지 않는 한 명시된 기준 값의 (보다 크거나 보다 작음) 어느 한 방향으로 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 또는 그 미만에 속하는 값의 범위를 지칭한다.
본 발명이 보다 잘 이해되도록, 하기 실시예가 기술된다. 이들 실시예는 단지 예시를 위한 것이며, 어떠한 방식으로든 본 발명의 범위를 제한하는 것으로 간주되어서는 안 된다.
실시예
실시예 1: 임상 연구 설계 및 모집단
본 실시예는 피투시란 요법에 대한 임상 연구의 설계 및 환자 모집단을 설명한 것이다. 본 연구에서 억제인자가 존재하는 혈우병 A 또는 B 성인 17명에게 피투시란 50 mg(n = 6) 또는 80 mg(n = 11)의 3개월 고정 피하 용량을 투여하였다(도 2). 참여자들에 대해 최대 112일(또는 오픈 라벨 확장 연구로 전환한 참여자의 경우 최대 84일) 또는 AT 수준이 기준값의 80% 이상으로 돌아올 때까지 중 더 긴 기간 동안 추적관찰하였다. rFVIIa 또는 aPCC 요법으로 본 연구를 진행하는 동안 출혈 에피소드를 관리하였다. 모든 참여자가 본 연구를 완료하였다.
적격 대상체는 억제인자(베데스다 억제인자 분석에서 0.6 BU/mL 초과)가 존재하는, 중등도 또는 중증 혈우병 A 또는 혈우병 B(FVIII 또는 FIX가 5% 이하)가 있는 18세 내지 65세(포괄적)의 남성이었다. 참여자는 보충요법(on-demand treatment)을 받은 적이 있거나 이전에 예방요법을 받은 적이 있다.
주요 배제 기준에는 정맥 혈전색전증의 병력, 알려진 공존 혈전성 장애, 선별 시 정상 상한치(ULN)의 3.0배를 초과하는 D-dimer, 선별 시 AT 활성 60% 미만, 간 기능 장애, μL당 CD4 세포수 200 미만 또는 추정 사구체 여과율 45 mL/분/1.73 m2(Modification of Diet in Renal Disease 공식 사용)(문헌[Levey et al., Ann Intern Med. (2006) 145(4):247- 54]) 이하인 HIV 양성이 포함되었다.
통계 분석은 주로 기술적이며 SAS 소프트웨어 버전 9.2 이상을 사용하여 수행하였다. 기술적 통계는 연속 변수, 및 범주 및 순서 변수의 빈도 및 백분율에 대해 나타내었다. 백분율은 비결측값의 수를 기반으로 한다. 각 기간의 ABR은 해당 기간의 출혈 수를 해당 기간의 일수로 나눈 값에 365.25를 곱하여 계산하였다.
연구 모집단의 기준선 인구통계 및 임상 특성이 표 2에 제공되어 있다. SEM은 평균의 표준 오차를 나타낸 것이다.
연구의 모든 참여자는 중증 혈우병(인자 수준 1% 미만)이 있었다. 각 용량군의 한 참여자는 혈우병 B를, 나머지는 혈우병 A가 있었다. 연령, 체중, 및 연간 출혈 에피소드 수는 두 용량군 모두 대체로 유사했다. 연구에서 17명의 환자 중 11명이 C형 간염 병력이 있는 것으로 보고되었지만, 리바비린, 인터페론, 또는 기타 항바이러스 요법으로 치료를 받았던 대상체는 등록되지 않았다. 또한 선별시 병력당 임상적으로 유의한 간경변증 또는 알라닌/아스파르테이트 아미노트랜스퍼라제(ALT/AST)가 ULN의 3배를 초과한 경우를 포함하여 유의한 간 질환이 있는 대상체는 제외되었다.
실시예 2: 피투시란 치료의 안전성
앞서 기술한 연구의 목적은 억제인자가 존재하는 혈우병 A 또는 B 환자에서 피투시란의 안전성을 평가하는 것이었다. 안전성 분석 모집단에는 피투시란을 1회 이상 투여받은 모든 참여자가 포함되었다. 안전성 평가에는 이상사례(AE) 모니터링, 임상 실험실 평가(예를 들어 혈액학적, 생화학적(간 기능 검사 포함)), 응고 측정[활성화 부분 트롬보플라스틴 시간(aPTT)/프로트롬빈 시간(PT), 국제 표준화 비율, 혈소판, D-dimer, 피브리노겐], 및 항약물 항체 형성[검증된 인간 효소 결합 면역흡착 분석법 사용]), 활력 징후, 및 12-리드 심전도가 포함되었다. AE 및 중증 AE(SAE)는 연구 전반에 걸쳐 평가하였고, 국제의약용어(MedDRA®, 버전 16.0)에 따라 암호화하였다. AE는 중증도(경증, 중등도, 또는 중증) 및 연구 약물 또는 기록된 전투약과의 인과 관계에 근거하여 등급을 매겼다.
연구가 진행되는 동안 피투시란 치료 중단, 혈전증 사례, 피투시란과 관련된 것으로 간주되는 SAE는 없었다. 약물 유발 항약물 항체 형성 사례는 없었다. AE는 17명(100%)의 참여자에 의해 보고되었으며, 모든 사례에서 최대 중증도는 경증 또는 중등도였다. 아래 표 3은 적어도 1회 용량의 피투시란을 받은 모든 환자의 AE를 나타낸 것이다. 표 3에 기재된 모든 약물 관련 AE는 연구 약물과 관련이 있을 수 있거나 확실히 관련이 있는 것으로 간주되는 AE를 지칭한다. 표 3의 가장 일반적인 약물 관련 AE는 적어도 2명의 참여자에서 연구 기간 동안 보고되었다.
가장 일반적인 연구 약물 관련 AE(2명 이상의 환자에서 발생)는 주사 부위 홍반(n = 8; 47%), ALT/AST 증가, 간 효소 증가(알칼리 포스파타제, 빌리루빈), 또는 트랜스아미나제 증가(n = 5; 29%), 피브린 D-dimer 증가(n=2; 12%), 및 주사 부위 통증(n = 2; 12%)이었다. 주사 부위 반응은 모두 경미하고 일시적이었고 의학적 개입이 필요하지 않았다. ALT 상승은 일반적으로 경미하고 일시적이었다(최대 ALT가 ULN의 3배 이하인 대상체 4명, ALT가 ULN의 5배인 대상자 1명). ULN(참조 범위 3.4 내지 20.5 μmol/L)의 2배를 초과하는 관련 빌리루빈 상승은 없었으며, 더 큰 모집단에 적용하는 경우 약물이 중증 약물 유발 간 손상을 유발할 가능성이 있는지 여부를 예측하는 것으로 간주되는 Hy의 법칙 기준(문헌[Katarey, et al., Clin Med (Lond.) (2016) 16(Suppl 6):s104-9])을 충족하는 중증 약물 유발 간 기능 장애도 없었다.
3명의 참여자는 C형 간염 바이러스(HCV) 감염 병력이 있었다. HCV 병력이 있는 참여자(80 mg)에서 42일차(ULN의 5배; 254.9 U/L)에 ALT 증가가 ULN의 3배를 초과한 한 사례가 발생했으며 연구자에 의해 중등도로 보고되었다; 피투시란 투약은 98일차까지 ALT가 ULN의 3배 미만으로 감소하면서 계속되었고 연구 종료 시점에 회복되었다. 나머지 4건의 ALT 상승(ULN의 3배 미만) 사례는 연구 종료 시점에 회복되었거나(n=1) 또는 회복중이었다(n=3). 전반적으로, 피투시란과 관련된 것으로 간주되는 간 효소의 상승은 모두 무증상이었고, 연구자에 의해 경증 또는 중등도로 평가되었으며, 피투시란 투여 중단 또는 차질을 야기하지 않았다.
대다수의 참여자는 응고 매개변수(예를 들어 PT, aPTT, D-dimer, 및 피브리노겐)에서 기준선으로부터 어떠한 변화도 보이지 않았다. 연구자에 의해 임상적으로 유의한 것으로 보고된 PT 또는 aPTT의 변화는 없었다. D-dimer 증가는 3명의 참여자에서 AE로 보고되었으며, 2명은 관련이 있을 가능성이 있고 1명은 관련이 없을 가능성이 있다. D-dimer의 모든 증가는 연구자에 의해 경증으로 간주되었고 일시적이었다.
한 참여자(50 mg)는 D-dimer 증가(29일차에 412 μg/L에서 42일차에 1349 μg/L; 참조 범위: 0 내지 130 μg/L)를 경험하였으며, 이는 치료와 관련이 있을 가능성이 있는 것으로 간주되었고 경증이었으며 연구 종료 시점에 회복되었다(526 μg/L). 해당 참여자는 피투시란을 투여받기 전에 D-dimer가 증가(231 μg/L)했으며 이 사례는 중등도 위염 및 경미한 ALT 증가(ULN의 3배 미만)와 관련이 있었다.
또 다른 참여자(80 mg)는 D-dimer 증가(42일차에 2480 μg/L; 참조 범위: 0 내지 590 μg/L)를 경험하였으며 이는 치료와 관련이 있을 가능성이 있는 것으로 판단되고 경증이었다. 해당 참여자는 HCV 병력이 있었고 D-dimer 증가는 ALT의 경미한 증가(ULN의 3배 미만)과 관련이 있었다. 환자는 오픈 라벨 확장 연구에 등록되었고, 매달 고정 용량의 피투시란을 계속 투여받았고, AE로서 보고된 D-dimer 증가의 다른 에피소드를 보이지 않았다(도 3a 및 3b).
D-dimer 증가(42일차에 2090 μg/L; 참조 범위: 0 내지 590 μg/L)가 있는 최종 참여자(80 mg)는 피투시란 치료와 관련이 없을 것으로 판단되었으며 경증이었다. 해당 참여자는 피투시란을 투여받기 전에 HCV 병력과 D-dimer 증가(690 μg/L)가 있었다. 이 사례는 경미한 간 효소 증가(치료와 관련된 것으로 간주됨)의 심각하지 않은 AE와 관련이 있었으나, 투약을 계속하고 연구 종료 시점에 AE가 회복되었다(450 μg/L). D-dimer의 증가와 출혈 치료, 간 효소 이상, 또는 투여된 피투시란 용량 사이의 연관성은 관찰되지 않았다.
총 4개의 SAE가 연구 참여자에 의해 보고되었다. 한 참여자(18%)는 폐렴과 과오종의 두 가지 SAE를 보고했으며, 한 명은 십이지장 궤양 출혈이 있었고 다른 한 명은 근육 출혈이 있었다. 어떤 SAE도 연구 약물과 관련된 것으로 간주되지 않았으며 모든 SAE가 회복되었다.
실시예 3: 피투시란 요법의 약동학 및 약력학
실시예 1에 기술된 연구의 또 다른 목적은 피투시란의 약동학(PK)을 특성화하고 AT 활성 및 트롬빈 생성에 대한 피투시란의 약력학(PD) 효과를 평가하는 것이었다. PK/PD 모집단에는 피투시란을 1회 이상 투여받았고 평가할 수 있는 혈장 샘플이 1개 이상 있는 모든 참여자가 포함되었다.
PK/PD 분석을 평가하기 위해, 혈장 AT 단백질 수준과 트롬빈 생성을 활동 기반 발색 분석(자동 응고 수단에 대한 INNOVANCE® 항트롬빈 분석; Siemens BCSxp; 정량 하한(LLOQ) 3.13 ng/mL) 및 보정된 자동 혈전도 분석(Thromboscope BV, Maastricht)으로 측정하였다; 조직 인자 유발 트롬빈 생성의 실시간 분석을 측정하기 위해 친화성 형광 기질을 사용하였다. Thermo Fluoroskan으로 형광을 판독하고 각각 피크 높이로 표기하였다. AT 활성은 세계보건기구(WHO) 참조 혈장 표준(5% AT 활성의 LLOQ)의 AT 활성에 대해 보정된 기능적으로 활성인 AT의 정량화를 위해 검증된 발색 분석을 사용하여 인간 혈장에서 측정하였다. 비구획 분석 및 Phoenix WinNonlin 소프트웨어를 사용하여 혈장 농도-시간 데이터로부터 피투시란 PK 매개변수를 계산하였다.
1. 약동학
피투시란 50 mg 및 80 mg을 단회 투여 후, 약물의 평균 최고 혈장 수준(Cmax)은 각각 0일차에 85.4 및 142.9 ng/mL, 56일차에 96.5 및 157.1 ng/mL(3개월 투여 후)였다. 두 용량군 모두에서 Cmax는 두 평가일(0일차 및 56일차)에 투여한지 약 4시간 후(Tmax)에 달성되었다. 피투시란 수준은 혈장에서 빠르게 감소했다; 평균 제거 반감기는 3.4시간 내지 5.2시간 범위였으며, 이는 이전에 관찰된 결과와 유사하였다(문헌[Pasi, supra]). 피투시란 PK 매개변수는 억제인자가 존재하거나 존재하지 않는 혈우병 환자에서 유사했다.
억제인자가 존재하는 혈우병 환자에서 0일차(첫 월 SC 용량 후) 및 56일차(3개월 SC 용량 후)에 피투시란에 대한 혈장 PK 매개변수를 아래 표 4에 제공한다. 표 4의 AUCinf는 무한대로 외삽된 곡선 아래 영역을 나타내고; AUClast는 최종 측정가능한 농도에 대한 곡선 아래 영역을 나타내고; CL/F는 겉보기 클리어런스를 나타내고; Cmax는 최대 혈장 농도를 나타내고; CV는 변동 계수를 나타내고; t1/2는 제거 반감기를 나타내고; tmax는 최대 혈장 농도까지의 시간을 나타내고; Vz/F는 겉보기 분포 용적을 나타낸다. 반복 투약 후 D56에서의 AUCinf 값은 기록되지 않았다.
2. 약력학
AT 활성은 백분율로 측정된다(정상 범위는 약 80% 내지 120% 활성). 평균(평균[SEM]의 표준 오차) 기준선 AT 수준은 피투시란 50 mg 및 80 mg 용량군에서 각각 정상의 109.5%(4.4) 및 100.2%(4.8)였다. AT 활성의 일관된 감소가 있었고, 처음에는 7일차에 처음 분명해졌고 28일차 후에 최대 효과로 진전되었다. AT 활성의 평균(SEM) 최대 감소(AT 수준의 기준선으로부터 백분율 변화로서)는 용량군 간에 유사하여 50 mg 용량군에서 82.0%(2.2), 80 mg 용량군에서 87.4%(0.7)였다. 투여 후 최소 잔류 AT 수준은 9.8%였으며, 80 mg 용량군에서 관찰되었다. 시간 경과에 따른 AT 활성의 기준선으로부터의 평균(SEM) 감소를 도 4a에 제공한다. 감소된 AT 수준은 증가된 트롬빈 생성과 관련이 있다(도 4b).
트롬빈 피크 높이는 두 용량군 모두에서 AT 감소 정도와 관련이 있었고 기준선으로부터 75% 이상까지 AT 감소는 68.05 nM의 중위 피크 트롬빈 높이를 야기하였고, 이는 이전에 건강한 지원자에서 관찰된 낮은 범위(64 내지 210 nM)(도 5)(문헌[Pasi, supra])에 속하는 것이다.
실시예 4: 피투시란 요법에 의한 연간 출혈률 감소
실시예 1에 기술된 임상 연구의 한 목적은 연간 출혈률(ABR)에 대한 피투시란의 효과를 평가하는 것이었다. 모든 환자를 평가하였다.
ABR에 대한 피투시란의 효과를 평가하기 위해, 상세한 혈우병 병력을 수집하여 6개월 기간을 기준으로 참여자의 과거 ABR을 확인하는 데 사용하였다. 연구 기간 동안 모든 참여자는 출혈의 모든 에피소드, BPA 투여, 및 BPA 치료에 대한 반응을 기록하는 연구 특화 일지를 가졌다. 피투시란의 작용 기전을 기반으로 AT 감소가 75% 이상에 도달하는 예상 발병 기간은 약 28일이다. 발병 기간 출혈 에피소드는 연구 약물의 첫 번째 용량일 및 시간부터 28일차(포괄적)까지 발생한 출혈 에피소드였다. 관찰 기간 출혈 에피소드는 첫 번째 용량 후 4주(첫 용량일 + 29일)부터 피투시란 마지막 용량 후 8주(마지막 용량일 + 56일) 또는 연구의 마지막 방문일 중 더 이른 날짜까지 발생한 것이었다. 출혈 에피소드의 원인과 위치, 각 출혈에 적용되는 인자 및 BPA 치료 용량을 파악했다.
아래 표 5는 피투시란 치료 전 과거의 연간 출혈률과 비교하여 월 1회 피투시란 투여 후 연구 참여자의 ABR을 제시한다. 과거 ABR은 지난 12개월 동안 추정된 출혈 사례 수이다. 발병 기간 ABR은 연구 1일차부터 28일차까지였고, 관찰 기간 ABR은 29일차부터 마지막 용량 후 8주까지였다.
중위 ABR은 발병(1일차 내지 28일차) 및 관찰(마지막 용량 후 29일차 내지 8주) 기간 동안의 두 용량군에 대한 과거 중위 ABR보다 낮았다(표 5). 50 mg 및 80 mg 용량군을 합친(n=17) 관찰 기간 중위 ABR은, 과거 중위 ABR 36(범위 0~80)과 비교하여, 0(범위 0~46)이었다. 중위(범위) 관찰 ABR은, 치료 전 비율 33(0~80)회 및 36(8~54)회 출혈과 비교하여, 50 mg 용량군에서 7(0~46)회, 80 mg 용량군에서 0(0~45)회 출혈이었다(표 5). 전반적으로 17명 중 11명(65%)의 참여자가 피투시란 치료를 받는 동안 0번의 출혈 사례를 기록했으며 관찰 기간 동안 ABR이 0이었다. BPA로 치료한 출혈은, 피투시란을 동일한 위치에 사용하기 전의 출혈과 비교하여, 출혈을 제어하는 데 필요한 BPA의 양에 대한 참여자 등급 및 출혈당 주사 횟수로 평가하여 성공적으로 관리되었다. AT 감소가 75% 이상인 경우, aPCC로 치료한 출혈이 6건, rFVIIa로 치료한 출혈이 13건이었다. 전반적으로, aPCC로 치료한 출혈의 83.3%(5/6)는 정상보다 aPCC를 적게 사용하는 것으로 보고되었고, rFVIIa로 치료한 출혈의 61.5%(8/13)는 출혈 사례를 제어하기 위해 정상보다 더 적은 rFVIIa를 사용하는 것으로 보고되었다. BPA 용량 범위는 rFVIIa의 경우 93 내지 133 μg/kg(중위 108.6 μg/kg)이고, aPCC의 경우 14 내지 75 U/kg(중위 28.6 U/kg)이었다.
실시예 5: 피투시란 치료에 의한 환자자기평가결과의 개선
본 연구의 또 다른 목적은 참여자자기평가 혈우병 관련 증상(부종 통증 및 관절 통증의 존재), 신체 건강(움직임 통증 및 장거리 보행 어려움), 및 전반적인 삶의 질을 포함하여 환자자기평가결과(PRO)를 평가하는 것이었다. PRO는 혈우병 요법의 효능을 측정하는 중요한 지표이다. 실시예 1에 기술된 연구에서, PRO는 Haem-A-QoL 설문지 및 EuroQol 5-Dimensions(EQ-5D) 설문지를 사용하여 수집되었다. 모든 환자를 평가하였다.
Haem-A-QoL 영역 점수 및 기준선 점수로부터의 변화는 아래 표 6에 제공한다. 전반적으로, 기준선 점수의 평균 변화로 입증된 바와 같이 모든 영역 점수가 치료와 함께 개선되었다(표 6).
특히, Haem-A-QoL 총점(-9.2[2.9]) 및 신체 건강(-12.3[3.9]) 영역 점수(점수가 낮을수록 더 나은 HRQoL을 나타냄)에서, 기준선으로부터 연구 종료(112일)까지의 평균(SEM) 변화는 공개된 역치(문헌[Wyrwich, supra])를 기준으로 임상적으로 유의한 개선을 보였다. 또한, 전체 모집단에서, 기준선 점수의 평균 변화로 입증된 바와 같이 모든 영역 점수가 치료에 의해 개선되었다(표 6). 또한 PRO 점수의 변화는 용량 의존적인 것으로 보인다. 일반적으로 효과의 정도는 50 mg 용량 대비 80 mg 용량의 대상체에서 더 크다.
이러한 결과는 피투시란 요법이 관절 건강을 포함하여 환자의 경험과 삶의 질에 유익한 영향을 미친다는 것을 나타낸다. 또한 Haem-A-QoL의 다른 모든 영역이 80 mg 군에서 효과가 더 크고, 용량 의존적으로 나타나는 수치 감소(즉, 개선)를 입증했다는 점도 주목할 만하다.
SEQUENCE LISTING
<110> GENZYME CORPORATION
<120> METHODS AND COMPOSITIONS FOR TREATING HEMOPHILIA
<130> 022548.WO080
<150> 63/042,390
<151> 2020-06-22
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
oligonucleotide"
<400> 1
gguuaacacc auuuacuuca a 21
<210> 2
<211> 23
<212> RNA
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
oligonucleotide"
<400> 2
uugaaguaaa ugguguuaac cag 23
Claims (29)
- 혈우병 환자의 관절 기능을 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 피하 투여하는 단계를 포함하고, 임의로 환자는 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자인, 방법.
- 제1항에 있어서, 투여는 보행의 어려움을 감소시키거나 이동성을 증가시키는, 방법.
- 혈우병 환자의 관절 증상을 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 피하 투여하는 단계를 포함하고, 관절 증상은 관절 부종, 움직임 통증, 및 관절 통증으로부터 선택되고, 임의로 환자는 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자인, 방법.
- 혈우병 환자에서 환자자기평가결과(PRO)를 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 피하 투여하는 단계를 포함하고, 임의로 환자는 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자이고, 임의로 PRO는 하나 이상의 삶의 질 영역에서 개선되는, 방법.
- 혈우병 환자의 삶의 질(QoL)을 개선하는 방법으로서, 이를 필요로 하는 혈우병 환자에게 피투시란을 피하 투여하는 단계를 포함하고, QoL은 하나 이상의 QoL 영역에서 개선되고, 임의로 환자는 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B 환자인, 방법.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 피투시란은 용량당 40 내지 90 mg으로 투여되는, 방법.
- 제4항 또는 제5항에 있어서, 하나 이상의 QoL 영역은 QoL 설문지 내의 영역이고, 임의로 QoL 설문지는 성인을 위한 혈우병 삶의 질 설문지(Haem-A-QoL)인, 방법.
- 제7항에 있어서, 투여는 설문지의 총점, 스포츠 및 레저 영역 점수, 및 신체 건강 영역 점수 중 하나 이상에서 7단위 이상(임의로 8단위 이상, 9단위 이상, 또는 10단위 이상)의 감소로 표시되는 임상적으로 의미 있는 개선을 야기하는, 방법.
- 제1항 내지 제8항 중 어느 한 항에 있어서, 환자는 억제인자가 존재하거나 존재하지 않는 혈우병 A 또는 B가 있는 성인 또는 12세 이상의 청소년 환자인, 방법.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 환자는 혈우병 A가 있는, 방법.
- 제10항에 있어서, 환자는 인자 VIII 또는 우회제(BPA)로 치료받은 적이 있는, 방법.
- 제11항에 있어서, 환자는 억제인자가 있고, 임의로 억제인자의 수준은 베데스다 억제인자 분석법에 따른 측정시 0.6 BU/mL를 초과하는, 방법.
- 제10항 또는 제11항에 있어서, 환자는 억제인자가 없는, 방법.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 환자는 혈우병 B가 있는, 방법.
- 제14항에 있어서, 환자는 인자 IX 또는 BPA로 치료받은 적이 있는, 방법.
- 제15항에 있어서, 환자는 억제인자가 있고, 임의로 억제인자의 수준은 베데스다 억제인자 분석법에 따른 측정시 0.6 BU/mL를 초과하는, 방법.
- 제14항 또는 제15항에 있어서, 환자는 억제인자가 없는, 방법.
- 제11항 내지 제13항 또는 제15항 내지 제17항 중 어느 한 항에 있어서, BPA는 활성화 프로트롬빈 복합 농축물(aPCC) 및/또는 재조합 활성화 인자 VII(rFVIIa)인, 방법.
- 제1항 내지 제18항 중 어느 한 항에 있어서, 용량당 50 mg의 피투시란의 복수 용량을 환자에게 투여하는 단계를 포함하는 방법.
- 제1항 내지 제18항 중 어느 한 항에 있어서, 용량당 80 mg의 피투시란의 복수 용량을 환자에게 투여하는 단계를 포함하는 방법.
- 제1항 내지 제20항 중 어느 한 항에 있어서, 피투시란은 인산염 완충 식염수(pH 7) 중 50 내지 200 mg/mL의 농도, 임의로 100 mg/mL의 농도로 제공되는, 방법.
- 제1항 내지 제21항 중 어느 한 항에 있어서, 피투시란은 4주마다 1회 또는 월 1회 환자에게 투여되는, 방법.
- 제1항 내지 제22항 중 어느 한 항의 방법에 사용하기 위한 피투시란.
- 제1항 내지 제22항 중 어느 한 항의 방법에 사용하기 위한 제조 물품.
- 제24항에 있어서, 제조 물품은 0.8 mL의 인산염 완충 식염수(pH 7)에 80 mg의 피투시란을 함유하는 일회용 바이알인, 제조 물품.
- 제24항에 있어서, 제조 물품은 0.8 mL의 인산염 완충 식염수(pH 7)에 80 mg의 피투시란을 함유하는 일회용 사전충전형 시린지인, 제조 물품.
- 제24항에 있어서, 제조 물품은 0.5 mL의 인산염 완충 식염수(pH 7)에 50 mg의 피투시란을 함유하는 일회용 바이알인, 제조 물품.
- 제24항에 있어서, 제조 물품은 0.5 mL의 인산염 완충 식염수(pH 7)에 50 mg의 피투시란을 함유하는 일회용 사전충전형 시린지인, 제조 물품.
- 제1항 내지 제22항 중 어느 한 항의 방법에서 혈우병 A 또는 B를 치료하기 위한 약제의 제조를 위한 피투시란의 용도.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063042390P | 2020-06-22 | 2020-06-22 | |
| US63/042,390 | 2020-06-22 | ||
| PCT/US2021/038445 WO2021262695A1 (en) | 2020-06-22 | 2021-06-22 | Methods and compositions for treating hemophilia |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20230027277A true KR20230027277A (ko) | 2023-02-27 |
Family
ID=76943130
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237002631A KR20230027277A (ko) | 2020-06-22 | 2021-06-22 | 혈우병을 치료하기 위한 방법 및 조성물 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US20210393669A1 (ko) |
| EP (1) | EP4168018A1 (ko) |
| JP (1) | JP2023531679A (ko) |
| KR (1) | KR20230027277A (ko) |
| CN (1) | CN115942940A (ko) |
| AU (1) | AU2021296786A1 (ko) |
| BR (1) | BR112022026265A2 (ko) |
| CA (1) | CA3188137A1 (ko) |
| IL (1) | IL299295A (ko) |
| MX (1) | MX2023000164A (ko) |
| TW (1) | TW202216172A (ko) |
| WO (1) | WO2021262695A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20240075001A1 (en) * | 2022-05-24 | 2024-03-07 | Darren Rubin | Methods to reduce hemorrhage and mortality on the battlefield and applications for trauma patients |
| WO2023240199A2 (en) * | 2022-06-08 | 2023-12-14 | Genzyme Corporation | Treatment of hemophilia with fitusiran |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9127274B2 (en) | 2012-04-26 | 2015-09-08 | Alnylam Pharmaceuticals, Inc. | Serpinc1 iRNA compositions and methods of use thereof |
| IL259795B2 (en) * | 2015-12-07 | 2024-04-01 | Genzyme Corp | Methods and preparations for the treatment of diseases related to SERPINC1 |
| WO2019014187A1 (en) * | 2017-07-10 | 2019-01-17 | Genzyme Corporation | METHODS AND COMPOSITIONS FOR TREATING A BLEEDING EVENT IN A SUBJECT WITH HEMOPHILIA |
-
2021
- 2021-06-22 AU AU2021296786A patent/AU2021296786A1/en active Pending
- 2021-06-22 TW TW110122791A patent/TW202216172A/zh unknown
- 2021-06-22 KR KR1020237002631A patent/KR20230027277A/ko active Search and Examination
- 2021-06-22 EP EP21742607.1A patent/EP4168018A1/en active Pending
- 2021-06-22 CA CA3188137A patent/CA3188137A1/en active Pending
- 2021-06-22 WO PCT/US2021/038445 patent/WO2021262695A1/en active Application Filing
- 2021-06-22 CN CN202180044790.1A patent/CN115942940A/zh active Pending
- 2021-06-22 MX MX2023000164A patent/MX2023000164A/es unknown
- 2021-06-22 BR BR112022026265A patent/BR112022026265A2/pt unknown
- 2021-06-22 JP JP2022578970A patent/JP2023531679A/ja active Pending
- 2021-06-22 US US17/354,818 patent/US20210393669A1/en active Pending
-
2022
- 2022-12-20 IL IL299295A patent/IL299295A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| TW202216172A (zh) | 2022-05-01 |
| AU2021296786A1 (en) | 2023-02-23 |
| CN115942940A (zh) | 2023-04-07 |
| EP4168018A1 (en) | 2023-04-26 |
| BR112022026265A2 (pt) | 2023-01-17 |
| CA3188137A1 (en) | 2021-12-30 |
| IL299295A (en) | 2023-02-01 |
| US20210393669A1 (en) | 2021-12-23 |
| MX2023000164A (es) | 2023-07-06 |
| WO2021262695A1 (en) | 2021-12-30 |
| JP2023531679A (ja) | 2023-07-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20230027277A (ko) | 혈우병을 치료하기 위한 방법 및 조성물 | |
| Federici et al. | Clinical efficacy of highly purified, doubly virus‐inactivated factor VIII/von Willebrand factor concentrate (Fanhdi®) in the treatment of von Willebrand disease: a retrospective clinical study | |
| KR20230117403A (ko) | 피투시란을 이용한 혈우병의 치료 | |
| WO2022120291A1 (en) | Treatment of hemophilia with fitusiran | |
| KR20060126762A (ko) | 외상의 말기 합병증을 치료하기 위한 인자 ⅴⅰⅰa의 용도 | |
| JP4676585B2 (ja) | 血液凝固異常に基づく疾患の治療・予防用医薬組成物 | |
| TW202342065A (zh) | 治療血友病的方法和組成物 | |
| US20240002861A1 (en) | Compositions and methods for treatment of bleeding disorders | |
| US20240000744A1 (en) | Treatment of Hemophilia with Fitusiran | |
| CN116635040A (zh) | 用非妥西兰治疗血友病 | |
| KR20190111912A (ko) | 출혈의 치료 또는 예방에 사용하기 위한 혈액 응고 인자 대체품 | |
| WO2023240193A2 (en) | Treatment of hemophilia with fitusiran in pediatric patients | |
| CN118434425A (zh) | 用于改善血友病患者的患者报告结局的非妥西兰 | |
| KR20240138572A (ko) | 혈우병 환자에서 환자 보고 결과를 개선하는 데 사용하기 위한 피투시란 | |
| CN116723863A (zh) | 用于治疗出血性病症的组合物和方法 | |
| KR100831770B1 (ko) | t-PA 변이체와 저분자량 헤파린의 조합 치료 | |
| Van Creveld et al. | Dental extractions and the use of Christmas factor concentrate in cases of haemophilia B |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination |