KR20230004501A - 안지오텐신 ⅱ와 관련된 질병, 장애, 또는 병태의 치료 및/또는 예방에 유용한 신규 화합물 - Google Patents
안지오텐신 ⅱ와 관련된 질병, 장애, 또는 병태의 치료 및/또는 예방에 유용한 신규 화합물 Download PDFInfo
- Publication number
- KR20230004501A KR20230004501A KR1020227036148A KR20227036148A KR20230004501A KR 20230004501 A KR20230004501 A KR 20230004501A KR 1020227036148 A KR1020227036148 A KR 1020227036148A KR 20227036148 A KR20227036148 A KR 20227036148A KR 20230004501 A KR20230004501 A KR 20230004501A
- Authority
- KR
- South Korea
- Prior art keywords
- methyl
- sulfonyl
- imidazol
- butyl
- carbamate
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/64—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms, e.g. histidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/427—Thiazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Epidemiology (AREA)
- Urology & Nephrology (AREA)
- Pulmonology (AREA)
- Immunology (AREA)
- Vascular Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
Description
본 개시내용은 펩타이드 안지오텐신 Ⅱ와 관련된 질병, 장애, 또는 병태의 치료 및/또는 예방에 유용한 신규 화합물, 약학적 약물로서의 이들의 용도, 및 이러한 화합물의 제조 공정에 관한 것이다.
레닌-안지오텐신 시스템(RAS)은 혈압, 체액, 및 전해질 균형뿐만 아니라 체혈관 저항을 조절하는 호르몬 시스템이다. 레닌-안지오텐신 시스템(RAS)는 안지오텐시노겐(AGT), 레닌, 안지오텐신-전환 효소(ACE), 안지오텐신 Ⅱ(Ang Ⅱ), 및 두 개의 Ang Ⅱ 수용체 AT1 및 AT2를 포함한다. 452개의 아미노산을 갖는 단백질인 안지오텐시노겐은 효소 레닌에 의해 절단되어 펩타이드 안지오텐시노겐 I(Ang I)을 생성하며, 이어서 안지오텐신-전환 효소 ACE에 의해 Ang Ⅱ로 절단된다. Ang Ⅱ는 수용체 AT1 및 AT2를 활성화시킴으로써 생리학적 및 병태생리학적 병태를 조절하는 작용제로서 작용한다. 중요한 것은, Ang Ⅱ는 AT1 수용체에 의해 매개되는 강한 고혈압 효과를 제공하며, 다수의 심장혈관 기능을 조절한다.
레닌-안지오텐신 시스템(RAS)에서의 ACE 및 레닌 효소의 중심 역할은 구조 기반 약물 설계에 대한 출발점이 되었으며, 이들 효소를 억제하는 약학적 약물을 얻게 되었다. AT1 수용체에 대한 선택적 길항제로서 작용하는 약학적 약물 로사르탄이 1995년에 시장에 도입되었으며, 이후에 다수의 다른 "사르탄" 약물, 예컨대 발사르탄, 칸데사르탄, 및 이르베사르탄으로 이어졌다. 레닌 억제제 알리스키렌은 2007년에 미국에서 고혈압 치료용으로 승인되었다.
AT2 수용체에 선택적으로 작용하는 작용제가 레닌-안지오텐신 시스템(RAS)과 관련된 장애를 치료하는 데 사용될 수 있는 것으로 또한 제안되었으며, AT2 수용체의 그러한 활성화는 AT1 수용체에 의해 매개되는 것들에 빈번하게 역효과를 가졌다. AT1 수용체는 인간 신체의 대부분의 장기에서 발현되는 반면, AT2 수용체는 태아 조직에서 발견되었으며, 출생 이후 발현이 크게 감소된다. 그러나, AT2 수용체의 발현은 병리학적 병태, 예컨대 심부전, 신부전, 심근경색증, 뇌병변, 혈관 손상, 및 창상 치유에서 상향 조절된다.
AT2 수용체는 또한 아포토시스 및 세포 증식의 억제에 관여하는 것으로 알려져 있다(Pharmacol. Rev. 2000; 52: 415-472).
WO 02/096883호는 AT2 수용체에 선택적 작용제로서 유용한 삼고리형 화합물을 개시한다. 화합물은 이미다졸 모이어티를 포함할 수 있다. 화합물은 위장 질환, 예컨대 소화불량, 염증성 장질환(IBS), 및 복합장기부전(MOF)(예를 들어, 국제 특허 출원 WO 99/43339호 참조), 및 심장혈관 장애의 치료에 사용될 수 있다.
EP 0512675 A1호는 메틸렌을 통해 신규 치환된 페닐 티오펜 또는 페닐 퓨란 유도체에 부착된 치환된 이미다졸이 안지오텐신 II 길항제이며, 고혈압 및 울혈성 심부전의 치료에 유용한 것을 개시한다.
DE10 2012 004 589 A1호는 신경변성 질병, 바람직하게는 알츠하이머 치매, 파킨슨 질병, 헌팅톤 질병, 및 근위축성 측삭경화증을 치료하는 데 유용한 신규 안지오텐신 II 수용체 작용제를 개시한다.
미국 특허 출원 US 2004/0167176호는 안지오텐신 II 수용체 작용제로서 유용한 삼고리형 헤테로고리의 제조를 기술한다.
인간 간 마이크로솜에서 개선된 안정성을 갖는 AT2 수용체 리간드의 합성을 위한 에스테르교환 방법이 Bioorg. Med. Chem. Lett. 2018; 28:519-522에 기술된다.
Med. Res. Rev. 2018; 38:602-624는 소분자 AT2 수용체 작용제를 개시한다. 선택적 소분자 AT2 수용체 작용제 화합물 21 C21의 발견이 기술된다(또한, 국제 특허 출원 WO 2002/096883호 참조). C21은 현재 IPF를 포함하는 AT2 수용체 관련 장애의 치료에 대한 임상적 개발 중에 있다(예를 들어, 국제 특허 출원 WO 2016/139475호 참조).
C21은 또한 특히 뇌졸증, 척수 손상, 낫형 세포 질병, 근디스트로피, 암 치료 관련 심장독성, 말초 신경병증, 및 전신 경화증의 치료에의 잠재적 용도인 것으로 명시되었다(예를 들어, 국제 특허 출원 WO 2004/046141호, WO 2016/092329호, WO 2016/107879호, WO 2016/139475호, WO 2017/221012호, WO 2019/008393호, 및 미국 특허 출원 US 2012/035232호 참조).
화합물 C21은 CYP 패밀리로부터의 일련의 산화성 효소를 억제하는 것으로 보고되며, C21의 이미다졸 고리를 메틸기 또는 트리플루오로네틸기로 치환하는 것은 CYP 3A4 및 2C9의 억제 수준을 감소시켰다. 또한, C21의 약간의 구조적 변경은 이를 선택적 AT2 수용체 작용제에서 선택적 AT2 수용체 길항체 C38/M132로 전환시켰다.
사이토크롬 P450(CYP)은 예를 들어 포유동물에 존재하는 효소 패밀리이며, 그들은 약학적 약물과 같은 다양한 화합물의 청소(clearance)에 중요하다. 따라서, 다양한 CYP와 약물의 상호 작용은 원하지 않은 부작용을 방지하기 위해 고려하는 것이 중요하다. 너무 많은 정도의 CYP 억제는 잠재적으로 화합물의 약학적 약물로서의 유용성에 부정적 영향을 미칠 수 있다.
감소된 CYP 억제를 갖는 선택적 AT2 수용체 작용제는 Bioorg. Med. Chem. 2010; 18:4570-4590에 기술된다.
안지오텐신 II와 관련된 질병, 장애, 또는 병태를 치료 및/또는 예방하기 위한 AT2 수용체 작용제로서 작용하는 약학적-유효 화합물, 예컨대 소분자에 대한 요구가 존재하는 실정이다. 특히, 하나 이상의 CYP의 허용 가능한 CYP 억제 수준을 나타내는 이러한 약학적 약물에 대한 요구가 있다.
본 개시내용은 안지오텐신 II와 관련된 질병, 장애, 또는 병태를 치료 및/또는 예방하기 위한 AT2 수용체 작용제로서 작용하는 소분자와 같은 약학적 약물을 제공한다. 상기 약학적 약물은 하나 이상의 CYP의 허용 가능한 CYP 억제 수준을 나타낸다.
또한, 본 개시내용은 하나 이상의 CYP의 허용 가능한 CYP 억제 수준을 나타내는 AT2 수용체 작용제로서 작용하는 소분자와 같은 약학적 약물을 제공한다.
이러한 측면에서, 화학식 I의 화합물 또는 이의 약학적으로 허용 가능한 염이 제공된다:
화학식 I의 화합물에서,
R1은,
H;
OR6, SR7, NR8R9, 할로겐, 티아졸, 옥사졸, 및 피라졸로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된(즉, 선택적으로 1 또는 2개의 치환기로 치환된) C2-C6 알킬;
OR6, SR7,및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된(즉, 선택적으로 1 또는 2개의 치환기로 치환된) C3-C6 사이클로알킬;
티아졸;
벤질(여기서, 페닐 모이어티는 OR6, SR7, 및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환됨(즉, 선택적으로 1 또는 2개의 치환기로 치환됨)); 또는
(CH2)m-R10을 나타내고,
R2는,
H;
F;
Cl;
OR6, SR7, NR8R9, 할로겐, 티아졸, 옥사졸, 및 피라졸로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된(즉, 선택적으로 1 또는 2개의 치환기로 치환된) C2-C6 알킬;
OR6, SR7,및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된(즉, 선택적으로 1 또는 2개의 치환기로 치환된) C3-C6 사이클로알킬;
벤질(여기서, 페닐 모이어티는 OR6, SR7, 및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환됨(즉, 선택적으로 1 또는 2개의 치환기로 치환됨)); 또는
(CH2)m-R10을 나타내되,
단, R1 및 R2 둘 모두는 H가 아니고,
R3은,
H;
할로겐; 또는
F 및 Cl로 구성된 군으로부터 선택되는 0, 1, 2, 또는 3개의 할로겐으로 치환된(즉, 선택적으로 1, 2, 또는 3개의 할로겐으로 치환된) C1-C3 알킬을 나타내고,
R4 및 R5는 독립적으로 0, 1, 2, 또는 3개의 F로 치환된(즉, 선택적으로 1, 2, 또는 3개의 플루오로 치환기로 치환된) C1-C6 알킬을 나타내고,
X는 CH=CH, CH, N, NH, O, 또는 S를 나타내고;
Y는 CH=CH, CH, N, NH, O, 또는 S를 나타내되,
단, (a) X 및 Y는 동일하지 않고,
(b) X가 CH=CH를 나타낼 때, 그 때의 Y는 오직 CH를 나타내고,
(c) Y가 CH=CH를 나타낼 때, 그 때의 X는 오직 CH를 나타내고,
Z는 단일 결합, O, 또는 S를 나타내고;
R6, R7, R8, 및 R9는 독립적으로 H; 또는 0, 1, 2, 또는 3개의 F로 치환된(즉, 선택적으로 1, 2, 또는 3개의 플루오로 치환기로 치환된) C1-C3 알킬을 나타내고,
R10은 페닐, 티아졸, 옥사졸, 및 피라졸로 구성된 군으로부터 선택되고;
n은 0, 1, 2, 3, 또는 4이고;
m은 0 또는 1이다.
본원에 개시된 상기 언급된 화합물(이의 약학적으로 허용 가능한 염 포함)은 이하에서 "본 발명의 화합물", "본 개시내용의 화합물", "본원에 기재된 화합물", 또는 "화학식 I의 화합물"로 상호 교환적으로 지칭된다.
본원에 기재된 화학식 I의 화합물 또는 이의 약학적으로 허용 가능한 염의 치료적으로 유효량을 적어도 약학적으로 허용 가능한 담체, 부형제, 및/또는 희석제와 함께 포함하는 약학적 조성물이 또한 제공된다.
또한, 약제로서의 용도를 위한 본원에 기재된 화학식 I의 화합물 또는 이의 약학적으로 허용 가능한 염, 또한 본원에 기재된 약학적 조성물이 제공된다. 약제는 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태의 치료 및/또는 예방을 위한 약제일 수 있다.
폐색성 폐질병, 예컨대 만성 폐색성 폐질병, 자가면역 질병, 예컨대 류마티스 관절염, 바이러스성 기도 감염증, 예컨대 호흡기 바이러스 감염증(바이러스 폐렴)으로부터 초래된 폐렴 및 보다 바람직하게는 고혈압, 심부전, 뇌졸증, 만성 신장 질병(신증 포함), 폐섬유증, 예컨대 특발성 폐섬유증, 경화증, 예컨대 전신 경화증, 사르코이드증, 예컨대 폐사르코이드증, 및 상기 기재되지는 않지만 이하에서 열거되는 것들 중 하나 이상을 포함하는 기타 병태, 및 이의 임의의 조합으로 구성된 군으로부터 선택되는 질병, 장애, 및/또는 병태의 치료 및/또는 예방에의 용도를 위한 본원에 기재된 화합물 I의 화합물 또는 이의 약학적으로 허용 가능한 염, 또는 본원에 기재된 약학적 조성물이 또한 제공된다.
고혈압, 심부전, 뇌졸증, 신증, 폐섬유증, 예컨대 특발성 폐섬유증, 경화증, 예컨대 전신 경화증, 사르코이드증, 예컨대 폐사르코이드증, 및 상기 기재되지는 않지만 이하에서 열거되는 것들 중 하나 이상을 포함하는 기타 병태, 및 이의 임의의 조합으로 구성된 군으로부터 선택되는 질병, 장애, 및/또는 병태의 치료 및/또는 예방을 위한 약제의 제조를 위한 본원에 기재된 화합물 I의 화합물 또는 이의 약학적으로 허용 가능한 염, 또는 본원에 기재된 약학적 조성물이 또한 제공된다.
고혈압, 심부전, 뇌졸증, 신증, 폐섬유증, 예컨대 특발성 폐섬유증, 경화증, 예컨대 전신 경화증, 사르코이드증, 예컨대 폐사르코이드증, 및 상기 기재되지는 않지만 이하에서 열거되는 것들 중 하나 이상을 포함하는 기타 병태, 및 이의 임의의 조합으로 구성된 군으로부터 선택되는 질병, 장애, 및/또는 병태의 치료 및/또는 예방 방법이 또한 제공되며, 방법은 본원에 기재된 화합물 I의 화합물 또는 본원에 기재된 약학적 조성물의 치료적으로 유효량을 이를 필요로 하는 환자에게 투여하는 단계를 포함한다.
본 개시내용은 상기 정의된 화학식 I의 화합물 또는 이의 약학적으로 허용 가능한 염을 제공한다:
의심의 여지를 피하기 위해, 당업자는 본 발명의 특정 양태의 화합물에 대한 본원의 언급(예컨대, 상기 정의된 화학식 I의 화합물을 언급하는 본 발명의 임의의 양태)이 모든 실시형태 및 이의 특정 특성에 대한 언급을 포함할 것이며, 실시형태 및 특정 특성은 조합하여 취하여서 본 발명의 추가의 실시형태 및 특성을 형성할 수 있는 것으로 이해할 것이다.
달리 명시되지 않는 한, 본원에 사용된 모든 기술 및 과학 용어는 본 발명이 속하는 해당 분야의 당업자에 의해 이해되는 바와 공통된 이들의 의미를 가질 것이다.
용어 "알킬"은 직선형 또는 분지형 포화 또는 불포화 알킬 사슬을 나타낸다. "알킬"이 불포화 알킬 사슬, 즉, 알켄일 때, 이는 둘 이상의 탄소 원자를 포함하는 것으로 이해되어야 한다.
용어 "C1-C6 알킬"은 1 내지 6개의 탄소를 포함하는 직쇄형, 또는 충분한 수(즉, 적절한 경우 최소 2개 또는 3개)의 탄소 원자가 존재할 때, 분지쇄, 및/또는 고리형(따라서, C3-6 사이클로알킬기를 형성) 포화 또는 불포화 알킬 사슬을 나타낸다. 충분한 수(즉, 최소 4개)의 탄소 원자가 존재할 때, 이러한 기는 또한 부분-고리형(따라서, C4-6 부분 사이클로기를 형성)일 수 있다.
"C2-C6 알킬"의 예는 메틸, 에틸, 프로필, 이소프로필, n-부틸, sec-부틸, 이소부틸, tert-부틸, n-펜틸, 이소펜틸, 네오-펜틸, n-헥실, 이소헥실, 3-메틸펜틸, 2,3-디메틸부틸, 및 네오헥실을 포함하지만, 이로 제한되지는 않는다.
용어 "C2-C6 알킬"은 2 내지 6개의 탄소 원자를 포함하는 상기 정의된 직선형 또는 분지형 포화 또는 불포화 알킬 사슬을 나타낸다. "C2-C6 알킬"의 예는 에틸, 프로필, 이소프로필, n-부틸, sec-부틸, 이소부틸, tert-부틸, n-펜틸, 이소펜틸, 네오-펜틸, n-헥실, 이소헥실, 3-메틸펜틸, 2,3-디메틸부틸, 및 네오헥실을 포함하지만, 이로 제한되지는 않는다.
용어 "C1-C3 알킬"은 1 내지 3개의 탄소 원자를 포함하는 상기 정의된 직선형 또는 분지형 포화 또는 불포화 알킬 사슬을 나타낸다. "C1-C3 알킬"의 예는 에틸, 프로필, 및 이소프로필을 포함하지만, 이로 제한되지는 않는다.
용어 "C3-C6 사이클로알킬"은 3, 4, 5, 또는 6개의 탄소 원자로 구성된 상기 정의된 포화 또는 불포화 비-방향족 단고리형 고리를 나타낸다. "C3-C6 사이클로알킬"의 예는 사이클로프로필, 사이클로부틸, 사이클로펜틸, 및 사이클로헥실을 포함하지만, 이로 제한되지는 않는다.
언급될 수 있는 부분-고리형 알킬기("부분-사이클로알킬" 기로도 지칭될 수 있음)의 예는 사이클로프로필메틸을 포함한다. 충분한 수의 탄소 원자가 존재할 때, 이러한 기는 또한 다고리형(예를 들어, 이고리형 또는 삼고리형) 및/또는 스피로고리형일 수 있다.
용어 "할로겐"은 플루오로, 클로로, 브로모, 및 아이오도를 포함한다.
본원에 기재된 R1 치환기가 예를 들어 티아졸일 때, 이는 다음과 같이 화학식 I의 화합물의 이미다졸 고리에 결합될 수 있는 것으로 인식될 것이다:
본 발명의 화합물 내에 2개 이상의 치환기의 정체가 동일할 수 있는 경우, 각각의 치환기의 실제 정체는 어떠한 방식으로도 상호 의존적이지 않는다. 예를 들어, 둘 이상의 할로기가 존재하는 상황에서, 이들 기는 동일하거나 상이할 수 있다(예를 들어, 2개의 클로로기, 또는 플루오로 및 클로로기). 마찬가지로, 둘 이상의 알킬기가 존재하는 경우, 논의되는 기는 이들의 탄소 원자수 및/또는 이들이 직선형, 분지형, 불포화, 또는 달리 존재하는지 여부의 측면에서 동일하거나 상이할 수 있다.
달리 명시되지 않는 한, 치환기는 그들이 부착될 수 있는 기 상의 임의의 위치에 위치할 수 있다. 이러한 측면에서, 하나 이상의 치환기로 치환될 수 있는 알킬기(예를 들어)는 또한 이러한 치환기로 종결될 수 있다(이는, 본 발명자들은 예를 들어 알킬 사슬의 말단에 위치하는 것을 의미함).
의심의 여지를 피하기 위해, 치환기 자체가 1개 이상의 치환기(예를 들어, 1, 2, 또는 3개의 할로겐으로 치환된 C1-C3 알킬)로 치환된 것으로 명시된 경우, 이들 치환기(예를 들어, 할로겐)는 가능한 경우 동일하거나 상이한 원자 상에 배치될 수 있다.
당업자는 본 발명의 대상인 본 발명의 화합물이 수득 가능한 것들, 즉, 안정한 형태로 제조될 수 있는 것들을 포함하는 것으로 인식할 것이다. 즉, 본 발명의 화합물은 예를 들어 반응 혼합물로부터 유용한 순도 수준으로의 단리를 견딜만큼 충분히 튼튼한 것들을 포함한다.
화학식 I의 화합물은 예를 들어 이하 기재되는 당업자에게 잘 알려진 기술에 따라 제조될 수 있다.
일 실시형태에서, 화학식 I의 화합물의 X 및 Y를 함유하는 모이어티는 페닐 고리일 수 있어서 화학식 Ia 또는 화학식 Ib의 화합물을 제공한다:
대안적으로, 화학식 I의 화합물의 X 및 Y를 함유하는 모이어티는 티오펜일 수 있어서 화학식 Ic의 화합물을 제공한다.
다른 실시형태에서, 화학식 I의 화합물의 X 및 Y를 함유하는 모이어티는 티아졸일 수 있어서 화학식 Id의 화합물을 제공한다.
본원에 기재된 화학식 I의 화합물은 R1 및 R2에 대해 다음 값을 가질 수 있다:
R1은 OR6, SR7, NR8R9, 할로겐, 또는 티아졸, 옥사졸, 또는 피라졸로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된(즉, 선택적으로 1 또는 2개의 치환기로 치환된) C2-C6 알킬를 나타낼 수 있고, R2는 H를 나타낼 수 있다.
예를 들어, R1은 에틸, n-프로필, 이소프로필, n-부틸, sec-부틸, 이소부틸, 및 tert-부틸로 구성된 군으로부터 선택될 수 있고, R2는 H를 나타낼 수 있다.
추가의 예에서, R1은 OR6 또는 할로겐으로부터 선택되는 1 또는 2개의 치환기로 선택적으로 치환된 C2-6 알킬(예를 들어, 에틸, 프로필, 또는 부틸)을 나타낼 수 있고, R2는 H를 나타낼 수 있다.
예를 들어, R1은 -OH 기로 선택적으로 치환된 에틸 또는 프로필, 예를 들어 2-하이드록시프로프-2-일 또는 1-에탄올을 나타낼 수 있고, R2는 H를 나타낼 수 있다. R1은 또한 F로 선택적으로 치환된 에틸 또는 프로필, 예를 들어 2-플루오로프로프-2-일을 나타낼 수 있고, R2는 H를 나타낼 수 있다.
다른 예에서, R1은 C2-C6 알킬기, 예컨대 이소프로필 또는 사이클로프로필을 나타낼 수 있고, R2는 H를 나타낼 수 있다.
또 다른 예에서, R1은 티아졸을 나타낼 수 있고, R2는 H를 나타낼 수 있다.
또 추가의 예에서, R1은 2-하이드록시프로프-2-일 또는 보다 바람직하게는 tert-부틸을 나타낼 수 있고, R2는 H를 나타낼 수 있다.
언급될 수 있는 본 발명의 다른 화합물은 다음과 같은 것들을 포함한다:
R1은 H를 나타낼 수 있고,
R2는 OR6, SR7, NR8R9, 할로겐, 또는 티아졸, 옥사졸, 또는 피라졸로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된(즉, 선택적으로 1 또는 2개의 치환기로 치환된) C2-C6 알킬을 나타낼 수 있다.
예를 들어, R1은 H를 나타낼 수 있고, R2는 에틸, n-프로필, 이소프로필, n-부틸, sec-부틸, 이소부틸, 및 tert-부틸로 구성된 군으로부터 선택될 수 있다.
추가의 예에서, R1은 H를 나타낼 수 있고, R2는 tert-부틸을 나타낼 수 있다.
본원에 기재된 화학식 I의 화합물은 메틸, 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸, 및 tert-부틸로 구성된 군으로부터 선택되는 R4 치환기를 가질 수 있다. 예를 들어, R4 치환기는 tert-부틸, 메틸, 에틸, n-프로필, 또는 n-부틸, 예컨대 n-부틸, 또는 특히 메틸일 수 있다.
추가적으로 또는 대안적으로, 본원에 기재된 화학식 I의 화합물은 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸, 및 tert-부틸로 구성된 군으로부터 선택되는 R5 치환기를 가질 수 있다. 예를 들어, R5 치환기는 이소프로필 또는 이소부틸일 수 있다.
예를 들어, 본원에 기재된 화학식 I의 화합물이 제공되며, 여기서, R4는 메틸, 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸, 및 tert-부틸로 구성된 군으로부터 선택되고, R5는 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸, 및 tert-부틸로 구성된 군으로부터 선택된다.
또한, 본원에 기재된 화학식 I의 화합물이 제공되며, 여기서, R4는 메틸이고, R5는 이소프로필 또는 이소부틸이다.
추가의 예에서, 본원에 기재된 화학식 I의 화합물이 제공되며, 여기서, R4는 메틸이고, R5는 n-부틸이다.
또 추가의 예에서, 본원에 기재된 화학식 I의 화합물이 제공되며, 여기서, R4는 n-부틸이고, R5는 이소프로필 또는 이소부틸이다.
다른 예에서, 본원에 기재된 화학식 I의 화합물이 제공되며, 여기서, R4는 n-부틸이고, R5는 n-프로필이다.
본 발명의 바람직한 화합물은 화학식 Ia, Ib, Ic, 또는 Id 중 임의의 하나의 화합물을 포함하며, 여기서, R1은 OR6 또는 할로겐으로부터 선택되는 하나 이상의 치환기로 선택적으로 치환된 C2-4 알킬을 나타내고;
R2 및 R3은 둘 모두 H를 나타내고;
R4는 C1-2 알킬을 나타내고;
R5는 이소프로필 또는 이소부틸을 나타내고;
n은 0을 나타낸다.
본 발명의 보다 바람직한 화합물은 화학식 Ic 또는 보다 바람직하게는 화학식 Ia 중 임의의 하나의 화합물을 포함하며, 여기서, R1은 OH 또는 플루오로로 선택적으로 치환된 선형 또는 분지형 프로필 또는 부틸기를 나타내고, 예를 들어 R1은 tert-부틸 또는 2-하이드록시프로프-2-일을 나타내고;
R4는 메틸을 나타내고;
R5는 이소프로필을 나타낸다.
본 개시내용은 또한 본원에 기재된 화학식 I의 화합물을 제공하며, 여기서, 메틸렌기를 통해 이미다졸 모이어티의 질소 원자에 결합한 페닐 고리는 치환되지 않을 수 있다. 따라서, "n"에 대한 값은 0일 수 있다.
본 개시내용은 다음 화합물 중 하나 이상인 화합물 또는 전술한 화합물 중 임의의 하나의 약학적으로 허용 가능한 염을 제공한다:
메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트,
부틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트,
메틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐) 카바메이트,
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트,
메틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일) 설포닐)카바메이트,
부틸 ((2-이소부틸-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸 티아졸-5-일)설포닐)카바메이트,
부틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
메틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((2-프로필-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸-티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
2-메톡시에틸 ((5-이소부틸-3-(4-(2-(2-tert부틸)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸-티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸-티아졸-5-일)설포닐)카바메이트.
또한, 본 발명은 다음 화합물 중 하나 이상인 화합물 및 전술한 화합물 중 임의의 하나의 약학적으로 허용 가능한 염을 제공한다:
메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트,
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트,
메틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일) 설포닐)카바메이트,
부틸 ((2-이소부틸-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸 티아졸-5-일)설포닐)카바메이트,
부틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
메틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((2-프로필-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸-티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
2-메톡시에틸 ((5-이소부틸-3-(4-(2-(2-tert부틸)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-3'-플루오로-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 (4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-3'-플루오로-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐카바메이트.
임의의 경우에, 본 발명의 바람직한 화합물은 이하 기재된 예의 화합물을 포함한다.
약학적 제형 및 의학적 용도
본 개시내용은 또한 본원에 기재된 화학식 I의 화합물 또는 이의 약학적으로 허용 가능한 염의 치료적으로 허용 가능한 염을 적어도 하나의 약학적으로 허용 가능한 담체, 부형제, 또는 희석제와 함께 포함하는 약학적 조성물을 제공한다.
본 발명의 화합물은 임의의 상기 병태의 치료적, 임시방편적, 및/또는 진단적 치료뿐만 아니라 예방 치료(이는, 본 발명자들은 병태의 저하 및/또는 악화를 예방 및/또는 끝내는 것을 포함함)에 모두 권고된다.
본 발명의 화합물은 보통 경구, 정맥내, 피하, 구강, 직장, 피부, 비강, 기관, 기관지, 임의의 다른 비경구 경로, 또는 흡입을 통해, 또는 폐 경로, 또는 이의 임의의 조합으로, 약학적으로 허용 가능한 투여 형태로, 용액으로, 현탁액으로, 나노현탁액을 포함하는 에멀젼으로, 또는 리포좀 제형으로 투여될 것이다. 투여의 추가의 방법은 동맥내, 근육내, 복강내, 문정맥내, 피내, 경막외, 척추강내 투여, 또는 이의 임의의 조합을 포함하지만, 이로 제한되지는 않는다.
약학적 조성물은 로렌지, 캡슐, 또는 시럽과 같은 경구 투여 형태일 수 있다.
일부 실시형태에서, 본 발명의 화합물은 단독으로(예를 들어, 별도로), 및/또는 순차적으로, 및/또는 동일한 시간에 병렬적으로(예를 들어, 동시적으로), 여러 가지 투여 경로를 사용하여 투여될 수 있지만, 바람직하게는 경구 투여를 위한 정제, 캡슐, 또는 엘릭서, 직장 투여를 위한 좌약, 비경구 또는 근육내 투여, 또는 흡입 등을 통한 것을 위한 멸균 용액, 현탁액, 또는 에멀젼을 포함하는 알려진 약학적 제형의 방식으로 투여된다. 흡입을 통한 투여는 바람직하게는 네뷸라이저를 사용하여 이루어져서 본 발명의 화합물을 바람직하게는 치료되는 대상에 자극 또는 기침을 유발하지 않고 폐포 및 세기관지를 포함하는 소폐 조직에 전달한다.
본 발명의 화합물의 치료적으로 유효량의 투여는 별도로(예를 들어, 서로 약 2시간 이상 차이로), 순차적으로(예를 들어, 서로 약 2시간 내에), 또는 동일한 시간에 병렬적으로(예를 들어, 동시에), 흡입을 통해 그리고 경구를 포함하는 투여 경로의 조합으로 수행되어 효과적 투여를 획득할 수 있다.
본원에 사용된 표현 "치료적으로 유효량"은 소기의 치료적 효과를 화합물이 투여되는 환자에게 유도하기에 충분한 본원에 기재된 화합물의 양을 의미한다. 또한, 본원에 기재된 환자는 인간일 수 있다.
약제로서의 용도를 위한 본원에 기재된 화합물 또는 이의 약학적으로 허용 가능한 염, 또는 본원에 기재된 약학적 조성물이 또한 제공된다. 약제는 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태의 치료 및/또는 예방을 위한 약제일 수 있다. 약제는 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태의 치료 및/또는 예방에 사용될 수 있으며, 상기 약제는 하나 이상의 CYP의 허용 가능한 CYP 억제 수준을 나타낸다.
따라서, 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태의 치료 및/또는 예방에의 용도를 위한 본원에 기재된 화합물 또는 이의 약학적으로 허용 가능한 염, 또는 본원에 기재된 약학적 조성물이 제공된다. 따라서, 선택적으로 약학적 조성물의 형태인 본원에 기재된 화합물 및 이의 약학적으로 허용 가능한 염이 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태의 치료 및/또는 예방에 사용될 수 있으며, 상기 화합물, 이의 약학적으로 허용 가능한 염, 또는 약학적 조성물은 하나 이상의 CYP의 허용 가능한 CYP 억제 수준을 나타낸다.
또한, 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태의 치료 및/또는 예방을 위한 약제의 제조에 사용하기 위한 본원에 기재된 화합물 또는 이의 약학적으로 허용 가능한 염, 또는 본원에 기재된 약학적 조성물의 용도가 제공된다.
또한, 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태의 치료 및/또는 예방 방법이 제공되며, 방법은 본원에 기재된 화학식 I의 화합물 또는 이의 약학적으로 허용 가능한 염, 또는 본원에 기재된 약학적 조성물의 치료적으로 유효량을 이를 필요로 하는 환자에게 투여하는 단계를 포함한다.
의심의 여지를 피하기 위해, 표현 "허용 가능한 CYP 억제 수준을 나타낸다"는 CYP 억제를 원하지 않고/않거나 CYP 억제 수준이 예를 들어 50% 미만, 예컨대 40 내지 20%, 예를 들어 20% 미만, 예컨대 10 내지 0%, 예를 들어 0% 미만, 예컨대 -50%인 것을 의미한다.
의심의 여지를 피하기 위해, 표현 "펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태"은 AT2 수용체의 활성화를 원하거나 필요한 질병, 장애, 및/또는 병태를 의미한다.
따라서, 일부 실시형태에서, AT2 수용체의 활성화는 원하거나 필요하지만, CYP의 억제는 원하지 않는 질병, 장애, 및/또는 병태의 치료 방법이 제공되며, 방법은 유효량 또는 투여량을 획득하기 위해 본 발명의 화합물의 치료적으로 유효량을 별도로, 순차적으로, 또는 동일한 시간에 병렬적으로, 바람직하게는 흡입을 통해 그리고 경구로 이러한 요법을 필요로 하는 환자에게 투여하는 단계를 포함한다.
이러한 제형은 표준 및/또는 용인된 약학적 실시에 따라 제조될 수 있다.
본 발명의 제형으로 치료되기에 적합한 대상체는 포유동물 대상체, 특히 인간 대상체를 포함하지만, 이로 제한되지는 않는다.
본원에 기재된 화합물 또는 이의 약학적으로 허용 가능한 염은, AT2 수용체가 발현되며, 이들의 자극을 원하거나 필요한 이들 질병, 장애, 및/또는 병태에 유용할 것으로 예상된다. 특히, 본원에 기재된 화합물 또는 이의 약학적으로 허용 가능한 염은, AT2 수용체의 활성화는 원하거나 필요하지만, CYP의 억제는 원하지 않는 질병, 장애, 및/또는 병태의 치료에 유용하다.
"안지오텐신 II와 관련된 질병, 장애, 및/또는 병태"란, 본 발명자들은 AT2 수용체의 활성화에 의해 치료 가능한 것으로 알려진 질병, 장애, 및/또는 병태, 예컨대 이하에서 언급되는 것들을 포함하지만, 이러한 질환의 현존하는 치료는 CYP에 의해 대사되는 다른 치료제의 투여를 포함할 수 있다. 따라서, 이러한 질병, 장애, 및/또는 병태는 적어도 하나의 CYP 효소의 억제가 필요하지 않고/않거나, 이롭지 않고/않거나 바람직하지 않거나, 이러한 억제가 환자에게 유해하거나 유해할 질환을 포함할 수 있다.
본원에 기재된 바와 같이, 본 발명의 화합물은 약리학적 활성도를 보유하고/하거나 경구 또는 비경구 투여 후에 신체에서 대사되어 약리학적 활성도를 보유하는 화합물을 형성하기 때문에 유용한다.
특히, 본 발명의 화합물은 Ang II 수용체의 작용제이다. 따라서, 본 발명의 화합물은 Ang II의 내인성 생성이 결핍되고/되거나 Ang II 수용체의 활성도에의 증가를 원하거나 필요한 이들 질병, 장애, 및/또는 병태에 유용할 것으로 예상된다.
보다 특히, 본 발명의 화합물은 AT2 수용체의 작용제이며, 특히 예를 들어 하기 기재된 시험에서 입증될 수 있는 바와 같이 그 하위 수용체의 (AT1 수용체에 대해) 선택적 작용제이다.
AT2 수용체 작용제는 AT2 수용체를 전체적으로 활성화시키는 것들 그리고 부분적으로 활성화시키는 것들을 포함한다. 따라서, 본 발명의 화합물은 AT2 수용체에 선택적으로 결합될 수 있으며, AT2 수용체에 작용제 활성도를 나타낼 수 있다. AT2 수용체에 "선택적으로 결합하는" 화합물이란, 본 발명자들은 소정의 농도에서 관련 화합물에 대한 친화도 비율(AT2:AT1)이 적어도 50:1, 예컨대 적어도 100:1, 바람직하게는 적어도 1000:1이다.
이러한 측면에서, 본 발명의 화합물은 혈관 수축, 섬유증, 증가된 세포 성장 및/또는 분화, 증가된 심수축성, 증가된 심장 혈관의 비대, 및/또는 증가된 체액 및 전해질 불균형뿐만 아니라 피부 장애 및 근골격 장애를 특징으로 하는 질환의 치료에 권고된다.
본 발명의 화합물은 또한 트롬복산 수용체 활성도를 나타낼 수 있다. 이러한 측면에서, 본 발명의 화합물은 혈소판 활성화 및/또는 응집에 대한 억제 효과(그리고 따라서 예를 들어 항혈전증 효과)를 가질 수 있고/있거나, 치료적 방식으로 혈관 수축 및/또는 기관지 수축을 감소시킬 수 있다.
본 발명의 화합물은 또한 스트레스 관련 장애의 치료 및/또는 미세순환 및/또는 점막-보호성 메커니즘의 개선에 권고된다.
따라서, 본 발명의 화합물은, 상기 명시된 것을 특징으로 할 수 있으며, 예를 들어 위장관, 심혈관계, 기도, 신장, 눈, 여성 생식(배란) 기관, 및 중추신경계(CNS)의 것인 장애의 치료에 유용할 것으로 예상된다.
언급될 수 있는 위장관의 장애는 식도염, 바렛식도, 위궤양, 십이지장궤양, 소화불량(dyspepsia)(비궤양성 소화불량 포함), 위-식도 역류, 과민성 대장 증후군(IBS), 염증성 대장 질병(IBD), 췌장염, 간 장애(예컨대, 간염), 담낭 질병, 복합장기부전(MOF), 및 패혈증을 포함한다. 언급될 수 있는 다른 위장 장애는 구강 건조증, 위염, 위무력증, 위산 과다, 쓸개관의 장애, 코엘리시아(coelicia), 크론병, 궤양성 대장염, 설사, 변비, 산통, 연하 곤란, 구토, 구역질, 소화불량증(indigestion), 및 쇼그렌 증후군을 포함한다.
언급될 수 있는 기도 장애는 염증성 장애, 예를 들어 천식, 폐색성 폐질병(예컨대, 만성 폐색성 폐질병), 폐렴, 폐고혈압, 및 성인 호흡 곤란 증후군을 포함한다.
언급될 수 있는 신장 장애는 신부전, 신장염, 및 신장성 고혈압을 포함한다.
언급될 수 있는 눈 장애는 당뇨 망막병증, 미숙아 망막병증, 및 망막 미세혈관화(retinal microvascularisation)를 포함한다.
언급될 수 있는 여성 생식 기관의 장애는 배란 기능장애를 포함한다.
언급될 수 있는 심혈관 장애는 고혈압, 심장 비대증, 심부전(박출률 보존 심부전 포함), 동맥경화증, 동맥혈전증, 정맥혈전증, 내피 기능장애(endothelial dysfunction), 내피 병변(endothelial lesion), 포스트-발룬 확장 협심증(post-balloon dilatation stenosis), 혈관신행, 당뇨 합병증, 미세혈관 기능장애, 협심증, 심장 부정맥, 간헐성 파행증, 임신중독증, 심근경색증, 재경색증, 허혈성 장애, 발기 부전, 및 신생혈관내막 증식(neointima proliferation)을 포함한다.
언급될 수 있는 CNS 장애는 인지 장애, 음식 섭취 기능장애(배고픔/포만) 및 갈증, 뇌졸증, 뇌출혈, 뇌색전증 및 뇌경색증, 다발성 경화증(MS), 알츠하이머 질병, 파킨스 질병을 포함한다.
본 발명의 화합물은 또한 성장 대사 및 증식의 조절, 예를 들어 노화, 비대성 장애, 전립성 이상증식, 자가면역 장애(예를 들어, 관절염, 예컨대 류마티스 관절염, 또는 전신 홍반 루푸스), 건선, 비만, 뉴런 재생, 궤양 치유, 지방 조직 이상증식의 억제, 줄기세포 분화 및 증식, 섬유증 장애, 암(예를 들어, 위장관(식도 또는 위 포함), 전립선, 유방, 간, 신장 내의 또는 이의 것뿐만 아니라 림프암, 폐암, 난소암, 췌장암, 혈액암 등), 아포토시스, 종양(일반적으로) 및 비대증, 당뇨, 뉴런 병변, 및 장기 거부반응의 치료에 유용할 수 있다.
본 발명의 화합물은 또한 뇌졸증, 척수 손상, 낫형 세포 질병, 근디스트로피, 암 치료 관련 심장독성, 말초 신경변증, 및 특히 전신 경화증의 치료에 유용하다.
본원에 기재된 펩타이드 안지오텐신 II와 관련된 질병, 장애, 및/또는 병태는 고혈압, 심부전, 뇌졸증, 신증, 폐섬유증, 예컨대 특발성 폐섬유증, 경화증, 예컨대 전신 경화증, 사르코이드증, 예컨대 폐사르코이드증, 및 이의 임의의 조합으로 구성된 군으로부터 선택될 수 있다.
AT2 수용체의 활성화는 원하거나 필요하지만, CYP 효소의 억제는 원하지 않는 특정, 질병, 장애, 및/또는 병태는 간질성 폐질병(예를 들어, 폐섬유증, IPF, 전신 경화증, 및 사르코이드증), 자가면역 질병(예를 들어, 류마티스 관절염, 전신홍반 루푸스, 다발성 경화증, 건선, 및 염증성 대장 질병), 만성 신장 질병(예를 들어, 당뇨 신경병증), 폐고혈압, 폐동맥 고혈압 및/또는 경색증(예를 들어, 심근경색증 및 뇌졸증)이다. 따라서, 본 발명의 화합물은 간질성 폐질병, 예컨대 IPF; 자가면역 질병, 예컨대 류마티스 관절염; 만성 신장 질병, 예컨대 당뇨 신경병증; 폐동맥 고혈압을 포함하는 폐고혈압; 및/또는 경색증, 예컨대 심근경색증의 치료에 특히 유용하다.
본 발명의 화합물은 ILD, 예컨대 사르코이드증 또는 섬유증, 보다 구체적으로 폐섬유증 및 특히 IPF뿐만 아니라 ILD, 예컨대 전신 경화증, 류마티스 관절염, 근염, 또는 전신 홍반 루푸스를 유발할 수 있거나 ILD와 달리 관련된 것, 예컨대 폐고혈압 및/또는 폐동맥 고혈압인 질환의 치료 및/또는 예방에 특히 권고된다.
본 발명의 화합물은 폐섬유증, 특히 IPF의 치료에 특히 유용하다.
본 발명의 추가의 양태에 따르면, 폐섬유증 및 특히 IPF의 치료 방법이 제공되며, 방법은 본 발명의 화합물의 치료적으로 유효량을 이러한 질환을 앓는 사람에게 투여하는 단계를 포함한다.
IPF를 포함하는 폐섬유증의 치료에서, 본 발명의 화합물은 섬유증의 감소 및 세포외 기질의 추가 침착의 방지를 갖는 항섬유증 효과를 가질 수 있다. 본 발명의 화합물은 폐 흉터/상처 치유를 감소시키며, 또한 항아포토시스 효과를 가짐으로써 폐섬유증의 발병에 대한 개시 인자인 폐포 내피 세포의 아포토시스를 방지할 수 있다. 본 발명의 화합물은 또한 항증식 효과를 가짐으로써 폐섬유증에서의 섬유아세포 및 근섬유아세포의 암유사 증식을 감소시킬 수 있다. 본 발명의 화합물은 또한 폐섬유증에서의 혈관 재형성(vascular remodelling)을 개선시킴으로써 2차적 폐고혈압을 감소시킬 수 있다.
본 발명의 화합물은 항염증성, 항성장 인자(예를 들어, 전환 성장 인자 베타), 및/또는 항사이토카인 효과를 추가로 입증할 수 있다.
추가적으로, 본 발명의 화합물은 또한 섬유성 결합 조직의 과도한 축적을 특징으로 하는 하나 이상의 내부 장기의 임의의 섬유증 질환의 치료 또는 예방 및/또는 섬유화(fibrogenesis)의 치료 또는 예방, 이들과 관련될 수 있는 이환률 및 사망률에 유용할 수 있다. 이러한 섬유증은 급성 염증성 질환, 예컨대 급성 호흡 곤란 증후군(ARDS), 중증 급성 호흡 증후군(SARS), 및 복합 장기 염증(multiple-organ inflammation), 손상 및/또는 부전과 관련될 수 있으며, 이는 내부 또는 외부 트라우마(예를 들어, 손상)에 의해 또는 감염에 의해 유발될 수 있다.
따라서, 이러한 질환은 바이러스성, 세균성, 또는 진균성 감염에 의해 유발된 패혈증 또는 패혈성 쇼크로부터 기인할 수 있다. 또한, 급성 폐손상, ARDS, 및 특히 SARS는 바이러스, 예컨대 신규 SARS 코로나바이러스 2(SARS-CoV-2)를 포함하는 코로나바이러스에 의해 유발될 수 있으며, 내부 조직 손상, 관련 내부(예를 들어, 점막) 조직, 예컨대 호흡기 상피의 기능장애를 초래하고, 따라서 바이러스 유발 폐렴, 손상된 폐기능, 호흡 기능장애, 곤란, 및/또는 부전에 이르게 된다. 이러한 조직 손상은 또한 중증 섬유증을 일으킬 수 있다. 이러한 조직 손상은 또한 중증 섬유증을 일으킬 수 있다. 예를 들어, 신규 코로나바이러스 SARS-CoV-2(코로나바이러스 질병 2019 또는 COVID-19)에 의해 유발된 SARS 질병은 다수의 경우에 섬유증을 초래하는 것으로 알려진다.
본 발명의 화합물은 대사성 가수분해보다 더 강력하고/하거나 안정하고/하거나 상기 언급된 허용 가능한 CYP 효소의 억제 수준을 갖는 이점을 갖는다.
본 발명의 화합물은 또한 상기 언급된 임의의 질병 상태(예컨대, IPF)의 치료에의 용도 또는 다른 것을 위해서이든 종래에 알려진 화합물보다 더 효과적이고/이거나 덜 유독하고/하거나 더 길게 작용하고/하거나 더 강력하고/하거나 더 적은 부작용을 생성하고/하거나 더 용이하게 흡수되고/되거나 더 우수한 약동학적 프로파일(예를 들어, 더 높은 경구 생체이용률 및/또는 더 낮은 청소율)을 갖고/갖거나 기타 유용한 약리학적, 물리적, 또는 화학적 특성을 가질 수 있는 이점을 가질 수 있다. 이러한 효과는 헬스 케어 전문가, 치료 대상체 또는 관찰자에 의해 임상적으로, 객관적으로, 및/또는 주관적으로 평가될 수 있다.
병용물
본 개시내용의 화합물 또는 이의 약학적으로 허용 가능한 염은 병용 요법에서 하나 이상의 추가의 약학적 약물과 조합하여 사용되어 상기 언급된 것들을 포함하는 다양한 질환을 치료할 수 있다. 본 발명의 화합물은 최소의 CYP 효소 억제를 나타내기 때문에, 이러한 병용물은 관련 질환에의 용도를 위해 이용되는 다른 치료제가 그들 스스로 CYP 효소에 의해 대사될 때 특히 이롭다.
따라서, 본 발명의 화합물은 당업계에 알려진 다른 AT2 작용제, 예컨대 C21과 조합하여, 그리고 당업계에 알려진 AT1 수용체 길항제와 조합하여, 그리고/또는 안지오텐신 전환 효소(ACE)의 억제제와 조합하여 투여될 수 있다.
실시형태에 따라 사용될 수 있는 AT1 수용체 길항체의 비제한적이되, 예시적 예는 아질사르탄, 칸데사르탄, 에프로사르탄, 피마사르탄, 이르베사르탄, 로사르탄, 밀파사르탄, 올메사르탄, 포미사르탄, 프라토사르탄, 리피아사르탄, 사프리사르탄, 타소사르탄, 텔미사르탄, 발사르탄, 및/또는 이의 조합을 포함한다. 실시형태에 따라 사용될 수 있는 ACE 억제제의 비제한적이되, 예시적 예는 캡토프릴, 조페노프릴, 에날라프릴, 라미프릴, 퀴나프릴, 페린도프릴, 리시노프릴, 베나제프릴, 이미다프릴, 트란돌라프릴, 포시노프릴, 모엑시프릴, 실라자프릴, 스피라프릴, 테모카프릴, 알라세프릴, 세로나프릴, 델레프릴, 모벨티프릴, 및/또는 이의 조합을 포함한다.
본 발명의 화합물과 조합하여 투여될 수 있는 다른 유효 성분은 이나트륨 크로모글리케이트; 엔도텔린 수용체 길항체, 예컨대 보센탄, 암브리센탄, 시탁센탄, 및 마시텐탄; PDE5 억제제, 예컨대 실데나필 및 타다라필; 프로스타사이클린(에포프로스테놀) 및 이의 유사체, 예컨대 일로프로스트 및 트레프로스티닐; 인테페론 감마-1b, 에타너셉트, 인플릭시맙, 및 아달리무맙을 포함하는 다른 생물의약품; 및 메토트렉세이트를 포함한다. 본 발명의 화합물과 공동 투여될 수 있는 개발 중인 추가의 유효 성분은 팜레브루맙(항-CTGF, Fibrogen); GLPG1690(오토택신 억제제(autotaxin inhibitor), Galapagos), TD139(갈렉틴-3 억제제, Galecto), PRM-151(재조합 펜트락신-2, Promedior), BBT-877(오토택신 억제제, Boehringer/Bridge), CC-90001(JNK 억제제, Celgene), PBI-4050(이중 GPR40 작용제/GPR84 길항제, Prometic), BMS-986020(라이소포스파티드산 수용체 길항제, BMS), RVT-1601(비만 세포 안정화제, Respivant), SMO4646(wnt 신호 억제제, United Therapeutics), KD25(Rho 관련 키나아제 억제제, Kadmon Holdings), BG00011(인테그린 길항제, Biogen), PLN-74809(인테그린 길항제, Pilant Therapeutics), Saracatinib(src 키나아제 억제제, AstraZeneca), PAT-1251(라이실옥사다제 억제제 2, PharmAkea), ABM-125(IL-25 MAB, Abeome), 및 TA5-115(다중 키나아제 억제제, Otsuka)를 포함한다.
치료되는 질환이 당업계에 알려진 간질성 폐질병, 예컨대 IPF, 전신 경화증, 또는 섬유증 질병일 때, 본 발명의 화합물은 바람직하게는 갈렉틴-3 억제제, 라이소포스파티드산 수용체 1(LPA1) 길항제, 오토택신(ATX) 억제제, 재조합 인간 펜트락신-2 단백질, 또는 피르페니돈 및/또는 닌테다닙을 비제한적으로 포함하는 이러한 치료용으로 인정된 요법과 조합하여 투여된다. 바람직하게는, 본 발명의 화합물의 조합은 피르페니돈 또는 이의 약학적으로 허용 가능한 염과의 것이며, 이러한 화합물은 CYP 효소, 예컨대 CYP1A에 의해 대사되는 것으로 알려진다.
또한, 치료되는 질환이 만성 신장 관련 질병일 때, 본 발명의 화합물은 이러한 치료에 또한 사용되는 하나 이상의 다른 약물, 예컨대 이르베사르탄 및/또는 토르세미드와 조합하여 투여되며, 이러한 화합물은 CYP 효소, 예컨대 CYPC9에 의해 대사되는 것으로 알려진다.
치료되는 질환이 폐고혈압일 때, 본 발명의 화합물은 바람직하게는 이러한 치료에 또한 사용되는 하나 이상의 다른 약물, 예컨대 셀렉시팍 및/또는 실데나필과 조합하여 투여되며, 이러한 화합물은 CYP 효소, 예컨대 CYP3A4에 의해 대사되는 것으로 알려진다.
치료되거나 예방되는 질환이 심근경색증 및/또는 뇌졸증 관련 질병일 때, 본 발명의 화합물은 바람직하게는 이러한 치료에 또한 사용되는 하나 이상의 다른 약물, 예컨대 프로프라놀롤, 와파린, 클로피도그렐, 아토르바스타틴, 실로스타졸, 리도카인, 및/또는 심바스타틴, 또는 이의 약학적으로 허용 가능한 염과 조합하여 투여되며, 이러한 화합물은 CYP 효소, 예컨대 CYP1A, CYP2CP, 및/또는 CYP3A4에 의해 대사되는 것으로 알려진다.
치료되는 질환이 자가면역 질병, 예컨대 류마티스 관절염, 다발성 경화증 또는 건선일 때, 본 발명의 화합물은 비-스테로이드 항염증 약물(NSAID), 예컨대 나프록센, 셀레콕시브, 멜록시캄 또는 이의 유사체(예를 들어, 피록시캄), 또는 인도메타신; 또는 약물, 예컨대 티자니딘, 사이클로포스파미드, 사이클로스포린, 데플라자코르트, 및/또는 하이드로코르티손, 릴루졸을 비제한적으로 포함하는 이러한 치료에 또한 사용되는 하나 이상의 다른 약물, 또는 이의 약학적으로 허용 가능한 염과 조합하여 투여되며, 이러한 화합물은 CYP 효소, 예컨대 CYP1A, CYP2CP, CYP2C19, 및/또는 CYP3A4에 의해 대사되는 것으로 알려진다.
따라서, 본 발명의 화합물은 AT2 수용체의 활성화는 원하거나 필요하지만, CYP 효소의 억제는 원하지 않는 질병, 장애, 및/또는 병태의 치료에 특히 유용하며, 따라서 상기 언급된 것들을 포함하는 질병을 치료하기 위해 피르페니돈, 나프록센, 프로프라놀롤, 릴루졸, 티자니딘, 와파린, 셀레콕시브, 클로피도그렐, 이르베사르탄, 멜록시캄, 피록시캄, 토르세미드, 사이클로포스파미드, 인도메타신, 아토르바스타틴, 실로스타졸, 사이클로스포린, 데플라자코르트, 하이드로코르티포르덴, 리도카인, 셀렉시팍, 실데나필, 및/또는 심바스타틴을 포함하는, CYP 효소 경로를 통해 대사되는, 유용하거나 유용할 수 있는 상기 언급된 하나 이상의 다른 치료제와 조합하여 투여될 수 있다. 가장 바람직하게는, 본 발명의 화합물은 간질성 폐질병, 예컨대 IPF를 치료하기 위해 피르페니돈과 조합하여 투여된다.
본 발명의 조성물과 함께 사용될 수 있는 치료제는 항바이러스성 의약품(예를 들어, 오셀타미비르, 렘데시비르, 파빌라비르, 몰누피라비르, 시메프레비르, 다클라타스비르, 소포스부비르, 리바비린, 우미페노비르, 로피나비르, 리토나비르, 로피나비르/리토나비르(Kaletra; AbbVie Deutschland GmbH Co. KG), 테이코플라닌, 바리시티닙(Olumiant; Eli Lilly), 룩소리티닙(Jakavi; Novartis), 토파시티닙(Xeljanz; Pfizer), TMPRSS2 억제제 카모스타트 또는 카모스타트 메실레이트, Actemra(Roche), AT-100(rhSP-D), MK-7110(CD24Fc; Merck)), OYA1(OyaGen9), BPI-002 (BeyondSpring), NP-120(이펜프로딜; Algernon Pharmaceuticals), 및 갈리데시브(Biocryst Pharma), 및 항염증제(예를 들어, NSAID, 예컨대 이부프로펜, 케토로락, 나프록센 등), 클로로퀸, 하이드록시클로로퀸, 인터페론(예를 들어, 인터페론 베타(인터페론 베타-1a), 토실리주맙(Actemra), 레날리도미드, 포말리도미드, 및 탈리도미드), 진통제(예를 들어, 파라세타몰 또는 오피오이드), 진해제(예를 들어, 덱스트로메토르펜), 백신(예를 들어, 입수 가능한 경우, Inovio Pharmaceuticals 및 Beijing Advaccine Biotechnology의 INO-4800), COVID-19 회복기 혈장(CCP: convalescent plasma), 및/또는 SARS-CoV 또는 SARS-CoV-2로의 감염으로부터 회복되었던 사람의 혈액으로부터의 항체를 사용한 수동 항체 요법(passive antibody therapy)을 포함하여 항체 요법(예를 들어, LY-CoV555/LY-CoV016(밤라니비맙 및 에테세비맙), LY-CoV555(밤라니비맙, Eli Lilly), REGN-COV2(카시리비맙 및 임데비맙), REGN3048-3051, TZLS-501, SNG001(Synairgen), 에쿨리주맙(Soliris; Alexion Pharmaceuticals), 라불리주맙(Ultomiris; Alexion Pharmaceuticals), 렌질루맙, 레론리맙, 토실리주맙(Actemra; Roche), 사릴루맙(Kevzara; Regeneron Pharma), 및 옥타감(Okctapharma))을 포함하는 바이러스 감염을 위해 다양하게 적용되는 표준 치료를 포함한다.
언급될 수 있는 추가의 치료제는 항섬유증(예를 들어, 닌테다닙 및 특히 피르페니돈), 비타민(예를 들어, 비타민 B, C, 및 D), 및 점액용해제(mucolytics), 예컨대 아세틸시스테인 및 암브록솔을 포함한다.
본 발명의 화합물 또는 본 발명에 따른 이의 약학적으로 허용 가능한 염과 함께 사용될 수 있는 다른 치료제는 코르티코스테로이드를 포함한다. 코르티코스테로이드는 자연 발생 코르티코스세로이드 및 합성 코르티코스테로이드를 모두 포함한다.
언급될 수 있는 자연 발생 코르티코스테로이드는 코르티솔(하이드로코르티손), 알도스테론, 코르티코스테론, 코르티손, 프레그네놀론, 프로게스테론뿐만 아니라 코르티코스테로이드 생합성에서의 자연 발생 전구체 및 중간체, 및 자연 발생 코르키코스테로이드의 다른 유도체, 예컨대 11-데옥시코르티솔, 21-데옥시코르티솔, 11-데하이드로코르티코스테론, 11-데옥시코르티코스테론, 18-하이드록시-11-데옥시코르티코스테론, 18-하이드록시코르티코스테론, 21-데옥시코르티손, 11β-하이드록시프레그네놀론, 11β,17α,21-트리하이드록시프레그네놀론, 17α,21-디하이드록시프로그네놀론, 17α-하이드록시프레그네놀론, 21-하이드록시프레그네놀론, 11-케토프로게스테론, 11β-하이드록시프로게시테론, 17α-하이드록시프로게스테론, 및 18-하이드록시프로게스테론을 포함한다.
언급될 수 있는 합성 코르티코스테로이드는 하이드로코르티손 유형(그룹 A)의 것들, 예컨대 코르티손 아세테이트, 하이드로코르티손 아세포네이트, 하이드로코르티손 아세테이트, 하이드로코르티손 부테프레이트, 하이드로코르티손 부티레이트, 하이드로코르티손 발레레이트, 틱소코르톨 및 틱소코르톨 피발레이트, 프레드니솔론, 메틸프로드니솔론, 프로드니손, 클로로프레드니손, 클로프레드놀, 디플루프레드네이트, 플루드로코르티손, 플루오시놀론, 플루페롤론, 플루프레드니솔론, 로테프레드놀, 프레드니카르베이트, 및 트리암시놀론 아세토니드 및 관련 물질(그룹 B), 예컨대 암시노니드, 부데소니드, 데소니드, 플루오시놀론 세토니드, 플루오시노니드, 할시노니드, 트리암시놀론 아세토니드, 시클레소니드, 데플라자코르트, 포르모코르탈, 플루드록시코르티드, 플루니솔리드, 및 플루오시놀론; 아세토니드, (베타)메타손 유형의 것들(그룹 C), 예컨대 베클로메타손, 베타메타손, 베타메타손 디프로피오네이트 및 베타메타손 발레레이트, 덱사메타손, 플루오코르톨론, 할로메타손, 모메타손 및 모메타손 푸로에이트, 알클로메타손 및 알클로메타손 디프로피오네이트, 클로베타솔 및 클로베타솔 프로피오네이트, 클로베타손 및 클로베타손 부티레이트, 클로코르톨론, 데속시메타손, 디플로라손, 디플루오코르톨론, 플루클로롤론, 플루메타손, 플루오코르틴, 플루프레드니덴 및 플루프레드니덴 아세테이트, 플루티카손, 플루티카손 푸로에이트 및 플루티카손 프로피오네이트, 메프레드니손, 파라메타손, 프레드닐리덴, 리멕솔론, 및 울로베타솔; 프로게스테론 유형의 것들, 예컨대 플루게스톤, 플루오로메톨론, 메드리손, 및 프레베디올론 아세테이트, 및 프로게스테론 유도체(프로게스틴), 예컨대 클로르마디논 아세테이트, 사이프로테론 아세테이트, 메드로게스톤, 메드록시프로게스테론 아세테이트, 메게스트롤 아세테이트, 및 세게스테론 아세테이트; 그리고 기타 코르티코스테로이드, 예컨대 코르티바졸 및 6-메틸-11β,17β-디하이드록시-17α-(1-프로피닐)안드로스타-1,4,6-트리엔-3-온을 포함한다.
바람직한 코르티코스테로이드는 코르티손, 프레드니손, 프로드니솔론, 메틸프레드니솔론, 및 특히 덱사메타손을 포함한다.
또한, 본 발명의 화합물 또는 이의 약학적으로 허용 가능한 염과 함께 사용될 수 있는 치료제는 H2 수용체 차단체, 항응고제, 항혈소판 약물뿐만 아니라 스타틴(statin), 항미생물제, 및 항알러지/항천식 약물을 포함한다.
언급될 수 있는 H2 수용체 차단체는 파모디딘을 포함한다. 언급될 수 있는 항응고제는 헤파린 및 저분자량 헤파린(예를 들어, 베미파린, 나드로파린, 레비파린, 에녹사파린, 파르나파린, 세르토파린, 달테파린, 틴자파린); 직접 작용 경구 항응고제(예를 들어, 다비가트란, 아르가트로반, 리바록사반, 아픽사반, 에독사반, 베트릭스사반, 다렉사반, 오타믹사반, 레탁사반, 에리박사반, 히루딘, 레피루딘, 및 비발리루딘); 쿠마린 유형 비타민 K 길항제(예를 들어, 쿠마린, 아세노쿠마롤, 펜프로쿠몬, 아트로멘틴, 및 페닌디온), 및 인자 Xa의 합성 오당류 억제제를 포함한다. 언급될 수 있는 항혈소판 약물은 비가역적 사이클로옥시게나제 억제제(예를 들어, 아스피린 및 트리플루살); 아데노신 디포스페이트 수용체 억제제(예를 들어, 칸그렐로, 클로피도그렐, 프라수그렐, 티카그렐로, 및 티클로피딘); 포스포디에스테라제 억제제(예를 들어, 클리오스타졸); 프로테아제-활성화 수용체-1 길항제(예를 들어, 보라팍사르); 당단백질 IIB/IIIA 억제제(예를 들어, 압식시맙, 엡티피바티드, 및 티로피반); 아데노신 재흡수 억제제(예를 들어, 디프리다몰); 및 트롬복산 억제제(예를 들어, 테루트로반, 라마트로반, 세라트로다스트, 및 피코타미드)를 포함한다. 언급될 수 있는 스타틴은 아토르바스타틴, 심바스타틴, 및 로수바스타틴을 포함한다. 언급될 수 있는 항미생물제는 아지트로마이신, 세프트리악손, 세푸록심, 독시사이클린, 플루코나졸, 피페라실린, 타조박탐, 및 테이코플라닌을 포함한다. 언급될 수 있는 항알러지/항천식 약물은 클로르페나민, 레보세티리진, 및 몬테루카스트를 포함한다.
따라서, 대상체는 또한 상기 언급된 하나 이상의 임의의 다른 치료제를 수용할 수 있으며(그리고/또는 이미 수용하고 있을 수 있음), 본 발명자들은 이것이 본 발명의 화합물 또는 이의 약학적으로 허용 가능한 염의 치료 전 및/또는 후에 하나 이상의 이러한 다른 치료제의 처방된 투여량을 수용하는 것을 의미한다.
본 발명의 화합물이 상기 언급된 다른 치료제와 "조합"될 때, 유효 성분은 동일한 제형으로 함께 투여될 수 있거나, 상이한 제형으로 별도로(동시에 또는 순차적으로) 투여될 수 있다.
이러한 병용 제품은 다른 치료제와 함께 본 발명의 화합물의 투여를 제공하며, 따라서 이들 제형 중 적어도 하나는 본 발명의 화합물을 포함하고, 적어도 하나는 다른 치료제를 포함하는 별도의 제형으로 각각 제시될 수 있거나, 조합된 조제약(즉, 본 발명의 화합물 및 다른 치료제를 포함하는 단일 제형으로 제시됨)으로 제시(즉, 제형화)될 수 있다.
병용물은 선택적으로 사용을 위한 사용서를 포함하는 분품 키트(kit of parts)로서 제공될 수 있다. 대안적으로, 병용물은 이들 조성물 또는 제형 중 적어도 하나는 본 발명의 화합물을 포함하고, 적어도 하나는 다른 치료제를 포함하는 단일 조성물 또는 제형으로 제공될 수 있거나, 조합된 조제약(즉, 본 발명의 화합물 및 다른 치료제를 포함하는 단일 조성물 또는 제형으로 제시됨)으로 제시(즉, 제형화)될 수 있다.
따라서, 다음이 추가로 제공된다:
(1) 본 발명의 화합물; CYP 효소에 의해 대사되는 것으로 알려진 치료제, 예컨대 상기 언급된 임의의 것들; 및 약학적으로 허용 가능한 부형제(예를 들어, 보조제, 희석제, 또는 담체)를 포함하는 약학적 조성물 또는 제형으로서, "조합된 조제약"으로 이하에서 지칭되는, 약학적 조성물 또는 제형; 및
(2) 다음 성분을 포함하는 분품 키트:
(A) 본 발명의 화합물을 약학적으로 허용 가능한 보조제, 희석제, 또는 담체와 혼합물로 포함하는 약학적 조성물 또는 제형; 및
(B) CYP 효소에 의해 대사되는 것으로 알려진 치료제, 예컨대 상기 언급된 임의의 것들을 약학적으로 허용 가능한 보조제, 희석제, 또는 담체와 혼합물로 포함하는 약학적 조성물 또는 제형, 성분 (A) 및 (B)는 각각 다른 것과 함께 투여하기에 적합한 형태로 제공됨.
본 발명의 추가의 양태에서, 상기 정의된 조합된 조제약의 제조 공정이 제공되며, 공정은 본 발명의 화합물, 다른 치료제, 및 적어도 하나의(예를 들어, 약학적으로 허용 가능한) 부형제를 회합시키는 단계를 포함한다.
본 발명의 추가의 양태에서, 상기 정의된 분품 키트의 제조 공정이 제공되며, 공정은 성분 (A)와 (B)를 회합시키는 단계를 포함한다. 본원에 사용된 바와 같이, 회합시키는 것에 대한 언급은 2개의 성분이 서로 함께 투여하기에 적합하도록 만드는 것을 의미할 것이다.
따라서, 상기 정의된 분품 키트의 제조 공정과 관련하여, 2개의 성분을 서로 "회합"되도록 하는 것이란, 본 발명자들은 분품 키트의 2개의 성분이 다음과 같을 수 있는 것을 포함한다:
(ⅰ) 별도의 조성물 또는 제형으로(즉, 서로 독립적으로) 제공될 수 있으며, 이어서 병용 요법에서 서로 함께 사용하기 위해 함께 모으는 것; 또는
(ⅱ) 병용 요법에서 서로 함께 사용하기 위해 "병용 팩"의 별도의 성분으로 함께 포장 및 제시되는 것.
따라서, 다음을 포함하는 분품 키트가 추가로 제공된다:
(Ⅰ) 본원에 정의된 성분 (A) 및 (B) 중 하나; 이와 함께
(Ⅱ) 그 성분을 2개의 성분 중 다른 것과 함께 사용하기 위한 설명서.
치료되는 환자 및 투여 경로에 따라, 본 발명의 화합물은 다양한 투여량으로 투여될 수 있다. 투여량은 환자마다 다를 것이지만, 적합한 1일 투여량은 환자당 약 0.1 내지 약 1000 mg(예를 들어, 0.1, 0.5, 1, 2, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000 mg 등, 또는 그 안의 임의의 범위 또는 값)의 범위 내에 존재하고, 단일 또는 다수 투여량으로 투여된다. 보다 바람직한 1일 투여량 환자당 약 0.1 내지 약 250 mg(예를 들어, 0.2, 0.3, 0.4, 0.5, 1, 1.5, 2, 2.5, 3, 3.5, 4. 4.5, 5, 5.5, 6, 6.5, 7, 7.5, 8, 8.5, 9, 9.5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 210, 220, 230, 240, 250 mg 등, 또는 그 안의 임의의 범위 또는 값)의 범위 내에 존재한다. 특히 바람직한 1일 투여량은 환자당 약 0.3 내지 약 100 mg의 범위 내에 존재한다.
본 발명의 화합물의 개별 투여량은 약 0.1 내지 약 100 mg(예를 들어, 0.3, 0.5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 mg 등, 또는 그 안의 임의의 범위 또는 값)의 범위 내에 존재할 수 있다.
특정 값(예컨대, 양)과 관련하여 본원에 사용될 때, 용어 "약"(또는 유사 용어, 예컨대 "대략")은 이러한 값이 정의된 값의 최대 10%(특히, 최대 5%, 예컨대 최대 1%)만큼 달라질 수 있는 것을 명시하는 것으로 이해될 수 있다. 각각의 예에서, 이러한 용어는 표기법 "±10%" 등(또는 관련 값을 기준으로 계산된 특정 양의 분산을 명시하는 것에 의해)으로 대체될 수 있는 것으로 고려된다. 각각의 예에서 이러한 용어는 삭제될 수 있는 것으로 또한 고려된다.
이러한 경우에, 의사 또는 당업자는 개별 환자에게 가장 적합할 실제 투여량을 결정할 수 있을 것이며, 이는 치료되는 질환뿐만 아니라 연령, 체중, 성별, 및 치료되는 특정 환자의 반응에 따라 달라질 수 있다. 상기 언급된 투여량은 평균 사례의 전형적 양이며; 물론 더 높거나 더 낮은 투여량 범위가 이로운 개별 예가 존재할 수 있고, 이러한 것은 본 발명의 범주 내에 존재한다.
예를 들어 투여 경로의 조합을 통해, 별도로, 및/또는 순차적으로, 및/또는 동일한 시간에 병렬적으로 본 발명의 화합물을 사용하는 이점은 부작용의 예방 및/또는 감소 가능성으로 요법을 필요로 하는 환자에 대한 맞춤 치료를 생성하며, 또한 본 발명의 화합물의 치료적으로 유효량의 정확한 투여량 수준을 조절하는 점이다.
본원에 기재된 분품 키트는 반복 투여를 제공하기 위해 적절한 양/투여량의 본 발명의 화합물을 포함하는 하나 초과의 조성물 또는 제형, 및/또는 적절한 양/투여량의 다른 치료제를 포함하는 하나 초과의 조성물 또는 제형을 포함할 수 있다. 하나 초과의 조성물 또는 제형(각각은 유효 화합물을 포함)이 존재하는 경우, 이러한 조성물 또는 제형은 각각의 화합물의 투여, 화학적 조성(들), 및/또는 물리적 형태(들)의 관점에서 동일할 수 있거나, 상이할 수 있다.
따라서, 본 발명에 따른 병용 제품의 관점에서, 용어 "함께 투여"는 병용 제품(본 발명의 화합물 및 다른 치료제)의 2개의 성분이 함께 또는 충분히 가까운 시간 내에 투여되어 환자에 대한 유익한 효과가 가능하도록 하며, 이러한 효과는 본 발명의 화합물을 포함하는 조성물 또는 제형, 또는 다른 제제를 포함하는 조성물 또는 제형이 동일한 치료 과정에 걸쳐 다른 성분 없이 단독으로(선택적으로 반복적으로) 투여되는 경우보다 관련 질환의 치료 과정에 걸쳐 더 크다. 병용물이 특정 질환의 측면에서 그리고 이의 치료 과정에 걸쳐 보다 큰 유익한 효과를 제공하는지 여부의 결정은 치료되거나 예방되는 질환에 따라 좌우될 것이지만, 당업자에 의해 일반적으로 획득될 수 있다.
또한, 본 발명에 따른 분품 키트의 맥락에서, 용어 "~와 함께"는 2개의 조성물 또는 제형 중 하나 또는 다른 것이 다른 성분의 투여 전, 후, 및/또는 동일한 시간에 (선택적으로 반복적으로) 투여될 수 있는 것을 포함한다. 이 맥락에 사용될 때, 용어 "동시에 투여되는" 및 "동일한 시간에 투여되는"은 본 발명의 관련 화합물 및 다른 치료제의 개별 투여량이 서로 48시간 내(예를 들어, 24시간)에 투여되는 것을 의미한다.
본 발명의 추가의 양태에서, 상기 정의된 병용 제품 또는 분품 키트의 제조 공정이 제공되며, 공정은 상기 정의된 본 발명의 특정 화합물을 관련 질병, 장애, 및/또는 병태의 치료에 유용한 다른 치료제, 및 적어도 하나의 약학적으로 허용 가능한 부형제와 회합시키는 단계를 포함한다.
약학적으로-허용 가능한 염
본 개시내용 및/또는 본 발명의 화합물은 약학적으로 허용 가능한 염의 형태로 제공될 수 있다. 예를 들어, 약학적으로 허용 가능한 염은 산 부가염 또는 염기부가염일 수 있다. 산 부가염은 화학식 I의 화합물 및 산, 예컨대 유기산으로부터 형성될 수 있다. 유기산은 트리플루오로아세트산, 포름산, 아세트산, 벤조산, 옥살산, 푸마르산, 말레산, 바람직하게는 트리플루오로아세트산일 수 있다. 유기산은 또한 설폰산, 예컨대 메탄설폰산, 에탄설폰산, 톨루엔설폰산 등일 수 있다. 산은 또한 무기산, 예컨대 염산, 브롬화수소산 등일 수 있다. 산 부가염의 예는 화학식 I의 화합물의 양이온 및 산의 짝염기, 예컨대 CF3C(O)O-를 포함하는 염을 포함한다. 염기 부가염은 화학식 I의 화합물 및 염기, 예컨대 유기 염기로부터 형성될 수 있다. 언급될 수 있는 염기 부가염은 알칼리 금속, 예컨대 Li, Na, 및 K 염; 알칼리 토금속, 예컨대 Mg 및 Ca 염; 기타 금속, 예컨대 Al 및 Zn 염; 또는 아민 염기, 예컨대 암모니아, 에틸렌디아민, 에탄올아민, 디에탄올아민, 트리에탄올아민, 및 트로메타민으로부터 형성된 염일 수 있다. 염기 부가염의 예는 화학식 I의 화합물의 음이온 및 양이온, 예컨대 Na+ 또는 K+를 포함하는 염을 포함한다.
용매화물
본 발명의 화합물은 용매화 형태, 예컨대 유리 화합물의 용매화물 또는 상기 화합물의 약학적으로 허용 가능한 염의 용매화물로서 존재할 수 있는 것으로 이해되어야 한다. 용어 "용매화물"은 본 개시내용의 화합물 또는 이의 약학적으로 허용 가능한 염, 및 하나 이상의 약학적으로 허용 가능한 용매 분자, 예컨대 에탄올을 포함하는 분자 복합체를 설명하기 위해 본원에 사용된다. 용어 "수화물"은 용매가 물일 때 이용된다. 따라서, 용매화 형태는 일수화물, 이수화물, 반수화물, 삼수화물, 사수화물 등을 포함할 수 있다.
전구약물
본 개시내용의 화합물은 전구약물의 형태일 수 있다. 전구약물은 자체적으로 약리학적 활성도를 거의 갖지 않거나 갖지 않을 수 있는 화합물이지만, 이러한 화합물이 환자의 신체 내로 또는 상에 투여될 때, 이는 약리학적 활성도를 보유하는 화합물로 전환된다.
다형체
본 개시내용의 화합물은 완전한 무정형 내지 완전한 결정질 범위의 고체 상태의 연속체로서 존재할 수 있다. 본 개시내용의 화합물은 또한 오일로서 존재할 수 있다. 화학식 I의 화합물이 결정질 및 부분 결정질 형태로 존재하는 경우, 이러한 형태는 본 발명의 범주 내에 포함되는 용매화물을 포함할 수 있다. 모든 다형체, 예컨대 다형체 혼합물은 청구된 화합물의 범주 내에 포함되는 것으로 이해되어야 한다.
본 발명의 화합물은 또한 용액으로(즉, 적합한 용매 중의 용액으로) 존재할 수 있다. 예를 들어, 화학식 I의 화합물이 수용액 중에 존재할 수 있으며, 이러한 경우, 본 발명의 화합물은 수화물의 형태로 존재할 수 있다.
본 발명의 화합물은 이중 결합을 함유할 수 있으며, 달리 명시되지 않는 한, 따라서 각각의 개별 이중 결합에 대한 E(반대쪽(entgegen)) 및 Z(같은쪽(zusammen)) 기하 이성질체로서 존재할 수 있다. 달리 명시되지 않는 한, 이러한 모든 이성질체 및 이의 혼합물은 본 발명의 범주 내에 포함된다.
본 발명의 화합물은 또한 상호변이성을 나타낼 수 있다. 모든 상호변이성 형태 및 이의 혼합물은 본 발명의 범주 내에 포함된다(특히, 이의 단리를 허용하는 충분한 안정성의 것들).
본 발명의 화합물은 또한 하나 이상의 비대칭 탄소 원자를 함유할 수 있으며, 따라서 광학적 그리고/또는 디아스테레오이소머리즘(diastereoisomerism)(즉, 거울상 이성질체 또는 디아스테레오머 형태로 존재)을 나타낼 수 있다. 디아스테레오이소머는 종래의 기술, 예를 들어 크로마토그래피 또는 분별 결정을 사용하여 분리될 수 있다. 다양한 입체 이성질체(즉, 거울상 이성질체)는 종래의, 예를 들어 분별 결정 또는 HPLC 기술을 사용하여 화합물의 라세믹 또는 다른 혼합물의 분리에 의해 단리될 수 있다. 대안적으로, 소기의 거울상 이성질체 또는 디아스테레오이소머는 레세미화 또는 에피더화(epimerisation)(즉, '카이랄 풀' 방법)를 유발하지 않을 조건 하에서 적절한 광학적 활성 출발 물질로부터, 이후에 적절한 단계에서 제거될 수 있는 '카이랄 보조체'과 적절한 출발 물질의 반응에 의해, 또는 유도체화(즉, 동적 분해를 포함하는 분해; 예를 들어 호모카이랄산을 사용하며, 이후 크로마토그래피와 같은 종래의 수단에 의해 디아스테레오머 유도체의 분리가 수행됨)에 의해, 또는 적절한 카이랄 시약 또는 카이랄 촉매를 사용한 반응에 의해 수득될 수 있으며, 모든 방법 및 공정은 당업자에 알려진 조건 하에서 수행될 수 있다. 달리 명시되지 않는 한, 모든 입체 이성질체 및 이의 혼합물은 본 발명의 범주 내에 포함된다.
동위원소 표지된 화합물
본 개시내용의 화합물을 이들의 표지되거나 표지되지 않은 형태로 사용될 수 있다. 본 개시내용의 화합물은 그들의 하나 이상의 원자를 다음 동위원소 중 하나 이상로 대체하여 동위원소 표지될 수 있다: 2H(중수소), 3H (삼중수소), 11C, 13C, 14C, 18O, 17O, 19F, 18F.
따라서, 본 개시내용의 화합물은 자연에서 일반적으로 발견되는(또는 자연에서 가장 풍부하게 발견되는 것) 원자 질량 또는 질량수와 상이한 원자 질량 또는 질량수를 갖는 원자로 대체된 그들의 원자 중 하나를 가질 수 있다. 본원에 명시된 임의의 특정 원자 또는 원소의 모든 동위원소는 본 발명의 화합물의 범주 내에 있는 것으로 고려된다.
제조 방법
본원에 기재된 화합물 I의 화합물은 당업계에 알려지며, 본 문서에 기재된 방법을 사용하여 제조될 수 있다.
상기 및 이하에서 기재된 공정에서, 중간체 화합물의 작용기는 보호기에 의해 보호되는 것이 필요할 수 있는 것을 당업자에 의해 인식될 것이다.
보호하는 것이 바람직한 작용기는 설폰아미도, 아미도, 아미노, 및 알데히드를 포함한다. 설폰아미도, 아미도, 및 아미드를 위한 적합한 보호기는 tert-부틸옥시카보닐, 벤질옥시카보닐, 2-트리메틸실릴에톡시카보닐(Teoc), 또는 tert-부틸을 포함한다. 알데히드를 위한 적합한 보호기는 알코올, 예컨대 메탄올 또는 에탄올, 및 디올, 예컨대 1,3-프로판디올 또는 바람직하게는 1,2-에탄디올을 포함한다(따라서, 고리형 아세탈을 형성). 작용기의 보호 및 탈보호는 하기 반응식 1에 약술된 반응 전 또는 후에 발생할 수 있다.
보호기는, 당업게에 잘 알려지며, 이하 기재되는 기술에 따라 적용 및 제거될 수 있다. 예를 들어, 본원에 기재된 보호된 화합물/중간체는 표준 탈보호 기술을 사용하여 비보호된 화합물로 화학적으로 전환될 수 있다. 포함된 화학 물질의 유형은 보호기의 필요성 및 유형뿐만 아니라 합성을 달성하기 위한 순서를 좌우할 것이다. 보호기의 사용은 "Protective Groups in Organic Synthesis", 3rd edition, T.W. Greene & P.G.M. Wutz, Wiley-Interscience (1999)에 충분히 기술되며, 이의 내용은 본원에 인용되어 포함된다.
예를 들어, 화학식 I의 화합물은 하기 반응식 1에 약술된 바와 같이 합성될 수 있다.
반응식 1에서, 디브로마이드 1은 반응 조건 a) 하에서 헤테로고리형 화합물 2와 반응하여 화합물 3을 제공한다. 디브로마이드 1은 0, 1, 2, 3, 또는 4개의 F로 치환될 수 있으며, 즉, n은 0, 1, 2, 3, 또는 4일 수 있다. 헤테로고리형 화합물 2는 치환기 R1, R2, 및 R3으로 치환되며, 이는 본원에 기재된 화학식 I의 화합물에 대해 명시된 값을 가질 수 있다. 따라서, 헤테로고리형 화합물 2는 치환된 이미다졸일 수 있다. 화합물 3은 이후에 반응 조건 b)에 적용되어 보호된 설폰 아미드 4를 제공한다. 보호된 설폰 아미드 4에 대한 값 X, Y, 및 R5는 본원에 기재된 화학식 I의 화합물에 대한 것일 수 있으며, PG는 보호기, 예컨대 tert-부틸이다. 화학식 I의 화합물의 X 및 Y 함유 모이어티는 페닐 고리, 티오펜 고리, 또는 티아졸 고리일 수 있다. 반응 조건 b)는 스즈키 크로스 커플링 조건(Suzuki cross coupling condition)을 포함할 수 있다. 이후에 반응 조건 d)를 사용하여 보호기의 제거 및 수득된 설폰 아미드 5의 화학식 I의 화합물로의 전환이 이어진다.
a), b), 및 c)에 사용된 반응 조건은 합성되는 최종 화합 물질의 구조에 따라 달라질 수 있다.
예를 들어, 이미다졸을 함유하며, X 및 Y 함유 모이어티가 페닐 고리이고, R5-Z는 이소부틸을 나타내고, R4는 0, 1, 2, 또는 3개의 F로 치환된 C1-C6 알킬을 나타내는 화학식 I의 화합물은 다음 반응 조건을 사용하여 제조될 수 있다:
a) NaH, N,N'-디메틸포름아미드, 0℃ 내지 실온, 밤새 수행되는 반응,
b) 2-(N-tert-부틸)설파모일)-5-이소부틸페닐)보론산, Pd(PPh3)4, K2CO3, 톨루엔, 에탄올, 물, 120℃, 마이크로파 조사, 1시간,
c) 트리플루오로아세트산, 실온, 밤새; 및
d) 트리에틸아민, 적절한 알킬 클로로포름에이트, 디클로로메탄, 실온, 2시간.
단계 b)의 보론산은 Bioorg. Med. Chem. Lett. 2018, 28 (3), 519-522에 보고된 바와 같이 제조될 수 있는 것으로 인식될 것이다. 대안적으로, 합성은 보론산 에스테르, 예컨대 MIDA 유도체 또는 피나콜 에스테르를 포함할 수 있다.
R1, R2, R3, R4, R5, X, Y, 및 Z에 대한 값은 본 문서에 개시된 화합물, 예컨대 화학식 I의 화합물에 대해 기재된 바와 같을 수 있는 것으로 이해된다.
본 개시내용은 또한 본원에 기재된 화학식 4 또는 5의 화합물을 제공한다. 화학식 4 또는 5의 화합물은 본원에 기재된 화학식 I의 화합물의 제조에서의 중간체로서의 역할을 할 수 있다.
실시예
다음 약어가 본 문서 전반에 걸쳐 사용된다.
약어
ACN
아세토니트릴
DAST
디에틸아미노설퍼 트리플루오라이드
DCM
디클로로메탄
DMA
N,N`-디메틸아세트아미드
DMF
N,N`-디메틸포름아미드
Dppf
1,1'-페로세네디일-비스(디페닐포스핀)
EA
에틸 아세테이트
FCC
플래시 컬럼 크로마토그래피
h
시간(들)
HFBA
헵타플루오로부티르산
HLM
인간 간 마이크로솜
HPLC
고성능 액체 크로마토그래피
HRMS (ESI)
고분해능 질량 분광기(전자분무 이온화)
Hz
헤르츠
μM
마이크로 몰
MHz
메가 헤르츠
LCM
액체 크로마토그래피
LCMS
액체 크로마토그래피 질량 분광기
MIDA
메틸-이미노디아세트산
min
분(들)
MLM
마우스 간 마이크로솜
NMR
핵자기 공명
PA
프로피온산
PBS
인산 완충 생리 식염수
RLM
래트 간 마이크로솜
TFA
트리플루오로아세트산
Xantphos
4,5-비스(디페닐포스피노)-9,9-디메틸잔텐
본 문서에서의 화합물의 명명은 ChemDraw Professional 15.0 또는 ChemDraw Professional 16.0을 사용하여 이루어졌다. 본 문서에서, 화학 물질의 명칭 및 화학 물질의 구조가 일관되지 않는 경우, 화학물질의 구조가 정확한 것으로 간주되어야 한다.
일반
모든 화학 물질 및 용매는 Sigma Aldrich, Fisher Scientific, FluoroChem, 및 Enamine으로부터 구매하고, 추가의 정제 없이 사용하였다. 마이크로파 가열은 0 내지 400 W의 전력을 갖는 2450 MHz에서의 제어된 조사를 생성하는 Biotage 단일 모드 마이크로파 반응기에서 수행하였다. 반응 온도는 빌트인 온라인 IR-센서(built-in online IR-sensor)를 사용하여 결정하고, 제어하였다. 마이크로파 매개 반응은 0.5 내지 2.0 mL, 2.0 내지 5.0 mL, 또는 10 내지 20 mL 반응 부피로 설계된 격막 밀봉된 바이얼 내에서 수행하였다. 상업적 Isolute HM-N(규조토)가 사전 패킹된 컬럼을 사용하여 미량의 물을 제거하였다. 자동화 플래시 컬럼 크로마토그래피는 상업적 실리카 카트리지를 사용하여 Biotage Isolera 또는 Grace Reveleris 기기 상에서 수행하였다. 매뉴얼 플래시 크로마토그래피는 실리카 겔 60(40 내지 63 ㎛) 상에서 수행하였다. 전치 역상 HPLC(preparative reverse-phase HPLC)는 UV(254 ㎚) 검출 및 0.05%의 수성 포름상 중의 아세토니트릴 또는 0.1%의 수성 트리플루오로아세트산 중의 아세토니트릴의 정지상을 갖는 C18 컬럼(Macherey-Nagel VP 125/21 Nucleodur C18 HTec 5 ㎛)을 사용하여 수행하였다.
분석 HPLC/ESI-MS는 1.5 ml/분의 유량에서의 0.05%의 수성 포름산 중의 아세토니트릴의 구배를 정지상으로서 갖는 C18 컬럼(50x3.0 mm, 2.6 ㎛ 입자 크기, 100 Å 기공 크기) 및 전자분무 이온화(ESI)를 사용하여 수행하였다. 고분해능 분자 질량(HRMS)은 ESI 공급원 및 7-T 하이브리드 선형 이온 트랩(LTQ)으로 장착된 질량 분광기 상에서 결정하였다. 핵자기 공명(NMR) 스펙트럼은 Varian 기기 상에서 1H에 대해 400 MHZ 및 500 MHz, 13C에 대해 101 MHz 및 126 MHz, 및 19F에 대해 376 MHz에서 기록하였다. 화학 시프트(δ)는 ppm 단위로 기록하며, 잔류 용매 피크를 내부 표준으로 갖는다(1H: 7.26 ppm에서 클로로포름-d, 2.50 ppm에서 DMSO-d6, 2.05 ppm에서 아세톤-d6, 3.31 ppm에서 메탄올-d4; 13C: 77.2 ppm에서 클로로포름-d, 39.5 ppm에서 DMSO-d6; 19F: 0.00 ppm에서 FCCl3 모세관). 커플링 상수(J)는 헤르츠(Hz) 단위로 기록한다. 모든 최종 화합물은 달리 구체적으로 언급되지 않는 한, 분석 HPLC 및/또는 NMR에 의해 결정된 95% 이상의 순도였다.
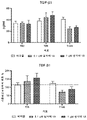
본 발명은 첨부된 도면을 참조하여 다음 실시예에 의해 예시되지만, 제한적 방식은 아니며, 도 1 내지 도 4는 C21, 실시예 1A, 실시예 12A, 및 실시예 3에 대한 48, 96, 및 144시간에서의 PCLus 배양 상청액 중의 분비된 Col1a1(Col1a1) 수준을 나타낸다. 도 5 내지 도 8은 C21, 실시예 1A, 실시예 12A, 및 실시예 3에 대한 48, 96, 및 144시간에서의 PCLus 배양 상청액 중의 분비된 TGF-β1 수준을 나타낸다. 도 9 및 도 10은 C21, 실시예 1A, 실시예 12A, 및 실시예 3의 치료를 갖는 Col1a1 및 TGF-β1(β-액틴으로 정규화됨)에 대한 144시간에서의 PCLus에서 분비된 유전자 전사 수준을 나타낸다.
실시예 1 내지 실시예 2에 대한 출발 물질의 제조
2-tert-부틸-1H-이미다졸은 Fluorochem으로부터 구매하였다.
헤테로고리의 N-알킬화
1-[(4-브로모페닐)메틸]-2-
tert
-부틸-이미다졸
NaH(0.184 g, 8.0 mmol, 2 당량)를 0℃에서 DMF(0.27 M) 중의 2-tert-부틸-1H-이미다졸(0.497 g, 4.0 mmol, 1 당량)의 교반된 용액에 첨가하였다. 20분 후에, 1-브로모-4-(브로모메틸)벤젠(1.05 g, 4.2 mmol, 1.05 당량)을 첨가하였다. 수득된 혼합물을 주위 온도로 가온되도록 하고, 밤새 교반한 다음, 물(15 mL)로 켄칭(quench)하였다. 생성물을 에틸 아세테이트(3 x 25 mL)로 추출하였다. 합친 유기층을 브라인(20 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 진공 하에서 농축하였다. 미정제 생성물을 배산(trituration)할 필요 없이 99%의 수율(1.16 g, 0.396 mmol)로 수득하였다.
MIDA 보로네이트 및
N
-알킬화 헤테로고리의 스즈키 크로스 커플링
N-tert
-부틸-2-[4-[(2-
tert
-부틸이미다졸-1-일)메틸]페닐]-4-이소부틸-벤젠설폰아미드
N-(tert-부틸)-4-이소부틸-2-(6-메틸-4,8-디옥소-1,3,6,2-디옥사자보로칸-2-일)벤젠설폰아미드(0.441 g, 1.04 mmol, 1.04 mmol), 탄산칼륨(0.083 g, 0.6 mmol, 1.5 당량), 및 테트라키스(트리페닐포스핀)팔라듐(0)(0.231 g, 0.02 mmol, 0.05 당량)을 톨루엔(0.18 M) 중에 현탁시켰다. 이 혼합물에 에탄올(0.5 M), 물(0.25 mL) 중의 1-[(4-브로모페닐)메틸]-2-tert-부틸-이미다졸(0.293 g, 1.0 mmol, 1 당량)을 첨가하였다. 수득된 반응 혼합물을 마이크로파 조사 하에 120℃에서 교반하고, 주위 온도로 냉각되도록 한고, 물(10 mL)을 첨가하고, 반응 혼합물을 에틸 아세테이트(2 x 25 mL)로 추출하였다. 합친 유기층을 브라인(25 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 FCC(이소-헥산 중의 15 내지 30% EA)에 의해 정제하여 표제 화합물을 36% 수율(0.171 g, 0.355 mmol)로 고체로서 제공하였다.
설폰아미드의 탈보호
2-[4-[(2-
tert
-부틸이미다졸-1-일)메틸]페닐]-4-이소부틸-벤젠설폰아미드
N-tert-부틸-2-[4-[(2-tert-부틸이미다졸-1-일)메틸]페닐]-4-이소부틸-벤젠설폰아미드(0.135 g, 0.28 mmol)를 주위 온도에서 트리플루오로아세트산(4.6 mL) 중에 밤새 교반하였다. 반응을 물(10 mL)로 희석하고, 생성물을 에틸 아세테이트(2 x 20 mL)로 추출하였다. 합친 유기층을 브라인(5 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 진공 하에서 농축하였다. 미정제 설폰아미드를 FCC(DCM 중의 5% MeOH)에 의해 정제하여 생성물을 86% 수율(0.102 g, 0.24 mmol)로 백색 무정형 고체로서 제공하였다.
실시예 3 내지 실시예 6에 대한 출발 물질의 제조
티아졸 설폰아미드의 합성을 위한 일반 절차
a) 2,4-디브로모티아졸의 2-알킬화
질소 분위기 하에서, Pd(OAc)2(0.03 mmol, 0.03 당량)를 건조 THF 중의 잔트포스(0.05 mmol, 0.05 당량)와 조합하였다. 5분 동안 교반 후에, 이 용액을 2,4-디브로모티아졸(1.03 mmol, 1 당량) 및 알킬아연 브로마이드(THF 중의 0.5 M, 1.08 mmol, 1.05 당량)를 보유하는 질소 하의 별도의 용기에 옮겼다. 밀봉된 용기를 80℃에서 16시간 가열하였다. 실온으로 냉각되면, 불용성 용액을 셀라이트 패드를 통한 여과에 의해 제거하였다(CH2Cl2로 용출). 여과물을 H2O(50 mL)로 희석하고, CH2Cl2(3 x 50 mL)로 추출하였다. 합친 유기 추출물을 브라인(30 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 진공 하에서 농축하여 미정제 생성물을 제공하였다. 미정제 생성물을 FCC(이소-헥산 중의 0 내지 10% 에틸 아세테이트)로 정제하여 상응하는 생성물을 55 내지 65% 수율로 제공하였다.
b) 티아졸의 설폰산 유도체의 합성
4-브로모-2-알킬화 티아졸(1 mmol, 1 당량)을 DMF(2 mL) 중에 용해시키고, 5℃로 냉각 후에, 클로로설폰산을 이러한 정도(5 mmol, 5 당량)로 천천히 첨가하였다. 이후에, 혼합물을 120℃에서 16시간 동안 교반하였다. 실온으로 냉각되면, 용매를 감압 하에서 제거하고, 미정제 물질을 컬럼 크로마토그래피(DCM 중의 10% MeOH)로 정제하여 상응하는 생성물을 제공하였다.
c) 설폰산으로부터 설포닐 클로라이드의 합성
4-브로모-2-알킬화 티아졸-5-설폰산(1 mmol, 1 당량)을 10 mL의 DCM 중에 용해시키고, PCl5(2 mmol, 2 당량)를 천천히 첨가하고, 반응 혼합물을 60℃에서 밤새 교반하였다. 반응을 물(50 mL)로 켄칭하고, 에틸 아세테이트(2 x 50 mL)로 추출하였다. 합친 유기층을 물(30 mL), 브라인(25 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 진공 하에서 농축하였다. 미정제 생성물을 FCC(이소-헥산 중의 0 내지 25% 에틸 아세테이트)로 정제하여 클로라이드 중간체를 80 내지 95% 수율로 제공하였다.
d) 4-브로모-N-(tert-부틸)-2-알킬화 티아졸-설폰아미드의 합성
클로라이드 중간체(1 mmol, 1 당량)를 DCM(2 mL) 중에 용해시키고, tert부틸아민(1.1 mmol, 1.1 당량)을 첨가하고, 반응 혼합물을 실온 하에서 밤새 교반하였다. 이어서, 반응 혼합물을 DCM(2 x 50 mL)으로 추출하였다. 합친 유기층을 물(30 mL), 브라인(25 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 진공 하에서 농축하였다. 미정제 생성물을 FCC(이소-헥산 중의 0 내지 30% 에틸 아세테이트)로 정제하여 상응하는 설폰아미드를 90 내지 95% 수율로 제공한다.
2-
tert
-부틸 이미다졸의
N
-알킬화
아세토니트릴(10 mL) 중의 2-tert-부틸 이미다졸(6.0 mol, 1 당량), 브로모벤질 브로마이드(6.0 mol, 1 당량), 및 염기 NaH(6.0 mol, 1 당량)를 실온에서 밤새 교반하였다. 반응을 물(50 mL)로 켄칭하고, 에틸 아세테이트(2 x 50 mL)로 추출하였다. 합친 유기층을 물(30 mL), 브라인(25 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 진공 하에서 농축하였다. 미정제 생성물을 FCC(이소-헥산 중의 50 내지 100% 에틸 아세테이트)로 정제하여 N-알킬화 헤테로고리를 80 내지 95% 수율로 제공하였다.
피나콜라토-보로네이트 에스테르의 합성
Pd(dppf)Cl2(0.03 mmol, 0.03 당량)를 DMF(5 mL) 중의 2-tert-부틸 이미다졸(1.0 mmol, 1 당량)과 KOAc(3.0 mmol, 3 당량)와 B2pin2(3.5 mmol, 3.5 당량)의 혼합물에 첨가하였다. 혼합물을 N2 하에 80℃에서 16시간 동안 교반하였다. 불용성 고체를 셀라이트 패드를 통한 여과에 의해 제거하였다(CH2Cl2로 용출). 여과물을 H2O(50 mL)로 희석하고, CH2Cl2(3 x 50 mL)로 추출하였다. 합친 유기 추출물을 브라인(30 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 진공 하에서 농축하여 미정제 생성물을 제공하였다. 미정제 생성물을 FCC(이소-헥산 중의 50 내지 100% 에틸 아세테이트)로 정제하여 상응하는 생성물을 80 내지 95% 수율로 제공하였다.
티아졸 설폰아미드 및 N-알킬화 헤테로고리의 보로네이트 에스테르의 스즈키 크로스 커플링에 대한 일반 절차
티아졸 설폰아미드(1 mmol, 1 당량), N-알킬화 생성물(1 mmol, 1 당량), 탄산칼륨(4 mmol, 4 당량), 및 Pd(dppf)Cl2(0.05 mmol, 0.05 당량)를 1,2-디메톡시에탄(3 mL) 및 물(0.5 mL) 중에 현탁시켰다. 밀봉된 바이얼 및 수득된 반응 혼합물을 마이크로파 조사 하에 120℃에서 60분 동안 교반하였다. 혼합물을 주위 온도로 냉각되도록 한 다음 클로로포름(3x2 mL)으로 추출하였다. 합친 유기층을 브라인(25 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 매뉴얼 FCC(DCM 중의 0 내지 10% MeOH)를 통해 단리하여 생성물을 70 내지 85% 수율로 제공하였다.
설폰아미드 생성물의 탈보호에 대한 일반 절차
스즈키 커플링된 생성물(0.15 mmol)을 50℃에서 트리플루오로아세트산(2.5 mL) 중에 밤새 교반하였다. 반응을 물(10 mL)로 희석하고, 생성물을 디클로로메탄(2 x 20 mL)으로 추출하였다. 합친 유기층을 브라인(15 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 농축하였다. 설폰아미드를 작은 실리카 플러그(아세토니트릴 중의 0 내지 5% MeOH)를 통해 정제하고, 추가의 정제 없이 다음 카바메이트 형성 반응에 사용하였다.
실시예 1A
메틸 ((4'-((2-(tert-부틸)-1
H
-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트
메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트를 기재된 바와 같이 합성하였다. 미정제 설폰아미드(55.3 mg, 0.13 mmol, 1 당량)를 DCM(0.05 M) 중에 용해시켰다. 트리에틸 아민(90 μL, 0.65 mmol, 5 당량) 및 메틸 클로로포름에이트(11 μL, 0.14 mmol, 1.1 당량)를 첨가하였다. 반응을 실온에서 2시간 동안 교반하였다. 반응 혼합물을 에틸 아세테이트(10 mL)로 희석하고, 에틸 아세테이트(3 x 5 mL)로 추출하고, 브라인(3 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 HPLC(0.05%의 포름산을 갖는 물 중의 30 내지 70% ACN)로 정제하였다. 동결건조 후에, 생성물을 백색 무정형 고체(17 mg, 27% 수율)로서 수득하였다. 1 H NMR (500 MHz, 아세톤-d 6) δ 8.11 (d, J = 8.2 Hz, 1H), 7.43 (dd, J = 8.3, 1.8 Hz, 1H), 7.41 - 7.36 (m, 2H), 7.18 - 7.09 (m, 3H), 6.91 (d, J = 1.3 Hz, 1H), 6.83 (d, J = 1.3 Hz, 1H), 5.48 (s, 2H), 3.54 (s, 2H), 2.62 (d, J = 7.2 Hz, 2H), 2.02 - 1.91 (m, 1H), 1.41 (s, 9H), 0.94 (d, J = 6.6 Hz, 6H). 13 C NMR (126 MHz, 아세톤-d 6) δ 154.6, 152.7, 148.1, 141.5, 139.7, 138.6, 136.7, 134.0, 131.1, 130.3, 129.1, 126.8, 126.7, 122.8, 53.1, 51.2, 45.3, 34.1, 30.8, 30.4, 22.6. HRMS (ESI) C26H34N3O4S+ [M+H]+에 대한 계산값 484.2270 실측값 484.2269.
실시예 1B
칼륨 ((4'-((2-(
tert
-부틸)-1
H
-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)(메톡시카보닐)아미드
칼륨 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)(메톡시카보닐)아미드를 기재된 바와 같이 제조하였다. 클로로포름(95 μM) 중의 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트(45.9 mg, 95 μmol, 1 당량)의 교반된 용액에 MeOH(0.59 M) 중의 KOH(11.1 mg, 0.198 mmol, 2 당량)를 첨가하였다. 수득된 용액을 실온에서 4시간 동안 교반하였고, 그 기간 동안 백색 고체의 침전물이 관찰되었다. 미정제 생성물을 부분 증발시키고, 펜탄(50 mL)을 사용하여 클로로포름으로부터 배산하였다. 수득된 고체를 여과한 다음, 물(5 mL) 중에 용해시켰다. 용액을 여과하여 유기 잔류물이 제거되도록 하였다. 동결 건조 후에 생성물을 93%의 수율(46.1 mg, 88 μmol)로 무정형 고체로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.86 (d, J = 8.0 Hz, 1H), 7.53 - 7.28 (m, 2H), 7.13 (dd, J = 8.1, 1.9 Hz, 1H), 7.02 - 6.90 (m, 3H), 6.86 (d, J = 1.8 Hz, 1H), 6.76 (d, J = 1.2 Hz, 1H), 5.38 (s, 2H), 3.15 (s, 3H), 2.46 (d, J = 7.1 Hz, 2H), 1.84 (dt, J = 13.6, 6.8 Hz, 1H), 1.34 (s, 9H), 0.87 (d, J = 6.6 Hz, 6H). LCMS C26H34N3O4S+ [M+H]+에 대한 계산값 484.2 실측값 484.1
실시예 2A
부틸 ((4'-((2-
(tert
-부틸)-1
H
-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트를 미정제 설폰아미드(21.3 mg, 50 μmol)이되, 부틸 클로로포름에이트(8.8 μL, 69.2 μmol)를 사용하여 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(DCM 중의 5% MeOH) 이후 미니 전치 TLC(DCM 중의 10% MeOH)로 정제하여 DCM으로부터 이소-헥산을 사용하여 배산 후에 생성물을 백색 무정형 고체(5 mg, 21% 수율)로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.11 (d, J = 8.2 Hz, 1H), 7.44 (dd, J = 8.2, 1.9 Hz, 1H), 7.37 (d, J = 8.2 Hz, 2H), 7.24 - 7.00 (m, 3H), 6.88 (d, J = 1.3 Hz, 1H), 6.80 (d, J = 1.3 Hz, 1H), 5.47 (s, 2H), 3.96 (t, J = 6.5 Hz, 2H), 2.62 (d, J = 7.2 Hz, 2H), 2.03 - 1.86 (m, 1H), 1.51 - 1.39 (m, 2H), 1.28 - 1.16 (m, 2H), 0.93 (d, J = 6.6 Hz, 6H), 0.85 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 154.6, 151.6, 148.3, 141.6, 139.5, 138.8, 136.5, 134.1, 131.1, 130.3, 129.2, 126.9, 126.9, 122.8, 66.5, 51.2, 45.3, 34.1, 31.3, 30.8, 30.4, 22.5, 19.5, 13.9. HRMS (ESI) C29H40N3O4S+ [M+H]+에 대한 계산값 526.2740 실측값 526.2731.
실시예 2B
칼륨 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)(부톡시카보닐)아미드
표제 화합물을 MeOH(0.59 M) 중의 부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)-카바메이트(20.4 mg, 38.5 μmol, 1.0 당량) 및 KOH(2.33 mg, 41.6 μmol, 1.08 당량)를 사용하여 실시예 1B에 대해 기재된 바와 합성하였다. 생성물을 백색 무정형 고체(16.5 mg, 76% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6 ) δ7.85 (d, J = 8.1 Hz, 1H), 7.45 -7.35 (m, 2H), 7.12 (dd, J = 8.1, 1.8 Hz, 1H), 6.94 (dd, J = 4.7, 3.4 Hz, 3H), 6.84 (d, J = 1.8 Hz, 1H), 6.76 (d, J = 1.2 Hz, 1H), 5.37 (s, 2H), 3.54 (t, J = 6.5 Hz, 2H), 2.45 (d, J = 7.1 Hz, 2H), 1.91 -1.74 (m, 1H), 1.34 (s, 9H), 1.30 (d, J = 6.8 Hz, 2H), 1.27 -1.13 (m, 2H), 0.87 (d, J = 6.6 Hz, 6H), 0.83 (t, J = 7.3 Hz, 3H). LCMS 29H40N3O4S+ [M+H]+에 대한 계산값 526.2734 실측값 526.2.
실시예 3
메틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트
DCM(2 mL) 중의 상응하는 설폰아미드(0.12 mmol, 1 당량)와 트리에틸아민(0.58 mmol, 5 당량)의 혼합물에 메틸 클로로포름에이트(0.17 mmol, 1.5 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 실온에서 20분 동안 교반하였다. 반응 혼합물을 물로 켄칭하고, DCM(25 mL)으로 희석한 다음, 10% 시트르산(수용액, 20 mL), 물(3 x 30 mL), 및 브라인(20 mL)으로 순차적으로 추출하였다. 합친 유기층을 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(40 mg, 71% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.26 (d, J = 8.4 Hz, 2H), 7.13 (d, J = 8.4 Hz, 2H), 7.09 (d, J = 1.5 Hz, 1H), 7.03 (d, J = 1.5 Hz, 1H), 5.56 (s, 2H), 3.40 (s, 3H), 2.83 (d, J = 7.1 Hz, 2H), 2.19 - 2.09 (m, 1H), 1.45 (s, 9H), 1.02 (d, J = 6.7 Hz, 6H). 13 C NMR (101 MHz, 아세톤-d 6) δ 168.5, 160.3, 153.5, 150.7, 137.7, 137.4, 133.9, 130.4, 125.6, 124.0, 122.7, 51.5, 50.8, 41.6, 33.4, 29.3, 29.1, 21.7. HRMS (ESI): C23H31N4O4S2 + [M+H]+에 대한 계산값 491.1781; 실측값: 491.1795.
실시예 4
부틸 ((4-(4-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트
DCM(2 mL) 중의 상응하는 설폰아미드(0.12 mmol, 1 당량)와 트리에틸아민(0.58 mmol, 5 당량)의 혼합물에, 부틸 클로로포름에이트(0.17 mmol, 1.5 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 실온에서 20분 동안 교반하였다. 반응 혼합물을 물로 켄칭하고, DCM(25 mL)으로 희석한 다음, 10% 시트르산(수용액 20 mL), 물(3 x 30 mL), 및 브라인(20 mL)으로 순차적으로 추출하였다. 합친 유기층을 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(39 mg, 63% 수율)로서 수득하였다. 1 H NMR (400 MHz, 클로로포름-d) δ 7.98 (d, J = 8.1 Hz, 2H), 7.03 (d, J = 8.1 Hz, 2H), 6.92 (d, J = 1.5 Hz, 1H), 6.80 (d, J = 1.5 Hz, 1H), 5.30 (s, 2H), 3.81 (t, J = 6.8 Hz, 2H), 2.77 (d, J = 7.1 Hz, 2H), 2.15 - 2.04 (m, 1H), 1.44-1.40 (m, 11H), 1.23 - 1.14 (m, 2H), 0.97 (d, J = 6.6 Hz, 6H), 0.80 (t, J = 7.3 Hz, 3H). 13 C NMR (101 MHz, 클로로포름-d) δ 170.5, 160.3, 153.9, 152.5, 137.0, 135.1, 133.7, 130.3, 126.1, 124.4, 122.5, 66.0, 51.0, 42.2, 33.5, 30.9, 29.6, 29.6, 22.3, 19.0, 13.8. HRMS (ESI): C26H37N4O4S2 + [M+H]+에 대한 계산값 533.2251; 실측값: 533.2241.
실시예 5
메틸 ((4-(4-((2-(
tert
-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트
DCM(2 mL) 중의 설폰아미드(0.12 mmol, 1 당량)와 트리에틸아민(0.60 mmol, 5 당량)의 혼합물에, 메틸 클로로포름에이트(0.14 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 실온에서 20분 동안 교반하였다. 반응 혼합물을 물로 켄칭하고, DCM(25 mL)로 희석한 다음, 10% 시트르산(수용액 20 mL), 물(3 x 30 mL), 및 브라인(20 mL)으로 순차적으로 추출하였다. 합친 유기층을 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(28 mg, 49% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.12 (d, J = 8.4 Hz, 2H), 7.03 (d, J = 3.7 Hz, 2H), 7.01 - 6.96 (m, 2H), 5.47 (s, 2H), 5.23 (s, 1H), 3.27 (s, 3H), 2.79 (t, J = 7.2 Hz, 2H), 1.77 - 1.60 (m, 2H), 1.34 (s, 9H), 0.89 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 169.7, 160.4, 153.4, 150.7, 137.5, 137.0, 134.0, 130.4, 125.7, 123.1, 123.0, 51.6, 51.0, 34.7, 33.5, 28.9, 22.8, 13.1. HRMS (ESI): C22H29N4O4S2 + [M+H]+에 대한 계산값 477.1625; 실측값: 477.1631.
실시예 6
부틸 ((4-(4-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐) 카바메이트
DCM(2 mL) 중의 상응하는 설폰아미드(0.12 mmol, 1 당량)와 트리에틸아민(0.60 mmol, 5 당량)의 혼합물에 부틸 클로로포름에이트(0.14 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 실온에서 20분 동안 교반하였다. 반응 혼합물을 물로 켄칭하고, DCM(25 mL)로 희석한 다음, 10% 시트르산(수용액 20 mL), 물(3 x 30 mL), 및 브라인(20 mL)으로 순차적으로 추출하였다. 합친 유기층을 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(43 mg, 69% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.26 (d, J = 8.5 Hz, 2H), 7.10 (d, J = 8.5 Hz, 2H), 7.05 (d, J = 1.5 Hz, 1H), 6.97 (d, J = 1.5 Hz, 1H), 5.86 (s, 1H), 5.54 (s, 2H), 3.84 (t, J = 6.6 Hz, 2H), 2.92 (t, J = 7.6 Hz, 2H), 1.88 - 1.76 (m, 2H), 1.48 - 1.43 (m, 11H), 1.32 - 1.23 (m, 2H), 1.03 (t, J = 7.4 Hz, 3H), 0.86 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 169.5, 160.0, 153.5, 150.6, 137.7, 137.6, 133.9, 130.4, 125.6, 124.4, 122.6, 64.4, 50.7, 34.7, 33.4, 31.1, 29.2, 22.8, 19.0, 13.3, 13.1. HRMS (ESI): C25H35N4O4S2 + [M+H]+에 대한 계산값 519.2094; 실측값: 519.2096.
실시예 7A
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트
실온에서 DCM(1.0 mL) 중의 상응하는 설폰아미드(74.3 mg, 0.156 mmol)와 트리에틸 아민(108.6 μL, 0.78 mmol, 5 당량)의 교반된 용액에 부틸 클로로포름에이트(27.5 μL, 0.216 mmol)를 첨가하였다. 20분 후에, 반응을 물(2 mL)로 켄칭하였다. 미정제 생성물을 DCM(3 x 5 mL)으로 추출하고, 브라인(5 mL)으로 세정하고, 무수 MgSO4 상에서 건조하고, 농축하였다. 미정제 생성물을 FCC(DCM 중의 5% MeOH)로 정제하여 생성물을 47% 수율로 백색 무정형 고체로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.11 (d, J = 8.2 Hz, 1H), 7.43 (dd, J = 8.2, 1.8 Hz, 1H), 7.38 - 7.29 (m, 2H), 7.29 - 7.23 (m, 2H), 7.14 (d, J = 1.8 Hz, 1H), 6.89 (d, J = 1.3 Hz, 1H), 6.77 (d, J = 1.3 Hz, 1H), 5.65 (s, 2H), 3.96 (t, J = 6.5 Hz, 2H), 2.62 (d, J = 7.2 Hz, 2H), 2.01 - 1.88 (m, 1H), 1.63 (s, 6H), 1.51 - 1.39 (m, 2H), 1.32 - 1.15 (m, 2H), 0.93 (d, J = 6.6 Hz, 6H), 0.85 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 153.0, 151.8, 148.1, 141.6, 139.5, 138.7, 136.6, 134.1, 131.1, 130.2, 129.1, 127.7, 126.7, 122.1, 71.1, 66.4, 50.9, 45.3, 31.3, 31.0, 30.8, 22.5, 19.5, 13.9. HRMS (ESI) C28H38N3O5S+ [M+H]+에 대한 계산값 528.2532 실측값 528.2526.
실시예 7B
칼륨 (부톡시카보닐)((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)아미드
클로로포름 중의 부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트(39 mg, 73.9 μmol)의 교반된 용액에 MeOH 중의 KOH(4.47 mg, 79.8 μmol)를 첨가하였다. 수득된 용액을 실온에서 4시간 동안 교반하고, 그 기간 동안 백색 고체의 침전물이 관찰되었다. 미정제 생성물을 부분 증발시키고, 펜탄(50 mL)을 사용하여 클로로포름으로부터 배산하였다. 수득된 고체를 여과한 다음, 물(5 mL) 중에 용해시켰다. 용액을 여과하여 유기 잔류물이 제거되도록 하였다. 생성물을 99% 수율(41.5 mg, 73.4 μmol)로 백색 무정형 고체로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.86 (d, J = 8.1 Hz, 1H), 7.40 (d, J = 8.1 Hz, 2H), 7.11 (t, J = 8.1 Hz, 3H), 6.93 (d, J = 1.3 Hz, 1H), 6.85 (d, J = 1.8 Hz, 1H), 6.74 (d, J = 1.2 Hz, 1H), 5.53 (s, 2H),5.42 (s, 1H), 3.54 (t, J = 6.5 Hz, 2H), 2.49 -2.42 (m, 2H), 1.90 -1.73 (m, 1H), 1.52 (s, 6H), 1.39 -1.26 (m, 2H), 1.27 -1.13 (m, 2H), 0.87 (d, J = 6.6 Hz, 6H), 0.83 (t, J= 7.3 Hz, 3H).
실시예 8A
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트(16.2 mg, 30.7 μmol)를 마이크로파 조사 하에 120도(7 bar 압력)에서 MeOH(1 mL) 중에 20분 동안 교반하였다. 미정제 생성물을 FCC(DCM 중의 2 내지 4% MeOH)로 정제하여 생성물을 백색 무정형 고체(14.7 mg, 99% 수율)로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.12 (d, J = 8.2 Hz, 1H), 7.42 (dd, J = 8.2, 1.8 Hz, 1H), 7.39 - 7.30 (m, 2H), 7.25 (d, J = 8.2 Hz, 2H), 7.13 (d, J = 1.8 Hz, 1H), 6.90 (d, J = 1.3 Hz, 1H), 6.77 (d, J = 1.3 Hz, 1H), 5.89 (s, 1H), 5.65 (s, 2H), 3.54 (s, 3H), 2.61 (d, J = 7.2 Hz, 2H), 2.02 - 1.84 (m, 1H), 1.63 (s, 6H), 0.92 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 아세톤-d 6) δ 153.0, 152.6, 148.0, 141.6, 139.6, 138.6, 136.6, 134.0, 131.2, 130.2, 129.0, 127.7, 126.5, 122.2, 71.1, 53.1, 50.9, 45.3, 30.9, 30.7, 22.5. HRMS (ESI + ) C25H32N3O5S+ [M+H]+에 대한 계산값 486.2063 실측값486.2060.
실시예 8B
칼륨 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)(메톡시카보닐)아미드
표제 화합물을 메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트(14.7 mg, 30.2 μmol) 및 KOH(1.83 mg, 32.7 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(2-하이드록시프로판-2-일)-1H이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(15.7 mg, 99% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.86 (d, J = 8.0 Hz, 1H), 7.42 (d, J = 8.2 Hz, 2H), 7.16 - 7.06 (m, 3H), 6.94 (d, J = 1.3 Hz, 1H), 6.86 (d, J = 1.8 Hz, 1H), 6.74 (d, J = 1.3 Hz, 1H), 5.53 (s, 2H), 5.43 (s, 1H), 3.15 (s, 3H), 2.46 (d, J = 7.1 Hz, 2H), 2.02 - 1.74 (m, 1H), 1.52 (s, 6H), 0.87 (d, J = 6.6 Hz, 6H).
실시예 9A
부틸 ((4'-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(107 mg, 0.261 mmol) 및 부틸 클로로포름에이트(45.8 μL, 0.360 mmol)를 사용하여 부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(48 mg, 36%)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.14 (d, J = 8.2 Hz, 1H), 7.46 (dd, J = 8.2, 1.9 Hz, 1H), 7.44 - 7.36 (m, 2H), 7.26 - 7.11 (m, 3H), 6.92 (d, J = 1.4 Hz, 1H), 6.83 (d, J = 1.4 Hz, 1H), 5.50 (s, 2H), 3.97 (t, J = 6.5 Hz, 2H), 2.80 - 2.64 (m, 2H), 1.80 - 1.66 (m, 2H), 1.53 - 1.44 (m, 2H), 1.44 (s, 9H), 1.30 - 1.18 (m, 2H), 0.97 (t, J = 7.3 Hz, 3H), 0.87 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 154.5, 152.2, 148.9, 141.5, 139.8, 138.2, 136.8, 133.4, 131.2, 130.3, 128.4, 126.9, 126.2, 122.8, 66.2, 51.3, 38.0, 34.1, 31.3, 30.3, 24.9, 19.5, 14.0, 13.9. HRMS (ESI + ) C28H38N3O4S+ [M+H]+에 대한 계산값: 512.2583; 실측값: 512.2577.
실시예 9B
칼륨 (부톡시카보닐)((4'-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트(18.8 mg, 36.4 μmol) 및 KOH(2.20 mg, 39.3 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(2-하이드록시프로판-2-일)-1H이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.85 (d, J = 8.1 Hz, 1H), 7.41 (d, J = 8.2 Hz, 2H), 7.16 (dd, J = 8.1, 1.8 Hz, 1H), 6.96 - 6.92 (m, 3H), 6.88 (d, J = 1.8 Hz, 1H), 6.76 (d, J = 1.3 Hz, 1H), 5.37 (s, 2H), 3.54 (t, J = 6.5 Hz, 2H), 2.60 - 2.52 (m, 2H), 1.73 - 1.49 (m, 2H), 1.36 - 1.30 (m, 2H), 1.34 (s, 9H), 1.25 - 1.11 (m, 2H), 0.89 (t, J = 7.3 Hz, 3H), 0.83 (t, J = 7.3 Hz, 3H).
실시예 10A
메틸 ((4'-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트(18.8 mg, 33.3 μmol)를 사용하여 메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(CH2Cl2 중의 4 내지 6% MeOH)로 정제하여 생성물을 백색 무정형 고체(41.5 mg, 86% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.12 (d, J = 8.2 Hz, 1H), 7.49 (s, br., 1H), 7.44 (dd, J = 8.2, 1.9 Hz, 1H), 7.42 - 7.36 (m, 2H), 7.21 - 7.04 (m, 3H), 6.91 (d, J = 1.4 Hz, 1H), 6.83 (d, J = 1.4 Hz, 1H), 5.49 (s, 2H), 3.53 (s, 3H), 2.71 (dd, J = 8.6, 6.7 Hz, 2H), 1.81 - 1.60 (m, 2H), 1.42 (s, 9H), 0.95 (t, J = 7.3 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 154.5, 152.9, 148.9, 141.5, 139.9, 138.1, 136.8, 133.3, 131.3, 130.3, 128.4, 126.9, 126.1, 122.9, 53.0, 51.3, 38.1, 34.1, 30.2, 24.9, 14.0. HRMS (ESI + ) C25H32N3O4S+ [M+H]+에 대한 계산값: 470.2114; 실측값: 470.2115.
실시예 10B
칼륨 ((4'-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)(메톡시카보닐)아미드
표제 화합물을 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트(42.4 mg, 89.4 μmol) 및 KOH(5.41 mg, 96.5 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(2-하이드록시프로판-2-일)-1H이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(42.2 mg, 93% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.86 (d, J = 8.1 Hz, 1H), 7.43 (d, J = 8.2 Hz, 2H), 7.16 (dd, J = 8.1, 1.9 Hz, 1H), 7.05 - 6.91 (m, 3H), 6.89 (d, J = 1.8 Hz, 1H), 6.77 (d, J = 1.2 Hz, 1H), 5.38 (s, 2H), 3.15 (s, 3H), 2.58 - 2.52 (m, 2H), 1.66 - 1.52 (m, 2H), 1.34 (s, 9H), 0.90 (t, J = 7.3 Hz, 3H).
실시예 11A
부틸 ((3-(4-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(168 mg, 0.389 mmol) 및 부틸 클로로포름에이트(68.3 μL, 0.537 mmol)를 사용하여 부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(DCM 중의 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(179 mg, 87%)로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.79 - 7.66 (m, 2H), 7.12 (d, J = 8.1 Hz, 2H), 7.03 (d, J = 1.5 Hz, 1H), 6.95 - 6.79 (m, 2H), 5.54 (s, 2H), 2.72 (d, J = 7.1 Hz, 2H), 2.00 - 1.87 (m, 6.7 Hz, 1H), 1.54 - 1.44 (m, 2H), 1.43 (s, 9H), 1.32 - 1.18 (m, 4H), 0.99 (d, J = 6.6 Hz, 6H), 0.86 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 154.3, 154.1, 149.4, 144.0, 137.8, 136.0, 135.3, 130.5, 130.0, 127.1, 124.5, 123.4, 65.8, 51.6, 39.5, 34.3, 31.5, 31.2, 29.9, 22.5, 19.6, 14.0. HRMS (ESI + ) C27H38N3O4S2 + [M+H]+에 대한 계산값 532.2304 실측값 532.2300.
실시예 11B
칼륨 (부톡시카보닐)((3-(4-((2-(
tert
-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)아미드
표제 화합물을 MeOH(0.59 M) 중의 부틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트(33.1 mg, 67 μmol, 1.0 당량) 및 KOH(4.06 mg, 72.3 μmol, 1.08 당량)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(29.7 mg, 87% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.77 (d, J = 8.3 Hz, 2H), 7.03 - 6.89 (m, 3H), 6.86 - 6.69 (m, 2H), 5.37 (s, 2H), 3.23 (s, 3H), 2.60 (d, J = 6.9 Hz, 6H), 1.91 - 1.70 (m, 1H), 1.31 (s, 9H), 0.93 (d, J = 6.6 Hz, 6H).
실시예 12A
메틸 ((3-(4-((2-
(tert-
부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트
부틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트(45.8 mg, 86.1 μmol)를 마이크로파 조사 하에 120℃에서 MeOH(1 mL) 중에 20분 동안 교반하였다. 미정제 생성물을 농축하고, FCC(DCM 중의 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(35.7 mg, 85% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.65 (d, J = 8.3 Hz, 2H), 7.21 - 7.03 (m, 4H), 6.74 (s, 1H), 5.51 (s, 2H), 3.47 (s, 3H), 2.73 - 2.61 (m, 2H), 1.97 - 1.83 (m, 1H), 1.50 (s, 9H), 0.97 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 메탄올-d 4) δ 158.5, 154.0, 148.5, 143.1, 136.9, 136.3, 135.2, 130.8, 129.5, 127.2, 124.3, 121.2, 52.7, 52.4, 39.7, 34.3, 31.2, 29.2, 22.5. HRMS (ESI + ) C24H33N3O4S2 + [M+H]+에 대한 계산값 490.1834 실측값 490.1838.
실시예 12B
칼륨 ((3-(4-((2-(
tert
-부틸)-1
H
-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)(메톡시카보닐)아미드
표제 화합물을 MeOH(0.59 M) 중의 메틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트(33.1 mg, 67 μmol, 1.0 당량) 및 KOH(4.06 mg, 72.3 μmol, 1.08 당량)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(29.7 mg, 87% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.77 (d, J = 8.3 Hz, 2H), 7.03 - 6.89 (m, 3H), 6.86 - 6.69 (m, 2H), 5.37 (s, 2H), 3.23 (s, 3H), 2.60 (d, J = 6.9 Hz, 6H), 1.91 - 1.70 (m, 1H), 1.31 (s, 9H), 0.93 (d, J = 6.6 Hz, 6H).
실시예 13
나트륨 ((3-(4-((1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)(부톡시카보닐)아미드
디클로로메탄(380 mL) 중의 부틸 ((3-(4-((1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트(100 g, 0.210 mol) 용액을 셀라이트 비드를 통해 여과하였다. 여과물에 메탄올(198 g) 중의 3.3% NaOH 용액을 25 내지 30℃에서 첨가하고, 교반 하에 동일한 온도에서 1시간 동안 유지하였다. 상기 용액을 농축하여 대략 200 mL를 얻었고, 잔류물을 25 내지 30℃로 냉각하고, 1.46 L의 이소프로필을 첨가하였다. 수득된 용액을 농축하여 대략 400 mL의 유성 시럽을 얻었다. 헵탄(1.18 l)을 교반 하에 유성 시럽에 천천히 첨가하였다. 수득된 고체를 여과하고, 헵탄(200 mL)으로 세정하였다. 고체 염을 50℃ 미만에서 8시간 동안 건조하여 85% 수율(89 g, 0.178 mol)의 나트륨 ((3-(4-((1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)(부톡시카보닐)아미드(C21)를 98% 초과의 HPLC 순도를 갖는 백색 고체로서 얻었다.
실시예 14
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.16 mmol, 1 당량) 및 트리에틸아민(0.8 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 부틸클로로포름에이트(0.2 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(48 mg, 55% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.81 (d, J = 8.4 Hz, 2H), 7.27 - 7.16 (m, 4H), 5.63 (s, 2H), 3.78 (t, J = 6.5 Hz, 2H), 2.89 (dd, J = 8.0, 7.2 Hz, 2H), 1.80 - 1.71 (m, 2H), 1.58 (s, 6H), 1.41 - 1.32 (m, 2H), 1.20 - 1.14 (m, 2H), 0.95 (t, J = 7.4 Hz, 3H), 0.77 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 173.1, 157.2, 152.9, 151.7, 136.3, 133.5, 135.0, 130.1, 126.9, 123.3, 120.1, 69.3, 64.8, 51.2, 34.6, 30.7, 28.4, 22.9, 18.7, 12.7, 12.5. HRMS (ESI): C24H33N4O5S2 + [M+H]+에 대한 계산값 521.1887; 실측값: 521.1879.
실시예 15
부틸 ((4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일) 설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.17 mmol, 1 당량) 및 트리에틸아민(0.86 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 부틸클로로포름에이트(0.2 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(51 mg, 58% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.32 - 8.19 (m, 2H), 7.8 - 7.16 (m, 3H), 7.01 (d, J = 1.5 Hz, 1H), 5.34 (s, 2H), 3.83 (t, J = 6.7 Hz, 2H), 3.26-3.18 (m, 1H), 2.97 - 2.85 (m, 2H), 1.80 (dt, J = 15.3, 7.6 Hz, 2H), 1.56 - 1.38 (m, 2H), 1.37 - 1.17 (m, 8H), 1.02 (t, J = 7.4 Hz, 3H), 0.86 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 169.4, 160.2, 152.6, 150.5, 137.9, 137.1, 134.1, 130.4, 126.0, 125.1, 120.1, 64.3, 48.9, 34.7, 31.1, 25.6, 22.8, 21.1, 19.0, 13.3, 13.1. HRMS (ESI): C24H33N4O4S2 + [M+H]+에 대한 계산값 505.1938; 실측값: 505.1930.
실시예 16
부틸 ((2-이소부틸-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.11 mmol, 1 당량) 및 트리에틸아민(0.54 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 부틸클로로포름에이트(0.13 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(31 mg, 51% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.97 (d, J = 8.4 Hz, 2H), 7.89 (d, J = 3.3 Hz, 1H), 7.62 (d, J = 3.3 Hz, 1H), 7.37 (d, J = 1.2 Hz, 1H), 7.35 (d, J = 8.7 Hz, 2H), 7.11 (d, J = 1.2 Hz, 1H), 6.02 (s, 2H), 3.97 (t, J = 6.5 Hz, 2H), 2.92 (d, J = 7.1 Hz, 2H), 2.16 (dt, J = 13.5, 6.8 Hz, 1H), 1.52 - 1.42 (m, 2H), 1.30 - 1.19 (m, 2H), 1.03 (d, J = 6.6 Hz, 6H), 0.86 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 172.3, 160.1, 154.5, 153.0, 143.3, 140.2, 138.9, 132.8, 132.3, 130.1, 129.5, 127.0, 123.7, 120.0, 65.7, 49.9, 41.7, 30.5, 29.4, 21.6, 18.7, 13.1. HRMS (ESI): C25H30N5O4S3 + [M+H]+에 대한 계산값 560.1454; 실측값: 560.1453.
실시예 17
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지된 것을 제외하고, 상응하는 설폰아미드(0.18 mmol, 1 당량) 및 트리에틸아민(0.9 mmol, 5 당량)을 사용하여 메틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 부틸클로로포름에이트(0.22 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(51 mg, 52% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.94 (d, J = 8.4 Hz, 2H), 7.37 - 7.28 (m, 4H), 5.75 (s, 2H), 3.90 (t, J = 6.5 Hz, 2H), 2.90 (d, J = 7.2 Hz, 2H), 2.18-2.11 (m, 1H), 1.70 (s, 6H), 1.55 - 1.44 (m, 2H), 1.34 - 1.23 (m, 2H), 1.05 (d, J = 6.7 Hz, 6H), 0.89 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 172.0, 157.3, 152.8, 151.6, 136.3, 135.3, 133.5, 130.1, 126.9, 123.3, 120.1, 69.4, 64.8, 51.2, 41.5, 30.7, 29.6, 28.4, 21.2, 18.7, 12.7. HRMS (ESI): C19H22N4O4S2 [M+H]+에 대한 계산값 435.1155; 실측값: 435.1174. HRMS (ESI): C25H35N4O5S2 + [M+H]+에 대한 계산값 535.2043; 실측값: 535.2035.
실시예 18
부틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(80.0 mg, 0.191 mmol) 및 부틸 클로로포름에이트(29.6 μL, 0.232 mmol)를 사용하여 부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(MeCN 중의 0 내지 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(51 mg, 51% 수율)로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.26 (d, J = 8.4 Hz, 2H), 7.20 -7.19 (m, 3H), 7.05 (d, J = 1.4 Hz, 1H), 5.36 (s, 2H), 3.83 (t, J = 6.7 Hz, 2H), 3.30 - 3.18 (m, 1H), 2.83 (d, J = 7.1 Hz, 2H), 2.20 - 2.08 (m, 1H), 1.49 - 1.40 (m, 2H), 1.33 - 1.21 (m, 8H), 1.02 (d, J = 6.6 Hz, 6H), 0.86 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d6) δ 168.4, 160.01, 152.5, 150.5, 138.0, 136.9, 134.1, 130.6, 126.1, 124.8, 120.2, 64.3, 49.0, 41.6, 31.1, 29.4, 25.6, 21.7, 21.0, 18.9, 13.2. HRMS (ESI + ): C25H35N4O4S2 + [M+H]+에 대한 계산값 519.2094; 실측값: 519.2084.
실시예 19
메틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.13 mmol, 1 당량) 및 트리에틸아민(0.69 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.16 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(41 mg, 60% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.81 (d, J = 8.4 Hz, 2H), 7.28 (d, J = 2.0 Hz, 1H), 7.27 (d, J = 2.0 Hz, 1H), 7.23 (d, J = 8.4 Hz, 2H), 5.64 (s, 2H), 3.37 (s, 3H), 2.79 (d, J = 7.2 Hz, 2H), 2.08 - 1.97 (m, 1H), 1.58 (s, 6H), 0.93 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 메탄올-d4) δ 172.2, 157.7, 152.9, 151.5, 135.9, 135.0, 133.7, 130.2, 126.9, 123.6, 119.3, 69.3, 51.5, 51.4, 41.4, 29.6, 28.2, 21.2. HRMS (ESI): C22H29N4O5S2 + [M+H]+에 대한 계산값 493.1574; 실측값: 493.1566.
실시예 20
메틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.16 mmol, 1 당량) 및 트리에틸아민(0.83 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.2 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(41 mg, 51% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.85 (d, J = 8.4 Hz, 2H), 7.09 (d, J = 8.6 Hz, 2H), 7.05 (d, J = 1.6 Hz, 1H), 6.95 (d, J = 1.6 Hz, 1H), 5.20 (s, 2H), 3.32 (s, 3H), 3.14 - 3.05 (m, 1H), 2.76 (d, J = 7.2 Hz, 2H), 2.01 (dt, J = 13.5, 6.8 Hz, 1H), 1.13 (d, J = 6.9 Hz, 6H), 0.92 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 메탄올-d 4) δ 171.0, 160.5, 153.1, 151.8, 136.8, 136.5, 133.5, 130.2, 126.0, 124.0, 120.4, 51.1, 49.0, 41.4, 29.6, 25.5, 21.2, 20.4. HRMS (ESI): C22H29N4O4S2 + [M+H]+에 대한 계산값 477.1625; 실측값: 477.1618.
실시예 21
부틸 ((2-프로필-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.11 mmol, 1 당량) 및 트리에틸아민(0.56 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 부틸클로로포름에이트(0.14 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(37 mg, 60% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.95 (d, J = 8.3 Hz, 2H), 7.89 (d, J = 3.3 Hz, 1H), 7.63 (d, J = 3.3 Hz, 1H), 7.38 (d, J = 1.2 Hz, 1H), 7.35 (d, J = 8.7 Hz, 2H), 7.12 (d, J = 1.2 Hz, 1H), 6.03 (s, 2H), 3.97 (t, J = 6.5 Hz, 2H), 3.02 (t, J = 7.5 Hz, 2H), 1.86 (h, J = 7.4 Hz, 2H), 1.52 - 1.41 (m, 2H), 1.29 - 1.19 (m, 2H), 1.04 (t, J = 7.4 Hz, 3H), 0.86 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 170.6, 160.2, 157.68, 151.9, 143.3, 140.2, 138.1, 135.8, 133.5, 130.2, 129.4, 126.8, 123.7, 119.9, 64.8, 50.0, 34.7, 30.9, 22.8, 18.8, 13.2, 13.0. HRMS (ESI): C24H28N5O4S3 + [M+H]+에 대한 계산값 546.1298; 실측값: 546.1295.
실시예 22
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.13 mmol, 1 당량) 및 트리에틸아민(0.68 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 부틸클로로포름에이트(0.16 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(44 mg, 64% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세토니트릴-d 3) δ 8.04 (d, J = 8.0 Hz, 2H), 7.19 (d, J = 7.9 Hz, 2H), 7.06 (s, 1H), 6.99 (s, 1H), 5.42 - 5.24 (m, 2H), 5.00 - 4.96 (m, 1H), 3.83 (t, J = 6.6 Hz, 2H), 2.85 (s, 2H), 2.11 (dt, J = 13.5, 6.7 Hz, 1H), 1.55 - 1.39 (m, 5H), 1.32 - 1.20 (m, 2H), 1.02 (d, J = 6.7 Hz, 6H), 0.88 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세토니트릴-d 3) δ 170.2, 159.8, 151.5, 138.1, 137.3, 134.6, 130.7, 127.1, 125.2, 121.9, 121.7, 64.9, 62.4, 49.9, 42.1, 31.5, 30.0, 22.3, 22.1, 19.5, 13.7. HRMS (ESI): C24H33N4O5S2 + [M+H]+에 대한 계산값 521.1887; 실측값: 521.1891.
실시예 23
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.13 mmol, 1 당량) 및 트리에틸아민(0.65 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.16 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(31 mg, 49% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.06 (d, J = 8.4 Hz, 2H), 7.35 (d, J = 1.7 Hz, 1H), 7.26 (d, J = 8.1 Hz, 2H), 7.21 (d, J = 1.7 Hz, 1H), 5.63 (s, 2H), 5.31 (q, J = 6.7 Hz, 1H), 3.51 (s, 3H), 2.92 (d, J = 7.1 Hz, 2H), 2.21 - 2.14 (m, 1H), 1.56 (d, J = 6.7 Hz, 3H), 1.05 (d, J = 6.7 Hz, 6H). 13 C NMR (101 MHz, 아세톤-d 6) δ 171.2, 156.0, 152.7, 150.2, 142.6, 136.2, 134.0, 130.3, 126.6, 122.2, 121.8, 61.8, 51.7, 50.0, 41.7, 29.4, 21.7, 21.6. HRMS (ESI): C21H27N4O5S2 + [M+H]+에 대한 계산값 479.1417; 실측값: 479.1418.
실시예 24
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.14 mmol, 1 당량) 및 트리에틸아민(0.68 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 부틸클로로포름에이트(0.16 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(38 mg, 55% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.95 (d, J = 8.3 Hz, 2H), 7.41 (d, J = 1.8 Hz, 1H), 7.39 - 7.29 (m, 3H), 5.50 (d, J = 2.2 Hz, 2H), 5.13 (q, J = 6.6 Hz, 1H), 3.88 (t, J = 6.5 Hz, 2H), 3.13 - 2.92 (m, 2H), 1.97 - 1.79 (m, 2H), 1.56 (d, J = 6.6 Hz, 3H), 1.50 - 1.44 (m, 2H), 1.33 - 1.26 (m, 2H), 1.07 (t, J = 7.4 Hz, 3H), 0.89 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 172.7, 158.2, 152.3, 150.0, 135.8, 135.5, 133.8, 130.2, 126.4, 122.4, 120.5, 64.6, 61.1, 50.1, 34.6, 30.7, 23.0, 20.5, 18.7, 12.7, 12.5. HRMS (ESI): C23H31N4O5S2 + [M+H]+에 대한 계산값 507.1730; 실측값: 507.1735.
실시예 25
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.13 mmol, 1 당량) 및 트리에틸아민(0.68 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.16 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(31 mg, 49% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 8.13 (d, J = 8.1 Hz, 2H), 7.63 (d, J = 1.8 Hz, 1H), 7.52 (d, J = 1.8 Hz, 1H), 7.30 (d, J = 8.1 Hz, 2H), 6.21 (s, 1H), 5.48 (s, 2H), 5.16 (q, J = 6.6 Hz, 1H), 3.31 (s, 3H), 2.90 (t, J = 7.5 Hz, 2H), 1.75 (q, J = 7.4 Hz, 2H), 1.44 (d, J = 6.5 Hz, 3H), 0.98 (t, J = 7.3 Hz, 3H). 13 C NMR (101 MHz, DMSO-d 6) δ 170.1, 163.5, 158.7, 150.1, 149.8, 135.5, 134.3, 130.6, 127.3, 123.0, 121.0, 60.7, 51.7, 50.1, 34.8, 23.0, 22.2, 13.9. HRMS (ESI): C20H25N4O5S2 + [M+H]+에 대한 계산값 465.1261; 실측값: 465.1267.
실시예 26
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.12 mmol, 1 당량) 및 트리에틸아민(0.60 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.14 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(31 mg, 54% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.98 (d, J = 8.3 Hz, 2H), 7.48 (d, J = 2.0 Hz, 1H), 7.35 (d, J = 8.2 Hz, 2H), 7.31 (d, J = 2.0 Hz, 1H), 5.51 (s, 2H), 3.46 (s, 3H), 2.89 (d, J = 7.2 Hz, 2H), 2.25 - 2.07 (m, 2H), 1.26 - 1.17 (m, 2H), 1.07 - 1.04 (m, 8H). 13 C NMR (101 MHz, 메탄올-d 4) δ 171.4, 159.5, 152.0, 148.8, 136.3, 134.9, 134.1, 130.3, 126.9, 122.2, 118.9, 51.2, 50.3, 41.4, 29.6, 21.2, 6.8, 5.5. HRMS (ESI): C22H27N4O4S2 + [M+H]+에 대한 계산값 475.1468; 실측값: 475.1457.
실시예 27
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.12 mmol, 1 당량) 및 트리에틸아민(0.60 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.15 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(38 mg, 61% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.97 (d, J = 8.1 Hz, 2H), 7.48 (d, J = 2.0 Hz, 1H), 7.36 (d, J = 8.0 Hz, 2H), 7.31 (d, J = 2.0 Hz, 1H), 5.52 (s, 2H), 3.87 (t, J = 6.5 Hz, 2H), 2.90 (d, J = 7.2 Hz, 2H), 2.27 - 2.08 (m, 2H), 1.48 (dq, J = 8.5, 6.6 Hz, 2H), 1.37 - 1.26 (m, 2H), 1.26 - 1.19 (m, 2H), 1.06 - 1.05 (m, 8H), 0.89 (t, J = 7.4 Hz, 3H). 13 C NMR (126 MHz, 메탄올-d 4) δ 171.6, 158.5, 152.1, 136.2, 148.9, 135.0, 134.0, 130.3, 126.9, 122.1, 119.1, 64.5, 50.3, 41.4, 30.8, 29.6, 21.2, 18.7, 12.7, 6.8, 5.5. HRMS (ESI): C25H33N4O4S2 + [M+H]+에 대한 계산값 517.1938; 실측값: 517.1950.
실시예 28
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.15 mmol, 1 당량) 및 트리에틸아민(0.73 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.15 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(41 mg, 60% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.97 (d, J = 8.3 Hz, 2H), 7.50 (d, J = 2.1 Hz, 1H), 7.36 (d, J = 8.1 Hz, 2H), 7.34 (d, J = 2.0 Hz, 1H), 5.52 (s, 2H), 3.47 (s, 3H), 3.00 (t, J = 7.6 Hz, 2H), 2.26 - 2.17 (m, 1H), 1.86 (q, J = 7.4 Hz, 2H), 1.23 (dd, J = 8.4, 2.5 Hz, 2H), 1.07 - 1.05 (m, 5H). 13 C NMR (101 MHz, 메탄올-d 4) δ 172.6, 159.3, 152.1, 148.8, 136.0, 134.8, 134.1, 130.3, 127.0, 122.2, 118.6, 51.3, 50.4, 34.6, 23.0, 12.5, 6.9, 5.5. HRMS (ESI): C21H25N4O4S2 + [M+H]+에 대한 계산값 461.1312; 실측값: 461.1309.
실시예 29
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트
표제 화합물을, 혼합물이 드라이 아이스 상에서 유지되는 것을 제외하고, 상응하는 설폰아미드(0.15 mmol, 1 당량) 및 트리에틸아민(0.74 mmol, 5 당량)을 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였으며, 메틸클로로포름에이트(0.15 mmol, 1.2 당량)를 대략 2분에 걸쳐 적가 방식으로 첨가하고, 반응 혼합물을 드라이 아이스 상에서 10분 동안 교반하였다. 미정제 생성물을 매뉴얼 FCC(아세토니트릴 중의 0 내지 5% MeOH)로 정제하고, 생성물을 백색 무정형 고체(44 mg, 59% 수율)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.97 (d, J = 7.9 Hz, 2H), 7.49 (d, J = 2.2 Hz, 1H), 7.37 (d, J = 8.0 Hz, 2H), 7.32 (s, 1H), 5.51 (s, 2H), 3.89 (t, J = 6.5 Hz, 2H), 2.99 (t, J = 7.6 Hz, 2H), 2.26 - 2.13 (m, 1H), 1.85 (q, J = 7.4 Hz, 2H), 1.47 (dd, J = 8.5, 6.2 Hz, 2H), 1.34 - 1.16 (m, 4H), 1.08 - 1.04 (m, 5H), 0.88 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 172.9, 157.7, 152.5, 148.7, 135.5, 134.9, 133.9, 130.3, 127.1, 122.3, 118.4, 64.7, 50.4, 34.6, 30.7, 23.0, 18.7, 12.7, 12.6, 7.1, 5.5. HRMS (ESI): C24H31N4O4S2 + [M+H]+에 대한 계산값 503.1781; 실측값: 503.1778.
실시예 30A
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 부틸 카바메이트(17.7 mg, 34.6 μmol)를 사용하여 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하고, FCC(CH2Cl2 중의 2 내지 4% MeOH)로 정제하여 생성물을 백색 무정형 고체(15.6 mg, 96%)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.05 (d, J = 8.2 Hz, 1H), 7.45 - 7.32 (m, 3H), 7.25 (d, J = 7.9 Hz, 2H), 7.12 (d, J = 1.6 Hz, 1H), 7.08 (d, J = 1.8 Hz, 1H), 7.03 (d, J = 1.6 Hz, 1H), 5.67 (s, 2H), 3.49 (s, 3H), 2.67 (t, J = 7.7 Hz, 2H), 1.74 - 1.60 (m, 2H), 1.66 (s, 6H), 0.96 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 155.8, 153.3, 149.0, 141.9, 140.9, 137.7, 137.5, 133.5, 131.1, 130.8, 128.6, 127.9, 124.5, 123.8, 71.1, 53.1, 52.0, 38.6, 30.3, 25.3, 14.1. HRMS (ESI + ) C27H36N3O5S+ [M+H]+에 대한 계산값 472.1901; 실측값: 472.1897.
실시예 30B
칼륨 (메톡시카보닐) ((4'-((2-(2-하이드록시프로판-2-일)-1
H
-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 상응하는 메틸 카바메이트(13.3 mg, 28 μmol) 및 KOH(1.70 mg, 30.2 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드에 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(14.3 mg, >99% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.86 (d, J = 8.0 Hz, 1H), 7.40 (d, J = 7.9 Hz, 2H), 7.21 - 7.14 (m, 1H), 7.10 (d, J = 8.0 Hz, 2H), 6.94 (s, 1H), 6.89 (s, 1H), 6.75 (s, 1H), 5.53 (s, 2H), 3.15 (s, 3H), 2.55 (t, J = 7.9 Hz, 4H), ), 1.67 - 1.52 (m, 2H), 1.51 (s, 6H), 0.89 (t, J = 7.2 Hz, 3H).
실시예 31A
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1
H
-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(74.3 mg, 0.156 mmol) 및 부틸 클로로포름에이트(27.5 μL, 0.216 mmol)를 사용하여 메틸((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(DCM 중의 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(39 mg, 47% 수율)로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.10 (d, J = 8.2 Hz, 1H), 7.45 (dd, J = 8.2, 1.8 Hz, 1H), 7.34 (d, J = 7.9 Hz, 2H), 7.26 (d, J = 7.9 Hz, 2H), 7.16 (d, J = 1.8 Hz, 1H), 6.92 (2, 1H), 6.81 (s, 1H), 5.65 (s, 2H), 3.95 (t, J = 6.5 Hz, 2H), 2.71 (t, J = 7.6 Hz, 2H), 1.70 (p, J = 7.5 Hz, 2H), 1.63 (s, 6H), 1.51 - 1.38 (m, 2H), 1.30 - 1.14 (m, 2H), 0.95 (t, J = 7.3 Hz, 3H), 0.85 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 153.0, 151.8, 149.1, 141.7, 139.5, 138.7, 136.6, 133.4, 131.2, 130.2, 128.4, 127.7, 126.5, 122.2, 71.1, 66.4, 50.9, 38.1, 31.3, 30.9, 24.9, 19.4, 14.0, 13.9. HRMS (ESI + ) C27H36N3O5S+ [M+H]+에 대한 계산값 514.2370; 실측값: 514.2371.
실시예 31B
칼륨 (부톡시카보닐) ((4'-((2-(2-하이드록시프로판-2-일)-1
H
-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 MeOH(1.0 mL) 중의 상응하는 부틸 카바메이트(15.0 mg, 29.0 μmol) 및 KOH(1.76 mg, 31.3 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(15.7 mg, 99% 수율)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.86 (d, J = 8.1 Hz, 1H), 7.53 - 7.34 (m, 2H), 7.15 (dd, J = 8.1, 1.9 Hz, 1H), 7.10 (d, J = 8.1 Hz, 2H), 6.93 (d, J = 1.3 Hz, 1H), 6.88 (d, J = 1.8 Hz, 1H), 6.74 (d, J = 1.3 Hz, 1H), 5.53 (s, 2H), 5.43 (s, 1H), 3.54 (t, J = 6.5 Hz, 2H), 2.60 - 2.49 (m, 2H), 1.68 - 1.54 (m, 2H), 1.52 (s, 6H), 1.45 - 1.26 (m, 2H), 1.26 - 1.14 (m, 2H), 0.89 (t, J = 7.3 Hz, 3H), 0.83 (t, J = 7.3 Hz, 3H).
실시예 32
부틸 ((4'-((2-(2-플루오로프로판-2-일)-1
H
-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트
상응하는 부틸 카바메이트(19.0 mg, 36.1 μmol, 1 당량)를 CH2Cl2(1 mL) 중에 용해시켰다. 용액을 -40℃로 냉각하였다. DAST(6.7 μL, 50.5 μmol, 1.4 당량)를 적가하였다. 반응 혼합물을 -20℃ 미만으로 유지하면서 2시간 동안 교반하였다. 반응을 물로 켄칭하고, CH2Cl2(3 x 5 mL)로 추출하고, 브라인(5 mL)으로 세정하고, Na2SO4 상에서 건조하고, 농축하였다. 미정제 생성물을 전치 HLPC(0.05% 포름산 첨가제를 갖는 물 중의 30 내지 80% MeCH)로 정제하여 생성물을 백색 무정형 고체(6.20 mg, 36%)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.06 (d, J = 8.2 Hz, 1H), 7.42 - 7.25 (m, 3H), 7.25 - 7.14 (m, 2H), ), 7.10 - 7.06 (m, 1H), 7.03 (d, J = 1.6 Hz, 1H), 6.94 (d, J = 1.4 Hz, 1H), 5.44 (s, 2H), 4.09 - 3.81 (m, 2H), 2.56 (d, J = 7.2 Hz, 2H), 1.99 - 1.87 (m, 1H), 1.79 (d, J = 21.7 Hz, 6H), 1.55 - 1.36 (m, 2H), 1.30 - 1.14 (m, 2H), 0.91 (d, J = 6.6 Hz, 6H), 0.85 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 152.4, 149.3 (d, 2 J C-F = 24.6 Hz), 148.5, 141.5, 139.7, 137.4, 135.7, 134.1, 130.9, 130.4, 129.2, 127.4, 127.0, 123.4, 94.5 (d, 1 J C-F = 165.5 Hz), 66.9, 51.3 (d, 4 J C-F = 8.9 Hz), 45.6, 31.2, 30.8, 28.1 (d, 2 J C-F = 24.5 Hz), 22.6, 19.5, 13.9. 19 F NMR (376 MHz, 메탄올-d 4) δ -140.02 (헵탄, J = 21.7 Hz). HRMS (ESI + ): C28H37N3O4S+ [M+H]+에 대한 계산값 530.2489; 실측값: 530.2482.
실시예 33A
메틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 부틸 카바메이트(18.8 mg, 34.0 μmol)를 사용하여 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 기재된 바와 같이 합성하였다. 미정제 생성물을 농축하고, FCC(CH2Cl2 중의 4 내지 6%)로 정제하여 생성물을 백색 무정형 고체(17.3 mg, 90% 수율)로서 제공하였다. 1 H NMR a (400 MHz, 메탄올-d 4) δ 8.06 (d, J = 8.2 Hz, 1H), 7.85 (d, J = 3.2 Hz, 1H), 7.48 (t, J = 3.3 Hz, 1H), 7.36 - 7.24 (m, 5H), 7.21 - 7.16 (m, 1H), 7.10 (d, J = 1.3 Hz, 1H), 7.03 (d, J = 1.8 Hz, 1H), 5.91 (s, 2H), 3.55 (s, 3H), 2.52 (d, J = 7.2 Hz, 2H), 1.97 - 1.80 (m, 1H), 0.88 (d, J = 6.6 Hz, 6H). 13 C NMR a (101 MHz, 메탄올-d 4) δ 159.6, 152.7, 148.5, 144.1, 141.5, 141.0, 139.6, 137.3, 135.3, 134.0, 130.9, 130.3, 129.5, 129.1, 127.7, 124.3, 121.0, 53.4, 51.2, 45.6, 30.7, 22.6. HRMS (ESI + ) C25H27N4O4S2 + [M+H]+에 대한 계산값 511.1471; 실측값: 511.1480.
[a] MeOD와 CDCl
3
의 혼합물로 기록된 스펙트럼
실시예 33B
칼륨 (메톡시카보닐) ((5-이소부틸-4'-((2-(티아졸-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 메틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트(107 mg, 0.261 mmol) 및 부틸 클로로포름(45.8 μL, 0.360 mmol)을 사용하여 칼륨 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)(메톡시카보닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(48 mg, 36%)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.96 (d, J = 3.3 Hz, 1H), 7.85 (d, J = 8.0 Hz, 1H), 7.77 (d, J = 3.3 Hz, 1H), 7.50 (d, J = 1.2 Hz, 1H), 7.38 (d, J = 8.0 Hz, 2H), 7.23 - 7.03 (m, 4H), 6.83 (s, 1H), 5.89 (s, 2H), 3.10 (s, 3H), 2.43 (d, J = 7.0 Hz, 2H), 1.94 - 1.74 (m, 1H), 0.85 (d, J = 6.6 Hz, 6H).
실시예 34
메틸 ((4'-((2-(2-플루오로프로판-2-일)-1
H
-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 메틸 카바메이트(18.2 mg, 35.6 μmol)를 사용하여 부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하고, HPLC(0.05% 포름산 첨가제를 갖는 물 중의 70% MeCN)로 정제하여 생성물을 백색 무정형 고체(6.20 mg, 36%)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.06 (d, J = 8.2 Hz, 1H), 7.52 - 7.23 (m, 6H), 7.20 (s, 1H), 7.09 (s, 1H), 5.54 (s, 2H), 3.56 (s, 3H), 2.58 (d, J = 7.2 Hz, 2H), 2.01 - 1.90 (m, 1H1.84 (d, J = 21.9 Hz, 6H), 0.92 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 메탄올-d 4) δ 153.3, 149.1 (d, 2 J C-F = 19.4 Hz), 149.1, 141.9, 140.7, 137.0, 136.2, 134.4, 131.3, 130.8, 129.6, 128.1, 124.9, 124.6, 94.4 (d, 1 J C-F = 168.1 Hz), 53.5, 52.2 (d, 4 J C-F = 8.4 Hz), 45.8, 31.2, 27.7 (d, 2 J C-F = 24.5 Hz), 22.6. 19 F NMR (376 MHz, 메탄올-d 4) δ -140.67 (헵탄, J = 21.6 Hz). HRMS (ESI + ) C25H31N3O4S+ [M+H]+ 488.2019에 대한 계산값; 실측값: 488.2019.
실시예 35A
부틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(92.7 mg, 0.205 mmol) 및 부틸 클로로포름에이트(36.0 μL, 0.238 μmol)를 사용하여 부틸 ((4'-((2 (tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(40.7 mg, 36%)로서 수득하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.05 (d, J = 8.2 Hz, 1H), 7.86 (d, J = 3.3 Hz, 1H), 7.58 (d, J = 3.3 Hz, 1H), 7.39 - 7.17 (m, 6H), 7.10 (d, J = 1.3 Hz, 1H), 6.99 (d, J = 1.8 Hz, 1H), 5.93 (s, 2H), 3.91 (t, J = 6.4 Hz, 2H), 2.50 (d, J = 7.2 Hz, 2H), 1.93 - 1.75 (m, 1H), 1.48 - 1.35 (m, 2H), 1.25 - 1.13 (m, 2H), 0.87 (d, J = 6.6 Hz, 6H), 0.83 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 160.0, 152.7, 148.9, 144.6, 142.0, 141.4, 140.1, 138.1, 136.3, 134.4, 131.3, 130.6, 129.9, 129.4, 128.2, 125.1, 121.6, 67.0, 51.4, 45.7, 31.6, 31.1, 22.6, 19.8, 13.9. HRMS (APCI + ) C28H33N4O4S2 + [M+H]+에 대한 계산값 553.1938; 실측값: 553.1935.
실시예 35B
칼륨 (부톡시카보닐) ((5-이소부틸-4'-((2-(티아졸-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 부틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트(107 mg, 0.261 mmol) 및 부틸 클로로포름에이트(45.8 μL, 0.360 mmol)를 사용하여 칼륨 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)(메톡시카보닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(48 mg, 36%)로서 수득하였다. 1 H NMR (400 MHz, DMSO-d 6) δ 7.96 (d, J = 3.3 Hz, 1H), 7.84 (d, J = 8.1 Hz, 1H), 7.77 (d, J = 3.3 Hz, 1H), 7.49 (d, J = 1.2 Hz, 1H), 7.39 - 7.33 (m, 2H), 7.20 - 7.07 (m, 4H), 6.82 (d, J = 1.8 Hz, 1H), 5.89 (s, 2H), 3.51 (t, J = 6.5 Hz, 2H), 2.43 (d, J = 7.0 Hz, 2H), 1.91 - 1.72 (m, 1H), 1.39 - 1.25 (m, 2H), 1.25 - 1.09 (m, 2H), 0.85 (d, J = 6.6 Hz, 6H), 0.81 (t, J = 7.3 Hz, 3H).
실시예 36
메틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 MeOH(1 mL) 중의 상응하는 부틸 카바메이트(48.0 mg, 93.8 μmol)를 사용하여 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 농축하고, FCC(CH2Cl2 중의 5 내지 7% MeOH)로 정제하여 생성물을 백색 무정형 고체(41.9 mg, 95% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.24 - 7.83 (m, 1H), 7.39 - 7.28 (m, 2H), 7.27 - 7.16 (m, 2H), 7.17 - 7.05 (m, 3H), 6.90 (d, J = 1.9 Hz, 1H), 5.27 (s, 2H), 3.32 - 3.12 (m, 1H), 2.43 (d, J = 7.2 Hz, 2H), 1.88 - 1.65 (m, 1H), 1.21 (d, J = 7.0 Hz, 6H), 0.81 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 메탄올-d 4) δ 158.6, 153.8, 146.9, 142.1, 141.3, 139.3, 135.5, 133.9, 131.2, 130.6, 129.1, 127.7, 122.7, 122.5, 52.8, 51.1, 45.8, 31.2, 26.7, 22.7, 21.3. HRMS (ESI + ) C25H32N3O4S+ [M+H]+에 대한 계산값 470.2114; 실측값: 470.2107.
실시예 37A
부틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(97.6 mg, 0.237 mmol) 및 부틸 클로로포름에이트(41.8 μL, 0.327 mmol)를 사용하여 부틸 ((4'-((2 (tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(CH2Cl2 중의 3 내지 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(72 mg, 59% 수율)로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.13 (d, J = 8.2 Hz, 1H), 7.60 - 7.35 (m, 3H), 7.29 - 7.13 (m, 2H), 7.10 (d, J = 1.8 Hz, 1H), 7.00 (d, J = 1.4 Hz, 1H), 6.83 (d, J = 1.4 Hz, 1H), 6.47 (bs, 1H), 5.30 (s, 2H), 3.94 (t, J = 6.5 Hz, 2H), 3.44 - 3.08 (m, 1H), 2.60 (d, J = 7.2 Hz, 2H), 2.01 - 1.81 (m, 1H), 1.71 - 1.38 (m, 2H), 1.25 (d, J = 6.9 Hz, 6H), 1.23 - 1.16 (m, 2H), 0.92 (d, J = 6.6 Hz, 6H), 0.85 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 154.4, 153.0, 146.8, 141.1, 141.0, 138.5, 136.5, 133.7, 131.0, 130.6, 128.7, 127.4, 125.1, 120.7, 65.6, 50.0, 45.3, 31.5, 30.7, 26.4, 22.6, 21.8, 19.5, 14.0. HRMS (ESI + ) C28H38N3O4S+ [M+H]+에 대한 계산값 512.2583; 실측값: 512.2579.
실시예 37B
칼륨 (부톡시카보닐) ((5-이소부틸-4'-((2-(이소프로판-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 MeOH(0.59 M) 중의 상응하는 부틸 카바메이트(13.7 mg, 26.6 μmol) 및 KOH(1.61 mg, 28.7 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(8.5 mg, 58% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.06 (d, J = 8.4 Hz, 1H), 7.52 (d, J = 7.8 Hz, 2H), 7.25 - 7.13 (m, 1H), 7.12 - 7.04 (m, 2H), 6.99 (d, J = 1.2 Hz, 1H), 6.96 (s, 1H), 6.84 (d, J = 1.3 Hz, 1H), 5.24 (s, 2H), 3.68 (t, J = 6.6 Hz, 2H), 3.20 - 3.01 (m, 1H), 2.52 (d, J = 7.1 Hz, 2H), 1.95 - 1.79 (m, 1H), 1.51 - 1.34 (m, 2H), 1.33 - 1.23 (m, 2H), 1.22 (d, J = 6.8 Hz, 6H), 0.91 (d, J = 6.6 Hz, 6H), 0.86 (t, J = 7.3 Hz, 3H).
실시에 38A
부틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(77.4 mg, 0.189 mmol) 및 부틸 클로로포름에이트(33.3 μL, 0.261mmol)를 사용하여 부틸 ((4'-((2 (tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(CH2Cl2 중의 3 내지 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(41 mg, 38% 수율)로서 제공하였다. 1 H NMR a (400 MHz, 메탄올-d 4) δ 8.05 (d, J = 8.2 Hz, 1H), 7.44 - 7.32 (m, 2H), 7.29 (dd, J = 8.2, 1.8 Hz, 1H), 7.19 (d, J = 8.1 Hz, 2H), 7.08 (d, J = 1.6 Hz, 1H), 7.03 (d, J = 1.8 Hz, 1H), 6.92 (d, J = 1.6 Hz, 1H), 5.33 (s, 2H), 3.91 (t, J = 6.5 Hz, 2H), 2.54 (d, J = 7.2 Hz, 2H), 2.15 - 1.80 (m, 2H), 1.58 - 1.37 (m, 2H), 1.32 - 1.12 (m, 2H), 1.06 - 0.93 (m, 4H), 0.90 (d, J = 6.6 Hz, 6H), 0.84 (t, J = 7.4 Hz, 3H). 13 C NMR a (101 MHz, 메탄올-d 4) δ 154.8, 150.0, 147.4, 141.1, 140.6, 137.1, 135.8, 133.7, 130.6, 130.5, 128.9, 127.2, 124.2, 121.6, 66.3, 50.4, 45.6, 31.3, 30.7, 22.6, 19.5, 13.9, 7.6, 7.2. HRMS (ESI + ) C28H36N3O4S+ [M+H]+에 대한 계산값 512.2583 실측값 512.2579.
[a] MeOD와 CDCl
3
의 혼합물로 기록됨
실시예 38B
칼륨 (부톡시카보닐) ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 MeOH(0.59 M) 중의 상응하는 부틸 카바메이트(13.5 mg, 26.2 μmol) 및 KOH(1.59 mg, 28.3 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(4.4 mg, 31% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.06 (d, J = 7.2 Hz, 1H), 7.54 (d, J = 8.2 Hz, 2H), 7.14 (t, J = 7.8 Hz, 3H), 7.02 (d, J = 1.3 Hz, 1H), 6.94 (d, J = 1.9 Hz, 1H), 6.75 (d, J = 1.3 Hz, 1H), 5.31 (s, 2H), 3.64 (t, J = 6.7 Hz, 2H), 2.51 (d, J = 7.1 Hz, 2H), 1.99 - 1.77 (m, 4H), 1.46 - 1.30 (m, 2H), 1.31 - 1.19 (m, 2H), 0.91 (d, J = 6.6 Hz, 6H), 0.89 - 0.86 (m, 3H), 0.86 - 0.83 (m, 3H).
실시예 39A
메틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을 MeOH(1 mL) 중의 상응하는 부틸 카바메이트(27.4 mg, 53.8 μmol)를 사용하여 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 농축하고, FCC(CH2Cl2 중의 5 내지 7% MeOH)로 정제하여 생성물을 백색 무정형 고체(21.6 mg, 86% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.05 (d, J = 8.2 Hz, 1H), 7.42 - 7.36 (m, 2H), 7.32 - 7.21 (m, 4H), 7.08 (d, J = 1.8 Hz, 1H), 7.01 (d, J = 1.8 Hz, 1H), 5.41 (s, 2H), 3.43 (s, 3H), 2.64 - 2.35 (m, 3H), 2.25 - 2.02 (m, 1H), 1.97 - 1.81 (m, J = 6.7 Hz, 1H), 1.19 - 1.03 (m, 2H), 1.03 - 0.97 (m, 2H), 0.91 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 메탄올-d 4) δ 158.0, 150.4, 147.2, 141.9, 141.4, 138.9, 135.8, 133.9, 131.1, 130.7, 129.2, 127.9, 122.7, 122.6, 52.9, 51.1, 45.8, 31.2, 22.7, 7.9, 7.3. HRMS (ESI + ) C25H30N3O4S+ [M+H]+에 대한 계산값 468.1957; 실측값: 468.1947.
실시예 39B
칼륨 (메톡시카보닐) ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1
H
-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)아미드
표제 화합물을 MeOH(0.59 M) 중의 상응하는 메틸 카바메이트(21.6 mg, 45.7 μmol) 및 KOH(2.77 mg, 49.3 μmol)를 사용하여 칼륨 (부톡시카보닐)((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)아미드에 대해 기재된 바와 같이 합성하였다. 생성물을 백색 무정형 고체(20.3 mg, 88% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 8.06 (d, J = 8.1 Hz, 1H), 7.61 - 7.48 (m, 2H), 7.22 - 7.08 (m, 3H), 7.03 (d, J = 1.3 Hz, 1H), 6.95 (d, J = 1.8 Hz, 1H), 6.75 (d, J = 1.3 Hz, 1H), 5.31 (s, 2H), 3.23 (s, 3H), 2.52 (d, J = 7.2 Hz, 2H), 1.99 - 1.83 (m, 2H), 0.91 (d, J = 6.6 Hz, 6H), 0.89 - 0.81 (m, 4H).
실시예 40
부틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1
H
-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(19.9 mg, 46.0 μmol) 및 부틸 클로로포름에이트(8.7 μL, 63.5 μmol)를 사용하여 부틸 ((4'-((2 (tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 HPLC(0.05% 포름산을 갖는 MeCN 중의 30 내지 50% 물)로 정제하여 동결 건조 후에 생성물을 백색 무정형 고체(10.3 mg, 42% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.67 - 7.54 (m, 2H), 7.26 (d, J = 8.1 Hz, 2H), 7.11 (d, J = 1.6 Hz, 1H), 7.05 (d, J = 1.6 Hz, 1H), 6.83 (s, 1H), 5.66 (s, 2H), 3.91 (t, J = 6.5 Hz, 2H), 2.73 (d, J = 7.1 Hz, 2H), 2.01 - 1.86 (m, 1H), 1.65 (s, 6H), 1.57 - 1.40 (m, 2H), 1.37 - 1.18 (m, 2H), 1.00 (d, J = 6.6 Hz, 6H), 0.88 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 156.5, 153.1, 150.0, 144.9, 137.7, 136.0, 132.2, 130.8, 130.3, 128.3, 123.9, 123.7, 71.0, 66.5, 52.1, 40.0, 31.9, 31.8, 30.2, 22.6, 20.0, 14.1. HRMS (ESI + ) C26H36N3O5S2 + [M+H]+에 대한 계산값 534.2096; 실측값: 534.2097.
실시예 41
메틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1
H
-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트
표제 화합물을 MeOH(1 mL) 중의 상응하는 부틸 카바메이트(10.0 mg, 18.7 μmol)를 사용하여 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 농축하고, FCC(CH2Cl2 중의 3 내지 6% MeOH)로 정제하여 생성물을 백색 무정형 고체(6.0 mg, 65% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.58 (d, J = 8.3 Hz, 2H), 7.26 (d, J = 8.2 Hz, 2H), 7.14 (d, J = 1.7 Hz, 1H), 7.09 (d, J = 1.6 Hz, 1H), 6.81 (s, 1H), 5.66 (s, 2H), 3.48 (s, 3H), 2.72 (d, J = 7.1 Hz, 2H), 2.10 - 1.85 (m, 1H), 1.65 (s, 6H), 1.00 (d, J = 6.6 Hz, 6H). HRMS (ESI + ) C23H30N3O5S2 + [M+H]+에 대한 계산값 492.1627; 실측값: 492.1628.
실시예 42
부틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1
H
-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트
표제 화합물을 상응하는 부틸 카바메이트(21.6 mg, 38.4 μmol) 및 DAST(5.1 μL, 38.4 μmol)를 사용하여 부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하고, HPLC(0.05% 포름산을 갖는 MeCN 중의 30 내지 70% 물)로 정제하여 동결 건조 후에 생성물을 백색 무정형 고체(5.7 mg, 28% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.59 - 7.46 (m, 2H), 7.24 (d, J = 8.0 Hz, 2H), 7.10 (s, 1H), 6.97 (s, 1H), 6.87 (s, 1H), 5.46 (s, 2H), 3.98 (t, J = 6.4 Hz, 2H), 2.75 (d, J = 7.1 Hz, 2H), 2.02 - 1.87 (m, 1H), 1.77 (d, J = 21.6 Hz, 6H), 1.58 - 1.40 (m, 2H), 1.34 - 1.15 (m, 2H), 1.00 (d, J = 6.6 Hz, 6H), 0.88 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 151.5, 150.6, 148.4 (d, 2 J C-F = 25.5 Hz), 145.2, 137.4, 133.9, 131.9, 129.4, 129.2, 126.8, 125.7, 122.6, 93.5 (d, 1 J C-F = 165.5 Hz), 65.7, 50.2 (d, 4 J C-F = 8.9 Hz), 38.6, 30.4, 30.3, 26.7 (d, 2 J C-F = 24.6 Hz), 21.1, 18.5, 12.6. 19 F NMR (376 MHz, 메탄올-d 4) δ -140.66 (헵탄, J = 21.5 Hz). HRMS (ESI + ) C26H36FN3O4S2 + [M+H]+에 대한 계산값 536.2053; 실측값: 536.2051.
실시예 43
메틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1
H
-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트
표제 화합물을 상응하는 메틸 카바메이트(18.9 mg, 38.5 μmol)를 사용하여 부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하고, HPLC(0.05% 포름산을 갖는 MeCN 중의 30 내지 70% 물)로 정제하여 동결 건조 후에 생성물을 백색 무정형 고체(6.5 mg, 34% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 7.53 - 7.35 (m, 2H), 7.21 - 7.10 (m, 3H), 7.05 (d, J = 1.6 Hz, 1H), 6.77 (s, 1H), 5.41 (s, 2H), 3.48 (s, 3H), 2.65 (d, J = 7.1 Hz, 2H), 1.96 - 1.78 (m, 1H), , 1.70 (d, J = 21.9 Hz, 6H), 0.90 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 메탄올-d 4) δ 153.3, 152.3, 149.4 (d, 2 J C-F = 24.8 Hz), 146.9, 138.1, 135.5, 133.0, 130.8, 128.3, 125.6, 124.5, 121.4, 94.8 (d, 1 J C-F = 168.1Hz), 53.6, 52.0 (d, 4 J C-F = 9.0 Hz), 40.0, 31.8, 27.8 (d, 2 J C-F = 24.4 Hz), 22.5. 19 F NMR (376 MHz, 메탄올-d 4) δ -140.93 (헵탄, J = 21.8 Hz). HRMS (ESI + ) C23H29FN3O4S2 + [M+H]+에 대한 계산값 494.1584; 실측값: 494.1588.
실시예 44
2-메톡시에틸 ((5-이소부틸-3-(4-(2-(2-tert부틸)-1
H
-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트
표제 화합물을 상응하는 설폰아미드(50.0 mg, 0.116 mmol) 및 2-메톡시에틸 클로로포름에이트(16.2 μL, 0.139 mmol)를 사용하여 부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 FCC(MeCN 중의 0 내지 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(36 mg, 58% 수율)로서 제공하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.65 (d, J = 7.9 Hz, 2H), 7.16 (d, J = 7.8 Hz, 2H), 7.01 (bs, 1H), 6.96 (s, 1H), 6.92 (bs, 1H), 5.55 (s, 2H), 4.11 (t, J = 4 Hz, 2H), 3.46 (t, J = 4 Hz, 2H), 3.26 (s, 3H), 2.79 (d, J = 7.0 Hz, 2H), 1.98 (dq, J = 13.4, 6.7 Hz, 1H), 1.44 (s, 9H), 1.01 (d, J = 6.5 Hz, 6H). 13 C NMR (101 MHz, 아세톤-d 6) δ 153.6, 151.9, 149.7, 144.4, 137.7, 134.0, 133.3, 129.6, 129.4, 126.3, 124.7, 122.3, 70.0, 64.7, 57.8, 50.6, 38.6, 33.3, 30.4, 29.2, 21.6. HRMS (ESI + ): C26H36N3O5S2 + [M+H]+에 대한 계산값 534.2091; 실측값: 534.2092.
실시예 45
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트
표제 화합물을 상응하는 부틸 카바메이트(40.0 mg, 0.073 mmol) 및 DAST(13.5 μL, 0.102 mmol)를 사용하여 부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 전치 HPLC(아세토니트릴 중의 15 내지 80% 물)로 정제하고, 동결 건조 후에 생성물을 백색 무정형 고체(19.0 mg, 45% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.91 (d, J = 7.9 Hz, 2H), 7.28 (d, J = 7.9 Hz, 2H), 7.14 (bs, 1H), 6.98 (bs, 1H), 5.53 (s, 2H), 4.04 (t, J = 6.5 Hz, 2H), 3.07 (t, J = 7.5 Hz, 2H), 1.96 - 1.85 (m, 2H), 1.77 (d, J = 21.6 Hz, 6H), 1.50 (p, J = 6.8 Hz, 2H), 1.26 (h, J = 7.4 Hz, 2H), 1.07 (t, J = 7.3 Hz, 3H), 0.88 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 174.7, 155.7, 150.6, 148.0 (d, 2 J C-F = 25.0 Hz), 139.3, 132.4, 130.4, 130.1, 126.7, 126.5, 122.6, 93.9 (d, 1 J C-F = 164.0 Hz). 66.1, 50.1 (d, 4 J C-F = 8.3 Hz), 35.0, 30.4, 27.2 (d, 2 J C-F = 24.6 Hz), 22.7, 18.5, 12.9, 12.9. 19 F NMR (376 MHz, 아세톤-d 6) δ -139.3 (헵탄, J = 21.5 Hz). HRMS (ESI + ): C24H32FN4O4S2 + [M+H]+에 대한 계산값 523.1844; 실측값: 523.1835.
실시예 46
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트
표제 화합물을 상응하는 메틸 카바메이트(40 mg, 0.0794 mmol) 및 DAST(0.015 mL, 0.111 mmol)를 사용하여 부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 전치 HPLC(아세토니트릴 중의 15 내지 80% 물)로 정제하고, 동결 건조 후에 생성물을 백색 무정형 고체(17 mg, 40% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.75 (d, J = 8.2 Hz, 2H), 7.12 (d, J = 8.0 Hz, 2H), 7.01 (bs, 1H), 6.83 (bs, 1H), 5.38 (s, 2H), 3.49 (s, 3H), 2.93 (t, J = 7.6 Hz, 2H), 1.80-1.70 (m, 2H), 1.62 (d, J = 21.6 Hz, 6H), 0.93 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 174.8, 155.8, 151.3, 148.0 (d, 2 J C-F = 25.2 Hz), 139.3, 132.4, 130.2, 130.1, 126.6, 126.6, 122.6, 94.0 (d, 1 J C-F = 163.9 Hz), 52.7, 50.1 (d, 4 J C-F = 8.3 Hz), 34.9, 27.2 (d, 2 J C-F = 24.6 Hz), 22.7, 12.9. 19 F NMR (376 MHz, 아세톤-d 6) δ -139.5 (헵탄, J = 21.4 Hz). HRMS (ESI + ): C21H26FN4O4S2 [M+H]+에 대한 계산값 481.1374; 실측값: 481.1378.
실시에 47
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트
표제 화합물을 상응하는 부틸 카바메이트(40 mg, 0.071 mmol) 및 DAST(13.0 μL, 0.100 mmol)를 사용하여 부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 전치 HPLC(MeCN 중의 15 내지 80% 물)로 정제하고, 동결 건조 후에 생성물을 백색 무정형 고체(20 mg, 47% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.91 (d, J = 8.3 Hz, 2H), 7.27 (d, J = 8.2 Hz, 2H), 7.11 (bs, 1H), 6.94 (bs, 1H), 5.51 (s, 2H), 4.04 (t, J = 6.5 Hz, 2H), 2.98 (d, J = 7.1 Hz, 2H), 2.20 (dt, J = 13.5, 6.8 Hz, 1H), 1.76 (d, J = 21.5 Hz, 6H), 1.50 (dq, J = 8.4, 6.6 Hz, 2H), 1.35 - 1.19 (m, 2H), 1.05 (d, J = 6.7 Hz, 6H), 0.88 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 아세톤-d 6) δ 173.7, 155.7, 150.7, 148.1 (d, 2 J C-F = 24.8 Hz), 139.4, 132.4, 130.5, 130.1, 126.8, 126.7, 122.5, 94.0 (d, 1 J C-F = 163.5 Hz). 66.1, 50.0 (d, 4 J C-F = 8.3 Hz), 41.7, 30.4, 29.4, 27.3 (d, 2 J C-F = 24.6 Hz), 21.6, 18.6, 13.0. 19 F NMR (376 MHz, 아세톤-d 6) δ -139.3 (헵탄, J = 21.6 Hz). HRMS (ESI + ): C25H34FN4O4S2 + [M+H]+에 대한 계산값 537.2000; 실측값: 537.1992.
실시예 48
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)2-이소부틸티아졸-5-일)설포닐)카보메이트
표제 화합물을 상응하는 부틸 카바메이트(40.0 mg, 0.077 mmol) 및 DAST(14.0 μL, 0.108 mmol)를 사용하여 부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 전치 HPLC(아세토니트릴 중의 15 내지 80% 물)로 정제하고, 동결 건조 후에 생성물을 백색 무정형 고체(21 mg, 50% 수율)로서 수득하였다. 1 H NMR (400 MHz, 아세톤-d 6) δ 7.90 (d, J = 8.2 Hz, 2H), 7.27 (d, J = 8.0 Hz, 2H), 7.17 (bs, 1H), 7.00 (bs, 1H), 5.54 (s, 2H), 3.63 (s, 3H), 2.98 (d, J = 7.1 Hz, 2H), 2.25 - 2.15 (m, 1H), 1.78 (d, J = 21.7 Hz, 6H), 1.05 (d, J = 6.6 Hz, 6H). 13 C NMR (101 MHz, 아세톤-d 6) δ 173.9, 161.5, 155.9, 151.1, 147.9 (d, 2 J C-F = 25.4 Hz), 139.2, 132.4, 130.1, 126.7, 126.3, 122.7, 93.9 (d, 1 J C-F = 164.4 Hz). 52.76, 50.2 (d, 4 J C-F = 8.4 Hz), 41.7, 29.4, 27.2 (d, 2 J C-F = 24.4 Hz), 21.5. 19 F NMR (376 MHz, 아세톤-d 6) δ -139.6 (헵탄, J = 21.6 Hz). HRMS (ESI + ): C22H28FN4O4S2 + [M+H]+에 대한 계산값 495.1531; 실측값: 495.1532.
실시예 49
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-3'-플루오로-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트
표제 화합물을, 부틸 클로로포름에이트(42.9 μL, 0.336 mmol, 1.2 당량)가 0℃에서 상응하는 설폰아미드(125 mg, 0.280 mmol, 1 당량)에 첨가되는 것을 제외하고, 부틸 ((4'-((2 (tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하고, 반응을 1시간 후에 켄칭하였다. 미정제 생성물을 FCC(CH2Cl2 중의 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(58.8 mg, 39% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.05 (d, J = 8.2 Hz, 1H), 7.34 (dd, J = 8.2, 1.8 Hz, 1H), 7.26 - 7.01 (m, 6H), 5.57 (s, 2H), 3.86 (t, J = 6.5 Hz, 2H), 2.56 (d, J = 7.2 Hz, 2H), 2.06 - 1.75 (m, 1H), 1.54 (s, 9H), 1.49 - 1.35 (m, 2H), 1.34 - 1.16 (m, 2H), 0.92 (d, J = 6.6 Hz, 6H), 0.85 (t, J = 7.4 Hz, 3H). 13 C NMR (101 MHz, 메탄올-d 4) δ 160.8 (d, 1 J C-F = 246.6 Hz), 156.8, 154.9, 147.6, 144.3 (d, 3 J C-F = 8.6 Hz), 140.0, 138.8, 133.6, 130.7, 129.9 (d, 4 J C-F = 4.0 Hz), 129.7, 127.0 (d, 3 J C-F = 3.3 Hz), 124.1, 123.0 (d, 2 J C-F = 14.6 Hz), 122.9, 117.9 (d, 2 J C-F = 22.0 Hz), 66.3, 47.3 (d, 3 J C-F = 4.1 Hz), 45.8, 34.7, 32.0, 31.2, 29.4, 22.7, 20.0, 14.1. 19 F NMR (376 MHz, 메탄올-d 4) δ -113.55 - -127.68 (m).
실시예 50
메틸 (4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-3'-플루오로-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐카바메이트
표제 화합물을 MeOH(1 mL) 중의 상응하는 부틸 카바메이트(33.0 mg, 60.7 μmol)를 사용하여 메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트에 대해 기재된 바와 같이 합성하였다. 미정제 생성물을 농축하고, FCC(CH2Cl2 중의 5% MeOH)로 정제하여 생성물을 백색 무정형 고체(17.5 mg, 58% 수율)로서 제공하였다. 1 H NMR (400 MHz, 메탄올-d 4) δ 8.05 (d, J = 8.2 Hz, 1H), 7.34 (dt, J = 8.2, 1.7 Hz, 1H), 7.27 - 7.14 (m, 4H), 7.13 - 7.03 (m, 2H), 5.58 (s, 2H), 3.45 (s, 3H), 2.57 (d, J = 7.1 Hz, 2H), 2.06 - 1.77 (m, J = 6.7 Hz, 1H), 1.55 (s, 9H), 0.93 (d, J = 6.6 Hz, 6H). 13 C NMR a (101 MHz, 메탄올-d 4) δ 160.6 (d, 1 J C-F = 246.7 Hz), 157.5, 154.6, 147.2, 144.2 (d, 3 J C-F = 8.5 Hz), 139.7, 138.6, 133.3, 130.5, 129.5 (d, 4 J C-F = 2.3 Hz), 126.8 (d, 3 J C-F = 3.3 Hz), 123.9, 122.7, 122.5 (d, 2 J C-F = 14.4 Hz), 117.8 (d, 2 J C-F = 22.0 Hz), 52.8, 47.1 (d, 3 J C-F = 4.0 Hz), 45.7, 34.5, 31.0, 29.3, 22.6. 19 F NMR (376 MHz, 메탄올-d 4) δ -116.33 - -132.46 (m).
생물학
결과
K
i
값, 간 마이크로솜에서의 안정성, 및 동적 용해도
K i 결정. 인간 AT2R로부터의 [125I][Sar1Ile8]-안지오텐신 II을 Eurofins의 HEK-293 세포 막 조제물에 옮기는 것에 의한 라디오작용제 검정(radioagonist assay)에서 화합물을 평가하였다. [Sar1Ile8]-안지오텐신 II(Sarile)는 비선택적 AT2R 작용제로서 작용한다.18 친화도는 8- 또는 9-지점 투여량-반응 곡선을 사용하여 결정하였으며, 각각의 지점을 두 차례 수행하였다. 인큐베이션 완충액(최종 농도)은 pH 7.4에서 45 mM Tris/HCl, 4.5 mM MgCl2, 0.9 mM EDTA/Tris, 0.09% BSA로 구성되었다. PD 123,319를 참조 화합물로서 사용하였다. 화합물을 또한 사랄라신을 참조 화합물로서 사용하여 Eurofins의 HEK-293 세포 막에서의 인간 AT1R에 대한 [125I][Sar1Ile8]-안지오텐신 II 결합 억제에 대해 평가하였다.
간 마이크로솜에서의 안정성. 인간, 마우스, 및 래트의 간 마이크로솜을 사용하여 화합물에 대한 대사 안정성을 평가하였다. 대사 안정성을 Eurofins에 의한 500 μL의 총 인큐베이션 부피 내의 100 mM의 인산칼륨 완충액(pH 7.4) 중의 1 μM의 화합물의 농도에서의 0.5 mg/mL 인간, 마우스, 래트의 간 마이크로솜에서 결정하였다. 검정 기질은 인간 간 마이크로솜: 혼합된 성별 및 50마리의 풀(pool), 래트 간 마이크로솜: 수컷, Sprague-Dawley, 100마리 이상의 풀, 및 마우스의 간 마이크로솜: 수컷, CD-1, 250마리 이상의 풀이었다. 최종 마이크로솜 단백질 농도: 0.1 mg/mL. 시험 농도는 디폴트(default)로 0.01 DMSO, 0.25% 아세토니트릴, 및 0.25% 메탄올을 갖는 0.1 μM이었다. 실험 프로토콜은 다음과 같았다: 시험 화합물을 37℃의 진탕 수조 내의 인산 완충액(pH 7.4) 내에서 간 마이크로솜 풀로 사전 인큐베이션하였다. NADPH-생성 시스템을 첨가하여 반응을 개시하고, 0, 15, 30, 45, 및 60분 동안 인큐베이션하였다. 인큐베이션 혼합물을 아세토니트릴/메탄올로 옮겨서 반응을 중단하였다. 이어서, 샘플을 혼합하고, 원심 분리하였다. 4개의 참조 화합물을 각각의 검정에서 시험하였다. 프로프라놀롤 및 이미프라민은 상대적으로 안정한 반면, 베라파밀 및 테르페나딘은 인간 간 마이크로솜 내에서 쉽게 대사된다. 샘플을 선택된 반응 모니터링을 사용하여 HPLC-MS/MS로 분석하였다. HPLC 시스템은 오토샘플러, C-18 컬럼, 및 구배를 갖는 바이너리(binary) LC 펌프로 구성되었다. 시험 화합물에 해당하는 피크 면적을 기록하였다. 잔류 화합물은 각각의 시점에서의 피크 면적을 0의 시간에 비교하여 계산하였다. 1차 반응속도론으로 가정하여 잔류 화합물(%) 대 시간의 대수 곡선의 초기 선형 범위의 기울기로부터 반감기를 계산하였다. 또한, 고유 청소율(intrinsic clearance)(Clint)을 계산하였다.19,20
동적 용해도. 둘베코의 PBS 완충액을 사용하였다(pH 7.4로 NaCl 137 mM, KCl 2.7 mM, Na2HPO4 8.1 mM, KH2PO4 1.5 mM). 시험 화합물을 10 mM의 DMSO 저장 용액으로부터 PBS 완충액 중의 200 μM로 제조하였다. 최종 DMSO의 농도는 2%였다. 완충액 샘플을 철저히 혼합한 다음 실온에서 24시간 동안 인큐베이션하였다. 인큐베이션의 종료 시, 완충액 샘플을 원심 분리하고, 상청액을 이어서 HPLC 분석을 위해 주입하였다. 시험 화합물의 보정 표준물은 HPLC 분석 날에 10 mM의 DMSO 저장 용액으로부터 메탄올/물(3/2, v/v) 중의 200 μM로 제조하였다. 분석은 광 다이오드 어레이 검출을 갖는 HPLC-UV/VIS로 실시하며, 205, 230, 260, 및 300 nm 파장에서 모니터링하였다. HPLC 시스템은 A와 B의 구배를 사용하는 C18 컬럼으로 구성되었다(A = 12 mM 암모늄 포름에이트, 물 중의 6 mM 포름산, pH 4.0, B = 6 mM 암모늄 포름메이트, 3 mM 포름산 아세토니트릴/물(9/1, v/v)). 사용되는 참조 화합물은 메토프롤롤, 리팜피신, 케토코나졸, 페니토인, 할로페리돌, 심바스타틴, 디에틸스틸베스트롤, 및 타목시펜이었으며, 완전한 용해성(200 μM)에서부터 난용성(<1 μM)까지로 평가하였다. 시험 화합물의 수성 용해도(μM)는 보정 표준물(200 μM)에서의 주요 피크의 피크 면적을 각각의 완충액 샘플에서의 상응하는 피크의 피크 면적과 비교하여 결정하였다. 검정의 범위는 대략 0.5 μM 내지 200 μM이었다. 크로마토그래피 순도(%)는 보정 표준물의 HPLC 크로마토그램에서의 총 적분 피크 면적에 대한 주요 피크의 피크 면적으로 결정하였다.
하기 표 1은 명시된 실시예의 화합물에 대한 Ki, 및 인간 간 마이크로솜(HLM), 마우스 간 마이크로솜(MLM), 및 래트 간 마이크로솜(RLM)에서의 안정성, 및 PBS 중의 동적 안정성을 나타낸다.
CYP450 억제 검정
시험 화합물이 96-웰 플레이트 형태 내의 인간 간 마이크로솜 풀에서 각각의 일반적 사이토크롬 P450(CYP) 효소의 활성도를 억제하는지를 평가하기 위해 다음 절차를 설계하였다. 화합물을 0.1% DMASO를 사용한 단일 농도(10 μM)에서 시험하였다. 시험 화합물을 37℃의 진탕 수조 내에서 인산 완충액(pH 7.4) 중의 인간 간 마이크로솜(혼합된 성별, 50명의 기증자 풀, 0.1 mg/mL) 및 기질로 5분 동안 사전 인큐베이션하였다. NADPH-생성 시스템을 첨가하여 반응을 개시하였다. 반응은 10분 동안 이루어지며, 반응 혼합물을 아세토니트릴/메탄올에 옮겨서 중단하였다. 샘플을 혼합하고, 원심 분리하였다. 상청액을 각각의 대사 물질의 HPLC-MS/MS에 사용하였다. 프로브 기질의 대사 물질의 형성에 따라 인간 사이토크롬 P450(CYP) 효소의 활성도를 결정하였다. 다음 효소를 열거된 참조 기질 및 참조 억제제를 사용하여 억제에 대해 평가하였다.
CYP1A - 페나세틴(참조 억제제 퓨라필린), CYP2B6 - 부프로피온(참조 억제제 클로피도그레), CYP2C8 - 아모디아퀸(참조 억제제 몬테루카스트), CYP2C9 - 디클로페낙(참조 억제제 설파페나졸), CYP2C19 - 오메프라졸(참조 억제제 옥시부티닌), CYP2D6 - 덱스트로메토르판(참조 억제제 퀴니딘), CYP3A - 미다졸람(참조 억제제 케토코나졸), 및 CYP3A - 테스토스테론(참조 억제제 케토코나졸). 참조 억제제를 각각의 검정에서 다수의 농도로 시험하여 IC50 값을 수득하였다. 대사 물질에 상응하는 피크 면적을 기록하였다. 대조군 활성도 백분율은 시험 화합물의 존재 하의 피크 면적을 동일한 샘플을 보유하는 대조군 샘플에 비교하여 계산하였다. 이어서, 억제 백분율을 100으로부터 대조군 활성도 백분율을 감산하여 계산하였다. IC50 값(대조군 값의 최대 억제의 절반 값을 유발하는 농도)을 Hill 방정식을 사용하여 농도-반응 곡선의 비-선형 회귀에 의해 결정하였다.
인간 IPF 정밀 절단 폐 슬라이스(PCLuS)에 대한 시험
다음 절차를 FibroFind(뉴캐슬 섬유증 연구 그룹, 영국 소재)에 의해 수행하고, 시험 화합물이 IPF-PCLuS(IPF 정밀 절단 폐 슬라이스)에서의 섬유증을 약화시키는지를 평가하도록 설계하였다. PCLus를 확인된 조직 검사로부터 제조하고, 폐 이식 시간에 수집된 IPF 인간 폐 조직을 외식하였다. 이어서, PCLus를 48시간 동안 그대로 두어서 실험이 시작하기 전에 슬라이싱-이후 스트레스 기간이 경과하도록 하였다. 또한, PCLus를 2개의 증가 투여량(0.1 μM 및 1 μM)에서의 시험 화합물의 존재 하에 배양하였다. 모든 PCLus를 144시간에 수확하였다.
n = 5 또는 8개의 인간 PCLus를 갖는 9개의 상이한 그룹을 하기 표 3에 나타낸 바와 같이 조사하였다. PCLus를 확인된 n = 1 조직 검사로부터 제조하고, 인간 IPF 폐를 외식하였다. 비히클은 배양 배지 중에 1:1000으로 DMSO 희석하였다.
PCLuS를 48시간의 휴식 기간 동안 인큐베이션하였다. 휴식 이후, PCLuS를 상기 약술된 시험 화합물의 존재 또는 부재 하에 추가의 96시간 동안 인큐베이션하였다. 모든 시험 화합물을 포함하는 PCLuS 배양 배지를 새로 공급하고, 48시간부터 24시간 간격으로 수확하였다. 모든 PCLuS를 144시간에 수확하였다. 각각의 배지 샘플을 약 150 μL의 3개의 분취액으로 분할하고, 단일 분취액을 용해성 마커의 측정에 사용하였다. 용해성 마커는 콜라겐 1a1(Col1a1) 및 전환 성장 인자-β1(TGF-β1)이다.
PCLuS 수확. 세포 배양 상청액(그룹 당 n=5 내지 12개)을 매일 수집하고, 하기 열거된 용해성 결과의 정량화를 위해 급동결하였다. 수확 시, n=5 내지 8개의 PCLuS를 RNA 단리 및 qPCR 분석을 위해 급동결하였다.
용해성 결과 분석. 세포 배양 상청액 중의 콜라겐 1a1의 수준을 R&D Duoset ELISA 키트를 사용하여 정량화하였다. 세포 배양 상청액 중의 TGF-β1의 수준을 SinglePlex ELISA(MesoScaleDiscovery™ (MSD))를 사용하여 정량화하였다.
정량적 실시간 PCR(qPCR). PCLuS로부터의 총 RNA 추출을 MagMAX™-96 총 RNA 단리 키트를 사용하여 모든 샘플에 대해 수행하였다. RNA를 cDNA로 역전사하고, qPCR에 사용하여 Col1a1, TGF-β1, β-액틴의 전사 수준을 측정하였다.
용해성 결과 분석. 세포 배양 상청액 중의 Col1a1의 수준을 R&D Duoset ELISA 키트를 사용하여 48시간, 96시간, 및 144시간에서 정량화하고, 용해성 TGF-β1의 수준은 SinglePlex ELISA MSD 키트를 사용하여 정량화하였다(도 1 내지 도 8).
정량적 실시간 PCR. PCLuS에서의 Col1a1 및 TGF-β1의 전사 수준을 β-액틴에 대해 정량화하였다(도 9 및 도 10).
도 1 내지 도 4는 C21, 실시예 1A, 실시예 12A, 및 실시예3을 사용하여 치료될 때의 PCLuS 배양 상청액 중의 분비된 콜라겐 1a1 수준을 나타낸다. 그래프는 조건당, 시점당 n = 5 내지 12개의 조직 배양 배지로 나타낸다. 데이터는 조직 배양 배지당 개별 값을 갖는 평균 ± SEM으로 제시된다.
도 5 내지 도 8은 C21, 실시예 1A, 실시예 12A, 및 실시예3을 사용하여 치료될 때의 PCLuS 배양 상청액 중의 분비된 TGF-β1 수준을 나타낸다. 그래프는 조건 당, 시점당 n = 5 내지 12개의 조직 배양 배지로 나타낸다. 데이터는 조직 배양 배지당 개별 값을 갖는 평균 ± SEM으로 제시된다.
도 9 및 도 10은 144시간에서의 C21, 실시예 1A, 실시예 12A, 및 실시예3의 치료를 사용한 Col1a1 및 TGF-β1에 대한 상대적 전사 차이 수준(RLTD%)의 형태로 PCLuS 중의 선택된 유전자 전사 수준을 나타낸다. 데이터는 대조군 및 비히클에 대한 유전자 발현 변화 백분율로 제시된다.
시험된 사실상 모든 화합물을 사용한 IPF PCLuS의 치료는 시험된 적어도 하나의 시점에서 TGF-β1 유전자 전사 및 단백질 분비를 확고하게 감소시켰다. 이들 화합물은 또한 콜라겐 1a1 유전자 전사를 감소시키는 데 매우 효과적이다.
추가의 실시예
상기 기재된 하나 이상의 합성 절차에 따라 제조될 수 있는 다음 화합물이 또한 제공된다.
[표 3]
결론
결론적으로, 화합물 C21 또는 이의 나트륨염과 비교하여, 본 개시내용의 화합물 또는 이의 염은 CYP 효소의 낮은 억제를 나타내는 것으로 발견되었다.
참조 문헌
1. Pharmacol. Rev. 2000; 52: 415-472.
2. WO 02/096883
3. WO 99/43339
4. EP 0512675 A1
5. DE10 2012 004 589 A1
6. US 2004/0167176
7. Med. Res. Rev. 2018; 38:602-624
8. WO 2002/096883
9. WO 2016/139475
10. WO 2004/046141
11. WO 2016/092329
12. WO 2016/107879
13. WO 2016/139475
14. WO 2017/221012
15. WO 2019/008393
16. US 2012/035232
17. Bioorg. Med. Chem. Lett. 2018, 28 (3), 519-522.
18. ACS Med. Chem. Lett. 2014, 5, 1129-1132.
19. Biochem. Pharmacol. 1994, 47, 1469-1479.
20. DRUG Metab. Dispos. 1999, 27, 1350-1359.
21. Bioorg. Med. Chem. 2010, 18 (12), 4570-4590
Claims (26)
- 화학식 I의 화합물 또는 이의 허용 가능한 염으로서,
화학식 I
상기 식에서, R1은,
H,
OR6, SR7, NR8R9, 할로겐, 티아졸, 옥사졸, 및 피라졸로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된 C2-C6 알킬,
OR6, SR7,및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된 C3-C6 사이클로알킬,
티아졸,
벤질(여기서, 페닐 모이어티는 OR6, SR7, 및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환됨), 또는
(CH2)m-R10을 나타내고,
R2는,
H,
F,
Cl,
OR6, SR7, NR8R9, 할로겐, 티아졸, 옥사졸, 및 피라졸로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된 C2-C6 알킬,
OR6, SR7,및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된 C3-C6 사이클로알킬,
벤질(여기서, 페닐 모이어티는 OR6, SR7, 및 NR8R9로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환됨), 또는
(CH2)m-R10을 나타내되,
단, R1 및 R2 둘 모두는 H가 아니고,
R3은,
H,
할로겐, 또는
F 및 Cl로 구성된 군으로부터 선택되는 0, 1, 2, 또는 3개의 할로겐으로 치환된 C1-C3 알킬을 나타내고,
R4 및 R5는 독립적으로 0, 1, 2, 또는 3개의 F로 치환된 C1-C6 알킬을 나타내고,
X는 CH=CH, CH, N, NH, O, 또는 S를 나타내고;
Y는 CH=CH, CH, N, NH, O, 또는 S를 나타내되,
단, (a) X 및 Y는 동일하지 않고,
(b) X가 CH=CH를 나타내는 경우, Y는 오직 CH를 나타내고,
(c) Y가 CH=CH를 나타내는 경우, X는 오직 CH를 나타내고,
Z는 단일 결합, O, 또는 S를 나타내고,
R6, R7, R8, 및 R9는 독립적으로
H, 또는
0, 1, 2, 또는 3개의 F로 치환된 C1-C3 알킬을 타나내고,
R10은 페닐, 티아졸, 옥사졸, 및 피라졸로 구성된 군으로부터 선택되고,
n은 0, 1, 2, 3, 또는 4이고,
m은 0 또는 1인, 화합물 또는 이의 약학적으로 허용 가능한 염. - 제1항 또는 제2항에 있어서, R1은 OR6, SR7, NR8R9, 할로겐, 티아졸, 옥사졸, 및 피라졸로 구성된 군으로부터 선택되는 0, 1, 또는 2개의 치환기로 치환된 C2-C6 알킬을 나타내는, 화합물.
- 제1항 내지 제3항 중 어느 한 항에 있어서, R2 및 R3은 독립적으로 H를 나타내는, 화합물.
- 제3항 또는 제4항에 있어서, R1은 tert-부틸, 이소프로필, 또는 사이클로프로필인, 화합물.
- 제3항 또는 제4항에 있어서, R1은 -OH 기 또는 F 원자로 치환된 C2-C6 알킬인, 화합물.
- 제6항에 있어서, R1은 2-하이드록시프로프-2-일, 1-에탄올, 또는 2-플루오로프로프-2-일인, 화합물.
- 제1항 내지 제7항 중 어느 한 항에 있어서, R4는 메틸, 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸, 및 tert-부틸로 구성된 군으로부터 선택되는, 화합물.
- 제8항에 있어서, R4는 메틸 또는 n-부틸인, 화합물.
- 제1항 내지 제9항 중 어느 한 항에 있어서, R5는 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸, 및 tert-부틸로 구성된 군으로부터 선택되는, 화합물.
- 제10항에 있어서, R5는 이소프로필 또는 이소부틸인, 화합물.
- 제1항 내지 제11항 중 어느 한 항에 있어서, n은 0인, 화합물.
- 제1항 내지 제12항 중 어느 한 항에 있어서, Z는 단일 결합인, 화합물.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 다음 화합물 중 하나 이상인, 화합물:
메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트,
부틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐) 카바메이트,
메틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐) 카바메이트,
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트,
메틸 ((3-(4-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)페닐)-5-이소부틸티오펜-2-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일) 설포닐)카바메이트,
부틸 ((2-이소부틸-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸 티아졸-5-일)설포닐)카바메이트,
부틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
메틸 ((4-(4-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((2-이소부틸-4-(4-((2-이소프로필-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((2-프로필-4-(4-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)페닐)티아졸-5-일) 설포닐)카바메이트,
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(1-하이드록시에틸)-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-사이클로프로필-1H-이미다졸-1-일)메틸)페닐)-2-프로필티아졸-5-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)-5-프로필-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((4'-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(티아졸-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(이소프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-4'-((2-(사이클로프로판-2-일)-1H-이미다졸-1-일)메틸)-[1,1'-바이페닐]-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-3-(4-(2-(2-하이드록시프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
부틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
메틸 ((5-이소부틸-3-(4-(2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
2-메톡시에틸 ((5-이소부틸-3-(4-(2-(2-tert부틸)-1H-이미다졸-1-일)메틸)페닐)-2-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-프로필 티아졸-5-일)설포닐)카바메이트,
부틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
메틸 ((4-(4-((2-(2-플루오로프로판-2-일)-1H-이미다졸-1-일)메틸)페닐)-2-이소부틸티아졸-5-일)설포닐)카바메이트,
부틸 ((4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-3'-플루오로-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐)카바메이트, 또는
메틸 (4'-((2-(tert-부틸)-1H-이미다졸-1-일)메틸)-3'-플루오로-5-이소부틸-[1,1'-바이페닐]-2-일)설포닐카바메이트. - 약제로서의 용도를 위한 제1항 내지 제14항 중 어느 한 항에 정의된 화합물.
- 제1항 내지 제14항 중 어느 한 항에 청구된 화합물의 치료적으로 유효량을 적어도 하나의 약학적으로 허용 가능한 담체, 부형제, 및/또는 희석제와 함께 포함하는, 약학적 조성물.
- 안지오텐신 II와 관련된 질병, 장애, 또는 병태를 치료 및/또는 예방하기 위한 제1항 내지 제16항 중 어느 한 항에 정의된 화합물로서, 하나 이상의 CYP의 허용 가능한 CYP 억제 수준을 나타내는, 화합물.
- 고혈압, 심부전, 뇌졸증, 만성 신장 질병, 신증, 폐섬유증 예컨대 특발성 폐섬유증, 경화증 예컨대 전신 경화증, 사르코이드증 예컨대 폐사르코이드증, 폐색성 폐질병 예컨대 만성 폐색성 폐질병, 자가면역 질병, 예컨대 류마티스 관절염, 바이러스성 기도 감염증 및 이의 결과로서의 폐렴, 및 이의 임의의 조합으로 구성된 군으로부터 선택되는 질병, 장애, 및/또는 병태의 치료 및/또는 예방에의 용도를 위한 제17항에 정의된 화합물.
- 고혈압, 심부전, 뇌졸증, 만성 신장 질병, 신증, 폐섬유증 예컨대 특발성 폐섬유증, 경화증 예컨대 전신 경화증, 사르코이드증 예컨대 폐사르코이드증, 폐색성 폐질병, 예컨대 만성 폐색성 폐질병, 자가면역 질병, 예컨대 류마티스 관절염, 바이러스성 기도 감염증 및 이의 결과로서의 폐렴, 및 이의 임의의 조합으로 구성된 군으로부터 선택되는 질병, 장애, 및/또는 병태의 치료용 약제의 제조를 위한 제17항에 정의된 화합물의 용도.
- 고혈압, 심부전, 뇌졸증, 만성 신장 질병, 신증, 폐섬유증, 예컨대 특발성 폐섬유증, 경화증, 예컨대 전신 경화증, 사르코이드증, 예컨대 폐사르코이드증, 폐색성 폐질병, 예컨대 만성 폐색성 폐질병, 자가면역 질병, 예컨대 류마티스 관절염, 바이러스성 기도 감염증 및 이의 결과로서의 폐렴으로 구성된 군으로부터 선택되는 질병, 장애, 및/또는 병태의 치료 방법으로서, 제1항 내지 제14항 중 어느 한 항에 정의된 화합물을 이러한 치료를 필요로 하는 환자에게 투여하는 단계를 포함하는, 치료 방법.
- 제18항에 청구된 용도를 위한 화합물, 제19항에 청구된 용도, 또는 제20항에 청구된 치료 방법에 있어서, 질병은 간질성 폐질병인, 용도를 위한 화합물, 용도, 또는 치료 방법.
- 제21항에 청구된 용도를 위한 화합물, 용도, 또는 치료 방법에 있어서, 간질성 폐질병은 특발성 폐섬유증 또는 사르코이드증인, 용도를 위한 화합물, 용도, 또는 치료 방법.
- 제18항에 청구된 용도를 위한 화합물, 제19항에 청구된 용도, 또는 제20항에 청구된 치료 방법에 있어서, 질병은 심부전, 만성 신장질병, 류마티드 관절염, 및 바이러스 유발 폐렴인, 용도를 위한 화합물, 용도, 또는 치료 방법.
- 제1항 내지 제14항 중 어느 한 항에 정의된 화합물, CYP 효소에 의해 대사되는 것으로 알려진 치료제; 및 약학적으로 허용 가능한 보조제, 희석제, 또는 담체를 포함하는 약학적 제형.
- (A) 제1항 내지 제14항 중 어느 한 항에 정의된 화합물을 약학적으로 허용 가능한 보조제, 희석제, 또는 담체와 혼합물로 포함하는 약학적 제형; 및
(B) CYP 효소에 의해 대사되는 것으로 알려진 치료제를 약학적으로 허용 가능한 보조제, 희석제, 또는 담체와 혼합물로 포함하는 약학적 제형을 포함하며,
성분 (A) 및 (B)는 각각 다른 것과 함께 투여하기에 적합한 형태로 제공되는, 분품 키트(kit of parts). - 제24항에 청구된 제형 또는 제25항에 청구된 분품 키트에 있어서, 치료제는 피르페니돈, 나프록센, 프로프라놀롤, 리루졸, 티자니딘, 와파린, 셀레콕시브, 클로피도그렐, 이르베사르탄, 멜록시캄, 피록시캄, 토르세미드, 사이클로포스파미드, 인도메타신, 아토르바스타틴, 실로스타졸, 사이클로스포린, 데플라자코트, 하이드로코르티손, 리토카인, 실렉시팍, 실데나필, 및/또는 심바스타틴으로 구성된 군으로부터 선택되는, 제형 또는 분품 키트.
제1항 내지 제26항 중 어느 한 항에 정의된 화학식 I의 화합물의 제조 공정으로서,
화학식 5
화학식 5의 화합물과 화학식 6의 화합물, R4OC(O)X (화학식 6)의 반응에 의해 선택적으로 화학식 4의 화합물의 탈보호 후에, 화학식 5의 화합물을 중간체로서 수득하는 제조 공정:
화학식 5에서, R1, R2, R3, R5, X, Y, Z, 및 n은 제1항에 정의된 바와 같고,
화학식 6에서, X는 적합한 이탈기, 예컨대 할로(예를 들어, 클로로)를 나타내고, R4는 제1항에 정의된 바와 같고,
화학식 4
화학식 4에서, PG는 보호기를 나타내고, R1, R2, R3, R5, X, Y, Z, 및 n은 상기 정의된 바와 같음.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SE2050301 | 2020-03-19 | ||
| SE2050301-7 | 2020-03-19 | ||
| SE2050782-8 | 2020-06-29 | ||
| SE2050782 | 2020-06-29 | ||
| PCT/GB2021/050680 WO2021186185A1 (en) | 2020-03-19 | 2021-03-18 | Novel compounds useful in the treatment and/or prevention of a disease, disorder or condition associated with angiotensin ii |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20230004501A true KR20230004501A (ko) | 2023-01-06 |
Family
ID=75339995
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227036148A KR20230004501A (ko) | 2020-03-19 | 2021-03-18 | 안지오텐신 ⅱ와 관련된 질병, 장애, 또는 병태의 치료 및/또는 예방에 유용한 신규 화합물 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US20230159467A1 (ko) |
| EP (1) | EP4121165A1 (ko) |
| JP (1) | JP2023518948A (ko) |
| KR (1) | KR20230004501A (ko) |
| CN (1) | CN115605265A (ko) |
| AU (1) | AU2021238939A1 (ko) |
| BR (1) | BR112022018549A2 (ko) |
| CA (1) | CA3175559A1 (ko) |
| CL (1) | CL2022002540A1 (ko) |
| CO (1) | CO2022014673A2 (ko) |
| IL (1) | IL296247A (ko) |
| MX (1) | MX2022011613A (ko) |
| WO (1) | WO2021186185A1 (ko) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB202104033D0 (en) * | 2021-03-23 | 2021-05-05 | Vicore Pharma Ab | New compounds |
| EP4313953A1 (en) * | 2021-03-23 | 2024-02-07 | Vicore Pharma AB | Selective angiotensin ii receptor ligands |
| AU2022306778A1 (en) * | 2021-07-09 | 2024-01-18 | Vicore Pharma Ab | New selective angiotensin ii compounds |
| WO2023085415A1 (ja) * | 2021-11-15 | 2023-05-19 | 株式会社アークメディスン | 化合物、アンジオテンシンiiタイプ1受容体拮抗剤及び医薬組成物 |
| WO2024133942A1 (en) | 2022-12-22 | 2024-06-27 | Vicore Pharma Ab | A method of treating a patient diagnosed with an interstitial lung disease |
| WO2024149712A1 (en) * | 2023-01-09 | 2024-07-18 | Vicore Pharma Ab | Selective angiotensin ii compounds |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5198438A (en) | 1991-05-07 | 1993-03-30 | Merck & Co., Inc. | Angiotensin ii antagonists incorporating a substituted thiophene or furan |
| SE9800550D0 (sv) | 1998-02-24 | 1998-02-24 | A & Science Invest Ab | A pharmaceutical preparation comprising an angiotensin II type 2 receptor agonist, and use thereof |
| DK1395566T3 (da) | 2001-05-31 | 2008-01-07 | Vicore Pharma Ab | Tricycliske forbindelser, der er nyttige som angiotensin Il-agonister |
| WO2004046141A1 (en) | 2002-11-21 | 2004-06-03 | Vicore Pharma Ab | New tricyclic angiotensin ii agonists |
| US8835471B2 (en) | 2010-06-11 | 2014-09-16 | Vicore Pharma Ab | Use of angiotensin II agonists |
| DE102012004589A1 (de) | 2012-03-09 | 2013-09-12 | Forschungszentrum Jülich GmbH | Agonisten des Angiotensin II AT2-Rezeptors zur Behandlung neurodegenerativer Erkrankungen |
| US20170266164A1 (en) | 2014-12-12 | 2017-09-21 | Vicore Pharma Ab | New methods and uses |
| WO2016107879A2 (en) | 2014-12-30 | 2016-07-07 | Vicore Pharma Ab | New use of angiotensin ii receptor agonists |
| CN107405406A (zh) | 2015-03-02 | 2017-11-28 | 维科尔药物公司 | 用于治疗肺纤维化的血管紧张素ii受体激动剂 |
| WO2017221012A1 (en) | 2016-06-21 | 2017-12-28 | Vicore Pharma Ab | Methods and compositions for preventing or reducing the risk of cancer treatment-related cardiotoxicity |
| GB201710906D0 (en) | 2017-07-06 | 2017-08-23 | Vicore Pharma Ab | Compounds and methods for treating peripheral neuropathy |
-
2021
- 2021-03-18 KR KR1020227036148A patent/KR20230004501A/ko unknown
- 2021-03-18 US US17/912,284 patent/US20230159467A1/en active Pending
- 2021-03-18 EP EP21715951.6A patent/EP4121165A1/en active Pending
- 2021-03-18 CA CA3175559A patent/CA3175559A1/en active Pending
- 2021-03-18 WO PCT/GB2021/050680 patent/WO2021186185A1/en active Application Filing
- 2021-03-18 JP JP2022556088A patent/JP2023518948A/ja active Pending
- 2021-03-18 MX MX2022011613A patent/MX2022011613A/es unknown
- 2021-03-18 AU AU2021238939A patent/AU2021238939A1/en active Pending
- 2021-03-18 CN CN202180033927.3A patent/CN115605265A/zh active Pending
- 2021-03-18 IL IL296247A patent/IL296247A/en unknown
- 2021-03-18 BR BR112022018549A patent/BR112022018549A2/pt unknown
-
2022
- 2022-09-16 CL CL2022002540A patent/CL2022002540A1/es unknown
- 2022-10-18 CO CONC2022/0014673A patent/CO2022014673A2/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| US20230159467A1 (en) | 2023-05-25 |
| IL296247A (en) | 2022-11-01 |
| BR112022018549A2 (pt) | 2022-11-29 |
| AU2021238939A1 (en) | 2022-11-10 |
| CN115605265A (zh) | 2023-01-13 |
| JP2023518948A (ja) | 2023-05-09 |
| CO2022014673A2 (es) | 2023-01-16 |
| CL2022002540A1 (es) | 2023-04-21 |
| WO2021186185A1 (en) | 2021-09-23 |
| EP4121165A1 (en) | 2023-01-25 |
| MX2022011613A (es) | 2022-10-21 |
| CA3175559A1 (en) | 2021-09-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20230004501A (ko) | 안지오텐신 ⅱ와 관련된 질병, 장애, 또는 병태의 치료 및/또는 예방에 유용한 신규 화합물 | |
| JP6002785B2 (ja) | ナトリウムチャネルモジュレーターとしてのベンゾイミダゾールおよびイミダゾピリジン誘導体 | |
| AU2013365742B2 (en) | Autotaxin inhibitors | |
| WO2021053344A1 (en) | New compounds | |
| CA3189240A1 (en) | Novel compounds for use in the treatment of diseases associated with angiotensin ii | |
| JP2024511452A (ja) | 選択的アンジオテンシンii受容体リガンド | |
| GB2605148A (en) | New compounds | |
| JP2024523576A (ja) | 新規の選択的アンジオテンシンii化合物 | |
| WO2022200785A1 (en) | Selective angiotensin ii receptor ligands | |
| JP2024511451A (ja) | 選択的アンジオテンシンii受容体リガンド | |
| WO2020210597A1 (en) | Benzimidazole derivatives and their uses | |
| WO2024149712A1 (en) | Selective angiotensin ii compounds | |
| CN117222624A (zh) | 选择性血管紧张素ii受体配体 |