KR20220156526A - 조작된 항-her2 이중특이성 단백질 - Google Patents
조작된 항-her2 이중특이성 단백질 Download PDFInfo
- Publication number
- KR20220156526A KR20220156526A KR1020227028989A KR20227028989A KR20220156526A KR 20220156526 A KR20220156526 A KR 20220156526A KR 1020227028989 A KR1020227028989 A KR 1020227028989A KR 20227028989 A KR20227028989 A KR 20227028989A KR 20220156526 A KR20220156526 A KR 20220156526A
- Authority
- KR
- South Korea
- Prior art keywords
- sequence
- seq
- identity
- polypeptide
- protein
- Prior art date
Links
- 108090000623 proteins and genes Proteins 0.000 title claims abstract description 494
- 102000004169 proteins and genes Human genes 0.000 title claims abstract description 485
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 claims abstract description 237
- 102000051957 human ERBB2 Human genes 0.000 claims abstract description 203
- 238000000034 method Methods 0.000 claims abstract description 77
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 37
- 201000011510 cancer Diseases 0.000 claims abstract description 31
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 1293
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 1287
- 229920001184 polypeptide Polymers 0.000 claims description 1284
- 238000006467 substitution reaction Methods 0.000 claims description 181
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 claims description 147
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 claims description 147
- 108010033576 Transferrin Receptors Proteins 0.000 claims description 124
- 150000001413 amino acids Chemical class 0.000 claims description 98
- 230000004048 modification Effects 0.000 claims description 75
- 238000012986 modification Methods 0.000 claims description 75
- 239000000539 dimer Substances 0.000 claims description 73
- 239000012636 effector Substances 0.000 claims description 42
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 claims description 34
- 239000012634 fragment Substances 0.000 claims description 22
- 108091033319 polynucleotide Proteins 0.000 claims description 22
- 102000040430 polynucleotide Human genes 0.000 claims description 22
- 239000002157 polynucleotide Substances 0.000 claims description 22
- 238000005734 heterodimerization reaction Methods 0.000 claims description 19
- 239000013598 vector Substances 0.000 claims description 17
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 16
- 210000004556 brain Anatomy 0.000 claims description 13
- 239000008194 pharmaceutical composition Substances 0.000 claims description 11
- 206010027476 Metastases Diseases 0.000 claims description 10
- 230000009401 metastasis Effects 0.000 claims description 10
- 125000003729 nucleotide group Chemical group 0.000 claims description 9
- 239000002773 nucleotide Substances 0.000 claims description 6
- 206010006187 Breast cancer Diseases 0.000 claims description 5
- 208000026310 Breast neoplasm Diseases 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 4
- 208000037819 metastatic cancer Diseases 0.000 claims description 3
- 208000011575 metastatic malignant neoplasm Diseases 0.000 claims description 3
- 238000002512 chemotherapy Methods 0.000 claims description 2
- 238000001959 radiotherapy Methods 0.000 claims description 2
- 102000007238 Transferrin Receptors Human genes 0.000 claims 5
- 230000001737 promoting effect Effects 0.000 claims 3
- 208000003174 Brain Neoplasms Diseases 0.000 abstract description 5
- 206010059282 Metastases to central nervous system Diseases 0.000 abstract description 5
- 235000018102 proteins Nutrition 0.000 description 347
- 102100026144 Transferrin receptor protein 1 Human genes 0.000 description 119
- 230000027455 binding Effects 0.000 description 119
- 238000009739 binding Methods 0.000 description 119
- 235000001014 amino acid Nutrition 0.000 description 105
- 229940024606 amino acid Drugs 0.000 description 94
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 92
- 125000003295 alanine group Chemical group N[C@@H](C)C(=O)* 0.000 description 57
- 230000008499 blood brain barrier function Effects 0.000 description 46
- 210000001218 blood-brain barrier Anatomy 0.000 description 46
- 210000004899 c-terminal region Anatomy 0.000 description 45
- 241000282414 Homo sapiens Species 0.000 description 41
- 230000035772 mutation Effects 0.000 description 35
- 102000005962 receptors Human genes 0.000 description 35
- 108020003175 receptors Proteins 0.000 description 35
- 230000006870 function Effects 0.000 description 34
- 210000004027 cell Anatomy 0.000 description 30
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 27
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 25
- 125000001493 tyrosinyl group Chemical group [H]OC1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 25
- 230000036961 partial effect Effects 0.000 description 23
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 22
- 125000003275 alpha amino acid group Chemical group 0.000 description 22
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 21
- 239000000427 antigen Substances 0.000 description 19
- 102000036639 antigens Human genes 0.000 description 19
- 108091007433 antigens Proteins 0.000 description 19
- 125000002987 valine group Chemical group [H]N([H])C([H])(C(*)=O)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 19
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 17
- -1 For example Chemical class 0.000 description 15
- 239000004472 Lysine Substances 0.000 description 15
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 15
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 12
- 150000007523 nucleic acids Chemical class 0.000 description 12
- 108060003951 Immunoglobulin Proteins 0.000 description 11
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 11
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 11
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 11
- 238000010586 diagram Methods 0.000 description 11
- 102000018358 immunoglobulin Human genes 0.000 description 11
- 102000039446 nucleic acids Human genes 0.000 description 11
- 108020004707 nucleic acids Proteins 0.000 description 11
- 125000000539 amino acid group Chemical group 0.000 description 10
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 9
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 9
- 102100026120 IgG receptor FcRn large subunit p51 Human genes 0.000 description 8
- 101710177940 IgG receptor FcRn large subunit p51 Proteins 0.000 description 8
- 125000000174 L-prolyl group Chemical group [H]N1C([H])([H])C([H])([H])C([H])([H])[C@@]1([H])C(*)=O 0.000 description 8
- 235000018417 cysteine Nutrition 0.000 description 8
- 239000003814 drug Substances 0.000 description 8
- 108020004414 DNA Proteins 0.000 description 7
- 208000017891 HER2 positive breast carcinoma Diseases 0.000 description 7
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 7
- 210000004881 tumor cell Anatomy 0.000 description 7
- 108010087819 Fc receptors Proteins 0.000 description 6
- 102000009109 Fc receptors Human genes 0.000 description 6
- 125000000010 L-asparaginyl group Chemical group O=C([*])[C@](N([H])[H])([H])C([H])([H])C(=O)N([H])[H] 0.000 description 6
- 241000699670 Mus sp. Species 0.000 description 6
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 6
- 239000004473 Threonine Substances 0.000 description 6
- 238000010494 dissociation reaction Methods 0.000 description 6
- 230000005593 dissociations Effects 0.000 description 6
- 230000002998 immunogenetic effect Effects 0.000 description 6
- 239000004475 Arginine Substances 0.000 description 5
- WHUUTDBJXJRKMK-GSVOUGTGSA-N D-glutamic acid Chemical compound OC(=O)[C@H](N)CCC(O)=O WHUUTDBJXJRKMK-GSVOUGTGSA-N 0.000 description 5
- 239000004471 Glycine Substances 0.000 description 5
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 5
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 5
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 5
- 230000002378 acidificating effect Effects 0.000 description 5
- 235000004279 alanine Nutrition 0.000 description 5
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 210000003038 endothelium Anatomy 0.000 description 5
- 239000013604 expression vector Substances 0.000 description 5
- 210000004602 germ cell Anatomy 0.000 description 5
- 230000009036 growth inhibition Effects 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 229920000642 polymer Polymers 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- 210000002966 serum Anatomy 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 230000004083 survival effect Effects 0.000 description 5
- 238000002560 therapeutic procedure Methods 0.000 description 5
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 5
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 4
- CKLJMWTZIZZHCS-UWTATZPHSA-N D-aspartic acid Chemical compound OC(=O)[C@H](N)CC(O)=O CKLJMWTZIZZHCS-UWTATZPHSA-N 0.000 description 4
- 102000053602 DNA Human genes 0.000 description 4
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 4
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 4
- 125000001931 aliphatic group Chemical group 0.000 description 4
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 238000010367 cloning Methods 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 230000003902 lesion Effects 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 241000894007 species Species 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 3
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 3
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 3
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 3
- 125000000510 L-tryptophano group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C(C([H])([H])[C@@]([H])(C(O[H])=O)N([H])[*])C2=C1[H] 0.000 description 3
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 3
- 108091005461 Nucleic proteins Proteins 0.000 description 3
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 3
- 102000004338 Transferrin Human genes 0.000 description 3
- 108090000901 Transferrin Proteins 0.000 description 3
- 102000014257 Transferrin receptor protein 1 Human genes 0.000 description 3
- 108050003222 Transferrin receptor protein 1 Proteins 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 230000004540 complement-dependent cytotoxicity Effects 0.000 description 3
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 3
- 150000001945 cysteines Chemical group 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 201000006585 gastric adenocarcinoma Diseases 0.000 description 3
- 201000007492 gastroesophageal junction adenocarcinoma Diseases 0.000 description 3
- 235000013922 glutamic acid Nutrition 0.000 description 3
- 239000004220 glutamic acid Substances 0.000 description 3
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 description 3
- 239000000833 heterodimer Substances 0.000 description 3
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 3
- 210000004408 hybridoma Anatomy 0.000 description 3
- 230000002209 hydrophobic effect Effects 0.000 description 3
- 230000001394 metastastic effect Effects 0.000 description 3
- 206010061289 metastatic neoplasm Diseases 0.000 description 3
- 229930182817 methionine Natural products 0.000 description 3
- KDYFGRWQOYBRFD-UHFFFAOYSA-N succinic acid Chemical compound OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 3
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- 239000012581 transferrin Substances 0.000 description 3
- 239000004474 valine Substances 0.000 description 3
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 2
- DCXYFEDJOCDNAF-UWTATZPHSA-N D-Asparagine Chemical compound OC(=O)[C@H](N)CC(N)=O DCXYFEDJOCDNAF-UWTATZPHSA-N 0.000 description 2
- XUJNEKJLAYXESH-UWTATZPHSA-N D-Cysteine Chemical compound SC[C@@H](N)C(O)=O XUJNEKJLAYXESH-UWTATZPHSA-N 0.000 description 2
- AGPKZVBTJJNPAG-RFZPGFLSSA-N D-Isoleucine Chemical compound CC[C@@H](C)[C@@H](N)C(O)=O AGPKZVBTJJNPAG-RFZPGFLSSA-N 0.000 description 2
- ONIBWKKTOPOVIA-SCSAIBSYSA-N D-Proline Chemical compound OC(=O)[C@H]1CCCN1 ONIBWKKTOPOVIA-SCSAIBSYSA-N 0.000 description 2
- MTCFGRXMJLQNBG-UWTATZPHSA-N D-Serine Chemical compound OC[C@@H](N)C(O)=O MTCFGRXMJLQNBG-UWTATZPHSA-N 0.000 description 2
- 229930195711 D-Serine Natural products 0.000 description 2
- QNAYBMKLOCPYGJ-UWTATZPHSA-N D-alanine Chemical compound C[C@@H](N)C(O)=O QNAYBMKLOCPYGJ-UWTATZPHSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-UHFFFAOYSA-N D-alpha-Ala Natural products CC([NH3+])C([O-])=O QNAYBMKLOCPYGJ-UHFFFAOYSA-N 0.000 description 2
- 150000008574 D-amino acids Chemical class 0.000 description 2
- ODKSFYDXXFIFQN-SCSAIBSYSA-N D-arginine Chemical compound OC(=O)[C@H](N)CCCNC(N)=N ODKSFYDXXFIFQN-SCSAIBSYSA-N 0.000 description 2
- 229930028154 D-arginine Natural products 0.000 description 2
- 229930182846 D-asparagine Natural products 0.000 description 2
- 229930182847 D-glutamic acid Natural products 0.000 description 2
- ZDXPYRJPNDTMRX-GSVOUGTGSA-N D-glutamine Chemical compound OC(=O)[C@H](N)CCC(N)=O ZDXPYRJPNDTMRX-GSVOUGTGSA-N 0.000 description 2
- 229930195715 D-glutamine Natural products 0.000 description 2
- HNDVDQJCIGZPNO-RXMQYKEDSA-N D-histidine Chemical compound OC(=O)[C@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-RXMQYKEDSA-N 0.000 description 2
- 229930195721 D-histidine Natural products 0.000 description 2
- 229930182845 D-isoleucine Natural products 0.000 description 2
- KDXKERNSBIXSRK-RXMQYKEDSA-N D-lysine Chemical compound NCCCC[C@@H](N)C(O)=O KDXKERNSBIXSRK-RXMQYKEDSA-N 0.000 description 2
- FFEARJCKVFRZRR-SCSAIBSYSA-N D-methionine Chemical compound CSCC[C@@H](N)C(O)=O FFEARJCKVFRZRR-SCSAIBSYSA-N 0.000 description 2
- 229930182818 D-methionine Natural products 0.000 description 2
- COLNVLDHVKWLRT-MRVPVSSYSA-N D-phenylalanine Chemical compound OC(=O)[C@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-MRVPVSSYSA-N 0.000 description 2
- 229930182832 D-phenylalanine Natural products 0.000 description 2
- 229930182820 D-proline Natural products 0.000 description 2
- 229930182827 D-tryptophan Natural products 0.000 description 2
- QIVBCDIJIAJPQS-SECBINFHSA-N D-tryptophane Chemical compound C1=CC=C2C(C[C@@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-SECBINFHSA-N 0.000 description 2
- OUYCCCASQSFEME-MRVPVSSYSA-N D-tyrosine Chemical compound OC(=O)[C@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-MRVPVSSYSA-N 0.000 description 2
- 229930195709 D-tyrosine Natural products 0.000 description 2
- KZSNJWFQEVHDMF-SCSAIBSYSA-N D-valine Chemical compound CC(C)[C@@H](N)C(O)=O KZSNJWFQEVHDMF-SCSAIBSYSA-N 0.000 description 2
- 229930182831 D-valine Natural products 0.000 description 2
- 229930195710 D‐cysteine Natural products 0.000 description 2
- 108010073807 IgG Receptors Proteins 0.000 description 2
- 102000009490 IgG Receptors Human genes 0.000 description 2
- 102000009786 Immunoglobulin Constant Regions Human genes 0.000 description 2
- 108010009817 Immunoglobulin Constant Regions Proteins 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 150000008575 L-amino acids Chemical class 0.000 description 2
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical group CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 2
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 108020004682 Single-Stranded DNA Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 150000001371 alpha-amino acids Chemical class 0.000 description 2
- 235000008206 alpha-amino acids Nutrition 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 235000009582 asparagine Nutrition 0.000 description 2
- 229960001230 asparagine Drugs 0.000 description 2
- 235000003704 aspartic acid Nutrition 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 239000000710 homodimer Substances 0.000 description 2
- 210000005260 human cell Anatomy 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 229940072221 immunoglobulins Drugs 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- 238000007913 intrathecal administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 2
- 229960000310 isoleucine Drugs 0.000 description 2
- 238000012004 kinetic exclusion assay Methods 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 230000004770 neurodegeneration Effects 0.000 description 2
- 208000015122 neurodegenerative disease Diseases 0.000 description 2
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 2
- 238000002823 phage display Methods 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 239000013612 plasmid Substances 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 238000001542 size-exclusion chromatography Methods 0.000 description 2
- JUJBNYBVVQSIOU-UHFFFAOYSA-M sodium;4-[2-(4-iodophenyl)-3-(4-nitrophenyl)tetrazol-2-ium-5-yl]benzene-1,3-disulfonate Chemical compound [Na+].C1=CC([N+](=O)[O-])=CC=C1N1[N+](C=2C=CC(I)=CC=2)=NC(C=2C(=CC(=CC=2)S([O-])(=O)=O)S([O-])(=O)=O)=N1 JUJBNYBVVQSIOU-UHFFFAOYSA-M 0.000 description 2
- 230000001954 sterilising effect Effects 0.000 description 2
- 238000004659 sterilization and disinfection Methods 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 125000000341 threoninyl group Chemical group [H]OC([H])(C([H])([H])[H])C([H])(N([H])[H])C(*)=O 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- 230000004614 tumor growth Effects 0.000 description 2
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 2
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 1
- UKAUYVFTDYCKQA-UHFFFAOYSA-N -2-Amino-4-hydroxybutanoic acid Natural products OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 241000024188 Andala Species 0.000 description 1
- 108091008875 B cell receptors Proteins 0.000 description 1
- 230000003844 B-cell-activation Effects 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 108010001017 CD71 antigen Proteins 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 102000000844 Cell Surface Receptors Human genes 0.000 description 1
- 108010001857 Cell Surface Receptors Proteins 0.000 description 1
- 241000699802 Cricetulus griseus Species 0.000 description 1
- ROHFNLRQFUQHCH-RXMQYKEDSA-N D-leucine Chemical compound CC(C)C[C@@H](N)C(O)=O ROHFNLRQFUQHCH-RXMQYKEDSA-N 0.000 description 1
- 229930182819 D-leucine Natural products 0.000 description 1
- AYFVYJQAPQTCCC-STHAYSLISA-N D-threonine Chemical compound C[C@H](O)[C@@H](N)C(O)=O AYFVYJQAPQTCCC-STHAYSLISA-N 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 108090000626 DNA-directed RNA polymerases Proteins 0.000 description 1
- 102000004163 DNA-directed RNA polymerases Human genes 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 206010014733 Endometrial cancer Diseases 0.000 description 1
- 206010014759 Endometrial neoplasm Diseases 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- 102000006395 Globulins Human genes 0.000 description 1
- 108010044091 Globulins Proteins 0.000 description 1
- 101000835093 Homo sapiens Transferrin receptor protein 1 Proteins 0.000 description 1
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 125000000570 L-alpha-aspartyl group Chemical group [H]OC(=O)C([H])([H])[C@]([H])(N([H])[H])C(*)=O 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-N L-arginine Chemical compound OC(=O)[C@@H](N)CCCN=C(N)N ODKSFYDXXFIFQN-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- UKAUYVFTDYCKQA-VKHMYHEASA-N L-homoserine Chemical group OC(=O)[C@@H](N)CCO UKAUYVFTDYCKQA-VKHMYHEASA-N 0.000 description 1
- QEFRNWWLZKMPFJ-ZXPFJRLXSA-N L-methionine (R)-S-oxide Chemical group C[S@@](=O)CC[C@H]([NH3+])C([O-])=O QEFRNWWLZKMPFJ-ZXPFJRLXSA-N 0.000 description 1
- QEFRNWWLZKMPFJ-UHFFFAOYSA-N L-methionine sulphoxide Chemical group CS(=O)CCC(N)C(O)=O QEFRNWWLZKMPFJ-UHFFFAOYSA-N 0.000 description 1
- 125000000393 L-methionino group Chemical group [H]OC(=O)[C@@]([H])(N([H])[*])C([H])([H])C(SC([H])([H])[H])([H])[H] 0.000 description 1
- 241000282560 Macaca mulatta Species 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- 102000048238 Neuregulin-1 Human genes 0.000 description 1
- 108090000556 Neuregulin-1 Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 241000282577 Pan troglodytes Species 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 206010057249 Phagocytosis Diseases 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 1
- 208000004337 Salivary Gland Neoplasms Diseases 0.000 description 1
- 206010061934 Salivary gland cancer Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000012491 analyte Substances 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 108010081355 beta 2-Microglobulin Proteins 0.000 description 1
- 102000015736 beta 2-Microglobulin Human genes 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 230000009702 cancer cell proliferation Effects 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- UHBYWPGGCSDKFX-UHFFFAOYSA-N carboxyglutamic acid Chemical compound OC(=O)C(N)CC(C(O)=O)C(O)=O UHBYWPGGCSDKFX-UHFFFAOYSA-N 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000022534 cell killing Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000009614 chemical analysis method Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 1
- 239000013611 chromosomal DNA Substances 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 239000013599 cloning vector Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000000112 colonic effect Effects 0.000 description 1
- 230000001447 compensatory effect Effects 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 239000003636 conditioned culture medium Substances 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000028023 exocytosis Effects 0.000 description 1
- 238000012239 gene modification Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 230000005017 genetic modification Effects 0.000 description 1
- 235000013617 genetically modified food Nutrition 0.000 description 1
- 125000000404 glutamine group Chemical group N[C@@H](CCC(N)=O)C(=O)* 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 125000001165 hydrophobic group Chemical group 0.000 description 1
- 229960002591 hydroxyproline Drugs 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 238000012933 kinetic analysis Methods 0.000 description 1
- 125000001909 leucine group Chemical group [H]N(*)C(C(*)=O)C([H])([H])C(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- LSDPWZHWYPCBBB-UHFFFAOYSA-O methylsulfide anion Chemical compound [SH2+]C LSDPWZHWYPCBBB-UHFFFAOYSA-O 0.000 description 1
- 238000002493 microarray Methods 0.000 description 1
- 108091005601 modified peptides Proteins 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 238000002703 mutagenesis Methods 0.000 description 1
- 231100000350 mutagenesis Toxicity 0.000 description 1
- 108010068617 neonatal Fc receptor Proteins 0.000 description 1
- 230000001613 neoplastic effect Effects 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000008782 phagocytosis Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- BZQFBWGGLXLEPQ-REOHCLBHSA-N phosphoserine Chemical compound OC(=O)[C@@H](N)COP(O)(O)=O BZQFBWGGLXLEPQ-REOHCLBHSA-N 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 210000004180 plasmocyte Anatomy 0.000 description 1
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 1
- 230000036515 potency Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 235000004252 protein component Nutrition 0.000 description 1
- 238000002818 protein evolution Methods 0.000 description 1
- 230000012846 protein folding Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 230000003362 replicative effect Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 210000001995 reticulocyte Anatomy 0.000 description 1
- 239000002336 ribonucleotide Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 239000012146 running buffer Substances 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 125000003607 serino group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(O[H])([H])[H] 0.000 description 1
- 239000013605 shuttle vector Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 238000011146 sterile filtration Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000001384 succinic acid Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- FGMPLJWBKKVCDB-UHFFFAOYSA-N trans-L-hydroxy-proline Natural products ON1CCCC1C(O)=O FGMPLJWBKKVCDB-UHFFFAOYSA-N 0.000 description 1
- 230000031998 transcytosis Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 230000004565 tumor cell growth Effects 0.000 description 1
- 230000010304 tumor cell viability Effects 0.000 description 1
- 241000701161 unidentified adenovirus Species 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 230000036642 wellbeing Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
- A61K39/001102—Receptors, cell surface antigens or cell surface determinants
- A61K39/001103—Receptors for growth factors
- A61K39/001106—Her-2/neu/ErbB2, Her-3/ErbB3 or Her 4/ErbB4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2881—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against CD71
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/526—CH3 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/53—Hinge
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/71—Decreased effector function due to an Fc-modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Abstract
일 양태에서, 인간 HER2의 서브도메인 II 및 인간 HER2의 서브도메인 IV 둘 모두에 특이적으로 결합하는 능력이 있는 이중특이성 단백질이 제공된다. 또 다른 양태에서, 서브도메인 II 및 인간 HER2의 서브도메인 IV에 특이적으로 결합하는 이중특이성 단백질을 사용하여 암을 치료하거나 또는 암의 뇌 전이를 치료하는 방법이 제공된다.
Description
관련 출원에 대한 상호-참조
본 출원은 2020년 2월 19일자로 출원된 미국 특허 가출원 제62/978,758호에 대한 우선권을 주장하며, 이의 개시내용은 모든 목적을 위해 그 전문이 참조에 의해 본 명세서에 원용된다.
유방암과 같은 암의 뇌 전이의 치료는 현재 어려운 임상적 도전을 제기한다. 유방암 환자 중에서, 뇌 전이의 발병률은 50%만큼 높다. 임상적 데이터는 HER2-양성 유방암이 뇌로 전이되는 성향이 있음을 나타낸다. 특히, 항-HER2 요법은 두개외 종양의 제어에는 유용하지만 두개내 병변에 대해서는 그렇지 않은 것으로 입증되었다. HER2-양성 유방암의 뇌 전이와 같은 전이성 병변을 제어하는 것에 대한 이러한 요법의 실패는 대부분 혈액 뇌 장벽(blood brain barrier: BBB)을 횡단하고 뇌 실질에 접근하지 못하는 것에 기인한다.
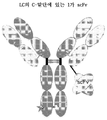
일 양태에서, 본 개시내용은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 단일쇄 가변 단편(scFv)에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 경쇄 폴리펩타이드
를 포함하는 단백질을 제공하되,
Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다. 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합한다. 다른 실시형태에서, Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다.
이러한 단백질의 일부 실시형태에서, 제2 Fc 폴리펩타이드는 제1 링커를 통해 scFv에 융합된다. 제1 링커는 1개 내지 20개의 아미노산 길이, 예를 들어, GGGGSGGGGS(서열번호 118)를 가질 수 있다.
이러한 단백질의 일부 실시형태에서, scFv는 제2 링커를 통해 연결된 VL 영역 및 VH 영역을 포함한다. 제2 링커는 1개 내지 20개의 아미노산 길이, 예를 들어, GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 가질 수 있다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 부위를 생성하는 본 명세서에 기재된 임의의 서열 변형을 포함함)에 특이적으로 결합한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함한다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함한다. 다른 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함한다. 소정의 실시형태에서, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다.
이러한 단백질의 일부 실시형태에서, 힌지 영역 또는 이의 일부는 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드의 N-말단에 연결된다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 특정 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 다른 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 21의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 20의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 19의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 4에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 18의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 15 또는 17의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 14의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 13의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 11 또는 12의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 22의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 및 (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 18의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
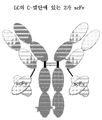
또 다른 양태에서, 본 개시내용은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하는 단백질을 특징으로 하되;
제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되거나, 또는
(a) 및/또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되거나, 또는
제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되고,
Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합된다. 일부 실시형태에서, (a) 및/또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합된다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합된다.
이러한 단백질의 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합한다. 다른 실시형태에서, Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드에 융합된 scFv는 동일한 서열을 포함한다. 다른 실시형태에서, (a) 및/또는 (b)의 Fd 부분에 융합된 scFv는 동일한 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 제1 링커를 통해 scFv에 융합된다. 일부 실시형태에서, (a) 및/또는 (b)의 Fd 부분은 제1 링커를 통해 scFv에 융합된다. 소정의 실시형태에서, 제1 링커는 1개 내지 20개의 아미노산 길이, 예를 들어, GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 갖는다.
이러한 단백질의 일부 실시형태에서, scFv는 제2 링커를 통해 연결된 VL 영역 및 VH 영역을 포함한다. 일부 실시형태에서, 제2 링커는 1개 내지 20개의 아미노산 길이, 예를 들어, GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 갖는다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 부위를 생성하는 본 명세서에 기재된 임의의 서열 변형을 포함함)에 특이적으로 결합한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함한다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함한다. 다른 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함한다. 소정의 실시형태에서, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환을 갖는다. 일부 실시형태에서, 힌지 영역 또는 이의 일부는 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드의 N-말단에 연결된다. 소정의 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 특정 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 다른 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 27 또는 28의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 29의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 30의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 31의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 33 또는 34의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 35의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 36의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 37 또는 39의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 37의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 157의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 27 또는 28의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 31의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 29의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 30의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 33 또는 34의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 37 또는 39의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 35의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 36의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 33의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 38의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 40의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 41의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 42의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 43의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 45 또는 46의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 47의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 48의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 49의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 44의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 50의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(xi) (a) 서열번호 156의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 40의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 43의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 41의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 42의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 45의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 49의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 47의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 48의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 45의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 50의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 46의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 156의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되고,
(i) (a) 서열번호 40의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 31의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 41의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 30의 서열의 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 42의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 29의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 43의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 27 또는 28의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 45의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 37 또는 39의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 47의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 36의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 48의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 35의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 49의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 33 또는 34의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
또 다른 양태에서, 본 개시내용은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하는 단백질을 제공하되,
경쇄 폴리펩타이드 중 하나 또는 둘 모두는 N-말단에서 scFv에 융합되거나, 또는
경쇄 폴리펩타이드 중 하나 또는 둘 모두는 C-말단에서 scFv에 융합되거나, 또는
제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고,
Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다.
이러한 단백질의 일부 실시형태에서, 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 N-말단에서 scFv에 융합된다. 일부 실시형태에서, 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 C-말단에서 scFv에 융합된다.
이러한 단백질의 일부 실시형태에서, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합된다.
이러한 단백질의 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합한다. 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다.
이러한 단백질의 일부 실시형태에서, 경쇄 폴리펩타이드 중 하나 또는 둘 모두에 융합되는 scFv는 동일한 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 제1 링커를 통해 scFv에 융합된다. 일부 실시형태에서, 제1 링커는 1개 내지 20개의 아미노산 길이인 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 갖는다.
이러한 단백질의 일부 실시형태에서, scFv는 제2 링커를 통해 연결된 VL 영역 및 VH 영역을 포함한다. 일부 실시형태에서, 제2 링커는 1개 내지 20개의 아미노산 길이인 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 갖는다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 부위를 생성하는 본 명세서에 기재된 임의의 서열 변형을 포함함)에 특이적으로 결합한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함한다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함한다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함한다. 이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함한다. 일부 실시형태에서, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다.
이러한 단백질의 일부 실시형태에서, 힌지 영역 또는 이의 일부는 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드의 N-말단에 연결된다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 특정 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 그리고 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 다른 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 그리고 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
또 다른 양태에서, 본 개시내용은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하는 단백질을 제공하되,
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 Fv 단편의 VH 영역 또는 VL 영역에 융합되고,
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VH 영역 또는 VL 영역 중 다른 하나에 융합되며,
VH 영역 및 VL 영역은 함께 Fv 단편을 형성하고, 그리고
Fab는 인간 HER2의 서브도메인 II에 결합하고, Fv 단편은 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, Fv 단편은 인간 HER2의 서브도메인 II에 결합한다.
이러한 단백질의 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 II에 결합하고, Fv 단편은 인간 HER2의 서브도메인 IV에 결합한다. 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 IV에 결합하고, Fv 단편은 인간 HER2의 서브도메인 II에 결합한다.
이러한 단백질의 일부 실시형태에서, (a) 및 (b)의 Fd 부분 각각은 N-말단에서 제1 링커를 통해 VH 영역 또는 VL 영역에 융합된다. 일부 실시형태에서, 제1 링커는 1개 내지 20개의 아미노산 길이, 예를 들어, ASTKGPSVF(서열번호 125)의 서열을 갖는다.
이러한 단백질의 일부 실시형태에서, 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 제2 링커를 통해 VH 영역 또는 VL 영역에 융합된다. 일부 실시형태에서, 제2 링커는 1개 내지 20개의 아미노산 길이, 예를 들어, RTVAAPSVFI(서열번호 126)의 서열을 갖는다.
이러한 단백질의 일부 실시형태에서, (a) 및 (b)의 Fd 부분 각각은 N-말단에서 Fv 단편의 VH 영역에 융합되고, 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VL 영역에 융합된다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 부위를 생성하는 본 명세서에 기재된 임의의 서열 변형을 포함함)에 특이적으로 결합한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 T366W 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함한다. 다른 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함한다. 특정 실시형태에서, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다.
이러한 단백질의 일부 실시형태에서, 힌지 영역 또는 이의 일부는 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드의 N-말단에 연결된다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 특정 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 다른 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 58의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 61의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 78의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함하거나; 또는
(ii) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 59의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 60의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 78의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함하거나; 또는
(iii) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 63의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 66의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 79의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함하거나; 또는
(iv) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 64의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 65의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 79의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함하거나; 또는
(v) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 63의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 67의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 79의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 68의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 71의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 80의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함하거나; 또는
(ii) 제1 폴리펩타이드는 (a) N-말단에서 VL 영역의 Fv 단편에 융합되며 서열번호 69의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 70의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 80의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함하거나; 또는
(iii) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 73의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 76의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 81의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함하거나; 또는
(iv) 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 74의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 75의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 각각 포함하며 서열번호 81의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 각각 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 다른 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
또 다른 양태에서, 본 개시내용은
(a) N-말단에서 Fab의 Fd 부분에 융합되며 C-말단에서 Fv 단편의 VH 영역 또는 VL 영역에 융합되는 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합되며 C-말단에서 (a)에 언급된 VH 영역 또는 VL 영역의 다른 부분에 융합되는 제2 Fc 폴리펩타이드로서,
VH 영역 및 VL 영역은 함께 Fv 단편을 형성하고, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하는 단백질을 제공하되,
Fab는 인간 HER2의 서브도메인 II에 결합하고, Fv 단편은 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, Fv 단편은 인간 HER2의 서브도메인 II에 결합한다. 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 II에 결합하고, Fv 단편은 인간 HER2의 서브도메인 IV에 결합한다. 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 IV에 결합하고, Fv 단편은 인간 HER2의 서브도메인 II에 결합한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 Fv 단편의 VH 영역에 융합되고, 제2 Fc 폴리펩타이드는 Fv 단편의 VL 영역에 융합된다. 일부 실시형태에서, 제1 Fc 폴리펩타이드는 Fv 단편의 VL 영역에 융합되고, 제2 Fc 폴리펩타이드는 Fv 단편의 VH 영역에 융합된다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 C-말단에서 제1 링커를 통해 VH 영역 또는 VL 영역에 융합된다.
이러한 단백질의 일부 실시형태에서, 제1 링커는 1개 내지 20개의 아미노산 길이, 예를 들어, GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 갖는다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR 결합 부위를 생성하는 본 명세서에 기재된 임의의 서열 변형을 포함함)에 특이적으로 결합한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함한다. 일부 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함한다. 다른 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함한다. 소정의 실시형태에서, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다.
이러한 단백질의 일부 실시형태에서, 힌지 영역 또는 이의 일부는 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드의 N-말단에 연결된다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 다른 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서,
(i) (a) 서열번호 82 또는 83의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 99 또는 100의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 84의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 98의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 85의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 97의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 86 또는 88의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 95 또는 96의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 89 또는 90의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 105 또는 107의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 91의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 104의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 92의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 103의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 93의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 102의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 82의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 99의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 82의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 100의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(xi) (a) 서열번호 90의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 107의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하거나; 또는
(xii) (a) 서열번호 90의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 158의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
이러한 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 다른 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
본 개시내용의 또 다른 양태에서, 본 개시내용은 본 명세서에 기재된 임의의 단백질 및 약제학적으로 허용 가능한 담체를 포함하는 약제학적 조성물을 제공한다.
본 개시내용의 또 다른 양태에서, 본 개시내용은 본 명세서에 기재된 단백질을 암호화하는 뉴클레오타이드 서열을 포함하는 단리된 폴리뉴클레오타이드를 제공한다.
본 개시내용의 또 다른 양태에서, 본 개시내용은 이전의 양태의 폴리뉴클레오타이드를 포함하는 벡터를 제공한다.
본 개시내용의 또 다른 양태에서, 본 개시내용은 폴리뉴클레오타이드 또는 벡터를 포함하는 숙주 세포를 제공한다.
본 개시내용의 또 다른 양태에서, 본 개시내용은 대상체에서 암을 치료하거나 또는 암의 뇌 전이를 치료하는 방법을 제공하며, 방법은 치료학적 유효량의 본 명세서에 기재된 단백질 또는 이를 포함하는 약제학적 조성물을 대상체에게 투여하는 단계를 포함한다.
방법의 일부 실시형태에서, 단백질은 화학요법 또는 방사선 요법과 조합하여 투여된다.
방법의 일부 실시형태에서, 암은 전이성 암이다. 일부 실시형태에서, 암은 유방암이다. 일부 실시형태에서, 암은 HER2 양성 암이다.
도 1a는 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 힌지 또는 부분적인 힌지 영역을 통해 TfR-결합 부위(별표) 및 놉 돌연변이(knob mutation)를 갖는 Fc 폴리펩타이드의 N-말단에 융합되는 반면, 다른 Fc 폴리펩타이드는 홀 돌연변이(hole mutation)를 갖는다.
도 1b는 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 힌지 또는 부분적인 힌지 영역을 통해 홀 돌연변이를 갖는 Fc 폴리펩타이드의 N-말단에 융합되는 반면, 다른 Fc 폴리펩타이드는 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는다.
도 2a는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 홀 돌연변이를 갖는 Fc 폴리펩타이드의 C-말단에 융합되는 반면, 다른 Fc 폴리펩타이드는 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는다.
도 2b는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 링커를 통해 Fd 부분의 N-말단에 융합된다. scFv는 홀 돌연변이를 갖는 Fc 폴리펩타이드를 포함하는 중쇄의 Fd 부분에 융합되는 반면, 다른 Fc 폴리펩타이드는 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는다.
도 2c는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 중쇄의 Fd 부분의 N-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 2d는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 중쇄의 Fc 폴리펩타이드의 C-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3a는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 링커를 통해 경쇄의 C-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3b는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 링커를 통해 경쇄의 N-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3c는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 경쇄의 N-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3d는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 경쇄의 C-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 4는 "HC 및 LC 상의 mAb/N-말단 VH VL" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 VH 영역은 각각 중쇄의 Fd 부분의 N-말단에 융합되고, 2개의 VL 영역은 각각 경쇄의 N-말단에 융합된다. VH 영역 및 VL 영역은 Fv 단편을 형성한다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 5는 "HC 상의 mAb/C-말단 VH VL" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 VH 영역은 홀 돌연변이를 갖는 Fc 폴리펩타이드의 C-말단에 융합되고, VL 영역은 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는 Fc 폴리펩타이드의 C-말단에 융합된다. VH 영역 및 VL 영역은 Fv 단편을 형성한다.
도 6a 및 도 6b는 각각 BT474 및 OE19 세포의 성장 저해 검정에서 제6일 및 제3일에 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 이중특이성 단백질에 의한 암 세포 증식의 저해를 보여준다.
도 7은 C57/BL6 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 혈장 PK 프로파일을 보여주는 플롯이다.
도 8a는 항-HER2 이중특이성 단백질 또는 항-HER2 대조군이 정맥내로 투여된 TfRmu/hu KI 마우스에서 망상적혈구 정량화를 보여주는 플롯이다.
도 8b는 TfRmu/hu KI 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 혈장 PK 프로파일을 보여주는 플롯이다.
도 8c는 TfRmu/hu KI 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 뇌 PK 프로파일을 보여주는 플롯이다.
도 8d는 TfRmu/hu KI 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 뇌-대-혈장 농도의 백분율을 보여주는 플롯이다.
도 9a 내지 도 9f는 항-HER2 이중특이성 단백질 및 항-HER2 대조군에 의한 NRG1이 있거나(도 9a 내지 도 9c) 또는 없는(도 9d 내지 도 9f) BT474 세포의 성장 저해 검정을 보여준다.
도 9g 내지 도 9i는 항-HER2 이중특이성 단백질 및 항-HER2 대조군에 의한 OE19 세포의 성장 저해 검정을 보여준다.
도 9j 내지 도 9l은 항-HER2 이중특이성 단백질 및 항-HER2 대조군에 의한 ZR75 세포의 성장 저해 검정을 보여준다.
도 1b는 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 힌지 또는 부분적인 힌지 영역을 통해 홀 돌연변이를 갖는 Fc 폴리펩타이드의 N-말단에 융합되는 반면, 다른 Fc 폴리펩타이드는 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는다.
도 2a는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 홀 돌연변이를 갖는 Fc 폴리펩타이드의 C-말단에 융합되는 반면, 다른 Fc 폴리펩타이드는 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는다.
도 2b는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 링커를 통해 Fd 부분의 N-말단에 융합된다. scFv는 홀 돌연변이를 갖는 Fc 폴리펩타이드를 포함하는 중쇄의 Fd 부분에 융합되는 반면, 다른 Fc 폴리펩타이드는 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는다.
도 2c는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 중쇄의 Fd 부분의 N-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 2d는 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 중쇄의 Fc 폴리펩타이드의 C-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3a는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 링커를 통해 경쇄의 C-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3b는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 scFv는 링커를 통해 경쇄의 N-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3c는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 경쇄의 N-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 3d는 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 scFv는 각각 링커를 통해 경쇄의 C-말단에 융합된다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 4는 "HC 및 LC 상의 mAb/N-말단 VH VL" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 2개의 VH 영역은 각각 중쇄의 Fd 부분의 N-말단에 융합되고, 2개의 VL 영역은 각각 경쇄의 N-말단에 융합된다. VH 영역 및 VL 영역은 Fv 단편을 형성한다. Fc 폴리펩타이드 상의 TfR-결합 부위는 별표로 표시된다.
도 5는 "HC 상의 mAb/C-말단 VH VL" 구조를 갖는 예시적인 이중특이성 단백질을 보여주는 개략도이며, 여기서 VH 영역은 홀 돌연변이를 갖는 Fc 폴리펩타이드의 C-말단에 융합되고, VL 영역은 TfR-결합 부위(별표) 및 놉 돌연변이를 갖는 Fc 폴리펩타이드의 C-말단에 융합된다. VH 영역 및 VL 영역은 Fv 단편을 형성한다.
도 6a 및 도 6b는 각각 BT474 및 OE19 세포의 성장 저해 검정에서 제6일 및 제3일에 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 이중특이성 단백질에 의한 암 세포 증식의 저해를 보여준다.
도 7은 C57/BL6 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 혈장 PK 프로파일을 보여주는 플롯이다.
도 8a는 항-HER2 이중특이성 단백질 또는 항-HER2 대조군이 정맥내로 투여된 TfRmu/hu KI 마우스에서 망상적혈구 정량화를 보여주는 플롯이다.
도 8b는 TfRmu/hu KI 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 혈장 PK 프로파일을 보여주는 플롯이다.
도 8c는 TfRmu/hu KI 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 뇌 PK 프로파일을 보여주는 플롯이다.
도 8d는 TfRmu/hu KI 마우스에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 뇌-대-혈장 농도의 백분율을 보여주는 플롯이다.
도 9a 내지 도 9f는 항-HER2 이중특이성 단백질 및 항-HER2 대조군에 의한 NRG1이 있거나(도 9a 내지 도 9c) 또는 없는(도 9d 내지 도 9f) BT474 세포의 성장 저해 검정을 보여준다.
도 9g 내지 도 9i는 항-HER2 이중특이성 단백질 및 항-HER2 대조군에 의한 OE19 세포의 성장 저해 검정을 보여준다.
도 9j 내지 도 9l은 항-HER2 이중특이성 단백질 및 항-HER2 대조군에 의한 ZR75 세포의 성장 저해 검정을 보여준다.
I. 도입
일 양태에서, 인간 HER2의 서브도메인 II 및 인간 HER2의 서브도메인 IV 모두에 결합할 수 있는 이중특이성 단백질이 제공된다. 이중특이성 단백질은 일반적으로 경쇄 미스페어링(mispairing) 또는 스티어링(steering) 없이 생성될 수 있다. 일부 실시형태에서, 이중특이성 단백질은 각 인간 HER2의 표적 서브도메인에 1가로 결합한다. 일부 실시형태에서, 이중특이성 단백질은 인간 HER2의 하나의 표적 서브도메인에 1가로 결합하고, 인간 HER2의 다른 표적 서브도메인에 2가로(예를 들어, 서브도메인 II에 1가로 그리고 서브도메인 IV에 2가로 또는 서브도메인 IV에 1가로 그리고 서브도메인 II에 2가로) 결합한다. 일부 실시형태에서, 이중특이성 단백질은 인간 HER2의 각 표적 서브도메인에 2가로 결합한다. 다양한 구조의 이중특이성 단백질이 본 명세서에서 추가로 상세히 기재되어 있다.
일부 실시형태에서, 이중특이성 단백질은 인간 HER2의 서브도메인 II(또는 서브도메인 IV)에 결합하는 scFv 및 인간 HER2의 서브도메인 IV(또는 서브도메인 II)에 결합하는 Fab를 포함한다(예를 들어, 부문 III의 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조 참조). 일부 실시형태에서, 이중특이성 단백질은 이중특이성 단백질의 중쇄의 N-말단 또는 C-말단에 연결된 하나 이상의 scFv를 포함하며, 여기서 scFv는 인간 HER2의 서브도메인 II(또는 서브도메인 IV)에 결합하고, 이중특이성 단백질의 Fab는 인간 HER2의 서브도메인 IV(또는 서브도메인 II)에 결합한다(예를 들어, 부문 III의 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조 참조). 일부 실시형태에서, 이중특이성 단백질은 이중특이성 단백질의 경쇄의 N-말단 또는 C-말단에 연결된 하나 이상의 scFv를 포함하며, 여기서 scFv는 인간 HER2의 서브도메인 II(또는 서브도메인 IV)에 결합하고, 이중특이성 단백질의 Fab는 인간 HER2의 서브도메인 IV(또는 서브도메인 II)에 결합한다(예를 들어, 부문 III의 "HC 상의 mAb/N-말단 또는 C-말단 scFv LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조 참조). 일부 실시형태에서, 이중특이성 단백질은 중쇄의 N-말단에 연결된 Fv 단편의 VH 영역(또는 VL 영역) 및 경쇄의 N-말단에 연결된 Fv 단편의 VL 영역(또는 VH 영역)을 포함하며, 여기서 Fv 단편은 인간 HER2의 서브도메인 II(또는 서브도메인 IV)에 결합하고, 이중특이성 단백질의 Fab는 인간 HER2의 서브도메인 IV(또는 서브도메인 II)에 결합한다(예를 들어, 부문 III의 "HC 및 LC 상의 mAb/N-말단 VH VL" 구조 참조). 또 다른 실시형태에서, 이중특이성 단백질은 이중특이성 단백질의 2개의 중쇄 중 하나의 C-말단에 연결된 Fv 단편의 VH 영역(또는 VL 영역) 및 2개의 중쇄 중 다른 하나의 C-말단에 연결된 Fv 단편의 VL 영역(또는 VH 영역)을 포함하며, 여기서 Fv 단편은 인간 HER2의 서브도메인 II(또는 서브도메인 IV)에 결합하고, 이중특이성 단백질의 Fab는 인간 HER2의 서브도메인 IV(또는 서브도메인 II)에 결합한다(예를 들어, 부문 III의 "HC 상의 mAb/C-말단 VH VL" 구조 참조).
이전의 요법은 주로 치료제가 혈액 뇌 장벽(BBB)을 가로질러 뇌 실질에 접근할 수 없기 때문에 HER2-양성 유방암의 뇌 전이를 제어하는 데 실패하였다. 따라서, BBB를 가로질러 뇌 실질에서 HER2를 표적화할 수 있는 새로운 치료제가 필요하다. 본 발명자들은 이전에 TfR의 발현이 뇌 내피 세포에서 고도로 발현되며 수용체-매개성 통과세포외배출(transcytosis)을 통해 BBB 전달을 가능하게 할 수 있기 때문에, 뇌 내피를 가로질러 BBB 전달을 가능하게 하는 방법으로 트랜스페린 수용체(TfR)-결합의 사용을 기술하였다. 흥미롭게도, TfR은 HER2-양성 유방암을 포함하는 다양한 암에서 고도로 발현된다. 암 세포가 증가된 TfR 발현을 획득하는 메커니즘은 종양 세포 증식 및 철 흡수와 같은 증가된 대사 요구와 관련될 가능성이 있다. 사실, 공개 마이크로어레이 데이터세트는 유방암 예후와 TfR 발현의 상관관계를 보여주었다(Miller et al., Cancer Res. 71:6728, 2011). 또한, 다양한 유형의 암에 대한 약리학적 표적으로 TfR을 사용하는 것에 대한 일부 보고가 있었다.
일부 실시형태에서, 이중특이성 단백질은 BBB 수용체, 예를 들어, TfR에 특이적으로 결합하는 하나 이상의 변형된 Fc 폴리펩타이드(즉, TfR-결합 Fc 폴리펩타이드)를 포함한다. 일부 실시형태에서, 이중특이성 단백질은 BBB를 통해 수송될 수 있다. 일부 실시형태에서, 본 명세서에 기재된 바와 같은 HER2 및 TfR 둘 모두에 결합하는 항-HER2 이중특이성 단백질은 HER2에만 결합하는 다른 치료제와 비교하여 높은 수준의 TfR을 또한 발현하는 HER2-양성 종양 세포에 결합 시 추가적인 항-종양 이점을 제공할 수 있다. 구체적으로, 이러한 단백질은 TfR과 HER2 둘 모두에 동시에 결합할 수 있으므로, 이는 이들의 효험 및/또는 효능을 향상시킬 수 있다.
II. 정의
본 명세서에서 사용되는 바와 같이, "단수" 형태는 문맥에서 명백히 달리 나타내지 않는 한 복수의 지시대상을 포함한다. 따라서, 예를 들어, "항체"에 대한 언급은 선택적으로 2개 이상의 이러한 분자 등의 조합을 포함한다.
본 명세서에서 사용되는 용어 "약" 및 "대략"은 숫자 값 또는 범위로 지정된 양을 수정하는 데 사용될 때 숫자 값뿐만 아니라 당업자에게 공지된 값으로부터의 합리적인 편차를 나타내며, 예를 들어 ± 20%, ± 10% 또는 ± 5%가 인용된 값의 의도된 의미 내에 있다.
본 명세서에서 사용되는 용어 "항체"는 이의 가변 영역을 통해 항원에 특이적으로 결합하는 면역글로불린 접힘을 갖는 단백질을 지칭한다. 용어는 온전한 다중클론 항체, 온전한 단일클론 항체, 단일쇄 항체, 다중특이성 항체, 예컨대, 이중특이성 항체, 단일특이성 항체, 1가 항체, 키메라 항체, 인간화된 항체 및 인간 항체를 포함한다. 본 명세서에서 사용되는 용어 "항체"는 또한 Fab, F(ab')2, Fv, scFv 및 2가 scFv를 포함하지만 이들로 제한되지 않는 항원-결합 특이성을 유지하는 항체 단편을 포함한다. 항체는 카파 또는 람다로 분류되는 경쇄를 포함할 수 있다. 항체는 감마, 뮤, 알파, 델타 또는 엡실론으로 분류되는 중쇄를 포함할 수 있으며, 이들은 차례로 면역글로불린 클래스인 IgG, IgM, IgA, IgD 및 IgE를 각각 정의한다.
예시적인 면역글로불린(항체) 구조 단위는 사량체를 포함한다. 각각의 사량체는 폴리펩타이드 사슬의 2개의 동일한 쌍으로 구성되며, 각각의 쌍은 하나의 "경쇄"(약 25kD) 및 하나의 "중쇄"(약 50kD 내지 70kD)를 갖는다. 각 사슬의 N-말단은 주로 항원 인식을 담당하는 약 100개 내지 110개 이상의 아미노산의 가변 영역을 정의한다. 용어 "가변 경쇄"(VL) 및 "가변 중쇄"(VH)는 각각 이들 경쇄 및 중쇄를 지칭한다.
용어 "가변 영역" 또는 "가변 도메인"은 생식세포계열 가변(V) 유전자, 다양성(D) 유전자 또는 결합(J) 유전자(및 불변(Cμ 및 Cδ) 유전자 분절로부터 유래되지 않음)로부터 유래되며, 항체에 항원에 대한 결합에 대한 특이성을 제공하는 항체 중쇄 또는 경쇄의 도메인을 지칭한다. 전형적으로, 항체 가변 영역은 3개의 초가변 "상보성 결정 영역"이 산재된 4개의 보존된 "프레임워크" 영역을 포함한다.
용어 "상보성 결정 영역" 또는 "CDR"은 경쇄 및 중쇄 가변 영역에 의해 확립된 4개의 프레임워크 영역을 중단시키는 각각의 사슬 내의 3개의 초가변 영역을 지칭한다. CDR은 주로 항원의 에피토프에 대한 항체의 결합을 담당한다. 각각 사슬의 CDR은 N-말단으로부터 출발하여 순차적으로 넘버링 되는 CDR1, CDR2 및 CDR3로 지칭되며, 또한 전형적으로 특정 CDR이 위치하는 사슬에 의해 식별된다. 따라서, VH CDR3 또는 CDR-H3은 이것이 발견되는 항체의 중쇄의 가변 영역에 위치하는 반면, VL CDR1 또는 CDR-L1은 이것이 발견되는 항체의 경쇄의 가변 영역으로부터의 CDR1이다.
상이한 경쇄 또는 중쇄의 "프레임워크 영역" 또는 "FR"은 종 내에서 상대적으로 보존된다. 구성요소 경쇄 및 중쇄의 조합된 프레임워크 영역인 항체의 프레임워크 영역은 3차원 공간에서 CDR을 위치시키고 정렬시키는 역할을 한다. 프레임워크 서열은 생식세포계열 항체 유전자 서열을 포함하는 공공 DNA 데이터베이스 또는 공개된 참조문헌으로부터 얻을 수 있다. 예를 들어, 인간 중쇄 및 경쇄 가변 영역 유전자에 대한 생식세포계열 DNA 서열은 인간 및 마우스 서열에 대한 "VBASE2" 생식세포계열 가변 유전자 서열 데이터베이스에서 찾을 수 있다.
CDR 및 프레임워크 영역의 아미노산 서열은 당업계에 잘 알려진 다양한 정의, 예를 들어, Kabat, Chothia, 국제 ImMunoGeneTics 데이터베이스(IMGT), AbM 및 관찰된 항원 접촉("Contact")을 사용하여 정의될 수 있다. 일부 실시형태에서, CDR은 Contact 정의에 따라 결정된다. 문헌[MacCallum et al., J. Mol. Biol. 262:732-745, 1996] 참조. 일부 실시형태에서, CDR은 Kabat, Chothia 및/또는 Contact CDR 정의의 조합에 의해 결정된다.
용어 "Fd 부분"은 면역글로불린 중쇄의 N-말단 부분을 지칭한다. 전형적으로, Fd 부분은 중쇄 가변(VH) 영역 및 중쇄 불변(CH1) 영역을 포함한다.
용어 "Fab"는 경쇄 가변 영역, 경쇄 불변 영역, 중쇄 가변 영역 및 중쇄 CH1 불변 영역으로 구성되는 항원-결합 단편을 지칭한다.
용어 "단일쇄 가변 단편" 또는 "scFv"는 펩타이드 링커를 통해 함께 연결되는 중쇄 가변 영역과 경쇄 가변 영역으로 구성되는 항원-결합 단편을 지칭한다. scFv는 불변 영역이 결여되어 있다.
용어 "Fv 단편"은 항원에 대한 결합 부위를 함께 형성하는 중쇄 가변 영역과 경쇄 가변 영역으로 구성되는 항원-결합 단편을 지칭한다.
용어 "에피토프"는 분자, 예를 들어, 항체의 CDR이 특이적으로 결합하는 항원의 구역 또는 영역을 지칭하며, 소수의 아미노산 또는 소수의 아미노산의 일부, 예를 들어, 5개 또는 6개 이상, 예를 들어, 20개 이상의 아미노산 또는 아미노산의 일부를 포함할 수 있다. 일부 경우에, 에피토프는 비단백질 성분, 예를 들어, 탄수화물, 핵산 또는 지질로부터의 성분을 포함한다. 일부 경우에, 에피토프는 3차원 모이어티이다. 따라서, 예를 들어, 표적이 단백질인 경우, 에피토프는 연속적인 아미노산(예를 들어, 선형 에피토프) 또는 단백질 폴딩에 의해 근접하게 되는 단백질의 상이한 부분으로부터의 아미노산(예를 들어, 불연속 또는 구조적 에피토프)으로 구성될 수 있다.
본 명세서에서 사용되는 바와 같이, 항체와 관련하여 사용되는 어구 "에피토프를 인식하다"는 항체 CDR이 해당 에피토프 또는 해당 에피토프를 포함하는 항원의 일부에서 항원과 상호작용하거나 또는 이에 특이적으로 결합하는 것을 의미한다.
"인간화된 항체"는 CDR 외부의 비인간 면역글로불린으로부터 유래되는 최소 서열을 포함하는 비인간 공급원(예를 들어, 뮤린)으로부터 유래되는 키메라 면역글로불린이다. 일반적으로, 인간화된 항체는 적어도 하나의(예를 들어, 2개) 가변 도메인(들)을 포함할 것이며, 여기서 CDR 영역은 실질적으로 비인간 면역글로불린의 것에 해당하고, 프레임워크 영역은 실질적으로 인간 면역글로불린 서열의 것에 해당한다. 일부 예에서, 인간 면역글로불린의 소정의 프레임워크 영역 잔기는, 예를 들어, 특이성, 친화성 및/또는 혈청 반감기를 개선하기 위해 비인간 종으로부터의 상응하는 잔기로 대체될 수 있다. 인간화된 항체는 또한 면역글로불린 불변 영역(Fc)의 적어도 일부, 전형적으로 인간 면역글로불린 서열의 것을 포함할 수 있다. 항체 인간화 방법은 당업계에 공지되어 있다.
"인간 항체" 또는 "완전 인간 항체"는 전형적으로 인간 생식세포계열 유전자로부터 유래되는 인간 중쇄 및 경쇄 서열을 갖는 항체이다. 일부 실시형태에서, 항체는 인간 세포, 인간 항체 레퍼토리(예를 들어, 인간 항체 서열을 발현하도록 유전자 조작된 트랜스제닉 마우스)를 이용하는 비인간 동물 또는 파지 디스플레이 플랫폼에 의해 생성된다.
용어 "특이적으로 결합한다"는 또 다른 에피토프 또는 비-표적 화합물(예를 들어, 구조적으로 상이한 항원)에 결합하는 것보다 샘플에서 해당 에피토프 또는 표적에 대해 더 큰 친화성, 더 큰 결합력 및/또는 더 긴 지속 시간으로 에피토프 또는 표적에 결합하는 분자(예를 들어, Fab, scFv 또는 변형된 Fc 폴리펩타이드(또는 이의 표적-결합 부분))를 지칭한다. 일부 실시형태에서, 에피토프 또는 표적에 특이적으로 결합하는 Fab, scFv 또는 변형된 Fc 폴리펩타이드(또는 이의 표적-결합 부분)는 다른 에피토프 또는 비-표적 화합물보다 적어도 5-배 더 큰 친화성, 예를 들어, 적어도 6-배, 7-배, 8-배, 9-배, 10-배, 25-배, 50-배, 100-배, 1000-배, 10,000-배 또는 더 큰 친화성으로 에피토프 또는 표적에 결합하는 Fab, scFv 또는 변형된 Fc 폴리펩타이드(또는 이의 표적-결합 부분)이다. 본 명세서에서 사용되는 용어 특정 에피토프 또는 표적에 "특이적인 결합", "특이적으로 결합한다" 또는 "특이적인"은, 예를 들어, 10-4 M 이하, 예를 들어, 10-5 M, 10-6 M, 10-7 M, 10-8 M, 10-9 M, 10-10 M, 10-11 M 또는 10-12 M로 결합하는, 예를 들어, 에피토프 또는 표적에 대한 평형 해리 상수 KD를 갖는 분자에 의해 나타날 수 있다. 한 종으로부터의 표적에 특이적으로 결합하는 Fab 또는 scFv는 또한 해당 표적의 오쏘로그에 특이적으로 결합할 수 있다는 것이 당업자에 의해 인식될 것이다.
용어 "결합 친화도"는 두 분자 사이, 예를 들어, Fab 또는 scFv와 항원 사이 또는 변형된 Fc 폴리펩타이드(또는 이의 표적-결합 부분)와 표적 사이의 비-공유적 상호작용의 강도를 지칭하기 위해 본 명세서에서 사용된다. 따라서, 예를 들어, 용어는 문맥에서 달리 나타내거나 또는 명확하지 않는 한 Fab 또는 scFv와 항원 사이 또는 변형된 Fc 폴리펩타이드(또는 이의 표적-결합 부분)와 표적 사이의 1:1 상호작용을 지칭할 수 있다. 결합 친화도는 해리 속도 상수(kd, 시간-1)를 결합 속도 상수(ka, 시간-1 M-1)로 나눈 것을 지칭하는 평형 해리 상수(KD)를 측정함으로써 정량화될 수 있다. KD는, 예를 들어, 표면 플라스몬 공명(SPR) 방법, 예를 들어, Biacore™ 시스템; 동역학 배제 검정, 예컨대, KinExA®; 및 BioLayer 간섭계(예를 들어, ForteBio® 옥텟 플랫폼 사용)를 사용하여 복합체 형성 및 해리의 동역학의 측정에 의해 결정될 수 있다. 본 명세서에서 사용되는 바와 같이, "결합 친화도"는 Fab 또는 scFv와 항원 사이 또는 변형된 Fc 폴리펩타이드(또는 이의 표적-결합 부분)와 표적 사이의 1:1 상호작용을 반영하는 것과 같은 형식적인 결합 친화도뿐만 아니라 강력한 결합을 반영할 수 있는 KD의 값이 계산되는 겉보기 친화도를 포함한다.
본 명세서에서 사용되는 바와 같이, "트랜스페린 수용체" 또는 "TfR"은 트랜스페린 수용체 단백질 1을 지칭한다. 인간 트랜스페린 수용체 1 폴리펩타이드 서열은 서열번호 150에 제시되어 있다. 다른 종으로부터의 트랜스페린 수용체 단백질 1 서열도 또한 공지되어 있다(예를 들어, 침팬지, 등록 번호 XP_003310238.1; 레수스 원숭이, NP_001244232.1; 개, NP_001003111.1; 소, NP_001193506.1; 마우스, NP_035768.1; 래트, NP_073203.1; 및 닭, NP_990587.1). 용어 "트랜스페린 수용체"는 또한 트랜스페린 수용체 단백질 1 염색체 유전자좌의 유전자에 의해 암호화되는 예시적인 참조 서열, 예를 들어, 인간 서열의 대립유전자 변이체를 포함한다. 전장 트랜스페린 수용체 단백질은 짧은 N-말단 세포내 영역, 막관통 영역 및 큰 세포외 도메인을 포함한다. 세포외 도메인은 3개의 도메인: 프로테이스-유사 도메인, 나선형 도메인 및 첨단(apical) 도메인을 특징으로 한다.
본 명세서에서 사용되는 용어 "Fc 폴리펩타이드"는 구조 도메인으로서 Ig 접힘을 특징으로 하는 자연 발생적 면역글로불린 중쇄 폴리펩타이드의 C-말단 영역을 지칭한다. Fc 폴리펩타이드는 적어도 CH2 도메인 및/또는 CH3 도메인을 포함하는 불변 영역 서열을 포함하고, 힌지 영역의 적어도 일부를 포함할 수 있지만, 가변 영역은 포함하지 않는다.
"변형된 Fc 폴리펩타이드"는 야생형 면역글로불린 중쇄 Fc 폴리펩타이드 서열과 비교하여 적어도 하나의 돌연변이, 예를 들어, 치환, 결실 또는 삽입을 가질 수 있지만, 고유의 Fc 폴리펩타이드의 전체 Ig 접힘 또는 구조를 보유하는 Fc 폴리펩타이드를 지칭한다.
본 명세서에서 사용되는 바와 같이, "FcRn"은 신생 Fc 수용체를 지칭한다. FcRn에 대한 Fc 폴리펩타이드의 결합은 청소율(clearance)을 감소시키고, Fc 폴리펩타이드의 혈청 반감기를 증가시킨다. 인간 FcRn 단백질은 주요 조직적합성(MHC) 클래스 I 단백질과 유사한 약 50kDa 크기의 단백질 및 약 15kDa 크기의 β2-마이크로글로불린으로 구성되는 이종이량체이다.
본 명세서에서 사용되는 바와 같이, "FcRn 결합 부위"는 FcRn에 결합하는 Fc 폴리펩타이드의 영역을 지칭한다. 인간 IgG에서, EU 인덱스를 사용하여 넘버링된 FcRn 결합 부위는 L251, M252, I253, S254, R255, T256, M428, H433, N434, H435 및 Y436을 포함한다. 이들 위치는 서열번호 130의 21번 내지 26번, 198번 및 203번 내지 206번 위치에 해당한다.
본 명세서에서 사용되는 바와 같이, "고유 FcRn 결합 부위"는 FcRn에 결합하며 FcRn에 결합하는 자연 발생적 Fc 폴리펩타이드의 영역과 동일한 아미노산 서열을 갖는 Fc 폴리펩타이드의 영역을 지칭한다.
본 명세서에서 사용되는 용어 "CH3 도메인" 및 "CH2 도메인"은 면역글로불린 불변 영역 도메인 폴리펩타이드를 지칭한다. 본 출원의 목적을 위해, CH3 도메인 폴리펩타이드는 EU 넘버링 체계에 따라 넘버링 시 약 341번 위치 내지 약 447번 위치의 아미노산의 분절을 지칭하고, CH2 도메인 폴리펩타이드는 EU 넘버링 체계에 따라 넘버링 시 약 231번 위치 내지 약 340번 위치의 아미노산의 분절을 지칭하며, 힌지 영역 서열은 포함하지 않는다. CH2 및 CH3 도메인 폴리펩타이드는 또한 IMGT(ImMunoGeneTics) 넘버링 체계에 의해 넘버링 될 수 있으며, 여기서 IMGT 사이언티픽 차트 넘버링(IMGT 웹사이트)에 따라 CH2 도메인 넘버링은 1번 내지 110번이고, CH3 도메인 넘버링은 1번 내지 107번이다. CH2 및 CH3 도메인은 면역글로불린의 Fc 영역의 일부이다. Fc 영역은 EU 넘버링 체계에 따라 넘버링 시 약 231번 위치 내지 약 447번 위치의 아미노산의 분절을 지칭하지만, 본 명세서에서 사용되는 바와 같이, 항체의 힌지 영역의 적어도 일부를 포함할 수 있다. 예시적인 힌지 영역 서열은 인간 IgG1 힌지 서열 EPKSCDKTHTCPPCP(서열번호 127)이다.
CH3 또는 CH2 도메인과 관련하여 사용되는 용어 "야생형", "고유" 및 "자연 발생적"은 자연에서 발생하는 서열을 갖는 도메인을 지칭한다.
돌연변이체 폴리펩타이드 또는 돌연변이체 폴리뉴클레오타이드와 관련하여 사용되는 본 명세서에서 사용되는 용어 "돌연변이체"는 "변이체"와 상호교환적으로 사용된다. 주어진 야생형 CH3 또는 CH2 도메인 참조 서열에 대하여 변이체는 자연 발생적 대립유전자 변이체를 포함할 수 있다. "비자연적으로" 발생하는 CH3 또는 CH2 도메인은 자연의 세포에 존재하지 않고 고유 CH3 도메인 또는 CH2 도메인 폴리뉴클레오타이드 또는 폴리펩타이드의 유전자 변형에 의해, 예를 들어, 유전 공학 기술 또는 돌연변이유발 기법을 사용하여 생성되는 변이체 또는 돌연변이체 도메인을 지칭한다. "변이체"는 야생형에 대하여 적어도 하나의 아미노산 돌연변이를 포함하는 임의의 도메인을 포함한다. 돌연변이는 치환, 삽입 및 결실을 포함할 수 있다.
핵산 또는 단백질과 관련하여 사용되는 용어 "단리된"은 핵산 또는 단백질이 천연 상태에서 회합되는 다른 세포 성분이 본질적으로 없음을 나타낸다. 이는 균질한 상태인 것이 바람직하다. 순도 및 균질성은 전형적으로 전기영동(예를 들어, 폴리아크릴아마이드 겔 전기영동) 또는 크로마토그래피(예를 들어, 고성능 액체 크로마토그래피)와 같은 분석 화학 기법을 사용하여 결정된다. 일부 실시형태에서, 단리된 핵산 또는 단백질은 적어도 85% 순수, 적어도 90% 순수, 적어도 95% 순수 또는 적어도 99% 순수하다.
용어 "아미노산"은 자연 발생적 및 합성 아미노산뿐만 아니라 자연 발생적 아미노산과 유사한 방식으로 기능하는 아미노산 유사체 및 아미노산 모방체를 지칭한다. 자연적으로 발생하는 것은 유전 코드에 의해 암호화된 아미노산뿐만 아니라 나중에 변형된 아미노산, 예를 들어, 하이드록시프롤린, γ-카복시글루타메이트 및 O-포스포세린이다. 자연 발생적 α-아미노산은 제한 없이 알라닌(Ala), 시스테인(Cys), 아스파르트산(Asp), 글루탐산(Glu), 페닐알라닌(Phe), 글리신(Gly), 히스티딘(His), 아이소류신(Ile), 아르기닌(Arg), 라이신(Lys), 류신(Leu), 메티오닌(Met), 아스파라긴(Asn), 프롤린(Pro), 글루타민(Gln), 세린(Ser), 트레오닌(Thr), 발린(Val), 트립토판(Trp), 타이로신(Tyr) 및 이들의 조합을 포함한다. 자연 발생적 α-아미노산의 입체이성질체는 제한 없이 D-알라닌(D-Ala), D-시스테인(D-Cys), D-아스파르트산(D-Asp), D-글루탐산(D-Glu), D-페닐알라닌(D-Phe), D-히스티딘(D-His), D-아이소류신(D-Ile), D-아르기닌(D-Arg), D-라이신(D-Lys), D-류신(D-Leu), D-메티오닌(D-Met), D-아스파라긴(D-Asn), D-프롤린(D-Pro), D-글루타민(D-Gln), D-세린(D-Ser), D-트레오닌(D-Thr), D-발린(D-Val), D-트립토판(D-Trp), D-타이로신(D-Tyr) 및 이들의 조합을 포함한다. "아미노산 유사체"는 자연 발생적 아미노산과 동일한 기본 화학 구조, 즉, 수소, 카복실기, 아미노기 및 R기에 결합된 α 탄소, 예를 들어, 호모세린, 노르류신, 메티오닌 설폭사이드, 메티오닌 메틸 설포늄을 갖는 화합물을 지칭한다. 이러한 유사체는 변형된 R기(예를 들어, 노르류신) 또는 변형된 펩타이드 골격을 갖지만, 자연 발생적 아미노산과 동일한 기본 화학 구조를 유지한다. "아미노산 모방체"는 아미노산의 일반 화학 구조와 상이한 구조를 갖지만, 자연 발생적 아미노산과 유사한 방식으로 기능하는 화합물을 지칭한다. 아미노산은 본 명세서에서 일반적으로 알려진 세 글자 기호 또는 IUPAC-IUB 생화학 명명 위원회(IUPAC-IUB Biochemical Nomenclature Commission)에 의해 권장되는 한 글자 기호로 지칭될 수 있다.
용어 "폴리펩타이드" 및 "펩타이드"는 본 명세서에서 단일 사슬의 아미노산 잔기의 중합체를 지칭하기 위해 상호교환적으로 사용된다. 용어는 하나 이상의 아미노산 잔기가 상응하는 자연 발생적 아미노산의 인공 화학 모방체인 아미노산 중합체뿐만 아니라 자연 발생적 아미노산 중합체 및 비자연 발생적 아미노산 중합체에도 적용된다. 아미노산 중합체는 전체 L-아미노산, 전체 D-아미노산 또는 L 아미노산과 D 아미노산의 혼합물을 포함할 수 있다.
본 명세서에서 사용되는 용어 "단백질"은 폴리펩타이드 또는 단일 사슬 폴리펩타이드의 이량체(즉, 2개) 또는 다량체(즉, 3개 이상)를 지칭한다. 단백질의 단일 사슬 폴리펩타이드는 공유 결합, 예를 들어, 이황화 결합 또는 비-공유적 상호작용에 의해 연결될 수 있다.
본 명세서에서 사용되는 용어 "링커"는 펩타이드 또는 폴리펩타이드를 연결 또는 융합시키기 위해 2개의 펩타이드 또는 폴리펩타이드(예를 들어, Fc 폴리펩타이드와 scFv 사이)를 연결(예를 들어, 공유적으로 연결)하는 모이어티를 지칭한다. 일부 실시형태에서, 링커는 화학적 연결을 포함한다. 일부 실시형태에서, 링커는 하나 이상의 아미노산 잔기의 길이를 갖는 펩타이드를 포함한다. 펩타이드 또는 폴리펩타이드를 연결 또는 융합시키기 위한 적합한 링커는 길이, 소수성, 유연성, 강성 또는 링커의 절단성과 같은 링커의 특성에 기초하여 선택될 수 있다.
용어 "폴리뉴클레오타이드" 및 "핵산"은 상호교환적으로 임의의 길이의 뉴클레오타이드의 사슬을 지칭하며, DNA 및 RNA를 포함한다. 뉴클레오타이드는 데옥시리보뉴클레오타이드, 리보뉴클레오타이드, 변형된 뉴클레오타이드 또는 염기 및/또는 이들의 유사체 또는, DNA 또는 RNA 폴리머레이스에 의해 사슬에 혼입될 수 있는 임의의 기질일 수 있다. 폴리뉴클레오타이드는 메틸화된 뉴클레오타이드 및 이의 유사체와 같은 변형된 뉴클레오타이드를 포함할 수 있다. 본 명세서에서 상정되는 폴리뉴클레오타이드의 예는 단일-가닥 및 이중-가닥 DNA, 단일-가닥 및 이중-가닥 RNA 및 단일-가닥과 이중-가닥 DNA 및 RNA의 혼합물을 갖는 하이브리드 분자를 포함한다.
용어 "보존적 치환" 및 "보존적 돌연변이"는 유사한 특징을 갖는 것으로 분류될 수 있는 또 다른 아미노산으로의 아미노산의 치환을 초래하는 변경을 지칭한다. 이러한 방식으로 정의된 보존적 아미노산 그룹의 범주의 예는 다음을 포함할 수 있다: Glu(글루탐산 또는 E), Asp(아스파르트산 또는 D), Asn(아스파라긴 또는 N), Gln(글루타민 또는 Q), Lys(라이신 또는 K), Arg(아르기닌 또는 R) 및 His(히스티딘 또는 H)를 포함하는 "하전/극성 그룹"; Phe(페닐알라닌 또는 F), Tyr(타이로신 또는 Y), Trp(트립토판 또는 W) 및 (히스티딘 또는 H)를 포함하는 "방향족 그룹"; 및 Gly(글리신 또는 G), Ala(알라닌 또는 A), Val(발린 또는 V), Leu(류신 또는 L), Ile(아이소류신 또는 I), Met(메티오닌 또는 M), Ser(세린 또는 S), Thr(트레오닌 또는 T) 및 Cys(시스테인 또는 C)를 포함하는 "지방족 그룹". 각 그룹 내에서, 하위 그룹도 또한 확인될 수 있다. 예를 들어, 하전 또는 극성 아미노산의 그룹은 다음을 포함하는 하위 그룹으로 세분화될 수 있다: Lys, Arg 및 His를 포함하는 "양으로 하전된 하위 그룹"; Glu 및 Asp를 포함하는 "음으로 하전된 하위 그룹"; 및 Asn 및 Gln을 포함하는 "극성 하위 그룹". 또 다른 예에서, 방향족 또는 고리형 그룹은 다음을 포함하는 하위 그룹으로 세분화될 수 있다: Pro, His 및 Trp를 포함하는 "질소 고리 하위 그룹"; 및 Phe 및 Tyr을 포함하는 "페닐 하위 그룹". 또 다른 추가의 예에서, 지방족 그룹은 하위 그룹, 예를 들어, Val, Leu, Gly 및 Ala를 포함하는 "지방족 비극성 하위 그룹"; 및 Met, Ser, Thr 및 Cys를 포함하는 "지방족 약간 극성인 하위 그룹"으로 세분화될 수 있다. 보존적 돌연변이의 범주의 예는 다음과 같지만 이들로 제한되지 않는 위의 하위 그룹 내 아미노산의 아미노산 치환을 포함한다: 양전하가 유지될 수 있도록 Arg에 대해 Lys로 또는 그 반대로; 음전하가 유지될 수 있도록 Asp에 대해 Glu로 또는 그 반대로; 유리-OH가 유지될 수 있도록 Thr에 대해 Ser로 또는 그 반대로; 및 유리-NH2가 유지될 수 있도록 Asn에 대해 Gln으로 또는 그 반대로. 일부 실시형태에서, 소수성 아미노산은 소수성을 보존하기 위해, 예를 들어, 활성 부위에서 자연 발생적 소수성 아미노산으로 대체된다.
2개 이상의 폴리펩타이드 서열의 맥락에서, 용어 "동일한" 또는 "동일성" 백분율은 서열 비교 알고리즘을 사용하거나 또는 수동 정렬 및 육안 검사에 의해 측정된 비교 창 또는 지정된 영역에 걸쳐 최대 일치성을 위해 비교되고 정렬될 때 명시된 영역에 걸쳐 동일한, 동일하거나 또는 특정 백분율, 예를 들어, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90% 또는 적어도 95% 이상의 아미노산 잔기를 갖는 2개 이상의 서열 또는 하위서열을 지칭한다.
폴리펩타이드의 서열 비교를 위해, 전형적으로 하나의 아미노산 서열은 후보 서열이 비교되는 참조 서열로 작용한다. 정렬은 당업자가 이용할 수 있는 다양한 방법, 예를 들어, 시각적 정렬을 사용하거나 또는 공지된 알고리즘을 사용하여 최대 정렬을 달성하는 공개적으로 이용 가능한 소프트웨어를 사용하여 수행될 수 있다. 이러한 프로그램은 BLAST 프로그램, ALIGN, ALIGN-2(제넨테크(Genentech), 캘리포니아주 사우스 샌프란시스코 소재) 또는 Megalign(DNASTAR)을 포함한다. 최대 정렬을 달성하기 위한 정렬에 사용되는 매개변수는 당업자에 의해 결정될 수 있다. 본 출원의 목적을 위한 폴리펩타이드 서열의 서열 비교를 위해, 2개의 단백질 서열을 디폴트 매개변수와 정렬하기 위한 BLASTP 알고리즘 표준 단백질 BLAST가 사용된다.
폴리펩타이드 서열에서 주어진 아미노산 잔기의 확인의 맥락에서 사용될 때 용어 "~에 상응하는", "참조로 결정된" 또는 "참조로 넘버링된"은 주어진 아미노산 서열이 최대로 정렬되고 참조 서열과 비교될 때 명시된 참조 서열의 잔기의 위치를 지칭한다. 따라서, 예를 들어, 변형된 Fc 폴리펩타이드의 아미노산 잔기는 서열번호 130에 최적으로 정렬되는 경우 잔기가 서열번호 130의 아미노산과 정렬될 때 서열번호 130의 아미노산에 "상응한다". 참조 서열에 정렬된 폴리펩타이드는 참조 서열과 동일한 길이일 필요는 없다.
본 명세서에서 상호교환적으로 사용되는 용어 "대상체", "개체" 및 "환자"는 인간, 비인간 영장류, 설치류(예를 들어, 래트, 마우스 및 기니피그), 토끼, 소, 돼지, 말 및 다른 포유동물 종을 포함하지만 이들로 제한되지 않는 포유동물을 지칭한다. 일 실시형태에서, 환자는 인간이다.
용어 "치료", "치료하는" 등은 본 명세서에서 일반적으로 목적하는 약리학적 및/또는 생리학적 효과를 얻는 것을 의미하기 위해 사용된다. "치료하는" 또는 "치료"는 경감, 관해, 환자 생존의 개선, 생존 시간 또는 생존률의 증가, 증상의 감소 또는 환자가 질환을 더 견딜 수 있게 하는 것, 퇴행 또는 쇠퇴의 속도를 늦추는 것 또는 환자의 신체적 또는 정신적 웰빙을 개선하는 것과 같은 임의의 객관적 또는 주관적 매개변수를 포함하여 신경퇴행성 질환(예를 들어, 알츠하이머병 또는 본 명세서에 기재된 또 다른 신경퇴행성 질환)의 치료 또는 개선의 임의의 성공 지표를 지칭할 수 있다. 증상의 치료 또는 개선은 객관적 또는 주관적인 매개변수를 기반으로 할 수 있다. 치료의 효과는 치료를 받지 않은 개체 또는 개체의 풀, 또는 치료 전 또는 치료 중 상이한 시간에 동일한 환자와 비교될 수 있다.
용어 "약제학적으로 허용 가능한 부형제"는 완충액, 담체 또는 보존제와 같지만 이들로 제한되지 않는 인간 또는 동물에서 사용하기 위해 생물학적으로 또는 약리학적으로 양립 가능한 비활성 약제학적 성분을 지칭한다.
본 명세서에서 사용되는 바와 같이, 작용제의 "치료학적 양" 또는 "치료학적 유효량"은 대상체에서 질환을 치료하는 작용제(예를 들어, 본 명세서에 기재된 임의의 단백질)의 양이다.
용어 "투여하다"는 작용제, 화합물 또는 조성물을 목적하는 생물학적 작용 부위에 전달하는 방법을 지칭한다. 이러한 방법은 국소 전달, 비경구 전달, 정맥내 전달, 피내 전달, 근육내 전달, 경막내 전달, 결장 전달, 직장 전달 또는 복강내 전달을 포함하지만 이들로 제한되지 않는다. 일 실시형태에서, 본 명세서에 기재된 바와 같은 단백질은 정맥내로 투여된다.
III. 항-HER2 이중특이성 단백질
일 양태에서, 인간 HER2의 서브도메인 II과 인간 HER2의 서브도메인 IV 모두에 특이적으로 결합하는 능력이 있는 이중특이성 단백질이 제공된다. 일부 실시형태에서, 이중특이성 단백질의 Fc 폴리펩타이드 중 하나 또는 둘 모두는 변형된 Fc 폴리펩타이드이다(예를 들어, TfR 결합을 촉진하고/하거나 Fc 폴리펩타이드의 이종이량체화를 향상시키도록 변형됨).
Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드
일부 실시형태에서, 이중특이성 단백질은 Fab 및 scFv의 일부에 융합된 Fc 폴리펩타이드를 포함한다. 이러한 이중특이성 단백질의 개략도는 도 1a 및 도 1b에 도시되어 있다. 일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 단일쇄 가변 단편(scFv)에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 경쇄 폴리펩타이드
를 포함하되,
Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다. 일부 실시형태에서, 단백질의 Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합한다. 다른 실시형태에서, 단백질의 Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다.
Fab는 제1 Fc 폴리펩타이드의 N-말단에 융합된 Fab의 Fd 부분과 경쇄의 페어링으로부터 형성된다. 일부 실시형태에서, 인간 HER2의 서브도메인 II에 특이적으로 결합하는 Fab는 서열번호 108의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다. 일부 실시형태에서, 인간 HER2의 서브도메인 IV에 특이적으로 결합하는 Fab는 서열번호 109의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다.
일부 실시형태에서, 이중특이성 단백질의 제2 Fc 폴리펩타이드는 N-말단에서 scFv 단편에 융합된다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 N-말단에서 제1 링커를 통해 scFv 단편에 융합된다. 일부 실시형태에서, 제1 링커는 약 1개 내지 약 50개의 아미노산, 예를 들어, 약 1개 내지 약 40개, 약 1개 내지 약 30개, 약 1개 내지 약 25개, 약 1개 내지 약 20개, 약 1개 내지 약 15개, 약 1개 내지 약 10개, 약 2개 내지 약 40개, 약 2개 내지 약 30개, 약 2개 내지 약 20개, 약 2개 내지 약 10개, 약 5개 내지 약 40개, 약 5개 내지 약 30개, 약 5개 내지 약 25개 또는 약 5개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제1 링커는 약 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 30개, 35개, 40개, 45개 또는 50개의 아미노산 길이를 갖는다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제1 링커는 GGGGSGGGGS(서열번호 118)의 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질의 scFv는 제2 링커를 통해 연결된 VH 영역 및 VL 영역을 포함한다. 일부 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VL 영역-VH 영역-(C-말단)이며, 여기서 scFv의 C-말단은 제1 링커를 통해 Fc 폴리펩타이드의 N-말단에 연결된다. 다른 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VH 영역-VL 영역-(C-말단)이며, 여기서 scFv의 C-말단은 제1 링커를 통해 Fc 폴리펩타이드의 N-말단에 연결된다.
일부 실시형태에서, scFv의 VL 영역 및 VH 영역은 제2 링커를 통해 연결된다. 일부 실시형태에서, 제2 링커는 약 10개 내지 약 25개의 아미노산, 예를 들어, 약 10개 내지 약 20개, 약 12개 내지 약 25개, 약 12개 내지 약 20개, 약 14개 내지 약 25개 또는 약 14개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제2 링커는 약 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개 또는 25개의 아미노산의 길이를 갖는다. 일부 실시형태에서, 제2 링커는 가요성 링커를 포함한다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제2 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함한다.
일부 실시형태에서, scFv의 VL 영역 및 VH 영역은 모두 Cys 치환을 포함한다. 일부 실시형태에서, VL 영역 및 VH 영역에서의 Cys 치환은 이황화 결합을 형성하고 scFv의 구조를 안정화시키는 데 도움이 될 수 있다. 일부 실시형태에서, scFv는 Kabat 가변 도메인 넘버링에 따른 위치 VH44 및 VL100 각각에 시스테인을 포함한다. 일부 실시형태에서, scFv는 위치 VH44 및 VL100에서 시스테인 사이에 이황화 결합을 포함한다.
예를 들어, 항-HER2DII VL 영역은 서열번호 110의 100번 위치에 Gln에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DII VL 영역은 서열번호 114의 서열을 가질 수 있다. 일부 실시형태에서, 항-HER2DIV VL 영역은 서열번호 111의 100번 위치에 Gln에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DIV VL 영역은 서열번호 115의 서열을 가질 수 있다.
예를 들어, 항-HER2DII VH 영역은 서열번호 108의 44번 위치에 Gly에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DII VH 영역은 서열번호 112의 서열을 가질 수 있다. 일부 실시형태에서, 항-HER2DIV VH 영역은 서열번호 109의 44번 위치에 Gly에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DIV VH 영역은 서열번호 113의 서열을 가질 수 있다.
일부 실시형태에서, "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 이중특이성 단백질의 (a) 부분에서, 제1 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 일부 실시형태에서, "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 이중특이성 단백질의 (b) 부분에서, 제2 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 scFv에 융합된다. 예시적인 힌지 영역 서열은 인간 IgG1 힌지 서열 EPKSCDKTHTCPPCP(서열번호 127)이다. 부분적인 힌지 영역은 서열번호 127의 서열의 일부, 예를 들어, DKTHTCPPCP(서열번호 128)의 서열을 갖는 부분적인 힌지 영역을 지칭한다.
추가의 실시형태에서, "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 이중특이성 단백질의 (b) 부분에서, 힌지 영역(예를 들어, 서열번호 127) 또는 부분적인 힌지 영역(예를 들어, 서열번호 128)은 제2 Fc 폴리펩타이드의 N-말단에 융합된다. 소정의 실시형태에서, 힌지 영역이 제2 Fc 폴리펩타이드의 N-말단에 융합되는 경우, 힌지 영역은 서열번호 127의 서열과 관련하여 5번 위치에 Cys에서 Ser로의 돌연변이를 포함할 수 있다. 예를 들어, Cys에서 Ser로의 돌연변이를 갖는 힌지 영역은 EPKSSDKTHTCPPCP(서열번호 129)의 서열을 가질 수 있다.
"Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 이중특이성 단백질에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 Fc 폴리펩타이드)에 특이적으로 결합할 수 있다. 상이한 Fc 폴리펩타이드 및 이의 변형은 본 명세서에서 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함할 수 있다. 예를 들어, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있다. 또 다른 예에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있다. 또한, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함할 수 있다. 예를 들어, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다. "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 이중특이성 단백질의 특정 실시형태에서, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366W 치환과 L234A 및 L235A 치환을 포함하는 TfR-결합 Fc 폴리펩타이드이고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366S, L368A 및 Y407V 치환을 포함한다. 예를 들어, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있다.
소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함하고, 제2 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않는다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않고, 제2 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함한다.
예시적인 이중특이성 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 단백질
일부 실시형태에서, 이중특이성 단백질은 다음을 포함한다:
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 단일쇄 가변 단편(scFv)에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 경쇄 폴리펩타이드.
일례에서, (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 21 또는 22의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 20의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 19의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 18의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
또 다른 예에서, (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 23의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (b) 서열번호 24의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 이러한 두 예에서, scFv 부분은 Gln에서 Cys로의 치환을 갖는 항-HER2DIV VL 영역(서열번호 115) 및 Gly에서 Cys로의 치환을 갖는 항-HER2DIV VH 영역(서열번호 113)을 포함한다는 것에 유의한다. 또한, 두 작제물에서, (b)의 힌지 영역은 5번 위치에 Cys에서 Ser로의 돌연변이를 갖는다(EPKSSDKTHTCPPCP(서열번호 129)).
일부 실시형태에서, 이중특이성 단백질은 다음을 포함한다:
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 단일쇄 가변 단편(scFv)에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 경쇄 폴리펩타이드.
일례에서, (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 15, 16 또는 17의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 14의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 13의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 11 또는 12의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 이의 C-말단 라이신(예를 들어, EU 넘버링에 따라 Fc 폴리펩타이드의 447번 위치의 Lys 잔기)이 제거될 수 있다. 일부 실시형태에서, Fc 폴리펩타이드에서 C-말단 라이신의 제거는 이중특이성 단백질의 안전성을 개선할 수 있다.
HC 상의 mAb/N-말단 또는 C-말단 scFv
일부 실시형태에서, 이중특이성 단백질은 각각 N-말단에서 인간 HER2의 서브도메인 II 또는 IV에 특이적으로 결합하는 Fab에 융합된 Fc 폴리펩타이드를 포함하고, Fc 폴리펩타이드 중 하나 또는 둘 모두는 C-말단에서 인간 HER2의 서브도메인 II 또는 IV에 특이적으로 결합하는 scFv에 융합된다. 일부 실시형태에서, 이중특이성 단백질은 각각 N-말단에서 인간 HER2의 서브도메인 II 또는 IV에 특이적으로 결합하는 Fab에 융합된 Fc 폴리펩타이드를 포함하고, Fab 중 하나 또는 둘 모두는 N-말단에서 인간 HER2의 서브도메인 II 또는 IV에 특이적으로 결합하는 scFv에 융합된다. 이러한 이중특이성 단백질의 개략도는 도 2a 내지 도 2d에 도시되어 있다. 일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되거나, 또는
(a) 및/또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되거나, 또는
제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되고, 그리고
Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다. 일부 실시형태에서, Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합한다. 다른 실시형태에서, Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다.
일부 실시형태에서, 인간 HER2의 서브도메인 II에 특이적으로 결합하는 Fab는 서열번호 108의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다. 일부 실시형태에서, 인간 HER2의 서브도메인 IV에 특이적으로 결합하는 Fab는 서열번호 109의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다.
소정의 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합된다. 특정 실시형태에서, 제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합된다. 특정 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드 각각은 C-말단에서 scFv에 융합된다. 소정의 실시형태에서, (a) 및/또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합된다. 특정 실시형태에서, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합된다. 특정 실시형태에서, (a) 및 (b)의 Fd 부분 각각은 N-말단에서 scFv에 융합된다. 추가의 실시형태에서, 제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합된다.
일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드가 각각 C-말단에서 scFv에 융합되는 경우, 2개의 scFv는 동일한 서열을 포함할 수 있다. 일부 실시형태에서, (a)의 Fd 부분 및 (b)의 Fd 부분이 각각 N-말단에서 scFv에 융합되는 경우, 2개의 scFv는 동일한 서열을 포함할 수 있다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드가 C-말단에서 scFv에 융합되는 경우, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되고, 2개의 scFv는 동일한 서열을 포함할 수 있다.
일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 제1 링커를 통해 C-말단에서 scFv에 융합된다. 다른 실시형태에서, (a)의 Fd 부분 및/또는 (b)의 Fd 부분은제1 링커를 통해 N-말단에서 scFv에 융합된다. 일부 실시형태에서, 제1 링커는 약 1개 내지 약 50개의 아미노산, 예를 들어, 약 1개 내지 약 40개, 약 1개 내지 약 30개, 약 1개 내지 약 25개, 약 1개 내지 약 20개, 약 1개 내지 약 15개, 약 1개 내지 약 10개, 약 2개 내지 약 40개, 약 2개 내지 약 30개, 약 2개 내지 약 20개, 약 2개 내지 약 10개, 약 5개 내지 약 40개, 약 5개 내지 약 30개, 약 5개 내지 약 25개 또는 약 5개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제1 링커는 약 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 30개, 35개, 40개, 45개 또는 50개의 아미노산 길이를 갖는다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 소정의 실시형태에서, 제1 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질의 scFv는 제2 링커를 통해 연결된 VH 영역 및 VL 영역을 포함한다. 일부 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VL 영역-VH 영역-(C-말단)이며, 여기서 scFv의 C-말단은 제1 링커를 통해 (a) 또는 (b)의 Fd 부분의 N-말단에 연결된다. 다른 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VH 영역-VL 영역-(C-말단)이며, 여기서 scFv의 C-말단은 제1 링커를 통해 (a) 또는 (b)의 Fd 부분의 N-말단에 연결된다. 일부 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VL 영역-VH 영역-(C-말단)이며, 여기서 scFv의 N-말단은 제1 링커를 통해 제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드의 C-말단에 연결된다. 다른 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VH 영역-VL 영역-(C-말단)이며, 여기서 scFv의 N-말단은 제1 링커를 통해 제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드의 C-말단에 연결된다.
일부 실시형태에서, scFv에서 VL 및 VH 영역을 연결하는 제2 링커는 약 10개 내지 약 25개의 아미노산, 예를 들어, 약 10개 내지 약 20개, 약 12개 내지 약 25개, 약 12개 내지 약 20개, 약 14개 내지 약 25개 또는 약 14개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제2 링커는 약 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개 또는 25개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제2 링커는 가요성 링커를 포함한다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제2 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함한다.
일부 실시형태에서, scFv의 VL 영역 및 VH 영역은 모두 Cys 치환을 포함한다. 일부 실시형태에서, VL 영역 및 VH 영역에서의 Cys 치환은 이황화 결합을 형성하고, scFv의 구조를 안정화시키는 데 도움이 될 수 있다. 일부 실시형태에서, scFv는 Kabat 가변 도메인 넘버링에 따라 위치 VH44 및 VL100에 각각에 시스테인을 포함한다. 일부 실시형태에서, scFv는 위치 VH44 및 VL100에서 시스테인 사이에 이황화 결합을 포함한다.
예를 들어, 항-HER2DII VL 영역은 서열번호 110의 100번 위치에 Gln에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DII VL 영역은 서열번호 114의 서열을 가질 수 있다. 일부 실시형태에서, 항-HER2DIV VL 영역은 서열번호 111의 100번 위치에 Gln에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DIV VL 영역은 서열번호 115의 서열을 가질 수 있다.
예를 들어, 항-HER2DII VH 영역은 서열번호 108의 44번 위치에 Gly에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DII VH 영역은 서열번호 112의 서열을 가질 수 있다. 일부 실시형태에서, 항-HER2DIV VH 영역은 서열번호 109의 44번 위치에 Gly에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DIV VH 영역은 서열번호 113의 서열을 가질 수 있다.
일부 실시형태에서, "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질의 (a) 부분에서, 제1 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 일부 실시형태에서, "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질의 (b) 부분에서, 제2 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 예시적인 힌지 영역 서열은 인간 IgG1 힌지 서열 EPKSCDKTHTCPPCP(서열번호 127)이다. 부분적인 힌지 영역은 서열번호 127의 서열의 일부, 예를 들어, DKTHTCPPCP(서열번호 128)의 서열을 갖는 부분적인 힌지 영역을 지칭한다.
"HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 Fc 폴리펩타이드)에 특이적으로 결합할 수 있다. 상이한 Fc 폴리펩타이드 및 이의 변형이 본 명세서에 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함할 수 있다. 예를 들어, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있다. 또 다른 예에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있다. 또한, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함할 수 있다. 예를 들어, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다. "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질의 특정 실시형태에서, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366W 치환과 L234A 및 L235A 치환을 포함하는 TfR-결합 Fc 폴리펩타이드이고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366S, L368A 및 Y407V 치환을 포함한다. 예를 들어, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드) 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있다.
소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함하고, 제2 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않는다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않고, 제2 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함한다.
예시적인 이중특이성 "HC 상의 mAb/N-말단 또는 C-말단 scFv" 단백질
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 27 또는 28의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 29의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 30의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 31 또는 32의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 33 또는 34의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 35의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 36의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 37, 38 또는 39의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드 각각은 C-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 27 또는 28의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 31 또는 32의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 29의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 30의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드 각각은 C-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 33 또는 34의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 37, 38 또는 39의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 35의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 36의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
(a) 또는 (b)의 Fd 부분은 N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 40의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 41의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 42의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 43 또는 44의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
(a) 또는 (b)의 Fd 부분은 N-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 45 또는 46의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 47의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 48의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 49 또는 50의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 40의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 43 또는 44의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 41의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 42의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 45의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 49 또는 50의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 47의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 48의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합되고, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 40의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 31 또는 32의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 41의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 30의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 42의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 29의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 43 또는 44의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 27 또는 28의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되,
제1 Fc 폴리펩타이드 또는 제2 Fc 폴리펩타이드는 C-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합되고, (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합된다.
일례에서, (a) 서열번호 45의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 37, 38 또는 39의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 47의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 36의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 48의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 35의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 49 또는 50의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 33 또는 34의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 이의 C-말단 라이신(예를 들어, EU 넘버링에 따라 Fc 폴리펩타이드의 447번 위치의 Lys 잔기)이 제거될 수 있다. 일부 실시형태에서, Fc 폴리펩타이드에서 C-말단 라이신의 제거는 이중특이성 단백질의 안전성을 개선할 수 있다.
LC 상의 mAb/N-말단 또는 C-말단 scFv
일부 실시형태에서, 이중특이성 단백질은 N-말단 및/또는 C-말단에서 인간 HER2의 서브도메인 II 또는 IV에 특이적으로 결합하는 scFv에 융합된 경쇄를 포함한다. 이러한 이중특이성 단백질의 개략도는 도 3a 내지 도 3d에 도시되어 있다. 일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
경쇄 폴리펩타이드 중 하나 또는 둘 모두는 N-말단에서 scFv에 융합되거나, 또는
경쇄 폴리펩타이드 중 하나 또는 둘 모두는 C-말단에서 scFv에 융합되거나, 또는
제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 그리고
Fab는 인간 HER2의 서브도메인 II에 결합하고, scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, scFv는 인간 HER2의 서브도메인 II에 결합한다.
일부 실시형태에서, 인간 HER2의 서브도메인 II에 특이적으로 결합하는 Fab는 서열번호 108의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다. 일부 실시형태에서, 인간 HER2의 서브도메인 IV에 특이적으로 결합하는 Fab는 서열번호 109의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다.
소정의 실시형태에서, 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 N-말단에서 scFv에 융합된다. 특정 실시형태에서, 경쇄 폴리펩타이드 중 하나는 N-말단에서 scFv에 융합된다. 특정 실시형태에서, 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 scFv에 융합된다. 소정의 실시형태에서, 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 C-말단에서 scFv에 융합된다. 특정 실시형태에서, 경쇄 폴리펩타이드 중 하나는 C-말단에서 scFv에 융합된다. 특정 실시형태에서, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합된다. 추가의 실시형태에서, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합된다.
일부 실시형태에서, 두 경쇄 폴리펩타이드가 각각 C-말단에서 scFv에 융합되는 경우, 2개의 scFv는 동일한 서열을 포함할 수 있다. 일부 실시형태에서, 두 경쇄 폴리펩타이드가 각각 N-말단에서 scFv에 융합되는 경우, 2개의 scFv는 동일한 서열을 포함할 수 있다.
일부 실시형태에서, 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 제1 링커를 통해 scFv에 융합된다. 일부 실시형태에서, 제1 링커는 약 1개 내지 약 50개의 아미노산, 예를 들어, 약 1개 내지 약 40개, 약 1개 내지 약 30개, 약 1개 내지 약 25개, 약 1개 내지 약 20개, 약 1개 내지 약 15개, 약 1개 내지 약 10개, 약 2개 내지 약 40개, 약 2개 내지 약 30개, 약 2개 내지 약 20개, 약 2개 내지 약 10개, 약 5개 내지 약 40개, 약 5개 내지 약 30개, 약 5개 내지 약 25개 또는 약 5개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제1 링커는 약 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 30개, 35개, 40개, 45개 또는 50개의 아미노산 길이를 갖는다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 소정의 실시형태에서, 제1 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질의 scFv는 제2 링커를 통해 연결된 VH 영역 및 VL 영역을 포함한다. 일부 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VL 영역-VH 영역-(C-말단)이며, 여기서 scFv의 C-말단은 제1 링커를 통해 경쇄 폴리펩타이드의 N-말단에 연결된다. 다른 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VH 영역-VL 영역-(C-말단)이며, 여기서 scFv의 C-말단은 제1 링커를 통해 경쇄 폴리펩타이드의 N-말단에 연결된다. 일부 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VL 영역-VH 영역-(C-말단)이며, 여기서 scFv의 N-말단은 제1 링커를 통해 경쇄 폴리펩타이드의 C-말단에 연결된다. 다른 실시형태에서, scFv에서 VL 영역 및 VH 영역의 배향은 (N-말단)-VH 영역-VL 영역-(C-말단)이며, 여기서 scFv의 N-말단은 제1 링커를 통해 경쇄 폴리펩타이드의 C-말단에 연결된다.
일부 실시형태에서, scFv에서 VL 및 VH 영역을 연결하는 제2 링커는 약 10개 내지 약 25개의 아미노산, 예를 들어, 약 10개 내지 약 20개, 약 12개 내지 약 25개, 약 12개 내지 약 20개, 약 14개 내지 약 25개 또는 약 14개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제2 링커는 약 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개 또는 25개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제2 링커는 가요성 링커를 포함한다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제2 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함한다.
일부 실시형태에서, scFv의 VL 영역 및 VH 영역은 모두 Cys 치환을 포함한다. 일부 실시형태에서, VL 영역 및 VH 영역에서의 Cys 치환은 이황화 결합을 형성하고, scFv의 구조를 안정화시키는 데 도움이 될 수 있다. 일부 실시형태에서, scFv는 가변 도메인 넘버링에 따른 위치 VH44 및 VL100 각각에 시스테인을 포함한다. 일부 실시형태에서, scFv는 위치 VH44 및 VL100에서 시스테인 사이에 이황화 결합을 포함한다.
예를 들어, 항-HER2DII VL 영역은 서열번호 110의 100번 위치에 Gln에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DII VL 영역은 서열번호 114의 서열을 가질 수 있다. 일부 실시형태에서, 항-HER2DIV VL 영역은 서열번호 111의 100번 위치에 Gln에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DIV VL 영역은 서열번호 115의 서열을 가질 수 있다.
예를 들어, 항-HER2DII VH 영역은 서열번호 108의 44번 위치에 Gly에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DII VH 영역은 서열번호 112의 서열을 가질 수 있다. 일부 실시형태에서, 항-HER2DIV VH 영역은 서열번호 109의 44번 위치에 Gly에서 Cys로의 치환을 가질 수 있다. 특정 실시형태에서, Cys 치환을 포함하는 항-HER2DIV VH 영역은 서열번호 113의 서열을 가질 수 있다.
일부 실시형태에서, "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질의 (a) 부분에서, 제1 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 일부 실시형태에서, "LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질의 (b) 부분에서, 제2 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 예시적인 힌지 영역 서열은 인간 IgG1 힌지 서열 EPKSCDKTHTCPPCP(서열번호 127)이다. 부분적인 힌지 영역은 서열번호 127의 서열의 일부, 예를 들어, DKTHTCPPCP(서열번호 128)의 서열을 갖는 부분적인 힌지 영역을 지칭한다.
"LC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 Fc 폴리펩타이드)에 특이적으로 결합할 수 있다. 상이한 Fc 폴리펩타이드 및 이의 변형이 본 명세서에 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함할 수 있다. 예를 들어, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있다. 또 다른 예에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있다. 또한, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함할 수 있다. 예를 들어, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다. "HC 상의 mAb/N-말단 또는 C-말단 scFv" 구조를 갖는 이중특이성 단백질의 특정 실시형태에서, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366W 치환과 L234A 및 L235A 치환을 포함하는 TfR-결합 Fc 폴리펩타이드이고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366S, L368A 및 Y407V 치환을 포함한다. 예를 들어, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있다.
소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함하고, 제2 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않는다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않고, 제2 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함한다.
예시적인 이중특이성 "LC 상의 mAb/N-말단 또는 C-말단 scFv" 단백질
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
경쇄 폴리펩타이드 중 하나는 C-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
경쇄 폴리펩타이드 중 하나는 C-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
2개의 경쇄 폴리펩타이드 각각은 C-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
일례에서, (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
2개의 경쇄 폴리펩타이드 각각은 C-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
일례에서, (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
경쇄 폴리펩타이드 중 하나는 N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
경쇄 폴리펩타이드 중 하나는 N-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
일례에서, (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드;
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
제1 경쇄 폴리펩타이드는 N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 scFv에 융합되고, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 1의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4 또는 5의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 2의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 52의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
제1 경쇄 폴리펩타이드는 N-말단에서 인간 HER2의 서브도메인 II에 결합하는 scFv에 융합되고, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합된다.
이중특이성 단백질의 일례에서, (a) 서열번호 6의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9 또는 10의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 7의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 56 또는 57의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고, 서열번호 53 또는 54의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 이의 C-말단 라이신(예를 들어, EU 넘버링에 따라 Fc 폴리펩타이드의 447번 위치의 Lys 잔기)이 제거될 수 있다. 일부 실시형태에서, Fc 폴리펩타이드에서 C-말단 라이신의 제거는 이중특이성 단백질의 안전성을 개선할 수 있다.
HC 및 LC 상의 mAb/N-말단 V
H
V
L
일부 실시형태에서, 이중특이성 단백질은 2개의 중쇄 각각의 N-말단에서 융합된 VH 영역(또는 VL 영역) 및 2개의 경쇄 각각의 N-말단에서 융합된 VL 영역(또는 VH 영역)을 포함한다. 이러한 이중특이성 단백질의 개략도는 도 4에 도시되어 있다. 일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 Fv 단편의 VH 영역 또는 VL 영역에 융합되고, 그리고
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VH 영역 또는 VL 영역 중 다른 하나에 융합되며, 그리고
VH 영역 및 VL 영역은 함께 Fv 단편을 형성하고, 그리고
Fab는 인간 HER2의 서브도메인 II에 결합하고, Fv 단편은 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, Fv 단편은 인간 HER2의 서브도메인 II에 결합한다.
이중특이성 단백질의 일부 실시형태에서, (a) 및 (b)의 Fd 부분 각각은 N-말단에서 Fv 단편의 VH 영역에 융합되고, 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VL 영역에 융합된다. 다른 실시형태에서, (a) 및 (b)의 Fd 부분 각각은 N-말단에서 Fv 단편의 VL 영역에 융합되고, 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VH 영역에 융합된다.
일부 실시형태에서, 인간 HER2의 서브도메인 II에 특이적으로 결합하는 Fab는 서열번호 108의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다. 일부 실시형태에서, 인간 HER2의 서브도메인 IV에 특이적으로 결합하는 Fab는 서열번호 109의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다.
일부 실시형태에서, 제1 링커는 VH 영역 또는 VL 영역을 (a) 및 (b)의 각각의 Fd 부분의 N-말단에 연결한다. 일부 실시형태에서, 제2 링커는 VH 영역 또는 VL 영역을 2개의 경쇄 폴리펩타이드 각각의 N-말단에 연결한다. 일부 실시형태에서, 제1 링커 또는 제2 링커는 약 1개 내지 약 50개의 아미노산, 예를 들어, 약 1개 내지 약 40개, 약 1개 내지 약 30개, 약 1개 내지 약 25개, 약 1개 내지 약 20개, 약 1개 내지 약 15개, 약 1개 내지 약 10개, 약 2개 내지 약 40개, 약 2개 내지 약 30개, 약 2개 내지 약 20개, 약 2개 내지 약 10개, 약 5개 내지 약 40개, 약 5개 내지 약 30개, 약 5개 내지 약 25개 또는 약 5개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제1 링커는 약 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 30개, 35개, 40개, 45개 또는 50개의 아미노산 길이를 갖는다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 소정의 실시형태에서, 제1 링커는 ASTKGPSVF(서열번호 125)의 서열을 포함한다. 소정의 실시형태에서, 제2 링커는 RTVAAPSVFI(서열번호 126)의 서열을 포함한다.
일부 실시형태에서, "HC 및 LC 상의 mAb/N-말단 VH VL" 구조를 갖는 이중특이성 단백질의 (a) 부분에서, 제1 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 일부 실시형태에서, "HC 및 LC 상의 mAb/N-말단 VH VL" 구조를 갖는 이중특이성 단백질의 (b) 부분에서, 제2 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 예시적인 힌지 영역 서열은 인간 IgG1 힌지 서열 EPKSCDKTHTCPPCP(서열번호 127)이다. 부분적인 힌지 영역은 서열번호 127의 서열의 일부, 예를 들어, DKTHTCPPCP(서열번호 128)의 서열을 갖는 부분적인 힌지 영역을 지칭한다.
구조 "HC 및 LC 상의 mAb/N-말단 VH VL" 구조를 갖는 이중특이성 단백질에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 Fc 폴리펩타이드)에 특이적으로 결합할 수 있다. 상이한 Fc 폴리펩타이드 및 이의 변형이 본 명세서에 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함할 수 있다. 예를 들어, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있다. 또 다른 예에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있다. 또한, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함할 수 있다. 예를 들어, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다. "HC 및 LC 상의 mAb/N-말단 VH VL" 구조를 갖는 이중특이성 단백질의 특정 실시형태에서, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366W 치환과 L234A 및 L235A 치환을 포함하는 TfR-결합 Fc 폴리펩타이드이고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366S, L368A 및 Y407V 치환을 포함한다. 예를 들어, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함하고, 제2 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않는다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않고, 제2 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함한다.
예시적인 이중특이성 "HC 및 LC 상의 mAb/N-말단 VH VL" 단백질
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fv 단편의 VH 영역에 융합되고,
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VL 영역 중 다른 하나에 융합되며, 그리고
VH 영역 및 VL 영역은 함께 Fv 단편을 형성한다.
일례에서, 이중특이성 단백질은 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 58의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 61 또는 62의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 78의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함한다. 또 다른 예에서, 이중특이성 단백질은 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 59의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 60의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 78의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fv 단편의 VH 영역에 융합되고,
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VL 영역 중 다른 하나에 융합되며, 그리고
VH 영역 및 VL 영역은 함께 Fv 단편을 형성한다.
일례에서, 이중특이성 단백질은 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 63의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 66 또는 67의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 79의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함한다. 또 다른 예에서, 제1 폴리펩타이드는 (a) N-말단에서 Fv 단편의 VH 영역에 융합되며, 서열번호 64의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 65의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 79의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fv 단편의 VL 영역에 융합되고,
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VH 영역 중 다른 하나에 융합되며, 그리고
VH 영역 및 VL 영역은 함께 Fv 단편을 형성한다.
일례에서, 이중특이성 단백질은 (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 68의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, 제2 폴리펩타이드는 (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 71 또는 72의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, 제3 및 제4 폴리펩타이드는 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 80의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, 이중특이성 단백질은 (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 69의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 70의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 80의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함한다.
일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a) 및 (b)에 언급된 각각의 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
(a) 및 (b)의 Fd 부분 각각은 N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fv 단편의 VL 영역에 융합되고,
2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VH 영역 중 다른 하나에 융합되며, 그리고
VH 영역 및 VL 영역은 함께 Fv 단편을 형성한다.
일례에서, 이중특이성 단백질은 (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 73의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 76 또는 77의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 81의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함한다. 또 다른 예에서, 이중특이성 단백질은 (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 74의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 75의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 81의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 이의 C-말단 라이신(예를 들어, EU 넘버링에 따라 Fc 폴리펩타이드의 447번 위치의 Lys 잔기)이 제거될 수 있다. 일부 실시형태에서, Fc 폴리펩타이드에서 C-말단 라이신의 제거는 이중특이성 단백질의 안전성을 개선할 수 있다.
HC 상의 mAb/C-말단 V
H
V
L
일부 실시형태에서, 이중특이성 단백질은 C-말단에서 2개의 Fc 폴리펩타이드 중 하나에 융합된 VH 영역(또는 VL 영역) 및 C-말단에서 2개의 Fc 폴리펩타이드 중 다른 하나에 융합된 VL 영역(또는 VH 영역)을 포함한다. 이러한 이중특이성 단백질의 개략도는 도 5에 도시되어 있다. 일부 실시형태에서, 이중특이성 단백질은
(a) N-말단에서 Fab의 Fd 부분에 융합되고 C-말단에서 Fv 단편의 VH 영역 또는 VL 영역에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합되고 C-말단에서 (a)에 언급된 VH 영역 또는 VL 영역 중 다른 하나에 융합된 제2 Fc 폴리펩타이드로서,
VH 영역 및 VL 영역은 함께 Fv 단편을 형성하고, 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
Fab는 인간 HER2의 서브도메인 II에 결합하고, Fv 단편은 인간 HER2의 서브도메인 IV에 결합하거나 또는 Fab는 인간 HER2의 서브도메인 IV에 결합하고, Fv 단편은 인간 HER2의 서브도메인 II에 결합한다.
이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 Fv 단편의 VH 영역에 융합되고, 제2 Fc 폴리펩타이드는 Fv 단편의 VL 영역에 융합된다. 일부 실시형태에서, 제1 Fc 폴리펩타이드는 Fv 단편의 VL 영역에 융합되고, 제2 Fc 폴리펩타이드는 Fv 단편의 VH 영역에 융합된다.
일부 실시형태에서, 인간 HER2의 서브도메인 II에 특이적으로 결합하는 Fab는 서열번호 108의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다. 일부 실시형태에서, 인간 HER2의 서브도메인 IV에 특이적으로 결합하는 Fab는 서열번호 109의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 VH 영역을 포함한다.
일부 실시형태에서, 제1 링커는 VH 영역 또는 VL 영역을 Fc 폴리펩타이드의 C-말단에 연결한다. 일부 실시형태에서, 제1 링커 또는 제2 링커는 약 1개 내지 약 50 아미노산, 예를 들어, 약 1개 내지 약 40개, 약 1개 내지 약 30개, 약 1개 내지 약 25개, 약 1개 내지 약 20개, 약 1개 내지 약 15개, 약 1개 내지 약 10개, 약 2개 내지 약 40개, 약 2개 내지 약 30개, 약 2개 내지 약 20개, 약 2개 내지 약 10개, 약 5개 내지 약 40개, 약 5개 내지 약 30개, 약 5개 내지 약 25개 또는 약 5개 내지 약 20개의 아미노산 길이를 갖는다. 일부 실시형태에서, 제1 링커는 약 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 30개, 35개, 40개, 45개 또는 50개의 아미노산 길이를 갖는다. 다양한 링커가 본 명세서에서 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제1 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함한다.
일부 실시형태에서, "HC 상의 mAb/C-말단 VH VL" 구조를 갖는 이중특이성 단백질의 (a) 부분에서, 제1 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 일부 실시형태에서, "HC 상의 mAb/C-말단 VH VL" 구조를 갖는 이중특이성 단백질의 (b) 부분에서, 제2 Fc 폴리펩타이드는 N-말단에서 힌지 영역 또는 부분적인 힌지 영역을 통해 Fab의 Fd 부분에 융합된다. 예시적인 힌지 영역 서열은 인간 IgG1 힌지 서열 EPKSCDKTHTCPPCP(서열번호 127)이다. 부분적인 힌지 영역은 서열번호 127의 서열의 일부, 예를 들어, DKTHTCPPCP(서열번호 128)의 서열을 갖는 부분적인 힌지 영역을 지칭한다.
"HC 상의 mAb/C-말단 VH VL" 구조를 갖는 이중특이성 단백질에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 트랜스페린 수용체(예를 들어, TfR-결합 Fc 폴리펩타이드)에 특이적으로 결합할 수 있다. 상이한 Fc 폴리펩타이드 및 이의 변형이 본 명세서에 추가로 상세히 기재되어 있다. 일부 실시형태에서, 제1 Fc 폴리펩타이드 및 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함할 수 있다. 예를 들어, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있다. 또 다른 예에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함할 수 있고, 제2 Fc 폴리펩타이드는 T366W 치환을 포함할 수 있다. 또한, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함할 수 있다. 예를 들어, 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환이다. "HC 상의 mAb/N-말단 VH VL" 구조를 갖는 이중특이성 단백질의 특정 실시형태에서, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366W 치환과 L234A 및 L235A 치환을 포함하는 TfR-결합 Fc 폴리펩타이드이고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 EU 넘버링에 따라 T366S, L368A 및 Y407V 치환을 포함한다. 예를 들어, 제1 Fc 폴리펩타이드(또는 제2 Fc 폴리펩타이드)는 서열번호 137의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있고, 제2 Fc 폴리펩타이드(또는 제1 Fc 폴리펩타이드)는 서열번호 133의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함할 수 있다.
소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함하고, 제2 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않는다. 소정의 실시형태에서, EU 넘버링에 따라, 제1 Fc 폴리펩타이드는 L234A 또는 L325A 치환을 포함하지 않고, 제2 Fc 폴리펩타이드는 TfR-결합 Fc 폴리펩타이드이며 L234A 및 L235A 치환을 포함한다.
예시적인 이중특이성 "HC 상의 mAb/C-말단 VH VL" 단백질
일부 실시형태에서, 이중특이성 단백질은 다음을 포함한다:
(a) N-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fab의 Fd 부분에 융합되며 C-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fv 단편의 VH 영역에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합되며 C-말단에서 Fv 단편의 VL 영역에 융합된 제2 Fc 폴리펩타이드.
이중특이성 단백질의 일례에서, (a) 서열번호 82 또는 83의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 99, 100 또는 101의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 84의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 98의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 85의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 97의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 86, 87 또는 88의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 95 또는 96의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
일부 실시형태에서, 이중특이성 단백질은 다음을 포함한다:
(a) N-말단에서 인간 HER2의 서브도메인 IV에 결합하는 Fab의 Fd 부분에 융합되며 C-말단에서 인간 HER2의 서브도메인 II에 결합하는 Fv 단편의 VH 영역에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합되며 C-말단에서 Fv 단편의 VL 영역에 융합된 제2 Fc 폴리펩타이드.
이중특이성 단백질의 일례에서, (a) 서열번호 89 또는 90의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 105, 106 또는 107의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 91의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 104의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 92의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 103의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다. 또 다른 예에서, (a) 서열번호 93 또는 94의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하고, (b) 서열번호 102의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 일부 실시형태에서, 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함한다. 소정의 실시형태에서, 단백질은 아래에 기재된 시스-LALA 배열을 포함한다.
위에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 이의 C-말단 라이신(예를 들어, EU 넘버링에 따라 Fc 폴리펩타이드의 447번 위치의 Lys 잔기)이 제거될 수 있다. 일부 실시형태에서, Fc 폴리펩타이드에서 C-말단 라이신의 제거는 이중특이성 단백질의 안전성을 개선할 수 있다.
IV. Fc 폴리펩타이드 및 이의 변형
일부 양태에서, 본 명세서에 기재된 임의의 항-HER2 이중특이성 단백질은 이량체 내의 Fc 폴리펩타이드 중 하나 또는 둘 모두가 야생형 Fc 폴리펩타이드에 대해 아미노산 변형을 포함하는 Fc 폴리펩타이드 이량체를 포함한다. 일부 실시형태에서, Fc 폴리펩타이드의 아미노산 변형(예를 들어, 변형된 Fc 폴리펩타이드)은 BBB 수용체(예를 들어, TfR)에 대한 Fc 폴리펩타이드 이량체의 결합을 초래하고, 이량체에서 2개의 Fc 폴리펩타이드의 이종이량체화를 촉진하며, 효과기 기능을 조절하고, 혈청 반감기를 연장하며, 글리코실화에 영향을 미치고/미치거나 인간의 면역원성을 감소시킬 수 있다. 일부 실시형태에서, 이중특이성 단백질에 존재하는 Fc 폴리펩타이드는 독립적으로 상응하는 야생형 Fc 폴리펩타이드(예를 들어, 인간 IgG1, IgG2, IgG3 또는 IgG4 Fc 폴리펩타이드)에 대해 적어도 약 85%, 90%, 95%, 96%, 97%, 98% 또는 99%의 아미노산 서열 동일성을 갖는다. 변형된 Fc 폴리펩타이드(예를 들어, TfR-결합 Fc 폴리펩타이드)의 예 및 설명은, 예를 들어, 그 전문이 참조에 의해 본 명세서에 원용되어 있는 국제 특허 공개 제WO 2018/152326호에서 찾을 수 있다.
BBB 수용체 결합을 위한 Fc 폴리펩타이드 변형
BBB를 가로질러 수송될 수 있는 항-HER2 이중특이성 단백질이 본 명세서에 제공된다. 이러한 단백질은 BBB 수용체에 결합하는 변형된 Fc 폴리펩타이드를 포함한다. BBB 수용체는 BBB 내피뿐만 아니라 다른 세포 및 조직 유형에서도 발현된다. 일부 실시형태에서, BBB 수용체는 TfR이다. TfR에 결합하는 변형된 Fc 폴리펩타이드는 또한 TfR-결합 부위를 갖는 것으로 지칭된다.
BBB 수용체, 예를 들어, TfR에 결합하는 변형된 Fc 폴리펩타이드에 도입된 것들을 포함하는 다양한 Fc 변형으로 지정된 아미노산 잔기는 본 명세서에서 EU 인덱스 넘버링을 사용하여 넘버링된다. 임의의 Fc 폴리펩타이드, 예를 들어, IgG1, IgG2, IgG3 또는 IgG4 Fc 폴리펩타이드는 본 명세서에 기재된 바와 같은 하나 이상의 위치에 변형, 예를 들어, 아미노산 치환을 가질 수 있다. 일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 활성에 대해 변형된 도메인은 IgG1 CH3 도메인과 같은 인간 Ig CH3 도메인이다. CH3 도메인은 임의의 IgG 하위유형, 즉, IgG1, IgG2, IgG3 또는 IgG4로부터의 것일 수 있다. IgG1 항체의 맥락에서, CH3 도메인은 EU 넘버링 체계에 따라 넘버링 시 약 341번 위치 내지 약 447번 위치의 아미노산의 분절을 지칭한다.
일부 실시형태에서, TfR에 특이적으로 결합하는 변형된 Fc 폴리펩타이드는 TfR의 첨단 도메인에 결합하며, TfR에 대한 트랜스페린의 결합을 차단하거나 또는 그렇지 않으면 저해하지 않고 TfR에 결합할 수 있다. 일부 실시형태에서, TfR에 대한 트랜스페린의 결합은 실질적으로 저해되지 않는다. 일부 실시형태에서, TfR에 대한 트랜스페린의 결합은 약 50% 미만(예를 들어, 약 45%, 40%, 35%, 30%, 25%, 20%, 15%, 10% 또는 5% 미만)만큼 저해된다.
일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 하나 이상의 적어도 1개, 2개 또는 3개의 치환; 일부 실시형태에서, EU 넘버링 체계에 따른 266번, 267번, 268번, 269번, 270번, 271번, 295번, 297번, 298번 및 299번을 포함하는 아미노산 위치에 적어도 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 치환을 포함한다. 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 적어도 1개, 2개 또는 3개의 치환; 일부 실시형태에서, EU 넘버링 체계에 따른 274번, 276번, 283번, 285번, 286번, 287번, 288번, 289번 및 290번을 포함하는 아미노산 위치에 적어도 4개, 5개, 6개, 7개, 8개 또는 9개의 치환을 포함한다. 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 적어도 1개, 2개 또는 3개의 치환; 일부 실시형태에서, EU 넘버링 체계에 따른 268번, 269번, 270번, 271번, 272번, 292번, 293번, 294번, 296번 및 300번을 포함하는 아미노산 위치에 적어도 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 치환을 포함한다. 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 적어도 1개, 2개 또는 3개의 치환; 일부 실시형태에서, EU 넘버링 체계에 따른 272번, 274번, 276번, 322번, 324번, 326번, 329번, 330번 및 331번을 포함하는 아미노산 위치에 적어도 4개, 5개, 6개, 7개, 8개 또는 9개의 치환을 포함한다. 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 적어도 1개, 2개 또는 3개의 치환; 일부 실시형태에서, EU 넘버링 체계에 따른 345번, 346번, 347번, 349번, 437번, 438번, 439번 및 440번을 포함하는 아미노산 위치에 적어도 4개, 5개, 6개 또는 7개의 치환을 포함한다.
일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 적어도 1개, 2개 또는 3개의 치환; 및 일부 실시형태에서, EU 넘버링 체계에 따른 384번, 386번, 387번, 388번, 389번, 390번, 413번, 416번 및 421번 아미노산 위치에 적어도 4개, 5개, 6개, 7개, 8개 또는 9개의 치환을 포함한다.
일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 서열번호 130에 대해 다음과 같은 치환을 갖는 적어도 하나의 위치를 포함한다: 384번 위치에 Leu, Tyr, Met 또는 Val; 386번 위치에 Leu, Thr, His 또는 Pro; 387번 위치에 Val, Pro 또는 산성 아미노산; 방향족 아미노산, 예를 들어, 388번 위치에 Trp 또는 Gly(예를 들어, Trp); 389번 위치에 Val, Ser 또는 Ala; 413번 위치에 산성 아미노산, Ala, Ser, Leu, Thr 또는 Pro; 416번 위치에 Thr 또는 산성 아미노산; 또는 421번 위치에 Trp, Tyr, His 또는 Phe. 일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 보존적 치환, 예를 들어, 세트 내의 하나 이상의 위치에서 특정 아미노산의 동일한 전하 그룹, 소수성 그룹, 측쇄 고리 구조 그룹(예를 들어, 방향족 아미노산) 또는 크기 그룹 및/또는 극성 또는 비극성 그룹의 아미노산을 포함할 수 있다. 따라서, 예를 들어, Ile는 384번, 386번 위치 및/또는 413번 위치에 존재할 수 있다. 일부 실시형태에서, 387번, 413번 및 416번 위치 중 1개, 2개 또는 각각의 위치에서 산성 아미노산은 Glu이다. 다른 실시형태에서, 위치 387번, 413번 및 416번 위치 중 1개, 2개 또는 각각에서 산성 아미노산은 Asp이다. 일부 실시형태에서, 384번, 386번, 387번, 388번, 389번, 413번, 416번 및 421번 위치 중 2개, 3개, 4개, 5개, 6개, 7개 또는 8개 모두는 이 단락에 명시된 바와 같은 아미노산 치환을 갖는다.
일부 실시형태에서, 384번, 386번, 387번, 388번, 389번, 390번, 413번, 416번 및/또는 421번 아미노산 위치에 변형을 갖는 Fc 폴리펩타이드는 390번 위치에 고유의 Asn을 포함한다. 일부 실시형태에서, Fc 폴리펩타이드는 390번 위치에 Gly, His, Gln, Leu, Lys, Val, Phe, Ser, Ala 또는 Asp를 포함한다. 일부 실시형태에서, Fc 폴리펩타이드는 380번, 391번, 392번 및 415번을 포함하는 위치에 1개, 2개, 3개 또는 4개의 치환을 추가로 포함한다. 일부 실시형태에서, Trp, Tyr, Leu 또는 Gln이 380번 위치에 존재할 수 있다. 일부 실시형태에서, Ser, Thr, Gln 또는 Phe가 391번 위치에 존재할 수 있다. 일부 실시형태에서, Gln, Phe 또는 His가 위치 392번 위치에 존재할 수 있다. 일부 실시형태에서, Glu가 415번 위치에 존재할 수 있다.
소정의 실시형태에서, Fc 폴리펩타이드는 다음으로부터 선택되는 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 위치를 포함한다: 380번 위치에 Trp, Leu 또는 Glu; 384번 위치에 Tyr 또는 Phe; 386번 위치에 Thr; 387번 위치에 Glu; 388번 위치에 Trp; 389번 위치에 Ser, Ala, Val 또는 Asn; 390번 위치에 Ser 또는 Asn; 413번 위치에 Thr 또는 Ser; 415번 위치에 Glu 또는 Ser; 416번 위치에 Glu; 및/또는 421번 위치에 Phe. 일부 실시형태에서, Fc 폴리펩타이드는 다음과 같은 11개의 위치 모두를 포함한다: 380번 위치에 Trp, Leu 또는 Glu; 384번 위치에 Tyr 또는 Phe; 386번 위치에 Thr; 387번 위치에 Glu; 388번 위치에 Trp; 389번 위치에 Ser, Ala, Val 또는 Asn; 390번 위치에 Ser 또는 Asn; 413번 위치에 Thr 또는 Ser; 415번 위치에 Glu 또는 Ser; 416번 위치에 Glu; 및/또는 421번 위치에 Phe.
소정의 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 384번 위치에 Leu 또는 Met; 386번 위치에 Leu, His 또는 Pro; 387번 위치에 Val; 388번 위치에 Trp; 389번 위치에 Val 또는 Ala; 413번 위치에 Pro; 416번 위치에 Thr; 및/또는 421번 위치에 Trp. 일부 실시형태에서, Fc 폴리펩타이드는 391번 위치에 Ser, Thr, Gln 또는 Phe를 추가로 포함한다. 일부 실시형태에서, Fc 폴리펩타이드는 380번 위치에 Trp, Tyr, Leu 또는 Gln 및/또는 392번 위치에 Gln, Phe 또는 His를 추가로 포함한다. 일부 실시형태에서, Trp는 380번 위치에 존재하고/하거나 Gln은 392번 위치에 존재한다. 일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 380번 위치에 Trp를 포함하지 않는다.
다른 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 384번 위치에 Tyr; 386번 위치에 Thr; 387번 위치에 Glu 또는 Val; 388번 위치에 Trp; 389번 위치에 Ser; 413번 위치에 Ser 또는 Thr; 416번 위치에 Glu; 및/또는 421번 위치에 Phe를 포함한다. 일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 390번 위치에 고유의 Asn을 포함한다. 소정의 실시형태에서, Fc 폴리펩타이드는 380번 위치에 Trp, Tyr, Leu 또는 Gln; 및/또는 415번 위치에 Glu를 추가로 포함한다. 일부 실시형태에서, Fc 폴리펩타이드는 380번 위치에 Trp 및/또는 415번 위치에 Glu를 추가로 포함한다.
일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 다음 치환 중 하나 이상을 포함한다: 380번 위치에 Trp; 386번 위치에 Thr; 388번 위치에 Trp; 389번 위치에 Val; 413번 위치에 Ser 또는 Thr; 415번 위치에 Glu; 및/또는 421번 위치에 Phe.
추가적인 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 다음으로부터 선택되는 1개, 2개 또는 3개의 위치를 추가로 포함한다: 414번 위치는 Lys, Arg, Gly 또는 Pro이고; 424번 위치는 Ser, Thr, Glu 또는 Lys이며; 426번 위치는 Ser, Trp 또는 Gly이다.
일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 서열번호 135의 서열을 갖는다. 본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 이량체 내의 2개의 Fc 폴리펩타이드 중 하나는 서열번호 135의 서열을 갖는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있는 반면, Fc 폴리펩타이드 이량체 내의 다른 Fc 폴리펩타이드는 야생형 Fc 폴리펩타이드의 서열(예를 들어, 서열번호 130)을 가질 수 있다. 본 명세서에 기재된 이중특이성 단백질의 다른 실시형태에서, Fc 폴리펩타이드 이량체 내의 두 Fc 폴리펩타이드는 서열번호 135의 서열을 갖는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있다.
본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 이량체 내의 2개의 Fc 폴리펩타이드 중 하나는 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있는 반면, Fc 폴리펩타이드 이량체 내의 다른 Fc 폴리펩타이드는 야생형 Fc 폴리펩타이드의 서열(예를 들어, 서열번호 130)을 가질 수 있다.
본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, 제1 Fc 폴리펩타이드 및/또는 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ala, 413번 위치에 Thr, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 140 내지 144로부터 선택되는 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100%)의 동일성을 갖는 서열을 포함한다.
본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 이량체 내의 2개의 Fc 폴리펩타이드 중 하나는 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ala, 413번 위치에 Thr, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 140의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있는 반면, Fc 폴리펩타이드 이량체 내의 다른 Fc 폴리펩타이드는 야생형 Fc 폴리펩타이드의 서열(예를 들어, 서열번호 130)을 가질 수 있다.
일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 서열번호 140의 서열을 갖는다. 본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 이량체 내의 2개의 Fc 폴리펩타이드 중 하나는 서열번호 140의 서열을 갖는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있는 반면, Fc 폴리펩타이드 이량체 내의 다른 Fc 폴리펩타이드는 야생형 Fc 폴리펩타이드의 서열(예를 들어, 서열번호 130)을 가질 수 있다. 본 명세서에 기재된 이중특이성 단백질의 다른 실시형태에서, Fc 폴리펩타이드 이량체 내의 두 Fc 폴리펩타이드는 서열번호 140의 서열을 갖는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있다.
일부 실시형태에서, BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드는 서열번호 145의 서열을 갖는다. 본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 이량체 내의 2개의 Fc 폴리펩타이드 중 하나는 서열번호 145의 서열을 갖는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있는 반면, Fc 폴리펩타이드 이량체 내의 다른 Fc 폴리펩타이드는 야생형 Fc 폴리펩타이드의 서열(예를 들어, 서열번호 130)을 가질 수 있다. 본 명세서에 기재된 이중특이성 단백질의 다른 실시형태에서, Fc 폴리펩타이드 이량체 내의 두 Fc 폴리펩타이드는 서열번호 145의 서열을 갖는 BBB(예를 들어, TfR) 수용체-결합 Fc 폴리펩타이드일 수 있다.
이종이량체화를 위한 Fc 폴리펩타이드 변형
일부 실시형태에서, 본 명세서에 기재된 임의의 이중특이성 단백질에 존재하는 Fc 폴리펩타이드는 이종이량체 형성을 촉진하고 동종이량체 형성을 방해하는 놉 및 홀 돌연변이를 포함한다. 일반적으로, 변형은 이종이량체 형성을 촉진하기 위해 돌기가 공동에 위치될 수 있어 동종이량체 형성을 방해할 수 있도록, 제1 폴리펩타이드의 계면에 돌기("놉")와 제2 폴리펩타이드의 계면에 상응하는 공동("홀")을 도입한다. 돌기는 제1 폴리펩타이드의 계면에서 작은 아미노산 측쇄를 더 큰 측쇄(예를 들어, 타이로신 또는 트립토판)로 대체함으로써 구성된다. 큰 아미노산 측쇄를 더 작은 측쇄(예를 들어, 알라닌 또는 트레오닌)로 대체함으로써 돌기와 동일하거나 또는 유사한 크기의 보상 공동(Compensatory cavity)이 제2 폴리펩타이드의 계면에 생성된다. 일부 실시형태에서, 이러한 추가적인 돌연변이는 BBB 수용체, 예를 들어, TfR에 대한 폴리펩타이드의 결합에 부정적인 영향을 미치지 않는 Fc 폴리펩타이드의 위치에 있다.
이량체화를 위한 놉 및 홀 접근 방식의 한 예시적인 실시형태에서, 이중특이성 단백질에 존재하는 Fc 폴리펩타이드 중 하나의 366번 위치(EU 넘버링 체계에 따라 넘버링 됨)는 고유한 트레오닌 대신에 트립토판을 포함한다. 이량체 내 다른 Fc 폴리펩타이드는 고유한 타이로신 대신에 407번 위치(EU 넘버링 체계에 따라 넘버링 됨)에 발린이 있다. 다른 Fc 폴리펩타이드는 366번 위치(EU 넘버링 체계에 따라 넘버링 됨)의 고유한 트레오닌이 세린으로 치환되고 368번 위치(EU 넘버링 체계에 따라 넘버링 됨)의 고유한 류신이 알라닌으로 치환된 치환을 추가로 포함할 수 있다. 따라서, 본 명세서에 기재된 이중특이성 단백질의 Fc 폴리펩타이드 중 하나는 T366W 놉 돌연변이를 갖고, 다른 Fc 폴리펩타이드는 전형적으로 T366S 및 L368A 홀 돌연변이를 수반하는 Y407V 돌연변이를 갖는다.
일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 Fc 폴리펩타이드 중 하나 또는 둘 모두는 또한 이종이량체화를 위한 다른 변형, 예를 들어, 자연적으로 하전되거나 또는 소수성 패치 변형인 CH3-CH3 계면 내의 접촉 잔기의 정전기적 조작을 포함하도록 조작될 수 있다.
예를 들어, 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 T366W 놉 돌연변이와 서열번호 131의 서열에 대해 적어도 90%(예를 들어, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99%)의 동일성을 갖는 하나의 Fc 폴리펩타이드 및 T366S, L368A 및 Y407V 홀 돌연변이와 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 다른 Fc 폴리펩타이드를 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다. 소정의 실시형태에서, Fc 폴리펩타이드 이량체 내 Fc 폴리펩타이드 중 하나 또는 둘 모두는 TfR-결합 Fc 폴리펩타이드일 수 있다. 특정 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) 서열번호 133의 서열을 갖는 제1 Fc 폴리펩타이드 및 (ii) 서열번호 136의 서열을 갖는 제2 Fc 폴리펩타이드를 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다. 특정 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) 서열번호 133의 서열을 갖는 제1 Fc 폴리펩타이드 및 (ii) 서열번호 141의 서열을 갖는 제2 Fc 폴리펩타이드를 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다. 특정 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 제1 Fc 폴리펩타이드 및 (ii) 서열번호 146의 서열을 갖는 제2 Fc 폴리펩타이드를 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다.
효과기 기능을 조절하기 위한 Fc 폴리펩타이드 변형
일부 실시형태에서, 본 명세서에 기재된 임의의 이중특이성 단백질에 존재하는 Fc 폴리펩타이드 중 하나 또는 둘 모두는 효과기 기능을 감소시키는 변형, 즉, 효과기 기능을 매개하는 효과기 세포에서 발현된 Fc 수용체에 결합 시 소정의 생물학적 기능을 유도하는 능력이 감소된 변형을 포함할 수 있다. 항체 효과기 기능의 예는 C1q 결합 및 보체 의존적 세포독성(complement dependent cytotoxicity: CDC), Fc 수용체 결합, 항체-의존적 세포-매개성 세포독성(antibody-dependent cell-mediated cytotoxicity: ADCC), 항체-의존적 세포-매개성 식세포작용(antibody-dependent cell-mediated phagocytosis: ADCP), 세포 표면 수용체(예를 들어, B 세포 수용체) 및 B-세포 활성화의 하향조절을 포함하지만 이들로 제한되지 않는다. 효과기 기능은 항체 클래스에 따라 다를 수 있다. 예를 들어, 고유한 인간 IgG1 및 IgG3 항체는 면역계 세포에 존재하는 적절한 Fc 수용체에 결합 시 ADCC 및 CDC 활성을 유도할 수 있고; 고유한 인간 IgG1, IgG2, IgG3 및 IgG4는 면역 세포에 존재하는 적절한 Fc 수용체에 결합 시 ADCP 기능을 유도할 수 있다.
일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 Fc 폴리펩타이드 중 하나 또는 둘 모두는 효과기 기능을 감소시키거나 또는 제거하는 변형을 포함할 수 있다. 효과기 기능을 감소시키는 예시적인 Fc 폴리펩타이드 돌연변이는, 예를 들어, EU 넘버링 체계에 따른 234번 및 235번 위치에 CH2 도메인의 치환을 포함하지만 이들로 제한되지 않는다. 예를 들어, 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 234번 및 235번 위치에 알라닌 잔기를 포함할 수 있다. 따라서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 L234A 및 L235A(본 명세서에서 "LALA"로도 지칭됨) 치환을 가질 수 있다.
효과기 기능을 조절하는 추가적인 Fc 폴리펩타이드 돌연변이는 다음을 포함하지만 이들로 제한되지 않는다: 329번 위치는 프롤린이 글리신, 알라닌, 세린 또는 아르기닌, 또는 Fc의 프롤린 329 및 트립토판 잔기 Trp 87 및 FcγRIII의 Trp 110 사이에 형성된 Fc/Fcγ 수용체 계면을 파괴하기에 충분히 큰 아미노산 잔기로 치환된 돌연변이를 가질 수 있다. 추가적인 예시적인 치환은 EU 넘버링 체계에 따라 S228P, E233P, L235E, N297A, N297D 및 P331S를 포함한다. 다중 치환, 예를 들어, EU 넘버링 체계에 따라 인간 IgG1 Fc 영역의 L234A 및 L235A; 인간 IgG1 Fc 영역의 L234A, L235A 및 P329G; 인간 IgG4 Fc 영역의 S228P 및 L235E; 인간 IgG1 Fc 영역의 L234A 및 G237A; 인간 IgG1 Fc 영역의 L234A, L235A 및 G237A; 인간 IgG2 Fc 영역의 V234A 및 G237A; 인간 IgG4 Fc 영역의 L235A, G237A 및 E318A; 및 인간 IgG4 Fc 영역의 S228P 및 L236E가 또한 존재할 수 있다. 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 ADCC를 조절하는 하나 이상의 아미노산 치환, 예를 들어, EU 넘버링 체계에 따라 298번, 333번 및/또는 334번에서 치환을 가질 수 있다.
"시스-LALA" 배열
본 명세서에 기재된 임의의 이중특이성 단백질의 일부 실시형태에서, 이중특이성 단백질 내의 2개의 Fc 폴리펩타이드 중 2개의 Fc 폴리펩타이드 중 하나만(Fc 폴리펩타이드 둘 모두가 아님)이 효과기 기능을 감소시키고 TfR에 결합하도록 변형된다. 다른 Fc 폴리펩타이드는 TfR-결합 부위 또는 임의의 효과기 기능을 감소시키는 변형을 포함하지 않는다. TfR-결합 부위 및 FcγR 결합을 감소시키는 변형(예를 들어, LALA 치환)을 둘 다 포함하는 2개의 Fc 폴리펩타이드 중 하나만을 갖는 반면, 다른 Fc 폴리펩타이드는 TfR-결합 부위 또는 FcγR 결합을 감소시키는 임의의 변형을 포함하지 않는 이중특이성 단백질 내 Fc 폴리펩타이드 이량체는 시스-LALA 배열을 갖는 것으로 지칭된다.
예를 들어, 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) TfR-결합 부위 및 LALA 치환뿐만 아니라 놉 변형 둘 다를 갖는 서열번호 137의 서열을 갖는 제1 Fc 폴리펩타이드 및 (ii) 홀 변형만을 갖는 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 제2 Fc 폴리펩타이드 갖는, 시스-LALA 배열을 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다. 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) TfR-결합 부위 및 LALA 치환뿐만 아니라 놉 변형 둘 다를 갖는 서열번호 142의 서열을 갖는 제1 Fc 폴리펩타이드 및 (ii) 홀 변형만을 갖는 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 제2 Fc 폴리펩타이드를 갖는, 시스-LALA 배열을 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다. 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) TfR-결합 부위 및 LALA 치환뿐만 아니라 놉 변형 둘 다를 갖는 서열번호 147의 서열을 갖는 제1 Fc 폴리펩타이드 및 (ii) 홀 변형만을 갖는 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 제2 Fc 폴리펩타이드를 갖는, 시스-LALA 배열을 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다.
특정 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 Fc 폴리펩타이드 및 (ii) EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 Fc 폴리펩타이드를 갖는, 시스-LALA 배열을 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다.
특정 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (ii) 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 시스-LALA 배열을 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다.
특정 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ala, 413번 위치에 Thr, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 142의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 Fc 폴리펩타이드 및 (ii) EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 Fc 폴리펩타이드를 갖는, 시스-LALA 배열을 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다.
특정 실시형태에서, 본 명세서에 기재된 이중특이성 단백질은 (i) EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 Fc 폴리펩타이드 및 (ii) EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ala, 413번 위치에 Thr, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 142의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 Fc 폴리펩타이드를 갖는, 시스-LALA 배열을 갖는 Fc 폴리펩타이드 이량체를 포함할 수 있다.
혈청 반감기를 연장시키기 위한 Fc 폴리펩타이드 변형
일부 실시형태에서, 혈청 반감기를 향상시키기 위한 변형이 본 명세서에 기재된 임의의 이중특이성 단백질에 도입될 수 있다. 예를 들어, 일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질에 존재하는 Fc 폴리펩타이드 중 하나 또는 둘 모두는 EU 넘버링 체계에 따라 넘버링 시 252번 위치에 타이로신, 254번 위치에 트레오닌 및 256번 위치에 글루탐산을 포함할 수 있다. 따라서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 M252Y, S254T 및 T256E 치환을 가질 수 있다. 대안적으로, Fc 폴리펩타이드 중 하나 또는 둘 모두는 EU 넘버링 체계에 따라 넘버링 시 M428L 및 N434S 치환을 가질 수 있다. 대안적으로, Fc 폴리펩타이드 중 하나 또는 둘 모두는 N434S 또는 N434A 치환을 가질 수 있다.
C-말단 라이신 잔기가 제거된 Fc 폴리펩타이드
본 명세서에 기재된 이중특이성 단백질의 일부 실시형태에서, Fc 폴리펩타이드 중 하나 또는 둘 모두는 이의 C-말단 라이신(예를 들어, EU 넘버링에 따라 Fc 폴리펩타이드의 447번 위치의 Lys 잔기)이 제거될 수 있다. C-말단 라이신 잔기는 많은 종에 걸쳐 면역글로불린에 고도로 보존되며, 단백질 생산 동안 세포 기구에 의해 완전히 또는 부분적으로 제거될 수 있다. 일부 실시형태에서, Fc 폴리펩타이드에서 C-말단 라이신의 제거는 이중특이성 단백질의 안전성을 개선할 수 있다.
V. 링커
본 명세서에 기재된 바와 같이, 이중특이성 단백질은 하나 이상의 링커를 포함할 수 있다. 링커는 이중특이성 단백질 내 2개의 요소(즉, VH 영역과 VL 영역 사이, scFv와 Fc 폴리펩타이드 사이, scFv와 Fd 부분 사이, scFv와 경쇄 사이, VH 영역 또는 VL 영역과 Fd 부분 사이, VH 영역 또는 VL 영역과 경쇄 사이 또는 VH 영역 또는 VL 영역과 Fc 폴리펩타이드 사이) 사이의 연결을 지칭한다. 일부 실시형태에서, 링커는 공간 및/또는 유연성을 제공하기 위해 이중특이성 단백질 내 두 요소를 연결할 수 있는 펩타이드 링커일 수 있다.
일부 실시형태에서, 링커는 1개 내지 100개의 아미노산(예를 들어, 1개 내지 90개, 1개 내지 80개, 1개 내지 70개, 1개 내지 90개, 1개 내지 60개, 1개 내지 50개, 1개 내지 40개, 1개 내지 30개, 1개 내지 20개, 1개 내지 10개, 1개 내지 8개, 1개 내지 6개, 1개 내지 4개, 5개 내지 100개, 10개 내지 100개, 15개 내지 100개, 20개 내지 100개, 30개 내지 100개, 40개 내지 100개, 50개 내지 100개, 60개 내지 100개, 70개 내지 100개, 80개 내지 100개, 90개 내지 100개, 10개 내지 90개, 10개 내지 80개, 10개 내지 70개, 10개 내지 60개, 10개 내지 50개, 10개 내지 40개, 10개 내지 30개, 10개 내지 25개, 10개 내지 20개 또는 10개 내지 15개의 아미노산)을 포함할 수 있다. 일부 실시형태에서, 2개의 Fc 도메인 단량체 사이의 링커는 1개 내지 30개의 아미노산(예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 26개, 27개, 28개, 29개 또는 30개의 아미노산)을 포함하는 아미노산 스페이서이다. 링커는 천연 아미노산, 비천연 아미노산 또는 이들의 조합을 포함할 수 있다. 일부 실시형태에서, 링커는, 예를 들어, Gly, Asn, Ser, Thr, Ala 등과 같은 아미노산을 포함하는 가요성 링커일 수 있다. 이러한 링커는 공지된 매개변수를 사용하여 설계될 수 있고, 임의의 길이일 수 있으며, 임의의 길이의 임의의 수의 반복 단위(예를 들어, Gly 및 Ser 잔기의 반복 단위)를 포함할 수 있다. 예를 들어, 링커는 2개, 3개, 4개, 5개 이상의 GGGGS(서열번호 117), GGSG(서열번호 151), GSGG(서열번호 152) 또는 SGGG(서열번호 153) 반복부 또는 단일 GGGGS(서열번호 117), GGSG(서열번호 151), GSGG(서열번호 152) 또는 SGGG(서열번호 153)와 같은 반복부를 가질 수 있다. Gly 및 Ser 잔기를 포함하는 가요성 링커의 예는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123)를 포함하지만 이들로 제한되지 않는다.
일부 실시형태에서, 링커는 또한 글리신 및 세린 이외의 아미노산, 예를 들어, GGGGSEPKSS(서열번호 124), ASTKGPSVF(서열번호 125) 또는 RTVAAPSVFI(서열번호 126)를 포함할 수 있다. 다른 링커의 예는 또한 당업계에 기술되어 있으며, 예를 들어, 문헌[Chen et al. Adv. Drug Deliv Rev. 65(10):1357-1369, 2013]을 참조한다.
VI. 이중특이성 단백질의 제조
본 명세서에 기재된 이중특이성 단백질을 제조하기 위해, 당업계에 공지된 많은 기법이 사용될 수 있다. 일부 실시형태에서, 관심 항체의 중쇄 및 경쇄를 암호화하는 유전자는 세포, 예를 들어, 하이브리도마로부터 클로닝될 수 있다. 단일클론 항체의 중쇄 및 경쇄를 암호화하는 유전자 라이브러리는 또한 하이브리도마 또는 혈장 세포로부터 만들어질 수 있다. 대안적으로, 파지 또는 효모 디스플레이 기술이 선택된 항원에 특이적으로 결합하는 항체 및 Fab 단편을 확인하기 위해 사용될 수 있다.
이중특이성 단백질은 원핵생물 및 진핵생물 발현 시스템을 비롯한 임의의 수의 발현 시스템을 사용하여 생산될 수 있다. 일부 실시형태에서, 발현 시스템은 하이브리도마 또는 CHO 세포 발현 시스템과 같은 포유동물 세포 발현 시스템이다. 많은 이러한 시스템은 상업적 공급업체로부터 널리 입수 가능하다. 일부 실시형태에서, 이중특이성 단백질을 포함하는 폴리펩타이드를 암호화하는 폴리뉴클레오타이드는, 예를 들어, 이중-시스트론성 발현 단위에서 또는 상이한 프로모터의 제어하에 단일 벡터를 사용하여 발현될 수 있다. 다른 실시형태에서, 이중특이성 단백질을 포함하는 폴리펩타이드를 암호화하는 폴리뉴클레오타이드는 별도의 벡터를 사용하여 발현될 수 있다.
일부 양태에서, 본 개시내용은 본 명세서에 기재된 바와 같은 이중특이성 단백질을 포함하는 임의의 폴리펩타이드를 암호화하는 핵산 서열을 포함하는 단리된 핵산; 이러한 핵산을 포함하는 벡터; 핵산을 복제하고/하거나 이중특이성 단백질을 발현하는 데 사용되는 핵산이 도입된 숙주 세포를 제공한다.
일부 실시형태에서, 폴리뉴클레오타이드(예를 들어, 단리된 폴리뉴클레오타이드)는 본 명세서에 개시된 바와 같은(예를 들어, 위의 부문 III에 기재된 바와 같은) 이중특이성 단백질을 포함하는 폴리펩타이드를 암호화하는 뉴클레오타이드 서열을 포함한다. 일부 실시형태에서, 폴리뉴클레오타이드는 아래의 약식 서열 목록에 개시된 하나 이상의 아미노산 서열(예를 들어, 중쇄, 경쇄 및/또는 Fc 폴리펩타이드 서열)을 암호화하는 뉴클레오타이드 서열을 포함한다. 일부 실시형태에서, 폴리뉴클레오타이드는 아래의 약식 서열 목록에 개시된 서열에 대해 적어도 85%의 서열 동일성(예를 들어, 적어도 85%, 적어도 90%, 적어도 91%, 적어도 92%, 적어도 93%, 적어도 94%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98% 또는 적어도 99%의 서열 동일성)을 갖는 아미노산 서열을 암호화하는 뉴클레오타이드 서열을 포함한다. 일부 실시형태에서, 본 명세서에 기재된 바와 같은 폴리뉴클레오타이드는 이종 핵산, 예를 들어, 이종 프로모터에 작동 가능하게 연결된다.
본 개시내용의 항체 또는 이의 단편을 암호화하는 폴리뉴클레오타이드를 포함하는 적합한 벡터는 클로닝 벡터 및 발현 벡터를 포함한다. 선택된 클로닝 벡터는 사용하고자 하는 숙주 세포에 따라 다양할 수 있지만, 유용한 클로닝 벡터는 일반적으로 자가 복제 능력이 있으며, 특정 제한 엔도뉴클레이스에 대한 단일 표적을 보유할 수 있고/있거나 벡터를 포함하는 클론을 선택하는 데 사용될 수 있는 마커를 위한 유전자를 운반할 수 있다. 예는 플라스미드 및 세균 바이러스, 예를 들어, pUC18, pUC19, Bluescript(예를 들어, pBS SK+) 및 이의 파생물, mpl8, mpl9, pBR322, pMB9, ColE1, pCR1, RP4, 파지 DNAs 및 셔틀 벡터, 예컨대, pSA3 및 pAT28을 포함한다. 이들 및 많은 다른 클로닝 벡터가 바이오래드(BioRad), 스트레이트진(Strategene) 및 인비트로젠(Invitrogen)과 같은 상업적 공급업체로부터 입수 가능하다.
발현 벡터는 일반적으로 본 개시내용의 핵산을 포함하는 복제 가능한 폴리뉴클레오타이드 작제물이다. 발현 벡터는 에피솜 또는 염색체 DNA의 통합 부위로서 숙주 세포에서 복제할 수 있다. 적합한 발현 벡터는 플라스미드, 아데노바이러스, 아데노-관련 바이러스, 레트로바이러스 및 임의의 다른 벡터를 포함하는 바이러스 벡터를 포함하지만 이들로 제한되지 않는다.
본 명세서에 기재된 바와 같은 폴리뉴클레오타이드 또는 벡터를 클로닝하거나 또는 발현시키는 데 적합한 숙주 세포는 원핵생물 또는 진핵생물 세포를 포함한다. 일부 실시형태에서, 숙주 세포는 원핵생물이다. 일부 실시형태에서, 숙주 세포는 진핵생물, 예를 들어, 차이니즈 햄스터 난소(Chinese Hamster Ovary: CHO) 세포 또는 림프성 세포이다. 일부 실시형태에서, 숙주 세포는 인간 세포, 예를 들어, 인간 배아 신장(Human Embryonic Kidney: HEK) 세포이다.
또 다른 양태에서, 본 명세서에 기재된 바와 같은 이중특이성 단백질을 제조하는 방법이 제공된다. 일부 실시형태에서, 방법은 이중특이성 단백질의 발현에 적합한 조건하에서 본 명세서에 기재된 바와 같은 숙주 세포(예를 들어, 본 명세서에 기재된 바와 같은 폴리뉴클레오타이드 또는 벡터를 발현하는 숙주 세포)를 배양하는 단계를 포함한다. 일부 실시형태에서, 이중특이성 단백질은 후속적으로 숙주 세포(또는 숙주 세포 배양 배지)로부터 회수된다. 일부 실시형태에서, 이중특이성 단백질은, 예를 들어, 크로마토그래피에 의해 정제된다.
VII. 치료적 방법
일부 양태에서, 치료학적 유효량의 본 명세서에 기재된 임의의 이중특이성 단백질 또는 이를 포함하는 약제학적 조성물을 대상체에게 투여함으로써 대상체에서 암(예를 들어, HER2-양성 암)을 치료하거나 또는 암(예를 들어, HER2-양성 암)의 뇌 전이를 치료하는 방법이 본 명세서에 제공된다. 또한, 내피를 가로질러 HER2(예를 들어, 인간 HER2) 또는 항원-결합 이의 단편에 결합할 수 있는 항체 가변 영역의 통과세포외배출 방법이 본 명세서에 제공된다. 일부 실시형태에서, 방법은 내피를 본 명세서에 기재된 이중특이성 단백질을 포함하는 조성물과 접촉시키는 단계를 포함한다. 일부 실시형태에서, 내피는 혈액 뇌 장벽(BBB)이다.
본 명세서에 제공된 방법에 따라 치료될 수 있는 비제한적인 예는 HER2-양성 유방암, 난소암, 방광암, 침샘암, 자궁내막암, 췌장암 및 비소세포 폐암(non-small-cell lung cancer: NSCLC)뿐만 아니라 HER2-양성 위 선암종 및/또는 HER2-양성 위식도 접합부 선암종을 포함한다. 일부 실시형태에서, HER2-양성 암은 HER2-양성 유방암이다. 일부 실시형태에서, HER2-양성 암은 HER2-양성 위 선암종 및/또는 HER2-양성 위식도 접합부 선암종이다. 일부 실시형태에서, HER2-양성 암은 전이성 암이다.
또 다른 양태에서, 암(예를 들어, HER2-양성 암)의 전이를 치료하는 방법이 본 명세서에 제공된다. 일부 실시형태에서, 방법은 치료학적 유효량의 본 명세서에 기재된 항-HER2 이중특이성 단백질을 대상체에게 투여하는 단계를 포함한다. 일부 실시형태에서, 전이는 위에 기재된 HER2-양성 암의 뇌 전이이다. 일부 실시형태에서, 전이는 HER2-양성 유방암의 뇌 전이이다. 일부 실시형태에서, 전이는 HER2-양성 위 선암종 및/또는 HER2-양성 위식도 접합부 선암종의 뇌 전이이다.
일부 실시형태에서, 치료적 이점은 종양 성장의 감소 또는 둔화, 종양 크기(예를 들어, 부피)의 감소, 종양 세포 생존 능력의 감소, 전이성 병변의 수의 감소, 암(예를 들어, HER2-양성 암)의 하나 이상의 징후 또는 증상의 개선 및/또는 환자 생존의 증가를 포함할 수 있다. 일부 실시형태에서, 종양 세포 생존, 종양 성장, 종양 크기 및/또는 전이성 병변의 수는 적어도 약 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 이상 감소된다.
일부 실시형태에서, 항-HER2 이중특이성 단백질은 HER2 활성을 길항한다. 일부 실시형태에서, HER2 활성은 (예를 들어, 적어도 약 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 이상) 저해된다.
본 명세서에 기재된 항-HER2 이중특이성 단백질의 투여 경로는 경구, 복강내, 경피, 피하, 정맥내, 근육내, 경막내, 흡입, 국소, 병변내, 직장, 기관지내, 비강, 경점막, 장, 안구 또는 귀 전달 또는 당업계에 공지된 임의의 다른 방법일 수 있다. 일부 실시형태에서, 항-HER2 이중특이성 단백질은 경구로, 정맥내로 또는 복강내로 투여된다.
VIII. 약제학적 조성물 및 키트
다른 양태에서, 본 개시내용에 따른 항-HER2 이중특이성 단백질을 포함하는 약제학적 조성물 및 키트가 제공된다.
약제학적 조성물
본 개시내용에 사용하기 위한 제형을 제조하기 위한 지침은 당업자에게 공지된 약제학적 제제 및 제형을 위한 임의의 수의 안내서에서 찾을 수 있다.
일부 실시형태에서, 약제학적 조성물은 본 명세서에 기재된 바와 같은 항-HER2 이중특이성 단백질을 포함하고, 하나 이상의 약제학적으로 허용 가능한 담체 및/또는 부형제를 추가로 포함한다. 약제학적으로 허용 가능한 담체는 생리학적으로 양립 가능하며, 활성제의 활성을 방해 또는 그렇지 않으면 저해하지 않는 임의의 용매, 분산 매질 또는 코팅제를 포함한다.
일부 실시형태에서, 이중특이성 단백질은 주사에 의한 비경구 투여용으로 제형화될 수 있다. 전형적으로, 생체내 투여에 사용하기 위한 약제학적 조성물은 멸균, 예를 들어, 가열 멸균, 증기 멸균, 멸균 여과 또는 조사(irradiation)이다.
본 명세서에 기재된 약제학적 조성물의 투여량 및 목적하는 약물 농도는 구상되는 특정 용도에 따라 달라질 수 있다.
키트
일부 실시형태에서, 본 명세서에 기재된 이중특이성 단백질을 포함하는 암(예를 들어, HER2-양성 암)을 치료하는데 사용하기 위한 키트가 제공된다. 일부 실시형태에서, 키트는 하나 이상의 추가적인 치료제를 추가로 포함한다. 예를 들어, 일부 실시형태에서, 키트는 본 명세서에 기재된 바와 같은 이중특이성 단백질을 포함하며, 암의 치료에 사용하기 위한 하나 이상의 추가적인 치료제를 추가로 포함한다. 일부 실시형태에서, 키트는 본 명세서에 기재된 방법의 실행에 대한 지침(즉, 프로토콜)(예를 들어, 이중특이성 단백질을 투여하기 위한 키트를 사용하기 위한 설명서)를 포함하는 지침 자료를 추가로 포함한다. 지침 자료는 전형적으로 서면 또는 인쇄된 자료로 구성되지만, 이러한 것에 제한되는 것은 아니다. 이러한 지침을 저장하고 이를 최종 사용자에게 전달할 수 있는 임의의 매체가 본 개시내용에 의해 상정된다. 이러한 매체는 전자 저장 매체(예를 들어, 자기 디스크, 테이프, 카트리지, 칩), 광학 매체(예를 들어, CD-ROM) 등을 포함하지만 이들로 제한되지 않는다. 이러한 매체는 이러한 지침 자료를 제공하는 인터넷 사이트의 주소를 포함할 수 있다.
IX. 예
본 발명은 구체적인 실시예에 의해 더욱 상세하게 설명될 것이다. 하기 실시예는 단지 예시의 목적으로 제공되며, 어떠한 방식으로도 본 발명을 제한하는 것으로 의도되지 않는다.
실시예 1. 이중특이성 단백질의 생성
인간 HER2의 서브도메인 II 및 인간 HER2의 서브도메인 IV를 표적으로 하기 위해, 본 명세서에 기재되고 도 1 내지 도 5에 도시된 바와 같은 이중특이성 단백질의 구조를 갖는 조작된 단백질을 생성하였다. 일부 작제물에서, Fc 폴리펩타이드의 C-말단 라이신을 제거하였다. 일부 작제물에서, Fd 부분(VH + CH1)을 Fc 폴리펩타이드를 암호화하는 서열을 포함하는 발현 벡터에 클로닝하였다. 일부 실시형태에서, Fc 폴리펩타이드는 TfR-결합 부위를 갖도록 조작하였다. 작제물의 일부 실시형태에서, Fc 폴리펩타이드 중 하나는 TfR-결합 부위 및 "놉"(T366W) 돌연변이(예를 들어, 서열번호 137)를 포함한 반면, 다른 Fc 폴리펩타이드는 "홀"(T366S/L368A/Y407V) 돌연변이(예를 들어, 서열번호 133)를 포함하였다. 추가적으로, Fc 폴리펩타이드 중 하나 또는 둘 모두는 또한 FcγR 결합이 약화된 돌연변이 L234A/L235A를 포함하였다.
벡터를 1:1:2의 놉:홀:경쇄의 비로 상응하는 경쇄 벡터와 함께 ExpiCHO 또는 Expi293 세포에 공동 형질감염시켰다. 발현된 단백질을 단백질 A 칼럼에 상청액을 로딩함으로써 조정 배지(conditioned 배지)로부터 정제하였다. 칼럼을 10 칼럼 부피의 PBS(pH 7.4)로 세척하였다. 단백질을 150mM NaCl을 포함하는 50mM 소듐 시트레이트(pH 3.0)로 용리하고, 즉시 200mM 아르기닌, 137mM 석신산(pH 5.0)으로 중화하였다. 200mM 아르기닌, 137mM 석신산(pH 5.0)을 전개 완충액으로 사용하여 크기-배제 크로마토그래피(SEC)(GE Superdex200)에 의해 단백질을 추가로 정제하였다. 정제된 단백질은 온전한 질량 LC/MS에 의해 확인하였으며, 95% 초과의 순도는 SDS-PAGE 및 분석 HPLC-SEC에 의해 확인하였다. 변형되지 않은 인간 IgG1 불변 영역을 포함하는 항-HER2 이중특이성 단백질을 생성하였다. 아래 표 1은 항-HER2 이중특이성 단백질 및 2개의 대조군 항-HER2 항체의 서열을 제공한다.
실시예 2. 이중특이성 단백질의 Biacore 평가
이중특이성 단백질의 친화도를 Biacore T200 또는 Biacore 8K를 사용하여 SPR에 의해 측정하였다. Biacore™ 시리즈 S CM5 센서 칩을 HER2 친화성 측정을 위한 단일클론 마우스 항-인간 IgG(Fc) 항체 또는 TfR 친화성 측정을 위한 마우스 항-인간 Fab(지이 헬스케어(GE Healthcare)의 인간 항체 또는 Fab 포획 키트)로 고정하였다. 분석물의 연속 3-배 희석액(재조합 HER2 세포외 도메인 또는 재조합 TfR 첨단 도메인)을 30 ㎕/분의 유속으로 주입하였다. HER2 세포외 도메인 결합의 경우 3-분 결합 및 10-분 해리 및 인간 TfR 첨단 도메인 결합의 경우 40-초 결합 및 3-분 해리를 사용하여 각각의 샘플을 분석하였다. 각각 주입 후, 칩은 pH 2.0에서 3M MgCl2 또는 50mM 글리신을 사용하여 재생시켰다. 유사한 밀도에서 관련 없는 IgG를 포획하는 유동 셀에서 RU를 빼서 결합 반응을 수정하였다. 동역학 분석을 위해 kon과 koff의 동시 피팅의 1:1 Languir 모델을 사용하였다. 작제물 "항-HER2_DIV/DII_scFv_1"에 대한 KD는 2.3nM이고, 작제물 "항-HER2_DIV/DII_scFv_2"에 대한 KD는 1.9nM이다. 두 작제물은 아래에 기재되어 있다.
두 작제물 "항-HER2_DIV/DII_scFv_1" 및 "항-HER2_DIV/DII_scFv_2"는 "Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는다. 작제물 "항-HER2_DIV/DII_scFv_1"에서, (a) 서열번호 1의 서열(힌지 영역을 통해 놉 LALA가 있는 CH3C.35.23.4의 N-말단에 융합된 항-HER2DII Fab)을 포함하고, (b) 서열번호 23의 서열(힌지 영역을 통해 홀 돌연변이가 있는 Fc 폴리펩타이드의 N-말단에 융합된 항-HER2DIV scFv)을 포함하며, (c) 서열번호 25의 서열을 포함한다. 작제물 "항-HER2_DIV/DII_scFv_2"에서, (a) 서열번호 5의 서열(힌지 영역을 통해 홀 돌연변이가 있는 Fc 폴리펩타이드의 N-말단에 융합된 항-HER2DII Fab)을 포함하고, (b) 서열번호 24의 서열(힌지 영역을 통해 놉 LALA가 있는 CH3C.35.23.4의 N-말단에 융합된 항-HER2DIV scFv)을 포함하며, (c) 서열번호 25의 서열을 포함한다. 두 작제물에서, scFv 부분은 100번 위치에 Gln에서 Cys로의 치환을 갖는 항-HER2DIV VL 영역(서열번호 115) 및 44번 위치에 Gly에서 Cys로의 치환을 갖는 항-HER2DIV VH 영역(서열번호 113)을 포함한다. 또한, 두 작제물에서, (b)의 힌지 영역은 5번 위치에 Cys에서 Ser로의 돌연변이를 갖는다(EPKSSDKTHTCPPCP(서열번호 129)).
아래 표 2는 항-HER2 이중특이성 단백질의 HER2 결합에 대한 KD 및 TfR 결합에 대한 KD를 추가로 나타낸다.
실시예 3. TfR 및 HER2 서브도메인 II 및 IV의 공동 표적화
BT474 및 OE19와 같은 많은 종양 세포 및 종양 세포주는 HER2 및 TfR을 모두 발현한다. HER2 서브도메인 IV를 표적으로 하는 항체가 일부 HER2+ 세포주에서 종양 세포 성장을 저해하고 종양 세포의 생존 능력을 감소시킬 수 있다는 것은 잘 확립되어 있지만, 본 발명자들은 HER2 서브도메인 IV 및 TfR을 공동 표적화하는 것이 향상된 세포 살해로 이어질지 여부를 이해하고자 하였다.
"Fab-Fc 폴리펩타이드/scFv-Fc 폴리펩타이드" 구조를 갖는 두 작제물을 사용하였다. 작제물 "항-HER2_DIV/DII_scFv_1" 및 작제물 "항-HER2_DIV/DII_scFv_2"는 이전의 실시예에 설명되어 있다.
본 발명자들은 먼저 항-HER2 요법에 민감한 HER2+ 종양 세포주 BT474를 사용하여 성장 저해 검정에서 두 작제물과 대조군 단일클론 항-HER2 항체를 비교하였다. BT474 세포를 96-웰 플레이트에 10,000개 세포/웰로 밤새 플레이팅하고, 166nM(25,000 ng/㎖)에서 시작하는 관심 분자의 1:3 연속 희석액 60㎕로 처리하였다. 배양 배지(RPMI) 및 약물은 제3일에 보충하였다. 제6일에, 세포 성장은 50㎕의 성장 배지에서 5㎕의 WST-1 시약(시그마 알드리치(Sigma Aldrich))을 사용하여 결정하였다. 플레이트를 WST-1 시약의 존재하에 4시간 동안 인큐베이션하고, 440㎚에서 흡광도를 결정하였다. 성장 저해/증식의 백분율을 A440nM을 기준으로 계산하였고, 처리되지 않은 대조군으로 정규화하였다. 도 6a에 도시된 바와 같이, 항-HER2-DIV와 항-HER2-DII의 조합은 대조군에 비해 최대 약 87%의 저해로 BT474 세포 생존 능력을 감소시켰다. 유사하게는, 항-HER2_DIV/DII_scFv_1 및 항-HER2_DIV/DII_scFv_2는 항-HER2-DIV 및 항-HER2-DII와 비교하여 유사한 최대 성장 저해를 보였다(도 6a).
다음으로, 본 발명자들은 두 작제물 및 대조군 단일클론 항-HER2 항체를 항-HER2 치료에 내성이 있는 또 다른 HER2+ 암 세포주 OE19와 비교하였다. 도 6b에 도시된 바와 같이, BT474와 달리, 두 항-HER2_DIV/DII_scFv 작제물 및 항-HER2-DIV와 항-HER2-DII의 조합의 최대 성장 저해 효과 사이에는 차이가 없었으며, OE19 세포주는 항-HER2_DIV/DII_scFv_1과 항-HER2_DIV/DII_scFv_2로 처리 시 약 80%의 최대 저해를 나타낸 반면, 세포는 항-HER2-DIV와 항-HER2-DII의 조합에 대해 최소한으로 반응하였다. 이러한 결과는 HER2 서브도메인 IV, HER2 서브도메인 II 및 TfR를 표적화하는 것이 HER2 서브도메인만을 표적으로 하는 것과 비교하여 항-HER2-저항성 세포주에서 향상된 세포 성장 저해를 초래할 수 있음을 나타낸다. 물론, 세포주가 이미 항-HER2 요법에 민감한 경우 임의의 향상은 차폐될 수 있다.
실시예 4. 항-HER2 이중특이성 단백질의 생체내 약동학 특성
TfR 결합의 부재하에 항-HER2 이중특이성 단백질의 생체내 혈장 약동학을 평가하기 위해, C57BL/6 마우스에 10 ㎎/㎏의 항-HER2 이중특이성 단백질을 정맥내로 투여하였다. 단일 투여 후 30분, 제1일, 제4일 및 제7일에 혈액을 수집하고, 혈장을 처리하여 분석할 때까지 -80℃에서 보관하였다. 혈장 내 이중특이성 단백질의 총 처리 농도는 항-인간 IgG 샌드위치 ELISA(도 7)를 사용하고 표준으로서 적절한 투여 용액을 사용하여 정량화하였다. 플레이트를 항-인간 IgG로 밤새 코팅한 다음, 세척 완충액으로 3회 세척하였다. 표준 및 관련 희석 샘플을 실온에서 2시간 동안 교반하면서 인큐베이션하였다. 인큐베이션 후, 플레이트를 세척 완충액으로 3회 세척하였다. 검출 항체를 차단 완충액에 희석하고, 플레이트를 실온에서 1시간 동안 교반하면서 인큐베이션하였다. 최종 3회 세척 후, 플레이트에 TMB 기질을 첨가하여 발색시키고, 5분 내지 10분 동안 인큐베이션하였다. 반응을 중지시키고, 450nM 흡광도(Biotek 플레이트 판독기)를 사용하여 판독하였다. 모든 항-HER2 이중특이성 단백질이 정상 IgG의 범위 내에서 청소율 값을 나타내었다.
실시예 5. 항-HER2 이중특이성 단백질의 생체내 뇌 흡수
뇌로의 항-HER2 이중특이성 단백질의 생체내 흡수를 평가하기 위해, TfRmu/hu KI 마우스에 50 ㎎/㎏의 항-HER2 이중특이성 단백질을 정맥내로 투여하였다. 투여 후 대략 24시간 후, 심장 천자를 통해 전혈을 EDTA 코팅된 튜브에 수집한 다음, 동물을 얼음 냉각된 PBS로 관류시켰다. 신선한 전혈을 사용하여 임상 혈액 화학 및 망상적혈구 정량화(도 8a)를 평가하였고, 별도의 분취물을 혈장에 대해 처리하였다. 대부분의 항-HER2 이중특이성 단백질은 대조군 처리된 마우스와 비교하여 정상 범위 내의 망상적혈구 값을 나타내었다.
혈장 및 신선한 뇌를 드라이 아이스 위에서 급속 냉동하여 -80℃에서 보관하였다. Qiagen Tissue Lyser II를 사용하여 프로테이스와 포스파테이스 저해제가 포함된 PBS 중 조직 중량 1% NP40 완충액으로 10x 부피로 뇌를 균질화하고; 상청액을 -80℃에서 보관하였다. 항-HER2 이중특이성 단백질의 혈장(도 8b) 및 뇌 용해물(도 8c) 농도를 샌드위치 ELISA를 사용하여 정량화하였다. 혈장 농도는 예상되는 TfR-매개성 약물 소인을 나타내었고; 항-HER2 이중특이성 단백질의 뇌 농도는 뇌에서 대략 15nM 내지 52nM의 범위였으며, 이는 이들 분자가 혈액-뇌 장벽의 TfR에 결합하여 뇌로 수송되는 능력을 입증한다. 뇌-대-혈장 농도의 결과 백분율은 대략 1% 내지 2%였으며(도 8d), TfR 또는 다른 수용체-매개성 통과세포외배출 표적화가 결여된 항체에 대해 예상되는 것보다 대략 10-배 더 높았다. 이러한 데이터는 본 명세서에 기재된 바와 같은 상이한 구조의 수많은 항-HER2 이중특이성 단백질이 뇌를 침투함을 입증하고 뒷받침한다.
실시예 6. 항-HER2 이중특이성 단백질의 시험관내 성장 저해
항-HER2 이중특이성 단백질 및 기존의 항-HER2 요법의 시험관내 성장 저해 효능을 항-HER2 요법에 민감한 다양한 HER2+ 종양 세포주(BT474(도 9a 내지 도 9f), OE19(도 9g 내지 도 9i) 및 ZR75(도 9j 내지 도 9l))로 평가하였다. 종양 세포를 96-웰 플레이트에 10,000개 세포/웰로 밤새 플레이팅하고, 166nM(25,000개 ng/㎖)에서 시작하는 관심 분자의 1:3 연속 희석액 60㎕로 처리하였다. 배양 배지(RPMI) 및 약물을 제3일에 보충하였다. 뉴레굴린 1(neuregulin 1: NRG1) 처리된 BT474-그룹(도 9d 내지 도 9f)의 경우, 세포를 50 ng/㎖의 NRG1의 존재하에 인큐베이션하였다. 제6일에, 50㎕의 성장 배지에서 5㎕의 WST-1 시약(시그마 알드리치)을 사용하여 세포 성장을 결정하였다. 플레이트를 WST-1 시약의 존재하에 4시간 동안 인큐베이션하고, 흡광도를 440㎚에서 결정하였다. 성장 저해/증식의 백분율은 A440nM을 기준으로 계산하였고, 처리되지 않은 대조군으로 정규화하였다. 아래 표 3은 세 가지 상이한 HER2+ 세포주에서 항-HER2 이중특이성 단백질 및 항-HER2 대조군의 성장 저해 효능을 추가로 보여준다. 도 9a 내지 도 9l 및 표 3은 전체 항-HER2 이중특이성 단백질이 야생형 Fc를 사용한 항-HER2DIV 대조군 및 항-HER2DII 대조군과 동등하거나 또는 우수한 성장 저해를 나타낸다는 것을 보여준다. 소정의 항-HER2 이중특이성 단백질을 갖는 일부 세포주에서, 성장 저해는 야생형 Fc를 사용한 항-HER2DIV 대조군 또는 항-HER2DII 대조군과 비교하여 감소되었으며, 이는 아마도 소정의 배열에서 결합 부위에 대한 경쟁으로 인한 것일 수 있다.
SEQUENCE LISTING
<110> DENALI THERAPEUTICS INC.
<120> ENGINEERED ANTI-HER2 BISPECIFIC PROTEINS
<130> 102342-004110PC-1234487
<140> PCT/US2021/018705
<141> 2021-02-19
<150> US 62/978,758
<151> 2020-02-19
<160> 158
<170> PatentIn version 3.5
<210> 1
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 1
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 2
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 2
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 3
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 3
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 4
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 4
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 5
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 5
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 6
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 6
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 7
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 7
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 8
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 8
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 9
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 9
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 10
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 10
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 11
<211> 483
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 11
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser
245 250 255
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
260 265 270
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
275 280 285
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
290 295 300
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
305 310 315 320
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
325 330 335
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
340 345 350
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
355 360 365
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
370 375 380
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
385 390 395 400
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
405 410 415
Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro
420 425 430
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
435 440 445
Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met
450 455 460
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
465 470 475 480
Pro Gly Lys
<210> 12
<211> 483
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 12
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr
180 185 190
Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser
245 250 255
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
260 265 270
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
275 280 285
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
290 295 300
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
305 310 315 320
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
325 330 335
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
340 345 350
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
355 360 365
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
370 375 380
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
385 390 395 400
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
405 410 415
Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro
420 425 430
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
435 440 445
Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met
450 455 460
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
465 470 475 480
Pro Gly Lys
<210> 13
<211> 488
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 13
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
260 265 270
Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
275 280 285
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
290 295 300
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
305 310 315 320
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
325 330 335
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
340 345 350
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
355 360 365
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
370 375 380
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
385 390 395 400
Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser
405 410 415
Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr
420 425 430
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val
435 440 445
Ser Lys Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe
450 455 460
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
465 470 475 480
Ser Leu Ser Leu Ser Pro Gly Lys
485
<210> 14
<211> 488
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 14
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
260 265 270
Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
275 280 285
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
290 295 300
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
305 310 315 320
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
325 330 335
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
340 345 350
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
355 360 365
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
370 375 380
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
385 390 395 400
Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser
405 410 415
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
420 425 430
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
435 440 445
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
450 455 460
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
465 470 475 480
Ser Leu Ser Leu Ser Pro Gly Lys
485
<210> 15
<211> 483
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 15
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser
245 250 255
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
260 265 270
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
275 280 285
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
290 295 300
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
305 310 315 320
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
325 330 335
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
340 345 350
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
355 360 365
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
370 375 380
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
385 390 395 400
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
405 410 415
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
420 425 430
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
435 440 445
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
450 455 460
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
465 470 475 480
Pro Gly Lys
<210> 16
<211> 483
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 16
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser
245 250 255
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
260 265 270
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
275 280 285
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
290 295 300
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
305 310 315 320
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
325 330 335
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
340 345 350
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
355 360 365
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
370 375 380
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
385 390 395 400
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
405 410 415
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
420 425 430
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
435 440 445
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
450 455 460
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
465 470 475 480
Pro Gly Lys
<210> 17
<211> 483
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 17
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr
180 185 190
Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser
245 250 255
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
260 265 270
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
275 280 285
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
290 295 300
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
305 310 315 320
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
325 330 335
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
340 345 350
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
355 360 365
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
370 375 380
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
385 390 395 400
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
405 410 415
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
420 425 430
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
435 440 445
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
450 455 460
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
465 470 475 480
Pro Gly Lys
<210> 18
<211> 484
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 18
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
245 250 255
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
260 265 270
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
275 280 285
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
290 295 300
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
305 310 315 320
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
325 330 335
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
340 345 350
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
355 360 365
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
370 375 380
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
385 390 395 400
Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
405 410 415
Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro
420 425 430
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
435 440 445
Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val
450 455 460
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
465 470 475 480
Ser Pro Gly Lys
<210> 19
<211> 489
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 19
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
260 265 270
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
275 280 285
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
290 295 300
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
305 310 315 320
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
325 330 335
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
340 345 350
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
355 360 365
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
370 375 380
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
385 390 395 400
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
405 410 415
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn
420 425 430
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
435 440 445
Val Ser Lys Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val
450 455 460
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
465 470 475 480
Lys Ser Leu Ser Leu Ser Pro Gly Lys
485
<210> 20
<211> 489
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 20
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
260 265 270
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
275 280 285
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
290 295 300
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
305 310 315 320
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
325 330 335
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
340 345 350
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
355 360 365
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
370 375 380
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
385 390 395 400
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
405 410 415
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
420 425 430
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
435 440 445
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
450 455 460
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
465 470 475 480
Lys Ser Leu Ser Leu Ser Pro Gly Lys
485
<210> 21
<211> 484
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 21
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
245 250 255
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
260 265 270
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
275 280 285
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
290 295 300
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
305 310 315 320
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
325 330 335
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
340 345 350
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
355 360 365
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
370 375 380
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
385 390 395 400
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
405 410 415
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
420 425 430
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
435 440 445
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
450 455 460
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
465 470 475 480
Ser Pro Gly Lys
<210> 22
<211> 484
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 22
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
245 250 255
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
260 265 270
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
275 280 285
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
290 295 300
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
305 310 315 320
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
325 330 335
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
340 345 350
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
355 360 365
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
370 375 380
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
385 390 395 400
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
405 410 415
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
420 425 430
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
435 440 445
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
450 455 460
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
465 470 475 480
Ser Pro Gly Lys
<210> 23
<211> 484
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 23
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
245 250 255
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
260 265 270
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
275 280 285
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
290 295 300
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
305 310 315 320
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
325 330 335
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
340 345 350
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
355 360 365
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
370 375 380
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
385 390 395 400
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
405 410 415
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
420 425 430
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
435 440 445
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
450 455 460
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
465 470 475 480
Ser Pro Gly Lys
<210> 24
<211> 484
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 24
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
245 250 255
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
260 265 270
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
275 280 285
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
290 295 300
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
305 310 315 320
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
325 330 335
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
340 345 350
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
355 360 365
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
370 375 380
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
385 390 395 400
Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
405 410 415
Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro
420 425 430
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
435 440 445
Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val
450 455 460
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
465 470 475 480
Ser Pro Gly Lys
<210> 25
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 26
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 26
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 27
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
450 455 460
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
465 470 475 480
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
485 490 495
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
500 505 510
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
515 520 525
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
530 535 540
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly
545 550 555 560
Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly
565 570 575
Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val Glu
580 585 590
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
595 600 605
Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg
610 615 620
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr
625 630 635 640
Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile
645 650 655
Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu
660 665 670
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp
675 680 685
Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
690 695 700
Ser Ser
705
<210> 28
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 28
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
450 455 460
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
465 470 475 480
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
485 490 495
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro
500 505 510
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
515 520 525
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
530 535 540
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
545 550 555 560
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
565 570 575
Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
580 585 590
Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr Gln Ser Pro Ser
595 600 605
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
610 615 620
Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly
625 630 635 640
Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly
645 650 655
Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu
660 665 670
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
675 680 685
Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu
690 695 700
Ile Lys
705
<210> 29
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 29
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
450 455 460
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
465 470 475 480
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
485 490 495
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
500 505 510
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
515 520 525
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
530 535 540
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly
545 550 555 560
Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly
565 570 575
Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val Glu
580 585 590
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
595 600 605
Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg
610 615 620
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr
625 630 635 640
Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile
645 650 655
Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu
660 665 670
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp
675 680 685
Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
690 695 700
Ser Ser
705
<210> 30
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 30
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
450 455 460
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
465 470 475 480
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
485 490 495
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
500 505 510
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
515 520 525
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
530 535 540
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly
545 550 555 560
Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly
565 570 575
Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val Glu
580 585 590
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
595 600 605
Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg
610 615 620
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr
625 630 635 640
Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile
645 650 655
Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu
660 665 670
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp
675 680 685
Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
690 695 700
Ser Ser
705
<210> 31
<211> 705
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 31
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
450 455 460
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
465 470 475 480
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
485 490 495
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
500 505 510
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
515 520 525
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
530 535 540
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly Thr
545 550 555 560
Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
565 570 575
Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val Glu Ser
580 585 590
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
595 600 605
Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln
610 615 620
Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn
625 630 635 640
Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
645 650 655
Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg
660 665 670
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly
675 680 685
Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
690 695 700
Ser
705
<210> 32
<211> 705
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 32
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
450 455 460
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
465 470 475 480
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
485 490 495
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
500 505 510
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
515 520 525
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
530 535 540
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly Thr
545 550 555 560
Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
565 570 575
Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val Glu Ser
580 585 590
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
595 600 605
Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln
610 615 620
Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn
625 630 635 640
Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
645 650 655
Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg
660 665 670
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly
675 680 685
Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
690 695 700
Ser
705
<210> 33
<211> 707
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 33
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
450 455 460
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
465 470 475 480
Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp
485 490 495
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala
500 505 510
Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
515 520 525
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
530 535 540
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly
545 550 555 560
Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly
565 570 575
Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu
580 585 590
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
595 600 605
Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp Trp
610 615 620
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val Asn
625 630 635 640
Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg Phe
645 650 655
Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
660 665 670
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn Leu
675 680 685
Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
690 695 700
Val Ser Ser
705
<210> 34
<211> 707
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 34
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln
450 455 460
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg
465 470 475 480
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp
485 490 495
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val
500 505 510
Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg
515 520 525
Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met
530 535 540
Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn
545 550 555 560
Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
565 570 575
Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly
580 585 590
Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr Gln Ser Pro
595 600 605
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys
610 615 620
Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln Gln Lys Pro
625 630 635 640
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr
645 650 655
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
660 665 670
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
675 680 685
Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val
690 695 700
Glu Ile Lys
705
<210> 35
<211> 707
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 35
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
450 455 460
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
465 470 475 480
Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp
485 490 495
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala
500 505 510
Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
515 520 525
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
530 535 540
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly
545 550 555 560
Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly
565 570 575
Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu
580 585 590
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
595 600 605
Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp Trp
610 615 620
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val Asn
625 630 635 640
Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg Phe
645 650 655
Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
660 665 670
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn Leu
675 680 685
Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
690 695 700
Val Ser Ser
705
<210> 36
<211> 707
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 36
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
450 455 460
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
465 470 475 480
Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp
485 490 495
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala
500 505 510
Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
515 520 525
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
530 535 540
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly
545 550 555 560
Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly
565 570 575
Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu
580 585 590
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
595 600 605
Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp Trp
610 615 620
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val Asn
625 630 635 640
Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg Phe
645 650 655
Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
660 665 670
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn Leu
675 680 685
Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
690 695 700
Val Ser Ser
705
<210> 37
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 37
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
450 455 460
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
465 470 475 480
Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr
485 490 495
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser
500 505 510
Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
515 520 525
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
530 535 540
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln
545 550 555 560
Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly
565 570 575
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val
580 585 590
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
595 600 605
Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp Trp Val
610 615 620
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val Asn Pro
625 630 635 640
Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg Phe Thr
645 650 655
Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
660 665 670
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn Leu Gly
675 680 685
Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
690 695 700
Ser Ser
705
<210> 38
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 38
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
450 455 460
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
465 470 475 480
Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr
485 490 495
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser
500 505 510
Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
515 520 525
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
530 535 540
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln
545 550 555 560
Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly
565 570 575
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val
580 585 590
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
595 600 605
Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp Trp Val
610 615 620
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val Asn Pro
625 630 635 640
Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg Phe Thr
645 650 655
Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
660 665 670
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn Leu Gly
675 680 685
Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
690 695 700
Ser Ser
705
<210> 39
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 39
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
450 455 460
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
465 470 475 480
Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp Trp
485 490 495
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val Asn
500 505 510
Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg Phe
515 520 525
Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
530 535 540
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn Leu
545 550 555 560
Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
565 570 575
Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
580 585 590
Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr Gln Ser Pro Ser
595 600 605
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala
610 615 620
Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln Gln Lys Pro Gly
625 630 635 640
Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly
645 650 655
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
660 665 670
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
675 680 685
Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu
690 695 700
Ile Lys
705
<210> 40
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 40
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
260 265 270
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
275 280 285
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
290 295 300
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
305 310 315 320
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
325 330 335
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
660 665 670
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 41
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 41
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
260 265 270
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
275 280 285
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
290 295 300
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
305 310 315 320
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
325 330 335
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
660 665 670
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 42
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 42
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
260 265 270
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
275 280 285
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
290 295 300
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
305 310 315 320
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
325 330 335
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 43
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 43
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
260 265 270
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
275 280 285
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
290 295 300
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
305 310 315 320
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
325 330 335
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 44
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 44
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
260 265 270
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
275 280 285
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
290 295 300
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
305 310 315 320
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
325 330 335
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 45
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 45
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
260 265 270
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
275 280 285
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
290 295 300
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
305 310 315 320
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
325 330 335
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
340 345 350
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
660 665 670
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 46
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 46
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr
180 185 190
Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
260 265 270
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
275 280 285
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
290 295 300
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
305 310 315 320
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
325 330 335
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
340 345 350
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
660 665 670
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 47
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 47
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 48
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 48
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
260 265 270
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
275 280 285
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
290 295 300
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
305 310 315 320
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
325 330 335
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
340 345 350
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 49
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 49
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
260 265 270
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
275 280 285
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
290 295 300
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
305 310 315 320
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
325 330 335
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
340 345 350
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 50
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 50
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
260 265 270
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
275 280 285
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
290 295 300
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
305 310 315 320
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
325 330 335
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
340 345 350
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 51
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 51
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr
180 185 190
Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
260 265 270
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
275 280 285
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
290 295 300
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
305 310 315 320
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
325 330 335
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
340 345 350
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 52
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 52
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
210 215 220
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
225 230 235 240
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr
245 250 255
Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
260 265 270
Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser
275 280 285
Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
290 295 300
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro
305 310 315 320
Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly
325 330 335
Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly
340 345 350
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
355 360 365
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
370 375 380
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
385 390 395 400
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
405 410 415
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
420 425 430
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
435 440 445
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
450 455 460
Gly Thr Leu Val Thr Val Ser Ser
465 470
<210> 53
<211> 470
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 53
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
210 215 220
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
225 230 235 240
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
245 250 255
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
260 265 270
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
275 280 285
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
290 295 300
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
305 310 315 320
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
325 330 335
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
340 345 350
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
355 360 365
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
370 375 380
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
385 390 395 400
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
405 410 415
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
420 425 430
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
435 440 445
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
450 455 460
Leu Val Thr Val Ser Ser
465 470
<210> 54
<211> 470
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 54
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
210 215 220
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
225 230 235 240
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
245 250 255
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
260 265 270
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
275 280 285
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
290 295 300
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
305 310 315 320
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
325 330 335
Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly
340 345 350
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr
355 360 365
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
370 375 380
Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln
385 390 395 400
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr
405 410 415
Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
420 425 430
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
435 440 445
Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly
450 455 460
Thr Lys Val Glu Ile Lys
465 470
<210> 55
<211> 471
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 55
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
145 150 155 160
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
210 215 220
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
245 250 255
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
260 265 270
Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile
275 280 285
Gly Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
290 295 300
Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser
305 310 315 320
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
325 330 335
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro
340 345 350
Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
355 360 365
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
370 375 380
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
385 390 395 400
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
405 410 415
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
420 425 430
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
435 440 445
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
450 455 460
Ser Phe Asn Arg Gly Glu Cys
465 470
<210> 56
<211> 470
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 56
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr
145 150 155 160
Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
165 170 175
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys
180 185 190
Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
260 265 270
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
275 280 285
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
290 295 300
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
305 310 315 320
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
325 330 335
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
340 345 350
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
355 360 365
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
370 375 380
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
385 390 395 400
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
405 410 415
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
420 425 430
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
435 440 445
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
450 455 460
Phe Asn Arg Gly Glu Cys
465 470
<210> 57
<211> 470
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 57
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr
180 185 190
Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
260 265 270
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
275 280 285
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
290 295 300
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
305 310 315 320
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
325 330 335
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
340 345 350
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
355 360 365
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
370 375 380
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
385 390 395 400
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
405 410 415
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
420 425 430
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
435 440 445
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
450 455 460
Phe Asn Arg Gly Glu Cys
465 470
<210> 58
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 58
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
145 150 155 160
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
165 170 175
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
180 185 190
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
530 535 540
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 59
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 59
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
145 150 155 160
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
165 170 175
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
180 185 190
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
530 535 540
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 60
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 60
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
145 150 155 160
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
165 170 175
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
180 185 190
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 61
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 61
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
145 150 155 160
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
165 170 175
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
180 185 190
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 62
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 62
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp
145 150 155 160
Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
165 170 175
Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg
180 185 190
Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 63
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 63
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
530 535 540
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 64
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 64
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
530 535 540
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 65
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 65
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 66
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 66
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 67
<211> 578
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 67
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
245 250 255
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
260 265 270
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
275 280 285
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
290 295 300
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
305 310 315 320
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
325 330 335
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
340 345 350
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
385 390 395 400
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
465 470 475 480
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
565 570 575
Gly Lys
<210> 68
<211> 565
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 68
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
130 135 140
Phe Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr
165 170 175
Asn Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys
180 185 190
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr
210 215 220
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
225 230 235 240
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
245 250 255
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
260 265 270
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
275 280 285
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
290 295 300
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
305 310 315 320
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
325 330 335
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
340 345 350
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
355 360 365
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
370 375 380
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
385 390 395 400
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
405 410 415
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
420 425 430
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
435 440 445
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
450 455 460
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
465 470 475 480
Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
485 490 495
Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr
500 505 510
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
515 520 525
Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser
530 535 540
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
545 550 555 560
Leu Ser Pro Gly Lys
565
<210> 69
<211> 565
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 69
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
130 135 140
Phe Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr
165 170 175
Asn Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys
180 185 190
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr
210 215 220
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
225 230 235 240
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
245 250 255
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
260 265 270
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
275 280 285
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
290 295 300
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
305 310 315 320
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
325 330 335
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
340 345 350
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
355 360 365
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
370 375 380
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
385 390 395 400
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
405 410 415
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
420 425 430
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
435 440 445
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
450 455 460
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
465 470 475 480
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
485 490 495
Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr
500 505 510
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
515 520 525
Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser
530 535 540
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
545 550 555 560
Leu Ser Pro Gly Lys
565
<210> 70
<211> 565
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 70
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
130 135 140
Phe Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr
165 170 175
Asn Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys
180 185 190
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr
210 215 220
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
225 230 235 240
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
245 250 255
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
260 265 270
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
275 280 285
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
290 295 300
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
305 310 315 320
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
325 330 335
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
340 345 350
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
355 360 365
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
370 375 380
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
385 390 395 400
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
405 410 415
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
420 425 430
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
435 440 445
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
450 455 460
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
465 470 475 480
Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
485 490 495
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
500 505 510
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
515 520 525
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
530 535 540
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
545 550 555 560
Leu Ser Pro Gly Lys
565
<210> 71
<211> 565
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 71
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
130 135 140
Phe Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr
165 170 175
Asn Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys
180 185 190
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr
210 215 220
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
225 230 235 240
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
245 250 255
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
260 265 270
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
275 280 285
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
290 295 300
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
305 310 315 320
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
325 330 335
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
340 345 350
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
355 360 365
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
370 375 380
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
385 390 395 400
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
405 410 415
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
420 425 430
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
435 440 445
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
450 455 460
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
465 470 475 480
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
485 490 495
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
500 505 510
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
515 520 525
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
530 535 540
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
545 550 555 560
Leu Ser Pro Gly Lys
565
<210> 72
<211> 565
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 72
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
130 135 140
Phe Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr
165 170 175
Asn Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys
180 185 190
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr
210 215 220
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
225 230 235 240
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
245 250 255
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
260 265 270
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
275 280 285
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
290 295 300
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
305 310 315 320
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
325 330 335
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
340 345 350
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
355 360 365
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
370 375 380
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
385 390 395 400
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
405 410 415
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
420 425 430
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
435 440 445
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
450 455 460
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
465 470 475 480
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
485 490 495
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
500 505 510
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
515 520 525
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
530 535 540
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
545 550 555 560
Leu Ser Pro Gly Lys
565
<210> 73
<211> 566
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 73
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn
130 135 140
Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr
165 170 175
Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys
180 185 190
Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp
210 215 220
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
225 230 235 240
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
245 250 255
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
260 265 270
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
275 280 285
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
290 295 300
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
305 310 315 320
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
325 330 335
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
340 345 350
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
355 360 365
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
370 375 380
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
385 390 395 400
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
405 410 415
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
420 425 430
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
435 440 445
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
450 455 460
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
465 470 475 480
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
485 490 495
Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr
500 505 510
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
515 520 525
Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys
530 535 540
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
545 550 555 560
Ser Leu Ser Pro Gly Lys
565
<210> 74
<211> 566
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 74
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn
130 135 140
Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr
165 170 175
Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys
180 185 190
Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp
210 215 220
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
225 230 235 240
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
245 250 255
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
260 265 270
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
275 280 285
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
290 295 300
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
305 310 315 320
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
325 330 335
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
340 345 350
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
355 360 365
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
370 375 380
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
385 390 395 400
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
405 410 415
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
420 425 430
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
435 440 445
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
450 455 460
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
465 470 475 480
Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile
485 490 495
Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr
500 505 510
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys
515 520 525
Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys
530 535 540
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
545 550 555 560
Ser Leu Ser Pro Gly Lys
565
<210> 75
<211> 566
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 75
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn
130 135 140
Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr
165 170 175
Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys
180 185 190
Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp
210 215 220
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
225 230 235 240
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
245 250 255
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
260 265 270
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
275 280 285
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
290 295 300
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
305 310 315 320
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
325 330 335
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
340 345 350
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
355 360 365
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
370 375 380
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
385 390 395 400
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
405 410 415
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
420 425 430
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
435 440 445
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
450 455 460
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
465 470 475 480
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
485 490 495
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
500 505 510
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
515 520 525
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
530 535 540
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
545 550 555 560
Ser Leu Ser Pro Gly Lys
565
<210> 76
<211> 566
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 76
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn
130 135 140
Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr
165 170 175
Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys
180 185 190
Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp
210 215 220
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
225 230 235 240
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
245 250 255
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
260 265 270
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
275 280 285
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
290 295 300
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
305 310 315 320
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
325 330 335
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
340 345 350
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
355 360 365
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
370 375 380
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
385 390 395 400
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
405 410 415
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
420 425 430
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
435 440 445
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
450 455 460
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
465 470 475 480
Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile
485 490 495
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
500 505 510
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys
515 520 525
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
530 535 540
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
545 550 555 560
Ser Leu Ser Pro Gly Lys
565
<210> 77
<211> 566
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 77
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Ala Ser Thr Lys Gly
100 105 110
Pro Ser Val Phe Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
115 120 125
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn
130 135 140
Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly
145 150 155 160
Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr
165 170 175
Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys
180 185 190
Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp
210 215 220
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
225 230 235 240
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
245 250 255
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
260 265 270
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
275 280 285
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
290 295 300
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
305 310 315 320
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
325 330 335
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
340 345 350
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
355 360 365
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
370 375 380
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
385 390 395 400
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
405 410 415
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
420 425 430
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
435 440 445
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
450 455 460
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
465 470 475 480
Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile
485 490 495
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
500 505 510
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys
515 520 525
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
530 535 540
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
545 550 555 560
Ser Leu Ser Pro Gly Lys
565
<210> 78
<211> 331
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 78
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln
130 135 140
Asp Val Ser Ile Gly Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr
195 200 205
Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
210 215 220
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
225 230 235 240
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
245 250 255
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
260 265 270
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
275 280 285
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
290 295 300
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
305 310 315 320
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330
<210> 79
<211> 331
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 79
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
210 215 220
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
225 230 235 240
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
245 250 255
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
260 265 270
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
275 280 285
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
290 295 300
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
305 310 315 320
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330
<210> 80
<211> 344
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 80
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Arg Thr Val Ala Ala Pro Ser Val
115 120 125
Phe Ile Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
130 135 140
Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser
145 150 155 160
Ile Gly Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
165 170 175
Leu Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe
180 185 190
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
195 200 205
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr
210 215 220
Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val
225 230 235 240
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys
245 250 255
Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg
260 265 270
Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn
275 280 285
Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser
290 295 300
Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys
305 310 315 320
Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
325 330 335
Lys Ser Phe Asn Arg Gly Glu Cys
340
<210> 81
<211> 343
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 81
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Arg Thr Val Ala Ala Pro Ser Val Phe
115 120 125
Ile Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
130 135 140
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr
145 150 155 160
Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
165 170 175
Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser
180 185 190
Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
195 200 205
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro
210 215 220
Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
225 230 235 240
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
245 250 255
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
260 265 270
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
275 280 285
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
290 295 300
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
305 310 315 320
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
325 330 335
Ser Phe Asn Arg Gly Glu Cys
340
<210> 82
<211> 580
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 82
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
450 455 460
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
465 470 475 480
Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp
485 490 495
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr
500 505 510
Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe
515 520 525
Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn
530 535 540
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly
545 550 555 560
Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
565 570 575
Thr Val Ser Ser
580
<210> 83
<211> 586
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 83
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
465 470 475 480
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
485 490 495
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
500 505 510
Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp
515 520 525
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
530 535 540
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
545 550 555 560
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
565 570 575
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 84
<211> 586
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 84
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
465 470 475 480
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
485 490 495
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
500 505 510
Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp
515 520 525
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
530 535 540
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
545 550 555 560
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
565 570 575
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 85
<211> 586
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 85
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
465 470 475 480
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
485 490 495
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
500 505 510
Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp
515 520 525
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
530 535 540
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
545 550 555 560
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
565 570 575
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 86
<211> 579
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 86
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
450 455 460
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
465 470 475 480
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
485 490 495
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro
500 505 510
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
515 520 525
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
530 535 540
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
545 550 555 560
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
565 570 575
Val Ser Ser
<210> 87
<211> 579
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 87
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
450 455 460
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
465 470 475 480
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
485 490 495
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro
500 505 510
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
515 520 525
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
530 535 540
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
545 550 555 560
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
565 570 575
Val Ser Ser
<210> 88
<211> 585
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 88
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
450 455 460
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
465 470 475 480
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp
485 490 495
Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
500 505 510
Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser
515 520 525
Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala
530 535 540
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
545 550 555 560
Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly
565 570 575
Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 89
<211> 580
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 89
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln
450 455 460
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg
465 470 475 480
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp
485 490 495
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val
500 505 510
Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg
515 520 525
Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met
530 535 540
Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn
545 550 555 560
Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
565 570 575
Thr Val Ser Ser
580
<210> 90
<211> 585
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 90
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
1 5 10 15
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
20 25 30
Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
35 40 45
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
85 90 95
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
465 470 475 480
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr
485 490 495
Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
500 505 510
Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln
515 520 525
Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr
530 535 540
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
545 550 555 560
Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly
565 570 575
Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 91
<211> 586
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 91
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly
450 455 460
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
465 470 475 480
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
485 490 495
Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
500 505 510
Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn
515 520 525
Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn
530 535 540
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
545 550 555 560
Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp
565 570 575
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 92
<211> 586
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 92
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly
450 455 460
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
465 470 475 480
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
485 490 495
Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
500 505 510
Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn
515 520 525
Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn
530 535 540
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
545 550 555 560
Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp
565 570 575
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 93
<211> 586
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 93
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly
450 455 460
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
465 470 475 480
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
485 490 495
Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
500 505 510
Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn
515 520 525
Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn
530 535 540
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
545 550 555 560
Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp
565 570 575
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 94
<211> 586
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 94
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly
450 455 460
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
465 470 475 480
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
485 490 495
Thr Asp Tyr Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
500 505 510
Glu Trp Val Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn
515 520 525
Gln Arg Phe Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn
530 535 540
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
545 550 555 560
Tyr Tyr Cys Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp
565 570 575
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
580 585
<210> 95
<211> 567
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 95
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
450 455 460
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
465 470 475 480
Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr
485 490 495
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser
500 505 510
Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly
515 520 525
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
530 535 540
Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln
545 550 555 560
Gly Thr Lys Val Glu Ile Lys
565
<210> 96
<211> 573
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 96
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
465 470 475 480
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn
485 490 495
Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
500 505 510
Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe
515 520 525
Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
530 535 540
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr
545 550 555 560
Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
565 570
<210> 97
<211> 573
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 97
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser Lys
405 410 415
Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
465 470 475 480
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn
485 490 495
Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
500 505 510
Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe
515 520 525
Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
530 535 540
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr
545 550 555 560
Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
565 570
<210> 98
<211> 573
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 98
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
465 470 475 480
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn
485 490 495
Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
500 505 510
Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe
515 520 525
Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
530 535 540
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr
545 550 555 560
Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
565 570
<210> 99
<211> 566
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 99
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
450 455 460
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
465 470 475 480
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
485 490 495
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
500 505 510
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
515 520 525
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
530 535 540
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly
545 550 555 560
Thr Lys Val Glu Ile Lys
565
<210> 100
<211> 566
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 100
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
450 455 460
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
465 470 475 480
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
485 490 495
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
500 505 510
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
515 520 525
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
530 535 540
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly
545 550 555 560
Thr Lys Val Glu Ile Lys
565
<210> 101
<211> 572
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 101
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
450 455 460
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
465 470 475 480
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr
485 490 495
Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
500 505 510
Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser
515 520 525
Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
530 535 540
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro
545 550 555 560
Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
565 570
<210> 102
<211> 568
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 102
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
450 455 460
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
465 470 475 480
Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp
485 490 495
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala
500 505 510
Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
515 520 525
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
530 535 540
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly
545 550 555 560
Gln Gly Thr Lys Val Glu Ile Lys
565
<210> 103
<211> 568
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 103
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Tyr Gly Thr Glu Trp Ser Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Ser
405 410 415
Lys Glu Glu Trp Gln Gln Gly Phe Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
450 455 460
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
465 470 475 480
Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp
485 490 495
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala
500 505 510
Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
515 520 525
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
530 535 540
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly
545 550 555 560
Gln Gly Thr Lys Val Glu Ile Lys
565
<210> 104
<211> 568
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 104
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
450 455 460
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
465 470 475 480
Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp
485 490 495
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala
500 505 510
Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
515 520 525
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
530 535 540
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly
545 550 555 560
Gln Gly Thr Lys Val Glu Ile Lys
565
<210> 105
<211> 567
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 105
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
450 455 460
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
465 470 475 480
Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr
485 490 495
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser
500 505 510
Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
515 520 525
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
530 535 540
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln
545 550 555 560
Gly Thr Lys Val Glu Ile Lys
565
<210> 106
<211> 567
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 106
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
450 455 460
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
465 470 475 480
Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr
485 490 495
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser
500 505 510
Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
515 520 525
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
530 535 540
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln
545 550 555 560
Gly Thr Lys Val Glu Ile Lys
565
<210> 107
<211> 573
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 107
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
465 470 475 480
Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser
485 490 495
Ile Gly Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
500 505 510
Leu Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe
515 520 525
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
530 535 540
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr
545 550 555 560
Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
565 570
<210> 108
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 108
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 109
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 109
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 110
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 110
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 111
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 111
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 112
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 112
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 113
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 113
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 114
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 114
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
100 105
<210> 115
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 115
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
100 105
<210> 116
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 116
Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Ser Gly
20
<210> 117
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 117
Gly Gly Gly Gly Ser
1 5
<210> 118
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 118
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 119
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 119
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 120
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 120
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
1 5 10
<210> 121
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 121
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
1 5 10
<210> 122
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 122
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 123
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 123
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
1 5 10 15
Ser
<210> 124
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 124
Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser
1 5 10
<210> 125
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 125
Ala Ser Thr Lys Gly Pro Ser Val Phe
1 5
<210> 126
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 126
Arg Thr Val Ala Ala Pro Ser Val Phe Ile
1 5 10
<210> 127
<211> 15
<212> PRT
<213> Homo sapiens
<400> 127
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 128
<211> 10
<212> PRT
<213> Homo sapiens
<400> 128
Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10
<210> 129
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 129
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 130
<211> 217
<212> PRT
<213> Homo sapiens
<400> 130
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 131
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 131
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 132
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 132
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 133
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 133
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 134
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 134
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 135
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 135
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 136
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 136
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 137
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 137
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 138
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 138
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 139
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 139
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ser Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Ser Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 140
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 140
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ala Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 141
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 141
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ala Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 142
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 142
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ala Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 143
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 143
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ala Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 144
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 144
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Tyr Gly Thr Glu Trp Ala Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 145
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 145
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Phe Gly Thr Glu Trp Ser Ser
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 146
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 146
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Phe Gly Thr Glu Trp Ser Ser
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 147
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 147
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Phe Gly Thr Glu Trp Ser Ser
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 148
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 148
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Phe Gly Thr Glu Trp Ser Ser
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 149
<211> 217
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 149
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
115 120 125
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ala Val Glu Trp Glu Ser Phe Gly Thr Glu Trp Ser Ser
145 150 155 160
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Val Ser Lys Leu Thr Val Thr Lys Glu Glu Trp Gln Gln Gly Phe Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 150
<211> 760
<212> PRT
<213> Homo sapiens
<400> 150
Met Met Asp Gln Ala Arg Ser Ala Phe Ser Asn Leu Phe Gly Gly Glu
1 5 10 15
Pro Leu Ser Tyr Thr Arg Phe Ser Leu Ala Arg Gln Val Asp Gly Asp
20 25 30
Asn Ser His Val Glu Met Lys Leu Ala Val Asp Glu Glu Glu Asn Ala
35 40 45
Asp Asn Asn Thr Lys Ala Asn Val Thr Lys Pro Lys Arg Cys Ser Gly
50 55 60
Ser Ile Cys Tyr Gly Thr Ile Ala Val Ile Val Phe Phe Leu Ile Gly
65 70 75 80
Phe Met Ile Gly Tyr Leu Gly Tyr Cys Lys Gly Val Glu Pro Lys Thr
85 90 95
Glu Cys Glu Arg Leu Ala Gly Thr Glu Ser Pro Val Arg Glu Glu Pro
100 105 110
Gly Glu Asp Phe Pro Ala Ala Arg Arg Leu Tyr Trp Asp Asp Leu Lys
115 120 125
Arg Lys Leu Ser Glu Lys Leu Asp Ser Thr Asp Phe Thr Gly Thr Ile
130 135 140
Lys Leu Leu Asn Glu Asn Ser Tyr Val Pro Arg Glu Ala Gly Ser Gln
145 150 155 160
Lys Asp Glu Asn Leu Ala Leu Tyr Val Glu Asn Gln Phe Arg Glu Phe
165 170 175
Lys Leu Ser Lys Val Trp Arg Asp Gln His Phe Val Lys Ile Gln Val
180 185 190
Lys Asp Ser Ala Gln Asn Ser Val Ile Ile Val Asp Lys Asn Gly Arg
195 200 205
Leu Val Tyr Leu Val Glu Asn Pro Gly Gly Tyr Val Ala Tyr Ser Lys
210 215 220
Ala Ala Thr Val Thr Gly Lys Leu Val His Ala Asn Phe Gly Thr Lys
225 230 235 240
Lys Asp Phe Glu Asp Leu Tyr Thr Pro Val Asn Gly Ser Ile Val Ile
245 250 255
Val Arg Ala Gly Lys Ile Thr Phe Ala Glu Lys Val Ala Asn Ala Glu
260 265 270
Ser Leu Asn Ala Ile Gly Val Leu Ile Tyr Met Asp Gln Thr Lys Phe
275 280 285
Pro Ile Val Asn Ala Glu Leu Ser Phe Phe Gly His Ala His Leu Gly
290 295 300
Thr Gly Asp Pro Tyr Thr Pro Gly Phe Pro Ser Phe Asn His Thr Gln
305 310 315 320
Phe Pro Pro Ser Arg Ser Ser Gly Leu Pro Asn Ile Pro Val Gln Thr
325 330 335
Ile Ser Arg Ala Ala Ala Glu Lys Leu Phe Gly Asn Met Glu Gly Asp
340 345 350
Cys Pro Ser Asp Trp Lys Thr Asp Ser Thr Cys Arg Met Val Thr Ser
355 360 365
Glu Ser Lys Asn Val Lys Leu Thr Val Ser Asn Val Leu Lys Glu Ile
370 375 380
Lys Ile Leu Asn Ile Phe Gly Val Ile Lys Gly Phe Val Glu Pro Asp
385 390 395 400
His Tyr Val Val Val Gly Ala Gln Arg Asp Ala Trp Gly Pro Gly Ala
405 410 415
Ala Lys Ser Gly Val Gly Thr Ala Leu Leu Leu Lys Leu Ala Gln Met
420 425 430
Phe Ser Asp Met Val Leu Lys Asp Gly Phe Gln Pro Ser Arg Ser Ile
435 440 445
Ile Phe Ala Ser Trp Ser Ala Gly Asp Phe Gly Ser Val Gly Ala Thr
450 455 460
Glu Trp Leu Glu Gly Tyr Leu Ser Ser Leu His Leu Lys Ala Phe Thr
465 470 475 480
Tyr Ile Asn Leu Asp Lys Ala Val Leu Gly Thr Ser Asn Phe Lys Val
485 490 495
Ser Ala Ser Pro Leu Leu Tyr Thr Leu Ile Glu Lys Thr Met Gln Asn
500 505 510
Val Lys His Pro Val Thr Gly Gln Phe Leu Tyr Gln Asp Ser Asn Trp
515 520 525
Ala Ser Lys Val Glu Lys Leu Thr Leu Asp Asn Ala Ala Phe Pro Phe
530 535 540
Leu Ala Tyr Ser Gly Ile Pro Ala Val Ser Phe Cys Phe Cys Glu Asp
545 550 555 560
Thr Asp Tyr Pro Tyr Leu Gly Thr Thr Met Asp Thr Tyr Lys Glu Leu
565 570 575
Ile Glu Arg Ile Pro Glu Leu Asn Lys Val Ala Arg Ala Ala Ala Glu
580 585 590
Val Ala Gly Gln Phe Val Ile Lys Leu Thr His Asp Val Glu Leu Asn
595 600 605
Leu Asp Tyr Glu Arg Tyr Asn Ser Gln Leu Leu Ser Phe Val Arg Asp
610 615 620
Leu Asn Gln Tyr Arg Ala Asp Ile Lys Glu Met Gly Leu Ser Leu Gln
625 630 635 640
Trp Leu Tyr Ser Ala Arg Gly Asp Phe Phe Arg Ala Thr Ser Arg Leu
645 650 655
Thr Thr Asp Phe Gly Asn Ala Glu Lys Thr Asp Arg Phe Val Met Lys
660 665 670
Lys Leu Asn Asp Arg Val Met Arg Val Glu Tyr His Phe Leu Ser Pro
675 680 685
Tyr Val Ser Pro Lys Glu Ser Pro Phe Arg His Val Phe Trp Gly Ser
690 695 700
Gly Ser His Thr Leu Pro Ala Leu Leu Glu Asn Leu Lys Leu Arg Lys
705 710 715 720
Gln Asn Asn Gly Ala Phe Asn Glu Thr Leu Phe Arg Asn Gln Leu Ala
725 730 735
Leu Ala Thr Trp Thr Ile Gln Gly Ala Ala Asn Ala Leu Ser Gly Asp
740 745 750
Val Trp Asp Ile Asp Asn Glu Phe
755 760
<210> 151
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 151
Gly Gly Ser Gly
1
<210> 152
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 152
Gly Ser Gly Gly
1
<210> 153
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 153
Ser Gly Gly Gly
1
<210> 154
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 154
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 155
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 155
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 156
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 156
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Ser Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Tyr
180 185 190
Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
260 265 270
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
275 280 285
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
290 295 300
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
305 310 315 320
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
325 330 335
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
340 345 350
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
355 360 365
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly Lys
705
<210> 157
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 157
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
450 455 460
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
465 470 475 480
Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Gly Val Ala Trp Tyr
485 490 495
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser
500 505 510
Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
515 520 525
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
530 535 540
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr Pro Tyr Thr Phe Gly Gln
545 550 555 560
Gly Thr Lys Val Glu Ile Lys Gly Gly Ser Gly Gly Gly Ser Gly Gly
565 570 575
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Glu Val Gln Leu Val
580 585 590
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
595 600 605
Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Tyr Thr Met Asp Trp Val
610 615 620
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Asp Val Asn Pro
625 630 635 640
Asn Ser Gly Gly Ser Ile Tyr Asn Gln Arg Phe Lys Gly Arg Phe Thr
645 650 655
Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
660 665 670
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asn Leu Gly
675 680 685
Pro Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
690 695 700
Ser Ser
705
<210> 158
<211> 573
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 158
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
465 470 475 480
Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser
485 490 495
Ile Gly Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
500 505 510
Leu Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Ser Arg Phe
515 520 525
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
530 535 540
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ile Tyr
545 550 555 560
Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
565 570
Claims (148)
- 단백질로서,
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 단일쇄 가변 단편(scFv)에 융합된 제2 Fc 폴리펩타이드로서, 상기 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) (a)에 언급된 상기 Fd 부분과 쌍을 이루어 Fab를 형성하는 경쇄 폴리펩타이드
를 포함하되,
상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 II에 결합하는, 단백질. - 제1항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 IV에 결합하는, 단백질.
- 제1항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 II에 결합하는, 단백질.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 상기 제2 Fc 폴리펩타이드는 제1 링커를 통해 상기 scFv에 융합되는, 단백질.
- 제4항에 있어서, 상기 제1 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제4항 또는 제5항에 있어서, 상기 제1 링커는 서열 GGGGSGGGGS(서열번호 118)를 포함하는, 단백질.
- 제1항 내지 제6항 중 어느 한 항에 있어서, 상기 scFv는 제2 링커를 통해 연결된 VL 영역 및 VH 영역을 포함하는, 단백질.
- 제7항에 있어서, 상기 제2 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제7항 또는 제8항에 있어서, 상기 제2 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함하는, 단백질.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 트랜스페린 수용체에 특이적으로 결합하는, 단백질.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및 상기 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함하는, 단백질.
- 제11항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하는, 단백질.
- 제11항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366W 치환을 포함하는, 단백질.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함하는, 단백질.
- 제14항에 있어서, 상기 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환인, 단백질.
- 제1항 내지 제15항 중 어느 한 항에 있어서, 힌지 영역 또는 이의 일부는 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드의 N-말단에 연결되는, 단백질.
- 제1항 내지 제16항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제1항 내지 제18항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제1항 내지 제19항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제1항 내지 제19항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제1항 내지 제21항 중 어느 한 항에 있어서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 21의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 20의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 19의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 18의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 15 또는 17의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 14의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 13의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 11 또는 12의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 22의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 5의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 18의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c) 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제22항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 제22항 또는 제23항에 있어서, 상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 단백질로서,
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 상기 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 각각 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되거나, 또는
상기 (a) 및/또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되거나, 또는
상기 제1 Fc 폴리펩타이드 또는 상기 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, 상기 (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되며,
상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 II에 결합하는, 단백질. - 제25항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되는, 단백질.
- 제25항에 있어서, 상기 (a) 및/또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되는, 단백질.
- 제25항에 있어서, 상기 제1 Fc 폴리펩타이드 또는 상기 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, 상기 (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되는, 단백질.
- 제25항 내지 제28항 중 어느 한 항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 IV에 결합하는, 단백질.
- 제25항 내지 제28항 중 어느 한 항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 II에 결합하는, 단백질.
- 제25항 내지 제30항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드에 융합된 scFv는 동일한 서열을 포함하는, 단백질.
- 제25항 내지 제30항 중 어느 한 항에 있어서, 상기 (a) 및/또는 (b)의 Fd 부분에 융합된 scFv는 동일한 서열을 포함하는, 단백질.
- 제25항 내지 제32항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 제1 링커를 통해 상기 scFv에 융합되는, 단백질.
- 제25항 내지 제33항 중 어느 한 항에 있어서, 상기 (a) 및/또는 (b)의 Fd 부분은 제1 링커를 통해 상기 scFv에 융합되는, 단백질.
- 제33항 또는 제34항에 있어서, 상기 제1 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제33항 내지 제35항 중 어느 한 항에 있어서, 상기 제1 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함하는, 단백질.
- 제25항 내지 제36항 중 어느 한 항에 있어서, 상기 scFv는 제2 링커를 통해 연결된 VL 영역 및 VH 영역을 포함하는, 단백질.
- 제37항에 있어서, 상기 제2 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제37항 또는 제38항에 있어서, 상기 제2 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함하는, 단백질.
- 제25항 내지 제39항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 트랜스페린 수용체에 특이적으로 결합하는, 단백질.
- 제25항 내지 제40항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및 상기 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함하는, 단백질.
- 제41항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하는, 단백질.
- 제41항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366W 치환을 포함하는, 단백질.
- 제25항 내지 제43항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함하는, 단백질.
- 제44항에 있어서, 상기 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환인, 단백질.
- 제25항 내지 제45항 중 어느 한 항에 있어서, 힌지 영역 또는 이의 일부는 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드의 N-말단에 연결되는, 단백질.
- 제25항 내지 제46항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제25항 내지 제47항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제25항 내지 제48항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제25항 내지 제49항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제25항 내지 제49항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제25항 내지 제51항 중 어느 한 항에 있어서,
(i) (a) 서열번호 27 또는 28의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 29의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 30의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 31의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 33 또는 34의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 35의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 36의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 37 또는 39의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 37의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 157의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제25항 내지 제51항 중 어느 한 항에 있어서,
(i) (a) 서열번호 27 또는 28의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 31의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 29의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 30의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 33 또는 34의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 37 또는 39의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 35의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 36의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 33의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 38의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제25항 내지 제51항 중 어느 한 항에 있어서,
(i) (a) 서열번호 40의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 41의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 42의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 43의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 45 또는 46의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 47의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 48의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 49의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 44의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 50의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(xi) (a) 서열번호 156의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제25항 내지 제51항 중 어느 한 항에 있어서,
(i) (a) 서열번호 40의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 43의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 41의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 42의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 45의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 49의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 47의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 48의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 45의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 50의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 46의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 156의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제25항 내지 제51항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 또는 상기 제2 Fc 폴리펩타이드는 C-말단에서 scFv에 융합되고, 상기 (a) 또는 (b)의 Fd 부분은 N-말단에서 scFv에 융합되되,
(i) (a) 서열번호 40의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 31의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 41의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 30의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 42의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 29의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 43의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 27 또는 28의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 45의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 37 또는 39의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 47의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 36의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 48의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 35의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 49의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 33 또는 34의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 폴리펩타이드 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제52항 내지 제56항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 제52항 내지 제57항 중 어느 한 항에 있어서, 상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 단백질로서,
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 상기 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
상기 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 N-말단에서 scFv에 융합되거나, 또는
상기 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 C-말단에서 scFv에 융합되거나, 또는
상기 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 상기 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되며, 그리고
상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 IV에 결합하거나 또는 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 II에 결합하는, 단백질. - 제59항에 있어서, 상기 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 N-말단에서 scFv에 융합되는, 단백질.
- 제59항에 있어서, 상기 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 C-말단에서 scFv에 융합되는, 단백질.
- 제59항에 있어서, 상기 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 상기 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되는, 단백질.
- 제59항 내지 제62항 중 어느 한 항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 IV에 결합하는, 단백질.
- 제59항 내지 제62항 중 어느 한 항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 scFv는 인간 HER2의 서브도메인 II에 결합하는, 단백질.
- 제59항 내지 제64항 중 어느 한 항에 있어서, 상기 경쇄 폴리펩타이드 중 하나 또는 둘 모두에 융합되는 scFv는 동일한 서열을 포함하는, 단백질.
- 제59항 내지 제65항 중 어느 한 항에 있어서, 상기 경쇄 폴리펩타이드 중 하나 또는 둘 모두는 제1 링커를 통해 상기 scFv에 융합되는, 단백질.
- 제66항에 있어서, 상기 제1 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제66항 또는 제67항에 있어서, 상기 제1 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함하는, 단백질.
- 제59항 내지 제68항 중 어느 한 항에 있어서, 상기 scFv는 제2 링커를 통해 연결된 VL 영역 및 VH 영역을 포함하는, 단백질.
- 제69항에 있어서, 상기 제2 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제69항 또는 제70항에 있어서, 상기 제2 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함하는, 단백질.
- 제59항 내지 제71항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 트랜스페린 수용체에 특이적으로 결합하는, 단백질.
- 제59항 내지 제72항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및 상기 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함하는, 단백질.
- 제73항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하는, 단백질.
- 제73항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366W 치환을 포함하는, 단백질.
- 제59항 내지 제75항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함하는, 단백질.
- 제76항에 있어서, 상기 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환인, 단백질.
- 제59항 내지 제77항 중 어느 한 항에 있어서, 힌지 영역 또는 이의 일부는 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드의 N-말단에 연결되는, 단백질.
- 제59항 내지 제78항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제59항 내지 제79항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제59항 내지 제80항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제59항 내지 제81항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제59항 내지 제81항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제59항 내지 제83항 중 어느 한 항에 있어서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 52의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 52의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 53 또는 54의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 53 또는 54의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제59항 내지 제83항 중 어느 한 항에 있어서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 52의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 52의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 53 또는 54의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 53 또는 54의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제59항 내지 제83항 중 어느 한 항에 있어서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고 서열번호 55의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고, 서열번호 55의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고 서열번호 56 또는 57의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고 서열번호 56 또는 57의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제59항 내지 제83항 중 어느 한 항에 있어서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 55의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 55의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 56 또는 57의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 2개의 경쇄 폴리펩타이드 각각은 C-말단에서 scFv에 융합되고 서열번호 56 또는 57의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제59항 내지 제83항 중 어느 한 항에 있어서,
(i) (a) 서열번호 1의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 4의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고 서열번호 55의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 52의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 2의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 3의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고 서열번호 55의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 52의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 6의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 9의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고 서열번호 56 또는 57의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 53 또는 54의 서열에 대해 적어도 90%의 동일성을 갖는 서열서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 7의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 8의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제1 경쇄 폴리펩타이드는 N-말단에서 scFv에 융합되고 서열번호 56 또는 57의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, 제2 경쇄 폴리펩타이드는 C-말단에서 scFv에 융합되고 서열번호 53 또는 54의 서열에 대해 적어도 90%의 동일성을 갖는 서열서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제84항 내지 제88항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 제84항 내지 제88항 중 어느 한 항에 있어서, 상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 단백질로서,
(a) N-말단에서 Fab의 Fd 부분에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합된 제2 Fc 폴리펩타이드로서, 상기 제1 및 상기 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 각각 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
상기 (a) 및 (b)의 Fd 부분 각각은 N-말단에서 Fv 단편의 VH 영역 또는 VL 영역에 융합되고, 그리고
상기 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VH 영역 또는 VL 영역 중 다른 하나에 융합되며, 그리고
상기 VH 영역 및 VL 영역은 함께 Fv 단편을 형성하고, 그리고
상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 IV에 결합하거나 또는 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 II에 결합하는, 단백질. - 제91항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 IV에 결합하는, 단백질.
- 제91항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 II에 결합하는, 단백질.
- 제91항 내지 제93항 중 어느 한 항에 있어서, 상기 (a) 및 (b)의 Fd 부분 각각은 N-말단에서 제1 링커를 통해 VH 영역 또는 VL 영역에 융합되는, 단백질.
- 제94항에 있어서, 상기 제1 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제94항 또는 제95항에 있어서, 상기 제1 링커는 ASTKGPSVF(서열번호 125)의 서열을 포함하는, 단백질.
- 제91항 내지 제96항 중 어느 한 항에 있어서, 상기 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 제2 링커를 통해 VH 영역 또는 VL 영역에 융합되는, 단백질.
- 제97항에 있어서, 상기 제2 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제97항 또는 제98항에 있어서, 상기 제2 링커는 RTVAAPSVFI(서열번호 126)의 서열을 포함하는, 단백질.
- 제91항 내지 제99항 중 어느 한 항에 있어서, 상기 (a) 및 (b)의 Fd 부분 각각은 N-말단에서 Fv 단편의 VH 영역에 융합되고, 상기 2개의 경쇄 폴리펩타이드 각각은 N-말단에서 Fv 단편의 VL 영역에 융합되는, 단백질.
- 제91항 내지 제99항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 트랜스페린 수용체에 특이적으로 결합하는, 단백질.
- 제91항 내지 제101항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및 상기 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함하는, 단백질.
- 제102항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하는, 단백질.
- 제102항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366W 치환을 포함하는, 단백질.
- 제91항 내지 제104항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함하는, 단백질.
- 제105항에 있어서, 상기 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환인, 단백질.
- 제91항 내지 제106항 중 어느 한 항에 있어서, 상기 힌지 영역 또는 이의 일부는 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드의 N-말단에 연결되는, 단백질.
- 제91항 내지 제107항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제91항 내지 제108항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제91항 내지 제109항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제91항 내지 제110항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제91항 내지 제110항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제91항 내지 제112항 중 어느 한 항에 있어서, 상기 단백질은
(i) (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 58의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 61의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 78의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드; 또는
(ii) (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 59의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 60의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 78의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드; 또는
(iii) (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 63의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 66의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 79의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드; 또는
(iv) (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 64의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 65의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 79의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드; 또는
(v) (a) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 63의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VH 영역에 융합되며 서열번호 67의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VL 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 79의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함하는, 단백질. - 제91항 내지 제112항 중 어느 한 항에 있어서, 상기 단백질은
(i) (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 68의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 71의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 80의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드; 또는
(ii) (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 69의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 70의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 80의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드; 또는
(iii) (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 73의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 76의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 81의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드; 또는
(iv) (a) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 74의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제1 폴리펩타이드, (b) N-말단에서 Fv 단편의 VL 영역에 융합되며 서열번호 75의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제2 폴리펩타이드, 및 각각 N-말단에서 Fv 단편의 VH 영역에 융합된 경쇄 폴리펩타이드를 포함하며 각각 서열번호 81의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는 제3 및 제4 폴리펩타이드를 포함하는, 단백질. - 제113항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 제113항에 있어서, 상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 단백질로서,
(a) N-말단에서 Fab의 Fd 부분에 융합되고 C-말단에서 Fv 단편의 VH 영역 또는 VL 영역에 융합된 제1 Fc 폴리펩타이드;
(b) N-말단에서 Fab의 Fd 부분에 융합되고 C-말단에서 (a)에 언급된 VH 영역 또는 VL 영역 중 다른 하나에 융합된 제2 Fc 폴리펩타이드로서,
상기 VH 영역 및 VL 영역은 함께 Fv 단편을 형성하고, 상기 제1 및 제2 Fc 폴리펩타이드는 Fc 이량체를 형성하는, 상기 제2 Fc 폴리펩타이드; 및
(c) 각각 (a) 및 (b)에 언급된 Fd 부분과 쌍을 이루어 Fab를 형성하는 2개의 경쇄 폴리펩타이드
를 포함하되;
상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 IV에 결합하거나 또는 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 II에 결합하는, 단백질. - 제117항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 II에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 IV에 결합하는, 단백질.
- 제117항에 있어서, 상기 Fab는 인간 HER2의 서브도메인 IV에 결합하고, 상기 Fv 단편은 인간 HER2의 서브도메인 II에 결합하는, 단백질.
- 제117항 내지 제119항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 상기 Fv 단편의 VH 영역에 융합되고, 상기 제2 Fc 폴리펩타이드는 상기 Fv 단편의 VL 영역에 융합되는, 단백질.
- 제117항 내지 제119항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 상기 Fv 단편의 VL 영역에 융합되고, 상기 제2 Fc 폴리펩타이드는 상기 Fv 단편의 VH 영역에 융합되는, 단백질.
- 제117항 내지 제121항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 상기 C-말단에서 제1 링커를 통해 상기 VH 영역 또는 VL 영역에 융합되는, 단백질.
- 제122항에 있어서, 상기 제1 링커는 1개 내지 20개의 아미노산 길이를 갖는, 단백질.
- 제122항 또는 제123항에 있어서, 상기 제1 링커는 GGSGGGSGGGSGGGSGGGSG(서열번호 116; (GGSG)5), GGGGS(서열번호 117; G4S), GGGGSGGGGS(서열번호 118; (G4S)2), GGGGSGGGGSGGGGS(서열번호 119; (G4S)3), GGGGSGGGGSGGGG(서열번호 120; (G4S)2-G4), GGGGSGGGGSGG(서열번호 121), GGGGGSGGGGS(서열번호 122) 및 GGGGGSGGGGGSGGGGS(서열번호 123) 중 어느 하나의 서열을 포함하는, 단백질.
- 재117항 내지 제124항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 트랜스페린 수용체에 특이적으로 결합하는, 단백질.
- 제117항 내지 제125항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및 상기 제2 Fc 폴리펩타이드는 각각 이종이량체화를 촉진하는 변형을 포함하는, 단백질.
- 제126항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366W 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하는, 단백질.
- 제126항에 있어서, EU 넘버링에 따라, 상기 제1 Fc 폴리펩타이드는 T366S, L368A 및 Y407V 치환을 포함하고, 상기 제2 Fc 폴리펩타이드는 T366W 치환을 포함하는, 단백질.
- 제117항 내지 제128항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 효과기 기능을 감소시키는 변형을 포함하는, 단백질.
- 제129항에 있어서, 상기 효과기 기능을 감소시키는 변형은 EU 넘버링에 따라 L234A 및 L235A 치환인, 단백질.
- 제117항 내지 제130항 중 어느 한 항에 있어서, 상기 힌지 영역 또는 이의 일부는 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드의 N-말단에 연결되는, 단백질.
- 제117항 내지 제131항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 131 내지 149로 이루어진 군으로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제117항 내지 제132항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제117항 내지 제133항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드 및/또는 상기 제2 Fc 폴리펩타이드는 독립적으로 EU 넘버링에 따라 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 135 내지 139로부터 선택되는 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질.
- 제117항 내지 제134항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제117항 내지 제134항 중 어느 한 항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 366번 위치에 Ser, 368번 위치에 Ala 및 407번 위치에 Val, 및 서열번호 133의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, 그리고
상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 위치에 Ala, 235번 위치에 Ala, 366번 위치에 Trp, 384번 위치에 Tyr, 386번 위치에 Thr, 387번 위치에 Glu, 388번 위치에 Trp, 389번 위치에 Ser, 413번 위치에 Ser, 415번 위치에 Glu, 416번 위치에 Glu 및 421번 위치에 Phe, 및 서열번호 137의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제117항 내지 제136항에 있어서,
(i) (a) 서열번호 82 또는 83의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 99 또는 100의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ii) (a) 서열번호 84의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 98의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iii) (a) 서열번호 85의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 97의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(iv) (a) 서열번호 86 또는 88의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 95 또는 96의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(v) (a) 서열번호 89의 서열 또는 90의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 105 또는 107의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vi) (a) 서열번호 91의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 104의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(vii) (a) 서열번호 92의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 103의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(viii) (a) 서열번호 93의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 102의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(ix) (a) 서열번호 82의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 99의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(x) (a) 서열번호 82의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 100의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 25의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(xi) (a) 서열번호 90의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 107의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하거나; 또는
(xii) (a) 서열번호 90의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하고, (b) 서열번호 158의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하며, (c)의 2개의 경쇄 각각은 서열번호 26의 서열에 대해 적어도 90%의 동일성을 갖는 서열을 포함하는, 단백질. - 제137항에 있어서, 상기 제1 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 제137항에 있어서, 상기 제2 Fc 폴리펩타이드는 EU 넘버링에 따라 234번 및 235번 위치에 Leu를 포함하는, 단백질.
- 약제학적 조성물로서, 제1항 내지 제139항 중 어느 한 항에 따른 단백질 및 약제학적으로 허용 가능한 담체를 포함하는, 약제학적 조성물.
- 단리된 폴리뉴클레오타이드로서, 제1항 내지 제139항 중 어느 한 항에 따른 단백질을 암호화하는 뉴클레오타이드 서열을 포함하는, 단리된 폴리뉴클레오타이드.
- 벡터로서, 제141항의 폴리뉴클레오타이드를 포함하는, 벡터.
- 숙주 세포로서, 제141항의 폴리뉴클레오타이드 또는 제142항의 벡터를 포함하는, 숙주 세포.
- 대상체에서 암을 치료하거나 또는 암의 뇌 전이를 치료하는 방법으로서, 치료학적 유효량의 제1항 내지 제139항 중 어느 한 항에 따른 단백질 또는 제140항의 약제학적 조성물을 상기 대상체에게 투여하는 단계를 포함하는, 방법.
- 제144항에 있어서, 상기 단백질은 화학요법 또는 방사선 요법과 조합하여 투여되는, 방법.
- 제144항 또는 제145항에 있어서, 상기 암은 전이성 암인, 방법.
- 제144항 내지 제146항 중 어느 한 항에 있어서, 상기 암은 유방암인, 방법.
- 제144항 내지 제147항 중 어느 한 항에 있어서, 상기 암은 HER2-양성 암인, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202062978758P | 2020-02-19 | 2020-02-19 | |
| US62/978,758 | 2020-02-19 | ||
| PCT/US2021/018705 WO2021168194A1 (en) | 2020-02-19 | 2021-02-19 | Engineered anti-her2 bispecific proteins |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220156526A true KR20220156526A (ko) | 2022-11-25 |
Family
ID=77391704
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227028989A KR20220156526A (ko) | 2020-02-19 | 2021-02-19 | 조작된 항-her2 이중특이성 단백질 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US20230192887A1 (ko) |
| EP (1) | EP4181950A1 (ko) |
| JP (1) | JP2023514371A (ko) |
| KR (1) | KR20220156526A (ko) |
| CN (1) | CN115361972A (ko) |
| AR (1) | AR121384A1 (ko) |
| AU (1) | AU2021224200A1 (ko) |
| BR (1) | BR112022016232A2 (ko) |
| CA (1) | CA3170338A1 (ko) |
| IL (1) | IL295729A (ko) |
| MX (1) | MX2022010161A (ko) |
| TW (1) | TW202144431A (ko) |
| WO (1) | WO2021168194A1 (ko) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2018221731C1 (en) | 2017-02-17 | 2021-11-18 | Denali Therapeutics Inc. | Engineered transferrin receptor binding polypeptides |
| CA3197506A1 (en) | 2020-10-14 | 2022-04-21 | Denali Therapeutics Inc. | Fusion proteins comprising sulfoglucosamine sulfohydrolase enzymes and methods thereof |
| WO2023038803A2 (en) * | 2021-08-25 | 2023-03-16 | Denali Therapeutics Inc. | Engineered anti-her2 bispecific proteins |
| WO2024028731A1 (en) * | 2022-08-05 | 2024-02-08 | Janssen Biotech, Inc. | Transferrin receptor binding proteins for treating brain tumors |
| WO2024028732A1 (en) * | 2022-08-05 | 2024-02-08 | Janssen Biotech, Inc. | Cd98 binding constructs for treating brain tumors |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015077891A1 (en) * | 2013-11-27 | 2015-06-04 | Zymeworks Inc. | Bispecific antigen-binding constructs targeting her2 |
| EP3129055B1 (en) * | 2014-04-11 | 2020-07-01 | MedImmune, LLC | Bispecific her2 antibodies |
| EP3313890A1 (en) * | 2015-06-24 | 2018-05-02 | H. Hoffnabb-La Roche Ag | Trispecific antibodies specific for her2 and a blood brain barrier receptor and methods of use |
-
2021
- 2021-02-19 JP JP2022549653A patent/JP2023514371A/ja active Pending
- 2021-02-19 AU AU2021224200A patent/AU2021224200A1/en active Pending
- 2021-02-19 CN CN202180027050.7A patent/CN115361972A/zh active Pending
- 2021-02-19 WO PCT/US2021/018705 patent/WO2021168194A1/en unknown
- 2021-02-19 CA CA3170338A patent/CA3170338A1/en active Pending
- 2021-02-19 EP EP21756590.2A patent/EP4181950A1/en active Pending
- 2021-02-19 MX MX2022010161A patent/MX2022010161A/es unknown
- 2021-02-19 TW TW110105842A patent/TW202144431A/zh unknown
- 2021-02-19 IL IL295729A patent/IL295729A/en unknown
- 2021-02-19 BR BR112022016232A patent/BR112022016232A2/pt unknown
- 2021-02-19 AR ARP210100440A patent/AR121384A1/es unknown
- 2021-02-19 KR KR1020227028989A patent/KR20220156526A/ko unknown
-
2022
- 2022-08-11 US US17/819,182 patent/US20230192887A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023514371A (ja) | 2023-04-05 |
| EP4181950A1 (en) | 2023-05-24 |
| AU2021224200A1 (en) | 2022-09-08 |
| CA3170338A1 (en) | 2021-08-26 |
| CN115361972A (zh) | 2022-11-18 |
| WO2021168194A1 (en) | 2021-08-26 |
| IL295729A (en) | 2022-10-01 |
| TW202144431A (zh) | 2021-12-01 |
| AR121384A1 (es) | 2022-06-01 |
| BR112022016232A2 (pt) | 2022-11-16 |
| US20230192887A1 (en) | 2023-06-22 |
| MX2022010161A (es) | 2022-11-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20230192887A1 (en) | Engineered anti-her2 bispecific proteins | |
| US20220002436A1 (en) | Anti-her2 polypeptides and methods of use thereof | |
| KR102505383B1 (ko) | Dll3 표적 다중 특이성 항원 결합 분자 및 그의 사용 | |
| KR20140033050A (ko) | 단일특이적 및 이중특이적 항-igf-1r 및 항 erbb3 항체 | |
| WO2020053300A1 (en) | Improved anti-flt3 antigen binding proteins | |
| KR20230157933A (ko) | 감마-델타 t 세포 수용체에 결합하는 항체 | |
| US20230192843A1 (en) | Mesothelin binding proteins and uses thereof | |
| EP3623383A1 (en) | Improved bispecific flt3xcd3 antigen binding proteins | |
| CN113454120A (zh) | 针对人免疫检查点CEACAM1(CD66a)的拮抗剂抗体及其制剂,试剂盒,和使用方法 | |
| WO2023038803A2 (en) | Engineered anti-her2 bispecific proteins | |
| AU2022333088A1 (en) | Anti-her2 antibodies and methods of use thereof | |
| CN117120478A (zh) | 一种抗原结合分子 | |
| JP2023551907A (ja) | 腫瘍関連抗原及びcd3結合タンパク質、関連する組成物、及び方法 | |
| WO2024026358A1 (en) | Mesothelin binding proteins and uses thereof | |
| WO2023069888A1 (en) | ANTI-EGFR ANTIBODIES, ANTI-cMET ANTIBODIES, ANTI-VEGF ANTIBODIES, MULTISPECIFIC ANTIBODIES, AND USES THEREOF | |
| TW202412838A (zh) | 包含結合γ-δ T細胞受體之抗體之組合物 | |
| WO2023006390A1 (en) | Mesothelin antibodies and use thereof | |
| CN117715932A (zh) | 一种cdc平台抗体 |