KR20210113279A - 지방 손실 효과를 달성하는데 사용하기 위한 a3 아데노신 수용체 리간드 - Google Patents
지방 손실 효과를 달성하는데 사용하기 위한 a3 아데노신 수용체 리간드 Download PDFInfo
- Publication number
- KR20210113279A KR20210113279A KR1020217024682A KR20217024682A KR20210113279A KR 20210113279 A KR20210113279 A KR 20210113279A KR 1020217024682 A KR1020217024682 A KR 1020217024682A KR 20217024682 A KR20217024682 A KR 20217024682A KR 20210113279 A KR20210113279 A KR 20210113279A
- Authority
- KR
- South Korea
- Prior art keywords
- subject
- ligand
- treatment
- pharmaceutical composition
- obesity
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4706—4-Aminoquinolines; 8-Aminoquinolines, e.g. chloroquine, primaquine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7076—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines containing purines, e.g. adenosine, adenylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Obesity (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Child & Adolescent Psychology (AREA)
- Molecular Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
본 발명은 피험자의 체중 감소; 피험자의 체지방량 감소; 피험자의 비만 치료; 및 피험자에서 지방세포 증식의 저해로부터 선택된 적어도 하나의 지방 손실 효과를 달성하는데 사용하기 위한 A3 아데노신 수용체 (A3AR) 리간드에 관한 것이다. 또한, 본 발명은 A3AR 리간드를 포함하는 약학 조성물, 치료 방법 및 키트에 관한 것이다.
Description
본 발명은 A3AR 리간드의 의약 용도에 관한 것이다.
현재 개시된 주제에 대한 배경으로 관련된 것으로 간주되는 참고문헌은 하기와 같다:
- 국제특허출원 공개 번호 WO04/007519
- 국제특허출원 공개 번호 WO2013/111132
- 국제특허출원 공개 번호 WO/17090036
본 명세서에서 상기 참고문헌에 대한 인정은 이들이 현재 개시된 주제의 특허성과 어떤 방식으로든 관련되어 있음을 의미하는 것으로서 추론되어서는 안된다.
배경
비만은 서구 사회에서 때때로 생명을 위협하는 주요 건강 문제로 간주되는 과량의 체지방을 포함하는 복잡한 질환이다.
비만은 음식 섭취, 기초 대사, 및 에너지 소모의 불균형으로 인해 발생한다. 개인 차원에서, 여러 내인성 또는 환경적 원인이 비만으로 이어질 수 있다. 그러나, 대부분의 경우, 과도한 칼로리 섭취와 열량 밀도가 높은 식사(energy-dense meals)의 유용성의 조합이 비만의 주요 원인 제공자로 생각된다.
체중 감량은 비만과 관련된 건강 문제를 개선하거나 또는 예방할 수 있지만, 체중 감량 절차와 약물 치료를 병행해야 하는 상황이 있다.
국제특허출원 공개 번호 WO04/007519는 부분 또는 완전 Al 아데노신 수용체 작용제인 화합물, 및 당뇨병, 비만 및 지방세포 기능의 변형을 포함하는 다양한 질환 상태에 대한 포유류의 치료에서 이들의 용도를 기재한다.
국제특허출원 공개 번호 WO2013/111132는 간세포 암종 (HCC)의 치료 및 만성 간 질환을 갖는 피험자에서 간 기능을 유지하기 위한 2-클로로-N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드 (Cl-IB-MECA, CF102) Cl-IB-MECA의 용도를 기재한다.
국제특허출원 공개 번호 WO17/090036은 특히 지방간에서 이소성 지방 축적을 감소시키기 위한, 구체적으로, 비-알콜성 지방간 질환 (NAFLD)을 치료하기 위한 A3AR 리간드, 구체적으로, Cl-IB-MECA의 용도를 기재한다.
제 1 측면에 따르면, 본 발명은 하기의 징후 중 어느 하나에 사용하기 위한 A3 아데노신 수용체 (A3AR) 리간드를 제공한다:
- 피험자의 체중 감소;
- 피험자의 체지방량(body fat mass) 감소;
- 피험자의 비만 치료;
- 피험자의 지방세포 수준의 감소; 및
- 피험자에서 지방세포 증식의 저해.
제 2 측면에 따르면, 본 발명은 하기로부터 선택된 적어도 하나의 지방 손실 효과를 달성하는데 효과적인 양의 A3AR 리간드를 활성 성분으로 포함하는 약학 조성물을 제공한다:
- 피험자의 체중 감소;
- 피험자의 체지방량 감소;
- 피험자의 비만 치료;
- 피험자의 지방세포 수준의 감소; 및
- 피험자에서 지방세포 증식의 저해.
또한, 본 발명은 하기로부터 선택된 적어도 하나의 지방 손실 효과를 달성하는데 효과적인 양인, A3AR 리간드의 양을 필요로 하는 피험자에게 A3AR 리간드의 양을 투여하는 단계를 포함하는 치료 방법을 제공한다:
- 피험자의 체중 감소;
- 피험자의 체지방량 감소;
- 피험자의 비만 치료;
- 피험자의 지방세포 수준의 감소; 및
- 피험자에서 지방세포 증식의 저해.
일 예에서, A3AR 리간드는 A3AR 작용제, 바람직하게는 2-클로로-N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드 (Cl-IB-MECA, 본 명세서에서 CF102 라고도 함) 이다.
본 발명은 A3AR에 대해 높은 친화도 및 선택도를 갖는 A3 아데노신 수용체 (A3AR) 작용제인 2-클로로-N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드 (Cl-IB-MECA, 본 명세서에서 CF102 라고도 함)가, in-vitro 지방세포 증식 모델에서 지방세포의 증식을 저해하였다는 결과에 기초한다.
이러한 예기치 않은 저해는, 특히, 지방세포 수준의 감소 (도 1) 및 3T3-L1 지방세포에 의해 생성된 지질 축적의 감소 (도 2a-2b 및 3)에 의해 나타났다.
또한, Cl-IB-MECA의 예기치 않은 효과는 고지방 식이 마우스의 통계적으로 유의한 체중 감량에서 나타났다.
또한, 예상외로, 체중 감량은 A3AR 알로스테릭 조절제 N-(3,4-디클로로-페닐)-2-시클로헥실-1H-이미다조[4,5-c]퀴놀린-4-아민 (때때로 약어 LUF6000 또는 CF602 라고 함)으로 처리 시 비만의 알려진 합병증인 당뇨병 동물 모델에서도 나타났다.
이러한 결과에 기초하여, 본 발명자들은 A3AR 선택적 작용제 또는 A3AR 선택적 알로스테릭 조절제인 A3AR에 대해 높은 친화도 및 선택도를 갖는 리간드가 하기 중 어느 하나 또는 조합에서 치료적으로 유익한 효과를 달성하기 위한 효과적인 도구라고 결론을 내렸다:
- 피험자의 체중 감소;
- 피험자의 체지방량 감소;
- 피험자의 비만 치료;
- 피험자의 지방세포 수준의 감소; 및
- 피험자에서 지방세포 증식의 저해.
이론에 얽매이지 않고, 상기 효과는 리간드가 지방세포의 증식에 미치는 저해 효과에 의해 직접 또는 간접적으로 함께 연결되는 것으로 간주되어, "지방 손실 효과"로 통칭된다.
본 발명의 맥락에서, 각각의 상기 효과들 또는 2 이상의 이러한 효과들의 임의의 조합은 별도의 실시예로 간주되어야 한다.
따라서, 본 발명은 상기 지방 손실 효과 중 어느 하나를 달성하는데 사용하기 위한 A3AR 리간드, 및 상기 지방 손실 효과 중 어느 하나를 달성하는데 사용하기 위한 A3AR 리간드를 포함하는 약학 조성물, 및 상기 지방 손실 효과 중 어느 하나를 필요로 하는 피험자의 치료 방법을 제공하며; 또한, 치료는 하기에서 더 논의되는 바와 같이, 지방 증가의 예방을 포함한다.
하나의 예에서, A3AR 리간드는 비만으로 고통받는 피험자의 치료에 사용하기 위한 것이다.
하나의 다른 예에서, A3AR 리간드는 피험자에서 체중 감량을 유도하거나 또는 촉진하는데 사용하기 위한 것이다.
또 다른 예에서, A3AR 리간드는 피험자에서 지방세포의 수준을 감소시키는 데 사용하기 위한 것이다.
또 하나의 추가 예에서, A3AR 리간드는 지방세포의 증식을 저해하기 위한 것이다.
본 발명의 맥락에서, 체중 감량 또는 비만의 치료를 언급할 때, 이는 지방 조직, 예를 들어 지방, 즉 피하 및/또는 말초 지방을 저장하기 위한 지방 조직의 감소, 및 이소성 지방, 예를 들어 간 조직에서의 이소성 지방의 배제와 동등하게 언급하는 것으로 이해하여야 한다. 일 예에서, 본 발명은 이소성 지방 조직, 특히 간에서 지방 조직의 감소를 배제한다.
하나의 바람직한 예에서, A3AR 리간드는 과량의 체지방을 갖는 피험자, 특히 비만으로 고통받는 피험자의 치료에 사용된다.
일 예에서, 체지방량의 감소는 말초 지방의 감소, 특히 지방 조직의 감소에 의해 나타난다.
일부 다른 예에서, 체지방량의 감소는 3T3-L1 지방세포의 지질 생성의 감소에 의해 나타난다.
과량의 체지방은 체질량 지수 (BMI)에 따라 결정될 수 있다. 25 이상의 BMI를 갖는 피험자는 과량의 체지방을 갖는 것으로 간주되며, 30 이상의 BMI는 피험자가 비만으로 고통받는 것으로 간주된다.
치료 효과, 예를 들어, 본 발명에 따른 측정량(measurands), 예를 들어 체중, 체지방량 및/또는 지방세포 수준의 감소는, 2개의 상이한 시점에서 취한 값에 의해 결정될 수 있다. 일 예에서, 제 1 시점은 치료가 시작되기 전이며, 제 2 시점은 치료 중이다.
일 예에서, 2개의 시점은 치료 중이다. 제 1 시점과 제 2 시점 사이의 시간 차이는, 예를 들어, 1일, 1주, 1개월 및 심지어 최대 1년일 수 있으며, 여기서 중간에 피험자는 본 발명의 실시예 중 어느 하나에 따른 A3AR 리간드를 제공받는다.
측정량 중 하나의 값의 감소를 언급할 때, 값의 감소는 의사가 유의한 것으로 간주하는 정도까지 이해하여야 한다. 이는 미리결정된 기준 시점에 비해, 1%, 5%, 10%, 15%, 20%, 25%, 30%, 40%, 50%, 60% 또는 때때로 70% 이상일 수 있다. 기준 시점과 평가 시점 사이에 값의 측정이 수행되는 다수의 시점이 있을 수 있다는 점에 유의해야 한다.
일 예에서, 기준 시점은 치료가 시작되기 전이다. 일부 다른 예에서, 기준 시점은 치료 중 시점이다.
일 예에서, 평가 시점은 치료의 종료로 결정된 시점이다. 일부 다른 예에서, 평가 시점은 기준 시점 이후의 치료 중 시점이다.
2개의 시점 사이에 피험자는 A3AR 리간드를 제공받는다는 점에 유의해야 한다. 그러나, A3AR 리간드를 사용한 치료는 만성적일 필요는 없으며, 예를 들어, 전체 기간 동안 피험자는 주기적으로 제공받을 수 있다.
하나의 예에서, A3AR 리간드를 사용한 치료는 만성 치료, 즉, 전체 치료 기간 동안의 치료이다.
본 발명의 맥락에서, "A 3 아데노신 수용체 리간드" 또는 "A 3 AR 리간드"는 A3 아데노신 수용체의 활성을 직접적으로 (예를 들어, 수용체 결합 부위를 통해) 또는 간접적으로 (예를 들어, 알로스테릭 결합 부위를 통해) 영향을 미치는 임의의 화합물을 나타내며, 이는 A3 아데노신 수용체의 완전 또는 부분 활성화를 포함한다.
본 발명에 따른 A3AR 리간드는 활성화가 결합 부위 또는 알로스테릭 결합 부위를 통한 것인지에 상관없이, A3AR의 활성을 통해 이의 주된 효과를 발휘하는 분자이다.
A3AR 리간드는 A3AR에 대해 높은 친화도 및 선택도를 가진다. 이는 이것이 투여되는 용량에서 본질적으로 A3AR에만 영향을 미친다는 것을 의미한다.
A3 아데노신 수용체에 대한 리간드의 특이도 및 높은 친화도는, 특히, A3AR 리간드를 이용할 때 없는 심혈관 부작용이 있는 것으로 알려진 A1 아데노신 수용체와 같은 다른 아데노신 수용체의 활성화보다 유익한 효과를 제공한다. 실제로, 연구는 A3AR 리간드가 보호 효과, 특히, 신경보호 효과, 화학보호 효과, 심장보호 효과 및 간보호 효과를 가짐을 나타내었다.
하나의 예에서, "A 3 아데노신 수용체 리간드"는 A3AR 작용제이다.
하나의 다른 예에서, "A 3 아데노신 수용체 리간드"는 A3AR 알로스테릭 조절제 (알로스테릭 효과기(allosteric effector) 라고도 함)이다.
"A 3 아데노신 수용체 작용제" 또는 "A 3 AR 작용제"를 언급할 때, A3 아데노신 수용체에 특이적으로 결합하여 A3 아데노신 수용체를 완전히 또는 부분적으로 활성화시킬 수 있는 임의의 리간드를 의미하는 것으로 이해하여야 한다.
분자는 이의 A3AR에 대한 친화도가 아데노신 수용체 중 임의의 다른 것 (즉, A1, A2a 및 A2b)에 대한 친화도보다 적어도 3배 (즉, 이의 A3AR에 대한 Ki가 적어도 3배 더 낮음), 바람직하게는 10배, 바람직하게는 20배, 가장 바람직하게는 적어도 50배 더 큰 경우, 본 발명의 맥락에서 A3AR 작용제 (즉, A3AR의 결합 및 활성화를 통해 이의 주된 효과를 발휘하는 분자)로 간주될 것이다.
인간 A3AR에 대한 A3AR 작용제의 친화도 및 다른 인간 아데노신 수용체에 대한 이의 상대적 친화도는 수많은 분석, 예를 들어 결합 분석에 의해 결정될 수 있다. 결합 분석의 예는 수용체를 함유하는 막을 제공하고 결합된 방사성 작용제를 대체하는 A3AR 작용제의 능력을 측정하는 것; 각각의 인간 아데노신 수용체를 나타내는 세포를 이용하고, 기능적 분석에서, 경우에 따라, cAMP 수준의 증가 또는 감소를 통해 측정된 아데닐레이트 시클라제에 대한 효과와 같은 하류 신호전달 결과를 활성화시키거나 또는 불활성화시키는 A3AR 작용제의 능력을 측정하는 것; 등을 포함한다. 만일 A3AR 작용제의 혈액 수준이 A1, A2a 및 A2b 아데노신 수용체의 Ki의 수준에 근접하는 수준에 도달하도록 A3AR 작용제의 투여 수준이 증가된다면, 이러한 투여 후에 A3AR의 활성화 이외에 이들 수용체의 활성화가 발생할 수 있다. 따라서, A3AR 작용제는 바람직하게는 혈액 수준이 본질적으로 A3AR만이 활성화되도록 하는 용량으로 투여된다.
하나의 예에서, A3AR 작용제는 100 nM 미만, 일반적으로 50 nM 미만, 바람직하게는 20 nM 미만, 더 바람직하게는 10 nM 미만 및 이상적으로는 5 nM 미만의 범위의 인간 A3AR에 대한 결합 친화도 (Ki)를 가진다. 2 nM 미만, 바람직하게는 1 nM 미만의 인간 A3AR에 대한 Ki를 가지는 A3AR 작용제가 특히 바람직하다.
그러나, 본 발명의 맥락에서, 일부 A3AR 작용제는 더 낮은 친화도 (즉, 더 높은 Ki)를 갖는, 다른 아데노신 수용체와 상호작용하고 활성화시킬 수도 있다고 이해하여야 한다.
일 예에서, A3AR 작용제는 퓨린 골격을 갖는 분자이다. 퓨린 함유 화합물은 허용가능한 구조-기능 활성 분석에 기초하여 A3AR 작용제로 결정될 수 있다.
본 발명에 따라 사용되는 일부 A3AR 작용제의 특성 및 이의 제조 방법은, 특히, US 5,688,774; US 5,773,423, US 5,573,772, US 5,443,836, US 6,048,865, WO 95/02604, WO 99/20284, WO 99/06053, WO 97/27173 및 WO 01/19360에 상세히 기재되어 있으며, 이들 모두는 참조로 본 명세서에 포함된다.
본 발명의 일 예에 따르면, A3AR 작용제는 화학식 (I)의 범위 내에 속하는 퓨린 유도체이다:
여기서,
- R 11 은 알킬, 히드록시알킬, 카복시알킬 또는 시아노알킬, 또는 하기 화학식 (II)의 기를 나타내며:
여기서,
- Y는 산소, 황 또는 CH2를 나타내고;
- X 11 은 H, 알킬, ReRfNC(=O)- 또는 HORg- 를 나타내며, 여기서
- R e 및 R f 는 동일하거나 상이할 수 있고, 수소, 알킬, 아미노, 할로알킬, 아미노알킬, BOC-아미노알킬 및 시클로알킬로 이루어진 군으로부터 선택되거나, 또는 함께 결합하여 2 내지 5의 탄소 원자를 함유하는 헤테로시클릭 고리를 형성하며;
- R g 는 알킬, 아미노, 할로알킬, 아미노알킬, BOC-아미노알킬 및 시클로알킬로 이루어진 군으로부터 선택되고;
- X 12 는 H, 히드록실, 알킬아미노, 알킬아미도 또는 히드록시알킬이며;
- X 13 및 X 14 는 독립적으로 수소, 히드록실, 아미노, 아미도, 아지도, 할로, 알킬, 알콕시, 카복시, 니트릴로, 니트로, 트리플루오로, 아릴, 알크아릴, 티오, 티오에스터, 티오에테르, -OCOPh, -OC(=S)OPh를 나타내거나, 또는 X 13 및 X 14 는 둘 다 >C=S에 연결되어 5-원 고리를 형성하는 산소이거나, 또는 X 12 및 X 13 은 화학식 (III)의 고리를 형성하고:
여기서, R' 및 R"는 독립적으로 알킬기를 나타내며;
- R 12 는 수소, 할로, 알킬에테르, 아미노, 히드라지도, 알킬아미노, 알콕시, 티오알콕시, 피리딜티오, 알케닐, 알키닐, 티오 및 알킬티오로 이루어진 군으로부터 선택되고;
- R 13 은 화학식 -NR15R16의 기이고, 여기서
- R 15 는 수소 원자, 또는 알킬, 치환된 알킬 또는 아릴-NH-C(Z)-로부터 선택되는 기이며, Z는 O, S 또는 NRa이고, R e 는 상기의 의미를 가지며; R 15 가 수소인 경우,
- R 16 은 하나 이상의 위치에서 알킬, 아미노, 할로, 할로알킬, 니트로, 히드록실, 아세토아미도, 알콕시, 및 술폰산 또는 이의 염으로 이루어진 군으로부터 선택된 치환기로 치환 또는 비치환된 R- 및 S-1-페닐에틸, 벤질, 페닐에틸 또는 아닐리드 기; 벤조디옥산메틸, 푸루릴(fururyl), L-프로필알라닐-, 아미노벤질, β-알라닐아미노-벤질, T-BOC-β-알라닐아미노벤질, 페닐아미노, 카바모일, 페녹시 또는 시클로알킬로 이루어진 군으로부터 선택되거나; 또는 R 16 은 하기 화학식 (IV)의 기이거나:
또는 R 15 가 알킬 또는 아릴-NH-C(Z)-인 경우, R 16 은 헤테로아릴-NRa-C(Z)-, 헤테로아릴-C(Z)-, 알크아릴-NRa-C(Z)-, 알크아릴-C(Z)-, 아릴-NR-C(Z)- 및 아릴-C(Z)-로 이루어진 군으로부터 선택되고; Z는 산소, 황 또는 아민을 나타낸다.
예시적인 A3AR 작용제 (US 5,688,774, 4열, 67줄 - 6열, 16줄; 5열 40-45줄; 6열, 21-42줄; 7열, 1-11줄; 7열, 34-36줄; 및 7열, 60-61줄에 개시됨):
N6-(3-아이오도벤질)-9-메틸아데닌;
N6-(3-아이오도벤질)-9-히드록시에틸아데닌;
R―N6-(3-아이오도벤질)-9-(2,3-디히드록시프로필)아데닌;
S―N6-(3-아이오도벤질)-9-(2,3-디히드록시프로필)아데닌;
N6-(3-아이오도벤질아데닌-9-일)아세트산;
N6-(3-아이오도벤질)-9-(3-시아노프로필)아데닌;
2-클로로-N6-(3-아이오도벤질)-9-메틸아데닌;
2-아미노-N6-(3-아이오도벤질)-9-메틸아데닌;
2-히드라지도-N6-(3-아이오도벤질)-9-메틸아데닌;
N6-(3-아이오도벤질)-2-메틸아미노-9-메틸아데닌;
2-디메틸아미노-N6-(3-아이오도벤질)-9-메틸아데닌;
N6-(3-아이오도벤질)-9-메틸-2-프로필아미노아데닌;
2-헥실아미노-N6-(3-아이오도벤질)-9-메틸아데닌;
N6-(3-아이오도벤질)-2-메톡시-9-메틸아데닌;
N6-(3-아이오도벤질)-9-메틸-2-메틸티오아데닌;
N6-(3-아이오도벤질)-9-메틸-2-(4-피리딜티오)아데닌;
(1S, 2R, 3S, 4R)-4-(6-아미노-2-페닐에틸아미노-9H-퓨린-9-일)시클로펜탄-1,2,3-트리올;
(1S, 2R, 3S, 4R)-4-(6-아미노-2-클로로-9H-퓨린-9-일)시클로펜탄-1,2,3-트리올;
(±)-9-[2α,3α-디히드록시-4β-(N-메틸카바모일)시클로펜트-1β-일)]-N6-(3-아이오도벤질)-아데닌;
2-클로로-9-(2'-아미노-2',3'-디데옥시-β-D-5'-메틸-아라비노-푸론아미도(furonamido))-N6-(3-아이오도벤질)아데닌;
2-클로로-9-(2',3'-디데옥시-2'-플루오로-β-D-5'-메틸-아라비노-푸론아미도)-N6-(3-아이오도벤질)아데닌;
9-(2-아세틸-3-데옥시-β-D-5-메틸-리보푸론아미도)-2-클로로-N6(3-아이오도벤질)아데닌;
2-클로로-9-(3-데옥시-2-메탄술포닐-β-D-5-메틸-리보푸론아미도)-N6-(3-아이오도벤질)아데닌;
2-클로로-9-(3-데옥시-β-D-5-메틸-리보푸론아미도)-N6-(3-아이오도벤질)아데닌;
2-클로로-9-(3,5-1,1,3,3-테트라이소프로필디실록실-β-D-5-리보푸라노실)-N6-(3-아이오도벤질)아데닌;
2-클로로-9-(2',3'-O-티오카보닐-β-D-5-메틸-리보푸론아미도)-N6-(3-아이오도벤질)아데닌;
9-(2-페녹시티오카보닐-3-데옥시-β-D-5-메틸-리보푸론아미도)-2-클로로-N6-(3-아이오도벤질)아데닌;
1-(6-벤질아미노-9H-퓨린-9-일)-1-데옥시-N,4-디메틸-β-D-리보푸라노시드우론아미드;
2-클로로-9-(2,3-디데옥시-β-D-5-메틸-리보푸론아미도)-N6 벤질아데닌;
2-클로로-9-(2'-아지도-2',3'-디데옥시-β-D-5'-메틸-아라비노-푸론아미도)-N6-벤질아데닌;
2-클로로-9-(β-D-에리트로푸라노시드)-N6-(3-아이오도벤질)아데닌;
N6-(벤조디옥산메틸)아데노신;
1-(6-푸르푸릴아미노-9H-퓨린-9-일)-1-데옥시-N-메틸-β-D-리보푸라노시드우론아미드;
N6-[3-(L-프롤릴아미노)벤질]아데노신-5'-N-메틸우론아미드;
N6-[3-(β-알라닐아미노)벤질]아데노신-5'-N-메틸우론아미드;
N6-[3-(N-T-Boc-β-알라닐아미노)벤질]아데노신-5'-N-메틸우론아미드;
6-(N'-페닐히드라지닐)퓨린-9-β-리보푸라노시드-5'-N-메틸우론아미드;
6-(O-페닐히드록실아미노)퓨린-9-β-리보푸라노시드-5'-N-메틸우론아미드;
9-(β-D-2',3'-디데옥시에리트로푸라노실)-N6-[(3-β-알라닐아미노)벤질]아데노신;
9-(β-D-에리트로푸라노시드)-2-메틸아미노-N6-(3-아이오도벤질)아데닌;
2-클로로-N-(3-아이오도벤질)-9-(2-테트라히드로푸릴)-9H-퓨린-6-아민;
2-클로로-(2'-데옥시-6'-티오-L-아라비노실)아데닌; 및
2-클로로-(6'-티오-L-아라비노실)아데닌.
US 5,773,423에 개시된 다른 예시적인 A3AR 작용제는 화학식 (V)의 화합물이다:
여기서,
X1은 RaRbNC(=O)이고, 여기서 Ra 및 Rb는 동일하거나 상이할 수 있으며, 수소, C1-C10 알킬, 아미노, C1-C10 할로알킬, C1-C10 아미노알킬, 및 C3-C10 시클로알킬로 이루어진 군으로부터 선택되고;
R2는 수소, 할로, C1-C10 알콕시, 아미노, C2-C10 알케닐, 및 C2-C10 알키닐로 이루어진 군으로부터 선택되며;
R5는 R- 및 S-1-페닐에틸, 비치환된 벤질기, 및 하나 이상의 위치에서 C1-C10 알킬, 아미노, 할로, C1-C10 할로알킬, 니트로, 히드록시, 아세트아미도, C1-C10 알콕시, 및 술포로 이루어진 군으로부터 선택된 치환기로 치환된 벤질기로 이루어진 군으로부터 선택된다.
더 구체적인 A3AR 작용제는 Ra 및 Rb가 동일하거나 상이할 수 있으며, 특히 R2가 수소 또는 할로, 특히 수소인 경우, 수소 및 C1-C10 알킬로 이루어진 군으로부터 선택되는 상기 화학식의 화합물을 포함한다.
추가의 구체적인 A3AR 작용제는 특히 R5가 비치환된 벤질인 경우, Ra가 수소이고 R2가 수소인 화합물이다.
더 구체적인 A3AR 작용제는 Rb가 C1-C10 알킬 또는 C3-C10 시클로알킬, 특히 C1-C10 알킬, 더 특히 메틸인 이러한 화합물이다.
특히 구체적인 A3AR 작용제는 Ra가 수소이고, Rb가 C1-C10 알킬 또는 C3-C10 시클로알킬이며, R5가 R- 또는 S-1-페닐에틸 또는 하나 이상의 위치에서 할로, 아미노, 아세트아미도, C1-C10 할로알킬, 및 술포로 이루어진 군으로부터 선택된 치환기로 치환된 벤질이며, 술포 유도체가 트리에틸암모늄 염과 같은 염인 화합물이다.
또한, US 5,773,423에는 특히 R2가 화학식 Rd-C=C-의 C2-C10 알케닐렌이며, 여기서 Rd가 C1-C8 알킬인 화합물이 기재되어 있다.
또한, 구체적인 화합물은 R2가 수소 이외의 것인 화합물, 특히 R2가 할로, C1-C10 알킬아미노 또는 C1-C10 알킬티오이며, 더 바람직하게는, 추가적으로 Ra가 수소인 경우, Rb가 C1-C10 알킬, 및/또는 R5가 치환된 벤질인 화합물이다.
US 5,773,423에 개시된 추가의 예시적인 A3AR 작용제는 화학식 (VI)를 갖는 변형된 잔틴-7-리보시드이다:
여기서,
X는 O이고;
R6는 RaRbNC(=O)이며, 여기서 Ra 및 Rb는 동일하거나 상이할 수 있으며, 수소, C1-C10 알킬, 아미노, C1-C10 할로알킬, C1-C10 아미노알킬, 및 C3-C10 시클로알킬로 이루어진 군으로부터 선택되고;
R7 및 R8은 동일하거나 상이할 수 있으며, C1-C10 알킬, R- 및 S-1-페닐에틸, 비치환된 벤질기, 및 하나 이상의 위치에서 C1-C10 알킬, 아미노, 할로, C1-C10 할로알킬, 니트로, 히드록시, 아세트아미도, C1-C10 알콕시, 및 술포로 이루어진 군으로부터 선택된 치환기로 치환된 벤질기로 이루어진 군으로부터 선택되고;
R9는 할로, 벤질, 페닐 및 C3-C10 시클로알킬로 이루어진 군으로부터 선택된다.
WO 99/06053은 실시예 19-33에 하기로부터 선택되는 화합물을 개시하고 있다:
N6-(4-비페닐-카보닐아미노)-아데노신-5'-N-에틸우론아미드;
N6-(2,4-디클로로벤질-카보닐아미노)-아데노신-5'-N-에틸우론아미드;
N6-(4-메톡시페닐-카보닐아미노)-아데노신-5'-N-에틸우론아미드;
N6-(4-클로로페닐-카보닐아미노)-아데노신-5'-N-에틸우론아미드;
N6-(페닐-카보닐아미노)-아데노신-5'-N-에틸우론아미드;
N6-(벤질카바모일아미노)-아데노신-5'-N-에틸우론아미드;
N6-(4-술폰아미도-페닐카바모일)-아데노신-5'-N-에틸우론아미드;
N6-(4-아세틸-페닐카바모일)-아데노신-5'-N-에틸우론아미드;
N6-((R)-α-페닐에틸카바모일)-아데노신-5'-N-에틸우론아미드;
N6-((S)-α-페닐에틸카바모일)-아데노신-5'-N-에틸우론아미드;
N6-(5-메틸-이속사졸-3-일-카바모일)-아데노신-5'-N-에틸우론아미드;
N6-(l,3,4-티아디아졸-2-일-카바모일)-아데노신-5'-N-에틸우론아미드;
N6-(4-n-프로폭시-페닐카바모일)-아데노신-5'-N-에틸우론아미드;
N6-비스-(4-니트로페닐카바모일)-아데노신-5'-N-에틸우론아미드; 및
N6-비스-(5-클로로-피리딘-2-일-카바모일)-아데노신-5'-N-에틸우론아미드.
본 발명에 따라 사용되는 더 구체적으로 개시된 A3AR 작용제는 하기의 화합물을 포함한다:
2-클로로-N6-(3-아이오도벤질)-9-[5-(메틸아미도)-β-D-리보푸라노실]-아데닌 (2-클로로-N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드 또는 약어 Cl-IB-MECA로도 알려져 있음);
N6-(3-아이오도벤질)-2-메틸아미노-9-[5-(메틸아미도)-β-D-리보푸라노실]-아데닌 (N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드로도 알려져 있거나 또는 1-데옥시-1-[6-[[(3-아이오도페닐)메틸]아미노]-9H-퓨린-9-일]-N-메틸-D-리보푸란우론아미드 또는 약어 IB-MECA로도 알려져 있음);
N6-2-(4-아미노페닐)에틸아데노신 (APNEA);
N6-(4-아미노-3-아이오도벤질)아데노신-5'-(N-메틸우론아미드) (AB-MECA).
특히 바람직한 A3AR 작용제의 예는 2-클로로-N6-(3-아이오도벤질)-2-메틸아미노-9-[5-(메틸아미도)-β-D-리보푸라노실]-아데닌 (2-클로로-N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드 또는 약어 Cl-IB-MECA로도 알려져 있음)이다.
일 예에서, Cl-IB-MECA는 지방 손실 효과를 달성하는데 사용된다.
하나의 특정 예에서, Cl-IB-MECA는 비만 치료에 사용된다.
"A 3 AR 알로스테릭 조절제" 또는 "A 3 ARM"을 언급할 때, 내인성 리간드 또는 이의 작용제의 결합 부위와 상이할 수 있는 수용체의 알로스테릭 부위에서 알로스테릭 조절제의 결합에 의한 수용체 활성의 양성 조절, 활성화 또는 증가를 나타내는 것으로 이해하여야 한다.
하나의 예에서, "조절"은 수용체의 알로스테릭 부위에 화합물을 결합시킴으로써 A3 아데노신 수용체의 효능의 적어도 15% 증가에 의해 및/또는 오르토스테릭 (orthosteric) 결합 부위에 대한 아데노신 또는 A3AR 작용제의 해리 속도의 감소에 의해 나타나는 수용체에 대한 A3AR 리간드의 효과를 나타낸다.
하나의 예에서, 조절은 이미다조퀴놀린 유도체인 A 3 AR 알로스테릭 조절제 (A 3 ARAM)에 의한 것이다.
하나의 예에서, A3ARAM, 또는 이미다조퀴놀린 유도체는 하기 화학식 (VII)을 가진다:
여기서,
- R1은 방향족 고리에서, C1-C10 알킬, 할로, C1-C10 알칸올, 히드록실, C1-C10 아실, C1-C10 알콕실, C1-C10-알콕시카보닐, C1-C10 알콕실알킬, C1-C10 티오알콕시, C1-C10 알킬에테르, 아미노, 히드라지도, C1-C10 알킬아미노, 피리딜티오, C2-C10 알케닐, C2-C10 알키닐, 티오, C1-C10 알킬티오, 아세토아미도, 술폰산으로 이루어진 군으로부터 선택된 하나 이상의 치환기로 임의로 치환되는 아릴 또는 알크아릴을 나타내거나; 또는 상기 치환기는 함께 상기 아릴에 융합된 시클로알킬 또는 시클로알케닐을 형성할 수 있으며, 시클로알킬 또는 시클로알케닐은 임의로 하나 이상의 헤테로원자를 포함하고; 단 상기 아릴은 비치환된 페닐기가 아니며;
- R2는 수소 또는 C1-C10 알킬, C2-C10 알케닐, C2-C10 알키닐, C4-C10 시클로알킬, C4-C10 시클로알케닐, 5 내지 7-원 헤테로시클릭 방향족 고리; C5-C15 융합된 시클로알킬, 비시클릭 방향족 또는 헤테로방향족 고리; C1-C10 알킬에테르, 아미노, 히드라지도, C1-C10 알킬아미노, C1-C10 알콕시, C1-C10-알콕시카보닐, C1-C10 알칸올, C1-C10 아실, C1-C10 티오알콕시, 피리딜티오, 티오, C1-C10 알킬티오, 아세토아미도, 및 술폰산으로 이루어진 군으로부터 선택되는 치환기를 나타낸다.
일 실시예 따르면, A3ARAM에서 R1 치환기는 하기 화학식 (VIII)을 가진다:
여기서, n은 0 또는 1-5에서 선택된 정수이며; 바람직하게는, n은 0, 1 또는 2이고;
- X1 및 X2는 동일하거나 상이할 수 있으며, 수소, 할로겐, 알킬, 알칸올, 알콕시, 인다닐, 또는 피롤린으로부터 선택되고; 단 상기 n이 0인 경우, X1 및 X2는 수소가 아니다.
또 다른 일 예에서, A3ARAM에서 R1은 상기 화학식 (VIII)을 갖는 치환기이며, 여기서 X1 또는 X2는 동일하거나 상이할 수 있고, 수소, 클로로, 메톡시, 메탄올 또는 화학식 (VIIIa) 또는 (VIIIb)를 갖는 치환기로부터 선택된다:
여기서, Y는 N 또는 CH로부터 선택된다.
또 다른 일 예에서, A3ARAM에서 R2는 H, C1-C10 알킬, C4-C10 시클로알킬로부터 선택되며, 알킬 사슬은 선형 또는 분지형이거나, 또는 4 내지 7-원 시클로알킬 고리를 형성할 수 있다.
하나의 예에서, A3ARAM에서 R2는 5 내지 7-원 헤테로시클릭 방향족 고리로부터 선택된다.
일 예에서, A3ARAM에서 R2 치환기는 H, n-펜틸, 또는 하기 화학식 (IX)를 갖는 5원 헤테로시클릭 방향족 고리로부터 선택된다:
여기서, Z는 O, S 또는 NH로부터 선택되며, 바람직하게는 O이다.
하나의 예에 따르면, A3ARAM에서 R2는 특히 비시클릭 치환기를 형성하기 위하여, 하나 이상의 융합된 고리를 포함한다.
A3ARAM의 맥락에서 치환기를 형성하는데 사용될 수 있는 비시클릭 화합물의 비-제한적인 예는, 비시클로[2.2.1]헵탄, 비시클로[4.1.0]헵탄, 비시클로[4.1.0]헵탄-3-카복실산, 비시클로[3.1.0]헥산-3-카복실산, 비시클로[4.1.0]헵탄-2-카복실산, 비시클로[3.1.0]헥산-2-카복실산, 및 비시클로[2.2.1]헵탄-2-카복실산을 포함한다.
또 다른 일 예에 따르면, A3ARAM에서 R2는 2-시클로헥센 및 3-시클로헥센으로부터 선택된다.
A3AR의 알로스테릭 조절제로서 사용될 수 있는 구체적인 이미다조퀴놀린 유도체는 하기에 열거되어 있다:
N-(4-메틸-페닐)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(4-메톡시-페닐)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(4-클로로-페닐)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3-메탄올-페닐)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-([3,4-c]인단)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(1H-인다졸-6-일)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(4-메톡시-벤질)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(1H-인돌-6-일)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(벤질)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(페닐에틸)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-시클로헵틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-푸릴-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-시클로부틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-시클로헥실-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민.
상기 이미다조퀴놀린 유도체는, 이들이 존재한다면, 한편으로는, A1 및 A2A, A2B 아데노신 수용체의 오르토스테릭 결합 부위에 대해 감소된 친화도 및 A3 아데노신 수용체의 오르토스테릭 결합 부위에 대해 감소된 친화도, 및 다른 한편으로는, A3 아데노신 수용체의 알로스테릭 부위에 대해 높은 친화도를 갖는 것으로 나타났기 때문에, 알로스테릭 조절제로 간주된다 [국제 특허 출원 번호 WO07/089507, 참조로 본 명세서에 포함됨].
본 발명에 따른 특히 바람직한 이미다조퀴놀린 유도체는 N-(3,4-디클로로-페닐)-2-시클로헥실-1H-이미다조[4,5-c]퀴놀린-4-아민 (때때로 약어 LUF6000 또는 CF602 라고도 함)이며, 이는 A3AR 알로스테릭 조절제이다.
본 명세서에 개시된 화학식의 맥락에서, 다양한 용어에 대해 하기의 의미가 고려되어야 한다:
용어 "알킬"은 1 내지 10의 탄소 원자, 더 바람직하게는 1 내지 6의 탄소 원자를 갖는 선형 또는 분지형 탄화수소 사슬을 나타내는 것으로 본 명세서에서 사용되며, 메틸, 에틸, n-프로필, 이소프로필, n-부틸, t-부틸, n-헵틸, 옥틸 등을 포함하나 이에 한정되지 않는다.
유사하게, 용어 "알케닐" 및 "알키닐"은 각각 2 내지 10 또는 3 내지 10의 탄소 원자, 및 더 바람직하게는, 2 내지 6 또는 3 내지 6의 탄소 원자를 갖는 선형 또는 분지형 탄화수소 사슬을 나타내며, 알케닐 또는 알키닐은 적어도 하나의 불포화 결합을 가진다.
알킬, 알케닐 또는 알키닐 치환기는 헤테로원자 함유 기로 치환될 수 있다. 따라서, 명시적으로 언급되지는 않았지만, 상기 및 하기에 정의되는 알킬 변형 중 임의의 것, 예를 들어, 알킬티오, 알콕시, 알칸올, 알킬아민 등은 상응하는 알케닐 또는 알키닐 변형, 예를 들어, 알케닐티오, 알케닐옥시, 알켄올, 알케닐아민, 또는 각각 알키닐티오, 알키닐옥시, 알킨올, 알키닐아민도 포함하는 것으로 이해하여야 한다.
용어 "아릴"은 단일 고리 (예를 들어, 페닐) 또는 다중 축합 고리 (예를 들어, 나프틸 또는 안트릴)를 갖는 5 내지 14의 탄소 원자의 불포화 방향족 카보시클릭 기를 나타낸다. 바람직한 아릴은 페닐, 인다닐, 벤즈이미다졸을 포함한다.
용어 "알크아릴"은 바람직하게는 알킬렌 부분에 1 내지 10의 탄소 원자 및 아릴 부분에 6 내지 14의 탄소 원자를 갖는 -알킬렌-아릴 기를 나타낸다. 이러한 알크아릴 기는 벤질, 페네틸 등으로 예시된다.
용어 "치환된 아릴"은 상기 정의된 1 내지 3의 치환기로 치환된 방향족 부분을 나타낸다. 통상의 기술자에 의해 이해되는 바와 같이, 다양한 치환기가 가능하다. 그럼에도 불구하고, 일부 바람직한 치환기는 할로겐, (치환된) 아미노, 니트로, 시아노, 알킬, 알콕시, 아실옥시 또는 알칸올, 술포닐, 술피닐을 포함하나 이에 한정되지 않는다.
용어 "할로" 또는 "할로겐"은 플루오로, 클로로, 브로모 및 아이오도를 나타내며, 바람직하게는 클로로를 나타낸다.
용어 "아실"은 H-C(O)- 및 알킬-C(0)- 기를 나타낸다.
용어 "알칸올"은 -COH 및 알크-OH 기를 나타내며, "알크(alk)"는 알킬렌, 알케닐렌 또는 알키닐렌 사슬을 나타낸다.
용어 "알콕시"는 -O-알킬을 의미하는 것으로 본 명세서에서 사용되며, 메톡시, 에톡시, 프로폭시, 이소프로폭시, n-부톡시 등을 포함하나 이에 한정되지 않는다.
용어 "알킬티오"는 -S-알킬을 의미하는 것으로 본 명세서에서 사용되며, 메틸티오, 에틸티오, n-프로필티오, 이소프로필티오, n-부틸티오 등을 포함하나 이에 한정되지 않는다.
용어 "알콕시알킬"은 -알킬-O-알킬을 의미하는 것으로 본 명세서에서 사용되며, 메톡시메틸, 에톡시메틸, n-프로폭시메틸, 이소프로폭시메틸, n-부톡시메틸, 이소부톡시메틸, t-부톡시메틸 등을 포함하나 이에 한정되지 않는다.
용어 "시클로알킬"은 고리형 탄화수소 라디칼을 의미하는 것으로 본 명세서에서 사용되며, 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헵틸 등을 포함하나 이에 한정되지 않는다.
용어 "알콕시카보닐"은 -C(0)0-알킬을 의미하는 것으로 본 명세서에서 사용되며, 메톡시카보닐, 에톡시카보닐, 프로폭시카보닐 등을 포함하나 이에 한정되지 않는다.
용어 "융합된 시클로알킬"은 (스피로시클릭 부분을 형성하기 위해) 단일 원자에서, 2개의 상호 결합된 원자에서 또는 일련의 원자를 가로질러 (교두보 (bridgehead)) 연결되는 적어도 2개의 지방족 고리를 포함하는 임의의 화합물 또는 치환기를 의미하는 것으로 본 명세서에서 사용된다. 융합된 고리는 임의의 비시클릭, 트리시클릭 및 폴리시클릭 부분을 포함할 수 있다. 본 발명의 일 실시예에 따르면, 비시클릭 치환기가 바람직하다.
또한, 본 발명은 상기 기재된 화합물과 같은 A3AR 선택적 리간드의 생리학적으로 허용가능한 염을 이용한다. "생리학적으로 허용가능한 염"은 당해 기술분야에서 알려진 방법으로 제조되는, 나트륨, 칼륨, 리튬, 칼슘, 마그네슘, 바륨, 암모늄 및 프로타민 아연 염을 포함하여, 제약 산업에서 상용되는 임의의 비-독성 알칼리 금속, 알칼리 토금속, 및 암모늄 염을 나타낸다. 또한, 용어는 리간드를 적당한 유기산 또는 무기산과 반응시켜 일반적으로 제조되는 비-독성 산 부가염을 포함한다. 산 부가염은 유리 염기의 생물학적 효과 및 질적 특성을 유지하고 독성이 없거나 또는 달리 바람직하지 않은 것이다. 예로는, 무기산으로부터 유래된 산, 특히, 염산, 브롬산, 황산, 질산, 인산, 메타인산 등을 포함한다. 유기산은, 특히, 타르타르산, 아세트산, 프로피온산, 시트르산, 말산, 말론산, 락트산, 푸마르산, 벤조산, 신남산, 만델산, 글리콜산, 글루콘산, 피루브산, 숙신산, 살리실산 및 아릴술폰산, 예를 들어 p-톨루엔술폰산을 포함한다.
A3AR 리간드는 수일, 수주, 또는 수개월 동안, 단일 용량 (일회성 약제) 또는 연속 치료로 투여될 수 있다.
하나의 예에서, A3AR 리간드는 장기간 치료 (만성 치료 및/또는 만성 질병의 치료)에 사용된다.
본 발명의 맥락에서, 장기간 치료는 예를 들어 충분한 지방 손실이 임의의 의사에게 잘 알려진 매개변수에 의해 나타날 때까지 적어도 수일, 수주, 또는 수개월 동안 지속되는 치료 창(treatment window)을 포함하는 것으로 이해되어야 한다.
또한, 본 발명의 일 예의 맥락에서, 장기간 치료는 만성 치료, 예를 들어 치료에 대해 예상되는 종료점이 없더라도 때때로 장기간 일일 투여를 포함한다. 일 예에서, 장기간 치료는 적어도 1주의 A3AR 리간드의 일일 투여, 때때로, 1개월 일일 치료, 때때로, 적어도 2, 3, 4, 5, 6, 또는 12개월의 리간드의 일일 투여를 포함한다.
A3AR 리간드에 의한 "치료"를 언급할 때, 비만의 세계에서 알려진 매개변수에 의해 결정된 바와 같이 피험자의 웰빙에서 의학적으로 유의한 개선을 야기하는 임의의 바람직한 약리학적 및 생리학적 효과를 나타내는 것으로 이해되어야 한다. 예를 들어, 개선은 피험자의 총 체질량 수준 또는 체지방량 수준에서 적어도 1%, 때때로 5%의 감소에 의해 결정될 수 있다.
일 예에서, 치료는 과도한 말초 지방 축적, 예를 들어 과도한 지방 조직과 관련된 질병으로 고통받는 것으로 정의되는 피험자에 대한 것이다.
일 예에서, 치료는 실제로 체중 증가의 경향 또는 소인이 있는 피험자에 대한 예방 치료이다. 때때로, A3AR 리간드를 사용한 치료는 (예를 들어, 부작용으로서) 체질량의 증가를 야기하는 것으로 알려진 다른 치료에 후속하거나 또는 조합될 수 있다.
A3AR 리간드는 매일 또는 투여 사이에 하루 또는 그 이상의 간격으로 투여될 수 있다. 일 실시예에서, A3AR 리간드는 만성 치료를 위해 매일 사용된다.
A3AR 리간드는 전신 또는 국소 투여될 수 있다. 이를 위해, A3AR 리간드는 약학적으로 허용가능한 담체와 혼합하여 특정 투여 방식에 적합한 유효량의 A3AR 리간드를 포함하는 약학 조성물을 형성한다.
용어 "약학적으로 허용가능한 담체"는 A3AR 리간드와 반응하지 않고 피험자에게 이의 전달을 용이하게 하기 위해 리간드에 첨가될 수 있는 불활성, 비-독성 물질 중 어느 하나를 의미한다.
하나의 실시예에서, 담체는 경구 투여용 단위 제형의 제조에 허용가능한 것이다.
경구 제형은 환제(pill), 캡슐, 시럽, 에멀젼, 방향산(aromatic powder), 및 기타 다양한 형태일 수 있다. 담체는 때때로 제형의 바람직한 형태에 기초하여 선택된다. 또한, 담체는 때때로, 약물의 안정성을 개선하고, 청소율(clearance rates)을 늦추고, 느린 방출 특성을 부여하고, 바람직하지 않은 부작용 등을 감소시키기 위해, 표적 조직으로의 활성 성분의 전달 또는 침투를 개선시키는 효과를 가질 수 있다. 또한, 담체는 제형에 식용 향미 등을 제공하기 위해, 제형을 안정화시키는 물질 (예를 들어, 보존제)일 수 있다. 담체는 통상적으로 사용되는 임의의 것일 수 있으며, A3AR 리간드와의 용해도 및 반응성 결여와 같은 화학적-물리적 고려사항 및 투여 경로에 의해서만 제한된다. 담체는 첨가제, 착색제, 희석제, 완충제, 붕해제, 습윤제, 보존제, 향미제, 및 약리학적으로 허용가능한 담체를 포함할 수 있다. 또한, 담체는 보조제일 수 있으며, 정의상 예측가능한 방식으로 활성 성분의 작용에 영향을 미치는 물질이다.
경구 투여에 적합한 담체의 일반적인 예는, (a) Cremphor RH40 또는 메틸셀룰로오스 (예를 들어, Methocel A4M Premium)와 같은 적당한 액체 내 현탁액 또는 에멀젼; (b) 캡슐 (예를 들어, 계면활성제, 윤활제 및 불활성 충전제를 함유하는 통상의 경질- 또는 연질-피막 젤라틴 유형), 정제, 로젠지 (여기서, 활성 물질은 수크로오스 및 아카시아 또는 트래거캔스와 같은 향미제 중에 존재하거나, 또는 활성 물질은 젤라틴 및 글리세린과 같은 불활성 염기 중에 존재함), 및 트로키제, 각각은 미리결정된 양의 트래거캔스를 고체 또는 과립으로 함유함; (c) 분말; (d) 일반적으로 가용화 증진제와 조합될 때, 용액; (e) 리포좀 제형; 등을 포함한다.
A3AR 리간드는 적어도 하나의 지방 손실 효과를 달성하는데 효과적인 양으로 사용된다. 본 발명에 따른 "유효량"은 다수의 시험 대상 피험자에게 다양한 양의 A3AR 리간드를 투여한 다음, 양의 함수로서 반응을 플로팅하여 (예를 들어, 여러 유익한 효과를 조합하여) 용이하게 결정될 수 있다. 때때로, 사용되는 양은 투여 방식, 연령, 체중, 체표면적, 성별, 건강 상태 및 피험자의 유전적 요인; 기타 투여 약물; 등과 같은 다양한 요인에 따라 달라질 수 있다.
A3AR 리간드의 유효량은 단위 제형에 의해 정의될 수 있다. 용어 "단위 제형"은 인간 피험자 및 기타 포유류에 대해 단일 투여량으로서 적합한 물리적으로 분리된 단위를 나타내며, 각 단위는 적당한 약학적 부형제와 함께 원하는 치료 효과를 야기하도록 계산된 활성 물질의 미리결정된 양을 함유한다.
A3AR 리간드가 A3AR 작용제인 경우, 유효량은 예를 들어 적어도 약 10 mg/day의 양, 예를 들어, 1일 1회 치료의 치료 요법에서 적어도 약 10 mg, 1일 2회 적어도 약 5 mg, 1일 3회 적어도 약 3.3 mg 등일 수 있다.
적어도 약 10 mg/day의 용량은 적어도 약 15 mg/day, 적어도 약 20 g/day, 적어도 약 25 mg/day의 용량일 수 있다. 일 실시예에서, 용량은 25±5mg/day 이다.
투여 횟수와 상관없이, 하루에 환자에게 제공되는 A3AR 리간드의 총량은 본 명세서에서 "일일 치료 용량"으로 언급된다.
따라서, 하나의 예에서, A3AR 리간드는 적어도 10mg/day의 일일 치료 용량의 투여를 위한 단위 제형으로 제형화된다. 제형이 하루에 n 용량을 포함하는 치료 요법으로 환자에게 투여하기 위한 경우, 단위 제형은 일일 치료 용량의 1/n 부분을 포함할 수 있다 (예를 들어, 계획된 일일 치료 용량이 20 mg이고 치료 요법이 1일 2회인 경우, 각 단위 제형은 10 mg의 용량을 가질 것이다; 또는 계획된 1일 치료 용량이 25 mg이고 치료 요법이 1일 2회인 경우, 각 단위 제형은 12.5 mg의 용량을 가질 것이다).
일 예에서, A3AR 리간드는 항-비만 치료와 조합하여 투여된다. 본 발명의 맥락에서, 항-비만 치료는 식사 계획 및 특수 식이, 신체 활동 계획, 약물 치료, 비만 수술(bariatric surgery), 체중 감량 장치를 포함하는 당해 기술분야에서 알려진 임의의 치료를 포함할 수 있다.
일 예에서, A3AR 리간드는 시판되고 의약적으로 허용가능한 체중 감량 약물과 조합하여 사용된다. 시판되고 FDA 승인된 약제의 예는 오를리스타트(Orlistat) (Alli, Xenical), 로르카세린(Lorcaserin) (Belviq), 펜테르민(Phentermine) 및 토피라메이트(Topiramate) (Qsymia), 부프로피온(Bupropion) 및 날트렉손 (Naltrexone) (Contrave), 리라글루티드(Liraglutide) (Saxenda, Victoza)를 포함한다.
비만이 있거나 또는 30 이상의 체질량 지수 (BMI)를 갖는 것으로 진단된 피험자에서 치료가 시작되기 전의 체중에 비해 총 체중의 적어도 3%, 때때로 적어도 4% 또는 적어도 5%의 적어도 체중 감량이 있는 경우, 치료가 효과적인 것으로 간주되어야 함을 이해하여야 한다. 일 예에서, 효과적인 치료는 치료가 시작되기 전의 총 체중의 적어도 3% 내지 6% 또는 5% 내지 10%의 체중 감량이 있는 것이다.
본 명세서에서 사용된 바와 같이, 형태 "a", "an" 및 "the"는 문맥이 명확하게 달리 지시하지 않은 한, 단수 및 복수 지시대상을 포함한다. 예를 들어, 용어 "A 3 AR 리간드"는 A3AR의 활성을 직접적으로 또는 간접적으로, 완전히 또는 부분적으로, 특이적으로 영향을 미칠 수 있는 하나 이상의 화합물을 포함한다.
또한, 본 명세서에서 사용된 바와 같이, 용어 "포함하는"은 조성물이 열거된 활성제, 즉, A3AR 리간드를 포함하나, 다른 요소, 예를 들어 생리학적으로 허용가능한 담체 및 부형제 뿐만 아니라 다른 활성제를 배제하지 않음을 의미하는 것이다. 용어 "본질적으로 이루어지는"은 열거된 요소를 포함하나, 지방 손실 효과 중 어느 하나에 본질적인 중요성을 가질 수 있는 다른 요소를 배제하는 조성물을 정의하는데 사용된다. 따라서, "이루어지는"은 미량 요소보다 많은 다른 요소들을 배제하는 것을 의미한다. 이러한 전이 용어들 각각에 의해 정의되는 실시예는 본 발명의 범위 내에 있다.
또한, 모든 수치는, 예를 들어, 활성 성분으로 A3AR 리간드를 포함하는 조성물을 구성하는 요소의 양 또는 범위를 언급할 때, 명시된 값의 최대 20%, 때때로 최대 10% 까지 (+) 또는 (-) 변화되는 근사치이다. 비록 모든 수명칭(numerical designations)에 용어 "약"이 선행한다고 항상 명확하게 명시하지 않더라도 이해하여야 한다.
본 명세서에 개시된 주제를 더 잘 이해하고 그것이 실제로 수행될 수 있는 방법을 예시하기 위하여, 이제 첨부된 도면을 참조하여 비-제한적인 예로서만 실시예를 설명할 것이다:
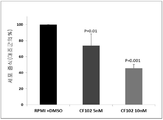
도 1은 대조군 (RPMI+DMSO)에 대하여, 2개 용량의 Cl-IB-MECA (CF102)를 이용한 지방세포 세포 증식의 용량 의존적 저해를 나타내는 막대 그래프이다.
도 2a-2b는 3T3-L1 지방세포에 의해 생성된 지질 액적의 축적을 나타내는 현미경 영상이다: 도 2a는 비히클만으로 처리한 후의 축적을 나타낸다; 도 2b는 5nM의 Cl-IB-MECA로 세포의 처리 후의 축적 수준을 나타낸다.
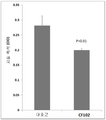
도 3은 대조군 (DMEM 고 글루코오스 + 10% FBS)에 비해, 5nM의 Cl-IB-MECA로 3T3-L1 지방세포의 처리 후 3T3-L1 지방세포에 의해 생성된 지질 액적 축적의 광학 밀도를 나타내는 막대 그래프이다.
도 4a-4b는 연구 기간 내내 일반 식이(regular diet)를 공급한 마우스 체중의 변화를 나타낸다. 12주에 CF102 또는 비히클로 처리가 시작되었거나 (도 4a), 또는 연구 기간 내내 고지방 식이 (HFD)를 공급한 마우스 체중의 변화가 시작되었다. 12주에 CF102 또는 비히클로 처리가 시작되었다(도 4b).
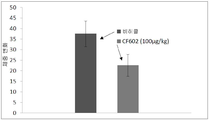
도 5는 STZ에 의해 유도된 당뇨병의 실험 랫트 모델에서, A3AR 알로스테릭 조절제(allosteric modulator)인 CF602가 체중에 미치는 영향을 나타내는 그래프이다.
도 1은 대조군 (RPMI+DMSO)에 대하여, 2개 용량의 Cl-IB-MECA (CF102)를 이용한 지방세포 세포 증식의 용량 의존적 저해를 나타내는 막대 그래프이다.
도 2a-2b는 3T3-L1 지방세포에 의해 생성된 지질 액적의 축적을 나타내는 현미경 영상이다: 도 2a는 비히클만으로 처리한 후의 축적을 나타낸다; 도 2b는 5nM의 Cl-IB-MECA로 세포의 처리 후의 축적 수준을 나타낸다.
도 3은 대조군 (DMEM 고 글루코오스 + 10% FBS)에 비해, 5nM의 Cl-IB-MECA로 3T3-L1 지방세포의 처리 후 3T3-L1 지방세포에 의해 생성된 지질 액적 축적의 광학 밀도를 나타내는 막대 그래프이다.
도 4a-4b는 연구 기간 내내 일반 식이(regular diet)를 공급한 마우스 체중의 변화를 나타낸다. 12주에 CF102 또는 비히클로 처리가 시작되었거나 (도 4a), 또는 연구 기간 내내 고지방 식이 (HFD)를 공급한 마우스 체중의 변화가 시작되었다. 12주에 CF102 또는 비히클로 처리가 시작되었다(도 4b).
도 5는 STZ에 의해 유도된 당뇨병의 실험 랫트 모델에서, A3AR 알로스테릭 조절제(allosteric modulator)인 CF602가 체중에 미치는 영향을 나타내는 그래프이다.
본 발명은 이제 본 발명에 따라 수행된 하기 실험의 설명에서 예시될 것이다. 이들 예는 제한이 아니라 예시의 성질을 갖는 것으로 이해하여야 한다. 명백하게, 상기 교시에 비추어 이들 예의 많은 변형 및 변화가 가능하다. 따라서, 첨부된 청구범위의 범위 내에서, 본 발명은 하기에 구체적으로 기재된 것과는 달리 무수히 많은 가능한 방법으로 실시될 수 있음을 이해하여야 한다.
비-제한적인 실시예
실시예 1 - 3T3-L1 지방세포 증식에 대한 CF102 효과
3T3-L1 전구-지방세포(pre-adipocytes)는 ATCC (American Type Culture Collection; Manassas, VA, USA)에서 구입하였다. 전구-지방세포는 5% CO2, 37℃에서 10% 신생아 송아지 혈청 (Hyclone) 및 항생제 (Hyclone)를 보충한 DMEM (Dulbecco's modified Eagle's medium; Hyclone, South Logan, UT, USA)에서 유지시켰다.
지방세포 분화를 유도하기 위해, 전구-지방세포를 24-웰 플레이트에 플레이팅하였다. 합류(confluence) 후, 배지를 교체하고 10 μg/ml 인슐린, 1 μM DEX 및 0.5 mM IBMX를 첨가하였다. 2일 후, 배지를 10% FBS 및 10 μg/ml 인슐린이 보충된 기본 배지로 교체하였다. 배지는 8-14일 동안 2일마다 교체하였다.
세포 증식을 평가하기 위해, 3H-티미딘 결합 분석을 사용하였다. 3T3-L1 세포 (5,000 세포/웰)를 48시간 동안 5 또는 10 nM CF102 96-웰 플레이트와 함께 배양하였다. 각 웰을 지난 24시간 동안 1mCi 3H-티미딘으로 펄스화하였다. 세포를 수확하고, LKB 액체 섬광 계수기 (LKB, Piscataway, NJ, USA)에서 3H-티미딘 흡수를 측정하였다.
결과:
도 1은 3T3-L1 지방세포의 증식에 대한 CF102의 용량 의존적 저해 효과를 나타낸다. CF102 5nM 및 10nM와 함께 배양된 지방세포는 대조군 측정에 비해, 각각 20% 및 40% 이상의 감소를 나타내었다.
실시예 2 - 3T3-L1 지방세포에서 지질 생성에 대한 CF102 효과
전구-지방세포를 10 μg/ml 인슐린, 1μM DEX 및 0.5 mM IBMX를 함유하는 분화 배지(DMEM 고 글루코오스 + 10% FBS)에서 배양하였으며, 48h 동안 5nM CF102로 처리하여 이의 잠재적인 항-지방생성 효과를 평가하였다.
Oil-Red-O로 염색하여 지질 액적의 축적을 평가하였다. 간략하게, 세포를 PBS로 세척하고, 1 hr 동안 3.7% HCHO와 함께 배양한 다음, 45분 동안 Oil-Red-O 용액과 함께 배양하였다. 세포를 아주 잘 세척하여 과량의 Oil-Red-O를 제거하고, 라이카 카메라(Leica camera)가 있는 올림푸스 현미경(Olympus microscope)으로 시각화하고 사진을 찍었다. 지질 축적의 정량화를 위해, 세포를 이소프로판올에 용해시키고 광학 밀도를 595 nm에서 Dynatech Corp. Microelisa 판독기 (Chantilly, VA)에서 판독하였다. 지질 액적의 축적 정도는 광학 밀도에 비례하였다.
지질 액적의 축적은 현미경 하에서 시각화하였으며 도 2a-2b에서 볼 수 있다. 여기서 도 2a는 대조군 측정의 현미경 영상을 나타내며, 도 2b는 5nM의 CF102로 처리된 전구-지방세포로부터 유래된 지질 액적의 현미경 영상을 나타낸다.
결과:
도 3은 5nM CF102에 미리-노출된 세포의 지질 축적의 저해를 나타낸다. 자료는 비히클 처리군 (대조군) 대 CF102 처리군에서 595nm에서의 OD 값으로 나타낸다. (p=0.01).
실시예 3 - 고지방 식이 (HFD) 마우스 대 일반 식이를 공급한 마우스의 체중에 대한 CF102 효과
당뇨병 및 심혈관 질환과 같은 비만으로 인한 합병증은 일반적으로 수십 년이 걸리기 때문에, 대리 동물 모델은 비만의 분자적 측면 및 이의 병태생리학적 효과를 연구하는데 중요하다. 증가하는 관심을 받고 있는 이러한 모델 중 하나는 마우스의 식이-유도 비만 모델이다. 본 프로토콜은 식이-유도 비만의 in vivo 마우스 모델에서 CF102의 효과를 평가하도록 설계되었다.
마우스
사용된 마우스는 4-6주령의 C57BL/6J 수컷이다 (The Jackson Laboratory, stock 000664).
식이
60 kcal% 지방 식이 (Research Diets, D12492i)
CF102 처리
2가지 유형의 처리인, 예방 및 치료를 연구할 것이다.
실험 계획:
군 I-II: 순진한 동물 (n=20)에게 대조군으로 제공된 일반 식이를 공급하고 '저지방 식이(Lean Diet)'로 정의하였다. 12주 후, 마우스를 2개의 군 (군당 n=10)으로 나누고, 제 1 군은 4주 동안 CF102 (Can-Fite BioPharma, Cat# A14402-10; 100μg/Kg)를 매일 경구 투여로 처리하고, 제 2 군은 비히클만으로 처리하였다.
군 III-IV: 순진한 마우스 (n=20)에게 12주 동안 HFD를 공급하였다. 12주 후, 마우스를 2개의 군 (군당 n=10)으로 나누고, 제 1 군은 4주 동안 CF102 (Can-Fite BioPharma, Cat# A14402-10; 100μg/Kg)를 매일 경구 투여로 처리하고, 제 2 군은 비히클만으로 처리하였다.
결과 및 분석
저지방 식이군에서, CF102는 대조군에 비해 동물에서 체중 감량을 야기하였다.
구체적으로, 도 4a는 CF102로 처리된 저지방 식이 하에서의 순진한 마우스가 미처리 순진한 마우스에 비해 어떠한 체중 감량을 나타내지 않았음을 나타낸다. 그러나, 도 4b에 나타난 바와 같이, HFD 하에서의 마우스는 CF102로 처리 시 유의한 (p<0.001) 체중 감량 효과를 나타내었다 (화살표는 처리 개시점을 나타냄).
실시예 4 - A
3
AR 알로스테릭 조절제인 CF602가 당뇨병 랫트의 체중에 미치는 영향
당뇨병은 비만의 합병증 중 하나이다. 따라서, A3AR 리간드가 당뇨병 모델의 체중에 미치는 영향도 평가하였다.
방법:
스프라그 돌리 수컷 랫트 (8-10주령)는 시트레이트 완충액 내 60 mg/kg의 용량 수준으로 스트렙토조토신 (STZ)을 IP 투여하여 당뇨병 모델을 생성하였다. 250 mg/dL 이상의 혈당 수치를 갖는 동물만 연구에 포함시켰다. 알로스테릭 A3AR 리간드인 CF602를 100μg/kg의 용량으로 5일 동안 1일 2회 경구 투여하였다. 5일 후에 체중을 모니터링하였다.
결과:
도 5는 기준선으로부터 체중 변화, 즉 치료 종료 시 체중에서 치료 전 체중을 뺀 것 (즉, 차이)을 나타낸다. 체중 감량은 CF602 처리 동물에서 체중의 유의한 (p<0.03) 감소였다.
Claims (22)
- (a) 피험자의 체중 감소;
(b) 피험자의 체지방량(body fat mass) 감소;
(c) 피험자의 비만 치료; 및
(d) 피험자에서 지방세포 증식의 저해
로부터 선택된 적어도 하나의 지방 손실 효과를 달성하는데 사용하기 위한 A3 아데노신 수용체 (A3AR) 리간드. - 제 1항에 있어서, 상기 리간드는 상기 피험자에게 일일 투여에 적합한 제형으로 존재하는 것을 특징으로 하는, A3AR 리간드.
- 제 2항에 있어서, 상기 제형은 하루에 1회 또는 2회 투여에 적합한 것을 특징으로 하는, A3AR 리간드.
- 제 1항 내지 제 3항 중 어느 한 항에 있어서, 상기 리간드는 경구 투여에 적합한 제형으로 존재하는 것을 특징으로 하는, A3AR 리간드.
- 제 1항 내지 제 4항 중 어느 한 항에 있어서, 상기 A3AR 리간드는 A3AR 작용제인 것을 특징으로 하는, A3AR 리간드.
- 제 5항에 있어서, 상기 A3AR 작용제는 N6-2-(4-아미노페닐)에틸아데노신 (APNEA), N6-(4-아미노-3-아이오도벤질)아데노신-5'-(N-메틸우론아미드) (AB-MECA), N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드 (IB-MECA) 및 2-클로로-N6-(3-아이오도벤질)-아데노신-5'-N-메틸우론아미드 (Cl-IB-MECA)로 이루어진 군으로부터 선택되는 것을 특징으로 하는, A3AR 리간드.
- 제 6항에 있어서, 상기 A3AR 작용제는 Cl-IB-MECA인 것을 특징으로 하는, A3AR 리간드.
- 제 1항 내지 제 4항 중 어느 한 항에 있어서, 상기 A3AR 리간드는 A3AR 알로스테릭 조절제인 것을 특징으로 하는, A3AR 리간드.
- 제 8항에 있어서, 상기 A3AR 알로스테릭 조절제는 하기로 이루어진 군으로부터 선택되는 것을 특징으로 하는, A3AR 리간드:
N-(3,4-디클로로-페닐)-2-시클로펜틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-시클로헵틸-1H-이미다조[4,5-c]퀴놀린-4-아민,
N-(3,4-디클로로-페닐)-2-시클로부틸-1H-이미다조[4,5-c]퀴놀린-4-아민, 및
N-(3,4-디클로로-페닐)-2-시클로헥실-1H-이미다조[4,5-c]퀴놀린-4-아민. - 제 1항 내지 제 9항 중 어느 한 항에 있어서, 항-비만 치료와 조합하는 것을 특징으로 하는, A3AR 리간드.
- - 피험자의 체중 감소;
- 피험자의 체지방량 감소;
- 피험자의 비만 치료; 및
- 피험자에서 지방세포 증식의 저해
로부터 선택된 적어도 하나의 지방 손실 효과를 달성하는데 효과적인 양의 A3AR 리간드를 활성 성분으로 및 약학적으로 허용가능한 담체를 포함하는 약학 조성물. - 제 11항에 있어서, 상기 피험자에게 상기 A3AR 리간드의 일일 투여에 적합한 제형으로 존재하는 것을 특징으로 하는, 약학 조성물.
- 제 12항에 있어서, 하루에 1회 또는 2회 투여에 적합한 제형으로 존재하는 것을 특징으로 하는, 약학 조성물.
- 제 11항 내지 제 13항 중 어느 한 항에 있어서, 상기 피험자의 만성 치료에 적합한 제형으로 존재하는 것을 특징으로 하는, 약학 조성물.
- 제 11항 내지 제 14항 중 어느 한 항에 있어서, 경구 투여에 적합한 제형으로 존재하는 것을 특징으로 하는, 약학 조성물.
- 제 11항 내지 제 15항 중 어느 한 항에 있어서, 상기 A3AR 리간드는 A3AR 작용제인 것을 특징으로 하는, 약학 조성물.
- 제 16항에 있어서, 상기 A3AR 작용제는 Cl-IB-MECA인 것을 특징으로 하는, 약학 조성물.
- 제 11항 내지 제 17항 중 어느 한 항에 있어서, 상기 A3AR 리간드는 A3AR 알로스테릭 조절제인 것을 특징으로 하는, 약학 조성물.
- 제 18항에 있어서, 상기 A3AR 알로스테릭 조절제는 N-(3,4-디클로로-페닐)-2-시클로헥실-1H-이미다조[4,5-c]퀴놀린-4-아민 (CF602)인 것을 특징으로 하는, 약학 조성물.
- - 피험자의 체중 감소;
- 피험자의 체지방량 감소;
- 피험자의 비만 치료; 및
- 피험자에서 지방세포 증식의 저해
로부터 선택된 적어도 하나의 지방 손실 효과를 달성하는데 효과적인 양인, A3AR 리간드의 양을 상기 피험자에게 투여하는 단계를 포함하는, 피험자의 치료 방법. - 제 20항에 있어서, 비만을 치료하기 위한, 방법.
- (a) 제 11항 내지 제 19항 중 어느 한 항에 따른 A3AR 리간드를 포함하는 약학 조성물;
(b) 하기의 효과 중 적어도 하나를 달성하는 약학 조성물의 사용 설명서:
- 피험자의 체중 감소;
- 피험자의 체지방량 감소;
- 피험자의 비만 치료; 및
- 피험자에서 지방세포 증식의 저해;
를 포함하는, 키트.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IL264112 | 2019-01-06 | ||
| IL264112A IL264112A (en) | 2019-01-06 | 2019-01-06 | Adenosine a3 receptor ligand for use in lowering adipocyte levels |
| PCT/IL2020/050011 WO2020141535A1 (en) | 2019-01-06 | 2020-01-05 | An a3 adenosine receptor ligand for use for achieving a fat loss effect |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210113279A true KR20210113279A (ko) | 2021-09-15 |
Family
ID=65656120
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217024682A KR20210113279A (ko) | 2019-01-06 | 2020-01-05 | 지방 손실 효과를 달성하는데 사용하기 위한 a3 아데노신 수용체 리간드 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20220079968A1 (ko) |
| EP (1) | EP3906034A1 (ko) |
| JP (2) | JP2022517753A (ko) |
| KR (1) | KR20210113279A (ko) |
| CN (1) | CN113543790A (ko) |
| AU (1) | AU2020205042B2 (ko) |
| BR (1) | BR112021013084A2 (ko) |
| CA (1) | CA3126002A1 (ko) |
| IL (2) | IL264112A (ko) |
| MX (1) | MX2021008172A (ko) |
| WO (1) | WO2020141535A1 (ko) |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5443836A (en) | 1993-03-15 | 1995-08-22 | Gensia, Inc. | Methods for protecting tissues and organs from ischemic damage |
| US5688774A (en) | 1993-07-13 | 1997-11-18 | The United States Of America As Represented By The Department Of Health And Human Services | A3 adenosine receptor agonists |
| ATE206432T1 (de) | 1993-07-13 | 2001-10-15 | Nasa | A3 -adenosin -rezeptor agonisten |
| WO1997027173A2 (en) | 1996-01-24 | 1997-07-31 | Sumitomo Chemical Company, Limited | Dihalopropene compounds, their use as insecticides/acaricides and intermediates for their production |
| AU8764398A (en) | 1997-07-29 | 1999-02-22 | Medco Research, Inc. | N6-substituted-adenosine-5'-uronamides as adenosine receptor modulators |
| US6048865A (en) | 1997-07-29 | 2000-04-11 | Medco Research, Inc. | N6 -substituted-adenosine-5'-uronamides as adenosine receptor modulator |
| US6329349B1 (en) | 1997-10-23 | 2001-12-11 | Trustees Of The University Of Pennsylvania | Methods for reducing ischemic injury of the heart via the sequential administration of monophosphoryl lipid A and adenosine receptor agents |
| IL133680A0 (en) | 1999-09-10 | 2001-04-30 | Can Fite Technologies Ltd | Pharmaceutical compositions comprising an adenosine receptor agonist or antagonist |
| US6946449B2 (en) | 2001-07-13 | 2005-09-20 | Cv Therapeutics, Inc. | Partial and full agonists of A1 adenosine receptors |
| CN101410114B (zh) | 2006-01-26 | 2012-07-04 | 美国政府卫生与公共服务部 | A3腺苷受体别构调节剂 |
| EP2806878A1 (en) | 2012-01-23 | 2014-12-03 | Can-Fite Biopharma Ltd. | Treatment of liver conditions |
| IL242723B (en) * | 2015-11-23 | 2019-12-31 | Can Fite Biopharma Ltd | A3 adenosine receptor ligand for the treatment of ectopic fat accumulation |
| KR101881441B1 (ko) * | 2017-01-20 | 2018-07-24 | 서울대학교산학협력단 | 다중 약리단 특성에 기반한 비정상적 아디포넥틴 관련 질환 치료용 조성물 |
-
2019
- 2019-01-06 IL IL264112A patent/IL264112A/en unknown
-
2020
- 2020-01-05 JP JP2021539140A patent/JP2022517753A/ja active Pending
- 2020-01-05 CN CN202080008167.6A patent/CN113543790A/zh active Pending
- 2020-01-05 US US17/309,952 patent/US20220079968A1/en active Pending
- 2020-01-05 AU AU2020205042A patent/AU2020205042B2/en active Active
- 2020-01-05 MX MX2021008172A patent/MX2021008172A/es unknown
- 2020-01-05 CA CA3126002A patent/CA3126002A1/en active Pending
- 2020-01-05 KR KR1020217024682A patent/KR20210113279A/ko unknown
- 2020-01-05 BR BR112021013084-5A patent/BR112021013084A2/pt unknown
- 2020-01-05 EP EP20700855.8A patent/EP3906034A1/en active Pending
- 2020-01-05 WO PCT/IL2020/050011 patent/WO2020141535A1/en active Application Filing
-
2021
- 2021-06-29 IL IL284463A patent/IL284463A/en unknown
-
2023
- 2023-05-10 JP JP2023078136A patent/JP2023100928A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CN113543790A (zh) | 2021-10-22 |
| BR112021013084A2 (pt) | 2021-09-21 |
| US20220079968A1 (en) | 2022-03-17 |
| JP2022517753A (ja) | 2022-03-10 |
| WO2020141535A1 (en) | 2020-07-09 |
| MX2021008172A (es) | 2021-08-11 |
| IL284463A (en) | 2021-08-31 |
| IL264112A (en) | 2020-07-30 |
| CA3126002A1 (en) | 2020-07-09 |
| AU2020205042B2 (en) | 2024-10-10 |
| JP2023100928A (ja) | 2023-07-19 |
| EP3906034A1 (en) | 2021-11-10 |
| AU2020205042A1 (en) | 2021-07-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2239455C2 (ru) | Фармацевтические композиции, содержащие агонист или антагонист аденозинового рецептора | |
| AU2015320975B2 (en) | Combination treatment of SGLT2 inhibitors and dopamine agonists for preventing metabolic disorders in equine animals | |
| US20080300213A1 (en) | Use of A3 Adenosine Receptor Agonist in Osteoarthritis Treatment | |
| US11291681B2 (en) | Method for treating fibrotic liver tissue using Cl-IB-MECA | |
| JP2007517019A (ja) | 多発性硬化症の治療方法 | |
| JP2008519029A (ja) | 加速骨吸収の治療的処置 | |
| KR20210113279A (ko) | 지방 손실 효과를 달성하는데 사용하기 위한 a3 아데노신 수용체 리간드 | |
| ES2315569T3 (es) | Procedimiento de tratamiento de trastornos del movimiento usando derivados de acido barbiturico. | |
| AU2021271500A1 (en) | Composition containing sesamin or like and NR and/or NMN | |
| JP6140825B2 (ja) | 性機能不全の治療に使用するためのa3アデノシン受容体リガンド | |
| JP2005526086A (ja) | 癌の治療用のcdk阻害剤と5−fuの組合せ | |
| US20210069227A1 (en) | A3 adenosine receptor ligand for managing cytokine release syndrome | |
| Chaudhari | Innovative Drug Discovery |