KR20210049026A - 뇌졸중의 혈액 바이오마커 - Google Patents
뇌졸중의 혈액 바이오마커 Download PDFInfo
- Publication number
- KR20210049026A KR20210049026A KR1020207035973A KR20207035973A KR20210049026A KR 20210049026 A KR20210049026 A KR 20210049026A KR 1020207035973 A KR1020207035973 A KR 1020207035973A KR 20207035973 A KR20207035973 A KR 20207035973A KR 20210049026 A KR20210049026 A KR 20210049026A
- Authority
- KR
- South Korea
- Prior art keywords
- stroke
- signature
- leu
- ala
- subject
- Prior art date
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/106—Pharmacogenomics, i.e. genetic variability in individual responses to drugs and drug metabolism
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Analytical Chemistry (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Physics & Mathematics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pathology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Biomedical Technology (AREA)
- General Physics & Mathematics (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
뇌졸중은 유의적으로 사망, 장애 및 건강 관리 비용의 원인이 되는, 대단히 파괴적인 장애이다. 현 도전과제는 후기의 세포 사멸을 예방하고, 동시 요법을 이용하여 치료창을 확장시키는 것이다. 뇌졸중을 진단하는 잠재적 진단 방법은 바이오마커로서 혈액 중 RNA를 사용하는 것이며, 이는 의학에서 새롭게 부상한 분야이다. 본원에서, 본 발명자들은 대뇌 허혈 발병 후, 뇌 및 혈액 중 유전자 발현을 연구한다. 뇌 및 혈액으로부터의 마카크 마이크로어레이 발현 데이터 연구를 통해 허혈성 및 비허혈성 샘플은 그의 발현 프로파일에 기초하여 구별될 수 있고, 고도로 차별적으로 발현된 유전자 대다수는 허혈 시나리오에서 허혈 후 6시간째 상향 조절된다는 것이 밝혀졌다. 뇌 및 혈액에서 차별적으로 발현된 유전자의 비교 결과, 유전자 발현 패턴이 유의적으로 중복되는 것으로 밝혀졌다. 데이터에서는 허혈성 뇌와 혈액 사이에 공통된 시그니쳐가 존재하는 것으로 나타났고, 이는 환자에서 신경보호 약물의 평가를 위해 이루어지는 동반 바이오마커 개발을 위한, 허혈성 뇌졸중 환자를 특징화하는 생검 트랜스크립톰 발현 프로파일링을 위한 도구로서의 혈액 트랜스크립톰의 개발을 뒷받침한다.
Description
본 발명의 기술분야
본 발명은 특히, 뇌졸중의 혈액 바이오마커(biomarker), 및 특히, 허혈성 뇌졸중(ischemic stroke)에서 요법의 효능을 모니터링하기 위한, 진단 목적으로, 단기간 및 장기간 예후를 위해서 뿐만 아니라, 위험도 평가를 위한 그의 용도에 관한 것이다.
본 발명의 배경
뇌졸중은 전세계 주요 사망 원인 중 2위이고, 장애의 주된 원인 중 3위이다 (문헌 [McKay & Mensah, 2005. The atlas of heart disease and stroke (1st ed.). Geneva: World Health Organization]). 대뇌 국소 허혈, 즉, 허혈성 뇌졸중은 경색 핵심에서 심각하고, 빠른 조직 손상을 일으킨다. 초기 손상 후, 뇌 세포 사멸은 느리게 진행되어, 반영부(penumbra)로 불리는 핵심 주변의 이질성 부위로까지 확장된다 (문헌 [Astrup et al., 1977. Stroke. 8(1):51-7]). 허혈성 반영부를 구제하면, 장애에 있어서의 결과를 개선시킨다 (문헌 [Emberson et al., 2014. Lancet. 384(9958):1929-35]).
현재까지, 유일한 응급 치료 해결 방법은 혈전용해 및/또는 혈전절제술을 통한 재소통(recanalization)이다. 그러나, 짧은 개입창(intervention window) (재소통의 경우, < 6 h, 및 혈전용해의 경우, 4 h 30) 및 출혈 변화 위험에 기인하여, 단지 소수의 급성 허혈성 뇌졸중 환자만이 상기 치료 자격이 있다. 예를 들어, AHA/ASA 기준에 따르면, 종합 뇌졸중 센터에 6시간 이내에 도착한 모든 환자 중에서 단 10.5%만이 혈전절제술을 받을 수 있는 혈관내-자격이 있는 것으로 추정된다 (문헌 [Vanacker et al., 2016. Stroke. 47(7):1844-9]).
그러므로, 치료창을 확장시키는 새로운 치료 전략법을 개발하는 것이 주요 공중 건강 문제가 된다. 이전에는 다수의 임상 시험이 실패하였지만, 재소통의 출현으로 인해 재소통과 연관된 신경보호는 여전히 치료창을 확장시킬 수 있는 잠재적으로 유망한 전략법이다. 말초 단백질, 핵산, 또는 지질을 이용하여 허혈성 뇌졸중 진단을 확인하고, 질환 진행을 모니터링할 수 있다는 것을 제안하는 증거가 증가하고 있다. 그러나, 현재까지, 어느 것도 임상 실습에서 시행되고 있지 않다 (문헌 [Kim et al., 2013. J Stroke. 15(1):27-37]).
바이오마커 검사란, 질환의 존재, 진행 또는 중증도, 또는, 치료 효과를 나타내는, 하나 또는 수개의 마커의 존재 또는 부재를 정성적으로 평가하거나, 또는 정량적으로 측정하는 데 사용될 수 있는, 영상화, 화학적 또는 다른 생물학적 검사를 지칭한다. 중추 신경계 (CNS) 영상화의 경우, 엄청난 발전이 이루어졌지만, 한편으로는 말초 생물한적 마커 확인은 덜 발달하였다. 혈액은 뇌와 직접 접촉하지 않기 때문에, CNS 질환 및 치료에 대한 강건한 바이오마커로서 적용되는 혈액 바이오마커를 확인하는 것이 현대 신경학에서 가장 중요한 도전과제 중 하나가 된다.
진단 마커로서 혈액 중 RNA를 사용하는 것은 유방암, 관상 동맥 질환 및 감염성 질환 진단에서의 그의 임상적 적용에 의해 뒷받침되는, 새롭게 부상한 분야이다 (문헌 [Rothstein & Jickling, 2013. Biomark Med. 7(1):37-47]). 추가로, 혈액 중 RNA는 조기 임상 시험에서 신경보호제의 효과를 평가하기 위한 동반 진단제로서 사용될 수 있다. 급성 허혈성 뇌졸중에서 진단 바이오마커로서의 RNA 연구는, 코딩 RNA의 경우, 극소수의 환자만이 급성기의 경색을 앓는 소수의 환자를 포함하는 것을 비롯하여 드물다 (문헌 [Tang et al., 2006. J Cereb Blood Flow Metab. 26(8):1089-102]; [Stamova et al., 2010. Stroke. 41(10):2171-7]). 최근, 급성기의 뇌졸중 경색이 아닌, 위험 인자로서의 뇌졸중의 잠재적인 바이오마커로서 비코딩 RNA에 대한 특별한 관심이 급증하고 있다 (문헌 [Mick et al., 2017. Stroke. 48(4):828-834]).
트랜스크립톰 분석은 대뇌 허혈을 이용하는 다수의 실험 연구에서 유전자 발현 변화를 측정하는 데 사용되고 있다. 대부분의 실험적 트랜스크립톰 연구는 국소 또는 전뇌 허혈을 앓는 래트 및 마우스 모델에서 수행되었다 (리뷰를 위해, 문헌 [Cox-Limpens et al., 2014. Brain Res. 1564:85-100] 참조). 허혈 이외에도, 전처치 또한 설치류에서 내인성 뇌 보호를 연구하기 위한 도구로서 사용되고 있다. 상기 설치류에서 트랜스크립톰을 조사한 마이크로어레이 연구 결과, 대뇌 허혈 동안 극초기 유전자, 스트레스 반응 유전자, 아폽토시스 유전자, 신호 전달 유전자, 신경전달 유전자, 이온 채널 유전자, 염증 유전자, 세포골격 유전자, 리보솜 유전자, 및 신경영양성 인자 유전자는 발현 변화를 겪는 것으로 밝혀졌다 (문헌 [Schmidt-Kastner et al., 2002. Brain Res Mol Brain Res. 108(1-2):81-93]; [Buttner et al., 2009. Brain Res. 1252:1-14]; [Wang et al., 2011. Brain Res. 1372:13-21]; [Wang et al., 2012. Neuroscience. 220:100-8]; [Lu et al., 2004. J Neurosci Res. 77(6):843-57]). 그러나, 본 발명자들이 아는 바로는, 단지 극소수의 실험만이 영장류에서 수행되었다 (문헌 [Cook et al., 2012. Nature. 483(7388):213-7]; [Cook & Tymianski, 2012. Neurotherapeutics. 9(2):371-9]). 영장류는 인간과 고도로 유사한 게놈 뿐만 아니라, 해부학적 상동성도 갖고 있는 바, 뇌 허혈을 연구하기 위한 고유의 모델을 나타낸다. 예를 들어, 그렇지 않은 설치류와 달리, 영장류 및 인간, 둘 모두 비-뇌회결손 뇌를 갖는다 (즉, 피질에서 주름을 나타낸다; 추뇌류). 추가로, 인간 및 침팬지, 둘 모두에서 대뇌 피질의 트랜스크립톰은 서로 매우 유사하고, 개체내 영역 사이에서보다 개체간에 더 많이 상이하다 (문헌 [Khaitovich et al., 2004. Genome Res. 14(8):1462-73]).
동물 연구로부터의 신경보호 요법을 인간에서의 적용으로 해석하는 데 있어 성공하지 못한 주요 원인으로서 4가지가 확인되었다 (문헌 [Moretti et al., 2015. Pharmacol Ther. 146:23-34]; [Timsit & Menn, 2012. Clin Pharmacol Ther. 91(2):327-32]):
i) 임상전 연구의 품질 불량:
임상전 연구를 위해, 본 분야에서의 도전과제는 예컨대, STAIR 기준 (문헌 [Stroke Therapy Academic Industry Roundtable (STAIR), 1999. Stroke. 30(12):2752-8]; [Fisher et al., 2009. Stroke. 40(6):2244-50])과 같은 임상전 연구에서의 품질 점수 기준의 개발; 및 인간에서의 무작위 맹검 연구 (문헌 [Llovera et al., 2015. Sci Transl Med. 7(299):299ra121])의 개발을 통해 계속해서 극복되고 있는 중이다.
ii) 조기 임상 개발에서 생물학적 동반 약력학적 바이오마커의 부재:
현재, 신약 개발을 위해 동반 바이오마커가 점점 더 많이 이용되고 있다. 이환된 환자에서 안전 용량으로 효능을 달성할 수 있는지 여부에 관한 신뢰를 얻기 위해, 추후 단계에서 필요한 큰 투자 이전에 비교적 짧은 지속 기간의 Ib 상 임상 연구가 관련 질환을 앓는 소수의 환자에서 수행된다. 이는 약력학적 바이오마커 중 일부의 가장 중요한 적용이다 (문헌 [Zhao et al., 2015. Clin Chem. 61(11):1343-53]).
iii) II 상 인구 연구에서 반영부 추정을 위한 예측 영상화 바이오마커의 부재:
선택된 환자에서 반영부를 구제하는 DAWN 연구에서 제시된 바와 같이, 혈전절제술에 적합한 환자를 확인하기 위해 대뇌 영상화에 기초하여 환자를 선별하는 것은 현재 중요하다 (문헌 [Jovin et al., 2017. Int J Stroke. 12(6):641-652]; [Chaisinanunkul et al., 2015. Stroke. 46(8):2238-43]; [Nogueira et al., 2018. N Engl J Med. 378(1):11-21]). 반영부 특징에 기초한 선별은 오직 소수의 신경보호 연구에서만 수행되어 왔다 (리뷰를 위해, 문헌 [Donnan et al., 2009. Lancet Neurol. 8(3):261-9] 참조). 오늘날, 이러한 신규 개념은 재소통 또는 재관류를 기다리면서, 치료 개입에 유용한 방안을 제공할 수 있다 (문헌 [Hillis & Baron, 2015. Front Neurol. 6:85]).
iv) 끝으로 재소통의 부재:
혈전절제술은 비록 그의 사용이 확산되어야 할 필요는 있지만, 급성기의 허혈성 뇌졸중에서 표준 치료가 되고 있다. AHA/ASA 기준에 따르면, 종합 뇌졸중 센터에 6시간 이내에 도착한 모든 환자 중에서 단 10.5%만이 혈전절제술을 받을 수 있는 "혈관내-자격이 있는 것"으로 추정된다 (문헌 [Vanacker et al., 2016. Stroke. 47(7):1844-9]).
대뇌 허혈에 걸린 조직에서의 유전자 발현 패턴을 더욱 잘 이해하는 것이 진단 기술을 개선시킬 수 있다. 여기서, 본 발명자들은 대뇌 허혈 발병 후, 뇌 및 혈액에서의 유전자 발현을 연구하였다. 뇌 및 혈액으로부터의 마카크 마이크로어레이 발현 데이터 연구 결과, 허혈성 및 비-허혈성 샘플은 그의 발현 프로파일에 기초하여 구별될 수 있고, 매우 차별적으로 발현되는 유전자는 대부분은 허혈 시나리오에서 허혈 후 6시간째 상향 조절된다. 뇌 및 혈액에서 차별적으로 발현된 유전자 비교 결과, 유전자 발현 패턴이 유의적으로 중복되는 것으로 밝혀졌다. 놀랍게도, 데이터에서는 허혈성 뇌와 혈액 사이에 공통된 코딩 시그니쳐(signature)가 존재하는 것으로 나타났고, 이는 환자에서 신경보호 약물의 평가를 위해 이루어지는 동반 바이오마커 개발을 위한, 허혈성 뇌졸중 환자를 특징화하는 생검 트랜스크립톰 발현 프로파일링을 위한 도구로서의 혈액 트랜스크립톰의 개발을 뒷받침한다.
요약
본 발명은
i) PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 2개의 바이오마커의 발현 수준을 측정함으로써 대상체로부터 수득된 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는 것인 단계;
ii) 단계 i)에서 결정된 시그니쳐를 참조 시그니쳐(reference signature)와 비교하는 단계; 및
iii) 시그니쳐 중 적어도 2개의 바이오마커의 발현 수준이 참조 시그니쳐 중의 동일한 적어도 2개의 바이오마커의 발현 수준보다 더 높은 경우, 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함하는, 대상체에서 뇌졸중을 진단하는 방법에 관한 것이다.
한 실시양태에서, 대상체에서 뇌졸중을 진단하는 방법의 단계 i)는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 3개의 바이오마커의 발현 수준을 측정하는 것을 포함한다.
한 실시양태에서, 대상체에서 뇌졸중을 진단하는 방법의 단계 i)는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM의 발현 수준을 측정하는 것을 포함한다.
한 실시양태에서, 참조 시그니쳐는 실질적으로 건강한 대상체로 이루어진 참조 집단(reference population)에서 바이오마커의 발현 수준을 측정함으로써 수득된다.
한 실시양태에서, 본 발명에 따른 대상체에서 뇌졸중을 진단하는 방법은 뇌졸중을 뇌졸중 유사 질환(stroke mimic)과 구별하는 것을 목적으로 한다.
본 발명은 추가로
i) PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 2개의 바이오마커의 발현 수준을 측정함으로써 대상체로부터 수득된 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는 것인 단계;
ii) 단계 i)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iii) 시그니쳐 중 적어도 2개의 바이오마커의 발현 수준이 참조 시그니쳐 중의 동일한 적어도 2개의 바이오마커의 발현 수준보다 더 낮은 경우, 대상체는 반응을 달성하였다고 결론짓는 단계를 포함하는, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법에 관한 것이다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법의 단계 i)은 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 9개의 바이오마커의 발현 수준을 측정하는 것을 포함한다.
한 실시양태에서, 참조 시그니쳐는 상기 요법 시작 전 동일한 대상체로부터 수득된 샘플 중 바이오마커의 발현 수준을 측정함으로써 수득된다.
본 발명은
i) PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 2개의 바이오마커의 발현 수준을 측정함으로써 대상체로부터 수득된 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는 것인 단계;
ii) 단계 i)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iii) 시그니쳐 중 적어도 3개의 바이오마커의 발현 수준이 참조 시그니쳐 중의 동일한 적어도 3개의 바이오마커의 발현 수준보다 더 높은 경우, 대상체는 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함하는, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법에 관한 것이다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법의 단계 i)는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로부터 선택되는 9개의 바이오마커의 발현 수준을 측정하는 것을 포함한다.
한 실시양태에서, 참조 시그니쳐는 실질적으로 건강한 대상체로 이루어진 참조 집단에서 바이오마커의 발현 수준을 측정함으로써 수득된다.
한 실시양태에서, 대상체는 뇌졸중을 경험하였고, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은 대상체가 재발성 뇌졸중을 앓을 위험이 있는지 여부를 결정하기 위한 것이다.
본 발명의 방법 중 임의의 것에 관한 한 실시양태에서, 뇌졸중은 허혈성 뇌졸중, 일과성 허혈 발작(transient ischemic attack) 또는 출혈성 뇌졸중(haemorrhagic stroke)이다.
본 발명의 방법 중 임의의 것에 관한 한 실시양태에서, 샘플은 혈액 샘플, 혈장 샘플 또는 혈청 샘플이다.
본 발명의 방법 중 임의의 것에 관한 한 실시양태에서, 샘플은 뇌 샘플이 아니다.
정의
본 발명에서, 하기 용어는 하기 의미를 갖는다:
본원에서 사용되는 바, "뇌졸중"이란, 뇌의 다른 부분으로의 혈액 또는 산소 흐름의 중단, 감소, 또는 정지로부터 발생하는 임의의 병태를 지칭한다. 특히, "뇌졸중"이라는 용어는 제한 없이, 허혈성 뇌졸중, 일과성 허혈 발작 (TIA) 및 출혈성 뇌졸중을 포함한다.
"허혈성 뇌졸중" (또는 "IS")은 급성 경색의 증거로 국소 뇌, 척수, 또는 망막 허혈에 의해 유발되는 신경 기능장애의 발작이다 (문헌 [Easton et al., 2009. Stroke. 40(6):2276-229). 혈류 차단의 원인으로는 적어도 4개의 상이한 원인이 존재한다:
(1) 혈관 중 혈괴;
(2) 뇌로부터 혈액을 배출하는 경막 정맥동 중 혈괴;
(3) 혈관을 막는 색전; 및/또는
(4) 혈압의 급격한 하강.
환자가 초기 손상으로부터 생존한다면, 뇌졸중 증상은 24시간 초과 지속될 수 있고, 빈번하게는 지속된다.
미니-뇌졸중으로도 불리는 "일과성 허혈 발작" 또는 "TIA"는 급성 경색의 증거 없이 국소 뇌, 척수, 또는 망막 허혈에 의해 유발되는 신경 기능장애의 일시적인 발작이다. TIA 증상은 처음에는 뇌졸중의 증상과 동일할 수 있지만, 단, 예외적으로는 증상은 단지 단기간, 전형적으로는 1시간 미만, 또는 최대 24시간 지속될 수 있다. 비록 TIA는 일시적이고, 일반적으로는 뇌 조직 손상을 유발하지는 않지만, 증상이 유사하기 때문에, TIA가 후속 허혈성 뇌졸중의 위험 인자이기 때문에, TIA를 경험한 환자는 즉시 전문적 도움을 추구할 것을 권고받게 된다.
"출혈성 뇌졸중"이란, 뇌의 혈관구조의 임의의 곳의 임의의 파열로부터 발생하는 뇌졸중을 지칭한다.
뇌졸중을 포함하거나, 뇌졸중과 함께 관찰되는 것과 같은 증상 또는 병인을 수반하는 급성 신경계 장애의 예는 상기에 열거되어 있고, 제한 없이, 대뇌 허혈 또는 경색 (색전성 폐색 및 혈전성 폐색 포함), 급성 허혈 후 재관류, 주산기 저산소성-허혈성 손상, 심장 정지 뿐만 아니라, 임의 유형의 두개내 (예를 들면, 예컨대, 경막외, 경막하, 지주막하 및 대뇌내) 출혈을 포함한다.
본원에서 사용되는 바, "대상체"란, 본 발명에 따라 진단 또는 치료되는 개체를 지칭한다. 대상체로는 포유동물 (예컨대, 뮤린, 시미안, 말, 소, 돼지, 개, 고양이 등), 바람직하게, 영장류, 및 가장 바람직하게, 인간을 포함하나, 이에 제한되지 않는다. 본 발명과 관련하여, "환자"라는 용어는 일반적으로 본 발명에 따른 진단 또는 치료를 받고 있거나, 또는 받았던 개체를 지칭한다.
본원에서 사용되는 바, "치료하는" 또는 "치료"란, 대상체에서 언급된 병태 (예컨대, 뇌졸중)를 경감시키고, 병태 (예컨대, 뇌졸중)의 증상을 제거 또는 감소시키고, 병태 (예컨대, 뇌졸중)의 진행을 저속화 또는 감소시키고, 병태 (예컨대, 뇌졸중)의 초기 발생을 예방 또는 지연시키거나, 또는 이전에 병에 걸렸던 대상체에서 병태 (예컨대, 뇌졸중)의 재발을 예방 또는 지연시키는 것을 지칭한다.
본원에서 사용되는 바, "진단하는" 또는 "진단"이란, 병태 (예컨대, 뇌졸중)의 발생 또는 진행을 평가하는 것을 지칭한다. 당업자에게 알려져 있는 바와 같이, 비록 진단받는 대상체 100%에 대하여 정확한 것으로 의도되기는 하지만, 평가는 통계학상 유의적인 대상체에 대해 정확하게 수행될 수 있다. 통계적 유의도는 당업계에 널리 공지된 방법, 예컨대, 신뢰 구간 결정, p-값 결정, t-검정, 만-휘트니(Mann-Whitney) 검정 등을 사용하여 당업자에 의해 쉽게 결정될 수 있다. 바람직한 신뢰 구간은 90% 이상, 95% 이상, 97% 이상, 98% 이상, 및 99%이다. 바람직한 p-값은 0.1, 0.05, 0.01, 0.005 또는 0.0001이다. 바람직하게, 본 발명에 따른 진단 결과는 대상체 군 중 60% 이상, 70% 이상, 80% 이상, 또는 90% 이상에 대해 정확할 것이다.
본원에서 사용되는 바, "예측하는" 또는 "예후"란, 특정 치료 또는 개입 후, 병태 (예컨대, 뇌졸중)를 앓는 대상체에 대한 결과를 예상하는 것을 지칭한다.
본원에서 사용되는 바, "혈액 샘플"이란, 대상체로부터 유래되거나, 또는 수득된 임의의 혈액 샘플을 의미한다. 혈액 샘플 수집은 당업자에게 널리 공지된 방법에 의해 수행될 수 있다. 일부 실시양태에서, 혈액 샘플은 전혈 샘플, 혈청 샘플 또는 혈장 샘플이다.
본원에서 사용되는 바, "바이오마커"란, 뇌 조직 또는 신경 세포 손상과 연관이 있고, 뇌졸중과는 상관관계가 있지만, 바람직하게는 다른 유형의 손상과는 상관이 없는, 유전자 발현의 생성물 세트 (예컨대, mRNA 및/또는 단백질)를 지칭한다. 본 발명자들에 의해 혈액 중에서 확인된 뇌졸중의 상기 구체적인 바이오마커로는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함한다. 이러한 구체적인 바이오마커는 이하에 상세하게 설명된다.
본 명세서에서, 관심 유전자들 각각의 명칭은 국제 공인 유전자 서열 및 단백질 서열 데이터베이스에서, 특히, 하기 인터넷 주소: http://www.gene.ucl.ac.uk/nomenclature/index.html에서 이용가능한, HUGO 유전자 명명법 위원회(HUGO Gene Nomenclature Committee)로부터의 데이터베이스에서 찾을 수 있는 것과 같은, 상응하는 유전자의 국제 공인 명칭을 지칭한다.
본 명세서에서, 다양한 관심 바이오마커들 각각의 명칭 또한 국제 공인 유전자 서열 및 단백질 서열 데이터베이스 ENTRE ID, 진뱅크(Genbank), TrEMBL 또는 ENSEMBL에서 찾을 수 있는 것과 같은, 상응하는 유전자의 국제 공인 명칭을 지칭할 수 있다. 이러한 국제 공인 서열 데이터베이스를 통해, 당업자는 본원에 기술된 관심 유전자들 각각에 상응하는 핵산 서열을 검색할 수 있다.
본원에서 사용되는 바, " PTGS2 "는 당업계에서 그에 대한 일반적인 의미를 갖고, 프로스타글라딘-엔도퍼옥시드 신타제 2 유전자 (유전자 ID: 5743)를 지칭한다. " PTGS2 " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_000954.1 (서열번호: 1)로 표시된다. " PTGS2 " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_000963.4 (서열번호: 2)로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 2의 잔기 134부터 잔기 1948까지이다.
본원에서 사용되는 바, " HMOX1 "은 당업계에서 그에 대한 일반적인 의미를 갖고, 헴 옥시게나제 1 유전자 (유전자 ID: 3162)를 지칭한다. " HMOX1 " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_002124.1 (서열번호: 3)로 표시된다. " HMOX1 " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_002133.3 (서열번호: 4)으로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 4의 잔기 79부터 잔기 945까지이다.
본원에서 사용되는 바, " LDLR "은 당업계에서 그에 대한 일반적인 의미를 갖고, 저밀도 지질단백질 수용체 유전자 (유전자 ID: 3949)를 지칭한다. " LDLR "" 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_000518.1 (서열번호: 5)로 표시된다. "LDLR" 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_000527.4 (서열번호: 6)로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 6의 잔기 188부터 잔기 2770까지이다.
본원에서 사용되는 바, " HSPA1B "는 당업계에서 그에 대한 일반적인 의미를 갖고, 열 충격 단백질 패밀리 A (Hsp70) 구성원 1B 유전자 (유전자 ID: 3304)를 지칭한다. " HSPA1B " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_005337.2 (서열번호: 7)로 표시된다. " HSPA1B " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_005346.5 (서열번호: 8)로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 8의 잔기 214부터 잔기 2139까지이다.
본원에서 사용되는 바, " G0S2 "는 당업계에서 그에 대한 일반적인 의미를 갖고, G0/G1 스위치 2 유전자 (유전자 ID: 50486)를 지칭한다. " G0S2 " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_056529.1 (서열번호: 9)로 표시된다. " G0S2 " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_015714.4 (서열번호: 10)로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 10의 잔기 171부터 잔기 482까지이다.
본원에서 사용되는 바, " BAG3 "은 당업계에서 그에 대한 일반적인 의미를 갖고, BCL2 연관 아타노진(athanogene) 3 유전자 (유전자 ID: 9531)를 지칭한다. " BAG3 " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_004272.2 (서열번호: 11)로 표시된다. " BAG3 " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_004281.3 (서열번호: 12)으로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 12의 잔기 307부터 잔기 2034까지이다.
본원에서 사용되는 바, " TM4SF1 "은 당업계에서 그에 대한 일반적인 의미를 갖고, 막관통 4 L 6 패밀리 구성원 1 유전자 (유전자 ID: 4071)를 지칭한다. " TM4SF1 " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 XP_016861874.1 (서열번호: 13)로 표시된다. " TM4SF1 " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 XM_017006385.2 (서열번호: 14)로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 14의 잔기 235부터 잔기 954까지이다.
본원에서 사용되는 바, " DUSP1 "은 당업계에서 그에 대한 일반적인 의미를 갖고, 이중 특이성 포스파타제 1 유전자 (유전자 ID: 1843)를 지칭한다. " DUSP1 " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_004408.1 (서열번호: 15)로 표시된다. " DUSP1 " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_004417.4 (서열번호: 16)로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 16의 잔기 244부터 잔기 1347까지이다.
본원에서 사용되는 바, " ADM "은 당업계에서 그에 대한 일반적인 의미를 갖고, 아드레노메둘린 유전자 (유전자 ID: 133)를 지칭한다. " ADM " 유전자에 의해 코딩되는 예시적인 인간 아미노산 서열은 NCBI 참조 서열 NP_001115.1 (서열번호: 17)로 표시된다. " ADM " 유전자의 예시적인 인간 mRNA 서열은 NCBI 참조 서열 NM_001124.3 (서열번호: 18)으로 표시되고, 여기서, 코딩 서열 (CDS) 범위는 서열번호: 18의 잔기 179부터 잔기 736까지이다.
상세한 설명
본 발명은 뇌졸중의 시그니쳐로서, 여기서, 상기 시그니쳐는, 그의 발현 수준이 뇌졸중에 특이적이거나, 또는 그를 나타내는 것인 바이오마커를 포함하는 것인, 뇌졸중의 시그니쳐에 관한 것이다. 이하, 상기 바이오마커는 "뇌졸중 바이오마커"로서 지칭될 것이다.
한 실시양태에서, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다. 한 실시양태에서, 본 발명의 시그니쳐는 허혈성 뇌졸중, 미니-뇌졸중 (이는 또한 일과성 허혈 발작, TIA로도 공지) 및/또는 출혈성 뇌졸중 (특히, 대뇌내 출혈에 의해 유발된 출혈성 뇌졸중)에 특이적이거나, 또는 그를 나타내는 것이다. 한 실시양태에서, 본 발명의 시그니쳐는 허혈성 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다. 한 실시양태에서, 본 발명의 시그니쳐는 일과성 허혈 발작에 특이적이거나, 또는 그를 나타내는 것이다. 한 실시양태에서, 본 발명의 시그니쳐는 출혈성 뇌졸중 (특히, 대뇌내 출혈에 의해 유발된 출혈성 뇌졸중)에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, 본 발명의 시그니쳐는 적어도 하나의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 2개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 3개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 4개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 5개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 6개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 7개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 8개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다. 한 실시양태에서, 본 발명의 시그니쳐는 적어도 9개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 뇌졸중 바이오마커는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택된다.
한 실시양태에서, 뇌졸중 바이오마커는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택된다.
한 실시양태에서, 뇌졸중 바이오마커는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 하나의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 하나의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 하나의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 2개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 2개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 2개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 2개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성되되, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 4개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 4개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 4개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 5개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 5개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 5개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 6개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 6개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 6개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 7개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 7개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 7개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 8개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 8개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 9개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
한 실시양태에서, 본 발명의 시그니쳐는 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 9개의 뇌졸중 바이오마커를 포함하거나, 또는 그로 구성된다.
따라서, 본 발명은 또한 그의 발현 수준(들)이 뇌졸중에 걸린 대상체와 실질적으로 건강한 대상체 사이에 차이가 나는 것인 하나 또는 수개의 바이오마커(들)를 함하거나, 또는 그로 구성된 뇌졸중의 시그니쳐에 관한 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 하나의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 하나의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 2개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있되; 바람직하게, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 2개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 4개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 4개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 5개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 5개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 6개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 6개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 7개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 7개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 8개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 9개의 뇌졸중 바이오마커의 발현 수준이 참조 시그니쳐와 비교하여 상향 조절되어 있다면, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이다.
한 실시양태에서, 대상체로부터의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중의, 본 발명의 뇌졸중 바이오마커의 발현 수준은 당업계에 공지된 표준 프로토콜을 이용하여 측정될 수 있다.
한 실시양태에서, 본 발명의 뇌졸중 바이오마커의 발현 수준은 그의 전사 수준 (즉, mRNA의 발현)에 또는 그의 번역 수준 (즉, 단백질 발현)에 상응한다.
한 실시양태에서, 뇌졸중 바이오마커의 발현 수준은 대상체로부터의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중 단백질 수준으로, 즉, 번역 수준으로 평가된다. 본 실시양태에서, 본 발명에 따른 시그니쳐는 프로테오믹 시그니쳐로서 지칭될 수 있다.
샘플 중 단백질 수준을 측정하는 방법은 당업계에 널리 공지되어 있다. 상기 방법의 예로는 면역조직화학법, 멀티플렉스 방법 (루미넥스(Luminex)), 웨스턴 블롯, 효소-결합 면역흡착 검정법 (ELISA), 샌드위치 ELISA, 형광성 결합 면역흡착 검정법 (FLISA), 효소 면역검정법 (EIA), 방사면역검정법 (RIA), 질량분석법 (MS), 마이크로어레이 등, 또는 그의 임의 조합을 포함하나, 이에 제한되지 않는다.
질량분석법 (MS)은 상이한 형태의 단백질을 분석하는 데 사용될 수 있는데, 그 이유는 상이한 형태는 전형적으로, 질량분석법에 의해 분석될 수 있는 상이한 질량을 갖기 때문이다. 따라서, 한 형태의 폴리펩티드 또는 단백질이 질환에 대하여 또 다른 형태의 바이오마커보다 더 우수한 바이오마커라면, 질량분석법은 유용한 형태를 특이적으로 검출하고, 측정하는 데 사용될 수 있다. MS는 비행 시간 (TOF) MS (예컨대, 매트릭스-보조 레이저 탈착/이온화 (MALDI)-TOF MS), 표면-증강 레이저 탈착/이온화 (MELDI) MS, 전기분무 이온화 MS, 또는 푸리에(Fourier) 변환 이온 사이클로트론 공명 (FT-ICR) MS를 포함할 수 있다.
면역검정법은 전형적으로 샘플을, 샘플 중 바이오마커와 선택적으로 상호작용할 수 있는 결합 파트너와 접촉시키는 것을 포함한다. 일부 실시양태에서, 결합 파트너는 항체, 예를 들면, 예컨대, 모노클로날 항체 또는 심지어는 압타머이다. 예를 들어, 결합은 경쟁적 면역검정법, 예컨대, 웨스턴 블롯과 같은 기술을 이용하는 비-경쟁적 검정법 시스템, 방사면역검정법, ELISA, "샌드위치" 면역검정법, 면역침강 검정법, 침강소 반응, 겔 확산 침강소 반응, 면역확산 검정법, 응집 검정법, 보체 고정 검정법, 면역방사측정 검정법, 형광성 면역검정법, 단백질 A 면역검정법, 면역침강 검정법, 면역조직화학 검정법, 경쟁 또는 샌드위치 ELISA, 방사면역검정법, 웨스턴 블롯 검정법, 면역조직 검정법, 면역세포화학 검정법, 도트 블롯 검정법, 형광 편광 검정법, 섬광 근접 검정법, 균일시간 분해 형광 검정법, IAsys 분석법, 및 BIA코어(BIAcore) 분석법의 사용을 통해 검출될 수 있다. 상기 언급된 검정법들은 일반적으로 고체 지지체에의 파트너 (즉, 항체 또는 압타머)의 결합을 포함한다. 본 발명의 실시에서 사용될 수 있는 고체 지지체로는 기판, 예컨대, 니트로셀룰로스 (예컨대, 막 또는 마이크로타이터 웰 형태의 것), 폴리비닐클로라이드 (예컨대, 시트 또는 마이크로타이터 웰), 폴리스티렌 라텍스 (예컨대, 비드 또는 마이크로타이터 플레이트), 폴리비닐리덴 플루오라이드, 디아조화 종이, 나일론 막, 활성화된 비드, 자기 반응성 비드 등을 포함한다.
멀티플렉스 검정법은 파지 디스플레이, 항체 프로파일링, 또는 루미넥스 플렛폼을 이용하는 검정법을 포함할 수 있다. 폴리펩티드의 프로파일을 분석하기 위한 마이크로어레이는 분석 마이크로어레이, 기능성 단백질 마이크로어레이, 또는 역상 단백질 마이크로어레이를 포함할 수 있다. 일부 경우에서, 폴리펩티드 또는 단백질의 프로파일은 프로테오믹 마이크로어레이를 이용하는 프로테오믹 스캔 (예컨대, 전체 프로테오믹 스캔)에 의해 측정될 수 있다.
한 실시양태에서, 뇌졸중 바이오마커의 발현 수준은 대상체로부터의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중 핵산 수준 (즉, RNA), 즉, 전사 수준으로 평가된다. 본 실시양태에서, 본 발명에 따른 시그니쳐는 트랜스크립톰 시그니쳐로서 지칭될 수 있다.
바이오마커의 전사 수준을 평가하는 방법은 당업계에 널리 공지되어 있다. 상기 방법의 예로는 중합효소 연쇄 반응 (PCR), RT-PCR, RT-qPCR, 노던 블롯, 하이브리드화 기술, 예컨대, 예를 들어, 마이크로어레이 사용, 및 그의 조합을 포함하나, 이에 제한되지 않고, 이는 RT-PCR에 의해 수득된 앰플리콘의 하이브리드화, 서열분석, 예컨대, 예를 들어, 차세대 DNA 서열분석 (NGS) 또는 RNA-seq (이는 또한 "전체 트랜스크립톰 샷건 서열분석"으로도 공지) 등, 또는 그의 임의 조합을 포함하나, 이에 제한되지 않는다.
통상의 방법으로는 전형적으로 중합효소 연쇄 반응 (PCR)을 포함한다. 예를 들어, 미국 특허 US4,683,202, US4,683,195, US4,800,159 및 US4,965,188에는 통상의 PCR 기술이 개시되어 있다. PCR은 전형적으로 선택된 표적 핵산 서열에 결합하는 2개의 올리고뉴클레오티드 프라이머를 이용한다. 본 발명에서 유용한 프라이머는 표적 핵산 서열 내에서 핵산 합성의 개시점으로서 작용할 수 있는 올리고뉴클레오티드를 포함한다. 프라이머는 통상의 방법에 의해 제한 분해로부터 정제될 수 있거나, 또는 합성적으로 제조될 수 있다. PCR은 열안정성 폴리머라제의 사용을 포함한다. "열안정성 폴리머라제"라는 용어는 열 안정성인 폴리머라제 효소를 지칭하며, 즉, 효소는 주형에 상보적인 프라이머 연장 생성물 형성을 촉매화하고, 이중 가닥 주형 핵산을 변성시키는 데 필요한시간 동안 승온에 가해졌을 때 비가역적으로 변성되지 않는다. 열안정성 폴리머라제는 써무스 플라부스(Thermus flavus), T. 루버(T. ruber), T. 써모필루스(T. thermophilus), T. 아쿠아티쿠스(T. aquaticus), T. 락테우스(T. lacteus), T. 루벤스(T. rubens), 바실루스 스테아로써모필루스(Bacillus stearothermophilus), 및 메타노써무스 페르비두스(Methanothermus fervidus)로부터 단리될 수 있다. 그럼에도 불구하고, 열안정성이 아닌 폴리머라제는 또한 효소가 보충된다면, PCR 검정법에 사용될 수 있다. 전형적으로, 폴리머라제는 Taq 폴리머라제 (즉, 써무스 아쿠아티쿠스 폴리머라제)이다.
정량적 PCR (qPCR)은 전형적으로 명시된 파장 빛의 빔을 각 샘플에 방사하고, 여기된 형광단에 의해 방출된 형광을 검출할 수 있는 능력이 있는 열 순환기에서 수행된다. 열 순환기는 또한 샘플을 빠르게 가열 및 냉각시킬 수 있고, 이로써, 핵산 및 열 폴리머라제의 물리화학적 특성을 이용할 수 있다. 샘플 중 앰플리콘 (즉, 증폭된 표적 핵산 서열)의 양을 검출 및 측정하기 위해, 증폭된 생성물의 양에 비례하는 측정가능한 신호가 발생되어야 한다. 모든 전류 검출 시스템은 형광 기술을 이용한다. 상기 기술 중 일부는 비-특이적인 기술이며, 그 결과, 한번에 단 하나의 표적만을 검출할 수 있다.
대안적으로, 특이적 검출 화학법은 비-특이적 증폭과 표적 증폭 사이를 구별지을 수 있다. 이들 특이적 기술은 검정법을 멀티플렉싱하는 데, 즉, 동일한 검정법에서 수개의 상이한 표적을 검출하는 데 사용될 수 있다. 예를 들어, SYBR® 그린 I(SYBR® Green I) 프로브, 하이 레졸루션 멜팅(High Resolution Melting) 프로브, 택맨(TaqMan)® 프로브, LNA® 프로브 및 몰레큘러 비콘(Molecular Beacon) 프로브가 적합할 수 있다. 택맨® 프로브가 가장 널리 사용되는 프로브 유형이다. 이는, 원래는 앰플리콘의 가닥 중 하나에 상보적인 단일 가닥 프로브 서열로 구성된, 방사선 표지 프로브를 이용한 (문헌 [Holland et al., 1991. Proc Natl Acad Sci U S A. 88(16):7276-80]) 검정법으로부터 로슈(Roche: 스위스 바젤) 및 ABI (미국 포스터 시티)에 의해 개발되었다. 형광단은 프로브의 5' 단부에 부착되고, 소광제는 3' 단부에 부착된다. 형광단은 장치에 의해 여기되고, 그의 에너지를 FRET (형광 공명 에너지 전달)를 통해 소광제로 전달할 수 있다. 전통적으로, FRET 쌍은 형광단으로서 FAM 및 소광제로서 TAMRA에 접합되어 왔다. 잘 디자인된 프로브에서, FAM은 그가 그의 에너지를 TAMRA로 전달함에 따라 형광을 내지 않는다. TAMRA 형광은 FAM에 대해 상이한 파장에서 검출되기 때문에, FAM의 배경 수준은 낮다. 프로브는 PCR의 각 어닐링 단계 동안 앰플리콘에 결합한다. Taq 폴리머라제는 앰플리콘에 결합된 프라이머로부터 신장될 때, 프로브의 5' 단부를 대체한 후, Taq 폴리머라제의 5'-3 엑소뉴클레아제 활성에 의해 분해된다. 남아있는 프로브가 앰플리콘을 용융시킬 때까지 절단은 계속 진행된다. 이 프로세스는 형광단 및 소광제를 용액 내로 유리시켜, (프로브에 의해 함께 결합되었을 때와 비교하여) 이들을 공간적으로 분리시킨다. 이로써, 비가역적으로, FAM으로부터의 형광은 증가하고, TAMRA는 감소하게 된다.
일부 실시양태에서, 핵산 수준 (즉, RNA)에서의 뇌졸중 바이오마커의 발현 수준은 RNA-seq에 의해 측정된다. 사용되는 바와 같이, "RNA-seq" 또는 "트랜스크립톰 서열분석"이라는 용어는, 전형적으로, 발현 수준을 측정하고, 융합 전사체, 선택적 스플라이싱, 및 RNA로부터 더욱 잘 평가될 수 있는 다른 게놈 변경을 검출하는 것을 1차 목표로 하는, DNA 대신 RNA (또는 cDNA)에 대해 수행되는 서열분석을 지칭한다. RNA-seq는 전형적으로 전체 트랜스크립톰 서열분석을 포함한다. 본원에서 사용되는 바, "전체 트랜스크립톰 서열분석"이라는 용어는 샘플의 RNA 함량에 대한 정보를 얻기 위하여 전체 트랜스크립톰을 서열분석하는 고처리량 서열분석을 사용하는 것을 지칭한다. 전체 트랜스크립톰 서열분석은 다양한 플랫폼, 예를 들어, 게놈 애널라이저(Genome Analyzer) (일루미나, 인크.(Illumina, Inc.: 미국 캘리포니아주 샌디에고)), 및 SOLiD™ 시퀀싱 시스템(SOLiD™ Sequencing System) (라이프 테크놀러지즈(Life Technologies: 미국 캘리포니아주 칼즈배드))을 사용하여 수행될 수 있지만, 전체 트랜스크립톰 서열분석에 유용한 어느 플랫폼이든 사용될 수 있다. 전형적으로, RNA를 추출하고, 미국 특허 US9,005,891에 기술되어 있는 바와 같이 리보솜 RNA를 결실시킬 수 있다. 상업적으로 이용가능한 키트, 예컨대, ScriptSeq™ M mRNA-Seq 라이브러리 프레퍼레이션 키트(ScriptSeq™ M mRNA-Seq Library Preparation Kit) (에피센터 바이오테크놀러지즈(Epicenter Biotechnologies: 미국 위스콘신주 매디슨))를 이용하여 방향성을 띠고, 싱글 또는 페어드-엔드(single or paired-end)인 cDNA 서열분석 라이브러리를 제조할 수 있다. 또한, 멀티플렉스 서열분석을 위해 라이브러리를 예컨대, 에피센터 바이오테크놀러지즈 (미국 위스콘신주 매디슨)로부터의 RNA-Seq 바코드 프라이머즈(RNA-Seq Barcode Primers)와 같은 상업적으로 이용가능한 바코드 프라이머를 이용하여 바코딩할 수 있다. 이어서, PCR을 수행하여 cDNA의 제2 가닥을 생성하여 바코드를 도입하고, 라이브러리를 증폭시킨다. 라이브러리를 정량화한 후, 서열분석 라이브러리를 서열분석할 수 있다. 핵산 서열분석 기술은 발현 분석에 적합한 방법이다. 상기 방법의 기초되는 원리는, DNA 서열이 샘플 중에서 검출되는 횟수가 상기 서열에 상응하는 상대적인 RNA 수준과 직접적인 관계가 있다는 것이다. 상기 방법은 종종, 생성된 데이터의 이산형, 숫자형 속성을 반영하는, "디지털 유전자 발현(Digital Gene Expression)" 또는 DOE라는 용어로 지칭된다. 상기 원리를 적용한 조기의 방법은 유전자 발현의 연속 분석(Serial Analysis of Gene Expression: SAGE) 및 대규모 병렬 시그니쳐 서열분석(Massively Parallel Signature Sequencing: MPSS)이었다. 예컨대, 문헌 [Brenner et al. (2000. Nat Biotechnol. 18(6):630-634)]를 참조한다. 전형적으로, RNA-seq는 차세대 서열분석(Next Generation Sequencing) (또는 NGS)을 이용한다. 본원에서 사용되는 바, "차세대 서열분석" 또는 "NGS"라는 용어는 전통적인 생어(Sanger) 서열분석 기술과 비교하여 비교적 새로운 서열분석 기술을 지칭한다. 리뷰를 위해, 문헌 [Shendure et al. (2008. Nat Biotechol. 26(10):1135-45)] (상기 문헌은 본 개시내용에서 참조로 포함된다)을 참조한다. 본 개시내용의 목적을 위해, NGS는 다른 것들 중에서도 특히 사이클릭 어레이 서열분석, 미세전기영동 서열분석, 하이브리드화에 의한 서열분석을 포함할 수 있다. 예를 들면, 사이클릭 어레이 방법을 이용하는 전형적인 NGS에서, 게놈 DNA 또는 cDNA 라이브러리를 먼저 제조한 후, 이어서, 공통 어댑터를 단편화된 게놈 DNA 또는 cDNA에 라이게이션시킬 수 있다. 상이한 프로토콜을 이용하여 제어가능한 방식의 거리 분포를 갖는 메이트-쌍 태그로 이루어진 점핑 라이브러리를 생성할 수 있다. 각 폴로니는 다수의, 단일 샷건 라이브러리 단편의 카피로 이루어진 것인, 공간적으로 고정화된 수백 만개의 PCR 콜로니 또는 "폴로니"로 이루어진 어레이를 생성한다. 폴로니는 평면 어레이에 테더링되기 때문에, 예컨대, 프라이머 하이브리드화를 위해, 또는 효소 신장 반응을 위해 어레이 피쳐를 병렬로 조작하기 위하여 단일의 마이크로리터 규모의 시약 부피가 적용될 수 있다. 각 신장부에 도입된 형광성 표지의 영상화 기반 검출을 사용하여 병렬로 된 모든 피쳐 상의 서열분석 데이터를 획득할 수 있다. 효소적 질의 및 영상화의 연속적인 방법 또한 이용하여 각 어레이 피쳐에 대한 인접한 서열분석 리드를 구축할 수 있다.
한 실시양태에서, 특정 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중 특정 뇌졸중 바이오마커의 발현 수준이 상향 조절되어 있는지 여부에 관하여 참조 시그니쳐 및/또는 미리 결정된 참조 값과 비교하여 결정한다.
한 실시양태에서, 참조 시그니쳐는 HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C- FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되고,
바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는, 바람직하게, 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9개 또는 그 초과의 관심 뇌졸중 바이오마커 각각에 대한 미리 결정된 참조 값을 포함하거나, 또는 그로 구성되되,
단, 바람직하게, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는다.
전형적으로, 참조 시그니쳐는 소프트웨어에서 실행될 수 있거나, 또는 측정값 간의 전체 중앙값 또는 다른 산술 평균이 구축될 수 있다.
한 실시양태에서, 참조 시그니쳐는 동일한 대상체로부터 유래된 참조 샘플 중의 본 발명에 따른 뇌졸중 바이오마커의 발현 수준의 이전 측정값으로부터 도출되고, 예컨대, 본 발명에 따른 뇌졸중 바이오마커의 발현 수준의 후속 측정 1개월 전에, 바람직하게, 6개월 전에, 더욱 바람직하게, 1년 전에, 또는 그 초과의 기간 전에 측정된 뇌졸중 바이오마커의 발현 수준; 또는 예컨대, 예를 들어, 요법 시작 전에 측정된 뇌졸중 바이오마커의 발현 수준으로부터 도출된다.
한 실시양태에서, 참조 시그니쳐는 참조 집단에서 본 발명에 따른 뇌졸중 바이오마커의 발현 수준의 측정값으로부터 도출된다.
한 실시양태에서, 참조 시그니쳐는 제한 없이, 연령 범위가 유사한 대상체, 인종 집단이 동일하거나, 또는 유사한 대상체, 암 병력 등이 유사한 대상체를 비롯한, 집단 연구로부터 도출된 상대적인 시그니쳐일 수 있다.
한 실시양태에서, 참조 시그니쳐는 1 이상의 실질적으로 건강한 대상체(들)로부터 유래된 대조군 샘플 중에서의 본 발명에 따른 뇌졸중 바이오마커의 발현 수준의 측정값으로부터 도출된다. 본원에서 사용되는 바, "실질적으로 건강한 대상 체"라는 용어는 뇌졸중을 앓거나, 또는 그로 고생하는 것으로 이전에 진단을 받았거나, 또는 확인된 바가 없는 대상체이다.
한 실시양태에서, 참조 집단은 실질적으로 건강한 대상체, 바람직하게, 적어도 50, 더욱 바람직하게, 적어도 100, 더욱 바람직하게, 적어도 200 및 더욱더 바람직하게, 적어도 500의 실질적으로 건강한 대상체를 포함한다.
참조 집단으로부터 다수의 샘플을 나타냄으로써, 각 뇌졸중 바이오마커에 대한 발현 수준의 중앙값 및/또는 평균을 각각 계산할 수 있다. 이들 결과와 관련하여, 뇌졸중 바이오마커는 표시된 차이로서 모니터링될 수 있다. 한 실시양태에서, 참조 시그니쳐는 참조 집단에서 측정된, 본 발명의 시그니쳐의 뇌졸중 바이오마커의 발현 수준의 평균에 상응한다. 한 실시양태에서, 참조 시그니쳐는 참조 집단에서 측정된, 본 발명의 시그니쳐의 뇌졸중 바이오마커의 발현 수준의 중앙값에 상응한다.
한 실시양태에서, 참조 시그니쳐는 알고리즘 및 다른 통계적 및 구조적 분류 방법을 사용하여 구축된다. 참조 집단으로부터의 샘플을 이용하여 본 발명에 따른 적어도 하나의 뇌졸중 바이오마커, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 평균 프로파일 (즉, 참조 시그니쳐)을 산정한다.
한 실시양태에서, 발현 변화 배수가 적어도 약 |1.1|보다 크다면, 바람직하게, 적어도 약 |1.2|, 약 |1.3|, 약 |1.4|, 약 |1.5|, 약 |1.6|, 약 |1.7|, 약 |1.8|, 약 |1.9|, 약 |2.0|, 약 |2.1|, 약 |2.2|, 약 |2.3|, 약 |2.4|, 약 |2.5|, 약 |3.0|, 약 |4.0|, 약 |5.0| 또는 그 초과로 그보다 크다면, 뇌졸중 바이오마커는 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받은 대상체와, 실질적으로 건강한 대상체 사이에 차별적으로 발현되는 것으로 간주된다.
한 실시양태에서, 발현 변화 배수가 적어도 약 1.1보다 크다면, 바람직하게, 적어도 약 1.2, 약 1.3, 약 1.4, 약 1.5, 약 1.6, 약 1.7, 약 1.8, 약 1.9, 약 2.0, 약 2.1, 약 2.2, 약 2.3, 약 2.4, 약 2.5, 약 3.0, 약 4.0, 약 5.0 또는 그 초과로 그보다 크다면, 뇌졸중 바이오마커는 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받은 대상체와, 실질적으로 건강한 대상체 사이에 차별적으로 발현되는 것으로 간주된다.
한 실시양태에서, log2 발현 변화 배수가 적어도 약 |0.1|보다 크다면, 바람직하게, 적어도 약 |0.2|, 약 |0.3|, 약 |0.4|, 약 |0.5|, 약 |0.6|, 약 |0.7|, 약 |0.8|, 약 |0.9|, 약 |1.0|, 약 |1.1|, 약 |1.2|, 약 |1.3|, 약 |1.4|, 약 |1.5|, 약 |1.6|, 약 |1.7|, 약 |1.8|, 약 |1.9|, 약 |2.0|, 약 |2.1|, 약 |2.2|, 약 |2.3| 또는 그 초과로 그보다 크다면, 뇌졸중 바이오마커는 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받은 대상체와, 실질적으로 건강한 대상체 사이에 차별적으로 발현되는 것으로 간주된다.
한 실시양태에서, log2 발현 변화 배수가 적어도 약 0.1보다 크다면, 바람직하게, 적어도 약 0.2, 약 0.3, 약 0.4, 약 0.5, 약 0.6, 약 0.7, 약 0.8, 약 0.9, 약 1.0, 약 1.1, 약 1.2, 약 1.3, 약 1.4, 약 1.5, 약 1.6, 약 1.7, 약 1.8, 약 1.9, 약 2.0, 약 2.1, 약 2.2, 약 2.3 또는 그 초과로 그보다 크다면, 뇌졸중 바이오마커는 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받은 대상체와, 실질적으로 건강한 대상체 사이에 차별적으로 발현되는 것으로 간주된다.
한 실시양태에서, 뇌졸중 바이오마커의 발현 수준이 실질적으로 건강한 대상체에서, 바람직하게, 참조 집단에서 측정된 동일한 바이오마커의 발현 수준보다 적어도 약 0.5, 약 1, 약 1.5, 약 2, 약 2.5, 약 3, 약 3.5, 약 4, 약 5, 약 6, 약 7, 약 8, 약 9, 약 10, 약 15, 약 20, 약 30, 약 40, 약 50, 또는 약 100배 더 높다면, 뇌졸중 바이오마커는 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받은 대상체와, 실질적으로 건강한 대상체 사이에 차별적으로 발현되는 것으로 간주된다.
한 실시양태에서, 1개 초과의 뇌졸중 바이오마커의 발현 수준을 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받은 대상체로부터 수득된 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중에서 측정할 때, 상기 발현 수준의 종합 점수인 점수는 계산되고, 미리 결정된 참조 값과 비교될 수 있다. 한 실시양태에서, 점수가 미리 결정된 참조 값보다 더 높다는 것은 대상체가 뇌졸중을 앓거나, 또는 앓았던 경험이 있음을 시사하는 것이다.
전형적으로, 미리 결정된 참조 값은 임계값 또는 컷-오프 값이다. 전형적으로, "임계값" 또는 "컷-오프 값"은 실험적으로, 경험적으로, 또는 이론상으로 결정될 수 있다. 임계값은 또한 당업계의 숙련가가 이해하는 바와 같이, 현행 실험상 및/또는 임상 조건에 기초하여 임의대로 선택될 수 있다. 예를 들어, 미리 결정된 참조 값을 확립하는 데 적절히 보관된 병력 대상체 샘플에서의 후향적 측정이 사용될 수 있다. 임계값은 시험 및 이익/위험 균형 (위양성 및 위음성의 임상적 결과)의 함수에 따라 최적의 민감도 및 특이도를 수득하도록 결정되어야 한다. 전형적으로, 최적의 민감도 및 특이도 (및 이로써, 임계값)는 실험 데이터에 기초하여 수신자 조작 특성(Receiver Operating Characteristic: ROC) 곡선을 사용하여 결정될 수 있다. 예를 들어, 참조 집단에서 본 발명의 바이오마커의 발현 수준을 측정한 후, 시험하고자 하는 샘플에서 측정된 발현 수준의 통계적 처리를 위해 알고리즘 분석을 사용할 수 있고, 이로써, 샘플 분류에 대해 유의성을 갖는 분류 표준을 수득할 수 있다. ROC 곡선의 완전한 전체 명칭은 수신자 조작자 특성 곡선이며, 이는 또한 수신자 조작 특성 곡선으로도 공지되어 있다. 이는 주로 임상 생화학적 진단 검사에 사용된다. ROC 곡선은 진양성률 (민감도) 및 위양성률 (1-특이도)의 연속 변수를 반영하는 종합 인디케이터이다. 이는 영상 합성 방법을 이용하여 민감도와 특이도 사이의 관계를 나타낸다. 상이한 컷-오프 값 시리즈 (임계값(thresholds or critical value), 진단 검사의 결과에서 정상과 비정상 사이의 경계 값)가 민감도 및 특이도 값 시리즈를 계산하기 위한 연속 변수로서 설정된다. 이어서, 곡선을 작성할 때 민감도는 수직 좌표로 사용되고, 특이도는 수평 좌표로 사용된다. 곡선하면적 (AUC)이 높을수록, 진단의 정확도는 높다. ROC 곡선상에서, 좌표 다이어그램의 맨 좌측 상단에 가장 가까운 지점이 높은 민감도 및 높은 특이도 값, 둘 모두를 갖는 임계점이다. ROC 곡선의 AUC 값은 1.0 내지 0.5이다. AUC > 0.5일 때, AUC가 1에 가까워질수록, 진단 결과는 더욱더 우수한 결과이다. 0.5 < AUC < 0.7일 때, 정확도는 낮다. 0.7 < AUC < 0.9일 때, 정확도는 중간 정도이다. AUC < 0.9일 때, 정확도는 높다. 알고리즘 방법은 바람직하게 컴퓨터를 이용하여 수행된다. 당업계의 현행 소프트웨어 또는 시스템, 예컨대, MedCalc 9.2.0.1 의학 통계 소프트웨어, SPSS 9.0, ROCPOWER.SAS, DESIGNROC.FOR, MULTIREADER POWER.SAS, CREATE-ROC.SAS, GB STAT VI0.0 (다이나믹 마이크로시스템즈, 인크.(Dynamic Microsystems, Inc.: 미국 메릴랜드주 실버 스프링)) 등이 ROC 곡선을 작성하는 데 사용될 수 있다.
본 발명은 추가로 본 발명의 뇌졸중의 시그니쳐를 이용하여 대상체에서 뇌졸중을 진단하는 방법에 관한 것이다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 특히 허혈성 뇌졸중, 미니-뇌졸중 (또는 일과성 허혈 발작, TIA) 및/또는 출혈성 뇌졸중 (특히, 대뇌내 출혈에 의해 유발된 출혈성 뇌졸중)을 진단하는 데 적합하다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 특히, 나타내느 증상이 뇌졸중 증상들 중 일부 또는 그들 모두와 동일할 수 있지만, 단, 예외적으로, 뇌졸중은 아니고, 뇌 허혈의 결과도 아닌 것인 뇌졸중 유사 질환과 뇌졸중을 구별하는 데 적합하다. 이론으로 제한하고자 하지 않으면서, 바이오마커의 수준이 상승된 것은 뇌졸중의 결과이기 때문에, 뇌졸중 유사 질환을 앓는 대상체는 상승된 바이오마커 수준을 갖지 않을 것이다 (다시 말해, 본 발명의 시그니쳐는 뇌졸중에 특이적이거나, 또는 그를 나타내는 것이기 때문에, 뇌졸중 유사 질환을 앓는 대상체는 동일한 시그니쳐를 나타내지는 않을 것이다).
일반 뇌졸중 유사 질환으로는 편두통, 실신(syncope), 말초 전정 장애 (peripheral vestibular disturbance) 및 BPPV (양성 돌발성 두위 현훈(benign paroxysmal positional vertigo)), 발작, 기능적 징후/불안, 일과성 완전 기억상실(transient global amnesia), 벨 마비(Bell's palsy), 말초 신경 질환/기능장애, 체위성 저혈압(postural hypotension), 종양, 바이러스성 질환, 심부정맥, 다발성 경화증 , 약물 관련, 저혈당증, 파킨슨병, 망막/안구 병상, 척수 병상, 삼차 신경통(trigeminal neuralgia), 요로 감염증, 섬망(delirium), 운동 뉴런증(motor neuron disease), 지주막하 출혈, 경막하 혈종(subdural hematoma) 등을 포함하나, 이에 제한되지 않는다 (문헌 [Nadarajan et al., 2014. Pract Neurol. 14(1):23-31] 참조).
따라서, 본 발명에 따른 뇌졸중을 진단하는 방법은 뇌졸중을 조기에 및 정확하게 진단할 수 있게 하는 이점을 제공하며, 이는 적어도 하기와 관련된 측면:
(1) 뇌졸중의 오진율을 감소시킬 수 있다는 측면; 및/또는
(2) 치료를 필요로 하는 대상체에서 조기에 및 적절한 치료를 허용함으로써 조직 사멸 정도를 제한할 수 있다는 측면에서 뇌졸중을 앓을 것으로 의심되는 대상체에게 도움이 될 수 있다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터 샘플을 제공하는 단계를 포함한다.
본원에서 사용되는 바, "샘플"이라는 용어는 일반적으로 바이오마커, 바람직하게, 본 발명에 따른 뇌졸중 마커의 발현 수준에 대하여 시험될 수 있는 임의의 샘플을 지칭한다.
한 실시양태에서, 샘플은 체액 샘플이다. 체액의 예로는 혈액, 혈장, 혈청, 림프, 복수액, 낭액, 소변, 담즙, 점액, 장액, 피지, 유두 삼출물, 활막액, 기관지 폐포 세척액, 객담, 양수, 복막액, 뇌척수액, 흉수, 심장막액, 정액, 타액, 누액, 점막 분비물, 땀 및 폐포 대식세포를 포함하나, 이에 제한되지 않는다.
한 실시양태에서, 샘플은 혈액 샘플이다. 본원에서 사용되는 바, "혈액 샘플"이라는 용어는 전혈 샘플, 혈청 샘플 및 혈장 샘플을 포함한다.
한 실시양태에서, 샘플은 전혈, 혈장 또는 혈청 샘플이다.
한 실시양태에서, 샘플은 신체 조직 샘플이 아니다. 신체 조직 샘플의 예로는 뇌, 근육, 신경, 심장, 폐, 간, 췌장, 비장, 휴선, 식도, 위, 장, 신장, 전립선, 고환, 난소, 모발, 피부, 뼈, 유방, 자궁, 방광 및 척수를 포함하나, 이에 제한되지 않는다,
한 실시양태에서, 샘플은 뇌 조직 샘플이 아니다. 그러므로, 본 실시양태에 따라, 본 발명의 방법은 대상체로부터 뇌 조직 샘플을 제공하는 단계를 포함하지 않는다.
한 실시양태에서, 샘플은 생검 샘플이 아니다. 한 실시양태에서, 샘플은 뇌 생검 샘플이 아니다.
한 실시양태에서, 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플은 이전에 대상체로부터 채취되었던 것이고, 즉, 본 발명에 따른 뇌졸중을 진단하는 방법은 샘플을 대상체로부터 능동적으로 채취하는 단계를 포함하지 않는다. 결과적으로, 본 실시양태에 따라, 본 발명의 방법은 비-침습형 방법, 즉, 시험관내 방법이다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 대상체로부터의 상기 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중에서 본 발명에 따른 시그니쳐를 결정하는 단계를 포함한다.
본 발명에 따른 시그니쳐를 결정하기 위한 수단 및 방법은 본원 상기에 설명되어 있다.
한 실시양태에서, 시그니쳐를 결정하는 단계는 본 발명에 따라 적어도 하나의 뇌졸중 바이오마커, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준을 측정하는 하위단계를 포함한다.
한 실시양태에서, 적어도 하나의 뇌졸중 바이오마커, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준은 DNA 마이크로어레이를 사용하여 측정되고, 이로써, 본 발명의 시그니쳐의 뇌졸중 바이오마커 각각의 발현 수준은 동시에 측정된다.
한 실시양태에서, 적어도 하나의 뇌졸중 바이오마커, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준은 RNAseq를 사용하여 측정된다.
한 실시양태에서, 적어도 하나의 뇌졸중 바이오마커, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준은 코드세트(CodeSet)를 사용하여 측정된다. (예컨대, 본원에 개시된 뇌졸중 바이오마커에 대한) 마커의 주어진 패널을 위한 커스텀 코드세트스(Custom CodeSets)는 상업적으로 디자인가능한 것이다. 이는 제한 없이, n카운터® 커스텀 코드세트스(nCounter® Custom CodeSets) (나노스트링(NanoString))를 포함한다 (문헌 [Malkov et al., 2009. BMC Res Notes. 2:80]; [Kulkarni, 2011. Curr Protoc Mol Biol. Chapter 25:Unit25B.10]).
한 실시양태에서, 1개 초과의 뇌졸중 바이오마커의 발현 수준이 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터의 상기 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중에서 측정될 때, 상기 발현 수준의 종합 점수가 계산된다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐를 본원 상기에 정의된 바와 같이, 참조 시그니쳐와 비교하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐를 본원 상기에 정의된 바와 같이, 미리 결정된 참조 값과 비교하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐 중 뇌졸중 바이오마커의 발현 수준을 본원 상기에 정의된 바와 같이, 참조 시그니쳐 중 뇌졸중 바이오마커의 발현 수준과 비교하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 참조 시그니쳐와 비교된, 상기 대상체로부터의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중 시그니쳐의 상관관계에 기초하여 대상체에서 뇌졸중을 진단하는 단계를 포함한다.
한 실시양태에서, 본원 상기에 정의된 바와 같이, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐가 참조 시그니쳐와 상이한 것으로 간주될 때, 대상체는 뇌졸중 진단을 받는다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 변화 배수가 적어도 약 |1.1|보다 크다면, 바람직하게, 적어도 약 |1.2|, 약 |1.3|, 약 |1.4|, 약 |1.5|, 약 |1.6|, 약 |1.7|, 약 |1.8|, 약 |1.9|, 약 |2.0|, 약 |2.1|, 약 |2.2|, 약 |2.3|, 약 |2.4|, 약 |2.5|, 약 |3.0|, 약 |4.0|, 약 |5.0| 또는 그 초과로 그보다 크다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 변화 배수가 적어도 약 1.1보다 크다면, 바람직하게, 적어도 약 1.2, 약 1.3, 약 1.4, 약 1.5, 약 1.6, 약 1.7, 약 1.8, 약 1.9, 약 2.0, 약 2.1, 약 2.2, 약 2.3, 약 2.4, 약 2.5, 약 3.0, 약 4.0, 약 5.0 또는 그 초과로 그보다 크다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 log2 발현 변화 배수가 적어도 약 |0.5|보다 크다면, 바람직하게, 적어도 약 |0.1|, 약 |0.2|, 약 |0.3|, 약 |0.4|, 약 |0.5|, 약 |0.6|, 약 |0.7|, 약 |0.8|, 약 |0.9|, 약 |1.0|, 약 |1.1|, 약 |1.2|, 약 |1.3|, 약 |1.4|, 약 |1.5|, 약 |1.6|, 약 |1.7|, 약 |1.8|, 약 |1.9|, 약 |2.0|, 약 |2.1|, 약 |2.2|, 약 |2.3| 또는 그 초과로 그보다 크다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 log2 발현 변화 배수가 적어도 약 0.5보다 크다면, 바람직하게, 적어도 약 0.1, 약 0.2, 약 0.3, 약 0.4, 약 0.5, 약 0.6, 약 0.7, 약 0.8, 약 0.9, 약 1.0, 약 1.1, 약 1.2, 약 1.3, 약 1.4, 약 1.5, 약 1.6, 약 1.7, 약 1.8, 약 1.9, 약 2.0, 약 2.1, 약 2.2, 약 2.3 또는 그 초과로 그보다 크다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준이 실질적으로 건강한 대상체에서, 바람직하게, 참조 집단에서 측정된 동일한 바이오마커의 발현 수준보다 적어도 약 0.5, 약 1, 약 1.5, 약 2, 약 2.5, 약 3, 약 3.5, 약 4, 약 5, 약 6, 약 7, 약 8, 약 9, 약 10, 약 15, 약 20, 약 30, 약 40, 약 50, 또는 약 100배 더 높다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본 발명에 따른 적어도 하나의, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준이 실질적으로 건강한 대상체에서, 바람직하게, 참조 집단에서의 동일한 뇌졸중 바이오마커의 발현 수준보다 높다면, 대상체는 뇌졸중 진단을 받는다.
한 실시양태에서, 본 발명에 따른 1개 초과의, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준에 대하여 계산된 종합 점수가 미리 결정된 참조 값, 즉, 실질적으로 건강한 대상체에서, 바람직하게, 참조 집단에서의 동일한 바이오마커의 발현 수준에 대하여 계산된 종합 점수보다 높다면, 대상체는 뇌졸중 진단을 받는다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은
i) 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은
i) 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9개, 또는 그 초과의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은
i) 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9개, 또는 그 초과의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은
i) 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은
i) 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은
i) 뇌졸중을 앓는 것으로 또는 그를 앓지 않는 것으로 진단받게 되는 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함한다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 i) 대상체로부터 수득된 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 바이오마커의 적어도 하나의 수준의 발현 수준을 측정하는 단계; ii) 단계 i)에서 측정된 수준을 그의 미리 결정된 참조 값과 비교하는 단계; 및 iii) 단계에서 측정된 발현 수준이 미리 결정된 참조 값보다 높을 때, 뇌졸중으로 진단하는 단계를 포함한다.
한 실시양태에서, 참조 시그니쳐는 참조 집단, 바람직하게, 적어도 하나의 실질적으로 건강한 대상체를 포함하는 참조로부터 도출, 또는 수득된 것이다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 뇌졸중의 모든 가능한 원인을 배제시키는 통상의 스크리닝을 받은 바 없는 뇌졸중의 증상을 보이는 대상체에게 적용된다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 예컨대, 제한 없이, 한쪽 눈 실명, 한쪽 팔 또는 다리 약화, 신체 한쪽 전체 약화, 어지럼증, 현훈, 복시, 신체 양측 모두 약화, 말하기 어려움, 어눌한 말씨, 또는 협응 상실과 같은, 뇌졸중의 증상을 보이는 대상체에 대해 수행되는 통상의 검사 세트의 일부일 수 있다.
한 실시양태에서, 본 발명에 따른 뇌졸중을 진단하는 방법은 추가로 특히 컴퓨터 단층촬영술 (CT) 및 자기 공명 영상화 (MRI)를 포함하는 다른 진단 도구로 수행될 수 있다.
본 발명은 추가로 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법에 관한 것이다. 본 발명은 추가로 뇌졸중을 앓는 대상체가 요법 동안 또는 요법 완료 이후에 반응을 달성하는지 여부를 결정하는 방법에 관한 것이다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은 i) PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 본 발명의 적어도 하나의 바이오마커의 발현 수준을 측정하는 단계, ii) 단계 i)에서 측정된 발현 수준을 미리 결정된 참조 값과 비교하는 단계, 및 iii) 단계 i)에서 측정된 수준이 미리 결정된 참조 값보다 더 낮은 경우, 대상체는 반응을 달성하였다고 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계, 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계, 및 상기 시그니쳐를 참조 시그니쳐와 비교하는 단계를 포함한다. 이들 단계들은 본원 상기에서 뇌졸중 진단 방법의 프레임에서 설명되었고, 이를 준용하여 본 방법에도 적용된다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 반응을 달성하였다고 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9개, 또는 그 초과의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 반응을 달성하였다고 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 반응을 달성하였다고 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 반응을 달성하였다고 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 반응을 달성하였다고 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 반응을 달성하였다고 결론짓는 단계를 포함한다.
한 실시양태에서, 참조 시그니쳐는 동일한 대상체로부터 유래된 참조 샘플 중 본 발명에 따른 뇌졸중 바이오마커의 발현 수준, 예컨대, 예를 들어, 요법 시작 전 측정된 뇌졸중 바이오마커의 발현 수준의 이전 측정값으로부터 도출, 또는 수득된 것이다.
한 실시양태에서, 본원 상기에 정의된 바와 같이, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주될 때, 대상체는 반응을 달성한 것으로 결론지어진다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 변화 배수가 적어도 약 |1.1|보다 낮다면, 바람직하게, 적어도 약 |1.2|, 약 |1.3|, 약 |1.4|, 약 |1.5|, 약 |1.6|, 약 |1.7|, 약 |1.8|, 약 |1.9|, 약 |2.0|, 약 |2.1|, 약 |2.2|, 약 |2.3|, 약 |2.4|, 약 |2.5|, 약 |3.0|, 약 |4.0|, 약 |5.0| 또는 그 초과로 그보다 낮다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 변화 배수가 적어도 약 1.1보다 낮다면, 바람직하게, 적어도 약 1.2, 약 1.3, 약 1.4, 약 1.5, 약 1.6, 약 1.7, 약 1.8, 약 1.9, 약 2.0, 약 2.1, 약 2.2, 약 2.3, 약 2.4, 약 2.5, 약 3.0, 약 4.0, 약 5.0 또는 그 초과로 그보다 낮다면, 본원 상기에 정의된 바와 같이, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 log2 발현 변화 배수가 약 |0.1|보다 낮다면, 바람직하게, 적어도 약 |0.2|, 약 |0.3|, 약 |0.4|, 약 |0.5|, 약 |0.6|, 약 |0.7|, 약 |0.8|, 약 |0.9|, 약 |1.0|, 약 |1.1|, 약 |1.2|, 약 |1.3|, 약 |1.4|, 약 |1.5|, 약 |1.6|, 약 |1.7|, 약 |1.8|, 약 |1.9|, 약 |2.0|, 약 |2.1|, 약 |2.2|, 약 |2.3| 또는 그 초과로 그보다 낮다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 log2 발현 변화 배수가 적어도 약 0.1보다 낮다면, 바람직하게, 적어도 약 0.2, 약 0.3, 약 0.4, 약 0.5, 약 0.6, 약 0.7, 약 0.8, 약 0.9, 약 1.0, 약 1.1, 약 1.2, 약 1.3, 약 1.4, 약 1.5, 약 1.6, 약 1.7, 약 1.8, 약 1.9, 약 2.0, 약 2.1, 약 2.2, 약 2.3 또는 그 초과로 그보다 낮다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본원에서 정의된 바와 같은 적어도 1, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준이 실질적으로 건강한 대상체에서, 바람직하게, 참조 집단에서 측정된 동일한 바이오마커의 발현 수준보다 적어도 약 0.5, 약 1, 약 1.5, 약 2, 약 2.5, 약 3, 약 3.5, 약 4, 약 5, 약 6, 약 7, 약 8, 약 9, 약 10, 약 15, 약 20, 약 30, 약 40, 약 50, 또는 약 100배 더 낮다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본 발명에 따른 적어도 하나의, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준이 실질적으로 건강한 대상체에서, 바람직하게, 참조 집단에서의 동일한 뇌졸중 바이오마커의 발현 수준보다 높지 않다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
한 실시양태에서, 본 발명에 따른 1개 초과의, 바람직하게, 적어도 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준에 대하여 계산된 종합 점수가 미리 결정된 참조 값, 즉, 실질적으로 건강한 대상체에서, 바람직하게, 참조 집단에서의 동일한 바이오마커의 발현 수준에 대하여 계산된 종합 점수보다 높지 않다면, 대상체의 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플로부터 결정된 시그니쳐는 참조 시그니쳐와 상이한 것으로 간주된다.
뇌졸중을 앓는 대상체가 요법으로 반응을 달성하는지 여부를 결정하는 방법은 "반응자"와 "비-반응자"를 구별하는 데 특히 적합하다.
본원에서 사용되는 바, "반응자"라는 용어는 치료 반응을 달성하게 되는 대상체, 또는 환자, 즉, 뇌졸중이 감소되거나, 경감되거나, 또는 치유되는 대상체 또는 환자를 지칭한다. 본 발명에 따라, 반응자는 객관적인 반응을 보이고, 그러므로, 상기 용어는 뇌졸중 질환이 요법 이후에는 진행하지 않는 안정화된 뇌졸중을 앓는 대상체 또는 환자는 포함하지 않는다.
본원에서 사용되는 바, "비- 반응자" (또는 난치성)라는 용어는 뇌졸중이 요법 이후에도 감소 또는 호전을 보이지 않는 대상체 또는 환자를 포함한다. 본 발명에 따라, "비-반응자"라는 용어는 또한 안정화된 뇌졸중을 앓는 대상체 또는 환자도 포함한다.
전형적으로, 대상체를 반응자 또는 비-반응자로 특징화하는 것은 표준 또는 훈련 세트를 참조하여 수행될 수 있다. 표준은 반응자 또는 비-반응자인 것으로 공지된 대상체의 프로파일 수 있거나, 또는 대안적으로, 수치 값일 수 있다. 상기 미리 결정된 표준은 임의의 적합한 형태로, 예컨대, 인쇄된 목록 또는 다이어그램, 컴퓨터 소프트웨어 프로그램, 또는 다른 매체로 제공될 수 있다. 일부 실시양태에서, 미리 결정된 값은 요법 이전에 측정된 발현 수준이다. 환자가 비-반응자인 것으로 결론지어 질 때, 의사는 임의의 추가의 유해한 부작용을 막기 위해 요법 중단 결정을 내릴 수 있다.
한 실시양태에서, 모니터링 목적을 위해, 발현 수준은 예를 들어, 2회, 3회, 4회, 5회, 6회, 7회, 8회, 9회, 10회 또는 그 초과로 다회 시점에서 측정될 수 있다. 이러한 방식에서, 발현 수준은, 발현 수준이 비록 더 느리기는 하지만, 감소될 수 있는 비치료 대상체와 비교하여, 치료가 성공적으로 이루어진 대상체에서는 더 빠르게 감소될 것으로 예상되는 바, 요법 이후 또는 그 동안 시간이 경과함에 따라 발현 수준을 모니터링하는 것은 치료의 성공 척도를 제공할 수 있다.
전형적으로, 요법은 당업자에게 공지된 임의의 방법으로 구성된다. 치료 옵션은 혈관내 시술 및 수술, 예컨대, 혈전절제술을 포함하나, 이에 제한되지 않는다.
본원에서 사용되는 바, "혈전절제술"이라는 용어는 응괴의 임의의 수술적 및/또는 기계적 제거 또는 파괴를 정의한다. 전형적으로, 3가지 부류의 기계식 혈전절제술 장치: 코일 리트리버(coil retriever), 흡인 장치, 및 스텐트 리트리버(stent retriever)가 공지되어 있다. 현재 개발 중에 있는 다른 장치 및 방법 또한 본원에서 사용되는 혈전절제술의 정의에 포함된다. 전형적으로, 카테터는 혈괴 제거를 위해 혈류가 막힌 부위로 보내진다. 혈전절제술 및 혈전용해의 조합이 환자에게 투여될 수 있다. 추가로, 허혈성 뇌졸중은 또한 혈전용해제를 투여하여 혈괴를 용해시킴으로써 ("혈전용해") 치료될 수 있다.
항혈전성제는 하기 3가지 서브유형: 항응고제, 항혈소판 약물, 및 혈전용해 약물로 추가로 분류된다.
항응고제의 예로는 쿠마린, 헤파린, 와파린, 아세노쿠마롤, 펜프로쿠몬, 아트로멘틴, 페닌디온, 폰다파리눅스, 이드라파리눅스, 직접 인자 Xa 억제제, 직접 트롬빈 억제제, 항트롬빈 단백질 치료제, 바트룩소빈, 및 헤멘틴을 포함하나, 이에 제한되지 않는다.
항혈소판 약물의 예로는 비가역성 시클로옥시게나제 억제제 (예컨대, 아스피린 또는 트리플루살), 아데노신 디포스페이트 수용체 억제제 (예컨대, 클로피도그렐, 프라수그렐, 티카그렐로, 또는 티클로피딘), 포스포디에스테라제 억제제 (예컨대, 실로스타졸), 당단백질 IIB/IIIA 억제제 (예컨대, 압식시맙, 엡티피바티드, 또는 티로피반), 아데노신 재흡수 억제제 (예컨대, 디피리다몰), 및 트롬복산 억제제 (예컨대, 트롬복산 신타제 억제제 또는 트롬복산 수용체 길항제)를 포함하나, 이에 제한되지 않는다.
혈전용해 약물의 예로는 조직 플라스미노겐 활성인자 t-PA (알테플라제 및 기타 (데스모테플라제, 레테플라제, 테네크테플라제 등), 아니스트레플라제, 스트렙토키나제, 및 유로키나제를 포함하나, 이에 제한되지 않는다. t-PA는 임의적으로 혈관내 시술 동안 투여될 수 있다.
한 실시양태에서, 요법은 신경보호제를 투여하는 것으로 구성된다.
신경보호제의 예로는 전형적으로 제한 없이, 자유 라디칼 방지제(anti-free radicals), 항-글루타메이제, 및 CDK 억제제를 포함한다.
일부 실시양태에서, 신경보호제는 시클린-의존성 키나제 (CDK) 억제제이다. 공지된 CDK 억제제는 일반적으로는 CDK를 억제시킬 수 있는 그의 능력에 따라, 또는 특이적인 CDK에 대한 그의 선택성에 따라 분류될 수 있다. 예를 들어, 플라보피리돌은 "범(pan)" CDK 길항제로서 작용하고, 이는 특이적인 CDK에 대한 특별한 선택성은 없다 (문헌 [Dai & Grant, 2003. Curr Opin Pharmacol. 3(4):362-70]). 퓨린-기반 CDK 억제제, 예컨대, 올로모우신, 로스코비틴, 푸바놀올소 및 CGP74514A는 CDK 1, 2 및 5에 대하여 더 큰 선택성을 보이지만, CDK 4 및 6에 대해서는 어떤 억제 활성도 보이지 않는 것으로 알려져 있다 (문헌 [Dai & Grant, 2003. Curr Opin Pharmacol. 3(4):362-70]). 추가로, 퓨린-기반 CDK 억제제, 예컨대, S-로스코비틴은 신경계에서 항-아폽토시스성 효과를 발휘할 수 있거나 (문헌 [O'Hare et al., 2002. Pharmacol Ther. 93(2-3):135-43]; [Timsit & Menn, 2012. Clin Pharmacol Ther. 91(2):327-32]; [Gutierrez-Vargas et al., 2017. J Cereb Blood Flow Metab. 37(6):2208-2223]) 또는 신경퇴행성 질환, 예컨대, 알츠하이머 질환에서 신경 세포 사멸을 예방할 수 있다 (문헌 [Filgueira de Azevedo et al., 2002. Biochem Biophys Res Commun. 297(5):1154-8]; [Knockaert et al., 2002. Trends Pharmacol Sci. 23(9):417-25]).
일부 실시양태에서, 요법은 체온저하로 구성된다 (예컨대, 문헌 [Kurisu & Yenari, 2018. Neuropharmacology. 134(Pt B):302-309]).
본 발명은 추가로, i) 대상체로부터 수득된 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 바이오마커의 적어도 하나의 수준의 발현 수준을 측정하는 단계, ii) 단계 i)에서 측정된 수준을 그의 미리 결정된 참조 값과 비교하는 단계, 및 iii) 단계에서 측정된 발현 수준이 미리 결정된 참조 값보다 높을 때, 대상체는 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함하는, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법에 관한 것이다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계, 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계, 및 상기 시그니쳐를 참조 시그니쳐와 비교하는 단계를 포함한다. 이들 단계들은 본원 상기에서 뇌졸중 진단 방법의 프레임에서 설명되었고, 이를 준용하여 본 방법에도 적용된다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함한다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9개, 또는 그 초과의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함한다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함한다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함한다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함한다.
한 실시양태에서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체가 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함한다.
한 실시양태에서, 참조 시그니쳐는 참조 집단, 바람직하게, 적어도 하나의 실질적으로 건강한 대상체를 포함하는 참조로부터 도출, 또는 수득된 것이다.
한 실시양태에서, 대상체는 뇌졸중을 유도할 수 있는 심혈관 질환 (예컨대, 아테롬성 동맥 경화증, 고혈압 등)을 앓고 있거나, 앓았거나, 그 진단을 받은 것이다.
한 실시양태에서, 대상체는 뇌졸중 경험이 있고, 본 발명의 발명의 방법은 특히 재발성 뇌졸중을 예측하는 데 특히 적합하다.
따라서, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법은 예후를 제공하고, 이로써, 위험이 있는 대상체를 확인하는 데 특히 적합하고, 이에, 상기 방법은 뇌졸중 예방을 위한 모든 치료 개입을 취한다.
본원에서 사용되는 바, "위험"이라는 용어는 이벤트가 특정 기간에 걸쳐 발생할 확률에 관한 것이고, 이는 대상체의 "절대 위험도" 또는 "상대 위험도"를 의미할 수 있다.
"절대 위험도"는 관련시간 코호트에 대한 측정 후의 실제 관찰결과를 참조하여, 또는 관련 기간 동안 진행된 통계학적으로 유효한 병력 코호트로부터 발생된 인덱스 값을 참조로 하여 측정될 수 있다.
"상대 위험도"는 저위험 코호트의 절대 위험 또는 평균 집단 위험 대비의 대상체의 절대 위험의 비를 지칭하며, 이는 임상적 위험 인자 평가 방법에 따라 달라질 수 있다. 주어진 시험 결과에 대한 음성 이벤트 대비 양성 이벤트의 비율인 오즈비는 또한 보편적으로 비-전환에 대하여 사용된다 (오즈는 공식 p/(1 - p)에 따른 값이고, 여기서, 이벤트의 확률이고, (1 - p)는 비이벤트 확률이다).
본 발명과 관련하여 "위험도 평가" 또는 "위험도의 평가"는 이벤트 또는 질환 상태가 발생할 수 있는 확률, 오즈, 또는 가능도, 이벤트 발생률, 또는 한 질환 상태에서 또 다른 것으로의 전환율을 예측하는 것을 포함한다. 위험도 평가는 이전에 측정된 집단을 참조로 하여 절대 또는 상대적인 방식으로 향후 미래의 임상적 파라미터, 전통적인 실험실 위험 인자 값, 또는 다른 재발 인덱스를 예측하는 것을 포함할 수 있다.
대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 것은 전환 위험의 연속적 또는 범주형 측정을 수행하고, 이로써, 전환 위험이 있는 것으로 정의된 대상체의 범주의 위험 스펙트럼을 진단 및 정의하는 데 사용될 수 있다. 범주형 시나리오에서, 본 발명은 정상적인 대상체 코호트와 더 높은 고위험의 다른 대상체 코호트를 구별하는 데 사용될 수 있다. 한 실시양태에서, 본 발명은 정상 대상체와 위험이 있는 대상체를 구별하기 위해 사용될 수 있다.
본 발명은 추가로, i) 대상체로부터 수득된 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플 중 DUSP1, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, ADM 및 TM4SF1로 구성된 군으로부터 선택되는 바이오마커의 적어도 하나의 수준의 발현 수준을 측정하는 단계, ii) 단계 i)에서 측정된 수준을 그의 미리 결정된 참조 값과 비교하는 단계, 및 iii) 단계 i)에서 측정된 수준이 미리 결정된 참조 값보다 낮을 때, 환자 예후가 우수하다고 결론짓거나, 또는 단계 i)에서 측정된 수준이 미리 결정된 참조 값보다 높을 때, 환자 예후가 불량하다고 결론짓는 단계를 포함하는, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법에 관한 것이다.
한 실시양태에서, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법은 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계, 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계, 및 상기 시그니쳐를 참조 시그니쳐와 비교하는 단계를 포함한다. 이들 단계들은 본원 상기에서 뇌졸중 진단 방법의 프레임에서 설명되었고, 이를 준용하여 본 방법에도 적용된다.
한 실시양태에서, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 환자 예후가 우수한 것으로 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9개, 또는 그 초과의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 환자 예후가 우수한 것으로 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 환자 예후가 우수한 것으로 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 환자 예후가 우수한 것으로 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 환자 예후가 우수한 것으로 결론짓는 단계를 포함한다.
한 실시양태에서, 뇌졸중을 앓는 대상체의 예후를 결정하는 방법은
i) 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 환자 예후가 우수한 것으로 결론짓는 단계를 포함한다.
한 실시양태에서, 참조 시그니쳐는 참조 집단, 바람직하게, 적어도 하나의 실질적으로 건강한 대상체를 포함하는 참조로부터 도출, 또는 수득된 것이다.
한 실시양태에서, 참조 시그니쳐는 동일한 대상체로부터 유래된 참조 샘플 중 본 발명에 따른 뇌졸중 바이오마커의 발현 수준, 예컨대, 예를 들어, 뇌졸중 후에, 바람직하게, 뇌졸중 후 6시간, 12시간, 18시간, 24시간, 36시간, 48시간, 60시간, 72시간, 84시간 또는 96시간 이상의 시간이 경과한 후에 측정된 뇌졸중 바이오마커의 발현 수준의 이전 측정값으로부터 도출, 또는 수득된 것이다.
본원에서 사용되는 바, "예후"라는 용어는 뇌졸중의 가능한 결과, 즉, 뇌졸중 과정 또는 환자 생존 기간 예측을 지칭한다.
본원에서 사용되는 바, "예후가 우수하다"라는 용어는 동일한 병태를 앓는 동일한 성별의 다른 구성원들과 비교하였을 때, 뇌졸중을 앓는 환자에 대한 평균 생존 가능도가 더 크다는 것을 지칭한다.
본원에서 사용되는 바, "예후가 불량하다"라는 용어는 동일한 병태를 앓는 동일한 성별의 다른 구성원들과 비교하였을 때, 뇌졸중을 앓는 환자에 대한 평균 생존 가능도가 더 작다는 것을 지칭한다.
본 발명은 추가로 뇌졸중에 걸린 대상체를 치료하는 방법에 관한 것이다.
한 실시양태에서, 뇌졸중에 걸린 대상체를 치료하는 방법은 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계, 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계, 및 상기 시그니쳐를 참조 시그니쳐와 비교하는 단계를 포함한다. 이들 단계들은 본원 상기에서 뇌졸중 진단 방법의 프레임에서 설명되었고, 이를 준용하여 본 방법에도 적용된다.
한 실시양태에서, 뇌졸중에 걸린 대상체를 치료하는 방법은
i) 상기 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 상기 샘플 중 본 발명의 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계;
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계; 및
v) 상기 대상체가 단계 iv)에서 뇌졸중에 걸린 것으로 진단받았다면, 대상체를 치료하는 단계를 포함한다.
한 실시양태에서, 뇌졸중에 걸린 대상체를 치료하는 방법은
i) 상기 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM 및 G0S2를 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9개, 또는 그 초과의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계;
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계; 및
v) 상기 대상체가 단계 iv)에서 뇌졸중에 걸린 것으로 진단받았다면, 대상체를 치료하는 단계를 포함한다.
한 실시양태에서, 뇌졸중에 걸린 대상체를 치료하는 방법은
i) 상기 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 1, 2, 3, 4, 5, 6, 7, 8 또는 9개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 하나 또는 2개의 뇌졸중 바이오마커는 DUSP1 및/또는 ADM으로 구성되지 않는 것인 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계;
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계; 및
v) 상기 대상체가 단계 iv)에서 뇌졸중에 걸린 것으로 진단받았다면, 대상체를 치료하는 단계를 포함한다.
한 실시양태에서, 뇌졸중에 걸린 대상체를 치료하는 방법은
i) 상기 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM을 포함하거나, 또는 그로 구성된 군으로부터 선택되는 적어도 3개의 뇌졸중 바이오마커의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계;
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계; 및
v) 상기 대상체가 단계 iv)에서 뇌졸중에 걸린 것으로 진단받았다면, 대상체를 치료하는 단계를 포함한다.
한 실시양태에서, 뇌졸중에 걸린 대상체를 치료하는 방법은
i) 상기 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 및 TM4SF1의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계;
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계; 및
v) 상기 대상체가 단계 iv)에서 뇌졸중에 걸린 것으로 진단받았다면, 대상체를 치료하는 단계를 포함한다.
한 실시양태에서, 뇌졸중에 걸린 대상체를 치료하는 방법은
i) 상기 대상체로부터 샘플, 바람직하게, 체액 샘플, 더욱 바람직하게, 혈액 샘플을 제공하는 단계;
ii) 바람직하게, PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM의 발현 수준을 측정함으로써 상기 샘플 중 시그니쳐를 결정하는 단계;
iii) 단계 ii)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계;
iv) 본원 상기에서 설명된 바와 같이, 참조 시그니쳐와 시그니쳐의 상관관계에 기초하여 대상체를 뇌졸중에 걸린 것으로 진단하는 단계; 및
v) 상기 대상체가 단계 iv)에서 뇌졸중에 걸린 것으로 진단받았다면, 대상체를 치료하는 단계를 포함한다.
한 실시양태에서, 참조 시그니쳐는 참조 집단, 바람직하게, 적어도 하나의 실질적으로 건강한 대상체를 포함하는 참조로부터 도출, 또는 수득된 것이다.
뇌졸중에 걸린 것으로 진단받은 대상체에 적합한 치료 및 요법의 예는 당업계에 널리 공지되어 있고, 이는 본원 상기에 상세하게 설명되어 있다.
본 발명은 하기 실시예 및 도면에 의해 추가로 예시될 것이다. 그러나, 본 실시예는 어느 방식으로든 본 발명의 범주를 제한하는 것으로 해석되지 않아야 한다.
도 1은 qRT-PCR에 의한, (a) HSPA1B, (b) GADD45G 및 (c) CDKN1A에 대한 mRNA 수준과 마이크로어레이 강도 값 사이의 상관관계를 보여주는, 3개의 그래프의 한 세트이다. x축은 SMC2에 대해 정규화된 qRT-PCR mRNA의 log2 비를 보여주는 것이고, y축은 올리고뉴클레오티드 마이크로어레이 신호를 보여주는 것이다. 만-휘트니 U 검정으로부터의 P-값.
도 2는 뇌에서 및 혈액에서 차별적으로 발현된 두 유전자 세트 사이의 가장 유의적인 중복을 나타내는, 2개의 벤다이어그램의 한 세트이다. 상단 패널은 하향 조절된 유전자를 보여주는 것이고; 하단 패널은 상향 조절된 유전자를 보여주는 것이다.
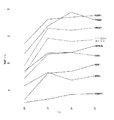
도 3은 상이한 시점: 허혈 이전 (T0) 및 허혈 이후 (T1, T2, T3)의 상이한 시점 사이에 수컷 레서스 마카크(rhesus macaque) S1에서 차별적으로 발현된 상위 9개의 유전자에 대한 혈중 혈액 유전자 강도 키네틱을 도시한 것이다.
도 4는 상이한 시점: 허혈 이전 (T0) 및 허혈 이후 (T1, T2, T3)의 상이한 시점 사이에 수컷 레서스 마카크 S2에서 차별적으로 발현된 상위 9개의 유전자에 대한 혈중 혈액 유전자 강도 키네틱을 도시한 것이다.
도 2는 뇌에서 및 혈액에서 차별적으로 발현된 두 유전자 세트 사이의 가장 유의적인 중복을 나타내는, 2개의 벤다이어그램의 한 세트이다. 상단 패널은 하향 조절된 유전자를 보여주는 것이고; 하단 패널은 상향 조절된 유전자를 보여주는 것이다.
도 3은 상이한 시점: 허혈 이전 (T0) 및 허혈 이후 (T1, T2, T3)의 상이한 시점 사이에 수컷 레서스 마카크(rhesus macaque) S1에서 차별적으로 발현된 상위 9개의 유전자에 대한 혈중 혈액 유전자 강도 키네틱을 도시한 것이다.
도 4는 상이한 시점: 허혈 이전 (T0) 및 허혈 이후 (T1, T2, T3)의 상이한 시점 사이에 수컷 레서스 마카크 S2에서 차별적으로 발현된 상위 9개의 유전자에 대한 혈중 혈액 유전자 강도 키네틱을 도시한 것이다.
실시예
본 발명은 하기 실시예에 의해 추가로 예시된다.
실시예
1: 혈전성
레서스
마카크
모델에서 허혈성 뇌와 혈액 사이에서 공통된
시그니쳐
확인
방법
동물 실험
12-13세이고, 체중이 16.5 내지 17.2 kg 범위인 수컷 레서스 마카크 (마카카 물라타(Macaca mulatta)) 2마리에서 실험을 수행하였다. 하기에서, 상기의 두 원숭이는 S1 및 S2로 언급될 것이다.
실험 프로토콜을 동물 실험 지역 윤리 위원회(Regional Ethics Committee for Animal Experimentation) (노르망디)에 제출하고, 연구 수행 권한을 승인받았다 (참조 번호 No. N/02-03-08/03/02-11). 실험은 자격증이 있는 연구원 (C.O.)에 의해 및 프랑스 및 유럽 윤리법(French and European ethical laws) 및 실험동물의 관리 및 사용에 대한 가이드라인(guidelines for the care and use of laboratory 동물s) (과학 목적으로 사용되는 동물 보호에 관한, 2010년 9월 22일 유럽 의회 및 심의회의 지침 2010/63/EU)에 따라 수행하였다. 본 연구를 진행하는 동안, 원숭이를 시세롱 리서치 센터(Cyceron Research Centre) (동물 실험 시설(Establishment for Animal Experimentation), 계약 번호 B14118001)에서 12시간/12시간 명/암 사이클로 50% 상대 습도하에 24로 유지되는 개별 케이지에서 하우징하고, 신선한 과일 및 식수가 보충된 시판용 사료를 무제한 필요한 만큼 사용할 수 있도록 공급하였다. 본 연구 전 기간 동안, 동물의 웰빙을 감독하기 위해 언제든 수의사를 만날 수 있었다.
동물 모델
혈전성 레서스 마카크 모델
앞서 기술된 바와 같이 실험을 수행하였다 (문헌 [Gauberti et al., 2012. Cerebrovasc Dis. 33(4):329-39]).
간략하면, 전신 마취 후, 핵 제거 후에 우측 중간 대뇌 동맥 (MCA)을 노출시켰다. M1 분지를 단리시키도록 두 봉합부를 위치시키고, M1 분지 안으로 마이크로피펫을 삽입하고, 인간 트롬빈을 주사하였다. 약 600 ㎕의 트롬빈을 1 U/㎕ 농도로 주사하였다. 100 ㎕의 1차 주사 후, 2분 간격으로 50 ㎕씩 6회에 걸쳐 주사한 후, 이어서, 근위 봉합부를 제거하고, 남은 트롬빈을 주사하였다. 이어서, 15분 후에 원위 봉합부를 제거하였다.
트롬빈 주사를 위한 전체 절차는 약 30분이 소요되었다.
마취 및 생리적 파라미터 제어
케타민 (0.1 mg/kg; IM; 이말진(Imalgene ) ®)을 이용하여 동물을 진정시켰다. 100% 산소 중 세보플루란 (2.5%; 세보란(Sevorane)®)에 의해 가스 마취를 유도하였다. 복재 정맥을 통해 아트라쿠리움 (0.5 mg/kg; IV; 트라크리움(Tracrium)®)에 의해 근육을 이완시켰다.
원숭이를 분당 22회인 고정된 호흡 빈도로 간헐 양압으로 기계로 환기시켰다. 일호흡량 (VT)을 조정하여 정상탄산상태 (PaCO2 = 38-42 mmHg)를 얻었다. 66% 아산화질소와 함께 세보플루란에 의해 마취를 유지시켰다.
수술 동안, 세보플루란 농도를 3%까지 증가시킨 후, 자기 공명 영상화 (MRI) 방법 동안 1.5-2%까지 감소시켰다. 정맥내 아트라쿠리움 관류를 0.75 mg/kg/h로 세팅하였다. 수술 전 동물을 정위 프레임에 위치시켰다.
생체내
MRI 획득
원숭이를 3T 임상 MRI (필리스 센스 플렉스 M(Philips Sense Flex M))에서 연구하였다.
축면 및 관상면으로 영상화를 수행하였고, 이는 하기 시퀀스를 포함하였다: 3D-비행 시간 혈관조영술, T2-강조, 유체 감쇠 반전 회복 (FLAIR), 확산-강조 영상화 (DWI), 및 조영 전 및 조영 후 T1-강조 및 관류-강조 영상화 (PWI).
혈액 샘플
수술 전이되, 전신 마취 후인 T0, 및 MCA 폐색 후 T1 = +2h, T2 = +3.5h 및 T3 = +4.5h에 혈액 샘플을 수득하였다.
각 혈액 샘플에 대해, RNA를 위해 2.5 mL씩 체혈하였다. 혈액 샘플은 PAX진즈 블러드(PAXgenes Blood) RNA 튜브 (PreAnalytix)를 이용하여 수집하였다.
뇌 샘플
각 원숭이로부터 12개의 뇌 샘플을 채취하였다. 각 원숭이에서, 6개의 샘플은 경색 부위 인근에서 채취하고, 6개의 샘플은 나머지 다른 한쪽 반구의 상응하는 위치로부터 채취하였다. 따라서, 총 12개의 허혈성 및 12개의 비-허혈성 뇌 샘플을 분석하였다.
두 원숭이를 수술하고, 폐색 발병 후 약 5.5시간 (S1: 5h 12; S2: 5h 35)째에 희생시켰다. 폐색 발병 후 약 3 내지 4시간 (S1: 3h 10; S2: 3h 05)째에 MRI를 수행하였다. 개흉술 후 동물에 심장내 주사에 의해 총 부피 약 8 L의 4℃ 염수 혈청을 주입하였다. 이어서, 개두술 후에 뇌를 제거하고, 두정 뇌 슬라이싱용으로 전문 디자인된 몰드에 배치하였다. 각각의 뇌 절편을 추가로, 허혈성 반구 및 대측 반구 상의 x 및 y 좌표를 확인할 수 있도록 하는 그리드 상에 배치하였다. 임의대로 그리드 상에서 로마 숫자는 우측 허혈성 반구 부위에 대한 것이고, 아라비아 숫자는 좌측 비-허혈성 반구 부위에 대한 것이었다.
허혈은 육안으로도 관찰할 수 있었고 (데이터는 제시되지 않음), 비-허혈성 대측 반구에서 수득된 분홍색을 띠는 염색과 비교하여, 흰색으로 보인, 테트라졸륨에 의해 처리된 대사저하 상태의 허혈성 조직으로 확인되었다.
동물 1마리당 3개의 허혈성 피질 샘플을 제조하였다: 하나는 잠재적으로 코어에 상응하는 것이고, 2개의 잠재적으로는 반영부 부위에 상응하는 변연부로부터의 것이었다. 동물 1마리당 대측 반구로부터 3개의 균질 샘플도 또한 제조하였다.
TTC
염색
대사 활성 및 이로써, 허혈성 조직을 평가하기 위해, 트랜스크립톰에 대해 연구하고자 하는 조직에 인접한 뇌 샘플을 1% 테트라졸륨 클로라이드 (TTC)로 염색하였다.
전체 RNA 추출
전체 RNA를 RN이지(RNeasy) 마이크로어레이 조직 키트를 이용하여 제조사의 설명서 (퀴아젠(Qiagen))에 따라 대뇌 피질로부터 단리시켰다. 애질런트 2100 바이오애널라이저(Agilent 2100 BioAnalyzer) (애질런트 테크놀러지즈(Agilent Technologies))를 이용하여 RIN (RNA 무결성 수)을 측정함으로써 RNA 무결성을 평가하였다 (문헌 [Schroeder et al., 2006. BMC Mol Biol. 7:3]). 측정된 RIN은 6.3 내지 8.8이었다.
PAX진즈 블러드 RNA 키트 (프리애널리틱스(PreAnalytix))를 사용하여 혈액 샘플로부터 전체 RNA를 단리시켰다. 글로빈클리어(GlobinClear) 키트 (앰비온(Ambion))을 이용하여 전체 RNA로부터 글로빈 mRNA를 제거하였다. 측정된 RIN는 7.8 내지 10이었다.
마카카
발현
마이크로어레이
및 샘플 선택
대뇌 피질 (30 ng)로부터의 및 혈액 샘플 (30 ng)로부터의 RNA를 로우 인풋 퀵 Amp Wt 라벨링(Low Input Quick Amp WT Labeling) 키트 (애질런트 테크놀러지즈)를 이용하여 표지하였다. RNA 스파이크-인(spike-in) 대조군을 사용하여 가능한 염료 효과를 조정하였다. 역전사 효소 및 WT 프라이머 (T7 프로모터 프라이머 및 T7 프로모터와 랜덤 프라이머)를 이용하여 RNA를 cDNA로 전환시켰다. T7 RNA 폴리머라제는 cRNA 합성 및 Cy3을 이용한 그의 표지를 위해 사용하였다. 형광 표지된 cRNA 프로브를 RN이지 미니 키트 (퀴아젠)를 이용하여 정제하였다.
동량 (3.75 ㎍)의 Cy3 cRNA 프로브를 4x44K 애질런트 DNA 칩 (카탈로그 번호: G2519F, 마카카 물라타) 상에 하이브리드화시켰다. 65에서 10 rpm으로 회전시키면서 17시간 동안 하이브리드화를 수행하였다. 이어서, 제조사의 설명서에 따라 샘플을 세척하고, 건조시켰다.
애질런트 DNA 마이크로어레이 스캐너를 이용하여 하이브리드화 영상을 수득하고, 피쳐 추출(Feature Extraction) 소프트웨어 (애질런트 테크놀러지즈)를 이용하여 강도 데이터를 추출하였다. 상기 어레이는 43803개의 레서스 마카크 원숭이 프로브를 함유한다. 이들 프로브는 RefSeq (릴리즈 37, 2009년 10월), 유니젠(Unigene) (릴리즈 13, 2009년 10월), UCSC MRNA (2009년 10월), Ensembl (릴리즈 56, 2009년 9월), UCSC RheMac2 (2006년 1월)로부터 공급받은 것이다. 다수의 프로브는 오솔로그성 인간 유전자에 기초하여 예측된다. 추가로, 일부 프로브는 오직 마카카 물라타 cDNA로서만 주석이 달리고, 인간과의 상동성으로부터 추론될 수 있는 것 이외의 다른 것은 기능이 알려져 있지 않다. 분석은 트랜스크립톰 분석 전문 회사인 게노스플라이스(Genosplice: 프랑스 에브리)와 협력하여 수행하였다.
마이크로어레이
분석
애질런트 마이크로어레이 발현 데이터의 차별적 발현 분석은 바이오컨던터(Bioconductor) 프로젝트로부터의 limma를 이용하여 수행하였다 (문헌 [Smyth, 2004. Stat Appl Genet Mol Biol . 3:Article3]). 먼저, 배경 보정을 수행한 후, 이어서, limma 또한 사용하여 모든 뇌 및 혈액 샘플에 대한 어레이 사이의 정규화를 진행함으로써 원시 데이터를 정규화하였다. 어레이 익스프레스(Array Express) (http://www.ebi. ac.uk/arrayexpress/arrays/A-GEOD-9861/?page=71&pagesize=100&sortby=organism&sortorder=descending)에서 제공받은 애질런트의 어레이 정보 및 게노스플라이스에 의해 제공받은 유전자 정보를 사용하여 프로브에 주석을 달았다
limma 패키지는 먼저 각 유전자의 발현 데이터를 선형 모델로 피팅함으로써 차별적 발현 분석을 수행한다. 이어서, 경험적 베이즈(Empirical Bayes) (e베이즈(eBayes))를 이용하여 유전자 간의 정보를 차용하고, 이를 통해 본 발명자들은 소수의 어레이 간에도 분석을 수행할 수 있다.
뇌 마이크로어레이 데이터의 모든 차별적 발현 분석은 limma e베이즈 방법을 이용하여 수행하였다 (문헌 [Smyth, 2005. limma: Linear Models for Microarray Data. In: Gentleman et al. (Eds), Bioinformatics and Computational Biology Solutions Using R and Bioconductor . Statistics for Biology and Health. New York, NY: Springer]).
통계
뇌에서 고도로 발현된 유전자 비교
두 원숭이를 따로 분석하였다. 허혈성 및 비-허혈성 뇌 샘플을 비교하였을 때, 두 원숭이 모두에서 유전자 변화 배수가 2 초과이고, 원숭이 사이에 허혈성 샘플을 비교하였을 때, 또는 원숭이 사이에 비-허혈성 샘플을 비교하였을 때, 그의 변화 배수가 2 미만인 경우, 유전자를 "고도로 차별적으로 발현"인 것으로 표지하였다.
혈액에서 고도로 발현된 유전자 비교
폐색 전 샘플과 각각의 폐색 후 샘플을 비교함으로써 혈액 샘플을 분석하였다. 두 원숭이를 따로 분석하였다. 추가 분석을 위해 변화 배수가 가장 큰 시점을 선택하였고, "S1 최대 혈액" 및 "S2 최대 혈액"으로 명명하였다 (표 1). 폐색 전 샘플과 "S1 최대 혈액" 및 "S2 최대 혈액"을 비교하였을 때, 두 원숭이 모두 유전자의 변화 배수가 1.5 초과인 경우, 유전자를 "고도로 차별적으로 발현"인 것으로 표지하였다.
본원에서 정의된 바와 같이 허혈성 뇌 및 폐색 후 혈액 샘플 둘 모두에서 고도로 차별적으로 발현된 유전자만 오직 비교하였고, 이를 사용하여 공통의 고도로 차별적으로 발현된 유전자를 확인하였다.
데이터의 품질 관리
내부 검증
프로브-특이적 2 단계 택맨 R 유전자 발현 검정법(TaqMan R Gene Expression Assay)을 이용하여 마이크로어레이 결과를 검증하였다 (어플라이드 바이오시스템즈(Applied Biosystems)). 차별적 발현의 순위화 및 허혈 관련의 생물학적 주석에 기초하여 검증을 위한 유전자를 선택하였다. 본 발명자들은 표적 유전자 간의 정규화를 위해 SMC2를 선택하였고, 상기 유전자의 경우, 허혈성 및 비-허혈성 조직 샘플에서 일정한 발현을 보였다. 유전자 발현 검정법 프로브 ID는 하기와 같았다: HSPA1B (A 01 P010726), GADD45G (A 01 P018040), CDKN1A (A 01 P002585), SMC2 (A 01 P019124).
제조사의 프로토콜에 따라 슈퍼스크립트® III 제1-가닥 합성 키트(SuperScript® III First-Strand Synthesis Kit) (써모피셔 사이언티픽(ThermoFisher scientific))을 이용하여 각 샘플의 100 ng의 전체 RNA를 사용하여 cDNA를 생성하였다. 로슈 라이트사이클러 R480 시스템(Roche LightCycler R480 System) 상에서 실시간 PCR 반응을 수행하였다. 프리즘(Prism) 소프트웨어 v6.0c (그래프패드(GraphPad: 미국 캘리포니아주 라호야)를 이용하여, 만-휘트니 U 검정 (윌콕슨(Wilcoxon))과 함께 비교 CT 방법 (ΔΔCT 방법)을 이용하여 허혈성 조직과 비-허혈성 조직 사이의 유전자 발현을 비교하였다.
외부 검증
본 발명자들은 쿡(Cook) 등의 연구 (문헌 [Cook et al. (2012. Nature. 483(7388):213-7)])로부터의 데이터를 사용하여 본 발명자들의 결과를 입증하고자 하였다. 그러나, 본 연구는 또한 마카카 물라타의 가까운 친척인 시노물구스 마카크를 이용하여 추뇌류 영장류에서 뇌졸중 트랜스크립톰도 조사하였다 (문헌 [Street et al., 2007. BMC Genomics. 8:480]). 마카카 물라타에서 관찰된 결과를 검증하기 위해, 본 발명자들은 상기 쿡 등의 연구로부터의 위약 및 비-허혈성 트랜스크립톰 데이터를 분석하였다. 위약 허혈성 및 비-허혈성 데이터를 GEO (수탁: GSE35589)로부터 액세스하고, 상기 기술된 방법을 이용하여 분석하였다.
뇌-혈액 유전자 중복
순위-순위 초기하 중복 검정을 이용하여 뇌 및 혈액 차별적 발현 결과 사이의 유의적인 중복을 결정하였다 (문헌 [Plaisier et al., 2010. Nucleic Acids Res. 38(17):e169]). 상기 방법은 두 세트 사이의 중복이 가장 유의적인 지점의 컷-오프를 확인하기 위하여 분류된 유전자 목록의 모든 가능한 중복에 대해 초기하 검정을 수행한다. 두 원숭이 사이의 평균 log 변화 배수에 의해 전체 유전자 목록을 분류하였다. 뇌 및 혈액에서 발현이 변화한 특이적 유전자를 조사하기 위해, 본 발명자들은 뇌에서 고도로 차별적으로 발현된 유전자의 필터링된 목록을 작성하였고 (상기 방법 참조), 혈액에서 상기 유전자 각각에 대한 최대 변화 배수 값을 계산하였다.
유전자 세트 보강 분석
GSEA 커맨드 라인 툴(command line tool)을 이용하여 유전자 세트 보강 분석을 수행하였다 (문헌 [Subramanian et al., 2005. Proc Natl Acad Sci U S A. 102(43):15545-50]). 상기 툴은 미리 정의된 유전자 세트를 제공하고, 표현형 역할을 나타내는, 분류된 실험 목록의 상단 또는 하단 부근에서 각 세트의 보강 여부를 결정한다. GSEA는 평가된 각 유전자 세트에 대한 보강 점수 (ES)를 계산한다. 상기 점수는 세트가 분류된 실험 유전자 목록의 상단 또는 하단에서 과다표출된 정도를 나타낸다. 정규화된 보강 점수 (NES)는 유전자 세트의 크기에 의해 정규화된다.
뇌 및 혈액 차별적 발현 분석으로부터의 결과를 log 변화 배수에 의해 점수화하였다. 이들 목록을 GSEA 사전 순위화 함수에 전달하였다. 100개의 순열을 이용하여 분석을 실행하고, 10개 미만의 유전자 세트를 배제시켰다. 생성된 유전자 세트를 NES에 의해 분류하였다. GSEA ES는 유전자 세트가 분류된 유전자 목록의 상단 또는 하단에서 과다표출된 정도를 나타낸다. 목록을 아래로 이동시키면서, 유전자가 존재할 때에는 점수를 증가시키고, 존재하지 않을 때에는 점수를 감소시키면서 ES를 계산한다. 점수가 증가하는 규모는 유전자와 표현형 (미리 정의된 유전자 세트) 사이의 상관관계에 의존한다. ES는 목록을 아래로 이동시킬 때 만나게 되는 0으로부터의 최대 편차이다. ES가 양의 값인 것은 (상향 조절된 유전자에서) 목록 상단에서의 보강을 나타내고, ES가 음의 값인 것은 하단에서의 보강을 나타낸다. 정규화된 ES가 유전자 세트의 크기 차이, 및 유전자 세트와 발현 데이터 사이의 상관관계를 설명하고, 이로써, 유전자 세트 사이를 비교할 수 있다.
이들 유전자 세트 중 유전자들 사이의 상호작용을 STRING 데이터베이스를 사용하여 시각화하였다 (문헌 [Szklarczyk et al., 2015 . Nucleic Acids Res. 43(Database issue):D447-52]). 유전자의 변화 배수가 뇌에서는 적어도 2이고, 혈액에서는 적어도 1.5인 경우에 유전자를 STRING에 입력하였다. 라인의 두께가 관계가 있음을 나타내는 신뢰도를 표시하고, 큰 노드는 3차 구조에 대한 정보가 있는 단백질을 표시한다.
결과
동물을 허혈 발병 후 약 5.5시간째에 희생시켰다. 축 MRI 확산 강조 영상은 두 동물 모두 MCA 국소 허혈을 보였다 (데이터는 나타내지 않음). 상이한 두 동물에서 허혈 부피 분석 결과, 경색 부피는 고도로 가변적인 것으로 나타났고: S1이 S2보다 시각적으로 더욱 큰 경색 부피를 가졌다. 동물 S1 및 S2, 둘 모두에 대해 표재성 및 심부 경색이 관찰되었다. 경색은 또한 두 동물 모두 T2 flair 영상에서 관찰가능하였다. 윌리스 안지오-MRI(Willis Angio-MRI) 결과, 동물 S1의 경우, MCA는 근위부에서 폐색된 반면, 동물 S2의 경우, 덜 뚜렷한 것으로 나타났다. 경색 또한 동물 S1 및 S2에서 기저핵 수준에서 T1 시퀀스 상에서 관찰되었다.
유전자 발현 변화: 허혈성 뇌 조직
대 비
-허혈성 뇌 조직
본 연구에서, 허혈성 뇌 조직과 비-허혈성 뇌 조직 사이의 발현 변화를 각 유전자에 대하여 측정하고, 이들 변화의 효과를 유전자 세트 수준에서 조사하였다. 허혈성 뇌 조직으로부터의 발현 데이터를 허혈에 걸리지 않은 대측 반구의 상응하는 영역으로부터의 데이터와 비교하여 차별적 발현 분석을 수득하였다.
본 분석 결과, 허혈성 및 비-허혈성 뇌 샘플의 발현 패턴은 시각적으로 상이한 것으로 나타났다 (데이터는 나타내지 않음). 각 원숭이 내에서 허혈성 및 비-허혈성 뇌 샘플을 비교하였을 때, 유전자 변화 배수가 2 초과인 경우, 유전자는 고도로 차별적으로 발현된 것으로 간주되었고, 원숭이 사이의 허혈성 조직을 비교하거나, 또는 원숭이 사이의 비-허혈성 조직을 비교하였을 때 (변화 배수 < 2), 이들 유전자는 차별적으로 발현되지 않았다. 계층적 클러스터링을 이들 차별적으로 상위의 유전자 (37개의 유전자)에 적용시켰을 때, 허혈성 샘플은 비-허혈성 샘플과는 독립적으로 뚜렷하게 클러스터링된다.
고도로 차별적으로 발현된 유전자 모두 상향 조절되었다 (표 1)
내부 검증
마이크로어레이 결과의 강건함을 확인하기 위해, 허혈성-민감성 유전자 3개 (HSPA1B, GADD45G , CDKN1A)의 mRNA 수준을 동물로부터의 샘플을 사용하여 RT-qPCR에 의해 정량화하였다. 모든 시험 샘플 간에 불변의 발현 수준을 보인 것으로 관찰된 SMC2를 내부 참조 (하우스키핑)로서 사용하였다. 각 RNA 샘플에 대해 3회의 역전사를 수행한 후, 표적 유전자 및 참조 유전자, 둘 모두에 대해 반복 검정 측정을 수행하면서 3회의 독립 qPCR 실행하였다. 모든 유전자의 경우, 변화 방향 및 규모는 마이크로어레이 데이터와 매우 일치하였다 (도 1 및 표 2).
외부 검증
마카카 파스시쿨라리스(Macaca fascicularis)에서 쿡 등의 뇌졸중 연구 (문헌 [2012 . Nature. 483(7388):213-7])로부터의 트랜스크립톰 데이터의 분석시, 본원에 기술된 것과는 매우 다른 결과를 얻었다. 마카카 물라타에서의 상기 분석에서는 뇌졸중에 이환된 조직에서 다수의 상향 조절된 유전자가 나타났지만, 마카카 파스시쿨라리스로부터의 데이터에서는 주로 하향 조절된 유전자가 나타났다. 이는 가능하게는 대개 영장류에서 뇌졸중을 유도하는 방법이 매우 다르기 때문인 것으로 보인다. 쿡 등에 의한 연구는, 보통 인간에서 관찰되는 더욱 중증의 뇌졸중을 일으키는 것으로 쿡 등 그들이 인정한 외과적 중간 대뇌 동맥 폐색 (MCAO)을 이용하였다. 가능하게는 상기 더욱 중증의 뇌졸중 모델이 대개는 하향 조절된 유전자를 초래하면서, 대량의 세포 사멸을 일으켰다.
유전자 세트 보강
브로드 인스티튜츠 진 세트 인리치먼트 애널리시스(Broad Institutes Gene Set Enrichment Analysis: GSEA)를 이용하여 허혈성 뇌 조직에서 보강된 유전자 세트를 확인하였다 (문헌 [Subramanian et al., 2005. Proc Natl Acad Sci U S A. 102(43):15545-50]). GSEA의 홀마크 유전자로부터의 상위 5개의 보강된 유전자는 NFKB를 통한 TNFA 신호전달, 아폽토시스, P53 경로, 저산소증, 및 UV 반응 상향이었고, 이들은 모두 상향 조절되었다(표 3).
108개의 유전자로 이루어진 세트 중 60개가 NFKB를 통한 TNFA 신호전달 유전자 세트에서 핵심 보강을 보였다 (NES = 2.96). 본 발명자들이 데이터를 갖고 있는 상기 세트 중의 거의 모든 유전자는 상향 조절되고, 유의적으로 하향 조절된 유전자는 없으며: 단지 15개의 유전자만이 약간 하향 조절되고, 최대 변화 배수는 1.17이다.
아폽토시스 유전자 세트에서, 98개의 유전자 중 26개가 핵심 보강을 보인다 (NES = 2.57).
저산소증 유전자 세트에서, 118개의 유전자 중 33개가 핵심 보강을 보인다 (NES = 2.38).
UV 반응 상향 유전자 세트는 96개의 유전자 중 31개가 핵심 보강을 보였다 (NES = 2.3).
가장 유의적으로 보강된 하향 조절된 유전자 세트는 산화 인산화였다. 120개 중 84개의 상기 유전자가 핵심 보강을 보였다 (NES = -2.57).
유전자 생성물의 상호작용
뇌의 상위 유전자 세트 내에서 뇌 및 혈액에서 고도로 차별적으로 발현된 유전자(뇌에서 변화 배수 ≥ 2, 혈액에서 변화 배수 ≥1.5) (데이터는 나타내지 않음)의 유전자 생성물의 상호작용을 시각화하기 위하여 STRING 데이터베이스 (문헌 [Szklarczyk et al., 2015. Nucleic Acids Res. 43(Database issue):D447-52])를 사용하였다.
IL-6은 NFKB를 통한 TNFA 신호전달, 아폽토시스, 및 저산소증을 나타내는 네트워크에서 고도로 관련이 있는 구성원인 것으로 주목되었다. 추가로, CDKN1A는 상기 4개의 네트워크 모두에서 나타난다. CDKN1A와 HMOX1 사이의 상호작용은 아폽토시스-, p53 경로-, 및 저산소증-관련 유전자의 네트워크에서 관찰되었다. 유전자 ATF3 또한 4개의 네트워크 모두에서 나타나고, 상기 언급된 3개에서 IL-6과 상호작용한다. 뇌에서 5번째 순위화 유전자 세트 (표 3)인 UV 반응 상향은 상기 세트에서 차별적으로 발현된 상위 유전자 중 어느 것도 어떤 공지된 상호작용을 보이지 않기 때문에 제시하지 않는다.
유전자 발현 변화: 폐색 전 혈액 샘플 대 폐색 후 혈액 샘플
모든 폐색 전 혈액 샘플과 모든 폐색 후 혈액 샘플을 비교함으로써 대뇌 허혈 동안 혈액에서 차별적으로 발현된 유전자를 확인하였다. 계층적 클러스터링을 차별적으로 발현된 상위 유전자에 적용시켰을 때, 폐색 전 샘플 및 폐색 후 샘플은 따로 클러스터링된다 (데이터는 나타내지 않음). 또한, 상기 유전자 클러스터링에 기초하였을 때, 두 마카크의 혈액에서의 발현 패턴은 상이한 것으로 보인다. 원숭이 S1이 원숭이 S2보다 상기 유전자들의 더욱 심도깊은 상향 조절을 보인다. 두 원숭이의 이와 같은 분리는 뇌의 발현 패턴에서는 보이지 않는다 (데이터는 나타내지 않음).
뇌 샘플에서와 같이, 혈액 차별적 발현 결과의 유전자 세트 보강을 분석하였다. 상위 5개의 보강된 유전자 세트는 NFKB를 통한 TNFA 신호전달, 저산소증, 헤지호그 신호전달, 염증 반응, 및 혈관신생이다 (표 4).
NFKB를 통한 TNFA 신호전달 및 저산소증 유전자 세트 또한 뇌에 대한 상위 5개의 유전자 세트에도 나타난다 (표 4).
NFKB를 통한 TNFA 신호전달 유전자 세트에서, 108개의 유전자 중 37개가 핵심 보강을 보였다 (NES = 1.92).
저산소증 유전자 세트에서 118개의 유전자 중 42개가 핵심 보강을 보였다 (NES = 1.91).
헤지호그 신호전달 유전자 세트에서 24개의 유전자 중 10개가 핵심 보강을 보였다 (NES = 1.77).
염증 반응 유전자 세트에서 110개의 유전자 중 35개가 핵심 보강을 보였다 (NES = 1.77).
혈관신생 유전자 세트에서 20개의 유전자 중 9개가 핵심 보강을 보였다 (NES = 1.76).
뇌 및 혈액 사이에서 공통된 차별적으로 발현된 유전자
유전자를 변화 배수에 의해 분류하였을 때, 뇌 및 혈액으로부터의 차별적 발현 결과를 유의적인 중복에 대해 조사하였다. 본 발명자들은 분류된 두 유전자 세트가 특히, 두 근단부: 허혈 동안 가장 크게 상향 조절된 유전자 및 가장 크게 하향 조절된 유전자에서 매우 유사하다고 제시한다. 본 발명자들은 또한 열지도로부터 뇌와 혈액 샘플 사이에서 유의적으로 중복되는 가장 유의적인 2,156개의 하향 조절된 유전자, 및 유의적으로 중복되는 493개의 상향 조절된 유전자인 중복 유전자도 제시하였다 (도 2). 이들 유전자 대다수는 비교적 낮은 발현 변화 배수를 보이고 있지만, 뇌와 혈액 샘플 사이에서 차별적으로 발현된 유전자의 중복은 매우 높다.
비록 이들 중복 세트 중의 다수의 유전자는 고도로 차별적으로 발현되지는 않았지만, 일부는 고도로 차별적으로 발현되었고, 이는 본 발명자들이 가장 관심을 갖고 있는 뇌에서 매우 높은 발현 변화을 보이는 것이다. 뇌에서 고도로 차별적으로 발현된 것으로 확인된 유전자들 중, 9개가 혈액에서도 또한 차별적으로 발현되었다 (변화 배수 ≥ 1.5; 표 1, 굵은체로 강조 표시). 상기 유전자들 중 9개의 유전자 모두 가장 유의적인 초기하 중복 (굵은체 표시) 내에 존재한다. 이들 유전자는 PTGS2 , G0S2 -유사, DUSP1 , LDLR -유사, HMOX1 , HSPA1B , BAG3 , ADM , 및 TM4SF1이다. 이들 유전자 대다수는 혈액에서 발현의 급격한 증가를 보이며, 이는 시간이 경과함에 따라 안정된다 (도 3 및 4).
논의
MCA 동맥에서 인간 트롬빈 주사를 맞은 비-인간 영장류 모델 (문헌 [Gauberti et al., 2012. Cerebrovasc Dis. 33(4):329-39])을 이용하여 허혈성 대뇌 뇌졸중 동안의 유전자 발현 변화 패턴을 연구하였다. 이는 부분 MCA 허혈을 동반한 국소 허혈의 색전성 모델이다. 6시간의 시간 프레임을 사용하였는데, 그 이유는 인간에서의 치료 개입이 가능한 시간창이기 때문이다 (혈전용해 최대 4h 30; 혈전절제술 발병 후 최대 6h).
뇌 및 혈액으로부터의 마카크 마이크로어레이 발현 데이터에 관한 본 발명자들의 연구 결과, 허혈성 및 비-허혈성 샘플은 그의 발현 프로파일에 기초하여 구별될 수 있고, 고도로 차별적으로 발현된 유전자 대다수는 허혈 후 6시간째 허혈 시나리오에서 상향 조절되는 것으로 밝혀졌다. 이들 상향 조절된 유전자 중 다수는 세포 사멸 및 DNA 손상 수복에 관여하는 경로에 속한다. 뇌 및 혈액에서 차별적으로 발현된 유전자 비교 결과, 유전자 발현 패턴이 유의적으로 중복되는 것으로 밝혀졌다.
이러한 결과는 뇌 및 혈액에서 트랜스크립톰을 통해 허혈성 뇌졸중을 확인할 수 있는 잠재성을 시사한다.
허혈성 뇌에서의 유전자 발현
PCA 분석에 의해 데이터의 품질을 확인하였고, 이는 유전자 발현에 의해 두 원숭이 모두를 구별할 수 있고, 비-허혈로부터 허혈을 구별할 수 있는 것으로 나타났다. 추가로, 내부 검증을 통해 생성된 결과를 추가로 입증하였다.
마카카 물라타 뇌 발현 데이터의 계층적 클러스터링으로 허혈성 및 비-허혈성 뇌 샘플의 강력한 독립적인 클러스터링이 밝혀졌다 (데이터는 나타내지 않음). 상기 결과는 발현 프로파일에 기초하여 허혈성 뇌 조직을 확인할 수 있는 잠재성을 시사하는 것이었다. 가장 유의적으로 차별적으로 발현된 유전자는 상향 조절되었고, 이는 마우스에서의 다수의 이전의 허혈 연구와 일치한다 (문헌 [Butner et al., 2009. Brain Res. 1252:1-14]; [Hori et al., 2012. Dis Model Mech . 5(2):270-83]). 본 연구에서는 뇌에서 고도로 차별적으로 발현된 유전자를, 두 원숭이 모두에서 최소 변화 배수가 2인 유전자로서 정의하였고, 상기 유전자는 두 원숭이 사이의 비-허혈성 샘플을 비교하였을 때, 또는 원숭이 사이의 허혈성 샘플을 비교하였을 때, 차별적으로 발현되지 않는다 (변화 배수 < 2). 본 발명자들의 분석 결과, 뇌에서 37개의 유전자가 상향 조절되었고, 하향 조절된 것은 없었다. 이러한 결과는 6시간 후에 115개의 유전자가 상향 조절되고, 19개의 유전자가 하향 조절된 것으로 나타난 버트너(Butter) 등의 결과와 유사하다 (문헌 [Buttner et al., 2009. Brain Res. 1252:1-14]). 버트너 등에 의해 확인된 유전자의 개수가 많을수록, 더욱 큰 사용 발현 프로파일 및 종 사이의 발현차에 의해 설명될 수 있다.
허혈성 뇌 조직에서 모든 고도로 차별적으로 발현된 유전자는 상향 조절되었다. 이들 유전자들 다수는 허혈성 뇌졸중에서 다양한 기능, 특히, 스트레스 반응, 아폽토시스, 및 신호 전달을 위해 상향 조절된 유전자인 것으로 이전에 확인된 것이다.
상향 조절된 스트레스 반응 유전자 중에는 7개의 열 충격 단백질 HSPA1B (Hsp70), HSP40, HSPB1, HSPA4L, 및 DNAJA4 (Hsp40-유사)가 있었다 (표 1). 다수의 연구를 통해 열 충격 단백질이 허혈에서 고도로 상향 조절되는 것으로 확인되었다 (문헌 [Schmidt-Kastner et al., 2002. Brain Res Mol Brain Res. 108(1-2):81-93]; [Buttner et al., 2009. Brain Res. 1252:1-14]; [Kawahara et al., 2004. J Cereb Blood Flow Metab. 24(2):212-23]; [Tang et al., 2002. Eur J Neurosci. 15(12):1937-52]). 상기 유전자의 인간 오솔로그는, 응집되지 않도록 단백질을 안정화시키고, 유비퀴틴-프로테아좀 경로에 관여하는, 스트레스 유도성 유전자인 것으로 잘 특징화되어 있다 (NCBI, 수탁: NM_005346.5). Hsp70은 허혈성 뇌졸중에서 가장 일반적으로 보고된 상향 조절된 열 충격 단백질이다 (문헌 [Cox-Limpens et al., 2014. Brain Res. 1564:85-100]). 마카카 물라타에서, 열 충격 단백질 패밀리 A (Hsp70) 구성원 1B (HSPA1B)가 허혈성 뇌 조직에서 가장 상향 조절된 유전자이다. 마우스에서의 HSPA1B의 넉아웃 연구 결과, 상기 유전자가 결핍된 심장 세포는 허혈에 의한 손상에 대해 더욱 민감한 것으로 나타났다 (문헌 [Kim et al., 2006. Circulation. 113(22):2589-97]). 대뇌 허혈 연구 결과, hsp70 넉아웃 마우스는 야생형 마우스보다 더욱 큰 경색 부피를 경험하였고 (문헌 [Lee et al., 2004. Stroke. 35(9):2195-9]), Hsp70을 과다발현하는 마우스는 축소된 경색 크기 및 개선된 신경 기능을 보인 것으로 나타났다 (문헌 [Zheng et al., 2008. J Cereb Blood Flow Metab. 28(1):53-63]). 마카크에서 HSPA1B의 높은 수준의 차별적 발현은 상기 유전자가 허혈을 앓는 영장류 뇌에서 신경보호 역할을 할 수 있음을 시사하는 것이다. 또한, 흥미롭게도, 이들 마이크로어레이로부터 가장 차별적으로 발현된 유전자들 중 하나는 열 충격 단백질 호몰로그인 DNAJB1이라는 것에 주목한다.
NPAS4는 이 또한 신경보호제로 알려져 있는, 또 다른 고도로 차별적으로 발현된 스트레스 반응 유전자이다 (문헌 [Choy et al., 2015. Int J Mol Sci. 16(12):29011-28]). 상기 전사 인자는 뇌의 뉴런에서 발현되고, 흥분성 및 억제성 뉴런에서의 조기 발현에서 중요한 역할을 한다. 그의 발현은 뉴런 세포가 스트레스하에 처해지는 다양한 상황에 의해 유도된다. 본 발명자들의 연구에서, NPAS4의 log2 변화 배수는 S1에서는 3.57이고, S2에서는 2.65였다 (표 1). NPAS4에 의해 제어되는 유전자 C- FOS (문헌 [Ramamoorthi et al., 2011. Science. 334(6063):1669-75]) 또한 본 발명자들의 연구에서 고도로 차별적으로 발현되고, 여기서, log2 변화 배수는 S1에서는 2.53이고, S2에서는 3.77이었다. C-FOS는 공통적으로 대뇌 허혈 존재하에서 상향 조절되는 것으로 관찰된다 (문헌 [Cox-Limpens et al., 2014. Brain Res. 1564:85-100]).
유전자 활성화 전사 인자 3 (ATF3)은 그 다음으로 가장 차별적으로 발현되는 유전자이다. ATF3은 cAMP 반응성 요소-결합 (CREB) 패밀리의 전사 인자의 구성원을 코딩한다. 이는 세포성 스트레스 반응에 관여한다. ATF3 log2 변화 배수는 S1에서는 2.99이고, S2에서는 3.38이었다 (표 1). 추가로, 상기 유전자는 상위 GSEA 유전자 세트 내에서 고도로 관련이 있는 구성원이다 (데이터는 나타내지 않음). 마우스에서의 이전 실험에서 ATF3 넉아웃이 뇌 허혈 후에 더욱 큰 경색 부피를 갖고, 신경 기능 악화를 보인 것으로 나타났다 (문헌 [Wang et al., 2012. Neuroscience. 220:100-8]).
허혈성 뇌 조직에서 상향 조절된, 다른 중요한 스트레스 반응 유전자는 2개의 손상 유도성 유전자, GADD45G 및 GADD45B이다 (문헌 [Growth Arrest and DNA-Damage inducible 45]). GADD45 유전자는 DNA 손상과 연루되어 있다. GADD45G log2 발현 변화 배수는 S1에서는 2.25이고, S2에서는 2.04였고, GADD45B의 경우, 각각, 1.08 및 2.17이었다. 열 충격 단백질과 같이, Gadd45 패밀리의 유전자는 대뇌 허혈을 조사하는 다수의 설치류 연구에 의하면, 상향 조절되는 것으로 보고되었다 (문헌 [Schmidt-Kastner et al., 2002. Brain Res Mol Brain Res. 108(1-2):81-93; 7-9, 20]). 이전의 허혈 동안 래트의 뇌에 관한 분석 결과, 이들 유전자의 발현은 일과성 완전 허혈에 의해 유도되는 것으로 밝혀졌다 (문헌 [Chen et al., 1998. J Cereb Blood Flow Metab. 18(6):646-57]). 상기 연구원들은 이것이 상기 유전자의 신경보호 역할을 시사하는 것일 수 있다고 결론지었다. 본 발명자들의 결과는 허혈 동안의 상기 발현 증가 또한 영장류에서 나타나고, 이는 추가로 허혈성 세포 반응에서의 그의 역할과 관련이 있다는 것을 나타낸다.
아폽토시스성 유전자 BAG3 또한 유의적으로 허혈성 뇌 조직에서 상향 조절되었고, 여기서, log2 변화 배수는 S1에서는 1.7이고, S2에서는 2.97이었다. 래트에서의 대뇌 허혈 발현 연구에서도 또한 상기 유전자가 고도로 상향 조절된다고 보고되었다 (문헌 [Schmidt-Kastner et al., 2002. Brain Res Mol Brain Res. 108(1-2):81-93]). 세포골격 단백질 분해는 허혈 후에 발생하는 것으로 공지되어 있으며 (문헌 [Lipton, 1999. Physiol Rev. 79(4):1431-568]), 흥미롭게도, 본 발명자들은 유전자 활성-조절된 세포골격-연관 단백질 (ARC)이 허혈성 뇌 조직에서 상향 조절되는 것을 관찰하였다 (log2 변화 배수 S1에서, 1.84 및 S2에서, 1.9). ARC의 상향 조절은 이전의 래트에서의 대뇌 허혈 연구에서도 관찰되었다 (문헌 [Buttner et al., 2009. Brain Res. 1252:1-14]).
대뇌 허혈에 연루된 또 다른 부류의 유전자로는 이중-특이적 포스파타제 (Dusp)가 있다 (문헌 [Wang et al., 2011. Brain Res. 1372:13-21]). 그의 단백질 생성물은 MAPK 단백질을 불활성화시킬 수 있다. 본 발명자들의 연구에서, 2개의 Dusp 유전자, DUSP1 (log2 변화 배수 S1에서, 1.43 및 S2에서, 1.43) 및 DUSP5 (log2 변화 배수 S1에서, 1.05 및 S2에서, 1.67)가 고도로 상향 조절되었다. 흥미롭게도, Dusp5는 p53의 표적인 것으로 제안되었다 (문헌 [Ueda et al., 2003. Oncogene. 22(36):5586-91]).
혈액에서의 유전자 발현 변화
혈액에서 관찰된 발현 패턴은 뇌에서의 것과 유사하였지만, 혈액 트랜스크립톰에 관한 본 연구에서는 일부 제한이 있었다. 샘플 개수가 비교적 적기 때문에 (각 원숭이마다 한 시점당 1개의 샘플), 시간 경과 분석은 실행 불가능하였다. 시간 경과 분석 대신, 폐색 전에 수집된 샘플을 각 폐색 후 샘플과 쌍별 방식으로 비교하였다. 유전자 세트 분석을 수행하기 위해, 가장 큰 발현 변화를 얻은 비교를 위한 차별적 발현 결과를 GSEA와 함께 사용하였다. 본 분석에 의해 연루된 유전자 세포는 뇌에서의 발현 패턴과 강력한 상관관계를 보였다.
혈액 발현 수준의 계층적 클러스터링 결과, 폐색 전 및 폐색 후 샘플은 독립적으로 클러스터링되는 것으로 나타났다 (데이터는 제시되지 않음). 비록 분리가 뇌 샘플에서만큼 극명하지는 않지만, 여전히 폐색 전과 폐색 후 사이의 유전자 발현에서의 차이는 뚜렷하다. 이러한 결과는 추가 실험을 통해 뇌졸중 진단에 사용될 수 있는 혈액 바이오마커 패널을 밝혀낼 수 있음을 시사한다. 본 연구에서는 샘플 및 개체의 수의 적기 때문에, 진단에 사용될 수 있는 유전자 서브세트를 특정하기는 어려울 수 있지만, 단, 상이한 발현 패턴은 샘플 크기가 더 커짐에 따라 가능할 것으로 보인다고 제안한다.
대뇌 허혈을 앓은 마카크의 혈액에서 차별적으로 발현된 유전자에 관한 본 발명자들의 분석을 통해 뇌와 같이, 혈액에서의 전사체 대다수는 상향 조절되는 것으로 밝혀졌다. 원숭이 사이에서 샘플을 풀링하고, 폐색 후 샘플을 풀링하였을 때, 651개의 유전자는 높은 수준의 차별적 발현을 보이고 (변화 배수 2 초과), 그 중 513개는 상향 조절된다.
이들 차별적으로 발현된 유전자 중에 4개의 S100 유전자: S100A8 , S100A12 , S100P, 및 S100A9가 있다는 점이 주목할 만하다. S100은 신경아교세포로부터의 칼슘-결합 단백질이다. 상기 군 중 가장 고도로 차별적으로 발현되는 것은 S100A8 이고(log2 변화 배수 3.29, p = 0.027; 데이터는 나타내지 않음), 이는 염증 유발성 기능과 강력한 연관성을 갖는다 (문헌 [Sedaghat & Notopoulos, 2008. Hippokratia. 12(4):198-204]).
대뇌 허혈에 연루된 유전자 세트
뇌
뇌 발현 데이터의 유전자 세트 보강 분석 결과, 허혈성 뇌 샘플에서 상향 조절되는 수개의 유전자 세트가 DNA 수복 및 아폽토시스에 관여하는 것으로 밝혀졌다. 상위 5개의 보강된 유전자 세트는 NFKB를 통한 TNFA 신호전달, 아폽토시스, p53 경로, 저산소증, 및 UV 반응 상향이었다. 이들 경로 중 일부는 이전 연구에서 대뇌 허혈과 관련이 있는 것으로 기술되었다.
뇌에서 가장 보강된 유전자 세트는 NF-κB를 통한 종양 괴사 인자 알파 (TNFA) 신호전달이다. TNFA 시토카인은 염증 반응에 관여하는 NFKB를 활성화시킨다. 다수의 이전 연구에서 염증 유발성 시토카인의 상향 조절이 보고되었다 (문헌 [Schmidt-Kastner et al., 2002. Brain Res Mol Brain Res. 108(1-2) :81-93]; [Lu et al., 2004. J Neurosci Res. 77(6): 843-57]; [Broughton et al., 2009 . Stroke. 40(5) :e331-9]).
또한, 아폽토시스 및 p53 경로에 관여하는 유전자 세트도 상향 조절되었다. 상기 경로는 DNA 손상 또는 세포 스트레스 발생시에 활성화되고, 이전 연구에서는 다양한 아폽토시스 유발성 인자의 상향 조절을 언급한 바 있다 (문헌 [Buttner et al., 2009. Brain Res. 1252:1-14]).
추가로, NFKB 및 p53 경로는 신경보호에 기여하는 것으로 밝혀졌다 (문헌 [Zhang et al., 2005. J Cereb Blood Flow Metab . 25(1):30-40]; [Chen et al., 2011. Antioxid Redox Signal. 14(8):1505-17]).
흥미롭게도, 유전자 IL-6은 TNFA 신호전달, 아폽토시스, 및 저산소증 경로의 고도로 관련이 있는 구성원인 것으로 주목된다 (데이터는 나타내지 않음). 상기 유전자는 log2 발현 증가 배수가 S1 및 S2 뇌 샘플에서 각각 1.08 및 1.53이다. HMOX1-CDKN1A 상호작용 또한 수개의 유전자 세트 (아폽토시스, p53, 및 저산소증) 사이에 공통되고, HMOX1 의 상향 조절 또한 유의적이다.
혈액
혈액으로부터의 차별적 발현 결과의 유전자 세트 보강 분석을 통해 신호전달, 저산소증, 및 염증 반응에 관여하는 경로가 밝혀졌다. 허혈성 혈액 샘플에서 보강된 상위 5개 유전자 세트는 NFKB를 통한 TNFA 신호전달, 저산소증, 헤지호그 신호전달, 염증 반응, 및 혈관신생이었다.
흥미롭게도, 뇌에서 가장 보강된 유전자 세트는 또한 혈액에서도 보강된다: NFKB를 통한 TNFA 신호전달 및 저산소증 반응. 이들 두 경로 모두 허혈 반응의 모델에서 잘 피팅된다. NFKB를 통한 TNFA 신호전달 유전자 세트에서 108개의 유전자 중 37개가 혈액에서 핵심 보강을 보이고 (NES = 1.92), 저산소증 반응 유전자 세트에서 118개의 유전자 중 42개가 핵심 보강을 보였다 (NES = 1.91). 유전자 세트 NFKB를 통한 TNFA 신호전달은 허혈에 가장 많이 관여하는 경로에서도 보이며, 뇌에서는 세트 중 50% 초과에서 핵심 보강을 보이고, 혈액에서는 30% 초과에서 핵심 보강을 보인다.
뇌 및 혈액 사이에서 공통된 발현
뇌 및 혈액 차별적 발현을 비교하기 위해, 모든 유전자를 변화 배수에 의해 분류하고, 모든 가능한 초기하 중복을 시험하였으며, 그 결과, 유전자 목록에서 상향 및 하향 조절되는 유전자, 둘 모두의 유의적인 중복이 있었다. 상향 및 하향 조절되는 유전자 중 가장 유의적인 초기하 중복에 관한 본 발명자들의 분석 결과, 교집함에 각각 493 및 2,156개의 유전자를 함유하는 것으로 나타났다 (도 2).
추가로, 각 원숭이에서 폐색 전 및 폐색 후 샘플을 따로 비교하고, 가장 큰 변화 배수를 초래하는 시점만 유지시킨 혈액 발현 데이터의 가장 엄격한 분석 또한 수행하였다. 이들 결과는 뇌 발현 데이터와 병합하였다. 유전자를 뇌 (변화 배수 ≥ 2) 및 혈액 (변화 배수 ≥1.5), 둘 모두에서 높은 차별적 발현에 대해 필터링하였다. 뇌 및 혈액, 둘 모두에서 9개의 유전자 유전자가 고도로 차별적으로 발현되는 것으로 확인되었다 (표 1). 이들 유전자 9개 모두 상기 기술된 가장 유의적인 초기하 중복에서 보인다.
이들 상위 9개의 유전자는 HSPA1B, PTGS2, BAG3, ADM, TM4SF1, DUSP1, HMOX1, LDLR-유사, 및 G0S2였다. HSPA1B, BAG3, 및 DUSP1은 이전 섹션에서 논의된 바 있다. 이들 유전자들 대다수는 발현의 급격한 증가를 보이며, 이는 시간이 경과함에 따라 안정된다 (도 3 및 4).
프로스타글라딘-엔도퍼옥시드 신타제 2 (PTGS2/COX2)는 프로스타글라딘 생합성에서 중요한 역할을 하는 효소이다. 상기 유전자는 염증 동안 상향 조절되는 것으로 알려져 있고, 이는 아스피린의 표적이다. 아스피린은 프로스타글라딘 생산을 억제시키고, 일부 투여량은 뇌졸중의 위험을 감소시킨다 (문헌 [Tohgi et al., 1992. Stroke. 23(10):1400-3]; [Eikelboom et al., 2002. Circulation. 105(14):1650-5]).
혈액에서 아드레노메둘린 (ADM) 유전자 발현 수준은 허혈성 뇌졸중의 중증도와 연관이 있는 것을 밝혀졌다 (문헌 [Liu et al., 2014. Int J Neurosci. 124(4):271-80]). 리우(Liu) 등은 말초 혈액 백혈구의 ADM 발현 수준이 조직 손상의 중증도를 나타낼 수 있다고 제안한다. 이러한 가설은, MRI에 의해 제시된 바와 같이, 원숭이 S1은 더욱 큰 경색 부피를 가지고 (데이터는 나타내지 않음), 이는 또한 S2에서보다 혈액 중에서 더 높은 수준의 ADM 발현을 보이는 바, 본 발명자들의 결과에 연루되어 있다.
헴 옥시게나제 1 (HMOX1)는 이전에 본 발명자들이 논의한 바 있는 열 충격 패밀리 단백질의 구성원이다. 이는 뇌졸증과 같은, 산화적 스트레스 매개 손상에 대한 세포 방어 시스템의 일부인 것으로 여겨진다 (문헌 [Chen & Maines, 2000. Cell Mol Biol (Noisy-le-grand). 46(3):609-17]). 추가로, 이전 연구에서는 대뇌 허혈 후에 HMOX1은 뇌에서 상향 조절된 것으로 나타났다 (Zhao et al., 2017. J Stroke Cerebrovasc Dis. 26(7):1622-1634).
결론
본 발명자들의 데이터는 허혈성 뇌 및 혈액 사이의 공통 시그니쳐가 존재한다는 것을 보여주고, 이는 생검 트랜스크립톰 발현 프로파일링을 위한, 허혈성 뇌졸중 환자를 특징화하기 위한, 및/또는 허혈성 뇌졸중 환자에서 신경보호 약물 평가를 위한 동반 바이오마커 개발을 위한 도구로서의 혈액 트랜스크립톰의 개발을 뒷받침한다.
비록 혈장 세포외 비코딩 RNA (ex-RNA)가 표적 조직에서 유전자 발현의 네트워크를 직접 조정하는 순환 RNA 분자 부류이지만 (문헌 [Mick et al., 2017. Stroke. 48(4):828-834]), 뇌 및 혈액에서 RNA 코딩 서열의 공통 프로파일을 확인하는 것은 전혀 예상하지 못했던 것이다. 대뇌 허혈 환자의 혈액에서 관찰되는 허혈 관련된 유전자의 상기와 같은 발현 패턴은 이전의 무어(Moore) 등에 의한 연구 (문헌 [Moore et al. (2005. Circulation. 111(2):212-21])에서도 언급된 바 있다. 그들은 비록 뇌는 저산소성이지만, PBMC 그 자체는 저산소성은 아니어도, PBMC에서 저산소증과 관련된 유전자를 발견하게 되었다. 본 발명자들의 결과는 더 나아가 혈액이 허혈성 뇌졸중을 확인하기 위한 진단 도구로서 사용될 수 있다는 무어 등의 결론에 이르게 된다.
실시예
2: 임상 연구 프로토콜
본 발명자들은 MCA 동맥에서 인간 트롬빈 주사를 맞은 비-인간 영장류 모델 (문헌 [Gauberti et al., 2012. Cerebrovasc Dis. 33(4):329-39])을 이용하였다. 본 발명자들의 연구를 통해 허혈성 및 비-허혈성 샘플이 허혈 후 6시간째의 그의 발현 프로파일에 기초하여 구별될 수 있다는 것이 밝혀졌다. 확인된 상향 조절된 유전자는 세포 사멸 및 DNA 손상 수복에 관여하는 경로에 속한다. 뇌 및 혈액에서 차별적으로 발현된 유전자 비교 결과, 유전자 발현 패턴이 유의적으로 중복되는 것으로 밝혀졌다.
종합하면, 이들 결과는 뇌 및 혈액에서의 트랜스크립톰 프로파일을 통해 허혈성 뇌졸중을 확인할 수 있는 잠재성을 시사하였다.
뇌 및 혈액에서 9개의 가장 유의적으로 중복되는 상향 조절된 유전자가 확인되었고, 이는 인간 연구에서 추가로 사용된다.
본 발명자들은 원숭이로부터 생성된 데이터를 인간으로 번역할 것을 제안한다. 허혈성 뇌졸중의 영장류 모델에서 허혈성 뇌 및 말초 혈액, 둘 모두에서 확인된 상향 조절된 유전자를 20명의 허혈성 환자, 20명의 출혈성 환자, 및 매칭되는 대조군으로부터의 샘플에서 연구한다. 이어서, 본 발명자들은 다른 심혈관 질환에서 이미 수행된 바와 같이 신속한 검출 시험을 잠재적으로 발생할 수 있도록 하기 위해 상응하는 단백질을 생각하고 있다.
파일럿 사례-대조군 연구
먼저 연령, 성별, 및 환자에서 인덱스 뇌졸중 전에 점수 (유럽 심장 점수(European Heart Score))에 의해 측정된 심혈관 위험도에 대하여 쌍을 이루는, 항상 허혈성 뇌졸중인 사례를 인용한 사례-대조군 연구.
허혈성 사례는 브레스트(Brest) 뇌졸중 등록소로부터 동원된다. 등록소는 년간 900명의 환자를 포함한다. 대조군은 한 센터 (브레스트 대학 병원(Brest University hospital))로부터 동원된다.
1차 목적:
그의 발현이 유의적으로 증가된 것으로 확인된 유전자에 기초하여 RNA 혈액 바이오마커 검사를 측정하고자 한다.
연구 디자인:
먼저 연령, 성별, 및 환자에서 인덱스 뇌졸중 전에 점수 (유럽 심장 점수)에 의해 측정된 심혈관 위험도에 대하여 쌍을 이루는, 항상 허혈성 뇌졸중인 사례를 인용한 사례-대조군 연구.
1차 종점:
허혈 발현 후 6시간째 확인된 각 유전자의 발현 (log2로 측정).
1차 통계학적 분석:
각 후보 유전자의 발현은 쌍별 데이터에 대한 스튜던트 검정법을 이용하여 사례 및 대조군에서 비교된다.
2차 통계학적 분석
:
각 유전자의 발현은 허혈성 뇌졸중의 급성기 내지 그 후 3개월 사이의 사례에 대해 비교된다.
전체 연구를 위한 샘플 크기 추정
:
사례와 대조군 사이의 차이는 log2 발현 강도의 표준 편차가 1 미만 (개인 데이터)인 경우, 대조군 대비 사례인 경우, 1.5배 (변환 배수 FC = 1.5 및 log2FC = 0.585)로 설정된다.
이러한 가설 (차이 = 0.585 및 표준 편차 = 1), 검정력 90% 및 시험 다중성에 대한 본페로니(Bonferroni) 보정하에, 필요한 대상체의 수는 사례의 경우, 110명 및 대조군의 경우, 110명인 것으로 추정된다. 반응 보정 수준이 알려져 있지 않은 바, 상기 계산은 쌍형성에 의해 제공되는 가능한 검정력 증가의 효과는 고려하지 않은 것이다.
포함 기준
환자의 경우
:
연령 > 18세; 6시간째보다 열등한 경동맥 허혈성 뇌졸중 발병; 6시간 이전에 T1 혈액 샘플을 가질 수 있는 능력; 혈전용해 또는 혈전절제술에 대한 유자격.
초기 NIHSS 점수 > 0; 허혈성 뇌졸중과 함께 화합성인 CT 또는 MRI 영상화를 보이는 환자; MRI 또는 CT 관류 및 혈관 대동맥 판막 위 혈관 및 대뇌내 혈관 (윌리스 서클(Willis circle)) 영상화를 통한 반영부 분석을 가능하게 하는 다중 모달 영상화를 보이는 환자.
배제 기준은 대뇌내 출혈을 보이는 환자를 포함한다.
대조군의 경우
연령 > 18세; 뇌졸중을 앓지 않는 표준화된 질문서; 심혈관 질환을 앓지 않고, 뇌졸증을 보이지 않는 고위험 심혈관 대상체.
사례 보고 양식 (
CRF
):
각 환자 및 대조군에 대해, 인구 통계학적 특징 및 임상적 특징, 심혈관 위험 인자 및 현행 치료를 브레스트 뇌졸중 등록소의 표준화된 보고 양식을 사용하여 보고한다.
대뇌 영상화:
급성기에서, 관류 MRI 또는 CT 및 안지오-MR 또는 안지오-스캔.
임상 및 영상화 추적 검사:
환자의 경우, 3개월 ± 15일째 순위화 점수 및 3개월 ± 15일째 대뇌 MRI.
환자당 샘플 개수:
42 mL의 혈액을 하기 6개의 상이한 시점에 채취: 뇌졸중 발병 후, < 6시간, 12시간 ± 2, 24시간 ± 4, 48시간 ± 4, 7일 ± 2일, 및 3개월 ± 15일째.
대조군당
샘플 개수:
각 대조군에 대하여 1번씩 42 mL의 혈액을 채취.
환자 및 대조군 수:
허혈성 사례의 경우, 20명의 환자; 연령, 성별, 및 유럽 심장 점수에 대해 허혈성 사례와 매칭되는 20명의 대조군.
출혈성 환자
출혈성 사례는 허혈성 군에서 동일한 환자당 샘플수를 갖는 상이한 군으로서 브레스트 뇌졸중 등록소로부터 동원된다.
포함 기준
환자의 경우:
연령 > 18세; 6시간째보다 열등한, 발병시 대뇌내 출혈; 6시간 이전에 T1 혈액 샘플을 가질 수 있는 능력.
초기 NIHSS 점수 > 0; 허혈성 출혈성과 함께 화합성인 CT 또는 MRI 영상화를 보이는 환자.
배제 기준은 외상성 대뇌내 출혈을 보이는 환자 및 허혈성 뇌졸중을 보이는 환자를 포함한다.
환자수
출혈성 사례의 경우, 20명의 환자
윤리적인 측면:
헬싱키 선언(Declaration of Helsinki)의 원리 및 임상시험 실시기준(GCP - ICHE6)에 따라 프로젝트를 수행한다. 이는 임상 실험을 위한 프랑스 규정에 따라 승인을 위해 인간 연구 윤리 위원회(Human Research Ethics Committee)에 제출된다. 사정 동의서는 각 참가자로부터 수거된다.
데이터 관리 및
바이오뱅킹
:
데이터 입력은 소프트웨어 클린사이트(Clinsight) (캡쳐 시스템(Capture system))에 의해 관리되는 데이터베이스 내로 데이터 관리자에 의해 수행된다. 바이오뱅크는 생물학적 공급원 (CRB - 생물 자원 센터(Centre de Ressources Biologiques)) 공인 NFS 96-900에 대해 브레스트 대학 병원 센터에 보관된다.
환자 및 대조군 동원
동원 센터:
환자 및 대조군 표현형 뿐만 아니라, 채혈을 브레스트의 CHRU를 통해 실행한다.
영상화
특징화
및
특징화된
후속 데이터 프로세싱
초기의 기능적 영상화 (CT 또는 MRI 관류)의 목적은 경색 코어 및 그의 반영부를 지도화하고, MRI 상에서 3개월째 상기 두 구역의 진화를 추적하고자 하는 것이다. 초기 영상화는 혈관 개방성을 고려한다. 소프트웨어를 통해 MRI 및 CT 스캔에 대한 표준화된 관류 분석을 할 수 있다. 또 다른 소프트웨어를 통해 MRI 상에서 최종 부피를 추정할 수 있고, 제1 영상화시 평가된 반영부와 비교를 할 수 있다.
영상화 플랫폼
:
초기 영상화를 위해 조영제와 함께, 64-행 (또는 그 이상) 다중-검출기 CT 스캔 또는 1.5 테슬라(Tesla) MRI 또는 3.0 테슬라 MRI 스캐너를 이용한다.
데이터 획득 방법:
하기 방법 중 하나:
- CT 비-대조 두부; CT 뇌 관류; 컴퓨터 단층촬영술 혈관조영술 (CTA) 두부 및 경구; 또는
- 확산-강조 영상화 (DWI), 유체 감쇠 반전 회복 (FLAIR), 및 경사 회복 에코 (GRE), 두부의 비행 시간 이용 자기 공명 혈관조영술 (MRA), 역동자화율 대조 (DSC)를 이용하는 MR 뇌 관류, 대동맥궁 및 심경동맥의 가돌리늄 MRA를 포함하는, 뇌 MR.
CT 군에서, 허혈성 코어는 상대적인 대뇌 혈류 또는 대뇌 혈액 부피 (CBV)에 의해 평가된다. 환자 MR 군에서, 허혈성 코어 (비가역적으로 손상된 것으로 간주되는 조직)는 겉보기 확산 계수 (ADC) 임계값에 기초하여 평가된다.
임계상 관류 저하 조직은 MR 및 CT 군에 대해 디콘볼루션 신호 강도 곡선의 최대 신호까지의 소요 시간 (T최대) 임계값 > 6초에 기초하여 평가된다. DWI 병변 부피 또는 CT 앨버타 뇌졸중 프로그램 조기 CT 점수(ASPECTS: CT Alberta Stroke Program Early CT Score)를 MRI 또는 CT에 대해 각각 기록한다. 폐색 위치 (내경동맥 (ICA), M1, M2, 두개기부, 또는 비폐색부)를 기록한다.
3개월째, DWI, 3D T2-FLAIR 및 3D T1 경사 에코, T2(GRE), 두부의 TOF 이용 MRA를 포함하는, 뇌 MR.
후속-영상화 프로세싱
관류 영상화 (CT 및 MRI)의 원시 DICOM 데이터를 관류 미스매치 분석기 소프트웨어를 이용하여 후속 프로세싱을 진행한다. 최종 경색 부피를 분할 방법에 따라 T2 FLAIR에서 측정한다. 라보라토리 오브 메디컬 인포메이션 프로세싱(Laboratory of Medical Information Processing) (LaTIM - INSERM UMR 1101 브레스트)로부터의 엔지니어가 본 연구에 참가한다.
SEQUENCE LISTING
<110> CENTRE HOSPITALIER REGIONAL ET UNIVERSITAIRE DE BREST
ETABLISSEMENT FRANCAIS DU SANG
INSERM (Institut National de la Sante et de la Recherche
Medicale)
UNIVERSITE DE BRETAGNE OCCIDENTALE
<120> BLOOD BIOMARKERS OF STROKE
<130> IPA201461-FR
<150> EP 18305600.1
<151> 2018-05-16
<160> 18
<170> BiSSAP 1.3.6
<210> 1
<211> 604
<212> PRT
<213> Homo sapiens
<220>
<223> PTGS2 ? Accession number NP_000954.1
<400> 1
Met Leu Ala Arg Ala Leu Leu Leu Cys Ala Val Leu Ala Leu Ser His
1 5 10 15
Thr Ala Asn Pro Cys Cys Ser His Pro Cys Gln Asn Arg Gly Val Cys
20 25 30
Met Ser Val Gly Phe Asp Gln Tyr Lys Cys Asp Cys Thr Arg Thr Gly
35 40 45
Phe Tyr Gly Glu Asn Cys Ser Thr Pro Glu Phe Leu Thr Arg Ile Lys
50 55 60
Leu Phe Leu Lys Pro Thr Pro Asn Thr Val His Tyr Ile Leu Thr His
65 70 75 80
Phe Lys Gly Phe Trp Asn Val Val Asn Asn Ile Pro Phe Leu Arg Asn
85 90 95
Ala Ile Met Ser Tyr Val Leu Thr Ser Arg Ser His Leu Ile Asp Ser
100 105 110
Pro Pro Thr Tyr Asn Ala Asp Tyr Gly Tyr Lys Ser Trp Glu Ala Phe
115 120 125
Ser Asn Leu Ser Tyr Tyr Thr Arg Ala Leu Pro Pro Val Pro Asp Asp
130 135 140
Cys Pro Thr Pro Leu Gly Val Lys Gly Lys Lys Gln Leu Pro Asp Ser
145 150 155 160
Asn Glu Ile Val Glu Lys Leu Leu Leu Arg Arg Lys Phe Ile Pro Asp
165 170 175
Pro Gln Gly Ser Asn Met Met Phe Ala Phe Phe Ala Gln His Phe Thr
180 185 190
His Gln Phe Phe Lys Thr Asp His Lys Arg Gly Pro Ala Phe Thr Asn
195 200 205
Gly Leu Gly His Gly Val Asp Leu Asn His Ile Tyr Gly Glu Thr Leu
210 215 220
Ala Arg Gln Arg Lys Leu Arg Leu Phe Lys Asp Gly Lys Met Lys Tyr
225 230 235 240
Gln Ile Ile Asp Gly Glu Met Tyr Pro Pro Thr Val Lys Asp Thr Gln
245 250 255
Ala Glu Met Ile Tyr Pro Pro Gln Val Pro Glu His Leu Arg Phe Ala
260 265 270
Val Gly Gln Glu Val Phe Gly Leu Val Pro Gly Leu Met Met Tyr Ala
275 280 285
Thr Ile Trp Leu Arg Glu His Asn Arg Val Cys Asp Val Leu Lys Gln
290 295 300
Glu His Pro Glu Trp Gly Asp Glu Gln Leu Phe Gln Thr Ser Arg Leu
305 310 315 320
Ile Leu Ile Gly Glu Thr Ile Lys Ile Val Ile Glu Asp Tyr Val Gln
325 330 335
His Leu Ser Gly Tyr His Phe Lys Leu Lys Phe Asp Pro Glu Leu Leu
340 345 350
Phe Asn Lys Gln Phe Gln Tyr Gln Asn Arg Ile Ala Ala Glu Phe Asn
355 360 365
Thr Leu Tyr His Trp His Pro Leu Leu Pro Asp Thr Phe Gln Ile His
370 375 380
Asp Gln Lys Tyr Asn Tyr Gln Gln Phe Ile Tyr Asn Asn Ser Ile Leu
385 390 395 400
Leu Glu His Gly Ile Thr Gln Phe Val Glu Ser Phe Thr Arg Gln Ile
405 410 415
Ala Gly Arg Val Ala Gly Gly Arg Asn Val Pro Pro Ala Val Gln Lys
420 425 430
Val Ser Gln Ala Ser Ile Asp Gln Ser Arg Gln Met Lys Tyr Gln Ser
435 440 445
Phe Asn Glu Tyr Arg Lys Arg Phe Met Leu Lys Pro Tyr Glu Ser Phe
450 455 460
Glu Glu Leu Thr Gly Glu Lys Glu Met Ser Ala Glu Leu Glu Ala Leu
465 470 475 480
Tyr Gly Asp Ile Asp Ala Val Glu Leu Tyr Pro Ala Leu Leu Val Glu
485 490 495
Lys Pro Arg Pro Asp Ala Ile Phe Gly Glu Thr Met Val Glu Val Gly
500 505 510
Ala Pro Phe Ser Leu Lys Gly Leu Met Gly Asn Val Ile Cys Ser Pro
515 520 525
Ala Tyr Trp Lys Pro Ser Thr Phe Gly Gly Glu Val Gly Phe Gln Ile
530 535 540
Ile Asn Thr Ala Ser Ile Gln Ser Leu Ile Cys Asn Asn Val Lys Gly
545 550 555 560
Cys Pro Phe Thr Ser Phe Ser Val Pro Asp Pro Glu Leu Ile Lys Thr
565 570 575
Val Thr Ile Asn Ala Ser Ser Ser Arg Ser Gly Leu Asp Asp Ile Asn
580 585 590
Pro Thr Val Leu Leu Lys Glu Arg Ser Thr Glu Leu
595 600
<210> 2
<211> 4510
<212> DNA
<213> Homo sapiens
<220>
<223> PTGS2 ? Accession number NM_000963.4
<400> 2
aattgtcata cgacttgcag tgagcgtcag gagcacgtcc aggaactcct cagcagcgcc 60
tccttcagct ccacagccag acgccctcag acagcaaagc ctacccccgc gccgcgccct 120
gcccgccgct gcgatgctcg cccgcgccct gctgctgtgc gcggtcctgg cgctcagcca 180
tacagcaaat ccttgctgtt cccacccatg tcaaaaccga ggtgtatgta tgagtgtggg 240
atttgaccag tataagtgcg attgtacccg gacaggattc tatggagaaa actgctcaac 300
accggaattt ttgacaagaa taaaattatt tctgaaaccc actccaaaca cagtgcacta 360
catacttacc cacttcaagg gattttggaa cgttgtgaat aacattccct tccttcgaaa 420
tgcaattatg agttatgtgt tgacatccag atcacatttg attgacagtc caccaactta 480
caatgctgac tatggctaca aaagctggga agccttctct aacctctcct attatactag 540
agcccttcct cctgtgcctg atgattgccc gactcccttg ggtgtcaaag gtaaaaagca 600
gcttcctgat tcaaatgaga ttgtggaaaa attgcttcta agaagaaagt tcatccctga 660
tccccagggc tcaaacatga tgtttgcatt ctttgcccag cacttcacgc atcagttttt 720
caagacagat cataagcgag ggccagcttt caccaacggg ctgggccatg gggtggactt 780
aaatcatatt tacggtgaaa ctctggctag acagcgtaaa ctgcgccttt tcaaggatgg 840
aaaaatgaaa tatcagataa ttgatggaga gatgtatcct cccacagtca aagatactca 900
ggcagagatg atctaccctc ctcaagtccc tgagcatcta cggtttgctg tggggcagga 960
ggtctttggt ctggtgcctg gtctgatgat gtatgccaca atctggctgc gggaacacaa 1020
cagagtatgc gatgtgctta aacaggagca tcctgaatgg ggtgatgagc agttgttcca 1080
gacaagcagg ctaatactga taggagagac tattaagatt gtgattgaag attatgtgca 1140
acacttgagt ggctatcact tcaaactgaa atttgaccca gaactacttt tcaacaaaca 1200
attccagtac caaaatcgta ttgctgctga atttaacacc ctctatcact ggcatcccct 1260
tctgcctgac acctttcaaa ttcatgacca gaaatacaac tatcaacagt ttatctacaa 1320
caactctata ttgctggaac atggaattac ccagtttgtt gaatcattca ccaggcaaat 1380
tgctggcagg gttgctggtg gtaggaatgt tccacccgca gtacagaaag tatcacaggc 1440
ttccattgac cagagcaggc agatgaaata ccagtctttt aatgagtacc gcaaacgctt 1500
tatgctgaag ccctatgaat catttgaaga acttacagga gaaaaggaaa tgtctgcaga 1560
gttggaagca ctctatggtg acatcgatgc tgtggagctg tatcctgccc ttctggtaga 1620
aaagcctcgg ccagatgcca tctttggtga aaccatggta gaagttggag caccattctc 1680
cttgaaagga cttatgggta atgttatatg ttctcctgcc tactggaagc caagcacttt 1740
tggtggagaa gtgggttttc aaatcatcaa cactgcctca attcagtctc tcatctgcaa 1800
taacgtgaag ggctgtccct ttacttcatt cagtgttcca gatccagagc tcattaaaac 1860
agtcaccatc aatgcaagtt cttcccgctc cggactagat gatatcaatc ccacagtact 1920
actaaaagaa cgttcgactg aactgtagaa gtctaatgat catatttatt tatttatatg 1980
aaccatgtct attaatttaa ttatttaata atatttatat taaactcctt atgttactta 2040
acatcttctg taacagaagt cagtactcct gttgcggaga aaggagtcat acttgtgaag 2100
acttttatgt cactactcta aagattttgc tgttgctgtt aagtttggaa aacagttttt 2160
attctgtttt ataaaccaga gagaaatgag ttttgacgtc tttttacttg aatttcaact 2220
tatattataa gaacgaaagt aaagatgttt gaatacttaa acactgtcac aagatggcaa 2280
aatgctgaaa gtttttacac tgtcgatgtt tccaatgcat cttccatgat gcattagaag 2340
taactaatgt ttgaaatttt aaagtacttt tggttatttt tctgtcatca aacaaaaaca 2400
ggtatcagtg cattattaaa tgaatattta aattagacat taccagtaat ttcatgtcta 2460
ctttttaaaa tcagcaatga aacaataatt tgaaatttct aaattcatag ggtagaatca 2520
cctgtaaaag cttgtttgat ttcttaaagt tattaaactt gtacatatac caaaaagaag 2580
ctgtcttgga tttaaatctg taaaatcagt agaaatttta ctacaattgc ttgttaaaat 2640
attttataag tgatgttcct ttttcaccaa gagtataaac ctttttagtg tgactgttaa 2700
aacttccttt taaatcaaaa tgccaaattt attaaggtgg tggagccact gcagtgttat 2760
cttaaaataa gaatattttg ttgagatatt ccagaatttg tttatatggc tggtaacatg 2820
taaaatctat atcagcaaaa gggtctacct ttaaaataag caataacaaa gaagaaaacc 2880
aaattattgt tcaaatttag gtttaaactt ttgaagcaaa ctttttttta tccttgtgca 2940
ctgcaggcct ggtactcaga ttttgctatg aggttaatga agtaccaagc tgtgcttgaa 3000
taatgatatg ttttctcaga ttttctgttg tacagtttaa tttagcagtc catatcacat 3060
tgcaaaagta gcaatgacct cataaaatac ctcttcaaaa tgcttaaatt catttcacac 3120
attaatttta tctcagtctt gaagccaatt cagtaggtgc attggaatca agcctggcta 3180
cctgcatgct gttccttttc ttttcttctt ttagccattt tgctaagaga cacagtcttc 3240
tcatcacttc gtttctccta ttttgtttta ctagttttaa gatcagagtt cactttcttt 3300
ggactctgcc tatattttct tacctgaact tttgcaagtt ttcaggtaaa cctcagctca 3360
ggactgctat ttagctcctc ttaagaagat taaaagagaa aaaaaaaggc ccttttaaaa 3420
atagtataca cttattttaa gtgaaaagca gagaatttta tttatagcta attttagcta 3480
tctgtaacca agatggatgc aaagaggcta gtgcctcaga gagaactgta cggggtttgt 3540
gactggaaaa agttacgttc ccattctaat taatgccctt tcttatttaa aaacaaaacc 3600
aaatgatatc taagtagttc tcagcaataa taataatgac gataatactt cttttccaca 3660
tctcattgtc actgacattt aatggtactg tatattactt aatttattga agattattat 3720
ttatgtctta ttaggacact atggttataa actgtgttta agcctacaat cattgatttt 3780
tttttgttat gtcacaatca gtatattttc tttggggtta cctctctgaa tattatgtaa 3840
acaatccaaa gaaatgattg tattaagatt tgtgaataaa tttttagaaa tctgattggc 3900
atattgagat atttaaggtt gaatgtttgt ccttaggata ggcctatgtg ctagcccaca 3960
aagaatattg tctcattagc ctgaatgtgc cataagactg accttttaaa atgttttgag 4020
ggatctgtgg atgcttcgtt aatttgttca gccacaattt attgagaaaa tattctgtgt 4080
caagcactgt gggttttaat atttttaaat caaacgctga ttacagataa tagtatttat 4140
ataaataatt gaaaaaaatt ttcttttggg aagagggaga aaatgaaata aatatcatta 4200
aagataactc aggagaatct tctttacaat tttacgttta gaatgtttaa ggttaagaaa 4260
gaaatagtca atatgcttgt ataaaacact gttcactgtt ttttttaaaa aaaaaacttg 4320
atttgttatt aacattgatc tgctgacaaa acctgggaat ttgggttgtg tatgcgaatg 4380
tttcagtgcc tcagacaaat gtgtatttaa cttatgtaaa agataagtct ggaaataaat 4440
gtctgtttat ttttgtacta tttaaaaatt gacagatctt ttctgaagat aaactttgat 4500
tgtttctata 4510
<210> 3
<211> 288
<212> PRT
<213> Homo sapiens
<220>
<223> HMOX1 ? Accession number NP_002124.1
<400> 3
Met Glu Arg Pro Gln Pro Asp Ser Met Pro Gln Asp Leu Ser Glu Ala
1 5 10 15
Leu Lys Glu Ala Thr Lys Glu Val His Thr Gln Ala Glu Asn Ala Glu
20 25 30
Phe Met Arg Asn Phe Gln Lys Gly Gln Val Thr Arg Asp Gly Phe Lys
35 40 45
Leu Val Met Ala Ser Leu Tyr His Ile Tyr Val Ala Leu Glu Glu Glu
50 55 60
Ile Glu Arg Asn Lys Glu Ser Pro Val Phe Ala Pro Val Tyr Phe Pro
65 70 75 80
Glu Glu Leu His Arg Lys Ala Ala Leu Glu Gln Asp Leu Ala Phe Trp
85 90 95
Tyr Gly Pro Arg Trp Gln Glu Val Ile Pro Tyr Thr Pro Ala Met Gln
100 105 110
Arg Tyr Val Lys Arg Leu His Glu Val Gly Arg Thr Glu Pro Glu Leu
115 120 125
Leu Val Ala His Ala Tyr Thr Arg Tyr Leu Gly Asp Leu Ser Gly Gly
130 135 140
Gln Val Leu Lys Lys Ile Ala Gln Lys Ala Leu Asp Leu Pro Ser Ser
145 150 155 160
Gly Glu Gly Leu Ala Phe Phe Thr Phe Pro Asn Ile Ala Ser Ala Thr
165 170 175
Lys Phe Lys Gln Leu Tyr Arg Ser Arg Met Asn Ser Leu Glu Met Thr
180 185 190
Pro Ala Val Arg Gln Arg Val Ile Glu Glu Ala Lys Thr Ala Phe Leu
195 200 205
Leu Asn Ile Gln Leu Phe Glu Glu Leu Gln Glu Leu Leu Thr His Asp
210 215 220
Thr Lys Asp Gln Ser Pro Ser Arg Ala Pro Gly Leu Arg Gln Arg Ala
225 230 235 240
Ser Asn Lys Val Gln Asp Ser Ala Pro Val Glu Thr Pro Arg Gly Lys
245 250 255
Pro Pro Leu Asn Thr Arg Ser Gln Ala Pro Leu Leu Arg Trp Val Leu
260 265 270
Thr Leu Ser Phe Leu Val Ala Thr Val Ala Val Gly Leu Tyr Ala Met
275 280 285
<210> 4
<211> 1554
<212> DNA
<213> Homo sapiens
<220>
<223> HMOX1 ? Accession number NM_002133.3
<400> 4
aacgcctgcc tcctctcgag cgtcctcagc gcagccgccg cccgcggagc cagcacgaac 60
gagcccagca ccggccggat ggagcgtccg caacccgaca gcatgcccca ggatttgtca 120
gaggccctga aggaggccac caaggaggtg cacacccagg cagagaatgc tgagttcatg 180
aggaactttc agaagggcca ggtgacccga gacggcttca agctggtgat ggcctccctg 240
taccacatct atgtggccct ggaggaggag attgagcgca acaaggagag cccagtcttc 300
gcccctgtct acttcccaga agagctgcac cgcaaggctg ccctggagca ggacctggcc 360
ttctggtacg ggccccgctg gcaggaggtc atcccctaca caccagccat gcagcgctat 420
gtgaagcggc tccacgaggt ggggcgcaca gagcccgagc tgctggtggc ccacgcctac 480
acccgctacc tgggtgacct gtctgggggc caggtgctca aaaagattgc ccagaaagcc 540
ctggacctgc ccagctctgg cgagggcctg gccttcttca ccttccccaa cattgccagt 600
gccaccaagt tcaagcagct ctaccgctcc cgcatgaact ccctggagat gactcccgca 660
gtcaggcaga gggtgataga agaggccaag actgcgttcc tgctcaacat ccagctcttt 720
gaggagttgc aggagctgct gacccatgac accaaggacc agagcccctc acgggcacca 780
gggcttcgcc agcgggccag caacaaagtg caagattctg cccccgtgga gactcccaga 840
gggaagcccc cactcaacac ccgctcccag gctccgcttc tccgatgggt ccttacactc 900
agctttctgg tggcgacagt tgctgtaggg ctttatgcca tgtgaatgca ggcatgctgg 960
ctcccagggc catgaacttt gtccggtgga aggccttctt tctagagagg gaattctctt 1020
ggctggcttc cttaccgtgg gcactgaagg ctttcagggc ctccagccct ctcactgtgt 1080
ccctctctct ggaaaggagg aaggagccta tggcatcttc cccaacgaaa agcacatcca 1140
ggcaatggcc taaacttcag agggggcgaa gggatcagcc ctgcccttca gcatcctcag 1200
ttcctgcagc agagcctgga agacacccta atgtggcagc tgtctcaaac ctccaaaagc 1260
cctgagtttc aagtatcctt gttgacacgg ccatgaccac tttccccgtg ggccatggca 1320
atttttacac aaacctgaaa agatgttgtg tcttgtgttt ttgtcttatt tttgttggag 1380
ccactctgtt cctggctcag cctcaaatgc agtatttttg ttgtgttctg ttgtttttat 1440
agcagggttg gggtggtttt tgagccatgc gtgggtgggg agggaggtgt ttaacggcac 1500
tgtggccttg gtctaacttt tgtgtgaaat aataaacaac attgtctgat agta 1554
<210> 5
<211> 860
<212> PRT
<213> Homo sapiens
<220>
<223> LDLR ? Accession number NP_000518.1
<400> 5
Met Gly Pro Trp Gly Trp Lys Leu Arg Trp Thr Val Ala Leu Leu Leu
1 5 10 15
Ala Ala Ala Gly Thr Ala Val Gly Asp Arg Cys Glu Arg Asn Glu Phe
20 25 30
Gln Cys Gln Asp Gly Lys Cys Ile Ser Tyr Lys Trp Val Cys Asp Gly
35 40 45
Ser Ala Glu Cys Gln Asp Gly Ser Asp Glu Ser Gln Glu Thr Cys Leu
50 55 60
Ser Val Thr Cys Lys Ser Gly Asp Phe Ser Cys Gly Gly Arg Val Asn
65 70 75 80
Arg Cys Ile Pro Gln Phe Trp Arg Cys Asp Gly Gln Val Asp Cys Asp
85 90 95
Asn Gly Ser Asp Glu Gln Gly Cys Pro Pro Lys Thr Cys Ser Gln Asp
100 105 110
Glu Phe Arg Cys His Asp Gly Lys Cys Ile Ser Arg Gln Phe Val Cys
115 120 125
Asp Ser Asp Arg Asp Cys Leu Asp Gly Ser Asp Glu Ala Ser Cys Pro
130 135 140
Val Leu Thr Cys Gly Pro Ala Ser Phe Gln Cys Asn Ser Ser Thr Cys
145 150 155 160
Ile Pro Gln Leu Trp Ala Cys Asp Asn Asp Pro Asp Cys Glu Asp Gly
165 170 175
Ser Asp Glu Trp Pro Gln Arg Cys Arg Gly Leu Tyr Val Phe Gln Gly
180 185 190
Asp Ser Ser Pro Cys Ser Ala Phe Glu Phe His Cys Leu Ser Gly Glu
195 200 205
Cys Ile His Ser Ser Trp Arg Cys Asp Gly Gly Pro Asp Cys Lys Asp
210 215 220
Lys Ser Asp Glu Glu Asn Cys Ala Val Ala Thr Cys Arg Pro Asp Glu
225 230 235 240
Phe Gln Cys Ser Asp Gly Asn Cys Ile His Gly Ser Arg Gln Cys Asp
245 250 255
Arg Glu Tyr Asp Cys Lys Asp Met Ser Asp Glu Val Gly Cys Val Asn
260 265 270
Val Thr Leu Cys Glu Gly Pro Asn Lys Phe Lys Cys His Ser Gly Glu
275 280 285
Cys Ile Thr Leu Asp Lys Val Cys Asn Met Ala Arg Asp Cys Arg Asp
290 295 300
Trp Ser Asp Glu Pro Ile Lys Glu Cys Gly Thr Asn Glu Cys Leu Asp
305 310 315 320
Asn Asn Gly Gly Cys Ser His Val Cys Asn Asp Leu Lys Ile Gly Tyr
325 330 335
Glu Cys Leu Cys Pro Asp Gly Phe Gln Leu Val Ala Gln Arg Arg Cys
340 345 350
Glu Asp Ile Asp Glu Cys Gln Asp Pro Asp Thr Cys Ser Gln Leu Cys
355 360 365
Val Asn Leu Glu Gly Gly Tyr Lys Cys Gln Cys Glu Glu Gly Phe Gln
370 375 380
Leu Asp Pro His Thr Lys Ala Cys Lys Ala Val Gly Ser Ile Ala Tyr
385 390 395 400
Leu Phe Phe Thr Asn Arg His Glu Val Arg Lys Met Thr Leu Asp Arg
405 410 415
Ser Glu Tyr Thr Ser Leu Ile Pro Asn Leu Arg Asn Val Val Ala Leu
420 425 430
Asp Thr Glu Val Ala Ser Asn Arg Ile Tyr Trp Ser Asp Leu Ser Gln
435 440 445
Arg Met Ile Cys Ser Thr Gln Leu Asp Arg Ala His Gly Val Ser Ser
450 455 460
Tyr Asp Thr Val Ile Ser Arg Asp Ile Gln Ala Pro Asp Gly Leu Ala
465 470 475 480
Val Asp Trp Ile His Ser Asn Ile Tyr Trp Thr Asp Ser Val Leu Gly
485 490 495
Thr Val Ser Val Ala Asp Thr Lys Gly Val Lys Arg Lys Thr Leu Phe
500 505 510
Arg Glu Asn Gly Ser Lys Pro Arg Ala Ile Val Val Asp Pro Val His
515 520 525
Gly Phe Met Tyr Trp Thr Asp Trp Gly Thr Pro Ala Lys Ile Lys Lys
530 535 540
Gly Gly Leu Asn Gly Val Asp Ile Tyr Ser Leu Val Thr Glu Asn Ile
545 550 555 560
Gln Trp Pro Asn Gly Ile Thr Leu Asp Leu Leu Ser Gly Arg Leu Tyr
565 570 575
Trp Val Asp Ser Lys Leu His Ser Ile Ser Ser Ile Asp Val Asn Gly
580 585 590
Gly Asn Arg Lys Thr Ile Leu Glu Asp Glu Lys Arg Leu Ala His Pro
595 600 605
Phe Ser Leu Ala Val Phe Glu Asp Lys Val Phe Trp Thr Asp Ile Ile
610 615 620
Asn Glu Ala Ile Phe Ser Ala Asn Arg Leu Thr Gly Ser Asp Val Asn
625 630 635 640
Leu Leu Ala Glu Asn Leu Leu Ser Pro Glu Asp Met Val Leu Phe His
645 650 655
Asn Leu Thr Gln Pro Arg Gly Val Asn Trp Cys Glu Arg Thr Thr Leu
660 665 670
Ser Asn Gly Gly Cys Gln Tyr Leu Cys Leu Pro Ala Pro Gln Ile Asn
675 680 685
Pro His Ser Pro Lys Phe Thr Cys Ala Cys Pro Asp Gly Met Leu Leu
690 695 700
Ala Arg Asp Met Arg Ser Cys Leu Thr Glu Ala Glu Ala Ala Val Ala
705 710 715 720
Thr Gln Glu Thr Ser Thr Val Arg Leu Lys Val Ser Ser Thr Ala Val
725 730 735
Arg Thr Gln His Thr Thr Thr Arg Pro Val Pro Asp Thr Ser Arg Leu
740 745 750
Pro Gly Ala Thr Pro Gly Leu Thr Thr Val Glu Ile Val Thr Met Ser
755 760 765
His Gln Ala Leu Gly Asp Val Ala Gly Arg Gly Asn Glu Lys Lys Pro
770 775 780
Ser Ser Val Arg Ala Leu Ser Ile Val Leu Pro Ile Val Leu Leu Val
785 790 795 800
Phe Leu Cys Leu Gly Val Phe Leu Leu Trp Lys Asn Trp Arg Leu Lys
805 810 815
Asn Ile Asn Ser Ile Asn Phe Asp Asn Pro Val Tyr Gln Lys Thr Thr
820 825 830
Glu Asp Glu Val His Ile Cys His Asn Gln Asp Gly Tyr Ser Tyr Pro
835 840 845
Ser Arg Gln Met Val Ser Leu Glu Asp Asp Val Ala
850 855 860
<210> 6
<211> 5292
<212> DNA
<213> Homo sapiens
<220>
<223> LDLR ? Accession number NM_000527.4
<400> 6
ctcttgcagt gaggtgaaga catttgaaaa tcaccccact gcaaactcct ccccctgcta 60
gaaacctcac attgaaatgc tgtaaatgac gtgggccccg agtgcaatcg cgggaagcca 120
gggtttccag ctaggacaca gcaggtcgtg atccgggtcg ggacactgcc tggcagaggc 180
tgcgagcatg gggccctggg gctggaaatt gcgctggacc gtcgccttgc tcctcgccgc 240
ggcggggact gcagtgggcg acagatgcga aagaaacgag ttccagtgcc aagacgggaa 300
atgcatctcc tacaagtggg tctgcgatgg cagcgctgag tgccaggatg gctctgatga 360
gtcccaggag acgtgcttgt ctgtcacctg caaatccggg gacttcagct gtgggggccg 420
tgtcaaccgc tgcattcctc agttctggag gtgcgatggc caagtggact gcgacaacgg 480
ctcagacgag caaggctgtc cccccaagac gtgctcccag gacgagtttc gctgccacga 540
tgggaagtgc atctctcggc agttcgtctg tgactcagac cgggactgct tggacggctc 600
agacgaggcc tcctgcccgg tgctcacctg tggtcccgcc agcttccagt gcaacagctc 660
cacctgcatc ccccagctgt gggcctgcga caacgacccc gactgcgaag atggctcgga 720
tgagtggccg cagcgctgta ggggtcttta cgtgttccaa ggggacagta gcccctgctc 780
ggccttcgag ttccactgcc taagtggcga gtgcatccac tccagctggc gctgtgatgg 840
tggccccgac tgcaaggaca aatctgacga ggaaaactgc gctgtggcca cctgtcgccc 900
tgacgaattc cagtgctctg atggaaactg catccatggc agccggcagt gtgaccggga 960
atatgactgc aaggacatga gcgatgaagt tggctgcgtt aatgtgacac tctgcgaggg 1020
acccaacaag ttcaagtgtc acagcggcga atgcatcacc ctggacaaag tctgcaacat 1080
ggctagagac tgccgggact ggtcagatga acccatcaaa gagtgcggga ccaacgaatg 1140
cttggacaac aacggcggct gttcccacgt ctgcaatgac cttaagatcg gctacgagtg 1200
cctgtgcccc gacggcttcc agctggtggc ccagcgaaga tgcgaagata tcgatgagtg 1260
tcaggatccc gacacctgca gccagctctg cgtgaacctg gagggtggct acaagtgcca 1320
gtgtgaggaa ggcttccagc tggaccccca cacgaaggcc tgcaaggctg tgggctccat 1380
cgcctacctc ttcttcacca accggcacga ggtcaggaag atgacgctgg accggagcga 1440
gtacaccagc ctcatcccca acctgaggaa cgtggtcgct ctggacacgg aggtggccag 1500
caatagaatc tactggtctg acctgtccca gagaatgatc tgcagcaccc agcttgacag 1560
agcccacggc gtctcttcct atgacaccgt catcagcaga gacatccagg cccccgacgg 1620
gctggctgtg gactggatcc acagcaacat ctactggacc gactctgtcc tgggcactgt 1680
ctctgttgcg gataccaagg gcgtgaagag gaaaacgtta ttcagggaga acggctccaa 1740
gccaagggcc atcgtggtgg atcctgttca tggcttcatg tactggactg actggggaac 1800
tcccgccaag atcaagaaag ggggcctgaa tggtgtggac atctactcgc tggtgactga 1860
aaacattcag tggcccaatg gcatcaccct agatctcctc agtggccgcc tctactgggt 1920
tgactccaaa cttcactcca tctcaagcat cgatgtcaac gggggcaacc ggaagaccat 1980
cttggaggat gaaaagaggc tggcccaccc cttctccttg gccgtctttg aggacaaagt 2040
attttggaca gatatcatca acgaagccat tttcagtgcc aaccgcctca caggttccga 2100
tgtcaacttg ttggctgaaa acctactgtc cccagaggat atggttctct tccacaacct 2160
cacccagcca agaggagtga actggtgtga gaggaccacc ctgagcaatg gcggctgcca 2220
gtatctgtgc ctccctgccc cgcagatcaa cccccactcg cccaagttta cctgcgcctg 2280
cccggacggc atgctgctgg ccagggacat gaggagctgc ctcacagagg ctgaggctgc 2340
agtggccacc caggagacat ccaccgtcag gctaaaggtc agctccacag ccgtaaggac 2400
acagcacaca accacccgac ctgttcccga cacctcccgg ctgcctgggg ccacccctgg 2460
gctcaccacg gtggagatag tgacaatgtc tcaccaagct ctgggcgacg ttgctggcag 2520
aggaaatgag aagaagccca gtagcgtgag ggctctgtcc attgtcctcc ccatcgtgct 2580
cctcgtcttc ctttgcctgg gggtcttcct tctatggaag aactggcggc ttaagaacat 2640
caacagcatc aactttgaca accccgtcta tcagaagacc acagaggatg aggtccacat 2700
ttgccacaac caggacggct acagctaccc ctcgagacag atggtcagtc tggaggatga 2760
cgtggcgtga acatctgcct ggagtcccgt ccctgcccag aacccttcct gagacctcgc 2820
cggccttgtt ttattcaaag acagagaaga ccaaagcatt gcctgccaga gctttgtttt 2880
atatatttat tcatctggga ggcagaacag gcttcggaca gtgcccatgc aatggcttgg 2940
gttgggattt tggtttcttc ctttcctcgt gaaggataag agaaacaggc ccggggggac 3000
caggatgaca cctccatttc tctccaggaa gttttgagtt tctctccacc gtgacacaat 3060
cctcaaacat ggaagatgaa aggggagggg atgtcaggcc cagagaagca agtggctttc 3120
aacacacaac agcagatggc accaacggga ccccctggcc ctgcctcatc caccaatctc 3180
taagccaaac ccctaaactc aggagtcaac gtgtttacct cttctatgca agccttgcta 3240
gacagccagg ttagcctttg ccctgtcacc cccgaatcat gacccaccca gtgtctttcg 3300
aggtgggttt gtaccttcct taagccagga aagggattca tggcgtcgga aatgatctgg 3360
ctgaatccgt ggtggcaccg agaccaaact cattcaccaa atgatgccac ttcccagagg 3420
cagagcctga gtcactggtc acccttaata tttattaagt gcctgagaca cccggttacc 3480
ttggccgtga ggacacgtgg cctgcaccca ggtgtggctg tcaggacacc agcctggtgc 3540
ccatcctccc gacccctacc cacttccatt cccgtggtct ccttgcactt tctcagttca 3600
gagttgtaca ctgtgtacat ttggcatttg tgttattatt ttgcactgtt ttctgtcgtg 3660
tgtgttggga tgggatccca ggccagggaa agcccgtgtc aatgaatgcc ggggacagag 3720
aggggcaggt tgaccgggac ttcaaagccg tgatcgtgaa tatcgagaac tgccattgtc 3780
gtctttatgt ccgcccacct agtgcttcca cttctatgca aatgcctcca agccattcac 3840
ttccccaatc ttgtcgttga tgggtatgtg tttaaaacat gcacggtgag gccgggcgca 3900
gtggctcacg cctgtaatcc cagcactttg ggaggccgag gcgggtggat catgaggtca 3960
ggagatcgag accatcctgg ctaacacgtg aaaccccgtc tctactaaaa atacaaaaaa 4020
ttagccgggc gtggtggcgg gcacctgtag tcccagctac tcgggaggct gaggcaggag 4080
aatggtgtga acccgggaag cggagcttgc agtgagccga gattgcgcca ctgcagtccg 4140
cagtctggcc tgggcgacag agcgagactc cgtctcaaaa aaaaaaaaca aaaaaaaacc 4200
atgcatggtg catcagcagc ccatggcctc tggccaggca tggcgaggct gaggtgggag 4260
gatggtttga gctcaggcat ttgaggctgt cgtgagctat gattatgcca ctgctttcca 4320
gcctgggcaa catagtaaga ccccatctct taaaaaatga atttggccag acacaggtgc 4380
ctcacgcctg taatcccagc actttgggag gctgagctgg atcacttgag ttcaggagtt 4440
ggagaccagg cctgagcaac aaagcgagat cccatctcta caaaaaccaa aaagttaaaa 4500
atcagctggg tacggtggca cgtgcctgtg atcccagcta cttgggaggc tgaggcagga 4560
ggatcgcctg agcccaggag gtggaggttg cagtgagcca tgatcgagcc actgcactcc 4620
agcctgggca acagatgaag accctatttc agaaatacaa ctataaaaaa ataaataaat 4680
cctccagtct ggatcgtttg acgggacttc aggttctttc tgaaatcgcc gtgttactgt 4740
tgcactgatg tccggagaga cagtgacagc ctccgtcaga ctcccgcgtg aagatgtcac 4800
aagggattgg caattgtccc cagggacaaa acactgtgtc ccccccagtg cagggaaccg 4860
tgataagcct ttctggtttc ggagcacgta aatgcgtccc tgtacagata gtggggattt 4920
tttgttatgt ttgcactttg tatattggtt gaaactgtta tcacttatat atatatatat 4980
acacacatat atataaaatc tatttatttt tgcaaaccct ggttgctgta tttgttcagt 5040
gactattctc ggggccctgt gtagggggtt attgcctctg aaatgcctct tctttatgta 5100
caaagattat ttgcacgaac tggactgtgt gcaacgcttt ttgggagaat gatgtccccg 5160
ttgtatgtat gagtggcttc tgggagatgg gtgtcacttt ttaaaccact gtatagaagg 5220
tttttgtagc ctgaatgtct tactgtgatc aattaaattt cttaaatgaa ccaatttgtc 5280
taaaaaaaaa aa 5292
<210> 7
<211> 641
<212> PRT
<213> Homo sapiens
<220>
<223> HSPA1B ? Accession number NP_005337.2
<400> 7
Met Ala Lys Ala Ala Ala Ile Gly Ile Asp Leu Gly Thr Thr Tyr Ser
1 5 10 15
Cys Val Gly Val Phe Gln His Gly Lys Val Glu Ile Ile Ala Asn Asp
20 25 30
Gln Gly Asn Arg Thr Thr Pro Ser Tyr Val Ala Phe Thr Asp Thr Glu
35 40 45
Arg Leu Ile Gly Asp Ala Ala Lys Asn Gln Val Ala Leu Asn Pro Gln
50 55 60
Asn Thr Val Phe Asp Ala Lys Arg Leu Ile Gly Arg Lys Phe Gly Asp
65 70 75 80
Pro Val Val Gln Ser Asp Met Lys His Trp Pro Phe Gln Val Ile Asn
85 90 95
Asp Gly Asp Lys Pro Lys Val Gln Val Ser Tyr Lys Gly Glu Thr Lys
100 105 110
Ala Phe Tyr Pro Glu Glu Ile Ser Ser Met Val Leu Thr Lys Met Lys
115 120 125
Glu Ile Ala Glu Ala Tyr Leu Gly Tyr Pro Val Thr Asn Ala Val Ile
130 135 140
Thr Val Pro Ala Tyr Phe Asn Asp Ser Gln Arg Gln Ala Thr Lys Asp
145 150 155 160
Ala Gly Val Ile Ala Gly Leu Asn Val Leu Arg Ile Ile Asn Glu Pro
165 170 175
Thr Ala Ala Ala Ile Ala Tyr Gly Leu Asp Arg Thr Gly Lys Gly Glu
180 185 190
Arg Asn Val Leu Ile Phe Asp Leu Gly Gly Gly Thr Phe Asp Val Ser
195 200 205
Ile Leu Thr Ile Asp Asp Gly Ile Phe Glu Val Lys Ala Thr Ala Gly
210 215 220
Asp Thr His Leu Gly Gly Glu Asp Phe Asp Asn Arg Leu Val Asn His
225 230 235 240
Phe Val Glu Glu Phe Lys Arg Lys His Lys Lys Asp Ile Ser Gln Asn
245 250 255
Lys Arg Ala Val Arg Arg Leu Arg Thr Ala Cys Glu Arg Ala Lys Arg
260 265 270
Thr Leu Ser Ser Ser Thr Gln Ala Ser Leu Glu Ile Asp Ser Leu Phe
275 280 285
Glu Gly Ile Asp Phe Tyr Thr Ser Ile Thr Arg Ala Arg Phe Glu Glu
290 295 300
Leu Cys Ser Asp Leu Phe Arg Ser Thr Leu Glu Pro Val Glu Lys Ala
305 310 315 320
Leu Arg Asp Ala Lys Leu Asp Lys Ala Gln Ile His Asp Leu Val Leu
325 330 335
Val Gly Gly Ser Thr Arg Ile Pro Lys Val Gln Lys Leu Leu Gln Asp
340 345 350
Phe Phe Asn Gly Arg Asp Leu Asn Lys Ser Ile Asn Pro Asp Glu Ala
355 360 365
Val Ala Tyr Gly Ala Ala Val Gln Ala Ala Ile Leu Met Gly Asp Lys
370 375 380
Ser Glu Asn Val Gln Asp Leu Leu Leu Leu Asp Val Ala Pro Leu Ser
385 390 395 400
Leu Gly Leu Glu Thr Ala Gly Gly Val Met Thr Ala Leu Ile Lys Arg
405 410 415
Asn Ser Thr Ile Pro Thr Lys Gln Thr Gln Ile Phe Thr Thr Tyr Ser
420 425 430
Asp Asn Gln Pro Gly Val Leu Ile Gln Val Tyr Glu Gly Glu Arg Ala
435 440 445
Met Thr Lys Asp Asn Asn Leu Leu Gly Arg Phe Glu Leu Ser Gly Ile
450 455 460
Pro Pro Ala Pro Arg Gly Val Pro Gln Ile Glu Val Thr Phe Asp Ile
465 470 475 480
Asp Ala Asn Gly Ile Leu Asn Val Thr Ala Thr Asp Lys Ser Thr Gly
485 490 495
Lys Ala Asn Lys Ile Thr Ile Thr Asn Asp Lys Gly Arg Leu Ser Lys
500 505 510
Glu Glu Ile Glu Arg Met Val Gln Glu Ala Glu Lys Tyr Lys Ala Glu
515 520 525
Asp Glu Val Gln Arg Glu Arg Val Ser Ala Lys Asn Ala Leu Glu Ser
530 535 540
Tyr Ala Phe Asn Met Lys Ser Ala Val Glu Asp Glu Gly Leu Lys Gly
545 550 555 560
Lys Ile Ser Glu Ala Asp Lys Lys Lys Val Leu Asp Lys Cys Gln Glu
565 570 575
Val Ile Ser Trp Leu Asp Ala Asn Thr Leu Ala Glu Lys Asp Glu Phe
580 585 590
Glu His Lys Arg Lys Glu Leu Glu Gln Val Cys Asn Pro Ile Ile Ser
595 600 605
Gly Leu Tyr Gln Gly Ala Gly Gly Pro Gly Pro Gly Gly Phe Gly Ala
610 615 620
Gln Gly Pro Lys Gly Gly Ser Gly Ser Gly Pro Thr Ile Glu Glu Val
625 630 635 640
Asp
<210> 8
<211> 2517
<212> DNA
<213> Homo sapiens
<220>
<223> HSPA1B ? Accession number NM_005346.5
<400> 8
aaacggccag cctgaggagc tgctgcgagg gtccgcttcg tctttcgaga gtgactcccg 60
cggtcccaag gctttccaga gcgaacctgt gcggctgcag gcaccggcgt gttgagtttc 120
cggcgttccg aaggactgag ctcttgtcgc ggatcccgtc cgccgtttcc agcccccagt 180
ctcagagcgg agcccacaga gcagggcacc ggcatggcca aagccgcggc gatcggcatc 240
gacctgggca ccacctactc ctgcgtgggg gtgttccaac acggcaaggt ggagatcatc 300
gccaacgacc agggcaaccg caccaccccc agctacgtgg ccttcacgga caccgagcgg 360
ctcatcgggg atgcggccaa gaaccaggtg gcgctgaacc cgcagaacac cgtgtttgac 420
gcgaagcggc tgatcggccg caagttcggc gacccggtgg tgcagtcgga catgaagcac 480
tggcctttcc aggtgatcaa cgacggagac aagcccaagg tgcaggtgag ctacaagggg 540
gagaccaagg cattctaccc cgaggagatc tcgtccatgg tgctgaccaa gatgaaggag 600
atcgccgagg cgtacctggg ctacccggtg accaacgcgg tgatcaccgt gccggcctac 660
ttcaacgact cgcagcgcca ggccaccaag gatgcgggtg tgatcgcggg gctcaacgtg 720
ctgcggatca tcaacgagcc cacggccgcc gccatcgcct acggcctgga cagaacgggc 780
aagggggagc gcaacgtgct catctttgac ctgggcgggg gcaccttcga cgtgtccatc 840
ctgacgatcg acgacggcat cttcgaggtg aaggccacgg ccggggacac ccacctgggt 900
ggggaggact ttgacaacag gctggtgaac cacttcgtgg aggagttcaa gagaaaacac 960
aagaaggaca tcagccagaa caagcgagcc gtgaggcggc tgcgcaccgc ctgcgagagg 1020
gccaagagga ccctgtcgtc cagcacccag gccagcctgg agatcgactc cctgtttgag 1080
ggcatcgact tctacacgtc catcaccagg gcgaggttcg aggagctgtg ctccgacctg 1140
ttccgaagca ccctggagcc cgtggagaag gctctgcgcg acgccaagct ggacaaggcc 1200
cagattcacg acctggtcct ggtcgggggc tccacccgca tccccaaggt gcagaagctg 1260
ctgcaggact tcttcaacgg gcgcgacctg aacaagagca tcaaccccga cgaggctgtg 1320
gcctacgggg cggcggtgca ggcggccatc ctgatggggg acaagtccga gaacgtgcag 1380
gacctgctgc tgctggacgt ggctcccctg tcgctggggc tggagacggc cggaggcgtg 1440
atgactgccc tgatcaagcg caactccacc atccccacca agcagacgca gatcttcacc 1500
acctactccg acaaccaacc cggggtgctg atccaggtgt acgagggcga gagggccatg 1560
acgaaagaca acaatctgtt ggggcgcttc gagctgagcg gcatccctcc ggcccccagg 1620
ggcgtgcccc agatcgaggt gaccttcgac atcgatgcca acggcatcct gaacgtcacg 1680
gccacggaca agagcaccgg caaggccaac aagatcacca tcaccaacga caagggccgc 1740
ctgagcaagg aggagatcga gcgcatggtg caggaggcgg agaagtacaa agcggaggac 1800
gaggtgcagc gcgagagggt gtcagccaag aacgccctgg agtcctacgc cttcaacatg 1860
aagagcgccg tggaggatga ggggctcaag ggcaagatca gcgaggcgga caagaagaag 1920
gttctggaca agtgtcaaga ggtcatctcg tggctggacg ccaacacctt ggccgagaag 1980
gacgagtttg agcacaagag gaaggagctg gagcaggtgt gtaaccccat catcagcgga 2040
ctgtaccagg gtgccggtgg tcccgggcct ggcggcttcg gggctcaggg tcccaaggga 2100
gggtctgggt caggccctac cattgaggag gtggattagg ggcctttgtt ctttagtatg 2160
tttgtctttg aggtggactg ttgggactca aggactttgc tgctgttttc ctatgtcatt 2220
tctgcttcag ctctttgctg cttcacttct ttgtaaagtt gtaacctgat ggtaattagc 2280
tggcttcatt atttttgtag tacaaccgat atgttcatta gaattctttg catttaatgt 2340
tgatactgta agggtgtttc gttcccttta aatgaatcaa cactgccacc ttctgtacga 2400
gtttgtttgt tttttttttt tttttttttt tttgcttggc gaaaacacta caaaggctgg 2460
gaatgtatgt ttttataatt tgtttattta aatatgaaaa ataaaatgtt aaacttt 2517
<210> 9
<211> 103
<212> PRT
<213> Homo sapiens
<220>
<223> G0S2 ? Accession number NP_056529.1
<400> 9
Met Glu Thr Val Gln Glu Leu Ile Pro Leu Ala Lys Glu Met Met Ala
1 5 10 15
Gln Lys Arg Lys Gly Lys Met Val Lys Leu Tyr Val Leu Gly Ser Val
20 25 30
Leu Ala Leu Phe Gly Val Val Leu Gly Leu Met Glu Thr Val Cys Ser
35 40 45
Pro Phe Thr Ala Ala Arg Arg Leu Arg Asp Gln Glu Ala Ala Val Ala
50 55 60
Glu Leu Gln Ala Ala Leu Glu Arg Gln Ala Leu Gln Lys Gln Ala Leu
65 70 75 80
Gln Glu Lys Gly Lys Gln Gln Asp Thr Val Leu Gly Gly Arg Ala Leu
85 90 95
Ser Asn Arg Gln His Ala Ser
100
<210> 10
<211> 876
<212> DNA
<213> Homo sapiens
<220>
<223> G0S2 ? Accession number NM_015714.4
<400> 10
tgccagcggc ggagtctcca actgggagag ctgcagctgc cgagaggagg agaacgctga 60
ggtcggtcgg accaacggac gcgctgaccg ctgccaactg cagctcgcgc tgcctcctgc 120
tcgcgccgtg ccactaaggt cattcccgcc tccgagagcc cagagccgag atggaaacgg 180
tccaggagct gatccccctg gccaaggaga tgatggccca gaagcgcaag gggaagatgg 240
tgaagctgta cgtgctgggc agcgtgctgg ccctcttcgg cgtggtgctc ggcctgatgg 300
agactgtgtg cagccccttc acggccgcca gacgtctgcg ggaccaggag gcagccgtgg 360
cggagctgca ggccgccctg gagcgacagg ctctccagaa gcaagccctg caggagaaag 420
gcaagcagca ggacacggtc ctcggcggcc gggccctgtc caaccggcag cacgcctcct 480
aggaactgtg ggagaccagc ggagtgggag ggagacgcag tagacagaga cagaccgaga 540
gaggaatgga gagacagagg gggcgcgcgc acaggagcct gactccgctg ggagagtgca 600
ggagcacgtg ctgtttttta tttggactta acttcagaga aaccgctgac atctagaact 660
gacctaccac aagcatccac caaaggagtt tgggattgag ttttgctgct gtgcagcact 720
gcattgtcat gacatttcca acactgtgtg aattatctaa atgcgtctac cattttgcac 780
tagggaggaa ggataaatgc tttttatgtt attattatta attattacaa tgaccaccat 840
tttgcatttt gaaataaaaa aactttttat accata 876
<210> 11
<211> 575
<212> PRT
<213> Homo sapiens
<220>
<223> BAG3 ? Accession number NP_004272.2
<400> 11
Met Ser Ala Ala Thr His Ser Pro Met Met Gln Val Ala Ser Gly Asn
1 5 10 15
Gly Asp Arg Asp Pro Leu Pro Pro Gly Trp Glu Ile Lys Ile Asp Pro
20 25 30
Gln Thr Gly Trp Pro Phe Phe Val Asp His Asn Ser Arg Thr Thr Thr
35 40 45
Trp Asn Asp Pro Arg Val Pro Ser Glu Gly Pro Lys Glu Thr Pro Ser
50 55 60
Ser Ala Asn Gly Pro Ser Arg Glu Gly Ser Arg Leu Pro Pro Ala Arg
65 70 75 80
Glu Gly His Pro Val Tyr Pro Gln Leu Arg Pro Gly Tyr Ile Pro Ile
85 90 95
Pro Val Leu His Glu Gly Ala Glu Asn Arg Gln Val His Pro Phe His
100 105 110
Val Tyr Pro Gln Pro Gly Met Gln Arg Phe Arg Thr Glu Ala Ala Ala
115 120 125
Ala Ala Pro Gln Arg Ser Gln Ser Pro Leu Arg Gly Met Pro Glu Thr
130 135 140
Thr Gln Pro Asp Lys Gln Cys Gly Gln Val Ala Ala Ala Ala Ala Ala
145 150 155 160
Gln Pro Pro Ala Ser His Gly Pro Glu Arg Ser Gln Ser Pro Ala Ala
165 170 175
Ser Asp Cys Ser Ser Ser Ser Ser Ser Ala Ser Leu Pro Ser Ser Gly
180 185 190
Arg Ser Ser Leu Gly Ser His Gln Leu Pro Arg Gly Tyr Ile Ser Ile
195 200 205
Pro Val Ile His Glu Gln Asn Val Thr Arg Pro Ala Ala Gln Pro Ser
210 215 220
Phe His Gln Ala Gln Lys Thr His Tyr Pro Ala Gln Gln Gly Glu Tyr
225 230 235 240
Gln Thr His Gln Pro Val Tyr His Lys Ile Gln Gly Asp Asp Trp Glu
245 250 255
Pro Arg Pro Leu Arg Ala Ala Ser Pro Phe Arg Ser Ser Val Gln Gly
260 265 270
Ala Ser Ser Arg Glu Gly Ser Pro Ala Arg Ser Ser Thr Pro Leu His
275 280 285
Ser Pro Ser Pro Ile Arg Val His Thr Val Val Asp Arg Pro Gln Gln
290 295 300
Pro Met Thr His Arg Glu Thr Ala Pro Val Ser Gln Pro Glu Asn Lys
305 310 315 320
Pro Glu Ser Lys Pro Gly Pro Val Gly Pro Glu Leu Pro Pro Gly His
325 330 335
Ile Pro Ile Gln Val Ile Arg Lys Glu Val Asp Ser Lys Pro Val Ser
340 345 350
Gln Lys Pro Pro Pro Pro Ser Glu Lys Val Glu Val Lys Val Pro Pro
355 360 365
Ala Pro Val Pro Cys Pro Pro Pro Ser Pro Gly Pro Ser Ala Val Pro
370 375 380
Ser Ser Pro Lys Ser Val Ala Thr Glu Glu Arg Ala Ala Pro Ser Thr
385 390 395 400
Ala Pro Ala Glu Ala Thr Pro Pro Lys Pro Gly Glu Ala Glu Ala Pro
405 410 415
Pro Lys His Pro Gly Val Leu Lys Val Glu Ala Ile Leu Glu Lys Val
420 425 430
Gln Gly Leu Glu Gln Ala Val Asp Asn Phe Glu Gly Lys Lys Thr Asp
435 440 445
Lys Lys Tyr Leu Met Ile Glu Glu Tyr Leu Thr Lys Glu Leu Leu Ala
450 455 460
Leu Asp Ser Val Asp Pro Glu Gly Arg Ala Asp Val Arg Gln Ala Arg
465 470 475 480
Arg Asp Gly Val Arg Lys Val Gln Thr Ile Leu Glu Lys Leu Glu Gln
485 490 495
Lys Ala Ile Asp Val Pro Gly Gln Val Gln Val Tyr Glu Leu Gln Pro
500 505 510
Ser Asn Leu Glu Ala Asp Gln Pro Leu Gln Ala Ile Met Glu Met Gly
515 520 525
Ala Val Ala Ala Asp Lys Gly Lys Lys Asn Ala Gly Asn Ala Glu Asp
530 535 540
Pro His Thr Glu Thr Gln Gln Pro Glu Ala Thr Ala Ala Ala Thr Ser
545 550 555 560
Asn Pro Ser Ser Met Thr Asp Thr Pro Gly Asn Pro Ala Ala Pro
565 570 575
<210> 12
<211> 2608
<212> DNA
<213> Homo sapiens
<220>
<223> BAG3 ? Accession number NM_004281.3
<400> 12
gcggagctcc gcatccaacc ccgggccgcg gccaacttct ctggactgga ccagaagttt 60
ctagccggcc agttgctacc tccctttatc tcctccttcc cctctggcag cgaggaggct 120
atttccagac acttccaccc ctctctggcc acgtcacccc cgcctttaat tcataaaggt 180
gcccggcgcc ggcttcccgg acacgtcggc ggcggagagg ggcccacggc ggcggcccgg 240
ccagagactc ggcgcccgga gccagcgccc cgcacccgcg ccccagcggg cagaccccaa 300
cccagcatga gcgccgccac ccactcgccc atgatgcagg tggcgtccgg caacggtgac 360
cgcgaccctt tgccccccgg atgggagatc aagatcgacc cgcagaccgg ctggcccttc 420
ttcgtggacc acaacagccg caccactacg tggaacgacc cgcgcgtgcc ctctgagggc 480
cccaaggaga ctccatcctc tgccaatggc ccttcccggg agggctctag gctgccgcct 540
gctagggaag gccaccctgt gtacccccag ctccgaccag gctacattcc cattcctgtg 600
ctccatgaag gcgctgagaa ccggcaggtg caccctttcc atgtctatcc ccagcctggg 660
atgcagcgat tccgaactga ggcggcagca gcggctcctc agaggtccca gtcacctctg 720
cggggcatgc cagaaaccac tcagccagat aaacagtgtg gacaggtggc agcggcggcg 780
gcagcccagc ccccagcctc ccacggacct gagcggtccc agtctccagc tgcctctgac 840
tgctcatcct catcctcctc ggccagcctg ccttcctccg gcaggagcag cctgggcagt 900
caccagctcc cgcgggggta catctccatt ccggtgatac acgagcagaa cgttacccgg 960
ccagcagccc agccctcctt ccaccaagcc cagaagacgc actacccagc gcagcagggg 1020
gagtaccaga cccaccagcc tgtgtaccac aagatccagg gggatgactg ggagccccgg 1080
cccctgcggg cggcatcccc gttcaggtca tctgtccagg gtgcatcgag ccgggagggc 1140
tcaccagcca ggagcagcac gccactccac tccccctcgc ccatccgtgt gcacaccgtg 1200
gtcgacaggc ctcagcagcc catgacccat cgagaaactg cacctgtttc ccagcctgaa 1260
aacaaaccag aaagtaagcc aggcccagtt ggaccagaac tccctcctgg acacatccca 1320
attcaagtga tccgcaaaga ggtggattct aaacctgttt cccagaagcc cccacctccc 1380
tctgagaagg tagaggtgaa agttccccct gctccagttc cttgtcctcc tcccagccct 1440
ggcccttctg ctgtcccctc ttcccccaag agtgtggcta cagaagagag ggcagccccc 1500
agcactgccc ctgcagaagc tacacctcca aaaccaggag aagccgaggc tcccccaaaa 1560
catccaggag tgctgaaagt ggaagccatc ctggagaagg tacaggggct ggagcaggct 1620
gtagacaact ttgaaggcaa gaagactgac aaaaagtacc tgatgatcga agagtatttg 1680
accaaagagc tgctggccct ggattcagtg gaccccgagg gacgagccga tgtgcgtcag 1740
gccaggagag acggtgtcag gaaggttcag accatcttgg aaaaacttga acagaaagcc 1800
attgatgtcc caggtcaagt ccaggtctat gaactccagc ccagcaacct tgaagcagat 1860
cagccactgc aggcaatcat ggagatgggt gccgtggcag cagacaaggg caagaaaaat 1920
gctggaaatg cagaagatcc ccacacagaa acccagcagc cagaagccac agcagcagcg 1980
acttcaaacc ccagcagcat gacagacacc cctggtaacc cagcagcacc gtagcctctg 2040
ccctgtaaaa atcagactcg gaaccgatgt gtgctttagg gaattttaag ttgcatgcat 2100
ttcagagact ttaagtcagt tggtttttat tagctgcttg gtatgcagta acttgggtgg 2160
aggcaaaaca ctaataaaag ggctaaaaag gaaaatgatg cttttcttct atattcttac 2220
tctgtacaaa taaagaagtt gcttgttgtt tgagaagttt aaccccgttg cttgttgttc 2280
tgcagccctg tctacttggg cacccccacc acctgttagc tgtggttgtg cactgtcttt 2340
tgtagctctg gactggaggg gtagatgggg agtcaattac ccatcacata aatatgaaac 2400
atttatcaga aatgttgcca ttttaatgag atgattttct tcatctcata attaaaatac 2460
ctgactttag agagagtaaa atgtgccagg agccatagga atatctgtat gttggatgac 2520
tttaatgcta cattttaaaa aaagaaaata aagtaataat ataactcaaa aaaaaaaaaa 2580
aaaaaaaaaa aaaaaaaaaa aaaaaaaa 2608
<210> 13
<211> 239
<212> PRT
<213> Homo sapiens
<220>
<223> TM4SF1 ? Accession number XP_016861874.1
<400> 13
Met Cys Tyr Gly Lys Cys Ala Arg Cys Ile Gly His Ser Leu Val Gly
1 5 10 15
Leu Ala Leu Leu Cys Ile Ala Ala Asn Ile Leu Leu Tyr Phe Pro Asn
20 25 30
Gly Glu Thr Lys Tyr Ala Ser Glu Asn His Leu Ser Arg Phe Val Trp
35 40 45
Phe Phe Ser Gly Ile Val Gly Gly Gly Leu Leu Met Leu Leu Pro Ala
50 55 60
Phe Val Phe Ile Gly Leu Glu Gln Asp Asp Cys Cys Gly Cys Cys Gly
65 70 75 80
His Glu Asn Cys Gly Lys Arg Cys Ala Met Leu Ser Ser Val Leu Ala
85 90 95
Ala Leu Ile Gly Ile Ala Gly Ser Gly Tyr Cys Val Ile Val Ala Ala
100 105 110
Leu Gly Leu Ala Glu Gly Pro Leu Cys Leu Asp Ser Leu Gly Gln Trp
115 120 125
Asn Tyr Thr Phe Ala Ser Thr Glu Gly Gln Tyr Leu Leu Asp Thr Ser
130 135 140
Thr Trp Ser Glu Cys Thr Glu Pro Lys His Ile Val Glu Trp Asn Val
145 150 155 160
Ser Leu Phe Ser Ile Leu Leu Ala Leu Gly Gly Ile Glu Phe Ile Leu
165 170 175
Cys Leu Ile Gln Val Ile Asn Gly Val Leu Gly Gly Ile Cys Gly Phe
180 185 190
Cys Cys Ser His Gln Gln Val Arg Thr Cys Met Lys Ile Asn Met Thr
195 200 205
Ala Lys Arg Thr Asn Pro Gly Gln Ser His Asn Leu Pro Leu Phe His
210 215 220
Cys Asn Leu Tyr Ile Ser Leu Val Phe Ile Cys Lys Thr Leu Tyr
225 230 235
<210> 14
<211> 972
<212> DNA
<213> Homo sapiens
<220>
<223> TM4SF1 ? Accession number XM_017006385.2
<400> 14
aagggcggga cattccccct gcctcttcgc accacagcca gagcctgcca ttaggaccaa 60
tgaaagcaaa gtacctcatc ccctcagtga ctaagaatcg cagtatttaa gaggtagcag 120
gaatgggctg agagtggtgt ttgctttctc caccagaagg gcacactttc atctaatttg 180
gggtatcact gagctgaaga caaagagaag ggggagaaaa cctagcagac caccatgtgc 240
tatgggaagt gtgcacgatg catcggacat tctctggtgg ggctcgccct cctgtgcatc 300
gcggctaata ttttgcttta ctttcccaat ggggaaacaa agtatgcctc cgaaaaccac 360
ctcagccgct tcgtgtggtt cttttctggc atcgtaggag gtggcctgct gatgctcctg 420
ccagcatttg tcttcattgg gctggaacag gatgactgct gtggctgctg tggccatgaa 480
aactgtggca aacgatgtgc gatgctttct tctgtattgg ctgctctcat tggaattgca 540
ggatctggct actgtgtcat tgtggcagcc cttggcttag cagaaggacc actatgtctt 600
gattccctcg gccagtggaa ctacaccttt gccagcactg agggccagta ccttctggat 660
acctccacat ggtccgagtg cactgaaccc aagcacattg tggaatggaa tgtatctctg 720
ttttctatcc tcttggctct tggtggaatt gaattcatct tgtgtcttat tcaagtaata 780
aatggagtgc ttggaggcat atgtggcttt tgctgctctc accaacaggt aagaacctgc 840
atgaaaatca atatgactgc taaaagaacc aacccaggac agagccacaa tcttcctcta 900
tttcattgta atttatatat ttcacttgta ttcatttgta aaactttgta ttagtgtaac 960
atactcccca ca 972
<210> 15
<211> 367
<212> PRT
<213> Homo sapiens
<220>
<223> DUSP1 ? Accession number NP_004408.1
<400> 15
Met Val Met Glu Val Gly Thr Leu Asp Ala Gly Gly Leu Arg Ala Leu
1 5 10 15
Leu Gly Glu Arg Ala Ala Gln Cys Leu Leu Leu Asp Cys Arg Ser Phe
20 25 30
Phe Ala Phe Asn Ala Gly His Ile Ala Gly Ser Val Asn Val Arg Phe
35 40 45
Ser Thr Ile Val Arg Arg Arg Ala Lys Gly Ala Met Gly Leu Glu His
50 55 60
Ile Val Pro Asn Ala Glu Leu Arg Gly Arg Leu Leu Ala Gly Ala Tyr
65 70 75 80
His Ala Val Val Leu Leu Asp Glu Arg Ser Ala Ala Leu Asp Gly Ala
85 90 95
Lys Arg Asp Gly Thr Leu Ala Leu Ala Ala Gly Ala Leu Cys Arg Glu
100 105 110
Ala Arg Ala Ala Gln Val Phe Phe Leu Lys Gly Gly Tyr Glu Ala Phe
115 120 125
Ser Ala Ser Cys Pro Glu Leu Cys Ser Lys Gln Ser Thr Pro Met Gly
130 135 140
Leu Ser Leu Pro Leu Ser Thr Ser Val Pro Asp Ser Ala Glu Ser Gly
145 150 155 160
Cys Ser Ser Cys Ser Thr Pro Leu Tyr Asp Gln Gly Gly Pro Val Glu
165 170 175
Ile Leu Pro Phe Leu Tyr Leu Gly Ser Ala Tyr His Ala Ser Arg Lys
180 185 190
Asp Met Leu Asp Ala Leu Gly Ile Thr Ala Leu Ile Asn Val Ser Ala
195 200 205
Asn Cys Pro Asn His Phe Glu Gly His Tyr Gln Tyr Lys Ser Ile Pro
210 215 220
Val Glu Asp Asn His Lys Ala Asp Ile Ser Ser Trp Phe Asn Glu Ala
225 230 235 240
Ile Asp Phe Ile Asp Ser Ile Lys Asn Ala Gly Gly Arg Val Phe Val
245 250 255
His Cys Gln Ala Gly Ile Ser Arg Ser Ala Thr Ile Cys Leu Ala Tyr
260 265 270
Leu Met Arg Thr Asn Arg Val Lys Leu Asp Glu Ala Phe Glu Phe Val
275 280 285
Lys Gln Arg Arg Ser Ile Ile Ser Pro Asn Phe Ser Phe Met Gly Gln
290 295 300
Leu Leu Gln Phe Glu Ser Gln Val Leu Ala Pro His Cys Ser Ala Glu
305 310 315 320
Ala Gly Ser Pro Ala Met Ala Val Leu Asp Arg Gly Thr Ser Thr Thr
325 330 335
Thr Val Phe Asn Phe Pro Val Ser Ile Pro Val His Ser Thr Asn Ser
340 345 350
Ala Leu Ser Tyr Leu Gln Ser Pro Ile Thr Thr Ser Pro Ser Cys
355 360 365
<210> 16
<211> 2013
<212> DNA
<213> Homo sapiens
<220>
<223> DUSP1 ? Accession number NM_004417.4
<400> 16
gcgaaggaca tttgggctgt gtgtgcgacg cgggtcggag gggcagtcgg gggaaccgcg 60
aagaagccga ggagcccgga gccccgcgtg acgctcctct ctcagtccaa aagcggcttt 120
tggttcggcg cagagagacc cgggggtcta gcttttcctc gaaaagcgcc gccctgccct 180
tggccccgag aacagacaaa gagcaccgca gggccgatca cgctgggggc gctgaggccg 240
gccatggtca tggaagtggg caccctggac gctggaggcc tgcgggcgct gctgggggag 300
cgagcggcgc aatgcctgct gctggactgc cgctccttct tcgctttcaa cgccggccac 360
atcgccggct ctgtcaacgt gcgcttcagc accatcgtgc ggcgccgggc caagggcgcc 420
atgggcctgg agcacatcgt gcccaacgcc gagctccgcg gccgcctgct ggccggcgcc 480
taccacgccg tggtgttgct ggacgagcgc agcgccgccc tggacggcgc caagcgcgac 540
ggcaccctgg ccctggcggc cggcgcgctc tgccgcgagg cgcgcgccgc gcaagtcttc 600
ttcctcaaag gaggatacga agcgttttcg gcttcctgcc cggagctgtg cagcaaacag 660
tcgaccccca tggggctcag ccttcccctg agtactagcg tccctgacag cgcggaatct 720
gggtgcagtt cctgcagtac cccactctac gatcagggtg gcccggtgga aatcctgccc 780
tttctgtacc tgggcagtgc gtatcacgct tcccgcaagg acatgctgga tgccttgggc 840
atcactgcct tgatcaacgt ctcagccaat tgtcccaacc attttgaggg tcactaccag 900
tacaagagca tccctgtgga ggacaaccac aaggcagaca tcagctcctg gttcaacgag 960
gccattgact tcatagactc catcaagaat gctggaggaa gggtgtttgt ccactgccag 1020
gcaggcattt cccggtcagc caccatctgc cttgcttacc ttatgaggac taatcgagtc 1080
aagctggacg aggcctttga gtttgtgaag cagaggcgaa gcatcatctc tcccaacttc 1140
agcttcatgg gccagctgct gcagtttgag tcccaggtgc tggctccgca ctgttcggca 1200
gaggctggga gccccgccat ggctgtgctc gaccgaggca cctccaccac caccgtgttc 1260
aacttccccg tctccatccc tgtccactcc acgaacagtg cgctgagcta ccttcagagc 1320
cccattacga cctctcccag ctgctgaaag gccacgggag gtgaggctct tcacatccca 1380
ttgggactcc atgctccttg agaggagaaa tgcaataact ctgggagggg ctcgagaggg 1440
ctggtcctta tttatttaac ttcacccgag ttcctctggg tttctaagca gttatggtga 1500
tgacttagcg tcaagacatt tgctgaactc agcacattcg ggaccaatat atagtgggta 1560
catcaagtcc atctgacaaa atggggcaga agagaaagga ctcagtgtgt gatccggttt 1620
ctttttgctc gcccctgttt tttgtagaat ctcttcatgc ttgacatacc taccagtatt 1680
attcccgacg acacatatac atatgagaat ataccttatt tatttttgtg taggtgtctg 1740
ccttcacaaa tgtcattgtc tactcctaga agaaccaaat acctcaattt ttgtttttga 1800
gtactgtact atcctgtaaa tatatcttaa gcaggtttgt tttcagcact gatggaaaat 1860
accagtgttg ggtttttttt tagttgccaa cagttgtatg tttgctgatt atttatgacc 1920
tgaaataata tatttcttct tctaagaaga cattttgtta cataaggatg acttttttat 1980
acaatggaat aaattatggc atttctattg aaa 2013
<210> 17
<211> 185
<212> PRT
<213> Homo sapiens
<220>
<223> ADM ? Accession number NP_001115.1
<400> 17
Met Lys Leu Val Ser Val Ala Leu Met Tyr Leu Gly Ser Leu Ala Phe
1 5 10 15
Leu Gly Ala Asp Thr Ala Arg Leu Asp Val Ala Ser Glu Phe Arg Lys
20 25 30
Lys Trp Asn Lys Trp Ala Leu Ser Arg Gly Lys Arg Glu Leu Arg Met
35 40 45
Ser Ser Ser Tyr Pro Thr Gly Leu Ala Asp Val Lys Ala Gly Pro Ala
50 55 60
Gln Thr Leu Ile Arg Pro Gln Asp Met Lys Gly Ala Ser Arg Ser Pro
65 70 75 80
Glu Asp Ser Ser Pro Asp Ala Ala Arg Ile Arg Val Lys Arg Tyr Arg
85 90 95
Gln Ser Met Asn Asn Phe Gln Gly Leu Arg Ser Phe Gly Cys Arg Phe
100 105 110
Gly Thr Cys Thr Val Gln Lys Leu Ala His Gln Ile Tyr Gln Phe Thr
115 120 125
Asp Lys Asp Lys Asp Asn Val Ala Pro Arg Ser Lys Ile Ser Pro Gln
130 135 140
Gly Tyr Gly Arg Arg Arg Arg Arg Ser Leu Pro Glu Ala Gly Pro Gly
145 150 155 160
Arg Thr Leu Val Ser Ser Lys Pro Gln Ala His Gly Ala Pro Ala Pro
165 170 175
Pro Ser Gly Ser Ala Pro His Phe Leu
180 185
<210> 18
<211> 1492
<212> DNA
<213> Homo sapiens
<220>
<223> ADM ? Accession number NM_001124.3
<400> 18
actcagtggt ttcttggtga cactggatag aacagctcaa gccttgccac ttcgggcttc 60
tcactgcagc tgggcttgga cttcggagtt ttgccattgc cagtgggacg tctgagactt 120
tctccttcaa gtacttggca gatcactctc ttagcagggt ctgcgcttcg cagccgggat 180
gaagctggtt tccgtcgccc tgatgtacct gggttcgctc gccttcctag gcgctgacac 240
cgctcggttg gatgtcgcgt cggagtttcg aaagaagtgg aataagtggg ctctgagtcg 300
tgggaagagg gaactgcgga tgtccagcag ctaccccacc gggctcgctg acgtgaaggc 360
cgggcctgcc cagaccctta ttcggcccca ggacatgaag ggtgcctctc gaagccccga 420
agacagcagt ccggatgccg cccgcatccg agtcaagcgc taccgccaga gcatgaacaa 480
cttccagggc ctccggagct ttggctgccg cttcgggacg tgcacggtgc agaagctggc 540
acaccagatc taccagttca cagataagga caaggacaac gtcgccccca ggagcaagat 600
cagcccccag ggctacggcc gccggcgccg gcgctccctg cccgaggccg gcccgggtcg 660
gactctggtg tcttctaagc cacaagcaca cggggctcca gcccccccga gtggaagtgc 720
tccccacttt ctttaggatt taggcgccca tggtacaagg aatagtcgcg caagcatccc 780
gctggtgcct cccgggacga aggacttccc gagcggtgtg gggaccgggc tctgacagcc 840
ctgcggagac cctgagtccg ggaggcaccg tccggcggcg agctctggct ttgcaagggc 900
ccctccttct gggggcttcg cttccttagc cttgctcagg tgcaagtgcc ccagggggcg 960
gggtgcagaa gaatccgagt gtttgccagg cttaaggaga ggagaaactg agaaatgaat 1020
gctgagaccc ccggagcagg ggtctgagcc acagccgtgc tcgcccacaa actgatttct 1080
cacggcgtgt caccccacca gggcgcaagc ctcactatta cttgaacttt ccaaaaccta 1140
aagaggaaaa gtgcaatgcg tgttgtacat acagaggtaa ctatcaatat ttaagtttgt 1200
tgctgtcaag attttttttg taacttcaaa tatagagata tttttgtacg ttatatattg 1260
tattaagggc attttaaaag caattatatt gtcctcccct attttaagac gtgaatgtct 1320
cagcgaggtg taaagttgtt cgccgcgtgg aatgtgagtg tgtttgtgtg catgaaagag 1380
aaagactgat tacctcctgt gtggaagaag gaaacaccga gtctctgtat aatctattta 1440
cataaaatgg gtgatatgcg aacagcaaac caataaactg tctcaatgct ga 1492
Claims (15)
- i) PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 2개의 바이오마커(biomarker)의 발현 수준을 측정함으로써 대상체로부터 수득된 샘플 중 시그니쳐(signature)를 결정하는 단계로서,
바람직하게는, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는 것인 단계;
ii) 단계 i)에서 결정된 시그니쳐를 참조 시그니쳐(reference signature)와 비교하는 단계; 및
iii) 시그니쳐 중 적어도 2개의 바이오마커의 발현 수준이 참조 시그니쳐 중의 동일한 적어도 2개의 바이오마커의 발현 수준보다 더 높은 경우, 대상체를 뇌졸중에 걸린 것으로 진단하는 단계를 포함하는, 대상체에서 뇌졸중을 진단하는 방법. - 제1항에 있어서, 단계 i)이 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 3개의 바이오마커의 발현 수준을 측정하는 단계를 포함하는 것인 방법.
- 제1항 또는 제2항에 있어서, 단계 i)이 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM의 발현 수준을 측정하는 단계를 포함하는 것인 방법.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 참조 시그니쳐가 실질적으로 건강한 대상체로 이루어진 참조 집단(reference population)에서 바이오마커의 발현 수준을 측정함으로써 수득되는 것인 방법.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 뇌졸중을 뇌졸중 유사 질환(stroke mimic)과 구별하기 위한 방법.
- i) PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 2개의 바이오마커의 발현 수준을 측정함으로써 대상체로부터 수득된 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는 것인 단계;
ii) 단계 i)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iii) 시그니쳐 중 적어도 2개의 바이오마커의 발현 수준이 참조 시그니쳐 중의 동일한 적어도 2개의 바이오마커의 발현 수준보다 더 낮은 경우, 대상체는 반응을 달성하였다고 결론짓는 단계를 포함하는, 뇌졸중을 앓고 있는 대상체가 요법(therapy)으로 반응을 달성하는지 여부를 결정하는 방법. - 제6항에 있어서, 단계 i)이 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로부터 선택되는 9개의 바이오마커의 발현 수준을 측정하는 단계를 포함하는 것인 방법.
- 제6항 또는 제7항에 있어서, 참조 시그니쳐가 상기 요법 시작 전 동일한 대상체로부터 수득된 샘플 중 바이오마커의 발현 수준을 측정함으로써 수득되는 것인 방법.
- i) PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로 구성된 군으로부터 선택되는 적어도 2개의 바이오마커의 발현 수준을 측정함으로써 대상체로부터 수득된 샘플 중 시그니쳐를 결정하는 단계로서,
바람직하게는, 단, 적어도 2개의 바이오마커는 DUSP1 및 ADM으로 구성되지 않는 것인 단계;
ii) 단계 i)에서 결정된 시그니쳐를 참조 시그니쳐와 비교하는 단계; 및
iii) 시그니쳐 중 적어도 3개의 바이오마커의 발현 수준이 참조 시그니쳐 중의 동일한 적어도 3개의 바이오마커의 발현 수준보다 더 높은 경우, 대상체는 뇌졸중을 앓을 위험이 있다고 결론짓는 단계를 포함하는, 대상체가 뇌졸중을 앓을 위험이 있는지 여부를 결정하는 방법. - 제9항에 있어서, 단계 i)이 PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 및 ADM으로부터 선택되는 9개의 바이오마커의 발현 수준을 측정하는 단계를 포함하는 것인 방법.
- 제9항 또는 제10항에 있어서, 참조 시그니쳐가 실질적으로 건강한 대상체로 이루어진 참조 집단에서 바이오마커의 발현 수준을 측정함으로써 수득되는 것인 방법.
- 제9항 내지 제11항 중 어느 한 항에 있어서, 대상체가 뇌졸중을 경험하였고, 방법은 대상체가 재발성 뇌졸중을 앓을 위험이 있는지 여부를 결정하기 위한 것인 방법.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 뇌졸중이 허혈성 뇌졸중(ischemic stroke), 일과성 허혈 발작(transient ischemic attack) 또는 출혈성 뇌졸중(haemorrhagic stroke)인 것인 방법.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 샘플이 혈액 샘플, 혈장 샘플 또는 혈청 샘플인 것인 방법.
- 제1항 내지 제14항 중 어느 한 항에 있어서, 샘플이 뇌 샘플이 아닌 것인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18305600.1 | 2018-05-16 | ||
| EP18305600 | 2018-05-16 | ||
| PCT/EP2019/062653 WO2019219831A1 (en) | 2018-05-16 | 2019-05-16 | Blood biomarkers of stroke |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210049026A true KR20210049026A (ko) | 2021-05-04 |
Family
ID=62386311
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207035973A KR20210049026A (ko) | 2018-05-16 | 2019-05-16 | 뇌졸중의 혈액 바이오마커 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US20210214793A1 (ko) |
| EP (1) | EP3794355A1 (ko) |
| JP (1) | JP7463351B2 (ko) |
| KR (1) | KR20210049026A (ko) |
| CN (1) | CN112424609A (ko) |
| AU (1) | AU2019270404A1 (ko) |
| BR (1) | BR112020023259A2 (ko) |
| CA (1) | CA3100171A1 (ko) |
| MA (1) | MA52617A (ko) |
| MX (1) | MX2020012297A (ko) |
| SG (1) | SG11202011369VA (ko) |
| WO (1) | WO2019219831A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020154398A1 (en) * | 2019-01-22 | 2020-07-30 | Arizona Board Of Regents On Behalf Of The University Of Arizona | Noninvasive real-time patient-specific assessment of stroke severity |
| CN114107487B (zh) * | 2021-12-23 | 2024-01-09 | 太原市精神病医院 | 一种可用于诊断脑卒中的产品 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4965188A (en) | 1986-08-22 | 1990-10-23 | Cetus Corporation | Process for amplifying, detecting, and/or cloning nucleic acid sequences using a thermostable enzyme |
| US4683195A (en) | 1986-01-30 | 1987-07-28 | Cetus Corporation | Process for amplifying, detecting, and/or-cloning nucleic acid sequences |
| US4800159A (en) | 1986-02-07 | 1989-01-24 | Cetus Corporation | Process for amplifying, detecting, and/or cloning nucleic acid sequences |
| WO2003008647A2 (en) * | 2000-11-28 | 2003-01-30 | University Of Cincinnati | Blood assessment of injury |
| US9005891B2 (en) | 2009-11-10 | 2015-04-14 | Genomic Health, Inc. | Methods for depleting RNA from nucleic acid samples |
| US9410204B2 (en) * | 2012-01-07 | 2016-08-09 | The Regents Of The University Of California | Biomarkers for diagnosing ischemia |
| WO2014120731A1 (en) | 2013-02-01 | 2014-08-07 | West Virginia University | A biomarker algorithm for determining the time of stroke symptom onset and method |
| WO2015054700A2 (en) * | 2013-10-13 | 2015-04-16 | The Research Foundation For Suny | Biomarkers for predicting risk of acute ischemic stroke and methods of use thereof |
| CA2992139A1 (en) * | 2015-07-10 | 2017-01-19 | West Virginia University | Markers of stroke and stroke severity |
| WO2018067571A2 (en) * | 2016-10-03 | 2018-04-12 | West Virginia University | Computer implemented discovery of biomarkers for blood brain barrier disruption |
-
2019
- 2019-05-16 MA MA052617A patent/MA52617A/fr unknown
- 2019-05-16 WO PCT/EP2019/062653 patent/WO2019219831A1/en unknown
- 2019-05-16 US US17/054,820 patent/US20210214793A1/en active Pending
- 2019-05-16 SG SG11202011369VA patent/SG11202011369VA/en unknown
- 2019-05-16 MX MX2020012297A patent/MX2020012297A/es unknown
- 2019-05-16 JP JP2021514483A patent/JP7463351B2/ja active Active
- 2019-05-16 CN CN201980047566.0A patent/CN112424609A/zh active Pending
- 2019-05-16 CA CA3100171A patent/CA3100171A1/en active Pending
- 2019-05-16 EP EP19723441.2A patent/EP3794355A1/en active Pending
- 2019-05-16 KR KR1020207035973A patent/KR20210049026A/ko unknown
- 2019-05-16 BR BR112020023259-9A patent/BR112020023259A2/pt unknown
- 2019-05-16 AU AU2019270404A patent/AU2019270404A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021523744A (ja) | 2021-09-09 |
| SG11202011369VA (en) | 2020-12-30 |
| CA3100171A1 (en) | 2019-11-21 |
| JP7463351B2 (ja) | 2024-04-08 |
| CN112424609A (zh) | 2021-02-26 |
| BR112020023259A2 (pt) | 2021-02-23 |
| US20210214793A1 (en) | 2021-07-15 |
| AU2019270404A1 (en) | 2020-12-10 |
| MA52617A (fr) | 2021-03-24 |
| WO2019219831A1 (en) | 2019-11-21 |
| EP3794355A1 (en) | 2021-03-24 |
| MX2020012297A (es) | 2021-03-25 |
| AU2019270404A2 (en) | 2020-12-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11136626B2 (en) | Biomarkers for the diagnosis of lacunar stroke | |
| CN106978480A (zh) | 用于癌症的分子诊断试验 | |
| JP2008537474A5 (ko) | ||
| US11021750B2 (en) | Biomarkers for predicting risk of acute ischemic stroke and methods of use thereof | |
| KR20210049026A (ko) | 뇌졸중의 혈액 바이오마커 | |
| Chang et al. | Level and prognostic value of serum myeloperoxidase in patients with acute myocardial infarction undergoing primary percutaneous coronary intervention | |
| JP2023157965A (ja) | アトピー性皮膚炎の検出方法 | |
| US20160244845A1 (en) | Method for determining the prognosis of pancreatic cancer | |
| US20130274127A1 (en) | Gene expression markers for prediction of response to phosphoinositide 3-kinase inhibitors | |
| JP6784673B2 (ja) | 膵臓がんに冒された患者の生存予後を判断する方法 | |
| US20140221235A1 (en) | Biomarker algorithm for determining the time of stroke symptom onset and method | |
| US20210087634A1 (en) | Determination of risk for development of cardiovascular disease by measuring urinary levels of podocin and nephrin messenger rna | |
| JP2023501760A (ja) | 子癇前症に特異的な循環rnaシグネチャー | |
| KR20190052397A (ko) | 다발성 골수종 환자에서 레날리도마이드 및 덱사메타손의 치료에 대한 예후 예측용 바이오 마커 | |
| US20230332236A1 (en) | Method for diagnosing stroke utilizing gene expression signatures | |
| Chang et al. | BIOM-23. IDENTIFICATION OF NOVEL BIOMARKERS FOR BRAIN TUMOR USING PRECISION MEDICINE APPROACHES: ORC6 PLAYS A CRITICAL ROLE IN GLIOBLASTOMA THERAPEUTICS | |
| JP2022134126A (ja) | アトピー性皮膚炎の症度悪化の検出方法 | |
| JP2022134127A (ja) | アトピー性皮膚炎による皮膚痒みの症度悪化の検出方法 | |
| CN116635526A (zh) | 特应性皮炎的重症度的检测方法 | |
| CN117385034A (zh) | 标志物组合在制备预测肝癌患者预后治疗疗效产品中的应用 | |
| WO2009097080A1 (en) | Protein phosphatase-1 inhibitor-1 polymorphism and methods of use | |
| KR20130141044A (ko) | 급성 심근경색 조기 진단 마커 | |
| Cockayne et al. | Whole blood gene expression and serum biomarker profiling in a COPD cohort identifies markers related to neutrophilic inflammation, wound healing and altered b cell signaling | |
| Luque Gómez et al. | Usefulness of circulating microRNAs for the prediction of early preeclampsia at first-trimester of pregnancy |