KR20200055067A - 성인의 초점성 뇌전증의 치료를 위한 합성 경피성 칸나비디올 - Google Patents
성인의 초점성 뇌전증의 치료를 위한 합성 경피성 칸나비디올 Download PDFInfo
- Publication number
- KR20200055067A KR20200055067A KR1020207011219A KR20207011219A KR20200055067A KR 20200055067 A KR20200055067 A KR 20200055067A KR 1020207011219 A KR1020207011219 A KR 1020207011219A KR 20207011219 A KR20207011219 A KR 20207011219A KR 20200055067 A KR20200055067 A KR 20200055067A
- Authority
- KR
- South Korea
- Prior art keywords
- cbd
- effective amount
- seizure
- seizures
- transdermal
- Prior art date
Links
- QHMBSVQNZZTUGM-ZWKOTPCHSA-N cannabidiol Chemical compound OC1=CC(CCCCC)=CC(O)=C1[C@H]1[C@H](C(C)=C)CCC(C)=C1 QHMBSVQNZZTUGM-ZWKOTPCHSA-N 0.000 title claims abstract description 181
- QHMBSVQNZZTUGM-UHFFFAOYSA-N Trans-Cannabidiol Natural products OC1=CC(CCCCC)=CC(O)=C1C1C(C(C)=C)CCC(C)=C1 QHMBSVQNZZTUGM-UHFFFAOYSA-N 0.000 title claims abstract description 180
- 229950011318 cannabidiol Drugs 0.000 title claims abstract description 177
- ZTGXAWYVTLUPDT-UHFFFAOYSA-N cannabidiol Natural products OC1=CC(CCCCC)=CC(O)=C1C1C(C(C)=C)CC=C(C)C1 ZTGXAWYVTLUPDT-UHFFFAOYSA-N 0.000 title claims abstract description 177
- PCXRACLQFPRCBB-ZWKOTPCHSA-N dihydrocannabidiol Natural products OC1=CC(CCCCC)=CC(O)=C1[C@H]1[C@H](C(C)C)CCC(C)=C1 PCXRACLQFPRCBB-ZWKOTPCHSA-N 0.000 title claims abstract description 177
- 206010061334 Partial seizures Diseases 0.000 title claims description 16
- 201000007186 focal epilepsy Diseases 0.000 title description 6
- 206010010904 Convulsion Diseases 0.000 claims abstract description 139
- 238000000034 method Methods 0.000 claims abstract description 37
- 206010015037 epilepsy Diseases 0.000 claims abstract description 21
- 239000001961 anticonvulsive agent Substances 0.000 claims description 15
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 13
- 230000002411 adverse Effects 0.000 claims description 11
- 208000035475 disorder Diseases 0.000 claims description 10
- 230000009885 systemic effect Effects 0.000 claims description 10
- 230000007423 decrease Effects 0.000 claims description 9
- 206010043994 Tonic convulsion Diseases 0.000 claims description 7
- 208000001654 Drug Resistant Epilepsy Diseases 0.000 claims description 6
- 230000000694 effects Effects 0.000 claims description 5
- 208000022540 Consciousness disease Diseases 0.000 claims description 3
- 206010041349 Somnolence Diseases 0.000 claims description 3
- KJADKKWYZYXHBB-XBWDGYHZSA-N Topiramic acid Chemical compound C1O[C@@]2(COS(N)(=O)=O)OC(C)(C)O[C@H]2[C@@H]2OC(C)(C)O[C@@H]21 KJADKKWYZYXHBB-XBWDGYHZSA-N 0.000 claims description 3
- -1 clovazam Chemical compound 0.000 claims description 3
- 230000035515 penetration Effects 0.000 claims description 3
- 229960004394 topiramate Drugs 0.000 claims description 3
- BMPDWHIDQYTSHX-AWEZNQCLSA-N (S)-MHD Chemical compound C1[C@H](O)C2=CC=CC=C2N(C(=O)N)C2=CC=CC=C21 BMPDWHIDQYTSHX-AWEZNQCLSA-N 0.000 claims description 2
- CXOFVDLJLONNDW-UHFFFAOYSA-N Phenytoin Chemical compound N1C(=O)NC(=O)C1(C=1C=CC=CC=1)C1=CC=CC=C1 CXOFVDLJLONNDW-UHFFFAOYSA-N 0.000 claims description 2
- 229960000623 carbamazepine Drugs 0.000 claims description 2
- FFGPTBGBLSHEPO-UHFFFAOYSA-N carbamazepine Chemical compound C1=CC2=CC=CC=C2N(C(=O)N)C2=CC=CC=C21 FFGPTBGBLSHEPO-UHFFFAOYSA-N 0.000 claims description 2
- 229960003120 clonazepam Drugs 0.000 claims description 2
- DGBIGWXXNGSACT-UHFFFAOYSA-N clonazepam Chemical compound C12=CC([N+](=O)[O-])=CC=C2NC(=O)CN=C1C1=CC=CC=C1Cl DGBIGWXXNGSACT-UHFFFAOYSA-N 0.000 claims description 2
- 230000002708 enhancing effect Effects 0.000 claims description 2
- 229960004028 eslicarbazepine Drugs 0.000 claims description 2
- 229960002623 lacosamide Drugs 0.000 claims description 2
- VPPJLAIAVCUEMN-GFCCVEGCSA-N lacosamide Chemical compound COC[C@@H](NC(C)=O)C(=O)NCC1=CC=CC=C1 VPPJLAIAVCUEMN-GFCCVEGCSA-N 0.000 claims description 2
- 229960001848 lamotrigine Drugs 0.000 claims description 2
- PYZRQGJRPPTADH-UHFFFAOYSA-N lamotrigine Chemical compound NC1=NC(N)=NN=C1C1=CC=CC(Cl)=C1Cl PYZRQGJRPPTADH-UHFFFAOYSA-N 0.000 claims description 2
- 229960004002 levetiracetam Drugs 0.000 claims description 2
- HPHUVLMMVZITSG-ZCFIWIBFSA-N levetiracetam Chemical compound CC[C@H](C(N)=O)N1CCCC1=O HPHUVLMMVZITSG-ZCFIWIBFSA-N 0.000 claims description 2
- 230000003908 liver function Effects 0.000 claims description 2
- 229960001816 oxcarbazepine Drugs 0.000 claims description 2
- CTRLABGOLIVAIY-UHFFFAOYSA-N oxcarbazepine Chemical compound C1C(=O)C2=CC=CC=C2N(C(=O)N)C2=CC=CC=C21 CTRLABGOLIVAIY-UHFFFAOYSA-N 0.000 claims description 2
- 229960002036 phenytoin Drugs 0.000 claims description 2
- AEQFSUDEHCCHBT-UHFFFAOYSA-M sodium valproate Chemical compound [Na+].CCCC(C([O-])=O)CCC AEQFSUDEHCCHBT-UHFFFAOYSA-M 0.000 claims description 2
- 229940102566 valproate Drugs 0.000 claims description 2
- 239000000499 gel Substances 0.000 description 83
- 239000000902 placebo Substances 0.000 description 31
- 229940068196 placebo Drugs 0.000 description 31
- 230000009467 reduction Effects 0.000 description 30
- 101100110009 Caenorhabditis elegans asd-2 gene Proteins 0.000 description 29
- 230000008859 change Effects 0.000 description 11
- 210000004556 brain Anatomy 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 229960003965 antiepileptics Drugs 0.000 description 6
- 239000003814 drug Substances 0.000 description 6
- 230000037317 transdermal delivery Effects 0.000 description 6
- 230000004044 response Effects 0.000 description 5
- CYQFCXCEBYINGO-UHFFFAOYSA-N THC Natural products C1=C(C)CCC2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3C21 CYQFCXCEBYINGO-UHFFFAOYSA-N 0.000 description 4
- 238000009098 adjuvant therapy Methods 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 229930003827 cannabinoid Natural products 0.000 description 4
- 239000003557 cannabinoid Substances 0.000 description 4
- CYQFCXCEBYINGO-IAGOWNOFSA-N delta1-THC Chemical compound C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@@H]21 CYQFCXCEBYINGO-IAGOWNOFSA-N 0.000 description 4
- 238000012423 maintenance Methods 0.000 description 4
- 230000036470 plasma concentration Effects 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 241000218236 Cannabis Species 0.000 description 3
- 208000033001 Complex partial seizures Diseases 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 229940065144 cannabinoids Drugs 0.000 description 3
- 230000006735 deficit Effects 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 229960004242 dronabinol Drugs 0.000 description 3
- 206010016256 fatigue Diseases 0.000 description 3
- 230000002496 gastric effect Effects 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 239000002207 metabolite Substances 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- 230000003442 weekly effect Effects 0.000 description 3
- 206010019233 Headaches Diseases 0.000 description 2
- 206010057190 Respiratory tract infections Diseases 0.000 description 2
- 206010046306 Upper respiratory tract infection Diseases 0.000 description 2
- 230000003556 anti-epileptic effect Effects 0.000 description 2
- 229940125681 anticonvulsant agent Drugs 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 230000002743 euphoric effect Effects 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 231100000869 headache Toxicity 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 239000003961 penetration enhancing agent Substances 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- 229940002612 prodrug Drugs 0.000 description 2
- 239000000651 prodrug Substances 0.000 description 2
- 208000020029 respiratory tract infectious disease Diseases 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 238000009097 single-agent therapy Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 102000008102 Ankyrins Human genes 0.000 description 1
- 108010049777 Ankyrins Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 208000028698 Cognitive impairment Diseases 0.000 description 1
- XXGMIHXASFDFSM-UHFFFAOYSA-N Delta9-tetrahydrocannabinol Natural products CCCCCc1cc2OC(C)(C)C3CCC(=CC3c2c(O)c1O)C XXGMIHXASFDFSM-UHFFFAOYSA-N 0.000 description 1
- 206010012735 Diarrhoea Diseases 0.000 description 1
- 201000007547 Dravet syndrome Diseases 0.000 description 1
- 208000024658 Epilepsy syndrome Diseases 0.000 description 1
- 208000002877 Epileptic Syndromes Diseases 0.000 description 1
- 206010015150 Erythema Diseases 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- 108091006027 G proteins Proteins 0.000 description 1
- 102000030782 GTP binding Human genes 0.000 description 1
- 108091000058 GTP-Binding Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- 208000034693 Laceration Diseases 0.000 description 1
- 201000006792 Lennox-Gastaut syndrome Diseases 0.000 description 1
- 206010024264 Lethargy Diseases 0.000 description 1
- 208000036572 Myoclonic epilepsy Diseases 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 102000019055 Nucleoside Transport Proteins Human genes 0.000 description 1
- 208000037158 Partial Epilepsies Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 208000028017 Psychotic disease Diseases 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- 206010073677 Severe myoclonic epilepsy of infancy Diseases 0.000 description 1
- 206010040703 Simple partial seizures Diseases 0.000 description 1
- 208000032140 Sleepiness Diseases 0.000 description 1
- 206010047700 Vomiting Diseases 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 230000037374 absorbed through the skin Effects 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000004596 appetite loss Effects 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 230000006931 brain damage Effects 0.000 description 1
- 231100000874 brain damage Toxicity 0.000 description 1
- 208000029028 brain injury Diseases 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 229960001403 clobazam Drugs 0.000 description 1
- CXOXHMZGEKVPMT-UHFFFAOYSA-N clobazam Chemical compound O=C1CC(=O)N(C)C2=CC=C(Cl)C=C2N1C1=CC=CC=C1 CXOXHMZGEKVPMT-UHFFFAOYSA-N 0.000 description 1
- 208000010877 cognitive disease Diseases 0.000 description 1
- 230000001149 cognitive effect Effects 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 239000000599 controlled substance Substances 0.000 description 1
- 230000036461 convulsion Effects 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- XXJWXESWEXIICW-UHFFFAOYSA-N diethylene glycol monoethyl ether Chemical compound CCOCCOCCO XXJWXESWEXIICW-UHFFFAOYSA-N 0.000 description 1
- 229940075557 diethylene glycol monoethyl ether Drugs 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 208000028329 epileptic seizure Diseases 0.000 description 1
- 208000028316 focal seizure Diseases 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 210000004211 gastric acid Anatomy 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 230000010224 hepatic metabolism Effects 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 230000005976 liver dysfunction Effects 0.000 description 1
- 208000019017 loss of appetite Diseases 0.000 description 1
- 235000021266 loss of appetite Nutrition 0.000 description 1
- 230000000116 mitigating effect Effects 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 230000008587 neuronal excitability Effects 0.000 description 1
- 108091006527 nucleoside transporters Proteins 0.000 description 1
- 229940126701 oral medication Drugs 0.000 description 1
- 230000037368 penetrate the skin Effects 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000037321 sleepiness Effects 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 238000013271 transdermal drug delivery Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 230000008673 vomiting Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/047—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates having two or more hydroxy groups, e.g. sorbitol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/357—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having two or more oxygen atoms in the same ring, e.g. crown ethers, guanadrel
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/4015—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil having oxo groups directly attached to the heterocyclic ring, e.g. piracetam, ethosuximide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4166—1,3-Diazoles having oxo groups directly attached to the heterocyclic ring, e.g. phenytoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
- A61K31/5513—1,4-Benzodiazepines, e.g. diazepam or clozapine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Pain & Pain Management (AREA)
- Dermatology (AREA)
- Molecular Biology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
본 기술은 뇌전증을 갖는 대상에게 칸나비디올(CBD)의 유효량을 경피 투여함으로써 발작 빈도가 감소하는, 뇌전증을 갖는 대상의 발작 빈도를 감소시키는 방법에 관한 것이다.
Description
관련 출원에 대한 상호 참조
본 출원은 미국 가출원 제62/560,446호(2017년 9월 19일 출원), 제62/593,575호(2017년 12월 1일 출원), 제62/613,160호(2018년 1월 3일 출원), 제62/652,995호(2018년 4월 5일 출원), 및 제62/660,198호(2018년 4월 19일 출원)의 이익 및 우선권을 주장한다. 상기 출원들 각각의 전체 내용은 그 전문이 본원에 참조로 포함된다.
기술 분야
본 개시내용은 뇌전증을 갖는 대상에게 칸나비디올(CBD)의 유효량을 경피 투여함으로써 발작 빈도가 감소하는, 뇌전증을 갖는 대상의 발작 빈도를 감소시키는 방법에 관한 것이다.
칸나비노이드는 칸나비스 식물에서 발견되는 일종의 화합물이다. 칸나비스(Cannabis)에 함유된 두 가지 주요 칸나비노이드는 칸나비디올, 또는 CBD, 및 Δ9-테트라히드로칸나비놀, 또는 THC이다. CBD에는 THC의 정신활성 효과가 없다. 연구들은 뇌전증, 관절염, 및 암과 같은 장애를 치료하는 데 CBD가 사용될 수 있음을 보여주었다.
뇌전증은 발작을 일으키는 지속적인 소인, 및 병태의 신경생물학적, 인지적, 정신적 및 사회적 결과를 특징으로 하는 질환이다. 뇌전증성 발작은 뇌의 비정상적으로 과도한 또는 동시적인 신경 활동으로 인한 징후 및/또는 증상의 일시적인 발생이다. 뇌전증 발작은 유전적 장애, 또는 외상 또는 뇌졸중과 같은 뇌 손상과 관련있을 수 있지만, 대부분 원인은 알려지지 않았다. 미국에서는 매년 20만 건보다 많은 뇌전증이 발생한다.
전신 뇌전증은 발생시 뇌의 두 반구 모두에 영향을 미친다. 초점성 뇌전증(이전에는 부분 발생 발작으로 불림)은 초기에 뇌의 한 반구 또는 엽(lobe)에만 영향을 미치는 발작이다. 초점성 뇌전증의 증상은 발작이 발생하는 뇌의 반구 또는 엽에 따라 다르다.
본 개시내용은 뇌전증을 갖는 대상의 발작 빈도를 감소시키는 방법으로서, 상기 대상에게 칸나비디올(CBD)의 유효량을 경피 투여하는 것을 포함하고, 발작 빈도가 감소하는 것인 방법에 관한 것이다.
발작 빈도는 25% 감소할 수 있다. 일부 실시양태에서, 발작 빈도는 30% 감소한다. 발작 빈도는 50% 감소할 수 있다. 발작 빈도는 65% 감소할 수 있다. 발작 빈도의 감소는 CBD의 유효량을 투여하기 전 베이스라인 발작 빈도로부터의 감소일 수 있다. 일부 실시양태에서, 발작 빈도의 감소는 주간 발작 감소로 측정된다. 일부 실시양태에서, 발작 빈도의 감소는 28일 기간당 발작 빈도로 측정된다. 일부 실시양태에서, 발작 빈도의 감소는 월간 발작 빈도로 측정된다.
일부 실시양태에서 성인의 초점성 발생 발작(이전에는 부분 발생 발작으로 알려짐)이 감소한다. 성인은 18세 이상인 대상이다. 일부 실시양태에서 초점성 의식 발작(이전에는 단순 부분 발작으로 알려짐)이 감소한다. 초점성 의식 장애 발작(이전에는 복합 부분 발작으로 알려짐)이 감소할 수 있다. 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작(이전에는 전신 강직 간대 발작을 동반한 복합 부분 발작으로 알려짐)이 감소할 수 있다.
대상은 높은 발작 빈도를 가질 수 있다. 뇌전증은 약물 내성 뇌전증(이전에는 난치성 뇌전증로 알려짐)일 수 있다.
일부 실시양태에서, 상기 방법은 또한 레베티라세탐, 카바마제핀, 토피라메이트, 라모트리진, 라코사미드, 클로나제팜, 발프로에이트, 페니토인, 에슬리카바제핀, 클로바잠, 및 옥스카바제핀으로 이루어진 군으로부터 선택되는 1종 이상의 항뇌전증약을 투여하는 단계를 포함한다. 항뇌전증약은 예를 들어 항경련제일 수 있다. CBD 경피성 겔은 1종 이상의 항뇌전증약과 함께 보조 요법으로 사용될 수 있다. 일부 실시양태에서, CBD 경피성 겔은 2종 또는 3종의 항뇌전증약과 함께 보조 요법으로 사용될 수 있다. CBD 경피성 겔은 단일요법으로 사용될 수도 있다.
일부 실시양태에서, CBD는 (-)-CBD이다. CBD는 합성 CBD일 수 있다. CBD는 순수 CBD일 수 있다.
CBD의 유효량은 일일 총 약 195 mg 내지 약 780 mg일 수 있다. CBD는 단회의 일일 용량으로 투여될 수 있다. 일부 실시양태에서, CBD는 2회의 일일 용량으로 투여된다.
일부 실시양태에서, CBD의 유효량은 분할된 일일 용량으로 195 mg이다. CBD의 유효량은 분할된 일일 용량으로 390 mg일 수 있다. 일부 실시양태에서, CBD의 유효량은 분할된 일일 용량으로 585 mg이다. CBD의 유효량은 분할된 일일 용량으로 780 mg일 수 있다.
CBD의 유효량은 97.5 mg 일회용 사셰로 제공될 수 있다. 일부 실시양태에서, CBD의 유효량은 195 mg 일회용 사셰로 제공된다. CBD의 유효량은 390 mg 일회용 사셰로 제공될 수 있다.
CBD는 겔로 제제화된다. 일부 실시양태에서, CBD는 침투 강화 겔로 제제화된다. 겔은 4.2%(wt/wt) CBD 또는 7.5%(wt/wt) CBD를 함유할 수 있다.
일부 실시양태에서, 경피성 조제물은 크림, 고약(salve) 또는 연고일 수 있다. CBD는 붕대, 패드 또는 패치에 의해 전달될 수 있다.
CBD의 유효량을 경피 투여하는 것은 CBD를 경구 투여하는 것에 비해 하나 이상의 이상 사례의 강도를 감소시킬 수 있다. 하나 이상의 이상 사례는 졸림, 정신활성 효과, 간 기능, GI 관련 이상 사례, 설사, 식욕 감소, 피로, 발열, 구토, 무기력, 상기도 감염, 경련, 또는 이들의 조합일 수 있다. 일부 실시양태에서, CBD의 유효량을 경피 투여하는 것은 CBD를 경구 투여하는 것에 비해 하나 이상의 이상 사례의 강도를 약 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 또는 95% 감소시킨다.
일부 실시양태에서, 대상은 성인, 즉 18세 이상이다.
일부 실시양태에서, 발작 빈도의 감소는 3개월 후 나타난다. 발작 빈도의 감소는 12주 후 나타날 수 있다. 일부 실시양태에서, 발작 빈도의 감소는 6개월 후 나타난다. 발작 빈도의 감소는 24주 후 나타날 수 있다.
본 개시내용은 뇌전증을 갖는 대상의 발작 빈도를 감소시키는 방법에 관한 것이다. 상기 방법은 일정 기간 동안 상기 대상에게 칸나비디올(CBD)의 제1 유효량을 경피 투여하는 단계로서, 발작 빈도가 감소하는 것인 단계를 포함한다. 상기 방법은 또한 일정 기간 후 상기 대상에게 CBD의 제2 유효량을 경피 투여하는 단계를 포함하며, 여기에서 CBD의 제2 유효량은 CBD의 제1 유효량보다 적고, 감소된 발작 빈도가 유지된다.
기간은 12주일 수 있다. 기간은 24주일 수 있다.
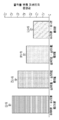
도 1은 본 기술의 실시양태에 따른, 월간 발작률 감소 퍼센트의 중앙값(효능 집단)을 나타내는 그래프이다.
도 2는 본 기술의 실시양태에 따른, 초점성 의식 발작(B형)을 갖는 환자에 대한 발작률 감소 퍼센트의 중앙값을 나타내는 그래프이다.
도 3은 본 기술의 실시양태에 따른, 초점성 의식 장애 발작(C형)을 갖는 환자에 대한 발작률 감소 퍼센트의 중앙값을 나타내는 그래프이다.
도 4는 본 기술의 실시양태에 따른, 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작(D형)을 갖는 환자에 대한 발작률 감소 퍼센트의 중앙값을 나타내는 그래프이다.
도 5는 본 기술의 실시양태에 따른, 제12주(STAR 1) 및 제3월 및 제6월(STAR 2)에서의 발작률 변화 퍼센트의 중앙값을 나타내는 그래프이다.
도 6은 본 기술의 실시양태에 따른, 각각의 3개월 간격의 시간별 SF28의 중앙값을 나타내는 그래프이다.
도 7은 본 기술의 실시양태에 따른, STAR 2의 제6월까지의 각각의 3개월 간격의 시간별 SF28의 중앙값을 나타내는 그래프이다.
도 8은 본 기술의 실시양태에 따른, AED 변화가 없는 환자에 대한 시간별 SF28의 중앙값을 나타내는 그래프이다.
도 9는 본 기술의 실시양태에 따른, STAR 2의 모든 CBD 경피성 겔로 치료된 환자에 대한 제3월, 제6월, 제9월, 및 제12월에서의 발작률 변화(%)의 중앙값을 나타내는 그래프이다.
도 10은 본 기술의 실시양태에 따른, STAR 1의 위약 또는 CBD 경피성 겔(195 mg 및 390 mg)로 치료된 환자에 대한 제3월, 제6월, 제9월, 및 제12월에서의 발작률 변화(%)의 중앙값을 나타내는 그래프이다.
도 2는 본 기술의 실시양태에 따른, 초점성 의식 발작(B형)을 갖는 환자에 대한 발작률 감소 퍼센트의 중앙값을 나타내는 그래프이다.
도 3은 본 기술의 실시양태에 따른, 초점성 의식 장애 발작(C형)을 갖는 환자에 대한 발작률 감소 퍼센트의 중앙값을 나타내는 그래프이다.
도 4는 본 기술의 실시양태에 따른, 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작(D형)을 갖는 환자에 대한 발작률 감소 퍼센트의 중앙값을 나타내는 그래프이다.
도 5는 본 기술의 실시양태에 따른, 제12주(STAR 1) 및 제3월 및 제6월(STAR 2)에서의 발작률 변화 퍼센트의 중앙값을 나타내는 그래프이다.
도 6은 본 기술의 실시양태에 따른, 각각의 3개월 간격의 시간별 SF28의 중앙값을 나타내는 그래프이다.
도 7은 본 기술의 실시양태에 따른, STAR 2의 제6월까지의 각각의 3개월 간격의 시간별 SF28의 중앙값을 나타내는 그래프이다.
도 8은 본 기술의 실시양태에 따른, AED 변화가 없는 환자에 대한 시간별 SF28의 중앙값을 나타내는 그래프이다.
도 9는 본 기술의 실시양태에 따른, STAR 2의 모든 CBD 경피성 겔로 치료된 환자에 대한 제3월, 제6월, 제9월, 및 제12월에서의 발작률 변화(%)의 중앙값을 나타내는 그래프이다.
도 10은 본 기술의 실시양태에 따른, STAR 1의 위약 또는 CBD 경피성 겔(195 mg 및 390 mg)로 치료된 환자에 대한 제3월, 제6월, 제9월, 및 제12월에서의 발작률 변화(%)의 중앙값을 나타내는 그래프이다.
본원에 사용된 바와 같이, "치료하는 것" 또는 "치료"라는 용어는 인간과 같은 대상에서 병태, 질환 또는 장애의 하나 이상의 증상을 완화(mitigating), 개선, 경감 또는 완화(alleviating)시키는 것, 또는 병태, 질환 또는 장애와 관련된 확인가능한 측정의 개선을 지칭한다.
본원에 사용된 바와 같이, "임상 효능"이라는 용어는 식품의약국(FDA) 임상 시험을 통해 나타나는 바와 같이 인간에게 원하는 효과를 생성하는 능력을 지칭한다.
본원에 사용된 바와 같이, "칸나비디올" 또는 "CBD"라는 용어는 칸나비디올; 칸나비디올 전구약물; 칸나비디올, 칸나비디올 전구약물, 및 칸나비디올 유도체의 약학적으로 허용가능한 염을 포함하는, 칸나비디올의 약학적으로 허용가능한 유도체를 지칭한다. CBD는 2-[3-메틸-6-(1-메틸에테닐)-2-시클로헥센-1-일]-5-펜틸-1,3-벤젠디올 뿐만 아니라 이의 약학적으로 허용가능한 염, 용매화물, 대사물(예를 들어, 피부 대사물), 및 대사물 전구체를 포함한다. CBD의 합성은 예를 들어 문헌 [Petilka et al., Helv. Chim. Acta, 52:1102 (1969)] 및 [Mechoulam et al., J. Am. Chem. Soc., 87:3273 (1965)]에 기술되어 있으며, 상기 문헌들은 본원에 참조로 포함되어 있다.
본원에 사용된 바와 같이, "높은 발작 빈도"라는 용어는 15 이상의 28일 기간당 발작 빈도(SF28)를 지칭한다.
본원에 사용된 바와 같이, "약물 내성 뇌전증"이라는 용어는 의약이 발작을 적절하게 치료하지 못하는 뇌전증을 지칭한다. 약물 내성 뇌전증은 지속성 무발작을 달성하기 위한 2가지의 내약성이 있고, 적절하게 선택되고 사용되는 항뇌전증약 스케줄(단일요법 또는 조합으로)의 적절한 시도의 실패이다.
본원에 사용된 바와 같이, "초점성 발생 발작"(이전에는 "부분 발생 발작"으로 알려짐)이라는 용어는 초기에 뇌의 한 반구 또는 엽에만 영향을 미치는 발작을 지칭한다.
본원에 사용된 바와 같이, "초점성 의식 장애 발작"(이전에는 "복합 부분 발작"으로 알려짐)이라는 용어는 초기에 뇌의 한 반구 또는 엽에만 영향을 미치고 의식 장애을 유발하는 발작을 지칭한다.
본원에 사용된 바와 같이, "전신 강직 간대 발작을 동반한 초점성 의식 장애 발작"이라는 용어는 강직(경직되는 것) 및 간대(주기적인 경련)의 특징을 갖는 초점성 의식 장애 발작을 지칭한다.
"보조 요법"이라는 용어는, 이미 기존의 다른 치료제를 투여받고 있는 대상에게 치료제를 투여하는 것을 지칭하지만, 반드시 치료제가 동시에 또는 동일한 경로로 투여되거나 제공되는 것을 의미하지는 않는다. 예를 들어, CBD는 기존 경구 약물 요법에 부가적으로 또는 보조적으로 투여될 수 있다.
본원에 사용된 바와 같이, "경피 투여"라는 용어는 CBD가 피부에 침투하기에 효과적인 조건 하에서 CBD와 환자 또는 대상의 피부를 접촉시키는 것을 지칭한다.
"28일 기간당 발작 빈도" 또는 "SF28"은 다음 식으로 계산된다:
SF28 = (D일 동안의 총 발작 수)×(28/D)
상기 식에서 D는 특정 시간 간격 동안 발작 정보가 수집되는 총 일 수이다.
유지 기간 동안 베이스라인으로부터의 발작 빈도의 감소(RedSF)는 다음과 같이 정의된다:
RedSF = SF28(베이스라인) - SF28(유지)
베이스라인은 CBD 겔이 투여되지 않고 그 기간 동안 발작 수가 계수되는 기간을 지칭한다. 다시 말해, 베이스라인 기간은 환자가 평상시의 AED를 사용하는 동안 발작 빈도가 포착되는 기간이다. 베이스라인 기간은 예를 들어 8주일 수 있다. 대상은 베이스라인 기간 동안 높은 발작 빈도를 가질 수 있다. 유지는 CBD 경피성 겔이 투여되고 그 기간 동안 발작 수가 계수되는 기간을 지칭한다. 유지 기간은 예를 들어 12주, 3개월, 6개월, 9개월, 12개월, 15개월, 18개월 또는 20개월일 수 있다.
유지 기간 동안의 베이스라인으로부터의 발작 빈도의 감소 퍼센트는 다음과 같이 정의된다:
%RedSF = 100×[SF28(베이스라인) - SF28(유지)]/SF28(베이스라인)
환자의 %RedSF가 50% 이상인 경우, 특정 치료 기간 동안 상기 환자를 50% 반응자로 정의한다.
일부 실시양태에서, 주간 발작 빈도 값을 제공하기 위해 발작 빈도는 7일 기간마다 계산된다. 주간 발작 빈도는 25%, 30%, 50% 또는 65% 감소할 수 있다. 발작 빈도의 감소는 CBD의 유효량을 투여하기 전 베이스라인 발작 빈도로부터의 감소일 수 있다.
본 개시내용은 뇌전증을 갖는 환자의 발작 빈도를 감소시키는 방법으로서, 상기 대상에게 칸나비디올(CBD)의 유효량을 경피 투여하는 것을 포함하고, 발작 빈도가 감소하는 것인 방법에 관한 것이다.
CBD는 칸나비스 식물에서 발견되는 주요 비정신활성 칸나비노이드이고, CB1 및 CB2 수용체에 대한 친화력이 낮다. CBD는 평형 뉴클레오시드 수송체, 오펀(orphan) G-단백질 수용체 GPR-55, 및 일시적 수용체 전위 안키린 1형 채널을 차단하고, 칼슘의 세포내 효과를 조절하는 것을 포함하여 여러 효과를 생성한다. 각각이 뉴런 흥분성에 역할을 하는 것으로 알려진 이들 표적에 대한 CBD의 영향은 항뇌전증성 잠재력에 대한 과학적 근거이다. 인간의 넓은 안전 한계에 대한 기대는, 여러 투여 방식에 걸쳐 CBD가 높은 내약성을 나타내는 잘 통제된 연구의 결과에 기초한다.
인간 환자의 뇌전증 치료는 일반적으로 항뇌전증약 및 항경련제를 포함한다. CBD가 레녹스 가스토(Lennox Gastaut) 증후군 및 드라베(Dravet) 증후군(뇌전증 증후군의 한 유형)을 효과적으로 치료할 수 있음을 보여주는 연구가 수행되었지만, 이러한 연구는 뇌전증을 앓는 소아에 대한 경구 전달 칸나비디올(CBD)에 초점을 두었다.
칸나비노이드, 예를 들어, CBD의 경피 전달은 경구 투약에 비해 이점이 있는데, 왜냐하면 경피 전달은 약물이 피부를 통해 혈류로 직접 흡수될 수 있게 하기 때문이다. 이는 초회 통과 간 대사를 방지하여, 생체이용률이 높고(약 25%) 안전성 프로파일이 개선된 활성 제약 성분의 낮은 복용량 수준을 잠재적으로 가능하게 한다. 경피 전달은 또한 위장(GI) 관을 피하여, GI 관련 이상 사례에 대한 가능성, 및 원치 않는 정신활성 효과 및/또는 행복감 효과와 관련될 수 있는, 위산에 의한 CBD의 THC로의 잠재적 분해를 줄인다. 또한, 경구 CBD는 낮고(6%) 가변적인 생체이용률을 제공한다. CBD의 경피 전달은, 통상적으로 CBD의 경구 투약에 존재하는 졸림 이상 사례를 피하거나 감소시킬 수 있다. CBD의 경피 전달은, 또한 통상적으로 CBD의 경구 투약에 존재하는 정신활성 효과 및/또는 행복감 효과 및/또는 GI 관련 이상 사례를 피할 수 있다. CBD의 경피 전달은, 통상적으로 CBD의 경구 투약에 존재하는 간 기능 이상 사례를 피할 수 있다. 일부 실시양태에서, CBD의 유효량의 경피 투여는 CBD의 경구 투여에 비해 하나 이상의 이상 사례의 강도를 약 15% 내지 약 95% 감소시킨다.
2회의 일일 투약(약 12시간 마다)으로 일관된, 제어된 CBD 전달을 제공하기 위해 투명한 경피성 겔이 개발되었다. 4.2%(wt/wt) 또는 7.5%(wt/wt) CBD 겔이 사용될 수 있다. CBD는 겔 형태일 수 있고, 1회 또는 2회의 일일 투약으로 제어된 경피 약물 전달을 제공하도록 설계된 투명한, 침투성이 강화된 겔로 약학적으로 제조될 수 있다. CBD 겔은 환자 또는 간병인에 의해 환자의 팔, 등, 다리, 또는 이들의 임의의 조합에 국소적으로 적용될 수 있다.
CBD 겔의 경피 도포로부터의 0차 전달은 경구 또는 구강 전달 경로보다 더 낮은 Cmax를 제공할 수 있기 때문에, CBD 경피성 겔 사용은 전신 노출을 줄여서, 경구, 흡입 및 주사용 제제의 더 높은 전신 용량에서 확립된 인간의 안전성 한계치보다 훨씬 낮게 배치될 수 있다.
경구 투약과 경피 투약 사이에 0차 역학이 있을 것으로 예상되었지만, 그렇지 않았다. 이론에 얽매이지 않고, 2개의 흡수율(지체 시간을 갖는 더 빠른 것 및 지체 시간이 없는 더 느린 것)을 갖는 2구획 모델이 합쳐졌는데, 왜냐하면 CBD 겔의 경피 도포가 피부에 적용되고, 적용 부위에서 피부를 통해 흡수되고, 혈류로 들어가고, 대상의 신체(예를 들어, 간) 뿐만 아니라 작용 부위(예를 들어, 뇌) 전체의 지방 조직으로 들어간다고 여겨지기 때문이다. 이러한 모델은 예상치 못한 새로운 것이었으며, 정상 상태 수준에 도달하면, 1회의 일일 투약 내지 2회의 일일 용량을 지원한다. 또한, 궁극적으로, 정상 상태에 도달하면, 대상은 투약을 절반 이하로 줄일 수 있다. 또한, CBD 경피성 겔의 유도 기간은 약 12주 내지 약 24주이며, 이는 경피 투약의 새롭고 예상치 못한 모델에 의한 것일 수 있다.
CBD는 사실상 물에 불용성이기 때문에, 가용화제로서 에탄올 및 프로필렌 글리콜을 사용할 수 있고 침투 증진제로서 디에틸렌 글리콜 모노에틸 에테르를 사용할 수 있다. CBD 경피성 겔의 알코올 함량은 약 54%(wt/wt)이다.
CBD 겔은 희석제 및 담체 뿐만 아니라 습윤제, 방부제, 및 현탁제 및 분산제와 같은 다른 통상적인 부형제를 포함할 수 있다.
CBD 겔은 가용화제, 침투 증진제, 가용화제, 항산화제, 증량제, 증점제, 및/또는 pH 조절제를 포함할 수 있다. CBD 겔의 조성은, 예를 들어, a. 조성물 중 약 0.1%(wt/wt) 내지 약 20%(wt/wt)의 양으로 존재하는 칸나비디올; b. 조성물 중 약 15%(wt/wt) 내지 약 95%(wt/wt)의 양으로 존재하는, 1개 내지 6개의 탄소 원자를 갖는 저급 알코올; c. 조성물 중 약 0.1%(wt/wt) 내지 약 20%(wt/wt)의 양으로 존재하는 제1 침투 증진제; 및 d. 조성을 총 100%(wt/wt)로 하는 데 충분한 양의 물일 수 있다. CBD 겔의 다른 배합은 국제 공개 번호 WO 2010/127033에서 찾을 수 있으며, 이의 전체 내용은 본원에 참조로 포함되어 있다.
실시예
이 연구는 성인의 초점성 뇌전증 치료를 위한 보조 요법으로서의 CBD 경피성 겔의 안전성 및 효능을 평가한다. CBD 경피성 겔은 1회 또는 2회의 일일 투약으로 제어된 약물 전달을 제공하도록 설계된 투명한, 침투성이 강화된 겔이다. 이 연구에서 4.2%(wt/wt) CBD 겔을 평가한다.
방법
초점성 뇌전증을 갖는 성인에게 12주(유지 기간) 동안 경피성 겔 BID(일일 2회)로서 투여되는 칸나비디올을 평가하는, 2상, 무작위, 이중 맹검, 위약 대조 연구인 STAR 1(Synthetic Transdermal C a nnabidiol for the T r eatment of Epilepsy)을 참조하여 연구를 수행하였다. 8주 베이스라인(베이스라인 기간) 후, 분할된 일일 용량으로 CBD 390 mg(예를 들어, 일일 2회 195 mg), 분할된 일일 용량으로 CBD 195 mg(예를 들어, 일일 2회 97.5 mg), 또는 위약으로 환자를 무작위 배정하였다(1:1:1). 분할된 일일 용량을 12시간(±2시간)마다 제공하였다. CBD 경피성 겔 및 위약을, 부위가 건조될 때까지 오른쪽 및 왼쪽 어깨 모두 및/또는 상완에 마사지하였다. 1차 효능 종점은 베이스라인에 대한 전체 치료 기간에 걸친 발작 빈도의 변화이다. 1차 효능 종점은 베이스라인 기간과 유지 기간을 비교한 28일 기간(SF28)당 발작 빈도 감소에 기초한다.
제12주 말에, 환자는 초점성 뇌전증을 갖는 성인 환자에서 390 mg의 CBD 경피성 겔을 평가하는 진행중인 STAR 2 18개월(24개월로 수정됨) 개방 표지 확대 연구에 참여할 것을 선택할 수 있었다. CBD 경피성 겔에 총 9개월 동안 노출된 데이터는 다음과 같다(STAR 1 치료 3개월 및 STAR 2 치료 6개월).
인구학적 정보 및 베이스라인 특성
환자(N = 188)를 STAR 1에 무작위 배정하였다. 평균 연령은 39세(18 내지 71)이었다. 베이스라인에서, 월간 발작의 중앙값이 10.6(3 내지 330)인 환자는 평균 2.5의 항뇌전증약(AED)을 복용하였다. 그룹별로, 베이스라인에서의 월간 발작 빈도의 중앙값은, 위약 그룹에서 10.5, 195 mg의 분할된 일일 용량 그룹에서 14.0, 및 390 mg의 분할된 용량 그룹에서 10.14이었다.
188명의 무작위로 배정된 환자 중, 186명을 효능에 대해 분석하였고, 174명이 12주 STAR 1 연구를 완료하였다. 171명의 환자(STAR 1 완료자 중 98%)는 STAR 2를 계속하였다. 환자는 중앙값이 3.0 AED인 넓은 범위의 AED를 복용하였다. 클로바잠과 CBD 사이의 알려진 상호작용으로 인해, STAR 1 및 STAR 2 연구 둘 다에서 클로바잠의 사용은 제외하였다.
효능
도 1을 참조하면, 12주의 맹검 치료 후, 초점성 발작 감소의 중앙값은, CBD 경피성 겔 195 mg/일에서 18.42%(n = 62), CBD 경피성 겔 390 mg/일에서 14.03%(n = 61), 및 위약에서 8.70%(n = 63)이었다. 195 mg/일(p = 0.431), 390 mg/일(p = 0.846) 및 위약 사이에 효능의 통계적으로 유의한 차이는 없었다. 2차 종점은 195 mg/일, 390 mg/일 및 위약의 통계적으로 유의한 차이를 나타내지 않았다. 50% 반응자 비율은 모든 치료 그룹에 걸쳐 유사하였다: 위약 = 23.8%, 195 mg/일 = 21%(p = 0.414), 및 390 mg/일 = 16.4%(p = 0.21).
도 2 및 3을 참조화면, 초점성 의식 발작(B형)을 갖는 환자 또는 초점성 의식 장애 발작(C형)을 갖는 환자에 대해, 195 mg/일, 390 mg/일 및 위약 사이에 효능의 통계적으로 유의한 차이가 없다는 것을 확인할 수 있다. 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작을 갖는 환자에 대해, 195 mg/일(p = 0.071)과 위약 사이에 통계적으로 거의 유의한 차이가 있다는 것은 예상치 못한 놀라운 것이었다. 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작을 갖는 환자에 대해, CBD 경피성 겔의 더 낮은 복용량이 더 큰 효능을 가져왔다는 것도 예상치 못한 놀라운 것이었다.
도 4를 참조하면, 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작으로부터의 결과가 흥미로운데, 여기에서 390 mg/일 그룹에 대한 22.2%의 감소 중앙값(p = 0.308) 및 위약 그룹에 대한 0.41%의 감소 중앙값과 비교하여, 195 mg/일 치료 그룹에서 60%의 감소 중앙값(p = 0.071)이 관찰되었다. CBD 경피성 겔의 더 낮은 용량이 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작에 대한 중앙값을 더 크게 감소시킬 수 있다는 것은 예상치 못한 것이었다.
STAR 1에서 위약으로부터 CBD 경피성 겔의 분리 부족은, 부분적으로, 초점성 발작이 50% 이상 감소한 15명의 위약 치료 환자(24%)로 인한 것일 수 있다; 이들 15명의 환자 중 13명은 베이스라인 발작률이 비교적 낮았다(매월 15 미만의 초점성 발작). 표 1은 대다수의 위약 "수퍼(super)" 반응자(>50%)가 여성임을 보여준다.
또한, 위약 반응자는 넓은 집단보다 토피라메이트를 복용했을 가능성이 더 크다. 표 2는 "수퍼 반응자" 및 전체 환자 집단에서 사용된 AED를 보여준다.
STAR 1에서, 195 mg/일 또는 390 mg/일의 CBD 경피성 겔을 복용한, 높은 발작 빈도(매월 15 이상의 베이스라인 발작 빈도로 정의됨)를 갖는 환자는, 위약을 복용한 높은 발작 빈도를 갖는 환자와 비교하여 더 큰 발작 감소 퍼센트를 가졌다.
171명의 환자가 STAR 2에 참여하였다.
STAR 2의 제3월에 의한 사후 분석은, STAR 1 및 STAR 2에서 CBD 경피성 겔을 투여받은 환자는(총 6개월의 CBD 경피성 겔), STAR 2에서 3개월 동안만 CBD 경피성 겔을 투여받은 환자(즉, STAR 1에서 위약을 투여받은 환자)에 비해 발작 빈도가 더 크게 감소하였다는 것을 나타내었다. 표 3을 참조한다.
* STAR 1에서의 지정된 치료. 모든 환자는 STAR 2에서 390 mg/일의 CBD 경피성 겔을 투여받았다.
또한, 9개월 동안의 CBD 경피성 겔의 사용은 더 나은 이점을 제공한다. 지속적인 치료로 효능이 유지된다. STAR 1에서 위약을 투여받고 6개월의 STAR 2를 완료한 환자는, STAR 1 동안 CBD 경피성 겔(195 mg 또는 390 mg)을 투여받은 환자보다 발작이 덜 감소되었다. 표 4를 참조한다.
* STAR 1에서의 지정된 치료. 모든 환자는 STAR 2에서 390 mg/일의 CBD 경피성 겔을 투여받았다.
STAR 2(모든 환자가 390 mg/일을 투여받음)에서 CBD 경피성 겔에 지속적으로 노출되면 발작이 임상적으로 의미있게 감소하였다. 6개월 동안(STAR 1 동안 3개월 및 STAR 2 동안 3개월) CBD 경피성 겔을 투여받은 환자는 베이스라인으로부터 30% 초과의 발작의 중앙값 감소를 겪었다. 9개월 동안(STAR 1 동안 3개월 및 STAR 2 동안 6개월) CBD 경피성 겔을 투여받은 환자는 베이스라인으로부터 65% 초과(STAR 1에서 195 mg/일 및 STAR 2에서 390 mg/일) 및 48% 초과(STAR 1 및 STAR 2에서 390 mg/일)의 발작의 중앙값 감소를 겪었다. 결과를 상기 표 4 및 도 5에 요약하였다.
초기 무작위 그룹 또는 용량에 관계없이, CBD 경피성 겔의 지속시간의 함수로서 발작 제어를 평가하였다. CBD 경피성 겔에 더 오래 노출되면, 발작의 변화 퍼센트의 중앙값이 제3월에서 -16.3%(n = 170), 제6월에서 -27.3%(n = 148), 제9월에서 -50.2%(n = 98), 및 제12월에서 -58.0%(n = 70)으로 발작 빈도가 크게 개선되었다.
표 5에 나타낸 바와 같이, CBD 경피성 겔을 6개월 동안 투여받은 환자가 가장 좋은 반응을 나타내었다.
* STAR 1에서의 지정된 치료. 모든 환자는 STAR 2에서 390 mg/일의 CBD 경피성 겔을 투여받았다.
이들 결과는, 각각의 3개월 간격마다 시간에 따른 SF28 중앙값을 나타내는 도 6에서도 확인할 수 있다. 도 6에서 확인할 수 있는 바와 같이, 2개의 비위약 그룹은 더 긴 노출로 지속적으로 개선되었다. 도 7은 STAR 2에서 제6월까지 각각의 3개월 간격마다 시간에 따른 SF28 중앙값을 도시한다. 발작 빈도의 지속적인 개선 또는 유지된 감소는 2개의 비위약 그룹에서 확인할 수 있다.
도 8은 어떠한 AED 변화도 없는 환자의 시간에 따른 SF28 중앙값을 도시한다. 도 8의 그래프는 누적 CBD 경피성 겔이 많을수록 통계적으로 유의한 결과로 효능이 커짐을 나타낸다.
사후 분석은 위약 반응자가 여성일 가능성이 높고 390 mg/일 비반응자는 가장 높은 CBD 혈장 농도를 가짐(그러나 이는 매우 가변적임)을 나타내었다. 표 6은 인구학적 정보에 따른 베이스라인부터 치료까지 위약에서의 발작률의 감소 퍼센트를 나타낸다.
분석은 또한 26세 내지 40세 환자가 가장 좋은 반응을 나타내고, 가장 나이가 적고 나이가 많은 환자는 미미하게 악화되었음을 나타내었다. 표 7은 연령에 따른 베이스라인부터 치료까지 위약에서의 발작률(SF28)의 감소 퍼센트를 나타낸다.
분석은 또한 195 mg/일 용량에서 남성만이 긍정적인 반응을 나타낸 반면, 2가지 용량에서 여성은 좋지 못한 반응을 나타낸 것을 보여주었다. 표 8은 성별에 따른 베이스라인부터 치료까지 위약에서의 발작률(SF28)의 감소 퍼센트를 나타낸다.
STAR 1에서, CBD 경피성 겔 195 mg/일의 이상 사례 비율은 49.2%이었고, CBD 경피성 겔 390 mg/일의 이상 사례 비율은 51.6%이었고, 위약의 이상 사례 비율은 41.3%이었다. 가장 흔한 이상 사례는 상기도 감염(바이러스성 및 박테리아성; 16%), 두통(11%), 피로(7%), 및 열상(5%)이었다. CBD 경피성 겔 환자의 5% 초과에서, 위약에서보다 더 많이 발생하는 2가지의 치료 관련 이상 사례는 피로(CBD 경피성 겔에 대해 5.6%; 위약에 대해 1.6%) 및 두통(CBD 경피성 겔에 대해 5.6%; 위약에 대해 3.2%)이었다. CBD의 혈장 수준은 용량 비례적이지만, 혈장 수준과 효능 사이에는 상관관계가 없었다.
제4주와 제8주 사이에 제4주 양 25% 반응자에서의 혈장 농도 중앙값은 비반응자에 비해 더 낮았지만, 그 차이는 미미하였다. 제8주와 제12주 사이에 반응자와 비반응자 사이의 제8주에서의 농도 중앙값은 차이가 없었다. 4명의 대상에서의 252 mg BID 용량을 포함하는 연구에서 Cmax는 시뮬레이션한 Cmax(PopPK 모델)보다 더 높았지만, 둘 다 정확한 Cmax를 나타내는 동일한 개연성을 보여준다. CBD 경피성 겔의 대상 사이의 약동학적 가변성은 경피성 제품에 대한 예상 범위 내에 있다.
STAR 2에서 소수의 환자는 백그라운드 AED가 증가하였다. STAR 2에서 관찰된 발작 빈도의 개선은 백그라운드 AED의 이러한 변화로 인한 것이 아니었다. 이는 AED 변화가 없는 환자들 사이의 반응을 도시하는 도 8과 모든 환자를 포함하는 도 7의 비교에서 확인할 수 있다. 확인할 수 있는 바와 같이, 이들 두 수치는 매우 유사하다.
안전성
CBD 경피성 겔은 위약에 필적하여, 이상 사례의 발생률에 대해 매우 내약성이 우수하였으며, 활성 치료 그룹 사이에 임상적으로 유의한 차이가 없었다. CBD 경피성 겔의 안전성 프로파일은 1상 및 2상 시험의 데이터와 일치하였다. CBD 경피성 겔을 투여받은 환자의 ECG 또는 실험실 결과에서 임상적으로 유의한 변화가 없었다. 또한, CBD 경피성 겔은 피부 홍반을 최소화하는 우수한 피부 내약성을 가졌다.
결과 요약
STAR 1의 베이스라인 기간으로부터의 초점성 발작의 감소로 측정된, CBD 경피성 겔에 대한 임상적으로 유의한 반응은 CBD 경피성 겔로의 지속적인 치료와 관련있다. 총 9개월 동안 CBD 경피성 겔을 투여받은(3개월 동안의 STAR 1에서 195 mg/일 및 STAR 2에서 6개월 동안 390 mg/일) 환자는 65%의 발작 감소 중앙값을 달성하였다. CBD 경피성 겔을 투여받은(STAR 1에서 3개월 및 STAR 2에서 6개월 동안 390 mg/일) 환자는 베이스라인으로부터 48%의 발작 감소 중앙값을 달성하였다. 또한, CBD 경피성 겔은 9개월의 노출을 통해 매우 내약성이 우수한 것으로 나타났다.
CBD 경피성 겔로의 지속적인 치료와 STAR 1의 베이스라인 기간으로부터의 초점성 발작의 감소의 상관관계는 12개월 동안 지속되는 것으로 밝혀졌다. 도 9는 STAR 2에서 CBD 경피성 겔로 치료된 모든 환자에 대한 제3월, 제6월, 제9월, 및 제12월에서의 발작률 변화(%)의 중앙값을 도시한다. 도 10은 STAR 1에서 위약 또는 CBD 경피성 겔(195 mg 및 390 mg)로 치료된 환자에 대한 제3월, 제6월, 제9월, 및 제12월에서의 발작률 변화(%)의 중앙값을 도시한다. 도 9 및 10에서 확인할 수 있는 바와 같이, CBD 경피성 겔에 더 오래 노출되면, STAR 1에서 원래 무작위 배정된 CBD 용량에 의해 검사되는 경우를 포함하여(도 10), 모든 CBD 경피성 겔 환자에서(도 9) 발작 빈도가 더 크게 개선된다.
데이터는 성인의 초점성 발작이 약학적으로 제조된 칸나비디올의 경피성 겔 전달에 의해 효과적으로 치료될 수 있음을 입증한다. 이러한 환자 집단에서, CBD 경피성 겔로의 지속적인 치료는 베이스라인과 비교하여 발작률을 상당히 감소시키는 것으로 나타났다. 중요하게도, 베이스라인 발작 빈도는 반응의 중요한 지표인 것으로 보인다. 데이터는 CBD 경피성 겔이 약물 내성 뇌전증을 앓는 성인의 초점성 발작에 영향을 줄 수 있음을 입증한다. 최적의 내약성 프로파일을 갖는 CBD 기반 치료의 가능성은 이들 환자에게 중요할 것이다.
수정된 STAR 2 시험
관찰된 결과에 기초하여, 다양한 용량의 CBD 경피성 겔의 적정을 가능하게 하기 위해 STAR 2 임상 시험의 프로토콜을 수정하였다. 새로운 프로토콜은 의사가 195 mg/일, 390 mg/일, 585 mg/일 또는 780 mg/일의 CBD 경피성 겔을 처방할 수 있게 한다. 수정된 프로토콜은 의사가 CBD 경피성 겔의 용량을 늘이거나 줄이는 적정을 할 수 있게 한다.
수정된 STAR 2 시험에서, 모든 환자는 12시간(±2시간)마다 195 mg의 CBD 경피성 겔로 시작하며(390 mg/일), 1개월 후 CBD 경피성 겔의 용량을 증가시키거나 감소시키는 옵션이 있다. 용량은 12시간(±2시간)마다 292.5 mg으로 증가할 수 있다(585 mg/일). 585 mg/일 용량에서 1개월 후, 용량은 12시간(±2시간)마다 390 mg으로 다시 증가할 수 있다(780 mg/일).
1개월 후, CBD 경피성 겔 복용량은 12시간(±2시간)당 97.5 mg로 감소할 수 있다(195 mg/일). 일일 용량으로 195 mg을 투여받는 환자에 대하여, 용량을 다시 390 mg/일로 늘리고 최대 585 mg/일까지 늘리는 옵션이 있다.
CBD 경피성 겔의 용량이 증가하거나 감소할 때마다, 용량이 다시 바뀌기 전에, 정상 상태를 달성하기 위해 환자는 1개월 동안 그 용량을 유지한다.
Claims (28)
- 뇌전증을 갖는 대상의 발작 빈도를 감소시키는 방법으로서, 상기 대상에게 칸나비디올(CBD)의 유효량을 경피 투여하는 것을 포함하고, 발작 빈도가 감소하는 것인 방법.
- 제1항에 있어서, 발작 빈도가 30% 감소하는 것인 방법.
- 제1항에 있어서, 발작 빈도가 50% 감소하는 것인 방법.
- 제1항에 있어서, 성인의 초점성 발생 발작이 감소하는 것인 방법.
- 제1항에 있어서, 초점성 의식 발작이 감소하는 것인 방법.
- 제1항에 있어서, 초점성 의식 장애 발작이 감소하는 것인 방법.
- 제1항에 있어서, 전신 강직 간대 발작을 동반한 초점성 의식 장애 발작이 감소하는 것인 방법.
- 제1항에 있어서, 대상이 높은 발작 빈도를 갖는 것인 방법.
- 제1항에 있어서, 뇌전증은 약물 내성 뇌전증인 방법.
- 제1항에 있어서, 레베티라세탐, 카바마제핀, 토피라메이트, 라모트리진, 라코사미드, 클로나제팜, 발프로에이트, 클로바잠, 페니토인, 에슬리카바제핀, 및 옥스카바제핀으로 이루어진 군으로부터 선택되는 1종 이상의 항뇌전증약을 투여하는 방법.
- 제1항에 있어서, CBD는 (-)-CBD인 방법.
- 제1항에 있어서, CBD의 유효량은 일일 총 약 195 mg 내지 약 780 mg인 방법.
- 제1항에 있어서, CBD의 유효량은 분할된 일일 용량으로 195 mg인 방법.
- 제1항에 있어서, CBD의 유효량은 분할된 일일 용량으로 390 mg인 방법.
- 제1항에 있어서, CBD의 유효량은 분할된 일일 용량으로 585 mg인 방법.
- 제1항에 있어서, CBD의 유효량은 분할된 일일 용량으로 780 mg인 방법.
- 제1항에 있어서, CBD의 유효량이 97.5 mg 일회용 사셰로 제공되는 것인 방법.
- 제1항에 있어서, CBD의 유효량이 195 mg 일회용 사셰로 제공되는 것인 방법.
- 제1항에 있어서, CBD의 유효량이 390 mg 일회용 사셰로 제공되는 것인 방법.
- 제1항에 있어서, CBD가 겔로 제제화되는 것인 방법.
- 제20항에 있어서, CBD가 침투 강화 겔로 제제화되는 것인 방법.
- 제1항에 있어서, CBD가 단회의 일일 용량으로 투여되는 것인 방법.
- 제1항에 있어서, CBD가 2회의 일일 용량으로 투여되는 것인 방법.
- 제1항에 있어서, CBD는 합성 CBD인 방법.
- 제1항에 있어서, CBD는 순수 CBD인 방법.
- 제1항에 있어서, CBD의 유효량을 경피 투여하는 것이 CBD를 경구 투여하는 것에 비해 하나 이상의 이상 사례의 강도를 감소시키는 것인 방법.
- 제26항에 있어서, 하나 이상의 이상 사례는 졸림, 정신활성 효과, 간 기능, 및 GI 관련 이상 사례로 이루어진 군으로부터 선택되는 것인 방법.
- 제1항에 있어서, 대상은 성인인 방법.
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762560446P | 2017-09-19 | 2017-09-19 | |
| US62/560,446 | 2017-09-19 | ||
| US201762593575P | 2017-12-01 | 2017-12-01 | |
| US62/593,575 | 2017-12-01 | ||
| US201862613160P | 2018-01-03 | 2018-01-03 | |
| US62/613,160 | 2018-01-03 | ||
| US201862652995P | 2018-04-05 | 2018-04-05 | |
| US62/652,995 | 2018-04-05 | ||
| US201862660198P | 2018-04-19 | 2018-04-19 | |
| US62/660,198 | 2018-04-19 | ||
| PCT/IB2018/057189 WO2019058261A1 (en) | 2017-09-19 | 2018-09-18 | TRANSDERMAL SYNTHETIC CANNABIDIOL FOR THE TREATMENT OF FOCAL EPILEPSY IN ADULTS |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200055067A true KR20200055067A (ko) | 2020-05-20 |
Family
ID=63762572
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207011219A KR20200055067A (ko) | 2017-09-19 | 2018-09-18 | 성인의 초점성 뇌전증의 치료를 위한 합성 경피성 칸나비디올 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US20190083388A1 (ko) |
| EP (1) | EP3684411A1 (ko) |
| JP (2) | JP2020534362A (ko) |
| KR (1) | KR20200055067A (ko) |
| AU (1) | AU2018337933A1 (ko) |
| BR (1) | BR112020004947A2 (ko) |
| CA (1) | CA3075719A1 (ko) |
| IL (2) | IL301910A (ko) |
| JO (1) | JOP20200045A1 (ko) |
| MX (1) | MX2020003004A (ko) |
| WO (1) | WO2019058261A1 (ko) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3733156A1 (de) * | 2019-05-02 | 2020-11-04 | Gábor Fóti | C.b.d.m therapie |
| JP2022547136A (ja) * | 2019-09-17 | 2022-11-10 | ジナーバ・ファーマシューティカルズ・インコーポレイテッド | 発達性及びてんかん性脳症における行動障害の治療 |
| EP4041209A4 (en) * | 2019-10-11 | 2024-01-24 | Pike Therapeutics Inc | TRANSDERMAL COMPOSITIONS CONTAINING CANNABIDIOL (CBD) FOR USE IN THE TREATMENT OF SEIZURE DISORDERS |
| GB2597287A (en) * | 2020-07-20 | 2022-01-26 | Gw Res Ltd | Use of cannabidiol in the treatment of seizures associated with rare epilepsy syndromes related to structural abnormalities of the brain |
| CA3187588A1 (en) * | 2020-08-17 | 2022-02-24 | Fotios M. Plakogiannis | Transdermal pharmaceutical formulations of cannabinoids |
| EP4319730A1 (en) * | 2021-04-08 | 2024-02-14 | Pike Therapeutics, Inc. | Pharmaceutical composition and method for treating seizure disorders |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5801794B2 (ja) | 2009-04-28 | 2015-10-28 | ジネルバ ファーマシューティカルズ, インコーポレイティド | カンナビジオールの製剤及びその使用方法 |
| ES2635084T3 (es) * | 2009-08-31 | 2017-10-02 | Zynerba Pharmaceuticals, Inc. | Uso de profármacos de cannabidiol en administración tópica y transdérmica con microagujas |
| GB2530001B (en) * | 2014-06-17 | 2019-01-16 | Gw Pharma Ltd | Use of cannabidiol in the reduction of convulsive seizure frequency in treatment-resistant epilepsy |
| GB2541191A (en) * | 2015-08-10 | 2017-02-15 | Gw Pharma Ltd | Use of cannabinoids in the treatment of epilepsy |
-
2018
- 2018-09-18 CA CA3075719A patent/CA3075719A1/en active Pending
- 2018-09-18 JO JOP/2020/0045A patent/JOP20200045A1/ar unknown
- 2018-09-18 US US16/133,930 patent/US20190083388A1/en not_active Abandoned
- 2018-09-18 BR BR112020004947-6A patent/BR112020004947A2/pt unknown
- 2018-09-18 AU AU2018337933A patent/AU2018337933A1/en active Pending
- 2018-09-18 IL IL301910A patent/IL301910A/en unknown
- 2018-09-18 EP EP18782520.3A patent/EP3684411A1/en active Pending
- 2018-09-18 KR KR1020207011219A patent/KR20200055067A/ko not_active Application Discontinuation
- 2018-09-18 MX MX2020003004A patent/MX2020003004A/es unknown
- 2018-09-18 JP JP2020537297A patent/JP2020534362A/ja active Pending
- 2018-09-18 WO PCT/IB2018/057189 patent/WO2019058261A1/en unknown
-
2020
- 2020-02-20 IL IL272818A patent/IL272818A/en unknown
- 2020-08-18 US US16/996,082 patent/US20210030665A1/en not_active Abandoned
-
2023
- 2023-09-08 JP JP2023145851A patent/JP2023171776A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU2018337933A1 (en) | 2020-03-12 |
| MX2020003004A (es) | 2020-11-06 |
| EP3684411A1 (en) | 2020-07-29 |
| JP2023171776A (ja) | 2023-12-05 |
| US20210030665A1 (en) | 2021-02-04 |
| CA3075719A1 (en) | 2019-03-28 |
| US20190083388A1 (en) | 2019-03-21 |
| IL301910A (en) | 2023-06-01 |
| IL272818A (en) | 2020-04-30 |
| WO2019058261A9 (en) | 2019-07-04 |
| JOP20200045A1 (ar) | 2020-02-27 |
| JP2020534362A (ja) | 2020-11-26 |
| WO2019058261A1 (en) | 2019-03-28 |
| BR112020004947A2 (pt) | 2020-09-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20200055067A (ko) | 성인의 초점성 뇌전증의 치료를 위한 합성 경피성 칸나비디올 | |
| McElroy et al. | Open-label adjunctive zonisamide in the treatment of bipolar disorders: a prospective trial. | |
| AU2021202956A1 (en) | Method of treatment with tradipitant | |
| JP6353577B2 (ja) | 組み合わせ組成物 | |
| AU2016255707A1 (en) | Uses of cannabidiol for treatment of infantile spasms | |
| US20240148669A1 (en) | Methods of treatment of osteoarthritis with transdermal cannabidiol gel | |
| CA2735834C (en) | Composition comprising ibuprofen and paracetamol to treat pain caused by osteoarthritis and rheumatoid arthritis | |
| JP2023552390A (ja) | 難治性発作の治療 | |
| Hattori et al. | Clinical evaluation of ropinirole controlled-release formulation at 18–24 mg/day in Japanese patients with Parkinson's disease | |
| RU2369393C2 (ru) | Применение окскарбазепина для лечения диабетической нейропатической боли и для улучшения сна | |
| US20190134063A1 (en) | Compositions and Methods for the Treatment of Skin Lesions | |
| IL230174A (en) | Pharmaceutical composition for the treatment of premature ejaculation | |
| KR20230137404A (ko) | Cbd를 사용한 수면 무호흡증의 치료 | |
| Kappos et al. | Uses | |
| US20170354667A1 (en) | Composition and method for treating bipolar disorder |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal |