KR20180098412A - 종양의 심층 서열분석 프로파일링 - Google Patents
종양의 심층 서열분석 프로파일링 Download PDFInfo
- Publication number
- KR20180098412A KR20180098412A KR1020187023352A KR20187023352A KR20180098412A KR 20180098412 A KR20180098412 A KR 20180098412A KR 1020187023352 A KR1020187023352 A KR 1020187023352A KR 20187023352 A KR20187023352 A KR 20187023352A KR 20180098412 A KR20180098412 A KR 20180098412A
- Authority
- KR
- South Korea
- Prior art keywords
- sample
- sequencing
- genomic material
- capture
- amplification
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6869—Methods for sequencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6806—Preparing nucleic acids for analysis, e.g. for polymerase chain reaction [PCR] assay
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6869—Methods for sequencing
- C12Q1/6874—Methods for sequencing involving nucleic acid arrays, e.g. sequencing by hybridisation
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2527/00—Reactions demanding special reaction conditions
- C12Q2527/146—Concentration of target or template
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2531/00—Reactions of nucleic acids characterised by
- C12Q2531/10—Reactions of nucleic acids characterised by the purpose being amplify/increase the copy number of target nucleic acid
- C12Q2531/113—PCR
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Physics & Mathematics (AREA)
- Immunology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Genetics & Genomics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Orthopedics, Nursing, And Contraception (AREA)
- Respiratory Apparatuses And Protective Means (AREA)
- Prostheses (AREA)
Abstract
Description
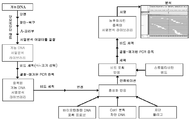
도 1은 2회의 증폭 단계를 도입하는 서열 포획 작업흐름을 기재한다.
도 2는 개시된 서열 포획 방법과 비교한 전통적인 서열 포획 방법의 비교를 제공한다.
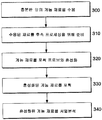
도 3a는 개시된 서열 포획 방법의 단계들을 예시하는 흐름도를 기재하고, 특히 증폭 단계가 서열분석 이전에 수행되지 않는다.
도 3b는 개시된 서열 포획 방법의 단계들을 예시하는 흐름도를 기재하고, 특히 선택적 증폭 단계가 서열분석 이전에 수행될 수 있다.
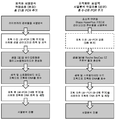
도 4는 개시된 표적화된 표상적 서열분석 작업흐름과 비교하여 전통적인 표적화된 서열분석 작업흐름의 추가 비교를 제공한다. 현행의 표적화된 서열분석 프로토콜 (좌측 컬럼), 예컨대 바이오틴화된 포획 올리고뉴클레오티드와의 혼성화에 의존적인 것들은 작업흐름 동안 샘플 DNA 질량을 증가시키기 위해 많은 PCR 증폭 주기 (이 예에서는 총 21회 주기)를 도입한다. 표적화된 표상적 서열분석 작업흐름 (우측 컬럼)은 본 명세서의 다른 구체예에 도시되거나 (0-2회의 증폭 주기) 또는 기술된 바와 같은 작업흐름 동안 전체 증폭을 감소시킨다. 작업흐름에서 PCR 증폭 단계는 흰색 박스로 표시된다.
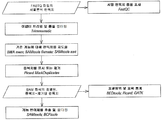
도 5는 기본 SeqCap EZ 서열 포획 데이타 분석 작업흐름의 개략도를 도시한다. 서열 포획 실험으로부터의 서열분석 판독치는 광범위하게 사용되는 "FASTQ" 파일 형식으로 체계화된다. 서열 판독 품질은 데이타가 분석을 계속하는데 충분한 품질인지를 결정하기 위해 프로그램 "FastQC"를 사용하여 평가한다. 임의의 서열분석 어댑터 및 불충분한 품질 판독치는 나머지 판독치를 프로그램 "BWA mem"을 사용하여 기준 게놈에 대해 효율적으로 지도화시킬 수 있도록 프로그램 "Trimmomatic"을 사용하여 필터링된다. "SAMtools fixmate" 프로그램은 쌍형성된 양쪽 판독치에 대해 일관적인 정보가 보이도록 보장한다. "SAMtools sort" 프로그램이 이후에 사용되어 게놈 분류 순서에 따라서 출력 파일을 정리한다. 지도화 이후, "Picard MarkDuplicates" 명령을 사용하여 변이체 호출 중 대립유전자 증폭 편향성을 방지하기 위해 PCR 중복을 제거하거나 또는 표시한다. 증폭 연관된 중복이 제거된 지도화된 판독치를 이후에 후속 분석을 위해 "BAM" 형식으로 전환시킨다. 서열 포괄범위 및 포획 통계를 프로그램 "BEDtools", "Picard", 및 "GATK"를 사용하여 생성시키면서 게놈 서열 변이체를 "SAMtools" 및 "BCFtools"을 사용하여 호출하고 필터링한다. 이들 방법의 상세한 설명은 "How to Evaluate NimbleGen SeqCap EZ Target Enrichment Data"라는 명칭의 Roche 기술 노트 문서에 기술되어 있다 (8월 25일, 이 개시내용은 그 전문을 본 명세서에 참조로 포함함).
도 6은 게놈에 대해 지도화되고 포획 표적 ("표적 상 (On-target)")에 대해 정렬되거나, 또는 포획 표적의 100 염기쌍 이내 ("표적 근처 (Near Target)")에 위치된 모든 비중복 서열분석된 염기의 백분율이 0, 1, 2, 4, 6, 10 또는 14회 주기의 포획 후 증폭을 이용했는지에 따라 실질적으로 상이하지 않다는 것을 보여준다. 도시된 어떠한 실험도 포획 전 증폭 단계를 포함하지 않았다. 표적 상 또는 표적 근처에 있는 서열분석된 염기를 사용하여 포획 실험에서 서열 변이체를 확인하였다. 실험에서 표적 상 또는 표적 근처 염기의 백분율의 감소는 서열 변이체를 확인하기 위해 유용한 데이타의 동일한 절대량을 획득하기 위해 값비싼 추가의 보충적인 서열분석이 필요할 수 있다. 증폭을 명시하는 프로토콜과 비교하여, 양호한 표적 상 비율을 유지하기 위한 증폭-비포함 포획 프로토콜의 예상치않은 수용력은, 보충적인 서열분석에 대한 비용 상승의 발생 없이 증폭 단계에 대한 비용 절감 및 시간 절약을 촉진할 것이라는 것을 시사한다.
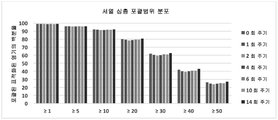
도 7은 일부 최소 판독 심도 (≥1, ≥5, ≥10, ≥20, ≥30, ≥40, 및 ≥50)로 포괄되는 포획 표적을 포함하는 모든 염기의 백분율은 실험이 0, 1, 2, 4, 6, 10 또는 14회 주기의 포획 후 증폭을 이용하는지 간에 실질적으로 상이하지 않았음을 보여준다. 서열 심도 포괄 분포는 전체 포획 표적 전체에서 서열 변이체를 검출하기 위한 검정의 감도의 핵심 결정인자이다. 따라서, 데이타는 증폭-비포함 포획 프로토콜이 증폭을 명시하는 포획 프로토콜과 유사하게 서열 변이체를 검출하는 감도를 가져야한다는 것을 시사한다.
도 8은 반수체 게놈 크기 (∼3,000,000,000 염기쌍)를 포획 표적 크기 (4,571,289 염기쌍)로 나누고 포획 표적 내에 지도화된 서열분석된 염기의 백분율을 곱해서 계산된 (전체 7회 실험의 평균 = 0.667), 전체 기준 게놈에 대한 포획 표적 중 서열의 농축 배수를 도시한다.
도 9는 기준 게놈의 서열 대비, 도 5에 기술된 데이타 분석 파이프라인에 의해 호출된 단일 뉴클레오티드 다형성 (SNP)의 총 개수를 도시한다. 데이타는 증폭-비포함 포획 프로토콜이 증폭을 명시하는 포획 프로토콜과 비교하여 유사한 개수의 SNP를 생성시켰음을 시사한다.
도 10은 수행한 포획 실험에서 확인된 이러한 특정 DNA 샘플 (NA1281, 국제 HapMap 프로젝트에 의해 이전에 유전자형 분석됨)의 포획 표적에 존재하는 것으로 알려진 SNP의 백분율을 보여준다. 0.903 내지 0.919 범위의 감도가 모든 7회 실험 중에서 계산되었고, PCR-비포함 포획 프로토콜의 감도는 0.911로 계산되어, 다른 것들 중에서 중간이었다.
도 11은 7회 포획 실험에서 SNP 분류의 특이성을 도시한다. 샘플 (NA12891)에서 검출된 공지된 변이체들의 경우, SNP 분류의 특이성은 올바른 접합성 (동형접합 대 이형접합)을 갖는 백분율로서 정의된다. SNP 분류의 특이성의 감소는 증폭-관련 대립유전자 편향성의 예측 결과이다 (예를 들어, 이형접합 유전자형이 아마도 더 동형접합 유전자형으로서 나타날 수 있음). 증폭-비포함 포획 프로토콜은 정의상, 증폭-관련 대립유전자 편향성의 부재와 일관되게, 증폭을 명시하는 포획 프로토콜과 유사하거나 또는 그를 초과하는 SNP 분류의 특이성을 입증하였다.
Claims (50)
- 샘플 내 게놈 재료를 서열분석하는 방법으로서, 종양 샘플 및/또는 림프절 샘플을 균질화하여 균질화된 샘플을 제공하는 단계; 균질화된 샘플로부터 적어도 0.5 마이크로그램의 게놈 재료를 단리하는 단계; 서열분석을 위해 적어도 0.5 마이크로그램의 단리된 게놈 재료를 제조하는 단계; 및 제조된 게놈 재료를 서열분석하는 단계를 포함하는, 샘플 내 게놈 재료의 서열분석 방법.
- 제1항에 있어서, 서열분석 이전에 임의의 증폭 단계를 포함하지 않는, 샘플 내 게놈 재료의 서열분석 방법.
- 제1항에 있어서, 적어도 하나의 포획 전 또는 포획 후 증폭 단계를 포함하고, 적어도 하나의 포획 전 또는 포획 후 증폭 단계 동안 수행되는 증폭 주기의 총 횟수는 최대 4회 주기인, 샘플 내 게놈 재료의 서열분석 방법.
- 제3항에 있어서, 증폭 주기의 총 횟수가 3회인, 샘플 내 게놈 재료의 서열분석 방법.
- 제3항에 있어서, 증폭 주기의 총 횟수가 2회인, 샘플 내 게놈 재료의 서열분석 방법.
- 제1항에 있어서, 서열분석을 위해 적어도 0.5 마이크로그램의 단리된 게놈 재료를 제조하는 단계가 적어도 0.5 마이크로그램의 단리된 게놈을 포획 프로브와 혼성화시키고 혼성화된 게놈 재료를 포획하는 단계를 포함하는, 샘플 내 게놈 재료의 서열분석 방법.
- 제6항에 있어서, 포획된 게놈 재료의 양이 약 90 ng 내지 약 900 ng 범위인, 샘플 내 게놈 재료의 서열분석 방법.
- 제6항에 있어서, 1회 또는 2회의 증폭 주기가 포획된 게놈 재료에 대해 수행되는, 샘플 내 게놈 재료의 서열분석 방법.
- 제1항에 있어서, 균질화된 샘플이 세포의 대표적인 샘플링 (sampling)을 포함하는, 샘플 내 게놈 재료의 서열분석 방법.
- 제1항에 있어서, 적어도 1 마이크로그램의 게놈 재료가 균질화된 샘플로부터 단리되는, 샘플 내 게놈 재료의 서열분석 방법.
- 제1항에 있어서, 적어도 5 마이크로그램의 게놈 재료가 균질화된 샘플로부터 단리되는, 샘플 내 게놈 재료의 서열분석 방법.
- 제1항에 있어서, 적어도 10 마이크로그램의 게놈 재료가 균질화된 샘플로부터 단리되는, 샘플 내 게놈 재료의 서열분석 방법.
- 샘플 내 DNA를 서열분석하는 방법으로서, 적어도 0.5 마이크로그램의 DNA를 혈액 샘플로부터 단리하는 단계; 서열분석을 위해 적어도 0.5 마이크로그램의 단리된 DNA를 제조하는 단계; 및 제조된 DNA를 서열분석하는 단계를 포함하는, 샘플 내 DNA의 서열분석 방법.
- 제13항에 있어서, 서열분석 이전에 0회의 증폭 단계를 포함하는, 샘플 내 DNA의 서열분석 방법.
- 제13항에 있어서, 서열분석을 위해 적어도 0.5 마이크로그램의 단리된 DNA를 제조하는 단계가 적어도 0.5 마이크로그램의 단리된 게놈을 포획 프로브와 혼성화시키고 혼성화된 게놈 재료를 포획하는 단계를 포함하는, 샘플 내 DNA의 서열분석 방법.
- 제15항에 있어서, 포획된 게놈 재료의 양이 약 90 ng 내지 약 900 ng 범위인, 샘플 내 DNA의 서열분석 방법.
- 제15항에 있어서, 1회 또는 2회의 증폭 주기가 포획된 게놈 재료에 대해 수행되는, 샘플 내 DNA의 서열분석 방법.
- 제13항에 있어서, 적어도 1 마이크로그램의 DNA가 혈액 샘플로부터 단리되는, 샘플 내 DNA의 서열분석 방법.
- 표적화된 표상적 (representational) 서열분석 방법으로서, (i) 적어도 종양의 일부분, 하나 이상의 전체 또는 부분 림프절, 또는 이의 임의 조합을 균질화하여 균질화된 샘플을 제공하는 단계; (ii) 균질화된 샘플로부터 게놈 재료를 추출하는 단계; (iii) 추출된 게놈 재료를 비드 상에서 포획하는 단계; 및 (iv) 포획된 게놈 재료를 서열분석하는 단계를 포함하고, 표적화된 표상적 서열분석이 포획된 게놈 재료의 서열분석 이전에 최대 4회의 증폭 주기를 수행하는 단계를 포함하는, 표적화된 표상적 서열분석 방법.
- 제19항에 있어서, 최대 4회의 증폭 주기가 추출된 게놈 재료의 포획 이전 또는 추출된 게놈 재료의 포획 이후, 또는 이의 임의 조합에서 수행될 수 있는, 표적화된 표상적 서열분석 방법.
- 제19항에 있어서, 포획 전 증폭 주기가 수행되지 않는, 표적화된 표상적 서열분석 방법.
- 제21항에 있어서, 포획된 게놈 재료의 양이 약 90 ng 내지 약 900 ng 범위인, 표적화된 표상적 서열분석 방법.
- 제19항에 있어서, 1회 내지 3회의 증폭 주기가 추출된 게놈 재료의 포획 이후, 그러나 서열분석 이전에 수행되는, 표적화된 표상적 서열분석 방법.
- 제19항에 있어서, 적어도 1 마이크로그램의 게놈 재료가 균질화된 샘플로부터 추출되는, 표적화된 표상적 서열분석 방법.
- 제19항에 있어서, 4회 초과의 증폭 주기를 요구하는 서열분석 방법에서 사용되는 투입 재료의 양과 비교하여, 적어도 100배 더 많은 게놈 재료가 균질화된 샘플로부터 유래되는, 표적화된 표상적 서열분석 방법.
- 샘플 내 DNA를 서열분석하는 방법으로서, 적어도 0.5 마이크로그램의 게놈 재료를 투입 샘플로부터 단리하는 단계 (투입 샘플은 종양 샘플, 림프절 샘플, 혈액 샘플 또는 이의 임의 조합으로부터 유래됨); 서열분석을 위해 단리된 게놈 재료를 제조하는 단계; 및 제조된 게놈 재료를 서열분석하는 단계를 포함하고, 임의의 증폭 단계를 포함하지 않는, 샘플 내 DNA의 서열분석 방법.
- 제26항에 있어서, 적어도 0.5 마이크로그램의 게놈 재료가 다수의 조직학 및/또는 생검 표본으로부터 유래되는, 샘플 내 DNA의 서열분석 방법.
- 제26항에 있어서, 적어도 0.5 마이크로그램의 게놈 재료가 균질화된 종양 샘플로부터 유래되는, 샘플 내 DNA의 서열분석 방법.
- 제26항에 있어서, 적어도 0.5 마이크로그램의 게놈 재료가 균질화된 림프절 샘플로부터 유래되는, 샘플 내 DNA의 서열분석 방법.
- 제26항에 있어서, 적어도 0.5 마이크로그램의 게놈 재료가 그것이 유래되는 종양 샘플, 림프절 샘플, 또는 혈액 샘플의 대표적인 샘플링인, 샘플 내 DNA의 서열분석 방법.
- 제26항에 있어서, 서열분석이 차세대 서열분석 방법을 사용하여 수행되는, 샘플 내 DNA의 서열분석 방법.
- 제26항에 있어서, 서열분석이 합성 서열분석 방법론을 사용하여 수행되는, 샘플 내 DNA의 서열분석 방법.
- 서열분석 동안 PCR-도입된 돌연변이를 감소시키는 방법으로서, 게놈 재료의 충분한 양을 포함하는 샘플로부터 DNA를 단리하는 단계; 서열분석을 위해 단리된 DNA를 제조하는 단계; 및 제조된 DNA를 서열분석하는 단계를 포함하고, 서열분석 이전에 최대 3회의 증폭 주기를 포함하는, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 서열분석 이전에 1회 또는 2회의 증폭 주기를 포함하는, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 투입 게놈 재료의 충분한 양이 포획 전 증폭 주기를 이용하지 않게 하는 양인, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 샘플이 암을 갖는 것으로 의심되는 환자로부터 유래되는, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 샘플이 암으로 진단받은 환자로부터 유래되는, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 샘플이 암이 발생될 위험성이 있는 환자로부터 유래되는, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 샘플이 건강한 조직 샘플로부터 유래되는, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 약 0.5 마이크로그램의 DNA가 샘플로부터 단리되는, PCR-도입된 돌연변이 감소 방법.
- 제33항에 있어서, 적어도 0.5 마이크로그램의 DNA가 샘플로부터 단리되는, PCR-도입된 돌연변이 감소 방법.
- 특정 처치 또는 활성 약학 성분에 반응하는 암 아형을 확인하여 암을 치료하는 방법으로서, 암 아형이 종양, 림프절, 또는 혈액의 대표적인 샘플링을 포함하는 투입 샘플을 서열분석하여 확인되고, 투입 샘플이 게놈 재료의 충분한 양을 포함하며, 최대 4회의 증폭 주기가 서열분석 이전에 수행되는, 암 치료 방법.
- 제42항에 있어서, 최대 3회의 증폭 주기가 서열분석 이전에 수행되는, 암 치료 방법.
- 제42항에 있어서, 최대 2회의 증폭 주기가 서열분석 이전에 수행되는, 암 치료 방법.
- 제42항에 있어서, 최대 1회의 증폭 주기가 서열분석 이전에 수행되는, 암 치료 방법.
- 제42항에 있어서, 0회의 증폭 주기가 서열분석 이전에 수행되는, 암 치료 방법.
- 제42항에 있어서, 게놈 재료의 양이 적어도 0.5 마이크로그램인, 암 치료 방법.
- 제42항에 있어서, 게놈 재료의 양이 적어도 1 마이크로그램인, 암 치료 방법.
- 제42항에 있어서, 게놈 재료의 양이 적어도 5 마이크로그램인, 암 치료 방법.
- 제42항에 있어서, 게놈 재료의 양이 적어도 10 마이크로그램인, 암 치료 방법.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662279126P | 2016-01-15 | 2016-01-15 | |
| US62/279,126 | 2016-01-15 | ||
| US201662415952P | 2016-11-01 | 2016-11-01 | |
| US62/415,952 | 2016-11-01 | ||
| PCT/US2016/060835 WO2017123316A1 (en) | 2016-01-15 | 2016-11-07 | Deep sequencing profiling of tumors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20180098412A true KR20180098412A (ko) | 2018-09-03 |
| KR102398465B1 KR102398465B1 (ko) | 2022-05-13 |
Family
ID=57396824
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187023352A Active KR102398465B1 (ko) | 2016-01-15 | 2016-11-07 | 종양의 심층 서열분석 프로파일링 |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US11649492B2 (ko) |
| EP (1) | EP3402896B1 (ko) |
| JP (2) | JP7232643B2 (ko) |
| KR (1) | KR102398465B1 (ko) |
| CN (1) | CN108463559A (ko) |
| AU (1) | AU2016386032B2 (ko) |
| CA (1) | CA3011342C (ko) |
| IL (1) | IL260304B2 (ko) |
| SA (1) | SA518392005B1 (ko) |
| SG (1) | SG11201805600VA (ko) |
| WO (1) | WO2017123316A1 (ko) |
| ZA (1) | ZA201804322B (ko) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2986436T3 (es) | 2011-04-15 | 2024-11-11 | Univ Johns Hopkins | Sistema de secuenciación segura |
| ES2886507T5 (es) | 2012-10-29 | 2024-11-15 | Univ Johns Hopkins | Prueba de Papanicolaou para cánceres de ovario y de endometrio |
| US11286531B2 (en) | 2015-08-11 | 2022-03-29 | The Johns Hopkins University | Assaying ovarian cyst fluid |
| SG11201805600VA (en) * | 2016-01-15 | 2018-07-30 | Ventana Med Syst Inc | Deep sequencing profiling of tumors |
| CN111868260B (zh) | 2017-08-07 | 2025-02-21 | 约翰斯霍普金斯大学 | 用于评估和治疗癌症的方法和材料 |
| US20200004928A1 (en) | 2018-06-29 | 2020-01-02 | Roche Sequencing Solutions, Inc. | Computing device with improved user interface for interpreting and visualizing data |
| CN109234356B (zh) * | 2018-09-18 | 2021-10-08 | 南京迪康金诺生物技术有限公司 | 一种构建杂交捕获测序文库的方法及应用 |
| CN113383089A (zh) * | 2018-11-29 | 2021-09-10 | 文塔纳医疗系统公司 | 经由代表性DNA测序进行个性化ctDNA疾病监测 |
| WO2020136133A1 (en) | 2018-12-23 | 2020-07-02 | F. Hoffmann-La Roche Ag | Tumor classification based on predicted tumor mutational burden |
| WO2020249704A1 (en) | 2019-06-13 | 2020-12-17 | F. Hoffmann-La Roche Ag | Systems and methods with improved user interface for interpreting and visualizing longitudinal data |
| EP4103748A4 (en) | 2020-02-14 | 2024-03-13 | The Johns Hopkins University | METHOD AND MATERIALS FOR ASSESSING NUCLEIC ACIDS |
| JPWO2022244856A1 (ko) | 2021-05-20 | 2022-11-24 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009099602A1 (en) * | 2008-02-04 | 2009-08-13 | Massachusetts Institute Of Technology | Selection of nucleic acids by solution hybridization to oligonucleotide baits |
| WO2012024658A2 (en) * | 2010-08-20 | 2012-02-23 | IntegenX, Inc. | Integrated analysis system |
| US20150126379A1 (en) * | 2013-10-28 | 2015-05-07 | The Translational Genomics Research Institute | Long insert-based whole genome sequencing |
| WO2017123316A1 (en) * | 2016-01-15 | 2017-07-20 | Ventana Medical Systems, Inc. | Deep sequencing profiling of tumors |
| EP3564395A1 (en) * | 2010-12-30 | 2019-11-06 | Foundation Medicine, Inc. | Optimization of multigene analysis of tumor samples |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4000159A (en) | 1974-06-28 | 1976-12-28 | Phillips Petroleum Company | Preparation of n,n-disubstituted thioamides |
| US5176995A (en) | 1985-03-28 | 1993-01-05 | Hoffmann-La Roche Inc. | Detection of viruses by amplification and hybridization |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| US4965188A (en) | 1986-08-22 | 1990-10-23 | Cetus Corporation | Process for amplifying, detecting, and/or cloning nucleic acid sequences using a thermostable enzyme |
| US4683195A (en) | 1986-01-30 | 1987-07-28 | Cetus Corporation | Process for amplifying, detecting, and/or-cloning nucleic acid sequences |
| US20080119367A1 (en) * | 2004-12-17 | 2008-05-22 | Mayo Foundation For Medical Education And Research | Prognosis of Renal Cell Carcinoma |
| WO2009061840A1 (en) * | 2007-11-05 | 2009-05-14 | Complete Genomics, Inc. | Methods and oligonucleotide designs for insertion of multiple adaptors employing selective methylation |
| US8592150B2 (en) * | 2007-12-05 | 2013-11-26 | Complete Genomics, Inc. | Methods and compositions for long fragment read sequencing |
| EP2227563B1 (en) | 2007-12-05 | 2012-06-06 | Complete Genomics, Inc. | Efficient base determination in sequencing reactions |
| JP5757572B2 (ja) | 2009-07-03 | 2015-07-29 | 国立大学法人 東京大学 | 癌細胞の存否を判定する方法および癌患者の予後を判定する方法 |
| DK2539450T3 (da) * | 2010-02-25 | 2016-05-30 | Advanced Liquid Logic Inc | Fremgangsmåde til fremstilling af nukleinsyrebiblioteker |
| GB2497510A (en) | 2011-11-10 | 2013-06-19 | Harry Cuppens | Methods for determining mononucleotide sequence repeats |
| US10138519B2 (en) | 2012-12-28 | 2018-11-27 | Quest Diagnostics Investments Incorporated | Universal sanger sequencing from next-gen sequencing amplicons |
| EP2971122B1 (en) * | 2013-03-15 | 2020-08-26 | Memorial Sloan Kettering Cancer Center | Biomarkers for response to rapamycin analogs |
| US20140278461A1 (en) | 2013-03-15 | 2014-09-18 | Memorial Sloan-Kettering Cancer Center | System and method for integrating a medical sequencing apparatus and laboratory system into a medical facility |
| KR20160062763A (ko) | 2013-10-18 | 2016-06-02 | 세븐 브릿지스 지노믹스 인크. | 유전자 샘플을 유전자형 결정하기 위한 방법 및 시스템 |
-
2016
- 2016-11-07 SG SG11201805600VA patent/SG11201805600VA/en unknown
- 2016-11-07 AU AU2016386032A patent/AU2016386032B2/en active Active
- 2016-11-07 CA CA3011342A patent/CA3011342C/en active Active
- 2016-11-07 CN CN201680078974.9A patent/CN108463559A/zh active Pending
- 2016-11-07 WO PCT/US2016/060835 patent/WO2017123316A1/en not_active Ceased
- 2016-11-07 EP EP16801647.5A patent/EP3402896B1/en active Active
- 2016-11-07 IL IL260304A patent/IL260304B2/en unknown
- 2016-11-07 JP JP2018536830A patent/JP7232643B2/ja active Active
- 2016-11-07 KR KR1020187023352A patent/KR102398465B1/ko active Active
-
2018
- 2018-06-27 ZA ZA2018/04322A patent/ZA201804322B/en unknown
- 2018-07-11 SA SA518392005A patent/SA518392005B1/ar unknown
- 2018-07-13 US US16/034,392 patent/US11649492B2/en active Active
-
2021
- 2021-07-02 JP JP2021110459A patent/JP7379418B2/ja active Active
-
2023
- 2023-04-06 US US18/131,577 patent/US20230250476A1/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009099602A1 (en) * | 2008-02-04 | 2009-08-13 | Massachusetts Institute Of Technology | Selection of nucleic acids by solution hybridization to oligonucleotide baits |
| WO2012024658A2 (en) * | 2010-08-20 | 2012-02-23 | IntegenX, Inc. | Integrated analysis system |
| EP3564395A1 (en) * | 2010-12-30 | 2019-11-06 | Foundation Medicine, Inc. | Optimization of multigene analysis of tumor samples |
| US20150126379A1 (en) * | 2013-10-28 | 2015-05-07 | The Translational Genomics Research Institute | Long insert-based whole genome sequencing |
| WO2017123316A1 (en) * | 2016-01-15 | 2017-07-20 | Ventana Medical Systems, Inc. | Deep sequencing profiling of tumors |
Non-Patent Citations (1)
| Title |
|---|
| BMC Genomics, 16(1):589 (2015.08.07.)* * |
Also Published As
| Publication number | Publication date |
|---|---|
| IL260304A (en) | 2018-08-30 |
| US11649492B2 (en) | 2023-05-16 |
| EP3402896B1 (en) | 2021-03-31 |
| JP2019503182A (ja) | 2019-02-07 |
| EP3402896A1 (en) | 2018-11-21 |
| US20230250476A1 (en) | 2023-08-10 |
| AU2016386032B2 (en) | 2021-08-12 |
| KR102398465B1 (ko) | 2022-05-13 |
| WO2017123316A1 (en) | 2017-07-20 |
| CA3011342A1 (en) | 2017-07-20 |
| AU2016386032A1 (en) | 2018-07-12 |
| BR112018014349A2 (pt) | 2019-02-12 |
| JP7232643B2 (ja) | 2023-03-03 |
| ZA201804322B (en) | 2022-10-26 |
| SA518392005B1 (ar) | 2022-02-08 |
| CA3011342C (en) | 2023-03-14 |
| US20180320229A1 (en) | 2018-11-08 |
| IL260304B2 (en) | 2025-04-01 |
| CN108463559A (zh) | 2018-08-28 |
| SG11201805600VA (en) | 2018-07-30 |
| JP7379418B2 (ja) | 2023-11-14 |
| JP2021176302A (ja) | 2021-11-11 |
| IL260304B1 (en) | 2024-12-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7379418B2 (ja) | 腫瘍のディープシークエンシングプロファイリング | |
| JP5986572B2 (ja) | 固定化プライマーを使用した標的dnaの直接的な捕捉、増幅、および配列決定 | |
| US9133513B2 (en) | High throughput methylation detection method | |
| JP7653924B2 (ja) | 近接ライゲーションのための方法および組成物 | |
| TWI864378B (zh) | 用於準確的平行定量核酸的高靈敏度方法 | |
| JP2024035109A (ja) | 核酸の正確な並行検出及び定量のための方法 | |
| CA3208896A1 (en) | Highly sensitive methods for accurate parallel quantification of variant nucleic acids | |
| US20060121461A1 (en) | Methods for identifying and isolating unique nucleic acid sequences | |
| US20180073023A1 (en) | Circular single-stranded nucleic acid, method for preparing the same, and method for using the same | |
| HK1260078A1 (en) | Deep sequencing profiling of tumors | |
| CN117265116A (zh) | 一种tfe3融合基因的检测方法、试剂盒以及探针库 | |
| HK40072445A (en) | Highly sensitive methods for accurate parallel quantification of nucleic acids | |
| EP3696279A1 (en) | Methods for noninvasive prenatal testing of fetal abnormalities | |
| JP2024543250A (ja) | 等温線形増幅されたプローブを利用する標的の濃縮および定量 | |
| CN119932164A (zh) | 准确地平行定量核酸的高灵敏度方法 | |
| BR112018014349B1 (pt) | Método de sequenciamento representacional direcionado | |
| JP2022521209A (ja) | 改良された核酸標的濃縮および関連方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20180813 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20200110 Comment text: Request for Examination of Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20210220 Patent event code: PE09021S01D |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20210824 Patent event code: PE09021S01D |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20220322 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20220511 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20220511 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration |