KR20180040407A - 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법 - Google Patents
피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법 Download PDFInfo
- Publication number
- KR20180040407A KR20180040407A KR1020160132272A KR20160132272A KR20180040407A KR 20180040407 A KR20180040407 A KR 20180040407A KR 1020160132272 A KR1020160132272 A KR 1020160132272A KR 20160132272 A KR20160132272 A KR 20160132272A KR 20180040407 A KR20180040407 A KR 20180040407A
- Authority
- KR
- South Korea
- Prior art keywords
- skin
- reservoir
- microfluidic
- chip
- medium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0697—Artificial constructs associating cells of different lineages, e.g. tissue equivalents
- C12N5/0698—Skin equivalents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/02—Form or structure of the vessel
- C12M23/16—Microfluidic devices; Capillary tubes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/20—Material Coatings
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0625—Epidermal cells, skin cells; Cells of the oral mucosa
- C12N5/0629—Keratinocytes; Whole skin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0656—Adult fibroblasts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/069—Vascular Endothelial cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/50—Proteins
- C12N2533/54—Collagen; Gelatin
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Cell Biology (AREA)
- Clinical Laboratory Science (AREA)
- Sustainable Development (AREA)
- Vascular Medicine (AREA)
- Dermatology (AREA)
- Immunology (AREA)
- Dispersion Chemistry (AREA)
- Rheumatology (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
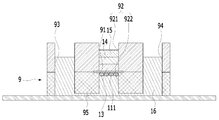
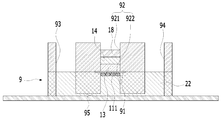
도 2는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, 미세유체 스킨칩의 개략적인 단면도이다.
도 3a는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, 멤브레인의 하면을 콜라젠으로 코팅하는 단계를 설명하기 위한 개략적인 단면도이다.
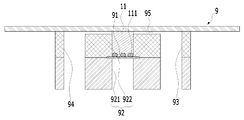
도 3b는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, 멤브레인의 하면 상에 HUVEC(혈관 내피 세포)를 배치하는 단계를 설명하기 위한 개략적인 개념도이다.
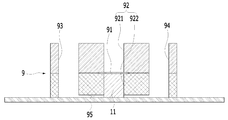
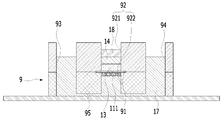
도 4a는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, 멤브레인의 상면을 콜라젠 혼합물로 코팅하는 단계를 설명하기 위한 개략적인 단면도이다.
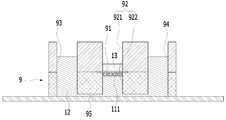
도 4b는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, 코팅된 콜라젠 혼합물의 상면 상에 Fibroblast(섬유아세포)가 혼합된 셀룰러 콜라젠 혼합물을 주입하여 굳히는 단계를 설명하기 위한 개략적인 단면도이다.
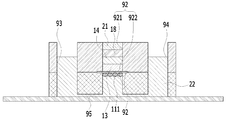
도 5a는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, Keratinocyte의 cell line이 혼합된 cell suspension을 주입하는 단계를 설명하기 위한 개략적인 개념도이다.
도 5b 및 도 5c는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, 주입된 cell suspension의 Keratinocyte의 cell line 상에 배지를 채우고, 제1 리저버 및 제2 리저버를 배지(22)로 채우는 단계를 설명하기 위한 개략적인 단면도이다.
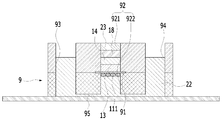
도 5d는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, S700 단계의 공기 노출 시키는 단계를 설명하기 위한 개략적인 단면도이다.
도 6은 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법의 다른 구현예를 설명하기 위한 개략적인 순서도이다.
도 7a는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, Master fabrication 단계를 설명하기 위한 개략적인 개념도이다.
도 7b 및 도 7c는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, PDMS layer를 제작하는 단계를 설명하기 위한 개략적인 개념도이다.
도 7d는 본원의 일 실시예에 따른 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법에 있어서, S100 단계의 Chip bonding 단계를 설명하기 위한 개략적인 개념도이다.
111: 멤브레인의 하면 상에 붙어 배양된 HUVEC
12: HUVEC 포함 액체
13: 콜라젠 혼합물
14: 셀룰러 콜라젠 혼합물
15: 배지 DMEM
16: 배지 EGM-2MV
18: cell suspension
21: 배지 DMEM
22: 배지 EGM-2MV
23: 칼슘이 첨가된 DMEM
9: 미세유체 스킨칩
91: 멤브레인
92: 챔버
921: 챔버의 상부
922: 챔버의 하부
93: 제1 리저버
94: 제2 리저버
95: 채널
Claims (28)
- 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법으로서,
(a) 수평으로 배치되는 멤브레인에 의해 내부가 상부와 하부로 분리되는 챔버, 상기 챔버의 일측 및 타측 각각에 형성되는 제1 리저버와 제2 리저버, 및 유체가 이동 가능하도록 제1 리저버, 상기 챔버의 하부 및 상기 제2 리저버를 연결하는 채널을 포함하는 미세유체 스킨칩을 준비하는 단계;
(b) 상기 멤브레인의 하면 상에 혈관 내벽 조직을 형성하는 단계;
(c) 상기 멤브레인의 상면 상에 진피층(dermis)을 형성하는 단계; 및
(d) 상기 진피층의 상면 상에 표피층(epidermis)을 형성하는 단계를 포함하는, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제1항에 있어서,
상기 (b) 단계는,
(b1) 상기 멤브레인의 하면을 코팅물질로 코팅하는 단계;
(b2) 상기 멤브레인의 하면 상에 HUVEC(혈관 내피 세포)를 배치하는 단계; 및
(b3) 상기 제1 리저버, 상기 챔버의 상부 및 상기 제2 리저버를 배지로 채워두는 단계를 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제2항에 있어서,
상기 (b1) 단계는,
상기 제1 리저버 및 상기 제2 리저버 중 하나에 코팅물질을 주입하여 상기 챔버의 하부를 코팅물질로 소정의 시간 동안 채워두는 단계; 및
상기 미세유체 스킨칩의 내부를 워싱(washing)하는 단계를 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제3항에 있어서,
상기 미세유체 스킨칩의 내부를 워싱하는 단계는,
상기 채널에 PBS 및 EGM-2MV를 순차적으로 흘려주는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제2항에 있어서,
상기 (b2) 단계는,
상기 챔버의 하부를 HUVEC 포함 액체로 채우는 단계; 및
상기 챔버의 하부가 상측을 향하도록, 상기 미세유체 스킨칩을 뒤집는 단계를 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제5항에 있어서,
상기 챔버의 하부를 HUVEC 포함 액체로 채우는 단계는,
상기 제1 리저버 및 상기 제2 리저버 중 하나에 HUVEC 포함 액체가 주입된 후, 나머지 하나로 HUVEC 포함 액체가 배출되면, 상기 챔버의 하부가 HUVEC 포함 액체로 채워진 것으로 판단하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제2항에 있어서,
상기 (b3) 단계에서, 상기 제1 리저버, 상기 챔버의 상부 및 상기 제2 리저버에 채워지는 배지는 EGM-2MV인 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제2항에 있어서,
상기 (b) 단계는,
(b4) 상기 (b3) 단계의 상태에서 미리 설정된 시간 동안 배지의 흐름 없이 배양이 이루어지는 단계; 및
(b5) 상기 (b4) 단계 이후 상기 미세유체 스킨칩 내에서 배지의 흐름을 형성시키며 배양이 이루어지는 단계를 더 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제8항에 있어서,
상기 (b5) 단계 이후에, 상기 (c) 단계의 수행을 위해, 상기 (b3) 단계에서 제1 리저버, 상기 챔버의 상부 및 상기 제2 리저버를 채웠던 배지가 적어도 일부 제거되는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제1항에 있어서,
상기 (c) 단계는,
(c1) 상기 멤브레인의 상면을 콜라젠 혼합물로 코팅하는 단계;
(c2) 코팅된 상기 콜라젠 혼합물의 상면 상에 Fibroblast(섬유아세포)가 혼합된 셀룰러 콜라젠 혼합물을 주입하여 굳히는 단계; 및
(c3) 상기 굳은 셀룰러 콜라젠 혼합물 상에 배지를 채우고, 상기 제1 리저버 및 상기 제2 리저버를 배지로 채우는 단계를 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제10항에 있어서,
상기 (c) 단계에서,
상기 콜라젠 혼합물은, 콜라젠, 10X DMEM media, 0.5N NaOH 및 DMEM 배지를 섞은 혼합물인 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제10항에 있어서,
상기 (c) 단계에서,
상기 셀룰러 콜라젠 혼합물은, 콜라젠, 10X DMEM media, 0.5N NaOH 및 Fibroblast를 섞은 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제10항에 있어서,
상기 (c3) 단계에서, 상기 셀룰러 콜라젠 혼합물 상에 채워지는 배지는 DMEM인 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제10항에 있어서,
상기 (c3) 단계에서, 상기 제1 리저버 및 상기 제2 리저버에 채워지는 배지는 EGM-2MV인 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제10항에 있어서,
상기 (c) 단계는,
상기 (c3) 단계 이후에,
(c4) 상기 미세유체 스킨칩 내에서 배지의 흐름을 형성시키며 배양이 이루어지는 단계를 더 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제15항에 있어서,
상기 (c4) 단계 이후에, 상기 (d) 단계의 수행을 위해, 상기 (c3) 단계에서 상기 셀룰러 콜라젠 혼합물 상에 채워졌던 배지 및 상기 제1 리저버와 상기 제2 리저버를 채웠던 배지가 제거되는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제1항에 있어서,
상기 (d) 단계는,
(d1) 상기 진피층 상에 Keratinocyte의 cell line이 혼합된 cell suspension을 주입하는 단계;
(d2) 주입된 상기 cell suspension의 Keratinocyte의 cell line 상에 배지를 채우고, 상기 제1 리저버 및 상기 제2 리저버를 배지로 채우는 단계를 포함하되,
상기 (d2) 단계는 상기 (d1) 단계로부터 미리 설정된 시간 이후에 수행되는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제17항에 있어서,
상기 (d) 단계에서, 상기 cell line은 HaCaT인 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제17항에 있어서,
상기 (d2) 단계는,
소정의 시간 동안, 상기 cell suspension의Keratinocyte의 cell line 상에DMEM을 채워두고 상기 제1 리저버 및 상기 제2 리저버를 EGM-2MV로 채워두는 단계; 및
소정의 시간 이후에, 상기 cell suspension의Keratinocyte의 cell line 상에 DMEM과 Ca2 +를 채워두고 상기 제1 리저버 및 상기 제2 리저버를 EGM-2MV로 채워두는 단계를 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제17항에 있어서,
상기 (d) 단계는,
상기 (d2) 단계 이후에,
(d3) 상기 cell suspension의Keratinocyte의 cell line 상에 채워진 배지 및 상기 제1 리저버 및 상기 제2 리저버를 채우는 배지의 적어도 일부를 제거하고, 상기 미세유체 스킨칩 내에서의 배지의 흐름을 형성시키며, 상기 cell suspension의 Keratinocyte의 cell line을 공기 노출(Air exposure)시키는 단계를 더 포함하는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 제1항에 있어서,
상기 (b) 단계는, 상기 (c) 단계의 전 또는 상기 (d) 단계의 후에 수행되는 것인, 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법. - 피부 모델로서,
수평으로 배치되는 멤브레인에 의해 내부가 상부와 하부로 분리되는 챔버, 상기 챔버의 일측 및 타측 각각에 형성되는 제1 리저버와 제2 리저버, 및 유체가 이동 가능하도록 제1 리저버, 상기 챔버의 하부 및 상기 제2 리저버를 연결하는 채널을 포함하는 미세유체 스킨칩;
상기 멤브레인의 하면 상에 형성되는 혈관 내벽 조직;
상기 멤브레인의 상면 상에 형성되는 진피층; 및
상기 진피층의 상면 상에 형성되는 표피층을 포함하는, 피부 모델. - 제22항에 있어서,
상기 혈관 내벽 조직은 HUVEC(혈관 내피 세포)가 배양되어 형성되는 것인, 피부 모델. - 제22항에 있어서,
상기 진피층은 Fibroblast(섬유아세포)가 배양되어 형성되는 것인, 피부 모델. - 제24항에 있어서,
상기 진피층은 상기 멤브레인 상에 Fibroblast(섬유아세포)가 혼합된 셀룰러 콜라젠 혼합물이 주입되어 형성되는 것인, 피부 모델. - 제25항에 있어서,
상기 셀룰러 콜라젠 혼합물은, 콜라젠, 10X DMEM media, 0.5N NaOH 및 Fibroblast를 섞은 것인, 피부 모델. - 제22항에 있어서,
상기 표피층은 Keratinocyte의 cell line이 배양되어 형성되는 것인, 피부 모델. - 제27항에 있어서,
상기 cell line은 HaCaT인 것인, 피부 모델.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160132272A KR101866494B1 (ko) | 2016-10-12 | 2016-10-12 | 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160132272A KR101866494B1 (ko) | 2016-10-12 | 2016-10-12 | 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20180040407A true KR20180040407A (ko) | 2018-04-20 |
| KR101866494B1 KR101866494B1 (ko) | 2018-06-11 |
Family
ID=62088463
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160132272A Active KR101866494B1 (ko) | 2016-10-12 | 2016-10-12 | 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101866494B1 (ko) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200031018A (ko) * | 2018-09-13 | 2020-03-23 | 한국과학기술연구원 | 생체피부와 물리적 및 생물학적으로 유사한 인공 표피층, 인공 진피층 및 이를 포함하는 인공피부 |
| WO2021137455A1 (ko) * | 2019-12-30 | 2021-07-08 | 인제대학교 산학협력단 | 피부칩, 피부칩 제조방법 및 피부칩의 세포배양방법 |
| KR20210086461A (ko) | 2019-12-30 | 2021-07-08 | 인제대학교 산학협력단 | 피부칩, 피부칩 제조방법 및 피부칩의 세포배양방법 |
| KR20230143375A (ko) | 2022-04-05 | 2023-10-12 | 한림대학교 산학협력단 | 장기 모사 칩 구조체 제조방법 |
| KR20230143372A (ko) | 2022-04-05 | 2023-10-12 | 한림대학교 산학협력단 | 장기 모사 칩 |
| KR20240017570A (ko) * | 2022-08-01 | 2024-02-08 | 한국과학기술연구원 | 인공 피부 배양 방법 및 장치 |
| CN118308187A (zh) * | 2024-04-12 | 2024-07-09 | 丹望医疗科技(上海)有限公司 | 皮肤芯片及皮肤模型的构建方法 |
| CN119823870A (zh) * | 2025-03-19 | 2025-04-15 | 安徽骆华生物科技有限公司 | 皮肤芯片、皮肤模型及其应用 |
-
2016
- 2016-10-12 KR KR1020160132272A patent/KR101866494B1/ko active Active
Non-Patent Citations (2)
| Title |
|---|
| Lap Chip. 2015, 15:882-888.* * |
| Nature Biotechnology. 2014, 32(8):760-772.* * |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200031018A (ko) * | 2018-09-13 | 2020-03-23 | 한국과학기술연구원 | 생체피부와 물리적 및 생물학적으로 유사한 인공 표피층, 인공 진피층 및 이를 포함하는 인공피부 |
| WO2021137455A1 (ko) * | 2019-12-30 | 2021-07-08 | 인제대학교 산학협력단 | 피부칩, 피부칩 제조방법 및 피부칩의 세포배양방법 |
| KR20210086461A (ko) | 2019-12-30 | 2021-07-08 | 인제대학교 산학협력단 | 피부칩, 피부칩 제조방법 및 피부칩의 세포배양방법 |
| US12221596B2 (en) | 2019-12-30 | 2025-02-11 | Inje University Industry-Academic Cooperation Foundation | Skin chip, method for manufacturing skin chip and cell skin chip, method for manufacturing skin chip and cell |
| KR20230143375A (ko) | 2022-04-05 | 2023-10-12 | 한림대학교 산학협력단 | 장기 모사 칩 구조체 제조방법 |
| KR20230143372A (ko) | 2022-04-05 | 2023-10-12 | 한림대학교 산학협력단 | 장기 모사 칩 |
| KR20240017570A (ko) * | 2022-08-01 | 2024-02-08 | 한국과학기술연구원 | 인공 피부 배양 방법 및 장치 |
| CN118308187A (zh) * | 2024-04-12 | 2024-07-09 | 丹望医疗科技(上海)有限公司 | 皮肤芯片及皮肤模型的构建方法 |
| CN119823870A (zh) * | 2025-03-19 | 2025-04-15 | 安徽骆华生物科技有限公司 | 皮肤芯片、皮肤模型及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR101866494B1 (ko) | 2018-06-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101866494B1 (ko) | 피부조직과 혈관을 모사한 무펌프 미세유체 스킨칩의 제작과 다중세포배양 방법 | |
| US20230287324A1 (en) | Open-top microfluidic device with structural anchors | |
| US20220403313A1 (en) | Open-top microfluidic devices and methods for simulating a function of a tissue | |
| JP7588582B2 (ja) | 細胞内において又は細胞によって誘導された機械的歪みの評価のための装置 | |
| CA2720261C (en) | Three-dimensional microfluidic platforms and methods of use thereof | |
| EP2721141B1 (en) | Device and method for culturing cells in a biomimetic environment | |
| Musick et al. | Three-dimensional micro-electrode array for recording dissociated neuronal cultures | |
| US12163112B2 (en) | Production of cellular spheroids | |
| US20230365908A1 (en) | Dynamic cell culture platform for combinatorial and biomechanical stimulation | |
| CN103789206A (zh) | 基于微流控技术的成骨细胞电刺激系统及其操作方法 | |
| KR101902521B1 (ko) | 인공 지방간 형성 방법 , 지방간 분석 방법과 이를 위한 지방간 칩 및 지방간-지방세포 칩 | |
| EP3620508B1 (en) | Microfluidic device for electrical measurement and/or stimulation | |
| ES3024481T3 (en) | Methods and systems for generating three-dimensional biological structures | |
| Gómez Vázquez | Development of in vitro blood-brain barrier models: from traditional 2D models to microfluidics | |
| Zhou | Investigating the Effects of Cyclic Stretching on Lung Cancer Cells using an Automated Microfluidic System | |
| CN121013900A (zh) | 用于形成三维组织屏障的微流体设备 | |
| Lee et al. | Fabrication of microfluidic system for the assessment of cell migration on 3D micropatterned substrates | |
| HK40026474A (en) | Production of cellular spheroids | |
| Zheng et al. | A Microfluidic Chip for Analysis of Mechanical Forces Generated During Cell Migration | |
| Ugolini | Multi-layer microdevices for advanced cell culture applications | |
| Devarasetty et al. | 12 Body-on-a-Chip | |
| VanDersarl | Interrogating, Manipulating, and Controlling Nano-Bio Interfaces | |
| Wei | Cell Co-culture and Signaling Analysis Based on Microfluidic Devices Coupling with ESI-Q-TOF MS |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| S17-X000 | Non-exclusive voluntary license recorded |
St.27 status event code: A-4-4-S10-S17-lic-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| P14-X000 | Amendment of ip right document requested |
St.27 status event code: A-5-5-P10-P14-nap-X000 |
|
| P14-X000 | Amendment of ip right document requested |
St.27 status event code: A-5-5-P10-P14-nap-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R14-asn-PN2301 |
|
| R18 | Changes to party contact information recorded |
Free format text: ST27 STATUS EVENT CODE: A-5-5-R10-R18-OTH-X000 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |