KR20170117614A - 이미노슈가 및 아레나바이러스성 감염을 치료하는 방법 - Google Patents
이미노슈가 및 아레나바이러스성 감염을 치료하는 방법 Download PDFInfo
- Publication number
- KR20170117614A KR20170117614A KR1020177029196A KR20177029196A KR20170117614A KR 20170117614 A KR20170117614 A KR 20170117614A KR 1020177029196 A KR1020177029196 A KR 1020177029196A KR 20177029196 A KR20177029196 A KR 20177029196A KR 20170117614 A KR20170117614 A KR 20170117614A
- Authority
- KR
- South Korea
- Prior art keywords
- virus
- substituted
- unsubstituted
- group
- alkyl group
- Prior art date
Links
- 0 C***c1c(*)c(*)c(*)c(*)c1* Chemical compound C***c1c(*)c(*)c(*)c(*)c1* 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/02—Suppositories; Bougies; Bases therefor; Ovules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/12—Aerosols; Foams
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Virology (AREA)
- Oncology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Communicable Diseases (AREA)
- Dispersion Chemistry (AREA)
- Molecular Biology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Pulmonology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Hydrogenated Pyridines (AREA)
Abstract
아레나비리데 과에 속하는 바이러스에 의해 유발되거나 그와 관련된 질환 또는 증상을 이미노슈가, 예컨대 DNJ 유도체를 사용하여 치료하는 방법을 제공한다.
Description
<관련 출원>
본 출원은 2009년 2월 24일자로 출원된 미국 가출원 제61/202,391호 및 2009년 9월 4일자로 출원된 미국 가출원 제61/272,251호를 우선권으로 주장하며, 둘 다 참고문헌으로 전체로서 삽입된다.
본 출원은 이미노슈가 및 이미노슈가로 바이러스성 감염을 치료하는 방법, 특히 아레나비리데(Arenaviridae) 과에 속하는 바이러스에 의해 유발되거나 그와 관련된 바이러스성 감염의 치료 및 예방을 위한 이미노슈가의 용도에 관한 것이다.
본 출원은 이미노슈가 및 이미노슈가로 바이러스성 감염을 치료하는 방법, 특히 아레나비리데(Arenaviridae) 과에 속하는 바이러스에 의해 유발되거나 그와 관련된 바이러스성 감염의 치료 및 예방을 위한 이미노슈가의 용도에 관한 것이다.
한 실시양태는 아레나비리데과에 속하는 바이러스에 의해 유발되거나 그와 관련된 질환 또는 증상을 치료 또는 예방하는 방법이며, 이 방법은 치료를 요하는 환자에게 하기 화학식의 화합물을 투여하는 단계를 포함한다:
상기 식에서,
R은 치환 또는 비치환된 알킬기, 치환 또는 비치환된 시클로알킬기, 치환 또는 비치환된 아릴기, 또는 치환 또는 비치환된 옥사알킬기로부터 선택된 것이거나; 또는
R은
(여기서, R1은 치환 또는 비치환 알킬기이며;
X1-5는 H, NO2, N3, 또는 NH2로부터 독립적으로 선택된 것이고;
Y는 부재 또는 카보닐을 제외한 치환 또는 비치환된 C1-알킬기이며; 및
Z는 결합 또는 NH에서 선택된 것이되; 단 Z가 결합일 경우, Y는 부재이고, 단 Z가 NH일 경우에는, Y는 카보닐을 제외한 치환 또는 비치환된 C1-알킬기이다); 및
W1-4는 수소, 치환 또는 비치환된 알킬기, 치환 또는 비치환된 할로알킬기, 치환 또는 비치환된 알카노일기, 치환 또는 비치환된 아로일기, 또는 치환 또는 비치환된 할로알카노일기로부터 독립적으로 선택된 것이다.
본 발명자들은 특정 이미노슈가, 예컨대 데옥시노지리마이신 유도체가 아레나비리데 과에 속하는 바이러스에 대하여 효과적일 수 있다는 것을 밝혀냈다.
도 1(A)-(E)는 하기 이미노슈가의 화학식을 도시한다: A) N-부틸 데옥시노지리마이신(NB-DNJ 또는 UV-1); B) N-노닐 데옥시노지리마이신(NN-DNJ 또는 UV-2); C) N-(7-옥사데실)데옥시노지리마이신(N7-O-DNJ 또는 N7-DNJ 또는 UV-3); D) N-(9-메톡시노닐)데옥시노지리마이신(N9-DNJ 또는 UV-4); E) N-(N-{4'-아지도-2'-니트로페닐}-6-아미노헥실)데옥시노지리마이신(NAP-DNJ 또는 UV-5).
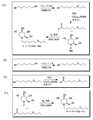
도 2는 NN-DNJ의 합성 반응식이다.
도 3A-D는 N7-O-DNJ의 합성을 도시한다. 특히, 도 3A는 N7-O-DNJ을 야기하는 반응 순서를 도시하고; 도 3B는 6-프로필옥시-1-헥사놀의 제조를 도시하고; 도 3C는 6-프로필옥시-1-헥사날의 제조를 도시하고; 도 3D는 N7-O-DNJ의 합성을 도시한다.
도 4A-C는 N-(9-메톡시노닐)데옥시노지리마이신의 합성에 관한 것이다. 특히, 도 4A는 9-메톡시-1-노나놀의 제조를 도시하고; 도 4B는 9-메톡시-1-노나날의 제조를 도시하고; 도 4C는 N-(9-메톡시노닐)데옥시노지리마이신의 합성을 도시한다.
도 5는 NB-DNJ; N7-O-DNJ 및 N9-DNJ에 의한 피친데(Pichinde) 바이러스 방출의 억제 데이터를 도시한다.
도 6은 피친데 바이러스(PICV) 및 주닌(Junin) 바이러스(JUNV)에 대한 선택된 이미노슈가의 활성을 도시한다.
도 7은 PICV에 대한 NB-DNJ, N7-O-DNJ 및 N9-DNJ의 항바이러스 활성을 도시한다.
도 8은 JUNV에 대한 NB-DNJ, NN-DNJ, N7-O-DNJ, N9-DNJ 및 NAP-DNJ의 항바이러스 활성을 도시한다.
도 2는 NN-DNJ의 합성 반응식이다.
도 3A-D는 N7-O-DNJ의 합성을 도시한다. 특히, 도 3A는 N7-O-DNJ을 야기하는 반응 순서를 도시하고; 도 3B는 6-프로필옥시-1-헥사놀의 제조를 도시하고; 도 3C는 6-프로필옥시-1-헥사날의 제조를 도시하고; 도 3D는 N7-O-DNJ의 합성을 도시한다.
도 4A-C는 N-(9-메톡시노닐)데옥시노지리마이신의 합성에 관한 것이다. 특히, 도 4A는 9-메톡시-1-노나놀의 제조를 도시하고; 도 4B는 9-메톡시-1-노나날의 제조를 도시하고; 도 4C는 N-(9-메톡시노닐)데옥시노지리마이신의 합성을 도시한다.
도 5는 NB-DNJ; N7-O-DNJ 및 N9-DNJ에 의한 피친데(Pichinde) 바이러스 방출의 억제 데이터를 도시한다.
도 6은 피친데 바이러스(PICV) 및 주닌(Junin) 바이러스(JUNV)에 대한 선택된 이미노슈가의 활성을 도시한다.
도 7은 PICV에 대한 NB-DNJ, N7-O-DNJ 및 N9-DNJ의 항바이러스 활성을 도시한다.
도 8은 JUNV에 대한 NB-DNJ, NN-DNJ, N7-O-DNJ, N9-DNJ 및 NAP-DNJ의 항바이러스 활성을 도시한다.
용어의 정의
별도의 언급이 없는 경우, "한(a)" 또는 "하나(an)"는 "하나 이상"을 의미한다.
본원에서 사용한, 용어 "바이러스성 감염"은 바이러스가 건강한 세포에 침투하여 세포의 번식 기구를 사용하여 증식 또는 복제하고 궁극적으로 세포를 용해시켜 세포사와, 바이러스 입자의 방출 및 새로 생성된 자손 바이러스에 의한 다른 세포의 감염을 유발하는 질환 상태를 말한다. 특정 바이러스에 의한 잠복 감염 또한 바이러스성 감염의 가능한 결과이다.
본원에서 사용한, 용어 "바이러스성 감염을 치료 또는 예방"은 특정 바이러스의 복제를 억제하는 것, 바이러스 전달을 억제하는 것, 또는 바이러스가 숙주 내에 자리잡는 것을 예방하는 것, 및 바이러스성 감염으로 유발된 질환의 증상을 완화 또는 경감하는 것을 의미한다. 치료는 바이러스성 적하의 감소, 사망률 및/또는 이환률의 감소가 있다면 치료적인 것으로 간주된다.
IC50 또는 IC90(억제 농도 50 또는 90)은 각각 바이러스성 감염의 50% 또는 90% 감소를 달성하는데 사용된 치료제, 예컨대 이미노슈가의 농도이다.
관련 출원
본 출원은 2009년 2월 24일자로 출원된, 미국 가출원 제61/202,391호를 참고문헌으로 전체로서 삽입한다.
개시
본 발명자들은 특정 이미노슈가, 예컨대 데옥시노지리마이신 유도체가 아레나비리데 과에 속하는 바이러스에 대하여 효과적일 수 있다는 것을 밝혀냈다.
특히, 데옥시노지리마이신 유도체는 아레나비리데 과에 속하는 바이러스에 의해 유발되거나 그와 관련된 질환 또는 증상을 치료 또는 예방하는데 유용할 수 있다.
아레나비리데 과에 속하는 바이러스는 아레나바이러스속에 속하는 아레나바이러스를 포함한다. 아레나바이러스는 많은 바이러스성 출혈열을 유발할 수 있다. 아레나바이러스 속은 입피 바이러스(Ippy virus); 라사 바이러스(Lassa virus); 림프구성 맥락수막염 바이러스; 모발라 바이러스(Mobala virus); 모페이아 바이러스(Mopeia virus); 아마파리 바이러스(Amapari virus); 플렉살 바이러스(Flexal virus); 구아나리토 바이러스(Guanarito virus); 주닌 바이러스(Junin virus); 라티노 바이러스(Latino virus); 마추포 바이러스(Machupo virus); 올리베로스 바이러스(Oliveros virus); 파라나 바이러스(Parana virus); 피친데 바이러스(Pichinde virus); 피리탈 바이러스(Pirital virus); 사비아 바이러스(Sabia virus); 타카리베 바이러스(Tacaribe virus); 타미아미 바이러스(Tamiami virus); 화이트워터 아로요 바이러스(Whitewater Arroyo virus); 및 샤페어 바이러스(Chapare virus)를 포함한다. 아레나바이러스는 바이러스 저장소로 쓰일 수 있는 설치류와의 접촉으로 종종 전염될 수 있다. 아레나바이러스 감염은 전세계적으로 풍토적일 수 있으며, 매년 백만개 이상의 사례와 수천명의 사망을 유발한다. 다른 아레나바이러스만큼 인간에게 위험하지는 않은 피친데 바이러스(아레나바이러스 속의 구성원)가 이 속에 대한 화합물의 활성을 시험하기 위한 모델로 자주 사용된다.
아레나바이러스에 의해 유발되거나 그와 관련된 질환은 림프구성 맥락수막염 바이러스에 의해 유발되는 림프구성 맥락수막염; 라사 바이러스에 의해 유발되는 라사열; 주닌 바이러스에 의해 유발되는 아르헨티나 출혈열; 마추포 바이러스에 의해 유발되는 볼리비아 출혈열; 구아라니토 바이러스에 의해 유발되는 베네수엘라 출혈열; 사비아 바이러스에 의해 유발되는 브라질 출혈열; 타카리베 바이러스와 관련된 타카리베열; 플렉살 바이러스와 관련된 인플루엔자-유사 질병; 화이트워터 아로요 바이러스와 관련된 출혈열을 포함한다.
많은 실시양태에서, 이미노슈가는 N-치환 데옥시노지리마이신일 수 있다. 몇몇 실시양태에서, 그러한 N-치환 데옥시노지리마이신은 하기 화학식의 화합물일 수 있다:
상기 W1-4는 수소, 치환 또는 비치환된 알킬기, 치환 또는 비치환된 할로알킬기, 치환 또는 비치환된 알카노일기, 치환 또는 비치환된 아로일기, 또는 치환 또는 비치환된 할로알카노일기로부터 독립적으로 선택된 것이다.
몇몇 실시양태에서, R은 치환 또는 비치환된 알킬기, 치환 또는 비치환된 시클로알킬기, 치환 또는 비치환된 아릴기, 또는 치환 또는 비치환된 옥사알킬기로부터 선택된 것일 수 있다.
몇몇 실시양태에서, R은 1개 내지 16개의 탄소 원자, 4개 내지 12개의 탄소 원자 또는 8개 내지 10개의 탄소 원자를 포함하는 치환 또는 비치환된 알킬기 및/또는 치환 또는 비치환된 옥사알킬기일 수 있다. 용어 "옥사알킬"은 1개 내지 5개 또는 1개 내지 3개 또는 1개 내지 2개의 산소 원자를 함유할 수 있는 알킬 유도체를 지칭한다. 용어 "옥사알킬"은 히드록시기 및 메톡시기를 말단으로 하는 알킬 유도체를 포함한다.
몇몇 실시양태에서, R은 -(CH2)6OCH3, -(CH2)6OCH2CH3, -(CH2)6O(CH2)2CH3, -(CH2)6O(CH2)3CH3, -(CH2)2O(CH2)5CH3, -(CH2)2O(CH2)6CH3,; -(CH2)2O(CH2)7CH3; -(CH2)9-OH; -(CH2)9OCH3로부터 선택된 것일 수 있으나 이에 제한되지는 않는다.
몇몇 실시양태에서, R은 분지 또는 비분지, 치환 또는 비치환된 알킬기일 수 있다. 특정 실시양태에서, 알킬기는 C6-C20 알킬기; C8-C16 알킬기; 또는 C8-C10 알킬기일 수 있는 장쇄 알킬기일 수 있다. 몇몇 실시양태에서, R은 장쇄 옥사알킬기, 즉 1개 내지 5개 또는 1개 내지 3개 또는 1개 내지 2개의 산소 원자를 함유할 수 있는 장쇄 알킬기일 수 있다.
몇몇 실시양태에서, R은 하기 화학식을 가질 수 있다:
여기서 R1은 치환 또는 비치환된 알킬기이며;
X1-5는 H, NO2, N3, 또는 NH2로부터 독립적으로 선택된 것이고;
Y는 부재 또는 카보닐을 제외한 치환 또는 비치환된 C1-알킬기이며; 및
Z는 결합 또는 NH에서 선택된 것이되; 단 Z가 결합일 경우, Y는 부재이고, 단 Z가 NH일 경우에는 Y는 카보닐을 제외한 치환 또는 비치환된 C1-알킬기이다.
몇몇 실시양태에서, Z는 NH이고 R1-Y는 치환 또는 비치환된 알킬기, 예컨대 C2-C20 알킬기 또는 C4-C12 알킬기 또는 C4-C10 알킬기이다.
몇몇 실시양태에서, X1은 NO2이고 X3는 N3이다. 몇몇 실시양태에서 각 X2, X4, 및 X5는 수소이다.
몇몇 실시양태에서, 이미노슈가는 미국 특허 공개 출원 제2007/0275998호에 개시된 DNJ 유도체일 수 있으며, 참고문헌으로 전체로서 삽입된다. 몇몇 실시양태에서, 데옥시노지리마이신 유도체는 도 1에 도시된 화합물 중 하나일 수 있다.
데옥시노지리마이신 유도체의 합성 방법은 예컨대 미국 특허 제5,622,972호, 제5,200,523호, 제5,043,273호, 제4,994,572호, 제4,246,345호, 제4,266,025호, 제4,405,714호, 및 제4,806,650호, 및 미국 공개 특허 출원 제US2007/0275998호에 개시되어 있으며, 모두가 본원의 참고문헌으로 전체로서 삽입된다.
몇몇 실시양태에서, 이미노슈가는 무기 또는 유기산으로부터 유래된 염의 형태일 수 있다. 제약상 허용가능한 염 및 염 형태를 제조하기 위한 방법은 예를 들어 문헌(Berge et al. (J. Pharm . Sci . 66:1-18, 1977))에 개시되어 있다. 적절한 염의 예로는 하기를 포함하지만 이에 제한되지는 않는다: 아세테이트, 아디페이트, 알기네이트, 시트레이트, 아스파테이트, 벤조에이트, 벤젠술포네이트, 비술페이트, 부티레이트, 캄포레이트, 캄포술포네이트, 디글루코네이트, 시클로펜탄프로피오네이트, 도데실술페이트, 에탄술포네이트, 글루코헵타노에이트, 글리세로포스페이트, 헤미술페이트, 헵타노에이트, 헥사노에이트, 푸마레이트, 히드로클로라이드, 히드로브로마이드, 히드로요오다이드, 2-히드록시에탄술포네이트, 락테이트, 말레에이트, 메탄술포네이트, 니코티네이트, 2-나프탈렌술포네이트, 옥살레이트, 팔모에이트, 펙티네이트, 퍼술페이트, 3-페닐프로피오네이트, 피크레이트, 피발레이트, 프로피오네이트, 숙시네이트, 타르트레이트, 티오시아네이트, 토실레이트, 메실레이트, 및 운데카노에이트.
몇몇 실시양태에서, 이미노슈가는 전구약물의 형태로 사용될 수 있다. DNJ 유도체의 전구약물들, 예컨대 6-인산화된 DNJ 유도체는 미국 특허 제5,043,273호 및제5,103,008호에 개시되어 있다.
몇몇 실시양태에서, 이미노슈가는 제약상 허용가능한 운반체 및/또는 동물에게 조성물을 전달하는데 유용한 성분을 추가로 포함하는 조성물의 일부로 사용될 수 있다. 인간에게 조성물을 전달하는데 유용한 수많은 제약상 허용가능한 캐리어 및 다른 동물 예컨대 소에게 조성물을 전달하는데 유용한 성분은 당업계에 알려져 있다. 본 발명의 조성물에 그러한 캐리어 및 성분의 추가는 당업계의 통상의 기술 수준 내이다.
몇몇 실시양태에서, 제약 조성물은 N-치환된 데옥시노지리마이신으로 본질적으로 구성될 수 있으며, 이는 N-치환된 데옥시노지리마이신이 조성물 내 유일한 유효 성분이라는 것을 의미할 수 있다.
또다른 실시양태에서, N-치환된 데옥시노지리마이신은 하나 이상의 추가 항바이러스 화합물과 같이 투여될 수 있다.
몇몇 실시양태에서, 이미노슈가는 예컨대 미국 공개 2008/0138351; 2009년 3월 25일자로 출원된 미국 출원 제12/410,750호 및 2009년 3월 27일자로 출원된 미국 가출원 제61/202,699호에 개시된 것과 같은 리포좀 조성물에서 사용될 수 있다.
이미노슈가, 예컨대 DNJ 유도체는 바이러스가 침범한 세포 또는 동물에 투여될 수 있다. 이미노슈가는 바이러스의 형태형성을 억제하거나 개체를 치료할 수 있다. 치료는 동물에서 바이러스 감염을 감소, 약화 또는 저하할 수 있다.
아레나비리데 과에 속하는 바이러스에 감염될 수 있는 동물은 척추동물, 예컨대 영장류, 인간, 설치류 및 박쥐를 포함하는 조류 및 포유류를 포함한다.
본 발명의 방법으로 동물 또는 동물 세포에 투여되는 이미노슈가의 양은 아레나비리데 과에 속하는 바이러스의 세포에서의 형태형성을 억제하는데 효과적인 양일 수 있다. 본원에서 사용된 용어 "억제"는 이미노슈가의 부재에서 보이는 검출 가능한 생물학적 활성의 감소 및/또는 제거를 지칭할 수 있다. 본원에서 사용된 용어 "유효량"은 나타낸 효과를 달성하는데 필요한 이미노슈가의 양을 지칭할 수 있다. 본원에서 사용된 용어 "치료"는 환자의 증상을 감소 또는 완화, 악화 또는 진행을 예방, 원인물질을 억제 또는 제거, 또는 아레나비리데 과에 속하는 바이러스가 없는 환자에서 그와 관련된 감염 또는 장애를 예방하는 것을 지칭할 수 있다.
그러므로, 예를 들어, 바이러스에 의해 유발되거나 그와 관련된 질환의 치료는 감염 요소의 파괴, 그것의 성장 또는 성숙의 억제 또는 방해 및 그것의 병리학적 영향의 중화를 포함할 수 있다. 세포 또는 동물에게 투여될 수 있는 이미노슈가의 양은 바람직하게는 그것의 투여로 동반되는 장점보다 더 큰 독성 효과를 유도하지 않는 양이다.
제약 조성물 내 유효 성분의 실제 투여량 수준은 특정 환자에 대해서 원하는 치료 반응을 달성하는데 효율적인 적절량의 활성 화합물(들)을 투여하기 위해서 차이가 날 수 있다.
선택된 용량 수준은 이미노슈가의 활성, 투여 경로, 치료하는 증상의 심각성, 및 치료하는 환자의 증상과 이전 병력에 달려있을 수 있다. 그러나, 화합물(들)의 용량을 원하는 치료 효과를 달성하는데 요구되는 것보다 더 낮은 수준으로 시작하여 원하는 효과가 달성될 때까지 점차 용량을 증가시키는 것은 당업계 내의 기술이다. 만약 원한다면, 유효 1일 용량은 투여 목적으로 복수회 용량으로, 예를 들어 하루에 2번 내지 4번 투여와 같이 분할될 수 있다. 그러나, 이는 특정 환자에 대한 특정 용량 수준은 체중, 일반적인 건강, 식이요법, 투여 시간 및 경로, 및 다른 치료제와의 조합 및 치료하는 증상 또는 질환의 심각성을 포함하는 여러 가지 인자에 달려있을 수 있음을 이해할 수 있을 것이다. 성인 인간 1일 투여량은 체중 10 킬로그램 당 약 1 마이크로그램 내지 약 1 그람, 또는 약 10 mg 및 100 mg 사이의 범위의 이미노슈가일 수 있다. 물론, 세포 또는 동물에 투여되어야 하는 이미노슈가의 양은 당업자가 잘 이해하고 있는 수많은 인자, 예컨대 이미노슈가의 분자량 및 투여 경로에 달려있을 수 있다.
본 발명의 방법에서 유용한 제약 조성물은 경구 고형 제제, 점안제, 좌제, 에어로졸제, 국소제 또는 다른 유사한 제제로 전신성으로 투여될 수 있다. 예를 들어, 파우더, 정제, 캡슐, 로젠지(lozenge), 겔, 용액, 현탁액, 시럽 등의 성상(physical form)일 수 있다. 이미노슈가에 추가로, 그러한 제약 조성물은 약 투여를 용이하게 하고 증진시키는 것으로 알려진 제약상 허용가능한 운반체 및 다른 성분을 함유할 수 있다. 다른 가능한 제제, 예컨대 나노입자, 리포좀 방출 적혈구, 및 면역학적 기초 시스템이 또한 이미노슈가를 투여하는데 사용될 수 있다. 그러한 제약 조성물은 많은 경로로 투여될 수 있다. 본원에서 사용된 용어 "비경구"는 피하, 정맥내, 동맥내, 경막내, 및 주사 및 주입 기술을 제한 없이 포함한다. 예로서, 제약 조성물은 경구, 국소, 비경구, 전신성 또는 폐 경로로 투여될 수 있다.
이 조성물들은 1회 용량 또는 다른 시간으로 투여되는 복수회 용량으로 투여될 수 있다. 아레나비리데 과에 속하는 바이러스에 대한 조성물의 억제 효과가 지속될 수 있기 때문에, 숙주 세포는 최소한으로 영향받게 하는 반면 바이러스 증식은 지연시킬 수 있도록 투여 요법을 조정할 수 있다. 예로서, 동물에게 본 발명의 조성물의 1회 분을 1주에 한번씩 투여할 수 있으며, 이로써 숙주 세포 기능은 단지 1주에 한번 짧은 기간 동안만 억제되는 반면, 바이러스 증식은 일주일 내내 지연된다.
본원에 기술된 실시양태는 추가적으로 하기 실시예로 설명되지만, 이에 제한되지는 않는다.
(실시예)
1. N-노닐 DNJ의 합성
방법 : 50-ml, 자석 교반기를 갖춘 1구 둥근 바닥 플라스크에 실온에서 DNJ(500 mg), 에탄올(100 mL), 노나날(530 mg), 및 아세트산(0.5 mL)을 채웠다. 반응 혼합물을 40-45℃로 가열하였고 30-40분 동안 질소 하에서 교반하였다. 반응 혼합물을 상온으로 냉각하였고 Pd/C를 첨가하였다. 반응 플라스크를 배기하였고, 풍선 내 수소 가스로 대체하였다. 이 과정을 세 번 반복하였다. 최종적으로, 반응 혼합물을 상온에서 밤새 교반하였다. 반응의 진행은 TLC(주석 1)로 관찰하였다. 반응 혼합물을 셀라이트(Celite) 패드를 통해 여과하였고 에탄올로 세척하였다. 여과액을 진공 속에서 농축시켜 미정제 생성물을 얻었다. 미정제 생성물을 칼럼 크로마토그래피(230-400 메시(mesh) 실리카 겔)로 정제하였다. 디클로로메탄 내 메탄올의 용매 구배(10-25%)를 사용하여 생성물을 칼럼으로부터 용리하였다. 원하는 생성물을 함유하는 모든 분획물을 합하였고, 진공 속에서 농축시켜 순수한 생성물(420 mg)을 얻었다. 반응의 완결은 박층 실리카 겔 판; 용리액; 메탄올:디클로로메탄 = 1:2를 사용하는 박층크로마토그래피(TLC)로 관찰하였다.
2. N-7-옥사데실 DNJ의 합성
2a. 6-프로필옥시-1-헥사놀의 합성
방법 : 500-ml, 자석 교반기를 갖춘 1구 둥근 바닥 플라스크에 실온에서 1,6-헥산디올(6.00 g), 포타슘 tert-부톡시드(5.413 g)를 채웠다. 반응 혼합물을 1시간 동안 교반하였고, 그 후 1-요오도프로판(8.63 g)을 첨가하였다. 반응 혼합물을 70-80℃로 가열하였고 밤새 교반하였다. 반응의 진행은 TLC(주석 1)로 관찰하였다. 반응의 완결 후, 반응 혼합물에 물을 첨가하였고, 에틸 아세테이트(2 x 100 mL)로 추출하였다. 합한 유기 층들을 진공 속에서 농축시켜서 미정제 생성물을 얻었다. 미정제 생성물을 디클로로메탄에 용해하였고 물, 그 다음 염수로 세척하였고, 소듐 술페이트로 건조하였다. 유기 층을 진공 속에서 농축하여 미정제 생성물을 얻었다. 미정제 생성물을 230-400 메시 실리카 겔을 사용하는 칼럼 크로마토그래피로 정제하였다. 헥산 내 에틸 아세테이트의 용매 구배(10-45%)를 사용하여 생성물을 칼럼으로부터 용리하였다. 원하는 순수한 생성물을 함유하는 모든 분획물을 합하였고, 진공 속에서 농축시켜 순수한 6-프로필옥시-1-헥사놀(품목 D-1029-048, 1.9 g, 25%)을 얻었다. 반응의 완결은 박층크로마토그래피(TLC)(용리액: 헥산 내 60% 에틸 아세테이트)로 관찰하였다.
2b. 6-프로필옥시-1-헥사날의 제조
방법 : 50-ml, 자석 교반기를 갖춘 1구 둥근 바닥 플라스크에 실온에서 6-프로필옥시-1-헥사놀(1.0 g), PDC(4.7 g), 디클로로메탄(10 mL), 셀라이트(1.0 g), 및 소듐 아세테이트(100 mg)를 채웠다. 반응 혼합물을 실온에서 질소 하에서 5분 동안 교반하였다. PDC(4.70 g)를 반응 혼합물에 첨가하였고, 밤새 교반하였다. 반응의 진행은 TLC(주석 1)로 관찰하였다. 반응의 완결 후에, 반응 혼합물을 칼럼(230-400 메시 실리카 겔)에 곧바로 로드하였다. 에틸 아세테이트 내 디클로로메탄의 용매 구배(10-20%)를 사용하여 생성물을 칼럼으로부터 용리하였다. 원하는 순수한 생성물을 함유하는 모든 분획물을 합하였고 진공 속에서 농축시켜 순수한 6-프로필옥시-1-헥사날(품목 D-1029-050, 710 mg, 71%)을 얻었다. 반응의 완결은 박층크로마토그래피(TLC)(용리액: 헥산 내 60% 에틸 아세테이트)로 관찰하였다.
2c N-7-옥사데실-DNJ의 합성
방법 : 50-ml, 자석 교반기를 갖춘 1구 둥근 바닥 플라스크에 실온에서 DNJ(500 mg), 에탄올(15 mL), 6-프로필옥시-1-헥사날(585 mg), 및 아세트산(0.1 mL)을 채웠다. 반응 혼합물을 40-45℃로 가열하였고 질소 하에서 30-40분 동안 교반하였다. 반응 혼합물을 상온으로 냉각하였고 Pd/C를 첨가하였다. 반응 플라스크를 배기하였고, 풍선 내 수소 가스로 대체하였다. 이 과정을 세 번 반복하였다. 최종적으로, 반응 혼합물을 상온에서 밤새 교반하였다. 반응의 진행은 TLC(주석 1)로 관찰하였다. 반응 혼합물을 셀라이트(Celite) 패드를 통해 여과하였고 에탄올로 세척하였다. 여과액을 진공 속에서 농축시켜 미정제 생성물을 얻었다. 미정제 생성물을 칼럼 크로마토그래피(230-400 메시 실리카 겔)로 정제하였다. 디클로로메탄 내 메탄올의 용매 구배(10-40%)를 사용하여 생성물을 칼럼으로부터 용리하였다. 원하는 생성물을 함유하는 모든 분획물을 합하였고, 진공 속에서 농축시켜 순수한 생성물(품목: D-1029-052 (840 mg))을 얻었다. 반응의 완결은 박층크로마토그래피(TLC)(용리액: 디클로로메탄 내 50% 메탄올)로 관찰하였다.
3. N-(9-메톡시)-노닐 DNJ의 합성
3a 9-메톡시-1-노나놀의 제조
방법 : 500-ml, 자석 교반기 및 교반바(stir bar)를 갖춘 1구 둥근 바닥 플라스크에 실온에서 디메틸 술폭시드(100 mL) 및 H2O(100 mL) 내 1,9-노난디올(10.00 g, 62.3 mmol)을 채웠다. 이것에 H2O(10 mL) 내 소듐 히드록시드(5.0 g, 125.0 mmol)의 용액을 실온에서 천천히 첨가하였다. 소듐 히드록시드의 첨가 동안 반응 혼합물은 열을 발생하여 온도가 약 40℃로 올랐다. 혼합물을 한 시간 동안 교반하였고, 그 후 반응 혼합물의 온도를 약 40℃로 유지하면서 디메틸 술페이트(16.52 g, 131 mmol)를 네 번에 걸쳐 첨가하였다. 반응 혼합물을 실온에서 밤새 교반하였다. 반응의 진행은 TLC(주석 1)로 관찰하였다. TLC 관찰은 반응이 25% 전환인 것으로 나타났다. 이 단계에서 추가 디메틸 술페이트(24.78 g, 196.44 mmol)을 첨가하였고 생성된 혼합물을 실온에서 추가 24시간 동안 교반하였다. 반응의 완결 후에, 소듐 히드록시드(물 중 10% 용액)를 반응 혼합물에 첨가하여 용액의 pH를 11-13으로 조정하였다. 혼합물을 실온에서 2시간 동안 교반하였고 디클로로메탄(3 x 100 mL)으로 추출하였다. 합한 유기 층들을 H2O(200 mL), 염수(150 mL)로 세척하였고, 무수 소듐 술페이트(20 g)로 건조하였고, 진공 속에서 여과 및 농축하여 미정제 생성물(14 g)을 수득하였다. 미정제 생성물을 250-400 메시 실리카 겔을 사용하는 칼럼 크로마토그래피로 정제하였다. 헥산 내 에틸 아세테이트의 용매 구배(10-50%)를 사용하여 생성물을 칼럼으로부터 용리하였다. 원하는 순수한 생성물을 함유하는 모든 분획물을 합하였고 진공 속에서 농축시켜 순수한 9-메톡시-1-노나놀(품목 D-1027-155, 2.38 g, 21.9%)을 얻었다. 반응의 완결은 박층 실리카 겔 판; 용리액 : 헥산 내 60% 에틸 아세테이트를 사용하는 박층크로마토그래피(TLC)로 관찰하였다.
3b. 9-메톡시-1-노나날의 제조
방법 : 50-ml, 자석 교반기 및 자석바를 갖춘 1구 둥근 바닥 플라스크에 실온에서 9-메톡시-노나놀(1.0 g, 5.9 mmol), 디클로로메탄(10 mL), 분자 체(1.0 g, 3A), 소듐 아세테이트(0.1 g)를 채웠다. 반응 혼합물에 실온에서 질소 하에서 5분 동안 교반하였다. 반응 혼합물을 피리디늄 디클로메이트(4.7 g, 12.5 mmol)를 채웠고 밤새 교반하였다. 반응의 진행은 TLC(주석 1)로 관찰하였다. 반응의 완결 후에, 반응 혼합물을 실리카 겔 층(약 15 g)을 통해 여과하였다. 여과액을 진공 속에서 증발시켜 미정제 화합물을 얻었다. 이를 실리카 겔 칼럼(250-400 메시, 40 g)을 사용하는 칼럼 크로마토그래피로 정제하였다. 헥산 내 에틸 아세테이트의 용매 구배(10-50%)를 사용하여 생성물을 칼럼으로부터 용리하였다. 원하는 순수한 생성물을 함유하는 모든 분획물을 합하였고, 진공 속에서 농축시켜 9-메톡시-노나날(품목: D-1027-156, 553 mg, 54.4%)을 얻었다. 반응의 완결은 박층 실리카 겔 판; 용리액: 헥산 내 60% 에틸 아세테이트를 사용하는 박층크로마토그래피(TLC)로 관찰하였다.
3c N-(9-메톡시)-노닐 DNJ의 합성
방법 : 50-ml, 자석 교반기 및 자석바를 갖춘 2구 둥근 바닥 플라스크에 실온에서 DNJ(300 mg, 1.84 mmol), 에탄올(20 mL), 9-메톡시-1-노나날(476 mg, 2.76 mmol)을 채웠다. 반응 혼합물을 질소 하에서 5-10분 동안 교반하였고 실온에서 Pd/C를 첨가하였다. 반응 혼합물을 배기하였고, 풍선 내 수소 가스로 대체하였다. 이 과정을 세 번 반복하였고 그 후 반응 혼합물을 실온에서 대기 수소 하에 교반하였다. 반응의 진행은 TLC(주석 1)로 관찰하였다. 반응 혼합물을 셀라이트 층을 통해 여과하였고 에탄올(20 mL)로 세척하였다. 여과액을 진공 속에서 농축시켜 미정제 생성물을 얻었다. 미정제 생성물을 250-400 메시 실리카 겔(20 g)을 사용하는 칼럼 크로마토그래피로 정제하였다. 에틸 아세테이트 내 메탄올의 용매 구배(5-25%)를 사용하여 생성물을 칼럼으로부터 용리하였다. 원하는 순수한 생성물을 함유하는 모든 분획물을 합하였고, 진공 속에서 농축시켜 황백색 고체를 얻었다. 이 고체를 에틸 아세테이트(20 mL) 중에 배산시키고, 여과시키고 고진공으로 건조시켜 백색 고체(품목: D-1027-158 (165.3 mg, 28.1%))를 얻었다. 반응의 완결은 박층 실리카 겔 판; 용리액; 디클로로메탄 내 50% 메탄올을 사용하는 박층크로마토그래피(TLC)로 관찰하였다.
4. 피친데 바이러스에 대한 이미노슈가의 효과
도 5는 하기 UV 이미노슈가 화합물에 의한 피친데 바이러스 방출 억제 데이터를 도시한다: NB-DNJ(UV-1); NN-DNJ(UV-2); N7-O-DNJ(UV-3); N9-DNJ(UV-4); NAP-DNJ(UV-5). 대조군 베로 세포 배양물 및 100 μM의 화합물로 처리된 베로 세포 배양물을 바이러스에 감염시켰고 7일 동안 37℃에서 5% CO2 배양기 내에서 배양했다. 화합물로 처리된 바이러스에 감염된 세포 배양물로부터의 감염성 바이러스 입자의 생산 억제를 플라크 분석으로 측정하였다. 바이러스 플라크 분석을 2%의 우태아혈청, 2 mM L-글루타민, 100 U/ml 페니실린, 100 μg/ml 스트렙토마이신으로 보충된 1x 변형 이글 배지(깁코) 내에 웰 당 5x105 세포 수로 6-웰 플레이트에서 평판배양된 베로 세포에서 수행하였다. 화합물로 처리된 감염된 세포 배양물로부터 수집된 상등액으로부터 역가측정되어야 하는 바이러스를 세포 배양 배지에서 희석하였고 100 μl 부피로 세포에 접종하였고 한 시간 동안 37℃에서 흡착하게 했다. 세포를 2 mM L-글루타민, 100 U/ml 페니실린, 100 μg/ml 스트렙토마이신으로 보충된 1x 변형 이글 배지(깁코) 내 0.6% 아가로스에 덮어씌웠다. 세포를 감염시키고 죽인 감염성 바이러스 입자 각각을 나타내는 죽은 세포의 플라크를 37℃에서 5% CO2 배양기에서 성장시켰고 세포 단층을 뉴트럴 레드로 생-염색시켜 가시화하였다. 실험은 감염성 피친데 바이러스의 방출이 UV 이미노슈가 화합물의 처리 후에 상당히 감소됨을 입증한다.
5. 피친데 및 주닌 바이러스에 대한 이미노슈가의 효과
도 6은 하기 UV 이미노슈가 화합물에 의한 피친데 바이러스 및 주닌 바이러스 방출 억제 데이터를 도시한다: NB-DNJ(UV-1); NN-DNJ(UV-2); N7-O-DNJ(UV-3); N9-DNJ(UV-4); NAP-DNJ(UV-5).
화합물. 하기 화합물의 기준 모액을 디메틸술폭시드(DMSO)에서 0.5%의 최종 최대 DMSO 농도까지 제조하였다: UV-1, UV-2, UV-3, UV-4 및 UV-5. 모든 화합물을 기준 모액으로부터 그것의 실험상 농도까지 희석하였다.
바이러스. 화합물을 피친데 바이러스(아레나바이러스) CoAn 3739 균주, 및 주닌(아레나바이러스) 후보 #1 균주에 대한 억제에 대해 스크리닝하였다. 2%의 우태아혈청, 2 mM L-글루타민, 100 U/ml 페니실린, 100 μg/ml 스트렙토마이신으로 보충된 변형 이글 배지(MEM, 시그마)를 사용하는 베로 세포에서의 증식으로 바이러스 모액을 만들었고 표준 플라크 분석(방법은 아래에 나타냈다)을 사용하여 역가측정하였다. 바이러스 모액을 사용하기 전까지 -80℃에서 저장하였다.
바이러스 수득 감소 분석. 바이러스 수득 분석을 다른 이미노슈가의 농도에서 배양한 바이러스-감염 세포에서 발생한 상등액 샘플에 대한 표준 플라크 분석으로 수행하였다. 24-웰 세포 배양 플레이트에 2 mM L-글루타민, 100 U/mL 페니실린/스트렙토마이신, 및 2%의 열-불활성 우태아혈청으로 보충된 얼스 염(Earl's salt)(시그마, 세인트루이스, MO)을 가지는 MEM 내 10%의 우태아혈청 베로 세포(ATCC, 만나사스, VA; ATCC 번호 CCL-81)를 가지는 1 mL MEM 내 세포를 뿌렸고, 37℃에서 24시간 동안 또는 약 80% 조밀도 까지 인큐베이션하였다. 배지를 2%의 우태아혈청으로 보충된 배지로 대체하였고 500 μM, 250 μM 또는 125 μM의 화합물 농도를 사용하여 시작하였고 8번의 희석을 사용하여 3번 시험하였다.
화합물을 적절한 웰에 첨가하였고 1시간 동안 37℃, 5% CO2에서 인큐베이션하였다. 한시간 인큐베이션 후에 바이러스를 각 웰에 첨가하였다. PICV 바이러스 감염에 대해서는 4일, JUNV 바이러스 감염에 대해서는 5일이 필요하다. 감염의 완료시, 역가측정하기 위해 상등액을 수집하였다. PICV 및 JUNV를 역가측정하기 위해서, 성장 배지에서 80%의 조밀도의 베로 세포를 가지는 12-웰 플레이트를 사용하였다. 바이러스 상등액을 10-3 내지 10-8로 희석하였고 세포에 첨가하였고(100 μL) 37℃에서 1시간 동안 매 5-10분마다 흔들면서 인큐베이션하였다. 바이러스 감염 배지(100 μL)를 흡입하였고 사전에 따뜻하게 해놓은 2% 저용융(low-melt) 아가로스 1 mL와 2X MEM(5%의 신생우아혈청)이 1:1로 혼합된 것으로 교체하였고 37℃, 5% CO2에서 6일 동안 인큐베이션하였고 그 후에 플라크를 뉴트럴 레드 염색으로 가시화하였다. IC50을 50% 바이러스 억제를 야기하는 화합물의 농도로 정하였다.
도 7은 대조군, UV-1, UV-3 및 UV-4 화합물에 대한 피친데 바이러스의 억제를 비교한다.
화합물. 하기 화합물의 기준 모액을 디메틸술폭시드(DMSO)에서 0.5%의 최종 최대 DMSO 농도까지 제조하였다: UV-1, UV-2, UV-3, UV-4, UV-5. 모든 화합물을 기준 모액으로부터 그것의 실험상 농도까지 희석하였다.
바이러스. 화합물을 피친데 바이러스 CoAn 3739 균주에 대한 억제에 대해 스크리닝하였다.
결과: 바이러스 수득 분석을 상기 기술한 것과 같이 수행하였다. 화합물 NB-DNJ, N7-O-DNJ, 및 N9-DNJ에 대한 PICV CoAn 3739 균주 바이러스 억제를 밝혀냈다. 시험관내 PICV 억제는 100 μM의 이미노슈가 농도에서 NB-DNJ에 의해서는 50% 초과의 억제, N7-O-DNJ에 의해서는 70% 초과의 억제, N9-DNJ에 의해서는 99% 초과의 억제를 초래하였다.
도 8은 UV-1, UV-2, UV-3, UV-4 및 UV-5 이미노슈가에 의한 주닌 바이러스에 대한 억제 플롯을 이미노슈가 화합물의 농도 대 대조군과 비교한 바이러스 감염성의 백분율로 도시한다.
화합물. 하기 화합물의 기준 모액을 디메틸술폭시드(DMSO)에서 0.5%의 최종 최대 DMSO 농도까지 제조하였다: UV-1, UV-2, UV-3, UV-4, UV-5. 모든 화합물을 기준 모액으로부터 그것의 실험상 농도까지 희석하였다.
바이러스. 화합물을 주닌 바이러스 후보 #1 균주에 대한 억제에 대해 스크리닝하였다.
결과: 바이러스 수득 분석을 상기 기술한 것과 같이 수행하였다. 350 μM의 EC50을 가지는 화합물 NB-DNJ에 대한 주닌 바이러스 억제를 밝혀냈다. 60 μM의 EC50을 가지는 NN-DNJ 및 10 μM의 EC50을 가지는 NAP-DNJ는 보호를 보였다. 화합물 N7-O-DNJ 및 N9-DNJ는 500 μM가 넘는 EC50을 가졌다.
* * *
비록 앞서 말한 것은 특정 바람직한 실시양태를 나타낸 것이지만, 본 발명이 이렇게 제한되지 않는 것으로 이해될 것이다. 당업자가 개시된 실시양태에 대한 다양한 변형을 행할 수 있고 그러한 변형이 본 발명의 범위 내로 의도되는 것이 있을 수 있다. 본 명세서에서 인용된 모든 공개, 특허 출원 및 특허는 참고문헌으로 전체로서 삽입된다.
Claims (23)
- 치료를 요하는 환자에게 하기 화학식의 화합물 또는 그의 제약상 허용가능한 염 유효량을 투여하는 것을 포함하는, 아레나비리데(Arenaviridae) 과에 속하는 바이러스에 의해 유발되거나 그와 관련된 질환 또는 증상의 치료 또는 예방 방법:
상기 식에서,
R은 치환 또는 비치환된 알킬기, 치환 또는 비치환된 시클로알킬기, 치환 또는 비치환된 아릴기, 또는 치환 또는 비치환된 옥사알킬기로부터 선택된 것이거나; 또는
R은
이고
(여기서, R1은 치환 또는 비치환 알킬기이며;
X1-5는 H, NO2, N3, 또는 NH2로부터 독립적으로 선택된 것이고;
Y는 부재 또는 카보닐을 제외한 치환 또는 비치환된 C1-알킬기이며; 및
Z는 결합 또는 NH에서 선택된 것이되; 단 Z가 결합일 경우, Y는 부재이고, 단 Z가 NH일 경우에는, Y는 카보닐을 제외한 치환 또는 비치환된 C1-알킬기이다); 및
W1-4는 수소, 치환 또는 비치환된 알킬기, 치환 또는 비치환된 할로알킬기, 치환 또는 비치환된 알카노일기, 치환 또는 비치환된 아로일기, 또는 치환 또는 비치환된 할로알카노일기로부터 독립적으로 선택된 것이다. - 제1항에 있어서, 상기 각 W1, W2, W3 및 W4는 수소인 방법.
- 제1항에 있어서, 상기 R은 치환 또는 비치환된 알킬기, 치환 또는 비치환된 시클로알킬기, 치환 또는 비치환된 아릴기, 또는 치환 또는 비치환된 옥사알킬기로부터 선택된 것인 방법.
- 제1항에 있어서, 상기 R은 C2-C12 알킬기인 방법.
- 제1항에 있어서, 상기 R은 C3-C6 알킬기인 방법.
- 제1항에 있어서, 상기 투여가 B-부틸 데옥시노지리마이신 또는 그의 제약상 허용가능한 염을 투여하는 것을 포함하는 방법.
- 제1항에 있어서, 상기 R은 옥사알킬기인 방법.
- 제1항에 있어서, 상기 R은 1개 내지 3개의 산소 원자를 함유하는 C2-C16 옥사알킬기인 방법.
- 제1항에 있어서, 상기 R은 1개 내지 2개의 산소 원자를 함유하는 C6-C12 옥사알킬기인 방법.
- 제1항에 있어서, 상기 투여가 N-(7-옥사데실)데옥시노지리마이신 또는 그의 제약상 허용가능한 염을 투여하는 것을 포함하는 방법.
- 제1항에 있어서, 상기 투여가 N-(9-메톡시노닐)데옥시노지리마이신 또는 그의 제약상 허용가능한 염을 투여하는 것을 포함하는 방법.
- 제12항에 있어서, 상기 X1은 NO2이고, X3는 N3인 방법.
- 제12항에 있어서, 상기 각 X2, X4 및 X5는 수소인 방법.
- 제1항에 있어서, 상기 투여가 N-(N-{4'-아지도-2'-니트로페닐}-6-아미노헥실)데옥시노지리마이신 또는 그의 제약상 허용가능한 염을 투여하는 것을 포함하는 방법.
- 제1항에 있어서, 상기 환자는 포유류인 방법.
- 제1항에 있어서, 상기 환자는 인간인 방법.
- 제1항에 있어서, 상기 바이러스는 입피 바이러스(Ippy virus); 라사 바이러스(Lassa virus); 림프구성 맥락수막염 바이러스; 모발라 바이러스(Mobala virus); 모페이아 바이러스(Mopeia virus); 아마파리 바이러스(Amapari virus); 플렉살 바이러스(Flexal virus); 구아나리토 바이러스(Guanarito virus); 주닌 바이러스(Junin virus); 라티노 바이러스(Latino virus); 마추포 바이러스(Machupo virus); 올리베로스 바이러스(Oliveros virus); 파라나 바이러스(Parana virus); 피친데 바이러스(Pichinde virus); 피리탈 바이러스(Pirital virus); 사비아 바이러스(Sabia virus); 타카리베 바이러스(Tacaribe virus); 타미아미 바이러스(Tamiami virus); 화이트워터 아로요 바이러스(Whitewater Arroyo virus); 및 샤페어 바이러스(Chapare virus)로부터 선택된 것인 방법.
- 제1항에 있어서, 상기 바이러스는 피친데 바이러스인 방법.
- 제1항에 있어서, 상기 바이러스는 주닌 바이러스인 방법.
- 제1항에 있어서, 상기 질환 또는 증상은 림프구성 맥락수막염; 라사열; 아르헨티나 출혈열; 볼리비아 출혈열; 브라질 출혈열; 타카리베열; 베네수엘라 출혈열; 플렉살 바이러스와 관련된 인플루엔자-유사 질병; 및 화이트워터 아로요 바이러스와 관련된 출혈열로부터 선택된 것인 방법.
- 제1항에 있어서, 상기 질환 또는 증상은 아르헨티나 출혈열인 방법.
- 제1항에 있어서, 상기 질환 또는 증상은 라사열인 방법.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US20239109P | 2009-02-24 | 2009-02-24 | |
| US61/202,391 | 2009-02-24 | ||
| US27225109P | 2009-09-04 | 2009-09-04 | |
| US61/272,251 | 2009-09-04 | ||
| PCT/US2010/024914 WO2010099064A1 (en) | 2009-02-24 | 2010-02-22 | Iminosugars and methods of treating arenaviral infections |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020117021910A Division KR101787434B1 (ko) | 2009-02-24 | 2010-02-22 | 이미노슈가 및 아레나바이러스성 감염을 치료하는 방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170117614A true KR20170117614A (ko) | 2017-10-23 |
Family
ID=42665853
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177029196A KR20170117614A (ko) | 2009-02-24 | 2010-02-22 | 이미노슈가 및 아레나바이러스성 감염을 치료하는 방법 |
| KR1020117021910A KR101787434B1 (ko) | 2009-02-24 | 2010-02-22 | 이미노슈가 및 아레나바이러스성 감염을 치료하는 방법 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020117021910A KR101787434B1 (ko) | 2009-02-24 | 2010-02-22 | 이미노슈가 및 아레나바이러스성 감염을 치료하는 방법 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20100222384A1 (ko) |
| EP (1) | EP2400843B1 (ko) |
| JP (1) | JP5951996B2 (ko) |
| KR (2) | KR20170117614A (ko) |
| CN (1) | CN102625660B (ko) |
| CA (1) | CA2753194A1 (ko) |
| ES (1) | ES2562635T3 (ko) |
| HK (1) | HK1165675A1 (ko) |
| WO (1) | WO2010099064A1 (ko) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102655746B (zh) | 2009-02-23 | 2016-08-03 | 联合治疗公司 | 亚氨基糖以及治疗病毒性疾病的方法 |
| IN2014MN02539A (ko) | 2012-06-06 | 2015-07-24 | Unither Virology Llc | |
| CN102775384B (zh) * | 2012-07-27 | 2015-05-27 | 中国科学院化学研究所 | 小钩树碱i和j类似物及其制备方法与应用 |
| CN106102464A (zh) * | 2013-05-02 | 2016-11-09 | 牛津大学之校长及学者 | 采用亚氨基糖的糖脂抑制 |
| RU2702133C2 (ru) | 2013-09-16 | 2019-10-04 | ЭМЕРГЕНТ ВИРОЛОДЖИ ЭлЭлСи | Производные дезоксинойиримицина и способы их применения |
| IT202000008917A1 (it) * | 2020-04-24 | 2021-10-24 | Biovalley Invest Partner S R L | Composizioni antivirali |
Family Cites Families (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1555654A (en) * | 1977-06-25 | 1979-11-14 | Exxon Research Engineering Co | Agricultural burner apparatus |
| NO154918C (no) * | 1977-08-27 | 1987-01-14 | Bayer Ag | Analogifremgangsmaate til fremstilling av terapeutisk aktive derivater av 3,4,5-trihydroksypiperidin. |
| DE2834122A1 (de) * | 1978-08-03 | 1980-02-14 | Bayer Ag | Verfahren zur herstellung von 6-amino-6-desoxy-l-sorbose |
| DE2839309A1 (de) * | 1978-09-09 | 1980-03-27 | Bayer Ag | 3,4,5-trihydroxypiperidin-derivate |
| DE2853573A1 (de) * | 1978-12-12 | 1980-07-03 | Bayer Ag | Herstellung von n-substituierten derivaten des l-desoxynojirimycins |
| DE3038901A1 (de) * | 1980-10-15 | 1982-05-06 | Bayer Ag, 5090 Leverkusen | Verfahren zur herstellung von n-substituierten derivaten des 1-desoxynojirimycins |
| DE3611841A1 (de) * | 1986-04-09 | 1987-10-15 | Bayer Ag | Verfahren zur herstellung von 1-desoxynojirimycin und dessen n-derivaten |
| US5043273A (en) * | 1989-08-17 | 1991-08-27 | Monsanto Company | Phosphorylated glycosidase inhibitor prodrugs |
| US5103008A (en) * | 1989-08-17 | 1992-04-07 | Monsanto Company | Compound, N-butyl-deoxynojirimycin-6-phosphate |
| US4994572A (en) * | 1989-10-12 | 1991-02-19 | Monsanto Company | Synthesis of nojirimycin derivatives |
| US5030638A (en) * | 1990-02-26 | 1991-07-09 | G. D. Searle & Co. | Method of antiviral enhancement |
| US5200523A (en) * | 1990-10-10 | 1993-04-06 | Monsanto Company | Synthesis of nojirimycin derivatives |
| US5206251A (en) * | 1992-04-01 | 1993-04-27 | G. D. Searle & Co. | 2- and 3- amino and azido derivatives of 1,5-iminosugars |
| US5399567A (en) * | 1993-05-13 | 1995-03-21 | Monsanto Company | Method of treating cholera |
| AU1876095A (en) * | 1994-02-25 | 1995-09-11 | G.D. Searle & Co. | Use of 1-deoxynojirimycin and its derivatives for treating mammals infected with respiratory syncytial virus |
| EP1037636A4 (en) * | 1997-12-11 | 2004-08-18 | Univ Oxford | INHIBITATION OF MEMBRANE-TIED VIRAL REPLICATION |
| US6689759B1 (en) * | 1998-02-12 | 2004-02-10 | G. D. Searle & Co. | Methods of Treating hepatitis virus infections with N-substituted-1,5-dideoxy-1,5-imino-d-glucitol compounds in combination therapy |
| US6610703B1 (en) * | 1998-12-10 | 2003-08-26 | G.D. Searle & Co. | Method for treatment of glycolipid storage diseases |
| GB9828474D0 (en) * | 1998-12-24 | 1999-02-17 | British Aerospace | Surface topology inspection |
| WO2000047198A2 (en) * | 1999-02-12 | 2000-08-17 | G.D. Searle & Co. | Use of substituted-1,5-dideoxy-1,5-imino-d-glucitol compounds for treating hepatitis virus infections |
| GB0100889D0 (en) * | 2001-01-12 | 2001-02-21 | Oxford Glycosciences Uk Ltd | Compounds |
| WO2001007078A1 (en) * | 1999-07-26 | 2001-02-01 | G.D. Searle & Co. | Use of long-chain n-alkyl derivates of deoxynojirimycin and a glucocerebrosidase enzyme for the manufacture of medicament for the treatment of glycolipid storage diseases |
| US7256005B2 (en) * | 1999-08-10 | 2007-08-14 | The Chancellor, Masters And Scholars Of The University Of Oxford | Methods for identifying iminosugar derivatives that inhibit HCV p7 ion channel activity |
| US6565487B1 (en) * | 2000-07-17 | 2003-05-20 | Hai Pin Kuo | Exerciser having a forward and rearward adjusting seat |
| PT2444102E (pt) * | 2003-01-31 | 2015-09-17 | Sinai School Medicine | Terapia combinada para o tratamento de distúrbios de deficiência proteica |
| US7446098B2 (en) * | 2003-02-18 | 2008-11-04 | Mount Sinai School Of Medicine Of New York University | Combination therapy for treating protein deficiencies |
| US20060211752A1 (en) * | 2004-03-16 | 2006-09-21 | Kohn Leonard D | Use of phenylmethimazoles, methimazole derivatives, and tautomeric cyclic thiones for the treatment of autoimmune/inflammatory diseases associated with toll-like receptor overexpression |
| US20050256168A1 (en) * | 2004-04-28 | 2005-11-17 | Block Timothy M | Compositions for oral administration for the treatment of interferon-responsive disorders |
| US7524829B2 (en) * | 2004-11-01 | 2009-04-28 | Avi Biopharma, Inc. | Antisense antiviral compounds and methods for treating a filovirus infection |
| GB0501352D0 (en) * | 2005-01-21 | 2005-03-02 | Slingsby Jason H | Use of glycosylation modulators in combination with membrane fusion inhibitors for treatment of infections caused by viruses bearing glycosylated envelope |
| JP2008533175A (ja) * | 2005-03-16 | 2008-08-21 | ユニバーシティ・オブ・オックスフォード | Hiv−1のためのマンノース免疫原 |
| CN101355971A (zh) * | 2005-05-17 | 2009-01-28 | 阿米库斯治疗学公司 | 使用1-去氧野尻霉素衍生物治疗庞皮病的方法 |
| MX2007014470A (es) * | 2005-05-17 | 2008-02-06 | Amicus Therapeutics Inc | Metodo para el tratamiento de enfermedad de pompe usando derivados de 1-desoxinojirimicina. |
| CA2616537A1 (en) * | 2005-07-27 | 2007-02-01 | University Of Florida Research Foundation, Inc. | Small compounds that correct protein misfolding and uses thereof |
| BRPI0615974A2 (pt) * | 2005-07-27 | 2011-05-31 | Univ Florida | uso de choque térmico para tratar uma doença ocular em um indivìduo, método para recrutar uma célula-tronco para um tecido ocular de um indivìduo com necessidade da mesma, uso de choque térmico para tratar uma doença ou um distúrbio ocular em um indivìduo com necessidade do mesmo, uso de choque térmico para regenerar a retina em um indivìduo com necessidade do mesmo, uso de choque térmico para reparar os danos ao epitélio pgmentar da retina em um indivìduo com necessidade do mesmo, uso de choque térmico para tratar a degeneração macular em um indivìduo com necessidade do mesmo, composição farmacêutica para o recrutamento de células-tronco, composição farmacêutica para recrutamento de células-tronco em um tecido ocular, kit e método para identificar um agente que aumenta o recrutamento de células-tronco em um tecido ocular |
| US20070244184A1 (en) * | 2006-01-09 | 2007-10-18 | Simon Fraser University | Glycosidase inhibitors and methods of synthesizing same |
| JP2009538276A (ja) * | 2006-04-24 | 2009-11-05 | アカデミッシュ メディシュ セントラム | 嚢胞性線維症の改良型治療 |
| EP2023927B1 (en) * | 2006-05-24 | 2015-02-25 | United Therapeutics Corporation | Deoxynojirimycin and d-arabinitol analogs and methods of using |
| EP2049126A2 (en) * | 2006-08-02 | 2009-04-22 | United Therapeutics Corporation | Liposome treatment of viral infections |
| WO2008063727A2 (en) * | 2006-08-21 | 2008-05-29 | United Therapeutics Corporation | Combination therapy for treatment of viral infections |
| WO2009118658A2 (en) * | 2008-03-26 | 2009-10-01 | University Of Oxford | Endoplasmic reticulum targeting liposomes |
| US9040488B2 (en) * | 2008-09-02 | 2015-05-26 | Baruch S. Blumberg Institute | Imino sugar derivatives demonstrate potent antiviral activity and reduced toxicity |
-
2010
- 2010-02-22 EP EP10746681.5A patent/EP2400843B1/en not_active Not-in-force
- 2010-02-22 KR KR1020177029196A patent/KR20170117614A/ko not_active Application Discontinuation
- 2010-02-22 WO PCT/US2010/024914 patent/WO2010099064A1/en active Application Filing
- 2010-02-22 CN CN201080017592.8A patent/CN102625660B/zh not_active Expired - Fee Related
- 2010-02-22 CA CA2753194A patent/CA2753194A1/en not_active Abandoned
- 2010-02-22 JP JP2011551272A patent/JP5951996B2/ja not_active Expired - Fee Related
- 2010-02-22 ES ES10746681.5T patent/ES2562635T3/es active Active
- 2010-02-22 US US12/656,993 patent/US20100222384A1/en not_active Abandoned
- 2010-02-22 KR KR1020117021910A patent/KR101787434B1/ko active IP Right Grant
-
2012
- 2012-07-04 HK HK12106531.9A patent/HK1165675A1/xx not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| ES2562635T3 (es) | 2016-03-07 |
| WO2010099064A1 (en) | 2010-09-02 |
| HK1165675A1 (en) | 2012-10-12 |
| CN102625660A (zh) | 2012-08-01 |
| EP2400843A4 (en) | 2012-01-04 |
| JP2012518648A (ja) | 2012-08-16 |
| US20100222384A1 (en) | 2010-09-02 |
| EP2400843B1 (en) | 2015-11-11 |
| KR20120042718A (ko) | 2012-05-03 |
| CN102625660B (zh) | 2015-03-11 |
| JP5951996B2 (ja) | 2016-07-13 |
| CA2753194A1 (en) | 2010-09-02 |
| KR101787434B1 (ko) | 2017-11-15 |
| EP2400843A1 (en) | 2012-01-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2440205B1 (en) | Iminosugars for use in the treatment of bunyaviral and togaviral diseases | |
| KR101787434B1 (ko) | 이미노슈가 및 아레나바이러스성 감염을 치료하는 방법 | |
| US9943532B2 (en) | Iminosugars and methods of treating viral diseases | |
| JP5752689B2 (ja) | フィロウイルス疾患を治療するイミノ糖および方法 | |
| KR101459530B1 (ko) | 폭스바이러스 감염의 치료 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |