KR20170086542A - 항-스타필로코쿠스 아우레우스 항체 리파마이신 콘주게이트 및 그것의 용도 - Google Patents
항-스타필로코쿠스 아우레우스 항체 리파마이신 콘주게이트 및 그것의 용도 Download PDFInfo
- Publication number
- KR20170086542A KR20170086542A KR1020177015225A KR20177015225A KR20170086542A KR 20170086542 A KR20170086542 A KR 20170086542A KR 1020177015225 A KR1020177015225 A KR 1020177015225A KR 20177015225 A KR20177015225 A KR 20177015225A KR 20170086542 A KR20170086542 A KR 20170086542A
- Authority
- KR
- South Korea
- Prior art keywords
- antibody
- antibiotic
- conjugate compound
- ser
- aac
- Prior art date
Links
- 0 C[C@@]([C@]([C@@](C)[C@@]([C@](C)[C@](C=CO[C@@]1(C)Oc2c(C)c(O)c(C(C(*C3*)NC(C(C)=CC=C[C@@]4C)=O)O)c3c2C1=O)OC)O*)O)[C@]4O Chemical compound C[C@@]([C@]([C@@](C)[C@@]([C@](C)[C@](C=CO[C@@]1(C)Oc2c(C)c(O)c(C(C(*C3*)NC(C(C)=CC=C[C@@]4C)=O)O)c3c2C1=O)OC)O*)O)[C@]4O 0.000 description 5
- LBVZINOLAFTARU-UHFFFAOYSA-N CNC(CBr)=O Chemical compound CNC(CBr)=O LBVZINOLAFTARU-UHFFFAOYSA-N 0.000 description 1
- LQCMHIRUSQXMHX-REVFNZDPSA-N C[C@H](C[C@@H](C)/C=C/C=C(/C)\C(NC1=C2Oc3cc(N(CC4)CCN4C(OCc(cc4)ccc4NC([C@H](CCCNC(N)=O)NC(C4(CCC4)C(NCCCCCN(C(C=C4)=O)C4=O)=O)=O)=O)=O)cc(O)c3N=C2c2c(C([C@](C)(O3)O/C=C/[C@@H]([C@@H](C)[C@H]([C@@H]4C)OC(C)=O)OC)=O)c3c(C)c(O)c2C1=O)=O)[C@H]4O Chemical compound C[C@H](C[C@@H](C)/C=C/C=C(/C)\C(NC1=C2Oc3cc(N(CC4)CCN4C(OCc(cc4)ccc4NC([C@H](CCCNC(N)=O)NC(C4(CCC4)C(NCCCCCN(C(C=C4)=O)C4=O)=O)=O)=O)=O)cc(O)c3N=C2c2c(C([C@](C)(O3)O/C=C/[C@@H]([C@@H](C)[C@H]([C@@H]4C)OC(C)=O)OC)=O)c3c(C)c(O)c2C1=O)=O)[C@H]4O LQCMHIRUSQXMHX-REVFNZDPSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A61K47/48384—
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5383—1,4-Oxazines, e.g. morpholine ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A61K47/48507—
-
- A61K47/48715—
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6889—Conjugates wherein the antibody being the modifying agent and wherein the linker, binder or spacer confers particular properties to the conjugates, e.g. peptidic enzyme-labile linkers or acid-labile linkers, providing for an acid-labile immuno conjugate wherein the drug may be released from its antibody conjugated part in an acidic, e.g. tumoural or environment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from bacteria
- C07K16/1267—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from bacteria from Gram-positive bacteria
- C07K16/1271—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from bacteria from Gram-positive bacteria from Micrococcaceae (F), e.g. Staphylococcus
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
Abstract
본 발명은 rF1 항체 항생제 콘주게이트 및 이를 사용하는 방법을 제공한다.
Description
관련
출원에 대한 교차참조
본원은 모든 목적을 위해 그 전체적으로 본 명세서에 참조로 편입되는, 2014년 12월 3일자로 출원된 미국 가출원 번호 62/087,213을 우선권으로 주장한다.
서열목록
본원은 ASCII 포맷으로 전자적으로 제출되고 이로써 전체적으로 참고로 편입되는 서열 목록을 포함한다. 2015년 12월 1일에 작성된 상기 ASCII 사본은 P32350WO_PCTSequenceListing.txt로 명명되며 크기는 26,747 바이트이다.
기술 분야
본 발명은 리파마이신-유형 항생제에 콘주게이트된 항-스타필로코쿠스 항체와 스타필로코쿠스 감염의 치료에 수득한 항체-항생제 콘주게이트의 사용에 대한 것이다.
스타필로코쿠스 아우레우스 및 S. 에피더미디스는 비공 및 피부에 주로 대량서식하는 성공적인 인간 공생자이다. 스타필로코쿠스 아우레우스 (S. 아우레우스; SA)는 또한 다양한 조직에 침투할 수 있어 생명을 위협하는 감염을 일으킬 수 있다; 이것은 전세계적으로 인간에게 박테리아 감염의 주된 원인이다. S. 아우레우스의 최근에 부각된 균주는 증가된 발병력을 보이고 그렇지 않은 경우 건강한 개체에게 질병을 야기하는 향상된 능력을 보인다. 지난 수십 년에 걸쳐, 모든 공지된 베타-락탐 항생제에 내성을 갖는 메티실린-내성있는 S. 아우레우스 (MRSA)의 출현 및 급속한 확산으로 인해 S. 아우레우스로의 감염은 치료하는 것이 점점 더 어려워졌다 (Boucher, H.W., 등 (2009) Clin Infect Dis 48, 1-12). 현재, 메티실린 내성있는 S. 아우레우스 (MRSA)의 가장 보편적이고 가장 독성이 강한 임상 균주는 다수의 발병력 인자를 생성하고 감염된 개체에서 사망을 유발할 수 있는 능력을 가진 USA300이다 (Chambers, HF 및 Deleo FR (2009) Nature Reviews Microbiology 7:629-641). 가장 심각한 감염 예컨대 심내막염, 골수염, 괴사성 폐렴 및 패혈증은 혈류로 박테리아의 전파에 따라 발생한다 (Lowy, F.D. (1998) N Engl J Med 339, 520-532). S. 아우레우스에 밀접하게 관련된 S. 에피더미디스는 종종 병원 획득 감염과 관련되고, 그리고 의료 기기에 살고있는 가장 흔한 감염원을 대표한다.
스타필로코쿠스에 존재하여, 숙주 조직에 스타필로코시(staphylococci) 접착 및 숙주 조직의 성공적인 군집화에 중요한, 콘주게이트 A-도메인에 인접한 세린-아스파르테이트 디펩티드 (SDR) 반복의 큰 연신부로 특성화되는, 세포벽 단백질의 계열이다 (Foster TJ, Hook M (1998) Trends Microbiol 6: 484-488). 부착에 중요한 그와 같은 단백질은 군집 인자 (Clf)A 및 ClfB를 포함한다 (Foster TJ, 상기). ClfA 및 ClfB에 부가하여, S. 아우레우스는 또한 게놈에서 일렬로 조직화된 세 개 SDR-단백질인, SdrC, SdrD 및 SdrE를 발현한다. 이들 단백질은 또한 조직 군집화에 관여되는 것으로 생각되며, 이들 중 임의의 하나의 제거는 박테리아 발병력을 감소시킨다 (Cheng AG, 등 (2009) FASEB Journal 23: 3393-3404). 이 계열의 세 가지 추가의 구성원인, SrdF, SdrG 및 SdrH는 대부분 S. 에피더미디스 균주에 존재한다 (McCrea KW, 등 (2000) The serine-aspartate repeat (Sdr) protein family in Staphylococcus epidermidis. Microbiology 146 (Pt 7): 1535-1546). 각각의 이들 단백질에서, 25 및 275 SD-디펩티드 반복 (서열 번호: 24) 사이에 포함하는 SDR-영역은 N-말단 리간드-결합 A-도메인과 C-말단 LPXTG-모티프 (서열 번호: 25) 사이에 위치되어, 트랜스펩티다아제 소르타제 A에 의한 세포벽에 고착을 매개한다. SDR-도메인의 기능은, 이들 단백질의 N 말단 리간드 결합 부위의 노출을 허용하는 세포벽 스패닝 도메인으로서 작용한다고 제안되었지만, 아직 미공지되어 있다 (Hartford O, 등 (1997) Mol Microbiol 25: 1065-1076).
S. 아우레우스 및 S. 에피더미디스의 모든 SDR-단백질의 SDR-도메인은 두 단계로 글리코실화에 관여하는 두 신규 글리코실전달효소인, SdgA 및 SdgB에 의해 크게 글리코실화됨이 발견되었다 (Hazenbos 등 (2013) PLOS Pathogens 9 (10):1-18). 이들 글리코실화 발생은 숙주 프로테아제에 의한 이들 단백질의 분해를 방지하고, 그렇게 함으로써 박테리아 숙주 조직 상호작용을 보전한다. Hazenbos 등 (2013)은 또한 SdgB-매개된 글리코실화가 인간에서 고도의 옵소닉 항체에 대한 면역우성 에피토프를 생성함을 보였다. 이들 항체는 총 항-스타필로코시 IgG 반응의 유의미한 부분을 차지한다.
침습성 MRSA 감염은 ~20%의 사망률로 치료하기 힘들고 그리고 미국에서 감염원에 의한 사망의 주된 원인이다. 반코마이신, 리네졸라이드 및 다프토마이신은 따라서 침습성 MRSA 감염을 치료하기 위한 선택의 소수 항생제가 되었다 (Boucher, H., Miller, L.G. & Razonable, R.R. (2010) Clin Infect Dis 51 Suppl 2, S183-197). 그러나, 반코마이신에 대한 감소된 감수성 리네졸라이드 및 다프토마이신에 대한 교차-내성이 MRSA 임상 균주에서 이미 보고되었다 (Nannini, E., Murray, B.E. & Arias, C.A. (2010) Curr Opin Pharmacol 10, 516-521). 경시적으로, 내성을 극복하기 위해 필요한 반코마이신 용량은 신장 독성이 나타나는 수준까지 상향 증진되었다. 따라서, 이들 항생제에도 불구하고 침습성 MRSA 감염으로부터 사망률과 이환율은 여전히 높다.
조사는 S. 아우레우스가 박테리아 청소능을 담당하는 식세포를 포함하여 포유동물 세포 내로 침투 및 생존할 수 있다는 것을 밝혔다 (Thwaites, G.E. & Gant, V. (2011) Nat Rev Microbiol 9, 215-222); Rogers, D.E., Tompsett, R. (1952) J. Exp . Med 95, 209-230); Gresham, H.D., 등 (2000) J Immunol 164, 3713-3722); Kapral, F.A. & Shayegani, M.G. (1959) J Exp Med 110, 123-138; Anwar, S., 등 (2009) Clin Exp Immunol 157, 216-224); Fraunholz, M. & Sinha, B. (2012) Front Cell Infect Microbiol 2, 43); Garzoni, C. & Kelley, W.L. (2011) EMBO Mol Med 3, 115-117). S. 아우레우스는 정맥내 감염 후 몇 분 내, 주로 호중구 및 대식세포인 숙주 식균세포에 의해 흡수된다 (Rogers, D.E. (1956) JEM 103, 713). 대다수의 박테리아가 이들 세포에 효과적으로 사멸되지만, 혈액 매개 식균세포 내에서 S. 아우레우스의 불완전한 청소능은 이들 감염된 세포가 초기 감염의 부위에 떨어져 박테리아의 전파를 위한 "트로이의 목마"로 작용하게 할 수 있다. 사실상, 정상 호중구 수가 있는 환자는 감소된 호중구 수가 있는 환자보다 파종성 질환에 더 쉽게 걸릴 수 있다 (Thwaites, G.E. & Gant, V. (2011) 상기). 일단 조직에 전달되면, S. 아우레우스는 다양한 비-식세포 세포 유형을 침범할 수 있고, 그리고 조직 내 세포내 S. 아우레우스는 만성적 또는 재발성 감염과 관련된다. 더욱이, 차선 항생제 농도에 세포내 박테리아의 노출은 항생제 내성있는 균주의 출현을 촉진할 수 있어, 이 임상 문제를 더욱 심각하게 만든다. 이들 관찰과 일치하게, 반코마이신 또는 다프토마이신으로 균혈증 또는 심내막염과 같은 침습성 MRSA 감염 환자의 치료는 50%보다 더 큰 실패율과 관련된다 (Kullar, R., Davis, S.L., Levine, D.P. & Rybak, M.J. Impact of vancomycin exposure on outcomes in patients with methicillin-resistant Staphylococcus aureus bacteremia: support for consensus guidelines suggested targets. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America 52, 975-981 (2011); Fowler, V.G., Jr. et al. Daptomycin versus standard therapy for bacteremia and endocarditis caused by Staphylococcus aureus. The New England journal of medicine 355, 653-665 (2006); Yoon, Y.K., Kim, J.Y., Park, D.W., Sohn, J.W. & Kim, M.J. Predictors of persistent methicillin-resistant Staphylococcus aureus bacteraemia in patients treated with vancomycin. The Journal of antimicrobial chemotherapy 65:1015-1018 (2010)). 따라서, 보다 성공적인 항-스타필로코시 요법은 세포내 박테리아의 제거를 포함하여야 한다.
안사마이신은 박테리아의 RNA 폴리머라제를 억제하고 그램-양성 및 선택적 그램-음성 박테리아에 대해 예외적인 효력을 가지는 리파마이신, 리팜핀, 리팜피신, 리파부틴, 리파펜틴, 리파라질, ABI-1657, 및 그것의 유사체를 포함하는 항생제의 부류이다 (Rothstein, D.M., 등 (2003) Expert Opin. Invest. Drugs 12(2):255-271; US 7342011; US 7271165).
S. 아우레우스 (MRSA 포함) 감염을 예방하고 치료하기 위한 면역요법이 보고되었다. US2011/0262477은 MRSA에 대한 면역 반응을 자극하기 위한 백신으로서 박테리아 접착 단백질 Eap, Emp 및 AdsA의 사용에 관한 것이다. WO2000071585는 특정 S. 아우레우스 균주 분리주에 반응성인 단리된 단클론성 항체 반응성를 개시한다. US20110059085A1은 비록 실제의 항체가 기술되지 않았지만, 1종 이상의 SA 캡슐 항원에 특이적인 IgM Ab를 이용하는 Ab-기반 전략을 제안한다.
면역콘주게이트로도 공지된, 항체-항생제 콘주게이트 (ADC)는 항원-발현 종양 세포에 강력한 세포독성 약물을 표적화함으로써 항체와 세포독성 약물 양자의 이상적인 특성을 결합하는 표적화된 화학치료적 분자이고 (Teicher, BA (2009) Curr. Cancer Drug Targets 9:982-1004), 그렇게 함으로써 효능을 최대화하고 부정확한 독성을 최소화함에 의해 치료 지수를 향상시킨다 (Carter, P.J. 및 Senter P.D. (2008) The Cancer J.. 14(3):154-169; Chari, R.V. (2008) Acc . Chem . Res. 41:98-107. ADC는 링커 단위체를 통해 세포독성 약물 모이어티에 공유 부착된 표적 항체를 포함한다. 면역콘주게이트는 종양에 약물 모이어티의 표적화된 전달 및 그 안에서 세포내 축적을 허용하여, 비콘주게이트 약물의 전신 투여가 제거하고자 하는 종양 세포뿐만 아니라 정상 세포에 허용될 수 없는 수준의 독성을 초래할 수 있다 (Polakis P. (2005) Curr. Opin. Pharmacol. 5:382-387).
패혈증을 표적화하는 항생제를 통해 표적 박테리아의 표면에 결합하는 비-특이적 면역글로불린-항생제 콘주게이트가 기재된다 (US 5545721; US 6660267). 박테리아 항원 (예컨대 SA 협막 다당질)에 특이적인 항원-결합 부분을 갖지만, 박테리아 Fc-결합 단백질, 예를 들면, 스타필로코시 단백질 A와 반응하는 불변 영역을 결하는 항생제-콘주게이트된 항체가 기재된다 (US 7569677).
종래의 항생제에 대한 MRSA의 놀라운 내성률과 침습성 MRSA 감염으로 인한 사망률 및 이환율에 비추어 볼 때, S. 아우레우스 감염을 치료하기 위한 신규 치료제에 대한 높은 미충족 욕구가 있다. 본 발명은 이러한 요구를 만족시키고, 그리고 현재의 치료 조성물의 제한을 극복할 뿐만 아니라 하기 상세한 설명으로부터 명백 해지는 추가적인 이점을 제공하는 조성물 및 방법을 제공함으로써 만족시킨다.
본 발명은 세포내 박테리아의 제거를 포함하는 독특한 치료제를 제공한다. 본 발명은 그와 같은 치료제가 반코마이신과 같은 종래의 항생제가 실패한 생체-내에서 유효하다는 것을 입증한다.
본 발명은 1종 이상의 리파마이신-유형 항생제 모이어티에 공유 부착에 의해 콘주게이트된 항체를 포함하는 "항체-항생제 콘주게이트", 또는 "AAC"로 지칭되는) 조성물을 제공한다.
본 발명의 일 측면은 리파마이신-유형 항생제에 프로테아제-절단가능한, 비-펩티드 링커에 의해 공유 부착된, rF1 항체를 포함하는 항체-항생제 콘주게이트 화합물이다.
본 발명의 예시적인 구현예는 다음 화학식을 갖는 항체-항생제 콘주게이트이다:
식 중:
Ab는 rF1 항체이고;
PML은 다음 화학식을 갖는 프로테아제-절단가능한, 비-펩티드 링커이고:
여기서 Str은 연신부 단위체이고; PM은 펩티드도미메틱 단위체이고, 그리고 Y는 스페이서 단위체이며;
abx는 리파마이신-유형 항생제이고; 그리고
p는 정수 1 내지 8이다.
임의의 이전의 구현예의 항체-항생제 콘주게이트 화합물은 임의의 하나 항-SDR Abs 및 특이적으로 본 명세서에 기재된 rF1 항체를 포함한다. 이들 rF1 항체는 스타필로코쿠스 아우레우스에 결합환다. 예시적인 rF1 항체에서, Ab는 경쇄(L) 쇄 및 중쇄(H)를 포함하는 단클론성 항체이고, 상기 L 쇄는 CDR L1, CDR L2, 및 CDR L3을 포함하고 그리고 상기 H 쇄는 CDR H1, CDR H2 및 CDR H3을 포함하고, 여기서 상기 CDR H1, CDR H2 및 CDR H3 및 상기 CDR L1, CDR L2, 및 CDR L3은 그리고 각각 표 4A 및 4B에 나타낸 바와 같이, Abs F1 (서열 번호 1-6), rF1 (서열 번호 1-5,7), rF1.v1 (서열 번호 1,8,3,4-6) 각각의 CDR들의 아미노산 서열을 포함한다.
일부 구현예에서, rF1 항체는 중쇄 가변 영역 (VH)을 포함하고, 여기서 상기 VH는 서열 번호 13의 VH 서열로부터 선택된 VH 영역의 길이에 걸쳐 적어도 95% 서열 동일성을 포함한다. 본 항체는 더욱이 L 쇄 가변 영역 (VL)을 포함할 수 있고 여기서 상기 VL은 각각 항체 rF1 및 rF1.v6의 서열 번호 14 및 서열 번호 15의 VL 서열로부터 선택된 VL 영역의 길이에 걸쳐 적어도 95% 서열 동일성을 포함한다.
특정 구현예에서, rF1 항체는 아래와 같이 L 및 H 쇄 쌍을 포함한다: L 쇄는 서열 번호 10의 서열을 포함하는 H 쇄과 쌍으로 된 서열 번호 9의 서열을 포함하고; L 쇄는 서열 번호 10의 서열을 포함하는 H 쇄과 쌍으로 된 서열 번호 11의 서열을 포함하고; L 쇄는 서열 번호 12의 서열을 포함하는 H 쇄과 쌍으로 된 서열 번호 11의 서열을 포함한다.
임의의 하나 이전의 구현예에서, 항체는 Fc 영역을 결하는 항원-결합 단편일 수 있다. 일부 구현예에서, 항체는 F(ab) 또는 F(ab')2이다. 일부 구현예에서, 본 항체는 더욱이 중쇄 불변 영역 및/또는 경쇄 불변 영역을 포함하고, 여기서 상기 중쇄 불변 영역 및/또는 상기 경쇄 불변 영역은 시스테인 잔기로 치환된 1종 이상의 아미노산을 포함한다. 일부 구현예에서, 상기 중쇄 불변 영역 아미노산 치환 A118C 및/또는 S400C를 포함하고, 및/또는 상기 경쇄 불변 영역은 아미노산 치환 V205C를 포함하고, 여기서 상기 넘버링 시스템은 EU 넘버링에 따른다.
상기에 기재된 임의의 항체의 일부 구현예에서, 상기 항체는 IgM 이소형이 아니다. 상기에 기재된 임의의 항체의 일부 구현예에서, 상기 항체는 IgG (예를 들면, IgG1, IgG2, IgG3, IgG4), IgE, IgD, 또는 IgA (예를 들면, IgA1 또는 IgA2) 이소형이다.
본 발명의 예시적인 구현예는 항체-항생제 콘주게이트 화합물, 및 약제학적으로 허용가능한 담체, 활윤제, 희석제, 또는 부형제를 포함하는 약제학적 조성물이다.
본 발명의 또 다른 측면은 임의의 이전의 구현예의 항체-항생제 콘주게이트의 치료적 유효량을 감염된 환자에게 투여하는 것을 포함하는 박테리아 감염을 치료하는 방법이다. 본 발명의 또 다른 측면은 본 발명의 항체-항생제 콘주게이트의 치료적 유효량을 상기 환자에게 투여하는 것을 포함하는 환자에 있어 스타필로코시 감염을 치료하는 방법이다. 일 구현예에서, 환자는 인간이다. 일 구현예에서 환자는 스타필로코쿠스 아우레우스 및/또는 스타필로코쿠스 에피더미디스 감염으로 감염된다. 일부 구현예에서, 환자는 S. 아우레우스 감염으로 진단되었다. 일부 구현예에서, 박테리아 감염을 치료하는 것은 박테리아 부하 또는 수를 감소하는 것을 포함한다.
본 발명의 또 다른 측면은 임의의 하나의 이전의 구현예의 항체-항생제 콘주게이트의 치료적 유효량을 상기 환자에게 투여하는 것을 포함하는 감염된 환자에서 스타필로코시 감염을 치료하는 방법이다. 일 구현예에서, 환자는 인간이다. 일 구현예에서 박테리아 감염은 스타필로코쿠스 아우레우스 감염이다. 일부 구현예에서, 환자는 S. 아우레우스 감염으로 진단되었다. 일부 구현예에서, 박테리아 감염을 치료하는 것은 박테리아 부하 또는 수를 감소하는 것을 포함한다.
임의의 이전의 치료 방법의 일 구현예에서, S. 아우레우스를 포함하는 박테리아 감염이 균혈증을 유도하는 환자에게 투여된다. 특정 구현예에서 본 방법은 스타필로코시 심내막염 또는 골수염을 치료하기 위해 사용된다. 일 구현예에서, 본 항체-항생제 콘주게이트 화합물은 약 50mg/kg 내지 100mg/kg의 범위의 용량으로 감염된 환자에게 투여된다.
또한 임의의 상기 구현예의 rF1 항생제 콘주게이트 화합물을 투여함에 의해 숙주세포를 죽이지 않고 S. 아우레우스 감염된 환자의 세포에서 세포내 S. 아우레우스를 사멸하는 방법이 제공된다. 임의의 이전의 구현예의 AAC와 존속성균 박테리아를 접촉함에 의해 생체내 지속 스타필로코시 박테리아 세포 (예를 들면, S. 아우레우스)를 사멸하는 또 다른 방법이 제공된다.
또 다른 구현예에서, 본 치료 방법은 제2 치료제를 투여하는 것을 더 포함한다. 추가 구현예에서, 상기 제2 치료제는 일반적으로 스타필 아우레우스 또는 특히는 MRSA에 대한 항생제를 포함하는 항생제이다.
일 구현예에서, 본 발명의 항체-항생제 콘주게이트 화합물과 조합하여 투여된 제2 항생제는 구조적 부류: (i) 아미노글리코시드; (ii) 베타-락탐; (iii) 매크롤라이드/환계 펩티드; (iv) 테트라사이클린; (v) 플루오로퀴놀린/플루오로퀴놀론; (vi) 및 옥사졸리디논으로부터 선택된다.
일 구현예에서, 본 발명의 항체-항생제 콘주게이트 화합물과 조합하여 투여된 제2 항생제는 클린다마이신, 노보바이오신, 레타파물린, 다프토마이신, GSK-2140944, CG-400549, 시타플록사신, 테이코플라닌, 트리클로산, 나프티리돈, 라데졸리드, 독소루비신, 암피실린, 반코마이신, 이미페넴, 도리페넴, 젬시타빈, 달바반신, 및 아지트로마이신으로부터 선택된다.
본 명세서에 일부 구현예에서, 감염된 환자에서 박테리아 부하는 치료 후에 검출불가능한 수준으로 감소되었다. 일 구현예에서, 환자의 혈액 배양물은 치료 전 양성 혈액 배양물과 비교하여 치료 후 음성이다. 본 명세서에 일부 구현예에서, 대상체 내 박테리아 내성은 검출 불가능하거나 낮다. 본 명세서에 일부 구현예에서, 환자는 메티실린 또는 반코마이신으로 치료에 반응하지 않는다.
본 발명의 예시적인 구현예는 rF1 항체에 리파마이신-유형 항생제를 콘주게이트하는 것을 포함하는 항체-항생제 콘주게이트를 제작하는 공정이다.
본 발명의 예시적인 구현예는 다음을 포함하는 박테리아 감염을 치료하기 위한 키트이다:
a) 항체-항생제 콘주게이트 화합물, 및 약제학적으로 허용가능한 담체, 활윤제, 희석제, 또는 부형제를 포함하는 약제학적 조성물; 및
b) 사용 설명서.
본 발명의 일 측면은 다음 화학식 II를 갖는 항생제-링커 중간체이다:
식 중:
점선은 선택적인 결합을 나타내고;
R은 H, C1-C12 알킬, 또는 C(O)CH3이고;
R1은 OH이고;
R2는 CH=N-(헤테로사이클릴)이고, 여기서 상기 헤테로사이클릴은 C(O)CH3, C1-C12 알킬, C1-C12 헤테로아릴, C2-C20 헤테로사이클릴, C6-C20 아릴, 및 C3-C12 카르보사이클릴로부터 독립적으로 선택된 1종 이상의 기로 임의로 치환되고;
또는 R1 및 R2는 5- 또는 6-원 융합된 헤테로아릴 또는 헤테로사이클릴을 형성하고, 그리고 임의로 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환을 형성하고, 여기서 상기 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환은 H, F, Cl, Br, I, C1-C12 알킬, 또는 OH로 임의로 치환되고;
PML은 R2 또는 R1 및 R2에 의해 형성된 융합된 헤테로아릴 또는 헤테로사이클릴에 부착된 프로테아제-절단가능한, 비-펩티드 링커이고; 그리고 다음 화학식을 가지고:
여기서 Str은 연신부 단위체이고; PM은 펩티드도미메틱 단위체이고, 그리고 Y는 스페이서 단위체이며; 및
X는 말레이미드, 티올, 아미노, 브로마이드, 브로모아세트아미도, 아이오도아세트아미도, p-톨루엔술포네이트, 아이오다이드, 하이드록실, 카복실, 피리딜 이황화, 및 N-하이드록시석신이미드로부터 선택된 반응성 작용기이다.
본 명세서에 기재된 다양한 구현예의 특성 중 하나, 일부 또는 전부가 조합될 수 있어 본 발명의 다른 구현예를 형성할 수 있음을 이해해야 한다. 본 발명의 이들 및 다른 측면는 당해 분야의 숙련가에게 명백할 것이다.
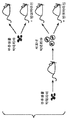
도 1a-1f: MRSA의 세포 내 저장은 생체내 및 시험관내에서 반코마이신으로부터 보호된다. 도 1a는 유리 박테리아 (부유생물) 대 세포내 박테리아를 생성하기위한 실험 디자인의 도식을 도시한다. 4 집단의 마우스가 거의 동등한 용량의 실용가능한 유리 박테리아 또는 세포내 박테리아로 정맥내 주사에 의해 감염되고 그리고 선택된 그룹은 감염 직후 및 그 다음 하루에 한번 씩 반코마이신으로 처리되었다 (실시예 2 참조). 도 1b 및 도 1c는 감염 4일 후 감염된 마우스의 각각에서 신장 및 뇌에서의 박테리아 부하를 나타낸다. 점선은 검정을 위한 검출의 한계를 나타낸다. 도 1d는 감염될 수 있는 세포의 단일층 상에서 배양될 때 반코마이신으로부터 MRSA가 보호되는 것을 나타낸다. (ND = 검출되지 않음). 도 1e 및 도 1f는 감염될 수 있는 세포의 단일층 상에서 배양될 때 반코마이신의 존재에서 MRSA가 성장할 수 있다는 것을 나타낸다. MRSA (유리 박테리아)는 배지, 배지 + 반코마이신, 또는 배지 + 반코마이신 및 MG63 골아세포 (도 1e) 또는 인간 뇌 미세혈관 내피 세포 (HBMEC, 도 1f)의 단일층 상에 플레이팅된 것에 씨딩된다. 세포외 박테리아 (유리 박테리아)는 배지 단독에서 잘 자라지만, 반코마이신에 의해 사멸되었다. 포유동물 세포 (세포내 + 반코)의 단일층을 함유하는 웰들에서 박테리아의 분획은 감염 후 처음 8시간 동안 반코마이신으로부터 보호되었고 그리고 24시간에 걸쳐 세포내 구획 내에서 신장할 수 있었다. 오차 막대는 트리플리케이트 웰들에 대한 표준 편차를 나타낸다.
도 2: 항체 항생제 콘주게이트 (AAC)의 개념을 도시한다. 일 예에서, 상기 AAC는 리소좀 프로테아제에 의해 절단된 링커를 통해 강력한 리파마이신-유형 항생제 (예를 들면 리팔로그)에 연결된 S. 아우레우스의 표면 상 에피토프에 대한 항체로 구성된다.
도 3은 항체-항생제 콘주게이트 (AAC)에 대한 약물 활성화의 가능한 기전을 도시한다. AAC는 항체의 항원 결합 도메인 (Fab)을 통해 세포외 박테리아에 결합하고 Fc-매개된 식균작용을 통해 옵소닌화된 박테리아의 흡수를 증진한다. 링커는 리소좀 프로테아제 예컨대 카텝신 B에 의해 절단된다. 링커의 절단에 따라, 링커는 가수분해되어 포식용해소체 내부에 유리 항생제를 방출한다. 유리 항생제는 동일한 구획에 존재하고 있는 임의의 이전에 내재화된 박테리아와 함께 옵소닌화되고 식균된 박테리아를 사멸시킨다.
도 4a 및 4b는 세린-아스파르테이트 (SDR) 단백질의 측면을 도시한다. 도 4a는 S. 아우레우스 및 S. 에피더미디스로부터 질량-분광분석법에 의해 드러난 SDR 단백질의 정렬을 도시한다. SDR-영역은 해치(hatch)로 나타낸다. S. 아우레우스 상에 다중 SDR 단백질 및 단백질 당 다중 에피토프가 있기 때문에 rF1 에피토프는 풍부하게 발현된다. 도 4a는 서열 번호: 27로 'SDSDSDSD'를 개시한다. 도 4b는 SdgA 및 SdgB에 의해 SDR 단백질의 단계적인 글리코실화를 보여주는 모델이다. 먼저, SdgB는 SDR 단백질 상 SD-영역 상에 GlcNAc 모이어티를 부가하고, 그 다음 SdgA에 의한 추가 GlcNAc 변형을 부가한다. mAb rF1에 대한 에피토프는 SdgB-의존성 GlcNAc 모이어티를 포함한다. 데이터는 rF1이 GlcNac 및 SD 골격의 일부에 결합함을 시사한다. 도 4b는 서열 번호: 28로 'SDSDSD'를 개시한다.
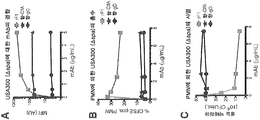
도 5a, 5b 및 5c는 mAb rF1이 S. 아우레우스 박테리아에 강력한 결합과 사멸을 나타내는 것을 보여준다. (도 a-c) 박테리아는 huIgG1 mAbs rF1 (정사각형), 4675 항-ClfA (삼각형), 또는 항-헤르페스 바이러스 gD (원)으로 사전 옵소닌화된다. (도 5a): WT (USA300-spa) 박테리아에 mAbs의 결합은 유세포측정에 의해 평가되었고, 그리고 평균 형광성 세기 (MFI)로 표시되었다. (도 5b): CFSE-표지된, 사전 옵소닌화된 WT (USA300-spa) 박테리아가 인간 PMN으로 배양되었다. 박테리아 흡수는 유세포측정에 의해 CD11b-양성 세포를 게이팅한 후, CFSE-양성 PMN의 %로 표현되었다. (그림 5c): 사전 옵소닌화된 WT (USA300- spa) 박테리아는 박테리아 사멸을 평가하기 위해 PMN으로 배양되었다. mL 당 생존가능한 CFU의 수는 적어도 세 번의 실험을 대표한다.
도 6은 다양한 감염된 조직으로부터의 S. 아우레우스에 rF1의 결합의 유세포측정 분석을 나타낸다. 균질화된 조직은 mAb rF1 (X-축)로, 그리고 항-펩티도글리칸 mAb 702로 이중 염색되어 조직 잔해 (Y-축) (좌측 패널; 화살표로 나타낸 게이트)로부터 박테리아를 구별하고, 그 다음 박테리아를 게이팅하여 히스토그램 도를 만든다 (또한, Hazenbos 등 (2013) PLOS Pathogens 9 (10):1-18 참조, 도 1D).
도 7은 유세포측정에 의해 다양한 스타필로코시 및 비-스타필로코시 그램-양성 박테리아 종에 rF1의 결합을 도시한다 (또한, Hazenbos 등 (2013) PLOS Pathogens 9 (10):1-18 참조, 도 1E).
도 8은 비-복제 MRSA를 사멸하는 그것의 능력에 대해 강력한 리파마이신-유형 항생제 (리팔로그) 디메틸pipBOR의 선택을 도시한다.
도 9: 무손상 TAC (AAC의 형태)는 항생제가 카텝신 B로 처리에 의해 방출되지 않으면 플랑크톤 박테리아를 죽이지 않는다는 것을 입증하는 성장 억제 검정. TAC는 완충액 단독 (개방된 원)에서 배양되거나 카텝신 B (폐쇄된 원)로 처리되었다. 무손상 TAC는 밤새 배양한 후에 박테리아 성장을 방지할 수 없었다. 카텝신 B로 TAC의 전처리는 .006ug/mL의 항생제를 함유할 것으로 예상되는 0.6ug/mL의 TAC에서 박테리아의 성장을 막기에 충분한 항생제 활성이 방출시켰다.
도 10은 실시예 19에 기재된 바와 같이, 시험관내 대식세포 검정에서 rF1-AAC의 효능을 도시한다.
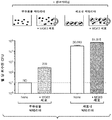
도 11a 및 11b는 실시예 20에 기재된 바와 같이, 생체내 rF1-AAC의 효능을 도시한다. rF1-AAC로 S. 아우레우스 감염된 마우스의 치료는 기존의 항체에 비교될 때 감염된 장기에서 박테리아 수를 크게 감소 또는 박멸했다. 도 11a는 항체 당 2 항생제 분자를 함유하는 AAC (AAR2)로 치료는 대략 30-배로 신장에서의 박테리아 부하를 감소하였고 그리고 항체 당 4 항생제 분자를 함유하는 AAC (AAR4)로 치료는 30,000-배 초과로 박테리아 부하를 감소하였다는 것을 보여준다. 도 11b는 AAC AAR2로의 치료는 심장에 검출불가능한 수준의 박테리아를 갖는 8마리 마우스 중 6마리에서 대략 70-배로 심장에서의 박테리아 부하를 감소하였고; AAC AAR4로의 치료는 검출불가능한 수준의 박테리아를 갖는 8마리 마우스 중 8마리에서 심장에서 감염을 완전히 박멸했다는 것을 보여준다.
도 2: 항체 항생제 콘주게이트 (AAC)의 개념을 도시한다. 일 예에서, 상기 AAC는 리소좀 프로테아제에 의해 절단된 링커를 통해 강력한 리파마이신-유형 항생제 (예를 들면 리팔로그)에 연결된 S. 아우레우스의 표면 상 에피토프에 대한 항체로 구성된다.
도 3은 항체-항생제 콘주게이트 (AAC)에 대한 약물 활성화의 가능한 기전을 도시한다. AAC는 항체의 항원 결합 도메인 (Fab)을 통해 세포외 박테리아에 결합하고 Fc-매개된 식균작용을 통해 옵소닌화된 박테리아의 흡수를 증진한다. 링커는 리소좀 프로테아제 예컨대 카텝신 B에 의해 절단된다. 링커의 절단에 따라, 링커는 가수분해되어 포식용해소체 내부에 유리 항생제를 방출한다. 유리 항생제는 동일한 구획에 존재하고 있는 임의의 이전에 내재화된 박테리아와 함께 옵소닌화되고 식균된 박테리아를 사멸시킨다.
도 4a 및 4b는 세린-아스파르테이트 (SDR) 단백질의 측면을 도시한다. 도 4a는 S. 아우레우스 및 S. 에피더미디스로부터 질량-분광분석법에 의해 드러난 SDR 단백질의 정렬을 도시한다. SDR-영역은 해치(hatch)로 나타낸다. S. 아우레우스 상에 다중 SDR 단백질 및 단백질 당 다중 에피토프가 있기 때문에 rF1 에피토프는 풍부하게 발현된다. 도 4a는 서열 번호: 27로 'SDSDSDSD'를 개시한다. 도 4b는 SdgA 및 SdgB에 의해 SDR 단백질의 단계적인 글리코실화를 보여주는 모델이다. 먼저, SdgB는 SDR 단백질 상 SD-영역 상에 GlcNAc 모이어티를 부가하고, 그 다음 SdgA에 의한 추가 GlcNAc 변형을 부가한다. mAb rF1에 대한 에피토프는 SdgB-의존성 GlcNAc 모이어티를 포함한다. 데이터는 rF1이 GlcNac 및 SD 골격의 일부에 결합함을 시사한다. 도 4b는 서열 번호: 28로 'SDSDSD'를 개시한다.
도 5a, 5b 및 5c는 mAb rF1이 S. 아우레우스 박테리아에 강력한 결합과 사멸을 나타내는 것을 보여준다. (도 a-c) 박테리아는 huIgG1 mAbs rF1 (정사각형), 4675 항-ClfA (삼각형), 또는 항-헤르페스 바이러스 gD (원)으로 사전 옵소닌화된다. (도 5a): WT (USA300-spa) 박테리아에 mAbs의 결합은 유세포측정에 의해 평가되었고, 그리고 평균 형광성 세기 (MFI)로 표시되었다. (도 5b): CFSE-표지된, 사전 옵소닌화된 WT (USA300-spa) 박테리아가 인간 PMN으로 배양되었다. 박테리아 흡수는 유세포측정에 의해 CD11b-양성 세포를 게이팅한 후, CFSE-양성 PMN의 %로 표현되었다. (그림 5c): 사전 옵소닌화된 WT (USA300- spa) 박테리아는 박테리아 사멸을 평가하기 위해 PMN으로 배양되었다. mL 당 생존가능한 CFU의 수는 적어도 세 번의 실험을 대표한다.
도 6은 다양한 감염된 조직으로부터의 S. 아우레우스에 rF1의 결합의 유세포측정 분석을 나타낸다. 균질화된 조직은 mAb rF1 (X-축)로, 그리고 항-펩티도글리칸 mAb 702로 이중 염색되어 조직 잔해 (Y-축) (좌측 패널; 화살표로 나타낸 게이트)로부터 박테리아를 구별하고, 그 다음 박테리아를 게이팅하여 히스토그램 도를 만든다 (또한, Hazenbos 등 (2013) PLOS Pathogens 9 (10):1-18 참조, 도 1D).
도 7은 유세포측정에 의해 다양한 스타필로코시 및 비-스타필로코시 그램-양성 박테리아 종에 rF1의 결합을 도시한다 (또한, Hazenbos 등 (2013) PLOS Pathogens 9 (10):1-18 참조, 도 1E).
도 8은 비-복제 MRSA를 사멸하는 그것의 능력에 대해 강력한 리파마이신-유형 항생제 (리팔로그) 디메틸pipBOR의 선택을 도시한다.
도 9: 무손상 TAC (AAC의 형태)는 항생제가 카텝신 B로 처리에 의해 방출되지 않으면 플랑크톤 박테리아를 죽이지 않는다는 것을 입증하는 성장 억제 검정. TAC는 완충액 단독 (개방된 원)에서 배양되거나 카텝신 B (폐쇄된 원)로 처리되었다. 무손상 TAC는 밤새 배양한 후에 박테리아 성장을 방지할 수 없었다. 카텝신 B로 TAC의 전처리는 .006ug/mL의 항생제를 함유할 것으로 예상되는 0.6ug/mL의 TAC에서 박테리아의 성장을 막기에 충분한 항생제 활성이 방출시켰다.
도 10은 실시예 19에 기재된 바와 같이, 시험관내 대식세포 검정에서 rF1-AAC의 효능을 도시한다.
도 11a 및 11b는 실시예 20에 기재된 바와 같이, 생체내 rF1-AAC의 효능을 도시한다. rF1-AAC로 S. 아우레우스 감염된 마우스의 치료는 기존의 항체에 비교될 때 감염된 장기에서 박테리아 수를 크게 감소 또는 박멸했다. 도 11a는 항체 당 2 항생제 분자를 함유하는 AAC (AAR2)로 치료는 대략 30-배로 신장에서의 박테리아 부하를 감소하였고 그리고 항체 당 4 항생제 분자를 함유하는 AAC (AAR4)로 치료는 30,000-배 초과로 박테리아 부하를 감소하였다는 것을 보여준다. 도 11b는 AAC AAR2로의 치료는 심장에 검출불가능한 수준의 박테리아를 갖는 8마리 마우스 중 6마리에서 대략 70-배로 심장에서의 박테리아 부하를 감소하였고; AAC AAR4로의 치료는 검출불가능한 수준의 박테리아를 갖는 8마리 마우스 중 8마리에서 심장에서 감염을 완전히 박멸했다는 것을 보여준다.
이제 본 발명의 특정 구현예에 대한 상세히 지칭될 것이며, 그것의 예들은 첨부된 구조 및 화학식에 예시된다. 본 발명이 방법, 물질 및 예시를 포함하는 열거된 구현예와 결합하여 기술될 것인 한편, 상기 기술은 비제한적이고, 대안물, 변형물, 및 동등물을, 이들이 일반적으로 알려져 있거나 본원에 포함될 경우 모두 망라하는 것으로 의도된다. 만일 하나 이상의 포함된 문헌, 특허 및 유사한 자료가 정의된 용어, 용어 사용, 서술된 기술, 등을 포함하지만 이에 제한되지 않고 본 명세서와 다르거나 본 명세서를 부정하는 경우, 본 명세서에 우선한다. 다르게 정의되지 않는다면, 사용된 본 명세서에서 모든 기술적 및 과학 용어는 본발명이 속하는 분야에서 통상의 지식을 가진 자에 의해 통상적으로 이해되는 것과 동일한 의미를 가진다. 당업자는 본 발명의 실시에 사용될 수 있는 본원에 기술된 것들과 유사하거나 동등한 많은 방법 및 물질을 인식할 것이다. 본 발명은 비제한적으로 기재된 방법 및 물질이다.
본원에서 지칭된 모든 공보, 특허 출원, 특허 및 다른 참고문헌은 이들의 전문이 참조로 도입된다.
I.
일반적인 기술
본원에 기술 또는 참조된 기술 및 절차는, 본 분야의 숙련가에 의하여 기존의 방법, 예컨대 예를 들어, 하기 기술된 널리 이용되는 방법들을 사용하여 잘 이해되고, 통상적으로 채용될 것이다: Sambrook et al., Molecular Cloning: A Laboratory Manual 3d edition (2001) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.; Current Protocols in Molecular Biology (F.M. Ausubel, et al. eds., (2003)); the series Methods in Enzymology (Academic Press, Inc.): PCR 2: A Practical Approach (M.J. MacPherson, B.D. Hames and G.R. Taylor eds. (1995)), Harlow and Lane, eds. (1988) Antibodies, A Laboratory Manual, and Animal Cell Culture (R.I. Freshney, ed. (1987)); Oligonucleotide Synthesis (M.J. Gait, ed., 1984); Methods in Molecular Biology, Humana Press; Cell Biology: A Laboratory Notebook (J.E. Cellis, ed., 1998) Academic Press; Animal Cell Culture (R.I. Freshney), ed., 1987); Introduction to Cell and Tissue Culture (J.P. Mather and P.E. Roberts, 1998) Plenum Press; Cell and Tissue Culture: Laboratory Procedures (A. Doyle, J.B. Griffiths, and D.G. Newell, eds., 1993-8) J. Wiley and Sons; Handbook of Experimental Immunology (D.M. Weir and C.C. Blackwell, eds.); Gene Transfer Vectors for Mammalian Cells (J.M. Miller and M.P. Calos, eds., 1987); PCR : The Polymerase Chain Reaction, (Mullis et al., eds., 1994); Current Protocols in Immunology (J.E. Coligan et al., eds., 1991); Short Protocols in Molecular Biology (Wiley and Sons, 1999); Immunobiology (C.A. Janeway and P. Travers, 1997); Antibodies (P. Finch, 1997); Antibodies: A Practical Approach (D. Catty., ed., IRL Press, 1988-1989); Monoclonal Antibodies: A Practical Approach (P. Shepherd and C. Dean, eds., Oxford University Press, 2000); Using Antibodies: A Laboratory Manual (E. Harlow and D. Lane (Cold Spring Harbor Laboratory Press, 1999); The Antibodies (M. Zanetti and J. D. Capra, eds., Harwood Academic Publishers, 1995); 및 Cancer: Principles and Practice of Oncology (V.T. DeVita et al., eds., J.B. Lippincott Company, 1993).
본 출원에서 사용된 명명법은, 달리 표지되지 않는다면, IUPAC 계통 명명법을 기준으로 한다. 다르게 정의되지 않는 한, 본 명세서에서 사용된 기술 및 과학 용어들은 본 발명이 속하는 당해 분야의 숙련가에 의해 통상적으로 이해되는 바와 동일한 의미를 가지고, 그리고: : 「Singleton 등 (1994) Dictionary of Microbiology and Molecular Biology, 2nd Ed., J. Wiley & Sons, New York, NY」; 및 「Janeway, C., Travers, P., Walport, M., Shlomchik (2001) Immunobiology, 5th Ed., Garland Publishing, New York」과 일치된다.
II.
정의
스타필로코쿠스 아우레우스는 또한 본원에서 속칭으로 Staph A 또는 S. 아우레우스로 지칭된다. 유사하게, 스타필로코쿠스 에피더미디스는 또한 본원에서 Staph E 또는 S. 에피더미디스로 지칭된다.
"항체 항생제 콘주게이트" 또는 AAC는, 링커에 의하여 항생제에 화학적으로 연결된 항체로 구성된 화합물이다. 항체는, 박테리아 표면, 예를 들어, 박테리아 세포 벽 성분 상의 항원 또는 에피토프에 결합한다. 본 발명에서 사용된 바와 같이, 링커는, 대부분의 포유동물 세포 유형에서 발견되는 카텝신 B, 리소좀 프로테아제를 포함하는, 프로테아제에 의하여 절단되도록 설계된, 프로테아제-절단가능한, 비-펩티드 링커이다 (Dubowchik et al (2002) Bioconj. Chem. 13:855-869). 이의 3개 성분을 갖는 AAC의 다이어그램이 도 2에 도시된다. “THIOMABTM 항생제 콘주게이트” 또는 “TAC”는, 항체가, 일반적으로 항원-결합 작용을 저해하지 않도록 항체 상의 특정 부위(들)에서 항체로 재조합 가공된 시스테인인, 하나 이상의 시스테인을 통하여 링커-항생제 단위체에 화학적으로 콘주게이트된, AAC의 형태이다.
치환체의 수를 표지할 경우, 용어 "하나 이상"은 일 치환체로부터 가장 높은 수의 가능한 치환 수까지의 범위, 즉, 치환에 의한, 일 수소의 교체로부터 모든 수소의 교체까지의 범위를 지칭한다. 용어 "치환체"는, 친계 분자 상에서 수소 원자를 대체하는 원자, 또는 원자 그룹을 나타낸다. 용어 "치환된"은 하나 이상의 치환체를 보유하는 특정 그룹을 나타낸다. 임의의 기가 다중 치환체를 가질 수 있고, 다양한 가능한 치환체가 제공될 경우, 치환체는 독립적으로 선택되며, 상동할 필요는 없다. 용어 "비치환된"은 치환체 보유하지 않는 특정 기를 의미한다. 용어 "임의로 치환된"은, 가능한 치환체의 군으로부터 독립적으로 선택된, 하나 이상의 치환체에 의하여 비치환 또는 치환된다. 치환체의 수를 표지할 경우, 용어 "하나 이상"은 일 치환체로부터 가장 높은 수의 가능한 치환 수까지의 범위, 즉, 치환에 의한, 일 수소의 교체 내지 모든 수소의 교체를 의미한다.
용어 “항생제” (abx 또는 Abx)는 미생물, 예컨대 박테리아를 사멸하거나 이의 성장을 특이적으로 억제하는, 그러나 투여된 농도 및 투여 간격에서 숙주에게는 비-치명적인, 임의의 분자를 포함한다. 특정 양태에서, 항생제는 투여된 농도 및 투여 간격에서 숙주에게 비-독성이다. 박테리아에 대해 유효한 항생제는 넓게는 살균성 (즉, 직접적으로 사멸) 또는 정균성 (즉, 분할 방지)로서 분류될 수 있다. 항-살균성 항생제는, 추가로 좁은-스펙트럼 또는 넓은-스펙트럼으로 하위-분류될 수 있다. 넓은 스펙트럼의 항생제는, 박테리아의 보다 작은 범위 또는 특정 패밀리에 대하여 유효한 좁은-스펙트럼 항생제와 대조적으로, 그람-양성 및 그람-음성 박테리아 둘 모두를 포함하는 박테리아의 넓은 범위에 대해 유효한 것이다. 항생제의 예는 하기를 포함한다: (i) 아미노글리코사이드, 예를 들어, 아미카신, 겐타마이신, 가나마이신, 네오마이신, 네틸마이신, 스트렙토마이신, 토브라마이신, 파로마이신, (ii) 아나마이신(예를 들어, 겔다나마이신, 허비마이신), (iii) 카바세펨(예를 들어, 로라카베프), (iv) 카바페넴(예를 들어, 에르타페눔, 도리페넴, 이미페넴, 실라스타틴, 메로페넴), (v) 세팔로스포린(제1 세대: 예컨대 세파드록실, 세파졸린, 세팔로틴 또는 세팔렉신; (vi) 세파로스포린(제2 세대), 예컨대, 세파클로르, 세파만돌, 세폭시틴, 세프프로질, 세푸록심; (vi) 세파로스포린(제3 세대), 예컨대, 세픽심, 세프디니르, 세프디토렌, 세포페라존, 세포탁심, 세프포독심, 세프타지딤, 세프티부텐, 세프티족심, 세프트리악손; (vii) 세파로스포린(제4 세대), 예컨대, 세페핌; (viii) 세파로스포린(제5 세대), 예컨대, 세프토비프롤, (ix) 당단백질(예를 들어, 테이코플라닌, 반코마이신), (x) 마크롤리드(예를 들어, 아지트로마이신, 클라리트로마이신, 디리트로마이신, 에리트로마이신, 록시트로마이신, 트롤레안도마이신, 텔리트로마이신, 스펙티노마이신), (xi) 모노박탐(예를 들어, 아즈트레오남), (xii) 페니실린(예를 들어, 아목시실린, 암피실린, 아슬로실린, 카베니실린, 클록사실린, 디클록사실린, 플루클록사실린, 메즐로실린, 메티실린, 나프실린, 옥사실린, 페니실린, 페페라실린, 티카르실린), (xiii) 항생제 폴리펩티드(예를 들어, 바시트라신, 콜리스틴, 폴리믹신 B), (xiv) 퀴놀론(예를 들어, 시프로플록사신, 에녹사신, 가티플록사신, 레보플록사신, 레메플록사신, 목시플록사신, 노르플록사신, 오르플록사신, 트로바플록사신), (xv) 술폰아미드(예를 들어, 마페니드, 프론토실, 술파세타미드, 술파메티졸, 술파닐아미드, 술파살라진, 설피속사졸, 트리메토프림, 트리메토프림-술파메톡사졸(TMP-SMX), (xvi) 테트라사이클린(예를 들어, 데메클로사이클린, 독시사이클린, 미노사이클린, 옥시테트라사이클린, 테트라사이클린), 및 (xvii) 기타, 예컨대 아르스펜아민, 클로람페니콜, 클린다마이신, 린코마이신, 에탐부톨, 포스포마이신, 푸시드산, 푸라졸리돈, 이소니아지드, 리네졸리드, 메트로니다졸, 무피로신, 니트로푸란토인, 플라텐시마이신, 피라진아미드, 퀴누프리스틴/달포프리스틴, 리팜핀/리팜피신 또는 티니다졸.
용어 “메티실린 내성 스타필로코쿠스 아우레우스” (MRSA) (대안적으로 다중약물 내성 스타필로코쿠스 아우레우스 또는 옥사실린 내성 스타필로코쿠스 아우레우스 (ORSA)로 공지됨)는, 페니실린 (예컨대, 메티실린, 디클로사실린, 나프실린, 옥사실린 등) 및 세파로스포린을 포함하는, 베타-락탐 항생제에 내성인 스타필로코쿠스 아우레우스의 임의의 균주를 지칭한다. “메티실린 민감성 스타필로코쿠스 아우레우스”(MSSA)는, 베타-락탐 항생제에 민감성인 스타필로코쿠스 아우레우스의 임의의 균주를 지칭한다.
용어 “최소 억제성 농도” (“MIC”) 는, 밤새 항온처리 한 후, 미생물의 가시적 성장을 억제할 것인 항미생물제의 가장 낮은 농도를 지칭한다. MIC 측정에 대한 검정은 잘 알려져 있다. 일 방법은 하기 실시예 섹션에 기술된 바와 같다.
용어 "항-Staph 항체" 및 “Staph에 결합하는 항체"는 항체가 S. 아우레우스를 표적화하는데 있어서 진단제 및/또는 치료제로서 유용하도록 하기에 충분한 친화도로 스타필로코쿠스 아우레우스 (“S. 아우레우스”)에 결합할 수 있는 항체를 나타낸다. 일 구현예에서, 비관련, 비-Staph 단백질에 대한 항-Staph 항체의 결합 정도는, 예를 들면, 방사면역검정법(RIA)으로 측정하여 약 10% 미만의 MRSA에 대한 항체의 결합이다. 특정 구현예에서, Staph에 결합하는 항체는 ≤ 1μM, ≤ 100 nM, ≤ 10 nM, , ≤ 5 Nm, , ≤ 4 nM, , ≤ 3 nM, , ≤ 2 nM, ≤ 1 nM, ≤ 0.1 nM, ≤ 0.01 nM, 또는 ≤ 0.001 nM (예를 들면, 10-8 M 이하, 예를 들면 10- 8 M 내지 10-13 M, 예를 들면, 10-9 M 내지 10-13 M)의 해리 상수 (Kd)를 갖는다. 특정 구현예에서, 항-Staph 항체는 상이한 종으로부터 Staph 중에 보존된 Staph의 에피토프에 결합한다. 본원에서의 항-Staph 항체는, S. 아우레우스에 부가하여, 하나 이상의 스타필로코쿠스 종에 결합하는 항체를 지칭할 것이다.
“SDR”은 세린-아스파르트산염 반복부를 지칭하며; SDR은 스타필로코시에 존재하는, 접착성 A-도메인에 인접한 세린-아스파르트산염 반복부의 큰 연신부에 의하여 특징화되는, 세포벽 단백질의 패밀리 내에 존재한다 (Foster TJ, Hook M (1998) Trends Microbiol 6: 484-488). 접착이 수반된 상기 단백질은 군집화 인자 (Clf)A 및 ClfB를 포함한다. ClfA 및 ClfB에 부가하여, S. 아우레우스는 또한 게놈에서 일렬로 조직화된 세 개 SDR-단백질인, SdrC, SdrD 및 SdrE를 발현하며, 이 계열의 세 가지 추가의 구성원인, SrdF, SdrG 및 SdrH는 대부분 S. 에피더미디스 균주에 존재한다 (McCrea KW, et al. (2000) The serine-aspartate repeat (Sdr) protein family in Staphylococcus epidermidis. Microbiology 146 ( Pt 7): 1535-1546). 이러한 단백질에서, 25 내지 275 SD 디펩티드 반복체 (서열 번호: 24)를 함유하는 SDR 영역은, N-말단 리간드 결합 A-도메인 및 C 말단 LPXTG 모티프 (서열 번호: 25) 사이에 위치한다.
“F1”로 지정된 항체는 하기를 갖는다: US 8,617,556에 도시된 바와 같은, 중쇄 및 경쇄 가변 도메인 서열 (이의 전체 내용은 본원에 참조로 편입됨). F1의 항원-결합 특성에 특히 기여하는, F1의 CDR 서열은, 또한 도 1에 도시되어 있다. 항체 F1은 완전히 인간의 것이며, 스타필로코쿠스 종 예컨대 S. 아우레우스 및 S. 에피더미디스에 특이적으로 결합할 수 있다. 중요하게는, 항체 F1은 생체내 뿐만 아니라 시험관내로, 전체 박테리아에 결합할 수 있다. 더욱이, 항체 F1은, 감염 조직, 예를 들어, 동물 내에서 성장한 박테리아에 결합할 수 있다. 본원에서 재조합 생산된 F1은, 또한 “rF1”으로 불리운다. rF1 (및 F1) 항체는 항-SDR 단클론성 Ab이다. mAb rF1에 대한 에피토프는 SdgB 의존적 GlcNAc 모이어티를 포함한다. 데이터는 SD 골격의 부분 및 GlcNac에 결합하는 rF1을 제안한다. 본원에 사용된 바와 같은 “rF1 항체” 는, F1 항체, rF1 항체 뿐만 아니라 rF1에 대한 아미노산 변경을 함유하는 모든 변이체를 포괄한다. rF1 및 변이체 항체의 아미노산 서열이 하기에 제공된다.
본 명세서에서 용어 "항체"는 가장 넓은 의미로 사용되고 그리고 구체적으로는 하기를 망라한다: 단클론성 항체, 다클론성 항체, 이량체, 다량체, 다중특이적 항체 (예를 들면, 이중특이적 항체), 및 이의 항원 결합 항체 단편 (Miller et al (2003) J. of Immunology 170:4854-4861). 항체는 뮤린, 인간, 인간화된, 키메라성일 수 있고, 또는 다른 종으로부터 유도될 수 있다. 항체는 특이적 항원을 인식할 수 있고 그리고 결합할 수 있는 면역계에 의해 생성된 단백질이다. (Janeway, C., Travers, P., Walport, M., Shlomchik (2001) Immuno Biology, 5th Ed., Garland Publishing, New York). 표적 항원은 일반적으로 다중 항체 상에 CDR에 의해 기술적으로 인식된, 또한 소위 에피토프로 불리는 수많은 결합 부위를 가진다. 상이한 에피토프에 특이적으로 결합하는 각 항체는 상이한 구조를 갖는다. 따라서, 하나의 항원은 1 초과의 상응하는 항체에 의하여 인식 및 결합될 수 있다. 항체는 전장 면역글로불린 분자 또는 전장 면역글로불린 분자의 면역학적으로 활성 부분, 즉 관심 표적 또는 이들의 일부의 항원에 면역 특이적으로 결합하는 항원 결합 부위를 함유하는 분자를 포함하며, 이러한 표적은, 비제한적으로, 암세포 또는 자가면역 질환, 감염 세포 또는 미생물 예컨대 박테리아와 관련된 자가면역 항체를 생산하는 세포를 포함한다. 본 명세서에서 개시된 면역글로불린 (Ig)는 IgM 이외의 이소형 (예컨대, IgG, IgE, IgD, 및 IgA) 및 하위부류 (예컨대, IgG1, IgG2, IgG3, IgG4, IgA1 및 IgA2)의 것일 수 있다. 본 면역글로불린은 임의의 종으로부터 유도될 수 있다. 일 양태에서, Ig는, 인간, 뮤린, 또는 래빗 유래의 것이다. 특정 구현예에서, Ig는 인간의 것이다.
항체의 “부류”는 이의 중쇄가 소유하는 불변 도메인 또는 불변 영역의 유형을 지칭한다. 5개 주요 부류의 항체가 있다: IgA, IgD, IgE, IgG, 및 IgM이 있으며, 이들 중 몇몇은 하위부류(이소형), 예를 들면 IgG1, IgG2, IgG3, IgG4, IgA1, 및 IgA2 로 추가 구분될 수 있다. 면역글로불린의 상이한 부류에 상응하는 중쇄 불변 도메인은 각각 α, δ, ε, γ, 및 μ로 불린다.
"천연 항체"는 다양한 구조를 갖는 천연 발생 면역글로불린 분자를 지칭한다. 예를 들면, 천연 IgG 항체는 이황화 결합된 두 개의 동일한 경쇄 및 두 개의 동일한 중쇄로 이루어진, 약 150,000 달톤의 이종사량체성 당단백질이다. N-말단에서 C-말단으로, 각 중쇄는 가변 중쇄 도메인 또는 중쇄 가변 도메인으로도 불리는 가변 영역(VH)에 이어 세 개의 불변 도메인(CH1, CH2, 및 CH3)을 갖는다. 유사하게, N-말단에서 C-말단으로, 각 경쇄는 가변 경쇄 도메인 또는 경쇄 가변 도메인으로도 불리는 가변 영역(VL)에 이어 불변(CL) 도메인을 갖는다. 항체의 경쇄는, 이의 불변 도메인의 아미노산 서열에 기초하여, (κ) 및 람다 (λ)라고 불리는 두 가지 타입 중의 하나에 할당될 수 있다.
용어 "전장 항체", "무손상 항체" 및 "전체 항체"는 천연 항체 구조와 실질적으로 유사한 구조를 갖거나 본원에 정의된 바와 같은 Fc 영역을 함유하는 중쇄를 갖는 항체를 나타내기 위해 상호교환 가능하게 본원에서 사용된다.
“항체의 항원-결합 단편"은 무손상 항체가 결합하는 항원에 결합하는 무손상 항체의 일부를 포함하는 무손상 항체 이외의 분자를 나타낸다. 항체 단편들의 예시들은 비제한적으로 Fv, Fab, Fab’, Fab’-SH, F(ab’)2 ; 디아바디; 선형 항체; 단일-쇄 항체 분자 (예컨대, scFv); 및 항체 단편으로부터 형성된 다가특이적 항체를 포함한다.
본원에서 사용된 바와 같이 용어 "단클론성 항체"는 실질적으로 균질 항체의 모집단으로부터 수득된 항체를 지칭한다, 즉, 모집단을 포함하는 개별 항체는, 예를 들면, 천연 발생 돌연변이를 함유하거나 또는 단클론성 항체 제제의 생산 동안 발생하는 가능한 변이체 항체 (상기 변이체는 일반적으로 소량으로 존재한다) (예컨대, 글리코실화에서의 천연 변이)를 제외하고, 상동하고/하거나 상동한 에피토프를 결합한다. IgG1 항체에 대한 일 그러한 가능한 변이체는 중쇄 불변 영역의 C 말단 리신 (K)의 절단부이다. 전형적으로 상이한 결정인자(에피토프)에 대해 유도된 상이한 항체가 포함되는 다클론성 항체 제조물과는 대조적으로, 단클론성-항체 제조물의 각각의 단클론성 항체는 항원 상의 단일 결정인자에 대해 유도된다. 따라서, 형용사 "단클론성"은 항체가 실질적으로 균일한 항체 집단에서 수득된 것이라는 속성을 명시하고, 어떤 특정한 방법에 의한 상기 항체의 생산을 요구하는 것으로 간주되지 않는다. 예를 들면, 본 발명에 따라 사용되는 단클론성 항체는 하이브리도마 방법, 재조합 DNA 방법, 파지-디스플레이 방법, 및 인간 면역글로불린 유전자좌의 전부 또는 일부를 함유하는 유전자도입 동물을 사용하는 방법을 포함하지만 이에 제한되지 않는 각종 기술들에 의해 제조될 수 있으며, 이러한 방법 및 단클론성 항체를 제조하기 위한 기타의 예시적인 방법들이 본원에 기재되어 있다. 이들의 특이성에 부가하여, 단클론성 항체는 이들이 다른 항체에 의해 오염되지 않고 합성될 수 있다는 점에서 유리하다.
용어 "키메라" 항체는 중쇄 및/또는 경쇄의 일부는 특정 공급원 또는 종으로부터 유도되는 반면 나머지 중쇄 및/또는 경쇄는 상이한 공급원 또는 종으로부터 유도되는 항체를 나타낸다.
"인간 항체"는 인간 또는 인간 세포에 의해 생산되거나 인간 항체 레퍼토리 또는 기타의 인간 항체-암호화 서열을 사용하는 비-인간 공급원으로부터 유도되는 항체의 아미노산 서열에 상응하는 아미노산 서열을 보유하는 것이다. 인간 항체의 이러한 정의는 특이적으로 비인간 항원-결합 잔기를 포함하는 인간화 항체를 배제한다.
"인간화" 항체는 비인간 HVR로부터 아미노산 잔기 및 인간 FR로부터 아미노산 잔기를 포함하는 키메라성 항체를 지칭한다. 특정 구현예에서, 인간화 항체는 적어도 1개, 및 전형적으로 2개의 가변 도메인의 실질적으로 모두를 포함할 것이고, 여기서 HVR (예를 들면, CDR)의 실질적으로 모두는 비인간 항체의 것에 일치하고, 그리고 FR의 모두 또는 실질적으로 모두는 인간 항체의 것에 일치한다. 인간화 항체는 임의로 인간 항체로부터 유도된 항체 불변 영역의 적어도 일부를 포함할 수 있다. 항체, 예를 들면, 비인간 항체의 "인간화 형태"는 인간화처리되는 항체를 지칭한다.
용어 "가변 영역" 또는 "가변 도메인"은 항체를 항원에 결합시키는데 관여하는 항체 중쇄 또는 경쇄의 도메인을 나타낸다. 천연 항체의 중쇄 및 경쇄 (각각 VH 및 VL)의 가변 도메인은 일반적으로 유사한 구조를 갖고, 각각의 도메인은 4개의 보존된 프레임워크 영역(FR) 및 3개의 초가변 영역(HVR)을 포함한다. (참고, 예를 들면, Kindt et al. Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007).) 단일 VH 또는 VL 도메인은 항원 결합 특이성을 부여하기에 충분할 수 있다. 더욱이, 특정 항원에 결합하는 항체는 항원에 결합하여 각각 상보성 VL 또는 VH 도메인의 라이브러리를 선별하는 항체로부터 VH 또는 VL 도메인을 사용하여 단리될 수 있다. 참고: 예를 들면, Portolano et al., J. Immunol. 150: 880-887 (1993); Clarkson et al, Nature 352: 624-628 (1991).
본원에서 사용되는 용어 "초가변 영역”, "HVR", 또는 “HV”는, 서열(상보성 결정 영역 또는 "CDR")에서 초가변이고/이거나 구조적으로 정의된 루프를 형성하고/하거나 항원-접촉 잔기("항원 접촉")을 함유하는 항체 가변 도메인의 영역을 나타낸다. 일반적으로, 항체는 6 개의 HVR; VH에 3 개(H1, H2, H3), 및 VL에 3 개(L1, L2, L3)를 포함한다. 천연 항체에서, H3 및 L3은 6 개 HVR의 가장 큰 다양성을 나타내며, H3은 특히 항체에 대해 미세한 특이성을 부여하는데 있어서 독특한 역할을 담당하는 것으로 여겨진다. 예를 들면, 다음을 참고: Xu et al., Immunity 13:37-45 (2000); Johnson and Wu, Methods in Molecular Biology 248:1-25 (Lo, ed., Human Press, Totowa, NJ, 2003). 사실상, 중쇄만으로 구성된 천연 발생 낙타과(camelid) 항체는 경쇄의 부재 하에서 작용적이고 안정하다 (Hamers-Casterman et al., (1993) Nature 363:446-448; Sheriff et al., (1996) Nature Struct. Biol. 3:733-736).
수많은 HVR 묘사가 사용되며, 본원에서 포괄된다. 카밧 상보성-결정 영역(CDR)은 서열 가변성에 기반하며, 가장 일반적으로 사용된다(Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991)). 초티아는 대신에, 구조적 루프의 위치를 지칭한다 (Chothia and Lesk, (1987) J. Mol. Biol. 196:901-917). 항원 접촉부에 대해, 하기를 참고한다: MacCallum et al. J. Mol . Biol. 262: 732-745 (1996). AbM HVR은 카밧 CDR 및 초티아 구조적 루프 간 절충을 나타내며, Oxford Molecular의 AbM 항체-모델링 소프트웨어에 의해 이용된다. "접촉" HVR은 이용 가능한 복합체 결정 구조의 분석에 기반한다. 이들 HVR 각각으로부터의 잔기가 아래에 주지된다.
루프
카밧
AbM
초티아
접촉점
L1
L24-L34
L24-L34
L26-L32
L30-L36
L2
L50-L56
L50-L56
L50-L52
L46-L55
L3
L89-L97
L89-L97
L91-L96
L89-L96
H1
H31-H35B
H26-H35B
H26-H32
H30-H35B (카밧 넘버링)
H1
H31-H35
H26-H35
H26-H32
H30-H35 (초티아 넘버링)
H2
H50-H65
H50-H58
H53-H55
H47-H58
H3
H95-H102
H95-H102
H96-H101
H93-H101
HVR은 하기와 같이 “연장된 HVR”을 포함할 수 있다: 24-36 또는 24-34 (L1), 46-56 또는 50-56 (L2) 및 89-97 또는 89-96 (L3) (VL 중쇄) 및 26-35 (H1), 50-65 또는 49-65 (H2) 및 93-102, 94-102, 또는 95-102 (H3) (VH 중쇄). 다르게 명시되지 않으면, 가변 도메인 (예를 들면, FR 잔기)에서 HVR 잔기, CDR 잔기 및 다른 잔기는 Kabat et al., 상기에 따라 본원에서 넘버링된다.
표현 "카밧에서의 가변-도메인 잔기-넘버링" 또는 "카밧에서의 아미노산-위치 넘버링" 및 이들의 변형은 [Kabat et al., 상기]에서 항체 편집의 중쇄 가변 도메인 또는 경쇄 가변 도메인에 대해 사용된 넘버링 시스템을 지칭한다. 상기 넘버링 시스템을 이용하여, 실제 선형 아미노산 서열은 가변 도메인의 FR 또는 HVR의 단축 또는 이것으로의 삽입에 대응하는 더 적거나 더 많은 아미노산을 포함할 수 있다. 예를 들면, 중쇄 가변 도메인에는 H2의 잔기 52 뒤에 단일 아미노산 삽입(카밧에 따른 잔기 52a) 및 중쇄 FR 잔기 82 뒤에 삽입된 잔기(예를 들면, 카밧에 따른 잔기 82a, 82b, 및 82c 등)가 포함될 수 있다. 잔기의 카밧 넘버링은 항체 서열의 상동성 영역에서 "표준" 카밧 넘버링된 서열과의 정렬에 의해 주어진 항체에 대해 결정될 수 있다.
"프레임워크" 또는 "FR"은 초가변 영역(HVR) 잔기 이외의 가변 도메인 잔기를 나타낸다. 가변 도메인의 FR은 일반적으로 4가지 FR 도메인으로 구성된다: FR1, FR2, FR3, 및 FR4. 따라서 HVR과 FR 서열은 일반적으로 VH (또는 VL)에서 하기 순서로 출현한다: FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
본원의 목적을 위해 "수용체 인간 프레임워크"는 아래에 정의된 바와 같은 인간 면역글로불린 프레임워크 또는 인간 공통 프레임워크로부터 유도된 경쇄 가변 도메인(VL) 프레임워크 또는 중쇄 가변 도메인(VH) 프레임워크의 아미노산 서열을 포함하는 프레임워크이다. 인간 면역글로불린 프레임워크 또는 인간 공통 프레임워크"로부터 유도된" 수용체 인간 프레임워크는 이의 동일한 아미노산 서열을 포함할 수 있거나, 또는 이것은 아미노산 서열 변화를 함유할 수 있다. 일부 구현예에서, 아미노산 변화의 수는 10개 이하, 9개 이하, 8개 이하, 7개 이하, 6개 이하, 5개 이하, 4개 이하, 3개 이하, 또는 2개 이하이다. 일부 구현예에서, VL 수용체 인간 프레임워크는 서열에 있어서 VL 인간 면역글로불린 프레임워크 서열 또는 인간 공통 프레임워크 서열과 동일하다.
“인간 공통 프레임워크”는 인간 면역글로불린 VL 또는 VH 프레임워크 서열의 선택에서 가장 통상적으로 존재하는 아미노산 잔기를 나타내는 프레임워크이다. 일반적으로, 인간 면역글로불린 VL 또는 VH 서열의 선택은 가변 도메인 서열의 하위그룹으로부터 이루어진다. 일반적으로, 서열의 하위그룹은 하기에서의 것과 같다: Kabat et al., Sequences of Proteins of Immunological Interest, Fifth Edition, NIH Publication 91-3242, Bethesda MD (1991), vols. 1-3. 일 구현예에서, VL에 대해, 하위그룹은 Kabat et al, 상기에서와 같이 하위그룹 카파 I이다. 일 구현예에서, VH에 대해, 하위그룹은 Kabat et al., 상기에서와 같이 하위그룹 III이다.
본원에서 용어 "Fc 영역"은 면역글로불린 중쇄의 C-말단 영역을 정의하기 위해 사용된다. 상기 용어는 천연 서열 Fc 영역 및 변이체 Fc 영역을 포함한다. 비록 면역글로불린 중쇄의 Fc 영역의 경계가 다양할지라도, 인간 IgG 중쇄 Fc 영역은 보통 위치 Cys226에서 아미노산 잔기로부터, 또는 Pro230으로부터 그 카복실-말단까지 연신하기 위해 정의된다. Fc 영역의 C 말단 리신 (잔기 447: EU 지수로 불리우는 EU 넘버링 시스템에 따르고 이는 하기 문헌에 기재된 바와 같다: Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991)은, 예를 들어 항체의 중쇄를 암호화하는 핵산을 재조합 가공함에 의하여, 또는 항체의 생산 또는 정제 동안, 제거될 수 있다. 따라서, 무손상 항체 조성물은 하기를 포함할 수 있다: 전체 K447 잔기가 제거된 항체 집단, K447 잔기가 전혀 제거되지 않은 항체 집단, 및 K447 잔기가 존재하는, 그리고 부재한 항체의 혼합물을 갖는 항체 집단. 용어 “Fc 수용체” 또는 "FcR"에는 또한 신생아 수용체, FcRn이 포함되며, 이는 친계 IgG의 태아로의 전달에 관여한다. Guyer et al., J. Immunol. 117: 587 (1976) 및 Kim et al., J. Immunol. 24: 249 (1994). FcRn로의 결합을 측정하는 방법이 공지된다 (예를 들어, 참고: Ghetie and Ward, Immunol. Today 18: (12): 592-8 (1997); Ghetie et al., Nature Biotechnology 15 (7): 637-40 (1997); Hinton et al., J. Biol. Med. Chem. 279(8): 6213-6 (2004); WO 2004/92219 (Hinton et al.). 279 (8): 6213-6 (2004); WO 2004/92219 (Hinton et al.). 생체내 FcRn로의 결합 및 인간 FcRn 고-친화도 결합 폴리펩티드의 혈청 반감기가 하기에서 검정될 수 있다: 예컨대, 인간 FcRn를 발현하는 형질전환 마우스 또는 형질감염 인간 세포주에서, 또는 변이체 Fc 영역을 갖는 폴리펩티드가 투여되는 영장류에서. WO 2004/42072 (Presta)는 FcR로의 개선되거나 감소된 결합을 갖는 항체 변이체를 기술한다. 예를 들면, 참고: Shields et al., J. Biol. Chem. 9(2): 6591-6604 (2001).
"친화도 성숙" 항체는 항원에 대한 항체의 친화도에 있어서의 개선을 야기하는 변경을 갖지 않는 친계 항체와 비교하여, 하나 이상의 초가변 영역(HVR)에 하나 이상의 변경을 갖는 항체를 나타내며, 이러한 변경은 항원에 대한 항체의 친화도에 있어서의 개선을 야기한다.
용어 “에피토프”는 항체가 결합하는 항원 분자 상의 부위를 가리킨다.
표준 항체와 “상동한 에피토프에 결합하는 항체”는 경쟁 검정에서 표준 항체의 이의 항원으로의 결합을 50% 이상 차단하는 항체를 지칭하고, 역으로, 표준 항체는 경쟁 검정에서 50% 이상으로 항체의 이의 항원으로의 결합을 차단한다. 예시적 경쟁 검정이 본원에 제공된다.
"네이키드 항체(naked antibody)"는 이종 잔기(예컨대, 세포독성 모이어티) 또는 방사성 표지에 콘주게이트되지 않은 항체를 지칭한다. 네이키드 항체는 약제학적 제형에 존재할 수 있다.
"효과기 기능"은 항체의 Fc 영역에 기인할 수 있는 생물학적 활성을 나타내며, 이것은 항체 이소형에 따라 변한다. 항체 효과기 기능의 예는 하기를 포함한다: 항체 효과기 기능의 예는 하기를 포함한다: C1q 결합 및 보체 의존적 세포독성 (CDC); Fc 수용체 결합; 항체-의존적 세포-매개된 세포독성 (ADCC); 식균작용; 세포 표면 수용체의 하향 조절 (예를 들면, B 세포 수용체); 및 B 세포 활성화.
"항체-의존적 세포-매개된 세포독성" 또는 "ADCC"는 특정 세포독성 세포 (예를 들면 자연 살해(NK) 세포, 호중구, 및 대식세포)에 존재한 Fc 수용체 (FcR) 상에서 결합된 분비된 Ig가 이들 세포독성 효과기 세포를 항원-보유 표적 세포에 특이적으로 결합시킬 수 있고 그 뒤에 표적 세포를 세포독소로 사멸시킬 수 있는 세포독성의 형태를 지칭한다. 항체 “아암”, 세포독성 세포는, 이러한 기전에 의하여 표적 세포의 사멸에 대해 요구된다. ADCC, NK 세포 매개용 1차 세포는 FcγRIII 만을 발현하고, 반면에 단핵구는 FcγRI, FcγRII 및 FcγRIII을 발현한다. 조혈 세포상의 Fc 발현은 다음 문헌의 464 페이지 상의 표 3에 요약되어 있다: Ravetch and Kinet, Annu. Rev. Immunol. 9: 457-92 (1991). 해당 분자의 ADCC 활성을 평가하기 위해, 예컨대 US 5,500,362 또는 US 5,821,337에 기재된, 시험관내 ADCC 검정이 수행될 수 있다. 이러한 검정을 위한 유용한 효과기 세포는 말초 혈액 단핵 세포 (PBMC) 및 자연 살해 (NK) 세포를 포함한다. 대안적으로 또는 추가로, 관심 분자의 ADCC 활성은 생체내, 예를 들면 [Clynes et al., PNAS USA 95:652-656 (1998)]에 개시된 것과 같은 동물 모델에서 평가될 수 있다.
“식균작용”은, 병원체가 숙주 세포 (예컨대, 대식세포 또는 호중구)에 의하여, 포식 또는 내부화된 공정을 지칭한다. 식균세포는 하기의 3개 경로에 의하여 식균 작용을 매개한다: (i) 직접 세포 표면 수용체 (예를 들어, 렉틴, 인테그린 및 스캐빈져 수용체) (ii) 보체 옵소닌화된 병원체에 결합하고, 이를 소화하기 위한, 보체 수용체를 사용한 증진된 보체 (C3b, CR3 및 CR4에 대한 CRI, 수용체 포함), 및 (iii) 항체 옵소닌화된 입자에 결합하고, 이후 내부화되고 리소좀과 결합하여 포식용해소체가 되기 위한, Fc 수용체를 사용한 증진된 보체 (Fc감마RI, Fc감마RIIA 및 Fc감마RIIIA). 본 발명에서, 경로 (iii)은 감염된 백혈구, 예컨대, 호중구 및 대식세포에 대한 항-MRSA AAC 치료제의 전달에 있어 중요한 역할을 하는 것으로 여겨진다 (Phagocytosis of Microbes: complexity in Action by D. Underhill and A Ozinsky. (2002) Annual Review of Immunology, Vol 20:825).
"보체의존적 세포독성" 또는 "CDC"는 보체의 존재하에 표적 세포의 용해를 지칭한다. 고전적 보체 경로의 활성화는, 그의 동원 항원에 결합되는, (적절한 하위부류의) 항체에 보체 시스템 (C1q)의 제1 성분의 결합에 의해 개시된다. 보체 활성화를 평가하기 위해, 예를 들면 [Gazzano-Santoro et al., J. Immunol. Methods 202: 163 (1996)]에 기재된 CDC 분석을 수행할 수 있다.
Fc 영역에 부착된 탄수화물은 변경될 수 있다. 포유동물 세포에 의해 생산된 천연 항체는 전형적으로 Fc 영역의 CH2 도메인의 Asn297에 대한 N-연결부에 의해 일반적으로 부착되는 분지형, 2분지형 올리고당을 포함한다. 예를 들면, 참고: Wright et al. (1997) TIBTECH 15:26-32. 올리고당은 다양한 탄수화물, 예를 들면, 만노스, N-아세틸 글루코사민 (GIcNAc), 갈락토오스, 및 시알산, 뿐만 아니라 2분지형 올리고당 구조의 "줄기"에서 GIcNAc에 부착된 푸코오스를 포함할 수 있다. 일부 구현예에서, 특정한 개선된 특성을 갖는 IgG를 생성하기 위해 IgG에서 올리고당의 변형이 이루어질 수 있다. 예를 들어, Fc 영역에 (직접적으로 또는 간접적으로) 부착된 푸코오스가 결핍된 탄수화물 구조를 갖는 항체 변형이 제공된다. 이와 같은 변형은 ADCC 작용을 향상시킬 가능성이 있다. 예를 들면, US 2003/0157108(Presta, L.); US 2004/0093621(Kyowa Hakko Kogyo Co., Ltd)를 참조한다. “탈푸코실화된” 또는 “푸코오스-결핍” 항체 변형과 관련된 공보의 예는 다음을 포함한다: US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO2005/053742; WO2002/031140; Okazaki et al., J. Mol. Biol. 336: 1239-1249 (2004); Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004). 탈푸코실화 항체를 생산할 수 있는 세포주의 예는, 단백질 푸코실화가 결핍된 Lee 13 CHO 세포(Ripka et al. Arch. Biochem. Biophys. 249:533-545 (1986); 미국 특허 출원 공보 번호 US 2003/0157108 A1, Presta, L; 및 WO 2004/056312 A1, Adams et al., 특히 실시예 11), 및 녹아웃 세포주, 예컨대 알파1,6-푸코실전달효소 유전자, FUT8, 녹아웃 CHO 세포 (참고, 예를 들면, Yamane-Ohnuki et al., Biotech. Bioeng. 87: 614 (2004); Kanda, Y. et al, Biotechnol. Bioeng., 94(4):680-688 (2006); 및 WO2003/085107)를 포함한다.
"단리된" 항체는 그 자연 환경의 성분으로부터 분리되는 것이다. 일부 구현예에서, 항체는 다음 기술에 의한 측정시 95% 또는 99% 초과의 순도로 정제된다: 예를 들어, 전기영동 (예를 들어, SDS-PAGE, 등전점 포커싱 (IEF), 모세관 전기영동) 또는 크로마토그래피(예를 들어, 이온 교환 또는 역상 HPLC). 항체 순도의 평가를 위한 방법의 검토를 위해, 예를 들면, 문헌[참조: Flatman et al., J. Chromatogr. B 848:79-87 (2007)]을 참고한다.
“단리된” 핵산은 이의 천연 환경의 성분으로부터 분리된 핵산 분자를 지칭한다. 단리된 핵산은 핵산 분자를 원래 함유하는 세포에 함유된 핵산 분자를 포함하지만, 핵산 분자는 염색체외에 또는 이의 자연 염색체 위치와는 다른 염색체 위치에 존재한다.
“rF1 항체를 암호화하는 단리된 핵산"은 항체 중쇄 및 경쇄를 암호화하는 하나 이상의 핵산 분자를 이러한 핵산 분자(들)를 단일 벡터 또는 별도의 벡터로 포함하여 나타내며, 이러한 핵산 분자(들)는 숙주 세포의 하나 이상의 위치에 존재한다.
본원에 사용된 바와 같이, 용어 “이에 특이적으로 결합하는” 또는 “이에 특이적인”은, 표적 및 항체 간의 결합과 같은 측정가능하고 재생가능한 상호작용을 지칭하며, 이는 생물학적 분자를 포함하는 분자의 이종성 집단의 존재 하에서의 표적의 존재에 대한 결정요인이다. 예를 들면, 표적 (에피토프일 수 있음)에 특이적으로 결합하는 항체는 다른 표적에 결합하는 것보다 더 큰 친화도, 결합능으로, 더욱 쉽게, 및/또는 더 긴 지속시간으로 상기 표적에 결합하는 항체이다. 일 구현예에서, rF1에 대한 비관련 표적에 대한 항체의 결합 정도는, 예를 들면, 방사면역검정법(RIA)으로 측정 시, 약 10% 미만의 항체의 결합이다. 특정 구현예에서, rF1에 특이적으로 결합하는 항체는 ≤ 1μM, ≤ 100 nM, ≤ 10 nM, ≤ 1 nM, 또는 ≤ 0.1 nM의 해리 상수 (Kd)를 갖는다. 특정 구현예에서, 항체는 상이한 종으로부터의 보존된 에피토프에 특이적으로 결합한다. 또 다른 구현예에서, 특이적 결합은 필연적으로 (비록 포함할 수 있어도) 배타적인 결합을 요구하지 않는다.
"결합 친화도"는 일반적으로 분자(예를 들면, 항체)의 단일 결합 부위와 이의 결합 파트너(예를 들면, 항원) 사이의 비공유 상호작용의 전체 합의 강도를 의미한다. 다르게 명시되지 않으면, 본원에서 사용된 바와 같이, "결합 친화도"는 결합 쌍 (예를 들면, 항체 및 항원)의 구성원 사이의 1:1 상호작용을 반영하는 고유 결합 친화도를 지칭한다. 파트너 Y에 대한 분자 X의 친화도는 일반적으로 해리 상수 (Kd)로 나타내어질 수 있다. 친화도는 본원에서 기재된 것을 포함하여 당해분야에서 공지된 공통의 방법으로 측정될 수 있다. 저-친화도 항체는 일반적으로 항원에 서서히 결합하고 쉽게 해리하는 경향이 있는 반면, 고-친화도 항체는 일반적으로 항원에 더 빨리 결합하고 더 오래 결합된 채 유지되는 경향이 있다. 결합 친화도를 결정하는 다양한 방법이 당해 분야에 공지되어 있고, 이들 중 임의의 것이 본 발명의 목적을 위해 사용될 수 있다. 결합 친화도를 측정하기 위한 특정의 구체적이고 예시적인 구현예들이 아래에 기재되어 있다.
일 양태에서, 본 발명에 따른 “Kd” 또는 “Kd 값”은 하기의 검정에 의해 기재된 바와 같은 목적하는 항체의 Fab 버전 및 이의 항원과 함께 수행된 방사능표지된 항원 결합 검정(RIA)에 의해 측정된다. 항원에 대한 Fab의 용액 결합 친화도는 일련의 적정된 비표지된 항원의 존재하에 최소 농도의 (125I)-표지된 항원으로 Fab를 평형화시키고 이어서 결합된 항원을 항-Fab 항체 코팅된 플레이트로 포획함에 의해 측정된다 (예를 들어, 참고: Chen et al., J. Mol. Biol. 293:865-881). 상기 검정에 대한 조건을 수립하기 위하여, 마이크로티터 플레이트 (DYNEX Technologies, Inc.)를 50 mM 탄산나트륨 (pH 9.6) 내의 5 (뮤 기호)g/ml의 포집 항-Fab 항체 (Cappel Labs)로 밤새 코팅하고, 이후 실온 (대락 23(온도 기호))에서 2 내지 5시간 동안 PBS 중 2% (w/v) 소 혈청 알부민으로 차단하였다. 비-흡착제 플레이트 (Nunc #269620)에서, 100 pM 또는 26 pM [125I]-항원은 해당 Fab의 연속 희석으로 혼합된다 (예를 들면, 항-VEGF 항체, Fab-12의 평가와 일치, Presta et al., Cancer Res. 57:4593-4599 (1997)). 그 다음 해당 Fab는 밤새 항온처리되지만; 그러나, 항온처리는 평형이 달성됨을 확인하기 위해 더 오랜 기간 (예를 들면, 약 65 시간)동안 계속할 수 있다. 그 후에, 혼합물은 실온에서 (예를 들면, 1 시간 동안) 항온처리를 위해 포착 플레이트로 이동된다. 용액을 이후 제거하고, 플레이트를 PBS 중 0.1% TWEEN-20TM 계면활성제로 8회 세정하였다. 플레이트를 건조시키는 경우, 150 μl/웰의 섬광제 (MICROSCINT-20 TM; Packard)를 첨가하고 플레이트는 10분 동안 TOPCOUNT TM 감마 카운터 (Packard) 상에서 계수한다. 최대 결합의 20% 이하를 제공하는 각각의 Fab의 농도는 경쟁 결합 검정에 사용하기 위해 선택한다.
또 다른 구현예에 따라서, BIACORE®-2000 또는 BIACORE®-3000 인스투르먼트 (BIAcore, Inc., Piscataway, NJ)을 이용한 표면-플라스몬 공명 검정은 ~10 반응 단위체 (RU)에서 고정된 항원 CM5 칩으로 25 ℃에서 수행된다. 간략하게, 카복시메틸화된 덱스트란 바이오센서 칩(CM5, BIACORE, Inc.)은 이의 공급업체의 설명서에 따라 N-에틸-N’-(3-디메틸아미노프로필)-카르보디이미드 하이드로클로라이드 (EDC) 및 N-하이드록시숙신이미드 (NHS)로 활성화시킨다. 항원은 pH 4.8, 10 mM 아세트산나트륨으로 5 μg/ml (0.2 μΜ) 까지 희석되고, 그 다음 5 μl/분의 유속으로 주입되어 커플링된 단백질의 대략 10 반응 단위체 (RU)를 달성한다. 항원 주사 후, 1 M 에탄올아민을 주사하여 미반응된 그룹을 차단시킨다. 역학적 측정을 위해, 2배 연속 희석된 Fab (0.78 nM 내지 500 nM)를 대략 25 μl/min의 유속으로 25°C 에서 PBS 중에서 0.05% 폴리소르베이트 20 (TWEEN-20TM) 계면활성제 (PBST)와 함께 사용한다. 결합율 (kon) 및 해리율 (koff)은 결합 및 해리 센서그램을 동시에 피팅함에 의해 단순한 1 대 1 랑무이르 결합 모델 (BIACORE ® 평가 소프트웨어 버젼 3.2)을 사용하여 계산한다. 평형 해리 상수(Kd)는 koff/kon 비율로서 산출된다. 참고: 예를 들면, Chen et al., J. Mol. Biol. 293:865-881 (1999). 만일 가역속도(on-rate)가 상기 표면 플라즈몬 공명 검정에 의해 106 M- 1 s-1 를 초과하면, 분광기, 예컨대 정지-유동 구비된 분광광도계 (Aviv Instruments) 또는 교반된 큐벳을 갖춘 8000-시리즈 SLM-AMINCOTM 분광광도계 (ThermoSpectronic)에서 측정된 바와 같이 항원의 증가 농도의 존재하에 25 ℃에서 pH 7.2, PBS내 20 nM 항-항원 항체 (Fab 형태)의 형광 방출 세기 (여기 = 295 nm; 방출 = 340 nm, 16 nm 대역통과)에서의 증가 또는 감소를 측정하는 형광성 켄칭 기술을 이용함으로써 가역 속도는 측정될 수 있다.
본 발명에 따른, "온-레이트", "결합의 속도", "결합 속도", 또는 “kon”은 또한 하기에 의하여 상기 기술된 바와 같이 측정된다: BIACORE® 2000 또는 BIACORE®-3000 시스템 (BIAcore, Inc., Piscataway, NJ).
용어 "숙주 세포", "숙주 세포주" 및 "숙주 세포 배양물"은 상호교환 가능하게 사용되며, 외인성 핵산이 도입되는 세포를 이러한 세포의 자손을 포함하여 나타낸다. 숙주 세포는 "형질전환체" 및 "형질전환된 세포"를 포함하며, 이것은 일차 형질전환 세포 및 계대배양의 횟수에 상관없이 이로부터 유도된 자손을 포함한다. 자손은 핵산 함량에 있어서 친계 세포와 완전히 동일하지 않을 수 있지만, 돌연변이를 함유할 수 있다. 원래 형질전환된 세포에 대해 선별되거나 선택된 바와 동일한 기능 또는 생물학적 활성을 갖는 돌연변이 자손이 본원에 포함된다.
본원에서 사용된 바와 같이, 용어 "벡터,"는 연결되는 또 다른 핵산을 전파시킬 수 있는 핵산 분자를 지칭한다. 용어는 자가-복제 핵산 구조로서의 벡터 뿐만 아니라 이것이 도입되는 숙주 세포의 게놈에 삽입되는 벡터를 포함한다. 특정 벡터는 이들이 작동적으로 연결되는 핵산의 발현을 지시할 수 있다. 상기 벡터는 본원에서 "발현 벡터"로서 지칭된다.
기준 폴리펩티드 서열에 관한 "아미노산 서열 동일성 퍼센트(%)"는, 서열 동일성의 일부로서 어떠한 보존적 치환도 고려하지 않고서 서열을 정렬하고, 필요에 따라, 갭을 도입하여 최대 서열 동일성 퍼센트를 달성한 후, 기준 폴리펩티드 서열에서의 아미노산 잔기와 동일한 후보 서열에서의 아미노산 잔기의 백분율로서 정의된다. 아미노산 서열 동일성 퍼센트를 측정하기 위한 목적으로의 정렬은, 예를 들면, BLAST, BLAST-2, ALIGN 또는 Megalign (DNASTAR) 소프트웨어와 같은 공개적으로 이용 가능한 컴퓨터 소프트웨어를 사용하여 당업계의 재량 내에 있는 다양한 방식으로 달성될 수 있다. 당업계의 숙련가들은 비교되는 서열의 전체 길이에 걸쳐 최대의 정렬을 달성하는데 필요한 알고리즘을 포함하여, 서열을 정렬하기 위한 적합한 파라미터를 결정할 수 있다. 그러나, 본원의 목적을 위해, % 아미노산 서열 동일성 값은 서열 비교 컴퓨터 프로그램 ALIGN-2를 사용하여 생성된다. ALIGN-2 서열 비교 컴퓨터 프로그램은 제조사 (Genentech, Inc.)에 의해 개발되었고, 소스 코드는 사용자 기록문서와 함께 하기와 같이 제출되었다: 미국 저작권 청, 워싱턴 D.C., 20559, 하기 하에서 등록됨: 미국 저작권 등록 번호 TXU510087. ALIGN-2 프로그램은 캘리포니아주 사우스 샌 프란시스코에 소재하는 Genentech, Inc.로부터 공개적으로 이용 가능하거나, 또는 소스 코드로부터 편집될 수 있다. ALIGN-2 프로그램은 디지털 UNIX V4.0D를 포함한 UNIX 운영 체제에서 사용하기 위해 편집되어야 한다. 모든 서열 비교 매개변수는 ALIGN-2 프로그램에 의해 설정되어 바뀌지 않는다.
ALIGN-2가 아미노산 서열 비교에 사용되는 상황에서, 소정의 아미노산 서열 A 내지, 및, 또는 소정의 아미노산 서열 B(이것은 소정의 아미노산 서열 B에 대해 특정의 아미노산 서열 동일성 %를 갖거나 포함하는 소정의 아미노산 서열 A로서 표현될 수 있음)의 아미노산 서열 동일성 %는 다음과 같이 계산된다: 분수 X/Y의 100배, 상기 식 중, X는 A 및 B의 프로그램 정렬에서 서열 정렬 프로그램 ALIGN-2에 의한 동일한 매치로서 스코어되는 아미노산 잔기의 수이고 Y는 B에서 아미노산 잔기의 총 수이다. 아미노산 서열 A의 길이가 아미노산 서열 B의 길이와 동일하지 않은 경우, A 대 B의 % 아미노산서열 동일성은 B 대 A의 % 아미노산 서열 동일성은 동일하지 않음을 인식할 것이다. 달리 구체적으로 기재하지 않은 경우, 본원에 사용된 모든 % 아미노산 서열 동일성 값은 기술된 바와 같이 수득한다.
용어 "리파마이신-유형 항생제"는, 리파마이신의 구조를 갖거나, 또는 이와 유사한 구조를 갖는 항생제 그룹의 부류를 의미한다.
용어 "리파라질-유형 항생제"는, 리파라질의 구조를 갖거나, 또는 이와 유사한 구조를 갖는 항생제 그룹의 부류를 의미한다.
치환체의 수를 표지할 경우, 용어 "하나 이상"은 일 치환체로부터 가장 높은 수의 가능한 치환 수까지의 범위, 즉, 치환에 의한, 일 수소의 교체로부터 모든 수소의 교체까지의 범위를 지칭한다. 용어 "치환체"는, 친계 분자 상에서 수소 원자를 대체하는 원자, 또는 원자 그룹을 나타낸다. 용어 "치환된"은 하나 이상의 치환체를 보유하는 특정 그룹을 나타낸다. 임의의 기가 다중 치환체를 가질 수 있고, 다양한 가능한 치환체가 제공될 경우, 치환체는 독립적으로 선택되며, 상동할 필요는 없다. 용어 "비치환된"은 치환체 보유하지 않는 특정 기를 의미한다. 용어 "임의로 치환된"은, 가능한 치환체의 군으로부터 독립적으로 선택된, 하나 이상의 치환체에 의하여 비치환 또는 치환된다. 치환체의 수를 표지할 경우, 용어 "하나 이상"은 일 치환체로부터 가장 높은 수의 가능한 치환 수까지의 범위, 즉, 치환에 의한, 일 수소의 교체 내지 모든 수소의 교체를 의미한다.
본원에서 사용된 용어 "알킬"은 1개 내지 12개 탄소 원자 (C1-C12)의 포화된 선형 또는 분지형-쇄 1가 탄화수소 라디칼을 지칭하고, 여기서 알킬 라디칼은 독립적으로 하나 이상의 하기 기술된 치환체로 임의로 치환될 수 있다. 또 다른 구현예에서, 알킬 라디칼은 1 내지 8개 탄소 원자 (C1-C8), 또는 1 내지 6개 탄소 원자 (C1-C6)이다. 예시는 비제한적으로 하기를 포함한다: 메틸 (Me, -CH3), 에틸 (Et, -CH2CH3), 1-프로필 (n-Pr, n-프로필, -CH2CH2CH3), 2-프로필 (i-Pr, i-프로필, -CH(CH3)2), 1-부틸 (n-Bu, n-부틸, -CH2CH2CH2CH3), 2-메틸-1-프로필 (i-Bu, i-부틸, -CH2CH(CH3)2), 2-부틸 (s-Bu, s-부틸, -CH(CH3)CH2CH3), 2-메틸-2-프로필 (t-Bu, t-부틸, -C(CH3)3), 1-펜틸 (n-펜틸, -CH2CH2CH2CH2CH3), 2-펜틸 (-CH(CH3)CH2CH2CH3), 3-펜틸 (-CH(CH2CH3)2), 2-메틸-2-부틸 (-C(CH3)2CH2CH3), 3-메틸-2-부틸 (-CH(CH3)CH(CH3)2), 3-메틸-1-부틸 (-CH2CH2CH(CH3)2), 2-메틸-1-부틸 (-CH2CH(CH3)CH2CH3), 1-헥실 (-CH2CH2CH2CH2CH2CH3), 2-헥실 (-CH(CH3)CH2CH2CH2CH3), 3-헥실 (-CH(CH2CH3)(CH2CH2CH3)), 2-메틸-2-펜틸 (-C(CH3)2CH2CH2CH3), 3-메틸-2-펜틸 (-CH(CH3)CH(CH3)CH2CH3), 4-메틸-2-펜틸 (-CH(CH3)CH2CH(CH3)2), 3-메틸-3-펜틸 (-C(CH3)(CH2CH3)2), 2-메틸-3-펜틸 (-CH(CH2CH3)CH(CH3)2), 2,3-디메틸-2-부틸 (-C(CH3)2CH(CH3)2), 3,3-디메틸-2-부틸 (-CH(CH3)C(CH3)3 , 1-헵틸, 1-옥틸, 등.
본원에서 사용된 용어 "알킬렌"은 1개 내지 12개 탄소 원자 (C1-C12)의 포화된 선형 또는 분지형-쇄 2가 탄화수소 라디칼을 지칭하고, 여기서 알킬렌 라디칼은 독립적으로 하나 이상의 하기 기술된 치환체로 임의로 치환될 수 있다. 또 다른 구현예에서, 알킬렌 라디칼은 1 내지 8개 탄소 원자 (C1-C8), 또는 1 내지 6개 탄소 원자 (C1-C6)이다. 전형적인 알킬렌 라디칼은 비제한적으로 하기를 포함한다: 메틸렌 (-CH2-), 에틸렌 (-CH2CH2-), 프로필렌 (-CH2CH2CH2-) 등.
용어 "알켄일"은, 적어도 하나의 불포화 부위, 즉, 탄소-탄소, sp2 이중 결합을 갖는, 2개 내지 8개 탄소 원자 (C2-C8)의 선형 또는 분지형-쇄 1가 탄화수소 라디칼을 지칭하고, 여기서 알켄일 라디칼은 독립적으로 하나 이상의 본원에 기술된 치환체로 임의로 치환될 수 있고, “시스” 및 “트랜스” 배향, 또는 대안적으로, “E” 및 “Z” 배향을 갖는 라디칼을 포함한다. 예시는 비제한적으로 에틸렌일 또는 비닐 (-CH=CH2), 알릴 (-CH2CH=CH2) 등을 포함한다.
용어 "알켄일렌"은, 적어도 하나의 불포화 부위, 즉, 탄소-탄소, sp2 이중 결합을 갖는, 2개 내지 8개 탄소 원자 (C2-C8)의 선형 또는 분지형-쇄 2가 탄화수소 라디칼을 지칭하고, 여기서 알켄일렌 라디칼은 독립적으로 하나 이상의 본원에 기술된 치환체로 임의로 치환될 수 있고, “시스” 및 “트랜스” 배향, 또는 대안적으로, “E” 및 “Z” 배향을 갖는 라디칼을 포함한다. 예시는 비제한적으로 에틸렌일렌 또는 비닐렌 (-CH=CH-), 알릴 (-CH2CH=CH-) 등을 포함한다.
용어 "알킨일"은, 적어도 하나의 불포화 부위, 즉, 탄소-탄소, sp 삼중 결합을 갖는, 2개 내지 8개 탄소 원자 (C2-C8)의 선형 또는 분지형 1가 탄화수소 라디칼을 지칭하고, 여기서 알킨일 라디칼은 독립적으로 하나 이상의 본원에 기술된 치환체로 임의로 치환될 수 있다. 예시는 비제한적으로 에티닐 (-C≡CH), 프로핀일 (프로파르길, -CH2C≡CH), 등을 포함한다.
용어 "알킨일렌"은, 적어도 하나의 불포화 부위, 즉, 탄소-탄소, sp 삼중 결합을 갖는, 2개 내지 8개 탄소 원자 (C2-C8)의 선형 또는 분지형 2가 탄화수소 라디칼을 지칭하고, 여기서 알킨일렌 라디칼은 독립적으로 하나 이상의 본원에 기술된 치환체로 임의로 치환될 수 있다. 예시는 비제한적으로 에티닐렌 (-C≡C-), 프로핀일렌 (프로파르길렌, -CH2C≡C-), 등을 포함한다.
용어 “탄소환”, “카르보사이클일”, “탄소환계 환” 및 “사이클로알킬”은, 3 내지 12 탄소 원자(C3-C12)를 단환계 환으로서, 또는 7 내지 12 탄소 원자를 이환계 환으로서 갖는 1가 비-방향족, 포화 또는 부분적으로 불포화된 환을 지칭한다. 7 내지 12개 원자를 갖는 이환계 탄소환은 예를 들면, 바이사이클로 [4,5], [5,5], [5,6] 또는 [6,6] 시스템으로서 배열될 수 있고, 그리고 9 또는 10개 환 원자를 갖는 이환계 탄소환은, 바이사이클로 [5,6] 또는 [6,6] 시스템으로서, 또는 가교된 시스템 예컨대 바이사이클로[2.2.1]헵탄, 바이사이클로[2.2.2]옥탄 및 바이사이클로[3.2.2]노난으로서 배열될 수 있다. 스피로 모이어티가 또한 본 정의의 범위 내에 포함된다. 단환계 탄소환의 예는 비제한적으로 하기를 포함한다: 사이클로프로필, 사이클로부틸, 사이클로펜틸, 1-사이클로펜트-1-에닐, 1-사이클로펜트-2-에닐, 1-사이클로펜트-3-에닐, 사이클로헥실, 1-사이클로헥스-1-에닐, 1-사이클로헥스-2-에닐, 1-사이클로헥스-3-에닐, 사이클로헥사디엔일, 사이클로헵트일, 사이클로옥트일, 사이클로노닐, 사이클로데실, 사이클로운데실, 사이클로도데실 등. 카르보사이클일 기는 독립적으로 본 명세서에 기술된 하나 이상의 치환체로 임의로 치환된다.
용어 "아릴"은 친계(parent) 방향족 환 시스템의 단일 탄소 원자로부터 하나의 수소 원자를 제거하여 유도된 6-20개 탄소 원자(C6-C20)의 1가 방향족 탄화수소 라디칼을 의미한다. 일부 아릴 기는 “Ar”로서 예시적 구조로 나타나 있다. 아릴은 포화된, 부분적으로 불포화된 환, 또는 방향족 탄소환계 환에 융합된 방향족 환을 포함하는 이환계 라디칼을 포함한다. 전형적인 아릴 기는 하기로부터 유도된 라디칼을 포함한다: 벤젠 (페닐), 치환된 벤젠, 나프탈렌, 안트라센, 바이페닐, 인데닐, 인다닐, 1,2-디하이드로나프탈렌, 1,2,3,4 테트라하이드로나프틸 등. 아릴 기는 독립적으로 본 명세서에 기술된 하나 이상의 치환체로 임의로 치환된다.
"아릴렌"은 친계 방향족 환 시스템의 2개 탄소 원자로부터 2개의 수소 원자를 제거하여 유도된 6-20개 탄소 원자(C6-C20)의 2가 방향족 탄화수소 라디칼을 의미한다. 일부 아릴렌 기는 “Ar”로서 예시적 구조로 나타나 있다. 아릴렌은 포화된, 부분적으로 불포화된 환, 또는 방향족 탄소환계 환에 융합된 방향족 환을 포함하는 이환계 라디칼을 포함한다. 전형적인 아릴렌 기는 하기로부터 유도된 라디칼을 포함한다: 벤젠 (페닐렌), 치환된 벤젠, 나프탈렌, 안트라센, 바이페닐렌, 인데닐렌, 인다닐렌, 1,2-디하이드로나프탈렌, 1,2,3,4 테트라하이드로나프틸 등. 아릴렌 기는 본 명세서에 기술된 하나 이상의 치환체로 임의로 치환된다.
용어 “헤테로환,” “헤테로사이클일” 및 “헤테로환계 환”은 본원에서 상호교환가능하게 사용되고, 3 내지 약 20개의 환 원자의, 부분적으로 불포화된 (즉, 환 내 하나 이상 이중 및/또는 삼중 결합을 가짐) 탄소환계 라디칼을 지칭하며, 여기서 적어도 하나의 환 원자는 질소, 산소, 인 및 황으로부터 선택된 헤테로원자이고, 나머지 환 원자는 C이고, 하나 이상의 환 원자는 독립적으로, 하기 기술된 하나 이상의 치환체로 임의로 치환된다. 헤테로환은 3 내지 7 환 구성원 (2 내지 6개 탄소 원자)을 갖는 단환, 또는 7 내지 10 환 구성원 (N, O, P, 및 S로부터 선택된 4 내지 9개 탄소 원자 및 1 내지 4개 헤테로원자)를 갖는 이환, 예를 들어: 바이사이클로 [4,5], [5,5], [5,6], 또는 [6,6] 계일 수 있다. 예시적 헤테로환은 하기에 기술된다: Paquette, Leo A.; “Principles of Modern Heterocyclic Chemistry” (W.A. Benjamin, New York, 1968), 특히 챕터 1, 3, 4, 6, 7, 및 9; “The Chemistry of Heterocyclic Compounds, A series of Monographs” (John Wiley & Sons, New York, 1950 to present), 특히 발행판 13, 14, 16, 19, 및 28; 및 J. Am. Chem. Soc. (1960) 82:5566. "헤테로사이클릴"은 또한 헤테로사이클 라디칼이 포화된, 부분적으로 불포화된 환 또는 방향족 탄소환계 또는 헤테로환계 환와 융합된 라디칼을 포함한다. 헤테로환계 환의 예는 모르폴린-4-일, 피페리딘-1-일, 피페라진일, 피페라진-4-일-2-온, 피페라진-4-일-3-온, 피롤리딘-1-일, 티오모르폴린-4-일, S-디옥소티오모르폴린 4-일, 아조칸-1-일, 아제티딘-1-일, 옥타하이드로피리도[1,2-a]피라진-2 일, [1,4]디아제판-1-일, 피롤리디닐, 테트라하이드로퓨란일, 디하이드로퓨란일, 테트라하이드로티에닐, 테트라하이드로피란일, 디하이드로피란일, 테트라하이드로티오피란일, 피페리디노, 모르폴리노, 티오모르폴리노, 티옥사닐, 피페라지닐, 호모피페라지닐, 아제티디닐, 옥세타닐, 티에타닐, 호모피페리디닐, 옥세파닐, 티에파닐, 옥사제핀일, 디아제핀일, 티아제핀일, 2-피롤린일, 3-피롤린일, 인돌린일, 2H-피란일, 4H-피란일, 디옥사닐, 1,3-디옥솔란일, 피라졸린일, 디티아닐, 디티올란일, 디하이드로피란일, 디하이드로티에닐, 디하이드로퓨란일, 피라졸리디닐이미다졸린일, 이미다졸리디닐, 3-아자바이사이클로[3.1.0]헥산일, 3-아자바이사이클로[4.1.0]헵타닐, 아자바이사이클로[2.2.2]헥산일, 3H-인돌릴 퀴놀리지닐 및 N-피리딜 우레아를 포함하지만 이에 제한되지 않는다. 스피로 모이어티가 또한 본 정의의 범위 내에 포함된다. 2 환 원자가 옥소 (=O) 모이어티로 치환된 헤테로환계 기의 예는 피리미디노닐 및 1,1-디옥소-티오모르폴린일이다. 본 명세서에서 헤테로사이클 기는 독립적으로 본 명세서에 기술된 하나 이상의 치환체로 임의로 치환된다.
용어 "헤테로아릴"은 5-, 6-, 또는 7-원 환의 일가 방향족 라디칼을 지칭하며 질소, 산소, 및 황으로부터 독립적으로 선택된 적어도 하나의 헤테로원자를 함유하는 5-20 원자의 융합된 환 시스템 (이 중 적어도 하나는 방향족)을 포함한다. 헤테로아릴 기의 예는 하기이다: 피리딘일 (예를 들어, 2-하이드록시피리딘일 포함), 이미다졸일, 이미다조피리딘일, 피리미딘일 (예를 들어, 4-하이드록시피리딘일 포함), 피라졸일, 트리아졸일, 피라진일, 테트라졸일, 푸릴, 티에닐, 이속사졸일, 티아졸일, 옥사디아졸일, 옥사졸일, 이소티아졸일, 피롤일, 퀴노린일, 이소퀴노린일, 테트라하이드로이소퀴노린일, 인돌일, 벤즈이미다졸일, 벤조푸란일, 신노린일, 인다졸일, 인도리진일, 프탈라진일, 피리다진일, 트리아진일, 이소인돌일, 프테리딘일, 푸린일, 옥사디아졸일, 트리아졸일, 티아디아졸일, 티아디아졸일, 푸라잔일, 벤조푸라잔일, 벤조티오펜일, 벤조티아졸일, 벤즈옥사졸일, 퀴나졸린일, 퀴녹사린일, 나프티리딘일, 및 푸로피리딘일. 헤테로아릴 기는 독립적으로 본 명세서에 기술된 하나 이상의 치환체로 임의로 치환된다.
헤테로환 또는 헤테로아릴 기는, 가능할 경우, 결합된 탄소 (탄소-연결됨), 또는 질소 (질소-연결됨)일 수 있다. 예로써 및 비제한적으로, 탄소 결합된 헤테로환 또는 헤테로아릴은 피리딘의 위치 2, 3, 4, 5, 또는 6, 피리다진의 위치 3, 4, 5, 또는 6, 피리미딘의 위치 2, 4, 5, 또는 6, 피라진의 위치 2, 3, 5, 또는 6, 푸란, 테트라하이드로푸란, 티오푸란, 티오펜, 피롤 또는 테트라하이드로피롤의 위치 2, 3, 4, 또는 5, 옥사졸, 이미다졸 또는 티아졸의 위치 2, 4, 또는 5, 이속사졸, 피라졸, 또는 이소티아졸의 위치 3, 4, 또는 5, 아지리딘의 위치 2 또는 3, 아제티딘의 위치 2, 3, 또는 4, 퀴놀린의 위치 2, 3, 4, 5, 6, 7, 또는 8 또는 이소퀴놀린의 위치 1, 3, 4, 5, 6, 7, 또는 8에서 결합된다.
예로써 및 비제한적으로, 질소 결합된 헤테로환 또는 헤테로아릴은 아지리딘, 아제티딘, 피롤, 피롤리딘, 2-피롤린, 3-피롤린, 이미다졸, 이미다졸리딘, 2-이미다졸린, 3-이미다졸린, 피라졸, 피라졸린, 2-피라졸린, 3-피라졸린, 피페리딘, 피페라진, 인돌, 인돌린, 1H-인다졸의 위치 1, 이소인돌, 또는 이소인돌린의 위치 2, 모폴린의 위치 4, 및 카바졸, 또는 β-카볼린의 위치 9에서 결합된다.
"대사물"은 명시된 화합물 또는 이의 염의 신체에서 대사를 통하여 생성된 생성물이다. 화합물의 대사물질은 본 분야에서 공지된 방법을 사용하여 식별될 수 있고, 그리고 이들의 활성은 본원에 기술된 것들과 같은 시험을 사용하여 측정된다. 그러한 생성물은 예를 들어 투여된 화합물의 산화, 환원, 가수분해, 아미드화, 탈아미드화, 에스터화, 탈에스터화, 효소 절단 등으로부터 기인할 수 있다. 따라서, 본 발명은 이의 대사성 생성물을 산출하기에 충분한 기간 동안 본 발명의 화학식 I 화합물을 포유동물에 접촉시키는 단계를 포함하는 방법에 의해 생성되는 화합물을 포함하는, 본 발명의 화합물의 대사물질을 포함한다.
용어 "약제학적 제형"은 그안에 함유된 활성 성분의 생물학적 활성이 효과적이도록 하기 위한 형태인, 그리고 제형이 투여되는 대상체에 허용불가능하게 독성인 추가의 성분을 함유하지 않는 제제를 지칭한다.
"멸균" 제형은 무균성으로 즉 모든 살아 있는 미생물과 이들의 포자가 없다.
“안정한” 제형은, 그 안의 단백질이 본질적으로 저장 시 이의 물리적 및 화학적 안정성 및 온전성을 보유하는 것이다. 단백질 안정성을 측정하기 위한 다양한 분석적 기술은 본 분야에서 수득가능하며 하기에 검토된다: Peptide and Protein Drug Delivery, 247-301, Vincent Lee Ed., Marcel Dekker, Inc., New York, New York, Pubs. (1991) and Jones, A. Adv. Drug Delivery Rev. 10: 29-90 (1993). 안정성은 선택된 기간 동안 선택된 온도에서 측정될 수 있다. 신속한 스크리닝을 위하여, 배합물은 안정성이 측정된 시간인, 2주 내지 1달 동안 40C에서 저장될 수 있다. 상기 제형은 2-8℃에서 저장될 것이며, 일반적으로 상기 제형은 적어도 1개월 동안 30℃ 또는 40℃, 및/또는 적어도 2년 동안 2-8℃에서 안정할 것이다. 상기 제형은 30℃에서 저장될 것이며, 일반적으로 상기 제형은 적어도 2년 동안 30℃, 및/또는 적어도 6년 동안 40℃에서 안정할 것이다. 예를 들면, 저장 동안의 응집의 정도는 단백질 안정성의 표지자로서 사용될 수 있다. 따라서, “안정한” 제형은, 약 10% 미만 및 바람직하게는 약 5% 미만의 단백질이 상기 제형 내 응집물로서 존재할 수 있는 것이다. 기타 구현예에서, 상기 제형의 저장 동안 응집물 형성의 임의의 증가가 측정될 수 있다.
“등장성” 제형은, 인간 혈액과 상동한 삼투압을 본질적으로 갖는 것이다. 등장성 제형은 일반적으로 약 250 내지 350 mOsm의 삼투압을 가질 것이다. 용어 “저삼투압”은 인간 혈액의 것 미만의 삼투압을 갖는 제형을 기술한다. 상응하게, 용어 “고삼투압”은 인간 혈액의 것 초과의 삼투압을 갖는 제형을 기술하기 위하여 사용된다. 등장성은, 예를 들어, 증기 압력 또는 얼음-동결 유형 삼투압계를 사용하여 측정될 수 있다. 본 발명의 제형은 염 및/또는 완충제의 부가의 결과로서 고삼투압성이다.
본원에 사용된 바와 같이, "담체”는 하기를 포함한다: 약제학적으로 허용가능한 담체, 부형제, 또는 안정화제 (이용된 투여량 및 농도에서 이에 노출된 세포 또는 포유동물에 비독성임). 생리학적으로 허용가능한 담체는, 종종, 수성 pH 완충액이다. 생리학적으로 허용되는 담체의 예는 완충제, 예를 들어, 포스페이트, 시트레이트, 및 기타 유기산; 아스코르브산을 포함하는 항산화제; 저분자량(약 10개 잔기 미만) 폴리펩티드; 단백질, 예를 들어, 혈청 알부민, 겔라틴, 또는 면역글로불린; 친수성 중합체, 예를 들어, 폴리비닐피롤리돈; 아미노산, 예를 들어, 글라이신, 글루타민, 아스파라긴, 아르기닌 또는 라이신; 글루코스, 만노스 또는 덱스트린을 포함하는 모노사카라이드, 디사카라이드, 및 다른 탄수화물; 킬레이팅제, 예를 들어, EDTA; 당 알콜, 예를 들어, 만니톨 또는 소르비톨; 염 형성 반대 이온, 예를 들어, 나트륨; 및/또는 비이온성 계면활성제, 예를 들어 TWEEN®, 폴리에틸렌글리콜(PEG), 및 PLURONICS™ 을 포함한다.
"약제학적으로 허용가능한 담체"는 활성 성분을 제외한, 대상체에 비독성인, 약제학적 제형 중 성분을 가리킨다. 약제학적으로 허용가능한 담체에는 비제한적으로, 완충제, 부형제, 안정제 또는 보존제가 포함된다. “약제학적으로 허용가능한 산”은, 이들이 제형화되는 농도 및 방식에서 비독성인 무기 및 유기 산을 포함한다. 예를 들어, 적합한 무기 산은 하기를 포함한다: 염산, 과염산, 브롬화수소산, 아이오딘화수소산, 질산, 황산, 술폰산, 술핀산, 술파닐산, 인산, 탄산 등. 적합한 유기 산은 하기를 포함하는 직쇄 및 분지형-쇄 알킬, 방향족, 환형, 지환족, 아릴지방족, 헤테로환, 포화, 불포화, 단일, 디- 및 트리-카르복실산을 포함한다: 예를 들어, 포름산, 아세트산, 2-하이드록시아세트산, 트리플루오로아세트산, 페닐아세트산, 트리메틸아세트산, t-부틸 아세트산, 안트란일산, 프로피온산, 2-하이드록시프로피온산, 2-옥소프로피온산, 프로판디온산, 사이클로펜탄프로피온산, 사이클로펜탄 프로피온산, 3-페닐프로피온산, 부탄산, 부탄디오산, 벤조산, 3-(4-하이드록시벤조일)벤조산, 2-아세톡시벤조산, 아스코브산, 신남산, 라우릴 황산, 스테아르산, 무콘산, 만델산, 석신산, 엠본산, 푸마르산, 말산, 말레산, 하이드록시말레산, 말론산, 락트산, 시트르산, 타르타르산, 글리콜산, 글리콘산, 글루콘산, 피루브산, 글리옥살산, 옥살산, 메실산, 석신산, 살리실산, 프탈산, 팔모산, 팔메산, 티오시안산, 메탄술폰산, 에탄술폰산, 1,2-에탄디술폰산, 2-하이드록시에탄술폰산, 벤젠술폰산, 4-클로로벤젠술폰산, 나프탈렌-2-술폰산, p-톨루엔술폰산, 캄포르술폰산, 4-메틸바이사이클로[2.2.2]- 옥트-2-에네-1-카르복실산, 글루코헵톤산, 4,4’-메틸렌비스-3-(하이드록시-2-에네-1-카복실산), 하이드록시나프토산.
“약제학적으로 허용가능한 염기”는, 이들이 제형화되는 농도 및 방식에서 비독성인 무기 및 유기 염기를 포함한다. 예를 들어, 적합한 염기는 무기 염기 형성 금속으로부터 형성된 것들이며, 예컨대 하기이다: 예컨대 리튬, 나트륨, 칼륨, 마그네슘, 칼슘, 암모늄, 철, 아연, 구리, 망간, 알루미늄, N-메틸글루카민, 모르폴린, 피페리딘 및 유기 비독성 염기 (1차, 2차 및 3차 아민, 치환 아민, 환형 아민 포함) 및 염기성 이온 교환 수지, [예컨대 N(R’)4 + (여기서 R’는 독립적으로 H 또는 C1-4 알킬, 예컨대 암모늄, 트리스임)], 예를 들어, 이소프로필아민, 트리메틸아민, 디에틸아민, 트리에틸아민, 트리프로필아민, 에탄올아민, 2-디에틸아미노에탄올, 트리메타민, 디사이클로헥실아민, 리신, 아르기닌, 히스티딘, 카페인, 프로카인, 하이드라바민, 콜린, 베타인, 에틸렌디아민, 글루코사민, 메틸글루코사민, 테오브로민, 푸린, 피페라진, 피페리딘, N-에틸피페리딘, 폴리아민 수지 등. 특히 바람직한 유기 비-독성 염기는 이소프로필아민, 디에틸아민, 에탄올아민, 트리메타민, 디사이클로헥실아민, 콜린, 및 카페인이다.
본 발명과 함께 사용가능한 추가의 약제학적으로 허용가능한 산 및 염기는 하기로부터 유도된 것들을 포함한다: 아미노산, 예를 들어, 히스티딘, 글리신, 페닐알라닌, 아스파르트산, 글루탐산, 리신 및 아스파라긴.
“약제학적으로 허용가능한” 완충제 및 염은 상기 표지된 산 및 염기의 산 및 염기 부가 염 둘 모두로부터 유도된 것들을 포함한다. 특정 완충제 및/ 또는 염은 히스티딘, 석시네이트 및 아세테이트를 포함한다.
“약제학적으로 허용가능한 당”은, 관심 단백질과 조합될 경우, 저장 시 단백질의 화학적 및/또는 물리적 불안정성을 유의미하게 예방하거나 감소시키는 분자이다. 제형이 동결건조되고, 이후 재구성될 것으로 의도되는 경우, “약제학적으로 허용가능한 당”은 또한 “동결건조보호제”로서 공지될 수 있다. 예시적 당 및 이들의 상응하는 당 알코올은 하기를 포함한다: 아미노산 예컨대 1나트륨 글루탐산염 또는 히스티딘; 메틸아민 예컨대 베타인; 유방성 염 예컨대 마그네슘 술페이트; 폴리올 예컨대 3수소 이상 분자량의 당 알코올, 예컨대 글리세린, 덱스트란, 에리트롤, 글리세롤, 아라비톨, 자일리톨, 소르비톨, 및 만니톨; 프로필렌 글리콜; 폴리에틸렌 글리콜; PLURONICS®; 및 이의 조합. 추가의 예시적 동결건조보호제는 하기를 포함한다: 글리세린 및 젤라틴, 및 당 멜리비오스, 멜레지토스, 라피노스, 만노트리오스 및 스타키오스. 환원 당의 예시는 하기를 포함한다: 글루코오스, 말토스, 락토스, 말투로스, 이소-말투로스, 및 락투로스. 비-환원 당의 예시는, 당 알코올 및 기타 직쇄 폴리알코올로부터 선택된 폴리하이드록시 화합물의 비-환원 글리코시드를 포함한다. 바람직한 당 알코올은 모노글리코시드, 특히 이당류 예컨대 락토스, 말토스, 락투로스, 및 말투로스의 환원에 의하여 수득된 화합물이다. 글리코시드 측면 기는 글루코시드류, 또는 갈락토시드류일 수 있다. 당 알코올의 추가 예시는 글루시톨, 말티톨, 락티톨 및 이소-말투로스이다. 바람직한 약제학적으로-허용가능한 당은 비-환원 당 트레할로오스 또는 수크로오스이다. 약제학적으로 허용가능한 당은, “보호량” (예컨대 사전-동결건조)으로 상기 제형에 첨가되며, 이는 단백질이 저장 동안 (예컨대 재구성 및 저장 후) 이의 물리적 및 화학적 안정성 및 온전성을 유지한다는 것을 의미한다.
본원에서 관심 “희석제”는, 액체 제형, 예컨대 동결건조 후 재구성된 제형의 제조에 유용하고, 약제학적으로 허용가능한 (인간으로의 투여에 안전하고 비-독성인) 것이다. 예시적 희석제는 멸균수, 정균 주사용 물 (BWFI), pH 완충된 용액 (예를 들면 포스페이트-완충된 염수), 멸균된 염수 용액, 링거 용액 또는 덱스트로오스 용액을 포함한다. 대안적 구현예에서, 희석제는 염 및/또는 완충제의 수성 용액을 포함할 수 있다.
“보존제”는, 박테리아 활성을 감소시키기 위하여 본원에서 상기 제형에 첨가될 수 있는 화합물이다. 보존제의 첨가는, 예를 들어, 다중-용도 (다중-용량) 제형의 생산을 촉진할 수 있다. 잠재적 보존제의 예시는 하기를 포함한다: 옥타데실디메틸벤질 암모늄 클로라이드, 헥사메토늄 클로라이드, 벤즈알코늄 클로라이드 (알킬 기가 장쇄 화합물인 알킬벤질디메틸암모늄 클로라이드의 혼합물), 및 벤즈에토늄 클로라이드. 보존제의 기타 유형은 하기를 포함한다: 방향족 알코올 예컨대 페놀, 부틸 및 벤질 알코올, 알킬 파라벤 예컨대 메틸 또는 프로필 파라벤, 카테콜, 레조르시놀, 사이클로헥사놀, 3-펜탄올, 및 m-크레졸. 본원에서 가장 바람직한 보존제는 벤질 알코올이다.
"개체" 또는 "대상체” 또는 “환자”는 포유동물이다. 포유동물에는 가축 (가령, 소, 양, 고양이, 개, 그리고 말), 영장류 (가령, 인간과 비-인간 영장류, 예를 들면, 원숭이), 래빗, 그리고 설치류 (가령, 생쥐와 쥐)가 포함되지만 이들에 국한되지 않는다. 특정 구현예에서, 개체 또는 대상체는 인간이다.
본원에 사용된 바와 같은 “치료” (및 “치료하다” 또는 “치료하는”의 문법적 변형어구)는 임상적 병리학 과정 동안에 치료받는 세포 또는 조직의 본래의 과정을 변화시키도록 설계된 임상적 처치를 지칭한다. 치료의 목적 효과는 비제한적으로 하기를 포함한다: 본 분야의 숙련가, 예컨대 진료의에 의하여 모두 측정가능한, 질환 진행 속도 감소, 질환 병태의 완화 또는 경감, 및 관해 또는 개선된 예후. 일 구현예에서, 치료는 하기를 의미할 수 있다: 증상의 완화, 질환의 임의의 직접적 또는 간접적 병리 결과의 약화, 감염성 질환 진행 속도의 감소, 질환 상태의 개선 또는 경감, 및 차도 또는 향상된 예후. 일부 구현예에서, 본 발명의 AAC 및 TAC는, 혈류 및/또는 감염 조직 및 장기 내 박테리아 부하를 감소시키거나, 감염성 질환의 진행을 늦추거나, 또는 질환의 발병을 지연시키기 위하여 사용된다.
본원에 사용된 바와 같이, "~와 결합하여”는 기타 치료 양식에 더하여 일 치료 양식을 투여하는 것을 지칭한다. 따라서, "~와 결합하여”는 개체에게 기타 치료 양식을 투여하기 전, 동안, 또는 후의 일 치료 양식을 투여하는 것을 지칭한다.
용어 “균혈증”은, 혈액 배양물을 통하여 가장 통상적으로 검출된, 혈류 내 박테리아의 존재를 지칭한다. 박테리아는 혈류에 진입하여, 수술 동안 (특히 점막 예컨대 위장관을 수단하는 경우), 또는 동맥 또는 정맥에 진입하는 기타 외래 개체로 인하여, 감염의 중증 합병증 (폐렴 또는 뇌수막염과 같은)을 초래할 수 있다. 균혈증은 몇몇 결과를 초래할 수 있다. 박테리아에 대한 면역 반응은, 상대적으로 높은 사망률을 갖는 패혈증 및 패혈성 쇼크를 야기할 수 있다. 박테리아는 또한, 혈류를 이용하여 몸체의 다른 부분으로 확산되어, 감염 본래 부위로부터 멀리 떨어진 곳의 감염을 야기할 수 있다. 예시는 심내막염 또는 골수염을 포함한다.
“치료적 유효량”은 특정 장애의 측정가능한 개선 또는 예방을 부여하는데 요구되는 최소 농도이다. 치료적 유효량은 개체의 질환 단계, 연령, 성별 및 체중과 같은 요인, 및 환자에서의 목적 반응을 일으키는 항체의 능력에 따라 가변될 수 있다. 치료적 유효량은 또한 항체의 임의의 독성 또는 유해 효과가 치료적 유익 효과를 능가하는 것이다. 일 구현예에서, 치료적 유효량은, 생체내 감염에서의 균혈증을 감소시키기에 효과적인 양이다. 일 양태에서, “치료적 유효량”은 약물 투여 전과 비교하여, 적어도 1 로그 만큼, 환자 샘플 예컨대 혈액으로부터 단리된 박테리아 부하 또는 콜로니 형성 단위체 (CFU)를 감소시키는데 적어도 효과적인 양이다. 추가의 특정 양태에서, 감소는 적어도 2 로그만큼이다. 또 다른 양태에서, 감소는 적어도 3, 4, 5 로그만큼이다. 추가의 또 다른 양태에서, 환원은, 본원에서 예시된 검정을 포함한 본 분야에서 공지된 검정을 사용한 검출 가능한 수준 미만으로 되게 하는 것이다. 또 다른 구현예에서, 치료적 유효량은, 감염 환자의 치료 개시에서의, 또는 그 전의 양성 혈액 배양물과 비교하여, 음성 혈액 배양물 (즉, AAC의 표적인 박테리아가 성장하지 않는)을 달성하는, 치료 기간 과정에 걸쳐 주어진 1회 이상의 용량으로의 AAC의 양이다.
"예방적 유효량"은 원하는 예방 결과를 달성하기 위해 필요한 기간 동안 그러한 투여량에서, 유효한 양을 나타낸다. 반드시 그런 것은 아니지만 통상적으로, 초기 질환 병기 전에, 또는 심지어 감염 위험이 증가하는 병태에 대한 노출 전에 대상체 내에서 예방항적 용량이 사용되므로, 예방학적 유효량은 치료학적 유효량보다 적을 수 있다. 일 구현예에서, 방지적 유효량은, 일 세포에서 또 다른 세포로의 감염의 발생 또는 이의 전파를 감소, 예방하기에 적어도 유효한 양이다.
“만성” 투여는, 연장된 기간 동안 초기 치료 효과 (활성)을 유지하기 위하여, 급성 형태와 반대로 연속적인 약제(들)의 투여를 지칭한다. “간헐적” 투여는 저해 없이 구성적으로 수행되지 않지만, 천연적으로 순환적인 치료이다.
용어 “팩키지 삽입물”은 치료학적 제품의 상업 팩키지에 통상적으로 포함되는 지침서를 지칭하기 위해 사용되고 이는 상기 치료학적 제품의 사용에 관한 지적사항, 용도, 투여량, 투여, 조합 치료요법, 사용금지 사항 및/또는 경고에 관한 정보를 함유한다.
용어 "키랄"은 거울상 파트너의 비-중첩성 (non-superimposability)의 특성을 갖는 분자를 나타내는 반면에, 용어 "아키랄 (achiral)"은 그들의 거울상 파트너 상에 중첩할 수 있는 분자를 나타낸다.
용어 "입체이성체"는 상동한 화학적 구성을 갖지만, 공간에서 원자 또는 그룹의 배열에 관해서는 상이한 화합물을 나타낸다.
"부분입체이성질체"는 둘 이상의 부제성(chirality) 중심을 가지고 그의 분자들이 서로 거울상이 아닌 입체이성질체를 지칭한다. 부분입체이성질체는 상이한 물리적 특성, 예컨대 녹는점, 끓는점, 스펙트럼 특성, 및 반응성을 가진다. 부분입체이성체의 혼합물은 전기영동 및 크로마토그래피와 같은 고분할 검정절차에 따라 분리시킬 수 있다.
"거울상이성질체"는 서로 비-중첩성인 거울상인 화합물의 두 입체이성질체를 지칭한다.
본 명세서에서 사용되는 입체화학적 정의 및 관용어는 일반적으로 하기에 따른다: S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, New York; 및 Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds (1994) John Wiley & Sons, Inc., New York. 많은 유기 화합물은 광학 활성 형태로 존재하는데, 즉 이들은 평면-편광의 평면을 회전시키는 능력을 갖는다. 광학 활성 화합물을 기술함에 있어서, 접두어 D 및 L, 또는 R 및 S는 그것의 키랄 중심(들)에 대한 분자의 절대 배열을 표시하기 위해 사용된다. 접두어 d 및 l 또는 (+) 및 (-)는 화합물에 의한 평면-편광의 회전의 부호를 표시하기 위해 이용되며, (-) 또는 1로 화합물이 좌측회전성임을 의미한다. (+) 또는 d가 접두사인 화합물은 우선성이다. 주어진 화학적 구조에 있어서, 이들 입체이성질체는 이들이 서로 거울상임을 제외하고 동일하다. 특정 입체이성질체는 또한 거울상이성질체로 지칭될 수 있고, 이러한 이성질체의 혼합물은 종종 거울상이성질체 혼합물로 불린다. 거울상이성질체의 50:50 혼합물은 화학 반응 또는 공정에서 입체선택 또는 입체특이성이 없는 경우에 발생할 수 있는 라세미 혼합물 또는 라세미체라 칭한다. 용어 "라세미 혼합물" 및 "라세미체"는 광학 활성이 없는 두 거울상이성질성 화학종의 등몰 혼합물을 지칭한다.
용어 "보호기"는 화합물 상의 특정 작용기를 차단 또는 보호하는 한편 다른 작용기와 반응하기 위하여 통상적으로 사용되는 치환체를 지칭한다. 예를 들어, "아미노-보호기"는 화합물 중의 아미노 작용기를 차단 또는 보호하는, 아미노 기에 부착된 치환체이다. 적합한 아미노-보호기는 아세틸, 트리플루오로아세틸, t-뷰톡시카르보닐(BOC), 벤질옥시카르보닐 (CBZ) 및 9-플루오렌일메틸렌옥시카르보닐(Fmoc)을 비제한적으로 포함한다. 보호기 및 이들의 사용에 대한 일반적인 기술에 대하여, 하기를 참고한다: T. W. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 1991, 또는 상기 이후의 간행판.
본원에 사용된 바와 같이 용어 "약"은 본 기술 분야의 숙련가에게 쉽게 공지된 각각의 값에 대한 통상적인 오차 범위를 나타낸다. 본원에서 "약(about)" 값 또는 파라미터에 대한 지칭은 상기 값 또는 파라미터 그 자체에 관한 구현예를 포함한다 (그리고 기술한다).
본원에서 및 첨부된 청구항에서 사용된 바와 같이, 단수 형태는 맥락이 명확히 다르게는 표지하지 않는 한 복수의 지시대상을 포함한다. 예를 들어, "항체"에 대한 지칭은 1 내지 다수의 항체, 예컨대 몰량에 대한 지칭이고, 당업자에게 공지된 이의 균등물 등을 포함한다.
III.
조성물 및 방법
항체-항생제
콘주게이트
(
AAC
)
본원에서 실험적 결과는, 세포내 박테리아를 제거하는 것을 목표로 하는 치료가 임상적인 성공을 개선시킬 것이라는 강한 표지이다. 이러한 목표를 향하여, 본 발명은, 숙주 세포의 세포내 구획을 침범한 S. 아우레우스 유기체를 임의로 사멸하는 고유한 치료법을 제공한다. 본 발명은 그와 같은 치료제가 반코마이신과 같은 종래의 항생제가 실패한 생체-내 모델에서 유효하다는 것을 입증한다.
본 발명은, 전통적인 항생제 요법을 회피하는, 박테리아 집단을 표적화함에 의하여 항생제 이탈을 예방하는 것을 목표로 하는 항박테리아 요법을 제공한다. 신규한 항박테리아 요법은 항체 항생제 콘주게이트 (AAC)로 달성되며, 여기서 S. 아우레우스 (MRSA 포함) 상에서 발견되는 세포 벽 성분에 특이적인 rF1 항체는 강력한 리파마이신-유형 항생제 (리파마이신 유도체)와 화학적으로 결합된다. 리파마이신-유형 항생제는, 대부분의 포유동물 세포 유형에서 발견되는 카텝신 B, 리소좀 프로테아제를 포함하는, 프로테아제에 의하여 절단되도록 설계된, 프로테아제-절단가능한, 비-펩티드 링커를 통하여 항체에 결합된다 (Dubowchik et al (2002) Bioconj. Chem. 13:855-869). 이의 3개 성분을 갖는 AAC의 다이어그램이 도 2에 도시된다. 임의의 이론에 구속됨이 없이, AAC 작용의 일 기전은 도 3에 도식화된다. AAC는, 리파마이신-유형 항생제가 링커가 절단되기까지 불활성 (항체의 큰 사이즈 때문에)이라는 점에서, 전구-약물로서 작용한다. 천연 감염사례 내 발견되는 S. 아 우레우스의 유의미한 비율이 숙주 내 감염 과정 동안 일정 시점에서 숙주 세포, 주로 호중구 및 대식세포에 의하여 흡수되므로, 숙주 세포 내 소비된 시간은 박테리아로 하여금 항생제 활성을 회피하기 위한 유의미한 기회를 제공한다. 본 발명의 AAC는, Staph 박테리아에 결합하고, 그리고 박테리아가 숙주 세포에 의하여 흡수된 후, 포식용해소체 내 항생제를 방출하도록 설계된다. 이러한 기전에 의하여, AAC는 전통적 항생제에 의하여 불량하게 치료된 위치에 특이적으로 활성인 항생제를 집중시킬 수 있다. 본 발명이 특정 작용 기전에 의하여 제한 또는 국한되지 않는 경우, AAC는 하기 3개의 잠재적 기전을 통하여 항생제 활성을 개선한다: (1) AAC는 박테리아를 흡수하는 포유동물 세포 내 항생제를 전달함으로써, 포식용해소체로 불량하게 확산된 항생제 효능을 증가시키며, 여기서 박테리아는 격리된다. (2) AAC는, 포식용해소체 내 격리되는 동안, 박테리아를 옵소닌화함으로써, 식세포에 의한 유리 박테리아의 흡수를 증가시키고, 항생제를 국소적으로 방출하여 박테리아를 사멸한다. 수천개의 AAC가 단일 박테리아와 결합할 수 있으므로, 이러한 플랫폼은 최대 항미생물 사멸을 지속하기 위하여 이들의 세포내 틈새 내로 충분한 항생제를 방출한다. 더욱이, 더욱 많은 박테리아가 기존 세포내 저장소로부터 방출될 수록, 이러한 항체-기반 요법의 더욱 빠른 개시 속도(on-rate)가, 이들이 인접 또는 윈위 세포로 일탈하기 전에 이들 박테리아의 즉각적인 “태깅(tagging)”을 보장하여, 이로써 감염의 추가 확산을 경감시킨다. (3) AAC는, 혈청으로부터 빠르게 청소된 항생제와 비교하여, 항생제를 항체에 연결시킴으로써 생체내 항생제의 반감기를 개선한다 (개선된 약동학). AAC의 개선된 약동학은 영역 내 충분한 항생제의 전달을 가능하게 하며, 여기서 전신 투여가 필요한 항생제의 전체 용량을 제한하는 한편 S . 아우레우스는 농축된다. 이러한 특성은 최소한의 항생제 부작용으로 끈질긴 감염을 표적화하여 AAC로의 장기 요법을 허용시킬 것이다.
본 발명의 항체-항생제 콘주게이트 화합물은 재조합 도입된 시스테인을 통하여 프로테아제-절단가능한 비-펩티드 링커에 의해, 리파마이신-유형 항생제에 공유 부착된, 항-SDR 항체를 포함한다.
예시적 구현예에서, 항-SDR 항체 (예컨대 rF1 항체)는 재조합 도입 시스테인 아미노산을 포함하는 시스테인 가공 항체이다.
예시적 구현예에서, 프로테아제-절단가능한, 비-펩티드 링커는, rF1, 항 SDR 항체 상에서, 재조합 도입 시스테인을 통하여 리파마이신-유형 항생제에 공유 부착된다.
예시적인 구현예는 다음 화학식을 갖는 항체-항생제 콘주게이트이다:
여기서:
Ab는 rF1 항체이고; 그리고
프로테아제-절단가능한, 비-펩티드 링커 PML은 하기 화학식을 갖는다:
여기서 Str은 연신부 단위체이고; PM은 펩티드도미메틱 단위체이고, 그리고 Y는 스페이서 단위체이며;
abx는 리파마이신-유형 항생제이고; 그리고
p는 정수 1 내지 8이다.
리파마이신-유형 항생제는 리파라질-유형 항생제일 수 있다.
리파마이신-유형 항생제는, 프로테아제-절단가능한, 비-펩티드 링커에 부착된 4차 아민을 포함한다.
항체-항생제 콘주게이트의 예시적인 구현예는 하기 화학식 I을 갖는다:
여기서:
상기 단속선은 임의의 결합을 나타내고;
R은 H, C1-C12 알킬, 또는 C(O)CH3 이고;
R1 는 OH이며;
R2는 CH=N-(헤테로사이클릴)이고, 여기서 상기 헤테로사이클릴은 C(O)CH3, C1-C12 알킬, C1-C12 헤테로아릴, C2-C20 헤테로사이클릴, C6-C20 아릴, 및 C3-C12 카르보사이클릴로부터 독립적으로 선택된 1종 이상의 기로 임의로 치환되고;
또는 R1 및 R2 는 5- 또는 6-원 융합된 헤테로아릴 또는 헤테로사이클릴을 형성하고, 그리고 임의로 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환을 형성하고, 여기서 상기 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환은 H, F, Cl, Br, I, C1-C12 알킬, 또는 OH로 임의로 치환되고;
PML은 R2 또는 R1 및 R2에 의해 형성된 융합된 헤테로아릴 또는 헤테로사이클릴에 부착된 프로테아제-절단가능한 비-펩티드 링커이고; 그리고
Ab는 rF1 항체이고; 그리고
항체 분자에 반응성 링커 모이어티를 통해 콘주게이트될 수 있는 항생제 모이어티의 수는 본원에 기재된 방법에 의해 도입되는 유리 시스테인 잔기의 수에 의해 제한될 수 있다. 예시적 AAC는, 1, 2, 3, 또는 4개의 가공된 시스테인 아미노산을 갖는 항체를 포함한다 (Lyon, R. et al (2012) Methods in Enzym. 502:123-138).
MRSA 상에서 유효한 표적이 되기 위하여, 에피토프는 바람직하게는 모든 임상적 MRSA 균주 내 높은 정도로 보존되고, 감염 동안 높은 정도로 풍부하며, 안정적으로 발현된다. rF1 항체는 이러한 요건을 충족하며, 또한 뿐만 아니라 추가적으로, Staph 에피더미디스에 결합한다.
항-SDR 및
rF1
항체
항-SDR 항체는, F1 항체의 생성을 위하여 하기 기술된 바와 같이 생산될 수 있다. rF1, SD2, SD3 및 SD4를 포함한 항-SDR 항체의 몇몇 예시가 본원에 제공된다.
rF1 Ab는 본원에서 상세히 설명될 것이다.
rF1 항체는 완전히 인간의 것이며, 스타필로코쿠스 종 예컨대 S. 아우레우스 및 S. 에피더미디스에 특이적으로 결합할 수 있다. 중요하게는, rF1은 생체내 뿐만 아니라 시험관내로, 전체 박테리아에 결합할 수 있다. 더욱이, 항체 rF1은, 감염 조직, 예를 들어, 동물 내에서 성장한 박테리아에 결합할 수 있다. 본원에 제공된 rF1 또는 이의 작용성 등가물은, S. 아우레우스 표면 단백질 ClfA, ClfB, SdrC, SdrD 및 SdrE에 결합할 수 있다.
표 4A 및 표 4B는, 친계 항체 F1, rF1 항체 및 이의 변이체의 H 쇄 및 L 쇄 CDR 서열의 배열을 나타낸다. F1 및 rF1는, FW1 및 LC CDR3 내 서열과 상이하며 (QHYXRFPYT, 여기서 X는 I 또는 M일 수 있으며 (서열 번호: 26); F1은 I이며 (서열 번호: 6) 그리고 rF1 은 M이다 (서열 번호: 7).
표 4A: 중쇄 CDR 서열
표 4B
경쇄 CDR 서열
일 구현예에서, H 및 L 쇄 프레임워크 (FR) 서열은 하기와 같다:
다양한 아미노산 변형이 안정성 및 작용을 개선하기 위하여 rF1에 대해 이루어질 수 있다. HC CDR2에서, NG 탈아민화(deamindation) 부위는 4번째 잔기 N 내지 S를 교체함으로써 제거되며, 이로써 항체의 안정성이 개선된다. rF1 내 존재하는 심각한 항체 응집을 제거하기 위하여, LC 골격에 대한 TV의 보수가 이루어졌다.
본 발명의 치료 AAC를 형성하는 콘주게이션을 위하여, H 및 L 쇄의 하기 쌍형성이 이루어져 전체 4량체 항체를 형성할 수 있다. 박스 표시는 CDR1, CDR2, CDR3 서열이다. 도입 시스테인 (C)은 밑줄로 표시된다. 진한 표시의 잔기는 친계 F1 상의 아미노산 변화이다. L 쇄 내에서, 진한 표시의 “RTV” 후의 A는 불변 영역의 제1 잔기이다. H 쇄 내 카밧 위치 114에서의 밑줄로 표시된 C에서 불변 영역이 개시된다.
1A 및 2A에서, 전장 (FL) L 쇄 (서열 번호: 9, C 카파의 말단에 근접한 aa 205에서 가공된 Cys를 가짐)는 하기와 쌍형성한다: FL IgG1 H 쇄 (서열 번호: 10 (Cys 없음)). 이러한 항체는, AAC를 형성하기 위한, 링커 항생제 단위체에 대한 콘주게이션을 위하여, 각 L 쇄 상에 1개씩, 2개의 Cys 부위를 가질 것이다.
1A. rF1-V205C FL 경쇄
2A. rF1.v1 FL 중쇄 (Cys 없음), rF1 V205C 경쇄의 Cys205와의 쌍
1B 및 2A에서, rF1.v6 L 쇄 (서열 번호: 11, 가공된 Cys를 가짐)는 하기와 쌍형성한다: FL IgG1 H 쇄 (서열 번호: 10 (Cys 없음)). 이러한 항체는, 링커 항생제 단위체에 대한 콘주게이션을 위하여, 각 L 쇄 상에 1개씩, 2개의 Cys 부위를 가질 것이다.
1B. rF1.v6-V205C 경쇄
2B를 갖는 1B에서, 각 L 및 H 쇄는 가공된 Cys를 가지며, 이에 따라 사량체 항체는 최대 4 AAR (항생제:항체 비율)을 가질 수 있다.
2B.
Cys114를 갖는, rF1.v1 FL 중쇄 (114 카밧 넘버링, 또는 118 -Eu 넘버링 )
rF1.v1 H 쇄 가변 영역
rF1 L 쇄 가변 영역
rF1.v6 L 쇄 가변 영역
rF1를 포함하는 항-SDR Ab는 시스테인으로 대체되었던 시스테인 이외의 적어도 하나의 아미노산을 포함할 수 있다. 일부 구현예에서, 시스테인 이외의 적어도 하나 아미노산은 하기이다: 발린 (경쇄 위치 205) 및 또는 발린 (경쇄 위치 110), 및 또는 알라닌 (중쇄 위치 114), 여기서 아미노산 넘버링은, 카밧 (1991)에 따르며, 이는 Eu 넘버링 협약에 따른 위치 118과 상동하다.
리파마이신-유형 항생제 모이어티
항체-항생제 콘주게이트 (ADC)의 항생제 모이어티 (abx)는, 세포독성 또는 세포증식억제를 갖는 리파마이신-유형 항생제 또는 기이다. 리파마이신은, 노카르디아 메디테라네이(Nocardia mediterranei), 아미코라톱시스 메디테라네이(Amycolatopsis mediterranei)에 의하여 천연적으로 또는 인공적으로 수득되는 항생제의 군이다. 이들은 박테리아 RNA 폴리머라아제를 억제하는 보다 큰 안사마이신(Ansamycin) 패밀리의 하위부류이며 (Fujii et al (1995) Antimicrob. Agents Chemother. 39:1489-1492; Feklistov, et al (2008) Proc Natl Acad Sci USA, 105(39): 14820-5), 그람-양성 및 선택적 그람-음성 박테리아에 대한 효능을 갖는다. 리파마이신은 특히 마이코박테리아에 대해 효력이 있으며, 따라서 투베르쿨로시스, 한센병, 및 마이코박테리아 아비움 복합성 (MAC) 감염을 치료하는데 사용된다. 리파마이신-유형 군은 하기를 포함한다: “전통적” 리파마이신 약물, 뿐만 아니라 리파마이신 유도체 리팜피신 (리팜핀, CA Reg. No. 13292-46-1), 리파부틴 (CA Reg. No. 72559-06-9; US 2011/0178001), 리파펜틴 및 리파라질 (CA Reg. No. 129791-92-0, Rothstein et al (2003) Expert Opin. Investig. Drugs 12(2):255-271; Fujii et al (1994) Antimicrob. Agents Chemother. 38:1118-1122. 다수의 리파마이신-유형 항생제는 내성 진행의 유해한 특성을 공유한다 (Wichelhaus et al (2001) J. Antimicrob. Chemother. 47:153-156). 리파마이신은 1957년에 스트렙토마이세스 메디테라네이 (Streptomyces mediterranei)로부터 처음 단리되었다. 약 7종의 리파마이신이 발견되었으며, 리파마이신 A, B, C, D, E, S, 및 SV로 지칭된다 (US 3150046). 리파마이신 B이 상업적으로 처음 도입되었고, 이는 1960년대에 약물-내성 투베르쿨로시스를 치료하는데 유용하였다. 리파마이신은 다수의 질환, 가장 중요하게는 HIV-관련 투베르쿨로시스의 치료에 대해 사용되었다. 많은 수의 수득가능한 유사체 또는 유도체로 인하여, 리파마이신은 통상적으로 사용되는 항생제에 내성이 된 병원체 박테리아의 제거에 널리 이용되었다. 예를 들어, 리팜피신은 약물 내성을 예방하는 이의 강력한 효과 및 능력에 대해 알려져 있다. 이는 신속하게 급속-분열하는 바실루스 균주를 사멸하며, 뿐만 아니라 긴 기간 동안 생물학적으로 불활성으로 남아있어 이들로 하여금 항생제 활성에서 회피하도록 하는 “존속성균(persisters)” 세포도 사멸한다. 추가로, 리파부틴 및 리파펜틴은 둘 모두 HIV-양성 환자 내 획득된 투베르쿨로시스에 대해 사용되어 왔다.
화학식 I 항체-항생제 콘주게이트의 항생제 모이어티 (abx)는 하기 구조를 갖는 리파마이신 유형 모이어티이다:
여기서:
상기 단속선은 임의의 결합을 나타내고;
R은 H, C1-C12 알킬, 또는 C(O)CH3 이고;
R1 는 OH이며;
R2는 CH=N-(헤테로사이클릴)이고, 여기서 상기 헤테로사이클릴은 C(O)CH3, C1-C12 알킬, C1-C12 헤테로아릴, C2-C20 헤테로사이클릴, C6-C20 아릴, 및 C3-C12 카르보사이클릴로부터 독립적으로 선택된 1종 이상의 기로 임의로 치환되고;
또는 R1 및 R2 는 5- 또는 6-원 융합된 헤테로아릴 또는 헤테로사이클릴을 형성하고, 그리고 임의로 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환을 형성하고, 여기서 상기 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환은 H, F, Cl, Br, I, C1-C12 알킬, 또는 OH로 임의로 치환되고; 그리고
비-펩티드 링커 PML은 R2 에 공유 부착된다.
리파마이신-유형 모이어티의 구현예는 하기이다:
식 중, R3은 독립적으로 H 및 C1-C12 알킬로부터 선택되고; R4 는 H, F, Cl, Br, I, C1-C12 알킬, 및 OH로부터 선택되며; 그리고 Z는 NH, N(C1-C12 알킬), O 및 S로부터 선택되고; 그리고 비-펩티드 링커 PML은 N(R3)2 의 질소 원자에 공유 부착된다.
리팜피신-유형 모이어티의 구현예는 하기이다:
여기서,
식 중, R5은 H 및 C1-C12 알킬로부터 선택되고; 그리고 비-펩티드 링커 PML은 NR5 의 질소 원자에 공유 부착된다.
리파부틴-유형 모이어티의 구현예는 하기이다:
식 중, R5은 H 및 C1-C12 알킬로부터 선택되고; 그리고 비-펩티드 링커 PML은 NR5 의 질소 원자에 공유 부착된다.
벤조옥사진오리파마이신-유형 모이어티의 구현예는 하기이다:
식 중, R5은 H 및 C1-C12 알킬로부터 선택되고; 그리고 비-펩티드 링커 PML은 NR5 의 질소 원자에 공유 부착된다.
벤조옥사진오리파마이신-유형 모이어티의 구현예는, pipBOR로 본원에서 지칭되며, 하기이다:
식 중, R3은 독립적으로 H 및 C1-C12 알킬로부터 선택되고; 그리고 비-펩티드 링커 PML은 N(R3)2 의 질소 원자에 공유 부착된다.
벤조옥사진오리파마이신-유형 모이어티의 구현예는, 디메틸pipBOR로 본원에서 지칭되며, 하기이다:
비-펩티드 링커 PML은 N(CH3)2 의 질소 원자에 공유 부착된다.
반-합성 유도체 리파마이신 S, 또는 감소된, 나트륨 염 형태 리파마이신 SV는, 몇몇 단계에서 리파라질 유형 항생제로 전환될 수 있으며, 여기서 R은 H 또는 Ac이며, R3은 독립적으로 H 및 C1-C12 알킬로부터 선택되고; R4 는 H, F, Cl, Br, I, C1-C12 알킬, 및 OH로부터 선택되며; 그리고 Z는 NH, N(C1-C12 알킬), O 및 S로부터 선택된다 (예를 들어, 참고: WO 2014/194247의 도 23A 및 B, 및 도 25A 및 B). 벤족사지노 (Z = O), 벤즈티아지노 (Z = S), 벤즈디아지노 (Z = NH, N(C1-C12 알킬) 리파마이신이 제조될 수 있다 (US 7271165). 치환체를 함유하는 벤즈옥사진오리파마이신 (BOR), 벤즈티아진오리파마이신 (BTR), 및 벤즈디아진오리파마이신 (BDR) 유사체는 하기에 따라 넘버링된다: US 7271165 중 화학식 A (칼럼 28) (이는 본 목적을 위하여 참고로 편입됨). "25-O-데아세틸" 리파마이신은, 아세틸 기가 25-위치에서 제거된 리파마이신 유사체를 의미한다. 이러한 위치가 추가로 유도된 유사체는 "25-O-데아세틸-25-(치환체) 리파마이신”으로 지칭되며, 여기서 상기 유도화 기에 대한 명명법은 완전한 화합물 명칭으로의 “치환체”를 대체한다.
리파마이신-유형 항생제 모이어티는 하기에 개시된 것들과 유사한 방법에 의하여 합성될 수 있다: US 4610919; US 4983602; US 5786349; US5981522; US 4859661; US 7271165; US 2011/0178001; Seligson, et al., (2001) Anti-Cancer Drugs 12:305-13; Chem. Pharm. Bull., (1993) 41:148, 및 WO 2014/194247 (이의 각각은 본원에 참조로 인용됨). 리파마이신-유형 항생제 모이어티는 항미생물 활성에 대해 하기에 의하여 스크리닝될 수 있다: 이들의 최소 억제성 농도 (MIC)를 측정함에 의하여, 시험관내 검정으로 표준 MIC을 사용함에 의하여 (Tomioka et al., (1993) Antimicrob. Agents Chemother. 37:67).
리파마이신-S 벤족사진오리파마이신
프로테아제-절단가능한 비-펩티드 링커
“프로테아제-절단가능한, 비-펩티드 링커” (PML)는 화학식 I의 항체-항생제 콘주게이트 (AAC)를 형성하기 위하여 하나 이상의 항생제 모이어티 (abx) 및 항체 단위체 (Ab)에 공유 부착되는 이중작용적 또는 다중작용적 모이어티이다. AAC 내 프로테아제-절단가능한, 비-펩티드 링커는 세포내 프로테아제에 의한 절단 (리소좀성 조건하에서의 것을 포함)에 대한 기질이다. 프로테아제는 다양한 카텝신 및 카스파제를 포함한다. 세포 내로의 AAC의 비-펩티드 링커의 절단은 항-박테리아 효과를 갖는 리파마이신-유형 항생제를 방출할 수 있다.
항체-항생제 콘주게이트 (AAC)는, 항생제 (abx) 및 항체 (Ab)에 결합하기 위한 반응성 작용기를 갖는 링커 시약 또는 링커 항생제 중간체를 이용하여 편리하게 제조될 수 있다. 일 예시적 구현예에서, 시스테인 가공 항체 (Ab)의 시스테인 티올은 링커 시약, 항생제 모이어티 또는 항생제 링커 중간체의 작용기와의 결합을 형성할 수 있다.
AAC의 PML 모이어티는 1개의 아미노산 잔기를 포함할 수 있다.
AAC의 PML 모이어티는 펩티도미메틱 단위체를 포함할 수 있다.
일 양태에서, 링커 시약 또는 링커-항생제 중간체는 항체 상에 존재하는 친핵성 시스테인과 반응성인 친전자성 그룹을 갖는 반응성 부위를 갖는다. 항체의 시스테인 티올은 링커 시약 또는 링커-항생제 상의 친전자성 그룹과 반응성이고, 공유 부착을 형성한다. 유용한 친전자성 그룹은, 이로써 제한되는 것은 아니지만, 말레이미드 및 할로아세트아미드 그룹을 포함한다.
시스테인 가공된 항체는 문헌(page 766 of Klussman, et al (2004), Bioconjugate Chemistry 15(4):765-773)의 콘주게이션에 따라 및 실시예 18의 프로토콜에 따라, 링커 시약 또는 링커-항생제 중간체와, 친전자성 관능기 (예: 말레이미드 또는 α-할로 카르보닐)와 반응한다.
또 다른 구현예에서, 링커 시약 또는 링커-항생제 중간체의 반응성 그룹은 항체의 유리 시스테인 티올과 결합을 형성할 수 있는 티올-반응성 관능기를 함유한다. 티올-반응 관능기의 예는, 이로써 제한되는 것은 아니지만, 말레이미드, α-할로아세틸, 활성화된 에스테르, 예를 들어, 석신이미드 에스테르, 4-니트로페닐 에스테르, 펜타플루오로페닐 에스테르, 테트라플루오로페닐 에스테르, 무수물, 산 클로라이드, 술포닐 클로라이드, 이소시아네이트 및 이소티오시아네이트를 포함한다.
다른 구현예에서, 링커 시약 또는 항생제-링커 중간체는 항체 상에 존재하는 친전자성 그룹과 반응성인 친핵성 그룹을 갖는 반응성 관능기를 갖는다. 항체 상의 유용한 친전자성 그룹은, 이로써 제한되는 것은 아니지만, 피리딜 이황화, 알데히드 및 케톤 카르보닐 기를 포함한다. 링커 시약 또는 항생제-링커 중간체의 친핵성 그룹의 헤테로 원자는 항체 상의 친전자성 그룹과 반응하여, 항체 단위체에 공유 부착을 형성할 수 있다. 링커 시약 또는 항생제-링커 중간체 상에서 유용한 친핵성 기는, 비제한적으로, 하이드라자이드, 옥심, 아미노, 티올, 하이드라진, 티오세미카바존, 하이드라진 카복실레이트, 및 아릴하이드라자이드를 포함한다. 항체 상의 친전자성 그룹은 링커 시약 또는 항생제-링커 중간체에 대한 결합을 위해 용이한 부위를 제공한다.
PML 모이어티는 하나 이상의 링커 성분을 포함할 수 있다. 예시적 링커 성분은 하기를 포함한다: 단일 아미노산 예컨대 시트룰린 (“cit”), 6-말레이미도카프로일(“MC”), 말레이미도프로파노일 (“MP”), 및 p-아미노벤질옥시카르보닐 (“PAB”), N-석신이미딜-4-(2-피리딜티오) 펜타노에이트 (“SPP”), 및 4-(N-말레이미도메틸) 사이클로헥산-1 카복실레이트 (“MCC”). 다양한 링커 성분은 당해 기술에 공지되어 있고, 이의 일부는 아래에 기재되어 있다.
또 다른 구현예에서, 링커는 용해도 또는 반응성을 조절한 그룹에 의해 치환될 수 있다. 예를 들어, 하전된 치환체, 예를 들어, 술포네이트 (-SO3 -) 또는 암모늄은 시약의 수용해도를 증가시키고, AAC를 제조하는데 이용되는 합성 경로에 따라, 항체 또는 항생제 모이어티와 링커 시약의 커플링 반응을 용이하게 하거나, Ab-L (항체-링커 중간체)과 abx, 또는 abx-L (항생제-링커 중간체)와 Ab의 커플링 반응을 용이하게 할 수 있다.
본 발명의 화합물 AAC는 비제제한적으로 하기 링커 시약과 함께 제조된 것들을 명시적으로 고려한다: BMPEO, BMPS, EMCS, GMBS, HBVS, LC SMCC, MBS, MPBH, SBAP, SIA, SIAB, SMCC, SMPB, SMPH, 술포-EMCS, 술포-GMBS, 술포-KMUS, 술포-MBS, 술포-SIAB, 술포-SMCC, 술포-SMPB, SVSB (석신이미딜-(4-비닐술폰)벤조에이트), 및 비스-말레이미드 시약 예컨대 DTME, BMB, BMDB, BMH, BMOE, BM(PEG)2, 및 BM(PEG)3. 비스-말레이미드 시약은 순차적 또는 수렴적 방식으로 티올-함유 항생제 모이어티, 표지 또는 링커 중간체에 대한 시스테인 가공된 항체의 티올 그룹의 결합을 허용한다. 시스테인 가공된 항체, 항생제 모이어티, 또는 링커-항생제 중간체의 티올 그룹과 반응성인, 말레이미드 이외에 다른 관능기는 요오도아세트아미드, 브로모아세트아미드, 비닐 피리딘, 이황화, 피리딜 이황화, 이소시아네이트 및 이소티오시아네이트를 포함한다.
유용한 링커 시약은 또한 다른 상용 공급처, 예를 들어, [Molecular Biosciences Inc.(Boulder, CO)]로부터 입수하거나, 또는 문헌[Toki et al (2002) J. Org. Chem. 67:1866-1872; Dubowchik, et al. (1997) Tetrahedron Letters, 38:5257-60; Walker, M.A. (1995) J. Org. Chem. 60:5352-5355; Frisch et al (1996) Bioconjugate Chem. 7:180-186; US 6214345; WO 02/088172; US 2003130189; US2003096743; WO 03/026577; WO 03/043583; 및 WO 04/032828]에 기술된 절차에 따라 합성될 수 있다.
또 다른 구현예에서, AAC의 PML 모이어티는 항체에 분지화, 다관능성 링커-모이어티를 통해 1개 초과의 항생제 모이어티를 공유 부착시키기 위한 수지상 유형 링터를 포함한다 (Sun et al (2002) Bioorganic & Medicinal Chemistry Letters 12:2213-2215; Sun et al (2003) Bioorganic & Medicinal Chemistry 11:1761-1768). 수지상 링커는 항체에 대한 항생제의 몰 비, 즉 AAC의 효능에 관련된 부하를 증가시킬 수 있다. 이에 따라, 시스테인 가공된 항체가 단지 1개의 반응성 시스테인 티올 그룹을 함유하는 경우, 항생제 모이어티의 배수가 수지상 링커를 통해 결합될 수 있다.
화학식 I AAC의 특정 구현예에서, 프로테아제-절단가능한, 비-펩티드 링커 PML은 하기 화학식을 갖는다:
여기서 Str은 확대기 단위체이고; PM은 펩티드도미메틱 단위체이고, 그리고 Y는 스페이서 단위체이며;
abx는 리파마이신-유형 항생제이고; 그리고
p는 정수 1 내지 8이다.
일 구현예에서, 연신부 단위체 "Str”은 하기 화학식을 갖는다:
여기서 R6 은 하기로 이루어진 군으로부터 선택되며: C1-C12알킬렌, C1-C12 알킬렌 C(=O), C1-C12 알킬렌 NH, (CH2CH2O)r, (CH2CH2O)r-C(=O), (CH2CH2O)r-CH2, 및 C1-C12 -NHC(=O)CH2CH(티오펜-3-일), 여기서 r은 1 내지 10 범위의 정수이다.
예시적 연신부 단위체는 아래 보여진다 (여기에서 물결선은 항체에 공유 부착의 부위를 나타낸다):
일 구현예에서, PM 은 하기 식을 갖는다:
식 중, R7 및 R8 은 함께 C3-C7 사이클로알킬 환을 형성하고, 그리고
AA는 하기로부터 선택된 아미노산 측쇄이다: H, CH3, CH2(C6H5), CH2CH2CH2CH2NH2, CH2CH2CH2NHC(NH)NH2, CHCH(CH3)CH3, 및 CH2CH2CH2NHC(O)NH2.
일 구현예에서, 스페이서 단위체 Y는 파라-아미노벤질 (PAB) 또는 파라-아미노벤질옥시카르보닐 (PABC)을 포함한다.
스페이서 단위체는, 개별 가수분해 단계 없이 항생제 모이어티의 방출을 허용한다. 스페이서 단위체는 "자기-희생성" 또는 "비-자기-희생성"일 수 있다. 특정 구현예에서, 링커의 스페이서 단위체는 p-아미노벤질 단위체 (PAB)를 포함한다. 일 상기 구현예에서, p-아미노벤질 알코올은 하기에 부착된다: 아미노산 단위체 (아미드 결합을 통해), 카바메이트, 메틸카바메이트, 또는 p-아미노벤질 기 및 항생제 모이어티 사이의 카르보네이트 (Hamann et al. (2005) Expert Opin. Ther. Patents (2005) 15:1087-1103). 일 구현예에서, 스페이서 단위체는 p-아미노벤질옥시카르보닐 (PAB)이다.
일 구현예에서, 항생제는 하기를 포함한다: 4차 아민, 예컨대 디메틸아미노피페리딜 기 (비-펩티드 링커의 PAB 스페이서 단위체에 부착될 경우). 상기 4차 아민의 예시는 링커 항생제 중간체 (PLA)이다 (표 2 중 PLA 1 내지 4). 4차 아민 기는 AAC의 항박테리아 효과를 최적화하기 위하여 항생제 모이어티의 절단을 조절할 수 있다. 또 다른 구현예에서, 항생제는 AAC 중 카바메이트 작용기를 형성하는, 비-펩티드 링커의 PABC 스페이서 단위체에 연결된다. 상기 카바메이트 작용기는 AAC의 항박테리아 효과를 최적화할 수 있다. PABC 카바메이트 링커-항생제 중간체 (PLA)의 예시는 표 2 중 PLA-5 및 PLA-6이다.
자기-희생 스페이서의 다른 예는, 이로써 제한되는 것은 아니지만, PAB 그룹과 친전자적으로 유사한 방향족 화합물, 예를 들어, 2-아미노이미다졸-5-메탄올 유도체 (US 7375078; Hay et al. (1999) Bioorg. Med. Chem. Lett. 9:2237) 및 오르토- 또는 파라-아미노벤질아세탈을 포함한다. 아미드 결합 가수분해시 폐환되는 스페이서, 예를 들어, 치환 및 비치환 4-아미노부티르산 아미드 (Rodrigues et al (1995) Chemistry Biology 2:223), 적절히 치환된 비사이클로[2.2.1] 및 비사이클로[2.2.2] 환 시스템 (Storm et al (1972) J. Amer. Chem. Soc. 94:5815) 및 2-아미노페닐프로피온산 아미드 (Amsberry, et al (1990) J. Org . Chem. 55:5867)가 사용될 수 있다. 글리신에서 치환된 아민-함유 약물의 제거 (Kingsbury et al (1984) J. Med . Chem. 27:1447)가 또한 AAC에 유용한 자기-희생 스페이서의 예이다.
AAC의 절단으로부터 방출된 활성 항생제의 양은 카스파제 방출 검정에 의하여 측정될 수 있다.
AAC에 유용한 링커-항생제 중간체
화학식 II 및 표 2의 PML 링커-항생제 중간체 (PLA)는, 리파마이신-유형 항생제 모이어티를 링커 시약 (실시예 7-17)과 결합시킴으로써 제조하였다. 링커 시약은 하기에 개시된 것들에 의하여 제조하였다: WO 2012/113847; US 7659241; US 7498298; US 20090111756; US 2009/0018086; US 6214345; Dubowchik et al (2002) Bioconjugate Chem. 13(4):855-869
표 2
PML 링커 항생제 중간체
항체-항생제
콘주게이트의
구현예
시스테인 가공, rF1 항체는 유리 시스테인 티올 기를 통하여, 프로테아제-절단가능한, 비 펩티드 링커를 통하여, pipBOR 등으로 지칭되는 리파마이신 유도체에 연결되어 표 3에서의 항체-항생제 콘주게이트 화합물 (AAC)를 형성하였다. 링커는 카텝신 B, D 등을 포함하는 리소좀 프로테아제에 의하여 절단되도록 설계되며, 항생제 및 PML 링커 등으로 구성된 링커-항생제 중간체의 생성은 실시예 7-17에 자세히 기술된다. 링커는, PAB 모이어티에서의 아미드 결합의 절단이 활성 상태에서의 항생제로부터 항체를 분리하도록 설계된다.
"디메틸pipBOR”로 불리우는 AAC는, 링커 상에 옥시카르보닐 기 및 항생제 상에 디메틸화된 아미노 기를 제외하고, "pipBOR” AAC와 동일하다.
도 3은 항체-항생제 콘주게이트 (AAC)에 대한 약물 활성화의 가능한 기전을 도시한다. 활성 항생제 (Ab)는 포유동물 세포 내로의 AAC의 내재화 후에만 방출된다. AAC 중 항체의 Fab 부분은 S. 아우레우스와 결합하는 반면, AAC의 Fc 부분은 호중구 및 대식세포를 포함하는 식세포로의 Fc-수용체 매개된 결합에 의한, 박테리아의 흡수를 증진시킨다. 포식용해소체로의 내재화 후, 링커는 리소좀 프로테아제에 의하여 절단되어 포식용해소체 내로 활성 항생제를 방출한다.
본 발명의 일 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식 I을 포함한다:
여기서:
상기 단속선은 임의의 결합을 나타내고;
R은 H, C1-C12 알킬, 또는 C(O)CH3 이고;
R1 는 OH이며;
R2는 CH=N-(헤테로사이클릴)이고, 여기서 상기 헤테로사이클릴은 C(O)CH3, C1-C12 알킬, C1-C12 헤테로아릴, C2-C20 헤테로사이클릴, C6-C20 아릴, 및 C3-C12 카르보사이클릴로부터 독립적으로 선택된 1종 이상의 기로 임의로 치환되고;
또는 R1 및 R2 는 5- 또는 6-원 융합된 헤테로아릴 또는 헤테로사이클릴을 형성하고, 그리고 임의로 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환을 형성하고, 여기서 상기 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환은 H, F, Cl, Br, I, C1-C12 알킬, 또는 OH로 임의로 치환되고;
PML은 R2 또는 R1 및 R2에 의해 형성된 융합된 헤테로아릴 또는 헤테로사이클릴에 부착된 프로테아제-절단가능한 비-펩티드 링커이고;
Ab는 rF1 항체이고; 그리고
p는 정수 1 내지 8이다.
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
여기서,
R3 는 H 및 C1-C12 알킬로부터 독립적으로 선택되고;
n은 1 또는 2이며;
R4 는 H, F, Cl, Br, I, C1-C12 알킬 및 OH로부터 선택되고; 그리고
Z는 NH, N(C1-C12 알킬), O 및 S로부터 선택된다.
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
여기서,
R5 는 H 및 C1-C12 알킬로부터 선택되고; 그리고
n은 0 또는 1이다.
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
여기서,
R5 는 H 및 C1-C12 알킬로부터 선택되고; 그리고
n은 0 또는 1이다.
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
여기서,
R5 는 H 및 C1-C12 알킬로부터 독립적으로 선택되고; 그리고
n은 0 또는 1이다.
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
여기서,
R3 는 H 및 C1-C12 알킬로부터 독립적으로 선택되고; 그리고
n은 1 또는 2이다.
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
및
본 발명의 또 다른 구현예의 항체-항생제 콘주게이트 (AAC) 화합물은 하기 화학식을 포함한다:
및
AAC의 항생제 부하
항생제 부하는 p, 화학식 I의 분자 내 항체 당 항생제 (abx) 모이어티의 평균 수로 표시된다. 항생제 부하는 항체 당 1 내지 20개의 항생제 모이어티 (D) 범위일 수 있다. 화학식 I의 AAC는 하기를 포함한다: 1 내지 20개 범위의 항생제 모이어티와 콘주게이트된 항체의 집합체 또는 풀. 콘주게이션 반응으로부터의 AAC의 제조에서 항체 당 항생제 모이어티의 평균 개수는 질량 분광분석법, ELISA 분석 및 HPLC과 같은 통상의 수단에 의해 특성화될 수 있다. 또한 p의 관점에서 AAC의 정량 분포가 측정될 수 있다. 일부 예에서, p가 다른 항생제 부하의 AAC로부터의 특정 값인 경우, 동종 AAC의 분리, 정제 및 특성화는 역상 HPLC 또는 전기영동과 같은 수단에 의해 성취될 수 있다.
일부 항체-항생제 콘주게이트에서, p는 항체 상의 부착 부위의 수에 의해 제한될 수 있다. 예를 들어, 상기 예시적 구현예에서와 같이 부착이 시스테인 티올일 경우, 항체는 단지 하나의 또는 수 개의 시스테인 티올 기를 가질 수 있고, 링커가 부착될 수 있는 하나의 또는 수 개의 충분한 반응성의 티올 기를 가질 수 있다. 특정 구현예에서, 고 항생제 부하, 예를 들어 p >5는 특정 항체-항생제 콘주게이트의 세포 투과성의 손실, 응집, 불용성 또는 독성을 야기할 수 있다. 특정 구현예에서, 본 발명의 AAC에 대한 항생제 부하는 하기를 범위로 한다: 1 내지 약 8; 약 2 내지 약 6; 약 2 내지 약 4; 또는 약 3 내지 약 5; 약 4; 또는 약 2.
특정 구현예에서, 이론적 최대치 보다 적은 수의 항생제 모이어티가 콘주게이션 반응 동안 항체에 콘주게이트된다. 항체는, 예를 들어 항생제-링커 중간체 또는 링커 시약과 반응하지 않는 리신 잔기를 함유할 수 있다. 일반적으로, 항체는 항생제 모이어티에 연결될 수 있는 다수의 유리 및 반응성 시스테인 티올을 함유하지 않으며; 정말로, 항체 내 모스트 시스테인 티올 잔기는 이황화 가교로서 존재한다. 특정 구현예에서, 항체는, 반응성 시스테인 티올 기를 생성하기 위하여 부분적 또는 전체적 환원 조건하에서 환원제 예컨대 디티오트레이톨 (DTT) 또는 트리카르보닐에틸포스핀 (TCEP)으로 환원될 수 있다. 특정 구현예에서, 항체는 반응성 친핵성 기 예컨대 리신 또는 시스테인을 노출시키는 변성 조건으로 처리된다.
AAC의 부하 (항생제/항체 비율, "AAR”)는 하기의 방법을 포함하는 다수의 상이한 방법으로 조절될 수 있다: (i) 항체와 관련된 링커 시약 또는 몰 과량의 항생제-링커 중간체의 제한, (ii) 콘주게이션 반응 시간 또는 온도의 제한, 및 (iii) 시스테인 티올 변형을 위한 환원 조건의 부분적 또는 제한. 본원 및 도면에 지칭되는 경우, “DAR”는 “AAR”과 상동한 것을 의미할 것이다.
1개 초과의 친핵성 그룹이 항생제-링커 중간체 또는 링커 시약 이후 항생제 모이어티 시약과 반응하는 경우, 생성된 생성물은 항체에 결합된 하나 이상의 항생제 모이어티의 분포를 갖는 AAC 화합물의 혼합물임을 이해해야 한다. 항체 당 항생제의 평균 수는 항체에 대해 특이적이고 항생제에 대해 특이적인, 이중 ELISA 항체 검정에 의하여 혼합물로부터 산출될 수 있다. 개개 AAC 분자는 질량 분석법에 의해 혼합물에서 확인될 수 있고, HPLC, 예를 들어, 소수성 상호작용 크로마토그래피에 의해 분리시킬 수 있다 (참조예: McDonagh et al (2006) Prot. Engr. Design & Selection 19(7):299-307; Hamblett et al (2004) Clin. Cancer Res. 10:7063-7070; Hamblett, K.J., et al. “Effect of drug loading on the pharmacology, pharmacokinetics, and toxicity of an anti-CD30 antibody-drug conjugate,” Abstract No. 624, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004; Alley, S.C., et al. “Controlling the location of drug attachment in antibody-drug conjugates,” Abstract No. 627, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004). 특정 구현예에서, 단일 부하값을 갖는 균질한 AAC는 전기영동 또는 크로마토그래피에 의해 콘주게이션 혼합물로부터 분리시킬 수 있다. 본 발명의 시스테인 가공 항체는, 항체 상의 반응성 부위가 가공 시스테인 티올에 주로 제한되므로, 더욱 균질한 제제를 가능하게 한다. 일 구현예에서, 항체 당 항생제 모이어티의 평균 수는 약 1 내지 약 20의 범위이다. 일부 구현예에서, 1 내지 4의 범위가 선택 및 조절된다.
항체-항생제 콘주게이트의 제조 방법
화학식 I의 AAC는, 당업자에 공지된 유기 화학 반응, 조건 및 시약을 사용하여, 하기를 포함하는 다양한 경로에 의해 제조될 수 있다: (1) 공유 부착을 통하여 Ab-L을 형성하기 위하여, 2가 링커 시약과 항체의 친핵성 기와의 반응, 이후 항생제 모이어티 (abx)와의 반응; 및 (2) 공유 부착을 통하여 L-abx을 형성하기 위하여, 2가 링커 시약과 항생제 모이어티의 친핵성 기와의 반응, 이후 항체와의 반응. 후자의 경로를 통한 화학식 I의 AAC를 제조하기 위한 예시적 방법은 US 7498298에 기술되며, 이는 본원에서 참고로 명확히 편입된다.
항체 상의 친핵성 기는 비제한적으로 하기를 포함한다: (i) N-말단 아민 기, (ii) 측쇄 아민 기, 예컨대 리신, (iii) 측쇄 티올 기, 예컨대 시스테인, 및 (iv) 당 하이드록실 또는 아미노 기 (여기서 항체는 글리코실화됨). 아민, 티올, 및 하이드록실 기는 친핵성이며, 본 발명의 경우와 같은 링커 모이어티 상의 친전자성 그룹들과의 공유 부착을 형성하도록 반응할 수 있고, 링커 시약은 하기를 포함한다: (i) 활성 에스테르 예컨대 NHS 에스테르, HOBt 에스테르, 할로포르메이트, 및 산성 할라이드; (ii) 알킬 및 벤질 할라이드 예컨대 할로아세트아미드; 및 (iii) 알데하이드, 케톤, 카복실, 및 말레이미드 기. 특정의 항체는 환원가능한 쇄간 이황화, 즉 시스테인 가교를 갖는다. 항체는 DTT (디티오트레이톨) 또는 트리카르보닐에틸포스핀 (TCEP)과 같은 환원제를 이용한 처리에 의한 링커 시약과의 콘주게이션을 위해 반응하여 상기 항체가 완전히 또는 부분적으로 환원될 수 있도록 제조될 수 있다. 각각의 시스테인 가교는 따라서 이론적으로 2 개의 반응성 티올 친핵체를 형성할 것이다. 추가의 친핵성 기는, 리신 잔기의 변형, 예컨대, 아민을 티올로 전환시키는, 2-이미노티올란 (트라우트 (Traut) 시약)과 리신 잔기의 반응에 의하여 항체 내에 도입될 수 있다. 반응성 티올 기는 1, 2, 3, 4, 또는 그 이상의 시스테인 잔기를 도입 (예를 들어, 하나 이상의 비-천연 시스테인 아미노산 잔기를 포함하는 변이체 항체를 제조)함으로써, 항체로 도입될 수 있다.
본 발명의 항체-항생제 콘주게이트는 또한 항체 상에서 친전자성 기, 예컨대 알데하이드 또는 케톤 카르보닐 기와 링커 시약 또는 항생제 상에서 친핵성 기 사이의 반응에 의해 생산될 수 있다. 링커 시약 상에서 유용한 친핵성 기는, 비제한적으로, 하이드라자이드, 옥심, 아미노, 하이드라진, 티오세미카바존, 하이드라진 카복실레이트, 및 아릴하이드라자이드를 포함한다. 한 구현예에서, 항체는 링커 시약 또는 항생제 상에서 친핵성 치환체와 반응할 수 있는 친전자성 모이어티를 도입하기 위해 변형된다. 또 다른 구현예에서, 글리코실화된 항체의 당류는, 링커 시약 또는 항생제 모이어티의 아민 기와 반응할 수 있는 알데하이드 또는 케톤 기를 형성하기 위해, 예를 들면 퍼아이오데이트 산화 시약으로 산화될 수 있다. 수득한 이민 쉬프(Schiff) 염기 기는 안정한 연결을 형성할 수 있거나, 또는, 예를 들면 안정한 아민 연결기를 형성하기 위해 보로하이드라이드 시약에 의해 감소될 수 있다. 한 구현예에서, 갈락토오스 옥시다아제 또는 나트륨 메타-퍼아이오데이트와 글리코실화된 항체의 탄수화물 부분의 반응은 항생제 상에서 적절한 기와 반응할 수 있는 항체에서 카르보닐 (알데하이드 및 케톤) 기를 수득할 수 있다 (Hermanson, Bioconjugate Techniques). 또 다른 구현예에서, N-말단 세린 또는 트레오닌 잔기를 함유한 항체는 나트륨 메타-퍼아이오데이트와 반응할 수 있어서, 제1 아미노산 대신 알데하이드의 생산을 초래한다 (Geoghegan & Stroh, (1992) Bioconjugate Chem. 3:138-146, 5362852)에서 찾을 수 있다. 그와 같은 알데하이드는 항생제 모이어티 또는 링커 친핵체와 반응될 수 있다.
항생제 모이어티 상의 친핵성 그룹은, 이로써 제한되는 것은 아니지만, 하기를 포함하는, 링커 모이어티 및 링커 시약 상의 친전자성 그룹과 공유 부착을 형성하기 위해 반응할 수 있는 아민, 티올, 하이드록실, 하이드라지드, 옥심, 하이드라진, 티오세미카바존, 하이드라진 카복실레이트, 및 아릴하이드라지드 그룹을 포함한다: (i) 활성 에스테르 예컨대 NHS 에스테르, HOBt 에스테르, 할로포르메이트, 및 산성 할라이드; (ii) 알킬 및 벤질 할라이드 예컨대 할로아세트아미드; 및 (iii) 알데하이드, 케톤, 카복실, 및 말레이미드 기.
표 3에서의 항체-항생제 콘주게이트 (AAC)를 표 2의 상기 기술된 rF1 항체 및 링커 항생제 중간체의 콘주게이션에 의하여, 그리고 실시예 18에서 기술된 방법에 따라 제조하였다. AAC를 시험관내 대식세포 검정 (실시예 19) 및 생체내 마우스 신장 모델 (실시예 20)에 의한 효능에 대해 시험하였다.
표 3
rF1 항체-PML-항생제 콘주게이트 (AAC)
* AAR = 항생제/항체 비율 평균
야생형 ("WT"), 시스테인 가공된 돌연변이체 항체 ("티오"), 경쇄 ("LC"), 중쇄 ("HC"), 6-말레이미도카프로일 ("MC"), 말레이미도프로파노일 ("MP"), 사이클로부틸디케토 ("CBDK"), 시트룰린 (“cit”), 시스테인 (“cys”), p-아미노벤질 ("PAB"), 및 p-아미노벤질옥시카르보닐 ("PABC")
항체-항생제 콘주게이트로 감염을 치료 및 예방하는 방법
본 발명의 rF1-AAC는 인간 및 수의과의 스타필로코시, 예를 들어 S. 아우레우스, S. 사프로피티커스 및 S. 시무란스에 대해 효력이 있는 항미생물제로서 유용하다. 특정 양태에서, 본 발명의 AAC는 S. 아우레우스 감염을 치료하는데 유용하다.
혈류로의 진입 후, S. 아우레우스는 거의 모든 임의의 장기에서 전이성 감염을 야기할 수 있다. 2차 감염은 요법의 개시 전 약 1/3의 경우에서 발생하며 (Fowler et al., (2003) Arch. Intern. Med. 163:2066-2072), 요법 개시 후에도 10%의 환자에서 발생한다 (Khatib et al., (2006) Scand. J. Infect. Dis., 38:7-14). 감염의 특징은 고름의 큰 저장소, 조직 붕괴, 및 농양(abcesses)의 형성이다 (이들 모두는 많은 양의 호중구를 함유함). 약 40%의 환자에서, 균혈증이 3일 초과로 지속될 경우 합병증이 발병한다.
AAC 작용의 제안된 기전은 상기에 기술된다 (하위표제 항체-항생제 콘주게이트 하에서). 본 발명의 rF1 항체-항생제 콘주게이트 (AAC)는, 세포내 병원체를 치료하기 위하여, 유의미한 치료적 이점을 갖는다. AAC 링커는, 포식용해소체 효소에 대한 노출에 의하여 절단되어 활성 항생제를 방출한다. 국한된 공간 및 상대적으로 높은 국소적 항생제 농도 (박테리아 당 약 104 )로 인하여, 결과는 포식용해소체가 더이상 세포내 병원체의 생존을 지지하지 않는다는 것이었다. AAC가 본질적으로 비활성 전구약물이므로, 항생제의 치료 지수는 유리 (비콘주게이트된) 형태에 대하여 신장될 수 있다. 항체가 병원체 특이적 표적을 제공하는 한편, 절단가능 링커는 병원체의 세포내 위치에 특이적인 조건 하에서 절단된다. 상기 효과는 직접적으로 옵소닌화된 병원체 상에, 뿐만 아니라 포식용해소체 내 공동-국지화된 기타 병원체 상에, 둘 모두에 작용할 수 있다. 항생제 내성은, 항생제 및 기타 항미생물제에 의한 사멸을 거부한 질환-야기 병원체의 능력이며, 이는 다중약물 내성으로부터 기계론적으로 동떨어져 있다 (Lewis K (2007). "존속성균 세포, 동면 및 감염성 질환” Nature Reviews Microbiology 5 (1): 48-56. doi: 10.1038/nrmicro1557. 오히려, 이러한 내성 형태는 존속성균으로 불리우는 미생물 세포의 소 아-집단에 의하여 야기된다 (Bigger JW (14 October 1944). "Treatment of staphylococcal infections with penicillin by intermittent sterilization". Lancet 244 (6320): 497-500). 이러한 세포는 전통적인 의미에서 다중약물 내성이 아니며, 오히려 그들의 유전적으로 동일한 형제균을 사멸할 수 있는 항생제 치료에 내성인 동면 세포이다. 이러한 항생제 내성은 비- 또는 극도로 느린 분할적 생리학적 상태에 의하여 야기된다. 항미생물 치료가 이러한 존속성균 세포를 근절하는데 실패할 경우, 이들은 재발성 만성 감염을 위한 저장소가 된다. 본 발명의 항체-항생제 콘주게이트는 이러한 존속성균 세포를 사멸하는 고유한 특성을 가지고, 다중약물 내성 박테리아 집단의 발생을 억제한다.
또 다른 구현예에서, 본 발명의 rF1-AAC는, 병원체가 생존하는 세포내 구획과 관계 없이, 감염을 치료하기 위하여 사용된다.
또 다른 구현예에서, 본 발명의 rF1-AAC는 또한 부유생물 또는 생물막 형태 내 스타필로코시 박테리아를 표적화하는데 사용된다. 본 발명의 항체-항생제 콘주게이트 (AAC)로 치료가능한 박테리아 감염은 하기를 포함한다: 박테리아 폐 감염, 예컨대 S. 아우레우스 폐렴, 골수염, 재발성 비부비동염, 박테리아 심내막염, 박테리아 눈 감염, 예컨대 트라코마 및 결막염, 심장, 뇌 또는 피부 감염, 위장관 감염, 예컨대 여행자 설사증(travellers' diarrhea), 궤양성 대장염, 과민성 장 증후군 (IBS), 크론병, 및 IBD (염증 장 질환), 일반적으로, 박테리아 뇌수막염, 및 임의의 장기 예컨대 근육, 간, 뇌척수막, 또는 폐 내 농양. 박테리아 감염은, 몸체 예컨대 뇨관, 혈류, 손상부위, 또는 카테터 삽입 부위의 기타 부위에 존재할 수 있다. 본 발명의 AAC는 생물막, 임플란트 또는 보호성 부위 (예컨대, 골수염 및 보철성(prosthetic) 관절 감염)를 포함하는 난치성 감염, 및 높은 사망률 감염 예컨대 병원-획득성 폐렴 및 균혈증에 유용하다. 스타필로코쿠스 아우레우스 감염을 예방하기 위하여 치료될 수 있는 취약 환자군은 하기를 포함한다: 혈액투석 환자, 면역-무력화된 환자, 중증 치료 센터 내 환자, 및 특정 수술 환자. 또 다른 양태에서, 본 발명은 물, 바람직하게는 포유동물, 및 가장 바람직하게는 인간에서 미생물 감염을 사멸, 치료, 또는 예방하는 방법을 제공하며, 이는 상기 동물에게 본 발명의 AAC의 rF1 AAC 또는 약제학적 제형을 투여하는 단계를 포함한다. 본 발명은 추가로, 상기 미생물 감염으로부터 우연히 초래되거나, 또는 이와 연관된 질환을 치료 또는 예방하는 특징을 포함한다. 상기 치료 또는 예방 방법은, 본 발명의 조성물의 경구, 국소, 정맥내, 근육내, 또는 피하 투여를 포함할 수 있다. 예를 들어, IV 카테터의 수술 또는 삽입, ICU 케어에서, 이식 약제에서, 암-이후 화학요법, 또는 감염의 높은 위험도를 갖는 기타 활동 전에, 본 발명의 AAC는 감염의 개시 또는 확산을 예방하기 위하여 투여될 수 있다.
박테리아 감염은 활성 및 비활성 형태를 갖는 박테리아에 의하여 야기될 수 있으며, AAC는 박테리아 감염의 잠재 형태, 활성형 및 비활성형 둘 모두를 치료하기에 충분한 기간동안, 또른 이러한 양으로 투여되며, 이때 상기 기간은 박테리아 감염의 활성 형태를 치료하는데 필요한 기간보다 길다.
본 발명의 양태는 본 발명의 rF1 AAC의 치료적 유효량을 투여함으로써 S. 아우레우스 및/또는 리스테리아 모노사이토게네스에 감염된 환자를 치료하는 방법이다. 본 발명은 또한, 병원 환경, 예컨대 수술, 화상 환자, 장기이식 환자에서 본 발명의 rF1-AAC의 치료적 유효량을 투여함으로써 S. 아우레우스 또는 S. 에피더미디스, 또는 S. 사프로피티커스 또는 S. 시무란스 중 하나 이상에 의한 감염을 예방하는 방법을 고려한다.
본 분야의 숙련가에 의하여 측정 시, 박테리아 감염에 대한 치료가 필요한 환자는 그들이 감염되었던 박테리아의 종류로 진단될 필요는없다. 박테리아 감염을 갖는 환자는 수 시간 만에 매우 급속도로 악화될 수 있는 가능성이 있으므로, 병원의 허가 하에 환자는 본 발명의 rF1-AAC를 하나 이상의 표준 케어 Abx 예컨대 반코마이신 또는 시프로플록사신과 함께 투여받을 수 있다. 진단성 결과가 수득가능하고, 예컨대 감염 내 S. 아우레우스의 존재를 표지할 경우, 환자는 rF1 AAC로의 치료를 계속할 수 있다. 그러므로, 박테리아 감염 또는 구체적으로 S. 아우레우스 감염을 치료하는 방법의 일 구현예에서, 환자는 치료적 유효량의 rF1 AAC를 투여받는다. 본 발명의 치료 또는 예방 방법에서, 본 발명의 AAC는 단독 치료제 또는 기타 제제 예컨대 하기 기술된 것들과 결합하여 투여될 수 있다. 본 발명의 AAC는 사전-임상 모델 내 MRSA의 치료에서의 반코마이신보다 더 양호한 우수성을 나타낸다. SOC에 대한 AAC의 비교는, 예를 들어, 사망률의 감소에 의하여 측정될 수 있다. 치료될 환자는, 다양한 측정가능한 인자에 의한 AAC 치료에 대한 반응성에 대해 평가될 것이다. 이들 환자에서의 개선도를 평가하기 위하여 임상의가 이용할 수 있는 표지 및 증상의 예시는 하기를 포함한다: 백혈구 계수의 정상화 (진단 시 상승된 경우), 체온의 정상화 (진단 시 (열이) 상승된 경우), 혈액 배양물의 청소율, 보다 적은 홍반 및 고름의 배수를 포함하는, 상처부위의 가시적 개선, 벤틸레이터 치료를 받는 환자의 벤틸레이션 속도 감소 또는 보다 적은 양의 산소를 요구하는 것과 같은 벤틸레이터 필요의 감소, 벤틸레이터를 완전히 사용하지 않음 (진단 시 환자가 벤틸레이터 치료를 받고 있었을 경우), 안정한 혈압을 지지하는 약제의 보다 적은 사용 (이들 약제가 진단시 요구되었을 경우), 상승된 크레아티닌 또는 간 작용 시험과 같은 말기-장기 부전을 암시하는 실험실 비정상상태의 정상화 (그들이 진단시 비정상으로 진단되었을 경우), 및 방사선학적 이미지화의 개선 (예컨대 호전을 나타내는 사전의 암시된 폐렴의 흉선 x-선). ICU 내 환자에서, 이러한 인자는 적어도 매일 측정될 수 있다. 열은 하기와 함께 긴밀하게 모니터링된다: 무수 호중구 계수를 포함하는 백혈구 뿐만 아니라 “왼쪽 이동” (활성 감염에 반응하여 증가된 호중구 생산을 표지하는 아세포의 외관)이 호전되었다는 증거.
본 발명의 치료 방법의 맥락에서, 박테리아 감염을 갖는 환자는, 진단 시점에서 또는 치료 개시에서, 또는 그 전의 값, 표지, 또는 증상과 비교하여 선행 인자 중 적어도 2개 이상에서, 본 분야의 숙련의에 의하여 측정시 유의미하게 측정가능할 경우, 치료되었다고 고려된다. 일부 구현예에서, 상기 지칭된 인자 중 3, 4, 5, 6개 이상에서의 측정 가능한 개선점이 있다. 일부 구현예에서, 상기 측정 인자에서의 개선도는 치료 전의 값과 비교하여, 적어도 50%, 60%, 70%, 80%, 90%, 95% 또는 100% 만큼의 것이다. 전형적으로, 환자는, 상기 환자의 측정가능한 개선도가 하기를 포함할 경우, 박테리아 감염 (예컨대, S. 아우레우스 감염)이 완전히 치료되었다고 고려될 것이다: i) 본래 식별되었던 박테리아가 성장하지 않는 반복 혈액 또는 조직 배양물 (전형적으로 일부); ii) 열의 정상화; iii) WBC의 정상화; 및 iv) 말기-장기 부전(폐, 간, 신장, 혈관 붕괴)이 상기 환자가 가졌던 기존의 공동-병적상태에 근거하여 완전하게 또는 부분적으로 호전됨.
투약. 임의의 전술한 양태에서, 감염 환자의 치료에 있어서, AAC의 투여량은 보통 약 0.001 내지 1000 mg kg 일이다. 일 구현예에서, 박테리아 감염을 갖는 환자는 하기 범위의 AAC 용량에서 치료된다: 약 1 mg kg 내지 약 150mg kg, 전형적으로 약 5mg kg 내지 약 150mg kg, 더욱 특이적으로, 25mg kg 내지 125 mg kg, 50mg kg 내지 125mg kg, 더 더욱 특이적으로 약 50mg kg 내지 100mg kg. AAC는 매일 (예컨대, 단일 용량으로 5 내지 50 mg kg/일) 또는 보다 덜 빈번하게 (예컨대, 단일 용량으로 5, 10, 25 또는 50 mg kg/주)로 투여될 수 있다. 1회 용량은, 예를 들어, 1일에 25mg/kg, 그리고 그 다음 일에 25mg/kg로 2일에 걸쳐 분할될 수 있다. 환자는 매 3일에 1회 (q3D), 격주 마다 주 1회 용량으로 (qOW), 1-8주의 기간 동안 투여받을 수 있다. 일 구현예에서, 환자는 박테리아 감염 예컨대 Staph A 감염을 치료하기 위하여, 표준 케어 (SOC)와 함께 2-6주 동안 주 1회로 IV를 통하여 본 발명의 AAC를 투여받을 수 있다. 치료 길이는 환자의 병태 또는 감염의 정도에 따라, 예를 들어, 무-합병증 균형증에 대해 2주의 기간, 또는 심내막염을 갖는 균혈증에 대해 6주의 기간이 지시될 것이다.
일 구현예에서, AAC는 1 내지 7 연속 일 동안 2.5 내지 100 mg kg의 초기 용량에서 투여되고, 이후 1개월 동안 매 1 내지 7일간 1회로 0.005 내지 10 mg/kg의 유지 용량으로 투여된다.
투여 경로. 박테리아 감염을 치료하기 위하여, 본 발명의 AAC는 임의의 선행 투여량에서 정맥내 (i.v.) 또는 피하 투여될 수 있다. 일 구현예에서, rF1-AAC는 정맥내로 투여된다. 특정 구현예에서, rF1 AAC는 i.v.를 통하여 투여되며, 여기서 rF1 항체는 SDR 및 rF1Ab 및 표 4A 및 4B에 개시된 바와 같은 아미노산 서열을 갖는 Ab의 군으로부터 선택되는 것이다.
병용 요법. AAC는, 환자를 치료하는 의료진에 의하여 측정하는데 적절한 하나 이상의 추가, 예컨대 제2의, 치료적 또는 방지적 제제와 결합하여 투여될 수 있다.
일 구현예에서, 본 발명의 항체-항생제 콘주게이트 화합물과 조합하여 투여된 제2 항생제는 구조적 부류: (i) 아미노글리코시드; (ii) 베타-락탐; (iii) 매크롤라이드/환계 펩티드; (iv) 테트라사이클린; (v) 플루오로퀴놀린/플루오로퀴놀론; (vi) 및 옥사졸리디논으로부터 선택된다. 참조: Shaw, K. and Barbachyn, M. (2011) Ann. N.Y. Acad. Sci. 1241:48-70; Sutcliffe, J. (2011) Ann. N.Y. Acad. Sci. 1241:122-152.
일 구현예에서, 본 발명의 항체-항생제 콘주게이트 화합물과 조합하여 투여된 제2 항생제는 클린다마이신, 노보바이오신, 레타파물린, 다프토마이신, GSK-2140944, CG-400549, 시타플록사신, 테이코플라닌, 트리클로산, 나프티리돈, 라데졸리드, 독소루비신, 암피실린, 반코마이신, 이미페넴, 도리페넴, 젬시타빈, 달바반신, 및 아지트로마이신으로부터 선택된다.
이러한 추가 치료 또는 방지적 제제의 추가 예시는 하기이다: 항 염증 제제 (예컨대, 비-스테로이드 항 염증 약물 (NSAID; 예컨대, 데토프로펜, 디클로페낙, 디플루니살, 에토돌락, 페노프로펜, 플루르비프로펜, 이부프로펜, 인도메타신, 케토프로펜, 메클로펜아메에이트, 메펜아남 산, 멜록시캄, 나부메온, 나프록센 나트륨, 옥사프로진, 피록시캄, 술린닥, 톨메틴, 세레콕시브, 로페콕시브, 아스피린, 콜린 살리실레이트, 살살테, 및 나트륨 및 마그네슘 살리실레이트) 및 스테로이드 (예컨대, 코르티손, 덱사메타손, 하이드로코르티손, 메틸프레드니솔론, 프레드니솔론, 프레드니손, 트리암시놀론)), 항바이러스 제제 (예컨대, 아지트로마이신, 클라리트로마이신, 에리트로마이신, 가티플록사신, 레보플록사신, 아목시실린, 메트로니다졸, 페니실린 G, 페니실린 V, 메티실린, 옥사실린, 클로사실린, 디클로사실린, 나프실린, 암피실린, 카르베니실린, 티카르실린, 메즐로실린, 피페라실린, 아즐로실린, 테모실린, 세파로틴, 세파피린, 세프라딘, 세파로리딘, 세파졸린, 세파만돌, 세푸록심, 세파렉신, 세프프로질, 세파클로르, 로라카르베프, 세포시틴, 세프마토졸, 세포탁심, 세프티족심, 세프트리아손, 세포페라존, 세프트아지딤, 세픽심, 세프포독심, 세프티부텐, 세프디니르, 세프피롬, 세프에핌, BAL5788, BAL9141, 이미페넴, 에르페넴, 메로페넴, 아스트레오남 산, 클라불라네이트, 술박탐, 타조박탐, 스트렙토마이신, 네오마이신, 카나마이신, 파로마이신, 젠타마이신, 토브라마이신, 아미카신, 네틸마이신, 스펙티노마이신, 시소마이신, 디베칼린, 이세파마이신, 테트라사이클린, 클로르테트라사이클린, 데메클로사이클린, 미노사이클린, 옥시테트라사이클린, 메타사이클린, 독시사이클린, 테리트로마이신, ABT-773, 린코마이신, 클린다마이신, 반코마이신, 오리타밴신, 달바밴신, 테이코플라닌, 퀴누프리스틴 및 달포프리스틴, 술파닐아마이드, 파라-아미노벤조 산, 술파디아진, 술피속사졸, 술파메톡사졸, 술파타리딘, 린에졸리드, 날리딕스 산, 옥소린 산, 노르플록사신, 퍼플록사신, 에녹사신, 오플록사신, 시프로플록사신, 테마플록사신, 로메플록사신, 플레록사신, 그레파플록사신, 스파르플록사신, 트로바플록사신, 클린아플록사신, 목시플록사신, 제미플록사신, 시타플록사신, 답토마이신, 가레녹사신, 라모플라닌, 파로페넴, 폴리믹신, 티제사이클린, AZD2563, 또는 트리메토프림), ACC 표적 Ag 유래의 상동하거나 상이한 항원에 대한 항체를 포함하는 항바이러스성 항체, 혈소판 응집 억제제 (예컨대, 아브시시맙, 아스피린, 실로스타졸, 클로피도그렐, 디피리다몰, 에프티피바티드, 티클로피딘, 또는 티로피반), 항응고제 (예컨대, 달테파린, 다나파로이드, 에녹사파린, 헤파린, 틴자파린, 또는 와파린), 해열제 (예컨대, 아세트아미노펜), 또는 지질 저하 제제 (예컨대, 콜레스티라민, 콜레스티폴, 니코틴 산, 젬피브로질, 프로부콜, 에티미브, 또는 스타틴 예컨대 아토르바스타틴, 로수바스타틴, 로바스타틴 심바스타틴, 프라바스타틴, 세리바스타틴, 및 플루바스타틴). 일 구현예에서, 본 발명의 AAC는 S. 아우레우스 (메티실린 내성 및 메티실린 민감성 균주 포함)에 대한 표준 케어 (SOC)와 조합하여 투여된다. MSSA는 보통 전형적으로 나프실린 또는 옥사실린으로 치료되고, MRSA는 반코마이신 또는 세파졸린으로 치료된다.
이러한 추가 제제는, AAC 투여의 14 일내, 7 일내, 1 일내, 12 시간 내, 또는 1 시간내로, 또는 이와 동시에 투여된다. 추가 치료제는, AAC와 상동 또는 상이한 약제학적 조성물 내 존재할 수 있다. 상이한 약제학적 조성물이 존재할 경우, 투여의 상이한 경로가 사용될 수 있다. 예를 들어, AAC는 정맥내 또는 피하로 투여될 수 있으며, 한편 제2 제제는 경구로 투여될 수 있다.
약제학적 제형
본 발명은 또한, rF1-AAC를 함유하는 약제학적 조성물 및 AAC를 함유하는 약제학적 조성물을 사용하는 박테리아 감염을 치료하는 방법을 제공한다. 상기 조성물은 추가로 하기를 포함할 수 있다: 부형제, 예컨대 약제학적으로 허용가능한 부형제 (담체) (완충제 포함), 산, 염기, 당, 희석제, 활윤제, 보존제 등 (이는 본 분야에 잘 알려져 있고 본원에 기술됨). 본 발명의 방법 및 조성물은, 감염성 질환을 치료하기 위하여, 단독으로, 또는 기타 전통적 방법 및/또는 제제와 조합하여 사용될 수 있다. 일부 구현예에서, 약제학적 제형은 1) 본 발명의 rF1-AAC 및 2) 약제학적으로 허용가능한 담체를 포함한다. 일부 구현예에서, 약제학적 제형은 1) 본 발명의 AAC, 및 임의로, 2) 적어도 하나 추가 치료제를 포함한다.
본 발명의 AAC의 약제학적 제형은 상기 항체 또는 목적하는 정도의 순도를 갖는 AAC를 임의의 생리학적으로 허용되는 담체, 부형제 또는 안정화제와 혼합함으로써 저장용으로 제조된다 (Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)) (수성 용액 또는 동결건조 또는 기타 건조 제형의 형태로). 허용 가능한 담체, 부형제, 또는 안정제는 이용된 투여량 및 농도에서 수령체에 비독성이며, 버퍼, 예컨대 포스페이트, 시트레이트, 및 다른 유기산; 아스코르브산 및 메티오닌을 포함하는 항산화제; 보존제(예컨대 옥타데실디메틸벤질 암모늄 클로라이드; 헥사메토늄 클로라이드; 벤즈알코늄 클로라이드, 벤즈에토늄 클로라이드; 페놀, 부틸 또는 벤질 알코올; 알킬 파라벤, 예컨대 메틸 또는 프로필 파라벤; 카테콜; 레조르시놀; 주기로헥산올; 3-펜탄올; 및 m-크레졸); 저분자량(약 10 잔기 미만) 폴리펩티드; 단백질, 예컨대 혈청 알부민, 젤라틴, 또는 면역글로불린; 친수성 폴리머, 예컨대 폴리비닐피롤리돈; 아미노산, 예컨대 글리신, 글루타민, 아스파라긴, 히스티딘, 아르기닌, 또는 라이신; 모노사카라이드, 디사카라이드, 및 글루코스, 만노스, 또는 덱스트린을 포함하는 다른 탄수화물; 킬레이트제, 예컨대 EDTA; 당류, 예컨대 수크로스, 만니톨, 트레할로스 또는 소르비톨; 염 형성 짝이온, 예컨대 나트륨; 금속 착물(예를 들면, Zn-단백질 복합체); 및/또는 비-이온성 계면활성제, 예컨대 TWEEN™, PLURONICS™, 또는 폴리에틸렌 글리콜(PEG)이 포함된다. 생체내 투여용으로 사용될 약제학적 제형은 일반적으로 무균성이며, 무균 여과 막을 통하여 여과에 의해 용이하게 달성된다.
활성 성분은 또한 콜로이드성 약물 전달 시스템 (예: 리포좀, 알부민 마이크로구, 마이크로에멀젼, 나노-입자 및 나노캡슐)으로 또는 마크로에멀젼으로, 예를 들어, 코아세르베이션(coacervation) 기술에 의해 또는 계면 중합에 의해 제조된 마이크로캡슐에, 예를 들어, 각각 하이드록시셀룰로즈 또는 젤라틴-마이크로캡슐 및 폴리(메틸메타크릴레이트) 마이크로캡슐에 포함시킬 수 있다. 상기 기술은 하기에서 개시되어 있다: Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980).
지속-방출 제제는 제조될 수 있다. 지속-방출 제제의 적합한 예는, 매트릭스가 형상화된 물품, 예를 들면 필름, 또는 마이크로캡슐의 형태인, 항체 또는 본 발명의 AAC를 함유하는 고체 소수성 폴리머의 반투과성 매트릭스를 포함한다. 지속-방출 매트릭스의 예는 하기를 포함한다: 폴리에스테르, 하이드로겔 (예를 들면, 폴리(2-하이드록시에틸-메타크릴레이트), 또는 폴리(비닐알코올)), 폴리락타이드 (미국 특허 번호 3,773,919), L-글루탐산과 γ 에틸-L-글루타메이트와의 코폴리머, 비-분해성 에틸렌-비닐 아세테이트, 분해성 락트산-글리콜산 코폴리머 예컨대 LUPRON DEPOT™ (락트산-글리콜산 코폴리머 및 류프롤라이드 아세테이트로 구성된 주사가능 마이크로구형체), 및 폴리-D-(-)-3-하이드록시부티르산. 폴리머 예컨대 에틸렌-비닐 아세테이트 및 락트산-글리콜산은 분자 100 일에 걸쳐 분자의 방출을 가능하게 하지만, 특정 하이드로겔은 단기간 동안 단백질을 방출한다. 캡슐화된 항체 또는 AAC가 장시간 신체 내에 남아 있을 때, 37 °C에서 수분에 노출되면 변성되거나 응집되어, 생물학적 활성이 상실되고 면역원성이 변경될 수 있다. 합리적인 전략은 관여된 기전에 따라 안정화를 위해 고안될 수 있다. 예를 들면, 응집 기전이 티오-이황화 상호교환을 통한 분자간 S-S 결합 형성인 것으로 밝혀지면, 안정화는 설프하이드릴 잔기를 변형시키고, 산성 용액으로부터 동결건조시키고, 수분 함량을 조절하고, 적절한 첨가제를 사용하고, 특정 폴리머 기질 조성물을 개발함으로써 달성될 수 있다.
AAC는, 표적 세포/조직으로의 전달을 위하여, 임의의 적합한 형태로 제형화될 수 있다. 예를 들어, AAC는 포유동물로의 약물의 전달에 유용한 다양한 유형의 지질, 인지질 및/또는 계면활성제로 구성된, 소포체, 리포좀으로서 제형화될 수 있다. 리포좀의 성분은 통상적으로, 2중층 형태로 배열되며, 이는 생물학적 막의 지질 배열과 유사하다. 항체를 함유하는 리포좀은 당해분야에서 공지된 방법에 의하여 제조되며, 이는 예컨대 하기에 기술된다: Epstein et al., (1985) Proc. Natl. Acad. Sci. USA 82:3688; Hwang et al., (1980) Proc. Natl Acad. Sci. USA 77:4030; US 4485045; US 4544545; WO 97/38731; US 5013556.
증대된 순환 시간을 갖는 리포좀은 미국 특허 번호 5,013,556에서 개시되어 있다. 특히 유용한 리포좀은 포스파티딜콜린, 콜레스테롤 및 PEG-유도된 포스파티딜에탄올아민 (PEG-PE)을 포함하는 지질 조성물을 이용한 역상 증발 방법에 의해 발생될 수 있다. 리포좀은 정의된 기공 크기의 필터를 통해 압출되어 원하는 직경을 갖는 리포좀을 생산한다.
물질 및 방법
균주 및 배양:
모든 실험은 달리 명시되지 않는 한 NARSA(http://www.narsa.net/control/member/repositories)로부터 수득된 MRSA-USA300 NRS384로 수행되었다.
박테리아는 18시간 동안 37℃에서 5% 양 혈액 (TSA 플레이트)로 보강된 트립신 소이 한천 플레이트 상에서 성장되었다. 액체 배양에 대해, TSA 플레이트로부터 단일 콜로니가 트립신 소이 액체배지 (TSB)에 접종되고 그리고 18시간 동안 200rpm에서 진탕하면서 37℃에서 배양된다; 신선한 TSB에 이들 배양물의 100배 희석이 다양한 시간 동안 더 계대배양되었다.
세포외
박테리아에 대한
MIC
측정
세포외 박테리아에 대한 MIC는 트립신 소이 액체배지에 항생제의 일련의 2-배 희석을 준비함으로써 측정되었다. 항생제의 희석은 96 웰 배양 접시에서 4번 반복하여 만들어 졌다. MRSA (USA300의 NRS384 균주)를 기하급수적으로 성장하는 배양물로부터 취하여지고 그리고 1x104 CFU/mL로 희석되었다. 박테리아는 항생제의 존재에서 37℃에서 진탕하면서 18-24시간 동안 배양되고 그리고 박테리아 성장은 630nM에서 광학 밀도 (OD)를 판독함에 의해 측정되었다. MIC는 박테리아 성장을 >90%로 억제한 항생제의 용량으로 측정되었다.
세포내
박테리아에 대한
MIC
측정
세포내 MIC는 마우스 복막 대식세포 내에서 격리된 박테리아에서 측정되었다 (뮤린 복막 대식세포의 생성에 대해서는 하기 참고). 대식세포는 24 웰 배양 접시에 4x105 세포/mL의 밀도로 도말되고, 그리고 대식세포 당 10-20 박테리아의 비로 MRSA에 감염되었다. 대식세포 배양은 세포외 박테리아의 성장을 억제하기 위해 50ug/mL의 겐타마이신 (세포외 박테리아에서만 활성인 항생제)로 보강된 성장 배지에서 유지되었고 그리고 시험 항생제가 감염 후 1일째 성장 배지에 부가되었다. 세포내 박테리아의 생존은 항생제의 부가 24시간 후 평가되었다. 대식세포는 .1% 소 혈청 알부민 및 .1% 트리톤-X로 보강된 행크스 완충된 염수 용액으로 용해되고, 그리고 용해물의 연속 희석이 .05% 트윈-20을 함유하는 포스페이트 완충된 염수 용액에서 만들어졌다. 생존한 세포내 박테리아의 수는 5% 섬유소가 제거된 양 혈액을 갖는 트립신 소이 우무 평판에 도말함에 의해 측정되었다.
박테리아 세포 벽 조제 (
CWP
),
면역블롯팅
, 및
ELISA
CWP는 30% 라피노오스, 100g/ml의 라이소스파핀 (메사추세츠 주 캔턴 소재의 셀 사이언스), 및 EDTA-유리 프로테아제 억제제 칵테일 (캘리포니아 주 플레전턴 소재의 로슈)로 보강된 10mM 트리스-HCl (pH 7.4)의 mL 당 40mg의 펠렛화된 S. 아우레우스 또는 S. 에피더미디스를, 37℃에서 30분 동안 배양함에 의해 생성되었다. 용해물은 11,600 x g에서 5분 동안 원심분리되었고, 그리고 세포벽 성분를 함유하는 상청액이 수집되었다. 면역침강을 위해, CWP는 1g/mL의 지시된 1차 항체를 함유하는 NP-40 완충액 (120mM NaCl, 50mM 트리스-HCl pH 8.0, 1% NP-40, 완벽한 프로테아제 억제제 칵테일 (Roche) 및 2mM 디티오트레이톨)에서 4배 희석되고, 그리고 4℃에서 2시간 동안 배양되고, 그 다음 단백질 A/G 아가로스 (매사추세츠 주 월샘 소재의 써모)로 1h 배양되었다. 전체의 세포 용해물 (WCL)은 20mM 트리스-HCl (pH 7.4), 150mM NaCl, 100g/ml의 라이소스파핀, 1% 트리톤-X100 (써모) 및 EDTA-유리 프로테아제 억제제 칵테일에서 37℃에서 배양함에 의해 생성되었다. 면역블랏 분석을 위해, 단백질은 4-12% 트리스-글리신 겔 상에서 분리되고 그리고 니트로셀룰로오스 막 (캘리포니아 주 칼즈배드 소재의 인비트로젠)으로 이동되고, 그 다음 지시된 1차 항체 (1g/mL)로 블롯팅되었다. 사용된 항체는 표 1에 열거되었다. 렉틴 연구는 0.1mM CaCl2 및 0.01 mM MnCl2로 보강된 콘카나발린 A (ConA)- 또는 sWGA-아가로스 비드 (캘리포니아 주 벌링게임 소재의 벡터 랩스)로 여과된(0.2 micron) 밤새 배양 상청액을 면역침전시킴으로써 수행되었다.
ELISA 실험은 표준 프로토콜을 사용하여 수행되었다. 간단히, CWP로 사전-도포된 플레이트가 인간 IgG 제제, 즉 정제된 인간 IgG (시그마), 정맥내 면역글로불린 감마가드 액체 (캘리포니아 주 웨스트레이크 빌리지 소재의 박스터), 건강한 공여체 또는 MRSA 환자로부터 풀링된 혈청 (양자는 집-안에서 생성됨)과 반응되었다. 정제된 IgG 또는 혈청 내 존재하는 항-스타필로코시 IgG의 농도는 펩티도글리칸에 대한 mAb 28.9.9의 공지된 농도로 생성된 보정 곡선을 사용함에 의해 계산되었다.
인간
호중구
및 배양 세포로부터 인간
호중구
프로테아제 또는 리소좀 추출물로 박테리아의 치료
리소좀 추출물은 리소좀 풍부 키트 (써모)를 사용하여 인간 호중구, THP-1 세포, 및 RAW 세포로부터 단리되었다. 총 5x107 세포가 리소좀 내 300 내지 500 마이크로그램의 총 단백질을 얻기 위해 사용되었다. 프로테아제 억제제는 모든 단계로부터 생략되어 리소좀 내 프로테아제 활성을 유지한다. 세포의 혈장은 다운스 균질기 (뉴저지 주 밀빌 소재의 휘톤)를 사용하여 30 스트로크에 의해 교란되었다. 균질물은 5분 동안 500 x g에서 원심분리되어, 아이오딕사놀의 8%, 20%, 23%, 27% 및 30% (최상부부터 최하부까지)의 구배의 최상부 상에 로딩되는 후핵 상청액을 얻었다. 4℃에서 2시간 동안 145,000 x g에서 초원심분리 후, 8%와 20% 아이오딕사놀 사이에 층상으로 된 리소좀을 수득했다. 이 리소좀 분획은 PBS로 희석되고 그리고 4℃에서 30분 동안 18,000 x g에서 원심분리에 의해 펠렛화되었다. 상기 리소좀 펠렛은 PBS로 세정되고 그리고 트리스-완충된 염수를 갖는 2% CHAPS에 용해되어 리소좀 추출물을 얻었다.
숙주 프로테아제에 의한 SDR 단백질의 절단을 분석하기 위해, S. 아우레우스 박테리아가 150mM NaCl 및 2mM CaCl2를 갖는 50mM Tris (pH 8.0) 내 50nM의 정제된 인간 호중구 세린 프로테아제 또는 0.1mg/ml의 호중구 리소좀 추출물로; 또는 100mM NaCl 및 2mM DTT (pH 5.5)를 갖는 50mM Na 시트레이트 내 0.1mg/ml의 RAW 또는 THP-1 리소좀 추출물로 처리되었다. 카텝신 G 억제제 (메사츄세츠 주 빌레리카 소재의 칼바이오켐)가 100g/ml로 부가되었다. 이들 혼합물은 정제된 프로테아제를 사용할 때 30분 동안 또는 리소좀 용해물을 사용할 때 1시간 동안 37℃에서 배양되고 그리고 펠렛 박테리아로 원심분리되었다. 상청액은 절단 생성물을 검출하기 위한 면역블롯팅에 의해 분석되었다. 일부 실험에서, 세포벽 조제는 잔여 박테리아 펠렛으로부터 수득되었고 그리고 또한 면역블롯팅에 의해 분석되었다.
실시예
실시예 1 세포내 MRSA는 종래의 항생제로부터 보호되었다
포유동물 세포는 항생제 요법의 존재에서 S. 아우레우스에 대한 보호성 틈새를 제공한다는 가설을 확인하기 위해, 세포외 플랑크톤 박테리아 대 뮤린 대식세포 내에서 격리된 박테리아에 대한 침습성 MRSA 감염에 대한 표준 요법 (SOC)으로 현재 사용되는 3가지 주요 항생제 (반코마이신, 다프토마이신 및 리네졸라이드)의 효능이 비교되었다 (표 1).
세포외 박테리아에 대해, MRSA는 트립신 소이 액체배지에서 밤새 배양되었고, 그리고 MIC는 성장을 방지한 최소 항생제 용량인 것으로 측정되었다. 세포내 박테리아에 대해, 뮤린 복막 대식세포는 MRSA로 감염되고 그리고 세포외 박테리아를 사멸하기 위해 겐타마이신의 존재에서 배양되었다. 시험 항생제는 감염 1일 후 배양 배지에 부가되고 그리고 생존한 세포내 박테리아의 총 수가 24시간 후에 측정되었다. 임상적으로 관련된 항생제에 대해 예상된 혈청 농도는 항미생물제, Andre Bryskier. ASM 프레스, 워싱톤 DC (2005)에 보고되었다.
표 1: 액체 배양 내에서 성장된 세포외 박테리아 대 뮤린 대식세포 내에서 격리된 세포내 박테리아에 대한 몇 개의 항생제에 대한 최소 저해된 농도 (MIC).
매우 독성이 강한 공동체-획득된 MRSA 균주 USA300을 사용한 이 분석은 비록 세포외 MRSA가 액체 배양에서 저농도의 반코마이신, 다프토마이신, 및 리네졸라이드에 의한 성장 저해에 고감수성이지만, 세 가지 항생제 모두는 임상적으로 달성할 수 있는 농도의 항생제에 노출된 대식세포 내에서 격리된 MRSA의 동일한 균주를 죽이는데 실패하였다는 것을 밝혔다. 세포내 병원체를 박멸하는데 상대적으로 유효한 것으로 생각되는 리팜피신 조차도 (Vandenbroek, P.V. (1989) Antimicrobial Drugs, Microorganisms, and Phagocytes. Reviews of Infectious Diseases 11, 213-245), 대다수의 현존하는 항생제가 시험관내 및 생체내 양자에서 세포내 S. 아우레우스를 사멸하는데 비효율적인 것을 보여주는 다른 연구 (Sandberg, A., Hessler, J.H., Skov, R.L., Blom, J. & Frimodt-Moller, N. (2009) "Intracellular activity of antibiotics against Staphylococcus aureus in a mouse peritonitis model" Antimicrob Agents Chemother 53, 1874-1883)와 일치되어, 플랑크톤 박테리아의 성장을 억제하기 위해 요구된 용량 (MIC)에 비교하여 세포내 MRSA를 박멸하는데 6,000-배 높은 용량을 요구했다 (표 1).
실시예 2 세포내 MRSA로 감염의 전파
이들 실험은 유리-생존하는 플랑크톤 박테리아의 동등 용량 대 세포내 박테리아의 발병력을 비교하였고 그리고 세포내 박테리아가 생체 내 반코마이신 존재에서 감염을 일으킬 수 있는지를 측정했다. 네 집단의 마우스가 액체배지 배양물로부터 직접적으로 취해진 S. 아우레우스 실행가능한 유리 박테리아 (2.9 x 106) 또는 공여체 마우스의 복막 감염에 의해 생성된 호중구 숙주 대식세포 내에서 격리된 세포내 박테리아 (1.8 x 106)의 거의 동등 용량으로 정맥내 주사에 의해 감염되었고 (도 1a) 그리고 선택된 그룹은 감염 직후 그리고 그런 다음 1회/1일 반코마이신으로 처리되었다. 마우스는 마우스23 내에서 S. 아우레우스가 일관되게 대량서식되는 장기인, 신장 내 박테리아 군집화의 감염 4일 조사되었다. 세 개의 독립적인 실험에서, 동등 용량의 플랑크톤 박테리아로 감염된 것에 비교될 때 세포내 박테리아로 감염된 마우스의 신장에서 동등한 또는 보다 높은 박테리아 부하가 관측되었다 (도 1b). 놀랍게도, 세포내 박테리아로의 감염은 이 모델에서 플랑크톤 박테리아로 감염에 따라 효율적으로 대량서식하지 않는 장기인, 뇌의 보다 일치된 군집화를 초래한 것이 발견되었다 (도 1c). 더욱이, 플랑크톤 박테리아가 아닌 세포내 박테리아가 이 모델에서 반코마이신 요법에도 불구하고 감염을 확립할 수 있었다 (도 1b, 도1c)
시험관내 추가의 분석은 세포내 생존이 항생제 회피를 용이하게 하는 정도를 보다 정량적으로 다룬다. 이를 위해, MG63 골아세포가 반코마이신의 존재에서 플랑크톤 MRSA 또는 세포내 MRSA의 어느 하나로 감염되었다.
골아세포 또는 HBMEC 의 감염. MG63 세포주가 ATCC (CRL-1427)로부터 수득되고 그리고 10mM Hepes 및 10% 소태아 혈청 (RPMI-10)으로 보강된 RPMI 1640 조직 배양 배지에 유지된다. HBMEC 세포 (카탈로그 #1000) 및 ECM 배지 (카탈로그# 1001)은 사이언스셀 리서치 랩스 (캘리포니아 주 칼즈배드)로부터 수득되었다. 세포는 24 웰 조직 배양판에 도말되고 그리고 배양되어 융합성 층을 얻었다. 실험의 일에, 세포는 일단 RPMI (보충물 없음)에서 세정되었다. MRSA 또는 감염된 복막 세포는 완벽한 RPMI-10에서 희석되고 그리고 반코마이신이 감염 바로 전에 5ug/mL로 부가되었다. 복막 세포는 골아세포에 1x106 복막 세포/mL로 부가되었다. 세포의 샘플은 .1% 트리톤-x로 용해되어 감염 시에 살아있는 세포내 박테리아의 실제 농도를 측정했다. 모든 감염에 대한 실제 역가는 5% 섬유소가 제거된 양 혈액을 갖는 트립신 소이 한천 상에 박테리아의 연속 희석을 도말함에 의해 측정되었다.
MRSA (유리 박테리아)는 배지, 배지 + 반코마이신, 또는 배지 + 반코마이신 및 MG63 골아세포 (도 1e) 또는 인간 뇌 미세혈관 내피 세포 (HBMEC, 도 1f)의 단일층 상에 플레이팅된 것에 씨딩된다. 단일층과 박테리아의 접촉을 증진하기 위해 플레이트는 원심분리되었다. 각 시점에서, 배양 상청액이 수집되어 세포외 박테리아를 회수하거나 또는 부착 세포가 용해되어 세포내 박테리아를 방출한다.
반코마이신 단독에 노출된 플랑크톤 박테리아는 효율적으로 사멸되었다. 배양액에서 1일 후 생존한 박테리아는 회수되지 않았다 (도 1d). 유사한 수의 플랑크톤 박테리아가 MG63 골아세포 상에 도말될 때, 골아세포의 침습에 의한 반코마이신으로부터 보호되어 진, 감염 1일 후 MG63 세포와 연계된 작은 수의 생존한 박테리아 (대략 유입의 0.06%)가 회수되었다.
복막 세포 내에서 격리된 MRSA는 반코마이신의 존재에서 감염의 효율 및 생존 양자에서 극적인 증가를 보였다. 백혈구 내 약 15%의 세포내 MRSA는 반코마이신이 플랑크톤 박테리아의 배양액을 멸균하였던 동일한 조건 하에서 생존했다. 세포내 박테리아는 또한 반코마이신의 존재에서 MG63 골아세포의 단일층을 보다 잘 감염할 수 있어, 반코마이신에 노출 1일 후 회수된 박테리아의 배가를 초래했다 (도 1d). 또한, 세포내 S. 아우레우스는 유리 살아있는 박테리아를 죽이는 반코마이신의 농도에 일정한 노출 하에서 MG63 세포 (도 1e), 원발성 인간 뇌 내피 세포 (도 1f), 및 A549 장기지 상피 세포 (도시되지 않음)에서 24시간 기간에 걸쳐 거의 10-배 증가할 수 있다. 비록 항생제 사멸로부터 보호되었지만, 감염된 복막 대식세포와 호중구 배양에서 박테리아 성장은 일어나지 않았다 (도시되지 않음). 이와 함께 이들 데이터는 골수 세포에서 MRSA의 세포내 저장기가 활성 항생제 치료의 존재에서조차도 신규 부위에 대한 감염의 전파를 촉진할 수 있고 그리고 일정한 항생제 요법의 조건 하에서도 내피 및 상피 세포에서 세포내 성장이 일어날 수 있음을 뒷받침한다.
실시예 3 항-SDR 및 다른 항체의 생성
mAb rF1의 생성을 위해, CD19+CD3-CD27+IgD-IgA- 기억 B 세포가 FACSAria 세포 정렬기 (캘리포니아 주 산호세 소재의 BD)를 사용하여 MRSA-감염된 공여체의 말초 혈액으로부터 단리되었다. B-세포 림프종 (Bcl)-xL 및 Bcl-6 유전자로 바이러스 형질도입 전에, 기억 세포는 Kwakkenbos MJ, 등 (2010) Nat Med 16: 123-128에 이미 기재된 바와 같이 인터류킨-21의 존재에서 CD40L-발현 마우스 L 섬유아세포에서 활성화되었다. 형질도입된 B 세포는 동일한 배양 시스템에 유지되었다. 공여체 혈액의 사용은 장기의 위원회에 의해 승인되었다. 단클론성 항체 (mAb) rF1은 ELISA에 의해 MSSA 균주 뉴먼의 용해물과의 반응성에 의해 배양 상청액으로부터 선택되었다; 양성 웰들은 서브 클로닝되고 ELISA에 의해 2회 재-시험되었다. 재조합 rF1은 293T 세포 (ATCC) 안으로 형질감염 및 pcDNA3.1 (인비트로젠)을 사용하여 인간 IgG1 카파 불변 영역으로 중쇄 및 경쇄 가변 영역을 클로닝함에 의해 생성되었다. 정제된 IgG는 단백질 A-커플링된 세파로오스® (인비트로젠)을 사용하여 배양 상청액으로부터 수득되었다. mAb rF1 및 그것의 변이체의 생성은 본 명세서에 전체적으로 참고로 편입된, US 8,617,556 (Beaumont 등) 및 Hazenbos 등 (2103) PLOS Pathogens 9(10): 1-18에 기재된다.
인간 IgG1 mAbs SD2, SD3 및 SD4 (모두 글리코실화된 SDR 단백질에 대한 것) 및 4675 (인간 IgG1 항-ClfA)는 항체 중쇄 및 경쇄의 동원 쌍형성을 보존하는 Symplex™ 기술을 사용하여 S. 아우레우스 감염 후 환자로부터 말초 B 세포로부터 클로닝되었다 [34]. 혈장 및 기억 B-세포 양자는 재조합 전장 IgG 레퍼토리 (제조에 있어 원본)에 대한 유전적 공급원으로 사용되었다. 개별적인 항체 클론은 포유류 세포의 형질감염에 의해 발현되었다 [35]. 전장 IgG1 항체를 함유하는 상청액은 7일 후에 수거되었고 ELISA에 의한 항원 결합을 스크리닝하기 위해 사용되었다. 항체 4675, SD2, SD3 및 SD4는 USA300 또는 뉴먼 S. 아우레우스 균주로부터 세포벽 제제에 대한 결합에 대해 양성이었다. 항체는 그 뒤에 200-ml 일시적 형질감염에서 생산되고 그리고 추가 시험을 위해 단백질 A 크로마토그래피 (뉴저지 주 피스카타웨이 소재의 GE 라이프 사이언스의 MabSelect SuRe)로 정제되었다. 이들 항체의 단리 및 사용은 지역 윤리 검토위원회에 의해 승인되었다. rF1 변이체가 생성되었다.
ClfA (9E10), ClfB, (10D2), SdrD (17H4), IsdA (2D3) 및 비-변형된 SDR 단백질 (9G4)에 대한 마우스 mAb가 표준 프로토콜을 사용하여 E. 콜리에서 발현 후 정제되어 진, 각각의 재조합 단백질로 마우스를 면역화함에 의해 생성되었고; 하이브리도마 상청액은 단백질 A 친화도 크로마토그래피로 정제되었다. 래빗 mAb 28.9.9는 펩티도글리칸 (PGN)-유도된 펩티드 CKKGGG-(L-Ala)-(D-감마-Glu)-(L-Lys)-(D-Ala)-D-Ala)로 래빗를 면역화하고 그 다음 IgG를 클로닝하여 생성되었다.
실시예 4 MRSA 감염된 공여체로부터 단리된 고도로 옵소닌 단클론성 항체 (rF1)의 특성규명
MRSA-감염된 공여체의 말초 혈액에서 기억 B 세포로부터 몇 개의 S. 아우레우스-반응성 단클론성 항체 (mAb)가 상기에서 기재된 바와 같이 단리되었다. 이들 항체들을 특성규명할 때, 하나의 IgG1 mAb (이후에 rF1로 칭함)가 인간 다형핵 백혈구 (PMN)에 의해 강력한 옵소닌식세포 사멸 (OPK)을 유도한 S. 아우레우스 균주 패널에 대한 광범위한 반응성으로 확인되었다.
임상 MRSA 균주 USA300로부터의 박테리아에 mAb rF1의 최대 결합은 이소형-매칭된 항-ClfA mAb의 것보다 대략 10 배 높았다 (도 5a). 증가된 결합과 일치되게, rF1로 옵소닌화는 PMN에 의한 USA300의 증가된 흡수 (도 5b) 및 사멸 (도 5c)을 초래했다. 그에 반해서, 인간 항-ClfA로 사전 옵소닌화는 박테리아 생존력에 효과가 없었다 (도 5c). rF1 항체는 PMN의 부재에서 USA300의 생존력에 영향을 미치지 않았다. 따라서, rF1은 MRSA에 결합하여 PMN에 의한 MRSA의 강력한 사멸을 유도하는 능력을 갖는 mAb이다.
실시예 5 스타필로코쿠스 균주에 rF1의 결합
배양물 또는 감염된 조직으로부터 전체의 박테리아에 결합하는 rF1의 FACS 분석
전체의 박테리아는 TSA 플레이트 또는 TSB 배양물로부터 수거되고 그리고 0.1% IgG 유리 BSA (시그마) 및 10 mM Hepes, pH 7.4 (HB 완충액)로 보강된 페놀 레드 없는 HBSS로 세정되었다 박테리아 (20x108 CFU/mL)는 비특이적 IgG 결합을 차단하기 위해 실온(RT)에서 1시간 동안 HB 완충액 내 300g/mL의 래빗 IgG (시그마)로 배양되었다. 박테리아는 rF1 또는 이소형 대조 IgG1 mAb gD:5237 (Nakamura GR, 등 (1993) J Virol 67: 6179-6191)을 포함하는 2 μg/mL의 1차 항체로, 그리고 그 다음 형광성 항-인간 IgG 2차 항체 (펜실바니아 주 웨스트 글로브 소재의 잭슨 이뮤노리서치)로 염색되었다. 박테리아는 세정되고 그리고 FACSCalibur® (BD)에 의해 분석되었다.
감염된 마우스 조직으로부터 박테리아의 항체 염색을 위해, 6-8 주령 암컷 C57Bl/6 마우스 (매사추세츠 주 윌밍턴 소재의 찰스 리버)는 PBS 내 108 CFU의 로그상으로-성장된 USA300으로 정맥내로 주사되었다. 마우스 장기은 감염 2일 후 수거되었다. 래빗 감염성 심내막염 (IE)은 문헌[Tattevin P, et al. (2010) Antimicrobial agents and chemotherapy 54: 610-613]에 기재된 바와 같이 확립되었다. 래빗은 5x107 CFU의 고정-상으로 성장된 MRSA 균주 COL로 정맥내로 주사되었고 그리고 심장 병적증식물은 18시간 후에 수거되었다. 30mg/kg의 반코마이신으로의 치료가 7x107 CFU 고정-상으로 COL로 감염 18시간 후 정맥내로 b.i.d.로 주어졌다.
마우스 또는 래빗 세포를 용해하기 위해, 조직은 gentleMACS® 세포 해리기 (밀테니이)를 사용하여 M 튜브 (캘리포니아 주 오번 소재의 밀테니이)에서 균질화되고 그 다음 0.1% 트리톤-X100 (써모), 10g/mL의 DNAseI (로슈) 및 완벽한 미니 프로테아제 억제제 칵테일 (로슈)을 함유하는 PBS에서 10분 동안 RT에서 배양되었다. 현탁액은 40 마이크론 필터 (BD)를 통과되게 하고 그리고 박테리아는 상기에서 기재된 바와 같이 mAbs로 염색되었다. 박테리아는 20 μg/mL 마우스 mAb 702 항-S. 아우레우스 펩티도글리칸 (매사추세츠 주 케임브리지 소재의 에비캠) 및 형광색소-표지된 항-마우스 IgG 2차 항체 (잭슨 이뮤노리서치)로 이중 염색에 의해 마우스 장기 잔해로부터 분화되었다. 유세포측정 분석 동안, 박테리아는 이중 형광 플롯으로부터 mAb 702로 양성 염색을 위해 게이팅되었다. 모든 동물 실험은 샌 프란시스코의 캘리포니아 대학교 및 제넨텍의 장기 검토 위원회에 의해 승인되었다.
유세포측정 (FCM) 분석은 시험된 모든 15 S. 아우레우스 균주에 대한 rF1의 강력한 결합 활성을 보였다 (도 7). 이들 균주는 S. 아우레우스 계통발생을 걸쳐 광범위하게 분포되었다 [8]. 박테리아 세포 표면 항원의 발현 수준이 시험관내 및 생체내 성장 사이에서 다를 수 있으므로, 본 발명자 등은 또한 전신 감염 후 다양한 마우스 조직으로부터 단리된 USA300을 인지하는 rF1의 능력을 시험했다. rF1 mAb는 감염된 마우스 신장, 간 및 폐로부터 유도된 USA300에 강력하게 결합했다 (도 6). 마우스 신장으로부터의 USA300에 rF1가 결합하는 것은 감염 후 적어도 8일까지 지속되어 (도시되지 않음), 감염 동안 rF1 에피토프의 강력한 장기간 발현을 시사한다. 또한, rF1은 감염성 심내막염의 래빗 모델에서 심장 병적증식물로부터의 MRSA COL 박테리아에 강력하게 결합했다. 반코마이신으로의 치료는 MRSA와 rF1의 반응성에 영향을 미치지 않았다 (도 6). 따라서, rF1에 의해 기술적으로 인식된 항원은 다양한 균주에 걸쳐 보존되었고 다양한 성장 및 감염 증상에서 안정되게 발현되었다.
모든 S. 아우레우스 균주에 걸친 rF1-반응성의 도처에 존재하는 특성이 주어져, 그러한 반응성이 다른 그람-양성 박테리아로 확장되는지를 참고하기 위해 실험이 수행되었다. 현저히, rF1 결합은 단지 응고효소-음성 인간 병원체 S. 에피더미 디스에 대해서만 검출가능했다 (도표 7). rF1 mAb는 S. 사프로피티쿠스, S. 루그두 넨시스, S. 시물란스 및 S. 카르노수스, 또는 다른 그램-양성 종 예컨대 스트렙토코쿠스 파이오제네스 , 바실러스 서브틸리스, 엔테로코쿠스 파에칼리스, 및 리스테리아 모노사이토게네스를 포함하여, 시험된 임의의 다른 스타필로코시 종에 결합하지 않았다. 따라서, rF1은 인간-적응된 스타필로코시 병원체에서 안정되게-발현된 표면 항원(들)에 결합하고 그리고 인간 PMN에 의해 박테리아 사멸을 증진하는 인간 항체이다.
실시예 6 rF1 항체의 아미노산 변형
요약하면, 각각의 rF1 Abs의 VH 영역이 클로닝되어 지고 그리고 인간 H 쇄 감마1 불변 영역에 연결되고 그리고 VL은 카파 불변 영역에 연결되어 IgG1로 Abs를 발현한다. 야생형 서열은 특정 위치에서 변경되어 아래에서 기재된 바와 같이 항원 결합을 유지하면서 항체 안정성을 개선한다. 시스테인 가공된 Abs (ThioMabs, 또한 일명 THIOMAB™)가 그런 다음 생성된다.
i. 안정성
변이체
생성
rF1 Abs는 특정 특성 (탈아미드화, 아스파르트산 이성질체화, 산화 또는 N-연결된 글리코실화를 피하는 것)을 개선하기 위해 가공되고 그리고 항원 결합의 유지뿐만 아니라 아미노산 대체 후 화학 안정성에 대해 시험되었다. 제작된 아미노산 변경은 US 8,617,556에 기재된 바와 같다.
iii
.
Cys
가공된 돌연변이체 (
ThioMabs
) 생성
전장 ThioMabs은 이미 교시된 바와 같이 예정된 위치에, 예를 들면, 링커-항생제 중간체에 항체의 콘주게이션을 가능하도록 인간 감마 1 H 쇄 내 위치 A118 (Eu 조약에 따른 아미노산 위치 번호) 및 L 쇄의 카파 불변 영역 내 V205에 H 쇄 (CH1 내) 또는 L 쇄 (Cκ) 안으로 시스테인을 도입함에 의해 생산되었다. H 및 L 쇄는 그런 다음 별개의 플라스미드 안으로 클로닝되고 그리고 H 및 L 인코딩 플라스미드가 이들이 발현되고 무손상 Abs 안으로 조합되는 293 세포 안으로 공-형질감염된다. H 및 L 쇄 양자는 또한 동일한 발현 플라스미드 안으로 클로닝될 수 있다. 각각의 H 쇄 내의 것인, 2 가공된 Cys; 또는 각각의 L 쇄 내의 것인, 2 가공된 Cys; 또는 항체 사량체 당 4 가공된 Cys를 유도하는 각각의 H 및 L 쇄 내 가공된 Cys의 조합 (HC LC Cys)을 갖는 IgG1이 cys 돌연변이체 쇄 및 야생형 쇄의 원하는 조합을 발현함에 의해 생성되었다.
실시예 7 피페리딜 벤즈옥사지노 리파마이신 (pipBOR) 5
2-니트로벤젠-1,3-디올 1이 2-아미노벤젠-1,3-디올 2를 제공하기 위해 에탄올 용매 내에서 팔라듐/탄소 촉매로 수소 가스 하에서 수소화되고, 하이드로클로라이드 염으로 단리되었다. 디클로로메탄/테트라하이드로푸란 내에서 tert-부틸디메틸실릴 클로라이드 및 트리에틸아민으로 2의 단일-보호로 2-아미노-3-(tert-부틸디메틸실릴옥시)페놀 3을 얻었다. 리파마이신 S (캘리포니아 주 프리몬트 소재의 켐셔틀 인코포레이션, US 7342011; US 7271165; US 7547692)가 실온에서 톨루엔 내에서 망간 옥사이드 또는 산소 가스로 산화적 농축에 의해 3과 반응되어 TBS-보호된 벤즈옥사지노 리파마이신 4를 얻었다. LCMS (ESI): M+H+ = 915.41. 피페리딘-4-아민 및 망간 옥사이드와 4의 반응은 피페리딜 벤즈옥사지노 리파마이신 (pipBOR) 5를 제공한다. LCMS (ESI): M+H+ = 899.40
실시예 8 디메틸pipBOR 6
TBS-보호된 벤즈옥사지노 리파마이신 4와 N,N-디메틸피페리딘-4-아민의 반응은 디메틸피페리딜 벤즈옥사지노 리파마이신 (디메틸pipBOR) 6을 제공한다.
대안적으로, (5-플루오로-2-니트로-1,3-페닐렌)비스(옥시)비스(메틸렌)디벤젠 7은 테트라하이드로푸란/메탄올 용매 내에서 팔라듐/탄소 촉매로 수소 가스로 수소화되어 벤질 기를 제거하여 2-아미노-5-플루오로벤젠-1,3-디올 8을 얻었다. LCMS (ESI): M+H+ = 144.04. 상업적으로 이용가능한 리파마이신 S 또는 리파마이신 SV 나트륨 염 (캘리포니아 주 프리몬트 소재의 켐셔틀 인코포레이션)이 60℃에서 에틸 아세테이트 내 칼륨 제이철 시아나이드 또는 공기 중에서 산화적 농축에 의해 2-아미노-5-플루오로벤젠-1,3-디올 8과 반응되어 플루오로벤즈옥사지노 리파마이신 9를 얻었다. N,N-디메틸피페리딘-4-아민으로 플루오라이드의 대체로 디메틸pipBOR 6을 얻었다. LCMS (ESI): M+H+ = 927.43
실시예 9 (S)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)-N-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)사이클로부탄-1,1-디카복사마이드 10
단계 1: 1-(5-아미노펜틸)-1H-피롤-2,5-디온 하이드로클로라이드 10a의 제조
말레산 무수물, 푸란-2,5-디온 (150g, 1.53mol)이 HOAc (1000mL) 내 6-아미노헥산산 (201g, 1.53mol)의 교반된 용액에 부가되었다. 본 혼합물은 r.t.에서 2시간 동안 교반된 후, 이것은 환류에서 8시간 동안 가열된다. 유기 용매는 감압 하에서 제거되고 그리고 잔류물은 EtOAc (500mL × 3)로 추출되고, H2O로 세정된다. 조합된 유기 층들은 Na2SO4 상에서 건조되고 농축되어 조 생성물을 얻는다. 이것은 석유 에테르로 세정되어 6-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)헥산산을 백색 고형물로서 얻었다 (250g, 77.4%). DPPA (130g, 473mmol) 및 TEA (47.9g, 473mmol)가 t-BuOH (200mL) 내 6-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)헥산산 (100g, 473mmol)의 용액에 부가된다. 혼합물은 N2 하에서 8시간 동안 환류에서 가열되었다. 혼합물은 농축되고, 그리고 잔류물은 실리카 겔상 칼럼 크로마토그래피 (PE:EtOAc= 3:1)에 의해 정제되어 tert-부틸 5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸카바메이트 (13g, 10%)를 얻었다. 무수 EtOAc (30mL) 내 tert-부틸 5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸카바메이트 (28g, 992mmol)의 용액에 HCl/EtOAc (50mL)가 점적으로 부가되었다. 혼합물은 r.t.에서 5시간 동안 교반된 후, 이것은 여과되고 그리고 고형물은 건조되어 1-(5-아미노펜틸)-1H-피롤-2,5-디온 하이드로클로라이드 10a을 얻었다 (16g, 73.7%). 1H NMR (400 MHz, DMSO-d 6 ): δ 8.02 (s, 2H), 6.99 (s, 2H), 3.37-3.34 (m, 2H), 2.71-2.64 (m, 2H), 1.56-1.43 (m, 4H), 1.23-1.20 (m, 2H).
단계 2: (S)-1-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일카바모일)사이클로부탄카복실산 10b의 제조
디옥산 및 H2O (50mL/75mL)의 혼합물 내 (S)-2-아미노-5-우레이도펜탄산 10g (17.50g, 0.10mol)의 혼합물에 K2CO3 (34.55g, 0.25mol)가 부가되었다. Fmoc-Cl (30.96g, 0.12mol)기 0℃에서 서서히 부가되었다. 반응 혼합물은 2h에 걸쳐 실온으로 가온되었다. 유기 용매는 감압 하에서 제거되고, 그리고 물 슬러리는 6M HCl 용액으로 pH = 3로 조정되고 그리고 EtOAc (100mL × 3)로 추출되었다. 유기 층은 Na2SO4 상에서 건조되고, 여과되고, 그리고 감압 하에서 농축되어 (S)-2-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5-우레이도펜탄산 10f를 얻었다(38.0g, 95.6%). 10f는 상업적으로 이용가능하다.
DCM 및 MeOH (100mL/50mL)의 혼합물 내 10f (4g, 10mmol)의 용액에 (4-아미노페닐)메탄올 (1.6g, 13mmol, 1.3eq) 및 2-에톡시-1-에톡시카르보닐-1,2-디하이드로퀴놀린, EEDQ, 시그마-알드리치 CAS 등록 번호 16357-59-8 (3.2g, 13mmol, 1.3eq)가 부가되었다. 혼합물은 N2 하에서 r.t.에서 16시간 동안 교반된 후, 이것은 농축되어 갈색 고형물을 얻었다. MTBE (200 mL)이 부가되고 이것은 2시간 동안 15℃에서 교반되었다. 고형물은 여과로 수집되고, MTBE (50mL × 2)로 세정되어 (S)-(9H-플루오렌-9-일)메틸 (1-((4-(하이드록시메틸)페닐)아미노)-1-옥소-5-우레이도펜탄-2-일)카바메이트 10e를 오렌지 고형물로 얻었다 (4.2g, 84%). LCMS (ESI): m/z 503.0 [M+1].
건조 DMF (20ml) 내 10e (4.2g, 8.3mmol)의 교반된 용액에 피페리딘 (1.65mL, 17mmol, 2eq)이 r.t에서 점적으로 부가되었다. 혼합물은 30분 동안 r.t.에서 교반되고 그리고 고체 침전물이 형성되었다. 건조 DCM (50mL)이 부가되고, 그리고 혼합물은 즉시 투명하게 되었다. 혼합물은 또 다른 30 min 동안 r.t.에서 교반되고 그리고 LCMS는 10e가 소비된 것을 보였다. 이것은 감압 하에서 건조로 농축되어 (피페리딘이 잔존하지 않음을 확실하게 하고) 그리고 잔류물이 EtOAc와 H2O (50mL/20mL) 사이에서 분할되었다. 수성 상은 EtOAc (50mL × 2)로 세정되고 그리고 농축되어 (S)-2-아미노-N-(4-(하이드록시메틸)페닐)-5-우레이도펜탄아미드 10d를 유성 잔사로 얻었다 (2.2g, 94%) (소량의 DMF가 함유됨).
상업적으로 이용가능한 1,1-사이클로부탄디카복실산, 1,1-디에틸 에스테르 (CAS 등록 번호 3779-29-1)는 제한된 비누화에 의해 수성 염기로 반할산/에스테르 1,1-사이클로부탄디카복실산, 1-에틸 에스테르 (CAS Reg No. 54450-84-9)로, 그리고 커플링 시약 예컨대 TBTU (O-(벤조트리아졸-1-일)-N,N, N' , N'-테트라메틸우로늄 테트라플루오로보레이트, 또한 소위: N,N, N' , N'-테트라메틸-O-(벤조트리아졸-1-일)우로늄 테트라플루오로보레이트, CAS No. 125700-67-6, 시그마-알드리치 B-2903), 및 N-하이드록시석신이미드로 활성화로 NHS 에스테르, 1-(2,5-디옥소피롤리딘-1-일) 1-에틸 사이클로부탄-1,1-디카복실레이트로 전환되었다.
DME (50mL) 내 1-(2,5-디옥소피롤리딘-1-일) 1-에틸 사이클로부탄-1,1-디카복실레이트 (8g, 29.7mmol)의 용액에 물 (30mL) 내 10d (6.0g, 21.4mmol) 및 NaHCO3 (7.48g, 89.0mmol)의 용액이 부가되었다. 혼합물은 r.t.에서 16시간 동안 교반된 후, 이것은 감압 하에서 농축 건조되고 그리고 잔류물은 칼럼 크로마토그래피 (DCM:MeOH = 10:1)에 의해 정제되어 (S)-에틸 1-((1-(4-(하이드록시메틸)페닐)-2-옥소-6-우레이도헥산--3-일)카바모일)사이클로부탄카복실레이트 10c를 백색 고형물로서 얻었다 (6.4g, 68.7%). LCMS (ESI): m/z 435.0 [M+1]
THF 및 MeOH (20mL/10mL)의 혼합물 내 10c (6.4g, 14.7mmol)의 교반된 용액에 H2O (20mL) 내 LiOH·H2O (1.2g, 28.6mmol)의 용액이 r.t.에서 부가되었다. 반응 혼합물은 r.t.에서 16시간 동안 교반된 후, 용매는 감압 하에서 제거되고, 수득된 잔사는 분취-HPLC에 의해 정제되어 (S)-1-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일카바모일)사이클로부탄카복실산 10b를 얻었다 (3.5g, 수율: 58.5%). LCMS (ESI): m/z 406.9 [M+1]. 1HNMR (400MHz, 메탄올-d 4)δ 8.86 (d, J = 8.4 Hz, 2 H), 8.51 (d, J = 8.4 Hz, 2 H), 5.88 - 5.85 (m, 1 H), 5.78 (s, 2 H), 4.54 - 4.49 (m, 3 H), 4.38 - 4.32 (m, 1 H), 3.86 - 3.75 (m, 1 H), 3.84 - 3.80 (m, 2 H), 3.28 - 3.21 (m, 1 H), 3.30 - 3.24 (m, 1 H), 3.00 - 2.80 (m, 1 H), 2.37 - 2.28 (m, 2 H).
단계 3: S)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)-N-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)사이클로부탄-1,1-디카복사마이드 10의 제조
디이소프로필에틸아민, DIPEA (1.59g, 12.3mmol) 및 비스(2-옥소-3-옥사졸리딘일)포스핀산 클로라이드, BOP-Cl (CAS 등록 번호 68641-49-6, 시그마-알드리치, 692mg, 2.71mmol)이 DMF (10mL) 내 (S)-1-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일카바모일)사이클로부탄카복실산 10b (1g, 2.46mmol)의 용액에 0℃에서, 그 다음 1-(5-아미노펜틸)-1H-피롤-2,5-디온 하이드로클로라이드 10a (592mg, 2.71mmol)가 부가되었다. 혼합물은 0.5h 동안 0℃에서 교반되었다. 반응 혼합물은 시트르산 용액 (10mL)으로 켄칭되고, DCM/MeOH (10:1)로 추출되었다. 유기 층은 건조되고 농축되고, 그리고 잔류물은 실리카겔상 칼럼 크로마토그래피 (DCM:MeOH = 10:1)로 정제되어, 또한 MC-CBDK-cit-PAB-OH로 지칭되는, S)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)-N-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)사이클로부탄-1,1-디카복사마이드 10을 얻었다 (1.0g, 71%). LCMS (ESI): M+H+ = 571.28. 1H NMR (400 MHz, DMSO-d 6 ): δ 10.00 (s, 1H), 7.82-7.77 (m, 2H), 7.53 (d, J = 8.4 Hz, 2 H), 7.19 (d, J = 8.4 Hz, 2 H), 6.96 (s, 2H), 5.95 (t, J = 6.4 Hz, 1H), 5.39 (s, 2H), 5.08 (t, J = 5.6 Hz, 1H), 4.40-4.35 (m, 3H), 4.09 (d, J = 4.8 Hz, 1 H), 3.01 (d, J = 3.2 Hz, 2 H), 3.05-2.72 (m, 4H), 2.68-2.58 (m, 3H), 2.40-2.36 (m, 4H), 1.72-1.70 (m, 3H), 1.44-1.42 (m, 1H), 1.40-1.23 (m, 6H), 1.21-1.16 (m, 4H).
실시예 10 (S)-N-(1-(4-(클로로메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)사이클로부탄-1,1-디카복사마이드 11
N,N-디메틸포름아미드, DMF 또는 N-메틸피롤리돈, NMP (50mL) 내 (S)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)-N-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)사이클로부탄-1,1-디카복사마이드 10 (2.0g, 3.5mmol)의 용액이 0℃에서 점적으로 나누어서 티오닐 클로라이드, SOCl2 (1.25g, 10.5mmol)로 처리되었다. 반응물은 황색으로 잔존했다. 반응은 >90% 전환율을 나타내는 LC/MS에 의해 모니터링되었다. 반응 혼합물은 30분 또는 몇 시간 동안 20℃에서 교반된 후, 이것은 물 (50mL)로 희석되고 그리고 EtOAc (50mL x 3)로 추출되었다. 유기 층은 건조되고, 농축되고 그리고 플래시 칼럼 (DCM:MeOH = 20:1)에 의해 정제되어, 또한 일명 MC-CBDK-cit-PAB-Cl인, 11을 회색 고체로 형성한다. LCMS: (5-95, AB, 1.5 min), 0.696 min, m/z = 589.0 [M+1]+.
실시예 11 (S)-4-(2-(1-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸카바모일)사이클로부탄카복사미도)-5-우레이도펜탄아미도)벤질 4-니트로페닐 카르보네이트 12
무수 DMF 내 (S)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)-N-(1-(4-(하이드록시메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)사이클로부탄-1,1-디카복사마이드 10의 용액이 디이소프로필에틸아민 (DIEA), 그 다음 PNP 카르보네이트 (비스(4-니트로페닐) 카르보네이트)에 부가되었다. 반응 용액은 실온(r.t.)에서 4시간 동안 교반되고, 그리고 혼합물은 분취-HPLC에 의해 정제되어 12를 얻었다. LCMS (ESI): M+H+ = 736.29.
실시예 12 MC-(CBDK-cit)-PAB-(디메틸, 플루오로pipBOR)-PLA-1의 제조
PLA-2에 대한 절차에 따라, (S)-N-(1-(4-(클로로메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)사이클로부탄-1,1-디카복사마이드 11 및 불소화된 리파마이신-유도체인, 디메틸플루오로pipBOR 13 (LCMS (ESI): M+H+ = 945.43)이 반응되어 MC-(CBDK-cit)-PAB-(디메틸, 플루오로pipBOR)-PLA-1를 형성했다, 표 2. LCMS (ESI): M+H+ = 1499.7
실시예 13 MC-(CBDK-cit)-PAB-(디메틸pipBOR)-PLA-2의 제조
DMF 내 (S)-N-(1-(4-(클로로메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)-N-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸)사이클로부탄-1,1-디카복사마이드 11 (0.035mmol)이 0℃로 냉각되고 그리고 디메틸pipBOR 6, (10mg, 0.011mmol)이 부가되었다. 혼합물은 또 다른 0.5 mL의 DMF로 희석되었다. 30분 동안 공기에 개방하여 교반된다. N,N-디이소프로필에틸아민 (DIEA, 10μL, 0.05mmol)이 부가되고 그리고 반응물은 공기에 개방하여 밤새 교반했다. LC/MS에 의해, 50%의 원하는 생성물이 관측되었다. 반응물이 사라져 진행이 중단될 때까지 또 다른 6 시간 동안 공기에 개방하여 반응물이 교반되는 동안 추가의 0.2eq N,N-디이소프로필에틸아민 염기가 부가되었다. 반응 혼합물은 DMF로 희석되고 그리고 HPLC (H2O 내 20-60% ACN/HCOOH)에서 정제되어 MC-(CBDK-cit)-PAB-(디메틸pipBOR)-PLA-2를 얻었다, 표 2. LCMS (ESI): M+H+ = 1481.8, 수율 31%.
실시예 14 MC-((R)-티오펜-3-일-CBDK-cit)-PAB-(디메틸pipBOR) (PLA-3)의 제조
PLA-2에 대한 절차에 따라, (N-((S)-1-(4-(클로로메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)-N-((R)-3-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸아미노)-3-옥소-1-(티오펜-3-일)프로필)사이클로부탄-1,1-디카복사마이드 14 (LCMS (ESI): M+H+ = 742.3) 및 디메틸pipBOR 6이 반응되어 MC-((R)-티오펜-3-일-CBDK-cit)-PAB-(디메틸pipBOR)을 얻었다 (PLA-3, 표 2). LCMS (ESI): M+H+ = 1633.9
실시예 15 MC-((S)-티오펜-3-일-CBDK-cit)-PAB-(디메틸pipBOR) (PLA-4)의 제조
PLA-2에 대한 절차에 따라, (N-((R)-1-(4-(클로로메틸)페닐아미노)-1-옥소-5-우레이도펜탄-2-일)-N-((R)-3-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸아미노)-3-옥소-1-(티오펜-3-일)프로필)사이클로부탄-1,1-디카복사마이드 15 (LCMS (ESI): M+H+ = 742.3) 및 디메틸pipBOR 6이 반응되어 MC-((R)-티오펜-3-일-CBDK-cit)-PAB-(디메틸pipBOR)을 얻었다 (PLA-4, 표 2). LCMS (ESI): M+H+ = 1633.9
실시예 16 MC-(CBDK-cit)-PABC-(pipBOR) (PLA-5)의 제조
피페리딜 벤즈옥사지노 리파마이신 (pipBOR) 5 (15 mg, 0.0167 mmol), 및 그 다음 (S)-4-(2-(1-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸카바모일)사이클로부탄카복사미도)-5-우레이도펜탄아미도)벤질 4-니트로페닐 카르보네이트 12 (12mg, 0.0167mmol)이 바이알 안으로 칭량되었다. 디메틸포름아미드, DMF (0.3mL)가 부가되고, 그 다음 디이소프로필에틸아민, DIEA (0.006mL, 0.0334mmol)가 부가되고, 그리고 반응물은 실온에서 2시간 동안 교반되었다. 반응 용액은 직접적으로 HPLC (30 내지 70% MeCN/물 + 1% 포름산)로 정제되어 MC-(CBDK-cit)-PABC-(pipBOR)를 얻었다 (PLA-5, 표 2). LCMS (ESI): M+H+ = 1496.5
실시예 17 MC-(CBDK-cit)-PABC-(피페라즈BTR) (PLA-6)의 제조
PLA-5에 대한 절차에 따라, 피페리딘 리파마이신 유도체, 피페라즈BOR 16 (LCMS (ESI): M+H+ = 885.4) 및 (S)-4-(2-(1-(5-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)펜틸카바모일)사이클로부탄카복사미도)-5-우레이도펜탄아미도)벤질 4-니트로페닐 카르보네이트 12가 반응되어 MC-(CBDK-cit)-PABC-(피페라즈BTR)을 얻었다 (PLA-6. 표 2). LCMS (ESI): M+H+ = 1482.5
실시예 18 rF1 항체-항생제 콘주게이트의 제조
항체-항생제 콘주게이트 (AAC) 표 3이 표 2로부터의 것을 포함하는, PML 링커-항생제 중간체에 rF1 항체를 콘주게이트함에 의해 제조되었다. 콘주게이션에 앞서, F1 항체는, 그의 교시가 이러한 목적을 위해 참고로 편입된, WO 2004/010957에 기재된 방법론에 따른 표준 방법을 사용하여 TCEP로 부분적으로 환원되었다. 부분적으로 환원된 항체는, 예를 들면, Doronina 등 (2003) Nat. Biotechnol . 21:778-784 및 US 2005/0238649 A1에 기재된 방법론에 따른 표준 방법을 사용하여 링커-항생제 중간체에 콘주게이트된다. 간단히, 부분적으로 환원된 항체는 항체의 환원된 시스테인 잔기에 링커-항생제 중간체의 콘주게이션을 허용하도록 링커-항생제 중간체와 조합된다. 콘주게이션 반응이 켄칭되고, 그리고 AAC가 정제된다. 각 AAC에 대한 항생제 부하 (항체 당 항생제 모이어티의 평균 수)가 측정되고 그리고 단일 시스테인 돌연변이체 부위로 가공된 rF1 항체에 대해 약 1 내지 약 2 사이였다.
콘주게이션을 위한 ThioMabs의 환원/산화: CHO 세포에서 발현된 전장의 시스테인 가공된 단클론성 항체 (ThioMabs - Junutula, 등, 2008b Nature Biotech., 26(8):925-932; Dornan 등 (2009) Blood 114(13):2721-2729; US 7521541; US 7723485; WO2009/052249, Shen 등 (2012) Nature Biotech., 30(2):184-191; Junutula 등 (2008) Jour of Immun. Methods 332:41-52)가 37℃에서 3시간 동안 또는 실온에서 밤새 2mM EDTA를 갖는 50mM Tris pH 7.5 내에서 약 20-40배 과잉의 TCEP (트리스(2-카복시에틸)포스핀 하이드로클로라이드 또는 DTT (디티오트레이톨)로 환원되었다.(Getz 등 (1999) Anal. Biochem . Vol 273:73-80; 매사추세츠 주 베벌리 소재의 솔텍 벤쳐스). 환원된 ThioMab는 희석되고 그리고 10mM 아세트산나트륨, pH 5 내 HiTrap S 칼럼 상에 로딩되고 그리고 0.3M 염화나트륨을 함유하는 PBS로 용출되었다. 대안적으로, 항체는 10% 아세트산의 1/20의 용적의 부가에 의해 산성화되고, 10mM 석시네이트 pH 5로 희석되고, 칼럼 상에 로딩되고 그리고 그 다음 10 칼럼 용적의 석시네이트 완충액으로 세정되었다. 칼럼은 50mM Tris pH7.5, 2mM EDTA로 용출되었다.
용출된 환원된 ThioMab는 15배 몰 과잉의 DHAA (데하이드로아스코르브산) 또는 200nM 수성 구리 술페이트 (CuSO4)로 처리되었다. 쇄간 이황화 결합의 산화는 약 세 시간 또는 그 초과로 완료되었다. 주위 공기 산화 또한 유효하였다. 재-산화된 항체는 20mM 나트륨 석시네이트 pH 5, 150mM NaCl, 2mM EDTA 안에서 투석되었고 그리고 -20℃에서 냉동 보관되었다.
링커-항생제 중간체로 ThioMabs의 콘주게이션: 탈차단된, 재산화된, 티오-항체 (ThioMab)는 반응 혼합물의 LC-MS 분석에 의해 측정되는 바와 같이 반응이 완료될 때까지 (16-24 시간), 50mM Tris, pH 8 내에서 (20mM의 농도로 DMSO 스톡으로부터) 표 2의 6-8배 몰 과잉의 링커-항생제 중간체와 반응되었다.
조물질 항체-항생제 콘주게이트 (AAC)는 그런 다음 20mM 나트륨 석시네이트, pH 5로 희석 후 양이온 교환 칼럼에 적용되었다. 칼럼은 적어도 10 칼럼 용적의 20 mM 나트륨 석시네이트, pH 5로 세정되고, 그리고 항체는 PBS로 용출되었다. AAC는 겔 여과 칼럼을 사용하여 240mM 수크로오스를 갖는 20mM His/아세테이트, pH 5로 제형화되었다. AAC는 라이신 C 엔도펩티다아제로 치료 전후 응집 분석 및 LC-MS에 대한 단백질 농도, 분석적 SEC (크기-배제 크로마토그래피)를 측정하기 위해 UV 분광법에 의해 특성규명되었다.
크기 배제 크로마토그래피는 0.75ml/min의 유속으로 15% IPA 및 0.25mM 칼륨 클로라이드를 갖는 0.2M 인산칼륨 pH 6.2에서 Shodex KW802.5 칼럼을 사용하여 수행되었다. AAC의 응집 상태는 280nm에서 용출된 피크 면적 흡광도의 적분에 의해 측정되었다.
LC-MS 분석은 애질런드 QTOF 6520 ESI 기기를 사용하여 수행되었다. 예로서, 이 화학 물질을 사용하여 생성된 AAC는 37℃에서 30분 동안 Tris, pH 7.5 내 1:500 w/w Endo프로테이나제 Lys C (프로메가)로 처리되었다. 수득한 절단 단편은 80℃로 가열된 1000A, 8um PLRP-S 칼럼 상에 로딩되고 그리고 5분 내에 30% B 내지 40% B의 구배로 용출되었다. 이동상 A: 0.05% TFA를 갖는 H2O. 이동상 B: 0.04% TFA를 갖는 아세토니트릴. 유속: 0.5ml/min. 단백질 용출은 전기분무 이온화 및 MS 분석 전에 280nm에서 UV 흡광도 검출로 모니터링되었다. 비콘주게이트된 Fc 단편, 잔류 비콘주게이트된 Fab 및 항생제-Fab의 크로마토그래피 해상도가 일반적으로 달성되었다. 수득된 m/z 스펙트럼은 매스 헌터™ 소프트웨어(애질런트 테크놀로지스)를 사용하여 디콘볼류션되어 항체 단편의 질량을 계산하였다.
AAC, 103 (AAR = 1.9) 티오-rF1-HC-121C, LC-V205C-MC-(CBDK-cit)-PAB-(디메틸pipBOR)은 가공된 Cys 205를 함유하는 서열 번호 9의 rF1 L 쇄 및 서열 번호 10을 포함하는 rF1 H 쇄을 사용하여 제작되었다. AAC 102 (AAR = 3.9) 티오-rF1-HC-121C, LC-V205C-MC-(CBDK-cit)-PAB-(디메틸pipBOR)은 가공된 Cys 205를 함유하는 이전의 서열 번호 9의 rF1 L 쇄 및 가공된 Cys 114 (114 카밧 넘버링은 118 Eu 넘버링 및 121 순차적인 넘버링과 동일함)를 함유하는 서열 번호 12을 포함하는 rF1 H 쇄을 사용하여 제작되었다. Cys 가공된 L 및/또는 H 쇄는 표 2에서 나타낸 바와 같이 PML 링커 및 리파마이신-유형 항생제에 콘주게이트되었다.
실시예 19 rF1-AAC의 시험관내 효능
S. 아우레우스 (USA300 NRS384 균주)는 박테리아에 항체의 결합을 허용하도록 1시간 동안 다양한 용량 (100ug/mL, 10ug/mL, 1ug/mL 또는 0.1ug/mL)의 항-S. 아우레우스 비콘주게이트된 항체, 항체 (AAR2) 당 1.9 평균 항생제 분자로 로딩된 103 AAC 또는 항체 (AAR4) 당 3.9 평균 항생제 분자로 로딩된 102 AAC로 배양되었다. 수득한 옵소닌화된 박테리아는 식균작용 ( 시험관내 대식세포 검정)을 허용하도록 뮤린 대식세포에 공급되어 37℃에서 배양되었다. 2시간 후, 감염 혼합물은 제거되고 그리고 임의의 잔존하는 세포외 박테리아를 죽이기 위해 50ug/mL의 겐타마이신으로 보강된 정상 성장 배지로 대체되었다. 생존한 세포내 박테리아의 총 수는 트립신 소이 우무평판 상에 대식세포 용해물의 연속 희석을 도말함에 의해 2일 후에 측정되었다.
결과는 도 10에 도시되었다. 시험된 AAC (AAR2 vs. AAR4) 양자는 유사한 용량 반응을 나타냈고 그리고 1ug/mL 및 그 아래에서는 부분 또는 무 사멸로 10ug/mL 또는 그 이상의 용량으로 최대 사멸을 산출하여, 이는 AAC에 대한 용량 반응이 박테리아 상의 항체 결합 부위의 수에 의해 제한된다는 것을 시사한다. 항체 당 4 항생제 분자를 로딩함에 의해, AAC에 의한 박테리아 사멸 및 박테리아의 전체 사멸은 모든 시험된 용량에서 AAR4 AAC가 우수하였다. 시험된 최고 용량에서 2DAR AAC는 350-배 박테리아 부하를 감소하였고, 반면에 4AAR AAC는 4,000-배 초과로 박테리아 부하를 감소하였다. (점선은 도시된 검정에 대한 검출의 한계를 나타낸다).
본 실시예는 표 3으로부터 rF1-AAC, 102 (AAR = 3.9) 및 103 (AAR = 1.9) 티오-rF1-HC-121C, LC-V205C-MC-(CBDK-cit)-PAB-(디메틸pipBOR)이 시험관내 대식세포 검정에서 세포내 MRSA를 사멸하였다는 것을 입증한다. 결과는 도 10에 도시되었다.
실시예 20 rF1-AAC의 생체내 효능
본 실시예는 rF1-AAC는 뮤린 정맥내 감염 모델에서 세포내 S. 아우레우스 감염을 크게 감소하거나 또는 퇴치하는데 유효했다는 것을 입증한다.
복막염 모델. 7주령 암컷 A/J 마우스 (잭슨 라보라토리스)가 5x107 CFU의 USA300으로 복막 주사에 의해 감염되었다. 마우스는 감염 2일 후 희생되고 그리고 복막은 5mL의 차가운 포스페이트 완충된 염수 용액 (PBS)으로 씻어 내어 졌다. 신장은 정맥내 감염 모델에 대해 아래에서 기재된 바와 같이 5mL의 PBS에서 균질화되었다. 복막 세척물은 테이블 최상부 원심분리기에서 4℃에서 5분 동안 1,000rpm에서 원심분리되었다. 상청액은 세포외 박테리아로 수집되고 그리고 복막 세포를 함유하는 세포 펠렛은 세포내 분획으로 수집되었다. 세포는 37℃에서 20분 동안 50μg/mL의 라이소스파핀으로 처리되어 오염된 세포외 박테리아를 죽였다. 복막 세포는 얼음 냉각된 PBS로 3x 세정되어 분석 전 라이소스파핀을 제거한다. 세포내 CFUs의 수를 세기 위해, 복막 세포는 0.1% 트리톤-X를 갖는 HB (10mM HEPES 및 .1% 소 혈청 알부민으로 보강된 행크스 평형 염류액)에서 용해되었고 그리고 용해물의 연속 희석이 0.05% 트윈-20을 갖는 PBS에서 제조되었다.
뮤린 정맥내 감염 모델. 경쟁하는 인간 IgG (SCID IVIG 모델)를 포함하는 연구를 위해, CB17.SCID 마우스 (캘리포니아 주 홀리스터 소재의 찰스 리버 라보라토리스)가 혈청 내 적어도 10mg/mL의 인간 IgG의 일정한 혈청 수준을 달성하기 위해 최적화된 투여 레지멘을 사용하여 감마가드 S/D IGIV 면역 글로불린 (ASD 헬쓰케어, Brooks KY)으로 재구성되었다. IGIV는 마우스 당 30mg의 초기 정맥내 용량으로 그 다음 6시간 후 복강내 주사에 의해 15mg/마우스의 제2 용량, 그리고 3 연속적인 일 동안 복강내 주사에 의해 마우스 당 15mg의 후속의 매일 투약으로 투여된다.
마우스 (각각의 항체 또는 AAC에 대해 n=8)는 정맥내 주사에 의해 포스페이트 완충된 염수에서 희석된 1x107 CFU의 MRSA (USA300 NRS384 균주)를 갖는 IGIV의 제1 용량 4시간 후 감염되었다. 감염된 마우스는 50mg/kg의 rF1 기존의 항체, 103 AAC DAR2 또는 102 AAC DAR4로 처리되었다. 마우스는 정맥내 주사에 의해 감염 26h 후 단회 용량의 AAC가 주어지고 그리고 감염 후 4일에 희생되고 그리고 신장 및 심장은 5mL의 포스페이트 완충된 염수에 수거되었다. 조직 샘플은 GentleMACS Dissociator™ (캘리포니아 주 오번 소재의 밀테니 바이오택)을 사용하여 균질화되었다. 장기 당 회수된 박테리아의 총 수는 5% 섬유소가 제거된 양 혈액을 갖는 트립신 소이 한천 상에 PBS .05% 트윈 내 조직 균질물의 연속 희석을 도말함에 의해 측정되었다.
도 11a는 감염된 마우스의 신장 내 박테리아 부하에 대한 AAC로 생체내 치료의 결과를 도시한다. 항체 당 2 항생제 분자를 함유하는 AAC (DAR2)로 치료는 대략 30-배로 박테리아 부하를 감소하였고 그리고 항체 당 4 항생제 분자를 함유하는 AAC (AAR4)로 치료는 30,000-배 초과로 박테리아 부하를 감소하였다.
도 11b는 심장 내 박테리아 계수에 대한 AAC로 생체내 치료의 결과를 도시한다. AAC AAR2로의 치료는 심장에 검출불가능한 수준의 박테리아를 갖는 8마리 마우스 중 6마리에서 대략 70-배로 박테리아 부하를 감소하였고; AAC DAR4로의 치료는 검출불가능한 수준의 박테리아를 갖는 8마리 마우스 중 8마리에서 초래된 심장에서 감염을 완전히 박멸했다.
비록 전술한 발명이 이해의 명확함을 위해 설명 및 실시예로서 일부 상세히 기재되었지만, 설명 및 실시예는 본 발명의 범위를 제한하는 것으로 해석되어서는 안된다. 본 명세서 전반에 걸쳐 인용된 모든 특허, 특허 출원 및 참조는 명확히 참고로 포함된다.
<110> GENENTECH, INC. ET AL.
<120> ANTI-STAPHYLOCOCCUS AUREUS ANTIBODY RIFAMYCIN CONJUGATES AND USES
THEREOF
<130> P32350-WO
<150> 62/087,213
<151> 2014-12-03
<160> 28
<170> KoPatentIn 3.0
<210> 1
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 1
Arg Phe Ala Met Ser
1 5
<210> 2
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 2
Ser Ile Asn Asn Gly Asn Asn Pro Tyr Tyr Ala Arg Ser Val Gln Tyr
1 5 10 15
<210> 3
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 3
Asp His Pro Ser Ser Gly Trp Pro Thr Phe Asp Ser
1 5 10
<210> 4
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 4
Arg Ala Ser Glu Asn Val Gly Asp Trp Leu Ala
1 5 10
<210> 5
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 5
Lys Thr Ser Ile Leu Glu Ser
1 5
<210> 6
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 6
Gln His Tyr Ile Arg Phe Pro Tyr Thr
1 5
<210> 7
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 7
Gln His Tyr Met Arg Phe Pro Tyr Thr
1 5
<210> 8
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 8
Ser Ile Asn Ser Gly Asn Asn Pro Tyr Tyr Ala Arg Ser Val Gln Tyr
1 5 10 15
<210> 9
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 9
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ala Leu Pro Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Glu Asn Val Gly Asp Trp
20 25 30
Leu Ala Trp Tyr Arg Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Thr Ser Ile Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Met Arg Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Cys Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 10
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 10
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Arg Phe
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Ser Gly Asn Asn Pro Tyr Tyr Ala Arg Ser Val Gln
50 55 60
Tyr Arg Phe Thr Val Ser Arg Asp Val Ser Gln Asn Thr Val Ser Leu
65 70 75 80
Gln Met Asn Asn Leu Arg Ala Glu Asp Ser Ala Thr Tyr Phe Cys Ala
85 90 95
Lys Asp His Pro Ser Ser Gly Trp Pro Thr Phe Asp Ser Trp Gly Pro
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 11
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 11
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ala Leu Pro Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Glu Asn Val Gly Asp Trp
20 25 30
Leu Ala Trp Tyr Arg Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Thr Ser Ile Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ile Arg Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Cys Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 12
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 12
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Arg Phe
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Ser Gly Asn Asn Pro Tyr Tyr Ala Arg Ser Val Gln
50 55 60
Tyr Arg Phe Thr Val Ser Arg Asp Val Ser Gln Asn Thr Val Ser Leu
65 70 75 80
Gln Met Asn Asn Leu Arg Ala Glu Asp Ser Ala Thr Tyr Phe Cys Ala
85 90 95
Lys Asp His Pro Ser Ser Gly Trp Pro Thr Phe Asp Ser Trp Gly Pro
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Cys Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 13
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 13
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Arg Phe
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Ser Gly Asn Asn Pro Tyr Tyr Ala Arg Ser Val Gln
50 55 60
Tyr Arg Phe Thr Val Ser Arg Asp Val Ser Gln Asn Thr Val Ser Leu
65 70 75 80
Gln Met Asn Asn Leu Arg Ala Glu Asp Ser Ala Thr Tyr Phe Cys Ala
85 90 95
Lys Asp His Pro Ser Ser Gly Trp Pro Thr Phe Asp Ser Trp Gly Pro
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 14
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 14
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ala Leu Pro Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Glu Asn Val Gly Asp Trp
20 25 30
Leu Ala Trp Tyr Arg Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Thr Ser Ile Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Met Arg Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val
100 105 110
<210> 15
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 15
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ala Leu Pro Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Glu Asn Val Gly Asp Trp
20 25 30
Leu Ala Trp Tyr Arg Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Thr Ser Ile Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ile Arg Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val
100 105 110
<210> 16
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 16
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser
20 25 30
<210> 17
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 17
Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val Ala
1 5 10
<210> 18
<211> 32
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 18
Arg Phe Thr Val Ser Arg Asp Val Ser Gln Asn Thr Val Ser Leu Gln
1 5 10 15
Met Asn Asn Leu Arg Ala Glu Asp Ser Ala Thr Tyr Phe Cys Ala Lys
20 25 30
<210> 19
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 19
Trp Gly Pro Gly Thr Leu Val Thr Val Ser Ser
1 5 10
<210> 20
<211> 23
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 20
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ala Leu Pro Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys
20
<210> 21
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 21
Trp Tyr Arg Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr
1 5 10 15
<210> 22
<211> 32
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic polypeptide"
<400> 22
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys
20 25 30
<210> 23
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<400> 23
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val
1 5 10
<210> 24
<211> 550
<212> PRT
<213> Staphylococcus epidermidis
<220>
<221> VARIANT
<222> (51)..(550)
<223> /replace=" "
<220>
<221> UNSURE
<222> (1)..(550)
<223> /note="This sequence may encompass 25 to 275 'Ser-Asp' repeating
units, wherein some positions may be absent"
<220>
<221> UNSURE
<222> (1)..(550)
<223> /note="Variant residues given in the sequence have no preference
with respect to those in the annotations for variant positions"
<400> 24
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
1 5 10 15
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
20 25 30
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
35 40 45
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
50 55 60
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
65 70 75 80
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
85 90 95
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
100 105 110
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
115 120 125
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
130 135 140
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
145 150 155 160
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
165 170 175
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
180 185 190
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
195 200 205
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
210 215 220
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
225 230 235 240
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
245 250 255
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
260 265 270
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
275 280 285
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
290 295 300
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
305 310 315 320
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
325 330 335
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
340 345 350
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
355 360 365
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
370 375 380
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
385 390 395 400
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
405 410 415
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
420 425 430
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
435 440 445
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
450 455 460
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
465 470 475 480
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
485 490 495
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
500 505 510
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
515 520 525
Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp Ser Asp
530 535 540
Ser Asp Ser Asp Ser Asp
545 550
<210> 25
<211> 5
<212> PRT
<213> Staphylococcus epidermidis
<220>
<221> MOD_RES
<222> (3)
<223> Any amino acid
<400> 25
Leu Pro Xaa Thr Gly
1 5
<210> 26
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> /note="Description of Artificial Sequence: Synthetic peptide"
<220>
<221> VARIANT
<222> (4)
<223> /replace="Met"
<220>
<221> UNSURE
<222> (1)..(9)
<223> /note="Variant residues given in the sequence have no preference
with respect to those in the annotations for variant positions"
<400> 26
Gln His Tyr Ile Arg Phe Pro Tyr Thr
1 5
<210> 27
<211> 8
<212> PRT
<213> Staphylococcus sp.
<400> 27
Ser Asp Ser Asp Ser Asp Ser Asp
1 5
<210> 28
<211> 6
<212> PRT
<213> Staphylococcus sp.
<400> 28
Ser Asp Ser Asp Ser Asp
1 5
Claims (41)
- 리파마이신-유형 항생제에 프로테아제-절단가능한 비-펩티드 링커에 의해 공유 부착된, 항-세린-아스파르테이트 반복 (SDR) 항체를 포함하는 항체-항생제 콘주게이트 화합물.
- 제2항에 있어서, 상기 리파마이신-유형 항생제는 리파라질-유형 항생제인, 항체-항생제 콘주게이트 화합물.
- 제2항에 있어서, 상기 리파마이신-유형 항생제는 상기 프로테아제-절단가능한 비-펩티드 링커에 부착된 4차 아민을 포함하는, 항체-항생제 콘주게이트 화합물.
- 제2항에 있어서, 다음 화학식 I을 갖는 항체-항생제 콘주게이트 화합물:
식 중,
점선은 선택적인 결합을 나타내고;
R은 H, C1-C12 알킬, 또는 C(O)CH3이고;
R1은 OH이고;
R2는 CH=N-(헤테로사이클릴)이고, 여기서 상기 헤테로사이클릴은 C(O)CH3, C1-C12 알킬, C1-C12 헤테로아릴, C2-C20 헤테로사이클릴, C6-C20 아릴, 및 C3-C12 카르보사이클릴로부터 독립적으로 선택된 1종 이상의 기로 임의로 치환되고;
또는 R1 및 R2는 5- 또는 6-원 융합된 헤테로아릴 또는 헤테로사이클릴을 형성하고, 그리고 임의로 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환을 형성하고, 여기서 상기 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환은 H, F, Cl, Br, I, C1-C12 알킬, 또는 OH로 임의로 치환되고;
PML은 R2 또는 R1 및 R2에 의해 형성된 융합된 헤테로아릴 또는 헤테로사이클릴에 부착된 프로테아제-절단가능한 비-펩티드 링커이고; 그리고
Ab는 rF1 항체이다. - 제12항에 있어서, R6는 (CH2)5 인, 항체-항생제 콘주게이트 화합물.
- 제2항에 있어서, Y는 파라-아미노벤질 또는 파라-아미노벤질옥시카르보닐을 포함하는, 항체-항생제 콘주게이트 화합물.
- 제1항에 있어서, 상기 항-SDR 항체는 rF1 항체인 항체-항생제 콘주게이트 화합물.
- 제22항에 있어서, 상기 rF1 항체는 경쇄 (L) 및 중쇄(H)를 포함하고, 상기 L 쇄는 CDR L1, CDR L2, 및 CDR L3을 포함하고 그리고 상기 H 쇄는 CDR H1, CDR H2 및 CDR H3을 포함하고, 상기 CDR L1, CDR L2, 및 CDR L3 및 CDR H1, CDR H2 및 CDR H3은 각각 표 4A 및 4B에 나타낸 바와 같이, 각각의 Abs F1, rF1, rF1.v1 및 rF1.v6 (서열 번호1-8)의 CDR들의 아미노산 서열을 포함하는, 항체-항생제 콘주게이트.
- 제22항에 있어서, 상기 rF1 항체는 중쇄 가변 영역 (VH)을 포함하고, 상기 VH는 서열 번호: 13의 VH 영역의 길이에 걸쳐 적어도 95% 서열 동일성을 포함하는, 항체-항생제 콘주게이트.
- 제24항에 있어서, 상기 VL은 서열 번호 14 또는 서열 번호 15의 VL 영역의 길이에 걸쳐 적어도 95% 서열 동일성을 포함하는 항체-항생제 콘주게이트 화합물.
- 제1항 또는 제22항 중 어느 한 항에 있어서, 상기 항-SDR 항체는 생체내에서 스타필로코쿠스 아우레우스 및/또는 스타필로코쿠스 에피더미디스에 결합하는 항체-항생제 콘주게이트 화합물.
- 제1항 내지 제26항 중 어느 한 항에 있어서, 상기 항체는 F(ab) 또는 F(ab')2인 항체-항생제 콘주게이트 화합물.
- 청구항 1의 항체-항생제 콘주게이트 화합물, 및 약제학적으로 허용가능한 담체, 활윤제, 희석제, 또는 부형제를 포함하는 약제학적 조성물.
- 환자에서 스타필로코시(Staphyloccocal) 박테리아 감염을 치료하는 방법으로서,
치료적 유효량의 제1항의 항체-항생제 콘주게이트 화합물을 상기 환자에게 투여하는 단계를 포함하는, 방법. - 제29항에 있어서, 상기 환자는 스타필로코쿠스 아우레우스(Staphylococcus aureus)에 감염된, 방법.
- 제30항에 있어서, 상기 환자는 스타필로코쿠스 에피더미디스(Staphylococcus epidermidis)에 감염된, 방법.
- 제29항에 있어서, 상기 항체-항생제 콘주게이트 화합물은 약 50mg/kg 내지 100mg/kg의 범위인 용량으로 상기 환자에게 투여되는, 방법.
- 제29항에 있어서, 상기 환자는 제2 항생제를 갖는 치료와 결합된, 상기 항체-항생제 콘주게이트 화합물을 투여받는, 방법.
- 제1항의 항체-항생제 콘주게이트 화합물을 투여함에 의해, 상기 숙주세포를 사멸하지 않고 staph 아우레우스 감염된 환자의 세포에서 세포내 Staph 아우레우스를 사멸하는 방법.
- rF1 항체에 리파마이신-유형 항생제를 콘주게이트하는 단계를 포함하는, 제1항의 항체-항생제 콘주게이트 화합물을 제조하는 방법.
- a) 제23항의 약제학적 조성물; 및
b) 사용 설명서를 포함하는, 박테리아 감염을 치료하기 위한 키트. - 다음 화학식 II를 갖는 항생제-링커 중간체:
식 중,
점선은 임의의 결합을 나타내고;
R은 H, C1-C12 알킬, 또는 C(O)CH3이고;
R1은 OH이고;
R2는 CH=N-(헤테로사이클릴)이고, 상기 헤테로사이클릴은 C(O)CH3, C1-C12 알킬, C1-C12 헤테로아릴, C2-C20 헤테로사이클릴, C6-C20 아릴, 및 C3-C12 카르보사이클릴로부터 독립적으로 선택된 1종 이상의 기로 임의로 치환되고;
또는 R1 및 R2는 5- 또는 6-원 융합된 헤테로아릴 또는 헤테로사이클릴을 형성하고, 그리고 임의로 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환을 형성하고, 상기 스피로 또는 융합된 6-원 헤테로아릴, 헤테로사이클릴, 아릴, 또는 카르보사이클릴 환은 H, F, Cl, Br, I, C1-C12 알킬, 또는 OH로 임의로 치환되고;
PML은 R2 또는 R1 및 R2에 의해 형성된 융합된 헤테로아릴 또는 헤테로사이클릴에 부착된 프로테아제-절단가능한, 비-펩티드 링커이고; 그리고 다음 화학식을 갖고:
식 중, Str은 연신부 단위체이고; PM은 펩티드도미메틱 단위체이고, 그리고 Y는 스페이서 단위체이며; 그리고
X는 말레이미드, 티올, 아미노, 브로마이드, 브로모아세트아미도, 아이오도아세트아미도, p-톨루엔술포네이트, 아이오다이드, 하이드록실, 카복실, 피리딜 이황화, 및 N-하이드록시석신이미드로부터 선택된 반응성 작용기이다.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462087213P | 2014-12-03 | 2014-12-03 | |
| US62/087,213 | 2014-12-03 | ||
| PCT/US2015/063515 WO2016090040A1 (en) | 2014-12-03 | 2015-12-02 | Anti-staphylococcus aureus antibody rifamycin conjugates and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170086542A true KR20170086542A (ko) | 2017-07-26 |
Family
ID=55022690
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177015225A KR20170086542A (ko) | 2014-12-03 | 2015-12-02 | 항-스타필로코쿠스 아우레우스 항체 리파마이신 콘주게이트 및 그것의 용도 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20180125995A1 (ko) |
| EP (1) | EP3226908A1 (ko) |
| JP (1) | JP6751393B2 (ko) |
| KR (1) | KR20170086542A (ko) |
| CN (1) | CN107249642A (ko) |
| BR (1) | BR112017011478A2 (ko) |
| CA (1) | CA2966211A1 (ko) |
| HK (1) | HK1244230A1 (ko) |
| MX (1) | MX2017007231A (ko) |
| RU (1) | RU2017118792A (ko) |
| WO (1) | WO2016090040A1 (ko) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EA033456B1 (ru) | 2013-12-16 | 2019-10-31 | Genentech Inc | Конъюгаты антитело-лекарственное средство, содержащие пептидомиметические линкеры |
| WO2015095227A2 (en) | 2013-12-16 | 2015-06-25 | Genentech, Inc. | Peptidomimetic compounds and antibody-drug conjugates thereof |
| CN108064246A (zh) | 2015-06-15 | 2018-05-22 | 基因泰克公司 | 抗体和免疫结合物 |
| TWI814699B (zh) | 2015-12-04 | 2023-09-11 | 美商思進公司 | 四級胺化妥布賴森(tubulysin)化合物之結合物 |
| US11793880B2 (en) | 2015-12-04 | 2023-10-24 | Seagen Inc. | Conjugates of quaternized tubulysin compounds |
| CN108713020A (zh) * | 2016-03-04 | 2018-10-26 | 豪夫迈·罗氏有限公司 | 制备抗体-利福霉素缀合物的方法 |
| SG10202104259RA (en) | 2016-11-08 | 2021-06-29 | Regeneron Pharma | Steroids and protein-conjugates thereof |
| US11491237B2 (en) | 2017-05-18 | 2022-11-08 | Regeneron Pharmaceuticals, Inc. | Cyclodextrin protein drug conjugates |
| AU2018365946A1 (en) * | 2017-11-07 | 2020-05-14 | Regeneron Pharmaceuticals, Inc. | Hydrophilic linkers for antibody drug conjugates |
| EP3790899A1 (en) | 2018-05-09 | 2021-03-17 | Regeneron Pharmaceuticals, Inc. | Anti-msr1 antibodies and methods of use thereof |
| CN111939256B (zh) * | 2020-07-06 | 2022-05-31 | 中国药科大学 | 一种具有细菌调理特性的抗菌辅助材料及其制备方法和应用 |
| WO2023023378A1 (en) * | 2021-08-20 | 2023-02-23 | Rutgers, The State University Of New Jersey | DUAL-TARGETED RNA POLYMERASE INHIBITORS: CONJUGATES OF BENZOXAZINO- AND SPIRO-RIFAMYCINS WITH Nα-AROYL- N-ARYL-PHENYLALANINAMIDES |
| WO2023028593A2 (en) * | 2021-08-27 | 2023-03-02 | University Of Georgia Research Foundation, Inc. | Targeted nanoparticles and their uses related to infectious disease |
Family Cites Families (69)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB877732A (en) | 1958-08-12 | 1961-09-20 | Lepetit Spa | The antibiotic rifomycin, its components and methods of preparing same |
| US3773919A (en) | 1969-10-23 | 1973-11-20 | Du Pont | Polylactide-drug mixtures |
| US4485045A (en) | 1981-07-06 | 1984-11-27 | Research Corporation | Synthetic phosphatidyl cholines useful in forming liposomes |
| US4544545A (en) | 1983-06-20 | 1985-10-01 | Trustees University Of Massachusetts | Liposomes containing modified cholesterol for organ targeting |
| US4610919A (en) | 1985-06-14 | 1986-09-09 | Fiber Bond Corporation | Binder for fibrous padding |
| JP2544375B2 (ja) | 1986-07-14 | 1996-10-16 | 鐘淵化学工業株式会社 | アルキル置換ベンゾキサジノリフアマイシン誘導体 |
| IL85035A0 (en) | 1987-01-08 | 1988-06-30 | Int Genetic Eng | Polynucleotide molecule,a chimeric antibody with specificity for human b cell surface antigen,a process for the preparation and methods utilizing the same |
| CA1304363C (en) | 1988-11-01 | 1992-06-30 | Takehiko Yamane | 3'-hydroxybenzoxazinorifamycin derivative, process for preparing the same and antibacterial agent containing the same |
| US5013556A (en) | 1989-10-20 | 1991-05-07 | Liposome Technology, Inc. | Liposomes with enhanced circulation time |
| EP0590058B1 (en) | 1991-06-14 | 2003-11-26 | Genentech, Inc. | HUMANIZED Heregulin ANTIBODy |
| US5362852A (en) | 1991-09-27 | 1994-11-08 | Pfizer Inc. | Modified peptide derivatives conjugated at 2-hydroxyethylamine moieties |
| US6660267B1 (en) | 1992-12-21 | 2003-12-09 | Promega Corporation | Prevention and treatment of sepsis |
| US5545721A (en) | 1992-12-21 | 1996-08-13 | Ophidian Pharmaceuticals, Inc. | Conjugates for the prevention and treatment of sepsis |
| US6214345B1 (en) | 1993-05-14 | 2001-04-10 | Bristol-Myers Squibb Co. | Lysosomal enzyme-cleavable antitumor drug conjugates |
| US6214388B1 (en) | 1994-11-09 | 2001-04-10 | The Regents Of The University Of California | Immunoliposomes that optimize internalization into target cells |
| US5981522A (en) | 1995-09-01 | 1999-11-09 | Kaneka Corporation | Treatment of disease caused by infection of Helicobacter |
| JP3963976B2 (ja) | 1995-12-08 | 2007-08-22 | 株式会社カネカ | クラミジア感染症治療剤 |
| US6322788B1 (en) | 1998-08-20 | 2001-11-27 | Stanley Arthur Kim | Anti-bacterial antibodies and methods of use |
| DK2270147T4 (da) | 1999-04-09 | 2020-08-31 | Kyowa Kirin Co Ltd | Fremgangsmåde til at kontrollere aktiviteten af immunologisk funktionelt molekyle |
| US7101692B2 (en) * | 1999-04-15 | 2006-09-05 | The Regents Of The University Of California | Identification of sortase gene |
| AU5867100A (en) * | 1999-05-03 | 2000-12-12 | Medarex, Inc. | Human antibodies to staphylococcus aureus |
| AU7950400A (en) | 1999-10-19 | 2001-04-30 | Kyowa Hakko Kogyo Co. Ltd. | Process for producing polypeptide |
| US6946292B2 (en) | 2000-10-06 | 2005-09-20 | Kyowa Hakko Kogyo Co., Ltd. | Cells producing antibody compositions with increased antibody dependent cytotoxic activity |
| ES2651952T3 (es) | 2000-10-06 | 2018-01-30 | Kyowa Hakko Kirin Co., Ltd. | Células que producen unas composiciones de anticuerpo |
| US7064191B2 (en) | 2000-10-06 | 2006-06-20 | Kyowa Hakko Kogyo Co., Ltd. | Process for purifying antibody |
| US6884869B2 (en) | 2001-04-30 | 2005-04-26 | Seattle Genetics, Inc. | Pentapeptide compounds and uses related thereto |
| WO2003002885A1 (en) * | 2001-06-28 | 2003-01-09 | Freni Brembo S.P.A. | Composite disc for a disc brake having a splittable braking band |
| WO2003026577A2 (en) | 2001-09-24 | 2003-04-03 | Seattle Genetics, Inc. | P-amidobenzylethers in drug delivery agents |
| US7091186B2 (en) | 2001-09-24 | 2006-08-15 | Seattle Genetics, Inc. | p-Amidobenzylethers in drug delivery agents |
| KR100988949B1 (ko) | 2001-10-25 | 2010-10-20 | 제넨테크, 인크. | 당단백질 조성물 |
| WO2003043583A2 (en) | 2001-11-20 | 2003-05-30 | Seattle Genetics, Inc. | Treatment of immunological disorders using anti-cd30 antibodies |
| JP2005510534A (ja) * | 2001-11-21 | 2005-04-21 | アクティブバイオティクス インコーポレイティッド | 標的化治療薬およびその使用 |
| US20040093621A1 (en) | 2001-12-25 | 2004-05-13 | Kyowa Hakko Kogyo Co., Ltd | Antibody composition which specifically binds to CD20 |
| AU2003236015A1 (en) | 2002-04-09 | 2003-10-20 | Kyowa Hakko Kirin Co., Ltd. | Process for producing antibody composition |
| EP1498491A4 (en) | 2002-04-09 | 2006-12-13 | Kyowa Hakko Kogyo Kk | METHOD FOR INCREASING THE ACTIVITY OF AN ANTIBODY COMPOSITION FOR BINDING TO THE FC GAMMA RECEPTOR IIIA |
| WO2003085107A1 (fr) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | Cellules à génome modifié |
| EP1502603A4 (en) | 2002-04-09 | 2006-12-13 | Kyowa Hakko Kogyo Kk | AN ANTIBODY COMPOSITION CONTAINING MEDICAMENT FOR PATIENTS WITH Fc gamma RIIIa POLYMORPHISM |
| EP1500400A4 (en) | 2002-04-09 | 2006-10-11 | Kyowa Hakko Kogyo Kk | MEDICAMENT WITH ANTIBODY COMPOSITION |
| EP1500698B1 (en) | 2002-04-09 | 2011-03-30 | Kyowa Hakko Kirin Co., Ltd. | Cell with depression or deletion of the activity of protein participating in gdp-fucose transport |
| JP4741838B2 (ja) | 2002-07-31 | 2011-08-10 | シアトル ジェネティクス,インコーポレーテッド | 癌、自己免疫疾患または感染症を治療するための薬物結合体およびその使用 |
| US20050180972A1 (en) | 2002-07-31 | 2005-08-18 | Wahl Alan F. | Anti-CD20 antibody-drug conjugates for the treatment of cancer and immune disorders |
| US7217797B2 (en) | 2002-10-15 | 2007-05-15 | Pdl Biopharma, Inc. | Alteration of FcRn binding affinities or serum half-lives of antibodies by mutagenesis |
| CA2502413A1 (en) | 2002-11-01 | 2004-05-21 | The Regents Of The University Of Colorado, A Body Corporate | Quantitative analysis of protein isoforms using matrix-assisted laser desorption/ionization time of flight mass spectrometry |
| PT1572744E (pt) | 2002-12-16 | 2010-09-07 | Genentech Inc | Variantes de imunoglobulina e utilizações destas |
| JP2007503439A (ja) | 2003-08-22 | 2007-02-22 | アクティブバイオティクス インコーポレイティッド | リファマイシンアナログおよびそれらの使用法 |
| EP1688439A4 (en) | 2003-10-08 | 2007-12-19 | Kyowa Hakko Kogyo Kk | HYBRID PROTEIN COMPOSITION |
| EP1705251A4 (en) | 2003-10-09 | 2009-10-28 | Kyowa Hakko Kirin Co Ltd | PROCESS FOR PRODUCING ANTIBODY COMPOSITION BY RNA INHIBITION OF FUNCTION OF $ G (A) 1,6-FUCOSYLTRANSFERASE |
| PT2489364E (pt) | 2003-11-06 | 2015-04-16 | Seattle Genetics Inc | Compostos de monometilvalina conjugados com anticorpos |
| WO2005053742A1 (ja) | 2003-12-04 | 2005-06-16 | Kyowa Hakko Kogyo Co., Ltd. | 抗体組成物を含有する医薬 |
| CN1918172B (zh) | 2003-12-23 | 2011-09-14 | 活跃生物工艺学公司 | 利福霉素类似物及其用途 |
| US7375078B2 (en) | 2004-02-23 | 2008-05-20 | Genentech, Inc. | Heterocyclic self-immolative linkers and conjugates |
| DK1791565T3 (en) | 2004-09-23 | 2016-08-01 | Genentech Inc | Cysteingensplejsede antibodies and conjugates |
| WO2007008848A2 (en) | 2005-07-07 | 2007-01-18 | Seattle Genetics, Inc. | Monomethylvaline compounds having phenylalanine carboxy modifications at the c-terminus |
| WO2007008603A1 (en) | 2005-07-07 | 2007-01-18 | Seattle Genetics, Inc. | Monomethylvaline compounds having phenylalanine side-chain modifications at the c-terminus |
| AU2006339058B2 (en) * | 2005-08-11 | 2012-09-06 | Targanta Therapeutics Inc. | Phosphonated rifamycins and uses thereof for the prevention and treatment of bone and joint infections |
| WO2007070613A2 (en) | 2005-12-14 | 2007-06-21 | Activbiotics, Incorporated | Rifamycin analogs and uses thereof |
| EP2144628B1 (en) | 2007-05-08 | 2012-10-17 | Genentech, Inc. | Cysteine engineered anti-muc16 antibodies and antibody drug conjugates |
| MY188455A (en) | 2007-10-19 | 2021-12-09 | Genentech Inc | Cysteine engineered anti-tenb2 antibodies and antibody drug conjugates |
| AU2009246510B2 (en) | 2008-05-12 | 2014-02-13 | Strox Biopharmaceuticals, Llc | Staphylococcus aureus-specific antibody preparations |
| WO2010019511A2 (en) | 2008-08-13 | 2010-02-18 | Targanta Therapeutics Corp. | Phosphonated rifamycins and uses thereof for the prevention and treatment of bone and joint infections |
| WO2010042481A1 (en) | 2008-10-06 | 2010-04-15 | University Of Chicago | Compositions and methods related to bacterial eap, emp, and/or adsa proteins |
| CA2745980C (en) * | 2008-12-10 | 2017-10-31 | Cipla Limited | Rifaximin complexes |
| WO2011008092A2 (en) * | 2009-07-15 | 2011-01-20 | Aimm Therapeutics B.V. | Gram-positive bacteria specific binding compounds |
| ES2531471T3 (es) | 2011-02-25 | 2015-03-16 | Lonza Ltd | Enlazador ramificado para conjugados de proteínas-fármacos |
| AU2012395148B2 (en) * | 2012-11-24 | 2016-10-27 | Hangzhou Dac Biotech Co., Ltd. | Hydrophilic linkers and their uses for conjugation of drugs to cell binding molecules |
| LT3004162T (lt) | 2013-05-31 | 2020-06-10 | Genentech, Inc. | Antikūnai prieš ląstelės sienelės teicho rūgštį ir konjugatai |
| EP3004161B1 (en) * | 2013-05-31 | 2019-10-02 | Genentech, Inc. | Anti-wall teichoic antibodies and conjugates |
| WO2015095227A2 (en) * | 2013-12-16 | 2015-06-25 | Genentech, Inc. | Peptidomimetic compounds and antibody-drug conjugates thereof |
| EA033456B1 (ru) * | 2013-12-16 | 2019-10-31 | Genentech Inc | Конъюгаты антитело-лекарственное средство, содержащие пептидомиметические линкеры |
-
2015
- 2015-12-02 EP EP15816304.8A patent/EP3226908A1/en not_active Withdrawn
- 2015-12-02 KR KR1020177015225A patent/KR20170086542A/ko unknown
- 2015-12-02 CA CA2966211A patent/CA2966211A1/en not_active Abandoned
- 2015-12-02 WO PCT/US2015/063515 patent/WO2016090040A1/en active Application Filing
- 2015-12-02 CN CN201580075250.4A patent/CN107249642A/zh active Pending
- 2015-12-02 RU RU2017118792A patent/RU2017118792A/ru not_active Application Discontinuation
- 2015-12-02 BR BR112017011478-0A patent/BR112017011478A2/pt not_active Application Discontinuation
- 2015-12-02 JP JP2017528877A patent/JP6751393B2/ja active Active
- 2015-12-02 MX MX2017007231A patent/MX2017007231A/es unknown
-
2017
- 2017-06-02 US US15/612,193 patent/US20180125995A1/en not_active Abandoned
-
2018
- 2018-03-19 HK HK18103816.6A patent/HK1244230A1/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| RU2017118792A (ru) | 2019-01-09 |
| RU2017118792A3 (ko) | 2019-06-14 |
| CN107249642A (zh) | 2017-10-13 |
| JP2018507166A (ja) | 2018-03-15 |
| WO2016090040A9 (en) | 2017-06-29 |
| US20180125995A1 (en) | 2018-05-10 |
| EP3226908A1 (en) | 2017-10-11 |
| HK1244230A1 (zh) | 2018-08-03 |
| CA2966211A1 (en) | 2016-06-09 |
| WO2016090040A1 (en) | 2016-06-09 |
| BR112017011478A2 (pt) | 2018-02-27 |
| MX2017007231A (es) | 2017-11-08 |
| JP6751393B2 (ja) | 2020-09-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6751393B2 (ja) | 抗staphylococcus aureus抗体リファマイシン抱合体及びその使用 | |
| US9895450B2 (en) | Anti-wall teichoic antibodies and conjugates | |
| RU2731055C2 (ru) | Конъюгаты антитела к staphylococcus aureus с рифамицином и их применение | |
| EP3004162B1 (en) | Anti-wall teichoic antibodies and conjugates | |
| US10570192B2 (en) | Anti-wall teichoic antibodies and conjugates | |
| TWI692483B (zh) | 抗壁磷壁酸抗體(anti-wall teichoic acid antibodies)及結合物 |