KR20160079072A - Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells - Google Patents
Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells Download PDFInfo
- Publication number
- KR20160079072A KR20160079072A KR1020167014409A KR20167014409A KR20160079072A KR 20160079072 A KR20160079072 A KR 20160079072A KR 1020167014409 A KR1020167014409 A KR 1020167014409A KR 20167014409 A KR20167014409 A KR 20167014409A KR 20160079072 A KR20160079072 A KR 20160079072A
- Authority
- KR
- South Korea
- Prior art keywords
- cells
- cell
- differentiation
- day
- expression
- Prior art date
Links
- 230000004069 differentiation Effects 0.000 title claims abstract description 240
- 210000001778 pluripotent stem cell Anatomy 0.000 title claims abstract description 98
- 239000000725 suspension Substances 0.000 title claims abstract description 62
- 230000009996 pancreatic endocrine effect Effects 0.000 title abstract description 20
- 210000003890 endocrine cell Anatomy 0.000 title abstract description 19
- 210000004027 cell Anatomy 0.000 claims abstract description 893
- 238000000034 method Methods 0.000 claims abstract description 105
- 210000000130 stem cell Anatomy 0.000 claims abstract description 79
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 claims abstract description 14
- 230000014509 gene expression Effects 0.000 claims description 262
- 238000004114 suspension culture Methods 0.000 claims description 86
- 210000001900 endoderm Anatomy 0.000 claims description 85
- 102100031650 C-X-C chemokine receptor type 4 Human genes 0.000 claims description 84
- 101000922348 Homo sapiens C-X-C chemokine receptor type 4 Proteins 0.000 claims description 84
- 210000001671 embryonic stem cell Anatomy 0.000 claims description 70
- 102100039939 Growth/differentiation factor 8 Human genes 0.000 claims description 67
- 101000886562 Homo sapiens Growth/differentiation factor 8 Proteins 0.000 claims description 46
- 101000578254 Homo sapiens Homeobox protein Nkx-6.1 Proteins 0.000 claims description 41
- 101000578258 Homo sapiens Homeobox protein Nkx-6.2 Proteins 0.000 claims description 40
- 101150068520 wnt3a gene Proteins 0.000 claims description 39
- 230000001965 increasing effect Effects 0.000 claims description 36
- 238000004115 adherent culture Methods 0.000 claims description 26
- 101710196692 Actin A Proteins 0.000 claims description 24
- 239000003590 rho kinase inhibitor Substances 0.000 claims description 24
- 238000012258 culturing Methods 0.000 claims description 23
- 108010056852 Myostatin Proteins 0.000 claims description 21
- 239000001301 oxygen Substances 0.000 claims description 19
- 229910052760 oxygen Inorganic materials 0.000 claims description 19
- 102000004190 Enzymes Human genes 0.000 claims description 18
- 108090000790 Enzymes Proteins 0.000 claims description 18
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 18
- 102000044880 Wnt3A Human genes 0.000 claims description 16
- 108700013515 Wnt3A Proteins 0.000 claims description 16
- 230000003321 amplification Effects 0.000 claims description 15
- 238000003199 nucleic acid amplification method Methods 0.000 claims description 15
- 102000040945 Transcription factor Human genes 0.000 claims description 13
- 108091023040 Transcription factor Proteins 0.000 claims description 13
- 239000002243 precursor Substances 0.000 claims description 13
- 230000022131 cell cycle Effects 0.000 claims description 12
- 239000003112 inhibitor Substances 0.000 claims description 12
- 239000002738 chelating agent Substances 0.000 claims description 11
- 108091003079 Bovine Serum Albumin Proteins 0.000 claims description 9
- 229940098773 bovine serum albumin Drugs 0.000 claims description 9
- 150000003384 small molecules Chemical class 0.000 claims description 7
- 210000003954 umbilical cord Anatomy 0.000 claims description 6
- 230000001939 inductive effect Effects 0.000 claims description 5
- 230000001464 adherent effect Effects 0.000 claims description 3
- 230000002107 myocardial effect Effects 0.000 claims description 3
- 102000043168 TGF-beta family Human genes 0.000 claims description 2
- 108091085018 TGF-beta family Proteins 0.000 claims description 2
- 150000002632 lipids Chemical class 0.000 claims description 2
- 230000035519 G0 Phase Effects 0.000 claims 2
- 230000010190 G1 phase Effects 0.000 claims 2
- 210000004962 mammalian cell Anatomy 0.000 claims 2
- 210000005155 neural progenitor cell Anatomy 0.000 claims 2
- 102100028096 Homeobox protein Nkx-6.2 Human genes 0.000 claims 1
- 238000004519 manufacturing process Methods 0.000 abstract description 17
- 230000001537 neural effect Effects 0.000 abstract description 6
- 210000002064 heart cell Anatomy 0.000 abstract description 5
- 239000002609 medium Substances 0.000 description 198
- 108090000623 proteins and genes Proteins 0.000 description 93
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 62
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 62
- 239000008103 glucose Substances 0.000 description 61
- 102100037904 CD9 antigen Human genes 0.000 description 58
- 101000738354 Homo sapiens CD9 antigen Proteins 0.000 description 58
- -1 NANOG Proteins 0.000 description 54
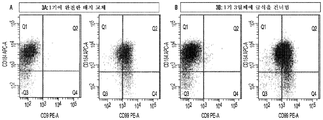
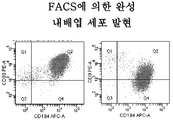
- 238000000684 flow cytometry Methods 0.000 description 45
- 102100041030 Pancreas/duodenum homeobox protein 1 Human genes 0.000 description 41
- 101710183548 Pyridoxal 5'-phosphate synthase subunit PdxS Proteins 0.000 description 41
- 210000001519 tissue Anatomy 0.000 description 41
- 102100028098 Homeobox protein Nkx-6.1 Human genes 0.000 description 40
- 102100035423 POU domain, class 5, transcription factor 1 Human genes 0.000 description 39
- 102100029284 Hepatocyte nuclear factor 3-beta Human genes 0.000 description 35
- 101001062347 Homo sapiens Hepatocyte nuclear factor 3-beta Proteins 0.000 description 35
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 33
- 239000000463 material Substances 0.000 description 31
- 239000012071 phase Substances 0.000 description 31
- 108010083123 CDX2 Transcription Factor Proteins 0.000 description 30
- 102100031671 Homeobox protein CDX-2 Human genes 0.000 description 30
- VOUAQYXWVJDEQY-QENPJCQMSA-N 33017-11-7 Chemical compound OC(=O)CC[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)NCC(=O)NCC(=O)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N1[C@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O)CCC1 VOUAQYXWVJDEQY-QENPJCQMSA-N 0.000 description 29
- 230000000977 initiatory effect Effects 0.000 description 29
- 239000000523 sample Substances 0.000 description 29
- 239000006285 cell suspension Substances 0.000 description 28
- 239000003550 marker Substances 0.000 description 28
- 230000015572 biosynthetic process Effects 0.000 description 27
- 239000011521 glass Substances 0.000 description 27
- 102000024905 CD99 Human genes 0.000 description 26
- 108060001253 CD99 Proteins 0.000 description 26
- 241001465754 Metazoa Species 0.000 description 26
- 101000652324 Homo sapiens Transcription factor SOX-17 Proteins 0.000 description 25
- 102100030243 Transcription factor SOX-17 Human genes 0.000 description 25
- 230000008569 process Effects 0.000 description 25
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 24
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 24
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 23
- 102100027886 Homeobox protein Nkx-2.2 Human genes 0.000 description 23
- 230000008859 change Effects 0.000 description 23
- 206010012601 diabetes mellitus Diseases 0.000 description 23
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 22
- 102100025745 Cerberus Human genes 0.000 description 22
- 241000202252 Cerberus Species 0.000 description 22
- 101100074833 Lotus japonicus CERBERUS gene Proteins 0.000 description 22
- 230000002354 daily effect Effects 0.000 description 22
- 101100518002 Danio rerio nkx2.2a gene Proteins 0.000 description 21
- 108700014808 Homeobox Protein Nkx-2.2 Proteins 0.000 description 21
- 101100460496 Homo sapiens NKX2-2 gene Proteins 0.000 description 21
- 101001094700 Homo sapiens POU domain, class 5, transcription factor 1 Proteins 0.000 description 21
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 21
- 238000011081 inoculation Methods 0.000 description 21
- 108010075254 C-Peptide Proteins 0.000 description 20
- 238000007792 addition Methods 0.000 description 20
- 102100028072 Fibroblast growth factor 4 Human genes 0.000 description 19
- 101001060274 Homo sapiens Fibroblast growth factor 4 Proteins 0.000 description 19
- 101000819074 Homo sapiens Transcription factor GATA-4 Proteins 0.000 description 19
- 101000819088 Homo sapiens Transcription factor GATA-6 Proteins 0.000 description 19
- 102100032063 Neurogenic differentiation factor 1 Human genes 0.000 description 19
- 102100021380 Transcription factor GATA-4 Human genes 0.000 description 19
- 102100021382 Transcription factor GATA-6 Human genes 0.000 description 19
- 239000000243 solution Substances 0.000 description 19
- 238000002054 transplantation Methods 0.000 description 19
- 101710126211 POU domain, class 5, transcription factor 1 Proteins 0.000 description 18
- 210000000496 pancreas Anatomy 0.000 description 18
- 101710123134 Ice-binding protein Proteins 0.000 description 17
- 101710082837 Ice-structuring protein Proteins 0.000 description 17
- 101710107540 Type-2 ice-structuring protein Proteins 0.000 description 17
- 239000011324 bead Substances 0.000 description 17
- 229940088598 enzyme Drugs 0.000 description 17
- 239000007788 liquid Substances 0.000 description 17
- 102100035308 Fibroblast growth factor 17 Human genes 0.000 description 16
- 102100024208 Homeobox protein MIXL1 Human genes 0.000 description 16
- 102100038146 Homeobox protein goosecoid Human genes 0.000 description 16
- 101000878124 Homo sapiens Fibroblast growth factor 17 Proteins 0.000 description 16
- 101001052462 Homo sapiens Homeobox protein MIXL1 Proteins 0.000 description 16
- 101001032602 Homo sapiens Homeobox protein goosecoid Proteins 0.000 description 16
- 241000699670 Mus sp. Species 0.000 description 16
- 102100034593 Tripartite motif-containing protein 26 Human genes 0.000 description 16
- 229910002091 carbon monoxide Inorganic materials 0.000 description 16
- 239000001963 growth medium Substances 0.000 description 16
- 230000006698 induction Effects 0.000 description 16
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 16
- 101150079937 NEUROD1 gene Proteins 0.000 description 15
- 230000000694 effects Effects 0.000 description 15
- 239000010410 layer Substances 0.000 description 15
- 239000002953 phosphate buffered saline Substances 0.000 description 15
- 101001002317 Homo sapiens Gastrin Proteins 0.000 description 14
- 101000576323 Homo sapiens Motor neuron and pancreas homeobox protein 1 Proteins 0.000 description 14
- 102100025170 Motor neuron and pancreas homeobox protein 1 Human genes 0.000 description 14
- 108010032788 PAX6 Transcription Factor Proteins 0.000 description 14
- 102100037506 Paired box protein Pax-6 Human genes 0.000 description 14
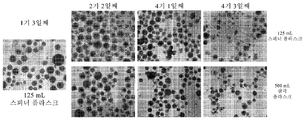
- 238000001000 micrograph Methods 0.000 description 14
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 14
- HJCMDXDYPOUFDY-WHFBIAKZSA-N Ala-Gln Chemical compound C[C@H](N)C(=O)N[C@H](C(O)=O)CCC(N)=O HJCMDXDYPOUFDY-WHFBIAKZSA-N 0.000 description 13
- 210000004263 induced pluripotent stem cell Anatomy 0.000 description 13
- 239000000047 product Substances 0.000 description 13
- 230000002829 reductive effect Effects 0.000 description 13
- 150000001875 compounds Chemical class 0.000 description 12
- 108010007718 Chromogranins Proteins 0.000 description 11
- 102000007345 Chromogranins Human genes 0.000 description 11
- 101000923091 Danio rerio Aristaless-related homeobox protein Proteins 0.000 description 11
- 102100031470 Homeobox protein ARX Human genes 0.000 description 11
- 101000923090 Homo sapiens Homeobox protein ARX Proteins 0.000 description 11
- 101000613495 Homo sapiens Paired box protein Pax-4 Proteins 0.000 description 11
- 102100040909 Paired box protein Pax-4 Human genes 0.000 description 11
- ZSJLQEPLLKMAKR-UHFFFAOYSA-N Streptozotocin Natural products O=NN(C)C(=O)NC1C(O)OC(CO)C(O)C1O ZSJLQEPLLKMAKR-UHFFFAOYSA-N 0.000 description 11
- 238000003491 array Methods 0.000 description 11
- 238000011534 incubation Methods 0.000 description 11
- 229910052757 nitrogen Inorganic materials 0.000 description 11
- 229960001052 streptozocin Drugs 0.000 description 11
- 102100030751 Eomesodermin homolog Human genes 0.000 description 10
- 101001064167 Homo sapiens Eomesodermin homolog Proteins 0.000 description 10
- 101000976075 Homo sapiens Insulin Proteins 0.000 description 10
- 101000603702 Homo sapiens Neurogenin-3 Proteins 0.000 description 10
- 102100023915 Insulin Human genes 0.000 description 10
- 102100038553 Neurogenin-3 Human genes 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 239000008280 blood Substances 0.000 description 10
- 238000004113 cell culture Methods 0.000 description 10
- 230000002596 correlated effect Effects 0.000 description 10
- 230000002572 peristaltic effect Effects 0.000 description 10
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 10
- 235000017557 sodium bicarbonate Nutrition 0.000 description 10
- 102100028071 Fibroblast growth factor 7 Human genes 0.000 description 9
- 101001060261 Homo sapiens Fibroblast growth factor 7 Proteins 0.000 description 9
- 101001053263 Homo sapiens Insulin gene enhancer protein ISL-1 Proteins 0.000 description 9
- 102100024392 Insulin gene enhancer protein ISL-1 Human genes 0.000 description 9
- 241000699666 Mus <mouse, genus> Species 0.000 description 9
- 108700020297 NeuroD Proteins 0.000 description 9
- 238000013019 agitation Methods 0.000 description 9
- 108010007093 dispase Proteins 0.000 description 9
- 238000010494 dissociation reaction Methods 0.000 description 9
- 230000005593 dissociations Effects 0.000 description 9
- 238000005516 engineering process Methods 0.000 description 9
- 239000012737 fresh medium Substances 0.000 description 9
- 238000001727 in vivo Methods 0.000 description 9
- 239000008188 pellet Substances 0.000 description 9
- 238000012546 transfer Methods 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 108010035532 Collagen Proteins 0.000 description 8
- 102000008186 Collagen Human genes 0.000 description 8
- 101000738523 Homo sapiens Pancreas transcription factor 1 subunit alpha Proteins 0.000 description 8
- 102000004877 Insulin Human genes 0.000 description 8
- 108090001061 Insulin Proteins 0.000 description 8
- 102100037878 Pancreas transcription factor 1 subunit alpha Human genes 0.000 description 8
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 8
- 239000002775 capsule Substances 0.000 description 8
- 229920001436 collagen Polymers 0.000 description 8
- 230000003247 decreasing effect Effects 0.000 description 8
- 210000004039 endoderm cell Anatomy 0.000 description 8
- 229940125396 insulin Drugs 0.000 description 8
- 229930002330 retinoic acid Natural products 0.000 description 8
- 238000003757 reverse transcription PCR Methods 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- 239000000758 substrate Substances 0.000 description 8
- 239000012591 Dulbecco’s Phosphate Buffered Saline Substances 0.000 description 7
- 101001021503 Homo sapiens Hematopoietically-expressed homeobox protein HHEX Proteins 0.000 description 7
- 101001069749 Homo sapiens Prospero homeobox protein 1 Proteins 0.000 description 7
- 101000976622 Homo sapiens Zinc finger protein 42 homolog Proteins 0.000 description 7
- 102100033880 Prospero homeobox protein 1 Human genes 0.000 description 7
- 102100023550 Zinc finger protein 42 homolog Human genes 0.000 description 7
- 239000007640 basal medium Substances 0.000 description 7
- 230000024245 cell differentiation Effects 0.000 description 7
- 239000007789 gas Substances 0.000 description 7
- 239000003102 growth factor Substances 0.000 description 7
- 210000003716 mesoderm Anatomy 0.000 description 7
- 239000002777 nucleoside Substances 0.000 description 7
- OZFAFGSSMRRTDW-UHFFFAOYSA-N (2,4-dichlorophenyl) benzenesulfonate Chemical compound ClC1=CC(Cl)=CC=C1OS(=O)(=O)C1=CC=CC=C1 OZFAFGSSMRRTDW-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- 102100035961 Hematopoietically-expressed homeobox protein HHEX Human genes 0.000 description 6
- 102100024894 PR domain zinc finger protein 1 Human genes 0.000 description 6
- 108010009975 Positive Regulatory Domain I-Binding Factor 1 Proteins 0.000 description 6
- 238000011161 development Methods 0.000 description 6
- 230000018109 developmental process Effects 0.000 description 6
- 230000002124 endocrine Effects 0.000 description 6
- 210000001035 gastrointestinal tract Anatomy 0.000 description 6
- 238000010348 incorporation Methods 0.000 description 6
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 6
- 238000013411 master cell bank Methods 0.000 description 6
- 108010082117 matrigel Proteins 0.000 description 6
- 230000035800 maturation Effects 0.000 description 6
- 108020004999 messenger RNA Proteins 0.000 description 6
- 150000003833 nucleoside derivatives Chemical class 0.000 description 6
- 239000004033 plastic Substances 0.000 description 6
- 229920003023 plastic Polymers 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 239000006228 supernatant Substances 0.000 description 6
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 5
- 102100036364 Cadherin-2 Human genes 0.000 description 5
- 108060005980 Collagenase Proteins 0.000 description 5
- 102000029816 Collagenase Human genes 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 5
- 102100031785 Endothelial transcription factor GATA-2 Human genes 0.000 description 5
- 102100021022 Gastrin Human genes 0.000 description 5
- 101150068639 Hnf4a gene Proteins 0.000 description 5
- 101000714537 Homo sapiens Cadherin-2 Proteins 0.000 description 5
- 101001066265 Homo sapiens Endothelial transcription factor GATA-2 Proteins 0.000 description 5
- 101000979190 Homo sapiens Transcription factor MafB Proteins 0.000 description 5
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 5
- 102000035195 Peptidases Human genes 0.000 description 5
- 108091005804 Peptidases Proteins 0.000 description 5
- 102100023234 Transcription factor MafB Human genes 0.000 description 5
- 101150045640 VWF gene Proteins 0.000 description 5
- 238000005119 centrifugation Methods 0.000 description 5
- 229960002424 collagenase Drugs 0.000 description 5
- 239000012634 fragment Substances 0.000 description 5
- 238000000338 in vitro Methods 0.000 description 5
- 210000003734 kidney Anatomy 0.000 description 5
- 210000004072 lung Anatomy 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 210000002966 serum Anatomy 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 238000010257 thawing Methods 0.000 description 5
- 229960001727 tretinoin Drugs 0.000 description 5
- 102100036537 von Willebrand factor Human genes 0.000 description 5
- CDOVNWNANFFLFJ-UHFFFAOYSA-N 4-[6-[4-(1-piperazinyl)phenyl]-3-pyrazolo[1,5-a]pyrimidinyl]quinoline Chemical compound C1CNCCN1C1=CC=C(C2=CN3N=CC(=C3N=C2)C=2C3=CC=CC=C3N=CC=2)C=C1 CDOVNWNANFFLFJ-UHFFFAOYSA-N 0.000 description 4
- 102100022054 Hepatocyte nuclear factor 4-alpha Human genes 0.000 description 4
- 102100030634 Homeobox protein OTX2 Human genes 0.000 description 4
- 101001045740 Homo sapiens Hepatocyte nuclear factor 4-alpha Proteins 0.000 description 4
- 101000584400 Homo sapiens Homeobox protein OTX2 Proteins 0.000 description 4
- 101000642523 Homo sapiens Transcription factor SOX-7 Proteins 0.000 description 4
- 101000711846 Homo sapiens Transcription factor SOX-9 Proteins 0.000 description 4
- 108050000588 Neurogenic differentiation factor 1 Proteins 0.000 description 4
- 102000035092 Neutral proteases Human genes 0.000 description 4
- 108091005507 Neutral proteases Proteins 0.000 description 4
- 238000010222 PCR analysis Methods 0.000 description 4
- 239000004793 Polystyrene Substances 0.000 description 4
- 102100036730 Transcription factor SOX-7 Human genes 0.000 description 4
- 102100034204 Transcription factor SOX-9 Human genes 0.000 description 4
- 238000004364 calculation method Methods 0.000 description 4
- 238000012512 characterization method Methods 0.000 description 4
- 238000005138 cryopreservation Methods 0.000 description 4
- 239000013530 defoamer Substances 0.000 description 4
- 238000003795 desorption Methods 0.000 description 4
- 210000003981 ectoderm Anatomy 0.000 description 4
- 230000005684 electric field Effects 0.000 description 4
- 230000002255 enzymatic effect Effects 0.000 description 4
- 230000000968 intestinal effect Effects 0.000 description 4
- 238000002955 isolation Methods 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 238000010899 nucleation Methods 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- 229920002223 polystyrene Polymers 0.000 description 4
- 238000012809 post-inoculation Methods 0.000 description 4
- 238000010079 rubber tapping Methods 0.000 description 4
- 230000003248 secreting effect Effects 0.000 description 4
- 239000002699 waste material Substances 0.000 description 4
- 102100027211 Albumin Human genes 0.000 description 3
- 108090000145 Bacillolysin Proteins 0.000 description 3
- 102000001893 Bone Morphogenetic Protein Receptors Human genes 0.000 description 3
- 108010040422 Bone Morphogenetic Protein Receptors Proteins 0.000 description 3
- 108091007854 Cdh1/Fizzy-related Proteins 0.000 description 3
- 102000038594 Cdh1/Fizzy-related Human genes 0.000 description 3
- 229920002307 Dextran Polymers 0.000 description 3
- 102100037060 Forkhead box protein D3 Human genes 0.000 description 3
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 3
- 102100023855 Heart- and neural crest derivatives-expressed protein 1 Human genes 0.000 description 3
- 101001029308 Homo sapiens Forkhead box protein D3 Proteins 0.000 description 3
- 101000905239 Homo sapiens Heart- and neural crest derivatives-expressed protein 1 Proteins 0.000 description 3
- 101000598781 Homo sapiens Oxidative stress-responsive serine-rich protein 1 Proteins 0.000 description 3
- 101000613717 Homo sapiens Protein odd-skipped-related 1 Proteins 0.000 description 3
- 101001098464 Homo sapiens Serine/threonine-protein kinase OSR1 Proteins 0.000 description 3
- 101000701142 Homo sapiens Transcription factor ATOH1 Proteins 0.000 description 3
- 102000036770 Islet Amyloid Polypeptide Human genes 0.000 description 3
- 108010041872 Islet Amyloid Polypeptide Proteins 0.000 description 3
- 102100040551 Protein odd-skipped-related 1 Human genes 0.000 description 3
- 230000018199 S phase Effects 0.000 description 3
- 102000004874 Synaptophysin Human genes 0.000 description 3
- 108090001076 Synaptophysin Proteins 0.000 description 3
- 102100029373 Transcription factor ATOH1 Human genes 0.000 description 3
- 108010076089 accutase Proteins 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 239000012190 activator Substances 0.000 description 3
- 108010023082 activin A Proteins 0.000 description 3
- 230000000735 allogeneic effect Effects 0.000 description 3
- PLOPBXQQPZYQFA-AXPWDRQUSA-N amlintide Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H]1NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CCCCN)CSSC1)[C@@H](C)O)C(C)C)C1=CC=CC=C1 PLOPBXQQPZYQFA-AXPWDRQUSA-N 0.000 description 3
- 238000010171 animal model Methods 0.000 description 3
- 238000002659 cell therapy Methods 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 210000000349 chromosome Anatomy 0.000 description 3
- 239000000306 component Substances 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 238000005538 encapsulation Methods 0.000 description 3
- 230000007515 enzymatic degradation Effects 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 239000012595 freezing medium Substances 0.000 description 3
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 3
- 238000000227 grinding Methods 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- 229940088597 hormone Drugs 0.000 description 3
- 239000005556 hormone Substances 0.000 description 3
- 210000004153 islets of langerhan Anatomy 0.000 description 3
- 239000004310 lactic acid Substances 0.000 description 3
- 235000014655 lactic acid Nutrition 0.000 description 3
- 210000004185 liver Anatomy 0.000 description 3
- 235000015097 nutrients Nutrition 0.000 description 3
- 230000015031 pancreas development Effects 0.000 description 3
- 238000002135 phase contrast microscopy Methods 0.000 description 3
- 230000035935 pregnancy Effects 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 230000002062 proliferating effect Effects 0.000 description 3
- 230000000717 retained effect Effects 0.000 description 3
- 239000002356 single layer Substances 0.000 description 3
- 239000010935 stainless steel Substances 0.000 description 3
- 229910001220 stainless steel Inorganic materials 0.000 description 3
- 230000003068 static effect Effects 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- WOLVEMPZUIFSII-IHHOKICGSA-N (2e,4e)-n-[(2s,5s)-5-(hydroxymethyl)-1-methyl-3-oxo-2-propan-2-yl-2,4,5,6-tetrahydro-1,4-benzodiazocin-8-yl]-5-[4-(trifluoromethyl)phenyl]penta-2,4-dienamide Chemical compound CN([C@H](C(N[C@H](CO)CC1=C2)=O)C(C)C)C1=CC=C2NC(=O)\C=C\C=C\C1=CC=C(C(F)(F)F)C=C1 WOLVEMPZUIFSII-IHHOKICGSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- 101100046776 Arabidopsis thaliana TPPB gene Proteins 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 108010051975 Glycogen Synthase Kinase 3 beta Proteins 0.000 description 2
- 102100038104 Glycogen synthase kinase-3 beta Human genes 0.000 description 2
- 108700031316 Goosecoid Proteins 0.000 description 2
- 102000050057 Goosecoid Human genes 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- 101000632186 Homo sapiens Homeobox protein Nkx-2.2 Proteins 0.000 description 2
- 101000581981 Homo sapiens Neural cell adhesion molecule 1 Proteins 0.000 description 2
- 208000004454 Hyperalgesia Diseases 0.000 description 2
- 108010085895 Laminin Proteins 0.000 description 2
- 102000007547 Laminin Human genes 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 102100027347 Neural cell adhesion molecule 1 Human genes 0.000 description 2
- 102100026844 Pancreatic prohormone Human genes 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 2
- 102000004243 Tubulin Human genes 0.000 description 2
- 108090000704 Tubulin Proteins 0.000 description 2
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 2
- 102000013814 Wnt Human genes 0.000 description 2
- 108050003627 Wnt Proteins 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 206010053552 allodynia Diseases 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 210000002459 blastocyst Anatomy 0.000 description 2
- 125000001246 bromo group Chemical group Br* 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 230000003833 cell viability Effects 0.000 description 2
- 230000019522 cellular metabolic process Effects 0.000 description 2
- 230000004186 co-expression Effects 0.000 description 2
- 230000001143 conditioned effect Effects 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 229920001971 elastomer Polymers 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 210000001654 germ layer Anatomy 0.000 description 2
- 201000001421 hyperglycemia Diseases 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 238000002513 implantation Methods 0.000 description 2
- 238000007901 in situ hybridization Methods 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 239000002054 inoculum Substances 0.000 description 2
- 230000033001 locomotion Effects 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 239000012092 media component Substances 0.000 description 2
- 230000002503 metabolic effect Effects 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 230000004660 morphological change Effects 0.000 description 2
- 210000002569 neuron Anatomy 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 150000007523 nucleic acids Chemical class 0.000 description 2
- 230000002018 overexpression Effects 0.000 description 2
- 210000004923 pancreatic tissue Anatomy 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 239000002464 receptor antagonist Substances 0.000 description 2
- 229940044551 receptor antagonist Drugs 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 235000015170 shellfish Nutrition 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 239000010703 silicon Substances 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 210000001082 somatic cell Anatomy 0.000 description 2
- 230000010473 stable expression Effects 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 210000002784 stomach Anatomy 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 210000001685 thyroid gland Anatomy 0.000 description 2
- 230000001052 transient effect Effects 0.000 description 2
- 230000035899 viability Effects 0.000 description 2
- KEQXNNJHMWSZHK-UHFFFAOYSA-L 1,3,2,4$l^{2}-dioxathiaplumbetane 2,2-dioxide Chemical compound [Pb+2].[O-]S([O-])(=O)=O KEQXNNJHMWSZHK-UHFFFAOYSA-L 0.000 description 1
- ZOOGRGPOEVQQDX-UUOKFMHZSA-N 3',5'-cyclic GMP Chemical compound C([C@H]1O2)OP(O)(=O)O[C@H]1[C@@H](O)[C@@H]2N1C(N=C(NC2=O)N)=C2N=C1 ZOOGRGPOEVQQDX-UUOKFMHZSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- HFDKKNHCYWNNNQ-YOGANYHLSA-N 75976-10-2 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@@H](NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](C)N)C(C)C)[C@@H](C)O)C1=CC=C(O)C=C1 HFDKKNHCYWNNNQ-YOGANYHLSA-N 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 238000012935 Averaging Methods 0.000 description 1
- 239000012583 B-27 Supplement Substances 0.000 description 1
- 241000167854 Bourreria succulenta Species 0.000 description 1
- 101710010675 Cerberus Proteins 0.000 description 1
- 241001463014 Chazara briseis Species 0.000 description 1
- 206010010099 Combined immunodeficiency Diseases 0.000 description 1
- 108010069241 Connexin 43 Proteins 0.000 description 1
- 102000001045 Connexin 43 Human genes 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 102000016942 Elastin Human genes 0.000 description 1
- 102100028412 Fibroblast growth factor 10 Human genes 0.000 description 1
- 102100037362 Fibronectin Human genes 0.000 description 1
- 108010067306 Fibronectins Proteins 0.000 description 1
- 230000010337 G2 phase Effects 0.000 description 1
- 102100039290 Gap junction gamma-1 protein Human genes 0.000 description 1
- 101800001586 Ghrelin Proteins 0.000 description 1
- 102000012004 Ghrelin Human genes 0.000 description 1
- 102400000321 Glucagon Human genes 0.000 description 1
- 108060003199 Glucagon Proteins 0.000 description 1
- 108010087745 Hepatocyte Nuclear Factor 3-beta Proteins 0.000 description 1
- 102000009094 Hepatocyte Nuclear Factor 3-beta Human genes 0.000 description 1
- 108700005087 Homeobox Genes Proteins 0.000 description 1
- 102100031672 Homeobox protein CDX-1 Human genes 0.000 description 1
- 101000693913 Homo sapiens Albumin Proteins 0.000 description 1
- 101001065295 Homo sapiens Fas-binding factor 1 Proteins 0.000 description 1
- 101000917237 Homo sapiens Fibroblast growth factor 10 Proteins 0.000 description 1
- 101000777808 Homo sapiens Homeobox protein CDX-1 Proteins 0.000 description 1
- 101001139134 Homo sapiens Krueppel-like factor 4 Proteins 0.000 description 1
- 101001128694 Homo sapiens Neuroendocrine convertase 1 Proteins 0.000 description 1
- 101000589873 Homo sapiens Parathyroid hormone/parathyroid hormone-related peptide receptor Proteins 0.000 description 1
- 101000835745 Homo sapiens Teratocarcinoma-derived growth factor 1 Proteins 0.000 description 1
- 101000638154 Homo sapiens Transmembrane protease serine 2 Proteins 0.000 description 1
- 101000777245 Homo sapiens Undifferentiated embryonic cell transcription factor 1 Proteins 0.000 description 1
- 101000976653 Homo sapiens Zinc finger protein ZIC 1 Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- YZCKVEUIGOORGS-UHFFFAOYSA-N Hydrogen atom Chemical class [H] YZCKVEUIGOORGS-UHFFFAOYSA-N 0.000 description 1
- 102100020677 Krueppel-like factor 4 Human genes 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 102100027754 Mast/stem cell growth factor receptor Kit Human genes 0.000 description 1
- 102000013013 Member 2 Subfamily G ATP Binding Cassette Transporter Human genes 0.000 description 1
- 108010090306 Member 2 Subfamily G ATP Binding Cassette Transporter Proteins 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 229920002274 Nalgene Polymers 0.000 description 1
- 102100032132 Neuroendocrine convertase 1 Human genes 0.000 description 1
- 102000052651 Pancreatic hormone Human genes 0.000 description 1
- 101800001268 Pancreatic hormone Proteins 0.000 description 1
- 102100032256 Parathyroid hormone/parathyroid hormone-related peptide receptor Human genes 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 101100247004 Rattus norvegicus Qsox1 gene Proteins 0.000 description 1
- 229920002385 Sodium hyaluronate Polymers 0.000 description 1
- 108010056088 Somatostatin Proteins 0.000 description 1
- 102000005157 Somatostatin Human genes 0.000 description 1
- 101000983124 Sus scrofa Pancreatic prohormone precursor Proteins 0.000 description 1
- 108091005735 TGF-beta receptors Proteins 0.000 description 1
- 102100026404 Teratocarcinoma-derived growth factor 1 Human genes 0.000 description 1
- 206010043276 Teratoma Diseases 0.000 description 1
- 102000016715 Transforming Growth Factor beta Receptors Human genes 0.000 description 1
- 102100031989 Transmembrane protease serine 2 Human genes 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 102100031278 Undifferentiated embryonic cell transcription factor 1 Human genes 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 102100023497 Zinc finger protein ZIC 1 Human genes 0.000 description 1
- 238000010306 acid treatment Methods 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 230000004520 agglutination Effects 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 210000004381 amniotic fluid Anatomy 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 239000002518 antifoaming agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 208000036815 beta tubulin Diseases 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000000648 calcium alginate Substances 0.000 description 1
- 235000010410 calcium alginate Nutrition 0.000 description 1
- 229960002681 calcium alginate Drugs 0.000 description 1
- OKHHGHGGPDJQHR-YMOPUZKJSA-L calcium;(2s,3s,4s,5s,6r)-6-[(2r,3s,4r,5s,6r)-2-carboxy-6-[(2r,3s,4r,5s,6r)-2-carboxylato-4,5,6-trihydroxyoxan-3-yl]oxy-4,5-dihydroxyoxan-3-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylate Chemical compound [Ca+2].O[C@@H]1[C@H](O)[C@H](O)O[C@@H](C([O-])=O)[C@H]1O[C@H]1[C@@H](O)[C@@H](O)[C@H](O[C@H]2[C@H]([C@@H](O)[C@H](O)[C@H](O2)C([O-])=O)O)[C@H](C(O)=O)O1 OKHHGHGGPDJQHR-YMOPUZKJSA-L 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000032823 cell division Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 239000002771 cell marker Substances 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 235000019693 cherries Nutrition 0.000 description 1
- 235000019504 cigarettes Nutrition 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000003636 conditioned culture medium Substances 0.000 description 1
- 108010015426 connexin 45 Proteins 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 230000000875 corresponding effect Effects 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 230000037416 cystogenesis Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 230000002900 effect on cell Effects 0.000 description 1
- 229920002549 elastin Polymers 0.000 description 1
- 238000005485 electric heating Methods 0.000 description 1
- 230000005611 electricity Effects 0.000 description 1
- 230000013020 embryo development Effects 0.000 description 1
- 210000002242 embryoid body Anatomy 0.000 description 1
- 230000002357 endometrial effect Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 235000013861 fat-free Nutrition 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 210000001647 gastrula Anatomy 0.000 description 1
- 230000007045 gastrulation Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- GNKDKYIHGQKHHM-RJKLHVOGSA-N ghrelin Chemical compound C([C@H](NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)CN)COC(=O)CCCCCCC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C1=CC=CC=C1 GNKDKYIHGQKHHM-RJKLHVOGSA-N 0.000 description 1
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 1
- 229960004666 glucagon Drugs 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- 210000005003 heart tissue Anatomy 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 230000002962 histologic effect Effects 0.000 description 1
- 210000003917 human chromosome Anatomy 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 230000008105 immune reaction Effects 0.000 description 1
- 238000012744 immunostaining Methods 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000003914 insulin secretion Effects 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- OGQSCIYDJSNCMY-UHFFFAOYSA-H iron(3+);methyl-dioxido-oxo-$l^{5}-arsane Chemical compound [Fe+3].[Fe+3].C[As]([O-])([O-])=O.C[As]([O-])([O-])=O.C[As]([O-])([O-])=O OGQSCIYDJSNCMY-UHFFFAOYSA-H 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 239000012533 medium component Substances 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 230000011278 mitosis Effects 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 230000009753 muscle formation Effects 0.000 description 1
- QNILTEGFHQSKFF-UHFFFAOYSA-N n-propan-2-ylprop-2-enamide Chemical compound CC(C)NC(=O)C=C QNILTEGFHQSKFF-UHFFFAOYSA-N 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 210000001178 neural stem cell Anatomy 0.000 description 1
- 235000020925 non fasting Nutrition 0.000 description 1
- 239000004025 pancreas hormone Substances 0.000 description 1
- 210000003577 pancreatic endocrine progenitor Anatomy 0.000 description 1
- 229940032957 pancreatic hormone Drugs 0.000 description 1
- 230000005298 paramagnetic effect Effects 0.000 description 1
- 239000002907 paramagnetic material Substances 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 210000004303 peritoneum Anatomy 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 210000002826 placenta Anatomy 0.000 description 1
- 210000005059 placental tissue Anatomy 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 229920005644 polyethylene terephthalate glycol copolymer Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000007542 postnatal development Effects 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- LDIJKUBTLZTFRG-UHFFFAOYSA-N pyrazolo[1,5-a]pyrimidine Chemical compound N1=CC=CN2N=CC=C21 LDIJKUBTLZTFRG-UHFFFAOYSA-N 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 238000009256 replacement therapy Methods 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 239000004017 serum-free culture medium Substances 0.000 description 1
- 208000002491 severe combined immunodeficiency Diseases 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 229940010747 sodium hyaluronate Drugs 0.000 description 1
- YWIVKILSMZOHHF-QJZPQSOGSA-N sodium;(2s,3s,4s,5r,6r)-6-[(2s,3r,4r,5s,6r)-3-acetamido-2-[(2s,3s,4r,5r,6r)-6-[(2r,3r,4r,5s,6r)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2- Chemical compound [Na+].CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 YWIVKILSMZOHHF-QJZPQSOGSA-N 0.000 description 1
- NHXLMOGPVYXJNR-ATOGVRKGSA-N somatostatin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CSSC[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N1)[C@@H](C)O)NC(=O)CNC(=O)[C@H](C)N)C(O)=O)=O)[C@H](O)C)C1=CC=CC=C1 NHXLMOGPVYXJNR-ATOGVRKGSA-N 0.000 description 1
- 229960000553 somatostatin Drugs 0.000 description 1
- 210000000273 spinal nerve root Anatomy 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 210000000701 subdural space Anatomy 0.000 description 1
- 239000001384 succinic acid Substances 0.000 description 1
- 229920002994 synthetic fiber Polymers 0.000 description 1
- 210000001541 thymus gland Anatomy 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 1
- 210000002993 trophoblast Anatomy 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 239000012808 vapor phase Substances 0.000 description 1
- 238000003260 vortexing Methods 0.000 description 1
- 238000003466 welding Methods 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0676—Pancreatic cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/0068—General culture methods using substrates
- C12N5/0075—General culture methods using substrates using microcarriers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0603—Embryonic cells ; Embryoid bodies
- C12N5/0606—Pluripotent embryonic cells, e.g. embryonic stem cells [ES]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0618—Cells of the nervous system
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0657—Cardiomyocytes; Heart cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/02—Atmosphere, e.g. low oxygen conditions
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/117—Keratinocyte growth factors (KGF-1, i.e. FGF-7; KGF-2, i.e. FGF-12)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/15—Transforming growth factor beta (TGF-β)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/155—Bone morphogenic proteins [BMP]; Osteogenins; Osteogenic factor; Bone inducing factor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/16—Activin; Inhibin; Mullerian inhibiting substance
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/19—Growth and differentiation factors [GDF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/30—Hormones
- C12N2501/38—Hormones with nuclear receptors
- C12N2501/385—Hormones with nuclear receptors of the family of the retinoic acid recptor, e.g. RAR, RXR; Peroxisome proliferator-activated receptor [PPAR]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/41—Hedgehog proteins; Cyclopamine (inhibitor)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/415—Wnt; Frizzeled
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/42—Notch; Delta; Jagged; Serrate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/70—Enzymes
- C12N2501/72—Transferases [EC 2.]
- C12N2501/727—Kinases (EC 2.7.)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/999—Small molecules not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/02—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from embryonic cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/45—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from artificially induced pluripotent stem cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2509/00—Methods for the dissociation of cells, e.g. specific use of enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2513/00—3D culture
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2531/00—Microcarriers
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Developmental Biology & Embryology (AREA)
- Gynecology & Obstetrics (AREA)
- Reproductive Health (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Cardiology (AREA)
- Rheumatology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Heart & Thoracic Surgery (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Plural Heterocyclic Compounds (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
본 발명은 내배엽 선조세포, 췌장 내분비 세포, 중배엽 세포 또는 외배엽 세포로의 분화를 위한 응집된 만능 줄기세포 클러스터를 제조하는 방법을 제공한다. 구체적으로, 본 발명은 현탁 클러스터링을 사용하여 만능 세포를 베타 세포, 심장 세포 및 신경 세포 계통으로 분화시키는 방법을 개시한다. 본 방법은 응집된 세포 클러스터를 제조하는 단계에 이어서 상기 클러스터를 분화시키는 단계를 포함한다. The present invention provides a method for producing aggregated pluripotent stem cell clusters for differentiation into endodermal progenitor cells, pancreatic endocrine cells, mesodermal cells or ectodermal cells. Specifically, the present invention discloses a method of differentiating pluripotent cells into beta cells, cardiac cells and neuronal lineage using suspension clustering. The method includes the step of producing an aggregated cell cluster followed by the step of differentiating the cluster.
Description
관련 출원과의 상호참조Cross reference to related application
본 출원은 미국 특허 출원 제13/998,974호(2013년 12월 30일에 출원됨)의 일부 계속 출원으로, 이는 미국 가출원 제61/747,799호(2012년 12월 31일에 출원됨) 및 미국 가출원 제61/962,158호(2013년 11월 1일에 출원됨)에 대한 우선권을 주장하며, 이들은 전체적으로 참고로 포함된다.This application is a continuation-in-part of U.S. Provisional Application No. 13 / 998,974, filed December 30, 2013, which is incorporated herein by reference in its entirety to U.S. Provisional Application No. 61 / 747,799 (filed December 31, 2012) 61 / 962,158 (filed November 1, 2013), which are incorporated by reference in their entirety.
본 발명은 내배엽 선조세포(endoderm progenitor cell), 췌장 내분비 세포, 중배엽 세포 또는 외배엽 세포로의 분화를 위한 응집된 세포 클러스터에서 만능성을 유지하는 배아줄기세포 및 다른 만능 세포를 제조함을 포함하는 세포 분화의 분야에 관한 것이다. 일 태양에서, 본 발명은 만능 줄기세포의 클러스터를 생성하고 이들을 췌장 내배엽, 췌장 내분비 전구세포(precursor cell), 및 단일-호르몬 췌장 내분비 세포로의 분화를 위하여 현탁 배양물 중에 유지하는 방법을 개시하고 있다.The present invention relates to a method for producing embryonic stem cells and other pluripotent cells which maintain pluripotency in aggregated cell clusters for differentiation into endoderm progenitor cells, pancreatic endocrine cells, mesoderm or ectodermal cells, To the field of differentiation. In one aspect, the invention discloses a method for producing clusters of pluripotent stem cells and maintaining them in suspension culture for differentiation into pancreatic endoderm, pancreatic endocrine precursor cells, and single-hormone pancreatic endocrine cells have.
제I형 진성 당뇨병 및 이식가능한 랑게르한스섬의 부족에 대한 세포-대체 요법에서의 진전은 생착(engraftment)에 적절한 인슐린-생성 세포, 또는 β 세포의 공급원을 개발하는 데 관심이 집중되어 왔다. 한 가지 접근법은 배아줄기세포와 같은 만능 줄기세포로부터 기능적 β 세포를 생성하는 것이다.Progress in cell-replacement therapy for Type I diabetes mellitus and lack of transplantable Langerhans islands has been focused on developing a source of insulin-producing cells, or beta cells, suitable for engraftment. One approach is to produce functional beta cells from pluripotent stem cells such as embryonic stem cells.
척추동물 배아 발생에서, 만능 세포는 낭배형성(gastrulation)으로 알려진 과정에서 3개의 배엽층(외배엽, 중배엽, 및 내배엽)을 포함하는 세포군을 발생시킨다. 갑상선, 흉선, 췌장, 장, 및 간과 같은 조직은 내배엽으로부터 중간 단계를 거쳐 발생할 것이다. 이 과정에서 중간 단계는 완성 내배엽(definitive endoderm)의 형성이다.In vertebrate animal embryogenesis, pluripotent cells produce a population of cells containing three embryonic layers (ectoderm, mesoderm, and endoderm) in a process known as gastrulation. Tissues such as the thyroid, thymus, pancreas, bowel, and liver will develop from the endoderm through the intermediate stage. The intermediate stage in this process is the formation of a definitive endoderm.
낭배형성 말기까지, 내배엽은 내배엽의 전방, 중간 및 후방 영역을 고유하게 표시하는 인자들의 패널의 발현에 의해 인식될 수 있는 전방-후방 도메인(anterior-posterior domain)으로 분할된다. 예를 들어, HHEX, 및 SOX2는 전방 영역을 확인해주며, 한편 CDX1, 2, 및 4는 내배엽의 후방 영역을 확인해준다.By the end of vestigial formation, endoderm is divided into anterior-posterior domains, which can be recognized by the expression of panels of factors uniquely representing the anterior, medial and posterior regions of endoderm. For example, HHEX and SOX2 identify the anterior region, while CDX1, 2, and 4 identify the posterior region of the endoderm.
내배엽 조직의 이주에 의해 내배엽은 상이한 중배엽 조직들과 아주 근접해지게 되며, 이는 장관(gut tube)의 국지화를 돕는다. 이는 FGF, Wnt, TGF-β, 레티노산("RA"), 및 BMP 리간드 및 이들의 길항제와 같은 다수의 분비 인자들에 의해 달성된다. 예를 들어, FGF4 및 BMP는 추정 후장 내배엽에서 CDX2 발현을 촉진하며 전방 유전자 HHEX 및 SOX2의 발현을 억제하는 것으로 보고되어 있다(문헌[2000 Development, 127:1563-1567]). 또한, WNT 신호전달(signaling)은 후장 발달을 촉진하고 전장 운명을 억제하도록 FGF 신호전달과 병행하여 작동하는 것으로 밝혀져 있다(문헌[2007 Development, 134:2207-2217]). 마지막으로, 중간엽에 의해 분비된 레티노산은 전장-후장 경계부를 조절한다(문헌[2002 Curr Biol, 12:1215-1220]).Migration of endoderm tissue causes the endoderm to become very close to the different mesoderm tissues, which helps localize the gut tube. This is accomplished by a number of secretion factors such as FGF, Wnt, TGF- [beta], retinoic acid ("RA"), and BMP ligands and their antagonists. For example, FGF4 and BMP have been reported to promote CDX2 expression in the putative endoderm and suppress the expression of the anterior genes HHEX and SOX2 (2000 Development , 127: 1563-1567). In addition, WNT signaling has been shown to work in parallel with FGF signaling to stimulate postnatal development and suppress full-length fate (2007 Development , 134: 2207-2217). Finally, retinoic acid secreted by the mesenchyme regulates the full-length border (2002 Curr < RTI ID = 0.0 > Biol. , 12: 1215-1220).
특정 전사 인자들의 발현 수준은 조직의 정체(identity)를 지정하는 데 사용될 수 있다. 완성 내배엽이 원시 장관(primitive gut tube)으로 형질전환하는 동안, 장관은 제한된 유전자 발현 패턴에 의해 분자 수준에서 관찰될 수 있는 폭넓은 도메인들로 국지화되게 된다. 예를 들어, 장관 내의 국지화된 췌장 도메인은 PDX1의 매우 높은 발현 및 CDX2 및 SOX2의 매우 낮은 발현을 나타낸다. PDX1, NKX6.1, PTF1A, 및 NKX2.2는 췌장 조직에서 고도로 발현되며; CDX2의 발현은 장 조직에서 높다.The level of expression of particular transcription factors can be used to specify the identity of the tissue. While the complete endoderm is transformed into a primitive gut tube, the intestinal tract is localized to a wide range of domains that can be observed at the molecular level by a limited gene expression pattern. For example, the localized pancreatic domain in the intestinal tract shows very high expression of PDX1 and very low expression of CDX2 and SOX2. PDX1, NKX6.1, PTF1A, and NKX2.2 are highly expressed in pancreatic tissues; Expression of CDX2 is high in intestinal tissue.
췌장의 형성은 완성 내배엽에서 췌장 내배엽으로의 분화로부터 생긴다. 배측(dorsal) 및 복측(ventral) 췌장 도메인은 전장 상피에서 생긴다. 또한, 전장은 식도, 기관, 폐, 갑상선, 위, 간, 췌장 및 담관계를 발생시킨다.The formation of the pancreas results from the differentiation of the endoderm into the pancreatic endoderm. The dorsal and ventral pancreatic domains occur in the epithelium. In addition, the battlefield develops esophagus, organs, lungs, thyroid, stomach, liver, pancreas and furcation.
췌장 내배엽의 세포는 췌장-십이지장 호메오박스(homeobox) 유전자 PDX1을 발현한다. PDX1의 부재 하에서는, 췌장은 복측 원기(bud) 및 배측 원기의 형성 이상으로는 발달하지 못한다. 따라서, PDX1 발현이 췌장 기관형성에서 중요한 단계를 표시한다. 성숙한 췌장은 췌장 내배엽의 분화로부터 발생하는 외분비 조직 및 내분비 조직 둘 모두를 함유한다.Pancreatic endoderm cells express the pancreatic-duodenal homeobox gene PDX1. In the absence of PDX1, the pancreas does not develop beyond the formation of the biceps bud and dorsal root. Thus, PDXl expression represents an important step in pancreatic organs formation. A mature pancreas contains both exocrine tissue and endocrine tissue arising from the differentiation of the pancreatic endoderm.
드아무르(D'Amour) 등은 고농도의 액티빈 및 저 혈청의 존재 하에서의 인간 배아줄기세포 유래 완성 내배엽의 풍부한 배양물의 생성을 기술하고 있다(문헌[Nature Biotechnol2005, 23:1534-1541]; 미국 특허 제7,704,738호). 전해지는 바에 의하면, 마우스의 신장 피막 아래에 이들 세포를 이식함으로써 내배엽 조직의 특징을 갖는 더욱 성숙한 세포로 분화되었다고 한다(미국 특허 제7,704,738호). 인간 배아줄기세포 유래 완성 내배엽 세포는 FGF10 및 레티노산의 첨가 후에 PDX1 양성 세포로 추가로 분화될 수 있다(미국 특허 출원 공개 제2005/0266554A1호). 후속하여 면역 결핍 마우스의 지방 패드 내에 이들 췌장 전구세포를 이식함으로써 3 내지 4개월의 성숙기 후에 기능적 췌장 내분비 세포의 형성을 가져왔다(미국 특허 제7,993,920호 및 미국 특허 제7,534,608호).D'Amour et al. Describe the production of abundant cultures of complete endoderm derived from human embryonic stem cells in the presence of high concentrations of actibin and low serum ( Nature Biotechnol 2005, 23: 1534-1541; USA Patent No. 7,704,738). It has been reported that these cells were transplanted under the renal capsule of the mouse to differentiate into more mature cells with characteristics of endoderm tissue (U.S. Patent No. 7,704,738). Completed endodermal cells derived from human embryonic stem cells can be further differentiated into PDX1-positive cells after addition of FGF10 and retinoic acid (US Patent Application Publication No. 2005 / 0266554A1). Subsequent transplantation of these pancreatic progenitor cells within the fat pad of immunodeficient mice resulted in the formation of functional pancreatic endocrine cells after 3 to 4 months of maturation (U.S. Patent No. 7,993,920 and U.S. Patent No. 7,534,608).
피스크(Fisk) 등은 인간 배아줄기세포로부터의 췌장 소도 세포의 생성 시스템을 보고한다(미국 특허 제7,033,831호). 또한, 소분자 억제제가 췌장 내분비 전구세포의 유도에 사용되어 왔다. 예를 들어, TGF-β 수용체 및 BMP 수용체(문헌[Development 2011, 138:861-871]; 문헌[Diabetes 2011, 60:239-247])의 소분자 억제제가 췌장 내분비 세포의 수를 유의하게 향상시키는 데 사용되어 왔다. 게다가, 소분자 활성화제가 완성 내배엽 세포 또는 췌장 전구세포를 생성하는 데 또한 사용되어 왔다(문헌[Curr Opin Cell Biol2009, 21:727-732]; 문헌[Nature Chem Biol 2009, 5:258-265]).Fisk et al. Report the production system of pancreatic islet cells from human embryonic stem cells (US Patent No. 7,033,831). In addition, small molecule inhibitors have been used to induce pancreatic endocrine precursor cells. For example, small molecule inhibitors of the TGF-beta receptor and BMP receptor ( Development 2011, 138: 861-871; Diabetes 2011, 60: 239-247) significantly improve the number of pancreatic endocrine cells Have been used. In addition, small molecule activators have also been used to generate complete endodermal cells or pancreatic progenitor cells ( Curr Opin Cell Biol 2009, 21: 727-732); Nature Chem Biol 2009, 5: 258-265).
만능 줄기세포와 같은 선조세포를 배양하기 위한 프로토콜을 개선하는 데에 있어서 큰 진전이 이루어져 왔다. PCT 공개 WO2007/026353호(아미트(Amit) 등)는 2차원 배양 시스템 내에서 미분화된 상태로 인간 배아줄기세포를 유지하는 것을 개시하고 있다. 문헌[루드비히(Ludwig) 등, 2006 (Nature Biotechnology, 24:185-7)]은 매트릭스 상에서 인간 배아줄기세포를 배양하기 위한 TeSR1 한정된 배지를 개시하고 있다. 미국 특허 출원 공개 제2007/0155013호(아카이케(Akaike) 등)는 만능 줄기세포에 부착하는 캐리어를 사용하여 현탁 상태로 만능 줄기세포를 성장시키는 방법을 개시하고 있으며, 미국 특허 출원 공개 제2009/0029462호(버드슬레이(Beardsley) 등)는 마이크로캐리어 또는 세포 캡슐화를 사용하여 현탁 상태로 만능 줄기세포를 증폭시키는(expanding) 방법을 개시하고 있다. PCT 공개 WO 2008/015682호(아미트 등)는 기질 부착성이 없는 배양 조건 하에서 현탁 배양물 중에서 인간 배아줄기세포를 증폭 및 유지하는 방법을 개시하고 있다.Significant progress has been made in improving protocols for culturing progenitor cells such as pluripotent stem cells. PCT Publication WO2007 / 026353 (Amit et al.) Discloses maintaining human embryonic stem cells in undifferentiated state in a two-dimensional culture system. Ludwig et al., 2006 ( Nature Biotechnology , 24: 185-7) discloses a TeSR1 defined medium for culturing human embryonic stem cells on a matrix. U.S. Patent Application Publication No. 2007/0155013 (Akaike et al.) Discloses a method for growing pluripotent stem cells in suspension using a carrier adhering to pluripotent stem cells. U.S. Patent Application Publication No. 2009 / 0029462 (Beardsley et al.) Discloses a method of expanding pluripotent stem cells in suspension using microcarriers or cell encapsulation. PCT Publication WO 2008/015682 (Amit et al.) Discloses a method for amplifying and maintaining human embryonic stem cells in suspension culture under culture conditions without substrate adherence.
미국 특허 출원 공개 제2008/0159994호(만탈라리스(Mantalaris) 등)는 3차원 배양 시스템 내에서 알기네이트 비드(bead) 내에 캡슐화된 인간 배아줄기세포를 배양하는 방법을 개시하고 있다.United States Patent Application Publication No. 2008/0159994 (Mantalaris et al.) Discloses a method of culturing human embryonic stem cells encapsulated in an alginate bead in a three-dimensional culture system.
이러한 진전에도 불구하고, 기능적 내분비 세포로 분화될 수 있는 만능 줄기세포를 3차원 배양 시스템 내에서 성공적으로 배양하기 위한 방법에 대한 필요성이 여전히 남아 있다.Despite these advances, there remains a need for a method for successfully culturing pluripotent stem cells capable of differentiating into functional endocrine cells in a three-dimensional culture system.
전술한 요약뿐만 아니라 하기의 발명의 상세한 설명도 첨부 도면과 함께 읽을 때 더 잘 이해될 것이다. 본 발명을 예시할 목적으로, 도면은 본 발명의 실시 형태를 보여준다. 그러나, 본 발명은 예시된 정확한 배열, 실시예 및 수단으로 제한되지 않음을 이해하여야 한다.
도 1a는 실시예 1에 따라 리프팅 직후(좌측 패널) 및 비부착성 정치 배양물 중에 있은 지 24시간 후(우측 패널)의 인간 배아줄기("hES") 세포주 H1의 디스파제(Dispase)®-처리된 세포의 현미경 사진을 나타낸다. 리프팅 후의 세포(좌측 패널)는 단층의 단편들과 유사하였는데, 이때 단편들의 평균 단편 직경은 약 20 내지 30 마이크로미터였으며, 각각의 단편은 세포의 군집(clump)으로 이루어졌다. 비부착성 정치 배양물 중에 있은 지 24시간 후에, 세포는 클러스터-유사 구조를 나타내었다.
도 1b는 실시예 1에 따라 25 mL의 mTeSR®1 배지가 담긴 125 mL 스피너 플라스크 내에서 4일 동안 배양한 후에 인간 배아줄기세포주 H1의 디스파제®-처리된 세포에 대한 CD9, SSEA4, CXCR4, TRA-1-60 및 TRA-1-81에 대한 유세포측정법의 결과를 나타낸다. 세포는 분화 마커인 CXCR4는 거의 발현하지 않으면서 만능성 마커(CD9, SSEA4, TRA-1-60, 및 TRA-1-81)에 대해서는 고 발현을 나타내었다.
도 1c는 1기 말기의 72 및 96시간 분화 후의 인간 배아줄기세포주 H1의 디스파제®-처리된 세포의 현미경 사진을 나타낸다. 도 1c에서는 4X 배율로의 72시간 후(좌측 패널)의, 4X 배율로의 96시간 후(중앙 패널)의 그리고 10X 배율로의 96시간 후(우측 패널)의 느슨한 세포 응집체를 볼 수 있다.
도 1d는 마커 CD9, CD184(CXCR4) 및 CD99에 대한 1기 분화 말기의 인간 배아줄기세포주 H1의 디스파제®-처리된 세포에 대한 유세포측정법의 결과를 나타낸다(실시예 1 참조). 도 1d에 나타낸 바와 같이, 만능성 마커인 CD9의 발현은 거의 제거되었으며, 한편 완성 내배엽 분화 마커인 CXCR4(CD184) 및 CD99의 발현은 매우 높았다.
도 1e는 미분화된 H1(WA01) hES 세포와 대비하여, 1기 말기의 인간 배아줄기세포주 H1의 디스파제®-처리된 세포에 대한 완성 내배엽과 관련된 유전자 및 만능성과 관련된 선택된 유전자의 발현에 대한 정량적인 역전사 폴리머라제 연쇄 반응(qRT-PCR) 결과를 나타낸다(실시예 1 참조). 1기 말기의 세포는, 미분화된 WA01 hES 세포와 대비하여, 만능성 유전자(CD9, NANOG, 및 POU5F1/OCT4)의 발현에 있어서는 급격한 감소를 그리고 완성 내배엽과 관련된 유전자(CXCR4, CERBERUS(CER1), GSC, FOXA2, GATA4, GATA6, MNX1, 및 SOX17)에 있어서는 큰 증가를 나타내었다.
도 1f는 세포가 완성 내배엽으로부터 췌장 내배엽을 향하여 추가로 분화됨에 따른 인간 배아줄기세포주 H1의 디스파제®-처리된 세포의 현미경 사진을 나타낸다(실시예 1 참조). 2기 1일째(상부 좌측 패널)로부터 2기 3일째(상부 우측 패널)에 이어서 3기 4일째(하부 좌측 패널) 및 4기 1일째(하부 우측 패널)로 분화가 진행됨에 따라 세포 및 세포 클러스터에 대한 명확한 형태학적 변화가 가시적이게 된다.
도 2a는 실시예 2에 따른 만능성 및 분화와 관련된 마커에 대해, EDTA 처리 후의 교반된 현탁 배양물 중에서 2일 배양 후에 그리고 분화 배양물로의 전이 전에 인간 배아줄기세포주 H1의 EDTA-처리된 세포에 대한 유세포측정법의 데이터를 나타낸다. 이 데이터는 분화 마커(CXCR4)는 거의 발현하지 않으면서 만능성 마커(CD9, SSEA4, TRA-1-60, 및 TRA-1-81)에 대해서는 고 발현을 나타내었다.
도 2b는 실시예 2에 따라 스피너 플라스크 내에서 성장된 1기 3일째 세포 및 스피너 플라스크 또는 삼각 플라스크 내에서 성장된 2기 2일째, 4기 1일째 및 4기 3일째 세포로 분화된 인간 배아줄기세포주 H1의 EDTA-처리된 세포의 현미경 사진을 나타낸다. 현탁 분화된 배양물은 구형 응집체로 실질적으로 균일하고 균질한 세포 집단을 형성하였다.
도 2c는 만능성 및 내배엽 분화의 세포 표면 마커에 대한 1기 말기의 인간 배아줄기세포주 H1의 EDTA-처리된 세포에 대한 유세포측정법의 데이터를 나타낸다. 도 2c에서 볼 수 있는 바와 같이, 만능성 마커인 CD9의 발현은 거의 제거되었으며, 한편 완성 내배엽 분화 마커인 CXCR4(CD184)에 대한 발현은 매우 높았다.
도 2d는 미분화된 H1(WA01) hES 세포와 대비하여, 1기 말기의 인간 배아줄기세포주 H1의 EDTA-처리된 세포에 대한 완성 내배엽과 관련된 유전자 및 만능성과 관련된 선택된 유전자의 발현에 대한 qRT-PCR 결과를 나타낸다(실시예 2 참조). 도 2d는 만능성 유전자(CD9, NANOG, 및 POU5F1/OCT4)의 발현에 있어서의 감소 및 완성 내배엽과 관련된 유전자(CXCR4, CERBERUS("CER1"), FOXA2, GATA4, GATA6, MNX1, 및 SOX17)에 있어서의 큰 증가를 나타낸다.
도 2e는 실시예 2에 따라 스피너 플라스크 또는 삼각 플라스크 내에서 1기로부터 췌장 내배엽 세포로 분화된 인간 배아줄기세포주 H1의 EDTA-처리된 세포에 대한 분화를 나타내는 마커(NKX6.1, CDX2, SOX2, 및 크로마그라닌)에 대한 유세포측정법의 데이터를 나타낸다. 유세포측정법의 데이터는 두 현탁 포맷 모두에 대해, 기능적 β 세포에 요구되는 전사 인자인 NKX6.1이 고수준이고, 시냅토파이신(데이터는 나타내지 않음) 및 크로모그라닌과 같은 내분비 췌장 마커가 고수준임을 나타낸다.
도 2f는 실시예 2에 따른 스피너 플라스크 또는 삼각 플라스크 내에서 현탁에 의해 1기로부터 췌장 내배엽 세포로 추가로 분화된 인간 배아줄기세포주 H1의 EDTA-처리된 세포에 대한 분화와 관련된 선택된 유전자의 발현에 대한 qRT-PCR 결과를 나타낸다. 이 데이터는 WA01 hES 세포에서의 발현과 대비된다. RT-PCR 결과는 췌장 전구체 유전자의 고수준의 발현을 나타낸다.
도 3a는 아큐타제(Accutase)®로 처리한 후의 정치 배양물로부터 리프팅된 인간 배아줄기세포주 H1의 세포의 현미경 사진을 나타낸다. 도 3a에 나타낸 바와 같이, 세포를 작은 응집체로서 표면으로부터 제거하였다.
도 3b는 아큐타제®로 처리한 후의 정치 배양물로부터 리프팅되고, 이어서 3일 동안 현탁 배양물 중에서 증폭된 인간 배아줄기세포주 H1의 세포의 위상차 현미경 사진을 나타낸다. 도 3b에서는 세포 클러스터의 실질적으로 균일한 구형 집단의 형성을 볼 수 있다.
도 3c는 아큐타제®로 처리한 후의 정치 배양물로부터 리프팅되고, 이어서 현탁 배양물 중에서 3일 동안 증폭된 다음, 아큐타제® 해리를 사용하여 연속 계대배양된 인간 배아줄기세포주 H1의 세포의 클러스터의 현미경 사진을 나타낸다.
도 4a는 분화의 상이한 단계에서 유도 분화 프로토콜(directed differentiation protocol)을 사용한 세포주 H1의 현탁 배양된 인간 배아줄기세포의 현미경 사진을 나타낸다. 도 4a에서는 분화의 각각의 단계에 있는 세포의 현미경 사진을 볼 수 있다.
도 4b는 분화의 상이한 단계(분화 개시 후의 시간)에서 유도 분화 프로토콜을 사용한 세포주 H1의 현탁 배양된 인간 배아줄기세포에 대한 분화 마커(CXCR4, CD56 및 PDX1)에 대한 유세포측정법의 결과를 나타낸다. 4기 4일째의 분화 과정의 말기에, 높은 백분율의 세포가 PDX1 발현에 대해 양성이었다.
도 4c는 테라사이트(TheraCyte)™ 장치 내에 캡슐화된 분화된 세포가 이식된 SCID-Bg 마우스의 비공복시 혈당 수준을 나타낸다.
도 5a는 만능성 및 분화와 관련된 마커에 대한 분화 배양물로의 전이 전에 인간 배아줄기세포주 H1의 EDTA-처리된 세포에 대한 유세포측정법의 데이터를 나타낸다. 도 5a에 나타낸 바와 같이, 만능성 마커 CD9, SSEA4, TRA-1-60 및 TRA-1-80의 고 발현이 관찰되었다.
도 5b는 1기 동안에 3가지 상이한 공급물 세팅에 대한 CXCR4/CD184 및 CD99(분화 마커) 및 CD9(만능성 마커)에 대한 세포의 위상차 영상 및 유세포측정법의 데이터를 나타낸다. 시험된 조건은 다음과 같았다: (A) 분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음; (B) 분화 개시 후 24시간째에 배지 교체 및 48시간째에 글루코스 볼루스(bolus) 첨가; 및 (C) 1기 전체에 걸쳐 배지 교체는 없으면서, 글루코스 및 GDF8 볼루스를 분화 개시 후 24시간째에 첨가하고, 이어서 글루코스 볼루스를 개시 후 48시간째에 첨가함.
도 5c는 완성 내배엽의 형성 동안 다음의 공급물 세팅을 사용하여 분화된, 췌장 내배엽 형태를 나타내는 분화된 세포의 위상차 영상을 나타낸다: (A) 분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음; (B) 분화 개시 후 24시간째에 배지 교체 및 48시간째에 글루코스 볼루스 첨가; 및 (C) 1기 전체에 걸쳐 배지 교체는 없으면서, 글루코스 및 GDF8 볼루스를 분화 개시 후 24시간째에 첨가하고, 이어서 글루코스 볼루스를 개시 후 48시간째에 첨가함.
도 5d는 완성 내배엽의 형성 동안 다음의 공급물 세팅을 사용하여 분화된, 4기 말기의 분화된 세포에 대한 췌장 유전자 발현의 선택 마커(NKX6.1 및 크로모그라닌) 및 선택 비-췌장 유전자(CDX2 및 SOX2)에 대한 유세포측정법의 결과를 나타낸다: (A) 분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음; (B) 분화 개시 후 24시간째에 배지 교체 및 48시간째에 글루코스 볼루스 첨가; 및 (C) 1기 전체에 걸쳐 배지 교체는 없으면서, 글루코스 및 GDF8 볼루스를 분화 개시 후 24시간째에 첨가하고, 이어서 글루코스 볼루스를 개시 후 48시간째에 첨가함.
도 5e는 완성 내배엽의 형성 동안 다음의 공급물 세팅을 사용하여 분화된, 4기 말기의 분화된 세포에 대한 선택 췌장 유전자 발현 및 비-췌장 유전자 발현에 대한 qRT-PCR 결과를 나타낸다: (A) 분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음; (B) 분화 개시 후 24시간째에 배지 교체 및 48시간째에 글루코스 볼루스 첨가; 및 (C) 1기 전체에 걸쳐 배지 교체는 없으면서, 글루코스 및 GDF8 볼루스를 분화 개시 후 24시간째에 첨가하고, 이어서 글루코스 볼루스를 개시 후 48시간째에 첨가함. 데이터는 미분화된 H1(WA01) hES 세포수(1의 베이스라인 발현)와 대비하여 발현에 있어서의 배수 차이로서 나타나 있다.
도 5f는 조건 A(분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음)에 따라 분화된 세포가 이식된 SCID-Bg 마우스에서의 C-펩타이드의 발현을 나타낸다. 각각의 SCID-Bg 마우스에 신장 피막 아래에 500만개의 세포를 이식하였다. 도 5f에 나타낸 바와 같이, 이식 후 12주째까지, 인간 C-펩타이드는 1 ng/mL 초과의 수준으로 검출가능하였으며, 16주째에 C-펩타이드 수준은 평균 2.5 ng/mL였다.
도 5g는 조건 A(분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음)에 따라 분화된 세포의 투여(예를 들어, 이식) 전 및 후에, 선택된 SCID-Bg 마우스에 대한 글루코스 처리의 영향을 나타낸다. 도 5g에 나타낸 바와 같이, 글루코스 처리는 순환 인간 C-펩타이드에 있어서 절식 상태에서의 평균 0.93 ng/mL로부터 급식 상태에서의 2.39 ng/mL로의 유의한 증가를 유도하였다.
도 5h는 조건 A(분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음)에 따라 분화된 세포가 투여된 SCID-Bg 마우스에 대한 스트렙토조토신(STZ) 투여(즉, STZ-유도 당뇨병)의 영향을 나타낸다. 도 5h로부터 명백한 바와 같이, 기능적 GSIS 컴피턴트(competent) 조직의 이식편을 갖는 동물(즉, 세포가 투여된 것)은 비처리된 대조군 - 이는 임상적으로 확실한 당뇨병이 발생되었음 - 과는 달리 정상의 혈당 수준을 유지하였다.
도 6a는 분화 전에 사이토덱스(Cytodex)® 3 마이크로캐리어 비드 상에서 성장된 인간 배아줄기세포주 H1의 세포의 현미경 사진을 나타낸다.
도 6b는 분화의 다양한 단계에서 사이토덱스® 3 마이크로캐리어 비드 상에서 성장된 인간 배아줄기세포주 H1의 세포의 현미경 사진을 나타낸다.
도 6c는 액티빈 A(AA) 및 WNT3A를 함유하는 배지 중의 플레이트(WTN3A/AA 플레이트), 액티빈 A 및 WNT3A를 함유하는 배지 중의 마이크로캐리어(WTN3A/AA 마이크로캐리어), MCX 및 GDF8을 함유하는 배지 중의 플레이트(MCX/GDF8 플레이트) 및 MCX 및 GDF8을 함유하는 배지 중의 마이크로캐리어(MCX/GDF8 마이크로캐리어) 상에서 성장 및 분화된 인간 배아줄기세포주 H1의 세포에 대한 분화 일수의 함수로서의 세포 카운트(세포수/㎠)를 나타낸다.
도 6d는 액티빈 A 및 WNT3A를 함유하는 배지 중의 플레이트(WTN3A/AA 플레이트), 액티빈 A 및 WNT3A를 함유하는 배지 중의 마이크로캐리어(WTN3A/AA 마이크로캐리어), MCX 및 GDF8을 함유하는 배지 중의 플레이트(MCX/GDF8 플레이트) 및 MCX 및 GDF8을 함유하는 배지 중의 마이크로캐리어(MCX/GDF8 마이크로캐리어) 상에서 성장 및 분화된 인간 배아줄기세포주 H1의 세포에 대한 분화 일수의 함수로서의 세포 카운트(세포수/ml)를 나타낸다.
도 6e는 다음의 존재 하에서 마이크로캐리어 배양물 또는 평면 배양물 상에서 성장된 세포의 제1 분화 단계에 대한 유세포측정법의 결과를 나타낸다: CXCR4/CD184(Y-축) 및 CD9(X-축)의 세포 발현의 점 도표로서의 (a) WNT3A 및 AA; 또는 (2) MCX 및 GDF8.
도 6f는 다음의 존재 하에서 마이크로캐리어 배양물 또는 평면 배양물 상에서 성장된 세포의 제1 분화 단계에 대한 유세포측정법의 결과를 나타낸다: 마커(CXCR4 및 CD9) 각각의 총 발현으로서의 (a) WNT3A 및 AA; 또는 (2) MCX 및 GDF8.
도 6g는 다음의 존재 하에서 평면 배양물 상에서 또는 현탁 배양물 중의 마이크로캐리어 비드 상에서 성장시킴으로써 분화된 인간 배아줄기세포주 H1의 세포에 대한 분화와 관련된 선택된 유전자의 발현에 대한 qRT-PCR 결과를 나타낸다: (a) WNT3A 및 AA; 또는 (2) MCX 및 GDF8.
도 7은 실시예 7의 프로토콜에 따라 분화된 세포에 대한 1기 1일째로부터 4기 3일째까지의 생물반응기 내에서의 다양한 분화 단계에서의 세포 카운트를 나타낸다. 세포 카운트는 영상-기반 세포측정기(뉴클레오카운터(NucleoCounter)®)에 의해 측정하였을 때의 백만개 세포/ml로 나타낸다.
도 8은 실시예 7의 분화 프로토콜 동안 시간(분화 일수)의 함수로서의 일평균 생물반응기 배지 pH 수준을 나타낸다. pH 수준은 노바(NOVA) 바이오프로파일(BioProfile)® 플렉스(FLEX)(노바 바이오메디칼 코포레이션(Nova Biomedical Corporation), 미국 매사추세츠주 월섬 소재)에 의해 측정하였다.
도 9는 실시예 7의 분화 프로토콜 동안 시간(분화 일수)의 함수로서의 일평균 생물반응기 배지 락테이트 수준을 나타낸다. 락테이트 수준은 노바 바이오프로파일® 플렉스(노바 바이오메디칼 코포레이션, 미국 매사추세츠주 월섬 소재)에 의해 측정하였다.
도 10은 실시예 7의 분화 프로토콜 동안 시간(분화 일수)의 함수로서의 일평균 생물반응기 배지 글루코스 수준을 나타낸다. 글루코스 수준은 노바 바이오프로파일® 플렉스(노바 바이오메디칼 코포레이션, 미국 매사추세츠주 월섬 소재)에 의해 측정하였다.
도 11은 실시예 7의 프로토콜에 따라 분화된 0기 1일째(즉, 접종 후 24시간째) 세포에 대한, 만능성과 관련된 선택 유전자를 함유하는 만능성 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 미분화된 유전자 발현을 나타낸다.
도 12는 0기 1일째(즉, 접종 후 24시간째) 세포에 대한, 완성 내배엽("DE")과 관련된 선택 유전자를 함유하는 완성 내배엽 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 미분화된 유전자 발현을 나타낸다(실시예 7 참조).
도 13은 0기 3일째(즉, 접종 후 72시간째) 세포에 대한, 만능성과 관련된 선택 유전자를 함유하는 만능성 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 미분화된 유전자 발현을 나타낸다(실시예 7 참조).
도 14는 0기 3일째(즉, 접종 후 72시간째) 세포에 대한, DE와 관련된 선택 유전자를 함유하는 DE 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 미분화된 유전자 발현을 나타낸다(실시예 7 참조).
도 15는 미분화된 0기 3일째(즉, 접종 후 72시간째) 세포에 대해 CD9, CD184/CXCR4, SSEA4, TRA-1-60 및 TRA-1-81에 대한 형광-활성화 세포 분류(FACS)의 결과를 나타낸다(실시예 7 참조). 결과가 또한 표 8에 나타나있다.
도 16은 실시예 7의 프로토콜에 따라 분화된 0기 1일째(즉, 접종 후 24시간째) 및 0기 3일째(즉, 접종 후 72시간째) 세포의 선택 유전자에 대해, qRT-PCR에 의해 측정하였을 때의 미분화된 유전자 발현을 나타낸다. 구체적으로, 도 16은 유도 분화 전 0기 과정 동안 GATA4, GSC, MIXL1 및 T에 대한 유전자 발현에 있어서의 보통의 증가 및 GATA2 발현에 있어서의 100x 이상의 증가를 나타낸다.
도 17은 실시예 7의 프로토콜에 따라 분화된 0기 1일째(즉, 접종 후 24시간째) 및 0기 3일째(즉, 접종 후 72시간째) 세포에 대한, DE와 관련된 선택 유전자를 함유하는 DE 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 미분화된 유전자 발현을 나타낸다. 구체적으로, 도 17은 유도 분화 전 0기 과정 동안 CER1, FGF17, 및 FGF4 발현에 있어서의 100x 이상의 증가를 나타낸다.
도 18 및 도 19는 실시예 7의 프로토콜에 따라 분화된 1기 1일째 세포에 대한 유전자 발현을 나타낸다. 도 18은 1기 1일째 세포에 대한, 만능성과 관련된 선택 유전자를 함유하는 만능성 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 19는 1기 1일째 세포에 대한, DE와 관련된 선택 유전자를 함유하는 DE 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 18 및 도 19는 FOXA2 발현에 있어서의 약 700x 증가 및 CER1, EOMES, FGF17, FGF4, GATA4, GATA6, GSC, MIXL1, 및 T 발현에 있어서의 1000x 증가와 같이 유전자 발현 패턴에서의 유의한 변경을 나타낸다.
도 20 및 도 21은 실시예 7의 프로토콜에 따라 분화된 1기 3일째 세포에 대한 유전자 발현을 나타낸다. 도 20은 1기 3일째 세포에 대한, 만능성과 관련된 선택 유전자를 함유하는 만능성 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 21은 1기 3일째 세포에 대한, DE와 관련된 선택 유전자를 함유하는 DE 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다.
도 22는 실시예 7의 프로토콜에 따라 분화된 1기 3일째 세포에 대해서의 CD9, CD184(CXCR4로도 알려짐) 및 CD99에 대한 FACS의 결과를 나타낸다. 분화 개시 시에 CD9 발현/CXCR4 음성 만능 세포 집단(도 15)으로부터 1기 말기에 CXCR4 발현 세포(98.3%의 세포가 CXCR4 양성임, ±1.9 SD)의 균질 집단(도 22)으로의 거의 완전한 전이가 관찰되었다.
도 23은 실시예 7의 프로토콜에 따라 분화된 1기 3일째; 2기 1일째; 및 2기 3일째 세포에 대한, DE와 관련된 선택 유전자를 함유하는 DE 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 23은 2기 1 및 3일째에 HNF4α 및 GATA6 발현 수준이 증가되었으며, 한편 1기 3일째에 고수준으로 발현된 유전자(CXCR4, EOMES, FGF17, FGF4, MNX1, PRDM1, SOX17, 및 VWF)는 2기 말기까지 감소된 발현을 나타내었음을 나타낸다.
도 24는 실시예 7의 프로토콜에 따라 분화된 2기 1일째 세포 및 2기 3일째 세포에 대해, qRT-PCR에 의해 측정하였을 때의 전장 유전자 AFP, PDX1, 및 PROX1의 유전자 발현을 나타낸다. 도 24에 나타낸 바와 같이, 이들 유전자의 발현은 증가하였다.
도 25는 실시예 7의 프로토콜에 따라 분화된 3기 배지(표 7) 중에서 성장된 3기 3일째 세포에 대해서의 PDX1, FOXA2, 크로모그라닌 NKX2.2 및 SOX2에 대한 FACS의 결과를 나타낸다. 도 25에 나타낸 바와 같이, 세포는 PDX1 및 FOXA2 발현에 의해 측정하였을 때 내배엽 췌장 계통과 일치하는 마커를 발현하였다(90.9% ± 11.9 SD가 PDX1 양성이고 99.2% ± 0.6 SD가 FOXA2 양성임).
도 26은 실시예 7의 프로토콜에 따라 분화된 4기, 3기 1일째 및 3기 3일째 세포와 관련된 선택 유전자를 함유하는 4기 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 26은 이들 세포가 췌장에서 공통으로 발현되는 다수의 유전자(ARX, GAST, GCG, INS, ISL1, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PAX6, PTF1A, 및 SST)의 증가된 수준을 나타냄을 예시한다.
도 27은 실시예 7의 프로토콜에 따라 분화된 4기 3일째 세포에 대해 NKX6.1, 크로마그라닌(CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 및 NEUROD에 대한 FACS 결과를 나타낸다. 도 27의 4기 3일째에 나타낸 바와 같이, 세포는 고수준의 PDX1 및 FOXA2 발현을 보유하였으며 췌장 내분비 세포(28.1% ± 12.5 SD가 크로모그라닌 양성임) 및 췌장 선조세포(58.3% ± 9.7 SD가 NKX6.1에 대해 양성임)의 혼합물과 일치하는 발현 패턴을 추가로 발생시켰다.
도 28은 실시예 7의 프로토콜에 따라 분화된 3기 3일째; 4기 1일째 및 4기 3일째 세포에 대한, 단계 4와 관련된 선택 유전자를 함유하는 4기 어레이에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 28은 췌장에서 공통으로 발현되는 유전자(ARX, GAST, GCG, IAPP, INS, ISL1, MAFB, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PAX6, PTF1A, 및 SST)의 증가된 발현 수준을 나타낸다.
도 29는 실시예 7의 프로토콜에 따라 분화된 4기 3일째 세포에 대해서의 NKX6.1, 크로마그라닌(CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 및 NEUROD에 대한 FACS의 평균 결과를 나타낸다. 구체적으로, 도 29는 상이한 시드 물질 로트(seed material lot)로부터 3 L 스케일로 생성된 췌장 전구체의 평균 FACS 발현 패턴을 나타낸다.
도 30은 실시예 7의 프로토콜에 따라 분화된 4기 3일째 세포에 대해서의NKX6.1, 크로마그라닌(CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 및 NEUROD에 대한 FACS의 평균 결과를 나타낸다. 4기 3일째 세포에서의 분화 전에, 세포를 증폭시켜 ISM을 형성하고, 이어서 둘 모두 0.5% BSA로 보충된, 주문제작 사내 배지(custom in-house medium) "IH3" 또는 이센셜8(Essential8)™ 중에서 0기에서 성장시켰다. IH3 배지 중에서 성장된 세포는 "IH3-P 성장 세포"이고 이센셜8™ 중에서 성장된 세포는 "EZ8 성장 세포"이다. 상이한 배지 중에서 성장된 세포들 사이에는 발현 패턴에 있어서 유의한 차이가 관찰되지 않았다.
도 31은 0기에서 상이한 pH 수준에서 미리 성장된 4기 3일째 세포에 대해서의 NKX6.1, 크로마그라닌(CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 및 NEUROD에 대한 FACS의 평균 결과를 나타낸다(실시예 7 참조). 4기 3일째의 세포 프로파일에 있어서 유의한 변화가 관찰되지 않았다.
도 32는 소포제(Anti-Foam) C로 처리되지 않은 4기 3일째 세포와 소포제 C 에멀젼(94 ppm)으로 처리된 4기 3일째 세포에 대해서의 NKX6.1, 크로모그라닌(CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 및 NEUROD에 대한 FACS의 결과를 비교한다(실시예 7 참조). 소포제 C 에멀젼(시그마(Sigma) 카탈로그 번호 A8011)은 4기 3일째 세포의 프로파일에 영향을 미치는 것으로 관찰되지 않았다.
도 33 내지 도 35는 실시예 8의 프로토콜에 따라 분화된 세포에 대한 선택 유전자에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 33은 분화 개시 전 24시간째에 세포의 선택 유전자에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다(실시예 8 참조). 도 33에 나타낸 바와 같이, 생물반응기로부터의 세포는 만능성에 특징적인 유전자(POU5F1, NANOG, SOX2, 및 ZFP42)에 대해서는 발현을 보유하였으며, 분화에 특징적인 유전자(AFP, 및 FOXA2: 50배 미만의 증가; FOXD3, GATA2, GATA4, GSC, HAND2, MIXL1 및 T: 10배 미만으로 증가된 발현)에 대해서는 최소한의 유도 또는 무유도를 나타내었다. 도 34는 분화 개시 후 24시간째에 세포의 선택 유전자에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 35는 분화 개시 후 72시간째에 세포의 선택 유전자에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다.
도 36a 내지 도 36e는 실시예 8의 프로토콜에 따라 2기 내지 3 및 4기로부터 분화된 세포에 대한 선택 유전자에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 구체적으로, 이들 도면은 2기 1일째; 2기 2일째; 2기 3일째; 3기 3일째; 및, 유전자에 따라서는, 4기 1일째의 세포의 유전자 발현을 나타낸다. 도 36a는 AFP, ATOH1 및 CDX2에 대한 유전자 발현을 나타낸다. 도 36b는 GAST, HAND1, HHEX 및 HNF4a에 대한 유전자 발현을 나타낸다. 도 36c는 NKX2.2, NKX6.1, OSR1, 및 PDX1에 대한 유전자 발현을 나타낸다. 도 36d는 PROX1, PFT1a, SOX17, 및 SOX2에 대한 유전자 발현을 나타낸다. 도 36e는 SOX9에 대한 유전자 발현을 나타낸다. 데이터는 미분화된 H1(WA01) hES 세포수(1의 베이스라인 발현)와 대비하여 발현에 있어서의 차이로서 나타나 있다.
도 37은 실시예 8에서의 프로토콜에 따른 분화의 4기 3일째 세포에 대한 선택 유전자에 대해, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 37에 나타낸 바와 같이, 3기 3일째의 분화 말기에, 세포는 미분화된 H1 인간 배아줄기세포와 대비하여, PDX1의 고 발현 수준(1×106배 초과의 유도) 및 다른 췌장 유전자의 고 발현 수준(ARX, GCG, GAST, INS, ISL, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PTF1a, 및 SST의 1000배 초과의 유도) 그리고 OCT4/POU5F1 발현의 거의 완전한 손실을 특징으로 하는 췌장 선조세포로 분화되었다.
도 38은 실시예 8에 따른 분화 프로토콜 동안의 일일 세포 카운트를 나타낸다. 구체적으로, 도 38은 과정 일수의 함수로서의 세포 밀도를 나타낸다. 도 38은 pH 6.8 및 7.2에서 수행된 2개의 반응기 실시(PRD1205 및 PRD1207)의 분화 프로토콜에 대한 세포 카운트를 나타낸다. 비교를 위해, 세포 드리프트(drift)에 대한 세포 카운트를 또한 나타낸다.
도 39a 내지 도 39d는 실시예 8의 프로토콜에 따라 분화되어 SCID-Bg 마우스 내로 이식된, 4기 3일째 세포의 생체내(in vivo) 생물활성을 나타낸다. 세포는 신장 피막 아래에 테라사이트™ 장치를 통해 피하 이식하거나, 또는 초저부착 디쉬 내에서 인큐베이션(incubation)한 후 이식하였다. 마우스를 혈당 및 C-펩타이드 수준에 대해 이식편 이식 후 매 4주마다 모니터링하였다. 도 39a는 시간의 함수로서의 테트라사이트™ 장치 내의 5 × 106 또는 10 × 106개의 4기 3일째 세포의 이식 후의 C-펩타이드 수준을 나타낸다. 도 39b는 테트라사이트™ 장치 내의 5 × 106 또는 10 × 106개의 4기 3일째 세포의 이식 후의 동물 내의 비공복시 글루코스 수준을 나타낸다. 도 39b에서의 마우스는 이식 전에 STZ로 처리하여 숙주 β-세포 기능을 제거하였다. 도 39c는 시간(이식 후 주수)의 함수로서의 테트라사이트™ 장치 내의 미리 동결보존된 4기 3일째 세포의 이식 후에 생성된 C-펩타이드 수준을 나타낸다. 도 39d는 해동 직후(D0) 또는 해동 후 1일째(D1)에 이식된 동결보존되지 않은/새로운 4기 3일째 세포 또는 동결보존된 4기 3일째 세포의 신장 이식편에 의해 처리된 마우스의 C-펩타이드 수준을 비교한다.
도 40a 내지 도 40d는 MCX 화합물 및 GDF-8(도 40a); MCX 단독(도 40b); WNT3A 및 액티빈 A(도 40c); 및 WNT3A 단독(도 40d)으로 1기 1일째에 처리된, 실시예 9의 프로토콜에 따라 3일 동안 분화된 세포의 CXCR4, CD99, 및 CD9에 대한 FACS 도표를 나타낸다. 이들 도면은 현탁 배양물 중에, 분화 1일째에 TGF-β 패밀리 구성원의 부재 하에서의 3 μM MCX의 첨가가, 1일째에 3 μM MCX + 100 ng/ml GDF-8 또는 20 ng/ml WNT-3a + 100 ng/ml 액티빈 A로 세포가 처리될 때 수득된 것과 비견되는 수준으로 완성 내배엽을 생성함을 나타낸다.
도 41a 내지 도 41d는 1기 1일째에 다양한 양의 MCX로 처리된, 실시예 10의 프로토콜에 따라 3일 동안 분화된 세포의 CXCR4, CD99 및 CD9에 대한 FACS 도표를 나타낸다. 구체적으로는, 1기 1일째의 세포를 4 μM의 MCX(도 41a); 3 μM의 MCX(도 41b); 2 μM의 MCX(도 41c); 및 1.5 μM의 MCX(도 41d)로 처리하였다.
도 42a 및 도 42b는 실시예 11의 프로토콜에 따라 3일 동안 분화된 세포의 CXCR4, CD99 및 CD9에 대한 FACS 도표를 나타낸다. 구체적으로, 이들 도면은 현탁 배양물에서의 배지 교체 빈도의 역할을 나타낸다. 도 42a는 1기에서의 완전한 배지 교체와 함께 실시예 10의 프로토콜에 따라 3일 동안 분화된 세포의 CXCR4, CD99 및 CD9에 대한 FACS 도표를 나타낸다. 도 42b는 3일째에 배지 교체 없이 실시예 10의 프로토콜에 따라 3일 동안 분화된 세포의 CXCR4, CD99 및 CD9에 대한 FACS 도표를 나타낸다. 데이터는, 현탁 배양 시스템 내에서, 분화 3일째에 배지 교체된 배양물(도 42a)이 3일째에 배지 교체되지 않은 배양물(도 42b)과 비견되는 효능으로 완성 내배엽을 생성하였음을 시사한다.
도 43a 및 도 43b는 실시예 12의 프로토콜에 따라 3일 동안 분화된 세포의 CXCR4, CD99 및 CD9에 대한 FACS 도표를 나타낸다. 구체적으로, 이들 도면은 현탁 배양물에서의 글루타맥스(GlutaMAX)™의 역할을 나타낸다. 1X 글루타맥스™로 보충되거나(도 43a) 또는 글루타맥스™ 또는 어떠한 글루타민도 없는(0 M 글루타맥스™)(도 43b) 배지 중에서 1기에서 세포를 배양하였다. 데이터는, 현탁 배양 시스템 내에서, 글루타맥스™의 첨가가 완성 내배엽이 생성되는 효능에 영향을 미치는 것으로 보이지 않음을 시사한다.
도 44a 내지 도 44d는 실시예 13의 프로토콜에 따라 분화된 세포에 대한 다양한 양의 중탄산나트륨의 영향을 나타낸다. 도 44a 및 도 44b는 1기에서 첨가된 3.64 g/l(도 44a) 또는 2.49 g/l(도 44b)를 사용하여 실시예 13의 프로토콜에 따라 3일 동안 분화된 세포의 CXCR4, CD99, 및 CD9에 대한 FACS 도표를 나타낸다. 도 44c 및 도 44d는 1기에서 첨가된 3.64 g/l(도 44c) 또는 2.49 g/l(도 44d)를 사용하여 실시예 13의 프로토콜에 따라 3일 동안 분화된 세포의 위상차 현미경 사진을 나타낸다.
도 45는 실시예 14의 프로토콜에 따라 분화된 세포에 대한 분화의 함수로서의 세포 밀도에 대한 일일 세포 카운트를 나타낸다. 세포 카운트는 영상-기반 세포측정기(뉴클레오카운터®)를 사용하여 수득하였다.
도 46은 실시예 14의 분화 프로토콜 동안 시간(분화 일수)의 함수로서의 일평균 생물반응기 배지 pH 수준을 나타낸다. pH 수준은 노바 바이오프로파일® 플렉스(노바 바이오메디칼 코포레이션, 미국 매사추세츠주 월섬 소재)에 의해 측정하였다.
도 47은 실시예 14의 분화 프로토콜 동안 시간(분화 일수)의 함수로서 일평균 생물반응기 배지 글루코스 수준을 나타낸다. 글루코스 수준은 노바 바이오프로파일® 플렉스(노바 바이오메디칼 코포레이션, 미국 매사추세츠주 월섬 소재)에 의해 측정하였다.
도 48은 실시예 14의 분화 프로토콜 동안 시간(분화 일수)의 함수로서의 일평균 생물반응기 배지 락테이트 수준을 나타낸다. 락테이트 수준은 노바 바이오프로파일® 플렉스(노바 바이오메디칼 코포레이션, 미국 매사추세츠주 월섬 소재)에 의해 측정하였다.
도 49는 실시예 14의 프로토콜에 따라 분화된 0기 1 내지 3일째 및 1기 1일째 내지 3일째 세포에 대한, 만능성과 관련된 선택 유전자를 함유하는 만능성 어레이에 대해, 미분화된 세포 대비 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 50은 실시예 14의 프로토콜에 따라 분화된 0기 1 내지 3일째, 1기 1일째 내지 3일째 및 2기 1일째 내지 3일째 세포에 대한, DE와 관련된 선택 유전자를 함유하는 DE 어레이에 대해, 미분화된 세포 대비 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다.
도 51은 실시예 14의 프로토콜에 따라 분화되기 전, 0기 세포에 대해서의 만능성과 관련된 마커(CD184/CXCR4, SSEA4, TRA-1-60 및 TRA-1-81)에 대한 FACS의 결과를 나타낸다. 구체적으로, 도 51은 만능성과 관련된 마커의 고 발현을 나타낸다.
도 52는 실시예 14의 프로토콜에 따라 1기 말기까지 분화된 세포의 완성 내배엽 마커 CXCR4, CD99, 및 CD9에 대한 FACS 도표를 나타낸다.
도 53은 실시예 14의 프로토콜에 따라 분화된 2기 1일째; 2기 2일째 및 2기 3일째 세포에 대한 GAPDH, AFP, HHEX, HNF4α, PDX1, 및 PROX1에 대해, 미분화된 세포 대비 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 53은 전장 유전자(AFP, HHEX, PDX1, 및 PROX1)의 발현에 있어서의 증가를 나타낸다.
도 54는 실시예 14의 프로토콜에 따라 분화된 2기 1일째 내지 3일째 및 3기 1일째 내지 3일째 세포에 대한 GAPDH, AFP, CDX2, GAST, HNF4A, NKX2-2, OSR1, PDX1 및 PFT1A에 대해, 미분화된 세포 대비 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 발현 수준을 나타낸다. 도 54에 나타낸 바와 같이, PDX1에 대한 발현은 2기 3일째 말기에 대조군에 비하여 12,000x로부터 3기 3일째 말기에 대조군에 비하여 739,000x까지 60배 증가하였다.
도 55는 실시예 14의 프로토콜에 따라 분화된 3기 1 내지 3일째 및 4기 1일째 내지 3일째 세포에 대한 소정 유전자에 대해, 미분화된 세포 대비 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 발현 수준을 나타낸다. 구체적으로, 도 55의 상부 패널은 GAPDH, AFP, ALB, ARX, CDX2, CHGA, GAST, GCG, IAAP, INS, ISL1, 및 MAFB에 대한 유전자 발현을 나타낸다. 도 55의 하부 패널은 MAFB, MUCS, NEUROD1, NEUROG3, NKX2-2, NKX6-1, PAX4, PDX1, POUSF1, PTF1A, SST 및 ZlC1의 유전자 발현을 나타낸다.
도 56은 실시예 14의 프로토콜에 따라 분화된 세포에 대한 말기 현미경 사진을 나타낸다. 도 56에서는 0기의 그리고 1 내지 4기의 분화 말기의 세포 클러스터의 대표적인 현미경 사진(4X)을 볼 수 있다.
도 57 내지 도 80은 다음의 유전자에 대한 0시간, 6시간, 24시간, 30시간, 48시간 및 72시간의 분화 후 실시예 15의 프로토콜의 다양한 실시 형태에 따라 분화된 세포에 대해, 미분화된 세포 대비 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다: AFP(도 57); CD99(도 58); CD9(도 59); CDH1(도 60); CDH2(도61); CDX2(도 62); CER1(도63); CXCR4(도 64); FGF17(도 65); FGF4(도 66); FOXA(도67); GADPH(도 68); GATA4(도 69); GATA6(도70); GSC(도 71); KIT(도 72); MIXL1(도 73); MNX1(도 74); NANOG(도 75); OTX2(도 76); POUF5F1(도 77); SOX17(도 78); SOX7(도 79) 및 T(도 80).
도 81은 실시예 15의 프로토콜의 다양한 실시 형태에 따라 6시간, 24시간, 30시간, 48시간, 및 72시간의 분화 후의 세포에 대한 세포 주기의 G0/G1에서의 세포의 백분율을 나타낸다. 구체적으로, 도 81은 다음의 6가지 조건 중 하나로 분화의 1일째에 처리된 클러스터에 대한 결과를 나타낸다: (1) 순수(neat), (2) 3 μM MCX + 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍(Peprotech)), (3) 3 μM MCX 단독, (4) 100 ng/ml GDF-8 단독, (5) 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈(R&D Systems), 미국 미네소타주 소재) + 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재), 또는 (6) 20 ng/ml WNT-3A 단독.
도 82는 실시예 15의 프로토콜에 따라 분화된 세포 클러스터에 대한 EDU 처리의 영향을 나타낸다. 좌측 패널은 실시예 15의 프로토콜의 다양한 실시 형태에 따라 0시간, 6시간, 24시간, 30시간, 48시간 및 72시간의 분화 후의 세포에 대한 세포 주기의 G2/M에서의 세포의 백분율을 나타낸다. 구체적으로, 좌측 패널은 다음의 6가지 조건 중 하나로 분화의 1일째에 처리된 클러스터에 대한 결과를 나타낸다: (1) 순수, (2) 3 μM MCX + 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍), (3) 3 μM MCX 단독, (4) 100 ng/ml GDF-8 단독, (5) 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈, 미국 미네소타주 소재) + 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재), 또는 (6) 20 ng/ml WNT-3A 단독. 하나의 데이터 세트에서는, 이들 클러스터를 또한 EDU로 처리하였다. 도 82의 우측 패널은 실시예 15의 프로토콜의 다양한 실시 형태에 따라 0시간, 6시간, 24시간, 30시간, 48시간, 및 72시간의 분화에서 EDU 양성인 세포의 %를 나타낸다.
도 83은 실시예 15의 프로토콜에서 사용된 일반적인 작동 파라미터를 나타낸다.
도 84는 실시예 15의 프로토콜의 다양한 실시 형태에 따라 6시간, 24시간, 30시간, 48시간 및 72시간의 분화 후의 세포의 EDU 혼입량을 나타낸다. 구체적으로, 도 84는 다음의 6가지 조건 중 하나로 분화의 1일째에 처리된 EDU 인큐베이션된 세포 클러스터에 대한 결과를 나타낸다: (1) 순수, (2) 3 μM MCX + 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍), (3) 3 μM MCX 단독, (4) 100 ng/ml GDF-8 단독, (5) 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈, 미국 미네소타주 소재) + 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재), 또는 (6) 20 ng/ml WNT-3A 단독.
도 85는 실시예 15의 프로토콜의 다양한 실시 형태에 따라 6시간, 24시간, 30시간, 48시간, 및 72시간의 분화 후의 세포에 대한 세포 주기의 G0/G1에서의 세포의 백분율을 나타낸다. 구체적으로, 도 85는 다음의 6가지 조건 중 하나로 분화의 1일째에 처리된 클러스터에 대한 결과를 나타낸다: (1) 순수, (2) 3 μM MCX + 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍), (3) 3 μM MCX 단독, (4) 100 ng/ml GDF-8 단독, (5) 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈, 미국 미네소타주 소재) + 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재), 또는 (6) 20 ng/ml WNT-3A 단독.
도 86은 실시예 15의 다양한 실시 형태에 따라 6시간, 24시간, 30시간, 48시간, 및 72시간의 분화 후의 세포에 대한 세포 주기의 S기에서의 세포의 백분율을 나타낸다. 구체적으로, 도 86은 다음의 6가지 조건 중 하나로 분화의 1일째에 처리된 클러스터에 대한 결과를 나타낸다: (1) 순수, (2) 3 μM MCX + 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍), (3) 3 μM MCX 단독, (4) 100 ng/ml GDF-8 단독, (5) 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈, 미국 미네소타주 소재) + 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재), 또는 (6) 20 ng/ml WNT-3A 단독.
도 87은 실시예 15의 프로토콜의 다양한 실시 형태에 따라 6시간, 24시간, 30시간, 48시간 및 72시간의 분화 후의 세포에 대한 세포 주기의 S기에서의 세포의 백분율을 나타낸다. 구체적으로, 도 87은 다음의 6가지 조건 중 하나로 분화의 1일째에 처리된 클러스터에 대한 결과를 나타낸다: (1) 순수, (2) 3 μM MCX + 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍), (3) 3 μM MCX 단독, (4) 100 ng/ml GDF-8 단독, (5) 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈, 미국 미네소타주 소재) + 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재), 또는 (6) 20 ng/ml WNT-3A 단독.
도 88a 내지 도 88e는 실시예 15의 프로토콜의 다양한 실시 형태에 따라 0시간, 6시간, 24시간, 30시간, 48시간 및 72시간의 분화 후의 분화된 세포에 대해, 미분화된 세포에 대한 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 88a는 CD99, CD9, CDH1 및 CDH2에 대해, 미분화된 세포에 대한 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 88a는 CXD2, CER1, CXCR4 및 FGF17에 대해, 미분화된 세포에 대한 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 88c는 FGF4, FOXA, GATA4 및 GATA6에 대해, 미분화된 세포에 대한 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 88d는 GSC, KIT, MIXL1 및 MNX1에 대해, 미분화된 세포에 대한 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 88e는 NANOG, OTX2, POUF5F1 및 SOX17에 대해, 미분화된 세포에 대한 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 88f는 SOX7 및 T에 대해, 미분화된 세포에 대한 발현 배수로서의, qRT-PCR에 의해 측정하였을 때의 유전자 발현을 나타낸다. 도 88a 내지 도 88f에 대한 기초 데이터는 도 58 내지 도 67 및 도 69 내지 도 80에 나타나 있다.
도 89는 실시예 16의 프로토콜에 따라 외배엽 분화 배지 중에서 배양된 만능 세포의, qRT-PCR에 의해 측정하였을 때의 유전자 발현 패턴을 나타낸다. 도 89에 나타낸 바와 같이, 세포는 신경 세포 계통을 향해 분화되었다. 구체적으로, 도 89의 좌측 패널은 제대 조직 세포(UTC)로부터 생성된 유도 만능 줄기세포주(induced pluripotent stem cell line)에 대한 유전자 발현 패턴을 나타낸다. 도 89의 우측 패널은 H1 hES 세포주의 WB0106 서브-클론(sub-clone)에 대한 유전자 발현 패턴을 나타낸다.
도 90은 실시예 16의 프로토콜에 따라 중배엽 분화 배지 중에서 배양된 만능 세포의, qRT-PCR에 의해 측정하였을 때의 유전자 발현 패턴을 나타낸다. 도 90에 나타낸 바와 같이, 세포는 심장 세포 계통을 향해 분화되었다. 구체적으로, 도 90의 좌측 패널은 제대 조직 세포(UTC)로부터 생성된 유도 만능 줄기세포주에 대한 유전자 발현 패턴을 나타낸다. 도 90의 우측 패널은 H1 hES 세포주의 WB0106 서브-클론에 대한 유전자 발현 패턴을 나타낸다.
도 91은 실시예 16의 프로토콜에 따라 외배엽 분화 배지 중에서 배양된 만능 세포의, qRT-PCR에 의해 측정하였을 때의 유전자 발현 패턴을 나타낸다. 도 91에 나타낸 바와 같이, 세포는 신경 세포 계통을 향해 분화되었다. 구체적으로, 도 91의 좌측 패널은 제대 조직 세포(UTC)로부터 생성된 유도 만능 줄기세포주에 대한 유전자 발현 패턴을 나타낸다. 도 91의 우측 패널은 H1 hES 세포주의 WB0106 서브-클론에 대한 유전자 발현 패턴을 나타낸다.
도 92는 실시예 16의 프로토콜에 따라 외배엽 분화 배지 중에서 3일 동안 배양된 만능 세포의, FACS에 의해 측정하였을 때의, PAX6, SOX2, 및 POU5F1/OCT4에 대한 단백질 발현 패턴을 나타낸다. 구체적으로, 도 92의 좌측 패널은 제대 조직 세포(UTC)로부터 생성된 유도 만능 줄기세포주에 대해서의 PAX6, SOX2, 및 POU5F1/OCT4에 대한 발현 패턴을 나타낸다. 도 92의 우측 패널은 H1 hES 세포주의WB0106 서브-클론에 대해서의 PAX6, SOX2, 및 POU5F1/OCT4에 대한 단백질 발현 패턴을 나타낸다.
도 93은 실시예 16의 프로토콜에 따라 중배엽 분화 배지 중에서 배양된 만능 세포의, qRT-PCR에 의해 측정하였을 때의 유전자 발현 패턴을 나타낸다. 도 93에 나타낸 바와 같이, 세포는 심장 세포 계통을 향해 분화되었다. 구체적으로, 도 93의 좌측 패널은 제대 조직 세포(UTC)로부터 생성된 유도 만능 줄기세포주에 대한 유전자 발현 패턴을 나타낸다. 도 93의 우측 패널은 H1 hES 세포주의 WB0106 서브-클론에 대한 유전자 발현 패턴을 나타낸다.
도 94는 실시예 16의 프로토콜에 따라 중배엽 분화 배지 중에서 분화된 세포에 대한 현미경 사진을 나타낸다. 도 94에 나타낸 바와 같이, 세포는 심장 세포 계통을 향해 분화되었다. 구체적으로, 도 94의 좌측 패널은 분화 3일째, 5일째 및 10일째에 H1 hES 세포주의 WB0106 서브-클론의 세포의 현미경 사진을 나타낸다. 도 94의 우측 패널은 분화 10일 후의 제대 조직 세포로부터 생성된 유도 만능 줄기세포주(UTC iPSC)의 현미경 사진을 나타낸다.
도 95는 실시예 16의 프로토콜에 따라 외배엽 분화 배지 중에서 분화된 세포에 대한 현미경 사진을 나타낸다. 도 95에 나타낸 바와 같이, 세포는 신경 세포 계통을 향해 분화되었다. 구체적으로, 도 95의 좌측 패널은 분화 3일째, 5일째 및 10일째에 H1 hES 세포주의 WB0106 서브-클론의 세포의 현미경 사진을 나타낸다. 도 95의 우측 패널은 분화 10일 후의 제대 조직 세포로부터 생성된 유도 만능 줄기세포주(UTC iPSC)의 현미경 사진을 나타낸다.The foregoing summary, as well as the following detailed description of the invention, will be better understood when read in conjunction with the accompanying drawings. For the purpose of illustrating the invention, the figures show an embodiment of the invention. It should be understood, however, that the invention is not limited to the precise arrangements, embodiments and means illustrated.
FIG. 1A shows the Dispase of human embryonic stem ("hES") cell line H1 immediately after lifting (left panel) and after 24 hours (right panel) ® - micrographs of treated cells. The cells after the lifting (left panel) were similar to those of the monolayer, where the average fragment diameter was about 20-30 micrometers, and each fragment was a clump of cells. After 24 hours in the nonadherent culture, the cells showed a cluster-like structure.
≪ RTI ID = 0.0 > 1B < / RTI > ® 1 medium in a 125 mL spinner flask for 4 days, and then cultured in the presence of disperase in human embryonic stem cell line H1 ® -CD9, < / RTI > SSEA4, CXCR4, TRA-1-60 and TRA-1-81 on the treated cells. Cells showed high expression for the universal markers (CD9, SSEA4, TRA-1-60, and TRA-1-81) while almost no expression of the differentiation marker CXCR4.
Fig. 1C is a graph showing the results of the disruption of the human embryonic stem cell line H1 after 72 and 96- ® - micrographs of treated cells. In FIG. 1c, loose cell aggregates can be seen after 72 hours (left panel) at 4X magnification, after 96 hours at 4X magnification (center panel) and after 96 hours at 10X magnification (right panel).
Figure 1d shows the expression of the first-line differentiation human embryonic stem cell line H1 against the markers CD9, CD184 (CXCR4) and CD99, ® - results of flow cytometry on treated cells (see Example 1). As shown in Fig. 1d, the expression of CD9, a universal marker, was almost completely eliminated, while the expression of CXCR4 (CD184) and CD99 as complete endodermal lobe differentiation markers was very high.
Fig. 1 (e) is a graph showing the comparison of the disrupted H1 (WA01) hES cells of the first stage of the human embryonic stem cell line H1 ® Quantitative reverse transcription polymerase chain reaction (qRT-PCR) results (see Example 1) for the expression of selected genes related to complete endoderm and genes associated with complete pluripotency for treated cells. (CXCR4, CERBERUS (CER1), and CERBERUS (CER1)) in the expression of allelic genes (CD9, NANOG, and POU5F1 / OCT4) in contrast to undifferentiated WA01 hES cells, GSC, FOXA2, GATA4, GATA6, MNX1, and SOX17).
Fig. 1F is a graph showing the results of the dissociation of human embryonic stem cell line H1 from the complete endoderm to the pancreatic endoderm ® - microscope photograph of the treated cells (see Example 1). As the differentiation proceeded from the first day of Day 2 (upper left panel) to the 3rd day of Day 2 (upper right panel), to the fourth day of Day 4 (lower left panel) and the first day of Day 4 (lower right panel) A clear morphological change to the eye becomes visible.
Figure 2a shows the effect of EDTA-treated cells of human embryonic stem cell line H1 on the markers associated with universal and differentiation according to Example 2 after two days of culture in stirred suspension culture after EDTA treatment and before transfer to differentiation cultures Lt; RTI ID = 0.0 > flow cytometry < / RTI > This data showed high expression for the universal markers (CD9, SSEA4, TRA-1-60, and TRA-1-81) with little expression of the differentiation marker (CXCR4).
FIG. 2B is a graph showing the distribution of human embryonic stem cells differentiated into the first day and third day cells grown in a spinner flask according to Example 2 and the second day, second day, fourth day and fourth day cells grown in a spinner flask or an Erlenmeyer flask Figure 2 shows a micrograph of EDTA-treated cells of cell line H1. The suspension-differentiated cultures formed spherical aggregates into a substantially uniform and homogeneous population of cells.
FIG. 2C shows flow cytometry data for EDTA-treated cells of human endometrial stem cell line H1 of the first stage to cell surface markers of pluripotent and endodermal differentiation. FIG. As can be seen in FIG. 2C, the expression of the universal marker CD9 was almost completely eliminated, while the expression of CXCR4 (CD184), a marker for complete endodermal development, was very high.
Figure 2d shows qRT-PCR for expression of selected endogenous genes associated with complete endoderm-related genes for EDTA-treated cells of the
FIG. 2E is a graph showing the results of the differentiation of EDTA-treated cells of human embryonic stem cell line H1 differentiated into pancreatic endoderm cells from a
Figure 2f shows the expression of selected genes involved in the differentiation of EDTA-treated cells of human embryonic stem cell line H1 further differentiated into pancreatic endoderm cells from
FIG. ® Lt; RTI ID = 0.0 > H1 < / RTI > As shown in Figure 3A, the cells were removed from the surface as small aggregates.
FIG. ® Lt; / RTI > shows a phase contrast microscope photograph of the cells of a human embryonic stem cell line H1 that has been lifted from a static culture after treatment with a human embryonic stem cell line H1 and then amplified in suspension culture for 3 days. In Figure 3b, formation of a substantially uniform spherical population of cell clusters can be seen.
FIG. 3c is a cross- ® And then amplified in suspension culture for 3 days, and then incubated with an incubator ® Lt; / RTI > shows a microscope photograph of a cluster of cells of human embryonic stem cell line H1 that has been continuously passaged using dissociation.
Figure 4a shows a micrograph of human embryonic stem cells suspended in culture of cell line H1 using differentiated protocols at different stages of differentiation. In Figure 4a, a micrograph of the cells in each step of differentiation can be seen.
Figure 4b shows the results of flow cytometry on differentiation markers (CXCR4, CD56 and PDX1) for suspension cultured human embryonic stem cells of cell line H1 using differentiation protocols at different stages of differentiation (time after onset of differentiation). At the end of the 4th day of differentiation, a high percentage of cells were positive for PDX1 expression.
Figure 4c shows the non-fasting blood glucose levels of SCID-Bg mice transplanted with differentiated cells encapsulated in a TheraCyte (TM) device.
Figure 5a shows data for flow cytometry on EDTA-treated cells of human embryonic stem cell line H1 prior to transfer to differentiation cultures for markers associated with universality and differentiation. As shown in Fig. 5A, high expression of pluripotency markers CD9, SSEA4, TRA-1-60 and TRA-1-80 was observed.
Figure 5b shows data of cell phase contrast and flow cytometry for CXCR4 / CD184 and CD99 (differentiation markers) and CD9 (universal marker) for three different feed settings during the first period. The conditions tested were as follows: (A) medium replacement at 24 hours after initiation of differentiation, no medium change at 48 hours; (B) 24 hours after the start of differentiation, and glucose bolus added at 48 hours; And (C) Glucose and GDF8 bolus were added at 24 hours after the start of differentiation, without replacing the medium throughout the first period, followed by addition of glucose bolus at 48 hours after initiation.
Figure 5c shows phase contrast images of differentiated cells exhibiting pancreatic endoderm morphology differentiated using the following feed settings during the formation of complete endoderm: (A) medium replacement at 24 hours after initiation of differentiation, at 48 hours No badge replacement; (B) 24 hours after the start of differentiation, and glucose bolus added at 48 hours; And (C) Glucose and GDF8 bolus were added at 24 hours after the start of differentiation, without replacing the medium throughout the first period, followed by addition of glucose bolus at 48 hours after initiation.
Figure 5d shows the selection markers of pancreatic gene expression (NKX6.1 and chromogranin) and the selective non-pancreatic gene (s) of the end-
Figure 5e shows the results of qRT-PCR for selective pancreas gene expression and non-pancreatic gene expression for differentiated cells at the
Figure 5f shows the expression of C-peptide in SCID-Bg mice transplanted with differentiated cells according to the condition A (medium replacement at 24 hours after initiation of differentiation and no medium change at 48 hours). Each SCID-Bg mouse was implanted with 5 million cells under the renal capsule. As shown in FIG. 5f, up to 12 weeks post-transplantation, human C-peptide was detectable at levels above 1 ng / mL and at 16 weeks the C-peptide level was 2.5 ng / mL on average.
Figure 5g shows the effect of glucose on selected SCID-Bg mice before and after administration of differentiated cells (e. G., Transplant) according to the condition A (medium replacement at 24 hours after start of differentiation and no medium change at 48 hours) Indicating the effect of treatment. As shown in Figure 5g, glucose treatment induced a significant increase in circulating human C-peptide from an average of 0.93 ng / mL in the fasted state to 2.39 ng / mL in the fed state.
Figure 5h shows the effect of streptozotocin (STZ) administration (i.e. STZ-Bg) on SCID-Bg mice to which differentiated cells were administered according to the condition A (medium replacement at 24 hours after start of differentiation and no medium change at 48 hours) Induced diabetes). As is apparent from Figure 5h, animals with functional GSIS competent tissue grafts (i. E., Those administered with cells), unlike the untreated controls - which had clinically significant diabetes mellitus - Blood glucose levels were maintained.
FIG. 6A is a
FIG. 6b shows the results of the cytotoxic < RTI ID = 0.0 > ® 3 microcarrier beads of human embryonic stem cell line H1.
Fig. 6C shows a graph showing the activity of microparticles containing microcarriers (WTN3A / AA microcarriers), MCX and GDF8 in media containing plates (WTN3A / AA plate), actin A and WNT3A in media containing actin A (AA) and WNT3A Cell counts as a function of differentiation days for cells of human embryonic stem cell line H1 grown and differentiated on microcarriers (MCX / GDF8 microcarriers) in medium containing plates (MCX / GDF8 plates) and MCX and GDF8 in medium Number / cm < 2 >).
FIG. 6D shows a plate (FIG. 6D) in a medium containing microcarriers (WTN3A / AA microcarrier), MCX and GDF8 in a medium containing plates (WTN3A / AA plate), actin A and WNT3A in a medium containing actin A and WNT3A (Number of cells / ml as a function of days of differentiation for cells of human embryonic stem cell line H1 grown and differentiated on microcarriers (MCX / GDF8 microcarrier) in media containing MCX / GDF8 plates and MCX / ).
Figure 6e shows the results of flow cytometry for the first differentiation stage of cells grown on microcarrier cultures or flat cultures in the presence of: cells of CXCR4 / CD184 (Y-axis) and CD9 (X-axis) (A) WNT3A and AA as point plot of expression; Or (2) MCX and GDF8.
Figure 6f shows the results of flow cytometry for the first differentiation stage of cells grown on microcarrier cultures or planar cultures in the presence of: (a) WNT3A and AA as the total expression of each of the markers (CXCR4 and CD9) ; Or (2) MCX and GDF8.
Figure 6g shows the results of qRT-PCR for the expression of selected genes involved in the differentiation of human embryonic stem cell line H1 differentiated by growing on microcavity beads in flat culture or suspension culture in the presence of: ( a) WNT3A and AA; Or (2) MCX and GDF8.
Figure 7 shows cell counts at various differentiation stages in the bioreactor from
Figure 8 shows the daily average bioreactor culture pH level as a function of time (number of days of differentiation) during the differentiation protocol of Example 7. The pH levels were measured by NOVA BioFile® FLEX (Nova Biomedical Corporation, Waltham, Mass., USA).
Figure 9 shows the daily average bioreactor culture lactate levels as a function of time (number of differentiation days) during the differentiation protocol of Example 7. Lactate levels were measured by Nova BioProfile 占 flex (Nova Biomedical Corporation, Waltham, Mass., USA).
Figure 10 shows the daily average bioreactor medium glucose level as a function of time (number of differentiation days) during the differentiation protocol of Example 7. Glucose levels were measured by Nova BioProfile ' Flex (Nova Biomedical Corporation, Waltham, Mass., USA).
11 was measured by qRT-PCR for a universal array containing selectable genes associated with pluripotency for cells on
Figure 12 is a graph showing the percentage of the total endoderm arrays containing the selected genes associated with complete endoderm ("DE") for cells on day 0 (ie, 24 hours post-inoculation) (See Example 7).
Figure 13 shows undifferentiated gene expression as measured by qRT-PCR for a universal array containing selectable genes associated with pluripotency on cells at day 0 (ie, 72 hours post-inoculation) at
Figure 14 shows the undifferentiated gene expression as measured by qRT-PCR on a DE array containing a DE-associated selection gene for cells on Day 0 (ie, 72 hours post-inoculation) on
Figure 15 shows the fluorescence-activated cell sorting (FACS) for CD9, CD184 / CXCR4, SSEA4, TRA-1-60 and TRA- 1-81 against cells on
16 is a graph showing the results of qRT-PCR for selected genes of cells differentiated according to the protocol of Example 7 on day 0 (
FIG. 17 is a graph showing the relationship between the content of the DE-related selection gene and the expression level of the selective gene for DE in the cells differentiated according to the protocol of Example 7 on day 0 (
FIGS. 18 and 19 show gene expression for the first day cell differentiated according to the protocol of Example 7. FIG. Figure 18 shows gene expression as measured by qRT-PCR for a universal array containing selectable genes associated with pluripotency for cells at
FIGS. 20 and 21 show gene expression for the third day cell differentiated according to the protocol of Example 7. FIG. Figure 20 shows gene expression as measured by qRT-PCR for a universal array containing selectable genes associated with pluripotency for cells at
Figure 22 shows the results of FACS on CD9, CD184 (also known as CXCR4) and CD99 for cells on
Figure 23 shows the results of the first day of the third day differentiated according to the protocol of Example 7;
FIG. 24 shows gene expression of the full-length genes AFP, PDX1, and PROX1 as measured by qRT-PCR for the first day-2 cells and the third day-two cells differentiated according to the protocol of Example 7. FIG. As shown in Fig. 24, the expression of these genes was increased.
Figure 25 shows the results of FACS for PDX1, FOXA2, chromogranin NKX2.2 and SOX2 against cells grown at
Figure 26 shows the gene expression when measured by qRT-PCR for a four-ary array containing a selection gene associated with the 4th, 3rd, and
FIG. 27 shows the FACS results for NKX6.1, chromagranin (CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 and NEUROD on the fourth day of
28 shows the third day of the third day differentiated according to the protocol of Example 7; Gene expression as measured by qRT-PCR for a four-ary array containing a selection gene associated with
Figure 29 shows the mean results of FACS for NKX6.1, chromagranin (CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 and NEUROD on the
Figure 30 shows the mean results of FACS for NKX6.1, chromagranin (CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 and NEUROD on the
Figure 31 shows the mean of FACS for NKX6.1, chromagranin (CHGA), CDX2, SOX2, NKX2.2, PDX1, FOXA2 and NEUROD versus NKX6.1, chromagranin (See Example 7). There was no significant change in the cell profile on
32 is a graph showing the results of NKX6.1, chromogranin (CHGA), and cholinergin (NOS) treatment on the third and fourth day cells untreated with Anti-Foam C and the third and fourth day cells treated with the defoamer C emulsion (94 ppm) CDX2, SOX2, NKX2.2, PDX1, FOXA2 and NEUROD (see Example 7). The defoamer C emulsion (Sigma catalog number A8011) was not observed to affect the profile of the cells at
33 to 35 show gene expression as measured by qRT-PCR for a selection gene for cells differentiated according to the protocol of Example 8. Fig. Fig. 33 shows gene expression when measured by qRT-PCR on the cell selection gene at 24 hours before the initiation of differentiation (see Example 8). As shown in Figure 33, the cells from the bioreactor retained expression for the genes characteristic of universality (POU5F1, NANOG, SOX2, and ZFP42), and the genes characteristic of differentiation (AFP, and FOXA2: Increased expression of FOXD3, GATA2, GATA4, GSC, HAND2, MIXL1 and T: less than 10-fold). Fig. 34 shows gene expression as measured by qRT-PCR on the cell selection gene at 24 hours after the initiation of differentiation. 35 shows gene expression when measured by qRT-PCR on the cell selection gene at 72 hours after the initiation of differentiation.
Figures 36A to 36E show gene expression as measured by qRT-PCR on select genes for cells differentiated from
Figure 37 shows gene expression as measured by qRT-PCR, with respect to the selection gene for the fourth day and third cell of differentiation according to the protocol in Example 8. As shown in Fig. 37, at the end of differentiation on the third day of the third day, the cells showed a high expression level of PDX1 (1 x 10 < 6 Induction of overexpression of overexpression of the pancreas gene (ARX, GCG, GAST, INS, ISL, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PTF1a, and SST) Lt; RTI ID = 0.0 > OCT4 / POU5F1 < / RTI > expression.
38 shows the daily cell count during the differentiation protocol according to Example 8. Fig. Specifically, Figure 38 shows the cell density as a function of the number of days of the process. Figure 38 shows the cell counts for the differentiation protocol of the two reactor runs (PRD1205 and PRD1207) performed at pH 6.8 and 7.2. For comparison, cell counts for cell drift are also shown.
Figures 39a-39d show in vivo (Fig. 39a-d) the cell of
Figures 40A-40D show MCX compounds and GDF-8 (Figure 40A); MCX alone (Fig. 40b); WNT3A and actin A (Figure 40c); And FACS charts for CXCR4, CD99, and CD9 of cells differentiated for 3 days according to the protocol of Example 9, treated on
Figures 41a-d show FACS plots for CXCR4, CD99 and CD9 of cells differentiated for 3 days according to the protocol of Example 10, treated with varying amounts of MCX on
42A and 42B show FACS charts for CXCR4, CD99 and CD9 of cells differentiated for 3 days according to the protocol of Example 11. FIG. Specifically, these figures show the role of the frequency of medium replacement in the suspension culture. Figure 42A shows a FACS chart for CXCR4, CD99 and CD9 of cells differentiated for 3 days according to the protocol of Example 10 with complete media change in one cell. Figure 42B shows a FACS chart for CXCR4, CD99 and CD9 of cells differentiated for 3 days according to the protocol of Example 10 without medium change on the third day. The data suggest that in the suspension culture system, the culture medium replaced on
Figures 43A and 43B show FACS charts for CXCR4, CD99 and CD9 of cells differentiated for 3 days according to the protocol of Example 12. Specifically, these figures illustrate the role of GlutaMAX ™ in suspension cultures. Cells were cultured in 1 medium supplemented with 1X Glutamax ™ (FIG. 43a) or in Glutamax ™ or no glutamine (0 M glutamax ™) (FIG. 43b) medium. The data suggest that, in suspension culture systems, the addition of glutamax ™ does not appear to affect the efficacy of producing complete endoderm.
44A-44D show the effect of varying amounts of sodium bicarbonate on the differentiated cells according to the protocol of Example 13. FIG. Figures 44a and 44b show CXCR4, CD99, and / or CXCR4 of cells differentiated for 3 days according to the protocol of Example 13 using 3.64 g / l (Figure 44a) or 2.49 g / l (Figure 44b) FACS diagram for CD9 is shown. Figures 44c and 44d show phase contrast microphotographs of cells differentiated for 3 days according to the protocol of Example 13 using 3.64 g / l (Figure 44c) or 2.49 g / l (Figure 44d) .
Figure 45 shows the daily cell counts for cell density as a function of differentiation for differentiated cells according to the protocol of Example 14. Cell counts were obtained using an image-based cell counter (NucleoCounter®).
46 shows the daily average bioreactor culture pH level as a function of time (number of differentiation days) during the differentiation protocol of Example 14. FIG. The pH levels were measured by Nova BioProfile 占 flex (Nova Biomedical Corporation, Waltham, Mass., USA).
Figure 47 shows daily average bioreactor medium glucose levels as a function of time (number of differentiation days) during the differentiation protocol of Example 14. Glucose levels were measured by Nova BioProfile ' Flex (Nova Biomedical Corporation, Waltham, Mass., USA).
Figure 48 shows the daily average bioreactor culture lactate levels as a function of time (number of days of differentiation) during the differentiation protocol of Example 14. Lactate levels were measured by Nova BioProfile 占 flex (Nova Biomedical Corporation, Waltham, Mass., USA).
49 is a graph showing the effect of a pluripotent cell-versus-expression ratio versus an undifferentiated cell-versus-host cell ratio for a pluripotent array containing pluripotency-related selection genes for
Figure 51 shows the results of FACS on markers (CD184 / CXCR4, SSEA4, TRA-1-60 and TRA-1-81) related to the universality for
52 shows FACS diagrams for the completed endoderm markers CXCR4, CD99, and CD9 of the cells differentiated to the
53 shows the first day of the second stage differentiated according to the protocol of Example 14; GAPDH, AFP, HHEX, HNF4 ?, PDX1, and PROX1 on
FIG. 54 is a graph showing the effect of GAPDH, AFP, CDX2, GAST, HNF4A, NKX2-2, OSR1, PDX1 and PFT1A on the cells of
FIG. 55 shows the results obtained when qRT-PCR, as a multiple of expression relative to undifferentiated cells, for a given gene for cells of
56 shows an end-stage micrograph of cells differentiated according to the protocol of Example 14. Fig. In Figure 56, a representative micrograph (4X) of cell clusters of the 0 and 1 to 4 differentiation stages can be seen.
Figures 57 to 80 show that for cells differentiated according to various embodiments of the protocol of Example 15 after differentiating 0 hours, 6 hours, 24 hours, 30 hours, 48 hours and 72 hours for the following genes, Expression of gene when measured by qRT-PCR as expression multiple relative to cells: AFP (Figure 57); CD99 (Figure 58); CD9 (Figure 59); CDH1 (Fig. 60); CDH2 (Figure 61); CDX2 (Figure 62); CER1 (Fig. 63); CXCR4 (Fig. 64); FGF17 (Fig. 65); FGF4 (Fig. 66); FOXA (Fig. 67); GADPH (Figure 68); GATA4 (Fig. 69); GATA6 (Fig. 70); GSC (Fig. 71); KIT (Fig. 72); MIXL1 (Fig. 73); MNX1 (Fig. 74); NANOG (Fig. 75); OTX2 (Figure 76); POUF5F1 (Fig. 77); SOX17 (Fig. 78); SOX7 (FIG. 79) and T (FIG. 80).
Figure 81 shows the percentage of cells in G0 / G1 of the cell cycle to cells after 6 hours, 24 hours, 30 hours, 48 hours, and 72 hours of differentiation according to various embodiments of the protocol of Example 15. Specifically, Figure 81 shows the results for clusters treated on the first day of differentiation in one of six conditions: (1) neat, (2) 3 μM MCX + 100 ng / ml GDF-8 (3) 3 μM MCX alone, (4) 100 ng / ml GDF-8 alone, (5) 20 ng / ml WNT-3A (catalog number 1324-WN- 002 (R & D Systems, Minnesota, USA) + 100 ng / ml Activin A (catalog number 338-AC from R & D Systems, Minn. .
82 shows the effect of EDU treatment on cell clusters differentiated according to the protocol of Example 15. Fig. The left panel shows the percentage of cells in G2 / M of the cell cycle to cells after differentiation at 0 hour, 6 hours, 24 hours, 30 hours, 48 hours and 72 hours according to various embodiments of the protocol of Example 15 . Specifically, the left panel shows the results for clusters treated on the first day of differentiation in one of the following six conditions: (1) pure, (2) 3 μM MCX + 100 ng / ml GDF-8 (3) 3 μM MCX alone, (4) 100 ng / ml GDF-8 alone, (5) 20 ng / ml WNT-3A (catalog number 1324-WN-002, MN, USA) or (6) 20 ng / ml WNT-3A alone. In one data set, these clusters were also processed with EDUs. The right panel of Figure 82 shows the percentage of EDU-positive cells at 0 hour, 6 hour, 24 hour, 30 hour, 48 hour, and 72 hour differentiation according to various embodiments of the protocol of Example 15.
83 shows the general operating parameters used in the protocol of Example 15. Fig.
84 shows the EDU incorporation of cells after 6 hours, 24 hours, 30 hours, 48 hours, and 72 hours of differentiation according to various embodiments of the protocol of Example 15. FIG. Specifically, Figure 84 shows the results for EDU incubated cell clusters treated on the first day of differentiation in one of six conditions: (1) pure, (2) 3 μM MCX + 100 ng / ml GDF-8 (Catalog No. 1324-WN-002, Catalog No. 120-00, Peprotec), (3) 3 μM MCX alone, (4) 100 ng / ml GDF- USA), or (6) 20 ng / ml WNT-3A alone, with the addition of 100 ng / ml Activin A (Catalog No. 338-AC, RAND Systems, Minn.
85 shows the percentage of cells in G0 / G1 of the cell cycle to cells after differentiation at 6 hours, 24 hours, 30 hours, 48 hours, and 72 hours, according to various embodiments of the protocol of Example 15. FIG. Specifically, Figure 85 shows the results for clusters treated on the first day of differentiation in one of six conditions: (1) pure, (2) 3 μM MCX + 100 ng / ml GDF-8 (3) 3 μM MCX alone, (4) 100 ng / ml GDF-8 alone, (5) 20 ng / ml WNT-3A (catalog number 1324-WN-002, MN, USA) or (6) 20 ng / ml WNT-3A alone.
86 shows the percentage of cells in the S phase of the cell cycle relative to the cells after 6 hours, 24 hours, 30 hours, 48 hours, and 72 hours of differentiation according to various embodiments of Example 15. FIG. Specifically, Figure 86 shows the results for clusters treated on the first day of differentiation in one of six conditions: (1) pure, (2) 3 μM MCX + 100 ng / ml GDF-8 (3) 3 μM MCX alone, (4) 100 ng / ml GDF-8 alone, (5) 20 ng / ml WNT-3A (catalog number 1324-WN-002, MN, USA) or (6) 20 ng / ml WNT-3A alone.
Figure 87 shows the percentage of cells in the S phase of the cell cycle versus cells after 6 hours, 24 hours, 30 hours, 48 hours, and 72 hours of differentiation according to various embodiments of the protocol of Example 15. Specifically, Figure 87 shows the results for clusters treated on the first day of differentiation in one of six conditions: (1) pure, (2) 3 μM MCX + 100 ng / ml GDF-8 (3) 3 μM MCX alone, (4) 100 ng / ml GDF-8 alone, (5) 20 ng / ml WNT-3A (catalog number 1324-WN-002, MN, USA) or (6) 20 ng / ml WNT-3A alone.
Figures 88a-88e are graphs showing the effect of differentiation times on differentiated cells after 0 hour, 6 hours, 24 hours, 30 hours, 48 hours and 72 hours of differentiation according to various embodiments of the protocol of Example 15 , As measured by qRT-PCR. 88a shows gene expression as measured by qRT-PCR as expression multiples for undifferentiated cells for CD99, CD9, CDH1 and CDH2. 88a shows gene expression as measured by qRT-PCR as expression multiples for undifferentiated cells for CXD2, CER1, CXCR4 and FGF17. Figure 88c shows gene expression as measured by qRT-PCR as an expression multiple for undifferentiated cells for FGF4, FOXA, GATA4 and GATA6. Figure 88d shows gene expression as measured by qRT-PCR as expression multiple for undifferentiated cells for GSC, KIT, MIXL1 and MNXl. Figure 88E shows gene expression as measured by qRT-PCR as an expression multiple for undifferentiated cells for NANOG, OTX2, POUF5F1 and SOX17. 88F shows gene expression as measured by qRT-PCR as an expression multiple for undifferentiated cells, for SOX7 and T; The basic data for Figs. 88A to 88F are shown in Figs. 58 to 67 and Fig. 69 to Fig.
89 shows gene expression patterns of pluripotent cells cultured in an exocytic differentiation medium according to the protocol of Example 16 as measured by qRT-PCR. As shown in Figure 89, the cells were differentiated toward the neuronal lineage. Specifically, the left panel of FIG. 89 shows a gene expression pattern for an induced pluripotent stem cell line generated from cord tissue cells (UTC). The right panel of Figure 89 shows the gene expression pattern for the WB0106 sub-clone of the H1 hES cell line.
90 shows gene expression patterns of pluripotent cells cultured in mesodermal differentiation medium according to the protocol of Example 16 as measured by qRT-PCR. As shown in Figure 90, the cells were differentiated toward the cardiac cell lineage. Specifically, the left panel of FIG. 90 shows a gene expression pattern for an induced pluripotent stem cell line generated from cord tissue cells (UTC). The right panel of Figure 90 shows the gene expression pattern for the WB0106 sub-clone of the H1 hES cell line.
91 shows gene expression patterns of pluripotent cells cultured in an exocytic differentiation medium according to the protocol of Example 16 as measured by qRT-PCR. As shown in FIG. 91, the cells were differentiated toward the neuronal lineage. Specifically, the left panel of FIG. 91 shows a gene expression pattern for an induced pluripotent stem cell line generated from umbilical cord tissue cells (UTC). The right panel of FIG. 91 shows the gene expression pattern for the WB0106 sub-clone of the H1 hES cell line.
92 shows a protein expression pattern for PAX6, SOX2, and POU5F1 / OCT4, as measured by FACS, of pluripotent cells cultured for 3 days in an exocytic differentiation medium according to the protocol of Example 16. Fig. Specifically, the left panel of FIG. 92 shows the expression pattern for PAX6, SOX2, and POU5F1 / OCT4 on the induced pluripotent stem cell lines generated from cord tissue cells (UTC). The right panel of Figure 92 shows the protein expression patterns for PAX6, SOX2, and POU5F1 / OCT4 on the WB0106 sub-clone of the H1 hES cell line.
93 shows gene expression patterns of pluripotent cells cultured in mesodermal differentiation medium according to the protocol of Example 16 as measured by qRT-PCR. 93, the cells were differentiated toward the cardiac cell line. Specifically, the left panel of FIG. 93 shows a gene expression pattern for an induced pluripotent stem cell line generated from cord tissue cells (UTC). The right panel of Figure 93 shows the gene expression pattern for the WB0106 sub-clone of the H1 hES cell line.
94 shows a photomicrograph of cells differentiated in mesodermal differentiation medium according to the protocol of Example 16. Fig. As shown in Figure 94, cells were differentiated toward the cardiac cell lineage. Specifically, the left panel of FIG. 94 shows a micrograph of cells of the WB0106 sub-clone of the H1 hES cell line on
95 shows a photomicrograph of cells differentiated in differentiation medium according to the protocol of Example 16. Fig. As shown in Figure 95, the cells were differentiated toward the neuronal lineage. Specifically, the left panel of Figure 95 shows a micrograph of the cells of the WB0106 sub-clone of the H1 hES cell line on
본 출원은 내배엽 선조세포, 췌장 내분비 세포, 중배엽 세포 또는 외배엽 세포로의 분화를 위한 응집된 세포 클러스터에서 만능성을 유지하는 배아줄기세포 및 다른 만능 세포를 제조하는 것에 관한 것이다. 개시내용의 명확함을 위하여, 그리고 제한하지 않고서, 본 발명의 상세한 설명은 본 발명의 소정의 특징, 실시 형태, 또는 응용을 설명하거나 예시하는 하기의 세부 항목으로 나뉘어진다.The present application relates to the production of embryonic stem cells and other pluripotent cells that maintain universality in aggregated cell clusters for differentiation into endodermal progenitor cells, pancreatic endocrine cells, mesodermal cells or ectodermal cells. For purposes of clarity of disclosure and without limitation, the detailed description of the invention is divided into the following subsections that describe or illustrate certain features, embodiments, or applications of the present invention.
정의Justice
줄기세포는 단일 세포 수준에서 그의 자가-재생 및 분화 능력 둘 모두에 의해 규정되는 미분화된 세포이다. 줄기세포는 자가-재생 선조세포, 비-재생 선조세포, 및 최종 분화된 세포를 포함하는 자손 세포를 생성할 수 있다. 줄기세포는 또한 시험관내(in vitro)에서 다수의 배엽층(내배엽, 중배엽 및 외배엽)으로부터 다양한 세포 계통의 기능적 세포로 분화하는 그의 능력을 특징으로 한다. 또한, 줄기세포는 이식 후에 다수의 배엽층의 조직을 발생시키며, 배반포 내로의 주입 이후, 비록 전부는 아니더라도, 실질적으로 대부분의 조직에 기여한다.Stem cells are undifferentiated cells that are defined by both their self-renewal and differentiation capacity at the single cell level. Stem cells can produce progeny cells that include self-renewing progenitor cells, non-regenerating progenitor cells, and terminally differentiated cells. Stem cells are also characterized in vitro by their ability to differentiate into multiple cell lineage functional cells from multiple germ layers (endoderm, mesoderm and ectoderm). In addition, stem cells give rise to a large number of germinal layer tissues after transplantation and contribute substantially to most tissues, although not all, after injection into blastocysts.
줄기세포는 그들의 발생능(developmental potential)에 의해 분류된다. "세포 배양물" 또는 "배양"은 일반적으로 살아있는 유기체로부터 취해져서 제어된 조건 하에서 성장된 ("배양물 중" 또는 "배양된") 세포를 말한다. 1차 세포 배양물은 첫 번째 계대배양(subculture) 전에 유기체로부터 직접 취해진 세포, 조직, 또는 기관의 배양물이다. 세포는 세포 성장 및 분열 중 하나 또는 둘 모두를 촉진시키는 조건 하에서 성장 배지 중에 놓여질 때, 배양물 중에서 증폭되어, 더 큰 세포 집단을 생성한다. 세포가 배양물 중에서 증폭되는 경우, 세포 증식의 속도는 때때로, 세포의 수가 2배가 되는 데 필요한 시간의 양으로 측정된다(배가 시간(doubling time)으로 지칭됨).Stem cells are classified by their developmental potential. "Cell culture" or "cultivation " refers generally to cells that are taken from a living organism and grown under controlled conditions (" in culture "or" cultured "). Primary cell cultures are cultures of cells, tissues, or organs taken directly from the organism prior to the first subculture. When cells are placed in a growth medium under conditions that promote either or both cell growth and division, they are amplified in culture to produce a larger population of cells. When cells are amplified in culture, the rate of cell proliferation is sometimes measured in terms of the amount of time required to double the number of cells (referred to as doubling time).
본 명세서에 사용되는 바와 같이, "증폭"은, 배양에 의해 만능 줄기세포의 수를, 예를 들어 적어도 약 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 75%, 90%, 100%, 200%, 500%, 1000% 또는 그 이상, 및 이들 백분율 이내의 수준으로 증가시키는 과정이다. 단일의 만능 줄기세포로부터 수득될 수 있는 만능 줄기세포의 수는 만능 줄기세포의 증식 능력에 의존하는 것으로 이해된다. 만능 줄기세포의 증식 능력은 세포의 배가 시간, 즉, 세포가 배양물 중에서 유사분열을 거치는 데 필요한 시간, 및 만능 줄기세포가 미분화된 상태로 유지될 수 있는 기간 - 이는 계대배양의 횟수에 각각의 계대배양 사이의 일수를 곱한 값에 상당함 - 에 의해 계산될 수 있다.As used herein, "amplification" means that the number of pluripotent stem cells is increased by culturing, for example at least about 5%, 10%, 15%, 20%, 25%, 30%, 35% %, 45%, 50%, 60%, 75%, 90%, 100%, 200%, 500%, 1000% or more, and levels within these percentages. It is understood that the number of pluripotent stem cells that can be obtained from a single pluripotent stem cell depends on the proliferative capacity of pluripotent stem cells. The proliferative capacity of pluripotent stem cells is determined by the time of doubling of the cells, the time required for the cells to undergo mitosis in the culture, and the period during which pluripotent pluripotent stem cells can be maintained in an undifferentiated state, Which corresponds to a value obtained by multiplying the number of days between subculture cultures.
분화는 특화되지 않은("미결정된(uncommitted)") 또는 덜 특화된 세포가 신경 세포 또는 근육 세포와 같은 특화된 세포의 특징을 획득하는 과정이다. 분화된 세포 또는 분화-유도된 세포는 세포 계통 내에서 더 특화된(결정된("committed")) 위치를 차지한 것이다. 분화 과정에 적용될 때, 용어 "결정된"은 분화 경로에서, 정상 환경 하에 특정 세포 유형 또는 세포 유형의 서브세트로 계속 분화될 것이며, 정상 환경 하에 상이한 세포 유형으로 분화될 수 없거나 덜 분화된 세포 유형으로 돌아갈 수 없는 시점까지 진행된 세포를 말한다. "탈분화(de-differenciation)"는 세포가 세포의 계통 내의 덜 특화된(또는 결정된) 위치로 되돌아가는 과정을 말한다. 본 명세서에 사용되는 바와 같이, 세포 "계통"은 세포의 유전, 즉, 그것이 어느 세포로부터 유래되었는지 그리고 그것이 어떤 세포를 발생시킬 수 있는지를 규정한다. 세포의 계통은 그 세포를 발생과 분화의 유전적 체계 내에 둔다. 계통 특이적 마커는 관심있는 계통의 세포의 표현형과 특이적으로 관련된 특징을 말하며, 미결정된 세포가 관심있는 계통으로 분화하는지를 평가하기 위해 사용될 수 있다.Differentiation is the process by which unspecialized ("uncommitted") or less specialized cells acquire the characteristics of specialized cells such as neurons or muscle cells. Differentiated or differentiated-derived cells have occupied a more specialized (committed) position within the cell lineage. When applied to a differentiation process, the term "determined" will continue to differentiate into a particular cell type or subset of cell types under normal circumstances in the differentiation pathway, and can not differentiate into different cell types under normal circumstances, It refers to a cell that has progressed to the point where it can not return. "De-differentiation" refers to the process by which a cell returns to a less specialized (or determined) location in a cell's system. As used herein, a cell "lineage" defines the genome of a cell, i.e., from which cell it is derived, and what cell it can produce. The cell system places the cell in the genetic system of development and differentiation. Lineage-specific markers are those characteristics that are specifically associated with the phenotype of a cell of the line of interest and can be used to assess whether undifferentiated cells differentiate into lines of interest.
본 명세서에 사용되는 바와 같이, "마커"는 관심있는 세포에서 차등적으로 발현되는 핵산 또는 폴리펩타이드 분자이다. 이러한 맥락에서, 차등 발현(differential expression)은 미분화된 세포와 대비하여 양성 마커에 대해서는 증가된 수준을 그리고 음성 마커에 대해서는 감소된 수준을 의미한다. 마커 핵산 또는 폴리펩타이드의 검출가능한 수준은 다른 세포와 대비하여 관심있는 세포에서 충분히 더 높거나 더 낮음으로써, 관심있는 세포가 당업계에 알려진 다양한 방법 중 임의의 것을 사용하여 다른 세포로부터 확인 및 구별될 수 있도록 한다.As used herein, a "marker" is a nucleic acid or polypeptide molecule that is differentially expressed in a cell of interest. In this context, differential expression refers to an increased level for positive markers and a reduced level for negative markers as compared to undifferentiated cells. The detectable level of the marker nucleic acid or polypeptide is sufficiently high or lower in the cell of interest compared to other cells so that the cell of interest is identified and distinguished from the other cell using any of the various methods known in the art .
본 명세서에 사용되는 바와 같이, 세포는 특정 마커에 "대하여 양성"이거나 또는 특정 마커가 그 세포에서 충분히 검출될 때 "양성"이다. 유사하게, 세포는 특정 마커에 "대하여 음성"이거나 또는 특정 마커가 그 세포에서 충분히 검출되지 않을 때 "음성"이다. 특히, FACS에 의한 양성은 통상 2% 초과인 반면, FACS에 의한 음성 역치(threshold)는 통상 1% 미만이다. PCR에 의한 양성은 통상 34회 주기(Ct) 미만인 반면; PCR에 의한 음성은 통상 34.5회 주기 초과이다.As used herein, a cell is "positive" for a particular marker or "positive" when a particular marker is sufficiently detected in the cell. Similarly, a cell is "negative" to a particular marker or "negative" when a particular marker is not fully detected in the cell. In particular, positive by FACS is usually more than 2%, whereas negative threshold by FACS is usually less than 1%. Positivity by PCR is usually less than 34 cycles (Ct); The negative by PCR is usually over 34.5 cycles.
본 명세서에 사용되는 바와 같이, "세포 밀도" 및 "시딩 밀도(seeding density)"는 본 명세서에서 상호교환가능하게 사용되며, 고체 또는 반고체 평면 또는 곡면 기질의 단위 면적당 시딩된 세포의 수를 지칭한다.As used herein, "cell density" and "seeding density" are used interchangeably herein and refer to the number of cells seeded per unit area of solid or semi-solid planar or curved substrate .
본 명세서에 사용되는 바와 같이, "현탁 배양물"은 표면에 부착되기보다는 오히려 배지 중에 현탁된 세포, 단일 세포 또는 클러스터의 배양물을 말한다.As used herein, "suspension culture" refers to a culture of cells, single cells or clusters suspended in a medium rather than attached to a surface.
본 명세서에 사용되는 바와 같이, "무혈청(serum free)"은 인간 또는 동물 혈청이 없음을 말한다. 따라서, 무혈청 배양 배지는 혈청 또는 혈청의 일부분을 포함하지 않는다.As used herein, "serum free" refers to the absence of human or animal serum. Therefore, the serum-free culture medium does not contain serum or a part of serum.
세포 배양물 중에서 만능 줄기세포의 기능적 췌장 내분비 세포로의 분화를 복제하기 위한 시도에서, 분화 과정은 종종 다수의 연속 단계를 통해 처리되는 것으로 여겨진다. 본 명세서에 사용되는 바와 같이, 다양한 단계들은 본 명세서에 포함된 실시예에 기재된 배양 시간, 및 시약에 의해 규정된다.In an attempt to replicate the differentiation of pluripotent stem cells into functional pancreatic endocrine cells in cell cultures, the differentiation process is often thought to be processed through a number of sequential steps. As used herein, the various steps are defined by the incubation times, and reagents described in the Examples included herein.
본 명세서에 사용되는 바와 같이, "완성 내배엽"은 낭배형성 동안 상배엽(epiblast)으로부터 생기는 세포의 특징을 보유하며, 위장관을 형성하는 세포 및 그의 파생 세포를 말한다. 완성 내배엽 세포는 다음 마커들 중 적어도 하나를 발현한다: FOXA2(간세포 핵 인자 3-β(HNF3β)로도 알려짐), GATA4, GATA6, MNX1, SOX17, CXCR4, 세르베루스(Cerberus), OTX2, 단미증(brachyury), 구스코이드(goosecoid), C-Kit, CD99, 및 MIXL1. 완성 내배엽 세포에 특징적인 마커는CXCR4, FOXA2 및 SOX17을 포함한다. 따라서, 완성 내배엽 세포는 CXCR4, FOXA2, 및 SOX17의 그의 발현을 특징으로 할 수 있다. 게다가, 세포가 1기에서 유지되도록 하는 시간의 길이에 따라, HNF4α의 증가가 관찰될 수 있다.As used herein, "complete endoderm" refers to a cell that retains the characteristics of a cell resulting from epiblast during cyst formation and forms a gastrointestinal tract and its derived cells. Completed endoderm cells express at least one of the following markers: FOXA2 (also known as hepatocyte nuclear factor 3-beta (HNF3 beta)), GATA4, GATA6, MNX1, SOX17, CXCR4, Cerberus, OTX2, brachyury, goosecoid, C-Kit, CD99, and MIXL1. Markers characteristic of complete endodermal cells include CXCR4, FOXA2 and SOX17. Thus, complete endodermal cells may be characterized by their expression of CXCR4, FOXA2, and SOX17. In addition, an increase in HNF4? May be observed, depending on the length of time that the cells are maintained at the first stage.
본 명세서에 사용되는 바와 같이, "췌장 내분비 세포"는 다음 호르몬들 중 적어도 하나를 발현할 수 있는 세포를 말한다: 인슐린, 글루카곤, 소마토스타틴, 그렐린, 및 췌장 폴리펩타이드. 이들 호르몬 외에, 췌장 내분비 세포에 특징적인 마커는 NGN3, NeuroD1, ISL1, PDX1, NKX6.1, PAX4, ARX, NKX2.2, 및 PAX6 중 하나 이상을 포함한다. β 세포에 특징적인 마커를 발현하는 췌장 내분비 세포는 인슐린 및 다음 전사 인자들 중 적어도 하나의 발현을 특징으로 할 수 있다: PDX1, NKX2.2, NKX6.1, NeuroD1, ISL1, HNF3β, MAFA, PAX4, 및 PAX6.As used herein, "pancreatic endocrine cells" refers to cells capable of expressing at least one of the following hormones: insulin, glucagon, somatostatin, ghrelin, and pancreatic polypeptide. In addition to these hormones, markers characteristic of pancreatic endocrine cells include one or more of NGN3, NeuroD1, ISL1, PDX1, NKX6.1, PAX4, ARX, NKX2.2, and PAX6. Pancreatic endocrine cells that express a marker characteristic of? cells may be characterized by the expression of at least one of insulin and the following transcription factors: PDX1, NKX2.2, NKX6.1, NeuroD1, ISL1, HNF3 ?, MAFA, PAX4 , And PAX6.
"d1", "d 1", 및 "1일째"; "d2", "d 2", 및 "2일째"; "d3", "d 3", 및 "3일째" 등은 본 명세서에서 상호교환가능하게 사용된다. 이들 숫자와 문자의 조합은 본 출원의 단계적 분화 프로토콜 동안의 상이한 단계에서의 인큐베이션의 특정일을 지칭한다."d1", "d1", and "first day"; "d2", "d2", and "second day"; "d3", "d3", and "third day" are used interchangeably herein. The combination of these numbers and letters refers to the specific day of incubation at different steps during the staged differentiation protocol of the present application.
"글루코스" 및 "D-글루코스"는 본 명세서에서 상호교환가능하게 사용되며, 천연에서 일반적으로 발견되는 당인 덱스트로스를 말한다."Glucose" and "D-glucose" are used interchangeably herein and refer to dextrose, a sugar commonly found in nature.
췌장 내분비 선조세포에서 발현되는 단백질 및 이를 인코딩하는 유전자임을 확인시켜 주는 "NeuroD" 및 "NeuroD1"은 본 명세서에서 상호교환가능하게 사용된다."NeuroD" and "NeuroD1" which confirm the protein expressed in pancreatic endocrine progenitor cells and the gene encoding the same are used interchangeably herein.
"LDN" 및 "LDN-193189"는 미국 매사추세츠주 케임브리지 소재의 스템젠트, 인크.(Stemgent, Inc.)로부터 상표명 스테몰레큘(STEMOLECULE)™로 입수가능한 BMP 수용체 억제제인 ((6-(4-(2-(피페리딘-1-일)에톡시)페닐)-3-(피리딘-4-일)피라졸로[1,5-a]피리미딘, 하이드로클로라이드; DM-3189))를 말한다."LDN" and "LDN-193189" were purchased from Stemgent, Inc., Cambridge, Mass., USA under the trade designation STEMOLECULE (TM) Yl) pyrazolo [1,5-a] pyrimidine, hydrochloride; DM-3189).
만능 줄기세포의 단리, 증폭 및 배양Isolation, amplification and culture of pluripotent stem cells
만능 줄기세포는 지정된 TRA-1-60 및 TRA-1-81 항체들 중 하나 이상을 발현할 수 있다(문헌[Thomson et al. 1998, Science 282:1145-1147]). 시험관내에서의 만능 줄기세포의 분화는 TRA-1-60, 및 TRA-1-81 발현의 손실로 이어진다. 미분화된 만능 줄기세포는 전형적으로 알칼리성 포스파타제 활성을 가지며, 이 활성은 상기 세포를 4% 파라포름알데하이드로 고정시키고, 이어서 기질로서 벡터(Vector)® 레드(Red)를 사용하여 발색시킴으로써 검출될 수 있는데, 이는 제조업체(벡터 래보러토리즈, 인크.(Vector Laboratories, Inc.), 미국 캘리포니아주 벌링게임 소재)에 의해 기재된 바와 같다. 미분화된 만능 줄기세포는 또한 RT-PCR에 의해 검출할 때, 전형적으로 OCT4 및 TERT를 발현한다.Allogeneic stem cells can express one or more of the designated TRA-1-60 and TRA-1-81 antibodies (Thomson et al. 1998, Science 282: 1145-1147). Differentiation of pluripotent stem cells in vitro leads to loss of TRA-1-60, and TRA-1-81 expression. Undifferentiated pluripotent stem cells typically have alkaline phosphatase activity, which can be detected by fixing the cells with 4% paraformaldehyde followed by color development using Vector (R) Red as a substrate , As described by the manufacturer (Vector Laboratories, Inc., Burlingame, Calif., USA). Undifferentiated pluripotent stem cells also typically express OCT4 and TERT when detected by RT-PCR.
증식된 만능 줄기세포의 다른 바람직한 표현형은 3개의 모든 배엽층, 즉 내배엽, 중배엽 및 외배엽의 조직의 세포로 분화될 잠재력이다. 줄기세포의 만능성은, 예를 들어 중증 복합형 면역결핍증("SCID") 마우스 내로 세포를 주사하고, 형성되는 기형종을 4% 파라포름알데하이드를 사용하여 고정시키고, 이어서 이들 3개의 배엽층으로부터의 세포 유형의 증거에 대해 조직학적으로 검사함으로써 확인될 수 있다. 대안적으로, 만능성은 배양체(embryoid body)를 생성하여 3개의 배엽층과 관련된 마커들의 존재에 대해 배양체를 평가함으로써 결정될 수 있다.Another desirable phenotype of pluripotent pluripotent stem cells is the potential to differentiate into cells of all three embryonic layers, endoderm, mesoderm and ectodermal tissue. The pluripotency of stem cells can be determined by injecting cells into, for example, severe combined immunodeficiency syndrome ("SCID") mice, fixing the resulting teratomas using 4% paraformaldehyde, Can be confirmed by histologic examination of evidence of cell type. Alternatively, universality can be determined by generating an embryoid body and evaluating the culture for the presence of markers associated with the three embryo layers.
증식된 만능 줄기세포주는 표준 G-밴딩(banding) 기술을 사용하여 핵형을 결정하고 상응하는 영장류 종의 공개된 핵형과 비교할 수 있다. "정상 핵형"을 가진 세포를 얻는 것이 바람직한데, 이는 세포가, 모든 인간 염색체가 존재하며 눈에 띄게 변경되지 않는 정배수체임을 의미한다. 다양한 영양세포 층(feeder layer)을 사용하는 배양물 중에서, 또는 기질 단백질 코팅된 용기를 사용함으로써, 만능 세포가 용이하게 증폭될 수 있다. 대안적으로, 세포의 일상적 증폭을 위해, mTeSR®1 배지(스템 셀 테크놀로지즈(Stem Cell Technologies), 캐나다 브리티시컬럼비아주 밴쿠버 소재)와 같은 한정 배지와 조합하여 화학적으로 한정된 표면이 사용될 수 있다.The proliferated universal stem cell line can be determined using the standard G-banding technique and compared to the published karyotype of the corresponding primate species. It is desirable to obtain cells with a "normal karyotype ", meaning that the cells are all orthotopic, with all human chromosomes present and not noticeably altered. Universal cultures can be easily amplified in cultures using a variety of feeder layers, or by using a substrate coated with a protein matrix. Alternatively, chemically defined surfaces can be used for routine amplification of cells in combination with defined media such as
본 발명의 일부 실시 형태의 방법에 따른 현탁 배양물 중에서의 배양은 세포 생존 및 증식은 촉진하지만 분화는 제한하는 세포 밀도로 만능 줄기세포를 배양 용기 내에 시딩함으로써 달성된다. 전형적으로, 세포의 미분화를 유지하는 시딩 밀도가 사용된다. 줄기세포의 단일-세포 현탁액이 시딩될 수 있지만, 세포의 작은 클러스터가 유리할 수 있음이 이해될 것이다.Culturing in suspension culture according to the method of some embodiments of the present invention is accomplished by seeding the pluripotent stem cells into the culture vessel with cell density promoting cell survival and proliferation but differentiation is limited. Typically, a seeding density is used to maintain the undifferentiation of the cells. It will be appreciated that although a single-cell suspension of stem cells can be seeded, a small cluster of cells may be advantageous.
현탁 배양물 중에 있는 동안에 만능 줄기세포에 영양물 및 성장 인자의 충분하고 지속적인 공급을 제공하기 위하여, 배양 배지가 매 1일 내지 5일과 같은 소정의 스케줄로 또는 일일 기준으로 교체 또는 보충될 수 있다. 만능 줄기세포의 큰 클러스터는 세포 분화를 야기할 수 있으며, 이에 따라 측정을 실시하여 큰 만능 줄기세포 응집체를 피할 수 있다. 본 발명의 일부 실시 형태에 따르면, 형성된 만능 줄기세포 클러스터는, 예를 들어 매 2 내지 7일마다 해리되고, 단일 세포 또는 작은 세포 군집은 추가의 배양 용기 내로 분할되거나(즉, 계대배양되거나) 동일한 배양 용기 내에 유지되고 대체 또는 추가 배양 배지로 처리된다.In order to provide a sufficient and continuous supply of nutrients and growth factors to the pluripotent stem cells while in suspension culture, the culture medium may be replaced or supplemented on a predetermined schedule, such as every 1 to 5 days, or on a daily basis. Large clusters of pluripotent stem cells can cause cell differentiation, and measurements can be made to avoid large allogenic stem cell aggregates. According to some embodiments of the present invention, the formed pluripotent stem cell clusters are dissociated, for example every 2 to 7 days, and single cells or small cell clusters are divided into additional culture vessels (i.e., subcultured) Maintained in a culture vessel and treated with an alternative or additional culture medium.
원심분리로부터 얻어진 만능 줄기세포의 펠렛을 포함하는 큰 만능 줄기세포 군집은 효소적 분해 및 기계적 해리 중 하나 또는 둘 모두를 거칠 수 있다. 만능 줄기세포 군집의 효소적 분해는 이 군집을 제IV형 콜라게나제, 디스파제® 또는 아큐타제®와 같은 효소에 노출시킴으로써 수행될 수 있다. 큰 만능 줄기세포 군집의 기계적 해리는 이 군집을 소정의 크기로 부수도록 설계된 장치를 사용하여 수행할 수 있다. 추가로, 또는 대안적으로, 기계적 해리는 니들(needle) 또는 피펫을 사용하여 수동으로 수행될 수 있다.The large allodynia stem cell clusters containing pellets of pluripotent stem cells obtained from centrifugation can undergo one or both of enzymatic degradation and mechanical dissociation. Quad enzymatic degradation of stem cell clusters may be performed by exposing the enzyme to the community, such as the Type IV collagenase, dispase or Accu hydratase ® ®. The mechanical dissociation of large allodynia stem cell clusters can be performed using an apparatus designed to break the clusters into a predetermined size. Additionally or alternatively, mechanical dissociation can be performed manually using a needle or pipette.
본 발명의 일부 실시 형태의 방법에 따라서 현탁 상태로 만능 줄기세포를 배양하는 데 사용된 배양 용기는, 내부에서 배양된 만능 줄기세포가 부착하거나 접착할 수 없도록 설계된 내부 표면을 갖는 (예를 들어, 만능 줄기세포를 배양하는 데 적합한 순도 등급을 가진) 임의의 조직 배양 용기(예를 들어, 그 표면에 대한 접착 또는 부착을 방지하기 위하여, 비-조직 배양물 처리된 용기)일 수 있다. 바람직하게는 스케일 조정가능한(scalable) 배양물을 수득하기 위하여, 본 발명의 일부 실시 형태에 따른 배양은 제어된 배양 시스템(바람직하게는 컴퓨터로 제어되는 배양 시스템)을 사용하여 달성되는데, 여기서는 적합한 장치를 사용하여 온도, 교반, pH, 및 산소와 같은 배양 파라미터가 자동적으로 모니터링되고 제어된다. 일단 원하는 배양 파라미터가 결정되면, 만능 줄기세포 증폭 및 분화를 향상시키기 위해 필요에 따라 배양 파라미터의 자동 조절을 위해 시스템을 설정할 수 있다.The culture container used for culturing the pluripotent stem cells in a suspended state according to the method of some embodiments of the present invention is a culture container having an inner surface designed to prevent adhesion or adhesion of the internally cultured pluripotent stem cells (for example, (For example, a non-tissue culture treated vessel to prevent adhesion or adhesion to its surface), which has a purity rating suitable for culturing pluripotent stem cells. In order to obtain a preferably scalable culture, cultivation according to some embodiments of the present invention is accomplished using a controlled culture system (preferably a computer controlled culture system) Are used to automatically monitor and control culture parameters such as temperature, agitation, pH, and oxygen. Once the desired culture parameters are determined, the system can be set up to automatically adjust the culture parameters as needed to enhance pluripotent stem cell amplification and differentiation.
만능 줄기세포는 동적 조건 하에서(즉, 만능 줄기세포가 현탁 배양물 중에, 예를 들어 교반 현탁 배양 시스템 내에 있는 동안에 일정하게 움직여지는 조건 하에서) 또는 비-동적 조건(즉, 정치 배양) 하에서, 다회의 계대배양에 걸쳐 이들의 증식성, 만능성 능력 및 핵형 안정성을 보존하면서 배양될 수 있다.The pluripotent stem cells can be cultured under dynamic conditions (i.e., under conditions in which the pluripotent stem cells are constantly moved in suspension culture, for example, while in a stirred suspension culture system) or under non-dynamic conditions Can be cultured while conserving their proliferative, universal ability and karyotypic stability throughout the subculture passage.
만능 줄기세포의 비-동적 배양의 경우, 만능 줄기세포는 코팅되거나 코팅되지 않은 페트리 디쉬, T-플라스크, 하이퍼플라스크(HyperFlask)®(코닝 인코포레이티드(Corning Incorporated), 미국 뉴욕주 코닝 소재), 셀스택(CellStack)®(코닝 인코포레이티드, 미국 뉴욕주 코닝 소재) 또는 셀 팩토리(Cell Factory)(눈크(NUNC)™ 셀 팩토리™ 시스템(서모 피셔 사이언티픽, 인크.(Thermo Fisher Scientific, Inc.), 미국 펜실베이니아주 피츠버그 소재) 중에서 배양될 수 있다. 만능 줄기세포의 동적 배양을 위해, 만능 줄기세포는 스피너 플라스크 또는 삼각 플라스크, 스테인리스 강, 유리 또는 일회용 플라스틱 진탕기 또는 교반 탱크 용기와 같은 적합한 용기 내에서 배양될 수 있다. 배양 용기는 제어 유닛에 연결되고, 이에 따라 제어된 배양 시스템을 제공할 수 있다. 배양 용기(예를 들어, 스피너 플라스크 또는 삼각 플라스크)는 연속적으로 또는 간헐적으로 교반될 수 있다. 바람직하게는, 배양 용기는 현탁 상태로 만능 줄기세포를 유지하기 위해 충분히 교반된다.In the case of non-dynamic culturing of pluripotent stem cells, the pluripotent stem cells were cultured in coated or uncoated Petri dishes, T-flasks, HyperFlask® (Corning Incorporated, Corning, NY, USA) (NUNC ™ Cell Factory ™ system (Thermo Fisher Scientific, Inc., Corning, NY, USA) or Cell Factory (Corning Inc., Corning, NY) Inc. For dynamic culturing of pluripotent stem cells, the pluripotent stem cells may be cultured in a spinner flask or an Erlenmeyer flask, stainless steel, glass or disposable plastic shaker or stirred tank vessel The culture vessel may be connected to a control unit and thus provide a controlled culture system. Fish, the spinner flask or may be conical flask) was stirred continuously or intermittently. Preferably, the culture vessel is stirred sufficiently to maintain the pluripotent stem cells in a suspended state.
만능 줄기세포는 성장 및 증폭을 촉진하기에 충분한 영양물 및 환경적 자극을 제공하는 임의의 배지 중에서 배양될 수 있다. 적합한 배지는 E8™, IH3 및 mTeSR®1 또는 mTeSR®2를 포함한다. 배지는 영양물 공급을 새롭게 하고 세포 부산물을 제거하기 위해 주기적으로 교체될 수 있다. 본 발명의 일부 실시 형태에 따르면, 배양 배지는 매일 교체된다.The pluripotent stem cells may be cultured in any medium that provides sufficient nutrients and environmental stimulation to promote growth and amplification. Suitable media include E8 ™, IH3 and
만능 줄기세포의 공급원A source of pluripotent stem cells
임의의 만능 줄기세포가 본 발명의 방법에 사용될 수 있다. 사용될 수 있는 만능 줄기세포의 예시적 유형은 임신 동안 임의의 시점에서, 전형적으로 그러나 반드시 그렇지는 않지만, 대략 임신 10 내지 12주 전에 취해진 태아 조직, 배아 조직, 또는 전-배아 조직(예를 들어, 배반포)을 비롯하여, 임신 후에 형성된 조직으로부터 유래된 확립된 만능 세포주를 포함한다. 비제한적인 예는, 예를 들어 인간 배아줄기세포주(hESC) H1, H7, 및 H9(위셀 리서치 인스티튜트(WiCell Research Institute), 미국 위스콘신주 매디슨 소재)와 같은, 확립된 인간 배아줄기세포주 또는 인간 배아생식세포주이다. 영양세포(feeder cell)의 부재 하에서 이미 배양된 만능 줄기세포 집단으로부터 취한 세포가 또한 적합하다.Any pluripotent stem cells can be used in the methods of the present invention. Exemplary types of pluripotent stem cells that can be used are fetal tissues, embryonic tissues, or pre-embryonic tissues taken at any time during pregnancy, typically, but not necessarily, about 10-12 weeks before gestation (e.g., Blastocysts), as well as established pluripotent cell lines derived from tissues formed after pregnancy. Non-limiting examples include established human embryonic stem cell lines or human embryonic stem cells such as human embryonic stem cell lines (hESCs) H1, H7, and H9 (WiCell Research Institute, Madison, Wis. It is a germ cell line. Cells taken from an already cultured pluripotent stem cell population in the absence of feeder cells are also suitable.
다수의 만능성 관련 전사 인자들, 예를 들어 OCT4, NANOG, Sox2, KLF4, 및 ZFP42의 강제 발현을 사용하여 성체 체세포로부터 유래될 수 있는 유도성 만능 세포(inducible pluripotent cell)(IPS) 또는 재프로그래밍된 만능 세포가 또한 적합하다(문헌[Annu Rev Genomics Hum Genet 2011, 12:165-185]). 본 발명의 방법에 사용되는 인간 배아줄기세포는 또한 톰슨(Thomson) 등에 의해 기재된 바와 같이 제조될 수 있다(미국 특허 제5,843,780호; 문헌[Science, 1998, 282:1145-1147]; 문헌[Curr Top Dev Biol 1998, 38:133-165]; 문헌[Proc Natl Acad SciU.S.A. 1995, 92:7844-7848]). 또한, 예를 들어 BG01v(브레사겐(BresaGen), 미국 조지아주 애선스 소재), 또는 성인 체세포로부터 유래된 세포, 예를 들어 문헌[Takahashi et al., Cell 131:1-12 (2007)]에 개시된 세포와 같은 돌연변이체 인간 배아줄기세포주가 적합하다. 본 발명에 사용하기에 적합한 만능 줄기세포는 문헌[Li et al. (Cell Stem Cell4: 16-19, 2009)]; 문헌[Maherali et al. (Cell Stem Cell 1: 55-70, 2007)]; 문헌[Stadtfeld et al. (Cell Stem Cell 2: 230-240)]; 문헌[Nakagawa et al. (Nature Biotechnology 26: 101-106, 2008)]; 문헌[Takahashi et al. (Cell131: 861-872, 2007)]; 및 미국 특허 출원 공개 제2011-0104805호에 기재된 방법에 따라 파생될 수 있다. 만능 줄기세포의 다른 공급원은 유도 만능 세포(IPS, 문헌[Cell, 126(4):663-676])를 포함한다. 본 발명의 방법에 사용하기에 적합한 세포의 다른 공급원은 인간 제대 조직 유래 세포, 인간 양수 유래 세포, 인간 태반 유래 세포, 및 인간 반수성 개체(parthenote)를 포함한다. 일 실시 형태에서, 제대 조직 유래 세포는 미국 특허 제7,510,873호의 방법을 사용하여 수득될 수 있으며, 이의 개시내용은 세포의 단리 및 특징규명에 관한 것인 것과 같이 전체적으로 참고로 포함된다. 다른 실시 형태에서, 태반 조직 유래 세포는 미국 특허 출원 공개 제2005/0058631호의 방법을 사용하여 수득될 수 있으며, 이의 개시내용은 세포의 단리 및 특징규명에 관한 것인 것과 같이 전체적으로 참고로 포함된다. 다른 실시 형태에서, 양수 유래 세포는 미국 특허 출원 공개 제2007/0122903호의 방법을 사용하여 수득될 수 있으며, 이의 개시내용은 세포의 단리 및 특징규명에 관한 것인 것과 같이 이의 전문이 참조로 포함되어 있다.Inducible pluripotent cells (IPS) or reprogrammable cells that can be derived from adult somatic cells using forced expression of a number of universality related transcription factors such as OCT4, NANOG, Sox2, KLF4, and ZFP42, Are also suitable ( Annu Rev Genomics Hum Genet 2011, 12: 165-185). Human embryonic stem cells used in the methods of the present invention can also be prepared as described by Thomson et al. (U.S. Patent No. 5,843,780; Science, 1998, 282: 1145-1147; Curr Top Dev Biol 1998, 38: 133-165; Proc Natl Acad Sci U S. 1995, 92: 7844-7848). Cells derived from adult somatic cells, such as Takahashi et al ., Cell 131: 1-12 (2007), for example BG01v (BresaGen, Athens, Mutant human embryonic stem cell lines such as the disclosed cells are suitable. Suitable pluripotent stem cells for use in the present invention are described in Li et al. ( Cell Stem Cell 4: 16-19, 2009); See Maherali et al. ( Cell Stem Cell 1: 55-70, 2007); Stadtfeld et al. ( Cell Stem Cell 2: 230-240); Nakagawa et < RTI ID = 0.0 > al. ( Nature Biotechnology 26: 101-106, 2008); Takahashi et al. ( Cell 131: 861-872, 2007); And U. S. Patent Application Publication No. < RTI ID = 0.0 > 2011-0104805. ≪ / RTI > Other sources of pluripotent stem cells include inducible pluripotent cells (IPS, Cell , 126 (4): 663-676). Other sources of cells suitable for use in the methods of the present invention include human umbilical cord tissue derived cells, human amniotic fluid cells, human placenta derived cells, and parthenotes. In one embodiment, umbilical cord tissue-derived cells can be obtained using the method of U.S. Patent No. 7,510,873, the disclosure of which is incorporated by reference in its entirety as it relates to the isolation and characterization of cells. In another embodiment, placental tissue-derived cells can be obtained using the methods of U.S. Patent Application Publication No. 2005/0058631, the disclosure of which is incorporated by reference in its entirety as it relates to the isolation and characterization of cells. In another embodiment, the amphotropic cell can be obtained using the method of U.S. Patent Application Publication No. 2007/0122903, the disclosure of which is incorporated herein by reference, as it relates to the isolation and characterization of cells have.
만능 줄기세포의 특징은 당업자에게 잘 알려져 있으며, 만능 줄기세포의 추가의 특징이 계속 확인되고 있다. 만능 줄기세포 마커는, 예를 들어 다음 중의 하나 이상(예를 들어, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14개 또는 모두)의 발현을 포함한다: ABCG2, 크립토(cripto), FOXD3, CONNEXIN43, CONNEXIN45, OCT4, SOX2, NANOG, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, TRA-1-60, TRA-1-81. 일 실시 형태에서, 본 발명의 방법에 사용하기에 적합한 만능 줄기세포는 유세포측정법에 의해 검출할 때 CD9, SSEA4, TRA-1-60, 및 TRA-1-81 중 하나 이상(예를 들어, 1, 2, 3개 또는 모두)을 발현하며, 분화 마커인 CXCR4(CD184로도 알려짐)의 발현은 결여되어 있다. 다른 실시 형태에서, 본 발명의 방법에 사용하기에 적합한 만능 줄기세포는 RT-PCR에 의해 검출할 때 CD9, NANOG 및 POU5F1/OCT4 중 하나 이상(예를 들어, 1, 2개 또는 모두)을 발현한다.The characteristics of pluripotent stem cells are well known to those skilled in the art, and additional features of pluripotent stem cells are still being identified. An allogeneic stem cell marker can be, for example, one or more of the following (e.g., 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, Expression includes: ABCG2, crypto, FOXD3, CONNEXIN43, CONNEXIN45, OCT4, SOX2, NANOG, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, TRA-1-60, TRA-1-81. In one embodiment, the pluripotent stem cells suitable for use in the methods of the present invention comprise one or more of CD9, SSEA4, TRA-1-60, and TRA-1-81 when detected by flow cytometry (e.g., , 2, 3, or both) and lacks the expression of the differentiation marker CXCR4 (also known as CD184). In another embodiment, the pluripotent stem cells suitable for use in the methods of the present invention express at least one (e.g., one, two or all) of CD9, NANOG and POU5F1 / OCT4 when detected by RT-PCR do.
예시적인 만능 줄기세포는 인간 배아줄기세포주 H9(NIH 코드: WA09), 인간 배아줄기세포주 H1(NIH 코드: WA01), 인간 배아줄기세포주 H7(NIH 코드: WA07) 및 인간 배아줄기세포주 SA002(셀라르티스(Cellartis), 스웨덴 소재)를 포함한다. 일 실시 형태에서, 만능 줄기세포는 인간 배아줄기세포, 예를 들어 H1 hES 세포이다. 대안적인 실시 형태에서, 비-배아 기원의 만능 줄기세포가 사용된다.Exemplary pluripotent stem cells include human embryonic stem cell line H9 (NIH code: WA09), human embryonic stem cell line H1 (NIH code: WA01), human embryonic stem cell line H7 (NIH code: WA07) and human embryonic stem cell line SA002 Cellartis, < / RTI > Sweden). In one embodiment, the universal stem cell is a human embryonic stem cell, such as a H1 hES cell. In an alternative embodiment, allogeneic stem cells of non-embryonic origin are used.
만능 줄기세포로부터 췌장 내배엽 계통에 특징적인 마커를 발현하는 세포의 분화Differentiation of cells expressing markers characteristic of pancreatic endoderm lineage from pluripotent stem cells
만능 줄기세포의 증폭Amplification of pluripotent stem cells
하기에 기술된 바와 같은 실시 형태들 중 일부에서, 본 발명은 줄기세포들을 단리 및 배양하는 것, 특히 줄기세포 클러스터들을 배양하는 것에 관한 것으로, 이들은 동적 현탁 배양 시스템 내에서 만능성을 유지한다. 만능 세포 클러스터는 분화되어 기능적 β 세포를 생성할 수 있다.In some of the embodiments as described below, the present invention relates to isolating and culturing stem cells, in particular culturing stem cell clusters, which maintain universality within the dynamic suspension culture system. Pluripotent clusters can be differentiated to produce functional beta cells.
본 발명의 방법에 사용된 만능 줄기세포는 바람직하게는, 원하는 종점을 향한 분화 전에 동적 현탁 배양물 중에서 증폭된다. 유리하게는, 만능 줄기세포가 만능성의 손실 없이 적합한 배지 중에서 현탁 상태로 세포의 클러스터로서 배양 및 증폭될 수 있는 것으로 확인되었다. 그러한 배양은 동적 현탁 배양 시스템 내에서 일어날 수 있는데, 여기서는 세포 또는 세포 클러스터가 만능성의 손실을 방지하기 충분하게 계속 움직임이 유지되고 있다. 유용한 동적 현탁 배양 시스템은 배양 성분들을, 예를 들어 교반(stirring), 진탕, 재순환 또는 배지를 통한 가스의 버블링(bubbling)을 통해, 교반(agitate)하기 위한 수단이 구비된 시스템을 포함한다. 그러한 교반은, 세포 클러스터의 충분한 움직임이 유지되어 증폭을 촉진시키고 미성숙 분화를 방지하는 한, 간헐적이거나 연속적일 수 있다. 바람직하게는, 교반은, 예컨대 특정 속도로 회전하는 임펠러를 통한, 연속 교반을 포함한다. 임펠러는 환형 또는 평탄형 바닥을 가질 수 있다. 임펠러의 교반 속도는, 클러스터가 현탁 상태로 유지되고 정착(settling)이 최소화되도록 하는 것이어야 한다. 또한, 임펠러 블레이드의 각은 세포 및 클러스터의 상향 운동을 보조하여 정착을 피하도록 조절될 수 있다. 또한, 임펠러 유형, 각 및 회전 속도는 모두, 세포 및 클러스터가 균일한 콜로이드성 현탁액으로서 나타나도록 조정될 수 있다.The pluripotent stem cells used in the method of the present invention are preferably amplified in a dynamic suspension culture prior to differentiation towards the desired endpoint. Advantageously, it has been found that pluripotent stem cells can be cultured and amplified as clusters of cells in suspension in a suitable medium without loss of universality. Such cultures can occur in a dynamic suspension culture system wherein cells or cell clusters are kept moving sufficiently to prevent loss of universality. Useful dynamic suspension culture systems include systems provided with means for agitating the culture components, for example, through stirring, shaking, recirculation or bubbling of the gas through the medium. Such agitation may be intermittent or continuous, as long as sufficient movement of the cell clusters is maintained to promote amplification and prevent immature differentiation. Preferably, the stirring includes continuous stirring, for example, through an impeller rotating at a specific speed. The impeller may have an annular or planar bottom. The stirring speed of the impeller should be such that the cluster remains suspended and settling is minimized. Also, the angle of the impeller blades can be adjusted to aid in upward movement of the cells and clusters to avoid settling. In addition, the impeller type, angle, and rotational speed can all be adjusted so that the cells and clusters appear as homogeneous colloidal suspensions.
만능 줄기세포 클러스터의 현탁 배양 및 증폭은 일회용 플라스틱, 재사용가능한 플라스틱, 스테인리스 강 또는 유리 용기, 예를 들어 스피너 플라스크 또는 삼각 플라스크와 같은 적절한 동적 배양 시스템에 정치 배양된 줄기세포를 옮김으로써 달성될 수 있다. 예를 들어, 부착성 정치 환경, 즉, 플레이트 또는 디쉬 표면에서 배양된 줄기세포를 먼저 킬레이트제 또는 효소로 처리하여 표면으로부터 제거할 수 있다. 적합한 효소는 제I형 콜라게나제, 디스파제®(시그마 알드리치 엘엘씨(Sigma Aldrich LLC), 미국 미주리주 세인트루이스 소재) 또는 상표명 아큐타제®(시그마 알드리치 엘엘씨, 미국 미주리주 세인트루이스 소재)로 시판되는 구매가능한 제형을 포함하지만 이로 한정되지 않는다. 아큐타제®는 콜라겐분해성 및 단백질분해성 효소(갑각류로부터 단리됨)를 포함하는 세포 탈착 용액(cell detachment solution)이고 포유류 또는 세균 유래 생성물을 함유하지 않는다. 따라서, 일 실시 형태에서, 효소는 콜라겐분해성 효소 또는 단백질분해성 효소이거나 콜라겐분해성 및 단백질분해성 효소를 포함하는 세포 탈착 용액이다. 적합한 킬레이트제는 에틸렌다이아민테트라아세트산(EDTA)을 포함하지만 이로 한정되지 않는다. 일부 실시 형태에서, 만능 줄기세포 배양물은 효소 또는 킬레이트제와 함께, 바람직하게는 콜로니 가장자리가 컬링되고 리프팅되기 시작하지만, 배양 표면으로부터 콜로니의 완전한 탈착이 일어나기 전까지 인큐베이션된다. 일 실시 형태에서, 세포 배양물은 실온에서 인큐베이션된다. 일 실시 형태에서, 세포는 20℃ 초과, 25℃ 초과, 30℃ 초과 또는 35℃ 초과의 온도에서, 예를 들어 약 20℃ 내지 약 40℃의 온도, 약 25℃ 내지 약 40℃의 온도, 약 30℃ 내지 약 40℃의 온도, 예를 들어 약 37℃의 온도에서 인큐베이션된다. 일 실시 형태에서, 세포는 적어도 약 1분, 적어도 약 5분, 적어도 약 10분, 적어도 약 15분, 적어도 약 20분, 예를 들어 약 1분 내지 약 30분, 약 5분 내지 약 30분, 약 10분 내지 약 25분, 약 15분 내지 약 25분, 예를 들어 약 20분 동안 인큐베이션된다. 일 실시 형태에서, 본 방법은 처리 후의 세포 배양물로부터 효소 또는 킬레이트제를 제거하는 단계를 포함한다. 일 실시 형태에서, 세포 배양물은 효소 또는 킬레이트제의 제거 후, 1회 또는 2회 또는 그 이상 세척된다. 일 실시 형태에서 세포 배양물은 mTeSR®1(스템 셀 테크놀로지즈, 캐나다 브리티시컬럼비아주 벤쿠버 소재)과 같은 적절한 배양 배지로 세척된다. 일 실시 형태에서, Rho-키나제 억제제(예를 들어, Y-27632, 악소라(Axxora) 카탈로그 번호 ALX-270-333, 미국 캘리포니아주 샌디에고 소재). Rho-키나제 억제제는 약 1 내지 약 100 μM, 약 1 내지 90 μM, 약 1 내지 약 80 μM, 약 1 내지 약 70 μM, 약 1 내지 약 60 μM, 약 1 내지 약 50 μM, 약 1 내지 약 40 μM, 약 1 내지 약 30 μM, 약 1 내지 약 20 μM, 약 1 내지 약 15 μM, 약 1 내지 약 10 μM, 또는 약 10 μM의 농도일 수 있다. 일 실시 형태에서, Rho-키나제 억제제는 적어도 1 μM, 적어도 5 μM 또는 적어도 10 μM로 첨가된다. 세포는 정치 배양 시스템의 표면으로부터 스크레이퍼(scraper) 또는 고무 폴리스맨(rubber policeman)을 사용하여 리프팅될 수 있다. 배지 및 세포는 유리 피펫 또는 다른 적합한 수단을 사용하여 동적 배양 시스템에 옮겨질 수 있다. 바람직한 실시 형태에서, 동적 배양 시스템 내의 배지는 매일 교체된다.Suspension culturing and amplification of pluripotent stem cell clusters can be accomplished by transferring stably cultured stem cells to a suitable dynamic culture system such as disposable plastic, reusable plastic, stainless steel or glass containers, for example, a spinner flask or an Erlenmeyer flask . For example, stem cells cultured in an adherent environment, i.e. on a plate or a dish surface, may first be treated with a chelating agent or enzyme to remove from the surface. Suitable enzymes are commercially available as type I collagenase, dispase ® (Sigma Aldrich El elssi (Sigma Aldrich LLC), Missouri St. Louis material), or trade names Accu hydratase ® (Sigma Aldrich El elssi, United States St. Louis, Missouri material) But are not limited to, commercially available formulations. Accu hydratase ® is a collagen (as isolated from shellfish) degradability and proteolytic enzyme solution desorption cell (cell detachment solution) containing and does not contain a bacterial or mammalian-derived products. Thus, in one embodiment, the enzyme is a collagenase or a proteolytic enzyme or a cell desorbent solution comprising a collagen degradable and proteolytic enzyme. Suitable chelating agents include, but are not limited to, ethylenediaminetetraacetic acid (EDTA). In some embodiments, the pluripotent stem cell cultures are incubated with the enzyme or chelating agent, preferably until the colony edges are curled and lifted, but until complete desorption of the colonies occurs from the culture surface. In one embodiment, the cell culture is incubated at room temperature. In one embodiment, the cells are incubated at a temperature of greater than 20 ° C, greater than 25 ° C, greater than 30 ° C, or greater than 35 ° C, for example, at a temperature of from about 20 ° C to about 40 ° C, And incubated at a temperature of from 30 째 C to about 40 째 C, for example, at a temperature of about 37 째 C. In one embodiment, the cells are cultured for at least about 1 minute, at least about 5 minutes, at least about 10 minutes, at least about 15 minutes, at least about 20 minutes, such as from about 1 minute to about 30 minutes, from about 5 minutes to about 30 minutes , About 10 minutes to about 25 minutes, about 15 minutes to about 25 minutes, for example about 20 minutes. In one embodiment, the method comprises removing the enzyme or chelating agent from the cell culture after treatment. In one embodiment, the cell culture is washed once or twice or more after removal of the enzyme or chelating agent. In one embodiment, cell cultures are washed with a suitable culture medium such as mTeSR®1 (Stem Cell Technologies, Vancouver, British Columbia, Canada). In one embodiment, Rho-kinase inhibitors (e.g., Y-27632, Axxora catalog number ALX-270-333, San Diego, CA). The Rho-kinase inhibitor may be administered at a dose of about 1 to about 100 [mu] M, about 1 to 90 [mu] M, about 1 to about 80 [mu] M, about 1 to about 70 [ 40 μM, about 1 to about 30 μM, about 1 to about 20 μM, about 1 to about 15 μM, about 1 to about 10 μM, or about 10 μM. In one embodiment, the Rho-kinase inhibitor is added at least 1 [mu] M, at least 5 [mu] M, or at least 10 [mu] M. The cells may be lifted from the surface of the stationary culture system using a scraper or a rubber policeman. The medium and cells may be transferred to a dynamic culture system using a glass pipette or other suitable means. In a preferred embodiment, the medium in the dynamic culture system is replaced daily.
일 실시 형태에서, 본 발명은 3차원 현탁 배양물 중에서 만능 줄기세포를 배양 및 증폭시키는 방법을 제공한다. 특히, 본 방법은 이들 만능 줄기세포의 응집된 세포 클러스터를 형성함으로써 배양 및 증폭 만능 줄기세포를 제공한다. 세포 클러스터는 세포를 배양하기 전에 만능 줄기세포 배양물을 효소(예를 들어, 중성 프로테아제, 예를 들어 디스파제®) 또는 킬레이트제로 처리한 결과로서 형성될 수 있다. 바람직하게는, 세포는 교반 또는 진탕 현탁 배양 시스템 내에서 배양될 수 있다. 일 실시 형태에서, 본 발명은 만능 줄기세포의 그러한 클러스터로부터 췌장 내배엽 계통에 특징적인 마커를 발현하는 세포의 형성을 추가로 제공한다.In one embodiment, the invention provides a method of culturing and amplifying pluripotent stem cells in a three-dimensional suspension culture. In particular, the method provides cultured and amplified pluripotent stem cells by forming aggregated cell clusters of these pluripotent stem cells. Cell cluster may be formed as a result of the enzyme pluripotent stem cell culture (e. G., Neutral protease, such as dispase ®) or a chelating agent treatment prior to culturing cells. Preferably, the cells can be cultured in a stirred or shaking suspension culture system. In one embodiment, the invention further provides for the formation of a cell expressing a marker characteristic of the pancreatic endoderm lineage from such clusters of pluripotent stem cells.
바람직하게는, 세포 클러스터는 응집된 만능 줄기세포이다. 응집된 줄기세포는 하나 이상의 만능성 마커, 예를 들어 마커 CD9, SSEA4, TRA-1-60, 및 TRA-1-81 중 하나 이상(예를 들어, 1, 2, 3개 또는 모두)을 발현하고, 하나 이상의 분화 마커의 발현은 결여되어 있는데, 예를 들어 CXCR4의 발현은 결여되어 있다. 일 실시 형태에서, 응집된 줄기세포는 만능성 마커 CD9, SSEA4, TRA-1-60, 및 TRA-1-81을 발현하고, 분화 마커 CXCR4의 발현은 결여되어 있다.Preferably, the cell clusters are aggregated pluripotent stem cells. Aggregated stem cells express one or more (e.g., one, two, three or all) of one or more universal markers, e.g., markers CD9, SSEA4, TRA-1-60, And the expression of one or more differentiation markers is lacking, for example, the expression of CXCR4 is lacking. In one embodiment, the aggregated stem cells express the universal markers CD9, SSEA4, TRA-1-60, and TRA-1-81, and the expression of the differentiation marker CXCR4 is absent.
일 실시 형태는 현탁 배양물 중에서 세포 클러스터로서 만능 줄기세포를 배양하는 방법이다. 세포 클러스터는 동적 교반 또는 진탕 현탁 배양 시스템 내에서 배양된 응집된 만능 줄기세포이다. 세포 클러스터는 세포 리프팅제로서 중성 프로테아제, 예를 들어 디스파제와 같은 효소를 사용하여 평면 부착성 배양물(planar adherent culture)로부터 교반 또는 진탕 현탁 배양 시스템에 옮겨질 수 있다. 예시적인 적합한 효소는 제IV형 콜라게나제, 디스파제® 또는 아큐타제®를 포함하지만 이로 한정되지 않는다. 세포는 교반 또는 진탕 현탁 배양 시스템, 특히 교반 현탁 배양 시스템 내에서 만능성을 유지한다.One embodiment is a method for culturing pluripotent stem cells as a cell cluster in a suspension culture. Cell clusters are aggregated pluripotent stem cells cultured in a dynamic agitation or shake suspension culture system. The cell clusters can be transferred from a planar adherent culture to a stirred or shake suspension culture system using enzymes such as neutral proteases, such as dispase, as cell lifting agents. Exemplary suitable enzymes include Type IV collagenase, dispase or Accu hydratase ® ®, but are not limited to. The cells maintain universality in a stirred or shake suspension culture system, particularly in a stirred suspension culture system.
본 발명의 다른 실시 형태는 현탁 배양물 중에서 세포 클러스터로서 만능 줄기세포를 배양하는 방법이며, 여기서 세포 클러스터는 킬레이트제, 예를 들어 EDTA를 사용하여 평면 부착성 배양물로부터 옮겨져서 교반 또는 진탕 현탁 배양 시스템 내에서 배양된 응집된 만능 줄기세포이다. 세포 클러스터는 교반 또는 진탕 현탁 배양 시스템, 특히 교반(동적 교반) 현탁 배양 시스템 내에서 만능성을 유지한다.Another embodiment of the present invention is a method for culturing pluripotent stem cells as a cell cluster in a suspension culture wherein the cell clusters are transferred from a flat adherent culture using a chelating agent such as EDTA and incubated in a stirred or shake- It is an aggregated pluripotent stem cell cultured in the system. Cell clusters maintain universality in stirred or shake suspension culture systems, particularly stirred (dynamic stirred) suspension culture systems.
본 발명의 다른 실시 형태는 현탁 배양물 중에서 세포 클러스터로서 만능 줄기세포를 배양하는 방법이며, 여기서 세포 클러스터는 효소 아큐타제®를 사용하여 평면 부착성 배양물로부터 옮겨져서 교반 또는 진탕 현탁 배양 시스템 내에서 배양된 응집된 만능 줄기세포이다. 세포 클러스터는 동적 교반 현탁 배양 시스템 내에서 만능성을 유지한다.Another embodiment of the present invention is a method for culturing pluripotent stem cells as a cell cluster in a suspension culture wherein the cell clusters are transferred from a flat adherent culture using an enzyme Accutase 占 and are incubated in a stirred or shake suspension culture system It is cultured aggregated pluripotent stem cells. Cell clusters remain universal within the dynamic stirred suspension culture system.
본 발명의 세포 클러스터는 중배엽 세포, 예를 들어 심장 세포, 외배엽 세포, 예를 들어 신경 세포, 단일 호르몬 양성 세포 또는 췌장 내배엽 세포로 분화될 수 있다. 본 방법은 분화, 예를 들어 췌장 내배엽 세포의 췌장 전구세포 및 췌장 호르몬 발현 세포로의 분화를 추가로 포함할 수 있다. 다른 실시 형태에서, 췌장 전구세포는 β 세포 전사 인자 PDX1 및 NKX6.1의 발현을 특징으로 한다.The cell clusters of the present invention can be differentiated into mesodermal cells, for example, heart cells, ectodermal cells, such as neurons, monohydrogen-positive cells or pancreatic endoderm cells. The method may further include differentiation, for example, differentiation of pancreatic endoderm cells into pancreatic progenitor cells and pancreatic hormone-expressing cells. In another embodiment, the pancreatic progenitor cells are characterized by the expression of the beta cell transcription factors PDX1 and NKX6.1.
일 실시 형태에서, 분화의 단계는 현탁 배양 시스템 내에서의 적어도 12시간, 적어도 24시간, 적어도 36시간, 적어도 48시간, 적어도 72시간, 적어도 96시간, 적어도 120시간, 적어도 144시간, 적어도 168시간, 적어도 196시간 이상, 바람직하게는 약 48시간 내지 약 72시간 후에 수행된다. 분화는 실시예에 기재된 것과 같은 배지 성분들의 단계적 진행을 사용하여 수행할 수 있다(예를 들어, 표 A 및 표 1a 및 표 1c 참조).In one embodiment, the step of differentiation is performed in a suspension culture system for at least 12 hours, at least 24 hours, at least 36 hours, at least 48 hours, at least 72 hours, at least 96 hours, at least 120 hours, at least 144 hours, at least 168 hours , At least 196 hours, preferably from about 48 hours to about 72 hours. Differentiation can be carried out using the stepwise progression of media components as described in the examples (see, for example, Tables A and Ia and Table Ic).
바람직한 실시 형태에서, 3차원 세포 클러스터는 평면 부착성 배양물 중에서 만능 줄기세포를 성장시키는 단계; 만능 줄기세포를 응집된 세포 클러스터로 증폭시키는 단계; 및 평면 부착성 배양물로부터의 만능 줄기세포의 클러스터를 효소 또는 킬레이트제를 사용하여 동적 현탁 배양물에 옮기는 단계에 의해 생성된다. 추가의 바람직한 실시 형태는 동적 교반 현탁 배양 시스템 내에서 만능 줄기세포를 증폭 및 분화시키는 방법으로서, 평면 부착성 배양물 중에서 만능 줄기세포를 성장시키는 단계; 만능 줄기세포를 응집된 세포 클러스터로 증폭시키는 단계; 및 평면 부착성 배양물로부터의 만능 줄기세포의 클러스터를 효소 또는 킬레이트제를 사용하여 동적 현탁 배양물에 옮기는 단계; 및 동적 교반 현탁 배양 시스템 내에서 만능 세포 클러스터를 분화시켜 췌장 전구세포 집단을 생성하는 단계에 의한, 방법이다.In a preferred embodiment, the three-dimensional cell cluster comprises the steps of growing pluripotent stem cells in a flat adherent culture; Amplifying pluripotent stem cells with aggregated cell clusters; And clustering of pluripotent stem cells from flat adherent cultures into a dynamic suspension culture using an enzyme or chelating agent. A further preferred embodiment is a method of amplifying and differentiating pluripotent stem cells in a dynamic stirred suspension culture system, comprising: growing pluripotent stem cells in a flat adherent culture; Amplifying pluripotent stem cells with aggregated cell clusters; And clusters of pluripotent stem cells from flat adherent cultures into a dynamic suspension culture using an enzyme or chelating agent; And dividing the universal cell cluster in a dynamic stirred suspension culture system to produce a population of pancreatic progenitor cells.
다른 실시 형태는 췌장 전구세포로 분화되는 증폭된 만능 줄기세포 클러스터의 현탁으로부터 제조된 분화된 줄기세포를 포함하는 이식가능한 줄기세포 유래 세포 생성물이다. 더 상세하게는, 이식가능한 줄기세포 유래 생성물은 평면 부착성 배양물 중에서 만능 줄기세포를 성장시키는 단계; 만능 줄기세포를 응집된 세포 클러스터로 증폭시키는 단계; 및 평면 부착성 배양물로부터의 만능 줄기세포의 클러스터를 효소 또는 킬레이트제를 사용하여 동적 현탁 배양물에 옮기는 단계; 및 동적 교반 현탁 배양 시스템 내에서 만능 세포 클러스터를 분화시키는 단계에 의해 생성된다. 이식가능한 줄기세포 유래 세포 생성물은 바람직하게는 당뇨병을 치료하는 데 사용된다.Another embodiment is an implantable stem cell-derived cell product comprising differentiated stem cells prepared from suspension of amplified pluripotent stem cell clusters differentiated into pancreatic progenitor cells. More specifically, the transplantable stem cell-derived product comprises the steps of growing pluripotent stem cells in a flat adherent culture; Amplifying pluripotent stem cells with aggregated cell clusters; And clusters of pluripotent stem cells from flat adherent cultures into a dynamic suspension culture using an enzyme or chelating agent; And dividing the universal cell clusters in a dynamic stirred suspension culture system. The transplantable stem cell-derived cell product is preferably used to treat diabetes.
다른 실시 형태에서, 본 방법은 기능적 췌장 내분비 세포로의 추가의 생체내 성숙을 위해 당뇨병 동물에의 이식을 포함한다.In another embodiment, the methods comprise transplantation into a diabetic animal for further in vivo maturation into functional pancreatic endocrine cells.
다른 실시 형태는 현탁 배양 시스템 내에서 만능 줄기세포를 증폭 및 분화시키는 방법으로서, 평면 부착성 배양물 중에서 만능 줄기세포를 성장시키는 단계; 효소를 사용하여 평면 부착성 배양물로부터 만능 줄기세포를 제거하는 단계; 만능 줄기세포를 정치 배양으로 마이크로캐리어에 부착시키는 단계; 동적 교반 현탁 배양 시스템 내에서 만능 세포를 증폭시키는 단계; 및 동적 교반 현탁 배양 시스템 내에서 만능 세포를 분화시켜 췌장 전구세포 집단을 생성하는 단계를 포함하는, 방법이다.Another embodiment is a method of amplifying and differentiating pluripotent stem cells in a suspension culture system, comprising: growing pluripotent stem cells in a flat adherent culture; Removing the pluripotent stem cells from the flat adherent culture using the enzyme; Attaching the pluripotent stem cells to the microcarriers in a stationary culture; Amplifying the pluripotent cells in a dynamic stirred suspension culture system; And dividing the pluripotent cells in a dynamic stirred suspension culture system to produce a population of pancreatic progenitor cells.
마이크로캐리어는 세포를 부착시키기 위한 당업계에 공지된 임의의 형태일 수 있으며, 특히 마이크로캐리어는 비드일 수 있다. 마이크로캐리어는 천연 물질 또는 합성 유래 물질로 구성될 수 있다. 예에는 콜라겐-기반 마이크로캐리어, 덱스트란-기반 마이크로캐리어, 또는 셀룰로스-기반 마이크로캐리어가 포함된다. 예를 들어, 마이크로캐리어 비드는 양으로 하전된 표면을 마이크로캐리어에 제공하기 위해 양이온성 트라이메틸 암모늄이 표면에 부착된, 개질된 폴리스티렌 비드일 수 있다. 비드 직경은 약 90 내지 약 200 μm, 대안적으로 약 100 내지 약 190 μm, 대안적으로 약 110 내지 약 180 μm, 대안적으로 약 125 내지 175 μm 직경의 범위일 수 있다. 마이크로캐리어 비드는 또한 가교결합된 덱스트란의 매트릭스에 화학적으로 커플링된 변성된 콜라겐의 얇은 층일 수 있다. 마이크로캐리어 비드는 유리, 세라믹, 중합체(예컨대, 폴리스티렌), 또는 금속일 수 있다. 또한, 마이크로캐리어는 코팅되지 않거나, 규소 또는 콜라겐과 같은 단백질로 코팅될 수 있다. 추가의 태양에서, 마이크로캐리어는 마이크로캐리어에 대한 세포의 결합을 향상시키고 마이크로캐리어로부터의 세포의 방출을 향상시키는 화합물로 구성되거나 이로 코팅될 수 있으며, 이러한 화합물에는 소듐 하이알루로네이트, 폴리(모노스테아로일글리세라이드 코-석신산), 폴리-D,L-락타이드-코-글리콜라이드, 피브로넥틴, 라미닌, 엘라스틴, 라이신, n-아이소프로필 아크릴아미드, 비트로넥틴, 및 콜라겐이 포함되지만 이로 한정되지 않는다. 예에는 저수준의 생물학적으로 관련된 전기를 생산하는 아연과 구리의 미립자상 갈바닉 커플(particulate galvanic couple)을 갖는 마이크로캐리어; 또는 상자성 칼슘-알기네이트 마이크로캐리어와 같은 상자성체인 마이크로캐리어와 같은, 미세전류를 갖는 마이크로캐리어가 추가로 포함된다.The microcarriers may be of any shape known in the art for attaching cells, and in particular the microcarriers may be beads. The microcarriers may be composed of natural or synthetic materials. Examples include collagen-based microcarriers, dextran-based microcarriers, or cellulose-based microcarriers. For example, the microcarrier bead may be a modified polystyrene bead having a cationic trimethylammonium attached to its surface to provide a positively charged surface to the microcarrier. The bead diameter may range from about 90 to about 200 [mu] m, alternatively from about 100 to about 190 [mu] m, alternatively from about 110 to about 180 [mu] m, alternatively from about 125 to 175 [mu] m. The microcarrier beads may also be a thin layer of denatured collagen chemically coupled to a matrix of cross-linked dextran. The microcarrier beads may be glass, ceramics, polymers (e.g., polystyrene), or metals. In addition, the microcarriers may not be coated or may be coated with proteins such as silicon or collagen. In a further aspect, the microcarrier may be comprised of or coated with a compound that enhances cell binding to the microcarrier and enhances the release of cells from the microcarrier, such compounds include sodium hyaluronate, poly (mono But are not limited to, stearoylglyceride co-succinic acid), poly-D, L-lactide-co- glycolide, fibronectin, laminin, elastin, lysine, n-isopropylacrylamide, It does not. Examples include microcarriers having a particulate galvanic couple of zinc and copper to produce low levels of biologically relevant electricity; Or a microcarrier having a microcurrent, such as a microcarrier, which is a paramagnetic material such as a paramagnetic calcium-alginate microcarrier.
일부 실시 형태에서, 췌장 내배엽 세포의 집단은 만능 세포 클러스터의 단계적 분화에 의해 수득된다. 일부 실시 형태에서, 만능 세포는 인간 배아 만능 줄기세포이다. 본 발명의 일 태양에서, 완성 내배엽 계통에 특징적인 마커를 발현하는 세포는 원시선 전구세포이다. 대안적 태양에서, 완성 내배엽 계통에 특징적인 마커를 발현하는 세포는 중내배엽 세포이다.In some embodiments, the population of pancreatic endoderm cells is obtained by staged differentiation of pluripotent clusters. In some embodiments, the universal cell is a human embryonic pluripotent stem cell. In one aspect of the invention, the cell expressing the marker characteristic of the completed endoderm lineage is a progenitor precursor cell. In an alternative embodiment, the cell expressing the marker characteristic of the complete endoderm lineage is a mesodermal endoderm cell.
일부 실시 형태에서, 본 발명은 동적 현탁 배양물 중에서 3 내지 5기 세포를 배양하는 단계를 포함하는 만능 세포를 분화시키는 단계적 방법에 관한 것이다. 일부 실시 형태에서, 생성된 췌장 내배엽 집단은 기능적 췌장 내분비 세포로의 추가의 생체내 성숙을 위해 당뇨병 동물에 이식된다. 본 발명은 또한 본 발명의 방법에 사용하기 위한 시스템 또는 키트를 제공한다.In some embodiments, the present invention relates to a step-wise method of differentiating pluripotent cells, comprising culturing 3-5 period cells in a dynamic suspension culture. In some embodiments, the resulting pancreatic endodermoblast population is implanted into a diabetic animal for further in vivo maturation into functional pancreatic endocrine cells. The present invention also provides a system or kit for use in the methods of the present invention.
본 발명은 또한 본 발명의 방법에 의해 수득가능한 세포 또는 세포 집단을 제공한다. 본 발명은 또한 본 발명의 방법에 의해 수득된 세포 또는 세포 집단을 제공한다.The present invention also provides a cell or cell population obtainable by the method of the present invention. The present invention also provides cells or cell populations obtained by the methods of the present invention.
본 발명은 치료 방법을 제공한다. 특히, 본 발명은 당뇨병을 앓고 있거나, 이것이 발병될 위험에 있는 환자를 치료하는 방법을 제공한다.The present invention provides a method of treatment. In particular, the present invention provides a method of treating a patient suffering from, or at risk of developing, diabetes.
본 발명은 또한 치료 방법에 사용하기 위한 본 발명의 방법에 의해 수득가능하거나 수득된 세포 또는 세포 집단을 제공한다. 특히, 본 발명은 당뇨병을 앓고 있거나, 이것이 발병될 위험에 있는 환자를 치료하는 방법에 사용하기 위한 본 발명의 방법에 의해 수득가능하거나 수득된 세포 또는 세포 집단을 제공한다. 당뇨병은 제1형 또는 제2형 당뇨병일 수 있다.The present invention also provides a cell or a population of cells obtained or obtained by the method of the present invention for use in a therapeutic method. In particular, the present invention provides a cell or cell population obtainable or obtained by the method of the present invention for use in a method of treating a patient suffering from, or at risk of developing, diabetes. Diabetes may be
일 실시 형태에서, 치료 방법은 본 발명의 방법에 의해 수득되거나 수득가능한 세포를 환자에게 이식하는 단계를 포함한다.In one embodiment, the method of treatment comprises implanting into a patient a cell obtainable or obtainable by the method of the present invention.
일 실시 형태에서, 치료 방법은 만능 줄기세포를 시험관내에서, 예를 들어 본 명세서에 기술된 바와 같은, 1기, 2기, 3기, 4기, 또는 5기 세포로 분화시키는 단계, 및 분화된 세포를 환자에게 이식시키는 단계를 포함한다.In one embodiment, the method of treatment comprises the steps of differentiating pluripotent stem cells in vitro, for example, as first, second, third, fourth, or fifth stage cells as described herein, Lt; RTI ID = 0.0 > cells. ≪ / RTI >
일 실시 형태에서, 본 방법은 만능 줄기세포를 분화시키는 단계 전에, 예를 들어 본 명세서에 기재된 바와 같이 만능 줄기세포를 배양하는 단계를 추가로 포함한다.In one embodiment, the method further comprises the step of culturing pluripotent stem cells as described herein, prior to the step of differentiating the pluripotent stem cells.
일 실시 형태에서, 본 방법은 이식 단계 후에, 생체내에서 세포를 분화시키는 단계를 추가로 포함한다.In one embodiment, the method further comprises, after the transplanting step, differentiating cells in vivo.
일 실시 형태에서, 환자는 포유동물, 바람직하게는 인간이다.In one embodiment, the patient is a mammal, preferably a human.
일 실시 형태에서, 세포는 분산된 세포로서 이식될 수 있거나, 또는 클러스터로 형성되어 간문맥 내로 주입될 수 있다. 대안적으로, 세포는 숙주 면역 반응으로부터 보호하기 위해 캡슐화되거나 생체적합성의 분해성 중합체 지지체, 다공성 비분해성 장치 내에 제공될 수 있다. 세포는 수령체의 적절한 부위 내로 이식될 수 있다. 이식 부위는, 예를 들어 간, 천연 췌장, 신장 피막하 공간, 장막, 복막, 장막하 공간, 장, 위, 또는 피하 주머니를 포함한다.In one embodiment, the cells can be implanted as dispersed cells, or they can be formed into clusters and injected into the portal tract. Alternatively, cells may be encapsulated or provided within a biocompatible degradable polymeric support, a porous non-degradable device, to protect against host immune reactions. The cells can be implanted into the appropriate site of the recipient. The transplantation site includes, for example, the liver, natural pancreas, subendicular space, draining membrane, peritoneum, subdural space, intestine, stomach, or subcutaneous pouch.
생체내에서 이식된 세포의 추가 분화, 생존 또는 활성을 향상시키기 위해, 성장 인자, 산화방지제 또는 항염증제와 같은 추가의 인자가 세포 투여 전에, 세포 투여와 동시에, 또는 세포 투여 후에 투여될 수 있다. 이들 인자는 내인성 세포에 의해 분비되어 원위치에서(in situ) 투여된 세포에 노출될 수 있다. 이식된 세포는 당업계에 알려진 내인성 성장 인자 및 당업계에 알려진 외부로부터 투여된 성장 인자의 임의의 조합에 의해 분화되도록 유도될 수 있다.Additional factors such as growth factors, antioxidants or anti-inflammatory agents may be administered prior to, concurrent with, or after administration of the cells to enhance the further differentiation, survival or activity of the transplanted cells in vivo. These factors can be secreted by endogenous cells and exposed to cells administered in situ. The transplanted cells may be induced to differentiate by any combination of endogenous growth factors known in the art and externally administered growth factors known in the art.
이식에 사용되는 세포의 양은 환자의 상태 및 요법에 대한 반응을 포함한 많은 다양한 인자에 의존하며, 당업자에 의해 결정될 수 있다.The amount of cells used for transplantation depends on many different factors including the patient ' s condition and response to therapy, and can be determined by one of ordinary skill in the art.
일 실시 형태에서, 치료 방법은 세포를 이식 전에 3차원 지지체 내로 도입하는 단계를 추가로 포함한다. 세포는 환자에게 이식되기 전에 이 지지체 상에서 시험관내에서 유지될 수 있다. 대안적으로, 세포를 포함하는 지지체는 추가의 시험관내 배양 없이 환자에게 직접 이식될 수 있다. 지지체에는 이식된 세포의 생존과 기능을 촉진하는 적어도 하나의 약제학적 제제가 선택적으로 도입될 수 있다.In one embodiment, the method of treatment further comprises introducing the cells into the three-dimensional support prior to implantation. The cells may be maintained in vitro on this support prior to implantation in the patient. Alternatively, the support comprising the cells may be directly implanted in the patient without further in vitro culture. The support may optionally include at least one pharmaceutical agent that promotes the survival and function of the transplanted cells.
본 발명의 소정 실시 형태에서, 다음 중 하나 이상이 본 발명의 방법에 사용될 수 있다.In certain embodiments of the invention, one or more of the following may be used in the methods of the invention.
[표 A][Table A]
본 명세서 전체에 걸쳐 인용된 간행물은 본 명세서에 전체적으로 참고로 포함된다. 본 발명을 하기 실시예에 의해 추가로 예시하지만 이에 의해 한정되지는 않는다.Publications cited throughout this specification are incorporated herein by reference in their entirety. The present invention is further illustrated by the following examples, but it is not limited thereto.
실시예Example
본 발명은 다음의 비제한적 실시예에 의해 추가로 예시된다.The invention is further illustrated by the following non-limiting examples.
실시예 1Example 1
디스파제/중성 프로테아제에 의한 세포주 H1의 인간 배아줄기세포의 현탁 및 클러스터링Suspension and Clustering of Human Embryonic Stem Cells of Cell Line H1 by Dispase / Neutral Protease
41회째 계대배양의 인간 배아줄기세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재)의 세포를 PBS(카탈로그 번호 14190, 인비트로겐(Invitrogen))로 1회 세척하고, DMEM/F12(인비트로겐 카탈로그 번호 11330, 미국 뉴욕주 그랜드 아일랜드 소재) 중 디스파제®(중성 프로테아제, 시그마 알드리치 컴퍼니 엘엘씨, 카탈로그 번호 D4818, 미국 미주리주 세인트루이스 소재)의 1 mg/mL 용액으로 처리하였다. 콜로니 가장자리가 컬링되고 리프팅되기 시작하지만, 배양 표면으로부터 콜로니의 완전한 탈착이 일어나기 전까지 37℃에서 15 내지 25분 동안 세포를 인큐베이션하였다. 이어서, 디스파제®를 제거하고 배양 디쉬를 10 μM Y-27632(악소라 카탈로그 번호 ALX-270-333, 미국 캘리포니아주 샌디에고 소재)를 함유하는 mTeSR®1(스템 셀 테크놀로지즈, 캐나다 브리티시컬럼비아주 밴쿠버 소재) 배지로 2회 세척하였다. 이어서, 10 μM Y-27632를 함유하는 mTeSR®1 배지를 배양 디쉬에 5 mL/60 ㎠로 첨가하고, 스크레이퍼 또는 고무 폴리스맨을 사용하여 표면으로부터 세포를 리프팅하였다. 이어서, 배지 및 세포를 유리 피펫을 사용하여 50 mL 원추형 튜브에 옮기고 클러스터를 90 g(rcf)로 3분 동안 원심분리하였다.Cells of human embryonic stem cell line H1 (WA01 cells, Wiscel, Wisconsin, Madison, Wis.) Were washed once with PBS (Cat. # 14190, Invitrogen) and resuspended in DMEM / F12 (Invitrogen Catalog No. 11 330, Grand Island, New York material) was of dispase ® (treated with 1 mg / mL solution of a neutral protease, Sigma-Aldrich Company, El elssi, catalog number D4818, St. Louis, Missouri, USA material). The colonies were curled and lifted, but the cells were incubated at 37 ° C for 15 to 25 minutes before complete desorption of the colonies occurred from the culture surface. Then, remove dispase ® and
원심분리 후, 배지를 흡인하고, 세포를 온화하게 재현탁시키고, 225 내지 240 ㎠의 총 평면 배양물(1개의 T225 플라스크 또는 4개의 10 cm 디쉬에 상당함, 대략 9000만개의 세포)당 10 μM Y-27632를 함유하는 mTeSR®1 배지 12 mL 중에서 짧은 시간에 분쇄하였다. 이어서, 10 μM Y-27632를 갖는 2 mL/웰의 새로운 mTeSR®1 배지가 담긴 초저결합 배양 6웰 디쉬(코닝 인코포레이티드, 카탈로그 번호 3471, 미국 뉴욕주 코닝 소재)에 세포 현탁액을 옮겼다. 이러한 방식으로 리프팅된 세포는 단층의 단편들과 유사하였는데, 이때 리프팅된 단편들의 평균 직경은 약 20 내지 30 마이크로미터였으며(도 1a), 각각의 단편은 세포의 군집으로 이루어졌다. 이들 단층 단편을 2시간 동안 현탁 상태로 인큐베이션하였으며(인큐베이션 시간은 0.5 내지 4시간의 범위일 수 있음), 이 시점에서 단편의 응집체가 관찰되었다. 이어서, 응집체를 10 ml 유리 피펫으로 짧은 시간에 분쇄하고, 하룻밤 인큐베이션(응집체는 현탁 상태로 직접 진행될 수 있음)을 저결합 플레이트 내에서 행하였다(응집체는 또한 비처리된 세포 배양 플라스틱 및 표준 조직 배양물 처리된 플라스틱 내에서 인큐베이션될 수 있다).After centrifugation, the medium is aspirated, the cells are mildly resuspended and incubated with 10 [mu] M / well of 225-240 cm2 total flat culture (equivalent to one T225 flask or four 10 cm dishes, approximately 90 million cells) In a short time in 12 mL of
하룻밤 인큐베이션(18 내지 24시간) 후, 세포 및 배지를 50 rpm(30 내지 80+ rpm의 범위일 수 있음)으로 교반되는 25 mL의 mTeSR®1 배지가 담긴 125 mL 스피너 플라스크(코닝 인코포레이티드, 카탈로그 번호 4500-125, 미국 뉴욕주 코닝 소재)에 직접 옮겨서 대략 75 mL의 최종 부피를 만들었다. 배지를 4일 동안 매일 교체하였다. 만능성을 배양물 중에 있은 지 4일 후에 측정하였으며, 유세포측정법의 결과는 분화 마커(CXCR4)는 거의 발현하지 않으면서 만능성 마커(CD9, SSEA4, TRA-1-60, 및 TRA-1-81)에 대해서는 고 발현을 나타내었다. 도 1b를 참조한다. 이들 데이터는, 세포 리프팅제로서 디스파제®를 사용하여 평면 부착성 배양 포맷으로부터 현탁 배양물로 H1 hES 세포가 세포 클러스터로서 성공적으로 옮겨지고 교반(동적) 현탁 배양 시스템 내에서 만능성을 유지할 수 있음을 보여준다. 이 실시예는 또한 교반 현탁 시스템보다는 오히려 플레이트 및 삼각 플라스크를 사용하는 진탕 현탁 시스템 내에서 비견되는 결과로 수행될 수 있다.After overnight incubation (18-24 hours), the cells and medium were transferred to a 125 mL spinner flask (manufactured by Corning Incorporated) containing 25 mL of mTeSR (R) 1 medium, which was stirred at 50 rpm (which may range from 30 to 80+ , Catalog number 4500-125, Corning, NY) to produce a final volume of approximately 75 mL. The medium was changed daily for 4 days. The pluripotency was measured 4 days after the culture, and the results of the flow cytometry showed that the pluripotency marker (CD9, SSEA4, TRA-1-60, and TRA-1-81 ). ≪ / RTI > See FIG. 1B. In these data, the number of a cell lifting claim maintain the universal property in the display using Paget ® flat-adhesive is from the culture format H1 hES cells in suspension culture are successfully transferred into a cell cluster stirring (dynamic) Suspension Culture Systems Lt; / RTI > This embodiment can also be performed as a result of being compared in a shaking suspension system using a plate and an Erlenmeyer flask rather than a stirred suspension system.
현탁 배양물 중에 있은 지 4일 후(분화는 또한 응집체의 형성 후 24 내지 120시간째에 개시될 수 있으며, 바람직하게는 분화 개시 전 2 내지 3일 동안 배양할 수 있음)에, 만능 세포 응집체를 배지 성분들의 단계적 진행으로 분화시켜, 췌장 운명을 형성하도록 세포를 유도하였다. 응집체의 분화를 위해 스피너 교반을 65 rpm의 속도로 높였다. 배지 및 성분이 표 1a에 나타나 있다.After 4 days in the suspension culture (the differentiation can also be initiated 24 to 120 hours after formation of the aggregate, preferably 2 to 3 days before the start of differentiation), pluripotent cell aggregates Cells were induced to differentiate into stepwise progression of media components to form pancreatic fate. Spinner agitation was increased at a rate of 65 rpm for agglutination. The media and components are shown in Table Ia.
1기 말기에, 샘플에 대해 세포측정법 및 PCR을 실시하였다. 현탁 분화된 배양물은 1기 말기에 느슨한 응집체로 균일하고 균질한 세포 집단을 형성하였는데(도 1c), 이때 만능성 마커(CD9)의 발현은 거의 제거되었으며, 한편 완성 내배엽 분화 마커는 매우 높아서, CXCR4(CD184)에 대해서는 97.2%가 양성이고 CD99에 대해서는 97.3%가 양성이었다(도 1d). 이들 결과는 미분화된 WA01 hES 세포와 대비하여, 만능성 유전자(CD9, NANOG, 및 POU5F1/OCT4)의 발현에 있어서는 급격한 감소를 그리고 완성 내배엽과 관련된 유전자(CXCR4, CERBERUS, GSC, FOXA2, GATA4, GATA6, MNX1, 및 SOX17)에 있어서는 큰 증가를 보여준 qRT-PCR 결과와 상관되었다(도 1e).At the end of
이어서, 완성 내배엽 클러스터를 TGF-β 패밀리 구성원인 GDF8을 제거하고, FGF7을 배지에 첨가함으로써 원시 전장을 향해 추가로 분화시켰다. 클러스터를 FGF7과 함께 3일 배양 후, 고 글루코스(25 mM) 및 저농도의 지질 풍부 소혈청 알부민(알부맥스®(라이프 테크놀로지즈 코포레이션(Life Technologies Corporation), 미국 캘리포니아주 칼스배드 소재))을 함유하는 배지 또는 상대적으로 낮은 글루코스 농도(8 mM) 및 2% 무지방산 소혈청 알부민을 함유하는 배지에 올(all)-트랜스-레티노산을 첨가함으로써 췌장 PDX1 발현 운명으로 클러스터를 분화시켰다. 이들 배지에 대한 성분의 상세한 부가사항은 표 1a에 열거되어 있다. 분화 말기에, 췌장 전구세포의 마커의 발현에 대해 샘플을 분석하였다. 조건 - 저 글루코스 + 2% FAF-BSA(A) 또는 고 글루코스 + 0.1% 알부맥스®(B) - 을 사용하여 분화된 클러스터는 유세포측정법에 의해 측정하였을 때, 기능적 β 세포에 요구되는 전사 인자인 NKX6.1을 고수준으로 그리고 시냅토파이신 및 크로모그라닌과 같은 내분비 췌장 마커를 고수준으로 발현한 것으로 관찰되었다(표 1b). 이들 결과는 조건 A 및 조건 B 둘 모두로부터 샘플에서 고수준의 다수의 췌장 전구체 유전자가 발현되었음을 보여준 RT-PCR 결과와 일치하였다(데이터는 도시되지 않음).The finished endoderm clusters were then further subdivided towards the native field by removing the TGF- [beta] family member GDF8 and adding FGF7 to the medium. The clusters were incubated with FGF7 for 3 days and then incubated with high glucose (25 mM) and low concentration of lipid-rich bovine serum albumin (Life Technologies Corporation, Carlsbad, Calif., USA) The clusters were differentiated into pancreatic PDX1 expression fates by adding medium or low-glucose concentration (8 mM) and 2% non-fat bovine serum albumin to the medium containing all-trans-retinoic acid. The detailed additions of ingredients to these media are listed in Table Ia. At the end of differentiation, samples were analyzed for expression of markers of pancreatic progenitor cells. Clusters differentiated using Condition-Low Glucose + 2% FAF-BSA (A) or High Glucose + 0.1% Albumax® (B) - are the transcription factors required for functional β cells High levels of NKX6.1 and endocrine pancreatic markers such as synaptophysin and chromogranin were observed at high levels (Table 1b). These results were consistent with RT-PCR results (data not shown) showing that a high number of high pancreatic precursor genes were expressed in samples from both condition A and condition B.
세포 클러스터들이 분화를 통해 완성 내배엽(DE)(도 1c)으로부터 원시 전장으로 그리고 췌장 내배엽(도 1f) 쪽으로 진행됨에 따라 이들의 전형적인 형태는 세포 및 세포 클러스터에 대한 가시적인 형태학적 변화를 보여주었다. 전형적으로, 만능 클러스터는 위상차 현미경법에 의해 조밀하고 어둡게 나타나며, 이어서 2기에서 세포가 원시 전장으로 진행됨에 따라 외관이 더 느슨해진다. 이러한 형태는 올-트랜스-레티노산 처리 후에 역전되고 클러스터는 매끄러운 클러스터 경계를 가지면서 다시 더 조밀해지고 균일해진다.As the cell clusters progressed from differentiation through the complete endoderm (DE) (Fig. 1c) to the primordial electric field and toward the pancreatic endoderm (Fig. 1f), their typical morphology showed a visible morphological change to the cells and cell clusters. Typically, universal clusters appear dense and dark by phase contrast microscopy, followed by a looser appearance as cells progress from the primitive field to the second. This morphology reverses after the all-trans-retinoic acid treatment and the clusters become smoother and homogeneous again with smooth cluster boundaries.
4기까지 조건 B에 따라 분화된 세포를 ALK5 억제제를 함유하는 5기 배지 중에 추가 5일 동안 유지하였다(표 1c 참조). 배양물 중에서 이러한 추가의 성숙은 내분비 마커 발현에 있어서 유의한 증가를 가져왔다: INS, GCG, SST, PPY, 및 PCSK1. 이어서, 세포 클러스터를 IACUC 승인된 연구 프로토콜에 따라 SCID-Bg 마우스의 신장 피막 내로 이식하고, 절식 상태/급식 상태에서의 C-펩타이드를 매 2 내지 4주마다 측정하면서 20주 동안 마우스를 추적하였다. 이식 후 4주째에, 20시간 절식 그리고 이어서 글루코스 자극 후에, C-펩타이드는 검출되지 않았다. 6주째까지, 5 마리의 마우스 중 2 마리는 인간 C-펩타이드에 대해 약간(0.087 및 0.137 ng/mL) 양성을 나타내었으며, 10주째까지, 5 마리의 마우스 중 5 마리가 C-펩타이드에 대해 양성(0.085 내지 0.291 ng/mL)이었다. 16주째에, 20시간 절식 및 글루코스 자극 후에, 모든 4 마리의 마우스(4/4)가 C-펩타이드 발현에 대해 양성(0.377 내지 3.627 ng/mL)이었다.Cells differentiated according to Condition B until
이들 결과는 만능 세포 응집체가 형성되고, 이어서 현탁 배양물 중에서 분화되어, PDX1 및 NKX6.1과 같은 β 세포 전사 인자의 발현을 특징으로 하는 췌장 전구세포 집단을 생성할 수 있음을 나타낸다. 더욱이, 생체내에 이식하여 성숙되게 한 분화된 세포 클러스터는 글루코스 시험투여(challenge)에 따라 인슐린을 생리학적으로 적절한 수준으로 발현하였다.These results show that pluripotent cell aggregates are formed and then differentiated in suspension cultures to produce a population of pancreatic progenitor cells characterized by the expression of beta cell transcription factors such as PDXl and NKX6.1. Moreover, differentiated cell clusters that have been transplanted and matured in vivo have expressed insulin at a physiologically relevant level according to the glucose challenge challenge.
[표 1a][Table 1a]
[표 1b][Table 1b]
[표 1c][Table 1c]
실시예 2Example 2
EDTA에On EDTA 의한 세포주 H1의 인간 배아줄기세포의 Of human embryonic stem cells 현탁suspension 및 클러스터링 And clustering
41회째 계대배양의 인간 배아줄기세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재)의 세포를 PBS(카탈로그 번호 14190, 인비트로겐)로 1회 세척하고 비효소적 세포 리프팅/계대배양제인 EDTA(론자(Lonza), 카탈로그 번호 17-7-11E)로 처리하였다. 세포를 실온에서 8분 동안 인큐베이션하였다. 이어서, EDTA를 제거하고 추가 1분 또는 2분(총 EDTA 노출 시간은 9 내지 10분임) 후에, 플레이트를 10 μM Y-27632(악소라 카탈로그 번호 ALX-270-333, 미국 캘리포니아주 샌디에고 소재)를 함유하는 mTeSR®1로 헹구고, 이탈된(dislodged) 세포를 유리 피펫을 사용하여 50 ml 원추형 튜브 내에 수집하였다. 10 μM Y-27632를 함유하는 mTeSR®1 배지로 플레이트에 1회의 추가 헹굼을 수행하고 이탈된 세포와 혼주하였다(pooled). 일부 세포가 실온에서 EDTA에 대한 9 내지 10분의 노출 후에 플레이트 상에 남았으며, 리프팅된 세포는 단일 세포 현탁액으로 완전히 분해되지 않았음에 주목한다. 대신, 세포를 작은 응집체로서 표면으로부터 제거하였다. 이어서, 배지 및 세포를 유리 피펫을 사용하여 50 ml 원추형 튜브에 옮기고 세포 카운트를 수행하였다(뉴클레오카운터®-케모메텍 에이/에스(ChemoMetec A/S), 카탈로그 번호 YC-T100, 덴마크 소재). 10 μM Y-27632를 함유하는 추가의 mTeSR®1 배지를 필요에 따라 첨가하여 세포의 농도가 100만 내지 150만개 세포/ml가 되게 하였다.Cells of human embryonic stem cell line H1 (WA01 cells, Wiscel, Wis., Madison, Wis.) Were washed once with PBS (Cat. # 14190, Invitrogen) and incubated with non-enzymatic cell lifting / Lonza, catalog number 17-7-11E). Cells were incubated at room temperature for 8 minutes. The plates were then incubated with 10 μM Y-27632 (Axora Catalog No. ALX-270-333, San Diego, CA) after removing EDTA and an additional 1 or 2 minutes (total EDTA exposure time of 9-10 minutes) , And the dislodged cells were harvested in 50 ml conical tubes using a glass pipette. One additional rinse was performed on the plate with
세포는 원심분리하지 않았는데, 클러스터가 느슨하게 응집되어 있어서 만약 원심분리하여 펠렛을 형성하고 피펫으로 재현탁시킨 경우 단일 세포로 분해될 것이기 때문이었다. 대신, 균일한 현탁액이 형성될 때까지, 튜브 내의 배지 및 세포를 온화하게 와동시켰다. 필요하다면, 또한 EDTA 처리의 기간을 연장시켜 단일 세포 현탁액에 가까운 세포를 취할 수 있다. 이어서, 37℃의 가습된 5% CO2 인큐베이터 내에서 2개의 비-조직 배양물 처리된 6웰 디쉬(벡톤 딕킨슨(Becton Dickinson), 카탈로그 번호 팔콘(Falcon) 351146, 미국 뉴저지주 프랭클린 레이크스 소재)에 유리 피펫을 사용하여 3 ml/웰로 세포 현탁액을 옮겼다. 세포를 2시간 동안 현탁 상태로 인큐베이션하였으며, 이 시점에서 응집체가 관찰되었다. 이어서, 응집체를 유리 피펫으로 온화하게 피펫팅함으로써 분쇄하여 큰 응집체를 파괴하여 균질하고 균일한 클러스터 현탁액을 생성하였으며, 이어서 하룻밤 교란되지 않은 상태로 인큐베이션하였다.The cells were not centrifuged because the clusters were loosely aggregated and if they were centrifuged to form pellets and resuspend in a pipette, they would break down into single cells. Instead, the media and cells in the tubes were gently vortexed until a uniform suspension was formed. If necessary, the duration of the EDTA treatment can also be extended to take cells close to a single cell suspension. (Becton Dickinson, catalog number Falcon 351146, Franklin Lakes, NJ) in a humidified 5% CO 2 incubator at 37 ° C in a non-tissue culture treated 6 well dish (Becton Dickinson, The cell suspension was transferred to 3 ml / well using a glass pipette. Cells were incubated in suspension for 2 hours, at which point aggregates were observed. The agglomerates were then milled by gentle pipetting with a glass pipette to break up the large agglomerates to produce homogeneous and uniform cluster suspensions, followed by overnight incubation without disturbance.
이어서, 18 내지 24시간 후에, 세포 및 배지를 50 mL 원추형 튜브 내에서 90 g(rcf)로 3분 동안 스핀 다운(spin down)시켰다. 폐배지 상층액(spent media supernatant)을 폐기하고, 세포 응집체를 새로운 mTeSR®1 중에 현탁시키고 현탁액을 37℃의 가습된 5% CO2 인큐베이터 내에서 55 rpm으로 교반되는 스피너 플라스크(코닝 인코포레이티드, 카탈로그 번호 4500-125, 미국 뉴욕주 코닝 소재)에 옮겼다. 배지를 2일 동안 매일 교체하였다. 분화 배양물로의 전이 전에, 교반된 현탁 배양물 중에 있은 지 2일 후에 만능성을 측정하였다. CD9, SSEA4, TRA-1-60, TRA-1-81, 및 CXCR4 발현에 대한 유세포측정법의 결과가 도 2a에서 산포도(scatter plot) 포맷으로 나타나 있다. 이들 데이터는 만능성 마커(CD9, SSEA4, TRA-1-60, TRA-1-81)에 대한 고 발현 및 분화 마커(CXCR4)의 저 발현 또는 비발현을 나타낸다. 이들 결과는 비효소적 리프팅 방법을 사용하여 평면 부착성 배양 포맷으로부터 현탁 배양물로 H1 hES 세포가 옮겨져서 동적 교반 현탁 배양 시스템 내에서 만능성을 유지할 수 있음을 나타낸다.Then, after 18-24 hours, the cells and media were spun down for 3 minutes at 90 g (rcf) in a 50 mL conical tube. The spent media supernatant was discarded and the cell aggregates were suspended in
현탁 배양물 중에 있은 지 2일 후에, 만능 세포 응집체를 배지 성분들의 단계적 진행으로 분화시켜, 췌장 운명을 형성하도록 세포를 유도하였다. 스피너 교반을 55 rpm의 속도로 유지하였다. 배지 및 성분들이 표 2a에 나타나 있다.Two days after the suspension culture, the pluripotent cell aggregates were differentiated into the progressive progression of the medium components and cells were induced to form pancreatic fate. The spinner agitation was maintained at a speed of 55 rpm. The media and components are shown in Table 2a.
1기 말기에, 샘플에 대해 세포측정법 및 PCR을 실시하였다. 현탁 분화된 배양물은 1기 말기에 느슨한 응집체로 균일하고 균질한 세포 집단을 형성하였는데(도 2b), 이때 만능성 마커(CD9)의 발현은 거의 제거되었으며, 한편 완성 내배엽 분화 마커인 CXCR4(CD184)는 3개의 스피너 플라스크에 걸쳐 매우 높아서 95.9% ± 1.8 SD였다(도 2c). 이들 결과는 미분화된 WA01 hES 세포와 대비하여, 만능성 유전자(CD9, NANOG, 및 POU5F1/OCT4)의 발현에 있어서는 급격한 감소를 그리고 완성 내배엽과 관련된 유전자(CXCR4, CERBERUS, GSC, FOXA2, GATA4, GATA6, MNX1, 및 SOX17)에 있어서는 큰 증가를 보여준 qRT-PCR 결과와 상관되었다(도 2d).At the end of
이어서, 스피너 플라스크로부터의 완성 내배엽 클러스터를 혼주하고 다른 스피너 플라스크 또는 삼각 플라스크(진탕 교반 시스템)에 분배하였으며, 그리고 GDF8을 제거하고 FGF7을 배지에 첨가함으로써 원시 전장을 향해 추가로 분화되도록 유도하였다. 클러스터를 FGF7과 함께 3일 배양 후, 상대적으로 낮은 글루코스 농도(8 mM) 및 2% 무지방산 소혈청 알부민을 함유하는 배지에 올-트랜스-레티노산을 첨가함으로써 췌장 PDX1 발현 운명으로 클러스터를 분화시켰다. 이들 배지에 대한 성분의 상세한 부가사항은 표 2a에 열거되어 있다. 분화 말기에, 췌장 전구세포의 마커의 발현에 대해 샘플을 분석하였다. 유세포측정법을 사용하여, 두 현탁 포맷 모두에 대해, 기능적 β 세포에 요구되는 전사 인자인 NKX6.1이 고수준이고, 시냅토피신 및 크로모그라닌과 같은 내분비 췌장 마커가 고수준인 것으로 관찰되었다(표 2b 및 도 2e). 이들 결과는 스피너 플라스크 포맷 또는 삼각 플라스크 포맷에서 생성된 샘플에서 매우 유사한 고수준의 다수의 췌장 전구체 유전자가 발현되었음을 보여준 RT-PCR 결과와 일치하였다(도 2f).The finished endoderm clusters from the spinner flasks were then harvested and dispensed into other spinner flasks or Erlenmeyer flasks (shaking agitation system), and GDF8 was removed and FGF7 was induced to further differentiate towards the native field by adding to the medium. The clusters were incubated with FGF7 for 3 days, and then clusters were differentiated into pancreatic PDX1 expression fates by adding all-trans-retinoic acid to a medium containing a relatively low glucose concentration (8 mM) and 2% nonfatty bovine serum albumin . The detailed additions of ingredients to these media are listed in Table 2a. At the end of differentiation, samples were analyzed for expression of markers of pancreatic progenitor cells. Using flow cytometry, for both suspension formats, the transcription factor NKX6.1 required for functional beta cells was high, and endocrine pancreatic markers such as synaptophysin and chromogranin were observed at high levels 2b and 2e). These results were consistent with RT-PCR results (Fig. 2f) showing that a very similar high level of a large number of pancreatic precursor genes was expressed in samples generated in the spinner flask format or the triangular flask format.
이들 결과는 만능 세포 응집체가 형성되고, 이어서 교반 시스템 또는 진탕 현탁 시스템을 포함한 다수의 현탁 배양 포맷으로 현탁 배양물 중에서 분화되어, PDX1 및 NKX6.1과 같은 β 세포 전사 인자의 발현을 특징으로 하는 췌장 전구세포 집단을 생성할 수 있음을 보여준다.These results indicate that pluripotent cell aggregates are formed and then differentiated into suspension cultures in a number of suspension culture formats including agitation systems or agitation suspension systems to form pancreatic cells that are characterized by the expression of beta cell transcription factors such as PDXl and NKX6.1 Progenitor cell population can be generated.
[표 2a][Table 2a]
[표 2b][Table 2b]
실시예 3Example 3
세포주 H1의 인간 배아줄기세포의 현탁 클러스터링 및 연속 현탁 계대배양Suspension clustering and continuous suspension passage of human embryonic stem cells of cell line H1
매트리겔(Matrigel)®(코닝 인코포레이티드, 미국 뉴욕주 코닝 소재)로 코팅된 조직 배양물 처리된 폴리스티렌 상에서 성장된 40회째 계대배양의 인간 배아줄기세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재)의 세포를 PBS(카탈로그 번호 14190, 인비트로겐)로 2회 세척하고 아큐타제®의 1/2 농도 용액(아큐타제® 1부에 대해 PBS 1부, 시그마-알드리치, 카탈로그 번호 A-6964, 미국 미주리주 세인트루이스 소재)으로 처리하였다. 세포를 실온에서 3.5분 동안 인큐베이션하였다. (아큐타제®는 콜라겐분해성 및 단백질분해성 효소(갑각류로부터 단리됨)로 구성된 세포 탈착 용액이고 포유류 또는 세균 유래 생성물을 함유하지 않는다.) 이어서, 아큐타제®를 제거하고 추가 3분(총 아큐타제® 노출 시간은 6.5분임) 후에, 플레이트를 10 μM Y-27632를 함유하는 mTeSR®1 배지로 헹구고, 이탈된 세포를 유리 피펫을 사용하여 50 ml 원추형 튜브 내에 수집하였다. 10 μM Y-27632를 함유하는 mTeSR®1 배지로 플레이트에 1회의 추가 헹굼을 수행하고 이탈된 세포와 혼주하였다. 일부 세포가 아큐타제®에 대한 노출 후에 플레이트 상에 남았으며, 리프팅된 세포는 단일 세포 현탁액으로 완전히 분해되지 않았다. 오히려, 세포를 작은 응집체로서 표면으로부터 제거하였다(도 3a). 이어서, 배지 및 세포를 유리 피펫을 사용하여 50 ml 원추형 튜브에 옮기고 세포 카운트를 수행하였다. 10 μM Y-27632를 함유하는 추가의 mTeSR®1 배지를 필요에 따라 첨가하여 세포의 농도가 100만 내지 150만개 세포/ml가 되게 하였다.Tissue cultures coated with Matrigel (Corning Incorporated, Corning, NY, USA) Human embryonic stem cell line H1 (WA01 cells, Wisconsin, USA) grown in 40th passage on growing treated polystyrene Madison material) PBS (Cat. No. 14 190 of the cells, Invitrogen) and washed with 2 times concentration solution of 1/2 Accu hydratase ® (
세포는 원심분리하지 않았는데, 클러스터가 느슨하게 응집되어 있어서 만약 원심분리하여 펠렛을 형성하고 피펫으로 재현탁시킨 경우 단일 세포로 분해될 것이기 때문이었다. 대신, 균일한 현탁액이 형성될 때까지, 튜브 내의 배지 및 세포를 온화하게 와동시켰다. 이어서, 37℃의 가습된 5% CO2 인큐베이터 내에서 2개의 초저결합 배양 6웰 디쉬에 유리 피펫을 사용하여 3ml/웰로 세포 현탁액을 옮겼다. 세포를 90분 동안 현탁 상태로 인큐베이션하였으며, 이 시점에서 응집체가 관찰되었다. 이어서, 응집체를 짧은 시간에 분쇄하고, 55 rpm으로 교반되는 25 ml mTeSR®1 배지가 담긴 125 ml 스피너 플라스크에 직접 옮겼다(총 최종 부피는 대략 75 mL였음). 배지를 3일 동안 매일 교체하고, 배양물 중에 있은 지 3일째에 만능성을 측정하였다. 클러스터의 위상차 현미경 영상은 정치 현탁 배양물 중에 있은 지 90분 후에 형성되어 배양물 중에서 3일에 걸쳐 증폭된 클러스터의 균일한 구형 집단을 나타낸다(도 3b). 현탁 배양물 중에 있은 지 3일째의 말기에, 마커 CD9, SSEA4, TRA-1-60, TRA-1-81, 및 CXCR4에 대한 유세포측정법의 결과에 의해 만능성에 대해 세포를 검정하였다. 세포는 만능성 마커(CD9, SSEA4, TRA-1-60, TRA-1-81)의 고 발현을 유지하였으며, 분화 마커인 CXCR4에 대해서는 거의 발현을 유지하지 않았다(표 3). 이들 데이터는 효소적 리프팅 방법, 예컨대 아큐타제®를 사용하여 평면 부착성 배양 포맷으로부터 현탁 배양물로 H1 hES 세포가 옮겨질 수 있으며, 동적 교반 현탁 배양 시스템 내에서 만능성을 유지할 것임을 나타낸다.The cells were not centrifuged because the clusters were loosely aggregated and if they were centrifuged to form pellets and resuspend in a pipette, they would break down into single cells. Instead, the media and cells in the tubes were gently vortexed until a uniform suspension was formed. Subsequently, the cell suspension was transferred to 3 ml / well using a glass pipette in two ultra low
이어서, 만능성 클러스터를 추가 20회의 계대배양 동안 아큐타제® 해리를 사용하여 연속 계대배양시켰다. 각각의 계대배양에서는, 5000만개의 세포를 50 ml 원추형 튜브 내에 2분 동안 중력 정착시키고, PBS로 2회 세척하고, 37℃ 수욕에서 아큐타제®의 1/2 농도 용액으로 처리하였는데, 이때 아큐타제®의 첨가 후 2분 및 4분째에 튜브를 온화하게 와동시켰다. 6분의 인큐베이션 후에, 세포 펠렛을 교란시키지 않으면서 아큐타제®를 튜브로부터 흡인하였다. 이어서, 세포를 추가 3분(총 아큐타제® 노출 시간은 9분임) 동안 인큐베이션하였다. 이어서, 튜브를 10 μM Y-27632를 함유하는 mTeSR®1 배지로 헹구고, 유리 피펫을 사용하여 2회 분쇄하고, 현탁된 세포를 70 마이크로미터 세포 여과기(비디 팔콘(BD Falcon), 카탈로그 번호 352350, 미국 뉴저지주 프랭클린 레이크스 소재)에 통과시켰다. 10 μM Y-27632를 함유하는 mTeSR®1 배지로 튜브에 2회 추가 헹굼을 수행하고 세포 여과기에 통과시켰다.Then, by using the Accu hydratase ® dissociation for a further 20 times of the all-round passages crystalline clusters were incubated serial passages. In each of the passages, of the 50 million cells and gravity settling for 2 minutes in a 50 ml conical tube, were washed twice with PBS, and treated at 37 ℃ water bath to half the concentration of the solution Accu hydratase ®, The Accu hydratase The tube was gently vortexed at 2 and 4 minutes after addition of < RTI ID = 0.0 > After incubation for 6 minutes, a standing Accu hydratase ® without disturbing the cell pellet was drawn from the tube. Then, add the cells incubated for 3 min (total occupancy hydratase ® exposure time was 9 minutes). The tubes were then rinsed with mTeSR.RTM. 1 medium containing 10 .mu.M Y-27632, pulverized twice using a glass pipette, and suspended in a 70 micrometer cell filter (BD Falcon, Cat. No. 352350, Franklin Lakes, New Jersey, USA). The cells were further rinsed twice with
균일한 현탁액이 형성될 때까지, 튜브 내의 배지 및 세포를 온화하게 와동시켰다. 이어서, 37℃의 가습된 5% CO2 인큐베이터 내에서 초저결합 배양 6웰 디쉬에 유리 피펫을 사용하여 3 ml/웰로 세포 현탁액을 옮기고, 2시간 동안 현탁 상태로 인큐베이션하였으며(0 내지 28시간 시험함), 이 시점에서 80 ml의 최종 부피의 배지가 담긴 유리 스피너 플라스크에 응집체를 옮겼다. 대안적으로, 세포 현탁액은 55 rpm으로 교반되는 스피너 플라스크 또는 40 rpm으로 진탕되는 삼각 플라스크 내에 직접 넣을 수 있었으며, 80 ml의 최종 부피의 배지 중의 교반된 현탁액 중에서 클러스터가 형성되었다(도 3c).The media and cells in the tubes were gently vortexed until a uniform suspension was formed. Subsequently, the cell suspension was transferred to a very low binding culture 6-well dish in a humidified 5% CO 2 incubator at 37 ° C using a glass pipette at 3 ml / well, and incubated for 2 hours in a suspension state (0 to 28 hours ), At which point the agglomerates were transferred to a glass spinner flask containing 80 ml of final volume of medium. Alternatively, the cell suspension could be placed directly in a spinner flask stirred at 55 rpm or in an Erlenmeyer flask shaken at 40 rpm and clusters were formed in a stirred suspension in a final volume of 80 ml medium (Fig. 3C).
이러한 연속 계대배양 방법을 사용하여, 세포를 20회 계대배양하였는데, 이때 각각의 계대배양에서는 대략 1:3의 분할비를 사용하였다. 만능성을 유세포측정법에 의해 각각의 계대배양에서 측정하고 핵형을 염색체 12 및 17에 대해 형광 계내 혼성화(florescent in-situ hybridization, FISH) 검정을 사용하여 결정하였으며; 2개의 염색체는 hES 세포에서 잠재적으로 불안정한 것으로 확인되었다. CD9, SSEA4, TRA-1-60, TRA-1-81, 및 CXCR4 발현에 대한 유세포측정법의 결과는 산포도 포맷으로 나타나 있고 만능성 마커에 대한 고 발현 및 분화 마커(CXCR4)의 저 발현 및 비발현을 나타내었으며, 한편 염색체 12 및 17에 대한 FISH 검정은 정상 카피수(copy number)를 나타내었다. 이들 데이터는 H1 hES 세포가 비포유동물의 효소적 세포 해리 방법인 아큐타제®를 사용하여 일상적인 연속 계대배양을 행하면서 현탁 배양물 중에서 유지될 수 있으며, 동적 교반 현탁 배양 시스템 내에서 만능성 및 안정한 핵형을 유지하여, 20회의 계대배양의 과정에 걸쳐 원래의 투입 세포당 1×109개의 세포를 생성할 것임을 나타낸다. EDTA가 또한 6회의 계대배양 동안 이러한 연속 현탁에 사용될 수 있다.Using this continuous subculture, cells were subcultured 20 times, with a split ratio of approximately 1: 3 in each subculture. For the karyotype was measured in each of the passages by the all-purpose property in flow cytometry measurement on
[표 3][Table 3]
실시예 4Example 4
세포주 H1의 현탁 배양된 인간 배아줄기세포의 유도 분화Induction Differentiation of Suspension Cultured Human Embryonic Stem Cells of Cell Line H1
40회째 계대배양의 인간 배아줄기세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재)의 세포를 아큐타제®를 사용하여 평면 부착성 배양물로부터 리프팅시키고 현탁 배양 포맷으로 옮겼다. 실시예 3에 기술된 방법을 사용하여 30회의 계대배양 동안 동적 교반 현탁 배양 시스템 내에서 세포를 유지하였다.The 40 th subculture the cells of the human embryonic stem cell line H1 (WA01 cells, wisel, Madison, Wisconsin, USA material) by using the Accu hydratase ® and lifted from the plane adhesive culture was transferred to suspension culture formats. Cells were maintained in a dynamic stirred suspension culture system for 30 passages using the method described in Example 3. [
표 3에 나타낸 바와 같이 처음 20회의 계대배양을 통해 만능성을 확인하였는데, 유세포측정법에 의해 측정된 바와 같이, 안정한 고수준의 만능성 마커가 배양 전체에 걸쳐 유지되었다. 만능성을 확인하고 당뇨병 치료용 세포 공급원을 제공하는 능력을 보여주기 위해, 정상 췌장 발생을 반복하도록 의도된 모르포겐 또는 성장 인자를 함유하는 상이한 배지의 단계적 진행을 통해 동적 교반 현탁 배양 시스템 내에서 세포를 췌장 전구체로 분화시켰다. 이 과정은 고 PDX1 및 NKX6.1 동시발현(co-expression)을 특징으로 하는 췌장 전구세포 집단을 발생시킨다. 이들 세포를 이식하였을 때, 이들은, 글루코스에 따라 인슐린을 분비할 수 있는 기능적 글루코스 자극 인슐린 분비 조직으로 추가로 성숙되어 스트렙토조토신 유도 당뇨병 모델에서 정상의 혈당을 유지하였다. 도 4c 및 표 4c를 참조한다.The pluripotency was verified through the first 20 passages as shown in Table 3, where stable, high-level universal markers were maintained throughout the culture as measured by flow cytometry. To demonstrate the ability to identify universality and provide a cellular source for the treatment of diabetes, it has been found that in a dynamic stirred suspension culture system, through stepwise progression of different media containing mofoGen or growth factors intended to repeat normal pancreas development The cells were differentiated into pancreatic precursors. This process generates a population of pancreatic progenitor cells characterized by high PDX1 and NKX6.1 co-expression. When these cells were transplanted, they were further matured as a functional glucose-stimulated insulin-secreting tissue capable of secreting insulin according to glucose and maintained normal glucose levels in the streptozotocin-induced diabetic model. See Figures 4c and 4c.
이들 췌장 전구세포를 생성하기 위하여, 16회의 계대배양 동안 동적 교반 현탁 배양 시스템 내에서 증폭시키고 유지한 H1 인간 배아줄기세포를 실시예 3에 기술된 방법을 사용하여 분화시켰다. 요약하면, 세포를 30회의 계대배양 동안 증폭시키고, 이들 계대배양의 처음 20회 동안에는 만능성에 대해 시험하였으며; 세포를 16번째 계대배양 시에 분화시켰다. 클러스터 포맷의 만능 세포를 mTeSR®1 배지로부터 FBC 용액(표 4a)으로 4℃에서 3시간 동안 옮겨 두었다. 이어서, 세포 클러스터를 사르토리우스 스테딤 바이오스탯(Sartorius Stedim Biostat) B-DCU(독일 괴팅엔 소재) 제어 유닛에 의해 조절된 3 리터 유리 현탁 생물반응기로 이동시켜서 표 4b에 따라 55만개 세포/mL로 분화 배지 중에 현탁시켰다. 온도, pH, 및 용존 산소(DO)에 대해 조절된 폐쇄된 멸균 현탁 생물반응기(펌프로브(FermProbe)® pH 전극 225 mm, 모델 번호 F-635, 및 용존 산소 옥시프로브(OxyProbe)® 12 mm 센서, 모델 번호 D-145, 미국 캘리포니아주 어바인 소재의 브로들리-제임스 코포레이션(Broadley-James Corporation)으로부터 입수됨) 내에서 세포를 14일 유지하였다.To generate these pancreatic progenitor cells, H1 human embryonic stem cells amplified and maintained in a dynamic stirred suspension culture system during 16 passages were differentiated using the method described in Example 3. Briefly, cells were amplified during 30 passages and tested for universality during the first 20 passages of these passages; Cells were differentiated during the 16th passage. Cluster-format pluripotent cells were transferred from
이 실시 내내, 1.6 리터 이하의 총 배지 부피에서 CO2 유동의 조절에 의해 pH를 pH 7.4로 유지하면서, 배지 중탄산염 수준을 3.64 g/L로 유지하였다. 150 cc/min의 일정 가스 유동으로, 1기에 대해서는 20% 용존 산소 설정점을 그리고 2기 이후에 대해서는 30% 용존 산소 설정점을 갖는 사르토리우스 제어 시스템의 제어 하에서 생물반응기의 헤드스페이스에 CO2, 공기, 및 O2를 관류시켰다. 산소 유동은 용존 산소 함량에 따라 조절하고, CO2 유동은 pH에 따라 조절하였다. 온도는 전기 가열식 재킷에 의해 실시 내내 37℃로 유지하였다. 실시 개시 시에 그리고 각각의 배지 교체 동안(교체 시마다 배지의 93%가 제거됨), 임펠러(3" 스테인리스 강 피치 블레이드 임펠러가 70 rpm으로 작동됨)를 정지시키고, 테루모(Terumo)™ 튜브 용접기를 사용하여 C-플렉스(C-Flex)® 튜빙에 연결된 생물반응기 내의 딥 튜브(dip tube)를 통해 연동 펌프에 의해 배지를 제거하거나 첨가하여 폐쇄된 시스템을 유지하였다. 세포/클러스터의 영상을 각각의 분화 단계의 말기에 촬영하고, 유세포측정법 샘플을 수집하여 1기 3일째에 그리고 3일 후인 2기 말기에 CXCR4 발현에 대해 검정하였다(도 4a). 분화의 개시(표 3, 16회째 계대배양) 시에 CXCR4 음성 만능 세포 집단으로부터의 CXCR4를 발현하는(98.5%의 세포가 CXCR4 양성임, 도 4b) 세포의 집단으로의 거의 완전한 집단 전이가 관찰되었다. 이어서, 이들 세포는 3일 후인 2기 말기에 거의 CXCR4가 음성인 상태(7.0%의 세포가 CXCR4 양성임)로 전이하였으며, 3기 말기까지 세포는 CD56 양성 단계로 거의 완전하게 전이하였다. 4기 4일째의 분화 과정의 말기에, 세포는 PDX1 발현에 대해 88.5%가 양성이었으며(도 4b), 췌장 내분비 세포 (33.5%가 크로모그라닌 양성임) 및 췌장 선조세포(65.7%가 NKX6.1에 대해 양성임)의 혼합물과 일치하는 발현 패턴을 나타내었다. 이러한 단계 특이적인 마커 발현 패턴은 만능성 집단으로부터 췌장 세포로의 효율적인 단계적 분화를 나타내었다. 분화 과정의 말기에, 277만개 세포/mL를 생성하였는데(1.5 리터 중 41억개의 세포), 이는 각각의 투입 hES 세포당 5개의 분화된 세포의 총 질량 증폭을 나타낸다.Throughout this run, the medium bicarbonate level was maintained at 3.64 g / L while the pH was maintained at pH 7.4 by control of the CO 2 flow at a total volume of the medium of 1.6 liters or less. Under the control of a Sartorius control system with a constant gas flow of 150 cc / min, with a 20% dissolved oxygen set point for the first stage and a 30% dissolved oxygen setpoint for the second stage and later, the headspace of the bioreactor was loaded with CO 2 , Air, and O 2 were perfused. Oxygen flow was controlled by dissolved oxygen content and CO 2 flow was controlled by pH. The temperature was maintained at 37 [deg.] C throughout the run by an electric heating jacket. The impeller (3 "stainless steel pitch blade impeller operated at 70 rpm) was stopped at the start of the run and during each medium change (93% of the medium was removed each time it was replaced) and the Terumo ™ tube welder Closed systems were maintained by removing or adding media by a peristaltic pump through a dip tube in a bioreactor connected to a C-Flex® tubing using the system. At the end of the differentiation phase, flow cytometry samples were collected and assayed for CXCR4 expression at the end of
실시 말기에, 500 mL를 원심분리 및 세척을 위하여 회수하여 생착, 성숙, 및 기능의 동물 모델에서 시험하였다. 나머지 1000 mL의 세포 현탁액을 kSep® 400 시스템(케이비아이 바이오시스템즈(KBI Biosystems), 미국 노스캐롤라이나주 더럼 소재) 내에서 처리하여 완전 폐쇄 루프 시스템으로 세포 생성물을 세척하고, 여과하고, 농축시켰다. 세포 생성물을 1 리터의 출발 부피로부터 4100만개 세포/mL의 최종 농도의 50 mL의 농축된 세포로 농축시켰다. 이어서, 이들 농축된 세포를 자동화 바이알 충전기(필-잇(Fill-It), TAP, 영국 허트포드셔 소재)를 사용하여 1.2 ml의 충전 부피를 갖는 24개 바이알에 분배하고 액체 질소 동결기 내로 넣어서 동결시켰다.At the end of the run, 500 mL was collected for centrifugation and washing and tested in animal models of engraftment, maturation, and function. The remaining 1000 mL of cell suspension was treated in a
세척하여 표준 원심분리로 농축시킨 500 mL의 분화된 세포를 SCID-Bg 마우스당 500만개의 세포의 투여량으로 이식시켰는데, 신장 피막 바로 아래에 두거나, 면역-보호성 거대 캡슐화 장치(미국 캘리포니아주 어바인 소재의 테트라사이트™) 내부에 넣어서 피하 이식시켰다(조건당 6마리의 동물). 이식 후 12주째까지, 이식된 세포는 절식 및 이후의 급식에 따라 ELISA(인간 C-펩타이드 주문제작 ELISA 메르코디아(Mercodia) 카탈로그 번호 10-1141-01)에 의해 검출하였을 때 유의한 수준의 순환 인간 C-펩타이드(0.1 ng/mL 초과)를 발현하였고, 16 내지 20주까지 동물은 1 ng/mL를 초과하는 순환 C-펩타이드를 가졌다(표 4c).500 mL of differentiated cells that had been washed and concentrated by standard centrifugation were transplanted at a dose of 5 million cells per SCID-Bg mouse, either placed directly beneath the kidney capsule or placed in an immunostimulatory macroencapsulation device (Tetrasite < (R) > in Irvine) (6 animals per condition). By 12 weeks post-transplantation, the transplanted cells had a significant level of circulation when detected by ELISA (human C-peptide custom ELISA Mercodia catalog number 10-1141-01) according to fasting and subsequent feeding Human C-peptide (greater than 0.1 ng / mL), and by 16-20 weeks the animals had circulating C-peptide greater than 1 ng / mL (Table 4c).
이식 후 27주(190일)째에, 장치에 의해 캡슐화된 면역-보호된 이식편을 갖는 2마리의 동물을 단회 고용량의 스트렙토조티신(STZ)으로 각각 처리하여 모든 내인성 마우스 β 섬 세포를 선택적으로 사멸시켜 당뇨병을 유도하였다(250 mg/Kg). 대조군 동물에서 임상적으로 확실한 당뇨병을 유도하는 데 충분한 STZ 처리 후 그 다음 2주 동안, 생착된 동물의 혈당 수준은 정상 범위(150 mg/dL 미만) 내로 유지되었다. 이어서, 이식 후 29주째에 그리고 STZ 투여 후 2주째에, 2 마리의 동물을 글루코스 자극 인슐린 분비(GSIS)에 대해 시험하였으며, 글루코스 투여에 따라 순환 인간 C-펩타이드에 있어서 현저한 증가를 나타내었다. 더욱이, 이식편 각각을 이식 후 209일째(29.5주째)에 제거하였을 때, 동물의 혈당 수준은 500 mg/dL 초과까지 급격히 증가하였다.At 27 weeks (190 days) after transplantation, two animals with immuno-protected grafts encapsulated by the device were each treated with a single high dose of streptozotocin (STZ) to selectively infuse all endogenous mouse beta islet cells Diabetes was induced by killing (250 mg / Kg). During the next two weeks after STZ treatment sufficient to induce clinically definite diabetes in control animals, blood glucose levels in engrafted animals were maintained within the normal range (less than 150 mg / dL). Then, at 29 weeks after transplantation and at 2 weeks after STZ administration, 2 animals were tested for glucose stimulated insulin secretion (GSIS) and showed a significant increase in circulating human C-peptide upon glucose administration. Moreover, when each graft was removed at 209 days (29.5 weeks) after transplantation, the blood glucose level of the animals increased sharply to above 500 mg / dL.
이들 결과는 당뇨병을 치료하기 위한 인간 배아줄기세포 유래 세포 생성물이 증폭 및 분화된 줄기세포의 현탁으로부터 제조될 수 있음을 보여준다. 생성물은 스케일 조정가능한 교반 폐쇄 루프 생물반응기 시스템 내에서 생성될 수 있으며, 세포 생성물은 시판되는 cGMP 제조를 위해 필요에 따라 폐쇄 루프 세척 및 농축으로 처리될 수 있다. 이러한 인간 배아줄기세포 유래 세포 생성물은 GSIS 컴피턴스(competence), 혈당 조절 능력, 및 세포 요법의 제거 시의 당뇨병 상태로의 복귀에 의해 보여지는 바와 같이 광범위하게 사용된 당뇨병 동물 모델에서 당뇨병을 치료할 수 있다.These results show that human embryonic stem cell-derived cell products for the treatment of diabetes can be prepared from the suspension of amplified and differentiated stem cells. The product can be produced in a scalable stirred closed loop bioreactor system and the cell product can be treated with closed loop washing and concentration as needed for commercial cGMP production. Such human embryonic stem cell-derived cell products can be used to treat diabetes in a widely used diabetic animal model, as shown by GSIS competence, ability to regulate blood glucose, and return to diabetic state upon removal of cell therapy have.
[표 4a][Table 4a]
[표 4b][Table 4b]
[표 4c][Table 4c]
실시예 5Example 5
세포주 H1의 부착성 배양된 인간 배아줄기세포의 현탁 포맷에서의 유도 분화Adherence of cell line H1 Induction differentiation in cultured human embryonic stem cells in suspension format
41회째 계대배양의 인간 배아줄기세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재)의 세포를, 실시예 2에 기술된 방법을 사용하여, EDTA를 사용하여 평면 부착성 배양물로부터 리프팅시키고 현탁 배양 포맷으로 옮겼다.Cells of human embryonic stem cell line H1 (WA01 cells, Wiscel, Wis., Madison, Wis., USA) at 41st passage were lifted from flat adherent cultures using EDTA using the method described in Example 2 and suspended Culture format.
세포 응집체의 만능성을 도 5a에 나타낸 바와 같이 유세포측정법으로 측정하여 세포가 고도로 만능성임을 나타내는, 만능성 마커 CD9, SSEA4, TRA-1-61, 및 TRA-1-80의 고 발현을 관찰하였다. 이어서, 이들 만능 세포를 정상 췌장 발생의 모르포겐 구동을 반복하도록 의도된 소분자 및 성장 인자를 함유하는 상이한 배지의 단계적 진행을 통해 동적 교반 현탁 배양 시스템 내에서 췌장 전구체로 분화시켰다. 이 과정은 췌장 세포 전사 인자인 PDX1 및 NKX6.1의 동시발현을 특징으로 하는 췌장 전구세포 집단을 생성한다. 이들 세포가 이식되는 경우, 이들은 스트렙토조토신 유도 당뇨병 모델에서 고 혈당을 교정할 수 있는 기능적 글루코스 자극 인슐린 분비 조직으로 추가로 성숙된다.The pluripotency of the cell aggregates was measured by flow cytometry as shown in Fig. 5A, and high expression of the pluripotency markers CD9, SSEA4, TRA-1-61, and TRA-1-80 was observed, indicating that the cells were highly versatile . These pluripotent cells were then differentiated into pancreatic precursors in a dynamic stirred suspension culture system via stepwise progression of different media containing small molecules and growth factors intended to repeat the mordogens drive of normal pancreas development. This process produces a population of pancreatic progenitor cells characterized by the co-expression of pancreatic cell transcription factors PDX1 and NKX6.1. When these cells are transplanted, they are further matured into a functional glucose-stimulated insulin-secreting tissue capable of correcting hyperglycemia in a streptozotocin-induced diabetic model.
췌장 전구세포 집단을 생성하기 위해, mTeSR®1 배지 중에 유지된 클러스터 포맷의 만능 세포를, 제어기 조절된 온도, pH, 및 용존 산소를 갖는 0.2 리터 유리 교반 현탁 생물반응기(다스깁(Dasgip), 카탈로그 번호 DS0200 TBSC, 미국 매사추세츠주 슈루즈버리 소재)에 옮겼다. 만능 세포 클러스터를 생물반응기 내에서 2일 동안 배양하였다. 그 시점에서(1기 0일째), 배지를 교체하고, 세포 응집체가 표 5a에 따라 분화 배지 중에 대략 70만개 세포/mL로 현탁되었을 때 분화를 개시하였다. 이어서, 이 폐쇄된 멸균 현탁 생물반응기 내에서 14일 동안 세포를 유지하였다. 분화 전체에 걸쳐, 0.3 리터의 총 부피에서 CO2 유동의 조절에 의해 pH를 7.4로 유지하면서, 배지 중탄산염 수준을 3.64 g/L로 유지하였다. 5 리터/시간의 일정 가스 유동 하에서 30% 용존 산소 설정점을 갖는 다스깁 제어 시스템의 제어 하에서 생물반응기의 헤드스페이스에 CO2 및 공기를 스파징하였다(sparged). 공기 유동은 용존 산소 함량에 따라 조절하고, CO2 유동은 pH에 따라 조절하였다.To produce a population of pancreatic progenitor cells, cluster cells in cluster format, maintained in
[표 5a][Table 5a]
이 실시예에 그리고 본 명세서 전체에 걸쳐 사용되는 바와 같이, SCIO는 화학명이 4-{[2-(5-클로로-2-플루오로페닐)-5-(1-메틸에틸)피리미딘-4-일]아미노}-N-(2-하이드록시프로필)피리딘-3-카르복스아미드이고 CAS 번호 674794-97-9를 갖는 Alk5 억제제이다. SCIO의 화학 구조가 하기에 나타나 있다:As used throughout this specification and throughout this disclosure, SCIO is a chemical compound that is a chemical name of 4- {[2- (5-chloro-2-fluorophenyl) -5- (1-methylethyl) pyrimidin- Amino] -N- (2-hydroxypropyl) pyridine-3-carboxamide and CAS No. 674794-97-9. The chemical structure of SCIO is shown below:
실시 내내 온도를 37℃로 유지하였다. 실시 개시 시에 그리고 각각의 배지 교체 동안(교체 시마다 배지의 95%가 제거됨), 임펠러를 정지시키고, 테루모™ 튜브 용접기를 사용하여 C-플렉스® 튜빙에 연결된 생물반응기 딥 튜브를 통해 연동 펌프에 의해 배지를 제거하고, 이어서 첨가하여 폐쇄된 시스템을 유지하였다.The temperature was maintained at 37 占 폚 throughout the run. At the start of the run and during each media change (95% of the media removed each time it was replaced), the impeller was stopped and placed in a peristaltic pump through a bioreactor dip tube connected to C-Flex® tubing using a Terumo ™ tube welder The medium was removed by subsequent addition, and the closed system was maintained.
몇몇 상이한 공급물 세팅을 1기 동안 시험하였다: (a) 분화 개시 후 24시간째에 배지 교체, 48시간째에는 배지 교체 없음; (b) 분화 개시 후 24시간째에 배지 교체 및 48시간째에 글루코스 볼루스 첨가; 및 (c) 1기 전체에 걸쳐 배지 교체는 없으면서, 글루코스 및 GDF8 볼루스를 분화 개시 후 24시간째에 첨가하고, 이어서 글루코스 볼루스를 개시 후 48시간째에 첨가함.Several different feed settings were tested for one period: (a) media change at 24 hours after initiation of differentiation, no media change at 48 hours; (b) 24 hours after the initiation of differentiation, medium was replaced, and glucose bolus was added at 48 hours; And (c) glucose and GDF8 boluses were added 24 hours after the start of differentiation, without replacing the medium throughout the first period, followed by addition of
이 과정의 초기, 중기, 및 말기에서의 세포 카운트를 각각의 반응기에 대해 표 5b에 열거된 바와 같이 얻었다. 1기 말기에, 유세포측정법에 의한 단백질 발현 패턴을 위하여 세포를 샘플링하였다. 조건 A - 완성 내배엽으로의 분화 개시 후 24시간째에 배지 교체, 이어서 그 다음 48시간째에는 배지 교체 없음 - 에서 분화된 세포는 분화 마커(CD99 및 CXCR4)의 유도 및 만능성 마커의 발현(CD9)에 있어서의 감소에 의해 측정된 바와 같이 최상의 결과를 나타내었다(도 5b). 완성 내배엽 형성의 말기에서의 CD9의 더 낮은 발현과 조합된 CXCR4 및 CD99의 더 높은 발현은 췌장 유전자의 더 높은 발현, 및 분화에서의 나중의 대안의 기관 운명을 나타내는 유전자의 더 낮은 발현과 상관되었다(도 5d 및 도 5e). 구체적으로, 제1 분화 단계 전체에 걸쳐 배지 교체 없음 또는 대량 급식 포맷으로의 1기에서의 배지에 대한 글루코스의 첨가 중 하나 또는 둘 모두는 1기 말기에 더 낮은 CXCR4 수준을 가져왔으며, 이는 4기 분화의 말기에 매우 상이한 응집체 형태와 상관되었다(도 5c). 구체적으로, 조건 B 및 조건 C는 유세포측정법에 의해 측정하였을 때, 4기 말기에 더 낮은 췌장 유전자 발현(NKX6.1 및 CHGA) 및 비-췌장 유전자(CDX2 및 SOX2)의 더 높은 발현을 가졌다(도 5d 및 표 5b). 이들 결과는 qRT-PCR에 의해 입증되었는데(도 5e), 조건 A는 조건 C보다 유의하게 더 높은 췌장 유전자의 발현을 나타내었으며, 조건 B는 조건 A와 조건 C에 대해 중간인 바와 같다. 더욱이, 조건 C는 대안의 비-췌장 운명을 나타내는 유전자, 예를 들어 CDX2, AFP, 및 알부민을 유의하게 더 높은 수준으로 발현하였다(도 5e). 이들 데이터는 완성 내배엽(DE) 형성의 마지막 48시간 동안 배지 교체 없이 생성된, 균질한 고 CXCR4 발현 DE가 순수한 췌장 내배엽 집단으로 나중에 전환될 수 있음을 나타낸다.Cell counts at the beginning, middle, and end of this process were obtained as listed in Table 5b for each reactor. At the end of
4기 분화의 말기에, 조건 A에 따라 분화된 세포를 생물반응기로부터 회수하여 0.1% FAF-BSA를 함유하는 MCDB131 배지로 세척하고 SCID-Bg 마우스에 이식하였다. 각각의 마우스에 500만개의 세포를 신장 피막 아래에 직접 이식하였다. 이식 후 매 4주째마다 채혈을 수행하고 혈당 및 C-펩타이드를 측정하였다. 이식 후 12주째까지, 인간 C-펩타이드는 ELISA에 의해 1 ng/mL 초과의 수준으로 검출가능하였으며, 16주째에 C-펩타이드 수준은 평균 2.5 ng/mL였다(도 5f). 이식 후 20주째에, 절식 상태 및 이후의 급식 상태의 동물에서 C-펩타이드를 측정하였다. 글루코스 처리는 순환 인간 C-펩타이드에 있어서 절식 상태에서의 0.93 ng/mL로부터 급식 상태에서의 2.39 ng/mL로의 유의한 증가를 유도하였는데(도 5g), 이는 이식된 세포가 기능적 GSIS 컴피턴트 조직으로 성숙하였음을 나타낸다. 더욱이, 동물에 스트렙토조토신(STZ) 투여(마우스 β 세포는 인간 β 세포와 비교하여 STZ에 대해 더 민감하여 우선적으로 파괴됨)를 제공하여 당뇨병 상태를 유도한 경우, 기능적 GSIS 컴피턴트 조직의 이식편을 갖는 동물은 임상적으로 확실한 당뇨병이 발생된 비처리된 대조군과는 달리 정상의 혈당 수준을 유지하였다(도 5h). 이들 결과는 hES 분화된 세포 이식편을 갖는 동물이 기능적 췌장 조직 이식편에 의해 STZ 유도 당뇨병으로부터 보호되었음을 보여준다.At the end of the four-phase differentiation, cells differentiated according to Condition A were recovered from the bioreactor, washed with MCDB131 medium containing 0.1% FAF-BSA, and transplanted into SCID-Bg mice. Five million cells per mouse were directly implanted under the kidneys. Blood was collected every 4 weeks after transplantation and blood glucose and C-peptide were measured. By 12 weeks post-transplantation, human C-peptide was detectable at levels greater than 1 ng / mL by ELISA and C-peptide levels averaged 2.5 ng / mL at 16 weeks (FIG. 5f). At 20 weeks post-transplantation, C-peptide was measured in fasted state and later fed animals. Glucose treatment induced a significant increase in circulating human C-peptide from 0.93 ng / mL in the fasted state to 2.39 ng / mL in the fed state (Fig. 5g), suggesting that the transplanted cells are functionally GSIS competent tissues Indicates maturity. Furthermore, when a diabetic state is induced by administration of streptozotocin (STZ) to animals (mouse beta cells are more susceptible to STZ than mouse beta cells and are preferentially destroyed), the grafts of functional GSIS competent tissues The animals had normal blood glucose levels unlike the untreated controls with clinically definite diabetes (Fig. 5h). These results show that animals with hES differentiated cell grafts were protected from STZ induced diabetes by functional pancreatic tissue grafts.
[표 5b][Table 5b]
실시예Example 6 6
세포주 H1의 마이크로캐리어 부착성 배양된 인간 배아줄기세포의 현탁 포맷에서의 유도 분화Microcarrier adhesion of cell line H1 Induction differentiation of human embryonic stem cells cultured in suspension format
사이토덱스(Cytodex)® 3 마이크로캐리어 비드(C3)(시스마-알드리치 컴퍼니 엘엘씨, 미국 미주리주 세인트루이스 소재, 카탈로그 번호 C3275) 400 mg을 15 ml의 둘베코(Dulbecco) PBS(DPBS)가 담긴 20 ml 부피 규소 코팅 유리 신틸레이션 바이알 내에 4 내지 24시간 동안 액침(soak)함으로써 배양을 위해 준비하였다. 사이토덱스® 3은 가교결합된 덱스트란의 매트릭스에 화학적으로 커플링된 변성된 콜라겐의 얇은 층으로 이루어진다. 사이토덱스® 3 상의 변성된 콜라겐 층은 트립신 및 콜라게나제를 포함한 다양한 프로테아제에 의한 효소분해에 취약하고, 최대 세포 생존력, 기능, 및 완전성(integrity)을 유지하면서 마이크로캐리어로부터 세포를 제거하는 능력을 제공한다.Saito index (Cytodex) ® 3 microcarrier beads (C3) (Sigma-Aldrich Company, El elssi, US St. Louis, Missouri material, Cat. No. C3275) two of the 400
액침 후, 비드를 오토클레이빙하고, 멸균 DPBS로 헹구고, 10 μM Y-27632로 보충된 마우스 배아 섬유아세포 컨디셔닝된 배지(MEF-CM) 중에서 재현탁시켰다. 이어서, 100 mg 비드/플라스크의 밀도로 비드를 125 ml 코닝® 유리 스피너 플라스크(코닝 인코포레이티드, 미국 뉴욕주 코닝 소재)에 옮겼다. 비드 및 Y-27632를 갖는 MEF-CM이 담긴 스피너를, 37℃의 가습된 5% CO2 인큐베이터 내에서 적어도 60분 동안 평형화시켰다.After immersion, the beads were autoclaved, rinsed with sterile DPBS and resuspended in mouse embryonic fibroblast conditioned medium (MEF-CM) supplemented with 10 [mu] M Y-27632. The beads were then transferred to a 125 ml Corning® glass spinner flask (Corning Incorporated, Corning, NY, USA) at a density of 100 mg beads / flask. Beads and MEF-CM with Y-27632 were equilibrated in a humidified 5% CO 2 incubator at 37 ° C for at least 60 minutes.
44회째 계대배양의 인간 배아줄기세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재)의 세포를 TrypLE™(라이프 테크놀로지즈 코포레이션, 미국 뉴욕주 그랜드 아일랜드 소재)를 사용하여 평면 부착성 배양물로부터 리프팅시켰다(37℃에서 8분 인큐베이션하여 단일 세포 현탁액을 형성함). 이어서, Y-27632를 갖는 MEF-CM 중에서 세포를 세척 및 현탁시키고, 1100만개의 hES 세포가 정치(정적) 인큐베이션 기간 내에 6시간 동안 비드에 부착되게 하였다. 이어서, Y-27632를 갖는 MEF-CM을 스피너 플라스크에 첨가하여 75 mL의 최종 배지 부피를 만들고, 세포 및 비드를 유리 스피너 플라스크 내에서 50 rpm의 임펠러 속도로 교반하였다. 이러한 방식으로 5일 동안 일일 MEF-CM의 50 mL 배지 교체를 행하면서 세포를 성장시켰다. 배양물 중에 있은 지 5일 후에, 플라스크에는 53×106개의 세포(±12×106 SD)가 들어 있었다. 대조군으로서, 100만개의 H1 hES 세포를 또한 매트리겔™의 1:30 희석물로 코팅된 6웰 조직 배양 폴리스티렌 디쉬에 시딩하고 일일 MEF-CM의 배지 교체를 유지하였다.Cells of human embryonic stem cell line H1 (WA01 cells, Wiscel, Madison, Wis., USA) for the 44th passage were lifted from flat adherent cultures using TrypLE (Life Technologies Corporation, Grand Island, NY, USA) (Incubation at 37 占 for 8 minutes to form a single cell suspension). The cells were then washed and suspended in MEF-CM with Y-27632 and 11 million hES cells were allowed to attach to the beads for 6 hours in a stationary (static) incubation period. The MEF-CM with Y-27632 was then added to the spinner flask to make a final volume of 75 mL, and the cells and beads were stirred in a glass spinner flask at an impeller speed of 50 rpm. Cells were grown in this manner for 5 days with 50 mL of medium replacement of MEF-CM per day. Five days after being in the culture, the flask contained 53 x 106 cells (+/- 12
이어서, 만능성 배양물 중에 있은 지 5일 후에, 이들 세포를 정상 췌장 발생 모르포겐을 반복하도록 의도된 소분자 및 성장 인자 중 하나 또는 둘 모두를 함유하는 상이한 배지의 단계별 진행을 통해 동적 교반 현탁 배양 시스템 내에서 췌장 전구체로 분화시켰다. 2가지 배지 제형을 정상 췌장 발생을 반복하기 위한 방법으로서 시험하였는데; 하나는 액티빈 A 및 Wnt3A를 사용하여 DE를 형성하였고, 다른 하나는 MCX 화합물을 GDF8과 함께 사용하여 DE를 형성하였다(각각 표 6a 및 표 6b). 배지를 매일 교체하고, 샘플을 RT-PCR 및 유세포측정법에 의해 특징규명하여 세포 특성을 결정하였다. 마이크로캐리어 상의 세포의 위상차 영상을 촬영하였으며, 세포의 분화가 개시되기 전의 만능성 배양물로서의 세포 형태의 시간 경과가 도 6a에 나타나 있다. 배양물 분화를 나타내는 시간 경과가 도 6b에 나타나 있다. 또한, 실험 전체에 걸쳐 다양한 시점에서 세포 카운트를 얻었으며, 결과는 평면 배양물 또는 현탁된 마이크로캐리어 배양물 중에서의 배지 제형에 대한 표면적(도 6c에서 세포수/㎠) 또는 배지 부피(도 6d에서 세포수/mL)의 함수로서 나타나 있다.Then, 5 days after being in universal culture, these cells were cultured in a dynamic stirred suspension culture with stepwise progression of different media containing either or both of the small molecules and growth factors intended to repeat normal pancreas-induced morphogen And differentiated into pancreatic precursors within the system. Two media formulations were tested as a method for repeating normal pancreas development; One using Actin A and Wnt3A to form DE, and the other using MCX compound with GDF8 to form DE (Table 6a and Table 6b, respectively). The medium was changed daily and the samples were characterized by RT-PCR and flow cytometry to determine cell characteristics. Phase contrast images of cells on the microcarriers were taken and the time course of the cell morphology as a pluripotent culture before the initiation of cell differentiation is shown in Figure 6a. The time lapse representing culture differentiation is shown in Figure 6b. In addition, cell counts were obtained at various time points throughout the experiment and the results are shown in Figure 6C as the surface area (number of cells / cm2 in Figure 6C) or medium volume (in Figure 6d) for the media formulation in the flat culture or suspended microcarrier culture Cell number / mL).
유세포측정법 및 RT-PCR 둘 모두에 의해 이 과정 전체에 걸쳐 다양한 시점에서 세포를 특징규명하였다. 제1 분화 단계인 완성 내배엽의 형성에 대한 유세포측정법의 결과는 도 6e에서 CXCR4(Y-축) 및 CD9(X-축)의 세포 발현의 점 도표로 나타나 있으며, 그 결과는 또한 도 6f에서 각각의 마커의 총 발현으로서 표현되어 있다. 결과는, 모든 조건에서 실질적으로 대부분의 세포가 완성 내배엽을 형성함을 나타내는데, 이때 완성 내배엽의 형성은 CXCR4 발현의 획득 및 만능성 표면 마커인 CD9의 손실에 의해 규정된 바와 같다. 더욱이, 완성 내배엽의 더 효율적인 형성은 MCX / GDF8 마이크로캐리어 > MCX / GDF8 평면 > WNT3A / AA 마이크로캐리어 > WNT3A / AA 평면의 처리의 순으로 순위가 나타난다. MCX / GDF8로 처리된 세포는 CERBERUS(Cer 1), GOOSECOID, 및 FGF17의 더 낮은 발현을 나타내는 바와 같이, 세포에 대한 배지 특이적 영향이 존재하는 것으로 보인다(도 6g). 그러나, 모든 처리 조건은 완성 내배엽 유전자, 즉 CD99, CXCR4, FOXA2, KIT, 및 SOX17의 유사한 발현 수준을 나타낸다(도 6g 및 표 6c). 이들 과정은 췌장 세포 전사 인자인 PDX1 및 NKX6.1의 동시발현을 특징으로 하는 췌장 전구세포 집단을 생성한다. 이들 세포가 이식되는 경우, 이들은 스트렙토조토신 유도 당뇨병 모델에서 고 혈당을 교정할 수 있는 기능적 글루코스 자극 인슐린 분비 조직으로 추가로 성숙된다.Cells were characterized at various time points throughout this process by both flow cytometry and RT-PCR. The results of flow cytometry on the formation of complete endoderm, the first differentiation stage, are shown in FIG. 6E as a dotted plot of cell expression of CXCR4 (Y-axis) and CD9 (X-axis) Lt; RTI ID = 0.0 > of < / RTI > The results indicate that, in all conditions, substantially all of the cells form complete endoderm, with the formation of complete endoderm as defined by the acquisition of CXCR4 expression and the loss of CD9, a universal surface marker. Moreover, the more efficient formation of complete endoderm is ranked in order of MCX / GDF8 microcarrier> MCX / GDF8 plane> WNT3A / AA microcarrier> WNT3A / AA plane processing. Cells treated with MCX / GDF8 appear to have a culture-specific effect on cells, as shown by lower expression of CERBERUS (Cer 1), GOOSECOID, and FGF17 (FIG. 6g). However, all treatment conditions represent similar expression levels of the completed endoderm genes, CD99, CXCR4, FOXA2, KIT, and SOX17 (FIG. 6g and Table 6c). These processes produce a population of pancreatic precursor cells characterized by coexpression of the pancreatic cell transcription factors PDX1 and NKX6.1. When these cells are transplanted, they are further matured into a functional glucose-stimulated insulin-secreting tissue capable of correcting hyperglycemia in a streptozotocin-induced diabetic model.
하기 표 6a에서 사용된 바와 같이, B27은 깁코(Gibco)® B-27® 보충물(라이프 테크놀로지즈 코포레이션, 미국 캘리포니아주 칼스배드 소재)이다.As used in Table 6a below, B27 is a Gibco B-27 supplement (Life Technologies Corporation, Carlsbad, CA).
이 실시예에 사용된 바와 같이, MCX 화합물은14-프로프-2-엔-1-일-3,5,7,14,17,23,27-헵타아자테트라사이클로[19.3.1.1~2,6-~.1~8,12.~]헵타코사-1(25),2(27),3,5,8(26),9,11,21,23-노나엔-16-온이며, 이는 하기 화학식(화학식 1)을 갖는다:As used in this example, the MCX compound is 14-prop-2-en-1-yl-3,5,7,14,17,23,27-heptaaza tetracyclo [19.3.1.1-2, (25), 2 (27), 3,5,8 (26), 9,11,21,23-nonanen-16-one , Which has the following formula:
다른 환형 아닐린-피리디노트라이아진이 또한 전술된 MCX 화합물 대신 사용될 수 있다. 그러한 화합물은 14-메틸-3,5,7,14,18,24,28-헵타아자테트라사이클로[20.3.1.1~2,6~.-1~8,12~]옥타코사-1(26),2(28),3,5,8(27),9,11,22,24-노나엔-17-온 및 5-클로로-1,8,10,12,16,22,26,32-옥타아자펜타사이클로[24.2.2.1~3,7~-1~9,13~.1~14,18~]트라이트라이아콘타-3(33),4,6,9(32),10-,12,14(31),15,17-노나엔-23-온을 포함하지만 이로 한정되지 않는다. 이들 화합물은 하기에 나타나 있다(화학식 2 및 화학식 3):Other cyclic aniline-pyridinotriazines may also be used in place of the MCX compounds described above. Such compounds include 14-methyl-3,5,7,14,18,24,28-heptaaza tetracyclo [20.3.1.1-2,6-. 1-8,12-] octacos-1 (26) , 2 (28), 3,5,8 (27), 9,11,22,24-nonanen-17-one and 5-chloro-1,8,10,12,16,22,26,32- Octaazapentacyclo [24.2.2.1 to 3,7 to -1 to 9,13 to 1-14, 18 to] tritriaconta-3 (33), 4,6,9 (32), 10-, 12,14 (31), 15,17-nonane-23-one. These compounds are shown below (
예시적인 적합한 화합물은 미국 특허 출원 공개 제2010/0015711호에 개시되어 있으며, 이의 개시내용은 MCX 화합물, 관련 환형 아닐린-피리디노트라이아진, 및 이들의 합성에 관한 것인 것과 같이 전체적으로 포함된다.Exemplary suitable compounds are disclosed in U.S. Patent Application Publication No. 2010/0015711, the disclosure of which is incorporated in its entirety as it relates to MCX compounds, related cyclic aniline-pyridinotriazines, and their synthesis.
이 실시예에서 4기에 사용된 Cyp26 억제제는 N-{4-[2-에틸-1-(1H-1,2,4-트라이아졸-1-일)부틸]페닐}-1,3-벤조티아졸-2-아민이었는데, 이는 CAS 번호가 201410-53-9이고 하기의 구조를 갖는다:The Cyp26 inhibitor used in this example in
이 Cyp26 억제제는 또한 "Cypi"로도 알려져 있다. 이 Cyp26 억제제의 구조 및 합성은 미국 특허 제7,378,433호에 개시되어 있으며, 이의 개시내용은 Cyp26 억제제 및 그의 합성에 관한 것인 것과 같이 전체적으로 포함된다.This Cyp26 inhibitor is also known as "Cypi ". The structure and synthesis of this Cyp26 inhibitor is disclosed in U.S. Patent No. 7,378,433, the disclosure of which is incorporated in its entirety as it relates to Cyp26 inhibitors and their synthesis.
[표 6a][Table 6a]
[표 6b][Table 6b]
[표 6c][Table 6c]
실시예 7Example 7
H1(WA01) hES 세포주의 서브-클론 - WB0106을 이 실시예에 사용하였다. WB0106은 위셀 리서치 인스티튜트(미국 위스콘신주 매디슨 소재)에서 DDL-13으로 명명된 H1 주 시드 물질로부터 유래되었다. H1 주의WB0106 서브-클론을 23회째 계대배양에서 해동된 DDL-13 바이알로부터 매트리겔™ 기질 상의 mTeSR®1 배지 내로 유도하고, EDTA를 사용하여 후속적으로 계대배양시켰다. WB0106을 28회째 계대배양에서 동결시키고, 정상 핵형(FISH 및 G-밴드), 췌장 선조세포로 분화하는 능력, 및 클러스터를 형성하여 현탁 배양물 중에서 증폭하는 컴피턴시에 기초하여 이들 연구를 위해 선택하였다.Sub-clone-WB0106 of the H1 (WA01) hES cell line was used in this example. WB0106 was derived from the Hl primary seed material designated DDL-13 in the Wixel Research Institute (Madison, WI). The H1 Ca2 WB0106 sub-clones were derived from the DDL-13 vials thawed in the 23rd pass subculture into the
이어서, WB0106 WCB 바이알을 T225 플라스크(코닝 인코포레이티드, 미국 뉴욕주 코닝 소재) 내에서 매트리겔™의 기질 상의 배지 내로 해동시키고, 제1 계대배양에서 세포를 다수의 T225 플라스크 내로 증폭시켰다. 제2 계대배양에서, 다수의 T225 플라스크로부터의 세포를 합하여 단일의 2-층 셀스택™(CS2)에 시딩하는 데 사용하였다. 일단 CS2가 70% 융합(confluent)을 나타내면, 인접한 펌프 튜빙을 갖는 C-플렉스® 튜빙 조립 캡을 배지 포트에 부착시켜 시스템을 폐쇄하였다. 시스템을 C-플렉스® 튜빙으로 폐쇄시킨 후에, 백(bag) 또는 병을 테루모 용접기를 통해 용접하고, 액체 부피(배지, PBS-/-, 아큐타제®, 또는 현탁된 세포)를 연동 펌프를 사용하여 옮겼다.The WB0106 WCB vials were then thawed into medium on a Matrigel ™ substrate in a T225 flask (Corning Incorporated, Corning, NY, USA) and the cells were amplified in a number of T225 flasks in the first subculture. In the second subculture, cells from multiple T225 flasks were combined and seeded into a single two-layered cell stack (CS2). Once CS2 exhibited 70% confluence, the system was closed by attaching a C-Plex® tubing assembly cap with adjacent pump tubing to the delivery port. After the system is closed with C-Flex® tubing, the bag or bottle is welded through a Terumo welder and the liquid volume (medium, PBS - / - , Accutase ® , or suspended cells) .
CS2로부터 세포를 리프팅하기 위해, 세포를 PBS-/-로 1회 세척하고, 이어서 PBS-/-로 희석된 아큐타제®의 1/2 농도 용액으로 처리하고 4 내지 5분 동안 인큐베이션하였다. 이어서, 아큐타제®를 제거하고, 효소 용액의 적용 후 3분째에, CS2를 탭핑하여 세포 리프팅을 조장하였다. 0.5% BSA로 보충되고 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 배지 한 병을 CS2 내로 펌핑하여 잔류하는 아큐타제®를 헹구어 불활성화시키고, 이어서 헹굼액을 수집하였다. 제2 헹굼 부피를 첨가하고, 수집하고, 제1 헹굼액과 혼주시켰다. 이어서, 200 mL 중 2.0 내지 2.5 × 108개의 세포를 1-층 셀스택® 내로 옮기고, 가습된 5% CO2 인큐베이터 내에서 37℃에서 2시간 동안 인큐베이션하였다. 2개의 셀스택® 배지 포트들 사이에 펌프 튜빙이 부착된 C-플렉스® 튜빙의 폐쇄 루프를 사용하여, 세포 현탁액을 연동 펌프에 의해 5분 동안 75 rpm으로 분쇄하여 응집체를 균질화하였다. 폐쇄 루프 튜빙을 멸균 0.2 마이크로미터 필터로 교체하여 가스 교환되도록 하고, 가습된 5% CO2 인큐베이터 내에서 37℃에서 하룻밤 셀스택®을 인큐베이션하였다. 하룻밤 인큐베이션(12 내지 22시간, 18시간이 최적임)한 후, 셀스택® 내의 세포는 만능 세포의 둥근 구형 응집체(클러스터)를 형성하였다.In order to lift the cells from the CS2, the cells PBS - / - washed once with, and then PBS-incubated for operation at the one-half the concentration of the solution was diluted with Accu hydratase ® and 4 to 5 minutes - /. Then, by removing the Accu hydratase ® and, after the application of the
현탁된 세포 클러스터를 함유하는 0.5% BSA로 보충된 배지를, 셀스택®으로부터, 0.5% BSA로 보충된 0.4 리터의 새로운 배지와 함께, 1 리터 일회용 스피너 플라스크(코닝, 미국 뉴욕주 코닝 소재)에 옮기고, 55 내지 65 rpm으로 유지하였다. 옮긴 후 24시간째에, 1 리터 일회용 스피너 플라스크를 가습된 5% CO2 인큐베이터로부터 꺼내고, 클러스터가 5 내지 10분 동안 정착되게 하였다. 이어서, 용기에 200 mL가 남을 때까지 배지를 흡인한 다음, 400 mL의 추가의 새로운 배양 배지를 스피너 플라스크에 첨가하였다. 이 과정을 2일째의 말기(옮긴 후 48시간째)에 반복하였다.The medium supplemented with 0.5% BSA containing the suspended cell clusters was transferred from Cell Stack ® to a 1 liter disposable spinner flask (Corning, Corning, NY, USA) with 0.4 L of fresh medium supplemented with 0.5% BSA Transferred, and maintained at 55-65 rpm. At 24 hours after transfer, a 1 liter disposable spinner flask was removed from the humidified 5% CO 2 incubator and the clusters were allowed to settle for 5-10 minutes. The medium was then aspirated until 200 mL remained in the vessel, and 400 mL of additional fresh culture medium was added to the spinner flask. This process was repeated at the end of the second day (48 hours after transfer).
3일째의 말기(CS2로부터 스피너 플라스크로 옮긴 후 72시간째)에, 세포 클러스터를 계대배양 및 추가 증폭을 위해 아큐타제® 처리에 의해 해리시켰다. 계대배양 과정은 가습된 5% CO2인큐베이터로부터 1 리터 일회용 스피너 플라스크를 꺼냄으로써 개시하였다. 플라스크를 생물안전 캐비닛(biosafety cabinet) 내부의 스피너 플레이트 상에 놓아서 세포의 균질한 현탁액을 유지하였다. 세포 현탁액을 100 mL 피펫에 의해 스피너 플라스크로부터 꺼내어서 4개의 175 mL 원추형 폴리카르보네이트 튜브(서모피셔-날진(ThermoFisher-Nalgene); 미국 뉴욕 버팔로 소재) 사이에 고르게 분포시키고 5분 동안 80 내지 200 rcf로 원심분리하였다. 세포 펠렛을 교란시키지 않으면서 폐배지를 흡인하였다. 이어서, 칼슘 또는 마그네슘(DPBS-/-)이 없는 25 mL의 DPBS를 각각의 튜브에 첨가하고, 세포를 1개의 원추형 튜브 내로 합치고 5분 동안 80 내지 200 rcf로 원심분리하였다. DPBS-/-를 원추형 튜브로부터 흡인하고, 30 mL의 50% 아큐타제®/50% DPBS-/- 용액을 튜브에 첨가하였다. 세포 클러스터를 1 내지 3회 상하로 피펫팅하고, 이어서 4분 동안 간헐적으로 와동시킨 다음, 5분 동안 80 내지 200 rcf로 원심분리하였다. 이어서, 세포 펠렛을 교란시키지 않으면서 아큐타제®를 가능한 한 완전히 흡인하고, 세포 현탁액이 균일한 유백색으로 나타날 때까지 원추형 튜브를 3 내지 5분 동안 연속적으로 그리고 온화하게 탭핑하였다. 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 0.5% BSA로 보충된 10 mL의 배지를 세포 현탁액에 첨가하고 2 내지 4회 분쇄하여, 잔류하는 아큐타제®를 불활성화시켰다. 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 0.5% BSA로 보충된 90 mL의 배지를 세포에 첨가하고 현탁액을 40 마이크로미터 세포 여과기(비디 팔콘; 미국 뉴저지주 프랭클린 레이크스 소재)에 통과시켰다.End of the third day (after moving from the spinner flask by CS2 second to 72 hours), the cell clusters were dissociated by Accu hydratase ® process for the subculture and further amplified. The subculture was initiated by removing a 1 liter disposable spinner flask from a humidified 5% CO 2 incubator. The flask was placed on a spinner plate inside a biosafety cabinet to maintain a homogeneous suspension of cells. The cell suspension was taken out of the spinner flask by a 100 mL pipette and distributed evenly between four 175 mL conical polycarbonate tubes (ThermoFisher-Nalgene; Buffalo, NY, USA) and maintained at 80 to 200 and centrifuged with rcf. The lung pellet was aspirated without disturbing the cell pellet. Then 25 mL of DPBS without calcium or magnesium (DPBS - / - ) was added to each tube and the cells were combined into one conical tube and centrifuged for 5 minutes at 80-200 rcf.
100 mL 부피의 여과된 세포 현탁액 중 세포 밀도를 NC-100 뉴클레오카운터®(케모메텍 에이/에스, 덴마크 알레로드 소재)로 측정하고 추가의 배지를 첨가하여 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 0.5% BSA로 보충된 배지 중에서 1 × 106개 세포/mL의 최종 세포 농도를 수득하였다. 이어서, 225 mL(2억2500만개의 세포)의 세포 현탁액을 1 리터 일회용 스피너 플라스크에 옮기고 가습된 5% CO2 인큐베이터 내에서 교반 없이 1시간 동안 인큐베이션하였다. 이어서, 플라스크를 인큐베이터로부터 꺼내어서 생물안전 캐비닛 내의 스피너 플레이트 상에서 1 내지 3분 동안 100 rpm으로 교반하였다. 세포 현탁액을 혼합하고 있는 동안, 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 0.5% BSA로 보충된 추가 225 mL의 배지를 세포 현탁액에 첨가하였다. 이어서, 스피너 플라스크를 가습된 5% CO2 인큐베이터에 30분 동안 되돌려 놓았다. 이어서, 플라스크를 인큐베이터로부터 꺼내어서 생물안전 캐비닛 내의 스피너 플레이트 상에서 1 내지 3분 동안 100 rpm으로 교반하였다. 세포 현탁액을 혼합하고 있는 동안, 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 0.5% BSA로 보충된 추가 150 mL의 배지를 세포 현탁액에 첨가하여 600 mL의 최종 부피를 만들고 플라스크를 인큐베이터 내에서 교반된 현탁으로 되돌렸다. 아큐타제® 해리 후 24시간째 및 48시간째 둘 모두에서, 5 내지 10분 동안 세포 클러스터가 플라스크의 바닥에 정착되게 하였다. 어떠한 클러스터 손실도 최소화하는 것을 확보하면서, 400 mL의 폐배지를 흡인에 의해 플라스크로부터 제거하고 새로운 배지로 교체하였다. 이 과정을 사용하여, H1 세포를 기질 상의 부착성 배양물로부터 세포 클러스터로서 현탁 배양물로 전환시켰다.The cell density of the filtered cell suspension in 100 mL volume of NC-100 nucleoside Counter ® (kemo metek A / S, Denmark Valley Road material) of 10 micromolar was measured and the addition of additional medium to the Rho kinase inhibitor Y-27632 1 to give a final cell concentration of gae × 10 6 cells / mL in a medium supplemented with 0.5% BSA containing. Then, 225 mL (225 million cells) of cell suspension was transferred to a 1 liter disposable spinner flask and incubated in a humidified 5% CO 2 incubator for 1 hour without agitation. The flask was then removed from the incubator and stirred for 1 to 3 minutes at 100 rpm on a spinner plate in a biological safety cabinet. While mixing the cell suspension, an additional 225 mL of medium supplemented with 0.5% BSA containing 10 micromolar Rho kinase inhibitor Y-27632 was added to the cell suspension. The spinner flask was then returned to a humidified 5% CO 2 incubator for 30 minutes. The flask was then removed from the incubator and stirred for 1 to 3 minutes at 100 rpm on a spinner plate in a biological safety cabinet. While mixing the cell suspension, an additional 150 mL of medium supplemented with 0.5% BSA containing 10 micromolar Rho kinase inhibitor Y-27632 was added to the cell suspension to make a final volume of 600 mL and the flask was placed in the incubator The suspension was returned to the stirred suspension. Accu hydratase ® dissociation after second 24 hours after and 48 hours in all, so the cell cluster is fixed on the bottom of the flask for 5 to 10 minutes. 400 mL of waste medium was removed from the flask by suction and replaced with fresh medium ensuring that any cluster losses were minimized. Using this procedure, H1 cells were converted from the adherent cultures on the substrate to suspension cultures as cell clusters.
초기 아큐타제® 처리 후 72시간째에, 세포 클러스터 해리 및 스피너 플라스크 시딩(계대배양)의 과정을 반복하여, 다회의 계대배양(시험된 범위: 1 내지 10회의 계대배양) 동안 현탁 상태로 세포를 유지하였다. 처음 24시간 후에 배지를 제거하지 않고, 200 mL의 새로운 배지를 첨가한 것을 제외하고는 상기 과정을 따랐다. 아큐타제® 해리 후 48시간째에, 5 내지 10분 동안 클러스터가 플라스크의 바닥에 정착되게 하고, 600 mL를 흡인하고, 400 mL의 새로운 배지를 플라스크에 첨가하였다.After the initial occupancy hydratase ® treatment in second 72 hours, to repeat the cell clusters dissociate and spinner flasks are seeded (passages), the conference passages: the cells in a suspended state during the (tested range from 1 to 10 times subculture) Respectively. Following the first 24 hours, the procedure was followed except that the medium was not removed and 200 mL of fresh medium was added. Accu hydratase ® at 48 hours after the dissociation, and the cluster is to be settled in the bottom of the flask for 5 to 10 minutes, and the
이어서, 현탁-계대배양 및 배양된 이들 세포는 나중의 사용을 위해 동결보존 및 저장될 수 있었다. 동결보존을 위한 현탁 증폭된 세포를 제조하기 위하여, 세포를 40 마이크로미터 세포 여과기에 통과시키지 않은 것을 제외하고는, 현탁 계대배양에 대하여 전술된 바와 같이 세포 클러스터를 아큐타제®로 해리시켰다. 각각 1 리터 일회용 플라스크로부터 생성된 100 mL 세포 현탁액에 대한 세포 카운트를 측정하였다. 이어서, 세포 현탁액을 합하고 5분 동안 80 내지 200 rcf로 원심분리하였다. 이어서, 세포 펠렛을 교란시키지 않으면서 가능한 한 완전히 원심분리 튜브로부터 배지를 제거하였다. 이어서, 차가운(4℃ 미만) 크라이오스토(CryoStor)®10(스템 셀 테크놀로지즈, 인크., 캐나다 브리티시컬럼비아주 밴쿠버 소재)을 적가하여 1억5000만개의 세포/mL의 최종 농도를 달성하고 세포 용액을 1.8 mL 코닝® 동결 바이알(코닝 인코포레이티드, 미국 뉴욕주 코닝 소재) 또는 15 mL 밀테니(Miltenyi) 동결 백(밀테니 바이오텍 인크.(Miltenyi Biotec Inc.), 미국 캘리포니아주 아우번 소재)에 옮기는 동안 빙욕 중에서 유지하였다.These suspension-passaged and cultured cells could then be cryopreserved and stored for later use. In order to prepare the suspension for cryopreservation amplified cells were dissociated the cell clusters as described above with respect to the cell and is suspended passages except that not pass a 40 micron cell strainer into Accu hydratase ®. Cell counts were determined for each 100 mL cell suspension generated from each 1 liter disposable flask. The cell suspension was then combined and centrifuged at 80 to 200 rcf for 5 minutes. The media was then removed from the centrifuge tube as completely as possible without disturbing the cell pellet. Subsequently, a final concentration of 150 million cells / mL was achieved by adding cold (less than 4 ° C) CryoStor® 10 (Stem Cell Technologies, Inc., Vancouver, British Columbia, Canada) The solution was added to a 1.8 mL Corning® freezing vial (Corning Incorporated, Corning, NY, USA) or a 15 mL Miltenyi freeze bag (Miltenyi Biotec Inc., ) In an ice bath.
이어서, 현탁 증폭된 세포를 바이알 내에서 다음과 같이 프로그램화 동결기(controlled rate freezer) 내에서 고밀도로 동결시켰다. 챔버를 4℃로 예비-냉각시키고 샘플 바이알 온도가 6℃에 도달할 때까지 온도를 유지하였다. 이어서, 샘플이 -7℃에 도달할 때까지 챔버 온도를 2℃/min으로 강하시켰다. 일단 샘플 바이알이 -7℃에 도달하면, 챔버가 -45℃에 도달할 때까지 챔버를 20℃/min으로 냉각시켰다. 이어서, 챔버 온도가 -25℃에 도달할 때까지 챔버 온도를 10℃/min으로 짧은 시간에 상승되게 한 다음, 샘플 바이알이 -45℃에 도달할 때까지 챔버를 0.8℃/min으로 추가로 냉각시켰다. 이어서, 챔버가 -160℃에 도달할 때까지 챔버 온도를 35℃/min으로 냉각시켰다. 이어서, 챔버 온도를 -160℃에서 적어도 10분 동안 유지하고, 이후에 바이알을 가스상 액체 질소 저장소에 옮겼다.The suspension-amplified cells were then frozen at high density in a vial in a controlled rate freezer as follows. The chamber was pre-cooled to 4 ° C and the temperature was maintained until the sample vial temperature reached 6 ° C. The chamber temperature was then lowered to 2 [deg.] C / min until the sample reached -7 [deg.] C. Once the sample vial reached -7 占 폚, the chamber was cooled to 20 占 폚 / min until the chamber reached -45 占 폚. The chamber temperature was then allowed to rise briefly at 10 [deg.] C / min until the chamber temperature reached -25 [deg.] C and the chamber was further cooled at 0.8 [deg.] C / min until the sample vial reached -45 [ . The chamber temperature was then cooled to 35 [deg.] C / min until the chamber reached -160 [deg.] C. The chamber temperature was then maintained at -160 DEG C for at least 10 minutes, after which time the vials were transferred to a gaseous liquid nitrogen reservoir.
교반 탱크 생물반응기에 접종하기 위하여, 고밀도 동결보존 세포를 액체 질소 저장소로부터 꺼내고, 해동시켜, 폐쇄된 3 리터 유리 생물반응기(다스깁; 독일 율리히 소재)에 시딩하는 데 사용하였다. 4개 또는 5개의 바이알을 가스상 액체 질소 저장소로부터 꺼내어서, 105초 동안 37℃ 수욕 중에 곧바로 넣어 두었다. 이어서, 해동된 바이알 성분을 2 ml 유리 피펫을 통해 50 ml 원추형 튜브에 옮겼다. 이어서, 0.5% BSA를 함유하고 10 마이크로몰의 Rho 키나제 억제제 Y-27632로 보충된 9 ml의 배지(IH3 또는 이센셜8™ 배지("E8™"))를 튜브에 적가하였다. 이어서, 세포를 80 내지 200 rcf로 5분 동안 원심분리하였다. 튜브로부터의 상층액을 흡인하고, 0.5% BSA를 함유하고 10 마이크로몰의 Rho 키나제 억제제 Y-27632로 보충된 10 ml의 새로운 배지(IH3 또는 E8™)를 첨가하고, 세포를 함유하는 부피를 배지 전달 병(Cap2V8®, 사니슈어(Sanisure), 미국 캘리포니아주 무어파크 소재) 내로 피펫팅하였다. 이어서, 병의 내용물을 멸균 C-플렉스 튜빙 용접부를 통해 연동 펌프에 의해 생물반응기 내로 직접 펌핑하였다. 만능 줄기세포 접종을 위한 준비 시에, 생물반응기에 1.5 L의 배지(0.5% BSA로 보충되고 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 IH3 또는 E8™)를 준비하고, 37℃로 예비-가온하고, 70 rpm으로 교반하고, CO2에 의해 6.8 내지7.1 pH로 조절하였는데, 이때 30%의 용존 산소 설정점(CO2, 공기, O2, 및 N2가 조절됨)을 가졌다. 접종 직후에, 생물반응기를 세포 카운트를 위해 샘플링하고, 배지 부피를 필요에 따라 조절하여 0.225 × 106개 세포/mL의 최종 세포 농도를 수득하였다.For inoculation in a stirred tank bioreactor, the high density cryopreserved cells were removed from the liquid nitrogen reservoir and thawed and used to seed in a closed 3 liter glass bioreactor (a dozen cigarettes, Yuli, Germany). Four or five vials were taken out of the gaseous liquid nitrogen reservoir and immediately placed in a 37 ° C water bath for 105 seconds. The thawed vial was then transferred to a 50 ml conical tube through a 2 ml glass pipette. Subsequently, 9 ml of medium (IH3 or Sensitive 8 ™ medium ("E8 ™") containing 0.5% BSA and supplemented with 10 micromolar Rho kinase inhibitor Y-27632) was added dropwise to the tube. The cells were then centrifuged at 80 to 200 rcf for 5 minutes. The supernatant from the tube was aspirated and 10 ml of fresh medium (IH3 or E8 (TM)) containing 0.5% BSA and supplemented with 10 micromoles of Rho kinase inhibitor Y-27632 was added and the volume containing the cells And pipetted into a delivery bottle (Cap2V8, Sanisure, Moore Park, CA). The contents of the bottle were then pumped directly into the bioreactor by a peristaltic pump through a sterile C-flex tubing weld. In preparation for universal stem cell inoculation, the bioreactor was supplemented with 1.5 L of medium (IH3 or E8 (TM) supplemented with 0.5% BSA and containing 10 micromolar Rho kinase inhibitor Y-27632) - warmed, stirred at 70 rpm and adjusted to pH 6.8 to 7.1 with CO 2 , with a 30% dissolved oxygen setpoint (CO 2 , air, O 2 , and N 2 controlled). Immediately after inoculation, the bioreactor was sampled for cell counting and the medium volume was adjusted as necessary to yield a final cell concentration of 0.225 x 10 6 cells / mL.
교반 탱크 생물반응기 내로 접종된 세포는 연속 교반 탱크 내에서 세포 클러스터를 형성하였으며, 총 3일 동안 반응기 내의 만능성 배지(0.5% BSA로 보충된 IH3 또는 E8™) 중에서 유지하였다. 배지를 매일 교체하였는데, 1 내지 1.3 리터의 폐배지를 제거하고 1.5 리터의 새로운 배지를 첨가하는 것으로서, 접종 후 24시간째에 부분 배지 교체를 행하였다. 접종 후 48시간째에, 1.5 내지 1.8 리터의 폐배지를 제거하고 1.5 리터의 새로운 배지를 첨가하였다. 접종 후 72시간째에, 폐배지를 90% 초과하여 제거하고 분화 배지(표 7)를 첨가함으로써 만능 세포 분화를 개시하였다.Cells inoculated into a stirred tank bioreactor formed cell clusters in a continuous stirred tank and maintained in universal media (IH3 or E8 (TM) supplemented with 0.5% BSA) in the reactor for a total of 3 days. The medium was changed every day. One to 1.3 liters of the waste medium was removed, and 1.5 liters of the new medium was added, and the partial medium was replaced at 24 hours after the inoculation. At 48 hours after inoculation, 1.5 to 1.8 liters of waste medium was removed and 1.5 liters of fresh medium was added. Seventy-two hours after inoculation, the lung medium was removed by more than 90% and pluripotent cell differentiation was initiated by adding differentiation medium (Table 7).
일단 단계화된 분화 과정이 개시되면, 12일 이상 동안 온도(37℃), pH(분화의 경우 7.4), 및 용존 산소(1기의 경우 10% DO 설정점 및 모든 다른 시기에서는 30% DO 설정점, CO2, O2, N2, 및 공기가 조절됨)에 대해 조절된 폐쇄된 멸균 현탁 생물반응기 내에서 세포를 유지하였다. 분화 과정 전체에 걸쳐, 각각의 배지 교체 시, 딥-튜브를 통한 배지 제거 전에 5 내지 20분 임펠러를 정지시켜 클러스터가 정착되게 하였다. 테루모™ 튜브 용접기를 사용하여 C-플렉스® 튜빙에 연결된 딥 튜브를 통해 연동 펌프에 의해 닫힌 병 또는 백으로/그로부터 생물반응기 내의 배지를 제거하거나 첨가하여 폐쇄된 시스템을 유지하였다. 일단 충분한 배지를 용기에 첨가하여 임펠러가 완전히 잠기면, 임펠러 및 가열기에 재동력공급하였다.Once the staged differentiation process is initiated, the temperature (37 ° C), pH (7.4 for differentiation) and dissolved oxygen (10% DO setpoint for
생물반응기 과정을 모니터링하기 위하여, 세포 클러스터를 함유하는 배지의 샘플을 매일 수거하여 세포수 및 생존력(뉴클레오카운터®)을 측정하였으며, 이는 도 7에 나타낸 바와 같다. 0.225 × 106개 생존 세포/mL의 접종물이 증폭되어 4기 3일째에 평균 0.92 × 106개 생존 세포/mL를 생성한 바와 같이, 세포의 일반적인 증폭이 이 과정 동안 관찰되었다. 생물반응기 접종과 만능 세포 클러스터링 및 배양 동안 산성 설정점(pH 7.0 내지 6.8)으로 세포를 유지함으로써, 4기 3일째에서의 평균 세포 산출량은 평균 1.3 × 106개 세포/mL로 증가하였다(도 7).In order to monitor a bioreactor process, by daily collection of samples of the medium containing the cell clusters was measured with the cell number and viability (nucleoside Counter ®), which is as shown in Fig. Normal amplification of the cells was observed during this process, as the inoculum of 0.225 × 10 6 viable cells / mL was amplified to produce an average of 0.92 × 10 6 viable cells / mL on the
일일 카운트 외에, 생물반응기 배지 샘플을 노바 바이오프로파일® 플렉스(노바 바이오메디칼 코포레이션, 미국 매사추세츠주 월섬 소재)에 의해 분석하였다. 반응기 설정점마다, 0기에서의 배지의 pH는 대부분의 배양 배지에 대해 일반적인 7.4의 항상성 표준 pH에 비해 산성이고 반응기 배지 pH는 세포 대사의 결과로서 0기에 걸쳐 감소한 것으로 관찰되었다(도 8). 이들 결과는 6일째의 분화의 말기에 걸쳐 증가하는 락트산 농도 및 감소하는 글루코스 수준의 경향과 상관되었다(도 9 및 도 10). 이와 함께, 이들 데이터는, 반응기 내의 세포가 0기의 그리고 분화의 처음 2개의 단계(1 내지 6일째)에 걸쳐 가장 급속하게 성장하고 글루코스 소비적임을 나타내었다. 그러나, 3기로부터 그 이후로, 반응기 내의 세포 대사(감소된 락테이트 수준 및 증가된 글루코스 수준)는 감소되었는데, 이는 3기에서의 세포수에 있어서의 피크에 이어지는 4기의 과정에 걸친 세포 밀도에 있어서의 감소와 상관되었다.In addition to daily counts, bioreactor media samples were analyzed by Nova BioProfile ' s Flex (Nova Biomedical Corporation, Waltham, Mass., USA). At each reactor set point, the pH of the medium at 0 was found to be acidic for most culture media compared to the normal 7.4 standard pH, and the reactor medium pH was observed to decrease over 0 as a result of cell metabolism (FIG. 8). These results correlated with increasing lactic acid concentration and decreasing glucose levels at the end of the 6 day differentiation (Figs. 9 and 10). Together, these data showed that the cells in the reactor grew most rapidly and glucose consumption over the first two phases of
pH 및 대사에 있어서의 단계 특이적인 변화가 mRNA 발현 패턴에 있어서의 단계 변화와 매칭되는지를 결정하기 위하여, 만능성, 완성 내배엽(DE), 장관(GT), 또는 4기(S4)로 지정된 4개의 어플라이드 바이오시스템즈(Applied Biosystems)® 저밀도 어레이(Low Density Array)(라이프 테크놀로지즈 코포레이션, 미국 캘리포니아주 칼스배드 소재)를 사용하여 생물반응기 세포 샘플의 시험을 수행하였으며, 그 결과를 모든 실시 및 어레이에 걸쳐 발현을 표준화하기 위하여 대조군으로서의 조직학적으로 미분화된 H1(WB0106) hES 세포 샘플과 대비하였다.(DE), intestinal tract (GT), or stage 4 (S4) to determine whether the stage specific changes in pH and metabolism match the stage changes in the mRNA expression pattern. Tests of bioreactor cell samples were performed using Applied Biosystems ' Low Density Array (Life Technologies Corporation, Carlsbad, Calif., USA) and the results are reported in all runs and arrays (WB0106) hES cell sample as a control to normalize expression over time.
이들 어레이를 사용하여, 유전자 발현을 분화의 각각의 단계에 대해 측정하였다. 생물반응기 내로 해동된 시드 물질 세포는 0기 1일째 및 0기 3일째(생물반응기 접종 후 24시간째 및 72시간째: 도 11, 도 12, 도 13, 및 도 14)에서 미분화된 유전자 발현 패턴을 나타낸 것으로 또한 관찰되었다. 이들 결과는 CD9, SSEA4, TRA-1-60, 및 TRA-1-81의 고 발현 수준, 및 CXCR4/CD184의 부재를 보여준 유세포측정법의 결과와 잘 상관되었다(도 15 및 표 8). 그렇더라도, 유전자 발현에 대한 유세포측정법 및 qRT-PCR 검정은 만능성 유전자(CD9, MANOG, POU5F1, SOX2, TDGF, 및 ZFP42)에 대한 견고하고 안정한 발현 패턴을 나타내었는데, 이러한 발현 패턴은 GATA4, GSC, MIXL1, 및 T에 대한 유전자 발현에 있어서 약간이긴 하지만 가변적인 증가; 및 유도 분화 전 0기 과정 동안에 일부 샘플에서 CER1, FGF17, FGF4 및 GATA2 발현에 있어서 100x 이상의 증가가 또한 주목되는 안정한 만능성 상태와 일치하였다(도 16 및 도 17).Using these arrays, gene expression was measured for each step of differentiation. The seed material cells thawed into the bioreactor were analyzed for undifferentiated gene expression patterns in the 0th day and the 0th day (
0기의 완료 시(반응기 접종 후 72시간째), MCX 및 GDF8을 함유하는 분화 배지(표 7) 내로 세포를 이동하였다. 이 배지 교체 후 24시간째에, FOXA2 발현에 있어서의 약 700x 증가 및 CER1, EOMES, FGF17, FGF4, GATA4, GATA6, GSC, MIXL1, 및 T 발현에 있어서의 1000x 증가와 같이 유전자 발현 패턴에 있어서의 유의한 변경이 주목되었다(도 18 및 도 19). 이들 증가된 발현 수준은, 세포가 중배엽 운명을 통해 전이되고 있음을 나타내었다. CDX2 수준은 미분화된 세포와 대비하여 1기 1일째에 상승하였지만(대조군과 대비하여 발현에 있어서 470x 증가), 이는 발현에 있어서의 일시적인 증가였으며 CDX2 수준은 1기 1일째부터 1기 3일째까지 94% 하락하여 분화 유도 전에 관찰된 것과 비견되는 수준으로 되돌아갔음이 또한 주목되었다(도 14, 도 19, 및 도 21).Upon completion of 0 (72 hours after reactor inoculation), cells were transferred into differentiation medium containing MCX and GDF8 (Table 7). At 24 hours after the medium was replaced, the expression level of FOXA2 in FOXA2 expression and the expression level of CER1, EOMES, FGF17, FGF4, GATA4, GATA6, GSC, MIXL1, Significant changes have been noted (Figures 18 and 19). These increased expression levels indicate that the cells are metastasizing through mesodermal fate. CDX2 levels were elevated on day 1 (compared to control) by 470x, compared with undifferentiated cells, but this was a temporary increase in expression, and CDX2 levels ranged from
DE 분화 배지에 노출 후 72시간째에, CXCR4 수준이 피크이고 FOXA2 및 SOX17은 과거 대조군(historical control)에 비하여 1000x 초과하여 발현된 바와 같이, 세포는 완성 내배엽으로의 예정화(specification)와 일치하는 프로파일을 발현하였다. 완성 내배엽과 일치하여, 유전자 CER1, EOMES, FGF17, FGF4, GATA4, GATA6, GSC, MIXL1, 및 T는 1기 1일째에 관찰된 상승된 수준으로부터 하락하였음이 또한 주목되었다(도 20 및 도 21).At 72 hours after exposure to DE differentiation medium, the cells matched the specification to complete endoderm, as CXCR4 levels were peak and FOXA2 and SOX17 were expressed above 1000x relative to historical control Profile. It was also noted that the genes CER1, EOMES, FGF17, FGF4, GATA4, GATA6, GSC, MIXL1, and T decreased from the elevated levels observed on
qRT-PCR에 의해 관찰된 유전자 발현에 있어서의 변화는 유세포측정법에 의해 관찰된 결과와 상관되었다. 분화 개시 시에 CD9 발현/CXCR4 음성 만능 세포 집단(도 15)으로부터 1기 말기에 CXCR4 발현 세포(98.3%의 세포가 CXCR4 양성임, ±1.9 SD)의 균질 집단(도 22)으로의 거의 완전한 전이가 또한 관찰되었다.The changes in gene expression observed by qRT-PCR correlated with the results observed by flow cytometry. From the CD9 expression / CXCR4 negative pluripotent cell population (Fig. 15) at the onset of differentiation to near homogeneous population (Fig. 22) of CXCR4 expressing cells (98.3% of the cells were CXCR4 positive, +/- 1.9 SD) Was also observed.
완성 내배엽 형성(1기)이 완료된 후에, 원시 전장 형성(2기)을 유도하기 위해 사용되는 모르포겐인 FGF7을 함유하는 것으로 배지를 교체하였다. 원시 전장의 형성과 일치하여, 2기 1 및 3일째에 HNF4α 및 GATA6 발현 수준이 증가되었으며, 한편 1기 3일째에 고수준으로 발현된 유전자(CXCR4, EOMES, FGF17, FGF4, MNX1, PRDM1, SOX17, 및 VWF)는 2기 말기까지 감소된 발현을 나타내었다(도 23). 전장 유전자(AFP, PDX1, 및 PROX1)의 발현은 증가되었다(도 24).After complete endogenous endoderm formation (phase 1) was completed, the medium was replaced with one containing FGF7, a mRNA used to induce primordial batogenesis (phase 2). Expression levels of HNF4α and GATA6 were increased on
세포를 72시간 동안 2기 배지 중에서 배양한 후, 배양물을 3기 배지(표 7)로 교체하였다. 일단 이 배지 중에 있으면, 세포는 PDX1 및 FOXA2 발현에 의해 측정하였을 때 내배엽 췌장 계통과 일치하는 마커를 발현하였으며, 이는 도 25에 나타나 있다(90.9% ± 11.9 SD가 PDX1 양성이고, 99.2% ± 0.6 SD가 FOXA2 양성임). 이들 결과는 유전자 발현에 대한 qRT-PCR에 의해 분석된 샘플로부터의 데이터에 의해 확인되었다. PDX1에 대한 유전자 발현은 2기 3일째의 말기(38,000x vs. H1)로부터 3기 1일째의 말기(200,000x vs. H1)까지 24시간 내에 5배 증가하였으며, 48시간 후에3기 3일째에 다시 2배가 되었다(435,000x vs. H1). 이들 데이터는 세포가 췌장 운명으로 예정화되고 있는 중임을 나타낸다(도 26). 이러한 관찰은 췌장에서 공통으로 발현되는 다수의 유전자(ARX, GAST, GCG, INS, ISL1, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PAX6, PTF1A, 및 SST)의 증가된 수준에 의해 추가로 지지되었는데, 이는 도 26에 나타낸 바와 같다. 게다가, OCT4/POU5F1의 매우 낮은 발현 또는 비발현(대조군의 2 내지 10% 또는 qRT-PCR에 의해 32 내지 37 샘플 Ct) 및 내배엽 계통 AFP, ALB, 및 CDX2-의 다른 마커에 대한 고 발현 수준이 또한 관찰되었는데, 이는 상대적으로 유연한 장관 운명으로부터 췌장 수명까지 생물반응기 내에서의 세포 집단의 예정화 및 전이를 추가로 나타낸다.The cells were cultured for 72 hours in a second medium, and then the culture was replaced with a third medium (Table 7). Once in the medium, the cells expressed markers consistent with the endoderm pancreas lineage as measured by PDX1 and FOXA2 expression, as shown in Figure 25 (90.9% +/- 11.9 SD is PDXl positive, 99.2% +/- 0.6 SD Is FOXA2-positive). These results were confirmed by data from samples analyzed by qRT-PCR for gene expression. The expression of the gene for PDX1 was increased 5-fold within 24 hours from the end of day 2 (38,000x vs. H1) to the end of
4기 3일째에서의 분화 과정의 말기에서, 세포는 고수준의 PDX1 및 FOXA2 발현을 보유하였으며 췌장 내분비 세포(28.1% ± 12.5 SD가 크로모그라닌 양성임) 및 췌장 선조세포(58.3% ± 9.7 SD가 NKX6.1에 대해 양성임)의 혼합물과 일치하는 발현 패턴을 추가로 발생시켰는데, 이는 도 27에 나타낸 바와 같다. 이러한 단계 특이적인 마커 발현 패턴은 만능 집단으로부터 췌장 전구세포로의 효율적인 단계적 분화를 나타내었다. 유세포측정법에 의해 관찰된 결과는 qRT-PCR로부터의 데이터에 의해 추가로 확인되었다. 췌장에서 공통으로 발현되는 다수의 유전자(ARX, GAST, GCG, IAPP, INS, ISL1, MAFB, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PAX6, PTF1A, 및 SST)는 모두 증가된 발현 수준을 나타내었다(도 28).At the end of the differentiation process on
상이한 시드 물질, 0기 배지, 0기 배지의 pH 및 소포제의 사용과 같은 다수의 과정 변수를 시험하였을 때, 도 27에서 관찰된 발현 패턴은 다수의 실시에 걸쳐 일관성 있게 유지되었다. 시드 물질의 다수의 공급원을 시험하였으며, 각각은 90% 초과의 FOXA2, 75% 초과의 PDX1, 및 50% 초과의 NKX6.1을 가지면서 췌장 내배엽 운명을 효율적으로 생성하였다(도 29). 더욱이, 0.5% BSA로 보충된 "IH3"로 불리는 주문제작 사내 배지 또는 구매가능한 배지, 즉 0.5% BSA로 보충된 이센셜8™ 중에서 세포를 0기에서 성장시켰을 때, 생물반응기 생성물의 발현 패턴에 있어서 유의한 차이가 없었음이 주목되었다(도 30). 0기 배양물에서의 pH의 역할을 검사하였을 때, 상대적으로 낮은 pH(6.8)에서 0기에서 성장된 세포는 평균 실시와 대비하여 생물반응기 내에서 증가된 증폭을 가졌지만(도 7), 4기 3일째 세포 프로파일에 있어서는 유의한 변화가 없었음(도 31)이 주목되었다. 추가로, 소포제 C 에멀젼(시그마 카탈로그 번호 A8011)을 94 ppm으로 사용함으로써 스파징에 의해 생성된 버블을 감소시키는 것으로 보였지만, 0기 말기부터 4기 3일째 세포까지의 세포의 프로파일에는 영향을 미치지 않는 것으로 나타났다(표 9 및 도 32).When testing a number of process parameters such as the use of different seed materials, O-phase medium, O-phase medium and the use of defoamer, the pattern of expression observed in FIG. 27 remained consistent over a number of implementations. Multiple sources of seed material were tested, each efficiently producing pancreatic endodermic fate with more than 90% of FOXA2, more than 75% of PDX1, and more than 50% of NKX6.1 (Figure 29). Moreover, when cells were grown at 0 ° C in custom-made in-house media or in commercially available media called "IH3" supplemented with 0.5% BSA, ie, supplemented with 0.5% BSA, the expression patterns of bioreactor products (Fig. 30). When the role of pH in the 0 phase culture was examined, cells grown at 0 at a relatively low pH (6.8) had an increased amplification in the bioreactor as compared to the mean run (Figure 7) There was no significant change in cell profile at day 3 (FIG. 31). In addition, the use of the defoamer C emulsion (Sigma catalog number A8011) at 94 ppm seemed to reduce the bubbles produced by sparging, but did not affect the profile of the cells from the
각각의 생물반응기 분화의 말기에 생성물 세포를 동결보존하였다. 3.63 g/L 중탄산나트륨을 갖는 MCDB131, 또는 3.63 g/L 중탄산나트륨, 글루코스(최종 8 mM), 및 1x 글루타맥스를 갖는 MCDB131 중에서 세포를 세척하고, 이어서 2.43 g/L 중탄산나트륨을 갖는 57.5% MCDB131, 30% 무제노(Xeno-free) KSR, 10% DMSO, 및 2.5% HEPES(최종 농도 25 mM)로 구성된 차가운(4℃ 미만) 동결보존 배지에 옮겼다. 이어서, 주위 온도에서 최대 15분 동안 동결보존 매체 중에서 세포 클러스터를 유지하는 냉각 프로파일을 사용하여, 프로그램화 동결기(CRF) 내에서 세포를 동결시키고, 45분 동안 4℃의 온도로 감소시키고, 2.00℃/min으로 -7.0℃(샘플)까지 추가로 감소시켰다. 이어서, 챔버의 온도를 25.0℃/min의 속도로 -45.0℃까지 감소시켜 샘플을 신속하게 냉각시켰다. 이어서, 챔버 온도를 10.0℃/min으로 -25.0℃(챔버)까지 증가시킴으로써 보상 증가를 제공하였다. 이어서, 온도가 -40.0℃에 도달할 때까지 0.2℃/min으로 샘플을 냉각시켰다. 이어서, 챔버를 35.0℃/min의 속도로 -160℃까지 냉각시키고 그 온도에서 15분 동안 유지하였다. 샘플을 CRF 실시의 종료 시에 가스상 액체 질소 저장 용기로 이동하였다.The product cells were cryopreserved at the end of each bioreactor differentiation. Cells were washed with MCDB131 with 3.63 g / L sodium bicarbonate, or MCDB131 with 3.63 g / L sodium bicarbonate, glucose (final 8 mM), and 1x glutamax, followed by washing with 57.5% (Less than 4 ° C) cryopreserved media consisting of MCDB131, 30% Xeno-free KSR, 10% DMSO, and 2.5% HEPES (
세포를 증기상 액체 질소 저장소로부터 꺼내어서 바이알을 37℃ 수욕에 옮김으로써 해동시킬 수 있었다. 작은 빙정이 바이알 내에 남을 때까지, 바이알을 수욕 중에서 2분 미만 동안 온화하게 와동시켰다. 이어서, 바이알 내용물을 50 ml 원추형 튜브에 옮기고,Cells were removed from the vapor phase liquid nitrogen reservoir and thawed by transferring the vial to a 37 ° C water bath. The vial was gently vortexed in a water bath for less than 2 minutes until a small ice crystal remained in the vial. The vial contents were then transferred to a 50 ml conical tube,
2.43 g/L 중탄산나트륨 및 2% BSA를 갖는 MCDB131 배지를 사용하여 총 20 ml의 최종 용적이 될 때까지 2분에 걸쳐 적가하여 희석시켰다. 이어서, 총 세포수를 뉴클레오카운터®로 측정하고, 세포 현탁액을 초저부착 배양 디쉬에 1시간 동안 옮겨 두었다. 이어서, 세포를 50 ml 원추형 튜브 내에서 배지로부터 단리하고, 상층액을 제거하고 분석 또는 생체내 연구를 위해 세포를 4기 배지 중에 재현탁시켰다.Using MCDB131 medium with 2.43 g / L sodium bicarbonate and 2% BSA, to a final volume of 20 ml. Then placed moved for one hour the total number of the cells, the cell suspension was measured with a nucleoside ® counter to the ultra-low attachment culture dish. The cells were then isolated from the medium in a 50 ml conical tube, the supernatant was removed and the cells resuspended in 4 medium for analysis or in vivo studies.
대안적으로, 해동 후, 바이알 처리된 세포를 빈 125 mL 유리 코닝® 스피너 플라스크(코닝, 인코포레이티드, 미국 뉴욕주 코닝 소재)에 옮기고 2.43 g/L 중탄산나트륨 및 2% BSA를 갖는 10 mL MCDB131 배지를 플라스크에 적가하였다. 이어서, 80 mL의 동일한 배지로 최종 부피를 조절하였다. 총 세포수를 뉴클레오카운터®로 측정하고, 세포 현탁액을 40 내지 65 rpm으로 하룻밤(12 내지 28시간) 교반하였다. 이어서, 세포를 특징규명하거나 생체내 연구를 위해 사용하였다.Alternatively, after thawing, the vial treated cells were transferred to an empty 125 mL glass Corning (R) Spinner flask (Corning, Corning, Corning, NY) and incubated with 10 mL of 2.43 g / L sodium bicarbonate and 2% BSA MCDB131 medium was added dropwise to the flask. The final volume was then adjusted with 80 mL of the same medium. The total cell count was measured with a NucleoCounter (R) and the cell suspension was stirred at 40-65 rpm overnight (12-28 h). Cells were then used for characterization or in vivo studies.
IH3 배지의 조성은 하기에뿐만 아니라 미국 특허 출원 공개 제2013/0236973호에도 나타나 있으며, 이의 개시내용은 적합한 세포 배양 배지에 관한 것인 것과 같이 전체적으로 포함된다. IH3 배지 중의 BSA의 양은 변동될 수 있다.The composition of the IH3 medium is shown in US Patent Application Publication No. 2013/0236973 as well as the following, the disclosure of which is incorporated in its entirety as it relates to a suitable cell culture medium. The amount of BSA in the IH3 medium can be varied.
[표 7][Table 7]
[표 8][Table 8]
[표 9][Table 9]
재료:material:
인간 배아줄기(hES) 세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재) Human embryonic stem (hES) cell line H1 (WA01 cells, Wiscel, Madison, Wis.)
PBS(카탈로그 번호 14190, 인비트로겐) PBS (catalog number 14190, Invitrogen)
Y-27632(악소라 카탈로그 번호 ALX-270-333, 미국 캘리포니아주 샌디에고 소재) Y-27632 (Axora Catalog No. ALX-270-333, San Diego, CA)
EDTA(론자, 카탈로그 번호 17-7-11E) EDTA (Theoretical, catalog number 17-7-11E)
뉴클레오카운터®(케모메텍 에이/에스, 카탈로그 번호 YC-T100, 덴마크 알레로드 소재) NucleoCounter® (Chemomette A / S, catalog number YC-T100, Aare Rod, Denmark)
비-조직 배양물 처리된 6웰 디쉬(벡톤 딕킨슨, 카탈로그 번호 팔콘351146, 미국 뉴저지주 프랭클린 레이스크 소재) Non-tissue culture treated 6 well dishes (Becton Dickinson, Cat. No. Falcon 351146, Franklin Lacek, NJ)
아큐타제®(시그마, 카탈로그 번호 A-6964, 미국 미주리주 세인트루이스 소재) Accu hydratase ® (Sigma, catalog number A-6964, St. Louis, Missouri, USA Material)
pH, 및 용존 산소(DO) 생물반응기 프로브(펌프로브® pH 전극 225 mm, 모델 번호 F-635, 및 DO 옥시프로브® 12 mm 센서, 모델 번호 D-145, 미국 캘리포니아주 어바인 소재의 브로들리-제임스 코포레이션으로부터 입수됨) pH, and dissolved oxygen (DO) Bioreactor probe (pump lobe ® pH electrode 225 mm, Model No. F-635, and DO
면역-보호성 거대 캡슐화 장치(테트라사이트™, 미국 캘리포니아주 어바인 소재) Immune-Protective Giant Encapsulation Device (Tetrasite ™, Irvine, CA)
Mm 인간 C-펩타이드 ELISA(메르코디아 카탈로그 번호 10-1141-01) Mm human C-peptide ELISA (Merckidia Catalog No. 10-1141-01)
글루타맥스™, MCDB131, 및 ITS-X; 인비트로겐 Glutamax ™, MCDB131, and ITS-X; Invitrogen
FAF-BSA(프롤리언트(Proliant)) FAF-BSA (Proliant)
레티노산, 글루코스 45%(2.5M), SANT(Shh 억제제)(시그마) Retinoic acid,
GDF8(페프로텍) GDF8 (Peptronic)
MCX MCX
FGF7(알앤디 시스템즈) FGF7 (R & D Systems)
LDN-193189(BMP 수용체 길항제)(스템젠트) LDN-193189 (BMP Receptor Antagonist) (StemGent)
TPPB(PKC 활성화제)(켐파트너(ChemPartner)) TPPB (PKC activator) (ChemPartner)
MCDB 131 주문제작 배지 MCDB 131 Custom Made Badge
실시예 8Example 8
동결보존된 생물반응기에 의해 생성된 췌장 선조세포 클러스터의 성숙 Maturation of pancreatic progenitor cell clusters produced by cryopreserved bioreactors 및 기능And function
각각의 생물반응기 연구를 위해 충분한 세포를 생성하기 위하여 H1 hES(WB0106) 세포의 31회째 계대배양 마스터 세포 뱅크 바이알 하나를 해동시켰다. 5개의 매트리겔™ 코팅된 2-층 셀스택®(CS2)에 시딩하기에 충분한 세포를 생성할 때까지, EDTA 계대배양을 사용하여 매트리겔™ 상에서 수 회의 계대배양 동안 mTeSR®1 배지 중에서 부착 조건 하에서 세포를 증폭시켰다. 일단 CS2 내에서 성장하는 부착성 세포가 70% 융합을 나타내면, 인접한 펌프 튜빙을 갖는 C-플렉스® 튜빙 조립 캡을 배지 포트에 부착시켜 시스템을 폐쇄하였다. 시스템을 폐쇄시킨 후에, 백 또는 병을 테루모 용접기를 통해 C-플렉스®에 용접하고, 모든 액체 부피(배지, PBS-/-, 아큐타제®, 또는 현탁된 세포)를 연동 펌프를 사용하여 옮겼다.One 31-pass subculture master cell bank vial of H1 hES (WB0106) cells was thawed to generate sufficient cells for each bioreactor study. Five ™ matrigel-coated two-layer cell stack ® (CS2) to until generate sufficient cells for seeding, EDTA passaged on Matrigel ™ may use the conference
CS2로부터 세포를 리프팅하기 위해, 칼슘 또는 마그네슘을 갖지 않는 둘베코 인산염 완충 식염수(PBS-/-)로 세포를 1회 세척하고, 이어서 동일 부의 PBS-/-로 희석된 아큐타제®의 1/2 농도 용액으로 처리하고 4 내지 5분 동안 인큐베이션하였다. 이어서, 아큐타제® 용액을 제거하고, 효소 용액의 적용 후 3분째에, CS2를 탭핑하여 세포 리프팅을 조장하였다. 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 mTeSR®1 한 병을 CS2 내로 펌핑하여 잔류하는 아큐타제®를 헹구어 불활성화시키고, 이어서 헹굼액을 수집하였다. 제2 헹굼 부피를 첨가하고, 수집하고, 제1 헹굼액과 혼주시켰다. 1.6 내지 2.0 × 109개 세포를 2 리터의 최종 부피로 CS2로부터 회수하였다. 층당 2.0 내지 2.5 × 108개 세포를 4개의 CS2 또는 8개의 1-층 셀스택™ 내로 옮기고 층당 200 mL의 부피로 가습된 5% CO2 인큐베이터 내에서 37℃에서 2시간 동안 인큐베이션하였다.In order to lift the cells from the CS2, Dulbecco's phosphate buffered saline with no calcium or magnesium (PBS - / -) cells were washed once with, and then the same portion PBS - / - in the Accu hydratase ® diluted with 1/2 Concentration solution and incubated for 4-5 minutes. Then, remove the Accu hydratase ® solution, after the application of the
셀스택® 배지 포트들 사이에 인접한 펌프 튜빙이 부착된 C-플렉스® 튜빙의 폐쇄 루프를 사용하여, 세포 현탁액을 연동 펌프에 의해 5분 동안 75 rpm으로 분쇄하여 응집체를 균질화하였다. 이어서, 셀스택®을 가습된 5% CO2인큐베이터 내에서 37℃에서 18시간 동안 하룻밤 인큐베이션하였다. 이어서, 셀스택으로부터의 2 리터의 세포 및 배지를 혼주하고, 2개의 3 리터 다스깁 생물반응기에 각각 1 리터씩, 생물반응기당 1.5 리터의 새로운 mTeSR® 배지와 함께, 옮겼다. 생물반응기 접종 후 24시간째에 완전한 배지 교체를 행하면서, 분화 개시 전에 추가 2일 동안 mTeSR® 배지와 함께 세포를 유지하였다. 이어서, 표 10에 기재된 바와 같이 분화를 개시하고 유도하였다. 온도(37℃), pH(드리프트, 또는 CO2에 의해 만능 세포의 경우 6.8 또는 7.2로 그리고 분화의 경우 7.4로 조절됨), 및 용존 산소(30% DO 설정점, CO2/공기가 조절됨)에 대해 조절된 폐쇄된 멸균 현탁 생물반응기 내에서 총 14일 또는 15일(2일의 mTeSR® + 12일 또는 13일의 단계화된 분화) 동안 세포를 유지하였다. 임펠러를 각각의 배지 교체 전에 5 내지 20분 동안 정지하여 클러스터가 정착되게 하였다. 테루모™ 튜브 용접기를 사용하여 C-플렉스® 튜빙(콜-파머 노스 아메리카(Cole-Parmer North America), 미국 일리노이주 버논힐즈 소재)에 연결된 딥 튜브를 통해 연동 펌프에 의해 배지를 제거하거나 첨가하여 폐쇄된 시스템을 유지하였다. 일단 충분한 배지를 첨가하여 임펠러가 잠기면, 임펠러 및 가열 재킷에 재동력공급하였다.Using a closed loop of C-Flex tubing with adjacent pump tubing between the Cell Stack® outlet ports, the cell suspension was homogenized by grinding at 75 rpm for 5 minutes with a peristaltic pump to homogenize the aggregates. Cell Stack® was then incubated overnight at 37 ° C for 18 hours in a humidified 5% CO 2 incubator. Two liters of cells and media from the cell stack were then harvested and transferred to two 3 liter Darth giblet bioreactors, each with 1 liter each, along with 1.5 liters of fresh mTeSR® media per bioreactor. Cells were maintained with mTeSR® medium for an additional 2 days prior to initiation of differentiation, with complete medium change at 24 hours after bioreactor inoculation. Differentiation was then initiated and induced as described in Table 10. A temperature (37 ℃), pH (drift, or in the case of universal cells by CO 2 6.8 or, in the case of 7.2 and differentiation regulated to 7.4), and dissolved oxygen (30% DO set-point, CO 2 / air is regulated) Cells were maintained for a total of 14 days or 15 days (staged differentiation of mTeSR (R) + 12 or 13 days in 2 days) in a controlled, closed sterile suspension bioreactor. The impeller was stopped for 5 to 20 minutes before each medium was replaced to allow the clusters to settle. The medium was removed or added by a peristaltic pump through a dip tube connected to C-Flex® tubing (Cole-Parmer North America, Vernon Hills, Ill., USA) using a Terumo ™ tube welder Closed systems were maintained. Once sufficient media were added to lock the impeller, the impeller and heating jacket were re-powered.
2개의 생성 실시를 이들 방법을 사용하여 3 리터 반응기 내에서 개시하였다. 첫 번째 반응기 실시에서는, 2개의 상이한 pH 설정점을 만능 배양 배지의 처음 2일에 걸쳐 시험하였다. 반응기 1은 5%의 고정된 CO2 가스 주입률과 함께 pH 7.2로 설정하여, 반응기 환경이 세포의 대사 활성으로 인해 시간이 지나면서 산성화됨에 따라 pH는 더 낮게 "드리프트"될 것이다. 반응기 2는 pH를 7.2로 설정하고, 이를 CO2 가스 수준에 의해 조절하였다. 두 번째 반응기 실시에서는, pH를 반응기 1의 경우 6.8로 그리고 반응기 2의 경우 7.2로 설정하고, 둘 모두 CO2 가스 수준에 의해 조절하였다.Two production runs were carried out in a 3 liter reactor using these methods. In the first reactor run, two different pH set points were tested over the first two days of the universal culture medium.
생물반응기 과정을 모니터링하기 위하여, 세포 클러스터를 분화의 각각의 단계 말기에 취하여 유세포측정법에 의해 분석하였다(표 11; 표 12). 분화 개시 시에 CD9 발현/CXCR4 음성 만능 세포 집단으로부터 한정 내배엽 형성의 완료 시에CXCR4 발현 세포(96.9 내지 98.1%의 세포가 CXCR4 양성임)의 균질 집단으로의 거의 완전한 전이가 관찰되었다.To monitor the bioreactor process, cell clusters were taken at the end of each stage of differentiation and analyzed by flow cytometry (Table 11; Table 12). Almost complete transition of CXCR4 expressing cells (96.9 to 98.1% of cells are CXCR4 positive) to a homogeneous population was observed at the completion of definite endoderm formation from the CD9 expression / CXCR4 negative pluripotent population at the onset of differentiation.
유세포측정법에 의해 관찰된 결과는 rt-PCR에 의해 분석된 쌍을 이룬 샘플로부터의 결과와 상관되었다. 만능성으로부터 췌장 운명까지의 단계화된 분화에 특징적인 유전자 발현에 대한 과정 전체에 걸쳐 샘플을 시험하였다. 유도 분화의 개시 전에, 만능성 또는 조기 분화 운명과 관련된 유전자 패널에 대한 저밀도 어레이 상에서 생물반응기 세포 클러스터로부터 mRNA를 시험하였다.The results observed by flow cytometry correlated with the results from the paired samples analyzed by rt-PCR. Samples were tested throughout the course of gene expression characteristic of staged differentiation from universality to pancreatic destiny. Prior to initiation of induction differentiation, mRNA was tested from bioreactor cell clusters on a low density array for gene panels associated with universal or premature differentiation destiny.
생물반응기로부터의 세포는 만능성에 특징적인 유전자(POU5F1, NANOG, SOX2, 및 ZFP42)에 대한 발현을 보유하였으며, 미분화된 H1 대조군과 대비하여 분화에 특징적인 유전자(AFP, 및 FOXA2: 50배 미만의 증가; FOXD3, GATA2, GATA4, GSC, HAND2, MIXL1 및 T: 10배 미만으로 증가된 발현)의 최소한의 유도 또는 무유도를 나타낸 것으로 관찰되었다(도 33). 그러나, 일단 세포가 1기 1일째의 분화 배지와 접촉하면, CDX2, CER1, FGF17, FGF4, FOXA2, GATA4, GATA6, GSC, MIXL1, MNX1, 및 단미증(T) 발현의 수준이 미분화된 H1 hES 세포보다 100 내지 1000배 더 크게 증가함에 따라 유전자 발현 패턴은 급격히 변화하였다(도 34). 1기 3일째의 말기(완성 내배엽의 형성)까지, CD9, CDX2, FGF4, MIXL1, NANOG, POU5F1, 및 단미증(T)은 1기 1일째와 대비하여 발현이 감소하였으며, 한편 CD99, CER1, CXCR4, FGF17, GATA4, GATA6, KIT, OTX, 또는 SOX17과 같은 특징적인 완성 내배엽 유전자의 발현은 피크였다(도 35).Cells from the bioreactor possessed expression for the universal characteristic genes (POU5F1, NANOG, SOX2, and ZFP42), and genes specific for differentiation (AFP, FOXA2: less than 50-fold Increased expression of FOXD3, GATA2, GATA4, GSC, HAND2, MIXL1 and T: less than 10-fold) (Fig. 33). However, once the cells come into contact with the differentiation medium on the first day of the first stage, the level of expression of CDX2, CER1, FGF17, FGF4, FOXA2, GATA4, GATA6, GSC, MIXL1, MNX1, The gene expression pattern changed drastically as it increased 100 to 1000 times larger than the cells (Fig. 34). Expression of CD9, CDX2, FGF4, MIXL1, NANOG, POU5F1, and thymocytes (T) was decreased compared to the first day of the first stage until the end of the first day of the first day (formation of complete endoderm) Expression of characteristic endoderm genes characteristic of CXCR4, FGF17, GATA4, GATA6, KIT, OTX, or SOX17 was a peak (Fig. 35).
1기의 말기에, 세포 배양 배지를 GDF8을 함유하는 것으로부터 FGF7을 함유하는 배지로 교체하였다. 몇몇 상이한 유전자 발현 패턴이 주목되었다: 2기의 과정에 걸쳐 소정 유전자(AFP, ATOH1, HHEX, OSR1, PDX1, PROX1, SOX2, 및 SOX9)의 발현에 있어서의 증가, (HAND1 및 SOX17)의 발현에 있어서의 감소, (HNF4α)의 전체에 걸친 안정한 고 발현, 또는 (CDX2, GAST, NKX2.2, NKX6.1, 및 PTF1a)의 저/비발현(도 36a 내지 도 36e). 이들 패턴은 반응기 내의 세포가 중배엽 마커(HAND1 및 SOX17)에 대한 전장(AFP, ATOH1, HHEX, HNF4α, OSR1, PDX1, PROX1, SOX2, 및 SOX9) 발현이 감소되어 가고 있음을 나타내었다. 그러나, 2기 말기까지, 세포는 더 성숙한 장 또는 췌장 운명(CDX2, GAST, NKX2.2, NKX6.1, 및 PTF1a)으로 여전히 예정화되지 않았다.At the end of
3기의 말기까지, 세포는 PDX1 발현에 의해 측정된 바와 같이 췌장 계통으로 예정화되었는데, PDX1 발현은 미분화된 대조군과 대비하여 mRNA에 있어서 100,000배 초과로 증가하였으며(도 36), 유세포측정법에 의해 PDX1을 발현하는 세포가 76 내지 98%인 것(표 11)에 의해 입증되었다. 또한, 췌장의 다른 유전자(GAST, NKX2.2, NKX6.1, PROX1, PTF1a, 및 SOX9) 및 AFP 및 CDX2와 같은 장의 유전자의 유도가 관찰되었는데; 이는, 세포가 더 성숙한 운명으로 예정화되기 시작하였음을 나타낸다.By the end of
4기 3 또는 4일째에서의 분화 과정의 말기까지, 세포는 췌장 내분비 세포(47 내지 54%가 크로모그라닌 양성임) 및 췌장 선조세포(33 내지 52%가 NKX6.1에 대해 양성임)의 혼합물과 일치하는 발현 패턴을 나타내었는데, 이는 표 11 및 표 12에 나타낸 바와 같다. 이러한 단계 특이적 마커 발현 패턴은 만능 집단으로부터, 미분화된 H1 인간 배아줄기세포와 대비하여, PDX1의 고 발현 수준(1×106배 초과의 유도) 및 다른 췌장 유전자의 고 발현 수준(ARX, GCG, GAST, INS, ISL, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PTF1a, 및 SST의 1000배 초과의 유도) 그리고 OCT4/POU5F1 발현의 거의 완전한 손실을 특징으로 하는 췌장 선조세포로의 효율적인 단계적 분화를 나타내었다(도 37).By the end of the differentiation process at
분화 과정의 말기에, 0.08 내지 0.45 × 106개 세포/mL를 생성하였다(도 38: 일일 세포 카운트). 이어서, 이 과정에서 생성된 세포를 동결보존하거나, 또는 테트라사이트™ 장치를 통해 동물 내에 직접 피하 이식하거나 신장 피막 아래에 두었다. 세포를 동결보존시키기 위해, 이를 2.43 g/L 중탄산나트륨을 갖는 57.5% MCDB131, 30% 무제노 KSR, 10% DMSO, 및 2.5% HEPES(최종 농도 25 mM)로 구성된 동결보존 배지에 옮겼다. 일단 세포 클러스터를 주위 온도에서 동결보존 배지 중에 현탁시키면, 동결-바이알을 프로그램화 동결기(CRF)로 15분 이내로 이동해 두었다. 이어서, 챔버 온도를 45분 동안 4℃로 감소시키고, 추가로 2.00℃/min으로 -7.0℃(샘플)까지 감소시켰다. 이어서, 챔버의 온도를 25.0℃/min의 속도로 -45.0℃까지 감소시켜 샘플을 신속하게 냉각시켰다. 이어서, 챔버 온도를 10.0℃/min으로 -25.0℃(챔버)까지 증가시킴으로써 보상 증가를 제공하였다. 이어서, 온도가 -40.0℃에 도달할 때까지 0.2℃/min으로 샘플을 냉각시켰다. 이어서, 챔버를 35.0℃/min의 속도로 -160℃까지 냉각시키고 그 온도에서 15분 동안 유지하였다. 샘플을 CRF 실시의 종료 시에 가스상 액체 질소 저장 용기로 이동하였다.At the end of the differentiation process, 0.08 to 0.45 × 10 6 cells / mL were generated (FIG. 38: daily cell count). Cells generated in this process were then cryopreserved or transplanted directly into the animal through a tetrasite ™ device or placed under the kidney capsule. For cryopreservation of cells, it was transferred to cryopreservation medium consisting of 57.5% MCDB131, 30% nonenzo KSR, 10% DMSO, and 2.5% HEPES (
세포를 가스상 액체 질소 중에 저장한 후에, 세포를 저장소로부터 꺼내어서 해동시키고 37℃ 수욕으로 옮겼다. 작은 빙정이 바이알 내에 남을 때까지, 바이알을 수욕 중에서 2분 미만 동안 온화하게 와동시켰다. 이어서, 바이알 내용물을 50 ml 원추형 튜브에 옮기고, 2.43 g/L 중탄산나트륨 및 2% BSA를 갖는MCDB131 배지를 사용하여 총 20 ml의 최종 용적이 될 때까지 2분에 걸쳐 적가하여 희석시켰다. 이어서, 총 세포수를 뉴클레오카운터®로 측정하고, 세포 현탁액을 초저부착 배양 디쉬에 1시간 동안 옮겨 두었다. 이어서, 세포를 50 ml 원추형 튜브 내에서 배지로부터 단리하고, 상층액을 제거하고 세포를 4기 배지 중에 재현탁시켰다. 이어서, 세포를 테트라사이트™ 장치를 통해 동물에 피하 이식하거나 또는 신장 피막 아래에 이식하거나 또는 세포를 초저부착 배양 디쉬 내에서 하룻밤 인큐베이션한 후 동물에 이식하였다.After storing the cells in gaseous liquid nitrogen, the cells were removed from the reservoir, thawed and transferred to a 37 ° C water bath. The vial was gently vortexed in a water bath for less than 2 minutes until a small ice crystal remained in the vial. The vial contents were then transferred to a 50 ml conical tube and diluted using MCDB131 medium with 2.43 g / L sodium bicarbonate and 2% BSA dropwise over 2 minutes to a final volume of 20 ml total. Then placed moved for one hour the total number of the cells, the cell suspension was measured with a nucleoside ® counter to the ultra-low attachment culture dish. The cells were then isolated from the medium in a 50 ml conical tube, the supernatant removed and the cells resuspended in 4 medium. The cells were then transplanted subcutaneously into the animal via the tetrasite ™ device or transplanted under the renal capsule, or the cells were implanted into the animal after overnight incubation in a ultra-low attachment culture dish.
동물을 혈당 및 C-펩타이드 수준에 대해 이식편 이식 후 매 4주마다 모니터링하였다. 테트라사이트™ 장치 내부의 비-동결보존된 췌장 전구세포로 처리되거나 또는 신장 피막 아래에 세포를 직접 둠으로써 처리된 동물은 성숙하여 16주까지 1 ng/mL 초과의 C-펩타이드를 발현하였으며 이식 후 20주까지 2 ng/mL의 C-펩타이드에 도달하였다(도 39a 및 도 39d). 더욱이, STZ로 처리하여 숙주 β-세포 기능을 제거한 경우, 생착된 동물은 이식편이 제거될 때까지 정상 혈당(normo-glycemia)을 유지하였는데, 이는, 이식편이 단회 고용량의 STZ에 의해 유도된 당뇨병으로부터 동물을 보호하는 데 컴피턴트를 나타내었음을 나타낸다(도 39b).Animals were monitored every 4 weeks after implant grafting for blood glucose and C-peptide levels. Treated animals treated with non-cryopreserved pancreatic progenitor cells inside the tetrasite ™ device or directly with cells underneath the renal capsule were mature and expressed more than 1 ng / mL C-peptide up to 16 weeks, Reaching 2 ng / mL C-peptide by 20 weeks (Figs. 39A and 39D). Furthermore, when treated with STZ to remove host β-cell function, the engrafted animals maintained normo-glycemia until the graft was removed, since the graft survived from a single high dose of STZ-induced diabetes Indicating competency in protecting the animal (Figure 39b).
이 패턴은 또한 동결보존된 세포로 처리된 동물에서 관찰되었다. 해동 후 1시간 동안 배양된 동결보돈된 췌장 전구세포(1207B)를 사용한 신장 피막 이식편에 의해 처리된 동물은 16주째 및 20주째에 각각 평균 0.56 ng/mL 및 1.09 ng/mL의 C-펩타이드를 가졌으며, 한편 해동 후 하룻밤 배양된 세포(1207C)는 16주째 및 20주째에 각각 평균 0.81 ng/mL 및 1.35 ng/mL의 C-펩타이드를 가졌다(도 39d). 테트라사이트™ 장치 내부의 동결보존된 췌장 전구세포로 처리된 동물은 16주까지 1 ng/mL 초과의 C-펩타이드를 가졌으며, 비-동결보존된 대조군과 유사하게, STZ 처리 후 1주째에 치료적 수준의 C-펩타이드를 발현할 수 있었다(0.98 ng/mL, 도 39c). 이들 결과는 동결보존된 췌장 전구세포가 동물 모델에서 시험될 때 비-동결보존된 대조군과 비견될 정도로 기능할 수 있음을 나타낸다.This pattern was also observed in animals treated with cryopreserved cells. Animals treated with kidney-coated grafts using frozen-thawed pancreatic progenitor cells (1207B) cultured for 1 hour after thawing had C-peptides averaging 0.56 ng / mL and 1.09 ng / mL at 16 weeks and 20 weeks, respectively While cells cultured overnight after thawing (1207C) had C-peptide averages of 0.81 ng / mL and 1.35 ng / mL at 16 weeks and 20 weeks, respectively (FIG. 39D). Animals treated with cryopreserved pancreatic progenitor cells inside the tetrasite device had> 1 ng / mL of C-peptide up to 16 weeks and, similar to the non-cryopreserved control, treated at 1 week after STZ treatment Gt; C-peptide < / RTI > (0.98 ng / mL, Figure 39c). These results indicate that cryopreserved pancreatic progenitor cells can function to an extent comparable to non-cryopreserved controls when tested in animal models.
[표 10][Table 10]
[표 11][Table 11]
[표 12][Table 12]
교반 탱크 생물반응기 내에서 세포 응집체에 가해진 전단 응력의 계산 Calculation of shear stress applied to cell aggregates in a stirred tank bioreactor
3 L 다스깁 생물반응기 내에서 70 rpm의 교반 속도로 혼합된 2.7 리터 다스깁 교반 현탁 생물반응기 내에서 세포 응집체에 가해진 전단 응력을 측정하였다. 전단 응력 값을 계산하기 위하여, 다음에 기재된 바와 같이 가정하였다.The shear stress applied to the cell aggregates in a 2.7 liter Dozen centrifuge suspension bioreactor mixed at a stirring rate of 70 rpm in a 3 L dozen biod bioreactor was measured. In order to calculate the shear stress value, it is assumed as described below.
가정:home:
1. 세포 응집체에 부과된 최대 전단 응력은 난류성 와류(turbulent eddy)의 결과가 아니다.One. The maximum shear stress imposed on cell aggregates is not the result of turbulent eddy.
2. 세포 응집체에 부과된 최대 전단 응력은 응집체-응집체 또는 응집체-임펠러 충돌의 결과가 아니다.2. The maximum shear stress imposed on cell aggregates is not the result of aggregate-aggregate or aggregate-impeller collisions.
3. 배플(baffle)(즉, 딥 튜브 및 프로브)에 의해 부과된 전단 응력은 이들 계산에 반영되지 않는다.3. Shear stresses imposed by baffles (i.e., dip tubes and probes) are not reflected in these calculations.
본 명세서에서의 계산을 위하여, 하기에 열거된 명명법 및 물리적 파라미터를 사용하였다.For the calculations herein, the nomenclature and physical parameters listed below were used.
명명법:nomenclature:
파라미터:parameter:
열거된 배지 파라미터 및 생물반응기 파라미터를 하기 식에 적용하였다.The enumerated media parameters and bioreactor parameters were applied to the following equation.
방정식:equation:
레이놀즈 수Reynolds Number
응집체에 대한 최대 전단 응력(문헌[Cherry and Kwon 1990])The maximum shear stress for agglomerates (Cherry and Kwon 1990)
단위 질량당 소산된 동력()Power dissipated per unit mass ( )
소비된 동력(P)Power Consumed (P)
동력수 계산은 배플이 없는 교반 탱크의 경우 나가타 (1975)에 의해 도출된 경험적 상관관계식에 기초하였다.The power calculation was based on an empirical correlation equation derived by Nagata (1975) for a baffle-less stirred tank.
여기서,here,
2.7 L 다스깁 생물반응기 내에서 70 rpm의 교반 속도로 세포 응집체에 부과된 최대 전단은 적어도 2.5 dyn/㎠인 것으로 계산되었다. 클러스터의 최외층을 포함하는 세포는 최고 수준의 전단 응력을 겪는다. 이들 전단 응력 값은 기술된 가정에 크게 의존한다.The maximum shear applied to the cell aggregates at a stirring rate of 70 rpm in a 2.7 L dozens bioreactor was calculated to be at least 2.5 dyn /
실시예 9Example 9
세포주 WA01로부터 완성 내배엽으로의 인간 배아줄기세포의 분화: 현탁 배양물에서의 MCX/GDF8의 역할Differentiation of Human Embryonic Stem Cells from Cell Line WA01 to Complete Endoderm: Role of MCX / GDF8 in Suspension Culture
삼각 플라스크/진탕 플라스크, 스피너 플라스크, 또는 코팅되지 않은 초저결합 또는 비-조직 배양물 처리된 6웰 플레이트 내에서, 2% 무지방산 BSA(카탈로그 번호 68700, 프롤리언트, 미국 아이오와주 소재), 1X 글루타맥스™(카탈로그 번호 35050-079, 인비트로겐, 미국 캘리포니아주 소재), 추가 2.5 mM 글루코스(카탈로그 번호 G8769, 시그마) 및 1:50,000 스톡 농도의 ITS-X(카탈로그 번호 51500056, 인비트로겐, 미국 캘리포니아주 소재)로 보충된, 3.64 g/ml 중탄산나트륨 및 5.5 mM 글루코스(카탈로그 번호 A13051 DJ, 인비트로겐, 미국 캘리포니아주 소재)를 함유하는 MCDB-131 배지 중에, 만능 인간 배아줄기세포주 H1(NIH 코드: WA01)로부터의 클러스터를 0.25 × 106 내지 2 × 106개 세포/ml 범위의 세포 밀도로 시딩하였다. 이러한 방식으로 보충된 MCDB-131 배지는 본 출원의 목적을 위해 "1기 기본 배지"로 지칭될 것이다. 3 μM MCX(GSK3B 억제제, 14-프로프-2-엔-1-일-3,5,7,14,17,23,27-헵타아자테트라사이클로[19.3.1.1~2,6~.1~8,12~]헵타코사-1(25),2(27),3,5,8(26),9,11,21,23-노나엔-16-온, 미국 특허 출원 제12/494,789호; 전체적으로 본 명세서에 참고로 포함됨) 및 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍), 또는 3 μM MCX 단독, 또는 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈, 미국 미네소타주 소재)와 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재) 또는 20 ng/ml WNT-3A 단독으로 이 배지 중의 클러스터를 분화 1일째에 처리하였다. 2일째에, 세포를 100 ng/ml GDF8 또는 100 ng/ml 액티빈 A로 보충된 새로운 1기 기본 배지에 옮겼다. 유세포측정법, PCR 및 웨스턴 블롯(Western Blot) 분석을 위해 0시간째(기본 배지 + 보충물의 첨가 직후)부터 분화 개시 후 72시간째까지에 이르는 범위의 다양한 시점에서 샘플을 수집하였다.(Cat # 68700, Propylene, Iowa, USA), 1X non-fatty acid BSA in a 6-well plate treated with an Erlenmeyer flask / shaker flask, spinner flask, ITS-X (Cat. # 51500056, Invitrogen, USA) was added to Glutamax ™ (Cat # 35050-079, Invitrogen, CA), additional 2.5 mM glucose (Cat # G8769, Sigma) and 1: (USA), supplemented with 3.64 g / ml sodium bicarbonate and 5.5 mM glucose (Catalog No. A13051 DJ, Invitrogen, Calif., USA) supplemented with the humanized human embryonic stem cell line H1 : WA01) was seeded at a cell density in the range of 0.25 x 10 6 to 2 x 10 6 cells / ml. The MCDB-131 medium supplemented in this manner will be referred to as the " primary base medium "for the purpose of this application. 3 μM MCX (GSK3B inhibitor, 14-prop-2-en-1-yl-3,5,7,14,17,23,27-heptaaza tetracyclo [19.3.1.1-2.6 ~ 8,12-] heptacosa- (25), 2 (27), 3,5,8 (26), 9,11,21,23-nonanen-16-one, U.S. Patent Application No. 12 / 494,789 WNT-3A (catalog number 1324-WN-3), alone or in combination with 100 ng / ml GDF-8 (catalog number 120-00, (Catalog No. 338-AC, R & D Systems, Minnesota, USA) or 20 ng / ml WNT-3A alone to differentiate clusters in this medium Lt; / RTI > On
각각의 조건 하에서, 분화 3일 후에 유세포측정법을 사용하여 세포 표면 마커 CXCR4, CD99 및 CD9를 발현하는 세포의 백분율을 측정함으로써, 완성 내배엽의 생성 효능을 측정하였다. (도 40a 내지 도 40d에서의 FACS 도표에 나타나 있고 표 13에 요약되어 있는 바와 같은) 데이터는 현탁 배양물 중에, 분화 1일째에 TGF-β 패밀리 구성원의 부재 하에서의 3 μM MCX의 첨가가, 1일째에 3 μM MCX + 100 ng/ml GDF-8 또는 20 ng/ml WNT-3A + 100 ng/ml 액티빈 A로 세포를 처리하는 경우 수득된 것과 비견되는 수준으로 완성 내배엽을 생성함을 나타낸다.Under each condition, the production of complete endoderm was determined by measuring the percentage of cells expressing cell surface markers CXCR4, CD99 and CD9 using
[표 13][Table 13]
실시예 10Example 10
세포주 WA01로부터 완성 내배엽으로의 인간 배아줄기세포의 분화: 현탁액 반응물 중 MCX 화합물 농도의 용량 반응Differentiation of Human Embryonic Stem Cells from Cell Line WA01 to Complete Endoderm: The Capacity Response of MCX Compound Concentrations in Suspension Reactions
삼각 플라스크/진탕 플라스크 또는 스피너 플라스크 내에서, 실시예 9에 기술된 바와 같은 1기 기본 배지 중에, 만능 인간 배아줄기세포주 H1(NIH 코드: WA01)로부터의 클러스터를 0.25 × 106 내지 2 × 106개 세포/ml 범위의 세포 밀도로 시딩하였다. 분화 1일째에는 1.5, 2, 3 또는 4 μM MCX를 함유하는 1기 기본 배지로 그리고 2일째에는 100 ng/ml GDF-8을 함유하는 새로운 1기 기본 배지로 클러스터를 처리하였다. 3일째에는 배지 교체를 수행하지 않았다. 유세포측정법 및 PCR 분석을 위해 분화의 3일째 말기에 샘플을 수집하였다.During the first phase basal medium as described in Example 9 in the Erlenmeyer flask / shaker flask or a spinner flask, a universal human embryonic stem cell line H1: the cluster from the (NIH code WA01) 0.25 × 10 6 to 2 × 10 6 0.0 > cells / ml. ≪ / RTI > Clusters were treated with fresh primary basal medium containing 1.5, 2, 3 or 4 μM MCX on the first day of differentiation and fresh primary basal medium containing 100 ng / ml GDF-8 on the second day. No media change was performed on the third day. Samples were collected at the end of the third day of differentiation for flow cytometry and PCR analysis.
이어서, 유세포측정법을 사용하여 세포 표면 마커 CXCR4, CD99 및 CD9를 발현하는 세포의 백분율을 측정함으로써, 완성 내배엽의 생성 효능을 측정하였다. (도 41a 내지 도 41d에서의 FACS 도표에 나타나 있고 표 14에 요약되어 있는 바와 같은) 데이터는 현탁 배양물 중에, 2 μM 미만의 농도에서의 MCX의 첨가가 (더 낮은 백분율의 CXCR4 양성 세포 및 더 높은 백분율의 CD9 양성 세포에 의해 입증되는 바와 같이) 점진적으로 더 적은 수의 완성 내배엽 양성 세포를 생성함을 나타낸다. 또한, 4 μM 초과의 농도에서, MCX는 세포에 해로운 영향을 나타내며, 그 결과 감소된 세포 생존력을 가져온다. 그러나, BSA 농도를 증가시킴으로써, MCX의 영향이 조절될 수 있어서, 4 마이크로몰 이상의 농도가 사용되게 할 수 있다. 역으로, 1.5 마이크로몰 이하의 농도를 사용하여, 더 낮은 BSA 농도와 함께 사용되는 경우에, 완성 내배엽을 생성할 수 있다.Then, the production efficiency of complete endoderm was measured by measuring the percentage of cells expressing cell surface markers CXCR4, CD99 and CD9 using flow cytometry. The data (as shown in the FACS charts in Figures 41a-41d and summarized in Table 14) indicate that the addition of MCX at a concentration of less than 2 [mu] M in suspension cultures (a lower percentage of CXCR4- (As evidenced by a high percentage of CD9-positive cells). ≪ / RTI > In addition, at concentrations above 4 μM, MCX exhibits deleterious effects on cells, resulting in reduced cell viability. However, by increasing the BSA concentration, the effect of MCX can be controlled so that concentrations above 4 micromolar can be used. Conversely, using concentrations less than 1.5 micromolar, when used with lower BSA concentrations, complete endoderm can be produced.
[표 14][Table 14]
실시예 11Example 11
세포주 WA01로부터 완성 내배엽으로의 인간 배아줄기세포의 분화: 현탁 배양물에서의 배지 교체 빈도의 역할Differentiation of Human Embryonic Stem Cells from Cell Line WA01 to Complete Endoderm: Role of Medium Replacement Frequency in Suspension Culture
삼각 플라스크/진탕 플라스크 또는 스피너 플라스크 내에서, 실시예 9에 기술된 바와 같은 1기 기본 배지 중에, 만능 인간 배아줄기세포주 H1(NIH 코드: WA01)로부터의 클러스터를 0.25 × 106 내지 2 × 106개 세포/ml 범위의 세포 밀도로 시딩하였다. 분화 1일째에는 3 μM MCX를 함유하는 1기 기본 배지로 그리고 2일째에는 100 ng/ml GDF-8을 함유하는 새로운 1기 기본 배지로 클러스터를 처리하였다. 대조군 배양물은 3일째에 배지 교체를 받았으며; 별개의 용기에 대해서는, 배지 교체를 3일째에 수행하지 않았다. 유세포측정법 및 PCR 분석을 위해 분화의 3일째 말기에 샘플을 수집하였다.During the first phase basal medium as described in Example 9 in the Erlenmeyer flask / shaker flask or a spinner flask, a universal human embryonic stem cell line H1: the cluster from the (NIH code WA01) 0.25 × 10 6 to 2 × 10 6 0.0 > cells / ml. ≪ / RTI > The clusters were treated with a primary culture medium containing 3 μM MCX on the first day of differentiation and a fresh primary culture medium containing 100 ng / ml GDF-8 on the second day. The control cultures received medium changes on
이어서, 각각의 조건 하에서, 유세포측정법을 사용하여 세포 표면 마커 CXCR4, CD99 및 CD9를 발현하는 세포의 백분율을 측정함으로써, 완성 내배엽의 생성 효능을 측정하였다. 결과는 도 42a 및 도 42b에 FACS 도표로 나타나 있고 표 15에 요약되어 있다.Subsequently, under the respective conditions, the production efficiency of the complete endoderm was measured by measuring the percentage of cells expressing the cell surface markers CXCR4, CD99 and CD9 using flow cytometry. The results are shown in FACS charts in Figures 42A and 42B and summarized in Table 15. < tb > < TABLE >
[표 15][Table 15]
실시예 12Example 12
세포주 WA01로부터 완성 내배엽으로의 인간 배아줄기세포의 분화: 세포 현탁액에서의 글루타맥스™ 의 사용Differentiation of Human Embryonic Stem Cells from Cell Line WA01 to Complete Endoderm: Use of Glutamax ™ in Cell Suspension
삼각 플라스크/진탕 플라스크 또는 스피너 플라스크 내에서, 만능 인간 배아줄기세포주 H1(NIH 코드: WA01)로부터의 클러스터를 0.25 × 106 내지 2 × 106개 세포/ml 범위의 세포 밀도로 시딩하였다.Clusters from versatile human embryonic stem cell line H1 (NIH code: WA01) were seeded at cell densities ranging from 0.25 x 10 6 to 2 x 10 6 cells / ml, in Erlenmeyer flasks / shake flasks or spinner flasks.
이 실시예를 수행하여 완성 내배엽을 생성하는 데 글루타맥스™ 보충물이 필요한지의 여부를 결정하였는데, 이는 분화 1일째에 3 μM MCX로 보충되고 2일째에 100 ng/ml GDF-8을 함유하는 새로운 1기 기본 배지로 보충된 글루타맥스™가 함유되거나 함유되지 않은 1기 기본 배지(실시예 9에 기술됨) 중에 클러스터를 현탁시킴으로써 수행하였다. 3일째에는 배지 교체를 수행하지 않았다. 유세포측정법 및 PCR 분석을 위해 분화의 3일째 말기에 샘플을 수집하였다.This example was performed to determine whether Glutamax ™ supplements were needed to generate complete endoderm, which was supplemented with 3 μM MCX on
각각의 조건 하에서, 유세포측정법을 사용하여 세포 표면 마커 CXCR4, CD99 및 CD9를 발현하는 세포의 백분율을 측정함으로써, 완성 내배엽의 생성 효능을 측정하였다. 데이터 및 결과는 도 43a 및 도 43b에 FACS 도표로 나타나 있고 표 16에 요약되어 있다.Under each condition, the production of complete endoderm was determined by measuring the percentage of cells expressing cell surface markers CXCR4, CD99 and CD9 using flow cytometry. The data and results are shown in FACS charts in Figures 43A and 43B and summarized in Table 16.
[표 16][Table 16]
실시예 13Example 13
세포주 WA01로부터 완성 내배엽으로의 인간 배아줄기세포의 분화: 현탁 배양물에서의 중탄산나트륨 농도의 역할Differentiation of Human Embryonic Stem Cells from Cell Line WA01 to Complete Endoderm: Role of Sodium Bicarbonate Concentration in Suspension Culture
삼각 플라스크/진탕 플라스크 또는 스피너 플라스크 내에서, 실시예 9에 기술된 바와 같은 1기 기본 배지(3.64 g/l 중탄산나트륨을 함유함) 중에, 또는 2.43 g/l 중탄산나트륨을 함유하는 변형된 1기 기본 배지 중에, 만능 인간 배아줄기세포주 H1(NIH 코드: WA01)로부터의 클러스터를 0.25 × 106 내지 2 × 106개 세포/ml 범위의 세포 밀도로 시딩하였다. 클러스터를 실시예 12에 기술된 바와 같이 MCX 및 GDF-8을 함유하는 1기 기본 배지로 처리하였다. 유세포측정법을 위해 분화의 3일째 말기에 샘플을 수집하였다. 위상차 영상을 또한 분화의 각각의 일수에 캡처하였다.In a Erlenmeyer flask / shake flask or spinner flask, a first batch of medium (containing 3.64 g / l sodium bicarbonate) as described in Example 9, or a modified first batch containing 2.43 g / l sodium bicarbonate Clusters from universal human embryonic stem cell line H1 (NIH code: WA01) were seeded at a cell density in the range of 0.25 x 10 6 to 2 x 10 6 cells / ml. The clusters were treated with a primary basal medium containing MCX and GDF-8 as described in Example 12. Samples were collected at the end of the third day of differentiation for flow cytometry. Phase contrast images were also captured in each day of differentiation.
이어서, 유세포측정법을 사용하여 세포 표면 마커 CXCR4, CD99 및 CD9를 발현하는 세포의 백분율을 측정함으로써, 완성 내배엽의 생성 효능을 측정하였다. 데이터는 도 44a 및 도 44b에 FACS 도표로 나타나 있고 표 17에 요약되어 있다. 현탁 배양물에서, 2.43 g/L로 낮은 중탄산나트륨 수준은, 세포가 3.64 g/L를 함유하는 배지 중에서 분화된 경우(평균 97.35%의 세포가 CXCR4를 발현함)보다 덜 효율적으로(평균 87.4%의 세포가 CXCR4를 발현함) 완성 내배엽을 생성하는 것으로 나타난다. 게다가, 위상차 현미경법에 의해 관찰된 바와 같이, 중탄산염 수준에 있어서의 차이는 1기 말기에 클러스터 형태에 있어서의 차이와 상관된 것으로 관찰되었다(도 44c 및 도 44d). 또한, 고 중탄산염 수준 하에 분화된 세포는 2.43 g/L의 중탄산염에서 분화된 세포보다 더 느슨한 클러스터를 형성하는 것으로 밝혀졌다.Then, the production efficiency of complete endoderm was measured by measuring the percentage of cells expressing cell surface markers CXCR4, CD99 and CD9 using flow cytometry. Data are shown in FACS charts in Figures 44A and 44B and summarized in Table 17. In the suspension culture, the sodium bicarbonate level as low as 2.43 g / L was less efficient (average 87.4%) than when cells were differentiated in medium containing 3.64 g / L (97.35% of the cells expressed an average of CXCR4) Of cells express CXCR4) to produce complete endoderm. In addition, as observed by phase contrast microscopy, differences in bicarbonate levels were observed to correlate with differences in cluster morphology at the end of the first phase (Figs. 44C and 44D). It was also found that cells differentiated under the high bicarbonate level form looser clusters than cells differentiated in 2.43 g / L bicarbonate.
[표 17][Table 17]
실시예 14Example 14
스케일 조정가능한 생물반응기 과정에서 인간 유도 만능 줄기세포로부터 췌장 선조세포 클러스터의 생성Generation of pancreatic progenitor cell clusters from human induced pluripotent stem cells in a scalable bioreactor process
세포 요법은 용량당 다수(108개 초과)의 세포를 필요로 할 것이다. 이 실시예는 현재의 세포 요법 제조 실시로 가능한 것보다 3 내지 5 자리수 더 큰 크기로 유도 만능 줄기세포(iPS 세포) 덩어리를 분화시킬 수 있는 과정을 보여준다.Cell therapy will require multiple (more than 10 8 ) cells per dose. This example demonstrates the process by which a mass of inducible pluripotent stem cells (iPS cells) can be differentiated by a size greater than three to five digits larger than is possible with current cell therapy manufacturing practices.
이 실시예에서는, iPS 세포주를 사용하였다 - UTC(미국 특허 출원 제13/330,931호(미국 특허 출원 공개 제2013/0157365호)에 이미 기술된 제대 조직 세포로부터 유래되었으며, 이의 개시내용은 iPS 세포주를 유도하는 것에 관한 것인 것과 같이 참고로 포함됨). "풋-프린트" 없는("foot-print" free) 방식으로 플라스미드 형질감염을 사용하여 마우스 배아 영양세포 상에서 세포를 유도하고 15회째 계대배양에서 동결보존하였다.In this example, an iPS cell line was used - derived from umbilical cord tissue cells previously described in UTC (U.S. Patent Application No. 13 / 330,931, U.S. Patent Application Publication No. 2013/0157365), the disclosure of which is incorporated herein by reference, Quot ;, < / RTI > which is incorporated herein by reference). Cells were induced on mouse embryonic trophoblast cells using plasmid transfection in a "foot-print" free manner and cryopreserved in the 15th passage.
이들 동결보존된 세포로부터, 공급원 물질 바이알을 라이프 테크놀로지즈 코포레이션(미국 뉴욕주 그랜드 아일랜드 소재)으로부터의 이센셜 8™ 배지(E8™) 중 인간 재조합 라미닌(hrLaminin, 카탈로그 번호 LN-521, 스웨덴 스톡홀름 소재의 바이오라미나(Biolamina)로부터 입수됨) 상에 직접 해동시켜 사내 시드 물질을 생성함으로써 일련의 세포 뱅크를 생성하였다. 해동 및 증폭된 이 물질은 "프리-프리 마스터 세포 뱅크(Pre-Pre Master Cell Bank)"(Pre-Pre MCB)로 명명되었으며, 이는 미래의 뱅크를 위한 시드 물질로서의 역할을 하였다. 이어서, pre-pre MCB 3을 사용하여, 순차적인 세포 뱅크, 즉 Pre-MCB, MCB, 및 작업 세포 뱅크(WCB)를 생성하였다. 이어서, 하나의 WCB 바이알을 E8™ 중에서 3회의 계대배양 동안 EDTA 계대배양을 사용하여 hrLaminin 상에서 해동시키고, 증폭시켰다. 세포를 먼저 해동물로부터 T225 플라스크(코닝; 미국 뉴욕주 코닝 소재) 내로 시딩하고, 이어서 다수의 T225 플라스크 내로 계대배양하였다. 이어서, 다수의 T225 플라스크를 계대배양하고 합하여 단일의 1-층 셀스택™(CS1)에 시딩하였다. 일단 CS1 내의 세포가 융합되면, 세포를 PBS-/-로 1회 세척하고, PBS-/-로 희석된 아큐타제®의 1/2 농도 용액으로 처리하고 4 내지 5분 동안 인큐베이션하였다. 이어서, 아큐타제®를 제거하고, 효소 용액의 적용 후 3분째에, CS1을 탭핑하여 세포 리프팅을 조장하였다. 0.5% BSA로 보충되고 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 E8™을 CS1에 첨가하여 잔류하는 아큐타제®를 헹구어 불활성화시켰다. 이어서, 헹굼액을 수집하고 제2 헹굼 부피를 첨가하고, 수집하고, 제1 헹굼액과 혼주시켰다.From these cryopreserved cells, the source material vials were incubated with human recombinant laminin (hrLaminin, Catalog No. LN-521, Stockholm, Sweden) in LifeSystems Corporation (Grand Island, (Obtained from Biolamina, Inc.), to produce a series of cell banks by producing in-house seed material. The thawed and amplified material was named "Pre-Pre Master Cell Bank" (Pre-Pre MCB), which served as the seed material for future banks. Subsequently,
1 리터의 일회용 스피너 플라스크(코닝; 미국 뉴욕주 코닝 소재)에, 0.5% BSA로 보충되고 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 배지 중에, 225 mL 리터 중 1 × 106개 세포/mL의 농도로 세포를 옮겼다. 가습된 5% CO2 인큐베이터 내에서 60분 동안 정치 현탁 상태로 세포를 클러스터링되게 하고, 이어서 5분 동안 55 내지 65 rpm으로 교반하고, 0.5% BSA로 보충되고 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 225 mL의 추가 배지를 첨가하였다. 정치 배양물 중에서 추가 30분 동안 세포를 정착되게 하고, 이어서 0.5% BSA로 보충되고 10 마이크로몰의 Rho 키나제 억제제 Y-27632를 함유하는 150 mL의 추가 배지를 스피너 플라스크에 첨가하였다. 이후에, 세포를 가습된 5% CO2 인큐베이터 내에서 50 내지 70 rpm으로 연속적으로 교반하였다. 24시간 후에, 스피너 플라스크를 인큐베이터로부터 꺼내고, 클러스터가 5 내지 10분 동안 정착되게 하였다. 이어서, 용기에 200 mL가 남을 때까지 배지를 흡인한 다음, 400 mL의 추가의 새로운 배양 배지를 스피너 플라스크에 첨가하였다. 이 과정을 2일째의 말기(옮긴 후 48시간째)에 반복하였다.1 x 10 < 6 > cells / well in 225 mL liters were placed in a 1 liter disposable spinner flask (Corning, Corning, NY, USA) in a medium supplemented with 0.5% BSA and containing 10 micromoles of Rho kinase inhibitor Y- mL. < / RTI > The cells were allowed to clump in a humidified 5% CO 2 incubator for 60 minutes in a static suspension, followed by stirring at 55-65 rpm for 5 minutes, supplemented with 0.5% BSA and incubated with 10 micromoles of Rho kinase inhibitor Y-27632 Was added. The cells were allowed to settle for an additional 30 minutes in the scrambled culture, and then 150 mL additional medium supplemented with 0.5% BSA and containing 10 micromoles of Rho kinase inhibitor Y-27632 was added to the spinner flask. Subsequently, the cells were continuously stirred at 50-70 rpm in a humidified 5% CO 2 incubator. After 24 hours, the spinner flask was removed from the incubator and the clusters were allowed to settle for 5-10 minutes. The medium was then aspirated until 200 mL remained in the vessel, and 400 mL of additional fresh culture medium was added to the spinner flask. This process was repeated at the end of the second day (48 hours after transfer).
이어서, 초기 아큐타제® 처리 후 72시간째에, 세포 클러스터 해리 및 스피너 플라스크 시딩(계대배양)의 과정을 반복하여, 다회의 계대배양(시험된 범위: 1 내지 10회의 계대배양) 동안 현탁 상태로 세포를 유지하였다.Then, after the initial occupancy hydratase ® treatment in second 72 hours, to repeat the cell clusters dissociate and spinner flasks are seeded (passages), the conference passages: a suspended state during the (tested range from 1 to 10 times subculture) Cells were maintained.
이 과정을 사용하여, UTC iPS 세포를 기질 상의 부착성 배양물로부터 세포 클러스터로서 현탁 배양물로 전환시키고, 이어서 현탁 상태로 증폭시켰다. 이어서, 현탁 계대배양 및 배양된 이들 세포를 나중의 사용을 위해 동결보존 및 저장하였다. 동결보존을 위한 현탁 증폭된 세포를 제조하기 위하여, 세포를 40 마이크로미터 세포 여과기에 통과시키지 않은 것을 제외하고는, 전술된 바와 같이 세포 클러스터를 아큐타제®로 해리시켰다.Using this procedure, UTC iPS cells were converted from the adherent cultures on the substrate to suspension cultures as cell clusters and then amplified in suspension. These cells were then incubated in suspension and incubated for cryopreservation and storage for later use. In order to prepare the suspension for cryopreservation amplified cells were dissociated, and a is, cell clusters, as described above, except that the cells do not pass a 40 micron cell strainer into Accu hydratase ®.
이어서, 각각 1 리터의 일회용 플라스크로부터 세포를 카운트하고, 필요에 따라 합하고, 80 내지 200 rcf로 5분 동안 원심분리하였다. 이어서, 세포 펠렛을 교란시키지 않으면서 가능한 한 완전히 상층액을 제거하였다. 이어서, 차가운(4℃ 미만) 크라이오스토®10을 적가하여 1억 5000만개의 세포/mL의 최종 농도를 달성하고 세포 용액을 1.8 mL 코닝® 동결 바이알(코닝, 미국 뉴욕주 코닝 소재) 또는 15 mL 밀테니 동결 백(밀테니 바이오텍 인크., 미국 캘리포니아주 아우번 소재)에 옮기는 동안 빙욕 중에서 유지하였다.Cells were then counted from each 1 liter disposable flask, combined as needed, and centrifuged at 80 to 200 rcf for 5 minutes. The supernatant was then completely removed as completely as possible without disturbing the cell pellet. The cell solution was then transferred to a 1.8 mL Corning < > freezing vial (Corning, Corning, NY, USA) or 15 ml Miltoni freeze bag (Miltenyi Biotech Inc., Auvane, CA).
이어서, 현탁 증폭된 세포를 바이알 내에서 다음과 같이 프로그램화 동결기 내에서 고밀도로 동결시켰다. 챔버를 4℃로 예비-냉각시키고 샘플 바이알 온도가 6℃에 도달할 때까지 온도를 유지하였다. 이어서, 샘플이 -7℃에 도달할 때까지 챔버 온도를 2℃/min으로 강하시켰다. 일단 샘플 바이알이 -7℃에 도달하면, 챔버가 -45℃에 도달할 때까지 챔버를 20℃/min으로 냉각시켰다. 이어서, 챔버 온도가 -25℃에 도달할 때까지 챔버 온도를 10℃/min으로 짧은 시간에 상승되게 한 다음, 샘플 바이알이 -45℃에 도달할 때까지 챔버를 0.8℃/min으로 추가로 냉각시켰다. 이어서, 챔버가 -160℃에 도달할 때까지 챔버 온도를 35℃/min으로 냉각시켰다. 이어서, 챔버 온도를 -160℃에서 적어도 10분 동안 유지하고, 이후에 바이알을 가스상 액체 질소 저장소에 옮겼다.Then, the suspension-amplified cells were frozen at high density in a programmed freezer in a vial as follows. The chamber was pre-cooled to 4 ° C and the temperature was maintained until the sample vial temperature reached 6 ° C. The chamber temperature was then lowered to 2 [deg.] C / min until the sample reached -7 [deg.] C. Once the sample vial reached -7 占 폚, the chamber was cooled to 20 占 폚 / min until the chamber reached -45 占 폚. The chamber temperature was then allowed to rise briefly at 10 [deg.] C / min until the chamber temperature reached -25 [deg.] C and the chamber was further cooled at 0.8 [deg.] C / min until the sample vial reached -45 [ . The chamber temperature was then cooled to 35 [deg.] C / min until the chamber reached -160 [deg.] C. The chamber temperature was then maintained at -160 DEG C for at least 10 minutes, after which time the vials were transferred to a gaseous liquid nitrogen reservoir.
교반 탱크 생물반응기에 접종하기 위하여, 고밀도 동결보존 세포를 액체 질소 저장소로부터 꺼내고, 해동시켜, 폐쇄된 0.2 리터 유리 생물반응기(다스깁; 독일 율리히 소재)에 시딩하는 데 사용하였다. 동결 바이알을 가스상 액체 질소 저장소로부터 꺼내어서, 105초 동안 37℃ 수욕 중에 곧바로 넣어 두었다. 이어서, 해동된 바이알 성분을 2 mL 유리 피펫을 통해 50 mL 원추형 튜브에 옮겼다. 이어서, 0.5% BSA를 함유하고 10 마이크로몰의 Rho 키나제 억제제 Y-27632로 보충된 9 mL의 E8™을 튜브에 적가하였다. 이어서, 세포를 80 내지 200 rcf로 5분 동안 원심분리하였다. 이후에, 상층액을 튜브로부터 흡인하고, 0.5% BSA를 함유하고 10 마이크로몰의 Rho 키나제 억제제 Y-27632로 보충된 10 ml의 새로운 E8을 첨가하였다. 세포를 함유하는 이 부피를 배지 전달 병(Cap2V8®, 사니슈어, 미국 캘리포니아주 무어파크 소재) 내로 피펫팅하고, 병 내용물을 멸균 C-플렉스 튜빙 용접부를 통해 연동 펌프에 의해 생물반응기 내로 직접 펌핑하였다. 만능 줄기세포 접종을 위한 준비 시에, 생물반응기에 10 마이크로몰의 Rho 키나제 억제제 Y-27632 및 0.5% BSA로 보충된 E8™ 0.15 L를 준비하고, 37℃로 예비-가온하고, 70 rpm으로 교반하고, CO2에 의해 6.8 내지 7.1 pH로 조절하였는데, 이때 30%의 용존 산소 설정점(CO2, 공기, O2, 및 N2가 조절됨)을 가졌다. 접종 직후에, 생물반응기를 세포 카운트를 위해 샘플링하고, 배지 부피를 필요에 따라 조절하여 0.225 × 106개 세포/mL의 최종 세포 농도를 수득하였다.For inoculation into a stirred tank bioreactor, the high density cryopreserved cells were removed from the liquid nitrogen reservoir and thawed and used to seed into a closed 0.2 liter glass bioreactor (Dahl, Germany). The vials were taken out of the gaseous liquid nitrogen reservoir and immediately placed in a 37 ° C water bath for 105 seconds. The thawed vial was then transferred to a 50 mL conical tube through a 2 mL glass pipette. Then, 9 mL of E8 (TM) containing 0.5% BSA and supplemented with 10 micromolar Rho kinase inhibitor Y-27632 was added dropwise to the tube. The cells were then centrifuged at 80 to 200 rcf for 5 minutes. The supernatant was then aspirated from the tube and 10 ml of fresh E8 containing 0.5% BSA and supplemented with 10 micromoles of Rho kinase inhibitor Y-27632 was added. This volume containing the cells was pipetted into a media transfer vessel (Cap2V8 ® , Sanity, Moore Park, CA) and the contents of the bottles were pumped directly into the bioreactor by a peristaltic pump through a sterile C-flex tubing weld . In preparation for universal stem cell inoculation, 10 micromoles of Rho kinase inhibitor Y-27632 and 0.15 L of E8 ™ supplemented with 0.5% BSA were prepared in the bioreactor, pre-warmed to 37 ° C, stirred at 70 rpm And adjusted to pH 6.8 to 7.1 with CO 2 , with a 30% dissolved oxygen set point (CO 2 , air, O 2 , and N 2 controlled). Immediately after inoculation, the bioreactor was sampled for cell counting and the medium volume was adjusted as necessary to yield a final cell concentration of 0.225 x 10 6 cells / mL.
교반 탱크 생물반응기 내로 접종된 세포는 연속 교반 탱크 내에서 세포 클러스터를 형성하였다. 접종 후, 세포 클러스터를 반응기 내의 0.5% BSA로 보충된 E8 배지 중에서 3일 동안 유지하였다. 배지를 매일 교체하였는데, 접종 후 24시간째에 폐배지의 90%를 제거하고 0.15 리터의 새로운 배지를 첨가하였다. 접종 후 48시간째에, 폐배지의 90%를 제거하고 0.15 리터의 새로운 배지를 첨가하였다. 접종 후 72시간째에, 폐배지를 90% 초과하여 제거하고 분화 배지(표 18)를 첨가함으로써 만능 세포 분화를 개시하였다.The cells inoculated into the stirred tank bioreactor formed cell clusters in a continuous stirred tank. After inoculation, the cell clusters were maintained in E8 medium supplemented with 0.5% BSA in the reactor for 3 days. The medium was replaced on a daily basis. At 24 hours after inoculation, 90% of the lung medium was removed and 0.15 liter of fresh medium was added. Forty-eight hours after inoculation, 90% of the waste medium was removed and 0.15 liter of fresh medium was added. Seventy-two hours after inoculation, the lung medium was removed by more than 90% and pluripotent cell differentiation was initiated by addition of differentiation medium (Table 18).
일단 단계화된 분화 과정이 개시되면, 12일 이상 동안 온도(37℃), pH(분화의 경우 7.4), 및 용존 산소(1기의 경우 10% DO 설정점 및 모든 다른 시기에서는 30% DO 설정점, CO2, O2, N2, 및 공기가 조절됨)에 대해 조절된 폐쇄된 멸균 현탁 생물반응기 내에서 세포를 유지하였다. 분화 과정 전체에 걸쳐, 각각의 배지 교체 시, 딥-튜브를 통한 배지 제거 전에 5 내지 20분 임펠러를 정지시켜 클러스터가 정착되게 하였다. 테루모™ 튜브 용접기를 사용하여 C-플렉스® 튜빙에 연결된 딥 튜브를 통해 연동 펌프에 의해 닫힌 병 또는 백으로/그로부터 생물반응기 내의 배지를 제거하거나 첨가하여 폐쇄된 시스템을 유지하였다. 일단 충분한 배지를 용기에 첨가하여 임펠러가 완전히 잠기면, 임펠러 및 가열기에 재동력공급하였다.Once the staged differentiation process is initiated, the temperature (37 ° C), pH (7.4 for differentiation) and dissolved oxygen (10% DO setpoint for
생물반응기 과정을 모니터링하기 위하여, 세포 클러스터를 함유하는 배지의 샘플을 매일 수거하여 세포수 및 생존력(뉴클레오카운터®)을 측정하였으며, 이는 도 45에 나타낸 바와 같다. 0.225 × 106개 생존 세포/mL의 접종물이 증폭되어 4기 3일째에 0.65 × 106개 생존 세포/mL를 생성한 바와 같이, 세포의 일반적인 증폭이 이 과정 동안 관찰되었다(도 45).In order to monitor a bioreactor process, by daily collection of samples of the medium containing the cell clusters was measured with the cell number and viability (nucleoside Counter ®), which are shown in Figure 45. Normal amplification of the cells was observed during this process, as the inoculum of 0.225 × 10 6 viable cells / mL was amplified to produce 0.65 × 10 6 viable cells / mL on the third day 4 (FIG. 45).
일일 카운트 외에, 생물반응기 배지 샘플을 노바 바이오프로파일® 플렉스(노바 바이오메디칼 코포레이션, 미국 매사추세츠주 월섬 소재)에 의해 분석하였다. 0기(pH 6.8)에서의 반응기 설정점마다, 0기에서의 배지의 pH는 0기에 걸쳐 산성(pH 6.8)이었다(도 46). 0기에서의 산성 설정점은 상대적으로 낮은 락트산에서 세포의 대사 활성을 감소시키는 것으로 나타났으며, 0기 배지 중의 고 글루코스 수준이 관찰되었다. 일단 세포가 3기 말기에 걸쳐 분화되기 시작하면, 세포는 배지 중의 거의 모든 글루코스를 소비하여(도 47) 고수준의 락트산을 생성하였다(도 48). 추가로, 세포 밀도에 있어서의 증가가 1 및 2기의 과정에 걸쳐 관찰되었다(도 45).In addition to eleven counts, the bioreactor medium samples were analyzed by Nova Bio-Flex ® profile (Nova Biomedical Corp., Waltham, Massachusetts materials). The pH of the medium at
pH 및 대사에 있어서의 단계 특이적인 변화가 qRT-PCR에 의해 측정하였을 때의 mRNA 발현 패턴에 있어서의 단계 변화와 매칭되는지를 결정하기 위하여, 다음을 행하였다. 만능성, 완성 내배엽(DE), 장관(GT), 또는 4기(S4)로 지정된 4개의 어플라이드 바이오시스템즈 저밀도 어레이를 사용하였다(라이프(Life)™, 미국 캘리포니아주 칼스배드 소재). 모든 실시 및 어레이에 걸쳐 발현을 표준화하기 위하여, 대조군으로서의 미분화된 UTCiPS 세포 샘플과 대비하여 배수 차이로서 결과를 제시하고 있다.In order to determine whether the step-specific change in pH and metabolism matched the step change in the mRNA expression pattern as measured by qRT-PCR, the following was done. We used four Applied Biosystems low density arrays designated as universal, complete endoderm (DE), intestinal (GT), or four (S4) (Life ™, Carlsbad, CA). To standardize expression across all runs and arrays, the results are presented as a multiple of the difference relative to the undifferentiated UTCiPS cell sample as a control.
이들 어레이를 사용하여, 유전자 발현을 분화의 각각의 단계에서 측정하였다. 이어서, 생물반응기 내로 해동된 시드 물질 세포는 0기 1, 2, 및 3일째(생물반응기 접종 후 24, 48, 및 72시간째: 도 49 및 도 50)에서 미분화된 유전자 발현 패턴을 나타낸 것으로 관찰되었다. 이들 결과는 CD9, SSEA4, TRA-1-60, 및 TRA-1-81의 고 발현 수준, 및 CXCR4/CD184의 부재를 보여준 유세포측정법의 결과와 잘 상관되었다(도 51). 이들 유세포측정법 및 qRT-PCR의 데이터는, 만능성 유전자(CD9, NANOG, POU5F1, SOX2, TDGF, 및 ZFP42)의 견고하고 안정한 발현 패턴, 및 분화 동안 특징적으로 발현되는 유전자(CD99, CDH2, CDX2, CER1, CXCR4, EOMES, FGF17, FGF4, FOXA2, GATA2, GATA4, GATA6, GSC, HAND2, HNF4α, KIT, MNX1, MIXL1, PRDM1, PTHR1R, SOX17, SOX7, T, TMPRSS2, 및 VWF)의 비발현을 나타내었는데, 이는 안정한 만능 상태와 일치하는 것이었다.Using these arrays, gene expression was measured at each step of differentiation. Subsequently, seed material cells thawed into the bioreactor showed undifferentiated gene expression patterns at
0기의 완료 시(반응기 접종 후 72시간째), MCX 및 GDF8을 함유하는 분화 배지(표 18) 내로 세포를 이동하였다. 이 배지 교체 후 24시간째에, 유전자 발현 패턴에 있어서의 유의한 변경(도 49 및 도 50; 미분화된 대조군 대비 발현 배수)이 주목되었는데, 예를 들어 FOXA2, HAND2, PRDM1, PTH1R 및 SOX17 발현에 있어서의 10x 초과의 증가, CER1, FGF4, GATA4, GATA6, GSC, 및 MNX1에 있어서의 100x 초과의 증가, 및 EOMES, FGF17, MIXL1, 및 T 발현에 있어서의 1000x 초과의 증가이다. 이들 증가된 발현 수준은, 세포가 중배엽 운명을 통해 전이되고 있음을 나타내었다. CDX2 수준은 미분화된 세포와 대비하여 1기 1일째에 상승하였지만(대조군과 대비하여 발현에 있어서 2700x 증가), 이는 발현에 있어서의 일시적인 증가였으며 CDX2 수준은 1기 3일째까지 97% 하락하여 분화 유도 전에 관찰된 것과 비견되는 수준이 되었음이 또한 주목되었다(도 49 및 도 50; 미분화된 대조군 대비 발현 배수).Upon completion of 0 (72 hours after reactor inoculation), cells were transferred into differentiation medium containing MCX and GDF8 (Table 18). At 24 hours after this medium change, significant changes in gene expression patterns (Figs. 49 and 50; expression multiples relative to undifferentiated control) have been noted, for example in the expression of FOXA2, HAND2, PRDM1, PTH1R and SOX17 An increase of more than 100x in CER1, FGF4, GATA4, GATA6, GSC, and MNX1, and an increase of more than 1000x in EOMES, FGF17, MIXL1, and T expression. These increased expression levels indicate that the cells are metastasizing through mesodermal fate. The level of CDX2 was elevated on day 1 (compared with control), compared to undifferentiated cells (increased by 2700x in expression), but it was a transient increase in expression and CDX2 level was decreased by 97% until
1기 분화 배지에 노출 후 72시간째에, CXCR4 수준이 과거 대조군에 비하여 약 400x로 피크이고 FOXA2는 과거 대조군에 비하여 136x로 발현되고, SOX17은 과거 대조군에 비하여 470,000x로 발현된 바와 같이, 세포는 완성 내배엽으로의 예정화와 일치하는 프로파일을 발현하였다. 완성 내배엽과 일치하여, 1기의 말기(3일째)에서의 CER1, EOMES, FGF4, GSC, MIXL1, 및 T의 유전자 발현은 1기, 1일째에 관찰된 상승된 수준으로부터 하락하였다(도 49 및 도 50; 미분화된 대조군 대비 발현 배수).At 72 hours after exposure to the 1 st stage differentiation medium, the level of CXCR4 peaked at about 400x compared to the control group, FOXA2 was expressed at 136x as compared with the control group, and SOX17 was expressed at 470,000x as compared with the control group Exhibited a profile consistent with the preincubation to complete endoderm. Gene expression of CER1, EOMES, FGF4, GSC, MIXL1, and T at the end of stage 1 (day 3) fell from the elevated levels observed at
qRT-PCR에 의해 관찰된 유전자 발현에 있어서의 이들 변화는 유세포측정법에 의해 관찰된 결과와 상관되었다. 분화 개시 시에 CD9 발현/CXCR4 음성 만능 세포 집단(도 51)으로부터 1기 말기에 CXCR4 발현 세포(98.6%의 세포가 CXCR4 양성임)의 균질 집단(도 52)으로의 거의 완전한 전이가 관찰되었다.These changes in gene expression observed by qRT-PCR correlated with the results observed by flow cytometry. Almost complete transfer of CXCR4 expressing cells (98.6% of cells are CXCR4 positive) to a homogeneous population (FIG. 52) was observed at the beginning of differentiation from the CD9 expression / CXCR4 negative universal cell population (FIG.
완성 내배엽 형성(1기)이 완료된 후에, 원시 전장 형성을 유도하기 위해 사용되는 모르포겐인 FGF7을 함유하는 것으로 배지를 교체하였다. 원시 전장의 형성과 일치하여, 2기 1 및 3일째에 HNF4α 및 GATA6 발현 수준이 증가되었으며, 한편 1기 3일째에 고수준으로 발현된 유전자(CXCR4, EOMES, FGF17, FGF4, MNX1, PRDM1, SOX17, 및 VWF)는 2기 말기까지 감소된 발현을 나타내었다(도 50 및 도 53; 미분화된 대조군 대비 발현 배수). 전장 유전자(AFP, PDX1, 및 PROX1)의 발현은 증가되었다(도 53; 미분화된 대조군 대비 발현 배수).After complete endoderm formation (stage 1) was completed, the medium was replaced with one containing FGF7, a mollipagen used to induce primordial electrical field formation. Expression levels of HNF4α and GATA6 were increased on
세포를 72시간 동안 2기 배지 중에서 배양한 후, 배양물을 3기 배지(표 18)로 교체하였다. 일단 이 배지 중에 있으면, 세포는 유전자 발현에 대해 qRT-PCR 검정에 의해 측정하였을 때 내배엽 췌장 계통과 일치하는 마커를 발현하였다. PDX1에 대한 유전자 발현은 2기 3일째 말기에 대조군에 비하여 12,000x로부터 3기 3일째 말기에 대조군에 비하여 739,000x까지 60배 증가하였다. 이들 데이터는 세포가 췌장 운명으로 예정화되고 있는 중임을 나타낸다(도 54). 이러한 관찰은 췌장에서 공통으로 발현되는 다수의 유전자(ARX, GAST, GCG, INS, ISL1, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PAX6, PTF1A, 및 SST)에 대한 미분화된 대조군과 대비하여 증가된 발현 수준에 의해 지지되었는데, 이는 도 54 및 도 55에 나타낸 바와 같다. 흥미롭게도, OCT4/POU5F1 비발현(qRT-PCR에 의한 37 샘플 Ct) 및 내배엽 계통의 다른 마커 AFP, ALB, 및 CDX2에 대한 고 발현 수준이 또한 관찰되었다. 이는, 생물반응기 내의 세포 집단이 만능 세포 집단으로부터 먼저 상대적으로 유연한 장관으로 분화되고, 이어서 췌장 운명으로 추가로 분화되었음을 나타낸다(도 54 및 도 55).The cells were cultured for 72 hours in a second medium, and then the culture was replaced with a third medium (Table 18). Once in the medium, the cells expressed markers consistent with the endoderm pancreatic lineage as measured by qRT-PCR assays for gene expression. The gene expression of PDX1 was increased from 12,000 × at the end of
4기 분화 과정의 말기에, 세포는 고수준의 PDX1(FACS에 의해 95.6% 양성, qRT-PCR에 의해 대조군에 비하여 약 1,000,000배 유도) 및 FOXA2(FACS에 의해 99.5% 양성) 발현을 보유하였다. 세포는 췌장 선조세포(FACS에 의해 NKX6.1에 대해 39.2%가 양성임) 및 췌장 내분비 세포의 집단(PAX6에 대해서는 9.4%가 양성이고, 크로모그라닌에 대해서는 2.4%가 양성이고, NKX2.2에 대해서는 15.2%가 양성임; 모두 FACS에 의함)과 일치하는 발현 패턴을 나타내었다. 이러한 단계 특이적인 마커 발현 패턴은 만능 집단으로부터 췌장 전구세포로의 효율적인 단계적 분화를 나타내었다. 유세포측정법에 의해 관찰된 이들 결과는 qRT-PCR에 의해 확인되었다. 췌장에서 공통으로 발현되는 다수의 유전자(ARX, GAST, GCG, IAPP, INS, ISL1, MAFB, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PAX6, PTF1A, 및 SST)는 모두4기 3일째에 증가된 발현 수준을 가졌음이 또한 주목되었다(도 55). 참고로, 각각의 단계의 말기에서의 세포 클러스터의 대표적인 현미경 사진(4x)이 도 56에 나타나 있다.At the end of the four-phase differentiation process, the cells retained high levels of PDX1 (95.6% positive by FACS, approximately 1,000,000 fold induction by qRT-PCR) and FOXA2 (99.5% positive by FACS). The cells were positive for pancreatic progenitor cells (39.2% positive for NKX6.1 by FACS) and a group of pancreatic endocrine cells (9.4% positive for PAX6, 2.4% positive for chromogranin, NKX2. 2, 15.2% were positive, all due to FACS). These phase specific marker expression patterns showed efficient stepwise differentiation from the universal population into pancreatic progenitor cells. These results observed by flow cytometry were confirmed by qRT-PCR. A number of genes commonly expressed in the pancreas (ARX, GAST, GCG, IAPP, INS, ISL1, MAFB, NEUROD1, NGN3, NKX2.2, NKX6.1, PAX4, PAX6, PTF1A and SST) Lt; RTI ID = 0.0 > (Figure 55). ≪ / RTI > For reference, representative micrographs (4x) of cell clusters at the end of each step are shown in FIG.
[표 18][Table 18]
[표 18a][Table 18a]
[표 18b][Table 18b]
재료:material:
인간 배아줄기(hES) 세포주 H1(WA01 세포, 위셀, 미국 위스콘신주 매디슨 소재) Human embryonic stem (hES) cell line H1 (WA01 cells, Wiscel, Madison, Wis.)
PBS(카탈로그 번호 14190, 인비트로겐) PBS (catalog number 14190, Invitrogen)
Y-27632(악소라 카탈로그 번호 ALX-270-333, 미국 캘리포니아주 샌디에고 소재) Y-27632 (Axora Catalog No. ALX-270-333, San Diego, CA)
EDTA(론자, 카탈로그 번호 17-7-11E) EDTA (Theoretical, catalog number 17-7-11E)
뉴클레오카운터®-(케모메텍 에이/에스, 카탈로그 번호 YC-T100, 덴마크 알레로드 소재) Nucleoside counter ® - (kemo metek A / S, catalog number YC-T100, Denmark Alessio loaded material)
비-조직 배양물 처리된 6웰 디쉬(벡톤 딕킨슨, 카탈로그 번호 팔콘351146, 미국 뉴저지주 프랭클린 레이스크 소재) Non-tissue culture treated 6 well dishes (Becton Dickinson, Cat. No. Falcon 351146, Franklin Lacek, NJ)
아큐타제®, (시그마-알드리치, 카탈로그 번호 A-6964, 미국 미주리주 세인트루이스 소재) Accu hydratase ®, (Sigma-Aldrich, catalog number A-6964, St. Louis, Missouri, USA Material)
pH, 및 용존 산소(DO) 생물반응기 프로브(펌프로브® pH 전극 225 mm, 모델 번호 F-635, 및 DO 옥시프로브® 12 mm 센서, 모델 번호 D-145, 미국 캘리포니아주 어바인 소재의 브로들리-제임스 코포레이션으로부터 입수됨) pH, and dissolved oxygen (DO) Bioreactor probe (pump lobe ® pH electrode 225 mm, Model No. F-635, and DO
면역-보호성 거대 캡슐화 장치(테트라사이트™, 미국 캘리포니아주 어바인 소재) Immune-Protective Giant Encapsulation Device (Tetrasite ™, Irvine, CA)
인간 C-펩타이드 ELISA(메르코디아 카탈로그 번호 10-1141-01) Human C-peptide ELISA (Merckidia Catalog No. 10-1141-01)
글루타맥스™, MCDB131, 및 ITS-X; 인비트로겐 Glutamax ™, MCDB131, and ITS-X; Invitrogen
FAF-BSA(프롤리언트) FAF-BSA (Proliferation)
레티노산, 글루코스45%(2.5M), SANT(Shh 억제제)(시그마) Retinoic acid,
GDF8(페프로텍) GDF8 (Peptronic)
MCX MCX
FGF7(알앤디 시스템즈) FGF7 (R & D Systems)
LDN-193189(BMP 수용체 길항제)(스템젠트) LDN-193189 (BMP Receptor Antagonist) (StemGent)
TPPB(PKC 활성화제)(켐파트너) TPPB (PKC activator) (Chem partner)
실시예Example 15 15
세포주 WA01로부터 완성 내배엽으로의 인간 배아줄기세포의 분화: 현탁 배양물에서의 세포 주기 조절인자로서의 MCX/GDF8의 역할Differentiation of Human Embryonic Stem Cells from Cell Line WA01 to Complete Endoderm: Role of MCX / GDF8 as a Cell Cycle Regulator in Suspension Culture
삼각 플라스크/진탕 플라스크 내에서, 2% 무지방산 BSA(카탈로그 번호 68700, 프롤리언트, 미국 아이오와주 소재), 1X 글루타맥스™(카탈로그 번호 35050-079, 인비트로겐, 미국 캘리포니아주 소재), 추가 2.5 mM 글루코스(카탈로그 번호 G8769, 시그마) 및 1:50,000 스톡 농도의 ITS-X(카탈로그 번호 51500056, 인비트로겐, 미국 캘리포니아주 소재)로 보충된, 3.64 g/ml 중탄산나트륨 및 5.5 mM 글루코스(카탈로그 번호 A13051 DJ, 인비트로겐, 미국 캘리포니아주 소재)를 함유하는 MCDB-131 배지 중에, 만능 인간 배아줄기세포주 H1(NIH 코드: WA01)로부터의 클러스터를 0.5 x 106개 세포/ml로 시딩하였다. 이러한 방식으로 보충된 MCDB-131 배지는 이 실시예의 목적을 위해 1기 기본 배지 또는 "순수" 배지로 지칭될 것이다. GSK3B 억제제, 14-프로프-2-엔-1-일-3,5,7,14,17,23,27-헵타아자테트라사이클로[19.3.1.1~2,6~.1~8,12~]헵타코사-1(25),2(27),-3,5,8(26),9,11,21,23-노나엔-16-온 - 전체적으로 본 명세서에 참조로 포함된 미국 특허 출원 제12/494,789호 - 은 "MCX"로 지칭될 것이다.(Catalog No. 68700, Proliant, Iowa, USA), 1X Glutamax ™ (Catalog No. 35050-079, Invitrogen, Calif., USA), in a triangular flask / shake flask 3.64 g / ml sodium bicarbonate and 5.5 mM glucose supplemented with 2.5 mM glucose (catalog number G8769, Sigma) and 1: 50,000 stock concentration of ITS-X (catalog number 51500056, Invitrogen, Calif. Clusters from universal human embryonic stem cell line H1 (NIH code: WA01) were seeded at 0.5 x 106 cells / ml in MCDB-131 medium containing A13051 DJ, Invitrogen, CA, USA. MCDB-131 medium supplemented in this manner will be referred to as a primary or "pure" medium for the purposes of this example. GSK3B inhibitor, 14-prop-2-en-1-yl-3,5,7,14,17,23,27-heptaaza tetracyclo [19.3.1.1-2,6- ] Heptacosa- 1 (25), 2 (27), -3,5, 8 (26), 9,11,21,23-nonanen-16-one-US Patents, Application No. 12 / 494,789 - will be referred to as "MCX ".
다음의 6가지 조건 중 하나로 분화의 1일째에 클러스터를 처리하였다: (1) 순수, (2) 3 μM MCX + 100 ng/ml GDF-8(카탈로그 번호 120-00, 페프로텍), (3) 3 μM MCX 단독, (4) 100 ng/ml GDF-8 단독, (5) 20 ng/ml WNT-3A(카탈로그 번호 1324-WN-002, 알앤디 시스템즈, 미국 미네소타주 소재) + 100 ng/ml 액티빈 A(카탈로그 번호 338-AC, 알앤디 시스템즈, 미국 미네소타주 소재), 또는 (6) 20 ng/ml WNT-3A 단독.The clusters were treated on the first day of differentiation in one of the following six conditions: (1) pure, (2) 3 μM MCX + 100 ng / ml GDF-8 (catalog number 120-00, (5) 20 ng / ml WNT-3A (Catalog No. 1324-WN-002, available from R & D Systems, Minn., USA) + 100 ng / ml solution (6) 20 ng / ml WNT-3A alone. ≪ RTI ID = 0.0 >
각각의 조건에서 배지를 분화 개시 후 24 및 48시간째에 교체하였다. 이들 시간에, 조건 1, 2, 3, 및 4에서의 세포는 100 ng/ml GDF8로 보충된 새로운 1기 기본 배지로 교체하였으며, 한편 조건 5 및 6에서의 세포는 100 ng/ml 액티빈 A로 보충된 새로운 1기 기본 배지로 교체하였다.At each condition, the medium was replaced at 24 and 48 hours after initiation of differentiation. At these times, cells in
분화 개시 전 1시간째에, 그리고 분화 개시("0시간째"로서 언급됨) 후 5, 23, 29, 47, 또는 71시간째에, 현탁 샘플을 비-조직 배양물 처리된 6웰 디쉬에 옮기고 EdU(클릭-잇(Click-iT)® EdU 키트, 라이프 테크놀로지즈 코포레이션, 미국 캘리포니아주 칼스배드 소재)와 함께 1시간 동안 인큐베이션하였다. 이어서, EdU 인큐베이션된 세포를 분화 개시 후 0, 6, 24, 30, 48, 또는 72시간째에 유세포측정법에 의해 검정하여 세포 주기의 G0/G1, S, 또는 G2/M기에서의 세포의 백분율을 측정하였다(도 81 내지 도 87).At 5 hours, 23, 29, 47, or 71 hours after the initiation of differentiation and at the onset of differentiation (referred to as "0 hour"), the suspended sample was transferred to a 6 well dish move EdU - incubated for 1 hour (with click-It (click-iT) ® EdU kit, Life Technologies Corp., Carlsbad, Calif.). Then, EdU incubated cells were assayed by flow cytometry at 0, 6, 24, 30, 48, or 72 hours after the onset of differentiation to determine the percentage of cells in the G0 / G1, S, or G2 / (Fig. 81 to Fig. 87).
이 프로토콜 후에, 세포 주기의 G0/G1, S, 또는 G2/M기에서 세포의 백분율에 있어서의 유의한 차이가 관찰되었으며(도 82 내지 도 87), MCX 및 MCX+GDF8 처리된 세포는 다른 4가지 처리 조건과 대비하여 EdU의 혼입 시에 거의 40% 감소를 가짐이 주목되었다(도 81). EdU 혼입에 있어서의 이러한 감소는 MCX+GDF8 처리된 샘플로부터의 G0/G1 세포에 있어서의 38% 증가에 의해 그리고 MCX 단독 처리된 세포에 대한 G0/G1 세포에 있어서의 54% 증가에 의해 매칭되었다. EdU 혼입에 대한 이러한 변화 및 분화 개시 후 6시간째에 G0/G1로의 증가된 전이는 GDF8, WNT3A, WNT-3A + 액티빈 A, 또는 순수 배지로 처리된 세포에서는 관찰되지 않았다. 오히려, GDF8, WNT-3A, WNT-3A + 액티빈 A, 또는 순수 배지로 처리된 세포는 EdU 혼입을 갖는 세포의 백분율에 있어서의 최소한의 감소(평균, 48.1%, SD±1.2) 및 분화 개시 후 6시간째에 G0/G1에서의 세포수에 있어서의 평균 13% 감소(표준편차, ± 5%)를 보여주었는데, 이는 도 81 및 도 82에 나타낸 바와 같다.After this protocol, a significant difference in the percentage of cells in the G0 / G1, S, or G2 / M phase of the cell cycle was observed (Figures 82-87), and MCX and MCX + It was noted that EdU incorporation resulted in a reduction of approximately 40% in comparison with the branching conditions (Fig. 81). This reduction in EdU incorporation was matched by 38% increase in G0 / G1 cells from MCX + GDF8 treated samples and by 54% increase in G0 / G1 cells on MCX alone treated cells . These changes to EdU incorporation and increased transduction to G0 / G1 at 6 hours after initiation of differentiation were not observed in cells treated with GDF8, WNT3A, WNT-3A + actin A, or pure media. Rather, cells treated with GDF8, WNT-3A, WNT-3A + actin A, or pure media showed a minimal decrease in the percentage of cells with EdU incorporation (mean, 48.1%, SD +/- 1.2) (Standard deviation, ± 5%) in the number of cells at G0 / G1 at 6 hours post-treatment, as shown in FIGS. 81 and 82.
다른 처리 조건과 대비하여 MCX 또는 MCX+GDF8로 처리된 세포의 경우 G0/G1 값 사이에서 유사한 차이가 연장 시 이 과정에서 나중에 관찰되었다. 0시간째 후 30시간째에, MCX 또는 MCX+GDF8 처리된 세포는 WNT-3A + 액티빈 A, GDF8, WNT-3A, 또는 순수 배지로 처리된 세포와 대비하여 G0/G1에서 43 내지 45% 더 적은 세포를 가졌다. MCX 또는 MCX+GDF8로 처리된 세포의 71.9 내지 75.5%가 세포 주기의 G0/G1에서 존재하였으며, 한편 GDF8 처리된 세포의 48.5%, WNT3A 처리된 세포의 55.8%, WNT-3A + 액티빈 A 처리된 세포의 57.7%, 또는 순수 배지 처리된 세포의 49%가 G0/G1에서 존재한 바와 같이, G0/G1 세포들의 백분율 사이의 이러한 갭은 분화 개시 후 48시간째에 유지되었다. EDU 혼입 및 G0/G1 프로파일에 있어서 관찰된 차이 외에, MCX 또는 MCX+GDF8 처리된 세포는 WNT3A + 액티빈 A, GDF8, WNT-3A, 또는 순수 배지 처리된 세포와 비교할 때 0시간째 후 30 및 48시간째에 세포 주기의 S기에서 15 내지 33% 더 많은 세포를 가졌다(도 84 및 도 85).For cells treated with MCX or MCX + GDF8 as opposed to other treatment conditions, a similar difference between G0 / G1 values was observed later in the course of the prolongation. Cells treated with MCX or MCX + GDF8 at
데이터(CD99, CD9, CDH1, CDH2, CDX2, CER1, CXCR4, FGF17, FGF4, FOXA2, GATA4, GATA6, GSC, KIT, MIXL1, MNX1, NANOG, OTX2, POU5F1, SOX17, SOX7, 및 T에 대한 유전자 발현, 도 57 내지 도 80 및 도 88a 내지 도 88f에 나타냄)는, 현탁 배양물에서, 분화의 1일째에 TGF-β 패밀리 구성원인 GDF8과 함께 또는 GDF8 없이 MCX를 첨가함으로써, 완성 내배엽 형성의 말기에 유전자 발현에 의해 측정하였을 때, 세포를 1일째에 20 ng/ml WNT-3A + 100 ng/ml 액티빈 A로 처리하여 수득된 것과 비견될 정도로 완성 내배엽을 생성하였음을 나타내었다. 그러나, 완성 내배엽을 형성하는 과정에 걸쳐 관찰된 세포 주기에 있어서의 차이와 일치하여, 유전자 발현에 있어서의 중간 차이가 관찰되었다. MCX 또는 MCX + GDF8로 처리된 샘플에서는, 분화의 처음 24시간 내에 WNT-3A + 액티빈 A로 처리된 세포 또는 다른 3가지 시험 조건으로 처리된 세포보다 실질적으로 더 높은 수준으로 유전자 T(단미증), GATA4, 및 CDX2를 유도하였다(도 88b, 도 88c, 및 도 88d). 역으로, 만능성(NANOG 및 POU5F1/OCT4)에 대한 유전자 발현은 개시 세포 집단 또는 시험한 다른 4가지 조건과 대비하여 MCX 또는 MCX + GDF8로 처리된 샘플에서 24시간까지 현저히 감소하였다(도 88e). FGF4, FOXA2, 및 SOX17과 같은 유전자에 대한 발현의 유도의 크기는 분화 개시 후 24시간째에 시험된 다른 4가지 조건과 대비하여 MCX 또는 MCX + GDF8 샘플에서 훨씬 더 낮았지만, 48시간까지 모든 샘플은 비견되는 수준으로 FGF4, FOXA2, 및 SOX17을 발현하였다(도 88c 및 도88e).Gene expression for CD99, CD9, CDH1, CDH2, CDX2, CER1, CXCR4, FGF17, FGF4, FOXA2, GATA4, GATA6, GSC, KIT, MIXL1, MNX1, NANOG, OTX2, POU5F1, SOX17, SOX7, , Figures 57-80 and 88A-88F) show that in suspension cultures, the addition of MCX with GDF8, a member of the TGF-? Family on the first day of differentiation, or MCX without GDF8, As measured by gene expression, the cells produced complete endoderm that was comparable to that obtained by treatment with 20 ng / ml WNT-3A + 100 ng / ml Actin A on
실시예 16Example 16
스케일 조정가능한 현탁 분화 과정을 사용한 외배엽 및 중배엽 조직의 생성Generation of ectodermal and mesodermal tissue using a scale-tunable suspension differentiation process
이 실시예는 만능 줄기세포(PSC)를 증폭 및 분화시켜, 외배엽 또는 중배엽 조직의 생성을 위한 스케일 조정가능한 제조 과정을 달성할 수 있는 과정을 보여준다.This example demonstrates the process of amplifying and differentiating pluripotent stem cells (PSCs) to achieve a scalable manufacturing process for the production of ectodermal or mesodermal tissue.
2가지 세포주를 현탁 증폭시켜 이들 연구를 위한 시드 물질을 제공하였다: H1(WA01) hES 세포주의 서브-클론 - WB0106 및 제대 조직 세포(UTC)로부터 생성된 유도 만능 줄기세포(iPSC)주. 앞서의 실시예에서 기술된 바와 같이, 현탁 증폭된 세포를 프로그램화 동결기 내에서 고밀도로 동결시키고, 이어서 해동시켜 폐쇄된 3 리터 유리 생물반응기(다스깁; 독일 율리히 소재) 또는 사용 후 버리는 3 리터 일회용 생물반응기(모비우스(Mobius)®, 이엠디 밀리포어 코포레이션(EMD Millipore Corporation), 미국 매사추세츠주 빌레리카 소재)에 0.225 × 106개 세포/mL의 최종 세포 농도로 접종하였다. 교반 탱크 생물반응기 내로 접종된 세포는 연속 교반 탱크 내에서 세포 클러스터를 형성하였으며, 총 3일 동안 반응기 내의 만능성 배지(0.5% BSA로 보충된 E8™) 중에서 유지하였다. 접종 후 72시간째에, 플라스틱 일회용 삼각 플라스크(PETG 125 mL 플라스크, 카탈로그 번호 4112, 서모 사이언티픽(Thermo Scientific), 미국 뉴욕주 로체스터 소재)에, 이들 각각의 분화 배지(표 19) 중에 세포 클러스터를 옮겨서 중배엽/심장 조직(1) 또는 외배엽/신경 조직(2)을 형성함으로써 만능 세포 분화를 개시하였다.Two cell lines were suspensively amplified to provide seed material for these studies: induced pluripotent stem cells (iPSC) produced from sub-clone-WB0106 and cord tissue cells (UTC) of the H1 (WA01) hES cell line. As described in the previous examples, the suspension-amplified cells were frozen at high density in a programmable freezer and then thawed to yield a closed 3 liter glass bioreactor (Das Gibb; liter disposable bioreactor (Mobius (Mobius) ®, EME di Millipore Corporation (EMD Millipore Corporation), Massachusetts Ville silica material) 0.225 × 10 was inoculated in 6 cells / mL final concentration of cells on. Cells inoculated into a stirred tank bioreactor formed cell clusters in a continuous stirred tank and maintained in universal media (E8 (TM) supplemented with 0.5% BSA) in the reactor for a total of 3 days. At 72 hours post-inoculation, cell clusters were grown in plastic disposable Erlenmeyer flasks (
일단 단계적 분화 과정이 개시되면, 가습된 5% CO2 인큐베이터 내의 진탕기 플랫폼(MAXQ 416hp, 서모 사이언티픽, 미국 뉴욕주 로체스터 소재) 상에서 100 rpm으로 10일 동안 세포를 유지하였다. 분화 개시 후 1일째, 3일째, 5일째 및 7일째에, 플라스크 내의 배지를 표 19에 기재된 바와 같이 제조된 새로운 배지로 교체하였다. qRT-PCR 샘플을 분화 개시 전에 참조용으로 취한 후 분화 개시 후 3, 5, 7, 및 10일째에 취하였다.Once the staged differentiation process was initiated, the cells were maintained for 10 days at 100 rpm on a shaker platform (MAXQ 416 hp, Thermo Scientific, Rochester, NY) in a humidified 5% CO 2 incubator. On
mRNA 발현 패턴에 있어서의 외배엽 또는 중배엽 특이적인 변화가 qRT-PCR에 의해 검출될 수 있는지를 판단하기 위하여, 만능성, 완성 내배엽(DE), 및 6기(S6)로 지정된 3개의 어플라이드 바이오시스템즈 저밀도 어레이(라이프™, 미국 캘리포니아주 칼스배드 소재)를 사용하였으며, 그 결과를 발현을 표준화하기 위해 대조군으로서의 적절한 미분화된 만능 줄기세포 샘플과 대비하였다.To determine whether ectodermal or mesodermal-specific changes in the mRNA expression pattern could be detected by qRT-PCR, three Applied Biosystems low-density (DE) and six (S6) (Life < (R) >, Carlsbad, Calif., USA) was used and the results compared with the appropriate undifferentiated pluripotent stem cell sample as a control to normalize expression.
이들 어레이를 사용하여, 외배엽(도 89) 또는 중배엽(도 90) 분화 배지 중에서 배양된 만능 세포의 유전자 발현 패턴을 결정하였다. 어떠한 조건 하에서든 진탕 플라스크 내에서 분화된 세포는 만능성 어레이에 의해 측정하였을 때 3일째 내지 10일째의 연장된 배양에 걸쳐 NANOG, POU5F1/OCT4, TDGF1, 및 ZFP42와 같은 만능성 유전자에 대한 감소된 만능성 유전자 발현을 보여준 것으로 관찰되었다. CXCR4의 발현은 외배엽 또는 중배엽으로 분화된 hES 또는 iPS 세포로부터의 샘플에서 증가하였다. 이들 결과는 분화에 특징적인 유전자의 고 발현을 나타내는 qRT-PCR 데이터와 상관되었다. 외배엽 분화 배지로 처리된 세포는 분화 개시 후 3 내지 10일째에 qRT-PCR에 의해 증가된 수준의 ARX, NEUROD, NKX6.1, PAX6(100배 초과), 및 ZIC1(1000배 초과)을 발현하였다(도 91). 이들 데이터는 FACS 어레이에 의해 확인되었는데, FACS 어레이는 외배엽 운명으로의 분화의 개시를 시작한 후 3일째에, iPSC 및 hES 세포 둘 모두는 SOX2(만능성 및 신경 줄기세포 둘 모두에 필요한 유전자)의 고 발현을 유지하였지만, POU5F1/OCT4(만능성에 필요한 유전자)의 발현을 상실하였으며, 한편 PAX6 발현(신경 및 내분비 분화의 유전자)은 획득하였음을 보여주었다(도 92).These arrays were used to determine gene expression patterns of pluripotent cells cultured in ectoderm (FIG. 89) or mesodermal (FIG. 90) differentiation medium. Cells differentiated in a shake flask under any condition were observed for a reduced number of allelic genes such as NANOG, POU5F1 / OCT4, TDGF1, and ZFP42 over extended cultures from
중배엽 분화 배지로 처리된 세포에서 분화의 유사한 동태(kinetics)가 또한 관찰되었다. 만능 유전자 발현이 10일의 분화 과정에 걸쳐 하락함에 따라(도 90), 3일째에 조기의 과도적 중배엽 운명에 특징적인 유전자(CER1, EOMES, CKIT, 및 VWF)에 대해 조기 유도가 관찰되었으며, 이들 유전자 발현 수준은 10일째에 거의 베이스라인까지 감소하였다(도 93). 분화 개시 후 3, 5, 7 및 10일째에 특징적인 중배엽 유전자의 발현이 조기에 증가하는 유전자 발현(도 93에서 CDH2, CDX2, GATA6, HNF4α, MNX1, PRDM1 및 SOX17)을 나타낸 것으로 또한 관찰되었다. 유전자 유도의 동일한 패턴이 iPS 및 hES 세포 샘플 둘 모두에서 관찰되었는데, 이는 분화 과정이 유도되었으며 본질적으로 자발적이지 않았음을 나타낸다.Similar kinetics of differentiation in cells treated with mesodermal differentiation medium were also observed. Early induction of genes (CER1, EOMES, CKIT, and VWF) characteristic of early transient mesodermal fate on the third day was observed as the expression of universal genes fell throughout the 10 day differentiation process (Fig. 90) These gene expression levels decreased to almost the baseline at day 10 (Figure 93). (CDH2, CDX2, GATA6, HNF4 ?, MNX1, PRDM1 and SOX17 in Fig. 93) that express characteristic mesodermal gene expression on
qRT-PCR에 의해 관찰된 유전자 발현에 있어서의 이들 변화는 위상차 현미경법에 의해 관찰되고 클러스터의 동결-단면을 면역염색한 결과와 상관되었다. 중배엽 분화된 현탁 배양물에서 10일째까지, 10개의 클러스터 중 대략 1개가 자발적으로 "억제(beat)"되기 시작하였는데, 이는, 세포가 심근 조직으로 분화되었음을 시사한다(도 94, 좌측 패널, 10일째, 백색 막대). 일부 클러스터의 염색된 단면은 근육 형성을 나타내는, 줄무늬 모양의 말단에서 말단까지의 β-투불린 염색 패턴을 나타내었다(도 94, 우측 패널).These changes in gene expression observed by qRT-PCR were observed by phase-contrast microscopy and correlated with the results of immunostaining of the frozen sections of the clusters. By
두드러지게 상이한 형태학적 패턴이, 중배엽으로 분화된 클러스터와 대비하여, 외배엽 운명으로 분화된 클러스터(도 95, 좌측 패널)에 대해 관찰되었다(도 94). 외배엽 분화 전체에 걸친 클러스터는 중배엽 운명으로 분화된 세포보다 더 크고 조밀하며, 외배엽 분화된 세포는 더 적은 총 β 투불린을 발현하였다. β 투불린을 발현하지 않은 세포들은 신경에 특징적인, 더 수지상인 염색 패턴(도 95, 우측 패널, 백색 화살표)을 나타내었다.A distinctly different morphological pattern was observed for clusters differentiated into ectodermal fates (Figure 95, left panel), as opposed to clusters differentiated into mesoderm (Figure 94). The clusters over the entire ectodermal differentiation were larger and denser than the cells differentiated into the mesodermal fate, and the ectodermal differentiated cells expressed less total β-tubulin. Cells that did not express beta tubulin exhibited a more dendritic staining pattern (Figure 95, right panel, white arrow) characteristic of nerves.
qRT-PCR 및 FACS 데이터와 조합하여, 이들 결과는 현탁 상태로 뱅킹(banking)되어 증폭된 세포가 유도 및 재현가능한 방식으로 중배엽 또는 외배엽 운명으로 현탁 배양물 중에서 분화될 수 있음을 나타낸다.In combination with qRT-PCR and FACS data, these results indicate that the cells can be bankaged in suspension to allow the amplified cells to differentiate in suspension cultures with mesodermal or ectodermal fate in a derivatized and reproducible manner.
[표 19][Table 19]
[표 20][Table 20]
본 발명을 다양한 특정한 재료, 절차 및 실시예를 참고로 하여 본 명세서에서 설명하고 예시하였지만, 본 발명은 그러한 목적을 위해 선택된 재료 및 절차의 특정한 조합에 제한되지 않음이 이해된다. 당업자에 의해 인지되는 바와 같이, 이러한 상세 사항에 대한 다양한 변화가 암시될 수 있다. 본 명세서 및 실시예는 단지 예시적인 것으로 간주되는 것으로 의도되며, 이때 본 발명의 진정한 범주 및 사상은 하기 청구범위에 의해 나타난다. 본 출원에서 언급되는 모든 참고문헌, 특허 및 특허 출원은 전체적으로 본 명세서에 참고로 포함된다.Although the present invention has been described and illustrated herein with reference to various specific materials, procedures and embodiments, it is understood that the invention is not limited to any particular combination of materials and procedures selected for that purpose. As will be appreciated by those skilled in the art, various changes to these details may be implied. It is intended that the specification and examples be considered as exemplary only, with a true scope and spirit of the invention being indicated by the following claims. All references, patents, and patent applications mentioned in this application are incorporated herein by reference in their entirety.
Claims (21)
평면 부착성 배양물(planar adherent culture) 중에서 만능 세포를 응집된 세포 클러스터로 배양하는 단계, 및
만능 세포 클러스터를 동적 교반 현탁 배양 시스템 내에서 분화시키는 단계를 포함하며,
상기 분화시키는 단계는 Cyp26 억제제의 사용을 포함하는, 방법.As a method for expanding and differentiating pluripotent cells in a dynamically agitated suspension culture system,
Culturing pluripotent cells in a planar adherent culture into an aggregated cell cluster, and
Dividing the universal cell cluster in a dynamic stirred suspension culture system,
Wherein the differentiating step comprises the use of a Cyp26 inhibitor.
약 0.1% 내지 약 2%의 소혈청 알부민을 포함하는 환경에서 평면 부착성 배양물 중에서 만능 세포를 응집된 세포 클러스터로 증폭시키는 단계,
상기 평면 부착성 배양물로부터의 만능 줄기세포의 클러스터를 동적 현탁액에 옮기는 단계, 및
상기 동적 현탁액 중의 세포를 소분자 및 선택적으로 TGFβ 패밀리 구성원으로 보충된 배지 중에서 배양하는 단계를 포함하는, 방법.As a method for increasing the percentage of cells in the G0 / G1 phase of the cell cycle,
Amplifying the pluripotent cells into a clustered cell cluster in a flat adherent culture in an environment comprising from about 0.1% to about 2% bovine serum albumin,
Transferring clusters of pluripotent stem cells from said flat adherent cultures to a dynamic suspension, and
Culturing the cells in the dynamic suspension in a medium supplemented with small molecules and optionally a TGF beta family member.
약 0.1% 내지 약 2%의 소혈청 알부민을 포함하는 환경에서 평면 부착성 배양물 중에서 만능 세포를 응집된 세포 클러스터로 증폭시키는 단계,
상기 평면 부착성 배양물로부터의 만능 줄기세포의 클러스터를 동적 현탁액에 옮기는 단계, 및
상기 동적 현탁액 중의 세포를 MCX 및 GDF8 또는 WNT3A 및 액티빈 A로 보충된 배지 중에서 배양하는 단계를 포함하는, 방법.As a method for differentiating pluripotent cells into complete endoderm,
Amplifying the pluripotent cells into a clustered cell cluster in a flat adherent culture in an environment comprising from about 0.1% to about 2% bovine serum albumin,
Transferring clusters of pluripotent stem cells from said flat adherent cultures to a dynamic suspension, and
Culturing the cells in the dynamic suspension in a medium supplemented with MCX and GDF8 or WNT3A and actin A.
평면 부착성 배양물 중에서 만능 줄기세포를 응집된 세포 클러스터로 증폭시키는 단계,
상기 평면 부착성 배양물로부터의 만능 줄기세포의 클러스터를 동적 현탁액에 옮기는 단계, 및
동적 교반 현탁 배양 시스템 내에서 상기 만능 세포 클러스터를 분화시키는 단계를 포함하며,
상기 세포는 약 0.1% 내지 약 2%의 소혈청 알부민을 포함하는 환경에서 응집된 세포 클러스터로 증폭되는, 방법.A method of amplifying and differentiating pluripotent stem cells in a dynamic stirred suspension culture system,
Amplifying pluripotent stem cells into clusters of cell clusters in a flat adherent culture,
Transferring clusters of pluripotent stem cells from said flat adherent cultures to a dynamic suspension, and
And dividing said universal cell cluster in a dynamic stirred suspension culture system,
Wherein said cells are amplified with agglutinated cell clusters in an environment comprising from about 0.1% to about 2% bovine serum albumin.
a. 약 0.1% 내지 약 2%의 소혈청 알부민을 포함하는 환경에서 평면 부착성 배양물 중에서 만능 세포를 응집된 세포 클러스터로 증폭시키는 단계,
b. 상기 평면 부착성 배양물로부터의 만능 세포 클러스터를 효소 또는 킬레이트제를 사용하여 동적 현탁 배양물(dynamic suspension culture)에 옮기는 단계,
c. 상기 세포 클러스터를 동적 교반 현탁 배양 시스템 내에서 유지하는 단계, 및
d. 상기 만능 세포 클러스터를 동적 교반 현탁 배양 시스템 내에서 분화시켜, 췌장 전구세포 집단, 신경 전구세포 집단 또는 심근세포 전구체 집단을 생성하는 단계를 포함하며,
분화 환경은 대략 저산소 내지 주위의 약 30% 범위의 산소, 0.1% 내지 약 2% 범위의 지질, 또는 이들의 조합을 포함하는, 방법.A method of amplifying and differentiating pluripotent cells in a dynamic stirred suspension culture system,
a. Amplifying the pluripotent cells into a clustered cell cluster in a flat adherent culture in an environment comprising from about 0.1% to about 2% bovine serum albumin,
b. Transferring the universal cell clusters from the planar adherent cultures to a dynamic suspension culture using an enzyme or a chelating agent,
c. Maintaining said cell clusters in a dynamic stirred suspension culture system, and
d. Differentiating the universal cell clusters in a dynamic stirred suspension culture system to produce a population of pancreatic progenitor cells, a population of neural progenitor cells or a population of myocardial cell precursors,
Wherein the differentiation environment comprises from about oxygen to about 30% oxygen, from about 0.1% to about 2% lipid, or a combination thereof.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361962158P | 2013-11-01 | 2013-11-01 | |
| US61/962,158 | 2013-11-01 | ||
| US13/998,974 | 2013-12-30 | ||
| US13/998,974 US10377989B2 (en) | 2012-12-31 | 2013-12-30 | Methods for suspension cultures of human pluripotent stem cells |
| PCT/US2014/038993 WO2015065524A2 (en) | 2013-11-01 | 2014-05-21 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187034291A Division KR20180128529A (en) | 2013-11-01 | 2014-05-21 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20160079072A true KR20160079072A (en) | 2016-07-05 |
Family
ID=53004904
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187034291A KR20180128529A (en) | 2013-11-01 | 2014-05-21 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
| KR1020167014409A KR20160079072A (en) | 2013-11-01 | 2014-05-21 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
| KR1020167014406A KR20160079071A (en) | 2013-11-01 | 2014-06-17 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
| KR1020187034483A KR20180130001A (en) | 2013-11-01 | 2014-06-17 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187034291A KR20180128529A (en) | 2013-11-01 | 2014-05-21 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020167014406A KR20160079071A (en) | 2013-11-01 | 2014-06-17 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
| KR1020187034483A KR20180130001A (en) | 2013-11-01 | 2014-06-17 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
Country Status (12)
| Country | Link |
|---|---|
| EP (2) | EP3063268A4 (en) |
| JP (2) | JP2016534731A (en) |
| KR (4) | KR20180128529A (en) |
| CN (2) | CN105793413A (en) |
| AU (4) | AU2014342995C1 (en) |
| BR (1) | BR112016009393A8 (en) |
| CA (2) | CA2928639A1 (en) |
| MX (2) | MX2016005657A (en) |
| PH (2) | PH12016500782A1 (en) |
| RU (2) | RU2689710C2 (en) |
| SG (2) | SG11201603045VA (en) |
| WO (2) | WO2015065524A2 (en) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20180128529A (en) * | 2013-11-01 | 2018-12-03 | 얀센 바이오테크 인코포레이티드 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
| US20190177687A1 (en) * | 2016-06-23 | 2019-06-13 | Tithon Biotech Inc. | Cells expressing parathyroid hormone 1 receptor and uses thereof |
| MX2019005476A (en) * | 2016-11-16 | 2019-07-04 | Cynata Therapeutics Ltd | Pluripotent stem cell assay. |
| US10391156B2 (en) | 2017-07-12 | 2019-08-27 | Viacyte, Inc. | University donor cells and related methods |
| CN111246864A (en) * | 2017-07-21 | 2020-06-05 | 森玛治疗公司 | Repopulation of Stem cell-derived pancreatic β cells |
| JP7000896B2 (en) * | 2017-08-23 | 2022-01-19 | 王子ホールディングス株式会社 | Cell sheet forming member, method for manufacturing cell sheet forming member, and method for manufacturing cell sheet |
| CN111836886A (en) * | 2018-01-05 | 2020-10-27 | 血小板生源说股份有限公司 | Compositions and methods for producing megakaryocytes |
| US12104173B2 (en) | 2018-01-18 | 2024-10-01 | Agency For Science, Technology And Research | Method for differentiation of human pluripotent stem cell lines in suspension culture |
| KR102115360B1 (en) * | 2018-05-30 | 2020-05-26 | 주식회사 바이블리오테카 | Adult stem cell culture fluid and a producing method thereof |
| US10724052B2 (en) | 2018-09-07 | 2020-07-28 | Crispr Therapeutics Ag | Universal donor cells |
| WO2020243663A1 (en) | 2019-05-31 | 2020-12-03 | W. L. Gore & Associates, Inc. | A biocompatible membrane composite |
| EP3975925A1 (en) | 2019-05-31 | 2022-04-06 | W.L. Gore & Associates, Inc. | A biocompatible membrane composite |
| WO2020243666A1 (en) | 2019-05-31 | 2020-12-03 | W. L. Gore & Associates, Inc. | A biocompatible membrane composite |
| EP3976237A1 (en) | 2019-05-31 | 2022-04-06 | W.L. Gore & Associates Inc. | Cell encapsulation devices with controlled oxygen diffusion distances |
| CN114364791A (en) | 2019-09-05 | 2022-04-15 | 克里斯珀医疗股份公司 | Universal donor cell |
| CN114375300A (en) | 2019-09-05 | 2022-04-19 | 克里斯珀医疗股份公司 | Universal donor cell |
| WO2021099532A1 (en) * | 2019-11-22 | 2021-05-27 | Novo Nordisk A/S | Spin-aggregated neural microspheres and the application thereof |
| EP4271795A1 (en) | 2020-12-31 | 2023-11-08 | CRISPR Therapeutics AG | Universal donor cells |
| WO2022203051A1 (en) * | 2021-03-25 | 2022-09-29 | 株式会社カネカ | Method for producing pluripotent stem cell population |
| CN116218766A (en) * | 2023-04-21 | 2023-06-06 | 北京意胜生物科技有限公司 | Method for preparing pancreatic precursor cells, culture medium and application of pancreatic precursor cells |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20110029155A (en) * | 2008-06-30 | 2011-03-22 | 센토코 오르토 바이오테크 인코포레이티드 | Differentiation of pluripotent stem cells |
| KR20120039025A (en) * | 2009-08-12 | 2012-04-24 | 고쿠리츠 다이가쿠 호진 교토 다이가쿠 | Method for inducing differentiation of pluripotent stem cells into neural precursor cells |
| WO2013056072A1 (en) * | 2011-10-13 | 2013-04-18 | Wisconsin Alumni Research Foundation | Generation of cardiomyocytes from human pluripotent stem cells |
| US20130189777A1 (en) * | 2011-12-22 | 2013-07-25 | Janssen Biotech, Inc. | Differentiation of Human Embryonic Stem Cells into Single Hormonal Insulin Positive Cells |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL374557A1 (en) * | 2001-11-09 | 2005-10-31 | Artecel Sciences, Inc. | Endocrine pancreas differentiation of adipose tissue-derived stromal cells and uses thereof |
| EP3441459B1 (en) * | 2006-08-02 | 2021-03-17 | Technion Research & Development Foundation Limited | Methods of expanding embryonic stem cells in a suspension culture |
| WO2008056779A1 (en) * | 2006-11-09 | 2008-05-15 | Japan As Represented By The President Of International Medical Center Of Japan | Method for culture and passage of primate embryonic stem cell, and method for induction of differentiation of the embryonic stem cell |
| US20090053182A1 (en) * | 2007-05-25 | 2009-02-26 | Medistem Laboratories, Inc. | Endometrial stem cells and methods of making and using same |
| MX2010000348A (en) * | 2007-07-01 | 2010-04-12 | Lifescan Inc | Single pluripotent stem cell culture. |
| GB0800524D0 (en) * | 2008-01-14 | 2008-02-20 | Univ Brighton | Cell culture system |
| SG188918A1 (en) * | 2008-03-17 | 2013-04-30 | Agency Science Tech & Res | |
| US8008075B2 (en) * | 2008-11-04 | 2011-08-30 | Viacyte, Inc. | Stem cell aggregate suspension compositions and methods of differentiation thereof |
| US8895300B2 (en) * | 2008-11-04 | 2014-11-25 | Viacyte, Inc. | Scalable primate pluripotent stem cell aggregate suspension culture and differentiation thereof |
| EP2582795B1 (en) * | 2010-06-15 | 2017-04-12 | Kyoto University | Method for selecting human induced pluripotent stem cells |
| WO2011160066A1 (en) * | 2010-06-17 | 2011-12-22 | Regents Of The University Of Minnesota | Production of insulin producing cells |
| PL2611910T3 (en) * | 2010-08-31 | 2018-06-29 | Janssen Biotech, Inc | Differentiation of human embryonic stem cells |
| MY177150A (en) * | 2011-02-28 | 2020-09-08 | Stempeutics Res Malaysia Sdn Bhd | Isolation and expansion of adult stem cells, their therapeutic composition and uses thereof |
| US10519422B2 (en) * | 2012-02-29 | 2019-12-31 | Riken | Method of producing human retinal pigment epithelial cells |
| CN105705634A (en) * | 2012-12-31 | 2016-06-22 | 詹森生物科技公司 | Suspension and clustering of human pluripotent cells for differentiation into pancreatic endocrine cells |
| KR20180128529A (en) * | 2013-11-01 | 2018-12-03 | 얀센 바이오테크 인코포레이티드 | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells |
-
2014
- 2014-05-21 KR KR1020187034291A patent/KR20180128529A/en active IP Right Grant
- 2014-05-21 WO PCT/US2014/038993 patent/WO2015065524A2/en active Application Filing
- 2014-05-21 EP EP14857034.4A patent/EP3063268A4/en not_active Withdrawn
- 2014-05-21 SG SG11201603045VA patent/SG11201603045VA/en unknown
- 2014-05-21 CA CA2928639A patent/CA2928639A1/en not_active Abandoned
- 2014-05-21 CN CN201480059910.5A patent/CN105793413A/en active Pending
- 2014-05-21 MX MX2016005657A patent/MX2016005657A/en unknown
- 2014-05-21 RU RU2016121409A patent/RU2689710C2/en active
- 2014-05-21 JP JP2016527338A patent/JP2016534731A/en active Pending
- 2014-05-21 AU AU2014342995A patent/AU2014342995C1/en not_active Ceased
- 2014-05-21 KR KR1020167014409A patent/KR20160079072A/en active Application Filing
- 2014-06-17 AU AU2014343007A patent/AU2014343007C1/en not_active Ceased
- 2014-06-17 KR KR1020167014406A patent/KR20160079071A/en active IP Right Grant
- 2014-06-17 BR BR112016009393A patent/BR112016009393A8/en not_active Application Discontinuation
- 2014-06-17 JP JP2016527450A patent/JP2017500013A/en active Pending
- 2014-06-17 CN CN201480059902.0A patent/CN105683362A/en active Pending
- 2014-06-17 CA CA2928741A patent/CA2928741A1/en not_active Abandoned
- 2014-06-17 KR KR1020187034483A patent/KR20180130001A/en not_active Application Discontinuation
- 2014-06-17 SG SG11201603047PA patent/SG11201603047PA/en unknown
- 2014-06-17 MX MX2016005658A patent/MX2016005658A/en unknown
- 2014-06-17 EP EP14859059.9A patent/EP3063269A4/en not_active Withdrawn
- 2014-06-17 RU RU2016121404A patent/RU2016121404A/en not_active Application Discontinuation
- 2014-06-17 WO PCT/US2014/042796 patent/WO2015065537A1/en active Application Filing
-
2016
- 2016-04-27 PH PH12016500782A patent/PH12016500782A1/en unknown
- 2016-04-27 PH PH12016500783A patent/PH12016500783A1/en unknown
-
2018
- 2018-07-26 AU AU2018208717A patent/AU2018208717A1/en not_active Abandoned
- 2018-07-26 AU AU2018208707A patent/AU2018208707A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20110029155A (en) * | 2008-06-30 | 2011-03-22 | 센토코 오르토 바이오테크 인코포레이티드 | Differentiation of pluripotent stem cells |
| KR20120039025A (en) * | 2009-08-12 | 2012-04-24 | 고쿠리츠 다이가쿠 호진 교토 다이가쿠 | Method for inducing differentiation of pluripotent stem cells into neural precursor cells |
| WO2013056072A1 (en) * | 2011-10-13 | 2013-04-18 | Wisconsin Alumni Research Foundation | Generation of cardiomyocytes from human pluripotent stem cells |
| US20130189777A1 (en) * | 2011-12-22 | 2013-07-25 | Janssen Biotech, Inc. | Differentiation of Human Embryonic Stem Cells into Single Hormonal Insulin Positive Cells |
Non-Patent Citations (4)
| Title |
|---|
| Nat Protoc., 2012, Vol. 6(8), p. 1229-1240 * |
| Nat Protoc., 2012, Vol. 6(8), p. 1229-1240 (2012.09.04.) * |
| PLoS ONE, 2012, Vol. 7(5), e37004, p.1-17 * |
| Regen. Med., 2012, Vol. 7(1), p. 71?84 * |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2687379C2 (en) | Suspending and clustering of human pluripotent cells with the purpose of their differentiation in pancreatic endocrine cells | |
| KR20160079072A (en) | Suspension and clustering of human pluripotent stem cells for differentiation into pancreatic endocrine cells | |
| KR102519502B1 (en) | Suspension culturing of pluripotent stem cells | |
| US10370644B2 (en) | Method for making human pluripotent suspension cultures and cells derived therefrom |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AMND | Amendment | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| E601 | Decision to refuse application | ||
| E801 | Decision on dismissal of amendment | ||
| A107 | Divisional application of patent |