KR100632429B1 - 프라이머 특이성 유무에 의한 멀티플렉스 역전사 중합효소연쇄반응을 이용한 재조합 독감 바이러스의 스크리닝 방법 - Google Patents
프라이머 특이성 유무에 의한 멀티플렉스 역전사 중합효소연쇄반응을 이용한 재조합 독감 바이러스의 스크리닝 방법 Download PDFInfo
- Publication number
- KR100632429B1 KR100632429B1 KR1020030053534A KR20030053534A KR100632429B1 KR 100632429 B1 KR100632429 B1 KR 100632429B1 KR 1020030053534 A KR1020030053534 A KR 1020030053534A KR 20030053534 A KR20030053534 A KR 20030053534A KR 100632429 B1 KR100632429 B1 KR 100632429B1
- Authority
- KR
- South Korea
- Prior art keywords
- virus
- htca
- dna
- artificial sequence
- pcr
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/70—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving virus or bacteriophage
- C12Q1/701—Specific hybridization probes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/686—Polymerase chain reaction [PCR]
Abstract
본 발명은 재조합 독감 바이러스(influenza virus)를 제조하는 과정 중 프라이머(primer)와 주형간의 결합특이성에 따른 멀티플렉스 역전사 중합효소 연쇄반응(multiplex RT-PCR)의 차이를 이용하여 재조합 독감 바이러스(influenza virus)의 유전자를 스크리닝하는 방법에 관한 발명이다. 보다 상세하게는, 약독화 독감 바이러스주의 유전자와 독성 바이러스주의 대응하는 유전자의 염기서열 중 상호간의 변이가 많은 부분에 해당하는 프라이머를 제작하고 하나의 반응에서 2 내지 3개의 중합효소 연쇄반응이 동시에 진행되도록 함으로써 약독화 독감 바이러스주의 6개의 유전자와 독성바이러스의 2개의 유전자를 갖는 6:2 재조합 바이러스를 효과적으로 스크리닝하는 방법에 관한 발명이다.
독감 바이러스, 생백신, 멀티플렉스 역전사 PCR, 재조합 바이러스, 스크리닝
Description
도 1는 약독화 바이러스주 HTCA-A101의 8개 RNA 단편 중 PB2에 대하여 수행한 표 1에 기재된 PB2 프라이머 세트를 사용한 RT-PCR 결과를 나타낸다. 이때, 상단에 표시된 M은 분자량 마커를 나타내며, 레인 1번 내지 9번은 본 발명에 따른 PB2의 프라이머 세트 1 내지 9번을 의미하며, C는 포지티브 PB2 프라이머 세트를 나타낸다.
도 2는 네 종류의 독성 바이러스 [A/New Caledonia/20/99 (H1N1), A/Moscow/10/99 (H3N2), A/Beijing/262/95 (H1N1), A/Shangdong/9/93 (H3N2)]의 8개 RNA 단편 중 PB2에 대하여 표 1에 기재된 PB2 프라이머 세트를 사용한 수행한 RT-PCR 결과를 나타낸다. 이때, 상단의 숫자 및 문자는 도 1의 설명에서와 동일하다.
도 3은 두 종류의 독성 바이러스 [A/New Caledonia/20/99 (H1N1), A/Moscow/10/99 (H3N2)]와 약독화 바이러스주의 cDNA를 주형으로 하여 동일 조건에서 동시에 멀티플렉스 PCR을 수행한 결과를 나타낸다. 도 3의 A는 독성 바이러스 A/New Caledonia/20/99 (H1N1)에 대한 결과를 나타내며 이때, 상단에 표시된 M은 분자량 마커를 나타내며, 약독화 바이러스주의 8개 RNA 에 대한 결과는 레인 1은 PB2, PB1, NP, 레인 2 는 M, NS, PA, 레인 3 은 HA, NA 에 대한 프라이머 세트, 보다 구체적으로는 레인 1 은 PB2-2 (1002bp), NP-4 (853bp), PB1-6 (559bp), 레인 2 는 PA-5 (730bp), NS-5 (521bp), M-6 (326bp), 레인 3 은 HA-4 (1086bp), NA-4 (504 bp)를 사용한 결과이고, 레인 4 내지 6은 레인 1 내지 3에서 사용한 프라이머와 동일한 프라이머 세트를 사용한 결과를 나타내며, 레인 7 내지 14는 8개 RNA 각각에 대한 포지티브 대조군의 결과이며 이중 레인 13 및 14는 각각 A/New Caledonia/20/99 (H1N1)의 H1 아형 및 N1 아형에 특이적인 프라이머 세트를 사용한 결과이다. 도 3의 B는 독성 바이러스 A/Moscow/10/99 (H3N2)에 대한 결과를 나타내며 이때, 상단에 표시된 M은 분자량 마커를 나타내며, 약독화 바이러스주의 8개 RNA 에 대한 결과는 레인 1은 PB2, PB1, NP, 레인 2 는 M, NS, PA, 레인 3 은 HA, NA 에 대한 프라이머 세트, 보다 구체적으로는 레인 1 은 PB2-2 (1002bp), NP-4 (853bp), PB1-6 (559bp), 레인 2 는 PA-5 (730bp), NS-5 (521bp), M-6 (326bp), 레인 3 은 HA-4 (1086bp), NA-4 (504 bp)를 사용한 결과이고, 레인 4 내지 6은 레인 1 내지 3에서 사용한 프라이머와 동일한 프라이머 세트를 사용한 결과를 나타내며, 레인 7 내지 14는 8개 RNA 각각에 대한 포지티브 대조군의 결과이며 이중 레인 13 및 14는 각각 A/Moscow/10/99 (H3N2)의 H3 아형 및 N2 아형에 특이적인 프라이머 세트를 사용한 결과이다.
도 4는 독성 바이러스 A/New Caledonia/20/99 (H1N1)와 약독화 바이러스주를 하나의 수정란에 동시에 감염시켜 생장시킨 뒤 얻은 바이러스를 약독화 바이러스주에 대한 항체와 반응시킨 후 플라크 분리(plaque isolation)하여 얻은 바이러스를 본 발명의 방법으로 분석한 결과로, 4개의 레인이 하나의 바이러스를 분석한 것으로 레인 1 내지 3 은 8개 유전자 유래를 알기 위한 멀티플렉스 PCR이며 레인 4는 RNA 준비 과정과 RT-PCR 과정에서의 유전자의 존재유무를 보여주기 위한 포지티브 대조군(positive control)으로서 여덟 개 유전자 중에서 M(649bp)에 대하여 PCR을 수행한 결과이다. 레인 1 은 PB2, PB1, NP, 레인 2 는 M, NS, PA, 레인 3 HA, NA, 레인 4는 M 에 대한 프라이머 세트, 보다 구체적으로는 레인 1 은 PB2-2 (1002bp), NP-4 (853bp), PB1-6 (559bp), 레인 2는 PA-5 (730bp), NS-5 (521bp), M-6 (326bp), 레인 3는 HA-4 (1086bp), NA-4 (504bp), 레인 4는 Positive M (649bp)를 사용한 결과이다.
독감 바이러스의 감염에 의해 유발되는 독감은 상,하부 호흡기 증상과 함께 발열, 두통, 근육통과 무력감 등이 동반되는 급성호흡기 질환이다. 독감은 보통 겨울철에 발병하는데 유행되는 아형(subtype)에 따라 다양한 증상과 중증도를 나타내며, 전염력이 강하고 폐렴 및 심폐질환의 합병증을 일으켜 높은 치사율을 보일 수 있으므로, 노인이나 소아 뿐만 아니라 성인의 경우에도 독감백신의 접종이 적극 권장되고 있다.
독감 바이러스(influenza virus)는 올소믹소비리데 (Orthomyxoviridae)에 속하며 PB2, PB1, PA, HA, NP, NA, M 및 NS의 여덟 개의 네가티브 센스 RNA 단편을 갖고 있는 바이러스이다. 이 중 외피 단백질을 이루고 있는 두개의 단백질 헤마글루티닌 (hemagglutinin: 이하 "HA"라 약칭함)과 뉴라미니다아제 (neuraminidase: 이하 "NA"라 약칭함)는 면역항체를 유도하는 중요한 면역원이며, 이들은 항원의 대/소변이(antigenic shift and drift) 과정을 통해 변형되는 특징을 갖고 있다. 이런 독감 바이러스의 변화는 동일 아종내의 다른 독감 바이러스에 대하여 형성된 면역도 회피할 수 있게 할 수 있으며, 일반적으로 독감 바이러스에 의해 유도된 면역은 단기간에 소실되기 때문에 매 시즌에 유행이 예측되는 바이러스에 대하여 새로이 면역을 유도해야 한다.
독감백신의 경우, 세계보건기구(WHO)에서 유행을 예측하는 독감 바이러스주(A 형 두 종류와 B 형 한 종류)에 대해 제조된 불활화 백신이 일반적으로 사용되고 있다. 불활화 백신으로는 불활화한 독감 바이러스 전체를 사용하는 인플루엔자 백신과 독감 바이러스 입자를 항원성이 유지되도록 분쇄 및 불활화하여 제조한 인플루엔자 분할백신, 그리고 독감 바이러스의 헤마글루티닌만을 분리하여 제조한 인플루엔자 에이취 에이 백신의 세 종류가 많이 사용되고 있다. 이들 불활화 백신에 소요되는 바이러스는 수정란에서 배양되는 것이 일반적이며 최근에는 세포배양을 통해서 생산하는 연구도 활발히 진행되고 있다.
그러나, 세계보건기구(WHO)에서 유행을 예측하는 독감 바이러스주의 경우 수 정란에서의 증식력이 낮아 생산성이 높지 않은 경우가 있으므로, 생산성 향상을 위해 수정란에서 고생산성을 보이는 바이러스주와 재조합하여 바이러스의 표면 항원인 HA와 NA의 유전자 단편은 예측된 바이러스의 것을 포함하며 나머지 여섯 개의 내부 유전자 단편은 고생산성 바이러스주의 것을 포함하는 6:2 재조합 바이러스를 제조하여 수정란에서의 생산성을 높이는 방법이 오래 전부터 사용되어 왔다 (Influenza, Plenum Medical Book Company, 291, 1987).
불활화 백신은 젊은 성인의 경우 70 % 이상의 예방효과를 보이며, 호흡기질환에 의한 입원, 2차 감염인 폐렴 등에 의한 입원율을 감소시키는 효과가 있지만, 면역 지속기간이 짧으며 근육주사로 접종하고 바이러스의 초기 감염을 방어할 수 있는 점막분비항체(sIgA)를 유도할 수 없는 단점을 가지고 있다. 또한 감염된 세포를 사멸시킬 수 있는 CTL 면역이 잘 유도되지 못하는 한계를 가지고 있다.
불활화 백신이 가지는 이런 단점들을 보완하면서 면역력을 높이며 코점막을 통한 투여를 가능케하는 독감 생백신 개발이 여러 연구진에 의해서 시도되어 왔으며, 1965년 구소련에서의 저온적응된 약독화 바이러스주를 사용한 생백신 바이러스주의 개발을 시작으로 현재까지 많은 연구가 진행되고 있다 (Rev Roum Inframicrobiol 2, 179-89, 1965). 구소련의 경우, A/Leningrad/134/47/57(H2N2) 바이러스를 생백신의 공여 바이러스주로 하여 재조합 바이러스를 제조하여 개발하였으며, 미국에서는 A/Ann Arbor/6/60 (H2N2)를 공여바이러스주로 하여 제조한 재조합 바이러스주를 사용한 생백신이 임상실험을 끝내고 미국 FDA에서 49세 이하와 5세 이상에서 예방접종이 허가된 상태이다.
불활화 백신과 생백신의 경우, 백신의 생산성 또는 안정성의 확보를 위해 수정란에서 생산성이 높은 균주 또는 약독화된 바이러스주와의 재조합 바이러스 제조 과정이 필요하다. 재조합 독감 바이러스의 제조과정 중 독감 바이러스의 8개의 분절된 RNA 단편들의 조합은 무작위적으로 일어나기 때문에 생성될 수 있는 재조합 바이러스의 종류는 최대 28가지, 즉 256가지이다. 이들 바이러스 중 공여 바이러스의 약독화 특성을 갖고 있으면서 독성 바이러스의 외피 단백질인 HA와 NA를 가진 6:2 재조합 바이러스를 신속하게 효율적으로 선별하는 방법의 확립이 매우 중요하다.
6:2 재조합 바이러스를 제조하는 방법은 우선 독성 바이러스와 공여 바이러스를 일정 비율로 혼합한 후 11일간 발육한 수정란에 접종하고 저온에서 배양하여 무작위적인 조합으로 이루어진 재조합 바이러스를 얻는다. 이들 바이러스들 중 공여바이러스의 특성인 저온 적응성을 가진 바이러스와 독성 바이러스의 외피단백질을 갖는 바이러스만을 선별하기 위해서 저온 배양과 공여바이러스 특이 항체 존재하에 수정란에서의 계대배양을 수행한다. 공여바이러스 특이 항체 존재 하에서의 플라크 분리 (plaque isolation)을 통해 단일 바이러스 클론을 얻은 후 다시 수정란에서의 배양으로 바이러스를 증폭시킨다. 증폭된 바이러스의 HA와 NA는 항체를 이용한 헤마그루티닌 억제 분석법(hemagglutinin inhibition assay; 이하 "HI"라 약칭함)와 뉴라미니다제(neuraminidase inhibition assay; 이하 "NI"라 약칭함)를 통하여 빠른 분석이 가능하지만, 나머지 내부 유전자 6개의 경우에는 유전자 차원 에서의 분석이 수행되어져야만 한다.
재조합 독감 바이러스의 유전자를 RNA상에서 분석하는 방법으로는 PAGE (Polyacrylamide gel electrophoreses) 젤 상에서 RNA 서열의 차이에 의한 단일 가닥 RNA의 이동성의 차이를 비교하는 방법 (J. Virol. 29,1142-1148,1979)과 노던 블랏팅 (Northern bloting)과 크롯 분석 (Crot analysis: RNA-DNA hybridization) 방법이 사용되어져 왔다 (J. Gen. Virol. 64, 2611-2620, 1983: Vaccine 3, 267-273, 1985). 그러나, 이들 방법들은 분해되기 쉬운 RNA를 분석에 직접 사용하여야 하며 PAGE 젤을 사용하여 장시간 전개(running)해야 하는 번거로움이 존재하며, 젤 상에서의 유전자 이동의 차이로 유전자 염기 서열의 차이를 분석하기 때문에 불확실한 결과가 나오는 경우도 흔히 발견되었다.
이런 단점들을 보완하기 위해 역전사 중합효소 연쇄반응 (Reverse Transcriptation-Polymerase Chain Reaction; 이하 RT-PCR이라 약칭함)과 제한효소의 특이성을 조합하여 유전자를 분석하는 RFLP (Restriction Fragment Length Polymorphism) 등의 방법이 도입되기 시작하였다 (J. Virol. Methods 52, 41-49, 1995). 이들 RFLP 방법은 공여바이러스와 독성 바이러스의 게놈이 제한효소에 의해 절단되어 생기는 양상을 비교하는 방법으로 현재 가장 많이 쓰이고 있으나, 독감 바이러스의 여덟 개 RNA 게놈을 각각 분리하여 RT-PCR로 증폭한 후 절단효소로 반응을 수행해야 하며, 분석에 적당한 절단효소를 찾기 위해서 독성 바이러스의 염기서열을 먼저 분석해야 하고, 공여 바이러스와 독성 바이러스를 구분할 수 있는 적당한 절단효소를 찾는데 많은 시간이 소요되며, 절단효소가 인식하는 염기서열 부분에 변이가 생길 경우 결과가 불확실해지는 등의 단점이 있다.
또한, RT-PCR 방법은 상기 목적 외에 독감 바이러스의 검출, 서브유형(subtype)의 구별 등에 사용되어 왔으나, 재조합 바이러스의 스크리닝에 이를 도입하는 것은 공여 바이러스와 독성 바이러스의 효율적인 구별과 신속한 반응에 한계를 보여 왔다.
이에, 본 발명자들은 다수의 공여바이러스 특이 프라이머의 설계와 PCR 방법의 개선을 통해 다양한 조합으로 구성된 바이러스 중 생백신 바이러스로 사용될 수 있는 재조합 바이러스만을 빠른 시간에 분석하는 방법을 개발하게 되었으며, 2개 내지 4개의 유전자를 동일 반응에서 증폭시켜 실제 재조합 바이러스의 스크리닝에 응용하여 확인함으로써 본 발명을 완성하였다.
첫째, 본 발명은 저온적응 독감 바이러스 HTCA-A101 바이러스(수탁번호 : KCTC 0400 BP)와 A형 독성 바이러스와의 재조합 바이러스의 신속한 스크리닝에 필요한 올리고뉴클레오타이드 프라이머를 제공한다.
둘째, 본 발명은 상기 올리고뉴클레오타이드 프라이머 세트를 이용한 멀티플렉스 역전사 PCR 방법을 사용하여 재조합 바이러스를 스크리닝하는 방법을 제공한다.
공여 바이러스의 약독화 특성과 독성 바이러스의 외피 단백질을 갖는 재조합 바이러스를 제조하기 위해서는, 얻어진 재조합 바이러스들의 유전자를 분석하여 그 유래를 밝혀 공여 바이러스의 내부 유전자들과 독성 바이러스의 외피 단백질 유전자들을 포함하는 바이러스주를 선별하는 것이 가장 중요하다.
그러나, 공여 바이러스와 독성 바이러스를 구별하는 프라이머의 설계에 많은 시간이 소요되며, 다양한 조합으로 만들어진 다수의 재조합 바이러스에서 RNA들을 분리하여 분석하는 작업은 많은 노력과 시간을 요구한다. 이런 작업은 북반구의 경우 매년 2월에 WHO에서 권장되는 바이러스를 입수하여 단기간(약 1~2 개월)에 생백신 바이러스주를 제조하여 생산에 도입해야 하는 과정을 고려할 경우 가장 집중적으로 연구되어져야 하며 단기간에 수행될 수 있는 방법이 개발되어져야 하는 시점이다.
이에, 본 발명자들은 현재까지 축적된 독감 바이러스 데이터 베이스를 분석하여 약독화된 공여 바이러스에 특이적인 프라이머를 다수 제작하였고, 매트릭스 형태로 공여 바이러스와 독성 바이러스에 대한 RT-PCR을 수행하여 두 바이러스를 구별할 수 있는 프라이머들을 선별할 수 있었으며, 이들 프라이머를 사용한 멀티플렉스 PCR (multiplex PCR) 방법을 도입하여 3 또는 4개 반응만으로 하나의 바이러스를 신속하게 판별하는 방법을 고안할 수 있었다.
따라서, 한 가지 양태에서, 본 발명의 목적은 공여 바이러스와 독감 바이러 스 A형의 6:2 재조합 바이러스를 찾는 스크리닝 과정 중, 공여 바이러스인 HTCA-A101에 특이적으로 반응하는 프라이머 세트 및 그들을 사용한 PCR 방법을 제공한다.
추가의 양태에서, 본 발명의 추가의 목적은 상기 PCR 방법을 동시에 다중 방식으로 수행하는 보다 간단하고 경제적인 멀티플렉스 PCR 방법을 제공하는 것이다.
또한, 본 발명에 따른 멀티플렉스 PCR 방법을 사용함으로써 6:2 재조합 바이러스를 신속하게 스크리닝할 수 있다.
보다 구체적으로, 본 발명은 독감 바이러스의 8개 유전자 RNA 게놈 절편으로부터 약독화 공여 바이러스주 게놈에 대해서는 PCR 산물을 생성하지만 독성 바이러스 게놈에 대해서는 PCR 산물을 생성하지 않는 PCR 프라이머 세트를 디자인하는 단계; 독성 바이러스와 약독화 공여 바이러스를 수정란에 감염시켜 두 종의 바이러스의 무작위 재조합을 통한 재조합 바이러스를 생산하는 단계; 재조합 바이러스의 RNA 게놈의 역전사를 통해 cDNA를 수득하는 단계; 상기 재조합 바이러스의 cDNA와 함께, 각각의 PCR 산물들이 구별될 수 있는 크기를 고려하여 선택된 8개 유전자 RNA 절편별로 한 가지 프라이머 세트를 사용하여 8개 유전자에 대한 PCR 반응을 수행하는 단계; 약독화 공여 바이러스에 특이적인 프라이머 세트에 의해 6개 내부 유전자(internal genes, PB2, PB1, PA, NP, M, NS) RNA 절편은 증폭되지만 외피 단백질(HA 및 NA)을 암호화하는 2개 RNA 절편은 증폭되지 않는 재조합 바이러스를 선택하는 단계를 포함함을 특징으로 하여, 독감 바이러스 생백신 생산을 위한 공여 바이러스와 독성 바이러스간의 6:2 재조합 바이러스를 스크리닝하기 위한 PCR 방법을 제공한다.
보다 바람직하게는, 본 발명은 약독화 공여 바이러스로서 HTCA-A101 균주 (KCTC 0400 BP)를 사용하는 PCR 방법을 제공한다.
또한, 본 발명에서 PCR을 사용하여 스크리닝하고자 하는 독성 바이러스로서 A형 독감 바이러스인 A/Moscow/10/99, A/New/Calenonia/20/99, A/Shangdong/9/93 및 A/Singapore/6/86 을 예시적으로 사용하지만, 이들 바이러스에 국한되지는 않는다.
본 발명은 또한, 상기한 PCR 방법에서 8개 유전자에 대한 PCR 반응이 3 내지 4개의 튜브에서 2 내지 3개의 반응이 동시에 수행됨을 특징으로 하는 멀티플렉스 PCR 방법을 제공한다. 이러한 다중 PCR 방법은 보다 빠르고 보다 저렴하게 원하는 재조합 바이러스에 대한 스크리닝을 가능하게 할 것이다.
보다 구체적으로, 본 발명은 제1 튜브에는 PB2, PB1 및 NP에 대한 프라이머 세트, 제2 튜브에는 M, NS 및 PA에 대한 프라이머 세트 및 제3 튜브에는 HA 및 NA에 대한 프라이머 세트를 넣어 재조합 바이러스에 대해서 제1 및 제2 튜브에서만 PCR 생성물이 증폭됨을 특징으로 하는 멀티플렉스 PCR 방법을 제공한다. 이때, HA 및 NA는 주된 면역원성 단백질이기 때문에 불활화 백신 또는 생백신으로서 재조합 바이러스를 사용하는 경우 이들은 독성 바이러스 유래의 것이어야 한다.
따라서, 바람직하게는, 본 발명은 약독화 공여 바이러스와 독성 바이러스 간의 6:2 재조합 바이러스를 스크리닝하는 멀티플렉스 PCR 방법을 제공한다.
본 발명에 따른 PCR 및 RT-PCR 반응은 통상적인 공지된 PCR 방법에 의해 수 행될 수 있으며, 바람직하게는 94℃에서 5분간 1회 변성시킨 후, 94℃에서 30초간 변성, 55℃에서 1분간 어닐링 및 72℃에서 1분 20초간 연장시키는 반응을 30회 수행함으로써 수행될 수 있으나, 이러한 PCR 조건으로 제한하고자 하는 것은 아니다.
본 발명은 또한, 표 1에서 제시된 바와 같은 상기 PCR 방법에서 사용하기 위한 약독화 공여 바이러스 특이적인 내부 유전자 6개 및 외피 단백질 유전자 2개를 포함하는 8개 유전자 RNA에 대한 프라이머 세트를 제공한다.
본 발명에서 언급되는 바와 같은 독감 바이러스의 비면역원성 6개 유전자는 PB2, PB1, PA, NP, M 및 NS이고 면역원성 2개 유전자는 HA 및 NA이며, 본 발명에 따른 PCR 방법에서는 약독화 공여 바이러스 HTCA-A101에 특이적으로 PCR 산물을 생성하지만 맹독성 바이러스에 대해서는 PCR 산물을 생성되지 않는 특이적인 프라이머 세트를 사용함으로써, 불활화 백신 또는 생백신으로 사용하기 위한 6:2 재조합 바이러스를 PCR 방법으로 신속하게 스크리닝하는 방법을 제공한다.
이하, 본 발명을 상세히 설명한다.
1. 올리고뉴클레오타이드 프라이머의 제작
독감 바이러스 염기서열의 데이터 베이스를 이용하여 공여 바이러스와 독성 바이러스와의 상동성 비교를 수행한 후, 상동성이 낮은 부분에 대한 프라이머를 제작하였다. 프라이머 제작 시 프라이머의 길이는 19-21 mer 정도로 하였으며, 그 중 최소한 2-3 mer는 공여 바이러스와 독성 바이러스에서 연속된 차이를 보이는 부 분을 선택하여 그 부분을 프라이머의 3' 말단으로 하였으며, 어닐링 온도가 58-60℃ 정도가 되도록 하여 멀티플렉스 PCR 수행시 유리하도록 설계하였다. 또한, 중간중간에 유전자 변이가 있는 것을 우선적으로 선택하였으며 한가지 염기의 서열이 연속되는 부분이 있는 곳은 선택에서 제외하여 공여 바이러스에 특이적인 프라이머를 제작하였다. 이렇게 제작된 상동성이 낮은 부분은 스크리닝을 위한 프라이머로 사용되었다. 반대로 상동성이 높은 부분은(데이터 베이스 에 기초하였을 때 100% 상동성) 포지티브 표준 프라이머(positive control)로서 RT-PCR에 사용하였다.구체적으로, 본 발명에서는 A/X-31 바이러스를 저온적응시킨 HTCA-A101 (이하 A101이라 약칭함)를 공여 바이러스로 사용하였다. 공여바이러스와의 상동성 비교를 위한 A형 바이러스들의 염기서열은 독감 바이러스 전문 데이터 베이스 사이트인 ()에서 얻었으며, 그 중 사람을 숙주로 하는 H3N2와 H1N1 서브타입의 바이러스들의 염기서열만을 사용하여 상동성을 비교하였다. 상동성 비교는 A101과 독성 바이러스간의 1:1 비교가 아니라 데이터베이스에 있는 바이러스들과 A101간의 비교이며, 데이터베이스에 있는 염기서열 중에서 전체 염기서열이 분석되어져 있으며 사람에게 감염되는 바이러스의 서열을 전부 추출하여 비교하였다. 프라이머의 선정에 있어서 각 절편(segment)별로 상동성에 차이가 있으므로 일률적인 기준은 적용하기가 어려웠으며, PCR 수행시의 산물의 크기도 고려해서 가장 큰 차이를 보이는 부분들을 선정해서 프라이머를 제작하였다.
2. A101과 독성 바이러스의 주형에 따른 RT-PCR 경향성 확인
본 발명에서는 우선 A101의 여덟 개의 RNA 게놈에 대하여 상기에서 제작한 프라이머 세트를 이용하여 모든 PCR 산물이 나오는 조건을 확립하였으며, 같은 조건 하에서 독성 바이러스의 PCR 산물을 비교 분석하였다.
3. 멀티플렉스 RT-PCR 조건 확립
공여 바이러스주의 게놈에 대해서는 PCR 산물을 생성하지만 독성 바이러스에 대해서는 생성하지 않는 프라이머를 검색하여 찾은 다음, 그 중 유전자별로 한 세트씩을 선택하여 8개의 PCR 반응이 3개의 튜브에서 이루어지도록 고안하였다.
멀티플렉스 RT-PCR 조건에 관한 선행기술들은 하나의 주형에서 여러 개의 PCR 산물을 얻기 위하여 산물과 프라이머 간의 상호작용을 줄이기 위한 조건들에 대한 것들이 대부분인데, 본 발명에서는 독감 바이러스의 8개의 주형에서 일어나는 각각의 PCR 반응이 동시에 일어나는 것을 특징으로 한다. 또한, 아가로오스 젤 상에서 PCR 산물들을 구별하기 위해서는 PCR 산물들의 크기를 고려한 조합을 설정해야만 했다. 멀티플렉스 RT-PCR을 통해 재조합된 바이러스의 유전자 유래를 파악할 수 있었으며 염기서열의 부분 분석에 의한 결과와 얻은 결과가 일치함을 확인할 수 있었다.
이하, 실시예에 의하여 본 발명을 상세히 설명한다. 하기 실시예는 본 발명을 구체적으로 예시하는 것이며 본 발명의 내용이 실시예에 의해 한정되는 것은 아니다.
<실시예 1> 올리고 뉴클레오타이드 프라이머의 설계 및 합성
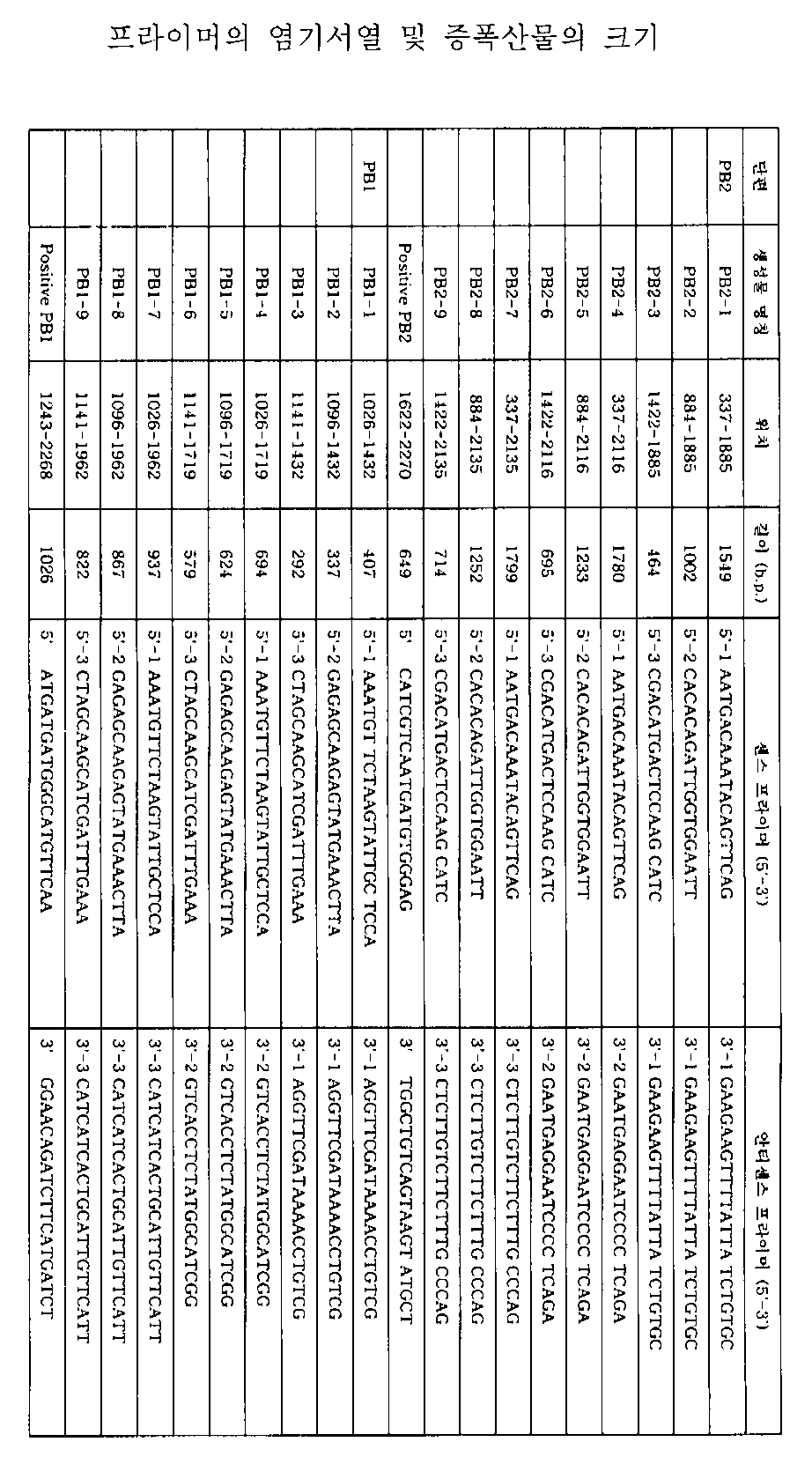
A형 독감 바이러스는 8개의 네가티브 센스 RNA 가닥으로 이루어져 있으며, 각각은 PB2, PB1, PA, HA, NP, NA, M, NS 단백질을 암호화하고 있다. 이들 8개의 유전자에 대해서 독감 바이러스 염기 서열 전문 사이트(http://www.flu.lanl.gov)에서 사람을 숙주로 하는 H3N2와 H1N1 서브유형 바이러스에 해당하는 염기서열과 약독화된 바이러스 HTCA-A101의 상동성 비교를 수행하였다. 다중 상동성 비교의 경우 VECTOR NTI의 얼라이먼트 프로그램(Aligment program)을 이용하였으며, 상동성이 낮은 부분을 선택하여 5' 프라이머 3개와 3' 프라이머 3개씩 각 유전자별 여섯 부분을 선택하였다. 이러한 유전자별 프라이머 조합으로 PB2, PB1, PA, NP, M, NS 각각에 대해서 9개 프라이머 세트를 디자인하였다. HA 및 NA에 대해서는 5 프라이머 2개와 3 프라이머 2개씩 각 유전자별로 네 부분이 선택되었으며, 각각 4개의 프라이머 세트를 디자인하였다. 이 프라이머 세트들을 사용하여 HTCA-A101 바이러스의 주형에 특이적으로 증폭되는 PCR 산물을 얻었다. 반면 포지티브 표준 (positive control)으로서 사용하기 위해 상동성이 높은 부분의 프라이머를 제작하였으며, PB2, PB1, PA, NP, M, NS에 대해서는 각각 1개의 포지티브 표준 프라이머를 디자인하고, HA 및 NA에 대해서는 2개의 포지티브 표준 프라이머를 디자인하였다. 각 프라이머의 염기서열 및 증폭산물의 크기는 표 1에 나타내었다.
<실시예 2> 독감 바이러스에서 RNA의 분리
RNA의 분리는 제조원(GibcoBRL사)의 TRIZOL LS 시약을 이용하였으며, 바이러스 배양액에서 바로 RNA를 분리하였다. 바이러스 배양액 300 ul에 TRIZOL LS 시약 900 ul를 가한 후, 200 ul의 클로로포름을 가하고 10초간 강하게 진탕한 다음 12000 rpm에서 10분간 원심분리하였다. 상등액을 취하여 새 튜브에 옮긴 다음 동일 부피의 이소프로필 알코올(isopropanol)을 가하고 상온에서 10분간 정치시키고 12000 rpm에서 5분간 원심분리하여 RNA를 침전시켰다. 상등액을 제거하고 75% 에탄올 1ml을 가하여 진탕한 후 다시 12000 rpm에서 10분간 원심분리하여 RNA 침전을 얻었다. RNase를 함유하지 않은 물로 RNA 침전물을 용해시키고 소량씩 분주하여 70℃에 보관하여 사용하였다.
독감 바이러스주로는 공여 바이러스주 외에 최근 유행한 독성 바이러스주 4종 A/New Caledonia/20/99 (H1N1), A/Moscow/10/99 (H3N2), A/Singapore/6/86 (H1N1), A/Shangdong/9/93 (H3N2)을 선택하였다.
<실시예 3> 독감 바이러스 RNA에서 cDNA 제조
생성된 RNA의 농도를 260nm에서의 흡광도에 근거하여 결정한 다음, 전체 2ug의 RNA를 주형으로 하여 퀴아젠(QIAGEN)사의 옴니스크립트(Omniscript) RT 키트를 사용하여 RT을 수행하였다. 반응 혼합액의 조성은 RNA 용액 12ul, 5mM dNTP 2ul, 10배 RT 완충액 2ul, 10pmol/ul 프라이머 1ul(독감 바이러스 8개 유전자의 네가티브 센스 RNA 3'에 공통적으로 보존되어 있는 염기서열 5'-AGCGAAAGCAGG-3'를 프라 이머로 이용) 및 역전사 효소(Reverse transcriptase) 1ul를 혼합하였다. 혼합액을 37℃에서 60분간 반응시켜 cDNA를 합성한 후 94℃에서 5분간 반응시켜 역전사 효소를 불활화하였다. 합성된 cDNA는 8개 유전자의 모든 PCR 반응에 사용되었다.
<실시예 4> 공여 바이러스와 독성 바이러스의 PCR 산물 생성 확인
프라이머 특이성에 의한 독성 바이러스와 공여 바이러스의 PCR 산물 생성 여부를 알아보기 위하여, 실시예 3에서 제조한 cDNA 용액 1ul와 실시예 1에서 합성한 각 유전자별 프라이머 세트를 각각 혼합하고 94℃에서 5분간 변성시킨 다음, 변성 (94℃에서 30초), 결합 (55℃에서 1분) 및 연장 (72℃에서 1분20초)을 총 30회 반복하는 PCR을 수행하였다.
제조된 PCR 산물을 아가로스 젤 상에서 분리한 결과, 공여 바이러스의 경우 각 유전자별 상동성이 낮은 프라이머 조합 즉 내부 유전자 6개에 대한 9가지 프라이머 세트와 외피 단백질 HA와 NA의 경우 4가지 프라이머 세트에 대한 PCR 산물이 모두 수득되었다. 이에 반해 독성 바이러스의 경우 양성 대조반응의 확인으로 cDNA가 존재함에도 불구하고 PCR 산물 검출빈도가 낮았으며, 아래 표 2와 같은 결과를 얻었다. 도 2는 이중에 PB2를 실례로 보여주고 있다. 이로써 같은 조건 하에서의 RT-PCR 수행시 프라이머의 공여 바이러스에 대한 특이적인 결합에 의해 공여 바이러스와 독성 바이러스의 PCR 결과가 현저한 차이가 있음을 확인할 수 있었다.
| 표 내 번호는 PCR 결과 포지티브를 나타내는 프라이머 세트의 번호이다. | ||||||||
| 유전자 바이러스 | PB2 | PB1 | PA | NP | M | NS | HA | NA |
| A/Moscow/10/99 (H3N2) | 2,3 | |||||||
| A/Shangdong/9/93 (H3N2) | ||||||||
| A/New Caledonia/20/99 (H1N1) | 2 | 1,2,4, 5,7,8 | 2,3,8, 9 | 1 | 1,2,3, 7,8,9 | 1,4,7 | ||
| A/Singapore/6/86 (H1N1) | 2,3,5, 6,9 | 1,2,3, 4,5,7, 8,9 | 1,2,3, 7,8,9 | 1,2,3, 5,7,8, 9 | 1,2,3, 4,5,6 | 1,3,4, 5,6,7 | ||
<실시예 5> 멀티플렉스 RT-PCR의 수행
실시예 4를 통하여 공여 바이러스에서는 PCR 산물을 생성하고 독성 바이러스에서는 PCR 산물을 생성하지 않았던 프라이머 세트를 이용하여 멀티플렉스 RT-PCR을 수행하였다. 프라이머 세트는 PB2-2 (1002bp), NP-4 (853bp), PB1-6 (559bp)를 한 튜브에 넣었으며, PA-5 (730bp), NS-5 (521bp), M-6 (326bp)를 한 튜브에 넣었고, HA-4 (1086bp), NA-4 (504 bp)를 한 튜브에 넣고 반응을 수행하였다. 독감 바이러스의 경우 유전자가 결절되어 있음에 착안하여 프라이머의 양이 3배 내지 2배로 첨가되는 것 외에는 모노플렉스(Monoplex) PCR 조건과 동일하게 하여 멀티플렉스 RT-PCR을 수행한 결과 공여 바이러스의 경우, 8개 유전자를 세 튜브의 반응에서 재현성 있게 모두 얻을 수 있었으며, 독성 바이러스 A/New Caledonia/20/99 (H1N1)와 A/Moscow/10/99 (H3N2)의 경우에는 8개 유전자에 대한 양성 대조군의 PCR 산물은 생성되나 멀티플렉스 PCR 튜브에서 PCR이 이루어지지 않았다(도 3 참조). 이에 반해, 공여 바이러스주의 주형에서는 8개 유전자 모두에 해당하는 멀티플렉스 PCR 산물을 확인 할 수 있다(도 3).
<실시예 6> 재조합 바이러스의 유전자 분석
공여 바이러스와 독성 바이러스간의 재현성 있는 멀티플렉스 PCR 결과를 얻은 후, 실제 재조합 바이러스 분석을 수행하였다.
독성 바이러스 A/New Caledonia/20/99(H1N1)와 공여 바이러스를 동시에 수정란에 감염시켜 생장시킨 결과, 두 종의 바이러스의 RNA 단편들의 무작위적인 조합을 통해 다양한 재조합 바이러스가 만들어졌으며, 재조합 바이러스들 중 저온에서의 배양과 공여 바이러스에 대한 항체를 이용하는 선별과정을 거쳐서 독성 바이러스의 HA와 NA를 갖으며 저온적응 특성을 갖는 바이러스를 선별하였다. 독성 바이러스도 저온에서 일부 생장하는 특성을 보이므로 결국 유전자의 분석과정을 거쳐야 공여 바이러스의 내부 유전자들을 포함하는 목적하는 재조합 바이러스를 얻을 수 있는 것이다.
재조합 바이러스들의 유전자 분석은 상기 실시예 5의 방법에 따라 수행하였으며, 그 결과는 표 3 및 도 4에 나타내었다. 분석 결과, 재조합 바이러스 7번은 내부유전자 6개에 대해서는 PCR 산물이 생성되고 외피 단백질을 암호화하는 2개 유전자에서는 PCR 산물이 생성되지 않는 6:2(PB2, PB1, PA, NP, M, NS는 공여 바이러스 유래, HA, NA는 독성 바이러스 유래)의 재조합 바이러스로 예상되었으며, 재조합 바이러스 2번은 5:3(PB2, PB1, NP, M, NS는 공여 바이러스주 유래, PA, HA, NA 는 독성 바이러스 유래)의 재조합 바이러스로 예상되었고, 그 외 4:4((PA, PB1, NP, M는 공여 바이러스주 유래, PB2, NS, HA, NA는 독성 바이러스 유래)와 7:1((PB2, PB1, PA, NP, M, NS, NA는 공여 바이러스주 유래, HA는 독성 바이러스 유래) 등의 여러 종류의 재조합 바이러스를 얻을 수 있었다.
또한 6:2의 조합인 재조합 바이러스 7번의 유전자를 부분 염기서열을 분석해 보거나 전체 유전자에 대해 9개의 프라이머 세트를 이용하여 PCR하여 그 결과를 독성 바이러스 및 공여 바이러스와 비교한 결과 (표 4 참조), 4 개의 튜브에서 반응하여 얻은 결과 (도 4를 참조)와 일치하는 결과를 얻었으며, 이로써 하나의 재조합 바이러스의 8개 유전자 유래 분석을 3 또는 4 튜브의 PCR을 통해 수행하는 것이 가능하였으며 빠른 시간에 많은 수의 재조합 바이러스 분석이 용이함을 알 수 있었다.
| 재조합 바이러스 번호 | 공여 바이러스 절편 개수 : 독성 바이러스 절편 개수 (공여 바이러스 유래 유전자) |
| 1 | 5:3 (PB2, PB1, NP, M, NS) |
| 2 | 5:3 (PB2, PB1, NP, M, NS) |
| 3 | 4:4 (PB1, NP, M, NS) |
| 4 | 4:4 (PB1, NP, PA, M) |
| 5 | 4:4 (PB1, NP, M, NS) |
| 6 | 4:4 (PB1, NP, M, NS) |
| 7 | 6:2 (PB2, PB1, PA, NP, M, NS) |
| 8 | 5:3 (PB2, PB1, NP, PA, NS) |
| 9 | 7:1 (PB2, PB1, PA, NP, M, NS, NA) |
| PCR 산물 | 부분서열분석위치 | 부분서열분석크기 | 상동성(%) |
| PB2 (1622-2270) 649bp | 1622-2270 | 649 bp | 100 |
| PB1 (1243-2268) 1026bp | 1345-1906 2002-253 | 754 bp (562 + 192) | 100 |
| PA (34-507) 474bp | 66-501 | 436 bp | 100 |
| NP (392-1505) 1114bp | 60-469 | 410 bp | 99 |
| M (248-914) 649bp | 444-849 | 406 bp | 100 |
| NS (1-612) 612bp | 25-578 | 554 bp | 99 |
| HA (1-600) 600bp | 유의한 유사성 없음 | ||
| NA (1-600) 600bp | 유의한 유사성 없음 |
본 발명에 따라 디자인된 공여 바이러스주에 특이적인 프라이머 세트를 이용하는 멀티플렉스 역전사 중합효소 반응을 통한 바이러스 스크리닝 방법은 재조합 바이러스의 제조과정 중 다양한 조합으로 형성된 중간 단계의 바이러스들로부터 적은 노동력과 짧은 시간 동안에 정확한 조합을 가진 바이러스를 선별 가능하게 하여, 독성 바이러스를 입수하여 단기간에 재조합 바이러스를 제조함으로써 생백신 바이러스의 원활한 생산 및 공급을 가능하게 하는 효과가 있다.
<110> CJ Corporation
Protheon
<120> Screening system of reassortant influenza viruses using primer
dependent multiplex RT-PCR
<160> 145
<170> KopatentIn 1.71
<210> 1
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-1 sense primer designed from HTCA-A101
<400> 1
aatgacaaat acagttcag 19
<210> 2
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-1 antisense primer designed from HTCA-A101
<400> 2
gaagaagttt tattatctgt gc 22
<210> 3
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-2 sense primer designed from HTCA-A101
<400> 3
cacacagatt ggtggaatt 19
<210> 4
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-2 antisense primer designed from HTCA-A101
<400> 4
gaagaagttt tattatctgt gc 22
<210> 5
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-3 sense primer designed from HTCA-A101
<400> 5
cgacatgact ccaagcatc 19
<210> 6
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-3 antisense primer designed from HTCA-A101
<400> 6
gaagaagttt tattatctgt gc 22
<210> 7
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-4 sense primer designed from HTCA-A101
<400> 7
aatgacaaat acagttcag 19
<210> 8
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-4 antisense primer designed from HTCA-A101
<400> 8
gaatgaggaa tcccctcaga 20
<210> 9
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-5 sense primer designed from HTCA-A101
<400> 9
cacacagatt ggtggaatt 19
<210> 10
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-5 antisense primer designed from HTCA-A101
<400> 10
gaatgaggaa tcccctcaga 20
<210> 11
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-6 sense primer designed from HTCA-A101
<400> 11
cgacatgact ccaagcatc 19
<210> 12
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-6 antisense primer designed from HTCA-A101
<400> 12
gaatgaggaa tcccctcaga 20
<210> 13
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-7 sense primer designed from HTCA-A101
<400> 13
aatgacaaat acagttcag 19
<210> 14
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-7 antisense primer designed from HTCA-A101
<400> 14
ctcttgtctt ctttgcccag 20
<210> 15
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-8 sense primer designed from HTCA-A101
<400> 15
cacacagatt ggtggaatt 19
<210> 16
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-8 antisense primer designed from HTCA-A101
<400> 16
ctcttgtctt ctttgcccag 20
<210> 17
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-9 sense primer designed from HTCA-A101
<400> 17
cgacatgact ccaagcatc 19
<210> 18
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB2-9 antisense primer designed from HTCA-A101
<400> 18
ctcttgtctt ctttgcccag 20
<210> 19
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive PB2 sense primer designed from HTCA-A101
<400> 19
catcgtcaat gatgtgggag 20
<210> 20
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive PB2 antisense primer designed from HTCA-A101
<400> 20
tggctgtcag taagtatgct 20
<210> 21
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-1 sense primer designed from HTCA-A101
<400> 21
aaatgttcta agtattgctc ca 22
<210> 22
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-1 antisense primer designed from HTCA-A101
<400> 22
aggttcgata aaacctgtcg 20
<210> 23
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-2 sense primer designed from HTCA-A101
<400> 23
gagagcaaga gtatgaaact ta 22
<210> 24
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-2 antisense primer designed from HTCA-A101
<400> 24
aggttcgata aaacctgtcg 20
<210> 25
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-3 sense primer designed from HTCA-A101
<400> 25
ctagcaagca tcgatttgaa a 21
<210> 26
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-3 antisense primer designed from HTCA-A101
<400> 26
aggttcgata aaacctgtcg 20
<210> 27
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-4 sense primer designed from HTCA-A101
<400> 27
aaatgttcta agtattgctc ca 22
<210> 28
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-4 antisense primer designed from HTCA-A101
<400> 28
gtcacctcta tggcatcgg 19
<210> 29
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-5 sense primer designed from HTCA-A101
<400> 29
gagagcaaga gtatgaaact ta 22
<210> 30
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-5 antisense primer designed from HTCA-A101
<400> 30
gtcacctcta tggcatcgg 19
<210> 31
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-6 sense primer designed from HTCA-A101
<400> 31
ctagcaagca tcgatttgaa a 21
<210> 32
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-6 antisense primer designed from HTCA-A101
<400> 32
gtcacctcta tggcatcgg 19
<210> 33
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-7 sense primer designed from HTCA-A101
<400> 33
aaatgttcta agtattgctc ca 22
<210> 34
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-7 antisense primer designed from HTCA-A101
<400> 34
catcatcact gcattgttca tt 22
<210> 35
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-8 sense primer designed from HTCA-A101
<400> 35
gagagcaaga gtatgaaact ta 22
<210> 36
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-8 antisense primer designed from HTCA-A101
<400> 36
catcatcact gcattgttca tt 22
<210> 37
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-9 sense primer designed from HTCA-A101
<400> 37
ctagcaagca tcgatttgaa a 21
<210> 38
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> PB1-9 antisense primer designed from HTCA-A101
<400> 38
catcatcact gcattgttca tt 22
<210> 39
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive PB1 sense primer designed from HTCA-A101
<400> 39
atgatgatgg gcatgttcaa 20
<210> 40
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive PB1 antisense primer designed from HTCA-A101
<400> 40
ggaacagatc ttcatgatct 20
<210> 41
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-1 sense primer designed from HTCA-A101
<400> 41
taatcgaggg aagagatcgc 20
<210> 42
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-1 antisense primer designed from HTCA-A101
<400> 42
tgtgttcaat tggagccaca 20
<210> 43
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-2 sense primer designed from HTCA-A101
<400> 43
acaacaccac gaccacttag 20
<210> 44
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-2 antisense primer designed from HTCA-A101
<400> 44
tgtgttcaat tggagccaca 20
<210> 45
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-3 sense primer designed from HTCA-A101
<400> 45
gatggaagga acccaatgtt 20
<210> 46
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-3 antisense primer designed from HTCA-A101
<400> 46
tgtgttcaat tggagccaca 20
<210> 47
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-4 sense primer designed from HTCA-A101
<400> 47
taatcgaggg aagagatcgc 20
<210> 48
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-4 antisense primer designed from HTCA-A101
<400> 48
tttatgatga aaccaacaag c 21
<210> 49
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-5 sense primer designed from HTCA-A101
<400> 49
acaacaccac gaccacttag 20
<210> 50
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-5 antisense primer designed from HTCA-A101
<400> 50
tttatgatga aaccaacaag c 21
<210> 51
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-6 sense primer designed from HTCA-A101
<400> 51
gatggaagga acccaatgtt 20
<210> 52
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-6 antisense primer designed from HTCA-A101
<400> 52
tttatgatga aaccaacaag c 21
<210> 53
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-7 sense primer designed from HTCA-A101
<400> 53
taatcgaggg aagagatcgc 20
<210> 54
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-7 antisense primer designed from HTCA-A101
<400> 54
gaacatgggc cttgaaacct 20
<210> 55
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-8 sense primer designed from HTCA-A101
<400> 55
acaacaccac gaccacttag 20
<210> 56
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-8 antisense primer designed from HTCA-A101
<400> 56
gaacatgggc cttgaaacct 20
<210> 57
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-9 sense primer designed from HTCA-A101
<400> 57
gatggaagga acccaatgtt 20
<210> 58
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PA-9 antisense primer designed from HTCA-A101
<400> 58
gaacatgggc cttgaaacct 20
<210> 59
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive PA sense primer designed from HTCA-A101
<400> 59
gtagtctgcc tttgtggcc 19
<210> 60
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive PA antisense primer designed from HTCA-A101
<400> 60
tcttgtctta tggtgaatag 20
<210> 61
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-1 sense primer designed from HTCA-A101
<400> 61
acctatatac aggagagtaa ac 22
<210> 62
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-1 antisense primer designed from HTCA-A101
<400> 62
aaagcttccc tcttgggagc 20
<210> 63
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-2 sense primer designed from HTCA-A101
<400> 63
gaacaatggt gatggaattg g 21
<210> 64
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-2 antisense primer designed from HTCA-A101
<400> 64
aaagcttccc tcttgggagc 20
<210> 65
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-3 sense primer designed from HTCA-A101
<400> 65
gtgggtacga ctttgaaagg 20
<210> 66
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-3 antisense primer designed from HTCA-A101
<400> 66
aaagcttccc tcttgggagc 20
<210> 67
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-4 sense primer designed from HTCA-A101
<400> 67
acctatatac aggagagtaa ac 22
<210> 68
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-4 antisense primer designed from HTCA-A101
<400> 68
agtgtacttg attccatagt c 21
<210> 69
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-5 sense primer designed from HTCA-A101
<400> 69
gaacaatggt gatggaattg g 21
<210> 70
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-5 antisense primer designed from HTCA-A101
<400> 70
agtgtacttg attccatagt c 21
<210> 71
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-6 sense primer designed from HTCA-A101
<400> 71
gtgggtacga ctttgaaagg 20
<210> 72
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-6 antisense primer designed from HTCA-A101
<400> 72
agtgtacttg attccatagt c 21
<210> 73
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-7 sense primer designed from HTCA-A101
<400> 73
acctatatac aggagagtaa ac 22
<210> 74
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-7 antisense primer designed from HTCA-A101
<400> 74
tgctgccata atggtggttc 20
<210> 75
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-8 sense primer designed from HTCA-A101
<400> 75
gaacaatggt gatggaattg g 21
<210> 76
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-8 antisense primer designed from HTCA-A101
<400> 76
tgctgccata atggtggttc 20
<210> 77
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-9 sense primer designed from HTCA-A101
<400> 77
gtgggtacga ctttgaaagg 20
<210> 78
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NP-9 antisense primer designed from HTCA-A101
<400> 78
tgctgccata atggtggttc 20
<210> 79
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive NP sense primer designed from HTCA-A101
<400> 79
taaggcgaat ctggcgccaa 20
<210> 80
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive NP antisense primer designed from HTCA-A101
<400> 80
taagatcctt cattactcat 20
<210> 81
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-1 sense primer designed from HTCA-A101
<400> 81
acgtactctc tatcatcccg 20
<210> 82
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> M-1 antisense primer designed from HTCA-A101
<400> 82
tctagcctga ctagcaacc 19
<210> 83
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-2 sense primer designed from HTCA-A101
<400> 83
ccatggggcc aaagaaatct 20
<210> 84
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> M-2 antisense primer designed from HTCA-A101
<400> 84
tctagcctga ctagcaacc 19
<210> 85
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> M-3 sense primer designed from HTCA-A101
<400> 85
tctagcctga ctagcaacc 19
<210> 86
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-3 antisense primer designed from HTCA-A101
<400> 86
acgtactctc tatcatcccg 20
<210> 87
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-4 sense primer designed from HTCA-A101
<400> 87
tgatatttgc ggcaatagtg 20
<210> 88
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-4 antisense primer designed from HTCA-A101
<400> 88
ccatggggcc aaagaaatct 20
<210> 89
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-5 sense primer designed from HTCA-A101
<400> 89
tgatatttgc ggcaatagtg 20
<210> 90
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-5 antisense primer designed from HTCA-A101
<400> 90
tgatatttgc ggcaatagtg 20
<210> 91
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> M-6 sense primer designed from HTCA-A101
<400> 91
attgctgact cccagcatc 19
<210> 92
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-6 antisense primer designed from HTCA-A101
<400> 92
tgatatttgc ggcaatagtg 20
<210> 93
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-7 sense primer designed from HTCA-A101
<400> 93
acgtactctc tatcatcccg 20
<210> 94
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-7 antisense primer designed from HTCA-A101
<400> 94
cttccctcat agactttggc 20
<210> 95
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-8 sense primer designed from HTCA-A101
<400> 95
ccatggggcc aaagaaatct 20
<210> 96
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-8 antisense primer designed from HTCA-A101
<400> 96
cttccctcat agactttggc 20
<210> 97
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> M-9 sense primer designed from HTCA-A101
<400> 97
attgctgact cccagcatc 19
<210> 98
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> M-9 antisense primer designed from HTCA-A101
<400> 98
cttccctcat agactttggc 20
<210> 99
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive M sense primer designed from HTCA-A101
<400> 99
gcagcgtaga cgctttgtc 19
<210> 100
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive M antisense primer designed from HTCA-A101
<400> 100
ccttccgtag aaggccctc 19
<210> 101
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-1 sense primer designed from HTCA-A101
<400> 101
agttgcagac caagaactag 20
<210> 102
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-1 antisense primer designed from HTCA-A101
<400> 102
gcaatattag agtctccagc 20
<210> 103
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-2 sense primer designed from HTCA-A101
<400> 103
atcaagacag ccacacgtgc 20
<210> 104
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-2 antisense primer designed from HTCA-A101
<400> 104
gcaatattag agtctccagc 20
<210> 105
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-3 sense primer designed from HTCA-A101
<400> 105
ggaaagcaga tagtggagcg 20
<210> 106
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-3 antisense primer designed from HTCA-A101
<400> 106
gcaatattag agtctccagc 20
<210> 107
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-4 sense primer designed from HTCA-A101
<400> 107
agttgcagac caagaactag 20
<210> 108
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-4 antisense primer designed from HTCA-A101
<400> 108
ctaattgttc ccgccatttc t 21
<210> 109
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-5 sense primer designed from HTCA-A101
<400> 109
atcaagacag ccacacgtgc 20
<210> 110
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-5 antisense primer designed from HTCA-A101
<400> 110
ctaattgttc ccgccatttc t 21
<210> 111
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-6 sense primer designed from HTCA-A101
<400> 111
ggaaagcaga tagtggagcg 20
<210> 112
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-6 antisense primer designed from HTCA-A101
<400> 112
ctaattgttc ccgccatttc t 21
<210> 113
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-7 sense primer designed from HTCA-A101
<400> 113
agttgcagac caagaactag 20
<210> 114
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-7 antisense primer designed from HTCA-A101
<400> 114
attctctgtt atcttcagtt 20
<210> 115
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-8 sense primer designed from HTCA-A101
<400> 115
atcaagacag ccacacgtgc 20
<210> 116
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-8 antisense primer designed from HTCA-A101
<400> 116
attctctgtt atcttcagtt 20
<210> 117
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-9 sense primer designed from HTCA-A101
<400> 117
ggaaagcaga tagtggagcg 20
<210> 118
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NS-9 antisense primer designed from HTCA-A101
<400> 118
attctctgtt atcttcagtt 20
<210> 119
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive NS sense primer designed from HTCA-A101
<400> 119
agcaaaagca gggtgacaaa 20
<210> 120
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive NS antisense primer designed from HTCA-A101
<400> 120
cagagactcg aactgtgtta 20
<210> 121
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-1 sense primer designed from HTCA-A101
<400> 121
ggtttcactt ggactggggt 20
<210> 122
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-1 antisense primer designed from HTCA-A101
<400> 122
tgagaattcc ttttcgattt ga 22
<210> 123
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-2 sense primer designed from HTCA-A101
<400> 123
tgaccaaatc aggaagca 18
<210> 124
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-2 antisense primer designed from HTCA-A101
<400> 124
tgagaattcc ttttcgattt ga 22
<210> 125
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-3 sense primer designed from HTCA-A101
<400> 125
ggtttcactt ggactggggt 20
<210> 126
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-3 antisense primer designed from HTCA-A101
<400> 126
gcatccagtc tttgtatcca 20
<210> 127
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-4 sense primer designed from HTCA-A101
<400> 127
tgaccaaatc aggaagca 18
<210> 128
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HA-4 antisense primer designed from HTCA-A101
<400> 128
gcatccagtc tttgtatcca 20
<210> 129
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive H1 control sense primer designed from HTCA-A101
<400> 129
atgaaagcaa aactactagt tca 23
<210> 130
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive H1 control antisense primer designed from HTCA-A101
<400> 130
agacgggtga tgaacacccc at 22
<210> 131
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive H2 control sense primer designed from HTCA-A101
<400> 131
cctcaacagg tagaatatgc gg 22
<210> 132
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive H2 control antisense primer designed from HTCA-A101
<400> 132
aggagcaatt agattccctg tg 22
<210> 133
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-1 sense primer designed from HTCA-A101
<400> 133
agatatgccc caaattagtg 20
<210> 134
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-1 antisense primer designed from HTCA-A101
<400> 134
cgattgttag ccagcccatg cca 23
<210> 135
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-2 sense primer designed from HTCA-A101
<400> 135
tgcgtttgta tcaatgggac 20
<210> 136
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-2 antisense primer designed from HTCA-A101
<400> 136
cgattgttag ccagcccatg cca 23
<210> 137
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-3 sense primer designed from HTCA-A101
<400> 137
agatatgccc caaattagtg 20
<210> 138
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-3 antisense primer designed from HTCA-A101
<400> 138
ctgcgatttg gaattaggtg 20
<210> 139
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-4 sense primer designed from HTCA-A101
<400> 139
tgcgtttgta tcaatgggac 20
<210> 140
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> NA-4 antisense primer designed from HTCA-A101
<400> 140
ctgcgatttg gaattaggtg 20
<210> 141
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive N1 control sense primer designed from HTCA-A101
<400> 141
agcaaaagca ggagtttaaa a 21
<210> 142
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive N1 control antisense primer designed from HTCA-A101
<400> 142
cgattgttag ccagcccatg cca 23
<210> 143
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive N2 control sense primer designed from HTCA-A101
<400> 143
atgaatccaa atcaaaagat aa 22
<210> 144
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Positive N2 control antisense primer designed from HTCA-A101
<400> 144
ttgccaggat cgcatgacac at 22
<210> 145
<211> 11
<212> DNA
<213> Artificial Sequence
<220>
<223> Uni12 primer designed from HTCA-A101
<400> 145
agcaaagcag g 11
Claims (5)
- 삭제
- 공여 바이러스와 독성 바이러스간의 6:2 재조합 독감 바이러스를 스크리닝하는 방법으로서,독감 바이러스의 8개 유전자 RNA 게놈 절편으로부터 약독화 공여 바이러스주 게놈에 대해서는 PCR 산물을 생성하지만 독성 바이러스 게놈에 대해서는 PCR 산물을 생성하지 않는 PCR 프라이머 세트를 디자인하는 단계,독성 바이러스와 약독화 공여 바이러스를 수정란에 감염시켜 두 종의 바이러스의 무작위 재조합을 통한 재조합 바이러스를 생산하는 단계,재조합 바이러스 RNA 게놈의 역전사를 통해 cDNA를 수득하는 단계,상기 재조합 바이러스의 cDNA와 함께, 상기 독감 바이러스의 8개 유전자의 RNA 절편별로 각 PCR 산물들이 구별될 수 있는 크기를 고려하여 각각 5′말단 및 3′말단 프라이머로 구성되는 한 가지씩의 프라이머 세트를 선택하여 8개 유전자에 대한 PCR 반응을 수행하는 단계, 및약독화 공여 바이러스에 특이적인 프라이머 세트에 의해 6개 내부 유전자(internal genes, PB2, PB1, PA, NP, M, NS)의 RNA 절편은 증폭되지만 외피 단백질(HA 및 NA)을 암호화하는 2개의 RNA 절편은 증폭되지 않는 재조합 바이러스를 선택하는 단계를 포함하는 것을 특징으로 하는 재조합 독감 바이러스의 스크리닝 방법.
- 제2항에 있어서, 약독화 공여 바이러스가 HTCA-A101 균주(KCTC 0400 BP)인 방법.
- 제2항에 있어서, 8개 유전자에 대해 3 내지 4 개의 튜브에서 2 내지 3 개씩의 PCR 반응을 동시에 수행함을 특징으로 하는 멀티플렉스 PCR을 사용하여 독감 재조합 바이러스를 스크리닝하는 방법.
- 약독화 공여 바이러스 HTCA-A101 균주에 특이적으로 결합하는 서열번호 1 내지 서열번호 145로 구성되는 군으로부터 선택되는 센스 및 앤티센스 프라이머 세트.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020030053534A KR100632429B1 (ko) | 2003-08-01 | 2003-08-01 | 프라이머 특이성 유무에 의한 멀티플렉스 역전사 중합효소연쇄반응을 이용한 재조합 독감 바이러스의 스크리닝 방법 |
| PCT/KR2004/001903 WO2005012572A1 (en) | 2003-08-01 | 2004-07-28 | Screening method of reassortant influenza viruses using primer dependent multiplex rt-pcr |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020030053534A KR100632429B1 (ko) | 2003-08-01 | 2003-08-01 | 프라이머 특이성 유무에 의한 멀티플렉스 역전사 중합효소연쇄반응을 이용한 재조합 독감 바이러스의 스크리닝 방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20050015063A KR20050015063A (ko) | 2005-02-21 |
| KR100632429B1 true KR100632429B1 (ko) | 2006-10-09 |
Family
ID=34114232
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020030053534A KR100632429B1 (ko) | 2003-08-01 | 2003-08-01 | 프라이머 특이성 유무에 의한 멀티플렉스 역전사 중합효소연쇄반응을 이용한 재조합 독감 바이러스의 스크리닝 방법 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR100632429B1 (ko) |
| WO (1) | WO2005012572A1 (ko) |
Families Citing this family (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040121335A1 (en) | 2002-12-06 | 2004-06-24 | Ecker David J. | Methods for rapid detection and identification of bioagents associated with host versus graft and graft versus host rejections |
| US7666588B2 (en) | 2001-03-02 | 2010-02-23 | Ibis Biosciences, Inc. | Methods for rapid forensic analysis of mitochondrial DNA and characterization of mitochondrial DNA heteroplasmy |
| US7226739B2 (en) | 2001-03-02 | 2007-06-05 | Isis Pharmaceuticals, Inc | Methods for rapid detection and identification of bioagents in epidemiological and forensic investigations |
| US20030027135A1 (en) | 2001-03-02 | 2003-02-06 | Ecker David J. | Method for rapid detection and identification of bioagents |
| US8073627B2 (en) | 2001-06-26 | 2011-12-06 | Ibis Biosciences, Inc. | System for indentification of pathogens |
| US7217510B2 (en) | 2001-06-26 | 2007-05-15 | Isis Pharmaceuticals, Inc. | Methods for providing bacterial bioagent characterizing information |
| EP1578399A4 (en) | 2002-12-06 | 2007-11-28 | Isis Pharmaceuticals Inc | METHODS FOR RAPID IDENTIFICATION OF PATHOGENS IN HUMANS AND BEETS |
| US8057993B2 (en) | 2003-04-26 | 2011-11-15 | Ibis Biosciences, Inc. | Methods for identification of coronaviruses |
| US7964343B2 (en) | 2003-05-13 | 2011-06-21 | Ibis Biosciences, Inc. | Method for rapid purification of nucleic acids for subsequent analysis by mass spectrometry by solution capture |
| US8158354B2 (en) | 2003-05-13 | 2012-04-17 | Ibis Biosciences, Inc. | Methods for rapid purification of nucleic acids for subsequent analysis by mass spectrometry by solution capture |
| US8242254B2 (en) | 2003-09-11 | 2012-08-14 | Ibis Biosciences, Inc. | Compositions for use in identification of bacteria |
| US8097416B2 (en) | 2003-09-11 | 2012-01-17 | Ibis Biosciences, Inc. | Methods for identification of sepsis-causing bacteria |
| US8546082B2 (en) | 2003-09-11 | 2013-10-01 | Ibis Biosciences, Inc. | Methods for identification of sepsis-causing bacteria |
| US8163895B2 (en) | 2003-12-05 | 2012-04-24 | Ibis Biosciences, Inc. | Compositions for use in identification of orthopoxviruses |
| US7666592B2 (en) | 2004-02-18 | 2010-02-23 | Ibis Biosciences, Inc. | Methods for concurrent identification and quantification of an unknown bioagent |
| WO2005117270A2 (en) | 2004-05-24 | 2005-12-08 | Isis Pharmaceuticals, Inc. | Mass spectrometry with selective ion filtration by digital thresholding |
| US20050266411A1 (en) | 2004-05-25 | 2005-12-01 | Hofstadler Steven A | Methods for rapid forensic analysis of mitochondrial DNA |
| US7811753B2 (en) | 2004-07-14 | 2010-10-12 | Ibis Biosciences, Inc. | Methods for repairing degraded DNA |
| US20060205040A1 (en) | 2005-03-03 | 2006-09-14 | Rangarajan Sampath | Compositions for use in identification of adventitious viruses |
| US8084207B2 (en) | 2005-03-03 | 2011-12-27 | Ibis Bioscience, Inc. | Compositions for use in identification of papillomavirus |
| CA2616281C (en) | 2005-07-21 | 2014-04-22 | Isis Pharmaceuticals, Inc. | Methods for rapid identification and quantitation of mitochondrial dna variants |
| US20070087337A1 (en) * | 2005-10-17 | 2007-04-19 | Rangarajan Sampath | Compositions for use in identification of influenza viruses |
| US9149473B2 (en) | 2006-09-14 | 2015-10-06 | Ibis Biosciences, Inc. | Targeted whole genome amplification method for identification of pathogens |
| US8871471B2 (en) | 2007-02-23 | 2014-10-28 | Ibis Biosciences, Inc. | Methods for rapid forensic DNA analysis |
| WO2008151023A2 (en) | 2007-06-01 | 2008-12-11 | Ibis Biosciences, Inc. | Methods and compositions for multiple displacement amplification of nucleic acids |
| US8354230B2 (en) | 2007-12-21 | 2013-01-15 | Quest Diagnostics Investments Inc. | Multiplex detection assay for influenza and RSV viruses |
| WO2010033625A1 (en) | 2008-09-16 | 2010-03-25 | Ibis Biosciences, Inc. | Microplate handling systems and related computer program products and methods |
| US8148163B2 (en) | 2008-09-16 | 2012-04-03 | Ibis Biosciences, Inc. | Sample processing units, systems, and related methods |
| WO2010033599A2 (en) | 2008-09-16 | 2010-03-25 | Ibis Biosciences, Inc. | Mixing cartridges, mixing stations, and related kits, systems, and methods |
| WO2010093943A1 (en) | 2009-02-12 | 2010-08-19 | Ibis Biosciences, Inc. | Ionization probe assemblies |
| BRPI1011432A2 (pt) * | 2009-05-08 | 2019-09-24 | Novartis Ag | ensaios genericos para deteccao de virus influenza |
| EP2454000A4 (en) | 2009-07-17 | 2016-08-10 | Ibis Biosciences Inc | SYSTEMS FOR IDENTIFYING BIOLOGICAL SUBSTANCES |
| WO2011008971A1 (en) | 2009-07-17 | 2011-01-20 | Ibis Biosciences, Inc. | Lift and mount apparatus |
| EP2488656B1 (en) | 2009-10-15 | 2015-06-03 | Ibis Biosciences, Inc. | Multiple displacement amplification |
-
2003
- 2003-08-01 KR KR1020030053534A patent/KR100632429B1/ko not_active IP Right Cessation
-
2004
- 2004-07-28 WO PCT/KR2004/001903 patent/WO2005012572A1/en active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| KR20050015063A (ko) | 2005-02-21 |
| WO2005012572A1 (en) | 2005-02-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100632429B1 (ko) | 프라이머 특이성 유무에 의한 멀티플렉스 역전사 중합효소연쇄반응을 이용한 재조합 독감 바이러스의 스크리닝 방법 | |
| Mahmood et al. | Isolation and molecular characterization of Sul/01/09 avian infectious bronchitis virus, indicates the emergence of a new genotype in the Middle East | |
| Fu et al. | Molecular detection and typing of duck hepatitis A virus directly from clinical specimens | |
| Hirst et al. | Novel avian influenza H7N3 strain outbreak, British Columbia | |
| Kottier et al. | Experimental evidence of recombination in coronavirus infectious bronchitis virus | |
| Kahya et al. | Presence of IS/1494/06 genotype-related infectious bronchitis virus in breeder and broiler flocks in Turkey. | |
| Pohuang et al. | Sequence analysis of S1 genes of infectious bronchitis virus isolated in Thailand during 2008–2009: identification of natural recombination in the field isolates | |
| CN113913394B (zh) | 人工重组的h5n6流感病毒及其制备方法和应用 | |
| Yi et al. | Development of a combined canine distemper virus specific RT-PCR protocol for the differentiation of infected and vaccinated animals (DIVA) and genetic characterization of the hemagglutinin gene of seven Chinese strains demonstrated in dogs | |
| CN113913395B (zh) | 人工重组的h5n8流感病毒及其制备方法和应用 | |
| Chen et al. | Identification of Taiwan and China-like recombinant avian infectious bronchitis viruses in Taiwan | |
| CN109321535A (zh) | 一种热稳定的新城疫病毒弱毒疫苗候选株 | |
| Ashmi et al. | Molecular characterization of canine distemper virus from Tamil Nadu, India | |
| CN113913396A (zh) | 人工重组的h7n9流感病毒及其制备方法和应用 | |
| CN109593892A (zh) | 一种扩增h5n6亚型禽流感病毒全基因组的通用引物组、试剂盒及方法 | |
| EP2454386B1 (en) | Influenza detection method and kit therefor | |
| CN116836244A (zh) | 赤羽病毒akav/jl/2022的全基因组序列及其扩增引物 | |
| CN109266623B (zh) | 一株疫苗株rSHA-△200及其构建方法和应用 | |
| CN109295011B (zh) | 一株疫苗株rSN-R92G-E93K及其构建方法和应用 | |
| Choi et al. | Genetic diversity of avian paramyxovirus type 6 isolated from wild ducks in the Republic of Korea | |
| Soltanialvar et al. | Genetic analysis of polymerase complex (PA, PB1 and PB2) genes of H9N2 avian influenza viruses from Iran (1999 to 2009) | |
| McFarlane et al. | Sequence analysis of the gene coding for the S1 glycoprotein of infectious bronchitis virus (IBV) strains from New Zealand | |
| CN102234637B (zh) | 重组甲型h1n1流感病毒灭活疫苗株(sc/pr8)的制备及应用 | |
| Downie | Reassortment of influenza A virus genes linked to PB1 polymerase gene | |
| KR101310873B1 (ko) | A형 인플루엔자 바이러스 검출용 프라이머 세트, 상기 프라이머 세트를 포함하는 a형 인플루엔자 바이러스 검출용 조성물 및 키트, 및 이를 이용한 a형 인플루엔자 바이러스 검출 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E90F | Notification of reason for final refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| N231 | Notification of change of applicant | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20121228 Year of fee payment: 7 |
|
| FPAY | Annual fee payment |
Payment date: 20130925 Year of fee payment: 8 |
|
| FPAY | Annual fee payment |
Payment date: 20140924 Year of fee payment: 9 |
|
| FPAY | Annual fee payment |
Payment date: 20150921 Year of fee payment: 10 |
|
| LAPS | Lapse due to unpaid annual fee |