JP7692002B2 - 新規な2-アリールチアゾール誘導体またはその塩、その製造方法、及びそれを含む医薬組成物 - Google Patents
新規な2-アリールチアゾール誘導体またはその塩、その製造方法、及びそれを含む医薬組成物 Download PDFInfo
- Publication number
- JP7692002B2 JP7692002B2 JP2022564122A JP2022564122A JP7692002B2 JP 7692002 B2 JP7692002 B2 JP 7692002B2 JP 2022564122 A JP2022564122 A JP 2022564122A JP 2022564122 A JP2022564122 A JP 2022564122A JP 7692002 B2 JP7692002 B2 JP 7692002B2
- Authority
- JP
- Japan
- Prior art keywords
- methylthiazole
- carboxamide hydrochloride
- cyano
- group
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/22—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
- C07D277/28—Radicals substituted by nitrogen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/56—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Neurosurgery (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Diabetes (AREA)
- Epidemiology (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Gastroenterology & Hepatology (AREA)
- Psychology (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
R1は、水素;C1~C4アルキル基;またはモノ-あるいはジ-C1~C5アルキルアミノで置換されているC1~C4アルキル基であり、
R2は、C1~C4アルキル基であり、
Aは、下記化学式1a~1dの基からなる群から選択される基であり、
*は、化学式1の化合物に結合する位置を表し、
nは、1、2、または3であり、
R3およびR4は、互いに独立して、水素;C1~C4アルキル基であるか、それらが結合している窒素原子と結合して、ピペリジン、モルホリン、またはピロリジンを形成し(前記ピペリジン、モルホリン、またはピロリジンは、C1~C4アルキルで任意選択的に置換されている)、
R5およびR6は、C1~C4アルキル基であるか、あるいはR5およびR6が環を形成して、シクロペンタン、シクロヘキサンまたはテトラヒドロピランを形成し、
Cyは、ホモピペラジニル、ピペリジニル、モルホリニル、およびピロリジニルからなる群から選択される含窒素複素環基であり、前記含窒素複素環基は、C1~C4アルキルまたはベンジルで任意選択的に置換されている。
N-(2-(ジエチルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジメチルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(3-(ジエチルアミノ)プロピル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(4-メチルホモピペラジノ)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(4-(1-メチル)ピペリジニル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(1-ピロリジノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(1-ピペリジノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((1-(ジメチルアミノ)シクロペンチル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((1-(ジメチルアミノ)シクロヘキシル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(3-(1-ベンジル)ピロリジニル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(2-(1-メチル)ピロリジノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((S)-2-(1-エチル)ピロリジノメチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(4-モルホリンアミノ)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(1-ピペリジンアミノ)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジエチルアミノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジメチルアミノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((S)-2-(1-エチル)ピロリジノメチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジエチルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジメチルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((S)-2-(1-エチル)ピロリジノメチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;及び
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩
からなる群から選択される1つ以上であってもよい。
N-(2-(ジイソプロピルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;及び
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩
からなる群から選択される1つ以上であってもよい。
R1X
式中、R1、R2、及びAは、前記で定義されているものと同一であり、Xは、ハロゲンである。
TLC Rf = 0.24 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.26 (d、1H、J = 2.4 Hz)、8.22 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.33 (d、1H、J = 8.8 Hz)、4.03 (d、2H、J = 6.4 Hz)、3.78 (t、2H、J = 6.4 Hz)、3.42 (t、2H、J = 6.4 Hz)、3.40 ~ 3.32 (m、4H)、2.74 (s、3H)、2.25 ~ 2.15 (m、1H)、1.40 (t、6H、J = 7.2 Hz)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.29 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.23 (d、1H、J = 2.4 Hz)、8.20 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.30 (d、1H、J = 8.8 Hz)、4.01 (d、2H、J = 6.4 Hz)、3.90 ~ 3.82 (m、2H)、3.75 (t、2H、J = 6.8 Hz)、3.38 (t、2H、J = 6.8 Hz)、2.72 (s、3H)、2.25 ~ 2.15 (m、1H)、1.46 (d、12H、J = 6.8 Hz)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.34 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.26 (d、1H、J = 2.4 Hz)、8.22 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.34 (d、1H、J = 9.2 Hz)、4.03 (d、2H、J = 6.4 Hz)、3.77 (t、2H、J = 6.0 Hz)、3.42 (t、2H、J = 6.0 Hz)、3.02 (s、6H)、2.74 (s、3H)、2.25 ~ 2.15 (m、1H)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.17 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.27 (d、1H、J = 2.4 Hz)、8.22 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.35 (d、1H、J = 8.8 Hz)、4.03 (d、2H、J = 6.4 Hz)、3.51 (t、2H、J = 6.4 Hz)、3.34 ~ 3.22 (m、6H)、2.73 (s、3H)、2.25 ~ 2.15 (m、1H)、2.15 ~ 2.05 (m、2H)、1.37 (t、6H、J = 7.2 Hz)、1.12 (d、6H、J = 6.4 Hz)
TLC Rf = 0.39 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.23 (d、1H、J = 2.4 Hz)、8.20 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.33 (d、1H、J = 8.8 Hz)、4.32 ~ 4.18 (m、1H)、4.02 (d、2H、J = 6.4 Hz)、3.90 ~ 3.60 (m、5H)、3.45 ~ 3.35 (m、2H)、3.00 (s、3H)、2.52 (s、3H)、2.35 ~ 2.25 (m、2H)、2.25 ~ 2.15 (m、1H)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.29 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.24 (d、1H、J = 2.4 Hz)、8.20 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.33 (d、1H、J = 8.8 Hz)、4.20 ~ 4.10 (m、1H)、4.02 (d、2H、J = 6.4 Hz)、3.65 ~ 3.55 (m、2H)、3.25 ~ 3.15 (m、2H)、2.97 (s、3H)、2.68 (s、3H)、2.35 ~ 2.25 (m、2H)、2.25 ~ 2.15 (m、1H)、2.05 ~ 1.90 (m、2H)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.61 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.26 (d、1H、J = 2.4 Hz)、8.22 (dd、1H、J = 2.4 Hz、9.2 Hz)、7.34 (d、1H、J = 9.2 Hz)、4.12 (dd、2H、J = 3.2、12.8 Hz)、4.03 (d、2H、J = 6.4 Hz)、3.92 ~ 3.85 (m、2H)、3.85 ~ 3.78 (m、2H)、3.73 (d、2H、J = 12.8 Hz)、3.44 (t、2H、J = 6.0 Hz)、3.30 ~ 3.20 (m、2H)、2.74 (s、3H)、2.25 ~ 2.15 (m、1H)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.14 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.26 (d、1H、J = 2.4 Hz)、8.22 (dd、1H、J = 2.4 Hz、9.2 Hz)、7.35 (d、1H、J = 8.8 Hz)、4.03 (d、2H、J = 6.4 Hz)、3.88 ~ 3.80 (m、2H)、3.77 (t、2H、J = 6.0 Hz)、3.48 (t、2H、J = 6.0 Hz)、3.25 ~ 3.15 (m、2H)、2.75 (s、3H)、2.25 ~ 2.15 (m、3H)、2.15 ~ 2.05 (m、2H)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.33 in 10% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.25 (d、1H、J = 2.4 Hz)、8.21 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.33 (d、1H、J = 8.8 Hz)、4.03 (d、2H、J = 6.4 Hz)、3.77 (t、2H、J = 6.0 Hz)、3.73 (d、2H、J = 11.6 Hz)、3.37 (t、2H、J = 6.0 Hz)、3.10 ~ 3.00 (m、2H)、2.73 (s、3H)、2.25 ~ 2.15 (m、1H)、2.05 ~ 1.95 (m、2H)、1.93 ~ 1.83 (m、3H)、1.62 ~ 1.53 (m、1H)、1.12 (d、6H、J = 6.8 Hz)
TLC Rf = 0.44 in 10% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 10.31 (t、1H、J = 4.8 Hz)、8.67 (t、1H、J = 6.4 Hz)、8.26 (d、1H、J = 2.4 Hz)、8.20 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.40 (d、1H、J = 8.8 Hz)、4.02 (d、2H、J = 6.4 Hz)、3.95 ~ 3.85 (m、2H)、3.83 (d、2H、J = 6.4 Hz)、3.65 ~ 3.55 (m、2H)、2.80 (s、3H)、2.79 (s、3H)、2.64 (s、3H)、2.15 ~ 2.05 (m、1H)、1.95 ~ 1.85 (m、4H)、1.03 (d、6H、J = 6.4 Hz)
TLC Rf = 0.34 in 10% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 10.73 (t、1H、J = 4.8 Hz)、8.73 (t、1H、J = 6.4 Hz)、8.26 (d、1H、J = 2.4 Hz)、8.20 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.40 (d、1H、J = 8.8 Hz)、4.02 (d、2H、J = 6.4 Hz)、3.61 (d、2H、J = 6.4 Hz)、2.81 (s、3H)、2.80 (s、3H)、2.64 (s、3H)、2.15 ~ 2.05 (m、1H)、2.00 ~ 1.90 (m、4H)、1.80 ~ 1.70 (m、4H)、1.02 (d、6H、J = 6.8 Hz)
TLC Rf = 0.31 in 10% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 9.90 (s、1H)、8.56 (t、1H、J = 6.0 Hz)、8.26 (d、1H、J = 2.4 Hz)、8.20 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.40 (d、1H、J = 8.8 Hz)、4.02 (d、2H、J = 6.4 Hz)、3.74 (d、2H、J = 6.4 Hz)、2.81 (s、3H)、2.79 (s、3H)、2.64 (s、3H)、2.15 ~ 2.05 (m、1H)、1.95 ~ 1.88 (m、2H)、1.75 ~ 1.52 (m、7H)、1.22 ~ 1.13 (m、1H)、1.02 (d、6H、J = 6.8 Hz)
TLC Rf = 0.41 in 10% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 11.20 (s、1H)、8.73 (dd、1H、J = 6.4、26 Hz)、8.25 ~ 8.15 (m、2H)、7.65 ~7.60 (m、2H)、7.50 ~ 7.40 (m、4H)、4.73 ~ 4.45 (m、1H)、4.42 (dd、2H、J = 6.0、14 Hz)、4.02 (dd、2H、J = 2.8、6.4 Hz)、3.60 ~ 3.40 (m、2H)、3.40 ~ 3.30 (m、1H)、3.22 ~ 3.10 (m、1H)、2.62 (d、3H、J = 4.0 Hz)、2.15 ~ 2.05 (m、1H)、1.02 (dd、6H、J = 1.6、6.8 Hz)
TLC Rf = 0.14 in 10% MeOH in Chloroform
1H NMR (400MHz、D2O) δ 7.58 (dd、1H、J = 2.4、8.8 Hz)、7.51 (d、1H、J = 2.4 Hz)、6.88 (d、1H、J = 8.8 Hz)、3.72 (d、2H、J = 6.8 Hz)、3.68 ~ 3.60 (m、1H)、3.37 (t、2H、J = 6.8 Hz)、3.32 ~ 3.25 (m、1H)、3.27 (s、2H)、3.15 ~ 3.05 (m、1H)、2.87 (s、3H)、2.35 ~ 2.25 (m、1H)、2.25 ~ 2.15 (m、1H)、2.15 ~ 1.92 (m、3H)、1.85 ~ 1.70 (m、2H)、0.92 (d、6H、J = 6.8 Hz)
TLC Rf = 0.24 in 10% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 10.39 (s、1H)、8.74 (t、1H、J = 5.6 Hz)、8.25 (d、1H、J = 2.0 Hz)、8.19 (dd、1H、J = 2.0 Hz、9.2 Hz)、7.40 (d、1H、J = 9.2 Hz)、4.01 (d、2H、J = 6.4 Hz)、3.75 ~ 3.52 (m、4H)、3.45 ~ 3.35 (m、1H)、3.13 ~ 3.03 (m、2H)、2.65 (s、3H)、2.20 ~ 1.80 (m、5H)、1.29 (t、3H、J = 7.2 Hz)、1.02 (d、6H、J = 6.8 Hz)
TLC Rf = 0.69 in 10% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 9.10 (s、1H)、8.35 (s、1H)、8.30 ~ 8.20 (m、1H)、7.35 ~ 7.40 (m、1H)、4.01 (d、2H、J = 6.4 Hz)、3.85 ~ 3.65 (m、4H)、2.95 ~ 2.70 (m、4H)、2.67 (s、3H)、2.15 ~ 2.05 (m、1H)、1.29 (t、3H、J = 7.2 Hz)、1.03 (d、6H、J = 6.8 Hz)
TLC Rf = 0.39 in 10% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 9.01 (s、1H)、8.28 (d、1H、J = 2.4 Hz)、8.23 (dd、1H、J = 2.0、8.8 Hz)、7.38 (d、1H、J = 8.8 Hz)、4.01 (d、2H、J = 6.4 Hz)、3.25 ~ 3.20 (m、1H)、3.05 ~ 2.95 (m、2H)、2.72 (s、3H)、2.70 ~ 2.65 (m、1H)、2.15 ~ 2.05 (m、1H)、1.82 ~ 1.65 (m、6H)、1.03 (d、6H、J = 6.4 Hz)
TLC Rf = 0.20 in 20% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.18 (d、1H、J = 2.4 Hz)、8.09 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.11 (d、1H、J = 8.8 Hz)、3.90 ~ 3.82 (m、2H)、3.74 (t、2H、J = 6.8 Hz)、3.38 (t、2H、J = 6.8 Hz)、2.73 (s、3H)、1.46 (d、12H、J = 6.8 Hz)
TLC Rf = 0.39 in 40% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 11.99 (s、1H)、10.40 (s、1H)、8.61 (t、1H、J = 6.0 Hz)、8.13 (d、1H、J = 2.4 Hz)、7.95 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.23 (d、1H、J = 8.8 Hz)、3.64 (q、2H、J = 6.4 Hz)、3.22 (q、2H、J = 6.4 Hz)、3.20 ~ 3.12 (m、4H)、2.64 (s、3H)、1.25 (t、6H、J = 7.2 Hz)
TLC Rf = 0.18 in 40% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 11.97 (s、1H)、10.19 (s、1H)、8.52 (t、1H、J = 6.0 Hz)、8.13 (d、1H、J = 2.4 Hz)、8.05 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.22 (d、1H、J = 8.8 Hz)、3.62 (q、2H、J = 6.0 Hz)、3.25 (q、2H、J = 6.0 Hz)、2.83 (s、3H)、2.82 (s、3H)、2.64 (s、3H)
TLC Rf = 0.67 in 20% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 12.03 (s、1H)、11.24 (s、1H)、8.64 (t、1H、J = 5.6 Hz)、8.13 (d、1H、J = 2.4 Hz)、8.05 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.24 (d、1H、J = 8.8 Hz)、4.00 ~ 3.80 (m、4H)、3.68 (q、2H、J = 6.0 Hz)、3.58 ~ 3.48 (m、2H)、3.45 ~ 3.35 (m、2H)、3.25 ~ 3.15 (m、2H)、2.64 (s、3H)
TLC Rf = 0.47 in 40% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 11.96 (s、1H)、10.43 (s、1H)、8.71 (t、1H、J = 5.6 Hz)、8.14 (d、1H、J = 2.4 Hz)、8.06 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.21 (d、1H、J = 8.8 Hz)、3.75 ~ 3.52 (m、4H)、3.45 ~ 3.35 (m、1H)、3.13 ~ 3.03 (m、2H)、2.64 (s、3H)、2.20 ~ 2.10 (m、1H)、2.05 ~ 1.80 (m、3H)、1.29 (t、3H、J = 7.2 Hz)
TLC Rf = 0.33 in 20% MeOH in Chloroform
1H NMR (400MHz、MeOH-d4) δ 8.34 (d、1H、J = 2.4 Hz)、8.30 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.43 (d、1H、J = 8.8 Hz)、4.65 (t、2H、J = 4.8 Hz)、3.90 ~ 3.80 (m、2H)、3.80 ~ 3.70 (m、4H)、3.52 ~ 3.43 (m、4H)、3.38 (t、2H、J = 6.8 Hz)、2.73 (s、3H)、1.50 ~ 1.46 (m、18H)
1H NMR (400MHz、DMSO-d6) δ 10.90 (s、1H)、10.14 (s、1H)、8.77 (t、1H、J = 5.6 Hz)、8.30 (d、1H、J = 2.4 Hz)、8.24 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.44 (d、1H、J = 9.2 Hz)、4.67 (t、2H、J = 4.4 Hz)、3.70 ~ 3.60 (m、6H)、3.30 ~ 3.15 (m、6H)、2.68 (s、3H)、1.40 ~ 1.40 (m、18H)
TLC Rf = 0.30 in 20% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 10.54 (s、1H)、10.31 (s、1H)、8.65 (t、1H、J = 5.2 Hz)、8.30 (d、1H、J = 2.4 Hz)、8.25 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.44 (d、1H、J = 8.8 Hz)、4.64 (s、2H)、3.70 ~ 3.60 (m、4H)、3.40 ~ 3.15 (m、10H)、1.35 ~ 1.20 (m、12H)
TLC Rf = 0.25 in 20% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 10.80 (s、1H)、10.45 (s、1H)、8.89 (t、1H、J = 5.2 Hz)、8.30 (d、1H、J = 2.4 Hz)、8.25 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.44 (d、1H、J = 8.8 Hz)、4.66 (t、2H、J = 4.8 Hz)、3.65 ~ 3.55 (m、4H)、3.30 ~ 3.20 (m、6H)、2.83 (s、3H)、2.82 (s、3H)、2.66 (s、3H)、1.35 ~ 1.28 (m、6H)
TLC Rf = 0.40 in 20% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 11.24 (s、1H)、10.86 (s、1H)、8.70 (t、1H、J = 5.6 Hz)、8.30 (d、1H、J = 2.4 Hz)、8.24 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.44 (d、1H、J = 8.8 Hz)、4.66 (t、2H、J = 4.8 Hz)、4.05 ~ 3.95 (m、2H)、3.90 ~ 3.80 (m、4H)、3.75 ~ 3.65 (m、2H)、3.65 ~ 3.60 (m、2H)、3.60 ~ 3.50 (m、2H)、3.45 ~ 3.25 (m、6H)、3.20 ~ 3.10 (m、2H)、2.66 (s、3H)、1.30 (t、6H、J = 7.2Hz)
TLC Rf = 0.08 in 20% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 10.70 (s、1H)、10.66 (s、1H)、8.80 (t、1H、J = 5.6 Hz)、8.31 (d、1H、J = 2.4 Hz)、8.25 (dd、1H、J = 2.4 Hz、8.8 Hz)、7.45 (d、1H、J = 8.8 Hz)、4.65 (t、2H、J = 4.4 Hz)、3.80 ~ 3.50 (m、6H)、3.45 ~ 3.35 (m、5H)、3.15 ~ 3.05 (m、2H)、2.67 (s、3H)、2.20 ~ 2.10 (m、1H)、2.05 ~ 1.80 (m、3H)、1.35 ~ 1.25 (m、9H)
TLC Rf = 0.48 in 20% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 11.98 (s、1H)、10.48 (s、1H)、8.67 (t、1H、J = 6.4 Hz)、8.15 (d、1H、J = 2.4 Hz)、8.06 (dd、1H、J = 6.4 Hz、8.8 Hz)、7.21 (d、1H、J = 8.8 Hz)、3.92 ~ 3.85 (m、2H)、3.83 (d、2H、J = 6.4 Hz)、3.68 ~ 3.58 (m、2H)、2.79 (s、6H)、2.63 (s、3H)、2.00 ~ 1.88 (m、4H)
TLC Rf = 0.38 in 20% MeOH in Chloroform
1H NMR (400MHz、DMSO-d6) δ 10.45 ~ 10.35 (m、2H)、8.72 (t、1H、J = 6.4 Hz)、8.33 (d、1H、J = 2.4 Hz)、8.27 (dd、1H、J = 6.4 Hz、8.8 Hz)、7.45 (d、1H、J = 8.8 Hz)、4.64 (t、2H、J = 4.4 Hz)、3.98 ~ 3.85 (m、2H)、3.84 (d、2H、J = 6.4 Hz)、3.70 ~ 3.60 (m、4H)、3.35 ~ 3.25 (m、4H)、2.80 (d、6H、J = 4.8Hz)、2.65 (s、3H)、1.95 ~ 1.88 (m、4H)、1.30 (t、6H、J = 7.2 Hz)
オートファジー検出キット(DAPGreen Autophagy detection、Dojindo、D676-10)を製造業者の説明書に従って使用することにより、Hela細胞(韓国細胞株バンク)において本発明の化合物のオートファジー誘導活性を測定した。具体的には、Hela細胞(8×104細胞)を、10%ウシ胎児血清(FBS)を含むFluroBrite DMEMと共に、96ウェルプレートの各ウェルに播種した後、CO2インキュベーター内で37℃で一晩インキュベートして細胞を安定化した。DAPGreen(Cat.D676-10、Dojindo)溶液(0.1mMのDMSO溶液)を培地(10%FBSを含むFluroBrite DMEM)で1/1000に希釈して、DAPGreen0.1μMを含む培地(DAPGreen/FBS含有培地)を調製した。細胞が単層状に付着した各ウェルから上清を除去した後、各ウェルをFluroBrite DMEMで洗浄した。上記で調製したDAPGreen/FBS含有培地(100ul)を各ウェルに加え、CO2インキュベーターで30分間インキュベートした。DAPGreen処理開始時と30分後に、蛍光値(EX:450nm/EM:535nm)をそれぞれ測定した。その差分値を細胞の基底吸収値とした。
CYTO-IDTM Autophagy Detection Kit(ENZ-51031-K200、Enzo Life Sciences、Inc.)を用いて、神経細胞におけるオートファジー小胞形成の程度を測定することにより、本発明の化合物によるオートファジーリソソーム経路(autophagy lysosomal pathway、ALP)活性化を検証した。神経細胞(すなわち、primary mouse cortical neuron cells)は、酵素消化法を使用してマウスから分離した。具体的には、16日齢のC57BL6マウス胚由来の皮質組織を20U/mlのパパイン(Worthington Biochemical Corporation、LK003176)および0.005%のDNase I(Worthington Biochemical Corporation、LK003170)と共に、37℃で30分間インキュベートして、初代マウス皮質神経細胞を分離した。
N2a細胞(ATCC、CCL-131、マウス神経芽細胞腫細胞株)(3×104細胞)及び培地(5%熱不活化ウシ胎児血清(FBS、Gibco、16000-044)および50μg/mlペニシリン-ストレプトマイシン(Gibco、15140-122)を補充したDMEM(Dulbecco’s modified Eagle’s medium、Gibco、11995-065)を6ウェルプレートの各ウェルに加え、37℃、CO2インキュベーターで一晩インキュベートした。実施例29の化合物(5μM)及びラパマイシン(10μM)をそれぞれ添加し、37℃、CO2インキュベーターで24時間インキュベートした。各群につき3ウェルで電子顕微鏡用のブロックを作製し、平板包埋法により前固定、後固定、脱水、置換、包埋を行った。厚さ70nmの超薄切片を作製し、各切片に対して重金属染色(酢酸ウラニル、クエン酸鉛)を行った後、細胞全体を画像化するモザイク画像法で撮影した。電子顕微鏡イメージングの結果を図1に示す。また、処理群別に細胞当たりの総オートファジー(オートファジー小胞)、オートファゴソーム、オートリソソームの数を測定して得られた結果を下記表3に示す。下記表3において、対照群は未処理の対照群を意味する。
ジメチルニトロソアミン(DMN)により肝障害を誘発した雄性SDラットに、本発明による化合物を3週間にわたり経口投与して、肝機能改善活性を評価した。具体的には、7週齢の雄性SDラット(Orient Bio社、韓国)を室温で7日間かけて実験室環境に適応させた。全体的な症状を観察し、健康なラットのみを実験に使用した。ラットを、4群(各群n=5)、すなわち、正常対照群、DMNのみを投与する群、および本発明の化合物(実施例2または実施例23の化合物)とDMNの両方を投与する群に分けた。DMNを精製水に溶解し、10mg/kgの用量で各週3日連続して腹腔内投与した(週3回、4週間)。第1週の肝障害の誘発完了後3日目に血液サンプルを採取し、血清ALT(アラニントランスアミナーゼ)値と血清AST(アスパラギン酸トランスアミナーゼ)値を測定して肝障害を確認した。本発明の化合物は、3週間にわたり投与し、すなわち、第1週の肝障害の誘発完了後4日目からDMN投与期間中にかけて投与した。本発明の化合物をそれぞれ精製水に溶解し、経口ゾンデを使用して、25mg/kgの用量で1日1回、3週間にわたり経口投与した。血液サンプルは、0日目(第1週の肝障害誘発が完了した3日後)および試験物質の投与後7日目、14日目および21日目に採取した。採取した血液を凝固促進剤の入ったバキュテイナチューブに注入し、室温で約20分間放置して各血液サンプルを凝固させた。10分間遠心分離した後、得られた血清を使用して血液生化学的検査を行った。実験方法の概要を図2に示す。測定から得られた結果は、SPSSを用いてパラメトリック多重比較または非パラメトリック多重比較によって、群間比較を行った。P<0.05の場合、統計的に有意であると判断した。
ジメチルニトロソアミン(DMN)により肝障害を誘発した雄性SDラットに、本発明による化合物を4週間にわたり経口投与して、肝機能改善活性を評価した。具体的には、7週齢の雄性SDラット(Orient Bio社、韓国)を室温で7日間かけて実験室環境に適応させた。全体的な症状を観察し、健康なラットのみを実験に使用した。ラットを、5群(各群n=10)、すなわち、正常対照群、DMNのみを投与する群、本発明の化合物(実施例23、26、または29の化合物)とDMNの両方を投与する群に分けた。DMNを精製水に溶解し、10mg/kgの用量で各週3日連続して腹腔内投与した(週3回、4週間)。第4週の肝障害の誘発完了後に血液サンプルを採取し、血清ALT(アラニントランスアミナーゼ)値と血清AST(アスパラギン酸トランスアミナーゼ)値を測定して肝障害を確認した。本発明の化合物は、第4週の肝障害の誘発完了後1日目から4週間投与した。本発明の化合物を精製水に溶解し、経口ゾンデを使用して、25mg/kgの用量で1日1回、4週間にわたり経口投与した。血液サンプルは、0日目(第4週の肝障害の誘発が完了した1日後)および試験物質の投与後7日目、14日目、21日目および28日目に採取した。採取した血液を凝固促進剤の入ったバキュテイナチューブに注入し、室温で約20分間放置して各血液サンプルを凝固させた。10分間遠心分離した後、得られた血清を使用して血液生化学的検査を行った。また、最後の投与から24時間後に、剖検して摘出した肝臓を固定して組織標本を作製した。組織標本からスライドを調製し、ヘマトキシリン・エオシン(H&E)染色を行って、肝臓組織への損傷および肝臓組織における炎症性細胞の浸潤を顕微鏡で観察した。また、マッソントリクローム染色を行って、肝臓組織におけるコラーゲン線維の沈着を顕微鏡で観察した。実験方法の概要を図3に示す。測定から得られた結果は、SPSSを用いてパラメトリック多重比較または非パラメトリック多重比較によって、群間比較を行った。P<0.05の場合、統計的に有意であると判断した。上記のように血液生化学的検査を行って得られた血清ALT値および血清AST値を以下の表6および表7に示す。
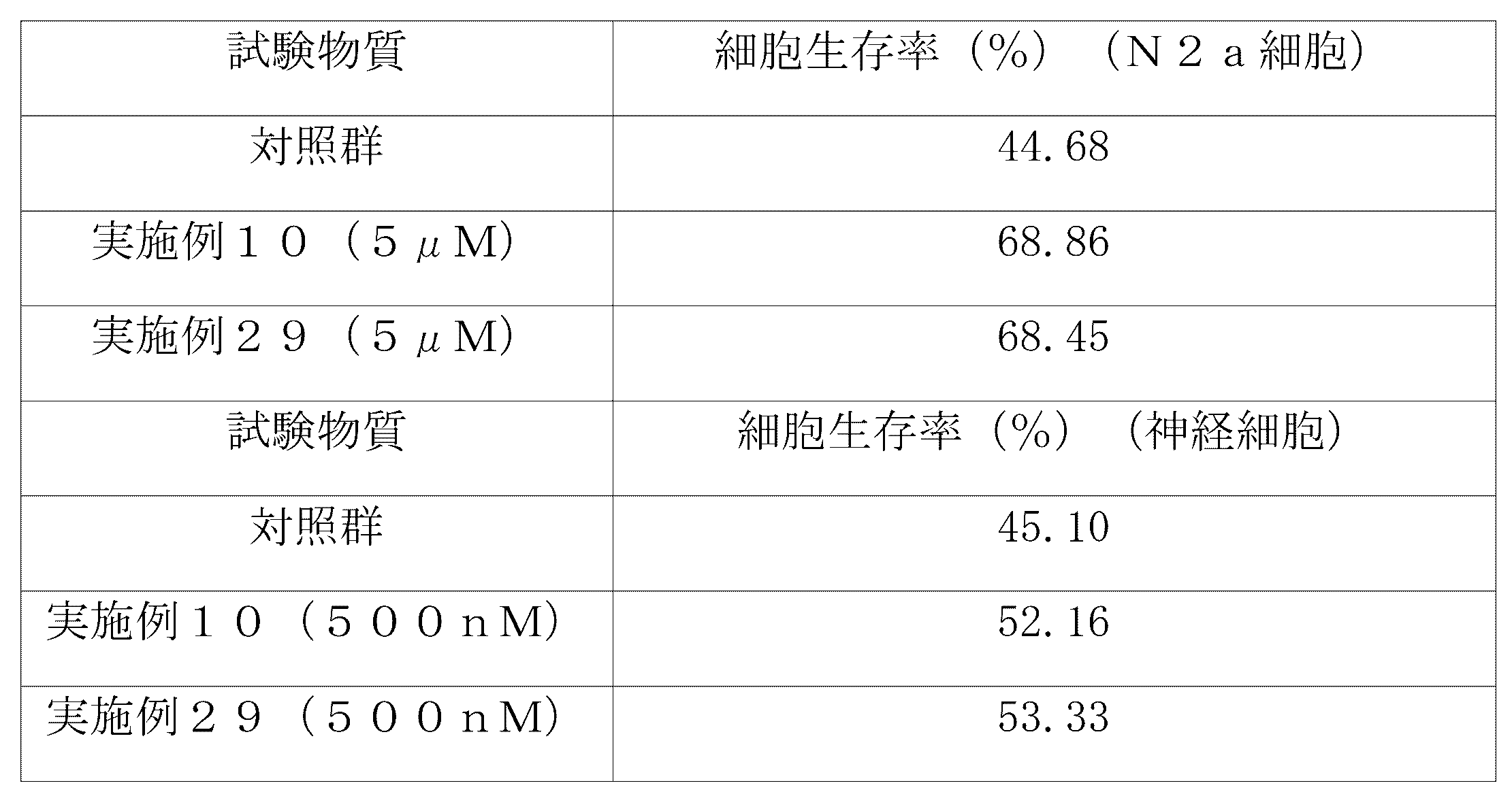
神経変性疾患における主要な細胞毒性物質として知られているベータアミロイドによる神経細胞死に対する、本発明の化合物の阻害活性を、N2a細胞(ATCC、CCL-131、mouse neuroblastoma cell line)および試験例2と同様の方法で単離した神経細胞(primary mouse cortical neuron cells)において分析した。N2a細胞用の培地としては試験例3で使用した培地を、神経細胞用の培地としては試験例2で使用した培地をそれぞれ使用した。具体的には、N2a細胞(3×104細胞)と神経細胞(8×104細胞)を、それぞれの培地と共に、96ウェルプレートの各ウェルに加え、37℃、CO2インキュベーターで一晩インキュベートした。細胞を実施例10の化合物および実施例29の化合物でそれぞれ5μMおよび500nMの濃度で処理し、30分後に20μMのベータアミロイドで処理し、37℃、CO2インキュベーターで72時間培養した。細胞を10μLのCCK-8試薬(Enzo Life Science、ALX-850-039-KI02)で処理した後、37℃、CO2インキュベーターで2時間インキュベートした。各群につき3つのウェルでテストし、各吸光度を450nmで測定した。未処理の対照群の吸光度値を、細胞生存率100%に設定した。各群の細胞生存率は、それぞれの吸光度値から計算した。結果を下記表9に示す。表9において、対照群は、20μMのベータアミロイドのみで処理した群を示す。
神経変性疾患における主要な細胞傷害物質として知られるロテノンによるミトコンドリア損傷に対する、本発明の化合物の阻害活性を、N2a細胞(ATCC、CCL-131、mouse neuroblastoma cell line)において分析した。具体的には、N2a細胞(3×104細胞)及び培地(5%熱不活化ウシ胎児血清(FBS、Gibco、16000-044)および50μg/mlペニシリン-ストレプトマイシン(Gibco、15140-122)を補充したDMEM(Dulbecco’s modified Eagle’s medium、Gibco、11995-065)をXF24ウェル培養プレートの各ウェルに加え、37℃、CO2インキュベーターで一晩インキュベートした。細胞を実施例10の化合物(5μM)で処理し、30分後に10μMのロテノンで処理した後、37℃、CO2インキュベーターで24時間インキュベートした。製造業者の説明書に従ってXF Cell Mito Stress Test Kit (Seahorse Bioscience、103015-100)で処理した後、XF24 Extracellular Flux Analyzer (Seahorse Bioscience)を使用して、ミトコンドリア呼吸のレベルを測定した。各群につき4つのウェルでテストし、基礎呼吸、ATP産生、最大呼吸、および予備呼吸能を測定した。各ミトコンドリア呼吸のレベルは、タンパク質定量値によって補正(normalization)した。未処理の対照群の基礎呼吸を100%に設定し、残りの値を示した。これらの結果を下記表10に示す。表10において、対照群は、10μMのロテノンのみで処理した群を表す。
Claims (12)
- 化学式1の化合物またはその薬学的に許容可能な塩:
R1は、水素;C1~C4アルキル基;またはモノ-あるいはジ-C1~C5アルキルアミノで置換されているC1~C4アルキル基であり、
R2は、C1~C4アルキル基であり、
Aは、下記化学式1a~1dの基からなる群から選択される基であり、
*は、化学式1の化合物に結合する位置を表し、
nは、1、2、または3であり、
R3およびR4は、互いに独立して、水素;C1~C4アルキル基であるか、それらが結合している窒素原子と結合して、ピペリジンまたはピロリジンを形成し(前記ピペリジンまたはピロリジンは、C1~C4アルキルで任意選択的に置換されている)、
R5およびR6は、C1~C4アルキル基であるか、あるいはR5およびR6が環を形成して、シクロペンタン、シクロヘキサンまたはテトラヒドロピランを形成し、
Cyは、ホモピペラジン-1-イル、ピペリジン-1-イル、ピペリジン-4-イル、モルホリン-4-イル、およびピロリジン-3-イルからなる群から選択される含窒素複素環基であり、前記含窒素複素環基は、C1~C4アルキルまたはベンジルで任意選択的に置換されている。 - R1が、水素;イソブチル基;またはジエチルアミノエチル基である、請求項1に記載の化合物またはその薬学的に許容可能な塩。
- R2が、メチル基である、請求項1に記載の化合物またはその薬学的に許容可能な塩。
- Aが、化学式1aの基または化学式1bの基である、請求項1に記載の化合物またはその薬学的に許容可能な塩。
- R3およびR4が、それらが結合している窒素原子と結合して、ピペリジンまたはピロリジンを形成する、請求項4に記載の化合物またはその薬学的に許容可能な塩。
- 前記ピペリジンまたはピロリジンが、C1~C4アルキルで置換されている、請求項5に記載の化合物またはその薬学的に許容可能な塩。
- N-(2-(ジエチルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジメチルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(3-(ジエチルアミノ)プロピル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(4-メチルホモピペラジノ)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(4-(1-メチル)ピペリジニル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(1-ピロリジノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(1-ピペリジノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((1-(ジメチルアミノ)シクロペンチル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((1-(ジメチルアミノ)シクロヘキシル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(3-(1-ベンジル)ピロリジニル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(2-(1-メチル)ピロリジノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((S)-2-(1-エチル)ピロリジノメチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(4-モルホリンアミノ)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(1-ピペリジンアミノ)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジエチルアミノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジメチルアミノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((S)-2-(1-エチル)ピロリジノメチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジエチルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジメチルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((S)-2-(1-エチル)ピロリジノメチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;及び
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩
からなる群から選択される化合物またはその薬学的に許容可能な塩。 - N-(2-(ジイソプロピルアミノ)エチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-イソブトキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(ジイソプロピルアミノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-(2-(4-モルホリノ)エチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(3-シアノ-4-ヒドロキシフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩;及び
N-((4-(ジメチルアミノ)テトラヒドロ-2H-ピラン-4-イル)メチル)-2-(4-(2-ジエチルアミノ)エトキシ-3-シアノフェニル)-4-メチルチアゾール-5-カルボキサミド塩酸塩
からなる群から選択される化合物またはその薬学的に許容可能な塩。 - 化学式2の化合物を、NH2-(CH2)n-NR3R4、NH2-CH2-CR5R6-NR3R4、Cy、およびNH2-Cyからなる群から選択されるN含有化合物(式中、n、R3、R4、R5、及びR6は、請求項1で定義されているものと同一であり;Cyは、ホモピペラジンであり、ホモピペラジンは、C1~C4アルキルで任意選択的に置換され;NH2-Cyは、ピペリジン-1-イルアミン、ピペリジン-4-イルアミン、モルホリン-4-イルアミン、およびピロリジン-3-イルアミンからなる群から選択される含窒素複素環式アミンであり、前記含窒素複素環式アミンは、C1~C4アルキルまたはベンジルで任意選択的に置換されている)を用いてアシル化する工程を含む、化学式1の化合物またはその薬学的に許容可能な塩の製造方法:
- 化学式3の化合物を、NH2-(CH2)n-NR3R4、NH2-CH2-CR5R6-NR3R4、Cy、およびNH2-Cyからなる群から選択されるN含有化合物(式中、n、R3、R4、R5、及びR6は、請求項1で定義されているものと同一であり;Cyは、ホモピペラジンであり、ホモピペラジンは、C1~C4アルキルで任意選択的に置換され;NH2-Cyは、ピペリジン-1-イルアミン、ピペリジン-4-イルアミン、モルホリン-4-イルアミン、およびピロリジン-3-イルアミンからなる群から選択される含窒素複素環式アミンであり、前記含窒素複素環式アミンは、C1~C4アルキルまたはベンジルで任意選択的に置換されている)を用いてアシル化して、化学式4の化合物を調製する工程;ならびに
化学式4の化合物を化学式5の化合物でアルキル化して、化学式1の化合物を調製する工程
を含む、化学式1の化合物またはその薬学的に許容可能な塩の製造方法:
R1X
式中、R1 は、C 1 ~C 4 アルキル基;またはモノ-あるいはジ-C 1 ~C 5 アルキルアミノで置換されているC 1 ~C 4 アルキル基であり、R2及びAは、請求項1で定義されているものと同一であり、Xは、ハロゲンである。 - 治療有効量の請求項1~8のいずれか1項に記載の化合物またはその薬学的に許容可能な塩を有効成分として含む、オートファジー誘導用医薬組成物。
- ハンチントン病、パーキンソン病、アルツハイマー病、プリオン病、多発性硬化症、およびルー・ゲーリック病からなる群から選択される神経変性疾患;肝線維症、肝硬変症、肝炎、および脂肪肝疾患からなる群から選択される肝疾患;糖尿病、高脂血症、肥満、および炎症からなる群から選択される代謝性疾患;または敗血症の予防用または治療用の請求項11に記載の医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2020-0048262 | 2020-04-21 | ||
| KR1020200048262A KR102871918B1 (ko) | 2020-04-21 | 2020-04-21 | 신규의 2-아릴티아졸 유도체 또는 이의 염, 이의 제조방법, 및 이를 함유하는 약학 조성물 |
| PCT/KR2021/000578 WO2021215624A1 (ko) | 2020-04-21 | 2021-01-15 | 신규의 2-아릴티아졸 유도체 또는 이의 염, 이의 제조방법, 및 이를 함유하는 약학 조성물 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023523417A JP2023523417A (ja) | 2023-06-05 |
| JP7692002B2 true JP7692002B2 (ja) | 2025-06-12 |
Family
ID=78231501
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022564122A Active JP7692002B2 (ja) | 2020-04-21 | 2021-01-15 | 新規な2-アリールチアゾール誘導体またはその塩、その製造方法、及びそれを含む医薬組成物 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US12503451B2 (ja) |
| EP (1) | EP4140989B1 (ja) |
| JP (1) | JP7692002B2 (ja) |
| KR (1) | KR102871918B1 (ja) |
| CN (1) | CN115667233B (ja) |
| AU (1) | AU2021261570A1 (ja) |
| CA (1) | CA3176088A1 (ja) |
| ES (1) | ES2987881T3 (ja) |
| WO (1) | WO2021215624A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4378932A1 (en) * | 2022-11-30 | 2024-06-05 | Universität Bern | Novel cd93 inhibitors |
| CN119528900B (zh) * | 2024-08-08 | 2026-03-13 | 河南科技大学 | 具有抗肝癌活性的甲基噻唑衍生物及其制备方法和应用 |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002105067A (ja) | 2000-09-28 | 2002-04-10 | Teijin Ltd | 2−フェニルチアゾール誘導体、およびそれを有効成分とする医薬組成物 |
| WO2006089076A2 (en) | 2005-02-18 | 2006-08-24 | Neurogen Corporation | Thiazole amides, imidazole amides and related analogues |
| JP2008534542A (ja) | 2005-03-31 | 2008-08-28 | ユセベ ファルマ ソシエテ アノニム | オキサゾール部分又はチアゾール部分を含む化合物、それらの製造方法及びそれらの使用 |
| JP2010037337A (ja) | 2008-07-09 | 2010-02-18 | Mitsubishi Tanabe Pharma Corp | 医薬組成物 |
| WO2010128163A2 (en) | 2009-05-08 | 2010-11-11 | Pike Pharma Gmbh | Small molecule inhibitors of influenza a and b virus and respiratory syncytial virus replication |
| WO2012073259A1 (en) | 2010-12-02 | 2012-06-07 | Indoco Remedies Limited | Novel process for the preparation of febuxostat |
| JP2018529653A (ja) | 2015-08-21 | 2018-10-11 | オートファジーサイエンシーズ インコーポレイテッド | 新規なカテコール誘導体およびこれを含む薬学的組成物 |
| CN110066258A (zh) | 2018-01-23 | 2019-07-30 | 湘北威尔曼制药股份有限公司 | 噻唑-5-甲酸衍生物及其制备方法与应用 |
| US20190336483A1 (en) | 2016-07-12 | 2019-11-07 | Industry-Academic Cooperation Foundation, Yonsei University | Autophagy enhancer and use thereof |
| WO2020017878A1 (en) | 2018-07-20 | 2020-01-23 | Hexapharmatec Co., Ltd. | Novel catechol derivatives or salt thereof, processes for preparing the same, and pharmaceutical compositions comprising the same |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20120131401A (ko) | 2011-05-25 | 2012-12-05 | 울산대학교 산학협력단 | 자가포식작용 촉진제의 신규 용도 |
| KR101731908B1 (ko) | 2015-08-18 | 2017-05-11 | 서울대학교산학협력단 | p62 ZZ 도메인에 결합하는 리간드 또는 아르기닌화된 BiP에 의해 매개되는 오토파지 활성을 통한 신경변성 질환 예방 및 치료 |
-
2020
- 2020-04-21 KR KR1020200048262A patent/KR102871918B1/ko active Active
-
2021
- 2021-01-15 CA CA3176088A patent/CA3176088A1/en active Pending
- 2021-01-15 JP JP2022564122A patent/JP7692002B2/ja active Active
- 2021-01-15 CN CN202180040070.8A patent/CN115667233B/zh active Active
- 2021-01-15 US US17/996,544 patent/US12503451B2/en active Active
- 2021-01-15 AU AU2021261570A patent/AU2021261570A1/en active Pending
- 2021-01-15 EP EP21792031.3A patent/EP4140989B1/en active Active
- 2021-01-15 ES ES21792031T patent/ES2987881T3/es active Active
- 2021-01-15 WO PCT/KR2021/000578 patent/WO2021215624A1/ko not_active Ceased
Patent Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002105067A (ja) | 2000-09-28 | 2002-04-10 | Teijin Ltd | 2−フェニルチアゾール誘導体、およびそれを有効成分とする医薬組成物 |
| WO2006089076A2 (en) | 2005-02-18 | 2006-08-24 | Neurogen Corporation | Thiazole amides, imidazole amides and related analogues |
| JP2008534542A (ja) | 2005-03-31 | 2008-08-28 | ユセベ ファルマ ソシエテ アノニム | オキサゾール部分又はチアゾール部分を含む化合物、それらの製造方法及びそれらの使用 |
| JP2010037337A (ja) | 2008-07-09 | 2010-02-18 | Mitsubishi Tanabe Pharma Corp | 医薬組成物 |
| WO2010128163A2 (en) | 2009-05-08 | 2010-11-11 | Pike Pharma Gmbh | Small molecule inhibitors of influenza a and b virus and respiratory syncytial virus replication |
| WO2012073259A1 (en) | 2010-12-02 | 2012-06-07 | Indoco Remedies Limited | Novel process for the preparation of febuxostat |
| JP2018529653A (ja) | 2015-08-21 | 2018-10-11 | オートファジーサイエンシーズ インコーポレイテッド | 新規なカテコール誘導体およびこれを含む薬学的組成物 |
| US20190336483A1 (en) | 2016-07-12 | 2019-11-07 | Industry-Academic Cooperation Foundation, Yonsei University | Autophagy enhancer and use thereof |
| CN110066258A (zh) | 2018-01-23 | 2019-07-30 | 湘北威尔曼制药股份有限公司 | 噻唑-5-甲酸衍生物及其制备方法与应用 |
| WO2020017878A1 (en) | 2018-07-20 | 2020-01-23 | Hexapharmatec Co., Ltd. | Novel catechol derivatives or salt thereof, processes for preparing the same, and pharmaceutical compositions comprising the same |
Non-Patent Citations (4)
| Title |
|---|
| Augmenting the Xanthine Oxidase Inhibitory Activity of Febuxostat by its Structural Modification,KURUVA, C. S. et al.,2014年,Vol.11, No.2,pp.207-210,DOI: 10.2174/15701808113109990056 |
| KILARU, R. B. et al.,Design, synthesis, in silico and in vitro studies of novel 4-methylthiazole-5-carboxylic acid derivatives as potent anti-cancer agents,Bioorganic & Medicinal Chemistry Letters,2014年,Vol.24, No.18,pp.4580-4585,DOI:10.1016/j.bmcl.2014.07.058 |
| Registry(STN)[online],2018年11月18日,p.1,[検索日 2024.10.09],CAS登録番号:2248935-86-4 |
| ZHU, Youquan,Design, Synthesis and Bioactivity of Novel 2-Aryl-4-alkylthiazole-5-carboxylic Acid Derivatives,Chinese Journal of Organic Chemistry,2012年,Vol.32, No.11,pp.2115~2121,DOI: 10.6023/cjoc201207004 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023523417A (ja) | 2023-06-05 |
| EP4140989A1 (en) | 2023-03-01 |
| KR20210130016A (ko) | 2021-10-29 |
| CN115667233B (zh) | 2024-05-24 |
| EP4140989C0 (en) | 2024-07-17 |
| EP4140989A4 (en) | 2023-10-18 |
| AU2021261570A1 (en) | 2022-12-08 |
| KR102871918B1 (ko) | 2025-10-17 |
| CA3176088A1 (en) | 2021-10-28 |
| CN115667233A (zh) | 2023-01-31 |
| US20230219908A1 (en) | 2023-07-13 |
| US12503451B2 (en) | 2025-12-23 |
| WO2021215624A1 (ko) | 2021-10-28 |
| ES2987881T3 (es) | 2024-11-18 |
| EP4140989B1 (en) | 2024-07-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3630755B1 (en) | 5-methyl-1,3,4-oxadiazol-2-yl compounds | |
| US10081625B2 (en) | 5-methyl-1,2,4-oxadiazol-3-yl compounds | |
| EP3268369A1 (en) | Anti-alphavbeta1 integrin inhibitors and methods of use | |
| CA2970546A1 (en) | Antimicrobial polymyxins for treatment of bacterial infections | |
| AU2018212436A1 (en) | Bis-heteroaryl derivatives as modulators of protein aggregation | |
| JP7692002B2 (ja) | 新規な2-アリールチアゾール誘導体またはその塩、その製造方法、及びそれを含む医薬組成物 | |
| KR20230106637A (ko) | 빈혈 및 암 치료용 vhl 억제제로서의 1-(2-(4-시클로프로필-1h-1,2,3-트리아졸-1-일)아세틸)-4-히드록시-n-(벤질)피롤리딘 e-2-카르복사미드 유도체 | |
| ES2653931T3 (es) | Tiazolo y oxazolo-pirimidinonas condensadas | |
| JP7371082B2 (ja) | 新規なカテコール誘導体またはその塩、その製造方法およびそれを含む医薬組成物 | |
| EP3037412A1 (en) | Indole amide compound as inhibitor of necrosis | |
| KR20090033583A (ko) | 글라이신 아릴 아마이드를 포함하는 신규한베타-세크리타제 저해용 화합물 | |
| RU2822057C1 (ru) | Новое производное 2-арилтиазола или его соль, способ его получения и содержащая его фармацевтическая композиция | |
| RU2795227C2 (ru) | Новые производные катехола или их соль, способы их получения и содержащие их фармацевтические композиции | |
| KR20090033752A (ko) | 인돌-사이아졸린을 포함하는 신규한 베타-세크리타제저해용 화합물 | |
| CA3250447A1 (en) | MACROCYCLIC PYRIMIDINE DERIVATIVE, ITS PREPARATION PROCESS, AND PHARMACEUTICAL COMPOSITION INTENDED FOR THE PREVENTION OR TREATMENT OF A NEURODEGENERATIVE DISEASE AND CONTAINING THIS DERIVATIVE AS AN ACTIVE INGREDIENT | |
| WO2024087783A1 (zh) | 一种gpr139受体激动剂、其制备方法及其应用 | |
| CN115433257A (zh) | 咪唑并哒嗪类双功能protac分子化合物及其制备和应用 | |
| KR20070031959A (ko) | 선택적 부티릴콜린에스테라제 저해제 | |
| NZ754849B2 (en) | N-[4-fluoro-5-[[(2s,4s)-2-methyl-4-[(5-methyl-1,2,4-oxadiazol-3-yl)methoxy]-1-piperidyl]methyl]thiazol-2-yl]acetamide as oga inhibitor | |
| BR112018001716B1 (pt) | Composto de derivado de 1,3,4-oxadiazol amida como inibidor de histona desacetilase 6 e composição farmacêutica contendo o mesmo | |
| KR20090034009A (ko) | 글라이신 모액을 포함하는 신규한 베타-세크리타제 저해용화합물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20221025 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231128 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20241031 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241105 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20241230 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250205 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250527 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250602 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7692002 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |