JP7569709B2 - サンプリング方法、及びサンプリング装置 - Google Patents
サンプリング方法、及びサンプリング装置 Download PDFInfo
- Publication number
- JP7569709B2 JP7569709B2 JP2021033666A JP2021033666A JP7569709B2 JP 7569709 B2 JP7569709 B2 JP 7569709B2 JP 2021033666 A JP2021033666 A JP 2021033666A JP 2021033666 A JP2021033666 A JP 2021033666A JP 7569709 B2 JP7569709 B2 JP 7569709B2
- Authority
- JP
- Japan
- Prior art keywords
- path
- sampling
- sample
- introduction
- branch
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000005070 sampling Methods 0.000 title claims description 186
- 238000000034 method Methods 0.000 title claims description 55
- 239000007788 liquid Substances 0.000 claims description 71
- 238000001514 detection method Methods 0.000 claims description 69
- 238000011144 upstream manufacturing Methods 0.000 claims description 22
- 238000012258 culturing Methods 0.000 claims description 5
- 230000009969 flowable effect Effects 0.000 claims 1
- 238000004140 cleaning Methods 0.000 description 34
- 230000007246 mechanism Effects 0.000 description 28
- 238000003860 storage Methods 0.000 description 27
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 26
- 230000008569 process Effects 0.000 description 25
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 24
- 239000001963 growth medium Substances 0.000 description 23
- 238000004113 cell culture Methods 0.000 description 20
- 239000002699 waste material Substances 0.000 description 20
- 210000004027 cell Anatomy 0.000 description 19
- 238000005259 measurement Methods 0.000 description 18
- 239000000243 solution Substances 0.000 description 18
- 239000012530 fluid Substances 0.000 description 15
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 13
- 239000008103 glucose Substances 0.000 description 13
- 239000012510 hollow fiber Substances 0.000 description 13
- 239000004310 lactic acid Substances 0.000 description 13
- 235000014655 lactic acid Nutrition 0.000 description 13
- 229910002092 carbon dioxide Inorganic materials 0.000 description 12
- 239000002609 medium Substances 0.000 description 8
- 238000010586 diagram Methods 0.000 description 7
- 239000012086 standard solution Substances 0.000 description 7
- 230000037452 priming Effects 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 239000007789 gas Substances 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 239000001569 carbon dioxide Substances 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 239000011148 porous material Substances 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 239000003855 balanced salt solution Substances 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- 239000002504 physiological saline solution Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- 239000003656 tris buffered saline Substances 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 238000007599 discharging Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
Images
Landscapes
- Sampling And Sample Adjustment (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Description
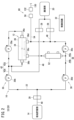
60、60A…サンプリング装置 64…サンプリング経路
68…コントローラ 75…検出部
130…サンプル導入経路 136…分岐経路
136A…第1分岐経路 136B…第2分岐経路
136C…第3分岐経路 137…合流経路
138…無菌フィルタ 138A…第1無菌フィルタ
138B…第2無菌フィルタ 138C…第3無菌フィルタ
144…切替部 144A…第1流通切替クランプ
144B…第2流通切替クランプ 144C…第3流通切替クランプ
146…圧力センサ 148…気泡センサ
Claims (9)
- 細胞を培養する培養装置から液体のサンプルを採取するサンプリング装置のサンプリング方法であって、
前記サンプリング装置は、
前記サンプルが流通するサンプリング経路と、
前記サンプリング経路に設けられ、前記サンプルの検出を行う検出部と、
前記培養装置と、前記検出部よりも上流側の前記サンプリング経路との間を接続するサンプル導入経路と、を備え、
前記サンプル導入経路は、複数の分岐経路と、前記複数の分岐経路毎に設けられた無菌フィルタと、を含み、
前記サンプリング方法は、
前記複数の分岐経路のうち一部を流通可能とする一方で、前記複数の分岐経路のうち他部を流通不能として、前記培養装置の前記サンプルを前記サンプリング経路に導入する第1導入工程と、
前記他部の分岐経路を流通可能とする一方で、前記一部の分岐経路を流通不能として、前記培養装置の前記サンプルを前記サンプリング経路に導入する第2導入工程と、
前記第1導入工程及び前記第2導入工程の前に、複数の前記無菌フィルタの詰まり状態に関わるフィルタ情報に基づいて前記一部の分岐経路の前記無菌フィルタが詰まっているか否かを判定し、前記一部の分岐経路の前記無菌フィルタが詰まっていないことを判定した場合には、前記第1導入工程に移行し、前記一部の分岐経路の前記無菌フィルタが詰まっていることを判定した場合には、前記第1導入工程に移行することなく前記フィルタ情報に基づいて前記他部の分岐経路の前記無菌フィルタが詰まっているか否かを判定し、前記他部の分岐経路の前記無菌フィルタが詰まっていないことを判定した場合には、前記第2導入工程に移行する選択工程と、を有する、
サンプリング方法。 - 請求項1記載のサンプリング方法において、
前記第1導入工程中に、前記一部の分岐経路の前記無菌フィルタが詰まっているか否かを判定する判定工程と、
前記判定工程において、前記一部の分岐経路の前記無菌フィルタが詰まっていることを判定した場合に、前記第1導入工程から前記第2導入工程に移行する
サンプリング方法。 - 請求項2記載のサンプリング方法において、
前記サンプリング装置は、前記サンプル導入経路内の圧力を検出する圧力センサを備え、
前記判定工程において、前記圧力センサの検出圧力が所定の圧力閾値を上回る場合に前記無菌フィルタが詰まっていると判定し、前記圧力センサの検出圧力が前記所定の圧力閾値以下の場合に前記無菌フィルタが詰まっていないと判定する
サンプリング方法。 - 請求項2又は3記載のサンプリング方法において、
前記サンプリング装置は、前記サンプル導入経路内の気泡を検出する気泡センサを備え、
前記判定工程において、前記気泡センサの検出気泡が所定量を上回る場合に前記無菌フィルタが詰まっていると判定し、前記気泡センサの検出気泡が前記所定量以下の場合に前記無菌フィルタが詰まっていないと判定する
サンプリング方法。 - 請求項1~4のいずれか1項に記載のサンプリング方法において、
前記複数の分岐経路は、3以上設けられ、
前記第1導入工程及び前記第2導入工程では、前記3以上の分岐経路のうちいずれか1つの分岐経路を流通可能とする一方で、前記1つの分岐経路以外の分岐経路全てを流通不能とする
サンプリング方法。 - 請求項1記載のサンプリング方法において、
前記サンプリング方法は、前記第1導入工程を所定期間実施した後、前記第1導入工程から前記第2導入工程に移行する
サンプリング方法。 - 細胞を培養する培養装置から液体のサンプルを採取するサンプリング装置であって、
前記サンプルが流通するサンプリング経路と、
前記サンプリング経路に設けられ、前記サンプルの検出を行う検出部と、
前記培養装置と、前記検出部よりも上流側の前記サンプリング経路との間を接続するサンプル導入経路と、
複数の分岐経路毎における前記サンプルの流通及び流通遮断を切り替える切替部と、
前記切替部を制御する制御部と、を備え、
前記サンプル導入経路は、前記複数の分岐経路と、前記複数の分岐経路毎に設けられた無菌フィルタと、を含み、
前記制御部は、
前記切替部を制御して、前記複数の分岐経路のうち一部を流通可能とする一方で、前記複数の分岐経路のうち他部を流通不能として、前記培養装置の前記サンプルを前記サンプリング経路に導入する第1導入工程と、
前記第1導入工程から前記切替部を切り替えることで、前記他部の分岐経路を流通可能とする一方で、前記一部の分岐経路を流通不能として、前記培養装置の前記サンプルを前記サンプリング経路に導入する第2導入工程と、
前記第1導入工程及び前記第2導入工程の前に、複数の前記無菌フィルタの詰まり状態に関わるフィルタ情報に基づいて前記一部の分岐経路の前記無菌フィルタが詰まっているか否かを判定し、前記一部の分岐経路の前記無菌フィルタが詰まっていないことを判定した場合には、前記第1導入工程に移行し、前記一部の分岐経路の前記無菌フィルタが詰まっていることを判定した場合には、前記第1導入工程に移行することなく前記フィルタ情報に基づいて前記他部の分岐経路の前記無菌フィルタが詰まっているか否かを判定し、前記他部の分岐経路の前記無菌フィルタが詰まっていないことを判定した場合には、前記第2導入工程に移行する選択工程と、を行う
サンプリング装置。 - 請求項7記載のサンプリング装置において、
前記切替部は、前記複数の分岐経路毎に配置された流通切替クランプにより構成される
サンプリング装置。 - 請求項7又は8記載のサンプリング装置において、
前記サンプル導入経路内の圧力を検出する圧力センサ、及び前記サンプル導入経路内の気泡を検出する気泡センサのうち少なくとも一方を備え、
前記制御部は、前記圧力センサの検出圧力又は前記気泡センサの検出気泡に基づき、前記第1導入工程から前記第2導入工程に切り替える
サンプリング装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021033666A JP7569709B2 (ja) | 2021-03-03 | 2021-03-03 | サンプリング方法、及びサンプリング装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021033666A JP7569709B2 (ja) | 2021-03-03 | 2021-03-03 | サンプリング方法、及びサンプリング装置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022134515A JP2022134515A (ja) | 2022-09-15 |
| JP7569709B2 true JP7569709B2 (ja) | 2024-10-18 |
Family
ID=83232002
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021033666A Active JP7569709B2 (ja) | 2021-03-03 | 2021-03-03 | サンプリング方法、及びサンプリング装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7569709B2 (ja) |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006034468A (ja) | 2004-07-23 | 2006-02-09 | Terumo Corp | フィルター監視システムおよび血小板採取装置 |
| JP2009095307A (ja) | 2007-10-18 | 2009-05-07 | Olympus Corp | 細胞処理容器および細胞処理装置 |
| US20090217777A1 (en) | 2008-03-03 | 2009-09-03 | Hanson William P | Analyte screening and detection systems and methods |
| JP2010081809A (ja) | 2008-09-29 | 2010-04-15 | Hitachi Plant Technologies Ltd | 培養装置及び培養方法 |
| JP2018038339A (ja) | 2016-09-08 | 2018-03-15 | 株式会社日立製作所 | 細胞分離装置および培養装置 |
| WO2019009044A1 (ja) | 2017-07-03 | 2019-01-10 | 株式会社村田製作所 | 濃縮装置 |
| WO2020152509A1 (en) | 2019-01-25 | 2020-07-30 | Enzene Biosciences Limited | Automated integrated continuous system and bioprocess for producing therapeutic protein |
-
2021
- 2021-03-03 JP JP2021033666A patent/JP7569709B2/ja active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006034468A (ja) | 2004-07-23 | 2006-02-09 | Terumo Corp | フィルター監視システムおよび血小板採取装置 |
| JP2009095307A (ja) | 2007-10-18 | 2009-05-07 | Olympus Corp | 細胞処理容器および細胞処理装置 |
| US20090217777A1 (en) | 2008-03-03 | 2009-09-03 | Hanson William P | Analyte screening and detection systems and methods |
| JP2010081809A (ja) | 2008-09-29 | 2010-04-15 | Hitachi Plant Technologies Ltd | 培養装置及び培養方法 |
| JP2018038339A (ja) | 2016-09-08 | 2018-03-15 | 株式会社日立製作所 | 細胞分離装置および培養装置 |
| WO2019009044A1 (ja) | 2017-07-03 | 2019-01-10 | 株式会社村田製作所 | 濃縮装置 |
| WO2020152509A1 (en) | 2019-01-25 | 2020-07-30 | Enzene Biosciences Limited | Automated integrated continuous system and bioprocess for producing therapeutic protein |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022134515A (ja) | 2022-09-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4212666B2 (ja) | 体液の分析装置 | |
| JP6998444B2 (ja) | 血液凝固検査システムおよび血液凝固検査システムの制御方法 | |
| US12492366B2 (en) | Biological component treatment system, biological component treatment device, and cell culturing method | |
| WO2007129463A2 (ja) | 生体成分測定装置及び生体成分測定装置の較正方法 | |
| JP7569709B2 (ja) | サンプリング方法、及びサンプリング装置 | |
| WO2021054280A1 (en) | Sensor calibration method and biological component treatment system | |
| ES2972580T3 (es) | Diagnóstico de sensor de medición de la concentración del dializado | |
| JP7818569B2 (ja) | サンプリング装置、及び細胞培養システム | |
| JP7756145B2 (ja) | サンプリング装置、及び細胞培養システム | |
| JP7818539B2 (ja) | サンプリング方法 | |
| JP7653434B2 (ja) | 細胞培養システム及び酵素センサの寿命判定方法 | |
| JP7830419B2 (ja) | サンプリング方法 | |
| JP7836693B2 (ja) | 細胞培養装置及び校正方法 | |
| EP4303294A1 (en) | Sampling device and cell cultivation system | |
| JP7781791B2 (ja) | サンプリング方法 | |
| JP7818538B2 (ja) | サンプリングシステム及びサンプリング方法 | |
| JP7527994B2 (ja) | サンプリングシステム | |
| JP2024500604A (ja) | 細胞培養システム | |
| US20240228930A9 (en) | Cell Culturing Device and Cell Culturing System | |
| CN117232902A (zh) | 一种可持续监测患者血气参数的系统及方法 | |
| JP2022118373A (ja) | サンプリングシステム及びサンプリング方法 | |
| JPH03118470A (ja) | 血液分析装置 | |
| JPH05154194A (ja) | 生化学物質の連続測定装置 | |
| JP2016106906A (ja) | 血液浄化システム |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231115 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240522 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240604 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240626 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241001 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241007 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7569709 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |