JP7546552B2 - ポリマーベースの高分子プロドラッグ - Google Patents
ポリマーベースの高分子プロドラッグ Download PDFInfo
- Publication number
- JP7546552B2 JP7546552B2 JP2021514531A JP2021514531A JP7546552B2 JP 7546552 B2 JP7546552 B2 JP 7546552B2 JP 2021514531 A JP2021514531 A JP 2021514531A JP 2021514531 A JP2021514531 A JP 2021514531A JP 7546552 B2 JP7546552 B2 JP 7546552B2
- Authority
- JP
- Japan
- Prior art keywords
- peg
- prodrug
- tumor
- treatment
- mice
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229940002612 prodrug Drugs 0.000 title claims description 99
- 239000000651 prodrug Substances 0.000 title claims description 99
- 229920000642 polymer Polymers 0.000 title description 53
- 206010028980 Neoplasm Diseases 0.000 claims description 97
- 206010029260 Neuroblastoma Diseases 0.000 claims description 89
- 238000011282 treatment Methods 0.000 claims description 59
- 239000000203 mixture Substances 0.000 claims description 8
- 239000000126 substance Substances 0.000 claims description 3
- FJHBVJOVLFPMQE-QFIPXVFZSA-N 7-Ethyl-10-Hydroxy-Camptothecin Chemical compound C1=C(O)C=C2C(CC)=C(CN3C(C4=C([C@@](C(=O)OC4)(O)CC)C=C33)=O)C3=NC2=C1 FJHBVJOVLFPMQE-QFIPXVFZSA-N 0.000 description 80
- 210000004027 cell Anatomy 0.000 description 48
- 241000699670 Mus sp. Species 0.000 description 46
- VSJKWCGYPAHWDS-FQEVSTJZSA-N camptothecin Chemical class C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-FQEVSTJZSA-N 0.000 description 42
- 229920001223 polyethylene glycol Polymers 0.000 description 36
- 239000002202 Polyethylene glycol Substances 0.000 description 35
- 238000002512 chemotherapy Methods 0.000 description 35
- 229920001983 poloxamer Polymers 0.000 description 34
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 33
- 229960004768 irinotecan Drugs 0.000 description 30
- UWKQSNNFCGGAFS-XIFFEERXSA-N irinotecan Chemical compound C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 UWKQSNNFCGGAFS-XIFFEERXSA-N 0.000 description 30
- 239000003814 drug Substances 0.000 description 26
- 230000003442 weekly effect Effects 0.000 description 26
- 229940079593 drug Drugs 0.000 description 25
- 210000003771 C cell Anatomy 0.000 description 21
- 241001465754 Metazoa Species 0.000 description 21
- 230000029918 bioluminescence Effects 0.000 description 19
- 238000005415 bioluminescence Methods 0.000 description 19
- 229960000502 poloxamer Drugs 0.000 description 19
- 230000004044 response Effects 0.000 description 18
- 239000003446 ligand Substances 0.000 description 17
- 230000004083 survival effect Effects 0.000 description 17
- 230000001225 therapeutic effect Effects 0.000 description 17
- 230000004663 cell proliferation Effects 0.000 description 14
- ABSNGNUGFQIDDO-UHFFFAOYSA-N 2-benzylguanidine Chemical compound NC(N)=NCC1=CC=CC=C1 ABSNGNUGFQIDDO-UHFFFAOYSA-N 0.000 description 13
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 13
- 108060001084 Luciferase Proteins 0.000 description 13
- 239000005089 Luciferase Substances 0.000 description 13
- -1 polyoxypropylene Polymers 0.000 description 13
- 230000035755 proliferation Effects 0.000 description 13
- 102000013013 Member 2 Subfamily G ATP Binding Cassette Transporter Human genes 0.000 description 12
- 108010090306 Member 2 Subfamily G ATP Binding Cassette Transporter Proteins 0.000 description 12
- 230000001028 anti-proliverative effect Effects 0.000 description 12
- 230000002601 intratumoral effect Effects 0.000 description 12
- 238000000034 method Methods 0.000 description 12
- 230000004962 physiological condition Effects 0.000 description 12
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 description 11
- 229960002748 norepinephrine Drugs 0.000 description 11
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 description 11
- 108010078791 Carrier Proteins Proteins 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- 230000002459 sustained effect Effects 0.000 description 10
- WAEXFXRVDQXREF-UHFFFAOYSA-N vorinostat Chemical compound ONC(=O)CCCCCCC(=O)NC1=CC=CC=C1 WAEXFXRVDQXREF-UHFFFAOYSA-N 0.000 description 10
- 229960000237 vorinostat Drugs 0.000 description 10
- KLWPJMFMVPTNCC-UHFFFAOYSA-N Camptothecin Natural products CCC1(O)C(=O)OCC2=C1C=C3C4Nc5ccccc5C=C4CN3C2=O KLWPJMFMVPTNCC-UHFFFAOYSA-N 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 229940127093 camptothecin Drugs 0.000 description 9
- VSJKWCGYPAHWDS-UHFFFAOYSA-N dl-camptothecin Natural products C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)C5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-UHFFFAOYSA-N 0.000 description 9
- 230000005764 inhibitory process Effects 0.000 description 9
- 208000006168 Ewing Sarcoma Diseases 0.000 description 8
- 201000010099 disease Diseases 0.000 description 8
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 8
- 238000003384 imaging method Methods 0.000 description 8
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 8
- 210000003462 vein Anatomy 0.000 description 8
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 7
- 230000004614 tumor growth Effects 0.000 description 7
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 239000002246 antineoplastic agent Substances 0.000 description 6
- 238000013459 approach Methods 0.000 description 6
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 6
- 230000003111 delayed effect Effects 0.000 description 6
- 230000012010 growth Effects 0.000 description 6
- 239000002243 precursor Substances 0.000 description 6
- 239000011780 sodium chloride Substances 0.000 description 6
- MYQKIWCVEPUPIL-QFIPXVFZSA-N 7-ethylcamptothecin Chemical compound C1=CC=C2C(CC)=C(CN3C(C4=C([C@@](C(=O)OC4)(O)CC)C=C33)=O)C3=NC2=C1 MYQKIWCVEPUPIL-QFIPXVFZSA-N 0.000 description 5
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 5
- 210000000577 adipose tissue Anatomy 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 229940127089 cytotoxic agent Drugs 0.000 description 5
- 230000002708 enhancing effect Effects 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 230000009036 growth inhibition Effects 0.000 description 5
- 230000002401 inhibitory effect Effects 0.000 description 5
- 230000014759 maintenance of location Effects 0.000 description 5
- QHFSFXIJOPKPMS-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine;4-methylbenzenesulfonic acid Chemical compound CN(C)C1=CC=CC=[NH+]1.CC1=CC=C(S([O-])(=O)=O)C=C1 QHFSFXIJOPKPMS-UHFFFAOYSA-N 0.000 description 5
- 210000000056 organ Anatomy 0.000 description 5
- 229920001451 polypropylene glycol Polymers 0.000 description 5
- 206010006895 Cachexia Diseases 0.000 description 4
- 206010012735 Diarrhoea Diseases 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 4
- 230000009471 action Effects 0.000 description 4
- 239000012190 activator Substances 0.000 description 4
- 230000001919 adrenal effect Effects 0.000 description 4
- 208000022531 anorexia Diseases 0.000 description 4
- 230000001093 anti-cancer Effects 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000003054 catalyst Substances 0.000 description 4
- 206010061428 decreased appetite Diseases 0.000 description 4
- 230000008034 disappearance Effects 0.000 description 4
- INVTYAOGFAGBOE-UHFFFAOYSA-N entinostat Chemical compound NC1=CC=CC=C1NC(=O)C(C=C1)=CC=C1CNC(=O)OCC1=CC=CN=C1 INVTYAOGFAGBOE-UHFFFAOYSA-N 0.000 description 4
- 229950005837 entinostat Drugs 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 229940121372 histone deacetylase inhibitor Drugs 0.000 description 4
- 239000003276 histone deacetylase inhibitor Substances 0.000 description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 4
- 230000001965 increasing effect Effects 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000011081 inoculation Methods 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 239000013642 negative control Substances 0.000 description 4
- 239000013641 positive control Substances 0.000 description 4
- 208000037922 refractory disease Diseases 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 231100000057 systemic toxicity Toxicity 0.000 description 4
- 230000008685 targeting Effects 0.000 description 4
- 230000001052 transient effect Effects 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 3
- PTJWCLYPVFJWMP-UHFFFAOYSA-N 2-[[3-hydroxy-2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol Chemical group OCC(CO)(CO)COCC(CO)(CO)COCC(CO)(CO)CO PTJWCLYPVFJWMP-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 102100025064 Cellular tumor antigen p53 Human genes 0.000 description 3
- 229940123780 DNA topoisomerase I inhibitor Drugs 0.000 description 3
- 206010059866 Drug resistance Diseases 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 238000005481 NMR spectroscopy Methods 0.000 description 3
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 3
- 239000000365 Topoisomerase I Inhibitor Substances 0.000 description 3
- 230000000259 anti-tumor effect Effects 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 201000011510 cancer Diseases 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 239000013604 expression vector Substances 0.000 description 3
- 238000007306 functionalization reaction Methods 0.000 description 3
- 230000004927 fusion Effects 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 210000004185 liver Anatomy 0.000 description 3
- 230000007774 longterm Effects 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 230000001394 metastastic effect Effects 0.000 description 3
- 206010061289 metastatic neoplasm Diseases 0.000 description 3
- 230000003647 oxidation Effects 0.000 description 3
- 238000007254 oxidation reaction Methods 0.000 description 3
- 230000000144 pharmacologic effect Effects 0.000 description 3
- 229920001993 poloxamer 188 Polymers 0.000 description 3
- 230000003389 potentiating effect Effects 0.000 description 3
- 230000035945 sensitivity Effects 0.000 description 3
- 210000000952 spleen Anatomy 0.000 description 3
- 230000002269 spontaneous effect Effects 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 229960004964 temozolomide Drugs 0.000 description 3
- 230000004584 weight gain Effects 0.000 description 3
- 235000019786 weight gain Nutrition 0.000 description 3
- 238000012447 xenograft mouse model Methods 0.000 description 3
- GWKLNCUXOUHWLL-UHFFFAOYSA-N 2-(2-phenylethyl)guanidine Chemical compound NC(=N)NCCC1=CC=CC=C1 GWKLNCUXOUHWLL-UHFFFAOYSA-N 0.000 description 2
- 208000003174 Brain Neoplasms Diseases 0.000 description 2
- 206010061818 Disease progression Diseases 0.000 description 2
- 208000014061 Extranodal Extension Diseases 0.000 description 2
- 102100039996 Histone deacetylase 1 Human genes 0.000 description 2
- 101001035024 Homo sapiens Histone deacetylase 1 Proteins 0.000 description 2
- 206010061598 Immunodeficiency Diseases 0.000 description 2
- 241000699660 Mus musculus Species 0.000 description 2
- 101150108975 Rhd gene Proteins 0.000 description 2
- 206010040943 Skin Ulcer Diseases 0.000 description 2
- 108700019146 Transgenes Proteins 0.000 description 2
- WGLPBDUCMAPZCE-UHFFFAOYSA-N Trioxochromium Chemical compound O=[Cr](=O)=O WGLPBDUCMAPZCE-UHFFFAOYSA-N 0.000 description 2
- DZGWFCGJZKJUFP-UHFFFAOYSA-N Tyramine Natural products NCCC1=CC=C(O)C=C1 DZGWFCGJZKJUFP-UHFFFAOYSA-N 0.000 description 2
- 208000025865 Ulcer Diseases 0.000 description 2
- 108700022368 Whn Proteins 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 125000002843 carboxylic acid group Chemical group 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 208000011654 childhood malignant neoplasm Diseases 0.000 description 2
- 238000011254 conventional chemotherapy Methods 0.000 description 2
- 238000011443 conventional therapy Methods 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 230000002900 effect on cell Effects 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 230000000977 initiatory effect Effects 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- OAOSXODRWGDDCV-UHFFFAOYSA-N n,n-dimethylpyridin-4-amine;4-methylbenzenesulfonic acid Chemical compound CN(C)C1=CC=NC=C1.CC1=CC=C(S(O)(=O)=O)C=C1 OAOSXODRWGDDCV-UHFFFAOYSA-N 0.000 description 2
- ITJNARMNRKSWTA-UHFFFAOYSA-N nisoxetine Chemical compound C=1C=CC=CC=1C(CCNC)OC1=CC=CC=C1OC ITJNARMNRKSWTA-UHFFFAOYSA-N 0.000 description 2
- 229950004211 nisoxetine Drugs 0.000 description 2
- 238000011580 nude mouse model Methods 0.000 description 2
- 230000035515 penetration Effects 0.000 description 2
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 2
- 230000002093 peripheral effect Effects 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 229920001992 poloxamer 407 Polymers 0.000 description 2
- 238000011127 radiochemotherapy Methods 0.000 description 2
- 230000000306 recurrent effect Effects 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 231100000019 skin ulcer Toxicity 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- MHYGQXWCZAYSLJ-UHFFFAOYSA-N tert-butyl-chloro-diphenylsilane Chemical compound C=1C=CC=CC=1[Si](Cl)(C(C)(C)C)C1=CC=CC=C1 MHYGQXWCZAYSLJ-UHFFFAOYSA-N 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 238000011830 transgenic mouse model Methods 0.000 description 2
- 229960003732 tyramine Drugs 0.000 description 2
- DZGWFCGJZKJUFP-UHFFFAOYSA-O tyraminium Chemical compound [NH3+]CCC1=CC=C(O)C=C1 DZGWFCGJZKJUFP-UHFFFAOYSA-O 0.000 description 2
- 230000036269 ulceration Effects 0.000 description 2
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 101100087409 Arabidopsis thaliana RH18 gene Proteins 0.000 description 1
- 101100468589 Arabidopsis thaliana RH30 gene Proteins 0.000 description 1
- 208000031648 Body Weight Changes Diseases 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 230000005778 DNA damage Effects 0.000 description 1
- 231100000277 DNA damage Toxicity 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 238000010268 HPLC based assay Methods 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 108700012912 MYCN Proteins 0.000 description 1
- 101150022024 MYCN gene Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- 108700026495 N-Myc Proto-Oncogene Proteins 0.000 description 1
- 102100030124 N-myc proto-oncogene protein Human genes 0.000 description 1
- 238000011887 Necropsy Methods 0.000 description 1
- 108010049586 Norepinephrine Plasma Membrane Transport Proteins Proteins 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 230000018199 S phase Effects 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 102100033929 Sodium-dependent noradrenaline transporter Human genes 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 206010066901 Treatment failure Diseases 0.000 description 1
- 238000010162 Tukey test Methods 0.000 description 1
- 102000015098 Tumor Suppressor Protein p53 Human genes 0.000 description 1
- 108010078814 Tumor Suppressor Protein p53 Proteins 0.000 description 1
- 238000010811 Ultra-Performance Liquid Chromatography-Tandem Mass Spectrometry Methods 0.000 description 1
- 241000021375 Xenogenes Species 0.000 description 1
- ZULJYVVAYGFYKU-UHFFFAOYSA-N acetonitrile;chloroform Chemical compound CC#N.ClC(Cl)Cl ZULJYVVAYGFYKU-UHFFFAOYSA-N 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 231100000899 acute systemic toxicity Toxicity 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 210000004100 adrenal gland Anatomy 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 230000004579 body weight change Effects 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000012829 chemotherapy agent Substances 0.000 description 1
- 229940044683 chemotherapy drug Drugs 0.000 description 1
- 208000012191 childhood neoplasm Diseases 0.000 description 1
- 210000000028 corpus adiposum pararenale Anatomy 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000002498 deadly effect Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 231100000517 death Toxicity 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 230000009429 distress Effects 0.000 description 1
- 239000003534 dna topoisomerase inhibitor Substances 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 230000002888 effect on disease Effects 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 230000007608 epigenetic mechanism Effects 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 238000009093 first-line therapy Methods 0.000 description 1
- 210000000609 ganglia Anatomy 0.000 description 1
- 230000024924 glomerular filtration Effects 0.000 description 1
- ZRALSGWEFCBTJO-UHFFFAOYSA-N guanidine group Chemical group NC(=N)N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- ZFGMDIBRIDKWMY-PASTXAENSA-N heparin Chemical compound CC(O)=N[C@@H]1[C@@H](O)[C@H](O)[C@@H](COS(O)(=O)=O)O[C@@H]1O[C@@H]1[C@@H](C(O)=O)O[C@@H](O[C@H]2[C@@H]([C@@H](OS(O)(=O)=O)[C@@H](O[C@@H]3[C@@H](OC(O)[C@H](OS(O)(=O)=O)[C@H]3O)C(O)=O)O[C@@H]2O)CS(O)(=O)=O)[C@H](O)[C@H]1O ZFGMDIBRIDKWMY-PASTXAENSA-N 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- CBOIHMRHGLHBPB-UHFFFAOYSA-N hydroxymethyl Chemical group O[CH2] CBOIHMRHGLHBPB-UHFFFAOYSA-N 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 108010082117 matrigel Proteins 0.000 description 1
- 231100000682 maximum tolerated dose Toxicity 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 230000035407 negative regulation of cell proliferation Effects 0.000 description 1
- 201000011519 neuroendocrine tumor Diseases 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- 208000037821 progressive disease Diseases 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- GRJJQCWNZGRKAU-UHFFFAOYSA-N pyridin-1-ium;fluoride Chemical compound F.C1=CC=NC=C1 GRJJQCWNZGRKAU-UHFFFAOYSA-N 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 230000003307 reticuloendothelial effect Effects 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 238000011301 standard therapy Methods 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 235000011149 sulphuric acid Nutrition 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000002626 targeted therapy Methods 0.000 description 1
- GOQZIPJCBUYLIR-UHFFFAOYSA-N tert-butyl n-[n-[(2-methylpropan-2-yl)oxycarbonyl]-n'-(trifluoromethylsulfonyl)carbamimidoyl]carbamate Chemical compound CC(C)(C)OC(=O)NC(=NS(=O)(=O)C(F)(F)F)NC(=O)OC(C)(C)C GOQZIPJCBUYLIR-UHFFFAOYSA-N 0.000 description 1
- 125000000037 tert-butyldiphenylsilyl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1[Si]([H])([*]C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- UEUXEKPTXMALOB-UHFFFAOYSA-J tetrasodium;2-[2-[bis(carboxylatomethyl)amino]ethyl-(carboxylatomethyl)amino]acetate Chemical compound [Na+].[Na+].[Na+].[Na+].[O-]C(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CC([O-])=O UEUXEKPTXMALOB-UHFFFAOYSA-J 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
- 229940044693 topoisomerase inhibitor Drugs 0.000 description 1
- 229960000303 topotecan Drugs 0.000 description 1
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 description 1
- 231100000440 toxicity profile Toxicity 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 229920000428 triblock copolymer Polymers 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 230000005748 tumor development Effects 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 208000016261 weight loss Diseases 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
本出願は、2018年9月17日に提出された米国仮出願第62/732,199号の出願日の利益を主張しており、その内容はすべての目的のためにその全体が参照により本明細書に組み込まれる。
カンプトテシン類似体が、生理学的条件下で不安定なエステル結合を介してポリマーに共有結合している高分子プロドラッグが提供される。高分子プロドラッグを用いて、癌、特に神経芽細胞腫を治療する方法も提供される。
第1の実施態様において、その中のカンプトテシン類似体の少なくとも2つの分子が、生理学的条件下(例えば22℃、pH=7.2)で不安定なエステル結合を介してポロキサマーポリマーに共有結合している、高分子プロドラッグが提供される。
別の実施態様において、ポリマーは、ポリエチレングリコール(PEG)ポリマーである。
別の実施態様において、ポリマーはマルチアームPEGポリマーである。
別の実施態様において、カンプトテシン類似体の4つの分子はポリマーに共有結合している。
別の実施態様において、カンプトテシン類似体の2~8つの分子はポリマーに共有結合している。
別の実施態様において、NEトランスポーター(NET)リガンドは、生理学的条件下で不安定であるエステル結合を介してカンプトテシン類似体に共有結合している。
別の実施態様において、カンプトテシン類似体はSN-38である。
別の実施態様において、NEトランスポーター(NET)リガンドは、フェネチルグアニジン又はチラミンである。
別の実施態様において、NEトランスポーター(NET)リガンドとカンプトテシン類似体とのエステル結合は、オキシエトキシプロパノイル又はオキシエトキシエトキシプロパノイルエステルである。
別の実施態様において、高分子プロドラッグはPF108-(SN22)2である。
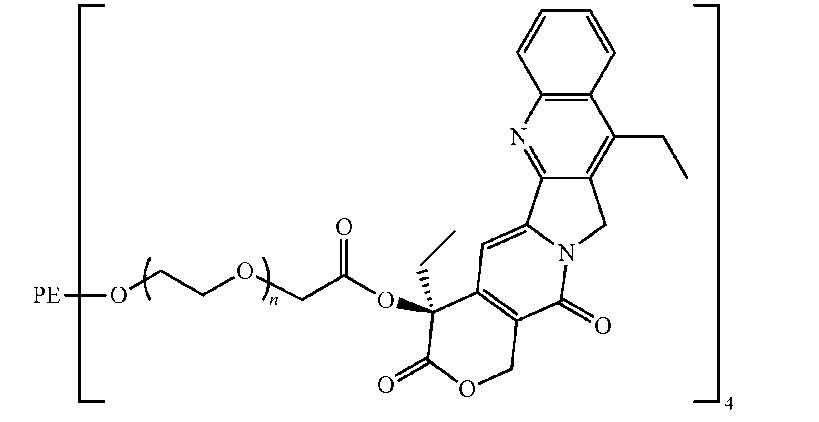
別の実施態様において、高分子プロドラッグはPEG-[SN22]4である。
別の実施態様において、エステル結合はオキシ酢酸エステル結合である。
別の実施態様において、上記で定義された高分子プロドラッグの有効量を、それを必要とする被験体に投与することにより、固形腫瘍を有する被験体を治療する方法が提供される。
別の実施態様において、上記で定義された高分子プロドラッグの有効量を、それを必要とする被験体に投与することにより、脳腫瘍を有する被験体を治療する方法が提供される。
別の実施態様において、上記で定義された高分子プロドラッグの有効量を、それを必要とする被験体に投与することにより、癌を治療する方法が提供される。
第1の実施態様
上記のプロドラッグの第1の実施態様において、カンプトテシン類似体の少なくとも2つの分子は、生理学的条件下(例えば22℃、pH=7.2)で不安定なエステル結合を介して、ポロキサマーポリマーに共有結合している。
上記プロドラッグの第2の実施態様において、SN22類似体の少なくとも2つの分子は、生理学的条件下で不安定であるエステル結合を介してPEGポリマーに共有結合している。
上記のプロドラッグの第3の実施態様において、カンプトテシン類似体の少なくとも2つの分子は、生理学的条件下で不安定であるエステル結合を介してポリマーに共有結合しており、ここで、少なくとも1つのカンプトテシン類似体は、少なくとも1つのNEトランスポーター(NET)リガンドで官能基化される。
上記のように、高分子プロドラッグは、有効量の高分子プロドラッグを、それを必要とする被験体に投与することにより、神経芽細胞腫を治療する方法において使用することができる。
PF108-(SN22)2
1. 2工程のプロドラッグ合成
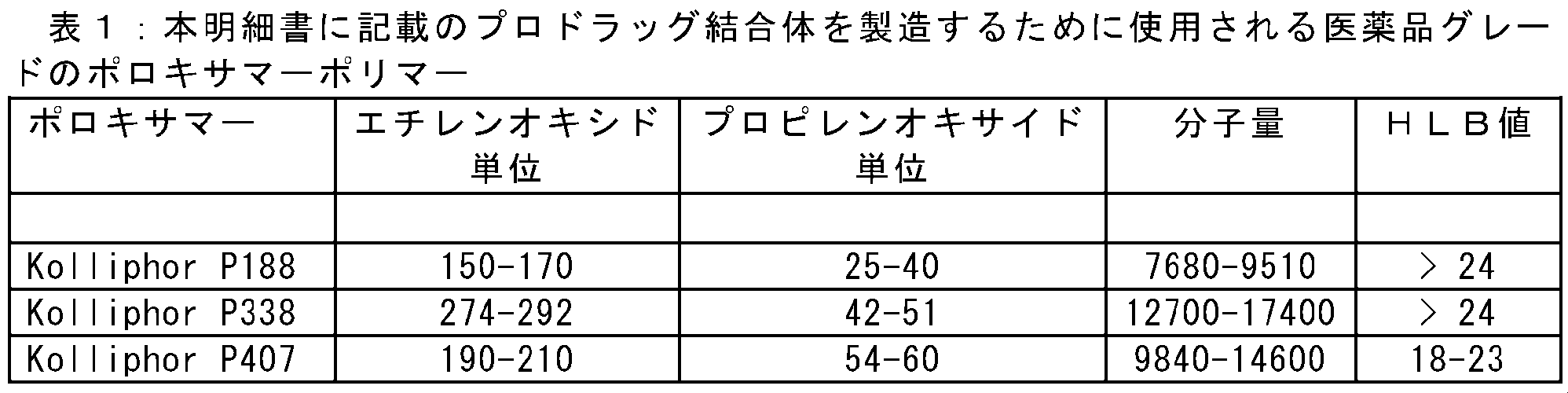
22~25°CのTHF中のジョーンズ試薬(CrO3/H2SO4)によるポロキサマーの酸化は、ポリマーの末端CH2OHを末端アルコキシアセテートカルボン酸基に変換し、これは次に、加水分解性エステル結合を介して種々のヒドロキシル含有薬物の可逆的共有結合に使用することができる。上記の条件下のプルロニックF-108(Kolliphor P338)の酸化は、OCH2COプロトンのシグナルにより1H NMRを使用して測定すると、0.18mmol/gのカルボキシル基を含むポリマーの結果を得た。同様に、プルロニックF-68の酸化は、0.23mmol/gの末端カルボン酸基を含むポリマーを与えた。カルボキシル基の活性化剤として1,3-ジシクロヘキシルカルボジイミド(DCC)、触媒として4-ジメチルアミノピリジントシレート(DPTS)、そして溶媒としてCH2Cl2を使用して、カルボキシル化プルロニックF-108をSN22とさらに結合させると、0.13mmol/g又は4.8重量%の薬物を含むポリマー結合体が形成された。1H NMRは、SN-22が、カルボキシル化プルロニックのカルボキシル基とSN22分子の20-OHとのエステル結合を介して、ポリマーに共有結合していることを示した。Kolliphorグレードのプルロニック(表1)及びSN22(純度:≧97%、HPLC)を、それぞれSigma-Aldrich (St. Louis, MO) 及び AK Scientific (Union City, CA)から購入した。
難治性NBは、NB細胞の増殖を阻害するために必要な薬物閾値レベルのシフトを特徴としている。導入治療中と治療前の診断時の進行性疾患の同じ患者に由来する、試験されたすべての細胞株の対で示されるこのシフトは、異なる化学的及び薬理学的ファミリーからの化学療法剤への応答に、同時に影響を与える。医薬品グレードのプルロニックF-108(kolliphor P338)とSN22から構築されたプロドラッグであるPF108-(SN22)2を、コドン135上のTP53変異の獲得とp53機能の喪失に関連する薬剤耐性表現型を示すBE(2)C細胞株に対して試験した。
化学放射線療法後の再発時に由来するBE(2)C細胞と、診断時の同じ患者に由来するBE(1)細胞との比較により、細胞増殖阻害を達成するために必要なカンプトテシン類似体SN38の濃度が、桁違いに90%(それぞれ25対2ng/ml)上昇することが証明された。重要なことに、SN38の対応する腫瘍内レベルは、その前駆体であるイリノテカン(CPT-11)による従来の治療を使用しては維持できないことが示された。最大許容量を超えずに有効な局所薬物レベルを維持できないことが、再発性及び難治性の高リスクNBの状況で、臨床的に使用されるカンプトテシン及び他の化学療法剤の効かない主な原因である。これらの報告と一致して、これらの結果は、イリノテカン(10mg/kg)の投与後それぞれ24時間及び72時間に、大きな(≧1cm3)BE(2)C同所性異種移植片で25ng/g及び2ng/g未満のSN38を示している。比較すると、PF108-(SN22)2と同等の用量で送達されたSN22は、腫瘍内に数倍高いレベルで安定して存在し、4、24、72時間目にそれぞれ2180±850ng/g、2140±520ng/g、及び1570±580ng/g(図2)であり、ポロキサマープロドラッグベースの送達が、SN22の安定した治療上有効なレベルを維持できることを示唆し、従って持続的なNB腫瘍増殖抑制の必要性に対処している。
1.5μg/gを超える腫瘍内レベルでの持続的な存在に一致して、ポロキサマーベースのプロドラッグとして週に1回処方及び投与されたSN22は、腫瘍の退縮を引き起こし、同所性BE(2)C異種移植片の再増殖を強力に抑制した(図3A及びB)。これは、著しく延長された動物の生存期間を意味し(図3C)、この試験で2倍頻繁に投与されたイリノテカンではわずかな抗腫瘍効果しかなかったこととは対照的である。このNBモデルにおけるイリノテカンのわずかな効果(図3)は、攻撃的で難治性のヒトNBの状況で持続的な治療応答を達成する上で重要な課題を再現する前臨床評価アプローチの妥当性を示している。特に、イリノテカンとは異なり、PF108-(SN22)2は腫瘍の縮小と疾患の安定化の両方を引き起こすことができ、週1回の投与を4週間(PF108-(SN22)2の最終投与は21日目;図3Bに示される)のみからなる治療期間中及びそれ以降の進行は観察されなかった。ポロキサマー-SN22プロドラッグの顕著な抗癌作用は、下痢、皮膚テンティング(脱水症による)、皮膚潰瘍、食欲不振、悪液質、又は体重増加遅延などの全身毒性の兆候を伴っていなかった。
独特の(化学療法未経験対化学療法抵抗性)表現型を有するNB細胞に対する高分子プロドラッグの抗増殖効果を比較研究する実行性を証明するために、治療開始前と集中的な化学放射線療法後の再発時の、攻撃的なMYCN増幅疾患を表す2つの細胞株(それぞれIMR-32及びBE(2)C)に対するPF108-(SN22)2の効果を比較した。
ポロキサマーベースのプロドラッグを使用する送達アプローチの有効性は、PF108-(SN22)2結合体として投与されたSN22の急速な腫瘍取り込みと持続的な腫瘍内保持を示すデータによって証明される(図2及び5)。PF108-(SN22)2は、化学療法抵抗性NB細胞の増殖を抑制するのに必要な報告された有効局所濃度よりも約2桁高いレベルで、同所性NB腫瘍における薬物存在時間の延長を達成する。
大小のNB腫瘍に対して持続的な抗癌効果を提供するポロキサマーベースのプロドラッグ戦略の有効性は、PF108-(SN22)2の週1回の投与処方で実験的に証明された(同所性IMR-32異種移植モデル、図6)。特に、化学療法を受けていない表現型にもかかわらず、MYCN増幅IMR-32細胞で確立された同所性NB腫瘍は、イリノテカンに対して一過性の応答しか示さなかった(週に2回投与)。難治性疾患のBE(2)C異種移植モデルにおけるプロドラッグアプローチの有効性を示す結果(図3)とともに、これは、従来の化学療法に対して限定的な応答を示すか又は応答しない高リスクNBの状況におけるポロキサマープロドラッグベースの送達を支持する強力な証拠を提供する。
PEG-[SN22]4
1. PEGの合成-[SN22]4
カルボキシル基の活性化剤として1,3-ジシクロヘキシルカルボジイミド(DCC)、触媒として4-ジメチルアミノピリジントシレート(DPTS)、そして溶媒としてCH2Cl2を使用して、カルボキシル化4-アーム-PEG(JenKem Technology、Mn=20,553Da)をSN22と結合させると、0.17mmol/g又は6.4重量%の薬物を含むポリマー結合体が形成された。1H NMRは、SN-22がカルボキシル化ポリマーのカルボキシル基とSN22の20-OHとのエステル結合によってポリマーに共有結合していることを示した。
ABCG2流出に対するSN38及びSN22の感受性を評価するために、ABCG2ヌルNB細胞株であるNLFが同定された。NLFにABCG2発現ベクターをトランスフェクトした後、痕跡レベル、低レベル、及び中レベルのABCG2発現を有する単一細胞クローンを選択した(図7A)。次に、異なる濃度のSN38又はSN22に対するNLF及びABCG2発現クローンの感受性と、IncuCyte(登録商標)S3生細胞分析システムを使用して継続的に追跡した増殖を評価した。高レベルのABCG2を有するクローンは、SN38に対する耐性が上昇したが、SN22に対しては完全に感受性のままであった(図7B)。これは、攻撃的なNB及びNB幹細胞を特徴付ける内因性ABCG2発現が、イリノテカン/SN38、及びおそらくABCG2流出に感受性の他の化学療法剤に対する薬剤耐性に寄与することを示唆している。
[PEG-SN38-BG]8
1. 3成分ポリマーベースのプロドラッグ合成
本明細書に記載のプロドラッグは、インサイチュで切断可能なエステル結合を介して、それぞれマルチアーム又は線形PEG担体に結合した8つ又は2つの薬物-リガンドハイブリッド分子を有する。これらの加水分解不安定性及び活性化率は、アルコキシアセチル基の強い電子置換効果のために、通常の(アシル)エステルのものと比較して上昇している。
1kgあたり10mgのSN-38に相当する同等用量で、8アームのPEGベースの及びBG官能基化プロドラッグ[PEG-SN38-BG]8として送達されたSN-38は、腫瘍内に何倍も高濃度(1時間、4時間、24時間目にそれぞれ2.82±0.53μg/g、4.46±1.59μg/g、2.63±0.85μg/g(図11))で安定して存在しており、標準的な治療に応答しない難治性腫瘍の増殖を抑制するために必要な安定な治療上有効な薬物レベルを提供できることを示唆した。
トポイソメラーゼI阻害剤とほとんど重複しない毒性プロフィールを有する強力な汎HDAC阻害剤であるボリノスタットは、DNA切断修復酵素の発現を阻害し、DNA損傷により誘発されるアポトーシスを促進することにより、NB腫瘍におけるNET発現を実質的に増加させ、腫瘍細胞をカンプトテシン薬に感作させることが示され[44]、どちらの効果も、SN-38のBG官能基化プロドラッグによる神経内分泌腫瘍の標的化療法の強化に関連している。[PEG-SN38-BG]8対SN-38によるBE(2)C細胞増殖阻害に対するボリノスタットの増強効果を調べた。
プロドラッグ構造に組み込まれた標的リガンドの特異的寄与を評価するために、NETを発現する化学療法抵抗性NB細胞に対する[PEG-SN38-BG]8の細胞増殖阻害活性を、同様に構築されたがBG部分を含まない対照分子[PEG-SN38]8と比較した。さらにNB細胞及び腫瘍異種移植片において、NET発現をアップレギュレートし取り込み-1を増強することが示された汎HDAC阻害剤が、NET発現NB細胞に対する[PEG-SN38-BG]8の抗増殖効果を強力に増強する(図13)ことが確立されたため、HDタイプ1サブファミリーに特異的な選択的HDAC阻害剤(エンチノスタット)も[PEG-SN38-BG]8と相乗作用するという仮説が取り上げられた。
プロドラッグベースの治療戦略の有効性は、[PEG-SN38-BG]83成分プロドラッグとして送達されたSN-38の急速な腫瘍取り込みと持続的な腫瘍内保持を示す試験で証明された(図11及び表2)。その臨床的に使用される薬理学的に不活性な前駆体(イリノテカン)の形で投与されたSN-38とは対照的に、プロドラッグベースの送達は、化学療法抵抗性NB細胞であるBE(2)Cの増殖を抑制するために必要な報告されたSN-38の濃度よりも約2桁高いレベルで、SN-38の局在化と持続的な腫瘍内存在を達成する。この分析は、HPLCアッセイを使用して、大きな同所性BE(2)C異種移植片(1.0±0.4cm3、n=5)で行われた。
攻撃的なNB腫瘍に対して持続的な抗癌効果を提供することにおける3成分プロドラッグ戦略の有効性は、同所性IMR-32異種移植モデルで実験的に証明された(図15)。週2回で4週間にわたって投与された[PEG-SN38-BG]8は、化学療法を受けていないMYCN増幅疾患のモデルでは、その後の再増殖を伴わずに急速な腫瘍縮小を引き起した。これは、SN-38前駆体であるイリノテカンで治療された動物群で治療中止直後に腫瘍が再増殖し始めるのとは対照的である(図15A、B)。難治性疾患のBE(2)C異種移植モデルにおけるプロドラッグアプローチの有効性を示す結果(図12)とともに、これは、従来の化学療法に対して限定された応答を示すか又は応答を示さない高リスクNBの状況で、3成分プロドラッグベースの送達を支持する強力な証拠を提供する。
ノルエピネフリントランスポーター(NET)を標的としたポリマー結合プロドラッグとして配合され4週間(週2回)にわたって投与されたSN-38は、急速な腫瘍退縮を引き起こし、化学療法抵抗性の同所性BE(2)C異種移植片の再増殖を完全に抑制し、無再発生存期間を著しく延長した(>14週間、図16A)。これは、このモデルにおいて抗腫瘍効果を持たないイリノテカンとは対照的であり、治療期間中のみ腫瘍増殖のみを阻害した2成分対照[PEG-SN38]4に対して劇的な改善でもある(図16A)。さらに、イリノテカンで治療中に急速に大きな腫瘍(2cm3)を発症した動物を[PEG-SN38-BG]8に切り替えると、腫瘍が縮小し、12週間以上検出されないままであった(「レスキュー試験」、図16B)。
播種性化学療法抵抗性NBに対する持続的な治療効果を達成することにおける3成分プロドラッグベースのNET標的化薬剤送達の有効性を、転移性で難治性疾患のマウスモデルで評価した(図18)。4週間にわたって投与された[PEG-SN38-BG]8は、確立された多発性腫瘍沈着物を急速に排除し、15週間を超えて検出可能な再増殖は見られなかった。対照的に、15mg/kgの用量で週2回投与されたイリノテカンは、疾患の進行に有意な影響を及ぼさなかった(図18A、B)。同所性の難治性腫瘍に対するNET標的化3成分プロドラッグの実験的に証明された有効性(図16)と合わせると、これらの結果は、プロドラッグ設計戦略の理論的根拠と、従来の治療法に応答しない局所的及び播種性の両方の高リスク疾患に対するその治療可能性を強く支持する。
化学療法抵抗性のNB細胞[BE(2)C]を、NET標的化3成分プロドラッグ(PF68-SN38-BG)で治療したときと、非標的化2成分対照(PF68-SN38)及び遊離SN-38で治療したときに、応答パターンに大きな違いが観察された。p53機能の喪失を示すBE(2)Cの化学療法抵抗性の表現型に一致して、BE(2)C細胞の増殖は遊離SN-38によってわずかに阻害された。これはまた、PF68-SN38に対しては限定的かつ一時的な応答を示した。ブランクのプルロニックF-68は細胞増殖に影響を与えなかった。しかし、5nM以上の用量のSN-38でPF68-SN38-BGに15分間曝露すると、強力で持続的な抗増殖効果が得られた(図19)。
同所性NB異種移植片において、化学療法抵抗性NB株SKNBE(2)Cを用いて、PEG-[SN22]4をPEG-[SN38]4と比較した。BE(2)C細胞にルシフェラーゼ発現ベクターをトランスフェクトして、生物発光イメージングを可能にした。マウスを週1回で4週間、PEG-[SN22]4(10mg/kg/用量)、PEG-[SN38]4(10mg/kg/用量)、又はCPT-11(15mg/kg/用量)のいずれかで治療した。この化学療法抵抗性モデルでは、CPT-11はほとんど効果がなかったが、PEG-[SN22]4とPEG-[SN38]4はどちらも腫瘍の縮小に極めて効果的であった(図22)。PEG-[SN22]4治療では、2~3週間で腫瘍が完全に消失したが、PEG-[SN38]4治療マウスでは小さな腫瘍が見られたままであった。これは、PEG-[SN22]4が、このヒトNB異種移植マウスモデルにおいて優れた有効性を有することを示唆している。
Claims (4)
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862732199P | 2018-09-17 | 2018-09-17 | |
| US62/732,199 | 2018-09-17 | ||
| PCT/US2019/051457 WO2020061007A1 (en) | 2018-09-17 | 2019-09-17 | Polymer-based macromolecular prodrugs |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2022501341A JP2022501341A (ja) | 2022-01-06 |
| JP2022501341A5 JP2022501341A5 (ja) | 2022-09-26 |
| JP7546552B2 true JP7546552B2 (ja) | 2024-09-06 |
Family
ID=69887739
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021514531A Active JP7546552B2 (ja) | 2018-09-17 | 2019-09-17 | ポリマーベースの高分子プロドラッグ |
Country Status (10)
| Country | Link |
|---|---|
| US (4) | US11253603B2 (ja) |
| EP (1) | EP3852793B1 (ja) |
| JP (1) | JP7546552B2 (ja) |
| KR (1) | KR20210072002A (ja) |
| CN (2) | CN112996533B (ja) |
| AU (1) | AU2019344783B2 (ja) |
| CA (1) | CA3112778A1 (ja) |
| EA (1) | EA202190799A1 (ja) |
| MX (1) | MX2021003116A (ja) |
| WO (1) | WO2020061007A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3112778A1 (en) * | 2018-09-17 | 2020-03-26 | The Children's Hospital Of Philadelphia | Polymer-based macromolecular prodrugs |
| CN115443947B (zh) * | 2022-10-12 | 2023-11-21 | 江苏省人民医院(南京医科大学第一附属医院) | 高血压动物模型的制备方法 |
| WO2025101904A1 (en) * | 2023-11-08 | 2025-05-15 | The Children's Hospital Of Philadelphia | Norepinephrine transporter-targeted prodrugs for cancer therapy |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999052861A1 (de) | 1998-04-09 | 1999-10-21 | Institut für Diagnostikforschung GmbH an der Freien Universität Berlin | Neue benzylguanidinderivate für die therapie, in-vivo- und in-vitro-diagnostik |
| JP2002255821A (ja) | 2001-03-06 | 2002-09-11 | Yakult Honsha Co Ltd | 抗癌剤耐性癌に対する治療剤 |
| JP2012503602A (ja) | 2008-09-23 | 2012-02-09 | ネクター セラピューティックス | 対象において持続的治療薬濃度を実現するための組成物及び方法 |
| JP2012506380A (ja) | 2008-10-21 | 2012-03-15 | エンゾン ファーマシューティカルズ,インコーポレーテッド | 7−エチル−10−ヒドロキシカンプトテシンのマルチアーム型ポリマーコンジュゲートによる神経芽腫の治療 |
| JP2013511539A (ja) | 2009-11-18 | 2013-04-04 | ネクター セラピューティックス | ポリマー−薬物コンジュゲートの酸性塩形態及びアルコキシル化方法 |
| JP2016531895A (ja) | 2013-10-04 | 2016-10-13 | プロリンクス エルエルシー | Sn−38の徐放性コンジュゲート |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7591994B2 (en) | 2002-12-13 | 2009-09-22 | Immunomedics, Inc. | Camptothecin-binding moiety conjugates |
| US20040258754A1 (en) * | 2003-06-18 | 2004-12-23 | Valery Alakhov | Compositions for oral administration of camptothecin and its analogs |
| CA2537336C (en) | 2003-09-17 | 2013-02-26 | Nektar Therapeutics Al, Corporation | Multi-arm polymer prodrugs |
| US8394365B2 (en) | 2003-09-17 | 2013-03-12 | Nektar Therapeutics | Multi-arm polymer prodrugs |
| WO2005042539A1 (en) * | 2003-10-29 | 2005-05-12 | Sonus Pharmaceuticals, Inc. | Tocopherol-modified therapeutic drug compounds |
| WO2007106549A2 (en) * | 2006-03-15 | 2007-09-20 | Alza Corporation | Method for treating brain cancer |
| BRPI0716808A2 (pt) * | 2006-09-15 | 2013-11-05 | Enzon Pharmaceuticals Inc | Ligantes poliméricos baseados em lisina |
| US20090074074A1 (en) | 2007-06-29 | 2009-03-19 | The Hong Kong University Of Science And Technology | Multiple description encoder and decoder for transmitting multiple descriptions |
| AU2009282413B2 (en) * | 2008-08-11 | 2014-07-17 | Nektar Therapeutics | Multi-arm polymeric alkanoate conjugates |
| CN101385860B (zh) * | 2008-10-31 | 2011-11-02 | 美国草药泉有限责任公司 | 喜树碱及其衍生物的非线性聚乙二醇前药 |
| US20120171201A1 (en) | 2009-07-22 | 2012-07-05 | Enzon Pharmaceuticals, Inc. | Methods of treating her2 positive cancer with her2 receptor antagonist in combination with multi-arm polymeric conjugates of 7-ethyl-10-hydroxycamptothecin |
| US20140371258A1 (en) | 2010-12-17 | 2014-12-18 | Nektar Therapeutics | Water-Soluble Polymer Conjugates of Topotecan |
| CN102626518B (zh) * | 2012-05-09 | 2014-05-28 | 中国药科大学 | 一种包载难溶性药物的泊洛沙姆/两亲性多糖混合胶束的制备和应用 |
| WO2014085571A1 (en) | 2012-11-28 | 2014-06-05 | Nektar Therapeutics | Method for assessing and predicting efficacy of breast cancer treatment with a long-acting topoisomerase i inhibitor |
| WO2014194289A1 (en) | 2013-05-31 | 2014-12-04 | Nektar Therapeutics | Method for predicting and evaluating responsiveness to cancer treatment with dna-damaging chemotherapeutic agents |
| WO2015191583A2 (en) | 2014-06-09 | 2015-12-17 | Biomed Valley Discoveries, Inc. | Combination therapies targeting tumor-associated stroma or tumor cells and topoisomerase |
| WO2016040848A1 (en) | 2014-09-12 | 2016-03-17 | G1 Therapeutics, Inc. | Treatment of rb-negative tumors using topoisomerase inhibitors in combination with cyclin dependent kinase 4/6 inhibitors |
| US11324827B2 (en) | 2014-10-01 | 2022-05-10 | Xiamen Sinopeg Biotech Co., Ltd. | Multifunctionalized polyethylene glycol derivative and preparation method therefor |
| CN104877127B (zh) | 2015-06-23 | 2017-11-10 | 厦门赛诺邦格生物科技股份有限公司 | 一种八臂聚乙二醇衍生物、制备方法及其修饰的生物相关物质 |
| CN107375288B (zh) | 2016-05-16 | 2019-08-23 | 博瑞生物医药(苏州)股份有限公司 | 多臂的聚合靶向抗癌偶联物 |
| US20200163956A1 (en) | 2016-09-06 | 2020-05-28 | Cerebral Therapeutics LLC | Direct brain administration of chemotherapeutics to the csf for patients with primary and secondary brain tumors |
| KR102279429B1 (ko) | 2017-04-21 | 2021-07-20 | 브라이트제네 바이오-메디컬 테크놀로지 코., 엘티디. | 멀티 암 표적 항암 콘쥬게이트 |
| JP7381083B2 (ja) | 2017-09-08 | 2023-11-15 | フォスプラティン テラピューティクス インコーポレイテッド | 免疫調節剤としてのホスファプラチン化合物およびその治療的使用 |
| WO2019090141A1 (en) | 2017-11-02 | 2019-05-09 | Vicus Therapeutics, Llc | Combination drug therapies for cancer and methods of making and using them |
| CA3099155A1 (en) | 2018-05-14 | 2019-11-21 | Nuvation Bio Inc. | Anti-cancer nuclear hormone receptor-targeting compounds |
| CA3112778A1 (en) | 2018-09-17 | 2020-03-26 | The Children's Hospital Of Philadelphia | Polymer-based macromolecular prodrugs |
| CN111603567B (zh) | 2019-02-22 | 2024-12-27 | 赣江新区博瑞创新医药有限公司 | Cd44靶向多臂偶联物 |
| CA3138197A1 (en) | 2019-05-14 | 2020-11-19 | Nuvation Bio Inc. | Anti-cancer nuclear hormone receptor-targeting compounds |
-
2019
- 2019-09-17 CA CA3112778A patent/CA3112778A1/en active Pending
- 2019-09-17 MX MX2021003116A patent/MX2021003116A/es unknown
- 2019-09-17 WO PCT/US2019/051457 patent/WO2020061007A1/en not_active Ceased
- 2019-09-17 CN CN201980060783.3A patent/CN112996533B/zh active Active
- 2019-09-17 US US16/969,790 patent/US11253603B2/en active Active
- 2019-09-17 JP JP2021514531A patent/JP7546552B2/ja active Active
- 2019-09-17 EP EP19863240.8A patent/EP3852793B1/en active Active
- 2019-09-17 CN CN202510008384.XA patent/CN119950749A/zh active Pending
- 2019-09-17 KR KR1020217011264A patent/KR20210072002A/ko active Pending
- 2019-09-17 EA EA202190799A patent/EA202190799A1/ru unknown
- 2019-09-17 AU AU2019344783A patent/AU2019344783B2/en active Active
-
2022
- 2022-02-11 US US17/670,218 patent/US11642414B2/en active Active
-
2023
- 2023-04-27 US US18/140,289 patent/US12311028B2/en active Active
-
2025
- 2025-05-13 US US19/206,574 patent/US20250387496A1/en active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999052861A1 (de) | 1998-04-09 | 1999-10-21 | Institut für Diagnostikforschung GmbH an der Freien Universität Berlin | Neue benzylguanidinderivate für die therapie, in-vivo- und in-vitro-diagnostik |
| JP2002255821A (ja) | 2001-03-06 | 2002-09-11 | Yakult Honsha Co Ltd | 抗癌剤耐性癌に対する治療剤 |
| JP2012503602A (ja) | 2008-09-23 | 2012-02-09 | ネクター セラピューティックス | 対象において持続的治療薬濃度を実現するための組成物及び方法 |
| JP2012506380A (ja) | 2008-10-21 | 2012-03-15 | エンゾン ファーマシューティカルズ,インコーポレーテッド | 7−エチル−10−ヒドロキシカンプトテシンのマルチアーム型ポリマーコンジュゲートによる神経芽腫の治療 |
| JP2013511539A (ja) | 2009-11-18 | 2013-04-04 | ネクター セラピューティックス | ポリマー−薬物コンジュゲートの酸性塩形態及びアルコキシル化方法 |
| JP2016531895A (ja) | 2013-10-04 | 2016-10-13 | プロリンクス エルエルシー | Sn−38の徐放性コンジュゲート |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2020061007A1 (en) | 2020-03-26 |
| EA202190799A1 (ru) | 2021-06-22 |
| CN119950749A (zh) | 2025-05-09 |
| CA3112778A1 (en) | 2020-03-26 |
| JP2022501341A (ja) | 2022-01-06 |
| CN112996533B (zh) | 2025-01-10 |
| NZ773863A (en) | 2024-10-25 |
| EP3852793A4 (en) | 2022-07-13 |
| US20210000967A1 (en) | 2021-01-07 |
| US20230414766A1 (en) | 2023-12-28 |
| US12311028B2 (en) | 2025-05-27 |
| CN112996533A (zh) | 2021-06-18 |
| EP3852793C0 (en) | 2025-11-19 |
| KR20210072002A (ko) | 2021-06-16 |
| EP3852793B1 (en) | 2025-11-19 |
| EP3852793A1 (en) | 2021-07-28 |
| US11642414B2 (en) | 2023-05-09 |
| AU2019344783A1 (en) | 2021-04-08 |
| US20220160886A1 (en) | 2022-05-26 |
| US20250387496A1 (en) | 2025-12-25 |
| MX2021003116A (es) | 2021-05-14 |
| US11253603B2 (en) | 2022-02-22 |
| AU2019344783B2 (en) | 2025-10-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US12311028B2 (en) | Polymer-based macromolecular prodrugs | |
| US20240131170A1 (en) | Cationic amphiphilic polymers for codelivery of hydrophobic agents and nucleic acids | |
| RU2315782C2 (ru) | Высокомолекулярные производные камптотецинов | |
| US9233976B2 (en) | Berbamine derivatives | |
| JP6949859B2 (ja) | Dbait分子の全身投与によるガンの処置 | |
| Fang et al. | HSP32 (HO-1) inhibitor, copoly (styrene-maleic acid)-zinc protoporphyrin IX, a water-soluble micelle as anticancer agent: In vitro and in vivo anticancer effect | |
| CN121513211A (zh) | Metap2抑制剂的生物标志物及其应用 | |
| US20240009321A1 (en) | Immunogenic nanovesicles for cancer immunotherapy | |
| Cho et al. | Sustained potentiation of bystander killing via PTEN-loss driven macropinocytosis targeted peptide-drug conjugate therapy in metastatic triple-negative breast cancer | |
| WO2022108992A9 (en) | Prostate-specific membrane antigen (psma)-targeted prodrug for selective killing of cells expressing psma | |
| US20150065443A1 (en) | Embelin-based delivery system for water-insoluble active agents | |
| CN104981245B (zh) | 无副作用的抗癌剂 | |
| EA045198B1 (ru) | Макромолекулярные пролекарства на полимерной основе | |
| JP5843086B2 (ja) | 治療活性物質の作用を増強するための高分子化環状ニトロキシドラジカル化合物の使用 | |
| CN102731518B (zh) | 用于抗肿瘤药物的邻硝基芳甲氧基喜树碱缺氧激活前药 | |
| WO2025101904A1 (en) | Norepinephrine transporter-targeted prodrugs for cancer therapy | |
| Ghorai et al. | Advances in camptothecin nanomedicine: enhancing targeted breast-cancer therapeutics using innovative drug delivery systems | |
| CN119950745B (zh) | 一种药物组合物及其在制备抗肿瘤药物中的应用 | |
| Picken | Prodrug approaches to reduce treprostinil toxicity | |
| CN107921282A (zh) | 选择性抑制肠羧酸酯酶2酶活性的组合物及方法 | |
| JP2025512450A (ja) | アプタマー、複合体及び組成物並びに製造方法及び使用 | |
| HK1214145B (en) | Anticancer agent having no side effects |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220914 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220914 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230829 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230831 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231129 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240109 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240403 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240730 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240827 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7546552 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |