JP7463565B2 - 抗腫瘍組成物 - Google Patents
抗腫瘍組成物 Download PDFInfo
- Publication number
- JP7463565B2 JP7463565B2 JP2022576573A JP2022576573A JP7463565B2 JP 7463565 B2 JP7463565 B2 JP 7463565B2 JP 2022576573 A JP2022576573 A JP 2022576573A JP 2022576573 A JP2022576573 A JP 2022576573A JP 7463565 B2 JP7463565 B2 JP 7463565B2
- Authority
- JP
- Japan
- Prior art keywords
- tumor
- akkermansia muciniphila
- cancer
- ssyd
- mpd
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/429—Thiazoles condensed with heterocyclic ring systems
- A61K31/43—Compounds containing 4-thia-1-azabicyclo [3.2.0] heptane ring systems, i.e. compounds containing a ring system of the formula, e.g. penicillins, penems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/7036—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin having at least one amino group directly attached to the carbocyclic ring, e.g. streptomycin, gentamycin, amikacin, validamycin, fortimicins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/12—Cyclic peptides, e.g. bacitracins; Polymyxins; Gramicidins S, C; Tyrocidins A, B or C
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
- C12N1/205—Bacterial isolates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Mycology (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biochemistry (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Wood Science & Technology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- General Engineering & Computer Science (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Biomedical Technology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Gastroenterology & Hepatology (AREA)
- Endocrinology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
(A)アッカーマンシアムシニフィラと、
(B)免疫チェックポイント阻害剤と、を含む抗腫瘍組成物を提供する。
本願に記載のアッカーマンシアムシニフィラ菌株は、市販のものであってもよいし、従来の技術により得られたものであってもよい。例えば、出願番号がCN201380070847.0で、公開番号がCN 104918626 Aである中国発明特許出願には、「代謝病の治療におけるアッカーマンシア属の使用」が開示されており、当該特許出願には、アッカーマンシアムシニフィラ菌株ATCC BAA835が開示されている。
本願で用いられる免疫チェックポイント阻害剤は、任意の市販の製品であってもよく、例えば、PD-1阻害剤、PD-L1阻害剤、CTLA-4阻害剤などが挙げられる。一つの好ましい実施態様において、前記免疫チェックポイント阻害剤は、キイトルーダ(Keytruda)、テセントリク(Tecentriq)、ニボルマブ注射液(Nivolumab Injection)、バベンチオ(アベルマブ)、Tuoyi(トリパリマブ注射液(Toripalimab Injection))を含む。
本願において、前記アッカーマンシアムシニフィラ菌株と免疫チェックポイント阻害剤は、混合されて単一製剤に調製されて共に使用されてもよいし、物理的に分離されて別々に使用されてもよい。本願の一つの実施態様において、前記アッカーマンシアムシニフィラ菌株と免疫チェックポイント阻害剤は、物理的に分離されて別々に使用される。本願の別の実施態様において、前記アッカーマンシアムシニフィラ菌株は、免疫チェックポイント阻害剤の投与前に、患者に投与されてもよい。一般的には、前記アッカーマンシアムシニフィラ菌株は、任意の適当な方式(経口、注射などを含むが、これらに限定されない)で患者に投与可能である。前記免疫チェックポイント阻害剤は、任意の適当な方式(経口、注射などを含むが、これらに限定されない)で患者に投与可能である。前記アッカーマンシアムシニフィラ菌株又は免疫チェックポイント阻害剤の使用方法は、本分野における通常の方法であり、当業者は、明細書の記載により、従来の技術を参照することで直接決定できる。
腫瘍体積:1週間ごとにノギスを使用して腫瘍体積を3回測定し、腫瘍の長径及び短径を測定し、その体積の計算式は、体積=0.5×長径×短径2である。
分離培地:0.4gのKH2PO4、0.53gのNa2HPO4、0.3gのNH4Cl、0.3gのNaCl、0.1gのMgCl2・6H2O、0.11gのCaCl2、0.5mgのレサズリン、4gのNaHCO3、0.25gのNa2S・7~9H2O、0.25%のムチン。
発酵培地1:ブレインハートインフュージョン培地(Brain Heart Infusion、BHI)
発酵培地2:5gのトリプトン、5gの大豆ペプトン、5gの牛肉粉末、5gの酵母粉末、4gのグルコース、3gのNaCl、1.5gのMgSO4、Na2HPO4、KH2PO4、1Lの水、pH=7.2。
分離培地及び発酵培地を121℃、高圧で、15min殺菌しておく。
(1)調製されたムチン分離培地を血清ボトル(液体充填量10/30mL)に置く
(2)健康な成人の糞便0.5gを採取し、無菌のPBSリン酸緩衝生理食塩水に均一に分散させ、糞便を順にPBS溶液にて10倍勾配で希釈し、希釈液1mLを採取してムチン分離培地の血清ボトルに接種する
(3)ムチン血清ボトルを37℃の嫌気環境に置いて48h培養する
(4)目視で濁っている最高の希釈勾配でのムチン発酵液を採取し、PBS緩衝液で10-6~10-9に希釈する
(5)希釈液をブレインハートインフュージョン寒天培地に塗布し、24~48h培養し、大きさが1mmであるコロニーを選び、純粋培養した後、細菌の16S rDNA菌種同定を行う
(1)アッカーマンシアムシニフィラを、画線法で三つの領域に分けてブレインハートインフュージョン寒天培地に接種し、37℃の嫌気環境で48h培養する。
(2)寒天平板培地からアッカーマンシアムシニフィラの単コロニーを選んで15mLのブレインハートインフュージョン液体培地に接種し、37℃の嫌気環境で24h培養する。
(3)15mLの嫌気性チューブから、10mLの発酵液を200mLのブレインハートインフュージョン液体培地に移し、37℃の嫌気環境で24h培養する。
(4)200mLのアッカーマンシアムシニフィラ発酵液をブレインハートインフュージョン液体培地に接種し、5Lの発酵タンクにおける充填体積が4Lであり、嫌気ガスが窒素と二酸化炭素との二成分混合ガス(N2:CO2=9:1)であり、撹拌の回転数が100r/minであり、温度が37℃であり、嫌気環境で24h培養する。
(1)凍結乾燥保護剤:トレハロース、ショ糖、粉乳。
(2)上記で得られた発酵液を8000Rで20min遠心分離して、菌体を回収する。
(3)アッカーマンシアムシニフィラを遠心分離することで得られた菌体、凍結乾燥保護剤、及び水を混合し、凍結乾燥前の溶液におけるトレハロース、ショ糖、粉乳の含有量(質量%)をそれぞれ5%、5%、10%にし、凍結乾燥して凍結乾燥粉末を得た。粉末における、寄託番号がCGMCC No.14764であるアッカーマンシアムシニフィラ菌株の生菌数は、1010CFU/gである。
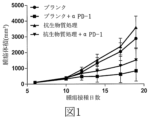
6~8週齢の雄性C57BL/6Jマウス(20~26g、SPF級)48匹を1週間、環境に適応させた後、体重により、1群12匹で、第1群(抗生物質処理なし、ブランク、i.p.)、第2群(抗生物質処理なし、抗mPD-1、10mg/kg、i.p.)、第3群(抗生物質処理あり、ブランク、i.p.)、第4群(抗生物質処理あり、抗mPD-1、10mg/kg、i.p.)の4群にランダムに分ける。抗生物質処理では、広域スペクトル抗生物質アンピシリン(1mg/mL)+コリスチン(1mg/mL)+ストレプトマイシン(5mg/mL)を5日飲水投与した。全ての群のマウスには、リン酸緩衝生理食塩水(PBS)に再懸濁したMC38腫瘍細胞を濃度1×107個/mLで接種し、100μL/匹で実験動物の右肋骨部皮下に接種した。第2群及び第4群のマウスには、腫瘍細胞を接種してから4日目に抗mPD-1を注射し、4日ごとに1回注射し、合計で4回注射した。マウスを、腫瘍接種してから19日目に安楽死させ、各群のマウスの腫瘍を摘出した。
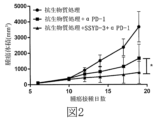
6~8週齢の雄性C57BL/6Jマウス(20~26g、SPF級)48匹を1週間、環境に適応させた後、体重により、第1群(抗生物質処理なし、ブランク、i.p.)、第2群(抗生物質処理あり、ブランク、i.p.)、第3群(抗生物質処理あり、抗mPD-1、10mg/kg、i.p.)、第4群(抗生物質処理あり、アッカーマンシアムシニフィラSSYD-3、p.o.、抗mPD-1、10mg/kg、i.p.)の4群にランダムに分けた。広域スペクトル抗生物質アンピシリン(1mg/mL)+コリスチン(1mg/mL)+ストレプトマイシン(5mg/mL)を5日飲水投与した。第4群のマウスには、先ずアッカーマンシアムシニフィラSSYD-3の凍結乾燥サンプルを投与し、胃内投与濃度が1.0×108CFU/匹/日である。胃内投与を2週間続けた後、全ての群では、PBSに再懸濁したMC38腫瘍細胞を濃度1×107個/mLで接種し、100μL/匹で実験動物の右肋骨部皮下に接種した。第3群及び第4群のマウスには、腫瘍細胞を接種してから4日目に抗mPD-1を注射し、4日ごとに1回注射し、合計で4回注射した。腫瘍接種してから19日目にマウスの体重を量った後、マウスを安楽死させ、マウスの腫瘍重量を測定して記録した。
実施例3におけるマウスを、腫瘍接種してから19日目に安楽死させ、フローサイトメトリー(艾森生物有限会社、NovoCyte 3130)で、腫瘍細胞内のCD3、CD4、CD8、FOXP3、CD25、CXCR3、Gata3、Granzyme B、CD69、PD-1、CTLA-4、CD11b、MHCII、CD206、CD40、CSF1R、PD-L1、及びGr-1を検出した。免疫因子分析は、TNF-α、IL-17、IL-13、IL-12p70、IL-10、IL-6、IL-5、IL-4、IL-2、IL-1b、IFNy、GM-CSF、G-CSF、M-CSF、MIG、IP-10、MIP1b及びMAC-1を含む。抗生物質処理されたマウスに対して、抗mPD-1による単独治療、及びアッカーマンシアムシニフィラSSYD-3と抗mPD-1との併用治療を施し、結果を図3に示す。結果から分かるように、アッカーマンシアムシニフィラSSYD-3と抗mPD-1の注射との併用治療を施した後、腫瘍浸潤CD8 T細胞数が顕著に増加し、アッカーマンシアムシニフィラSSYD-3が抗mPD-1の抗腫瘍効果を向上させたことを示す。
実施例3におけるマウスを、抗mPD-1による単独治療、及びアッカーマンシアムシニフィラSSYD-3と抗mPD-1との併用治療を施した後19日目に安楽死させ、フローサイトメトリー(艾森生物有限会社、NovoCyte 3130)で、腫瘍細胞内のCD3、CD4、CD8、FOXP3、CD25、CXCR3、Gata3、Granzyme B、CD69、PD-1、CTLA-4、CD11b、MHCII、CD206、CD40、CSF1R、PD-L1、及びGr-1を検出した。免疫因子分析は、TNF-α、IL-17、IL-13、IL-12p70、IL-10、IL-6、IL-5、IL-4、IL-2、IL-1b、IFNy、GM-CSF、G-CSF、M-CSF、MIG、IP-10、MIP1b及びMAC-1を含む。マウス体内の免疫細胞の変化結果を図4に示す。結果から分かるように、抗mPD-1の単独注射に比べて、抗mPD-1とアッカーマンシアムシニフィラSSYD-3との併用治療により、腫瘍組織内のCD3細胞のレベルが顕著に向上し、生体の免疫力が向上した。図では、いずれも抗生物質処理群と比較し、P<0.05は、顕著な差異があることを示し、*P<0.05、**P<0.01である。
実施例3におけるマウスを、抗mPD-1による単独治療、及びアッカーマンシアムシニフィラSSYD-3と抗mPD-1との併用治療を施した後19日目に安楽死させ、フローサイトメトリー(艾森生物有限会社、NovoCyte 3130)で、腫瘍細胞内のCD3、CD4、CD8、FOXP3、CD25、CXCR3、Gata3、Granzyme B、CD69、PD-1、CTLA-4、CD11b、MHCII、CD206、CD40、CSF1R、PD-L1、及びGr-1を検出した。免疫因子分析は、TNF-α、IL-17、IL-13、IL-12p70、IL-10、IL-6、IL-5、IL-4、IL-2、IL-1b、IFNy、GM-CSF、G-CSF、M-CSF、MIG、IP-10、MIP1b及びMAC-1を含む。実験結果を図5に示す。抗生物質で処理されたマウスの腫瘍組織内のTreg細胞数はわずかに増加したが、顕著な差異がなく、抗mPD-1により治療された抗生物質処理群では、Treg細胞数は顕著に低減し(P<0.01)、アッカーマンシアムシニフィラSSYD-3と抗mPD-1との併用治療によりも、マウス体内のTreg細胞数を顕著に低減させた(P<0.001)。上記した結果から分かるように、抗mPD-1の単独注射により、マウス体内の免疫阻害システムが一部解消され、アッカーマンシアムシニフィラSSYD-3との併用により、マウス体内の免疫阻害作用が更に解消され、生体の免疫活性及び抗腫瘍効果が回復した。抗生物質処理群と比較し、P<0.05は、顕著な差異があることを示し、**P<0.01、***P<0.001である。
6~8週齢の雄性C57BL/6Jマウス(20~26g、SPF級)36匹を1週間、環境に適応させた後、体重により、第1群(抗生物質処理あり、ブランク、i.p.)、第2群(抗生物質処理あり、抗mPD-1、10mg/kg、i.p.)、第3群(抗生物質処理あり、アッカーマンシアムシニフィラSSYD-3、p.o.、抗mPD-1、10mg/kg、i.p.)の3群にランダムに分けた。各群のマウスには、広域スペクトル抗生物質アンピシリン(1mg/mL)+コリスチン(1mg/mL)+ストレプトマイシン(5mg/mL)を5日飲水投与した。その後、第3群では、先ずアッカーマンシアムシニフィラSSYD-3の凍結乾燥サンプルを投与し、胃内投与濃度が1.0×108CFU/匹/日である。胃内投与を2週間続けた後、全ての群のマウスに対して、PBSに再懸濁した4T1腫瘍細胞を濃度1×107個/mLで接種し、100μL/匹で実験動物の右肋骨部皮下に接種した。第2群及び第3群のマウスには、腫瘍細胞を接種してから4日目に抗mPD-1を注射し、4日ごとに1回注射し、合計で4回注射した。腫瘍接種してから19日目にマウスの腫瘍体積を測定した後、各群のマウスを安楽死させ、腫瘍組織を摘出した。
6~8週齢の雄性C57BL/6Jマウス(20~26g、SPF級)36匹を1週間、環境に適応させた後、体重により、第1群(抗生物質処理あり、ブランク、i.p.)、第2群(抗生物質処理あり、抗mPD-1、10mg/kg、i.p.)、第3群(抗生物質処理あり、アッカーマンシアムシニフィラSSYD-3、p.o.、抗mPD-1、10mg/kg、i.p.)の3群にランダムに分けた。各群のマウスには、広域スペクトル抗生物質アンピシリン(1mg/mL)+コリスチン(1mg/mL)+ストレプトマイシン(5mg/mL)を5日飲水投与した。第3群のマウスには、先ずアッカーマンシアムシニフィラSSYD-3の凍結乾燥サンプルを投与し、胃内投与濃度が1.0×108CFU/匹/日である。胃内投与を2週間続けた後、全ての群では、PBSに再懸濁したLLC1肺癌細胞を濃度1×105個/mLで接種し、100μL/匹で実験動物の右肋骨部皮下に接種した。第2群及び第3群のマウスには、腫瘍細胞を接種してから4日目に抗mPD-1を注射し、4日ごとに1回注射し、合計で4回注射した。腫瘍接種してから19日目にマウスの腫瘍体積を測定した後、各群のマウスを安楽死させ、腫瘍組織を摘出した。
Claims (9)
- 抗PD-1抗体と組み合わせて使用するための、CGMCC No.14764の寄託番号を有するアッカーマンシアムシニフィラSSYD-3を含む抗腫瘍組成物。
- 患者の腫瘍成長阻害における抗PD-1抗体の効果を向上させるための、CGMCC No.14764の寄託番号を有するアッカーマンシアムシニフィラSSYD-3を含む抗腫瘍組成物。
- その他の菌(例えばビフィドバクテリウム、ラクトバチルス、クロストリディオイデス、エンテロコッカスフェシウム、プレボテラコプリ、ルミノコッカス)を更に含む、請求項1又は2に記載の抗腫瘍組成物。
- 前記アッカーマンシアムシニフィラSSYD-3が経口投与されるものである、請求項1~3のいずれか1項に記載の抗腫瘍組成物。
- 前記アッカーマンシアムシニフィラSSYD-3が、経口液、錠剤、カプセル、又は凍結乾燥粉末の剤型である、請求項4に記載の抗腫瘍組成物。
- 前記アッカーマンシアムシニフィラSSYD-3が、10 4 ~10 13 CFU/人/日の用量範囲で投与される、請求項1~5のいずれか1項に記載の抗腫瘍組成物。
- 前記抗PD-1抗体が、キイトルーダ、ニボルマブ、又はトリパリマブである、請求項1~6のいずれか1項に記載の抗腫瘍組成物。
- 前記腫瘍が、結腸癌、肺癌、胃癌、肝癌、頭頚部癌、子宮頸癌、乳癌、リンパ癌、黒色腫、腎癌又は尿路上皮癌から選択される、請求項1~7のいずれか1項に記載の抗腫瘍組成物。
- 前記抗PD-1抗体の投与前に投与される、請求項1~8のいずれか1項に記載の抗腫瘍組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202010123922.7 | 2020-02-27 | ||
| CN202010123922.7A CN111228315A (zh) | 2020-02-27 | 2020-02-27 | 抗肿瘤组合物 |
| PCT/CN2021/078434 WO2021170137A1 (zh) | 2020-02-27 | 2021-03-01 | 抗肿瘤组合物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023514756A JP2023514756A (ja) | 2023-04-07 |
| JP7463565B2 true JP7463565B2 (ja) | 2024-04-08 |
Family
ID=70862901
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022576573A Active JP7463565B2 (ja) | 2020-02-27 | 2021-03-01 | 抗腫瘍組成物 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20230233619A1 (ja) |
| EP (1) | EP4115893A4 (ja) |
| JP (1) | JP7463565B2 (ja) |
| KR (1) | KR20220133283A (ja) |
| CN (2) | CN111228315A (ja) |
| AU (1) | AU2021228100B2 (ja) |
| CA (1) | CA3173066A1 (ja) |
| WO (1) | WO2021170137A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111228315A (zh) * | 2020-02-27 | 2020-06-05 | 上海上药信谊药厂有限公司 | 抗肿瘤组合物 |
| JPWO2022071423A1 (ja) * | 2020-09-30 | 2022-04-07 | ||
| CN113413466B (zh) * | 2020-12-15 | 2022-08-19 | 和度生物医药(上海)有限公司 | 用于治疗癌症的amuc_1100和免疫检查点调节剂的组合疗法 |
| CN113862193B (zh) * | 2021-10-28 | 2023-12-22 | 江西普瑞森基因科技有限公司 | 一株嗜黏蛋白阿克曼氏菌及其在制备抗肿瘤药物中的应用 |
| WO2023113541A1 (en) * | 2021-12-16 | 2023-06-22 | Enterobiome Inc. | Pharmaceutical composition for preventing or treating cancer or inflammatory disease |
| CN116421630A (zh) * | 2022-07-29 | 2023-07-14 | 广州知易生物科技有限公司 | 一种防治肿瘤的嗜粘蛋白阿克曼氏菌产品及其应用 |
| CN118440861A (zh) * | 2024-05-15 | 2024-08-06 | 合肥瀚微生物科技有限公司 | 嗜黏蛋白阿克曼氏菌及其在抗肿瘤免疫治疗中的用途 |
| CN119552781B (zh) * | 2025-01-24 | 2025-07-08 | 中山大学 | 一种嗜粘蛋白阿克曼氏菌及其应用 |
| CN119950729B (zh) * | 2025-02-27 | 2025-12-02 | 中南大学 | 一种用于抗肿瘤的组合物及其应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018521013A (ja) | 2015-06-01 | 2018-08-02 | ザ・ユニバーシティ・オブ・シカゴThe University Of Chicago | 共生微生物叢の操作による癌の処置 |
| WO2020063646A1 (zh) | 2018-09-27 | 2020-04-02 | 上海上药信谊药厂有限公司 | 一种用于预防和治疗代谢疾病的菌株及其应用 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014075745A1 (en) | 2012-11-19 | 2014-05-22 | Université Catholique de Louvain | Use of akkermansia for treating metabolic disorders |
| CN106632021A (zh) * | 2016-09-27 | 2017-05-10 | 中国药科大学 | 2‑取代异烟酸类化合物、其制备方法及其用途 |
| US11723935B2 (en) * | 2017-02-06 | 2023-08-15 | New York University | Methods and compositions for treating and diagnosing pancreatic cancers |
| CA3211208A1 (en) * | 2017-04-03 | 2018-10-11 | Gusto Global, Llc | Rational design of microbial-based biotherapeutics |
| WO2019075452A1 (en) * | 2017-10-13 | 2019-04-18 | Evelo Biosciences, Inc. | IDENTIFICATION OF BACTERIA FOR CANCER THERAPY |
| WO2019178055A1 (en) * | 2018-03-12 | 2019-09-19 | Evelo Biosciences, Inc. | Extracellular vesicles from burkholderia |
| CN110496140B (zh) * | 2018-05-18 | 2022-05-31 | 瑞微(深圳)生物科技有限公司 | 脆弱拟杆菌或阿克曼粘细菌在制备用于预防或治疗肿瘤的药物中的应用 |
| CN110638838B (zh) * | 2018-06-26 | 2021-07-06 | 瑞微(深圳)生物科技有限公司 | 阿克曼粘细菌或普氏菌在制备用于增强抗肿瘤免疫功能的药物中的应用 |
| CN111228315A (zh) * | 2020-02-27 | 2020-06-05 | 上海上药信谊药厂有限公司 | 抗肿瘤组合物 |
-
2020
- 2020-02-27 CN CN202010123922.7A patent/CN111228315A/zh active Pending
- 2020-02-27 CN CN202410113467.0A patent/CN118340799A/zh active Pending
-
2021
- 2021-03-01 CA CA3173066A patent/CA3173066A1/en active Pending
- 2021-03-01 WO PCT/CN2021/078434 patent/WO2021170137A1/zh not_active Ceased
- 2021-03-01 EP EP21761700.0A patent/EP4115893A4/en active Pending
- 2021-03-01 US US17/904,956 patent/US20230233619A1/en not_active Abandoned
- 2021-03-01 JP JP2022576573A patent/JP7463565B2/ja active Active
- 2021-03-01 AU AU2021228100A patent/AU2021228100B2/en not_active Expired - Fee Related
- 2021-03-01 KR KR1020227030029A patent/KR20220133283A/ko not_active Ceased
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018521013A (ja) | 2015-06-01 | 2018-08-02 | ザ・ユニバーシティ・オブ・シカゴThe University Of Chicago | 共生微生物叢の操作による癌の処置 |
| WO2020063646A1 (zh) | 2018-09-27 | 2020-04-02 | 上海上药信谊药厂有限公司 | 一种用于预防和治疗代谢疾病的菌株及其应用 |
Non-Patent Citations (1)
| Title |
|---|
| Science,2018年,Vol.359 No.6371,p.91-97 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN118340799A (zh) | 2024-07-16 |
| KR20220133283A (ko) | 2022-10-04 |
| CN111228315A (zh) | 2020-06-05 |
| WO2021170137A1 (zh) | 2021-09-02 |
| EP4115893A1 (en) | 2023-01-11 |
| US20230233619A1 (en) | 2023-07-27 |
| JP2023514756A (ja) | 2023-04-07 |
| AU2021228100A1 (en) | 2022-09-22 |
| CA3173066A1 (en) | 2021-09-02 |
| AU2021228100B2 (en) | 2025-04-10 |
| EP4115893A4 (en) | 2024-04-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7463565B2 (ja) | 抗腫瘍組成物 | |
| JP7608482B2 (ja) | 抗腫瘍組成物 | |
| CN110496140B (zh) | 脆弱拟杆菌或阿克曼粘细菌在制备用于预防或治疗肿瘤的药物中的应用 | |
| US5716615A (en) | Dietary and pharmaceutical compositions containing lyophilized lactic bacteria, their preparation and use | |
| CA3084952A1 (en) | Bacteriophage treatment for acne and biofilms | |
| CN109771445B (zh) | 酪酸梭菌在制备诱导抗肿瘤免疫及免疫检查点抑制剂增敏制剂中的应用 | |
| ES2331650T3 (es) | Utilizacion de bacterias probioticas en el tratamiento de una infeccion. | |
| CN111110852A (zh) | 抗肿瘤组合物 | |
| JP2024050573A (ja) | 腫瘍浸潤リンパ球(tils)を活性化する方法 | |
| CN117503802A (zh) | Ac菌在抗肿瘤免疫治疗中的应用 | |
| CN109153706A (zh) | 源自乳酸菌的蛋白质及其制备方法 | |
| CN113041266B (zh) | 一株改善银屑病样小鼠病理特征的干酪乳杆菌及其应用 | |
| JP4509250B2 (ja) | Helicobacterpylori除菌性医薬品 | |
| CN110448681B (zh) | 一种用于恶性肿瘤免疫治疗的联合药物 | |
| HK40086386A (en) | Anti-tumor composition | |
| EP0686039B1 (en) | Method of enhancing immune response to oral vaccines | |
| IL149779A (en) | Vaccine comprising lactobacilli for treating prostate inflammation and benign prostate hyperplasias and its production | |
| HK40086346A (en) | Anti-tumor composition | |
| RU2454238C1 (ru) | Биопрепарат балис для профилактики и лечения инфекционных болезней | |
| JP2005225841A (ja) | 病原体感染防御剤 | |
| 김현정 | Investigation of The Anti-Tumor Effect and Underlying Molecular Mechanism of Clostridium scindens | |
| CN110090230B (zh) | 凝结芽孢杆菌在制备预防或治疗胆管癌制剂中的应用 | |
| CN108114004A (zh) | 可直接给药进行免疫治疗的复合益生菌菌剂及其制备方法 | |
| CN120241808A (zh) | 益生菌在制备与溶瘤病毒组合使用的抗肿瘤药物中的用途 | |
| WO2024079492A1 (en) | Corynebacterium strains, combinations, and lyophilized formulations thereof for use in the prevention of a viral infection |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220824 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220824 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230705 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230929 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20231124 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240221 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240304 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240327 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7463565 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |