JP7370832B2 - アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット - Google Patents
アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット Download PDFInfo
- Publication number
- JP7370832B2 JP7370832B2 JP2019216301A JP2019216301A JP7370832B2 JP 7370832 B2 JP7370832 B2 JP 7370832B2 JP 2019216301 A JP2019216301 A JP 2019216301A JP 2019216301 A JP2019216301 A JP 2019216301A JP 7370832 B2 JP7370832 B2 JP 7370832B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- nucleic acid
- amplification
- composition
- target nucleic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/70—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving virus or bacteriophage
- C12Q1/701—Specific hybridization probes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6888—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for detection or identification of organisms
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/16—Primer sets for multiplex assays
Description
本出願は、2017年3月25日に出願され、参照により本明細書に組み込まれる米国仮出願第62/476,753号の優先権の利益を主張する。
本開示は、感染性因子の検出、より具体的には、アデノウイルス、メタニューモウイルス、および/またはライノウイルスの検出に関する。インビトロ核酸増幅技法を使用することによる、アデノウイルス、メタニューモウイルス、および/またはライノウイルスの増幅および/または検出のための組成物、方法、およびキットが記載される。
感染性疾患は、細菌性、ウイルス性、またはその他の起源にかかわらず、人間の健康に急性および慢性の課題をもたらす。多くの一般的な感染症は気道に影響を及ぼす。気道疾患は、全ての年齢の患者によく見られるが、非常に若齢の患者および非常に高齢の患者においてより深刻であることが多い。ウイルスには、DNAウイルスおよびRNAウイルスが含まれる。
迅速、高感度、かつ特異的な複数のアデノウイルス血清型の検出を可能にする分子ベースのアッセイが、依然として当該技術分野で必要とされている。また、迅速、高感度、かつ特異的なhMPVの複数のサブタイプおよびサブグループの検出が、依然として当該技術分野で必要とされている。さらに、特にRVをEVから区別する能力に関して、迅速、高感度、かつ特異的な様式でRVを検出する方法が、依然として当該技術分野で必要とされている。
本開示の目的は、アデノウイルス、hMPV、およびHRV核酸のうちの1つ以上を特異的に増幅し、および/または高感度で検出するために使用できる方法、組成物、および
キットを提供することである。有利なことに、本方法、組成物、およびキットを使用して、アデノウイルス、hMPV、および/またはHRVの多くの(例えば、5個以上、10個以上、20個以上、30個以上、40個以上、または50個以上)または全ての既知の血清型およびサブグループを高感度で特異的に検出し得る。
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成された、組成物またはキット。
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、
(i)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号1
50の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成されたか、あるいは
(ii)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、
(i)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成されたか、あるいは
(ii)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、
(i)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成されたか、あるいは
(ii)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成され、かつ
(C)第3の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
の縮重塩基、またはそれらの組み合わせを含有する核酸配列を含むか、あるいはメタニューモウイルスアンプリコンを増幅するように構成された前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含むか、あるいはその両方である、請求項4または請求項6に記載の組成物またはキット。
物またはキット。
組成物またはキット。
定するための方法であって、
(A)試料を請求項1~58のいずれか一項に記載の増幅オリゴマーの組み合わせと接触させるステップと、
(B)試料中のアデノウイルス標的核酸、メタニューモウイルス標的核酸、またはライノウイルス標的核酸のうちのいずれかが、その標的核酸を増幅して増幅産物を生成するように構成された増幅オリゴマーの組み合わせによって使用される、インビトロ核酸増幅反応を行うステップと、
(C)前記増幅産物を検出するステップと、を含み、
それにより、前記試料中の前記標的核酸の有無を決定する、方法。
ルス標的核酸、またはそれらの組み合わせの前記インビトロ検出のための方法であって、前記方法が、アデノウイルス標的核酸、メタニューモウイルス標的核酸、および/またはライノウイルス標的核酸を、請求項29~43のいずれかに記載の検出プローブオリゴマーと接触させることを含み、前記検出プローブオリゴマーと、前記検出プローブオリゴマーがハイブリダイズするように構成された前記標的核酸とのハイブリダイゼーションが、その標的核酸の存在を示す、方法。
特定の実施形態では、例えば、以下が提供される:
(項目1)
少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(項目2)
少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(項目3)
少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(項目4)
2つ以上の標的酸に対して構成された少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、
(i)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/また
は配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成された、あるいは
(ii)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(項目5)
2つ以上の標的酸に対して構成された少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、
(i)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成された、あるいは
(ii)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(項目6)
2つ以上の標的酸に対して構成された少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~
525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、
(i)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成された、あるいは
(ii)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(項目7)
3つ以上の標的酸に対して構成された少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つのアデノウイルス位置を含む、少なくとも約50ヌクレオチド長のアデノウイルスアンプリコンを増幅するように構成され、かつ
(B)第2の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つのメタニューモウイルス位置を含む、少なくとも約50ヌクレオチド長のメタニューモウイルスアンプリコンを増幅するように構成され、かつ
(C)第3の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列
番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つのライノウイルス位置を含む、少なくとも約50ヌクレオチド長のライノウイルスアンプリコンを増幅するように構成された、組成物またはキット。
(項目8)
前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、項目1~3のいずれか一項に記載の組成物またはキット。
(項目9)
前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、項目1~3または8のいずれかに記載の組成物またはキット。
(項目10)
アデノウイルスアンプリコンを増幅するように構成された前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、および/またはアデノウイルスアンプリコンを増幅するように構成された前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、項目4または項目7に記載の組成物またはキット。
(項目11)
前記第2の標的核酸がアデノウイルス標的核酸であり、かつアデノウイルスアンプリコンを増幅するように構成された前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはアデノウイルスアンプリコンを増幅するように構成された前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはその両方である、項目5または項目6に記載の組成物またはキット。
(項目12)
メタニューモウイルスアンプリコンを増幅するように構成された前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはメタニューモウイルスアンプリコンを増幅するように構成された前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはその両方である、項目5または項目7に記載の組成物またはキット。
(項目13)
前記第2の標的核酸がメタニューモウイルス標的核酸であり、かつメタニューモウイルスアンプリコンを増幅するように構成された前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはメタニューモウイルスアンプリコンを増幅するように構成された前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはその両方である、項目4または項目6に記載の組成物またはキット。
(項目14)
ライノウイルスアンプリコンを増幅するように構成された前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはライノウイルスアンプリコンを増幅するように構成された前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはその両方である、項目6または項目7に記載の組成物またはキット。
(項目15)
前記第2の標的核酸がライノウイルス標的核酸であり、かつライノウイルスアンプリコンを増幅するように構成された前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはライノウイルスアンプリコンを増幅するように構成された前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、あるいはその両方である、項目4または項目5に記載の組成物またはキット。
(項目16)
前記アデノウイルス標的核酸について、前記第1の増幅オリゴマーが、配列番号1、5、11、12、25、26、31、32、33、34、35、38、71、72、73、74からなる群から選択される標的ハイブリダイズ配列を含む、項目1、4、7、8、10、または11のいずれか一項に記載の組成物またはキット。
(項目17)
前記第2の標的核酸が、アデノウイルスであり、かつ前記第1の増幅オリゴマーが、配列番号1、5、11、12、25、26、31、32、33、34、35、38、71、72、73、74からなる群から選択される標的ハイブリダイズ配列を含む、項目5、6、または9に記載の組成物またはキット。
(項目18)
前記アデノウイルス標的核酸について、前記第2の増幅オリゴマーが、配列番号2、3、6、7、8、9、13、14、15、16、27、28、42、43、44、45、46、61、62、138、139、140、141、142、143、144、145、146、147、148、149からなる群から選択される標的ハイブリダイズ配列を含む、項目1、4、7、8、10、または11のいずれか一項に記載の組成物またはキット。
(項目19)
前記第2の標的核酸がアデノウイルスであり、かつ前記第2の増幅オリゴマーが、配列番号2、3、6、7、8、9、13、14、15、16、27、28、42、43、44、45、46、61、62、138、139、140、141、142、143、144、145、146、147、148、149からなる群から選択される標的ハイブリダイズ配列を含む、項目5、6、または9に記載の組成物またはキット。
(項目20)
前記メタニューモウイルス標的核酸について、前記第1の増幅オリゴマーが、配列番号52、53、151、152、153、154、160からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目2、5、7、8、12、または13のいずれか一項に記載の組成物またはキット。
(項目21)
前記第2の標的核酸がメタニューモウイルスであり、かつ前記第1の増幅オリゴマーが、配列番号52、53、151、152、153、154、160からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目4、6、または9に記載の組成物またはキット。
(項目22)
前記メタニューモウイルス標的核酸について、前記第2の増幅オリゴマーが、配列番号56、68、158、177、178からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目2、5、7、8、12、または13のいずれか一項に記載の組成物またはキット。
(項目23)
前記第2の標的核酸がメタニューモウイルスであり、かつ前記第2の増幅オリゴマーが、配列番号56、68、158、177、178からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目4、6、または9に記載の組成物またはキット。
(項目24)
前記ライノウイルス標的核酸について、前記第1の増幅オリゴマーが、配列番号50、51、59、60、65、75、77~86、102~108、121~130からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目3、6、7、8、14、または15のいずれか一項に記載の組成物またはキット。
(項目25)
前記第2の標的核酸がライノウイルスであり、かつ前記第1の増幅オリゴマーが、配列番号50、51、59、60、65、75、77~86、102~108、121~130からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目4、5、または9に記載の組成物またはキット。
(項目26)
前記ライノウイルス標的核酸について、前記第2の増幅オリゴマーが、配列番号57、95~100、115~119、137からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目3、6、7、8、14、または15のいずれか一項に記載の組成物またはキット。
(項目27)
前記第2の標的核酸がライノウイルスであり、かつ前記第2の増幅オリゴマーが、配列番号57、95~100、115~119、137からなる群から選択される標的ハイブリダイズ配列を含む、それからなる、それから本質的になる、項目4、5、または9に記載の組成物またはキット。
(項目28)
前記組成物またはキットが、少なくとも1つの検出プローブオリゴマーをさらに含む、項目1~27のいずれか一項に記載の組成物またはキット。
(項目29)
前記組成物またはキットが、配列番号4、10、17、18、19、20、21、22、23、24、29、30、36、37、39、40、63、64、139、140からなる群から選択される配列を含むアデノウイルス検出プローブオリゴマーをさらに含む、項目1、4、7、8~11、および16~19のいずれか一項に記載の組成物またはキット。
(項目30)
前記第2の標的核酸がアデノウイルスであり、かつ前記組成物またはキットが、配列番号4、10、17、18、19、20、21、22、23、24、29、30、36、37、39、40、63、64、139、140からなる群から選択される配列を含む検出プローブオリゴマーをさらに含む、項目5または6のいずれか一項に記載の組成物またはキット。
(項目31)
前記組成物またはキットが、18~36個の核酸塩基長である配列を含むアデノウイルス検出プローブオリゴマーをさらに含み、前記18~36個の核酸塩基が、全て配列番号138内の連続した核酸塩基から選択される、項目1、4、7、8~11、および16
~19のいずれか一項に記載の組成物またはキット。
(項目32)
前記第2の標的核酸がアデノウイルスであり、前記組成物またはキットが、18~36個の核酸塩基長である配列を含む検出プローブオリゴマーをさらに含み、前記18~36個の核酸塩基が、全て配列番号138内の連続した核酸塩基から選択される、項目15または6のいずれか一項に記載の組成物またはキット。
(項目33)
前記組成物またはキットが、配列番号67、69、70、155、156、157、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、および176からなる群から選択される配列を含むメタニューモウイルス検出プローブオリゴマーをさらに含む、項目2、5、7、8、9、12、13、20、21、22、および23のいずれか一項に記載の組成物またはキット。
(項目34)
前記第2の標的核酸がメタニューモウイルスであり、前記組成物またはキットが、配列番号67、69、70、155、156、157、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、および176からなる群から選択される配列を含む検出プローブオリゴマーをさらに含む、項目4または6のいずれか一項に記載の組成物またはキット。
(項目35)
前記組成物またはキットが、18~36個の核酸塩基長である配列を含むメタニューモウイルス検出プローブオリゴマーをさらに含み、前記18~36個の核酸塩基が、全て配列番号161内または配列番号155内の連続した核酸塩基から選択される、項目2、5、7、8、9、12、13、20、21、22、および23のいずれか一項に記載の組成物またはキット。
(項目36)
前記第2の標的核酸がメタニューモウイルスであり、前記組成物またはキットが、18~36個の核酸塩基長である配列を含む検出プローブオリゴマーをさらに含み、前記18~36個の核酸塩基が、全て配列番号161内または配列番号155内の連続した核酸塩基から選択される、項目4または6のいずれか一項に記載の組成物またはキット。
(項目37)
前記組成物またはキットが、配列番号48、49、54、87~94、109~114、および131~136からなる群から選択される配列を含むライノウイルス検出プローブオリゴマーをさらに含む、項目3、6、7、8、9、14、15、および24~27のいずれか一項に記載の組成物またはキット。
(項目38)
前記第2の標的核酸がライノウイルスであり、前記組成物またはキットが、配列番号48、49、54、87~94、109~114、および131~136からなる群から選択される配列を含む検出プローブオリゴマーをさらに含む、項目4または5のいずれか一項に記載の組成物またはキット。
(項目39)
前記検出プローブオリゴマーのうちの少なくとも1つが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含む、項目28~38のいずれか一項に記載の組成物またはキット。
(項目40)
前記検出プローブオリゴマーのうちの少なくとも1つが、検出可能な標識を含む、項目28~39のいずれか一項に記載の組成物またはキット。
(項目41)
前記検出可能な標識がフルオロフォアである、項目40に記載の組成物またはキット
。
(項目42)
前記検出プローブオリゴマーが二重標識検出プローブオリゴマーである、項目40または項目41に記載の組成物またはキット。
(項目43)
前記検出プローブオリゴマーが、蛍光検出可能な標識と、前記蛍光標識からの蛍光発光を消光することができる消光剤部分とを含む、項目42に記載の組成物またはキット。
(項目44)
前記組成物またはキットが、1つ以上の追加の増幅オリゴマーをさらに含み、前記増幅オリゴマーの各々が、アデノウイルス標的核酸を増幅するように構成された、項目1、4、7~11、16~19、28~32、および39~43のいずれか一項に記載の組成物またはキット。
(項目45)
前記第2の標的核酸がアデノウイルスであり、前記組成物またはキットが、1つ以上の追加の増幅オリゴマーをさらに含み、前記増幅オリゴマーの各々が、アデノウイルス標的核酸を増幅するように構成された、項目5または項目6に記載の組成物またはキット。
(項目46)
前記1つ以上の追加の増幅オリゴマーの各々が、配列番号1~9、11~16、25~28、31~35、38、42~46、61、62、および71~74からなる群から別々に選択される標的ハイブリダイズ配列を含む、項目44または45に記載の組成物またはキット。
(項目47)
前記組成物またはキットが、1つ以上の追加の増幅オリゴマーをさらに含み、前記増幅オリゴマーの各々が、メタニューモウイルス標的核酸を増幅するように構成された、項目2、5、7、8、9、12、13、20~23、28、33~36、および39~43のいずれか一項に記載の組成物またはキット。
(項目48)
前記第2の標的核酸がメタニューモウイルスであり、前記組成物またはキットが、1つ以上の追加の増幅オリゴマーをさらに含み、前記増幅オリゴマーの各々が、メタニューモウイルス標的核酸を増幅するように構成された、項目4または項目6に記載の組成物またはキット。
(項目49)
前記1つ以上の追加の増幅オリゴマーの各々が、配列番号52、53、56、68、151、152、153、154、158、160、177、178からなる群から別々に選択される標的ハイブリダイズ配列を含む、項目47または48に記載の組成物またはキット。
(項目50)
前記組成物またはキットが、1つ以上の追加の増幅オリゴマーをさらに含み、前記増幅オリゴマーの各々が、ライノウイルス標的核酸を増幅するように構成された、項目3、6、7、8、9、14、15、24~28、および37~43のいずれか一項に記載の組成物またはキット。
(項目51)
前記第2の標的核酸がライノウイルスであり、前記組成物またはキットが、1つ以上の追加の増幅オリゴマーをさらに含み、前記増幅オリゴマーの各々が、ライノウイルス標的核酸を増幅するように構成された、項目4または項目5に記載の組成物またはキット。
(項目52)
前記1つ以上の追加の増幅オリゴマーの各々が、配列番号50、51、57、59、60、65、75、77~86、95~100、102~108、115~119、121
~130、137からなる群から別々に選択される標的ハイブリダイズ配列を含む、項目47または48に記載の組成物またはキット。
(項目53)
前記組成物またはキットが、少なくとも第1および第2の増幅オリゴマー、ならびにアデノウイルス標的核酸を増幅するように構成された1つ以上の追加の増幅オリゴマーを含み、前記増幅オリゴマーの各々が、配列番号61、62、71、72、73、および74からなる群から選択される配列を独立して含む、項目1、4、7~11、16~19、28~32、および39~47のいずれか一項に記載の組成物またはキット。
(項目54)
前記組成物またはキットが、少なくとも第1および第2の増幅オリゴマー、ならびにメタニューモウイルス標的核酸を増幅するように構成された1つ以上の追加の増幅オリゴマーを含み、前記増幅オリゴマーの各々が、配列番号52、53、56、および58からなる群から選択される配列を各々独立して含む、項目2、5、7、8、9、12、13、20~23、28、33~36、39~43、46~49、および53のいずれか一項に記載の組成物またはキット。
(項目55)
前記組成物またはキットが、少なくとも第1および第2の増幅オリゴマー、ならびにライノウイルス標的核酸を増幅するように構成された1つ以上の追加の増幅オリゴマーを含み、前記増幅オリゴマーの各々が、配列番号50、51、57、59、60、および65からなる群から選択される配列を各々独立して含む、項目3、6、7、8、9、14、15、24~28、37~43、および50~54のいずれか一項に記載の組成物またはキット。
(項目56)
前記組成物またはキットが、2つのアデノウイルス検出プローブオリゴマーをさらに含み、前記検出プローブオリゴマーの各々が、配列番号63および64からなる群から選択される配列を独立して含む、項目1、4、7~11、16~19、28~32、39~47、および53~55のいずれか一項に記載の組成物またはキット。
(項目57)
前記組成物またはキットが、3つのメタニューモウイルス検出プローブオリゴマーをさらに含み、前記検出プローブオリゴマーの各々が、配列番号67、69、および70からなる群から選択される配列を独立して含む、項目2、5、7、8、9、12、13、20~23、28、33~36、39~43、46~49、および53~56のいずれか一項に記載の組成物またはキット。
(項目58)
前記組成物またはキットが、3つのライノウイルス検出プローブオリゴマーをさらに含み、前記検出プローブオリゴマーの各々が、配列番号48、49、および54からなる群から選択される配列を独立して含む、項目3、6、7、8、9、14、15、24~28、37~43、および50~57のいずれか一項に記載の組成物またはキット。
(項目59)
前記組成物またはキットが、標的ハイブリダイズ配列と固定化プローブ結合領域とを含む核酸標的捕捉プローブをさらに含む、先行する項目のいずれか一項に記載の組成物またはキット。
(項目60)
前記標的ハイブリダイズ配列がポリKヌクレオチド配列である、項目59に記載の組成物またはキット。
(項目61)
前記ポリKヌクレオチド配列がランダムなポリGU配列である、項目60に記載の組成物またはキット。
(項目62)
固定化プローブ結合領域が、好ましくはT0-4A10-36からなる群から選択され
るヌクレオチド配列を含む、ホモポリマーヌクレオチド配列である、項目59、60、または61に記載の組成物またはキット。
(項目63)
前記組成物が、酵素、緩衝液、dNTP、またはそれらの組み合わせをさらに含む、項目1~62のいずれか一項に記載の組成物またはキット。
(項目64)
試料中のアデノウイルス標的核酸、メタニューモウイルス標的核酸、ライノウイルス標的核酸、またはそれらの組み合わせの非存在の存在(presence of absence)を決定する
ための方法であって、
(A)試料を項目1~58のいずれか一項に記載の増幅オリゴマーの組み合わせと接触させるステップと、
(B)試料中のアデノウイルス標的核酸、メタニューモウイルス標的核酸、またはライノウイルス標的核酸のうちのいずれかが、その標的核酸を増幅して増幅産物を生成するように構成された増幅オリゴマーの組み合わせによって使用される、インビトロ核酸増幅反応を実行するステップと、
(C)前記増幅産物を検出するステップと、を含み、
それにより、前記試料中の前記標的核酸の有無を決定する、方法。
(項目65)
前記試料がヒトに由来する試料である、項目64に記載の方法。
(項目66)
前記試料が粘膜試料である、項目65に記載の方法。
(項目67)
前記試料が、鼻咽頭スワブを使用して得られる、項目65または項目66に記載の方法。
(項目68)
ステップ(A)の前に、試料調製ステップを実行して、前記試料中のあらゆる標的核酸を他の試料成分から分離させる、項目64~67のいずれか一項に記載の方法。
(項目69)
前記試料調製ステップが標的捕捉ステップを含む、項目68に記載の方法。
(項目70)
前記標的捕捉ステップが、前記試料を、標的ハイブリダイズ配列および固定化プローブ結合領域を含む核酸標的捕捉プローブと接触させることを含む、項目69に記載の方法。
(項目71)
前記標的ハイブリダイズ配列がポリKヌクレオチド配列である、項目70に記載の方法。
(項目72)
前記ポリKヌクレオチド配列がランダムなポリGU配列である、項目71に記載の方法。
(項目73)
固定化プローブ結合領域が、好ましくはT0-4A10-36からなる群から選択されるヌクレオチド配列を含む、ホモポリマーヌクレオチド配列である、項目70、71、または72に記載の方法。
(項目74)
前記検出ステップ(C)が、1つ以上の検出プローブオリゴマーを使用して実行される、項目64~73のいずれか一項に記載の方法。
(項目75)
前記1つ以上の検出プローブオリゴマーの各々が、配列番号4、10、17、18、19、20、21、22、23、24、29、30、36、37、39、40、63、64、139、140、67、69、70、155、156、157、161、162、16
3、164、165、166、167、168、169、170、171、172、173、174、175、176、48、49、54、87~94、109~114、および131~136からなる群から個々に選択される、項目74に記載の方法。
(項目76)
前記検出プローブオリゴマーのうちの少なくとも1つが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含む、項目74または75に記載の方法。
(項目77)
前記検出プローブオリゴマーのうちの少なくとも1つが、検出可能な標識を含む、項目74、75、または76に記載の方法。
(項目78)
前記検出可能な標識がフルオロフォアである、項目77に記載の方法。
(項目79)
前記検出プローブオリゴマーが二重標識検出プローブオリゴマーである、項目77または項目78に記載の方法。
(項目80)
前記検出プローブオリゴマーが、蛍光検出可能な標識と、前記蛍光標識からの蛍光発光を消光することができる消光剤部分とを含む、項目79に記載の方法。
(項目81)
前記インビトロ核酸増幅反応が熱循環を含む、項目64~80のいずれか一項に記載の方法。
(項目82)
前記インビトロ核酸増幅反応が、5’から3’へのエキソヌクレアーゼ活性を有するポリメラーゼ酵素によるPCRを含む、項目64~81のいずれか一項に記載の方法。
(項目83)
前記インビトロ核酸増幅反応が、5’から3’へのエキソヌクレアーゼ活性を有する酵素を使用して実行される、項目75~80のいずれか一項に記載の方法。
(項目84)
前記インビトロ核酸増幅反応が、5’から3’へのエキソヌクレアーゼ活性を有する酵素を使用して実行され、増幅産物が、所定の閾値を超える蛍光値を決定することによって検出される、項目77~80のいずれか一項に記載の方法。
(項目85)
項目64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、または84に記載の方法の1つ以上のステップを実行するためのシステム。
(項目86)
前記システムが自動システムである、項目85に記載のシステム。
(項目87)
前記システムが、前記方法の前記ステップの全てを実行する、項目85または86に記載のシステム。
(項目88)
試料中のアデノウイルス標的核酸、メタニューモウイルス標的核酸、ライノウイルス標的核酸、またはそれらの組み合わせの前記インビトロ検出のための方法であって、前記方法が、アデノウイルス標的核酸、メタニューモウイルス標的核酸、および/またはライノウイルス標的核酸を、項目29~43のいずれかに記載の検出プローブオリゴマーと接触させることを含み、前記検出プローブオリゴマーと、前記検出プローブオリゴマーがハイブリダイズするように構成された前記標的核酸とのハイブリダイゼーションが、その標的核酸の存在を示す、方法。
(項目89)
前記方法が、前記アデノウイルス標的核酸、前記メタニューモウイルス標的核酸、およ
び/または前記ライノウイルス標的核酸からの増幅産物を、前記検出プローブオリゴマーと接触させることを含み、前記検出プローブオリゴマーと、前記検出プローブオリゴマーがハイブリダイズするように構成された前記増幅産物とのハイブリダイゼーションが、前記増幅産物の生成元であるその標的核酸の存在を示す、項目88に記載の方法。
(項目90)
前記インビトロ検出反応が、5’から3’へのエキソヌクレアーゼ活性を有する酵素を使用して実行される、項目88または89に記載の方法。
(項目91)
前記インビトロ検出反応が、5’から3’へのエキソヌクレアーゼ活性を有する酵素を使用して実行され、前記標的核酸またはそれから生成された前記増幅産物が、所定の閾値を超える蛍光値を決定することによって検出される、項目88~90のいずれか一項に記載の方法。
(項目92)
項目88~91のいずれか一項に記載のインビトロ検出反応を実行するためのシステム。
(項目93)
前記システムが自動システムである、項目92に記載のシステム。
(項目94)
前記システムが、前記方法の前記ステップの全てを実行する、項目92または93に記載のシステム。
(項目95)
項目1~27のいずれか一項に記載の増幅オリゴマーのうちの1つ以上を含む、乾燥組成物。
(項目96)
項目44~55のいずれか一項に記載の増幅オリゴマーうちの1つ以上を含む、乾燥組成物。
(項目97)
項目29~43または56~58のいずれかに記載の検出プローブオリゴマーのうちの1つ以上を含む、乾燥組成物。
(項目98)
項目1~58のいずれか一項に記載の増幅オリゴマーおよび/または検出プローブオリゴマーの組み合わせを含む、乾燥組成物。
(項目99)
前記乾燥組成物が、酵素、dNTP、またはその両方をさらに含む、項目95~98のいずれか一項に記載の乾燥組成物。
(項目100)
前記酵素が、5’から3’へのエキソヌクレアーゼ活性を有する、項目99に記載の乾燥組成物。
(項目101)
前記酵素がポリメラーゼ酵素である、項目99または項目100に記載の乾燥組成物。
(項目102)
前記乾燥組成物が、10mM以下の無機塩濃度を有する、項目95~101のいずれか一項に記載の乾燥組成物。
(項目103)
前記乾燥組成物が、7mM以下の無機塩濃度を有する、項目95~102のいずれか一項に記載の乾燥組成物。
(項目104)
前記乾燥組成物が、5mM以下の無機塩濃度を有する、項目95~103のいずれか一項に記載の乾燥組成物。
(項目105)
前記乾燥組成物が、約0.5mM~約10mMの無機塩濃度を有する、項目95~101のいずれか一項に記載の乾燥組成物。
アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸の増幅検出のためのプライマーとして役立ち得る核酸オリゴマー配列が開示される。これらの標的核酸は、PCR(例えば、Taqman(商標)PCR)などのインビトロ核酸増幅法またはTMAもしくはNASBAなどの転写媒介増幅法を使用して、試料中で検出され得る。増幅された核酸配列の検出のためのプローブも記載される。検出プローブは、増幅プロセスの完了後または増幅プロセス中に、増幅された配列の少なくとも一部に特異的にハイブリダイズする。本明細書に開示される方法は、動物およびヒトからのまたはそれらに由来する試料に存在するアデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を増幅および検出するために使用することができる。
5つ以上、6つ以上、またはさらには10以上)から生成され得る多重増幅反応の成分としてさらに企図される。例えば、本明細書に開示される増幅系のうちの2つ以上を組み合わせて、標的検出の能力、例えば、核酸を、少なくとも2つ、少なくとも3つ、少なくとも4つ以上の微生物から増幅および検出する能力が堅牢で幅広い多重アッセイをもたらす
ことができると企図される。例えば、本明細書で開示される増幅系を組み合わせて、以下の標的検出のための多重アッセイをもたらすことができる:アデノウイルス標的核酸および少なくとも1つの追加の標的核酸、メタニューモウイルス標的核酸および少なくとも1つの追加の標的核酸、ライノウイルス標的核酸および少なくとも1つの追加の標的核酸、アデノウイルス標的核酸およびメタニューモウイルス標的核酸および少なくとも1つの追加の標的核酸、アデノウイルス標的核酸およびライノウイルス標的核酸および少なくとも1つの追加の標的核酸、ライノウイルスの標的核酸およびメタニューモウイルスの標的核酸および少なくとも1つの追加の標的核酸、アデノウイルス標的核酸およびメタニューモウイルス標的核酸およびライノウイルス標的核酸および少なくとも1つの追加の標的核酸。本明細書に記載の多重アッセイは、種の異なるサブタイプまたはサブグループ、微生物の異なる種、またはそれらの組み合わせを各々増幅および検出する2つ以上の増幅系を提供することを含む。
Dictionary of Biology(Hale&Marham,1991,Harper Perennial,New York,NY)、および本明細書で引用される参考文献で提供され得るものなど、関連分野の当業者によって一般に理解されるのと同じ意味を有する。別途述べられない限り、本明細書で使用または企図される技法は、分子生物学の当業者に周知の標準的な方法である。
「a」または「an」、「the」の付く実体は、その実体の1つ以上を指すことに留意されたい。例えば、「核酸(a nucleic acid)」は、1つ以上の核酸を表すと理解される。したがって、「a」(または「an」)、「1つ以上の」、および「少なくとも1つの」という用語は、本明細書において互換的に使用され得る。
組み合わせのうちの1つ以上を含む様々な結合から構成され得る。核酸の糖部分は、リボースもしくはデオキシリボースのいずれか、または既知の置換、例えば、2’メトキシ置換および2’ハライド置換(例えば2’-F)を有する同様の化合物であり得る。窒素塩基は、従来の塩基(A、G、C、T、U)、その類似体(例えば、イノシン、5メチル2’デオキシシトシン(5-Me-dC)、イソグアニン;The Biochemistry of the Nucleic Acids 5-36,Adams et al.,ed.,11th ed.,1992、Abraham et al.,2007,BioTechniques 43:617-24)であってもよく、これは、プリンまたはピリミジン塩基の誘導体(例えば、N4-メチルデオキシグアノシン、デアザ-またはアザ-プリン、デアザ-またはアザ-ピリミジン、5または6位に置換基を有するピリミジン塩基、2、6、および/または8位に改変または置き換え置換基を有するプリン塩基、例えば、2-アミノ-6-メチルアミノプリン、O6-メチルグアニン、4-チオ-ピリミジン、4-アミノ-ピリミジン、4-ジメチルヒドラジン-ピリミジン、およびO4-アルキル-ピリミジン、ならびにピラゾロ-化合物、例えば、非置換または3-置換ピラゾロ[3,4-d]ピリミジン;米国特許第5,378,825号、同第6,949,367号、およびPCT第WO93/13121号)を含む。核酸は、骨格が1つ以上の残基に対して窒素塩基を含まない「無塩基」残基を含み得る(米国特許第5,585,481号)。核酸は、RNAおよびDNAに見られるような従来の糖、塩基、および結合のみを含んでもよく、または従来の成分および置換(例えば、2’メトキシ骨格によって結合される従来の塩基、もしくは従来の塩基および1つ以上の塩基類似体の混合物を含む核酸)を含んでもよい。核酸は、「ロックド核酸」(LNA)を含んでもよく、その中で、1つ以上のヌクレオチドモノマーは、糖立体配座を模倣するRNAにロックされた二環式フラノース単位を有し、一本鎖RNA(ssRNA)、一本鎖DNA(ssDNA)、または二本鎖DNA(dsDNA)中の相補的配列に対するハイブリダイゼーション親和性を増強する(Vester et al.,2004,Biochemistry 43(42):13233-41)。核酸は、核酸の機能または挙動を変化させるための修飾塩基、例えばさらなるヌクレオチドが核酸に付加されるのを阻止するための3’末端ジデオキシヌクレオチドの付加を含み得る。インビトロで核酸を作製するための合成方法は、当該技術分野において周知であるが、核酸は、日常的な技術を使用して天然源から精製されてもよい。
ゼーションを防止するかまたはプライマー伸長を妨げるように機能してもよい。
以上の成分が他の試料成分から除去または分離されることを意味する。試料成分は、通常、細胞断片、タンパク質、炭水化物、脂質、および他の核酸も含み得る、一般に水性の溶液相中の標的核酸を含む。分離することまたは精製することは、他の試料成分から標的核酸の少なくとも70%、または少なくとも80%、または少なくとも95%を除去する。純度%の範囲は、その範囲の全ての整数および有理数を含む。
している。多くの異なる化学基、例えば、アルキル基、非ヌクレオチドリンカー、アルカン-ジオールジデオキシヌクレオチド残基、およびコルジセピンが、3’末端をブロックするために使用され得る。
語は、一本鎖増幅産物、二本鎖増幅産物、または二本鎖増幅産物の鎖のうちの一方を指すために使用され得る。
RA(商標)化合物を含む。合成、ならびに標識を核酸に結合する方法、および標識を検出する方法は周知である(例えば、Sambrook et al.,Molecular Cloning,A Laboratory Manual,2nd ed.(Cold Spring Harbor Laboratory Press,Cold Spring Harbor,NY,1989),Chapter10、ならびに米国特許第5,658,737号、同第5,656,207号、同第5,547,842号、同第5,283,174号、および同第4,581,333号)。2つ以上の標識および2つ以上のタイプの標識が特定のプローブ上に存在してもよく、または検出は、異なる検出可能なシグナルを産生する化合物によって各プローブが標識されるプローブの混合物を使用してもよい(例えば、米国第6,180,340号および同第6,350,579号)。
とえ配列が完全に相補的でないとしても、適切なハイブリダイゼーション条件下で核酸オリゴマーとその標的配列との安定なハイブリダイゼーションを可能にする。ある一本鎖領域のヌクレオチドの連続した配列が、他の一本鎖領域のヌクレオチドの類似配列と一連の「基準の」水素結合塩基対を形成することが可能であり、これによりAがUまたはTと対になり、CがGと対になる場合、ヌクレオチド配列は、「完全に」相補的である。
Spring Harbor,NY,1989)の§§1.90-1.91、7.37-7.57、9.47-9.51、および11.47-11.57、特に§§9.50-9.51、11.12-11.13、11.45-11.47、および11.55-11.57)。
に本明細書で使用される。増幅反応の感度は、一般に、増幅系において確実に検出され得る標的核酸の最小コピー数の尺度であり、例えば、用いられている検出アッセイおよび増幅の特異性、例えば、副生成物に対する特異的アンプリコンの比に依存する。
アデノウイルス、メタニューモウイルス、および/またはライノウイルスの標的核酸の各々を増幅するためのオリゴヌクレオチドは、典型的には、標的あたり少なくとも2つの増幅オリゴマーを含む。本開示のいくつかの実施形態は、例えば多重増幅アッセイにおいて、標的あたり2つ、3つ、4つ、5つ、6つ、またはそれより多くの増幅オリゴマーを利用してもよい。したがって、例として、各標的微生物を増幅するためのオリゴヌクレオチドは、1つ、2つ、3つ、4つ、5つ、またはそれより多くの順方向増幅プライマーと、1つ、2つ、3つ、4つ、5つ、またはそれより多くの逆方向増幅プライマーとを含んでもよい。例えば、アデノウイルスを増幅するためのオリゴヌクレオチドは、1つ、2つ、3つ、4つ、5つ、またはそれより多くの順方向増幅プライマーと、1つ、2つ、3つ、4つ、5つ、またはそれより多くの逆方向増幅プライマーとを含んでもよい。hMPVを増幅するためのオリゴヌクレオチドは、1つ、2つ、3つ、4つ、5つ、またはそれより多くの順方向増幅プライマーと、1つ、2つ、3つ、4つ、5つ、またはそれより多くの逆方向増幅プライマーとを含んでもよい。HRVを増幅するためのオリゴヌクレオチドは、1つ、2つ、3つ、4つ、5つ、またはそれより多くの順方向増幅プライマーと、1つ、2つ、3つ、4つ、5つ、またはそれより多くの逆方向増幅プライマーとを含んでもよい。さらに、標的微生物のサブタイプまたはサブグループは、少なくとも2つの増幅オリゴマーを必要とし得、これらの増幅オリゴマーのそれぞれが、微生物のサブタイプ/サブグループのうちの1つ以上の異なるメンバー(単数または複数)に特異的なヌクレオチド配列を含む。
々を検出するためのオリゴヌクレオチドは、典型的には、標的あたり少なくとも1つの検出オリゴマーを含む。本開示のいくつかの実施形態は、例えば多重検出アッセイにおいて、標的あたり2つ、3つ、4つ、5つ、6つ、またはそれより多くの検出プローブオリゴマーを利用してもよい。例えば、アデノウイルスを検出するためのオリゴヌクレオチドは、1つ、2つ、3つ、4つ、またはそれより多くの検出プローブオリゴマーを含んでもよい。hMPVを検出するためのオリゴヌクレオチドは、1つ、2つ、3つ、4つ、またはそれより多くの検出プローブオリゴマーを含んでもよい。HRVを検出するためのオリゴヌクレオチドは、1つ、2つ、3つ、4つ、またはそれより多くの検出プローブオリゴマーを含んでもよい。さらに、標的微生物のサブタイプまたはサブグループは、少なくとも2つの検出プローブオリゴマーを必要とし得、これらの検出プローブオリゴマーのそれぞれが、微生物のサブタイプ/サブグループのうちの1つ以上の異なるメンバー(単数または複数)に特異的なヌクレオチド配列を含む。アデノウイルス、メタニューモウイルス、およびライノウイルス標的核酸のうちの1つ以上の多重増幅および検出のためのオリゴマーの組み合わせは、典型的には、少なくとも2つの順方向増幅オリゴマー、少なくとも2つの逆方向増幅オリゴマー、および少なくとも2つの検出プローブオリゴマーを含む。本開示のいくつかの実施形態は、意図される標的核酸各々に対して、2つ、3つ、4つ、5つ、またはさらに6つ、またはそれより多くの増幅オリゴマーと、2つ、3つ、4つ、5つ、またはさらに6つ、またはそれより多くのプローブとを利用してもよい。したがって、例として、いくつかの標的の多重増幅および検出のためのオリゴヌクレオチドは、6~40個の増幅オリゴマーと3~15個の検出プローブオリゴマーとを含んでもよい。
するように構成される。
標的ハイブリダイズ配列を含む、それからなる、またはそれから本質的になる増幅オリゴマーが含まれる。第1の増幅オリゴマーの実施形態には、配列番号52、53、151、152、153、154、160、またはそれらの2つ以上の組み合わせからなる群から選択される標的ハイブリダイズ配列を含む、それからなる、またはそれから本質的になる増幅オリゴマーが含まれる。第2の増幅オリゴマーの実施形態には、配列番号56、68、158、177、178、またはそれらの2つ以上の組み合わせからなる群から選択される標的ハイブリダイズ配列を含む、それからなる、またはそれから本質的になる増幅オリゴマーが含まれる。一実施形態では、hMPV標的核酸を増幅するための増幅オリゴマーのうちの1つ以上は、5-Me-dC、非ワトソンクリック塩基、縮重塩基、またはそれらの組み合わせのうちの少なくとも1つを含む。
れらの18~35個の核酸塩基は、全て配列番号96内の連続した核酸塩基から選択される。一実施形態では、18~27個の核酸塩基長である増幅オリゴヌクレオチドが提供され、これらの18~27個の核酸塩基は、全て配列番号115内の連続した核酸塩基から選択される。一実施形態では、18~27個の核酸塩基長である増幅オリゴヌクレオチドが提供され、これらの18~27個の核酸塩基は、全て配列番号137内の連続した核酸塩基から選択される。一実施形態では、HRV標的核酸を増幅するための増幅オリゴマーのうちの1つ以上は、5-Me-dC、非ワトソンクリック塩基、縮重塩基、またはそれらの組み合わせのうちの少なくとも1つを含む。
標的核酸配列の増幅および検出のための試料の調製は、試料中に含まれる微生物を他の試料成分から分離および/または濃縮する方法を含んでもよい。試料調製は、試料を破壊するかまたは試料を溶解して、標的核酸または標的核酸を含む遺伝子配列を含む細胞内含有物を放出する日常的な方法を含んでもよい。増幅前の試料調製は、標的核酸を他の試料成分から特異的または非特異的に分離するための任意選択の標的捕捉ステップを含んでもよい。非特異的標的捕捉法は、実質的に水性の混合物からの核酸の選択的沈殿、他の試料成分を除去するために洗浄される支持体への核酸の付着、アデノウイルス核酸および他の試料成分を含有する混合物から核酸を物理的に分離する他の方法を伴ってもよい。
2つ以上のプライマーを使用した標的核酸標的領域の増幅は、様々な既知の核酸増幅反応を使用して達成され得る。例えば、増幅は、PCR増幅(Mullisらの米国特許第4,683,195号、同第4,683,202号、および同第4,800,159号)を使用して、DNAポリメラーゼを使用することによって追加のdsDNA分子を作製するために、dsDNAおよび分離された鎖の一部に特異的なプライマーを分離する熱循環反応を使用することによって複数のDNA鎖を生成することで、達成されてもよい。また、基本的なPCR法の周知の変形、例えば、Taqman PCRなどのリアルタイム検出と組み合わせたPCRを使用してもよい。
核酸の検出は、様々な方法によって達成され得る。検出方法は、増幅産物の一部に相補的な標的ハイブリダイズ配列を含み、プローブ:産物複合体の存在を検出する核酸プローブを使用してもよく、または増幅産物と関連する検出可能なシグナルを増幅させ得るプローブの複合体を使用することによる(例えば、米国特許第5,424,413号、同第5,451,503号、同第5,849,481号、同第5,639,604号、および同
第5,283,174号)。増幅産物と特異的に会合する直接的または間接的に標識されたプローブは、試料中の標的核酸の存在を示す検出可能なシグナルを提供する。例えば、標的核酸がアデノウイルスDNAである場合、増幅産物は、アデノウイルス標的配列内の配列またはアデノウイルス標的配列に相補的な配列を含有することになる。プローブは、増幅産物の一部に直接または間接的に結合して、試験された試料中のアデノウイルスの存在を示すように構成される。
光シグナルが発生する。2つの蛍光レベル間の差は、検出可能かつ測定可能である。本開示に関連して使用され得るフルオロフォア/消光剤標識ペアの例には、フルオレセイン/テトラメチルローダミン、IAEDANS/フルオロレセイン、EDANS/D ABCYL、クマリン/D ABCYL、フルオレセイン/フルオレセイン、BODIPY FL/BODIPY FL、フルオレセイン/D ABCYL、ルシファーイエロー/D ABCYL、BODIPY/D ABCYL、エオシン/D ABCYL、エリスロシン/D ABCYL、テトラメチルローダミン/D ABCYL、CalOrange/BHQ1、CalRed/BHQ2、Texas Red/DABCYL、CY5/BH1、CY5/BH2、CY3/BH1、CY3/BH2、フルオレセイン/QSY7、FAM/BHQ1、およびQuasar/BHQ2が含まれる。当業者であれば、供与体色素と受容体色素が異なる場合、受容体の増感蛍光の出現または供与体蛍光の消光によって、エネルギー移動が検出され得ることを理解するであろう。供与体種と受容体種が同じである場合、エネルギーは、結果として生じる蛍光偏光解消によって検出され得る。DABCYLおよびQSY7色素などの非蛍光受容体は、直接(即ち、非増感)受容体励起から生じるバックグラウンド蛍光の潜在的な問題を有利に排除する。
Harbor Laboratory Press,Cold Spring Harbor,NY,1989),Chapter 10、Nelsonらの米国特許第5,658,737号、Woodheadらの米国特許第5,656,207号、Hoganらの米国特許第5,547,842号、Arnoldらの米国特許第5,283,174号、Kourilskyらの米国特許第4,581,333号)、およびBeckerらの欧州特許出願第0 747 706号を参照されたい。
本明細書に記載の方法において使用するためのオリゴマーは、キットの調製に好適である。そのようなキットは容器を含んでもよく、各々は、様々なオリゴマーのうちの1つ以上を、任意選択で本明細書に記載の方法を実施するのに必要な試薬(例えば、酵素)のうちの1つ以上とともに有する。キットの構成要素は、濃縮された形態で供給されてもよい。典型的には、キットの構成要素を使用するための一連の説明書も含まれることになる。キットがオリゴマーの組み合わせを含む場合には、個々のオリゴマーは、それらを混合するための適切な説明書を伴う個々の形態、またはすぐに混合できるそれらの組み合わせで提供されてもよい。
個体からの生体試料におけるアデノウイルス、メタニューモウイルス、および/またはライノウイルスに特徴的な増幅された標的配列の検出は、それぞれ、アデノウイルス、メタニューモウイルス、および/またはライノウイルスによる感染を示す。
材料および方法
最初の増幅反応では、次のものを使用した:1倍~2倍濃度のFast Start Master Buffer(Roche)、2単位のFast Start Taq DNAポリメラーゼ(Roche)、100nMの順方向増幅プライマー(配列番号5)
、および100nMの逆方向増幅プライマー(配列番号6または配列番号8)、および100nMのプローブ(配列番号10)。
使用したプライマーおよびプローブは、アデノウイルス核酸に高感度かつ特異的であるように見えた。
材料および方法
次の試薬を使用した:1倍~2倍濃度のFast Start Master Buffer(Roche)、2単位のFast Start Taq DNAポリメラーゼ(Roche)、200nMの順方向増幅プライマー(配列番号11または配列番号12)、および200nMの逆方向増幅プライマー(配列番号13または配列番号15)、および200nMのプローブ(配列番号17または配列番号19)。
配列番号11、13、および19、配列番号11、15、および19、配列番号12、15、および19、または配列番号12、13、および19の組み合わせは、アデノウイルス核酸に対して高感度および特異性であった。配列番号12の順方向プライマーを含む組み合わせは、配列番号11の順方向プライマーを含む組み合わせよりも良好な感度を有するようである。配列番号12、15、および19を含む組み合わせは、これらの実験で最も感度が高いようであった。
材料および方法
次の試薬を使用した:1倍濃度のFast Start Master Buffer(Roche)、2単位のFast Start Taq DNAポリメラーゼ(Roche)、400nMの順方向増幅プライマー(配列番号12)および400nMの逆方向増幅プライマー(配列番号15)を400nMプローブ(配列番号19)とともに使用。総反応量は20マイクロリットルで、反応ごとにアデノウイルスから抽出した5マイクロリットルの鋳型核酸を添加した。対照反応をセットアップしたが、鋳型核酸の添加はしなかった。使用した増幅サイクルは次のとおりであった:光学系をオフにして95℃で600秒間保持;光学系をオフにして95℃で30秒間および光学系をオンにして55℃で60秒間(5サイクル);光学系をオフにして95℃で10秒間および光学系をオンにして55℃で60秒間(40サイクル)。
配列番号12、15、および19の組み合わせは、試験されたアデノウイルスの全ての血清型を検出することができた。
材料および方法
次の試薬を使用した:1倍濃度のFast Start Master Buffer(Roche)、2単位のFast Start Taq DNAポリメラーゼ(Roche)、100nMの順方向増幅プライマー(配列番号12)および100nMの逆方向増幅プライマー(配列番号15)を、150nMプローブ(配列番号21)および50nMプローブ(配列番号24)、100nMプローブ(配列番号21)および100nMプローブ(配列番号24)、50nMプローブ(配列番号21)および150nMプローブ(配列番号24)のいずれかとともに使用。総反応量は20マイクロリットルで、反応ごとにアデノウイルスから抽出した5マイクロリットルの鋳型核酸を添加した。対照反応は、鋳型核酸を添加せずに設定した。使用した増幅サイクルは次のとおりであった:光学系をオフにして95℃で600秒間保持;光学系をオフにして95℃で30秒間および光学系をオンにして55℃で60秒間(5サイクル);光学系をオフにして95℃で10秒間および光学系をオンにして55℃で60秒間(40サイクル)。
配列番号12および15と組み合わせた配列番号21のプローブおよび配列番号24のプローブは、試験した様々な濃度でアデノウイルスを高感度かつ特異的に検出することができた。
材料および方法
次の試薬を使用した:
1倍濃度のFast Start Master Buffer(Roche)、2単位のFast Start Taq DNAポリメラーゼ(Roche)、および以下のいずれか:(i)50mMの順方向増幅プライマー(配列番号25)、50mMの順方向増幅プライマー(配列番号26)、50mMの逆方向増幅プライマー(配列番号27)、50mMの逆方向増幅プライマー(配列番号28)、および100nMのプローブ(配列番号21および配列番号23);(ii)50mMの順方向増幅プライマー(配列番号26)、50mMの逆方向増幅プライマー(配列番号27)、50mMの逆方向増幅プライマー(配列番号28)、および100nMのプローブ(配列番号21および配列番号23);(iii)50mMの順方向増幅プライマー(配列番号25)、50mMの逆方向増幅プライマー(配列番号27)、50mMの逆方向増幅プライマー(配列番号28)、および100nMのプローブ(配列番号21および配列番号23);(iv)50mMの順方向増幅プライマー(配列番号25)、50mMの順方向増幅プライマー(配列番号26)、50mMの逆方向増幅プライマー(配列番号28)、および100nMのプローブ(配列番号21および配列番号23);(v)50mMの順方向増幅プライマー(配列番号25)、50mMの順方向増幅プライマー(配列番号26)、50mMの逆方向増幅プライマー(配列番号28)、および100nMのプローブ(配列番号21および配列番号23);(vi)50mMの順方向増幅プライマー(配列番号25)、50mMの順方向増幅プライマー(配列番号26)、50mMの逆方向増幅プライマー(配列番号27)、50mMの逆方向増幅プライマー(配列番号28)、および100nMのプローブ(配列番号23);または(vii)50mMの順方向増幅プライマー(配列番号25)、50mMの順方向増幅プライマー(配列番号26)、50mMの逆方向増幅プライマー(配列番号27)、50mMの逆方向増幅プライマー(配列番号28)、および100nMのプローブ(配列番号21)。
アッセイからプライマーまたはプローブのうちの1つを除外しても、大部分でほとんど違いはなかった。しかし、プローブ配列番号23を省略すると、この特定の実験においては検出が低下した。
材料および方法
次の試薬を使用した:1倍濃度のFast Start Master Buffer(Roche)、3単位のFast Start Taq DNAポリメラーゼ(Roche)、150nM順方向増幅プライマー(配列番号25および配列番号26)および150nM逆方向増幅プライマー(配列番号27および配列番号28)を300nMプローブ(配列番号29)とともに使用。総反応量は20マイクロリットルで、反応ごとにアデノウイルス18から抽出した5マイクロリットルの鋳型核酸を添加した。使用した増幅サイクルは次のとおりであった:光学系をオフにして95℃で600秒間保持;光学系をオ
フにして95℃で30秒間および光学系をオンにして55℃で60秒間(5サイクル);光学系をオフにして95℃で10秒間および光学系をオンにして55℃で60秒間(40サイクル)。
プライマーおよびプローブのこの組み合わせにより、アデノウイルス18が首尾よく検出される。
材料および方法
次の試薬を使用した:1倍濃度のFast Start Master Buffer(Roche)、3単位のFast Start Taq DNAポリメラーゼ(Roche)、150nM順方向増幅プライマー(配列番号31および配列番号26)および150nM逆方向増幅プライマー(配列番号27および配列番号28)を150nMプローブ(配列番号21および配列番号23)とともに使用。総反応量は20マイクロリットルで、反応ごとに様々なアデノウイルス血清型から抽出した5マイクロリットルの鋳型核酸を添加した。使用した増幅サイクルは次のとおりであった:光学系をオフにして95℃で600秒間保持;光学系をオフにして95℃で30秒間および光学系をオンにして55℃で60秒間(5サイクル);光学系をオフにして95℃で10秒間および光学系をオンにして55℃で60秒間(40サイクル)。
血清型4を除き、このプライマーおよびプローブの組み合わせにより、試験した血清型の全てが首尾よく検出された。
材料および方法
次の試薬を使用した:1倍濃度のFast Start Master Buffer(Roche)、3単位のFast Start Taq DNAポリメラーゼ(Roche)、および以下のいずれか:(i)150nM順方向増幅プライマー(配列番号33および34)および150nM逆方向増幅プライマー(配列番号27および配列番号28)を150nMプローブ(配列番号21および配列番号23)とともに使用;(ii)150nM順方向増幅プライマー(配列番号33および35)および150nM逆方向増幅プライマー(配列番号27および配列番号28)を150nMプローブ(配列番号21および配列番号23)とともに使用;または(iii)150nMの順方向増幅プライマー(配列番号34および35)および150nMの逆方向増幅プライマー(配列番号27および配列番号28)を150nMのプローブ(配列番号21および配列番号23)とともに使用。総反応量は20マイクロリットルで、反応ごとに様々なアデノウイルス血清型から抽出した5マイクロリットルの鋳型核酸を添加した。使用した増幅サイクルは次のとおりであった:光学系をオフにして95℃で600秒間保持;光学系をオフにして95℃で30秒間および光学系をオンにして55℃で60秒間(5サイクル);光学系をオフにして95℃で10秒間および光学系をオンにして55℃で60秒間(40サイクル)。
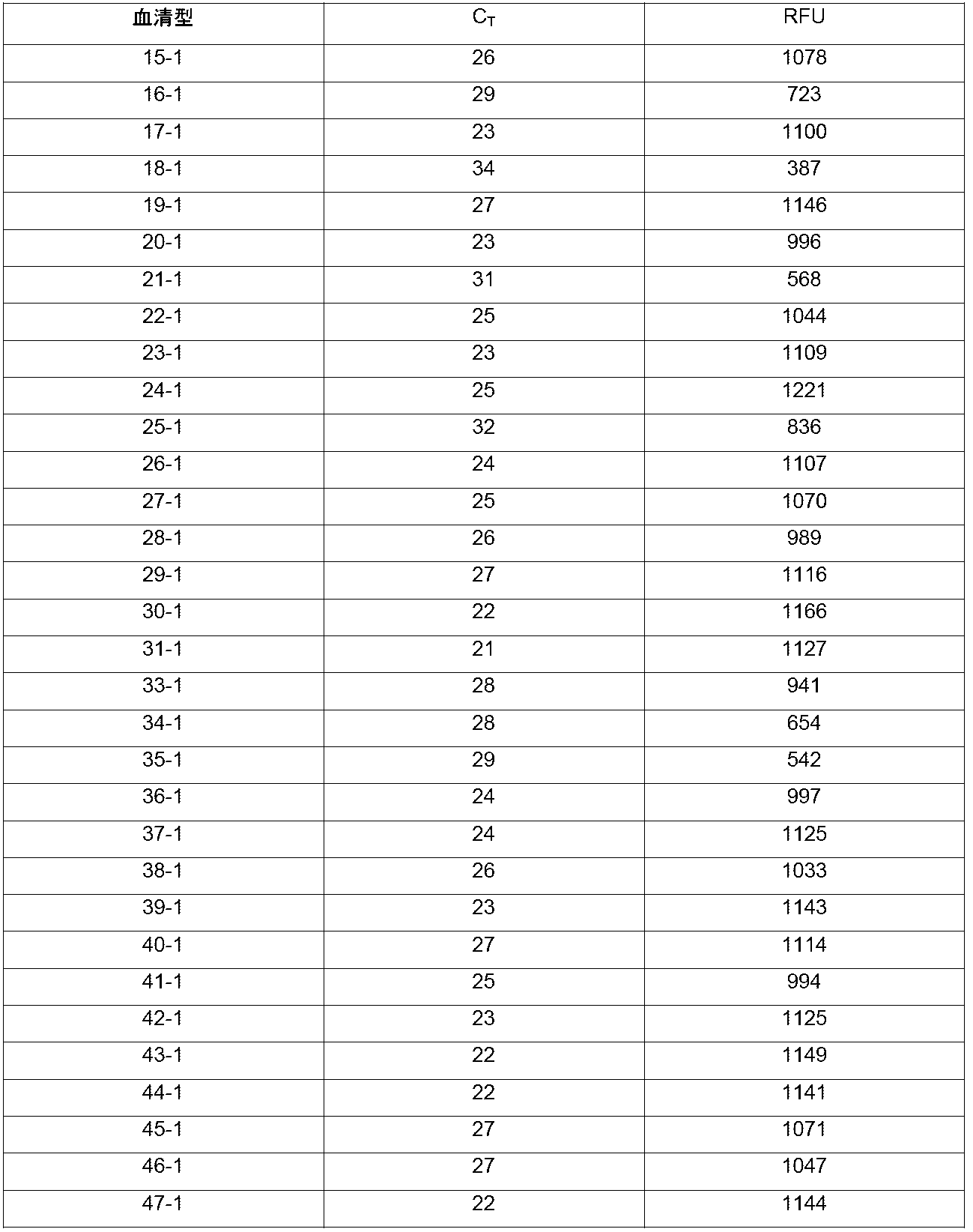
表8a~8c.プライマーおよびプローブの組み合わせを使用した様々なアデノウイル
ス血清型の増幅および検出
結果をCTおよびRFU値として提示する。Famチャネルは、鋳型核酸の検出結果を
示す。Cy5チャネルは、内部対照核酸の検出結果を示す。
表8aのプライマーおよびプローブにより、試験した血清型の全てが首尾よく検出された。表8bおよび8cにより、試験した大部分の血清型が検出された。
材料および方法
次の試薬を使用した:1倍濃度のFast Start Master Buffer(Roche)、3単位のFast Start Taq DNAポリメラーゼ(Roche)、ならびに150nMの順方向増幅プライマー(配列番号25および26)および150nMの逆方向増幅プライマー(配列番号27および配列番号28)を150nMプローブ(配列番号36および配列番号37)とともに使用。総反応量は20マイクロリットルで、アデノウイルス19血清型陽性対照プラスミドから抽出した5マイクロリットルの鋳型核酸を6つの異なる濃度で反応ごとに添加した。使用した増幅サイクルは次のとおりであった:光学系をオフにして95℃で600秒間保持;光学系をオフにして95℃で30秒間および光学系をオンにして55℃で60秒間(5サイクル);光学系をオフにして95℃で10秒間および光学系をオンにして55℃で60秒間(40サイクル)。
これらのプライマーおよびプローブにより、対照試験したアデノウイルス19血清型が首尾よく検出された。
材料および方法
次の試薬を使用した:1倍濃度のFast Start Master Buffer(Roche)、3単位のFast Start Taq DNAポリメラーゼ(Roche)、ならびに150nMの順方向増幅プライマー(配列番号25および26)および150nMの逆方向増幅プライマー(配列番号27および配列番号28)を150nMプローブ(配列番号36および配列番号37)とともに使用。総反応量は、様々なアデノウイルス血清型から抽出した5マイクロリットルの鋳型核酸を伴って20マイクロリットルであり、3×100の濃度で試験した。使用した増幅サイクルは次のとおりであった:光学系をオフにして95℃で600秒間保持;光学系をオフにして95℃で30秒間および光学系をオンにして55℃で60秒間(5サイクル);光学系をオフにして95℃で10秒間および光学系をオンにして55℃で60秒間(40サイクル)。
血清型6を除いて、試験した血清型の全てがこのプライマーおよびプローブ濃度を使用して検出された。この血清型は、3×101 TCID50/mL以上で首尾よく検出された。
材料および方法
分析感度および反応性:アデノウイルス、ヒトメタニューモウイルス、およびライノウイルスの増幅および検出用のプライマーおよびプローブを含有するPCR製剤を、以下を(反応ごとに)含むように調製した:15uLのSupermix(11.1単位Taq)、1.2uLのMMLV逆転写酵素(RT)(24単位)、2.0uLのPrimer
Probe Mix、0.084uLの0.5M EDTA、および1.716uLの水。(AMR製剤。)標的核酸をある数のストック微生物1から抽出し、各微生物について、0.1TCID50/mL、1TCID50/mL、および10TCID50/mLに希釈した。各希釈液からの10uLの標的核酸溶出液を、反応体積のPCR製剤と個別に組み合わせて、30uLの合計反応体積にした。この実験で使用したプライマーおよびプローブは、内部対照を含む配列番号48~49および51~74に示される。この例で使用したプローブは、消光剤およびフルオロフォアを含む二重標識プローブであった。
1標的核酸は、TriCore Reference Laboratories(Albuquerque,NM)、ZeptoMetrix Corporation(Buffalo,NY)、およびATCC(Manassas,VA)から入手した事前に特性評価されたストック微生物から単離した。
この総括で提示した増幅および検出オリゴヌクレオチドの多重化された組み合わせは、10TCID50/mL以下のウイルス濃度を検出することができる。
材料および方法
実施例11で上に列挙したプライマーおよびプローブの全てを含むPCR製剤(AMR製剤)(配列番号74を使用)を使用して、ライノウイルス陽性、hMPV陽性、および/もしくはアデノウイルス陽性、または3つ全てのウイルスについて陰性であると市販のアッセイによって同定された臨床検体を試験した。市販のアッセイには、BioFire
FilmArray RVP Respiratory Panel(BioFire
Diagnostics,Salt Lake City,UT)、GenMark eSensor Respiratory Virus Panel(RVP)(GenMark Diagnostics,Inc.,Carlsbad,CA)、およびLuminex xTAG Respiratory Virus Panel(Luminex Corporation,Austin,TX)が含まれる。全ての試料は、Pa
nther機器を使用して抽出し、PCR循環は、上記の卓上PCR熱循環機器上で実施した。AMRアッセイにより、既に特徴付けた臨床検体から、HRV、hMPV、およびアデノウイルスを検出し、一致は、HRVで94.8%(164/173)、hMPVで97.2%(279/287)、アデノウイルスで93.2%(466/500)であった。AMRアッセイでは、88の臨床検体のうち86が陰性であると同定され、参照アッセイ(Luminex xTAG Respiratory Virus Panel)と97.7%の一致が得られた。加えて、内部対照は、全ての臨床的に陰性の検体に対して有効であった。AMR製剤アッセイを使用して得た2つの「偽陽性」結果は、GenMark eSensor RVPアッセイおよびProdesse ProAdeno+Assay(Hologic,Inc.,San Diego,CA)を使用して真陽性であると判断した。したがって、Luminexアッセイで誤って陰性と同定された臨床検体を除去すると、AMRアッセイによって100%の一致が示された(86/86)。
この実施例で提示した増幅および検出オリゴヌクレオチドの多重化された組み合わせは、臨床検体中のウイルス標的を検出することができ、競合アッセイ(competitor assay)との良好な一致を示す。
材料および方法
実施例11に列挙したプライマーおよびプローブの全てを含むPCR製剤(AMR製剤)(配列番号74を使用して)を、他の微生物との交差反応性について評価した。これらの微生物は、アデノウイルス、hMPV、およびHRVのうちの1つ以上の有無についてクリニックで試験される検体種(鼻咽頭および下気道検体)で一般的に見られるものである。微生物を、プールして試験するか、または個別に試験した(表15のAMRパネル1~26を参照)。各パネルからの3つの反復をPanther機器上で個別に処理し、PCR循環を上記の卓上PCR熱循環機器上で実施した。表15は、AMR製剤(AMR24~26)の標的となるウイルスのみが検出されたことを示す。アッセイ(AMR1~23)で標的とされていない微生物との交差反応性は観察されなかった。
この総括で提示した増幅および検出オリゴヌクレオチドの多重化された組み合わせは、AdV/hMPV/RVアッセイの標的に対する特異性を呈する。
本表16は、本開示で有用な例示的な配列を提供する。この表は開示の範囲を制限するものではない。配列は、世界知的所有権機関(WIPO)のHandbook on Industrial Property Information and Documentation,Standard ST.25(1998)(付録2の表1~6を含む)に準拠して提示する。
配列記号は、World Intellectual Property Organization(WIPO)のHandbook on Industrial Property Information and Documentation,Standard ST.25(1998)(「WIPO ST.25(1998)」)の表1に従う。
請求される開示の範囲内で様々な修正が可能であることが認識される。したがって、本開示は好ましい実施形態および任意選択の特徴によって具体的に開示されてきたものの、本明細書で開示された本開示において具体化された本開示の修正および変形が当業者によって用いられてもよく、またそのような修正および変形は本開示の範囲内であるとみなされることを理解されたい。
Claims (58)
- 少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つの位置を含む、少なくとも50ヌクレオチド長のメタニューモウイルス標的核酸を増幅するように構成され、
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号52、53、56および68を含み、
前記組成物またはキットが、少なくとも1つの検出プローブオリゴマーをさらに含み、前記少なくとも1つの検出プローブオリゴマーが配列番号67、69および70を含む、組成物またはキット。 - 2つ以上の標的核酸に対して構成された少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つの位置を含む、少なくとも50ヌクレオチド長のメタニューモウイルス標的核酸を増幅するように構成され、
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号52、53、56および68を含み、
前記組成物またはキットが、少なくとも1つの検出プローブオリゴマーをさらに含み、前記少なくとも1つの検出プローブオリゴマーが配列番号67、69および70を含む、かつ
(B)第2の標的核酸について、
(i)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つの位置を含む、少なくとも50ヌクレオチド長のアデノウイルス標的核酸を増幅するように構成された、あるいは
(ii)前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つの位置を含む、少なくとも50ヌクレオチド長のライノウイルス標的核酸を増幅するように構成された、組成物またはキット。 - 3つ以上の標的核酸に対して構成された少なくとも第1および第2の増幅オリゴマーを含む組成物またはキットであって、
(A)第1の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号150の966~1147、および/または配列番号159のヌクレオチド844~1027、および/または配列番号150の1000~1040、および/または配列番号159の880~915、および/または配列番号150の1027~1080、および/または配列番号159の913~958、および/または配列番号150の1073~1115、および/または配列番号159の953~995から選択されるヌクレオチド位置の範囲にある少なくとも1つの位置を含む、少なくとも50ヌクレオチド長のメタニューモウイルス標的核酸を増幅するように構成され、
前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号52、53、56および68を含み、
前記組成物またはキットが、少なくとも1つの検出プローブオリゴマーをさらに含み、前記少なくとも1つの検出プローブオリゴマーが配列番号67、69および70を含む、かつ
(B)第2の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号47の52~74および/または76~99および/または40~56および/または65~87および/または1~18および/または7~23および/または28~45および/または27~45および/または26~45および/または139~155および/または103~123および/または159~175および/または83~99および/または83~98から選択されるヌクレオチド位置の範囲にある少なくとも1つの位置を含む、少なくとも50ヌクレオチド長のアデノウイルス標的核酸を増幅するように構成され、かつ
(C)第3の標的核酸について、前記第1の増幅オリゴマーおよび前記第2の増幅オリゴマーが、配列番号120の230~556、および/または配列番号101の199~525、および/または配列番号76の80~410、および/または配列番号120の263~303、および/または配列番号101の231~264、および/または配列番号76の106~156、および/または配列番号120の312~346、および/または配列番号101の279~314、および/または配列番号76の455~506、および/または配列番号120の480~533、および/または配列番号101の455~506、および/または配列番号76の338~397から選択されるヌクレオチド位置の範囲にある少なくとも1つの位置を含む、少なくとも50ヌクレオチド長のライノウイルス標的核酸を増幅するように構成された、組成物またはキット。 - 前記第1の増幅オリゴマーが、少なくとも1つの5-Me-dC、少なくとも1つの非ワトソンクリック塩基、少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、請求項1~3のいずれか一項に記載の組成物またはキット。
- 前記第2の増幅オリゴマーが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含有する核酸配列を含む、請求項1~3または4のいずれかに記載の組成物またはキット。
- 前記メタニューモウイルス標的核酸について、前記第1の増幅オリゴマーが、配列番号52および53を含む、請求項1~3のいずれかに記載の組成物またはキット。
- 前記メタニューモウイルス標的核酸について、前記第2の増幅オリゴマーが、配列番号56および68を含む、請求項1~3のいずれかに記載の組成物またはキット。
- 前記組成物またはキットが、18~36個の核酸塩基長である配列を含むメタニューモウイルス検出プローブオリゴマーをさらに含み、前記18~36個の核酸塩基が、全て配列番号161内または配列番号155内の連続した核酸塩基から選択される、請求項1~3のいずれかに記載の組成物またはキット。
- 前記検出プローブオリゴマーのうちの少なくとも1つが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含む、請求項8に記載の組成物またはキット。
- 前記検出プローブオリゴマーのうちの少なくとも1つが、検出可能な標識を含む、請求項8に記載の組成物またはキット。
- 前記検出可能な標識がフルオロフォアである、請求項10に記載の組成物またはキット。
- 前記検出プローブオリゴマーが二重標識検出プローブオリゴマーである、請求項10または請求項11に記載の組成物またはキット。
- 前記検出プローブオリゴマーが、蛍光検出可能な標識と、前記蛍光検出可能な標識からの蛍光発光を消光することができる消光剤部分とを含む、請求項12に記載の組成物またはキット。
- 前記組成物またはキットが、1つ以上の追加の増幅オリゴマーをさらに含み、前記増幅オリゴマーの各々が、メタニューモウイルス標的核酸を増幅するように構成された、請求項1~3のいずれかに記載の組成物またはキット。
- 前記1つ以上の追加の増幅オリゴマーの各々が、配列番号151、152、153、154、158、160、177、178からなる群から別々に選択される標的ハイブリダイズ配列を含む、請求項14に記載の組成物またはキット。
- 前記組成物またはキットが、標的ハイブリダイズ配列と固定化プローブ結合領域とを含む核酸標的捕捉プローブをさらに含む、請求項1~3のいずれかに記載の組成物またはキット。
- 前記標的ハイブリダイズ配列がポリKヌクレオチド配列である、請求項16に記載の組成物またはキット。
- 前記ポリKヌクレオチド配列がランダムなポリGU配列である、請求項17に記載の組成物またはキット。
- 前記固定化プローブ結合領域が、ホモポリマーヌクレオチド配列である、請求項16、17、または18に記載の組成物またはキット。
- 前記固定化プローブ結合領域が、T0-4A10-36からなる群から選択されるヌクレオチド配列を含む、請求項19に記載の組成物またはキット。
- 前記組成物が、酵素、緩衝液、dNTP、またはそれらの組み合わせをさらに含む、請求項1~3のいずれかに記載の組成物またはキット。
- 試料中のメタニューモウイルス標的核酸、ライノウイルス標的核酸、アデノウイルス標的核酸、またはそれらの組み合わせの有無を決定するための方法であって、
(A)試料を請求項1~21のいずれか一項に記載の組成物またはキットに含まれる増幅オリゴマーの組み合わせと接触させるステップと、
(B)試料中のアデノウイルス標的核酸、メタニューモウイルス標的核酸、またはライノウイルス標的核酸のうちのいずれかが、その標的核酸を増幅して増幅産物を生成するように構成された増幅オリゴマーの組み合わせによって使用される、インビトロ核酸増幅反応を実行するステップと、
(C)前記増幅産物を検出するステップと、を含み、
それにより、前記試料中の前記標的核酸の有無を決定する、方法。 - 前記試料がヒトに由来する試料である、請求項22に記載の方法。
- 前記試料が粘膜試料である、請求項23に記載の方法。
- 前記試料が、鼻咽頭スワブを使用して得られる、請求項23または請求項24に記載の方法。
- ステップ(A)の前に、試料調製ステップを実行して、前記試料中のあらゆる標的核酸を他の試料成分から分離させる、請求項22に記載の方法。
- 前記試料調製ステップが標的捕捉ステップを含む、請求項26に記載の方法。
- 前記標的捕捉ステップが、前記試料を、標的ハイブリダイズ配列および固定化プローブ結合領域を含む核酸標的捕捉プローブと接触させることを含む、請求項27に記載の方法。
- 前記標的ハイブリダイズ配列がポリKヌクレオチド配列である、請求項28に記載の方法。
- 前記ポリKヌクレオチド配列がランダムなポリGU配列である、請求項29に記載の方法。
- 固定化プローブ結合領域が、ホモポリマーヌクレオチド配列である、請求項28、29、または30に記載の方法。
- 前記固定化プローブ結合領域が、T0-4A10-36からなる群から選択されるヌクレオチド配列を含む、請求項31に記載の方法。
- 前記検出ステップ(C)が、1つ以上の検出プローブオリゴマーを使用して実行される、請求項22に記載の方法。
- 前記1つ以上の検出プローブオリゴマーが、配列番号48、49、54、63、64、67、69および70を含む、請求項33に記載の方法。
- 前記1つ以上の検出プローブオリゴマーがさらに、配列番号4、10、17、18、19、20、21、22、23、24、29、30、36、37、39、40、139、140、155、156、157、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、87~94、109~114、および131~136からなる群から選択される、請求項33に記載の方法。
- 前記検出プローブオリゴマーのうちの少なくとも1つが、少なくとも1つの5-Me-dC、または少なくとも1つの非ワトソンクリック塩基、または少なくとも1つの縮重塩基、またはそれらの組み合わせを含む、請求項33、34または35に記載の方法。
- 前記検出プローブオリゴマーのうちの少なくとも1つが、検出可能な標識を含む、請求項33、34、35または36に記載の方法。
- 前記検出可能な標識がフルオロフォアである、請求項37に記載の方法。
- 前記検出プローブオリゴマーが二重標識検出プローブオリゴマーである、請求項37または請求項38に記載の方法。
- 前記検出プローブオリゴマーが、蛍光検出可能な標識と、前記蛍光検出可能な標識からの蛍光発光を消光することができる消光剤部分とを含む、請求項39に記載の方法。
- 前記インビトロ核酸増幅反応が熱循環を含む、請求項22に記載の方法。
- 前記インビトロ核酸増幅反応が、5’から3’へのエキソヌクレアーゼ活性を有するポリメラーゼ酵素によるPCRを含む、請求項22に記載の方法。
- 前記インビトロ核酸増幅反応が、5’から3’へのエキソヌクレアーゼ活性を有する酵素を使用して実行される、請求項22に記載の方法。
- 前記インビトロ核酸増幅反応が、5’から3’へのエキソヌクレアーゼ活性を有する酵素を使用して実行され、増幅産物が、所定の閾値を超える蛍光値を決定することによって検出される、請求項22に記載の方法。
- 試料中のメタニューモウイルス標的核酸、ライノウイルス標的核酸、アデノウイルス標的核酸、またはそれらの組み合わせのインビトロ検出のための方法であって、前記方法が、アデノウイルス標的核酸、メタニューモウイルス標的核酸、および/またはライノウイルス標的核酸を、請求項8~13のいずれかに記載の組成物またはキットに含まれる検出プローブオリゴマーと接触させることを含み、前記検出プローブオリゴマーと、前記検出プローブオリゴマーがハイブリダイズするように構成された前記標的核酸とのハイブリダイゼーションが、その標的核酸の存在を示す、方法。
- 前記方法が、前記メタニューモウイルス標的核酸、前記アデノウイルス標的核酸、および/または前記ライノウイルス標的核酸からの増幅産物を、前記検出プローブオリゴマーと接触させることを含み、前記検出プローブオリゴマーと、前記検出プローブオリゴマーがハイブリダイズするように構成された前記増幅産物とのハイブリダイゼーションが、前記増幅産物の生成元であるその標的核酸の存在を示す、請求項45に記載の方法。
- 前記増幅産物が、5’から3’へのエキソヌクレアーゼ活性を有する酵素を使用して生成された、請求項46に記載の方法。
- 前記標的核酸またはそれから生成された前記増幅産物が、所定の閾値を超える蛍光値を決定することによって検出される、請求項47に記載の方法。
- 請求項1~21のいずれか一項に記載の組成物またはキットに含まれる増幅オリゴマーのうちの2つ以上を含む、メタニューモウイルス標的核酸、ライノウイルス標的核酸、アデノウイルス標的核酸、またはそれらの組み合わせの増幅のための乾燥組成物であって、前記2つ以上の増幅オリゴマーが、少なくとも配列番号52、53、56および68を含み、前記乾燥組成物は、少なくとも1つの検出プローブオリゴマーと組み合わせて使用され、前記少なくとも1つの検出プローブオリゴマーが、配列番号67、69および70を含む、乾燥組成物。
- 請求項8~13のいずれかに記載の組成物またはキットに含まれる検出プローブオリゴマーのうちの1つ以上を含む、メタニューモウイルス標的核酸、ライノウイルス標的核酸、アデノウイルス標的核酸、またはそれらの組み合わせの有無を判定するための乾燥組成物であって、前記検出プローブオリゴマーのうちの1つ以上が、配列番号67、69および70を含み、前記乾燥組成物は、配列番号52、53、56および68を含む2つ以上の増幅オリゴマーと組み合わせて使用される、乾燥組成物。
- 請求項1~21のいずれか一項に記載の組成物またはキットに含まれる2つ以上の増幅オリゴマーの組み合わせ、および/または、配列番号4、10、17、18、19、20、21、22、23、24、29、30、36、37、39、40、48、49、54、63、64、67、69、70、139、140、155、156、157、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、87~94、109~114、および131~136からなる群より選択される検出プローブオリゴマーを含む、メタニューモウイルス標的核酸、ライノウイルス標的核酸、アデノウイルス標的核酸、またはそれらの組み合わせの有無を判定するための乾燥組成物であって、前記2つ以上の増幅オリゴマーが、配列番号52、53、56および68を含み、前記検出プローブオリゴマーが、配列番号67、69および70を含む、乾燥組成物。
- 前記乾燥組成物が、酵素、dNTP、またはその両方をさらに含む、請求項51に記載の乾燥組成物。
- 前記酵素が、5’から3’へのエキソヌクレアーゼ活性を有する、請求項52に記載の乾燥組成物。
- 前記酵素がポリメラーゼ酵素である、請求項52または請求項53に記載の乾燥組成物。
- 前記乾燥組成物が、10mM以下の無機塩濃度を有する、請求項51に記載の乾燥組成物。
- 前記乾燥組成物が、7mM以下の無機塩濃度を有する、請求項51に記載の乾燥組成物。
- 前記乾燥組成物が、5mM以下の無機塩濃度を有する、請求項51に記載の乾燥組成物。
- 前記乾燥組成物が、0.5mM~10mMの無機塩濃度を有する、請求項51に記載の乾燥組成物。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022086064A JP2022105717A (ja) | 2017-03-25 | 2022-05-26 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
| JP2023187681A JP2023181438A (ja) | 2017-03-25 | 2023-11-01 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762476753P | 2017-03-25 | 2017-03-25 | |
| US62/476,753 | 2017-03-25 | ||
| JP2019552512A JP6956800B2 (ja) | 2017-03-25 | 2018-03-23 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019552512A Division JP6956800B2 (ja) | 2017-03-25 | 2018-03-23 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022086064A Division JP2022105717A (ja) | 2017-03-25 | 2022-05-26 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020074774A JP2020074774A (ja) | 2020-05-21 |
| JP7370832B2 true JP7370832B2 (ja) | 2023-10-30 |
Family
ID=61966083
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019552512A Active JP6956800B2 (ja) | 2017-03-25 | 2018-03-23 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
| JP2019216301A Active JP7370832B2 (ja) | 2017-03-25 | 2019-11-29 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
| JP2022086064A Pending JP2022105717A (ja) | 2017-03-25 | 2022-05-26 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
| JP2023187681A Pending JP2023181438A (ja) | 2017-03-25 | 2023-11-01 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019552512A Active JP6956800B2 (ja) | 2017-03-25 | 2018-03-23 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022086064A Pending JP2022105717A (ja) | 2017-03-25 | 2022-05-26 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
| JP2023187681A Pending JP2023181438A (ja) | 2017-03-25 | 2023-11-01 | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット |
Country Status (6)
| Country | Link |
|---|---|
| US (5) | US11384387B2 (ja) |
| EP (3) | EP3601618A1 (ja) |
| JP (4) | JP6956800B2 (ja) |
| AU (2) | AU2018244190C1 (ja) |
| CA (5) | CA3056135C (ja) |
| WO (1) | WO2018183124A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3056135C (en) | 2017-03-25 | 2024-02-20 | Gen-Probe Incorporated | Compositions, methods and kits to detect adenovirus nucleic acids |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130089859A1 (en) | 2011-10-05 | 2013-04-11 | GEN-PROBE PRODESSE, INC., c/o GEN-PROBE INCORPORATED | Compositions, methods and kits to detect adenovirus nucleic acids |
Family Cites Families (45)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2422956A1 (fr) | 1978-04-13 | 1979-11-09 | Pasteur Institut | Procede de detection et de caracterisation d'un acide nucleique ou d'une sequence de celui-ci, et reactif enzymatique pour la mise en oeuvre de ce procede |
| US4786600A (en) | 1984-05-25 | 1988-11-22 | The Trustees Of Columbia University In The City Of New York | Autocatalytic replication of recombinant RNA |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| US4683195A (en) | 1986-01-30 | 1987-07-28 | Cetus Corporation | Process for amplifying, detecting, and/or-cloning nucleic acid sequences |
| US4800159A (en) | 1986-02-07 | 1989-01-24 | Cetus Corporation | Process for amplifying, detecting, and/or cloning nucleic acid sequences |
| US5541308A (en) | 1986-11-24 | 1996-07-30 | Gen-Probe Incorporated | Nucleic acid probes for detection and/or quantitation of non-viral organisms |
| US5639604A (en) | 1987-09-21 | 1997-06-17 | Gen-Probe Incorporated | Homogeneous protection assay |
| US5585481A (en) | 1987-09-21 | 1996-12-17 | Gen-Probe Incorporated | Linking reagents for nucleotide probes |
| US5283174A (en) | 1987-09-21 | 1994-02-01 | Gen-Probe, Incorporated | Homogenous protection assay |
| KR960002561B1 (ko) | 1987-09-21 | 1996-02-22 | 젠-프로우브 인코퍼레이티드 | 균질보호분석법 |
| US5118801A (en) | 1988-09-30 | 1992-06-02 | The Public Health Research Institute | Nucleic acid process containing improved molecular switch |
| US5656207A (en) | 1989-06-24 | 1997-08-12 | Gen Probe Incorporated | Detecting or quantifying multiple analytes using labelling techniques |
| US5516663A (en) | 1990-01-26 | 1996-05-14 | Abbott Laboratories | Ligase chain reaction with endonuclease IV correction and contamination control |
| US5427930A (en) | 1990-01-26 | 1995-06-27 | Abbott Laboratories | Amplification of target nucleic acids using gap filling ligase chain reaction |
| US5378825A (en) | 1990-07-27 | 1995-01-03 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs |
| US5849481A (en) | 1990-07-27 | 1998-12-15 | Chiron Corporation | Nucleic acid hybridization assays employing large comb-type branched polynucleotides |
| CA2126691C (en) | 1991-12-24 | 2003-05-06 | Phillip Dan Cook | Gapped 2' modified oligonucleotides |
| US5424413A (en) | 1992-01-22 | 1995-06-13 | Gen-Probe Incorporated | Branched nucleic acid probes |
| US5422252A (en) | 1993-06-04 | 1995-06-06 | Becton, Dickinson And Company | Simultaneous amplification of multiple targets |
| US5925517A (en) | 1993-11-12 | 1999-07-20 | The Public Health Research Institute Of The City Of New York, Inc. | Detectably labeled dual conformation oligonucleotide probes, assays and kits |
| US5648211A (en) | 1994-04-18 | 1997-07-15 | Becton, Dickinson And Company | Strand displacement amplification using thermophilic enzymes |
| US5547861A (en) | 1994-04-18 | 1996-08-20 | Becton, Dickinson And Company | Detection of nucleic acid amplification |
| AU2522095A (en) | 1994-05-19 | 1995-12-18 | Dako A/S | Pna probes for detection of neisseria gonorrhoeae and chlamydia trachomatis |
| DE69535240T2 (de) | 1994-10-28 | 2007-06-06 | Gen-Probe Inc., San Diego | Zusammensetzungen und Verfahren für die gleichzeitige Detektion und Quantifizierung von einer Mehrheit spezifischer Nuklein Säure Sequenzen |
| US5731148A (en) | 1995-06-07 | 1998-03-24 | Gen-Probe Incorporated | Adduct protection assay |
| DE69738687D1 (de) | 1996-04-12 | 2008-06-26 | Phri Properties Inc | Sonden, kits und assays |
| ES2271994T3 (es) | 1997-05-02 | 2007-04-16 | Gen-Probe Incorporated | Hibridacion en dos pasos y captura de un polinucleotido. |
| US6180340B1 (en) | 1997-10-31 | 2001-01-30 | Gen-Probe Incorporated | Extended dynamic range assays |
| US6949367B1 (en) | 1998-04-03 | 2005-09-27 | Epoch Pharmaceuticals, Inc. | Modified oligonucleotides for mismatch discrimination |
| ATE440963T1 (de) | 1998-07-02 | 2009-09-15 | Gen Probe Inc | Molekulare fackeln |
| IL152420A0 (en) * | 2001-02-23 | 2003-05-29 | Novartis Ag | Novel oncolytic adenoviral vectors |
| EP1563088A1 (de) * | 2002-11-14 | 2005-08-17 | Medizinische Hochschule Hannover | Mittel und verfahren zum nachweis humaner adenoviren |
| US20060240412A1 (en) * | 2003-09-11 | 2006-10-26 | Hall Thomas A | Compositions for use in identification of adenoviruses |
| JP5020818B2 (ja) | 2004-07-01 | 2012-09-05 | ジェン−プローブ・インコーポレーテッド | 生物学的試料中の核酸を検出するための方法及び組成物 |
| US8318423B2 (en) * | 2004-07-06 | 2012-11-27 | Focus Diagnostics, Inc. | Methods and compositions for detecting rhinoviruses |
| JP2008531052A (ja) | 2005-02-28 | 2008-08-14 | ジェン−プローブ・インコーポレーテッド | 核酸ハイブリダイゼーションスイッチプローブを用いて被分析体を検出するための組成物及び方法 |
| WO2007130519A2 (en) * | 2006-05-02 | 2007-11-15 | Government Of The Usa, As Represented By The Secretary, Department Of Health And Human Services | Viral nucleic acid microarray and method of use |
| JP5635772B2 (ja) | 2006-08-01 | 2014-12-03 | ジェン−プロウブ インコーポレイテッド | 核酸の非特異的標的の捕捉方法 |
| US20090105092A1 (en) | 2006-11-28 | 2009-04-23 | The Trustees Of Columbia University In The City Of New York | Viral database methods |
| US20100086908A1 (en) * | 2007-05-17 | 2010-04-08 | Prudent James R | Methods for the detection of respiratory viruses |
| CA2782082A1 (en) | 2009-12-23 | 2011-06-30 | The Henry M. Jackson Foundation For The Advancement Of Military Medicine , Inc. | Methods and kits for identyfing human adenovirus serotypes |
| US9487838B2 (en) | 2010-12-28 | 2016-11-08 | Qiagen Hamburg Gmbh | Oligonucleotide probe for the detection of adenovirus |
| KR101749587B1 (ko) * | 2016-06-07 | 2017-06-21 | 주식회사 제넷바이오 | 측면 흐름 분석 시스템을 이용한 병원성 미생물 유전자 검출용 시약 및 이를 포함하는 검출용 키트 |
| CN106222304A (zh) * | 2016-08-16 | 2016-12-14 | 无锡市疾病预防控制中心 | 一种同时检测五种呼吸道病毒的rt‑pcr方法所用的五对上下游引物 |
| CA3056135C (en) | 2017-03-25 | 2024-02-20 | Gen-Probe Incorporated | Compositions, methods and kits to detect adenovirus nucleic acids |
-
2018
- 2018-03-23 CA CA3056135A patent/CA3056135C/en active Active
- 2018-03-23 CA CA3225593A patent/CA3225593A1/en active Pending
- 2018-03-23 EP EP18717485.9A patent/EP3601618A1/en active Pending
- 2018-03-23 AU AU2018244190A patent/AU2018244190C1/en active Active
- 2018-03-23 JP JP2019552512A patent/JP6956800B2/ja active Active
- 2018-03-23 WO PCT/US2018/024141 patent/WO2018183124A1/en unknown
- 2018-03-23 CA CA3225861A patent/CA3225861A1/en active Pending
- 2018-03-23 CA CA3225653A patent/CA3225653A1/en active Pending
- 2018-03-23 US US16/497,229 patent/US11384387B2/en active Active
- 2018-03-23 CA CA3225845A patent/CA3225845A1/en active Pending
- 2018-03-23 EP EP23156456.8A patent/EP4219769A3/en active Pending
- 2018-03-23 EP EP23156298.4A patent/EP4219768A3/en active Pending
-
2019
- 2019-11-29 JP JP2019216301A patent/JP7370832B2/ja active Active
-
2022
- 2022-05-17 AU AU2022203311A patent/AU2022203311A1/en active Pending
- 2022-05-26 JP JP2022086064A patent/JP2022105717A/ja active Pending
- 2022-06-07 US US17/834,578 patent/US20220372563A1/en active Pending
- 2022-08-17 US US17/820,256 patent/US20230087588A1/en active Pending
- 2022-12-27 US US18/146,508 patent/US20230203571A1/en active Pending
- 2022-12-27 US US18/146,589 patent/US20230203572A1/en active Pending
-
2023
- 2023-11-01 JP JP2023187681A patent/JP2023181438A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130089859A1 (en) | 2011-10-05 | 2013-04-11 | GEN-PROBE PRODESSE, INC., c/o GEN-PROBE INCORPORATED | Compositions, methods and kits to detect adenovirus nucleic acids |
Non-Patent Citations (1)
| Title |
|---|
| JOURNAL OF CLINICAL MICROBIOLOGY,2004年,Vol.42, No.3,pp.981-986 |
Also Published As
| Publication number | Publication date |
|---|---|
| US11384387B2 (en) | 2022-07-12 |
| CA3225861A1 (en) | 2018-10-04 |
| AU2018244190C1 (en) | 2022-09-15 |
| CA3056135A1 (en) | 2018-10-04 |
| EP4219768A2 (en) | 2023-08-02 |
| CA3225845A1 (en) | 2018-10-04 |
| AU2018244190B2 (en) | 2022-03-17 |
| CA3225653A1 (en) | 2018-10-04 |
| CA3056135C (en) | 2024-02-20 |
| US20220372563A1 (en) | 2022-11-24 |
| AU2022203311A1 (en) | 2022-06-02 |
| EP3601618A1 (en) | 2020-02-05 |
| JP2020074774A (ja) | 2020-05-21 |
| US20230203571A1 (en) | 2023-06-29 |
| AU2018244190A1 (en) | 2019-11-14 |
| US20200263242A1 (en) | 2020-08-20 |
| WO2018183124A1 (en) | 2018-10-04 |
| JP2023181438A (ja) | 2023-12-21 |
| JP6956800B2 (ja) | 2021-11-02 |
| JP2020511972A (ja) | 2020-04-23 |
| EP4219768A3 (en) | 2023-10-11 |
| US20230087588A1 (en) | 2023-03-23 |
| EP4219769A3 (en) | 2023-10-11 |
| JP2022105717A (ja) | 2022-07-14 |
| US20230203572A1 (en) | 2023-06-29 |
| CA3225593A1 (en) | 2018-10-04 |
| EP4219769A2 (en) | 2023-08-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2023181438A (ja) | アデノウイルス、メタニューモウイルス、および/またはライノウイルス核酸を検出するための組成物、方法、およびキット | |
| JP2024032995A (ja) | 水痘帯状疱疹ウイルスを増幅または検出するための組成物および方法 | |
| US10047406B2 (en) | Compositions and methods for detecting HEV nucleic acid | |
| US20230082096A1 (en) | Compositions and methods for detecting coronavirus nucleic acid | |
| EP3830302B1 (en) | Compositions and methods for detecting nucleic acids of epstein-barr virus | |
| EP3601617B3 (en) | Compositions and methods for detecting or quantifying parainfluenza virus |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210322 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220202 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220426 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220526 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220825 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221108 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230202 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230404 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230608 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230803 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230921 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20231018 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7370832 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |