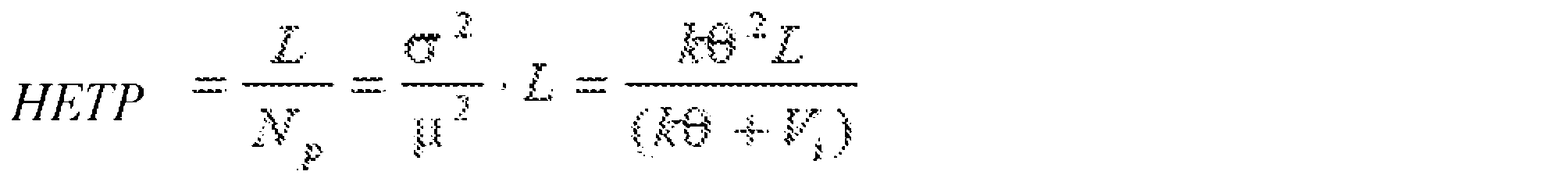JP7344902B2 - 抗tnf抗体組成物を産生するための製造方法におけるクロマトグラフィカラムの品質評価 - Google Patents
抗tnf抗体組成物を産生するための製造方法におけるクロマトグラフィカラムの品質評価 Download PDFInfo
- Publication number
- JP7344902B2 JP7344902B2 JP2020557253A JP2020557253A JP7344902B2 JP 7344902 B2 JP7344902 B2 JP 7344902B2 JP 2020557253 A JP2020557253 A JP 2020557253A JP 2020557253 A JP2020557253 A JP 2020557253A JP 7344902 B2 JP7344902 B2 JP 7344902B2
- Authority
- JP
- Japan
- Prior art keywords
- column
- chromatography column
- hetp
- mobile phase
- packing
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/86—Signal analysis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39591—Stabilisation, fragmentation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/10—Selective adsorption, e.g. chromatography characterised by constructional or operational features
- B01D15/16—Selective adsorption, e.g. chromatography characterised by constructional or operational features relating to the conditioning of the fluid carrier
- B01D15/166—Fluid composition conditioning, e.g. gradient
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/10—Selective adsorption, e.g. chromatography characterised by constructional or operational features
- B01D15/20—Selective adsorption, e.g. chromatography characterised by constructional or operational features relating to the conditioning of the sorbent material
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/10—Selective adsorption, e.g. chromatography characterised by constructional or operational features
- B01D15/20—Selective adsorption, e.g. chromatography characterised by constructional or operational features relating to the conditioning of the sorbent material
- B01D15/206—Packing or coating
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction, e.g. ion-exchange, ion-pair, ion-suppression or ion-exclusion
- B01D15/361—Ion-exchange
- B01D15/362—Cation-exchange
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction, e.g. ion-exchange, ion-pair, ion-suppression or ion-exclusion
- B01D15/361—Ion-exchange
- B01D15/363—Anion-exchange
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/38—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving specific interaction not covered by one or more of groups B01D15/265 and B01D15/30 - B01D15/36, e.g. affinity, ligand exchange or chiral chromatography
- B01D15/3804—Affinity chromatography
- B01D15/3809—Affinity chromatography of the antigen-antibody type, e.g. protein A, G or L chromatography
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/16—Extraction; Separation; Purification by chromatography
- C07K1/18—Ion-exchange chromatography
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/16—Extraction; Separation; Purification by chromatography
- C07K1/22—Affinity chromatography or related techniques based upon selective absorption processes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/06—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies from serum
- C07K16/065—Purification, fragmentation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/241—Tumor Necrosis Factors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/50—Conditioning of the sorbent material or stationary liquid
- G01N30/56—Packing methods or coating methods
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/86—Signal analysis
- G01N30/8665—Signal analysis for calibrating the measuring apparatus
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/89—Inverse chromatography
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/00584—Control arrangements for automatic analysers
- G01N35/00594—Quality control, including calibration or testing of components of the analyser
- G01N35/00613—Quality control
- G01N35/00623—Quality control of instruments
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/50—Conditioning of the sorbent material or stationary liquid
- G01N30/56—Packing methods or coating methods
- G01N2030/562—Packing methods or coating methods packing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
- G01N2030/8809—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample
- G01N2030/8813—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample biological materials
- G01N2030/8831—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample biological materials involving peptides or proteins
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
- G01N2030/889—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 monitoring the quality of the stationary phase; column performance
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Analytical Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Molecular Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Engineering & Computer Science (AREA)
- Quality & Reliability (AREA)
- Epidemiology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Treatment Of Liquids With Adsorbents In General (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Description
本願は、2018年4月20日に出願された米国特許仮出願第62/660,340号に対する優先権を主張するものであり、特許仮出願は参照によりその全体が本明細書に組み込まれる。
本発明は、抗TNF抗体、例えば抗TNFα抗体SIMPONI(登録商標)(ゴリムマブ)、及び当該抗体に関する特定の医薬組成物を産生するための製造方法におけるクロマトグラフィカラムの品質評価方法に関する。
本出願は、2019年4月12日付で作成された「JBI6083USNP1 Sequences」というファイル名のASCII形式の配列表としてEFS-Webを介して電子的に提出され、7kbのサイズを有する配列表を含む。EFS-Webを介して提出された配列表は、本明細書の一部であり、参照によりその全体が本明細書に組み込まれる。
カラム充填を含むクロマトグラフィカラムの初回の操作中に、少なくとも1つの移動相のトランジションフロントについて、2つ以上の間隔で、カラム出口信号及び累積流量パラメータを収集する工程と、
上昇するトランジションフロントについては式Iaを用い、又は下降するトランジションフロントについては式Ibを用い、少なくとも1つの移動相のトランジションフロントに関し収集したカラム出口信号と累積流量パラメータとに基づいて、ガンマモデルの累積分布曲線を決定する工程であって、式Ia又は式Ibは、
式IIと、ガンマモデルの累積分布曲線のパラメータk、θ、及びViとを用い、少なくとも1つの移動相のトランジションフロントについての理論段相当高さ(HETP)値を計算する工程であって、式IIは、
クロマトグラフィカラム充填について1回又は複数回の後の使用の各回の間に、収集されたカラム出口信号及び累積流量パラメータを用い、当該決定及び当該計算を実行する工程と、
当該実行する工程に基づき、当該1回又は複数回の後の使用の各回の間に、クロマトグラフィカラム充填のHETP値を決定する工程と、
2回以上の後の使用に関し、クロマトグラフィカラム充填について決定されたHETP値の傾向を蓄積する工程と、
当該蓄積した傾向に基づき、当該クロマトグラフィカラム充填の質における変化を検出する工程と、を更に含み、当該クロマトグラフィカラムのコンディショニング、交換又は再充填が、当該評価に基づくものである、方法を提供する。
2つ以上の異なる移動相トランジションフロントのそれぞれについてHETP値を計算するために、2つ以上の異なる移動相トランジションフロントのそれぞれについて別個に収集されたカラム出口信号及び累積流量パラメータを用い、当該決定する工程及び計算する工程を実行する工程と、
2つ又はそれ以上のHETP計算値に基づき、クロマトグラフィカラム充填の質を評価する工程と、を含み、クロマトグラフィカラムの当該コンディショニング、交換又は再充填は、当該評価に基づくものである。
HETP=L/Np
C=f(V,k,θ,Vi)式I
平均、μ=kθ+Vi
分散、σ2=kθ2
段数、Np=μ2/σ2
概論:
治療用抗体レミケード(登録商標)(インフリキシマブ)の製造プロセスは、複数の段階を含み、そのうちの4段階はクロマトグラフィによる精製を含む。カラムの品質評価のためのガンマ分布の推移分析(GDTA)を、これらのカラム工程のそれぞれの間の2つ又は3つの推移に適用した。本実施例は、レミケード(登録商標)(インフリキシマブ)の製造中に使用されるプロテインAカラム精製工程へのGDTA法の適用を記載する。精製プロセスは、本明細書に記載されるように、GDTAに適した2つのトランジションフロント、すなわち、平衡化フロント及び中間洗浄フロントを含む。
プロテインAカラム精製中、すなわち、洗浄及び平衡化中の各トランジションフロントについて、導電率及び累積流量を記録した。カラムがインラインに置かれた時点を特定するために、プレカラム導電率及び圧力の傾向を評価することによって、開始点の決定を行った。フロントの持続時間について、スプレッドシートを作成し、計算された10秒の間隔を使用して、サーバから流量及び導電率のデータを取得するように設定した。
正規性
平衡化フロント及び洗浄フロントの両方についてのHETP及びSSの結果を、確率プロットを作成することによって正規性について評価した。確率プロット(図3~図12)では、データ点(HETP又はSSの結果)は、試料で観察された実際の累積分布を表している。線は、試料から推定されるパラメータを使用した正規分布に基づいて、あてはめられた累積分布並びに信頼区間の上限値及び下限値を表している。パーセンタイルスケールを変換することにより、あてはめられた分布が直線を形成する。HETP及びSSのデータセットは、それぞれ下端が0に固定されているが、正規分布モデルは負の値を示唆している。得られた確率プロットは、曲線形状を示す。図3~図6を参照されたい。したがって、結果は、自然対数変換を用いて良好にあてはめられる。自然対数変換データの確率プロットについては、図7~図10を参照されたい。
外れ値を特定し、結果の変動性を評価するために、各パラメータについての管理図を作成した。図13~図22を参照されたい。管理図は、HETP及びSSの変換されたデータを使用し、自然対数変換が適用された。データはまた、これらのパラメータのそれぞれについて、変換された上方管理限界を有する時系列プロットでプロットされる。
データセットの平均流量及びプレカラム圧力を評価して、任意の外れ値を特定した。特定された差違と結果との間の関係を評価した。
HETP:
HETPは、カラム性能に直接関連するものであり、分散を増加させる可能性があるシステム内の他の要因によっても影響を受ける。結果は、0超でなければならない。HETPの管理限界は、平衡化について図13及び洗浄フロントについて図18に示すように、自然対数のBox-Cox変換(λ=0)を用いることによって最適に決定される。管理図は、平均+/-3の標準偏差を用いMinitabにより計算され変換されたデータの管理限界を示す(以下の表2も参照されたい)。標準偏差は、平均移動範囲に基づいて決定される。カラム寿命の間のカラム性能の変動を考慮するために、100の移動範囲を選択した。上方及び下方管理限界を逆変換(ex)して、変換されていないデータの管理限界を決定する。
SSは、ガンマモデルの分布がどのくらい良好にデータにあてはめられるかを示す尺度である。この尺度を使用して、GDTA法で計算されたHETP値がプロセスデータを表すことを確認する。下限は存在せず、結果は0超でなければならない。SSの上方管理限界は、平衡化フロントについて図15及び洗浄フロントについて図20に示すように、自然対数のBox-Cox変換(λ=0)を用いることによって最適に決定される。管理図は、平均+/-3の標準偏差を用いMinitabにより計算され変換されたデータの管理限界を示す。標準偏差は、平均移動範囲に基づいて決定される。カラム寿命の間のカラム性能の変動を考慮するために、100の移動範囲を選択した。管理図は、平衡化フロント及び洗浄フロントについてそれぞれ0.050及び0.989を与えるように逆変換した、変換されたデータの上方管理限界を示している(表2を参照されたい)。各フロントのSS結果及び管理限界の時系列プロットを図16及び図20に示す。限界内にある結果は、モデルがデータ及び過去の結果にあてはめられることを保証する。結果がこの範囲外である場合、特別な原因が考えられる。
平均値を、ガンマモデルの分布の精度についての第2の尺度として加えた。平均値は、フロントの理論的な質量中心を表し、システム内で当該値をシフトさせる、大過剰のカラム体積や移動相と樹脂との間の相互作用などといった他の要因がない限り、常に1カラム体積に近い値であるべきである。平衡化フロント及び洗浄フロントの両方の平均値はほぼ正規分布しており、変換を必要としない。図11及び図12を参照されたい。平衡化フロントの平均は1.07CV付近に密に分布しており、いくつかの外れ値がいずれかの側に存在し、高い側では1.2に接近している。図17を参照されたい。洗浄フロントは、わずかに多くの変動を示し、かつ0.99CVを中心としており、0.8付近に低い外れ値がいくつか存在する。図22を参照されたい。両フロントの平均については、0.80~1.20CVの管理限界を適用することが推奨される(表2を参照されたい)。平均値はカラム性能の尺度ではなく、分析が適切であったかを確認するためのチェックとして用いられるものであることから、これは適切である。より厳しい管理限界は、このチェックの感度としては必要とされていない。
治療抗体レミケード(登録商標)(インフリキシマブ)の製造プロセスは複数の段階を含み、そのうちの4段階はクロマトグラフィ精製を含む。カラムの品質評価のためのガンマ分布の推移分析(GDTA)を、これらのカラム工程のそれぞれの間の2つ又は3つの推移に適用した。本実施例は、レミケード(登録商標)(インフリキシマブ)の製造に使用されるプロテインAカラム精製工程へのGDTA法の適用を記載する。精製プロセスは、本明細書に記載されるように、GDTAに適した2つのトランジションフロント、すなわち、平衡化フロント及び中間洗浄フロントを含む。
概論:
上述のように、レミケード(登録商標)(インフリキシマブ)の製造プロセスは、複数の段階を含み、そのうちの4段階はクロマトグラフィ精製を含む。本実施例は、レミケード(登録商標)(インフリキシマブ)の製造に使用されるSP-セファロース高性能(SPHP)カラム精製工程にGDTA法を適用することを記載する。SPHPカラムは陽イオン交換クロマトグラフィカラムである。精製プロセスは、本明細書に記載されるように、GDTAに適した3つのトランジションフロント、すなわち、平衡化フロント、WFIフラッシュフロント、及びストレージフロントを含む。
HETP:
HETPは、カラム性能に直接関連するものであり、分散を増加させる可能性があるシステム内の他の要因によっても影響を受ける。結果は、0超でなければならない。HETPの管理限界は、自然対数のBox-Cox変換(λ=0)を用いることによって最良に決定される。変換されたデータの管理限界は、平均+/-3の標準偏差を用いMinitabにより計算した。標準偏差は、平均移動範囲に基づいて決定される。カラム寿命の間のカラム性能の変動を考慮するために、25の移動範囲を選択した。上方及び下方管理限界を逆変換(ex)して、変換されていないデータの管理限界を決定する。各フロントのHETP結果及び管理限界の時系列プロットを図33(平衡化フロント)、図34(WFIフラッシュフロント)、及び図35(ストレージフロント)に示す。この過去のレビューに基づき、これらの限界内での動作であれば、許容可能なクロマトグラフ性能が得られると期待されている。上方管理限界を超える値は、カラム流量の問題を示している可能性があり、更に評価する必要がある。下方管理限界を下回る値は、計算エラーを示している可能性がある。
SSは、ガンマモデルの分布がどのくらい良好にデータにあてはめられるかを示す尺度である。この尺度を使用して、GDTA法で計算されたHETP値がプロセスデータを表すことを確認する。下限は存在せず、結果は0超でなければならない。SSの上方管理限界は、自然対数のBox-Cox変換(λ=0)を用いることによって最良に決定される。変換されたデータの管理限界は、平均+/-3の標準偏差を用いMinitabにより計算した。標準偏差は、平均移動範囲に基づいて決定される。カラム寿命の間のカラム性能の変動を考慮するために、100の移動範囲を選択した。変換されたデータの上方管理限界を逆変換して、平衡化フロントについて0.110、WFIフラッシュフロントについて0.027、及びストレージフロントについて0.073を得た(表3を参照されたい)。限界内にある結果は、モデルがデータ及び過去の結果にあてはめられることを保証する。結果がこの範囲外である場合、特別な原因が考えられる。
平均値を、ガンマモデルの分布の精度についての第2の尺度として加えた。平均値は、フロントの理論的な質量中心を表し、システム内で当該値をシフトさせる、大過剰のカラム体積や移動相と樹脂との間の相互作用などといった他の要因がない限り、常に1カラム体積に近い値であるべきである。平衡化フロント、WFIフラッシュフロント及びストレージフロントの平均値は不規則な分布を有し、変換の恩恵を受けていない。フロントのそれぞれの平均については、0.80~1.20CVの管理限界を適用することが推奨される(表3を参照されたい)。平均値はカラム性能の尺度ではなく、分析が適切であったかを確認するためのチェックとして用いられるものであることから、これは適切である。これらの限界は、予想される計算結果からの有意な逸脱を特定するのに十分なものであると予想される。より厳しい管理限界は、このチェックの感度としては必要とされず、これについては各カラム充填で変化すると見られる。
概論:
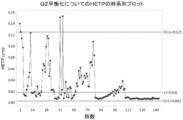
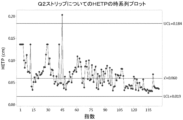
本実施例は、レミケード(登録商標)(インフリキシマブ)の製造に使用される二次陰イオン交換(Q2)カラム精製工程にGDTA法を適用することを記載する。Q2カラムは、陰イオン交換クロマトグラフィカラムである。精製プロセスは、本明細書に記載されるように、GDTAに適した3つのトランジションフロント、すなわち、平衡化フロント、ストリップフロント、及びストレージフロントを含む。
HETP:
HETPは、カラム性能に直接関連するものであり、分散を増加させる可能性があるシステム内の他の要因によっても影響を受ける。結果は、0超でなければならない。HETPの管理限界は、自然対数のBox-Cox変換(λ=0)を用いることによって最良に決定される。変換されたデータの管理限界は、平均+/-3の標準偏差を用いMinitabにより計算した。標準偏差は、平均移動範囲に基づいて決定される。カラム寿命の間のカラム性能の変動を考慮するために、100の移動範囲を選択した。上方及び下方管理限界を逆変換(ex)して、変換されていないデータの管理限界を決定する。
SSは、ガンマモデルの分布がどのくらい良好にデータにあてはめられるかを示す尺度である。この尺度を使用して、GDTA法で計算されたHETP値がプロセスデータを表すことを保証する。下限は存在せず、結果は0超でなければならない。SSの上方管理限界は、自然対数のBox-Cox変換(λ=0)を用いることによって最良に決定される。変換されたデータの管理限界は、平均+/-3の標準偏差を用いMinitabにより計算した。標準偏差は、平均移動範囲に基づいて決定される。カラム寿命の間のカラム性能の変動を考慮するために、100の移動範囲を選択した。移動範囲による方法ではより高い標準偏差が出ていたため、ストレージフロントについての集計データから標準偏差を決定した。管理限界を下の表4に報告する。限界内にある結果は、モデルがデータ及び過去の結果にあてはめられることを保証する。結果がこの範囲外である場合、特別な原因が考えられる。
平均値を、ガンマモデルの分布の精度についての第2の尺度として加えた。平均値は、フロントの理論的な質量中心を表し、システム内で当該値をシフトさせる、大過剰のカラム体積や移動相と樹脂との間の相互作用などといった他の要因がない限り、常に1カラム体積に近い値であるべきである。平衡化フロント、ストリップフロント、及びストレージフロントの平均値は不規則な分布を有し、変換の恩恵を受けていない。フロントのそれぞれの平均については、0.80~1.20CVの管理限界を適用することが推奨される(表4を参照されたい)。平均値はカラム性能の尺度ではなく、分析が適切であったかを確認するためのチェックとして用いられるものであることから、これは適切である。これらの限界は、予想される計算結果からの有意な逸脱を特定するのに十分なものであると予想される。より厳しい管理限界は、このチェックの感度としては必要とされず、これについては各カラム充填で変化すると見られる。
ゴリムマブのバックグラウンド
抗TNFα剤を用いた治療は炎症性関節炎の治療に成功裏に使用されてきたが、初期の抗TNFα剤は安全性、投与計画、費用及び/又は免疫原性に関して限界がある。いくつかの限界に対処するために、SIMPONI(登録商標)(ゴリムマブ)と表される完全ヒト抗抗TNFα mAbが開発された。ゴリムマブ(CNTO148及びrTNV148Bとしても既知である)は、免疫グロブリンG1(IgG1)重鎖アイソタイプ(G1m[z]アロタイプ)及びκ軽鎖アイソタイプを有する完全ヒトモノクローナル抗体である。ゴリムマブは、配列番号1のアミノ酸配列を含む重鎖(HC)及び配列番号2のアミノ酸配列を含む軽鎖(LC)を有する。ゴリムマブの分子量は、149,802~151,064ダルトンの範囲である。
強直性脊椎炎(AS)を対象としたゴリムマブ皮下(SC)投与のグローバル無作為化二重盲検プラセボ対照第3相試験(試験C0524T09)において、ゴリムマブは、強直性脊椎炎(AS)に罹患した被験者における徴候及び症状、身体機能、健康関連の生活の質(HRQOL)の改善に有効であることが実証された。更に、安全性分析では、SCゴリムマブは一般的に良好に忍容されることが示され、また他の抗TNFα剤で観察されたものと同様の安全性プロファイルを示された。
例示的抗TNFα抗体配列-SIMPONI(登録商標)(ゴリムマブ)
各重鎖CDR(HCDR)及び軽鎖CDR(LCDR)は、ゴリムマブの重鎖及び軽鎖(Kabatにより定義)に下線が引かれている。
本発明は核酸を含む組換え発現カセットを使用する。核酸配列、例えば本発明の方法に使用される抗体をコードするcDNA又はゲノム配列を使用して、少なくとも1つの所望の宿主細胞に導入することができる組換え体発現カセットを構築することができる。組換え発現カセットは、典型的には、意図される宿主細胞においてポリヌクレオチドの転写を導く、転写開始調節配列に操作可能に連結される、ポリヌクレオチドを含む。異種及び非異種(すなわち、内因性)プロモーターの両方を利用して、核酸の発現を導くことができる。
本発明は、単離された核酸分子を含むベクター、組換えベクターで遺伝子操作される宿主細胞、及び技術分野において周知である組換え技術による少なくとも1つの抗TNFα抗体の産生にも関する。
他にもいくつかの哺乳動物細胞株が利用可能性であるものの、現在生産されている治療用組換えタンパク質のほとんどは、チャイニーズハムスター卵巣(CHO)細胞で作成されている(Jayapal KPら、「Recombinant protein theo rapeutics from CHO cells-20 years and counting.」Chem.Eng.Prog.2007年;103:40-47;Kunert R、Reinhart D.「Advances in recombinant antibody manufacturing.」Appl Microbiol Biotechnol.2016年;100(8):3451-61)。それらの強みは、例えば、付着細胞としての又は懸濁液中での堅牢な増殖、無血清培地及び合成培地への適応性、高い生産性、並びに治療用の組換えタンパク質の産生についてこれまでに法的な承認が確立されていること、が挙げられる。これらはまた、非常に遺伝子改変を受け入れやすく、細胞のトランスフェクション、組換えタンパク質発現、及びクローン選択の方法は十分に特徴付けられる。CHO細胞はまた、ヒトに適合する翻訳後修飾を提供することができる。本明細書で使用するとき、「CHO細胞」としては、例えば、CHO-DG44、CHO-Kl、CHO-M、CHO-S、CHO GSノックアウト、並びにこれらの改変及び誘導体が挙げられるが、これらに限定されない。
CHO細胞での発現に一般的に使用されるベクターの一種に、pC4がある。プラスミドpC4は、プラスミドpSV2-dhfr(ATCC(登録商標)37146)の誘導体である。このプラスミドは、SV40初期プロモーターの制御下でマウスDHFR遺伝子を含有する。ジヒドロ葉酸の活性を欠損しており、これらのプラスミドでトランスフェクトされるチャイニーズハムスター卵巣細胞又はその他の細胞は、化学療法剤メトトレキサートを添加した選択培地(例えば、α-MEM、Life Technologies、Gaithersburg、MD)で細胞を増殖させることによって選択することができる。メトトレキサート(MTX)に対して耐性を有する細胞におけるDHFR遺伝子の増幅は、十分に実証されている(例えば、F.W.Altら、「Selective multiplication of dihydrofolate reductase genes in methotrexate-resistant variants of cultured murine cells.」J.Biol.Chem.253:1357-1370(1978年);並びにM.J.Page及びM.A.Sydenham、「High level expression of the humanized monoclonal antibody Campath-1H in Chinese hamster ovary cells.」Biotechnology 9:64-68(1991年))。MTX濃度が上昇する(increasing concentrations)中で成長した細胞は、DHFR遺伝子が増幅される結果として、標的酵素であるDHFRを過剰生産することにより、薬物に対する耐性を発達させる。第2の遺伝子がDHFR遺伝子に連結されている場合、通常、共増幅され、過剰発現される。このアプローチを使用して、増幅遺伝子の1,000を超えるコピーを有する細胞株を開発できることが、当該技術分野において知られている。続いて、メトトレキサートを取り除いたときに、宿主細胞の1つ以上の染色体に組み込まれた増幅遺伝子を含有する細胞株が得られる。
抗TNF抗体αは、プロテインA精製、硫酸アンモニウム又はエタノール沈殿、酸抽出、陰イオン又は陽イオン交換クロマトグラフィ、ホスホセルロースクロマトグラフィ、疎水性相互作用クロマトグラフィ、アフィニティクロマトグラフィ、ヒドロキシルアパタイトクロマトグラフィ及びレクチンクロマトグラフィが挙げられるがこれらに限定されない既知の方法により、組換え細胞培養物から回収し、精製することができる。高速液体クロマトグラフィ(「HPLC」)を精製に利用することもできる。
SIMPONI(登録商標)(ゴリムマブ)は、連続的な細胞の灌流培養、続いて精製を含む9段階のプロセスで製造される。製造工程の概要は、図39に示されている。
・前培養
・50Lの播種用リアクター/500Lの産生用バイオリアクター
・200Lの播種用バイオリアクター
・1000Lの産生用バイオリアクター
・直接的な生成物捕集
・下流処理
ステージ1
前培養及び増殖
SIMPONI(登録商標)(ゴリムマブ)の産生における第1の段階は、ゴリムマブのHC及びLC配列を発現するトランスフェクトされたSp2/0細胞のワーキングセルバンク(WCB)バイアルからの前培養の開始並びに培養フラスコ、使い捨て培養バッグ、及び50又は200Lの播種用バイオリアクターにおける細胞培養物の増殖である。500又は1000Lの産生用バイオリアクターへの接種に必要な細胞密度及び体積が得られるまで細胞を培養する。
WCBからの凍結バイアルを解凍し、6mMのL-グルタミン、0.5mg/Lのミコフェノール酸、2.5mg/Lのヒポキサンチン、及び50mg/Lのキサンチンを添加したハイブリドーマ用同性培地(CDH-A培地)で、0.2~0.4×106個(VC)/mLの播種密度になるように希釈した。解凍時の培養物生存率は≧50%なければならない。初期の継代は、バッチ記録に規定される範囲内で温度及びCO2を制御した加湿CO2インキュベーター内の培養フラスコに維持される。培養物を、0.6×106個VC/mLの最小細胞密度が得られるまで2~3日間インキュベートする。
バイオリアクター産生
製造プロセスにおける第2段階は、500L又は1000Lの産生用バイオリアクターにおける、細胞の灌流培養である。オルタネーティング・タンジェンタル・フロー(ATF)中空糸の細胞保持装置を介して細胞を保持しながら、産生用バイオリアクターから細胞培養物の透過液(permeate)(回収物)を回収し、培養物には新鮮な培地を補充する。
500L又は1000Lの産生用バイオリアクターの接種は、50又は200Lの播種用バイオリアクターの内容物を、6mMのL-グルタミン、0.5mg/Lのミコフェノール酸、2.5mg/Lのヒポキサンチン、及び50mg/Lのキサンチンを添加したハイブリドーマ用合成培地(CDH-A培地)を含む500又は1000Lの産生用バイオリアクターに移すことによって行う。移される体積は、≧0.3×106個生存細胞(VC)/mLの播種密度をもたらすのに十分なものでなければならない。培養物を34.0~38.0℃の温度、6.80~7.40のpH及び10~80%の溶存酸素濃度で維持する。生存細胞密度(VCD)、培養物生存率、バイオバーデン、及び免疫グロブリンG(IgG)濃度の測定のために、500又は1000Lの生産用プロセス全体を通してサンプリングを行う。
直接的な生成物捕集(DPC)
段階3では、1つ又は複数の500L又は1000Lの産生用バイオリアクターからの回収物は、MabSelect(商標)(GE Health care Bio-Sciences、ピッツバーグ、ペンシルベニア州、米国)プロテインAアフィニティクロマトグラフィカラム及び自動クロマトグラフィスキッドを使用して精製する。ゴリムマブ生成物は、回収物から捕捉され、培地成分及び宿主細胞に関連する不純物(例えば、DNA及び宿主細胞タンパク質)を含むプロセス関連不純物、並びに存在する可能性のあるウイルスが除去される。得られた直接的な生成物捕集(DPC)の溶出液は、更なる処理まで凍結する。
充填を回収する前に、MabSelect(商標)プロテインAカラムを、50mMのリン酸ナトリウム、150mMの塩化ナトリウム、0.1%のポリソルベート80(PS80)、pH7.3(平衡化バッファ)で平衡化する。カラムが平衡化されていることを確認するために、カラム溶出液をpH及び導電率についてモニタリングする。
回収物を0.45μmフィルタに通し、20~50g/Lの充填速度でプロテインAカラムに充填する。280nm(A280)での紫外線吸光度が経路長1mm当たり≦100mAUに戻るまで平衡化バッファでカラムを洗浄した後、結合したゴリムマブ生成物を有するカラムを、2~6カラム体積(CV)の更なる平衡化バッファで洗浄する。その後、4.5~7.0CVの0.1Mのクエン酸ナトリウム(pH5.0)で中間洗浄を行う。
直接的な生成物捕集(DPC)の溶出物の解凍及びプール
段階4では、複数の直接的な生成物捕集(DPC)溶出液を解凍し、濾過し、溶媒/洗剤処理前にプールする。
DPC溶出液を、DPCプールの質量加重平均の日齢が15~51日(両端を含む)になるように選択する。凍結したDPC溶出液を15~25℃で解凍する。視認される氷が溶出液に含まれていなければ、解凍は完了していると考えられる。解凍は120時間を超えてはならない。解凍、プール、混合後、プールしたDPC溶出液のpHを試験し、必要に応じて、1.0Mのトリス(未滴定)又は1.0Mのクエン酸(未滴定)のいずれかを添加することにより、5.9~6.5のpHに調整する。最終pHに達した後、プールしたDPC溶出液をバイオバーデンについての分析のためにサンプリングする。プールのタンパク質濃度は、総プール体積及びプール中の総タンパク質重量(g)に基づいて計算される。次いで、プールしたDPC溶出液を、混合容器内に0.2μmで濾過する。濾過し、プールしたDPC溶出液を、段階5で更に処理する前に、15~25℃で≦48時間及び2~8℃で≦168時間の累計時間にわたって保持することができる。
DPC溶出液の溶媒/洗剤(S/D)処理
段階5では、プールした直接的な生成物捕集(DPC)の溶出液を、トリ-n-ブチルホスファート(TNBP)及びポリソルベート80(PS80)(溶媒/洗剤[S/D]処理)と共にインキュベートして、存在する可能性があり脂質エンベロープを有する任意のウイルスを不活性化する。
0.08~0.12(v/v)の比が達成されるまで、2%TNBP/10%PS80(w/w)を含むS/Dストック溶液を、プールしたDPC溶出液が入っている混合容器に移す。溶液を混合して溶液の均質性を確保し、次いで不活性化容器内に移す。移した後、15~25℃の温度で少なくとも90分間インキュベートすることによってウイルスの不活性化が達成される。S/D処理されたゴリムマブ生成物の陽イオン交換クロマトグラフィカラムへの充填(段階6)は、S/D-化学物質の添加の≦20時間後に完了する(段階5)。
陽イオン交換クロマトグラフィ
段階6では、溶媒/洗剤(S/D)で処理した段階5の材料を、UNOsphere S(商標)(Bio-Rad、ハーキュリーズ、カリフォルニア州、米国)陽イオン交換クロマトグラフィカラム及び自動クロマトグラフィスキッドを使用して精製する。段階6は、製品からS/Dプロセスの化学物質(トリ-n-ブチルホスファート[TNBP]及びポリソルベート80[PS80])及び他の不純物を除去するように設計されている。
充填前に、充填カラムを、30mMのリン酸ナトリウム、pH6.5のバッファ(平衡化バッファ)で平衡化する。カラムが平衡化されていることを確認するために、カラム溶出液をpH及び導電率についてモニタリングする。
充填中、S/D処理した生成物を水でインラインで希釈して、1.5~4.5mS/cmの充填導電率を達成する。カラムを35~55gのゴリムマブ/Lの充填率に充填した後、カラムを1.6~6.7カラム体積(CV)の平衡化バッファで洗浄し、その後、5.2~9.8CVの50mMのトリス、pH7.6~8.0のバッファで洗浄する。
陰イオン交換樹脂
段階7では、段階6の材料を、Q Sepharose(商標)XL(GE Health care Bio-Sciences、ピッツバーグ、ペンシルベニア州、米国)陰イオン交換クロマトグラフィカラム及び自動クロマトグラフィスキッドを使用して精製する。ゴリムマブは樹脂を通って流れる一方で、DNA、他の不純物、及びウイルス(存在する場合)は保持される。
充填前に、陰イオン交換カラムを、50mMのトリス、50mMのNaCl、pH7.6~8.0(平衡化バッファ)で平衡化する。カラムが平衡化されていることを確認するために、カラム溶出液をpH及び導電率についてモニタリングする。
陽イオン交換クロマトグラフィ(段階6)によって精製された材料を、50~250cm/hの充填速度及び50~150g/Lの充填率で陰イオン交換カラムに装填する。ゴリムマブはカラムを通って流れ(非結合モード)、280nm(A280)での紫外線吸光度が≧30mAU/mm経路長まで上昇した時点で回収される。充填後、カラムを50~250cm/hの流量の平衡化バッファで洗浄する。生成物フロースルーの回収は、A280の読み取りが≧80mAU/mm経路長に戻るまで継続する。
ウイルス除去濾過
段階8では、陰イオン交換クロマトグラフィによって精製された段階7の材料を、NFP(商標)ウイルス保持フィルタを通して濾過する。この工程は、存在する可能性のある小型ウイルス及び大型ウイルスの両方を除去することを目的とする。
使用前に、NFP(商標)フィルタをNFP(商標)濾過システムに取り付け、注入用水(WFI)でフラッシュし、オートクレーブ処理する。オートクレーブ処理後、フィルタをWFIでフラッシュし、次いで、水透過性について試験する。フィルタを、50mMのトリス、50mMのNaCl、pH7.6~8.0のバッファで平衡化する。NFP(商標)フィルタが平衡化されていることを確認するために、濾液をpH及び導電率についてモニタリングする。
必要に応じて、生成物濾過の前に、陰イオン交換クロマトグラフィ(段階7)で精製した生成物を、50mMのトリス、50mMのNaCl、pH7.6~8.0で希釈して、≦6.5g/Lのタンパク質濃度にする。希釈後、生成物溶液を混合し、その後、0.2μmフィルタを通して濾過する。
製剤化されたバルク(FB)を得るための濃縮及び透析濾過
段階9では、段階8の材料を濃縮し、透析濾過して、製剤賦形剤を添加する。その後、ポリソルベート80(PS80)を、濃縮及び透析濾過したゴリムマブ溶液に添加し、製剤化されたバルク(FB)を得る。
使用前に、膜を含む限外濾過システムを、50mMのトリス、50mMのNaCl、pH7.6~8.0のバッファで平衡化する。膜が平衡化されていることを確認するために、濾液及び保持液をモニタリングする。
ウイルス除去濾過(段階8)により精製されたゴリムマブ生成物を40~90g/Lに濃縮し、8~12透析濾過体積の10mMのヒスチジン、4.5%のソルビトール、pH5.3のバッファ(透析濾過バッファ)を使用して透析濾過する。バッファ交換が完全に行われたことを確認するために、透析濾過後、濾液のpH、導電率、及び浸透圧を試験する。バッファの交換後、溶液を≦180g/Lに過剰濃縮し、次いで、システムを空にして回収する。濃縮、透析濾過、及び過剰濃縮の間、供給圧力及び保持液圧力は、それぞれ≦2.8バール及び≦2.1バールになるように制御することができる。あるいは、膜貫通圧力(TMP)は、濃縮、透析濾過、及び過剰濃縮の間、≦2.5バールで制御することができる。保持タンクの温度を≦35℃になるようにモニタリングする。
この実施例は、抗TNF抗体、例えば、抗TNFα抗体SIMPONI(登録商標)(ゴリムマブ)の製造中の精製における、クロマトグラフィカラム、例えば、段階3でのプロテインAアフィニティクロマトグラフィカラム、段階6での陽イオン交換クロマトグラフィカラム、及び段階7での陰イオン交換クロマトグラフィカラムへのGDTA法の適用を記載する。
段階3では、MabSelect(商標)プロテインAアフィニティクロマトグラフィカラムを使用し、分析されたトランジションフロントは、例えば、溶出フロント(図40)、グアニジンHClでの殺菌中に生成されるフロント(図41)、及び0.1Mのクエン酸ナトリウム、pH3.5での殺菌後のすすぎ中に生成されるフロント(図42)を含む。示される結果は、SIMPONI(登録商標)(ゴリムマブ)の160バッチの分析を表す。傾向の予備評価は、カラム性能において明らかないくらかのドリフト及びカラム充填間で観察されたいくらかの差違を示す。将来的にリアルタイムでプロセスをモニタリングするためのGDTA法を実施する際に使用するための管理限界を確立することを目的として、他の利用可能なバッチ情報及びカラム性能データとの比較を含む、このデータの完全な分析を完了させる。
段階6では、UNOsphere S(商標)陽イオン交換クロマトグラフィカラムを使用して、分析されたトランジションフロントは、例えば、溶媒/洗剤(S/D)処理した材料の充填中に生成されるフロント(図43)、溶出中に生成されるフロント(図44)、及びストリップの間に生成されるフロント(図45)を含む。示される結果は、SIMPONI(登録商標)(ゴリムマブ)の72バッチの分析を表す。傾向の予備評価は、カラム性能で明らかないくらかのドリフト及びカラム充填間で観察されたいくらかの差違を示す。将来的にリアルタイムでプロセスをモニタリングするためのGDTA法を実施する際に使用するための管理限界を確立することを目的として、他の利用可能なバッチ情報及びカラム性能データとの比較を含む、このデータの完全な分析を完了させる。
段階7では、Q Sepharose(商標)XL陰イオン交換クロマトグラフィカラムを使用して分析されたトランジションフロントは、例えば、水酸化ナトリウムで洗浄する間に生成されるフロント(図46)及びストリップの間に生成されるフロント(図47)を含む。示される結果は、SIMPONI(登録商標)(ゴリムマブ)の71バッチの分析を表す。傾向の予備評価は、カラム性能で明らかないくらかのドリフト及びカラム充填間で観察されたいくらかの差違を示す。将来的にリアルタイムでプロセスをモニタリングするためのGDTA法を実施する際に使用するための管理限界を確立することを目的として、他の利用可能なバッチ情報及びカラム性能データとの比較を含む、このデータの完全な分析を完了させる。
Claims (10)
- 抗TNF抗体を産生するための製造方法におけるクロマトグラフィカラムの操作方法であって、前記抗TNF抗体が、配列番号1のアミノ酸配列を含む重鎖(HC)及び配列番号2のアミノ酸配列を含む軽鎖(LC)、又はそれらの抗原結合フラグメントを含み、前記操作方法が、
カラム充填を含む前記クロマトグラフィカラムの初回の操作中に、少なくとも1つの移動相のトランジションフロントについて、2つ以上の間隔で、カラム出口信号及び累積流量パラメータを収集する工程と、
上昇するトランジションフロントについては式Iaを用い、又は下降するトランジションフロントについては式Ibを用い、前記少なくとも1つの移動相のトランジションフロントに関し前記収集したカラム出口信号と累積流量パラメータとに基づいて、ガンマモデルの累積分布曲線を決定する工程であって、式Ia又は式Ibは、
であり、各式中、Cは所与のVについてのカラム出口信号であり、Vは累積流量をカラム体積で除算したものであり、k、θ、及びViは前記曲線を画定するために使用される形状、スケール、及びオフセットについてのパラメータである、ガンマモデルの累積分布曲線を決定する工程と、
式IIと、前記ガンマモデルの累積分布曲線のパラメータk、θ、及びViとを用い、少なくとも1つの移動相のトランジションフロントについての理論段相当高さ(HETP)値を計算する工程であって、式IIは、
式中、
である、理論段相当高さ(HETP)値を計算する工程と、
前記計算されたHETP値に基づき、前記クロマトグラフィカラム充填の質を評価する工程と、を含む、方法。 - 前記評価に基づいて、前記クロマトグラフィカラムのコンディショニング、交換、又は再充填を行うことを更に含む、請求項1に記載の方法。
- 前記クロマトグラフィカラム充填について1回又は複数回の後の使用の間に、対応する移動相トランジションフロントについて、2つ以上の間隔で、カラム出口信号と、累積流量パラメータとを収集する工程と、
前記クロマトグラフィカラム充填について前記1回又は複数回の後の使用の各回の間に、収集された前記カラム出口信号及び累積流量パラメータを用い、前記決定する工程及び前記計算する工程を実行する工程と、
前記実行する工程に基づき、前記1回又は複数回の後の使用の各回の間に、前記クロマトグラフィカラム充填のHETP値を決定する工程と、
2回以上の後の使用の前記クロマトグラフィカラム充填の前記決定されたHETP値の傾向を蓄積する工程と、
前記蓄積した傾向に基づき、前記クロマトグラフィカラム充填の前記質における変化を検出する工程と、を含み、
前記クロマトグラフィカラムのコンディショニング、交換、又は再充填が、前記検出に基づくものである、請求項1に記載の方法。 - 前記カラム充填の前記1回又は複数回の後の使用における前記クロマトグラフィカラム充填の前記HETP値が、前記カラム充填の1回又は複数回の以前の使用における、前記クロマトグラフィカラム充填の前記HETP値と比較して、増加していることにより、前記クロマトグラフィカラム充填の品質の低下を検出する、請求項3に記載の方法。
- 前記カラム充填の前記初回の操作の間に、2つ以上の異なる移動相のトランジションフロントについてのカラム出口信号及び累積流量パラメータが収集され、
前記方法が、
前記2つ以上の異なる移動相トランジションフロントのそれぞれについてHETP値を計算するために、前記2つ以上の異なる移動相トランジションフロントのそれぞれについて別個に収集された前記カラム出口信号及び累積流量パラメータを用い、前記決定する工程及び前記計算する工程を実行する工程と、
前記2つ又はそれ以上のHETP計算値に基づき、前記クロマトグラフィカラム充填の質を評価する工程と、を含み、
前記クロマトグラフィカラムのコンディショニング、交換、又は再充填が、前記評価に基づくものである、請求項1に記載の方法。 - 前記クロマトグラフィカラムが、プロテインAアフィニティクロマトグラフィカラム、陽イオン交換クロマトグラフィカラム、及び陰イオン交換クロマトグラフィカラムからなる群から選択される、請求項1~5のいずれかに記載の方法。
- 前記プロテインAアフィニティクロマトグラフィカラムが、MabSelect(商標)プロテインAアフィニティクロマトグラフィカラムを含み、前記陽イオン交換クロマトグラフィカラムが、UNOsphere S(商標)陽イオン交換クロマトグラフィカラムを含み、前記陰イオン交換クロマトグラフィカラムが、Q Sepharose(商標)XL陰イオン交換クロマトグラフィカラムを含む、請求項6に記載の方法。
- 前記プロテインAアフィニティクロマトグラフィカラムにおける前記移動相のトランジションフロントが、抗TNF抗体の溶出中に生成されるフロント、グアニジンHClでのカラムの殺菌中に生成されるフロント、殺菌後のカラムの0.1Mのクエン酸ナトリウム(pH3.5)でのリンス中に生成されるフロントからなる群から選択される1つ又は複数のフロントから生成される、請求項6に記載の方法。
- 前記陽イオン交換クロマトグラフィカラムにおける前記移動相のトランジションフロントが、抗TNF抗体を含み溶媒/洗剤(S/D)処理された材料の充填中に生成されるフロント、抗TNF抗体の溶出中に生成されるフロント、及びカラムストリップ中に生成されるフロントからなる群から選択される1つ又は複数のフロントから生成される、請求項6に記載の方法。
- 前記陰イオン交換クロマトグラフィカラムにおける前記移動相のトランジションフロントが、水酸化ナトリウムでのカラムの洗浄中に生成されるフロント及びカラムストリップ中に生成されるフロントからなる群から選択される1つ又は複数のフロントから生成される、請求項6に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862660340P | 2018-04-20 | 2018-04-20 | |
| US62/660,340 | 2018-04-20 | ||
| PCT/US2019/028314 WO2019204721A1 (en) | 2018-04-20 | 2019-04-19 | Chromatography column qualification in manufacturing methods for produring anti-tnf antibody compositions |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021522471A JP2021522471A (ja) | 2021-08-30 |
| JP7344902B2 true JP7344902B2 (ja) | 2023-09-14 |
Family
ID=66429636
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020557993A Active JP7268054B2 (ja) | 2018-04-20 | 2019-04-19 | 抗il12/il23抗体組成物を産生するための製造方法におけるクロマトグラフィカラムの品質評価 |
| JP2020557253A Active JP7344902B2 (ja) | 2018-04-20 | 2019-04-19 | 抗tnf抗体組成物を産生するための製造方法におけるクロマトグラフィカラムの品質評価 |
| JP2020557994A Withdrawn JP2021522477A (ja) | 2018-04-20 | 2019-04-19 | クロマトグラフィカラムの品質評価のための遷移分析方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020557993A Active JP7268054B2 (ja) | 2018-04-20 | 2019-04-19 | 抗il12/il23抗体組成物を産生するための製造方法におけるクロマトグラフィカラムの品質評価 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020557994A Withdrawn JP2021522477A (ja) | 2018-04-20 | 2019-04-19 | クロマトグラフィカラムの品質評価のための遷移分析方法 |
Country Status (23)
| Country | Link |
|---|---|
| US (6) | US11225516B2 (ja) |
| EP (4) | EP4063850A1 (ja) |
| JP (3) | JP7268054B2 (ja) |
| KR (3) | KR102853122B1 (ja) |
| CN (3) | CN112041673A (ja) |
| AU (2) | AU2019256647B2 (ja) |
| CA (3) | CA3096902A1 (ja) |
| CY (1) | CY1125296T1 (ja) |
| DK (2) | DK3781943T3 (ja) |
| EA (4) | EA039018B1 (ja) |
| ES (1) | ES2914987T3 (ja) |
| FI (1) | FI3781941T3 (ja) |
| HR (2) | HRP20220676T1 (ja) |
| HU (1) | HUE058711T2 (ja) |
| IL (2) | IL278039B2 (ja) |
| LT (2) | LT3781941T (ja) |
| PL (1) | PL3781943T3 (ja) |
| PT (2) | PT3781941T (ja) |
| RS (2) | RS63424B1 (ja) |
| SG (1) | SG11202010019YA (ja) |
| SI (1) | SI3781943T1 (ja) |
| SM (1) | SMT202200264T1 (ja) |
| WO (3) | WO2019204721A1 (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018119142A1 (en) | 2016-12-21 | 2018-06-28 | Amgen Inc. | Anti-tnf alpha antibody formulations |
| WO2020059290A1 (ja) * | 2018-09-21 | 2020-03-26 | 株式会社日立ハイテクノロジーズ | 液体クロマトグラフを有する分析装置および液体クロマトグラフの分析方法 |
| GB2636487B (en) * | 2020-11-17 | 2025-09-24 | Agilent Technologies Inc | Gas Chromatography Systems and Methods with Diagnostic and Predictive Module |
| IL309997A (en) * | 2021-07-09 | 2024-03-01 | Janssen Biotech Inc | Production methods for the production of anti-TNF antibody compositions |
| CA3247416A1 (en) * | 2022-04-08 | 2023-10-12 | Csl Behring Ag | Methods of sanitizing and/or regenerating a chromatography medium |
| WO2024092203A1 (en) * | 2022-10-28 | 2024-05-02 | Amgen Inc. | Compositions of anti-interleukin 12/interleukin 23 antibody |
| CN116577449A (zh) * | 2023-05-16 | 2023-08-11 | 无锡药明生物技术股份有限公司 | 一种在线评估层析柱性能的方法及其应用 |
| CN116369936B (zh) * | 2023-05-31 | 2023-10-03 | 深圳市奋达智能技术有限公司 | 一种心电信号处理方法、系统、装置及存储介质 |
| CN116966875B (zh) * | 2023-07-31 | 2025-07-08 | 中国农业科学院郑州果树研究所 | 一种用于反向色谱柱中霜霉威检测的碳纳米材料的制备方法及应用 |
| CN117907511B (zh) * | 2024-03-20 | 2024-06-14 | 浙江灵析精仪科技发展有限公司 | 一种多组分重叠峰的自动化解析方法、装置及电子设备 |
| CN118243822A (zh) * | 2024-04-24 | 2024-06-25 | 上海交通大学医学院附属瑞金医院 | 一种基于lc-ms/ms的乌司奴单抗的检测方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007117490A2 (en) | 2006-04-05 | 2007-10-18 | Abbott Biotechnology Ltd. | Antibody purification |
| WO2009094203A2 (en) | 2008-01-25 | 2009-07-30 | Biogen Idec Ma Inc. | Automated system and method for monitoring chromatography column performance, and applications thereof |
Family Cites Families (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US894395A (en) | 1908-02-19 | 1908-07-28 | George K Reid | Curtain-stretching pin. |
| FR1353739A (fr) * | 1963-03-06 | 1964-02-28 | Gulf Research Development Co | Appareil de chromatographie |
| US4399216A (en) | 1980-02-25 | 1983-08-16 | The Trustees Of Columbia University | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US5179017A (en) | 1980-02-25 | 1993-01-12 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4634665A (en) | 1980-02-25 | 1987-01-06 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4656134A (en) | 1982-01-11 | 1987-04-07 | Board Of Trustees Of Leland Stanford Jr. University | Gene amplification in eukaryotic cells |
| US5149636A (en) | 1982-03-15 | 1992-09-22 | Trustees Of Columbia University In The City Of New York | Method for introducing cloned, amplifiable genes into eucaryotic cells and for producing proteinaceous products |
| US5168062A (en) | 1985-01-30 | 1992-12-01 | University Of Iowa Research Foundation | Transfer vectors and microorganisms containing human cytomegalovirus immediate-early promoter-regulatory DNA sequence |
| GB8601597D0 (en) | 1986-01-23 | 1986-02-26 | Wilson R H | Nucleotide sequences |
| US4956288A (en) | 1988-04-22 | 1990-09-11 | Biogen, Inc. | Method for producing cells containing stably integrated foreign DNA at a high copy number, the cells produced by this method, and the use of these cells to produce the polypeptides coded for by the foreign DNA |
| US5266491A (en) | 1989-03-14 | 1993-11-30 | Mochida Pharmaceutical Co., Ltd. | DNA fragment and expression plasmid containing the DNA fragment |
| US5580734A (en) | 1990-07-13 | 1996-12-03 | Transkaryotic Therapies, Inc. | Method of producing a physical map contigous DNA sequences |
| US5641670A (en) | 1991-11-05 | 1997-06-24 | Transkaryotic Therapies, Inc. | Protein production and protein delivery |
| US5733761A (en) | 1991-11-05 | 1998-03-31 | Transkaryotic Therapies, Inc. | Protein production and protein delivery |
| US5410928A (en) | 1993-10-27 | 1995-05-02 | The Whitaker Corporation | Scrap removal system for a stamping and forming machine |
| US5804420A (en) | 1997-04-18 | 1998-09-08 | Bayer Corporation | Preparation of recombinant Factor VIII in a protein free medium |
| US6475725B1 (en) | 1997-06-20 | 2002-11-05 | Baxter Aktiengesellschaft | Recombinant cell clones having increased stability and methods of making and using the same |
| CN1386196A (zh) * | 2000-07-28 | 2002-12-18 | 欧洲流程(英国)有限公司 | 用于填充色谱柱的方法和设备以及色谱柱 |
| US20060094104A1 (en) | 2004-10-29 | 2006-05-04 | Leopold Grillberger | Animal protein-free media for cultivation of cells |
| US20070021277A1 (en) | 2005-07-21 | 2007-01-25 | Kuo Hai P | Upper and lower body exerciser |
| EP2253644B1 (en) * | 2005-12-20 | 2013-10-16 | Bristol-Myers Squibb Company | Compositions and methods for producing a composition |
| US8833589B2 (en) | 2005-12-21 | 2014-09-16 | Pactiv Packaging Inc. | Enhanced tamper evident bowl with blocked tab |
| EP3653699A1 (en) | 2006-01-04 | 2020-05-20 | Baxalta Incorporated | Oligopeptide-free cell culture media |
| US20070215548A1 (en) * | 2006-01-05 | 2007-09-20 | Zhou Joe Xin H | Systems and methods for packing chromatography columns |
| US8028562B2 (en) * | 2007-12-17 | 2011-10-04 | Schlumberger Technology Corporation | High pressure and high temperature chromatography |
| US20090277254A1 (en) * | 2008-05-09 | 2009-11-12 | Medlmmune, Llc | Methods of improving packed-bed chromatography performance |
| MY153074A (en) * | 2008-08-14 | 2014-12-31 | Teva Pharmaceuticals Australia Pty Ltd | Anti-il-12/11-23 antibodies |
| JP5635509B2 (ja) * | 2008-08-15 | 2014-12-03 | バイオジェン・アイデック・エムエイ・インコーポレイテッド | クロマトグラフィーカラムの性能を評価するための方法 |
| AU2009347206C1 (en) * | 2008-10-20 | 2016-12-08 | Abbvie Inc. | Isolation and purification of antibodies using Protein A affinity chromatography |
| US7983852B2 (en) * | 2008-10-21 | 2011-07-19 | Thermo Finnigan Llc | Methods of automated spectral peak detection and quantification without user input |
| US20120282654A1 (en) * | 2009-04-29 | 2012-11-08 | Schering Corporation | Antibody purification |
| US8357301B2 (en) * | 2009-06-24 | 2013-01-22 | Hoffmann-La Roche, Inc. | Chromatography equipment characterization |
| EP2467713A2 (en) * | 2009-08-20 | 2012-06-27 | Spectrosense Ltd. | Gas chromatographic analysis method and system |
| NZ621655A (en) * | 2009-10-26 | 2015-08-28 | Nestec Sa | Assays for the detection of anti-tnf drugs and autoantibodies |
| JP5621052B2 (ja) | 2010-12-21 | 2014-11-05 | エフ.ホフマン−ラ ロシュアーゲーF.Hoffmann−La Roche Aktiengesellschaft | クロマトグラフィー装置の特徴決定 |
| FR2973880B1 (fr) * | 2011-04-06 | 2013-05-17 | Commissariat Energie Atomique | Procede et dispositif d'estimation de parametres biologiques ou chimiques dans un echantillon, procede d'aide au diagnostic correspondant |
| US9150645B2 (en) * | 2012-04-20 | 2015-10-06 | Abbvie, Inc. | Cell culture methods to reduce acidic species |
| CN103163237B (zh) * | 2013-02-03 | 2014-06-11 | 大连理工大学 | 获得有机化合物在碳纳米管上保留的热力学参数和吸附等温线的方法 |
| WO2014145744A1 (en) | 2013-03-15 | 2014-09-18 | Alder Biopharmaceuticals, Inc. | Antibody purification and purity monitoring |
| US10099156B2 (en) * | 2013-04-08 | 2018-10-16 | Chromacon Ag | Chromatographic purification method |
| EP3077938A4 (en) * | 2013-10-09 | 2017-10-04 | Spectrosense Ltd. | Modified data representation in gas chromatographic analysis |
| US8946395B1 (en) * | 2013-10-18 | 2015-02-03 | Abbvie Inc. | Purification of proteins using hydrophobic interaction chromatography |
| CN107106930B (zh) * | 2014-11-17 | 2019-09-06 | 通用电气健康护理生物科学股份公司 | 用于执行液相色谱纯化的方法和设备 |
| FR3040215B1 (fr) * | 2015-08-20 | 2019-05-31 | Commissariat A L'energie Atomique Et Aux Energies Alternatives | Procede d’estimation d’une quantite de particules reparties en classes, a partir d’un chromatogramme. |
| US10465003B2 (en) | 2016-02-05 | 2019-11-05 | Janssen Biotech, Inc. | Anti-TNF antibodies, compositions, methods and use for the treatment or prevention of type 1 diabetes |
| EP3493843A1 (en) | 2016-08-03 | 2019-06-12 | FYB 202 Project GmbH | Production of biosimilar ustekinumab in cho cells |
| EA201990986A1 (ru) * | 2016-10-25 | 2019-09-30 | Ридженерон Фармасьютикалз, Инк. | Способы и системы анализа хроматографических данных |
-
2019
- 2019-04-19 LT LTEPPCT/US2019/028314T patent/LT3781941T/lt unknown
- 2019-04-19 FI FIEP19722413.2T patent/FI3781941T3/fi active
- 2019-04-19 CA CA3096902A patent/CA3096902A1/en active Pending
- 2019-04-19 US US16/389,146 patent/US11225516B2/en active Active
- 2019-04-19 SI SI201930243T patent/SI3781943T1/sl unknown
- 2019-04-19 IL IL278039A patent/IL278039B2/en unknown
- 2019-04-19 EP EP22172686.2A patent/EP4063850A1/en not_active Withdrawn
- 2019-04-19 KR KR1020207033238A patent/KR102853122B1/ko active Active
- 2019-04-19 EP EP19722418.1A patent/EP3781942B1/en active Active
- 2019-04-19 EP EP19722413.2A patent/EP3781941B1/en active Active
- 2019-04-19 KR KR1020207033174A patent/KR20210003824A/ko not_active Ceased
- 2019-04-19 EA EA202092511A patent/EA039018B1/ru unknown
- 2019-04-19 JP JP2020557993A patent/JP7268054B2/ja active Active
- 2019-04-19 CN CN201980027172.9A patent/CN112041673A/zh active Pending
- 2019-04-19 CA CA3097559A patent/CA3097559C/en active Active
- 2019-04-19 AU AU2019256647A patent/AU2019256647B2/en active Active
- 2019-04-19 SG SG11202010019YA patent/SG11202010019YA/en unknown
- 2019-04-19 HR HRP20220676TT patent/HRP20220676T1/hr unknown
- 2019-04-19 WO PCT/US2019/028314 patent/WO2019204721A1/en not_active Ceased
- 2019-04-19 US US16/389,114 patent/US11079361B2/en active Active
- 2019-04-19 RS RS20220647A patent/RS63424B1/sr unknown
- 2019-04-19 SM SM20220264T patent/SMT202200264T1/it unknown
- 2019-04-19 EA EA202092510A patent/EA039041B1/ru unknown
- 2019-04-19 DK DK19722993.3T patent/DK3781943T3/da active
- 2019-04-19 JP JP2020557253A patent/JP7344902B2/ja active Active
- 2019-04-19 CN CN201980027174.8A patent/CN112041674B/zh active Active
- 2019-04-19 HR HRP20260325TT patent/HRP20260325T1/hr unknown
- 2019-04-19 US US16/389,055 patent/US12018075B2/en active Active
- 2019-04-19 EP EP19722993.3A patent/EP3781943B1/en active Active
- 2019-04-19 WO PCT/US2019/028332 patent/WO2019204734A1/en not_active Ceased
- 2019-04-19 LT LTEPPCT/US2019/028332T patent/LT3781943T/lt unknown
- 2019-04-19 IL IL278025A patent/IL278025B2/en unknown
- 2019-04-19 HU HUE19722993A patent/HUE058711T2/hu unknown
- 2019-04-19 PT PT197224132T patent/PT3781941T/pt unknown
- 2019-04-19 JP JP2020557994A patent/JP2021522477A/ja not_active Withdrawn
- 2019-04-19 PT PT197229933T patent/PT3781943T/pt unknown
- 2019-04-19 ES ES19722993T patent/ES2914987T3/es active Active
- 2019-04-19 WO PCT/US2019/028349 patent/WO2019204747A1/en not_active Ceased
- 2019-04-19 KR KR1020207033178A patent/KR102837419B1/ko active Active
- 2019-04-19 EA EA202192301A patent/EA202192301A1/ru unknown
- 2019-04-19 CA CA3097776A patent/CA3097776C/en active Active
- 2019-04-19 PL PL19722993.3T patent/PL3781943T3/pl unknown
- 2019-04-19 RS RS20260274A patent/RS67842B1/sr unknown
- 2019-04-19 DK DK19722413.2T patent/DK3781941T3/da active
- 2019-04-19 AU AU2019256635A patent/AU2019256635B2/en active Active
- 2019-04-19 EA EA202192300A patent/EA202192300A1/ru unknown
- 2019-04-19 CN CN201980041378.7A patent/CN112313511B/zh active Active
-
2021
- 2021-07-02 US US17/366,360 patent/US12234283B2/en active Active
- 2021-12-08 US US17/545,128 patent/US20220089716A1/en not_active Abandoned
-
2022
- 2022-06-21 CY CY20221100426T patent/CY1125296T1/el unknown
-
2025
- 2025-01-31 US US19/042,853 patent/US20250171529A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007117490A2 (en) | 2006-04-05 | 2007-10-18 | Abbott Biotechnology Ltd. | Antibody purification |
| WO2009094203A2 (en) | 2008-01-25 | 2009-07-30 | Biogen Idec Ma Inc. | Automated system and method for monitoring chromatography column performance, and applications thereof |
Non-Patent Citations (1)
| Title |
|---|
| LARSON T M et al.,Use of process data to assess chromatographic performance in production-scale protein purification columns,BIOTECHNOLOGY PROGRESS,vol.19,AMERICAN CHEMICAL SOCIETY,2003年01月01日,P485-492 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7344902B2 (ja) | 抗tnf抗体組成物を産生するための製造方法におけるクロマトグラフィカラムの品質評価 | |
| US20250361266A1 (en) | Use of raman spectroscopy in downstream purification | |
| BR112020021108B1 (pt) | Método de operação de uma coluna cromatográfica em métodos de fabricação para produzir anticorpos anti-tnf | |
| HK40045539B (en) | Chromatography column qualification in manufacturing methods for producing anti-il12/il23 antibody compositions | |
| HK40045539A (en) | Chromatography column qualification in manufacturing methods for producing anti-il12/il23 antibody compositions | |
| BR112020020480B1 (pt) | Método para operação de uma coluna cromatográfica em métodos de fabricação para produzir anticorpos anti-il-12/il-23p40 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220329 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230425 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230724 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230808 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230904 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7344902 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |