JP7293220B2 - アレルギーの処置のための組成物および方法 - Google Patents
アレルギーの処置のための組成物および方法 Download PDFInfo
- Publication number
- JP7293220B2 JP7293220B2 JP2020526142A JP2020526142A JP7293220B2 JP 7293220 B2 JP7293220 B2 JP 7293220B2 JP 2020526142 A JP2020526142 A JP 2020526142A JP 2020526142 A JP2020526142 A JP 2020526142A JP 7293220 B2 JP7293220 B2 JP 7293220B2
- Authority
- JP
- Japan
- Prior art keywords
- sequence
- seq
- nucleic acid
- bacterial strain
- composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/0208—Specific bacteria not otherwise provided for
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/08—Clostridium, e.g. Clostridium tetani
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
- A61K2039/577—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2 tolerising response
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/58—Medicinal preparations containing antigens or antibodies raising an immune response against a target which is not the antigen used for immunisation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4866—Organic macromolecular compounds
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Pulmonology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Virology (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Biomedical Technology (AREA)
- Coloring Foods And Improving Nutritive Qualities (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Description
本出願は、2017年11月9日に出願された米国仮出願番号62/583,777;2018年3月1日に出願された米国仮出願番号62/637,355;および2018年8月23日に出願された米国仮出願番号62/721,786の35 U.S.C. § 119(e)の下での利益を主張する。これらの参照の出願の各々の内容全体は、参照により本明細書に組み込まれる。
本明細書に提供されるのは、食物アレルギーなどのアレルギーの処置のための組成物および方法である。また本明細書に提供されるのは、アレルギーに関連する免疫応答を調節する、および/または食物アレルギーなどのアレルギーに対する免疫寛容または減感作を誘導するための組成物および方法である。
世界保健機関のアレルギーについての統計に従うと、アレルギーの発生率は、先進国において過去50年にわたり上昇しており、および世界中の学齢児童のほぼ40~50%が少なくとも1の一般的なアレルゲンに対して感受性がある。例として、Pawankar R, et al. The WAO White Book on Allergy (Update 2013)を参照されたい。アレルギーは、幼年時代の間に発生する可能性があるのだが、アレルギーはまた、一生を通じて発症または発生し得る。
アレルゲンへの暴露の際のアレルギー反応の重症度は、軽症から、ときには致死的な反応まで広く範囲をとり得る。したがって、アレルギーおよびアレルギー反応を処置するための改善された治療法が所望される。
本開示の側面は、本明細書に記載の組成物のいずれかを投与することを含む、アレルギーを処置する方法を提供する。また提供されるものは、本明細書に記載の組成物のいずれかを投与することを含む、アレルギーに関連する免疫応答を調節する方法である。また提供されるものは、本明細書に記載の組成物のいずれかを投与することを含む、anに対する免疫寛容または減感作を誘導する方法である。また提供されるものは、抗生物質を投与すること、および本明細書に記載の組成物のいずれかを投与することを含む、アレルギーに関連する免疫応答を調節する方法である。また提供されるものは、抗生物質を投与すること、および本明細書に記載の組成物のいずれかを投与することを含む、anに対する免疫寛容または減感作を誘導する方法である。
本開示の側面は、Clostridium hathewayi、Clostridium bolteae、Sellimonas intestinalis、およびClostridium種からなる群から選択される種の2以上の精製された細菌株を含む組成物の治療的に有効な量を、それを必要とする対象へ投与することを含む、食物アレルギーを処置する方法を提供する。いくつかの態様において、組成物は、精製された細菌株Clostridium hathewayi、Clostridium bolteae、Sellimonas intestinalis、およびClostridium種からなる。
いくつかの態様において、細菌株は、凍結乾燥されている。いくつかの態様において、細菌株の1以上は、芽胞形態にある。いくつかの態様において、細菌株の各々は、芽胞形態にある。いくつかの態様において、菌株の1以上は、栄養形態にある。いくつかの態様において、細菌株の各々は、栄養形態にある。
いくつかの態様において、食物アレルギーは、ナッツアレルギー、魚アレルギー、小麦アレルギー、ミルクアレルギー、落花生アレルギー、木の実アレルギー、甲殻類アレルギー、大豆アレルギー、種子アレルギー、ゴマ種子アレルギー、およびタマゴアレルギーからなる群から選択される。いくつかの態様において、対象は、ヒトである。
本開示の側面は、Clostridium bolteae、Anaerotruncus colihominis、Sellimonas intestinales、Clostridium symbiosum、Blautia producta、Dorea longicatena、Erysipelotrichaceae bacterium、およびSubdolinogranulum spp.からなる群から選択される種の2以上の精製された細菌株を含む組成物の治療的に有効な量を、それを必要とする対象へ投与することを含む、食物アレルギーに関連する免疫応答を調節する方法を提供する。いくつかの態様において、組成物は、精製された細菌株Clostridium bolteae、Anaerotruncus colihominis、Sellimonas intestinales、Clostridium symbiosum、Blautia producta、Erysipelotrichaceae bacterium、およびSubdolinogranulum spp.からなる。いくつかの態様において、組成物は、精製された細菌株Clostridium bolteae、Anaerotruncus colihominis、Sellimonas intestinales、Clostridium symbiosum、Blautia producta、Dorea longicatena、およびSubdolinogranulum spp.からなる。
いくつかの態様において、細菌株は、凍結乾燥されている。いくつかの態様において、細菌株は、噴霧乾燥されている。いくつかの態様において、細菌株の1以上は、芽胞形態にある。いくつかの態様において、細菌株の各々は、芽胞形態にある。いくつかの態様において、細菌株の1以上は、栄養形態にある。いくつかの態様において、細菌株の各々は、栄養形態にある。
いくつかの態様において、食物アレルギーは、ナッツアレルギー、魚アレルギー、小麦アレルギー、ミルクアレルギー、落花生アレルギー、木の実アレルギー、甲殻類アレルギー、大豆アレルギー、種子アレルギー、ゴマ種子アレルギー、およびタマゴアレルギーからなる群から選択される。いくつかの態様において、対象は、ヒトである。
いくつかの態様において、組成物は、1以上のアジュバントをさらに含む。いくつかの態様において、アジュバントは、アレルギー処置または免疫寛容に関連する。
本開示の側面は、Clostridium hathewayi、Clostridium bolteae、Sellimonas intestinalis、およびClostridium種からなる群から選択される種の2以上の精製された細菌株を含む組成物の治療的に有効な量をそれを必要とする対象へ投与することを含む、食物アレルギーに対する免疫寛容または減感作を誘導する方法を提供する。いくつかの態様において、組成物は、精製された細菌株Clostridium hathewayi、Clostridium bolteae、Sellimonas intestinalisおよびClostridium種からなる。
いくつかの態様において、方法は、制御性T細胞の増殖および/または蓄積の誘導をもたらす。いくつかの態様において、方法は、IgE抗体の産生の抑制をもたらす。いくつかの態様において、方法は、Th2免疫応答の抑制をもたらす。
いくつかの態様において、投与は、経口投与である。いくつかの態様において、組成物は、経口送達のために処方されている。いくつかの態様において、組成物は、直腸送達のために処方されている。いくつかの態様において、組成物は、腸への送達のために処方されている。いくつかの態様において、組成物は、結腸への送達のために処方されている。
いくつかの態様において、組成物は、1以上のアジュバントをさらに含む。いくつかの態様において、アジュバントは、アレルギー処置または免疫寛容に関連する。
いくつかの態様において、組成物は、1以上のアジュバントをさらに含む。いくつかの態様において、アジュバントは、アレルギー処置または免疫寛容に関連する。
本開示の側面はまた、本明細書に記載の組成物のいずれかおよび薬学的に許容し得る賦形剤を含む医薬組成物を提供する。いくつかの態様において、医薬組成物は、経口送達のために処方される。いくつかの態様において、医薬組成物は、直腸送達のために処方される。いくつかの態様において、医薬組成物は、腸への送達のために処方される。いくつかの態様において、医薬組成物は、結腸への送達のために処方される。
本開示の側面はまた、本明細書に記載の組成物のいずれかおよび栄養素を含む食物製品を提供する。
添付の図面は、一定の縮尺で描かれていると意図されない。図は、説明のみのためにあり、および本開示の実施可能のために必要とされない。明確性のために、すべての構成要素がすべての図面において標識されているとは限らない。図面において:
アレルギーまたはアレルギー反応を低減することを目的とする現行の処置レジメンは、アレルギー性の免疫応答の兆候を、例えば抗ヒスタミン、コルチコステロイド、またはエピネフリンを用いて処置することに焦点が当てられている。これらの方法は、アレルゲンへの接触または曝露の際に刺激される根本的な望ましくないアレルギー性の免疫応答を処理し損なう。追加のアプローチは、アレルゲン免疫治療とも称される減感作治療であり、これにはアレルギー反応を誘導する特定のアレルゲンの同定、および次いで望ましくない免疫応答を調節するためのアレルゲンの繰り返し投与、アレルゲンへの免疫応答を有効に「減感作する」ことが必要となる。しかしながら、アレルギーに関連する特定のアレルゲンを同定することは常に実行可能であるわけではなく、および無数の、繰り返し投与は、低い患者のコンプライアンスをもたらすであろう。アレルゲン免疫治療はまた、重篤なアレルギー反応に関連するアレルギーを有する個体については実行不可能であるだろう。
対象は、アレルギー反応を誘導するアレルゲンに、当該技術分野において知られているいずれかのルート、例えば、摂取、吸入、注射、または直接接触を通して接触または曝露されるであろう。アレルギー反応に関連する兆候は、アレルゲンへの接触または曝露の部位、例えば皮膚の領域、呼吸器、または胃腸管、末梢部位に局在していてもよく、またはアナフィラキシーのケースにおいてなどの全身性となっていてもよい。
本明細書に提供される組成物および方法に従って処置され得るアレルギーの例は、限定せずに、アレルギー性喘息、アレルギー性大腸炎、動物アレルギー、アトピー性アレルギー、花粉症、皮膚アレルギー、蕁麻疹、アトピー性皮膚炎、アナフィラキシー、アレルギー性鼻炎、薬物または医薬アレルギー、湿疹(アトピー性皮膚炎)、食物アレルギー、真菌アレルギー、昆虫アレルギー(虫刺され/昆虫毒アレルギーを包含する)、カビアレルギー、植物アレルギー、および花粉症(pollenosis)を包含する。いくつかの態様において、アレルギーは、食物アレルギーである。
いくつかの態様において、本明細書に記載の組成物および方法は、IgE媒介食物アレルギーを処置するために使用される。いくつかの態様において、本明細書に記載の組成物および方法は、IgE媒介食物アレルギーに関連する免疫応答を調節するために使用される。いくつかの態様において、本明細書に記載の組成物および方法は、IgE媒介食物アレルギーに対する免疫寛容または減感作を誘導するために使用される。本明細書に記載の組成物および方法は、非IgE培地媒介食物アレルギーおよび/または混合または結合性IgE媒介/非IgE媒介食物アレルギーの文脈においてもまた使用されるであろう。
食物アレルギーが生じるであろうアレルゲンを含有する食物の非限定例は、アワビ(abalone)(アワビ(perlemoen))、アセロラ、スケトウダラ、アーモンド、アニスの実、リンゴ、アンズ、アボカド、バナナ、大麦、ピーマン、ブラジルナッツ、ソバ、キャベツ、コイ、ニンジン、カシュー、トウゴマの実(caster bean)、セロリ、根セロリ、サクランボ、クリの実、ヒヨコマメ(ガルバンゾー、ベンガルグラム)、ココア(cococa)、ココナツ、タラ、綿の実、ズッキーニ(courgett)、カニ、ナツメヤシの実、タマゴ、イチジク、魚、亜麻仁(linseed)、カエル、栽培種のセイヨウスモモ、ニンニク、ブドウ、ヘーゼルナッツ、キウイフルーツ(kiwi fruit)(キウイフルーツ(Chinese gooseberry))、レンズマメ、レタス、ロブスター、ハウチワマメ(lupin)(ハウチワマメ(lupine))、レイシ、サバ、トウモロコシ(maize)(トウモロコシ(corn))、マンゴー、メロン、ミルク、カラシ、オート麦(oat)、カキ(oyster)、モモ、落花生(peanut)(落花生(ground nuts)、落花生(money nuts))、セイヨウナシ、ペカン、カキ、松の実、パイナップル、ザクロの実、芥子粒、ジャガイモ、カボチャ、コメ、ライムギ、サケ、ゴマ、ゴマ種子、エビ(ブラックタイガーエビ、ブラウンシュリンプ、ヨシエビ、インドエビ、サケエビ、ホワイトシュリンプ)、カタツムリ、大豆(soybean)(大豆(soya))、イカ、イチゴ、ヒマワリの種、トマト、マグロ、カブ、クルミ、および小麦(パン小麦、パスタ小麦、カムート、スペルト)を包含する。
いくつかの態様において、本明細書に記載の組成物および方法は、IgE抗体の増強されたレベルに関連する疾患または障害を処置するために使用される。IgE抗体の増強されたレベルに関連するであろう疾患または障害の例は、限定せずに、高IgE(ヨブ)症候群、IgE骨髄腫、リンパ増殖性障害、セザリー症候群、木村病、寄生虫疾患、HIV感染、血管炎、全身性紅斑性狼瘡、および若年性全身性紅斑性狼瘡を包含する。
本明細書に記載の方法のいずれかは、対象におけるアレルギーの処置のためのものであるだろう。本明細書に使用されるとき、アレルギーを処置する方法は、アレルギーに関連する少なくとも1の兆候を緩和することまたは軽減すること、またはアレルゲンへの接触または曝露の際のアレルギー反応の発生を遅らせることまたは予防することに関する。
いくつかの態様において、組成物は、2以上(例として、3または4)の細菌株を包含し、ここで2以上の細菌株は、配列番号10、配列番号11;配列番号13;および配列番号4から選択される核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含有する。いくつかの態様において、組成物は、4つの細菌株からなり、ここで4つの細菌株は、配列番号10、配列番号11;配列番号13;および配列番号4として表される核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含有する。
いくつかの態様において、本明細書に記載の組成物は、以下の細菌株の2以上(例として、3または4)を含有する:Clostridium indolis、Anaerostipes caccae、Lachnospiraceae bacterium、およびClostridium symbiosum。いくつかの態様において、本明細書に記載の組成物は、以下の細菌株からなる:Clostridium indolis、Anaerostipes caccae、Lachnospiraceae bacterium、およびClostridium symbiosum。
一側面において、精製された細菌株の16S rDNA配列は、細菌のゲノムデータベースにおける既知の細菌種/株の16S rDNA配列と比較され、本明細書に開示の細菌株に最も近い既知の関連細菌種を同定した。本明細書に開示の組成物の複数の細菌株が、同じ最も近い関連細菌種を有するであろうことを理解すべきである。
一側面において、本開示は、本明細書に記載の細菌株のいずれかを含む医薬組成物を提供する。いくつかの態様において、医薬組成物は、薬学的に許容し得る賦形剤を含む。いくつかの態様において、医薬組成物は、経口投与のために処方されている。いくつかの態様において、医薬組成物は、直腸投与のために処方されている。いくつかの態様において、医薬組成物は、腸への送達のために処方されている。いくつかの態様において、医薬組成物は、結腸への送達のために処方されている。
いくつかの態様において、医薬組成物は、胃腸管(例として、結腸)などの所望される部位への本開示の組成物の効率的な送達を可能にする追加の構成要素を包含してもよい。
いくつかの態様において、医薬組成物は、アレルギーの処置における利益を提供することに関連するアジュバンドを包含する。いくつかの態様において、医薬組成物は、経口免疫治療の、皮膚上免疫治療の、または舌下免疫治療の1以上の構成要素を包含する。
腸(例として、結腸)への送達を可能とするシステムの別の例は、胃の遠位部での細菌の発酵におけるガスの生成によって引き起こされる圧力の変化を利用することによって内容物が放出されるように、圧力変化によって結腸へと組成物を送達するシステムである。かかるシステムは、特に限定はされないが、そのより具体的な例としては、坐薬ベース中に内容物を分散し、および疎水性ポリマー(例えば、エチルセルロース)でコーティングされるカプセルである
本明細書に提供される組成物はまた、穴を通して(例として、鼻腔チューブ)または外科手術を通して送達することによって、腸などの特定の標的エリアへ送達され得る。加えて、特定のエリア(例として、盲腸または結腸)への送達のために処方される本明細書に提供される組成物は、チューブによって(例として、直接小腸内に)投与されてもよい。チューブなどの機械的な送達方法とpH特異的なコーティングなどの化学的な送達方法とを組み合わせることは、本明細書に提供される組成物の所望される標的エリア(例として、盲腸または結腸)への送達を可能とする。
いくつかの態様において、本明細書に記載の医薬組成物のいずれかは、経口免疫治療または舌下免疫治療と同時に対象に投与されてもよい。同時投与は、医薬組成物および特定された期間内に、好ましくは1月以内に、より好ましくは1週間以内に、さらにより好ましくは1日以内に、およびなおさらにより好ましくは1時間以内での経口免疫治療または舌下での投与を網羅していてもよい。態様において、材料/剤は、同時に繰り返し投与されてもよい;それは2以上の場合での同時投与である。
いくつかの態様において、腸管前処置は、本明細書に記載の組成物のいずれかの投与に先立ち実施される。
いくつかの態様において、糞便試料は、本明細書に記載の組成物のいずれかの投与の後に、組成物の細菌株が、対象のマイクロバイオーム中に生着しているかを査定するために収集される。いくつかの態様において、糞便試料は、本明細書に記載の組成物のいずれかの投与の後に、対象のマイクロバイオームの構成を分析するために収集される。いくつかの態様において、糞便試料は、本明細書に記載の組成物のいずれかの投与の後に、対象のマイクロバイオームの構成を分析し、および組成物の細菌株が、対象のマイクロバイオーム中に生着しているかを査定するために収集される。
本明細書に記載の細菌株のいずれかを含有するよう処方されるだろう食品製品の例は、限定せずに、飲料、ドリンク、バー、スナック、乳製品、菓子製品、シリアル製品、加工製品、栄養補助食品処方などの栄養学上の処方、食物または飲料添加剤を包含する。
ATGAGAGTTTGATCCTGGCTCAGGATGAACGCTGGCGGCGTGCCTAACACATGCAAGTCGAACGAAGCAATTAAAATGAAGTTTTCGGATGGATTTTTGATTGACTGAGTGGCGGACGGGTGAGTAACGCGTGGATAACCTGCCTCACACTGGGGGATAACAGTTAGAAATGACTGCTAATACCGCATAAGCGCACAGTACCGCATGGTACGGTGTGAAAAACTCCGGTGGTGTGAGATGGATCCGCGTCTGATTAGCCAGTTGGCGGGGTAACGGCCCACCAAAGCGACGATCAGTAGCCGACCTGAGAGGGTGACCGGCCACATTGGGACTGAGACACGGCCCAAACTCCTACGGGAGGCAGCAGTGGGGAATATTGCACAATGGGCGAAAGCCTGATGCAGCGACGCCGCGTGAGTGAAGAAGTATTTCGGTATGTAAAGCTCTATCAGCAGGGAAGAAAATGACGGTACCTGACTAAGAAGCCCCGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGGGGCAAGCGTTATCCGGATTTACTGGGTGTAAAGGGAGCGTAGACGGCGAAGCAAGTCTGAAGTGAAAACCCAGGGCTCAACCCTGGGACTGCTTTGGAAACTGTTTTGCTAGAGTGTCGGAGAGGTAAGTGGAATTCCTAGTGTAGCGGTGAAATGCGTAGATATTAGGAGGAACACCAGTGGCGAAGGCGGCTTACTGGACGATAACTGACGTTGAGGCTCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGATGAATGCTAGGTGTTGGGGGGCAAAGCCCTTCGGTGCCGTCGCAAACGCAGTAAGCATTCCACCTGGGGAGTACGTTCGCAAGAATGAAACTCAAAGGAATTGACGGGGACCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCAAGTCTTGACATCCTCTTGACCGGCGTGTAACGGCGCCTTCCCTTCGGGGCAAGAGAGACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTATCCTTAGTAGCCAGCAGGTAAAGCTGGGCACTCTAGGGAGACTGCCAGGGATAACCTGGAGGAAGGTGGGGATGACGTCAAATCATCATGCCCCTTATGATTTGGGCTACACACGTGCTACAATGGCGTAAACAAAGGGAAGCAAGACAGTGATGTGGAGCAAATCCCAAAAATAACGTCCCAGTTCGGACTGTAGTCTGCAACCCGACTACACGAAGCTGGAATCGCTAGTAATCGCGAATCAGAATGTCGCGGTGAATACGTTCCCGGGTCTTGTACACACCGCCCGTCACACCATGGGAGTCAGCAACGCCCGAAGTCAGTGACCCAACTCGCAAGAGAGGGAGCTGCCGAAGGCGGGGCAGGTAACTGGGGTGAAGTCGTAACAAGGTAGCCGTATCGGAAGGTGCGGCTGGATCACCTCCTTT
TCAAAGAGTTTGATCCTGGCTCAGGACGAACGCTGGCGGCGCGCCTAACACATGCAAGTCGAACGGAGCTTACGTTTTGAAGTTTTCGGATGGATGAATGTAAGCTTAGTGGCGGACGGGTGAGTAACACGTGAGCAACCTGCCTTTCAGAGGGGGATAACAGCCGGAAACGGCTGCTAATACCGCATGATGTTGCGGGGGCACATGCCCCTGCAACCAAAGGAGCAATCCGCTGAAAGATGGGCTCGCGTCCGATTAGCCAGTTGGCGGGGTAACGGCCCACCAAAGCGACGATCGGTAGCCGGACTGAGAGGTTGAACGGCCACATTGGGACTGAGACACGGCCCAGACTCCTACGGGAGGCAGCAGTGGGGGATATTGCACAATGGGCGAAAGCCTGATGCAGCGACGCCGCGTGAGGGAAGACGGTCTTCGGATTGTAAACCTCTGTCTTTGGGGAAGAAAATGACGGTACCCAAAGAGGAAGCTCCGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGGAGCAAGCGTTGTCCGGAATTACTGGGTGTAAAGGGAGCGTAGGCGGGATGGCAAGTAGAATGTTAAATCCATCGGCTCAACCGGTGGCTGCGTTCTAAACTGCCGTTCTTGAGTGAAGTAGAGGCAGGCGGAATTCCTAGTGTAGCGGTGAAATGCGTAGATATTAGGAGGAACACCAGTGGCGAAGGCGGCCTGCTGGGCTTTAACTGACGCTGAGGCTCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGATGATTACTAGGTGTGGGGGGACTGACCCCTTCCGTGCCGCAGTTAACACAATAAGTAATCCACCTGGGGAGTACGGCCGCAAGGTTGAAACTCAAAGGAATTGACGGGGGCCCGCACAAGCAGTGGAGTATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCAGGTCTTGACATCGGATGCATAGCCTAGAGATAGGTGAAGCCCTTCGGGGCATCCAGACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTATTATTAGTTGCTACGCAAGAGCACTCTAATGAGACTGCCGTTGACAAAACGGAGGAAGGTGGGGATGACGTCAAATCATCATGCCCCTTATGACCTGGGCTACACACGTACTACAATGGCACTAAAACAGAGGGCGGCGACACCGCGAGGTGAAGCGAATCCCGAAAAAGTGTCTCAGTTCAGATTGCAGGCTGCAACCCGCCTGCATGAAGTCGGAATTGCTAGTAATCGCGGATCAGCATGCCGCGGTGAATACGTTCCCGGGCCTTGTACACACCGCCCGTCACACCATGGGAGTCGGTAACACCCGAAGCCAGTAGCCTAACCGCAAGGGGGGCGCTGTCGAAGGTGGGATTGATGACTGGGGTGAAGTCGTAACAAGGTAGCCGTATCGGAAGGTGCGGCTGGATCACCTCCTTT
TACGAGAGTTTGATCCTGGCTCAGGATGAACGCTGGCGGCGTGCCTAACACATGCAAGTCGAGCGAAGCGCTGTTTTCAGAATCTTCGGAGGAAGAGGACAGTGACTGAGCGGCGGACGGGTGAGTAACGCGTGGGCAACCTGCCTCATACAGGGGGATAACAGTTAGAAATGACTGCTAATACCGCATAAGCGCACAGGACCGCATGGTGTAGTGTGAAAAACTCCGGTGGTATGAGATGGACCCGCGTCTGATTAGGTAGTTGGTGGGGTAAAGGCCTACCAAGCCGACGATCAGTAGCCGACCTGAGAGGGTGACCGGCCACATTGGGACTGAGACACGGCCCAAACTCCTACGGGAGGCAGCAGTGGGGAATATTGCACAATGGGGGAAACCCTGATGCAGCGACGCCGCGTGAAGGAAGAAGTATTTCGGTATGTAAACTTCTATCAGCAGGGAAGAAAATGACGGTACCTGAGTAAGAAGCACCGGCTAAATACGTGCCAGCAGCCGCGGTAATACGTATGGTGCAAGCGTTATCCGGATTTACTGGGTGTAAAGGGAGCGTAGACGGATAGGCAAGTCTGGAGTGAAAACCCAGGGCTCAACCCTGGGACTGCTTTGGAAACTGCAGATCTGGAGTGCCGGAGAGGTAAGCGGAATTCCTAGTGTAGCGGTGAAATGCGTAGATATTAGGAGGAACACCAGTGGCGAAGGCGGCTTACTGGACGGTGACTGACGTTGAGGCTCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGATGACTACTAGGTGTCGGTGTGCAAAGCACATCGGTGCCGCAGCAAACGCAATAAGTAGTCCACCTGGGGAGTACGTTCGCAAGAATGAAACTCAAAGGAATTGACGGGGACCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCTGGTCTTGACATCCGGATGACGGGCGAGTAATGTCGCCGTCCCTTCGGGGCGTCCGAGACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTATCTTCAGTAGCCAGCATATAAGGTGGGCACTCTGGAGAGACTGCCAGGGAGAACCTGGAGGAAGGTGGGGATGACGTCAAATCATCATGCCCCTTATGGCCAGGGCTACACACGTGCTACAATGGCGTAAACAAAGGGAAGCGAGAGGGTGACCTGGAGCGAATCCCAAAAATAACGTCTCAGTTCGGATTGTAGTCTGCAACTCGACTACATGAAGCTGGAATCGCTAGTAATCGCGGATCAGCATGCCGCGGTGAATACGTTCCCGGGTCTTGTACACACCGCCCGTCACACCATGGGAGTCAGTAACGCCCGAAGCCAGTGACCCAACCTTAGAGGAGGGAGCTGTCGAAGGCGGGACGGATAACTGGGGTGAAGTCGTAACAAGGTAGCCGTATCGGAAGGTGCGGCTGGATCACCTCCTTT
ATGAGAGTTTGATCCTGGCTCAGGATGAACGCTGGCGGCGTGCCTAACACATGCAAGTCGAACGAAGCGATTTAACGGAAGTTTTCGGATGGAAGTTGAATTGACTGAGTGGCGGACGGGTGAGTAACGCGTGGGTAACCTGCCTTGTACTGGGGGACAACAGTTAGAAATGACTGCTAATACCGCATAAGCGCACAGTATCGCATGATACAGTGTGAAAAACTCCGGTGGTACAAGATGGACCCGCGTCTGATTAGCTAGTTGGTAAGGTAACGGCTTACCAAGGCGACGATCAGTAGCCGACCTGAGAGGGTGACCGGCCACATTGGGACTGAGACACGGCCCAAACTCCTACGGGAGGCAGCAGTGGGGAATATTGCACAATGGGCGAAAGCCTGATGCAGCGACGCCGCGTGAGTGAAGAAGTATTTCGGTATGTAAAGCTCTATCAGCAGGGAAGAAAATGACGGTACCTGACTAAGAAGCCCCGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGGGGCAAGCGTTATCCGGATTTACTGGGTGTAAAGGGAGCGTAGACGGTAAAGCAAGTCTGAAGTGAAAGCCCGCGGCTCAACTGCGGGACTGCTTTGGAAACTGTTTAACTGGAGTGTCGGAGAGGTAAGTGGAATTCCTAGTGTAGCGGTGAAATGCGTAGATATTAGGAGGAACACCAGTGGCGAAGGCGACTTACTGGACGATAACTGACGTTGAGGCTCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGATGAATACTAGGTGTTGGGGAGCAAAGCTCTTCGGTGCCGTCGCAAACGCAGTAAGTATTCCACCTGGGGAGTACGTTCGCAAGAATGAAACTCAAAGGAATTGACGGGGACCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCAGGTCTTGACATCGATCCGACGGGGGAGTAACGTCCCCTTCCCTTCGGGGCGGAGAAGACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTATTCTAAGTAGCCAGCGGTTCGGCCGGGAACTCTTGGGAGACTGCCAGGGATAACCTGGAGGAAGGTGGGGATGACGTCAAATCATCATGCCCCTTATGATCTGGGCTACACACGTGCTACAATGGCGTAAACAAAGAGAAGCAAGACCGCGAGGTGGAGCAAATCTCAAAAATAACGTCTCAGTTCGGACTGCAGGCTGCAACTCGCCTGCACGAAGCTGGAATCGCTAGTAATCGCGAATCAGAATGTCGCGGTGAATACGTTCCCGGGTCTTGTACACACCGCCCGTCACACCATGGGAGTCAGTAACGCCCGAAGTCAGTGACCCAACCGCAAGGAGGGAGCTGCCGAAGGCGGGACCGATAACTGGGGTGAAGTCGTAACAAGGTAGCCGTATCGGAAGGTGCGGCTGGATCACCTCCTTT
ATCAGAGAGTTTGATCCTGGCTCAGGATGAACGCTGGCGGCGTGCTTAACACATGCAAGTCGAGCGAAGCACTTAAGTGGATCTCTTCGGATTGAAGCTTATTTGACTGAGCGGCGGACGGGTGAGTAACGCGTGGGTAACCTGCCTCATACAGGGGGATAACAGTTAGAAATGGCTGCTAATACCGCATAAGCGCACAGGACCGCATGGTCTGGTGTGAAAAACTCCGGTGGTATGAGATGGACCCGCGTCTGATTAGCTAGTTGGAGGGGTAACGGCCCACCAAGGCGACGATCAGTAGCCGGCCTGAGAGGGTGAACGGCCACATTGGGACTGAGACACGGCCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGCACAATGGGGGAAACCCTGATGCAGCGACGCCGCGTGAAGGAAGAAGTATCTCGGTATGTAAACTTCTATCAGCAGGGAAGAAAATGACGGTACCTGACTAAGAAGCCCCGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGGGGCAAGCGTTATCCGGATTTACTGGGTGTAAAGGGAGCGTAGACGGAAGAGCAAGTCTGATGTGAAAGGCTGGGGCTTAACCCCAGGACTGCATTGGAAACTGTTTTTCTAGAGTGCCGGAGAGGTAAGCGGAATTCCTAGTGTAGCGGTGAAATGCGTAGATATTAGGAGGAACACCAGTGGCGAAGGCGGCTTACTGGACGGTAACTGACGTTGAGGCTCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGATGAATACTAGGTGTCGGGTGGCAAAGCCATTCGGTGCCGCAGCAAACGCAATAAGTATTCCACCTGGGGAGTACGTTCGCAAGAATGAAACTCAAAGGAATTGACGGGGACCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCAAGTCTTGACATCCCTCTGACCGGCCCGTAACGGGGCCTTCCCTTCGGGGCAGAGGAGACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCCTATCCTTAGTAGCCAGCAGGTGAAGCTGGGCACTCTAGGGAGACTGCCGGGGATAACCCGGAGGAAGGCGGGGACGACGTCAAATCATCATGCCCCTTATGATTTGGGCTACACACGTGCTACAATGGCGTAAACAAAGGGAAGCGAGACAGCGATGTTGAGCAAATCCCAAAAATAACGTCCCAGTTCGGACTGCAGTCTGCAACTCGACTGCACGAAGCTGGAATCGCTAGTAATCGCGAATCAGAATGTCGCGGTGAATACGTTCCCGGGTCTTGTACACACCGCCCGTCACACCATGGGAGTCAGTAACGCCCGAAGTCAGTGACCCAACCTTACAGGAGGGAGCTGCCGAAGGCGGGACCGATAACTGGGGTGAAGTCGTAACAAGGTAGCCGTATCGGAAGGTGCGGCTGGATCACCTCCTTT
AACGAGAGTTTGATCCTGGCTCAGGATGAACGCTGGCGGCGTGCTTAACACATGCAAGTCGAGCGAAGCACTTAAGTTTGATTCTTCGGATGAAGACTTTTGTGACTGAGCGGCGGACGGGTGAGTAACGCGTGGGTAACCTGCCTCATACAGGGGGATAACAGTTAGAAATGACTGCTAATACCGCATAAGACCACGGTACCGCATGGTACAGTGGTAAAAACTCCGGTGGTATGAGATGGACCCGCGTCTGATTAGGTAGTTGGTGGGGTAACGGCCTACCAAGCCGACGATCAGTAGCCGACCTGAGAGGGTGACCGGCCACATTGGGACTGAGACACGGCCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGCACAATGGAGGAAACTCTGATGCAGCGACGCCGCGTGAAGGATGAAGTATTTCGGTATGTAAACTTCTATCAGCAGGGAAGAAAATGACGGTACCTGACTAAGAAGCCCCGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGGGGCAAGCGTTATCCGGATTTACTGGGTGTAAAGGGAGCGTAGACGGCACGGCAAGCCAGATGTGAAAGCCCGGGGCTCAACCCCGGGACTGCATTTGGAACTGCTGAGCTAGAGTGTCGGAGAGGCAAGTGGAATTCCTAGTGTAGCGGTGAAATGCGTAGATATTAGGAGGAACACCAGTGGCGAAGGCGGCTTGCTGGACGATGACTGACGTTGAGGCTCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGATGACTGCTAGGTGTCGGGTGGCAAAGCCATTCGGTGCCGCAGCTAACGCAATAAGCAGTCCACCTGGGGAGTACGTTCGCAAGAATGAAACTCAAAGGAATTGACGGGGACCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCTGATCTTGACATCCCGATGACCGCTTCGTAATGGAAGCTTTTCTTCGGAACATCGGTGACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCCTATCTTCAGTAGCCAGCAGGTTAAGCTGGGCACTCTGGAGAGACTGCCAGGGATAACCTGGAGGAAGGTGGGGATGACGTCAAATCATCATGCCCCTTATGACCAGGGCTACACACGTGCTACAATGGCGTAAACAAAGAGAAGCGAACTCGCGAGGGTAAGCAAATCTCAAAAATAACGTCTCAGTTCGGATTGTAGTCTGCAACTCGACTACATGAAGCTGGAATCGCTAGTAATCGCAGATCAGAATGCTGCGGTGAATACGTTCCCGGGTCTTGTACACACCGCCCGTCACACCATGGGAGTCAGTAACGCCCGAAGTCAGTGACCCAACCGTAAGGAGGGAGCTGCCGAAGGTGGGACCGATAACTGGGGTGAAGTCGTAACAAGGTAGCCGTATCGGAAGGTGCGGCTGGATCACCTCCTTT
ATGGAGAGTTTGATCCTGGCTCAGGATGAACGCTGGCGGCATGCCTAATACATGCAAGTCGAACGAAGTTTCGAGGAAGCTTGCTTCCAAAGAGACTTAGTGGCGAACGGGTGAGTAACACGTAGGTAACCTGCCCATGTGTCCGGGATAACTGCTGGAAACGGTAGCTAAAACCGGATAGGTATACAGAGCGCATGCTCAGTATATTAAAGCGCCCATCAAGGCGTGAACATGGATGGACCTGCGGCGCATTAGCTAGTTGGTGAGGTAACGGCCCACCAAGGCGATGATGCGTAGCCGGCCTGAGAGGGTAAACGGCCACATTGGGACTGAGACACGGCCCAAACTCCTACGGGAGGCAGCAGTAGGGAATTTTCGTCAATGGGGGAAACCCTGAACGAGCAATGCCGCGTGAGTGAAGAAGGTCTTCGGATCGTAAAGCTCTGTTGTAAGTGAAGAACGGCTCATAGAGGAAATGCTATGGGAGTGACGGTAGCTTACCAGAAAGCCACGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGTGGCAAGCGTTATCCGGAATCATTGGGCGTAAAGGGTGCGTAGGTGGCGTACTAAGTCTGTAGTAAAAGGCAATGGCTCAACCATTGTAAGCTATGGAAACTGGTATGCTGGAGTGCAGAAGAGGGCGATGGAATTCCATGTGTAGCGGTAAAATGCGTAGATATATGGAGGAACACCAGTGGCGAAGGCGGTCGCCTGGTCTGTAACTGACACTGAGGCACGAAAGCGTGGGGAGCAAATAGGATTAGATACCCTAGTAGTCCACGCCGTAAACGATGAGAACTAAGTGTTGGAGGAATTCAGTGCTGCAGTTAACGCAATAAGTTCTCCGCCTGGGGAGTATGCACGCAAGTGTGAAACTCAAAGGAATTGACGGGGGCCCGCACAAGCGGTGGAGTATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCAGGCCTTGACATGGAAACAAATACCCTAGAGATAGGGGGATAATTATGGATCACACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTGTCGCATGTTACCAGCATCAAGTTGGGGACTCATGCGAGACTGCCGGTGACAAACCGGAGGAAGGTGGGGATGACGTCAAATCATCATGCCCCTTATGGCCTGGGCTACACACGTACTACAATGGCGGCCACAAAGAGCAGCGACACAGTGATGTGAAGCGAATCTCATAAAGGTCGTCTCAGTTCGGATTGAAGTCTGCAACTCGACTTCATGAAGTCGGAATCGCTAGTAATCGCAGATCAGCATGCTGCGGTGAATACGTTCTCGGGCCTTGTACACACCGCCCGTCAAACCATGGGAGTCAGTAATACCCGAAGCCGGTGGCATAACCGTAAGGAGTGAGCCGTCGAAGGTAGGACCGATGACTGGGGTTAAGTCGTAACAAGGTATCCCTACGGGAACGTGGGGATGGATCACCTCCTTT
TATTGAGAGTTTGATCCTGGCTCAGGATGAACGCTGGCGGCGTGCTTAACACATGCAAGTCGAACGGGGTGCTCATGACGGAGGATTCGTCCAACGGATTGAGTTACCTAGTGGCGGACGGGTGAGTAACGCGTGAGGAACCTGCCTTGGAGAGGGGAATAACACTCCGAAAGGAGTGCTAATACCGCATGATGCAGTTGGGTCGCATGGCTCTGACTGCCAAAGATTTATCGCTCTGAGATGGCCTCGCGTCTGATTAGCTAGTAGGCGGGGTAACGGCCCACCTAGGCGACGATCAGTAGCCGGACTGAGAGGTTGACCGGCCACATTGGGACTGAGACACGGCCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGGGCAATGGGCGCAAGCCTGACCCAGCAACGCCGCGTGAAGGAAGAAGGCTTTCGGGTTGTAAACTTCTTTTGTCGGGGACGAAACAAATGACGGTACCCGACGAATAAGCCACGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGTGGCAAGCGTTATCCGGATTTACTGGGTGTAAAGGGCGTGTAGGCGGGATTGCAAGTCAGATGTGAAAACTGGGGGCTCAACCTCCAGCCTGCATTTGAAACTGTAGTTCTTGAGTGCTGGAGAGGCAATCGGAATTCCGTGTGTAGCGGTGAAATGCGTAGATATACGGAGGAACACCAGTGGCGAAGGCGGATTGCTGGACAGTAACTGACGCTGAGGCGCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGATGGATACTAGGTGTGGGGGGTCTGACCCCCTCCGTGCCGCAGTTAACACAATAAGTATCCCACCTGGGGAGTACGATCGCAAGGTTGAAACTCAAAGGAATTGACGGGGGCCCGCACAAGCGGTGGAGTATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCAGGGCTTGACATCCCACTAACGAAGCAGAGATGCATTAGGTGCCCTTCGGGGAAAGTGGAGACAGGTGGTGCATGGTTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTATTGTTAGTTGCTACGCAAGAGCACTCTAGCGAGACTGCCGTTGACAAAACGGAGGAAGGTGGGGACGACGTCAAATCATCATGCCCCTTATGTCCTGGGCCACACACGTACTACAATGGTGGTTAACAGAGGGAGGCAATACCGCGAGGTGGAGCAAATCCCTAAAAGCCATCCCAGTTCGGATTGCAGGCTGAAACCCGCCTGTATGAAGTTGGAATCGCTAGTAATCGCGGATCAGCATGCCGCGGTGAATACGTTCCCGGGCCTTGTACACACCGCCCGTCACACCATGAGAGTCGGGAACACCCGAAGTCCGTAGCCTAACCGCAAGGAGGGCGCGGCCGAAGGTGGGTTCGATAATTGGGGTGAAGTCGTAACAAGGTAGCCGTATCGGAAGGTGCGGCTGGATCACCTCCTTT
GATGAACGCTGGCGGCGGTGCTTAACACATGCAAGTCGAGCGAAGCGGTTTCGAGTGAAGTTTTGGATGGAATTGAAATTGACTTAGCGGCGGACGGGTGAGTAACGCGTGGGTAACCTGCCTTACACTGGGGGATAACAGTTAGAAATGACTGCTAATACCGCATAAGCGCACAGGGCCGCATGGTCTGGTGCGAAAAACTCCGGTGGTGTAAGATGGACCCGCGTCTGATTAGGTAGTTGGTGGGGTAACGGCCCACCAAGCCGACGATCAGTAGCCGACCTGAGAGGGTGACCGGCCACATTGGGACTGAGACACGGCCCAA
配列番号10 株10 VE202-9 Clostridium indolis/Anaerostipes caccae
GATGAACGCTGGCGGCGTGCTTAACACATGCAAGTCGAACGAAGCATTTTGGAAGGAAGTTTTCGGATGGAATTCCTTAATGACTGAGTGGCGGACGGGTGAGTAACGCGTGGGGAACCTGCCCTATACAGGGGGATAACAGCTGGAAACGGCTGCTAATACCGCATAAGCGCACAGAATCGCATGATTCGGTGTGAAAAGCTCCGGCAGTATAGGATGGTCCCGCGTCTGATTAGCTGGTTGGCGGGGTAACGGCCCACCAAGGCGACGATCAGTAGCCGGCTTGAGAGAGTGGACGGCCACATTGGGACTGAGACACGGCCCA
配列番号11 株11 VE202-27 Lachnospiraceae bacterium
GATGAACGCTGGCGGCGTGCCTAACACATGCAAGTCGAACGGAGTTATGCAGAGGAAGTTTTCGGATGGAATCGGCGTAACTTAGTGGCGGACGGGTGAGTAACGCGTGGGAAACCTGCCCTGTACCGGGGGATAACACTTAGAAATAGGTGCTAATACCGCATAAGCGCACAGCTTCACATGAAGCAGTGTGAAAAACTCCGGTGGTACAGGATGGTCCCGCGTCTGATTAGCCAGTTGGCAGGGTAACGGCCTACCAAAGCGACGATCAGTAGCCGGCCTGAGAGGGTGAACGGCCACATTGGGACTGAGACACGGCCCA
GATGAACGCTGGCGGCGTGCCTAACACATGCAAGTCGAACGAAGCATCCCATAGGAAGTTTTCGGATGGAATATGGGATGACTGAGTGGCGGACGGGTGAGTAACGCGTGGATAACCTGCCTCACACTGGGGGATAACAGTTAGAAATGGCTGCTAATACCGCATAAGCGCACAGTACCGCATGGTACGGTGTGAAAAACCCAGGTGGTGTGAGATGGATCCGCGTCTGATTAGCCAGTTGGCGGGGTAACGGCCCACCAAAGCGACGATCAGTAGCCGACCTGAGAGGGTGACCGGCCACATTGGGGACTGAGACACGGCCCA
配列番号13 株13 VE202-29 Lachnospiraceae bacterium
GATGAACGCTGGCGGCGTGCCTAACACATGCAAGTCGAACGAAGTTAGACAGAGGAAGTTTTCGGATGGAATCGGTATAACTTAGTGGCGGACGGGTGAGTAACGCGTGGGAAACCTGCCCTGTACCGGGGGATAACACTTAGAAATAGGTGCTAATACCGCATAAGCGCACGGAACCGCATGGGTTCTGTGTGAAAACTCCGGTGGTACAGGATGGTCCCGCGTCTGATTAGCCAGTTGGCAGGGTAACGGCCTACCAAAGCGACGATCAGTAGCCGGCCTGAGAGGGTGAACGGCCACATTGGGACTGAGACACGGCCCAA
例1:組成物Bは、制御性T細胞(Treg)を誘導する
組成物Bの細菌株の各々を、対数期に増殖させ、1つに合わせ1マウス当たり約108cfuの全用量とした。無菌マウスに組成物Bまたは陰性対照を経口の強制飼養によって接種し、および4週間のコロニー形成に続いて屠殺した。粘膜固有層の白血球を、標準的な手順により個々のマウスの結腸組織から単離し、およびフローサイトメトリーにより査定した。制御性T細胞の含量を、CD4+T細胞の中のFoxp3-陽性細胞のパーセンテージとして評価した。
図1に示されるとおり、組成物Bを接種したマウスは、対照を接種したマウスと比較して、有意に多い制御性T細胞を有することが見出された。
例1に記載されるように、無菌マウスに試験のコンソーシアを接種した。マウスを屠殺した時点での全血を血清チューブ内に収集し、およびさらなる分析を実施するまで凍結した。続いて血清を解凍し、1:25で希釈し、および血清中の全IgEを標準的なELISA法を使用して測定した。
図2に示されるとおり、対照の無菌(GF)マウスは、正常な片利共生微生物叢を有する特定病原体除去(SPF)マウスと比較して、上昇した血清IgEレベルを有した。組成物Bを伴うコロニー形成は、血清IgEレベルを低減し、組成物が、接種された無菌マウスにおけるTh2型炎症反応を抑制することを指し示した。
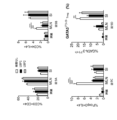
表2および3に示されるとおり、組成物Bからの選択される細菌株を選択し、組成物CおよびDを形成した。細菌株の各々を増殖し、指し示される組み合わせに1つに合わせ、および経口の強制飼養によって無菌マウスに接種するために使用した。マウスを屠殺し、および粘膜固有層の白血球を単離し、および例1のように査定した。屠殺の時点での全血を血清チューブ内に収集し、およびさらなる分析を実施するまで凍結した。
血清試料を続いて解凍し、希釈し、および血清中の全IgEを、標準的なELISA法を使用して測定した。図4に示されるとおり、対照の無菌(GF)マウスは、正常な片利共生微生物叢を有する特定病原体除去(SPF)マウスと比較して、上昇した血清IgEレベルを有した。組成物B、C、およびDの各々を伴うコロニー形成は、血清IgEレベルを低減させ、組成物が、接種された無菌マウスにおけるTh2型炎症反応を抑制することを指し示した。
制御性T細胞の誘導およびブチラートの産生の両方が、調節性のクロストリジウムが炎症を抑制するであろう機序に提案されている(例として、Atarashi et al. (2013);Stefka et al (2014)を参照されたい)。これらの潜在的な機序を分離するために、細菌のコンソーシアを、(1)Treg誘導活性はほとんどなく、主としてブチラート産生するもの、または(2)ブチラートの産生はなく、高くTregを誘導するもの、で同定した。これらのコンソーシアを、実験用食物アレルギーからの保護におけるそれらの有効性について評価した。
細菌株についてのTreg誘導(TrIS)の量に、数理モデルによって予測されるスコアを与えた。高い、中間の、および低いレベルのTregを誘導すると予測される細菌のコンソーシアを、実験的検証のために選択した。
簡潔に言うと、無菌のC57BL/6マウス(5~6週齢)に、1マウス当たり>=108CFUの用量で細菌組成物を1回経口的に強制飼養した。コロニー形成を、4週間にわたってモニターした。4周目に、マウスを屠殺し、および粘膜固有層の白血球を結腸から単離した。LBP1およびLBP2と称される例の細菌組成物における細菌株を、夫々表4および5に提示する。
図5に示されるとおり、TregをFoxp3-陽性CD4+T細胞として定量した。予測されるように、LBP2の投与は、より高いレベルのTreg誘導をもたらし、LBP1の投与は、より低いレベルのTreg誘導をもたらした。
細菌組成物による短鎖脂肪酸(SCFA)の産生を、Narushima et al. Gut Microbes (2014) 5(3): 333-339に記載されるように査定した。簡潔に言うと、個々の株を、O.D.>0.3まで増殖させ、上清を採取し、およびコロニー形成単位(CFU)のカウントを各株について決定した。上清を、7の短鎖脂肪酸の標的化されたメタボロームのプロファイリングに送り、および結果をCFUに対して正規化した。図6Aおよび6Bは、組成物の個々の株によるブチラートの産生に基づく、LBP1およびLBP2によって産生されるブチラートおよびアセタートの予測されるレベルを示す。LBP1は、高いレベルのブチラートおよび低いレベルのアセタートを産生すると予測され、一方でLBP2は、低いレベルのブチラートおよび高いレベルのアセタートを産生すると予測された。
SCFAの産生もまた、LBP1またはLBP2を接種したマウスからの糞便試料においてin vivoで査定された。糞便試料を、コロニー形成後第3日目、第7日目、第14日目、および第28日目に収集した。予測されるように、LBP1の接種は、糞便試料においてより高いレベルのブチラートおよびより低いレベルのアセタートをもたらした;およびLBP2の接種は、より低いレベルのブチラートおよびより高いレベルのアセタートをもたらした(図6Cおよび6D)。
細菌組成物を、例えば、Mathias et al. JACI (2011) 127(3): 795-805に記載されるように、食物アレルギーのマウスモデルにおいて評価した。簡潔に言うと、Balb/c背景上のIL4raF709マウスは、IL4Rシグナリングに過敏反応性を有し、および食物アレルギーのためのモデルとして使用されるであろう。これらのマウスは、食物アレルゲンの感作に応じて遺伝子学的にアナフィラキシーを起こしやすい。図7に示されるとおり、マウスを抗生物質で前処置し、生着のためのニッチを作り出し、これに続き8週間OVA(オボアルブミン)+SEB(ブドウ球菌エンテロトキシンB)で感作し、および細菌組成物を接種した。マウスを、次いでOVAで抗原投与し、および評価した。
肥満細胞およびIgE応答もまた、食物アレルギーからの保護の測定として評価した。図10A~10Dに示されるとおり、LBP1またはLBP2を接種されたマウスは、mMCP-1の低減したレベル、肥満細胞の低減した数、および低減した肥満細胞およびB細胞IgEを有すると見出された。要するに、LBP1およびLBP2は、アレルギー関連T細胞および顆粒球の応答における低減を伴って、食物アレルギーに対する保護を誘導すると見出された。
LBP1およびLBP2、組成物B、C、およびDを使用して観察された結果に基づき、SCFAの産生、Treg誘導、および食物アレルギーからの保護についてもまた評価した。
上に記載のとおり、組成物B、C、およびDからの細菌株を、in vitroでブチラートおよびアセタートの産生について査定した。各組成物についてのブチラートおよびアセタートの産生のレベルを、個々の株の産生に基づき予測した。組成物B、C、およびDについて、LBP1と同様のレベルのブチラート産生を有すると予測した(図11Aおよび11B)。このことを組成物Bおよび組成物Cについてin vivoで確認した(図11Cおよび11D)。組成物B、C、およびDについて、LBP2よりも高いレベルのブチラート産生を有すると予測した(図12Aおよび12B)。このことを組成物Bおよび組成物Cについてin vivoで確認した(図12Cおよび12D)。
無菌マウスの細菌組成物の接種は、同様のレベルのTreg誘導をもたらした(図13)。IgEレベルは、組成物を接種した無菌マウス(図14)と同様の程度で低減することが見出された。
本明細書に記載の組成物のいずれかを接種したマウスから得られた試料はまた、IL-33、IL25、TSLP(例として、腸管内の転写産物)、TGFβ、IL-10のレベルについて評価してもよい。代替的に、または加えて、マウスについて組成物の1以上の株を包含する組成物の相対的なコロニー形成(例として、生着)を査定してもよい。マウスから得られた試料はまた、RNAseq、または他の発現分析の対象としてもよい。
食物アレルギーのための処置としての組成物CおよびBの有効性を評価した。細菌組成物CおよびBを、例えば、PCT公報WO2017/079450において記載されるような、食物アレルギーを処置するための「治癒的」マウスモデルにおいて評価した。簡潔に言うと、Balb/c背景上のIL4raF709マウスは、IL4Rシグナリングに過敏反応性を有し、および食物アレルギーのためのモデルとして使用されるであろう。これらのマウスは、遺伝子学的に食物アレルゲンの感作に応じてアナフィラキシーを起こしやすい。図19に示されるとおり、マウスを、OVA(オボアルブミン)+SEB(ブドウ球菌エンテロトキシンB)で8週間感作した。マウスに、次いで抗生物質で前処置し、生着のためのニッチを作り出し、細菌組成物の週2回の接種が4週間(全8回の接種)これに続いた。この期間中、マウスをOVA+SEBの投与で感作し続けた。マウスに次いでOVAで抗原投与し、および評価した。
本明細書の例1~3において使用されたものなどの無菌マウスは、常在微生物叢を欠き、および腸の制御性T細胞の相対的な欠乏および上昇したTh2型免疫応答を包含する、従来のマウスと比較して変更された免疫系を有する。組成物BおよびCが、無菌マウスにおいて制御性T細胞の応答を優先的に誘導することを示し、次いでこれらの細菌組成物が、常在微生物叢および正常な免疫系を所有するマウスにおいて免疫調節性の効果を誘導することができるかどうかを調査した。抗生物質での前処置が、組成物BおよびCの種の生着を容易にするためのニッチを作り出すために、およびそれらが腸管免疫を調節することを可能とするために必要であるかどうか、または細菌組成物が抗生物質の不在において効果を有し得るかどうかをさらに探求した。
Claims (38)
- 食物アレルギーに関連する免疫応答を低減または抑制する、食物アレルギーに対する免疫寛容または減感作を誘導する、または食物アレルギーを処置するための組成物であって、
(i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号6の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDorea longicatenaの精製された細菌株、
(vii)配列番号7の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium innocuumの精製された細菌株、および
(viii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株を含む、
前記組成物。 - (i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号6の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDorea longicatenaの精製された細菌株、
(vii)配列番号7の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium innocuumの精製された細菌株、および
(viii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株からなる、請求項1に記載の組成物。 - 食物アレルギーに関連する免疫応答を低減または抑制する、食物アレルギーに対する免疫寛容または減感作を誘導する、または食物アレルギーを処置するための組成物であって、
(i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号7の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium innocuumの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株を含む、
前記組成物。 - (i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号7の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium innocuumの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株からなる、請求項3に記載の組成物。 - 食物アレルギーに関連する免疫応答を低減または抑制する、食物アレルギーに対する免疫寛容または減感作を誘導する、または食物アレルギーを処置するための組成物であって、
(i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号6の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDorea longicatenaの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株を含む、
前記組成物。 - (i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号6の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDorea longicatenaの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株からなる、請求項5に記載の組成物。 - IgE抗体の産生の抑制、制御性T細胞の増殖および/または蓄積の誘導、Th2免疫応答の抑制、食物アレルギーに関連する免疫応答の抑制、および/または、食物アレルギーに対する免疫寛容または減感作をもたらす、請求項1~6のいずれか一項に記載の組成物。
- 細菌株が、凍結乾燥または噴霧乾燥されている、請求項1~7のいずれか一項に記載の組成物。
- 細菌株の1以上が、芽胞形態にある、および/または、細菌株の1以上が、栄養形態にある、請求項1~8のいずれか一項に記載の組成物。
- 細菌株の各々が、芽胞形態にある、または、細菌株の各々が、栄養形態にある、請求項1~9のいずれか一項に記載の組成物。
- 経口的に投与される、請求項1~10のいずれか一項に記載の組成物。
- 経口送達、直腸送達、腸への送達、および/または結腸への送達のために処方されている、請求項1~11のいずれか一項に記載の組成物。
- カプセルの形態である、請求項1~12のいずれか一項に記載の組成物。
- 食物アレルギーが、ナッツアレルギー、魚アレルギー、小麦アレルギー、ミルクアレルギー、落花生アレルギー、木の実アレルギー、甲殻類アレルギー、大豆アレルギー、種子アレルギー、ゴマ種子アレルギー、およびタマゴアレルギーからなる群から選択される、請求項1~13のいずれか一項に記載の組成物。
- ヒトに投与される、請求項1~14のいずれか一項に記載の組成物。
- 1以上のアジュバントをさらに含む、請求項1~15のいずれか一項に記載の組成物。
- アジュバントが、アレルギー処置または免疫寛容に関連する、請求項16に記載の組成物。
- 1以上の腸溶性ポリマーをさらに含む、請求項1~17のいずれか一項に記載の組成物。
- 細菌株が、2以上のヒトドナー由来である、請求項1~18のいずれか一項に記載の組成物。
- 抗生物質の投与後に投与される、請求項1~19のいずれか一項に記載の組成物。
- 抗生物質が、バンコマイシンである、請求項20に記載の組成物。
- 5日間1日当たり125mgのバンコマイシンの4用量で投与される、請求項21に記載の組成物。
- (i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia producta、
(vi)配列番号7の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium innocuumの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株を含み、およびここで、配列番号6の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDorea longicatenaの精製された細菌株を含まない、組成物。 - (i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号7の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium innocuumの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株からなる、請求項23に記載の組成物。 - (i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号6の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDorea longicatenaの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株を含み、およびここで、配列番号7の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium innocuumの精製された細菌株を含まない、組成物。 - (i)配列番号1の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium bolteaeの精製された細菌株、
(ii)配列番号2の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むAnaerotruncus colihominisの精製された細菌株、
(iii)配列番号3の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDrancourtella massiliensisの精製された細菌株、
(iv)配列番号4の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むClostridium symbiosumの精製された細菌株、
(v)配列番号5の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むBlautia productaの精製された細菌株、
(vi)配列番号6の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むDorea longicatenaの精製された細菌株、および
(vii)配列番号8の核酸配列と少なくとも97%の配列同一性を有する16S rDNA配列を含むFlavonifractor plautiiの精製された細菌株からなる、請求項25に記載の組成物。 - 制御性T細胞の増殖および/または蓄積を誘導する、IgE抗体産生を抑制する、および/または、Th2免疫応答を抑制する、請求項23~26のいずれか一項に記載の組成物。
- 1以上のアジュバントをさらに含む、請求項23~27のいずれか一項に記載の組成物。
- アジュバントが、アレルギー処置または免疫寛容に関連する、請求項28に記載の組成物。
- 細菌株が、凍結乾燥または噴霧乾燥されている、請求項23~29のいずれか一項に記載の組成物。
- 細菌株の1以上が、芽胞形態にある、および/または、細菌株の1以上が、栄養形態にある、請求項23~30のいずれか一項に記載の組成物。
- 細菌株の各々が、芽胞形態にある、または、細菌株の各々が、栄養形態にある、請求項23~31のいずれか一項に記載の組成物。
- カプセルの形態である、請求項23~32のいずれか一項に記載の組成物。
- 1以上の腸溶性ポリマーをさらに含む、請求項23~33のいずれか一項に記載の組成物。
- 細菌株が、2以上のヒトドナー由来である、請求項23~34のいずれか一項に記載の組成物。
- 請求項23~35のいずれか一項に記載の組成物、および、薬学的に許容し得る賦形剤を含む、医薬組成物。
- 経口送達、直腸送達、腸への送達、および/または結腸への送達のために処方されている、請求項36に記載の医薬組成物。
- 請求項23~35のいずれか一項に記載の組成物および栄養素を含む、食品製品。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023093879A JP2023121755A (ja) | 2017-11-09 | 2023-06-07 | アレルギーの処置のための組成物および方法 |
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762583777P | 2017-11-09 | 2017-11-09 | |
| US62/583,777 | 2017-11-09 | ||
| US201862637355P | 2018-03-01 | 2018-03-01 | |
| US62/637,355 | 2018-03-01 | ||
| US201862721786P | 2018-08-23 | 2018-08-23 | |
| US62/721,786 | 2018-08-23 | ||
| PCT/US2018/060187 WO2019094837A1 (en) | 2017-11-09 | 2018-11-09 | Compositions and methods for the treatment of allergy |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023093879A Division JP2023121755A (ja) | 2017-11-09 | 2023-06-07 | アレルギーの処置のための組成物および方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2021502391A JP2021502391A (ja) | 2021-01-28 |
| JP2021502391A5 JP2021502391A5 (ja) | 2021-12-16 |
| JP7293220B2 true JP7293220B2 (ja) | 2023-06-19 |
Family
ID=66438676
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020526142A Active JP7293220B2 (ja) | 2017-11-09 | 2018-11-09 | アレルギーの処置のための組成物および方法 |
| JP2023093879A Pending JP2023121755A (ja) | 2017-11-09 | 2023-06-07 | アレルギーの処置のための組成物および方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023093879A Pending JP2023121755A (ja) | 2017-11-09 | 2023-06-07 | アレルギーの処置のための組成物および方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20220054556A1 (ja) |
| EP (1) | EP3706767A4 (ja) |
| JP (2) | JP7293220B2 (ja) |
| CN (1) | CN111526882A (ja) |
| AU (1) | AU2018365071A1 (ja) |
| CA (1) | CA3081978A1 (ja) |
| WO (1) | WO2019094837A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2024507827A (ja) | 2021-02-18 | 2024-02-21 | ヴェダンタ バイオサイエンシーズ インコーポレーテッド | 病原性生物を抑制するための組成物及び方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015500792A (ja) | 2011-12-01 | 2015-01-08 | 国立大学法人 東京大学 | 制御性t細胞の増殖または集積を誘導するヒト由来細菌 |
| WO2015095241A2 (en) | 2013-12-16 | 2015-06-25 | Seres Health, Inc. | Bacterial compositions and methods of use thereof for treatment of immune system disorders |
| WO2017079450A1 (en) | 2015-11-03 | 2017-05-11 | The Brigham And Women's Hospital | Therapeutic microbiota for the treatment and/or prevention of food allergy |
| JP7168558B2 (ja) | 2016-06-14 | 2022-11-09 | ヴェダンタ バイオサイエンシーズ インコーポレーテッド | Clostridium difficile感染症の処置 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007027751A2 (en) * | 2005-08-30 | 2007-03-08 | University Of Miami | Immunomodulating tumor necrosis factor receptor 25 (tnfr25) agonists, antagonists and immunotoxins |
| US8906668B2 (en) * | 2012-11-23 | 2014-12-09 | Seres Health, Inc. | Synergistic bacterial compositions and methods of production and use thereof |
| US10300137B2 (en) * | 2014-04-10 | 2019-05-28 | Riken | Compositions and methods for induction of TH17 cells |
| US11260083B2 (en) * | 2016-03-15 | 2022-03-01 | The Regents Of The University Of Michigan | Compositions and methods for treating and preventing graft versus host disease |
| CA3211208A1 (en) * | 2017-04-03 | 2018-10-11 | Gusto Global, Llc | Rational design of microbial-based biotherapeutics |
-
2018
- 2018-11-09 CA CA3081978A patent/CA3081978A1/en active Pending
- 2018-11-09 EP EP18875281.0A patent/EP3706767A4/en active Pending
- 2018-11-09 JP JP2020526142A patent/JP7293220B2/ja active Active
- 2018-11-09 WO PCT/US2018/060187 patent/WO2019094837A1/en unknown
- 2018-11-09 CN CN201880084621.9A patent/CN111526882A/zh active Pending
- 2018-11-09 AU AU2018365071A patent/AU2018365071A1/en active Pending
-
2021
- 2021-04-19 US US17/234,158 patent/US20220054556A1/en active Pending
-
2023
- 2023-06-07 JP JP2023093879A patent/JP2023121755A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015500792A (ja) | 2011-12-01 | 2015-01-08 | 国立大学法人 東京大学 | 制御性t細胞の増殖または集積を誘導するヒト由来細菌 |
| WO2015095241A2 (en) | 2013-12-16 | 2015-06-25 | Seres Health, Inc. | Bacterial compositions and methods of use thereof for treatment of immune system disorders |
| WO2017079450A1 (en) | 2015-11-03 | 2017-05-11 | The Brigham And Women's Hospital | Therapeutic microbiota for the treatment and/or prevention of food allergy |
| JP7168558B2 (ja) | 2016-06-14 | 2022-11-09 | ヴェダンタ バイオサイエンシーズ インコーポレーテッド | Clostridium difficile感染症の処置 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3706767A4 (en) | 2021-12-15 |
| JP2021502391A (ja) | 2021-01-28 |
| CA3081978A1 (en) | 2019-05-16 |
| WO2019094837A1 (en) | 2019-05-16 |
| CN111526882A (zh) | 2020-08-11 |
| AU2018365071A1 (en) | 2020-05-21 |
| US20220054556A1 (en) | 2022-02-24 |
| JP2023121755A (ja) | 2023-08-31 |
| EP3706767A1 (en) | 2020-09-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7097838B2 (ja) | 制御性t細胞の増殖または集積を誘導するヒト由来細菌 | |
| TWI821168B (zh) | 誘導cd8+ t細胞的組成物及方法 | |
| CN107405394B (zh) | 混合变应原组合物及其使用方法 | |
| US10071157B2 (en) | Method of inducing tolerance to an allergen | |
| CN103079582B (zh) | 诱导调节性t细胞的增殖或积累的组合物 | |
| US11000556B2 (en) | Compositions and methods for the treatment of allergy | |
| JP2023121755A (ja) | アレルギーの処置のための組成物および方法 | |
| US20230346826A1 (en) | Compositions and methods for treating and/or preventing autoimmune disorders | |
| Miles | Adverse immune reactions to foods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211108 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20211108 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220824 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220830 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20221129 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230228 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230510 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230607 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7293220 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |