JP7202563B2 - 電気化学センサー用電極、電気化学センサー、及び電気化学的検出装置 - Google Patents
電気化学センサー用電極、電気化学センサー、及び電気化学的検出装置 Download PDFInfo
- Publication number
- JP7202563B2 JP7202563B2 JP2018206584A JP2018206584A JP7202563B2 JP 7202563 B2 JP7202563 B2 JP 7202563B2 JP 2018206584 A JP2018206584 A JP 2018206584A JP 2018206584 A JP2018206584 A JP 2018206584A JP 7202563 B2 JP7202563 B2 JP 7202563B2
- Authority
- JP
- Japan
- Prior art keywords
- electrode
- electrochemical sensor
- electrochemical
- filtration membrane
- aptamer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Investigating Or Analyzing Materials By The Use Of Electric Means (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Description
本実施形態の電気化学的検出装置及び方法は、その電気化学センサーに特徴があるものであって、特に、そのセンサーには新規な電気化学センサー用電極を用いることにより、検出対象物質を簡便、かつ正確に検出することができるものである。
まず、本実施形態の電気化学センサー用電極について説明する。この電気化学センサー用電極は、例えば、図1に示したような構造を有するものであり、図1は電気化学センサー用電極の構成を示した概略断面図である。
検出対象物質が細菌の場合、孔径は、たとえば、1.0μm~20.0μmが好ましい。
表面に導電膜3が設けられたろ過膜2に対して、固定するアプタマー4を導電膜3上に固定するには、導電膜3上に直接アプタマー4を固定してもよいし、間接的にアプタマー4を固定してもよい。
本発明の電気化学センサーは、孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜と、前記ろ過膜の表面に形成された導電膜と、前記導電膜の表面に固定されたアプタマーと、を有する作用極となる電気化学センサー用電極と、孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜の表面に導電膜を形成した対極となる電気化学センサー用電極と、を有し、これらの電気化学センサー用電極を短絡しないように重ねてなるものである。
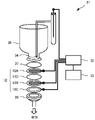
本発明の電気化学的検出装置は、上記したように、例えば、図2及び図3に示した構成のものが挙げられる。なお、この図2及び図3は、構成を説明するために、積層体を展開して示したものである。
(実施例1)
孔径が20.0μm、厚さ9.5μm、直径47mmのトラックエッチドメンブレンフィルター(GVS社製)の両表面に、イオンスパッター装置(日立製作所製、商品名:E-1030型)を用いて、スパッタリング電流40mAの条件で金を200秒間真空蒸着した。
実施例1において、トロンビンアプタマーを含有するリン酸緩衝液の代わりに濃度1×10-6Mでリゾチームアプタマーを含有するリン酸緩衝生理食塩水(pH 6.8)を用いて、導電層の表面に密度1×10-10mol/cm2以下のリゾチームアプタマーが固定された電気化学センサー用電極を製造した。
Claims (7)
- 孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜と、
前記ろ過膜の表面に形成された導電膜と、
前記導電膜の表面に固定されたアプタマーと、
を有し、
前記ろ過膜がトラックエッチメンブレンフィルターであることを特徴とする電気化学センサー用電極。 - 前記ろ過膜の孔径が、0.01~20.0μmである請求項1に記載の電気化学センサー用電極。
- 前記アプタマーが、特定のタンパク質を捕捉可能なアプタマーである請求項1又は2に記載の電気化学センサー用電極。
- 前記アプタマーが、トロンビンアプタマー又はリゾチームアプタマーである請求項3に記載の電気化学センサー用電極。
- 孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜と、前記ろ過膜の表面に形成された導電膜と、前記導電膜の表面に固定されたアプタマーと、を有する作用極となる電気化学センサー用電極と、
孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜の表面に導電膜を形成した対極となる電気化学センサー用電極と、を有し、
前記作用極及び前記対極となる電気化学センサー用電極が短絡しないように重ねられていることを特徴とする電気化学センサー。 - 孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜と、前記ろ過膜の表面に形成された導電膜と、前記導電膜の表面に固定されたアプタマーと、を有する作用極となる電気化学センサー用電極を複数有することを特徴とする電気化学センサー。
- 孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜と、前記ろ過膜の表面に形成された導電膜と、前記導電膜の表面に固定されたアプタマーと、を有する作用極となる電気化学センサー用電極、対極及び参照極を有する電気化学センサーと、
前記作用極及び前記対極間の電位差を一定にする電位制御手段と、
前記電気化学センサー用電極において、検出対象物質の捕捉に起因する酸化又は還元による電流値の変化を測定する電流測定手段と、
を有し、
前記対極が、孔道が円筒状かつ真直であり、均一な孔径を有するろ過膜の表面に導電膜を形成した電気化学センサー用電極であり、
前記作用極及び前記対極となる電気化学センサー用電極が短絡しないように重ねられていることを特徴とする電気化学的検出装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018206584A JP7202563B6 (ja) | 2018-11-01 | 2018-11-01 | 電気化学センサー用電極、電気化学センサー、及び電気化学的検出装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018206584A JP7202563B6 (ja) | 2018-11-01 | 2018-11-01 | 電気化学センサー用電極、電気化学センサー、及び電気化学的検出装置 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020071172A JP2020071172A (ja) | 2020-05-07 |
| JP7202563B2 true JP7202563B2 (ja) | 2023-01-12 |
| JP7202563B6 JP7202563B6 (ja) | 2023-02-03 |
Family
ID=70547694
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018206584A Active JP7202563B6 (ja) | 2018-11-01 | 2018-11-01 | 電気化学センサー用電極、電気化学センサー、及び電気化学的検出装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7202563B6 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7231923B2 (ja) * | 2019-01-15 | 2023-03-02 | 国立大学法人東京工業大学 | 複合体の検出方法、並びにそれに用いる担体及び検出キット |
| CN113000079B (zh) * | 2020-06-02 | 2023-09-22 | 山东大学 | 一种重金属离子检测电化学微流控传感芯片及其制备方法 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001091512A (ja) | 1999-07-16 | 2001-04-06 | Matsushita Electric Ind Co Ltd | 血液成分分析装置 |
| JP2002207026A (ja) | 2001-01-10 | 2002-07-26 | Shimadzu Corp | 核酸アプタマー自己集積化バイオセンサー及びそれを検出部として備えたチップデバイス |
| US20090283424A1 (en) | 2008-03-07 | 2009-11-19 | Carson Charles A | Sensor electrode and method for the electrochemical detection of nucleotides |
| JP2011080773A (ja) | 2009-10-02 | 2011-04-21 | Nomura Micro Sci Co Ltd | 電気化学センサー用電極の製造方法 |
| US20130264221A1 (en) | 2010-12-16 | 2013-10-10 | Min Gon Kim | Membrane phase electrode using printing and bio-molecule detection using same |
| JP2014518567A (ja) | 2011-03-31 | 2014-07-31 | サピエント センサーズ リミテッド | アプタマーコーティングされた測定電極及び基準電極並びにこれらを使用してバイオマーカーを検出する方法 |
| JP2015081843A (ja) | 2013-10-23 | 2015-04-27 | 大日本印刷株式会社 | バイオセンサ用導電材およびバイオセンサ |
-
2018
- 2018-11-01 JP JP2018206584A patent/JP7202563B6/ja active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001091512A (ja) | 1999-07-16 | 2001-04-06 | Matsushita Electric Ind Co Ltd | 血液成分分析装置 |
| JP2002207026A (ja) | 2001-01-10 | 2002-07-26 | Shimadzu Corp | 核酸アプタマー自己集積化バイオセンサー及びそれを検出部として備えたチップデバイス |
| US20090283424A1 (en) | 2008-03-07 | 2009-11-19 | Carson Charles A | Sensor electrode and method for the electrochemical detection of nucleotides |
| JP2011080773A (ja) | 2009-10-02 | 2011-04-21 | Nomura Micro Sci Co Ltd | 電気化学センサー用電極の製造方法 |
| US20130264221A1 (en) | 2010-12-16 | 2013-10-10 | Min Gon Kim | Membrane phase electrode using printing and bio-molecule detection using same |
| JP2014518567A (ja) | 2011-03-31 | 2014-07-31 | サピエント センサーズ リミテッド | アプタマーコーティングされた測定電極及び基準電極並びにこれらを使用してバイオマーカーを検出する方法 |
| JP2015081843A (ja) | 2013-10-23 | 2015-04-27 | 大日本印刷株式会社 | バイオセンサ用導電材およびバイオセンサ |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2020071172A (ja) | 2020-05-07 |
| JP7202563B6 (ja) | 2023-02-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Rezaei et al. | Electrochemical detection techniques in biosensor applications | |
| Pereira et al. | Electrochemical sensing of lactate by using an electrode modified with molecularly imprinted polymers, reduced graphene oxide and gold nanoparticles | |
| JP3574137B2 (ja) | 電気化学的電池 | |
| US20170067889A1 (en) | Lateral Flow Diagnostic Devices with Integrated Electronic Components and Methods of Use Thereof | |
| US20150219593A1 (en) | Sample analysis method | |
| Wen et al. | Fabrication of layer-by-layer assembled biomimetic nanochannels for highly sensitive acetylcholine sensing. | |
| JP7202563B2 (ja) | 電気化学センサー用電極、電気化学センサー、及び電気化学的検出装置 | |
| JP6853194B2 (ja) | 体液試料中の少なくとも1つの分析物を電気化学的に検出するための方法および試験要素 | |
| US20200155048A1 (en) | Biofluid sensing devices with ph-buffered eab sensors | |
| Brownlee et al. | 3D interdigitated vertically aligned carbon nanotube electrodes for electrochemical impedimetric biosensing | |
| Kececi et al. | Resistive-pulse detection of short dsDNAs using a chemically functionalized conical nanopore sensor | |
| Du et al. | Direct electrochemical detection of glucose in human plasma on capillary electrophoresis microchips | |
| Hoa et al. | An Arrayed Micro‐glutamate Sensor Probe Integrated with On‐probe Ag/AgCl Reference and Counter Electrodes | |
| WO2022187075A2 (en) | Electrochemical sensor device for rapid analyte detection and methods of making and using the same | |
| Castillo et al. | Impedimetric aptasensor for thrombin recognition based on CD support | |
| Punter-Villagrasa et al. | Amperometric and impedance monitoring systems for biomedical applications | |
| KR101924415B1 (ko) | 복합 임피던스 측정 장치 및 측정 방법 | |
| Dhull et al. | Microfluidics integrated NiO based electrolyte-gated FETs for the detection of cortisol | |
| KR20140143999A (ko) | 당화 헤모글로빈의 일회용 전류식 검출방법 | |
| Chen et al. | Simultaneous determination of dopamine and ascorbic acid at a poly (toluidine blue) modified electrode | |
| Covaci et al. | Optimization of acetylcholinesterase immobilization on microelectrodes based on nitrophenyl diazonium for sensitive organophosphate insecticides detection | |
| JP2009250746A (ja) | 電気化学センサー用電極、電気化学センサー、電気化学的検出装置及び電気化学的検出方法 | |
| Hayashi et al. | Microfabricated On‐Line Electrochemical Flow Cell Integrated with Small Volume Pre‐Reactor for Highly Selective Detection of Biomolecules | |
| CN114199971A (zh) | 基于化学修饰的纳米孔对整合素构象检测的方法 | |
| JP4649767B2 (ja) | バイオセンサ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181115 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20211011 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220812 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220906 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220927 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20221206 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20221216 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7202563 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |