JP6997623B2 - オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 - Google Patents
オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 Download PDFInfo
- Publication number
- JP6997623B2 JP6997623B2 JP2017550092A JP2017550092A JP6997623B2 JP 6997623 B2 JP6997623 B2 JP 6997623B2 JP 2017550092 A JP2017550092 A JP 2017550092A JP 2017550092 A JP2017550092 A JP 2017550092A JP 6997623 B2 JP6997623 B2 JP 6997623B2
- Authority
- JP
- Japan
- Prior art keywords
- oligonucleotide
- editing
- oligonucleotides
- edited
- target
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/102—Mutagenizing nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/04—Drugs for disorders of the muscular or neuromuscular system for myasthenia gravis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/111—General methods applicable to biologically active non-coding nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/33—Chemical structure of the base
- C12N2310/333—Modified A
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/33—Chemical structure of the base
- C12N2310/335—Modified T or U
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/344—Position-specific modifications, e.g. on every purine, at the 3'-end
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/34—Allele or polymorphism specific uses
Description
以下の出願は、2015年11月9日出願の仮特許出願第62/252,693号、2015年6月16日出願の同第62/180,175号、2015年3月31日出願の同第62/141,077号、および2014年12月12日出願の同第62/091,027号の優先権を主張するものである。
連邦政府資金による研究開発の記載
該当なし
共同研究契約の当事者の名称
該当なし
コンパクトディスクで提出された資料の参照による援用
該当なし
1. 3個のホスホロチオエート残基を編集オリゴヌクレオチドの各端部に付加すること(しかしながら、細胞内での急速なエンドヌクレアーゼ消化に依然として影響されやすい場合の結果として生じる編集オリゴヌクレオチド、そしてホスホロチオエートはそれらの毒性を増加させる);
2. 細胞がS期の間に編集オリゴヌクレオチドで処置されるように細胞周期を同調させること。残念ながら、これは編集効率をある程度上昇させたが、この手法は煩雑であり、必ずしもインビボ治療に実用的とは限らない;そして
3. 複製フォークの進行を減速させ、かつ/または細胞内でDNA鎖切断を誘導する試薬で、細胞を処置し、これにより細胞内のDNA修復の増加をもたらすこと(しかしながら、これは編集効率をある程度上昇させたが、この手法も煩雑であり、必ずしもインビボ治療に実用的とは限らない。
4. PNAクランプ、すなわち標的編集の近傍に結合する鎖侵入一本鎖PNAを付加すること(Bahal et al.Current Gene Therapy Vol.14(5):331-42(2014)、Chin et al.PNAS Vol 105(36):13514-13519(2008)、Rogers et al.PNAS Vol.99(26):16695-16700(2002)、米国特許第8,309,356号。
の構造を含み得、式中、各オリゴヌクレオチドは、該標的核酸に実質的に相補的であり、約10~約50または10~約200ヌクレオチドであり、Xは、H、OH、ハロゲン、R1、SR1、またはOR1であり、ハロゲンは、Cl、F、Br、またはIであり、R1は、-CH3、-CH2CH3、または-CH2OCH3である。標的核酸は、RNAまたはDNAであり得る。標的がRNAである場合、それはmRNAであることが好ましい。
ある特定の実施形態において、本発明の編集オリゴヌクレオチドは、式(I)に従う構造を有する。
T5-P5-E5-SE-E3-P3-T3
(I)
3’末端はDNA延長のプライミングにおいて機能し得、これが3’末端セグメントを概して遊離した3’ヒドロキシルを有する修飾に限定し得るため、5’末端セグメントは、多数の異なる種類の修飾に3’末端よりも適している場合がある。このプライミング機能は、5’末端において通常は必要ではない。0~5ヌクレオチド長であり得る任意選択の5’末端セグメントは、さもなければ体液(例えば、血液もしくは間質液)、培養培地、飲食作用経路、または細胞質もしくは核細胞質において編集オリゴヌクレオチドを容易に分解し得る、5’エキソヌクレアーゼを遮断するよう機能する。このセグメントは、5’近位セグメントよりもヌクレアーゼ抵抗性である非ヌクレオチド末端ブロッキング基および/または修飾ヌクレオチド(複数可)(例えば、逆位Tなどの逆位塩基)を含んでもよい。5’末端セグメントが用いられない場合、5’近位セグメントは単純に、編集オリゴヌクレオチドの最も5’側の部分である。非ヌクレオチド末端ブロッキング基は、この作業の実行に使用するための当業者に既知の任意のリンカー、例えば、3’C3アミノリンカー、3’C7アミノリンカー、5’&3’C6アミノリンカー、5’C12アミノリンカー、5’光切断可能アミノリンカー、3’C3ジスルフィドリンカー、5’&3’C6、ジスルフィドリンカー、ジチオールリンカー、4-ホルミルベンズアミド、アルデヒド、C8-アルキン-チミジン、カルボキシ-dTリンカー、DADEリンカー(5’カルボキシルリンカー)、3’グリセリル、5’ヘキシニル、チミジン-5-C2およびC6アミノリンカー、2’-デオキシアデノシン、8-C6アミノリンカー、2’-デオキシシチジン-5-C6アミノリンカー、2’-デオキシグアノシン-8-C6アミノリンカー、C7、ならびに内部アミノリンカーなどを含んでもよい。リンカー長は、炭素1個から炭素約20個、または他の化学構造の同等の長さに及び得るが、好ましくは、炭素10個未満または10個の炭素と同等の長さである。
5’近位セグメントは、上記の5’末端セグメントに関して前述したものと同じ理由のうちのいくつかのために、多数の異なる種類の修飾に3’末端よりも適している場合がある。それは、1~150ヌクレオチド長、好ましくは約5~約20ヌクレオチド長であり得る。5’近位セグメントの主な機能は、標的配列にハイブリダイズする編集オリゴヌクレオチドの親和性および能力を向上させることである。したがって、このセグメントは、任意選択により、編集セグメントよりも実質的に修飾されていてもよい。5’近位セグメントは、本明細書で言及されるオリゴヌクレオチド修飾のいずれを含有してもよい。このセグメントは、DNAまたはRNA(任意選択により、LNAおよび他の拘束された骨格を含むよう広く定義されている2’修飾RNA)から構成されていてもよい。この領域内の追加のホスホロチオエート(例えば、向上したキラル純度を有するジホスホロチオエートおよびホスホロチオエート)は、ヌクレアーゼ安定性のために厳密には必要とされないが、追加のホスホロチオエートは、RNAおよびDNA結合のヌクレアーゼ安定性を向上させるために有用である。また、このセグメント内のホスホロチオエートがヌクレアーゼ安定性に必要でない場合であっても、それらは、全体的なホスホロチオエート含有量を増加させ得、これは、ホスホロチオエートの化学的に「粘着性の」性質に起因して、血清タンパク質結合および細胞結合を増加させ、動物およびヒトにおける血清中半減期の増加につながり、細胞質取り込みを向上させる。これらの理由のため、好ましい実施形態において、編集オリゴヌクレオチドの全ホスホロチオエート含有量は、5個、10個、15個、または20個を上回り得る。約20個のホスホロチオエートの含有量は、多くの場合、優れた血清タンパク質結合および細胞結合/取り込みをもたらす。しかしながら、編集オリゴヌクレオチドの相補的領域内のより多くの数(例えば、6個超)のホスホロチオエート結合は編集効率を抑制し得るため、ホスホロチオエートの尾部が、標的DNAに相補的な領域の5’または3’末端に付加され得る。この尾部は、1~約4、約5~約9ヌクレオチド、または約10~約25ヌクレオチドの長さであり得、好ましくは、標的に非相補的な領域内に位置付けられ得る。
5’編集セグメントは、1~約10ヌクレオチド、または1~約100ヌクレオチド、または1~約200ヌクレオチドの長さであり、編集部位の5’末端に位置付けられ、この位置は、対向するゲノムDNA鎖の編集をもたらすように細胞機構に影響を及ぼすのに十分に編集部位に近接している。いかなる理論にも束縛されるものではないが、このDNAミスマッチ修復系は、編集セグメント(これは5’編集セグメント、編集部位、および3’編集セグメントである)を、編集のための鋳型鎖として使用する場合がある。したがって、5’編集セグメント、編集部位、および3’編集セグメント内のヌクレオチドは、天然DNAまたは天然DNA化学構造と好ましくは実質的に同様であり(例えば、図2において、化合物100013は、編集部位の5’に約8個の未修飾ヌクレオチドを有し、これは、親化合物と比較して全体的な編集効率を抑制しなかった)、また、未修飾であってもよく、または、ホスホロチオエート、5’S、2’F、2’アミノ、もしくは3’S、可逆的に電荷を中和するホスホホトリエステル(phosphophotriester)、および核酸塩基修飾などの、1個以上の修飾を含んでもよい。
編集部位は、標的ゲノムDNAに相補的でないヌクレオチド(複数可)を含有し、1~6ヌクレオチド長であり得るが、必要に応じてより長くてもよい。トランジション/トランスバージョン修飾の場合、編集部位は、ミスマッチ塩基の数(例えば、1個~約6個、特に1個のヌクレオチド)に等しい。欠失を作り出すための編集の場合、編集部位は、ゲノムDNA内の塩基対合を形成しないヌクレオチドのちょうど反対側で標的ゲノムDNA鎖と塩基対合を形成する、2個の5’および3’ヌクレオチド間の接合部である。いくつかの場合では、1つの編集オリゴヌクレオチドが、集団内の異なる患者において発生し得る、標的DNAに対する相補性領域内にある近隣部位における異なる変異を治療するために使用され得る。この場合、患者の変異体遺伝子型に応じて、異なる編集部位が存在する。これらの場合において、編集部位は、最も5’側および最も3’側の変異、ならびにこれらの変異間の領域を含むことになる。好ましい一実施形態では、編集部位は、標的遺伝子内の全エクソンにハイブリダイズする。
3’編集セグメントは、その位置が編集部位の3’にあることを除いて、E5の3’編集セグメントと同じ範囲の特徴、特性、およびパラメータを有する。
3’近位セグメントは、他のセグメントに対するその位置を除いて、5’近位セグメントと同じ範囲の特徴およびパラメータを有する。好ましい実施形態において、3’近位セグメントは、2’修飾ヌクレオチドから構成され、より好ましい実施形態では、2’F修飾ヌクレオチドから構成される。最も好ましい実施形態では、それは、8個の2’F修飾ヌクレオチドを含む(図2)。
3’末端セグメントは、以下に詳解することを除いて、5’末端セグメントと同じ範囲の特徴および特性を含み得る。3’末端セグメントは、DNA複製および修復間にDNA合成のプライマーとして機能し、ひいては編集オリゴヌクレオチドがゲノムDNA内に近接して組み込まれることを可能にし得る。その結果、一実施形態において、このセグメントは、遊離3’ヒドロキシを有することになり、天然様の修飾または未修飾のDNAもしくはRNAから成ってもよい。
編集オリゴヌクレオチドをより効率的にする別の手法は、化学修飾によって親和性を増加させることである。本明細書に記載される修飾は、編集オリゴヌクレオチド内で組み合わされてもよく、2’-O-メチルRNA、2’F RNA、およびLNAを含む拘束核酸を含む。これらの修飾は、それらが免疫刺激を低減させることもできるという追加の利点を有する。修飾は、ハイブリダイゼーションのための高親和性「シード」領域を形成するようにグループ化され得る。好ましい実施形態において、このシード領域は、約2個~約12個の連続した修飾と共に、5’近位セグメント内に位置付けられることになる。他の実施形態では、シード領域は、3’近位セグメント内に位置付けられてもよい。あまり好ましくない実施形態では、修飾は、「編集セグメント」内に位置付けられ得る。編集セグメントは細胞修復機構と相互作用しなければならず、このセグメント内のある特定の修飾は修復に干渉し得るため、これはあまり好ましくない。修飾は、5’セグメント、編集セグメント、および/または3’セグメントにおいて、交互になっている、すなわち、3個おきまたは4個おきの結合であってもよい。5’セグメント、3’セグメント、または編集セグメント内にある化学修飾された核酸塩基の全割合は、独立して、約20%、30%、50%、60%、70%、80%、90%、または100%の範囲であり得る。
編集組成物中に外因性タンパク質を厳密に必要としないことが有利である一方で、ある特定の外因性タンパク質は、編集オリゴヌクレオチドをヌクレアーゼ分解から保護することによって、また標的ゲノムDNAに対する編集オリゴヌクレオチドの結合を強化することによって、上述の実施形態を向上させることができる。次のタンパク質またはリボ核タンパク質のうちの1つ以上が、編集オリゴヌクレオチドと併せて添加され得る。ジンクフィンガーヌクレアーゼ(Carroll D.Genetics 188:773e82.(2011))、TALEN、メガTALEN、他のホーミングエンドヌクレアーゼを含む、プログラム可能ヌクレアーゼ、CRISPR-Cas9(Jinek et al.Elife 2013;2:e00471)、または、相同のもしくは同様に作用するリボ核タンパク質(すなわち、Cpf1、C2C1、またはC2C3)(DNA結合親和性を低減させることによって標的特異性を増加させるように選択されているそれらの変異形態(eSpCas9、Slaymaker et al.,Rationally Engineered Cas9 Nucleases with Improved Specificity,Science(2015))と、「crRNA」が編集のためのドナーDNAとして作用し得るように、crRNA領域内のより多くのDNA置換に耐えるよう選択されている変異形態と、Cas9ヌクレアーゼが不活性化されている変異形態とを含む)、RecA、ラムダファージベータタンパク質(米国特許第7,566,535号)、ssDNA結合タンパク質、RAD、またはアルゴノート。
本発明の編集オリゴヌクレオチドとして利用される特定のオリゴヌクレオチドの合成に関する教示は、次の米国特許に見出され得る:ポリアミン接合オリゴヌクレオチドに関する米国特許第5,138,045号および同第5,218,105号;キラルリン結合を有するオリゴヌクレオチドの調製のためのモノマーに関する米国特許第5,212,295号;修飾された骨格を有するオリゴヌクレオチドに関する米国特許第5,378,825および同第5,541,307号;骨格修飾オリゴヌクレオチドおよび還元カップリングによるその調製に関する米国特許第5,386,023号;3-デアザプリン環系に基づく修飾核酸塩基およびその合成方法に関する米国特許第5,457,191号;N-2置換プリンに基づく修飾核酸塩基に関する米国特許第5,459,255号;キラルリン結合を有するオリゴヌクレオチドを調製するためのプロセスに関する米国特許第5,521,302号;ペプチド核酸に関する米国特許第5,539,082号;.ベータ.-ラクタム骨格を有するオリゴヌクレオチドに関する米国特許第5,554,746号;オリゴヌクレオチドの合成のための方法および材料に関する米国特許第5,571,902号;アルキルチオ基を有するヌクレオシドに関する米国特許第5,578,718号(かかる基は、ヌクレオシドの様々な位置のいずれかにおいて結合した他の部分とのリンカーとして使用され得る);高いキラル純度のホスホロチオエート結合を有するオリゴヌクレオチドに関する米国特許第5,587,361および同第5,599,797号;2’-O-アルキルグアノシンおよび2,6-ジアミノプリン化合物を含む関連化合物の調製のためのプロセスに関する米国特許第5,506,351号;N-2置換プリンを有するオリゴヌクレオチドに関する米国特許第5,587,469号;3-デアザプリンを有するオリゴヌクレオチドに関する米国特許第5,587,470号;両方とも接合4’-デスメチルヌクレオシド類似体に関する米国特許第5,223,168号および米国特許第5,608,046号;骨格修飾オリゴヌクレオチド類似体に関する米国特許第5,602,240号および同第5,610,289号;2’-フルオロ-オリゴヌクレオチドの合成方法にとりわけ関する米国特許第6,262,241号および同第5,459,255号。
多くの場合、保護基は、本発明の化合物の調製中に使用される。本明細書で使用される場合、「保護される」という用語は、指示される部分が、付加された保護基を有することを意味する。本発明のいくつかの好ましい実施形態では、化合物は、1個以上の保護基を含有する。広範な保護基を本発明の方法に用いることができる。概して、保護基は、化学官能基を特定の反応条件に対して不活性にするものであり、分子の残部を実質的に損傷することなく、分子内のそのような官能基に付加し、そこから取り除くことができる。
多くの固体支持体が市販されており、当業者であれば、固相合成ステップにおいて使用される固体支持体を容易に選択することができる。ある特定の実施形態において、ユニバーサルサポートが使用される。ユニバーサルサポートは、オリゴヌクレオチドの3’末端に位置する異常なまたは修飾されたヌクレオチドを有するオリゴヌクレオチドの調製を可能にする。Universal Support 500およびUniversal Support IIは、Glen Research(22825 Davis Drive,Sterling,Va)から市販されているユニバーサルサポートである。ユニバーサルサポートに関するさらなる詳細については、Scott et al.,Innovations and Perspectives in solid-phase Synthesis,3rd International Symposium,1994,Ed.Roger Epton,Mayflower Worldwide,115-124]、Azhayev,A.V.Tetrahedron,55,787-800,1999、およびAzhayev and Antopolsky Tetrahedron,57,4977-4986,2001を参照されたい。加えて、オリゴヌクレオチドが、塩基性加水分解をより容易に受けるsyn-1,2-アセトキシホスフェート基を介して固体支持体に結合しているとき、オリゴヌクレオチドは、より穏和な反応条件下でユニバーサルサポートから切断され得ることが報告されている。Guzaev,A.I.;Manoharan,M.J.Am.Chem.Soc.,125:2380,2003を参照されたい。
好ましい修飾されたヌクレオシド間結合または骨格としては、例えば、ホスホロチオエート、キラルホスホロチオエート、ホスホロジチオエート、ホスホトリエステル、アミノアルキルホスホトリエステル、メチルならびに3’-アルキレンホスホネートおよびキラルホスホネートを含む他のアルキルホスホネート、ホスフィネート、3’-アミノホスホロアミデートおよびアミノアルキルホスホロアミデートを含むホスホロアミデート、チオノホスホロアミデート、チオノアルキルホスホネート、チオノアルキルホスホトリエステル、および正常な3’-5’結合を有するボラノホスフェート、これらの2’-5’連結類似体、ならびにヌクレオシド単位の隣接する対が3’-5’対5’-3’または2’-5’対5’-2’で連結している逆転した極性を有するものが挙げられる。様々な塩、混合塩、および遊離酸形態も含まれる。図20も参照されたい。
他の好ましいオリゴヌクレオチド模倣物において、ヌクレオシド単位の糖とヌクレオシド間結合との両方、すなわち骨格が、新規の基で置き換えられる。核酸塩基単位は、適切な核酸標的合物とのハイブリダイゼーションのために維持される。優れたハイブリダイゼーション特性を有することが示されているそのようなオリゴヌクレオチド、すなわちオリゴヌクレオチド模倣物の1つは、ペプチド核酸(PNA)と称される。PNA化合物において、オリゴヌクレオチドの糖骨格は、アミド含有骨格、具体的にはアミノエチルグリシン骨格で置き換えられる。核酸塩基は保持され、骨格のアミド部分の原子に直接的または間接的に結合している。PNA化合物の調製を教示する代表的な米国特許としては、米国特許第5,539,082号、同第5,714,331号、および同第5,719,262号が挙げられるが、これらに限定されない。PNA化合物のさらなる教示は、Nielsen et al.,Science,254:1497,1991に見出すことができる。
本発明の編集オリゴヌクレオチドに用いられるオリゴヌクレオチドは、追加または代替として、核酸塩基修飾または置換を含んでもよい。本明細書で使用される場合、「未修飾」または「天然」の核酸塩基は、プリン塩基であるアデニン(A)およびグアニン(G)、ならびにピリミジン塩基であるチミン(T)、シトシン(C)、およびウラシル(U)を含む。修飾された核酸塩基は、他の合成および天然の核酸塩基、例えば5-メチルシトシン(5-me-C)、5-ヒドロキシメチルシトシン、キサンチン、ヒポキサンチン、2-アミノアデニン、アデニンならびにグアニンの6-メチルおよび他のアルキル誘導体、アデニンならびにグアニンの2-プロピルおよび他のアルキル誘導体、2-チオウラシル、2-チオチミンおよび2-チオシトシン、5-ハロウラシルおよびシトシン、5-プロピニルウラシルおよびシトシン、6-アゾウラシル、シトシン、およびチミン、5-ウラシル(シュードウラシルとしても知られる)、4-チオウラシル、8-ハロ、8-アミノ、8-チオール、8-チオアルキル、8-ヒドロキシルおよび他の8-置換アデニンおよびグアニン、5-ハロ、特に5-ブロモ、5-トリフルオロメチル、ならびに他の5-置換ウラシルおよびシトシン、7-メチルグアニンおよび7-メチルアデニン、8-アザグアニンおよび8-アザアデニン、7-デアザグアニンおよび7-デアザアデニン、ならびに3-デアザグアニンおよび3-デアザアデニンなどを含む。図21および22も参照されたい。
編集オリゴヌクレオチドと標的核酸とは、所望の作用が起こる(例えば、ハイブリダイゼーション後に所望の塩基修飾が起こることを許容する)ように、オリゴヌクレオチドの十分な数の核酸塩基が、標的核酸の対応する核酸塩基と水素結合することができるとき、互いに相補的である。
A. ハイブリダイゼーション
編集オリゴヌクレオチドと標的核酸とのハイブリダイゼーションは、異なるストリンジェントな条件下で起こり得、配列依存性であり、ハイブリダイズされる核酸分子の性質および組成によって決定される。最も一般的なハイブリダイゼーション機構は、核酸分子の相補的な核酸塩基間の水素結合(例えば、ワトソン-クリック型、フーグスティーン型、または逆フーグスティーン型の水素結合)を伴う。
本発明の編集オリゴヌクレオチドは、DNAまたはRNAを標的にするように設計される。編集ヌクレオチド(複数可)の片側または両側には、標的核酸に対して完全に相補的または実質的に相補的なオリゴヌクレオチドが位置してもよい。
編集オリゴヌクレオチドは、任意選択により、送達部分をオリゴヌクレオチドに共有結合させる「リンカー」を含有してもよい。リンカー結合は、編集オリゴヌクレオチド内の任意の核酸塩基に対するもの、5’末端に対するもの、3’末端に対するもの、糖残基に対するもの、または骨格に対するものであってもよい。リンカーは、この作業の実行に使用するための、当業者に既知の任意のリンカーであってよい。代替的に、リンカーは、編集オリゴヌクレオチドにおけるその性能を決定するために利用および試験されてもよい。例えば、本発明で利用され得るリンカーとしては、3’C3アミノリンカー、3’C7アミノリンカー、5’&3’C6アミノリンカー、5’C12アミノリンカー、5’光切断可能アミノリンカー、3’C3ジスルフィドリンカー、5’&3’C6、ジスルフィドリンカー、ジチオールリンカー、4-ホルミルベンズアミドアルデヒド、C8-アルキン-チミジン、カルボキシ-dTリンカー、DADEリンカー(5’カルボキシルリンカー)、3’グリセリル、5’ヘキシニル、チミジン-5-C2およびC6アミノリンカー、2’-デオキシアデノシン、8-C6アミノリンカー、2’-デオキシシチジン-5-C6アミノリンカー、2’-デオキシグアノシン-8-C6アミノリンカー、C7、内部アミノリンカー、光切断可能リンカー、または、介入基が、反応性基を標的核酸塩基の付近に位置付けるように機能する、介入物質含有リンカーが挙げられる。リンカー長は、炭素1個から炭素約20個、または他の化学構造の同等の長さに及び得るが、好ましくは、炭素10個未満または10個の炭素と同等の長さである。
図19は、化学修飾様式の編集のために本発明の編集オリゴヌクレオチドを利用する編集の機構を示す。編集オリゴヌクレオチドの長さは、例えば、編集を行うために利用されている化学構造の種類、標的に対して行われる編集の種類、およびリンカーの長さを含む、編集プロセスのいくつかの物理的態様に応じて異なり得る。
本発明の化学修飾様式を用いる編集オリゴヌクレオチドは、アルキル化および脱アミノ化を含む様々な特異的化学反応によって、それらの機能を実行する。各種の反応において、任意選択の反応性基は、特異性を増加させ(Singh,et al.The resurgence of covalent drugs Nature Reviews:Drug Discovery Volume 10 April 2011)、合成、精製、および貯蔵の間の反応性を回避するために用いられ得、また、標的細胞に達する前に、細胞のpH、例えばエンドソームまたはリソソーム内の低いpHなど、細胞内エステラーゼ、温度、光、または還元環境によって、放出され得る。
本発明は、様々な変異から生じる作用を低減させるか、または排除することのできる、編集オリゴヌクレオチドを提供する。
A. 疾患
本発明の編集オリゴヌクレオチドは、疾患の作用を低減させるか、減少させるか、または排除するために利用され得る。本発明の編集オリゴヌクレオチドで治療され得る疾患としては、アデノシンデアミナーゼ欠損症;アルファ1アンチトリプシン欠損症;アルツハイマー病;アミノアシラーゼ2欠損症;アスパルトアシラーゼ欠損症;動脈硬化、粥状動脈硬化、カナバン-ファン・ボガエール-バートランド病(Canavan-Van Bogaert-Bertrand disease);シャルコー・マリー・トゥース病;嚢胞性線維症;乳がん素因変異;インスリン受容体変異により生じる糖尿病1型;糖尿病2型(例えば、標的遺伝子PTP-1BおよびABCA1C69Tアレル(Alharbi et al.,J.Biosci.38(5):893-897(2013))、鎌形赤血球症;ファブリー病;家族性大腸腺腫症;家族性アミロイド心筋症;家族性アミロイド多発ニューロパチー;家族性自律神経障害;家族性高コレステロール血症;フリートライヒ運動失調症;ゴーシェ病I型;ゴーシェ病I型I;糖原貯蔵障害II型;GM2ガングリオシドーシス;血色素症;血友病A;血友病B;血友病C;遺伝性盲目(rd1の変異を補正する編集オリゴヌクレオチドの網膜への送達の一例について、Andrieu-Soler Molecular Vision 13:692-706,2007を参照されたい);遺伝性高チロシン血症I型(HTI)(フマリルアセト酢酸ヒドラーゼ(FAH)の変異により生じる、Yin,et al.Nature biotechnology 32(6),2014)ヘキソサミニダーゼA欠損症;高コレステロール血症、卵巣がん素因変異;フェニルケトン尿症;多嚢胞性腎疾患;プリオン病;老人性全身性アミロイドーシス;鎌状赤血球症;鎌状赤血球貧血;スミス・レムリ・オピッツ症候群;脊髄性筋萎縮症;およびウィルソン病が挙げられる。
本発明の薬学的組成物は、標的遺伝子の発現をもたらすのに十分な投与量で投与される。概して、編集オリゴヌクレオチドの好適な用量は、受容者の体重1キログラム当たり1日に0.01~5.0ミリグラムの範囲、または必要であれば1キログラム当たり最大50ミリグラム、好ましくは体重1キログラム当たり1日に0.1~200マイクログラムの範囲、より好ましくは体重1キログラム当たり1日に0.1~100マイクログラムの範囲、さらにより好ましくは体重1キログラム当たり1日に1.0~50マイクログラムの範囲、最も好ましくは体重1キログラム当たり1日に1.0~25マイクログラムの範囲である。本薬学的組成物が1日1回投与されてもよく、あるいは、編集オリゴヌクレオチドが、1日を通して適切な間隔における2回、3回、4回、5回、6回、もしくはそれを超える部分用量で、またはさらには継続的輸注を使用して投与されてもよい。その場合、各部分用量に含有される編集オリゴヌクレオチドは、1日の全投与量を達成するために、相応により少量でなければならない。投与量単位は、例えば、数日の期間にわたって編集オリゴヌクレオチドの徐放をもたらす従来の徐放性製剤を使用した、数日間にわたる送達のために調合することもできる。徐放性製剤は、当該技術分野で周知である。この実施形態において、投与量単位は、対応する複数の1日用量を含む。
当業者であれば、疾患または障害の重症度、以前の治療、対象の全体的な健康および/または年齢、ならびに存在する他の疾患を含むがこれらに限定されない、ある特定の要因が、対象を効果的に治療するために必要とされる投与量およびタイミングに影響し得ることを理解するであろう。さらに、治療有効量の組成物を用いた対象の治療は、単一の治療または一連の治療を含むことができる。本発明に包含される個別の編集オリゴヌクレオチドの有効な投与量およびインビボ半減期の推定は、従来の方法論を使用して、または本明細書の他の箇所に記載される適切な動物モデルを使用したインビボ試験に基づいて、行うことができる。
本発明に包含される薬学的組成物は、経口、または、静脈内、筋肉内、腹腔内、皮下、経皮、気道(エアロゾル)、直腸、膣、ならびに局所(口腔および舌下を含む)投与を含む非経口経路を含むがこれらに限定されない、当該技術分野で既知の任意の手段によって投与されてよい。好ましい実施形態において、本薬学的組成物は、静脈内投与される。
かかる化合物の毒性および治療有効性は、例えば、LD50(集団の50%に対して致死的な用量)およびED50(集団の50%において治療上有効な用量)を決定するための、細胞培養液または実験動物における標準的な薬学的手順によって決定することができる。毒性効果と治療効果との用量比が治療指数であり、これは、LD50/ED50比として表すことができる。高い治療指数を示す化合物が好ましい。
本発明のオリゴヌクレオチドは、組成物および方法において提供される。
表1に提示されるオリゴヌクレオチド構造物は、細胞培養液中のそれらの活性が親化合物未満であり得るとしても、研究および治療用途に有用であるが、それは、これらのオリゴヌクレオチドの各々が化学構造を付加し、免疫刺激の低減、ヌクレアーゼ安定性の上昇、標的特異性の上昇、化学毒性の低減、および/または親和性の上昇といった、他の予測される治療利益に寄与するからである。
Kmiec法は、化学反応基が編集オリゴヌクレオチドに結合することを必要とせず、塩基を任意の他の天然塩基にする編集を達成し、小さな挿入または欠失を可能にするため、Kmiec法を用いる本発明の実施形態は、化学修飾法に勝るいくつかの利点を有する。
表1および図2は、本発明の編集オリゴヌクレオチドの実施例を記載する。表1図2における編集オリゴヌクレオチド配列は、緑色蛍光タンパク質中のヌル変異を標的にし、この変異を補正して、蛍光のアッセイにより容易に監視することのできる機能性配列にする(Erin E.BrachmanおよびEric B.Kmiec(上記))。これらの化学修飾パターンは、変異を標的にする編集オリゴヌクレオチド、保護的アレルを作り出す編集オリゴヌクレオチド、または他の望ましいゲノムの変化を作り出す編集オリゴヌクレオチドに適用することができる。これらの実施例の各事例において、開示される配列により既に決定されていない場合、また本発明の他の実施形態において、編集部位は、編集オリゴヌクレオチドの中央領域内にあってもよく、または、5’末端もしくは3’末端の方に片寄っていてもよい。好ましい実施形態において、編集部位は、いずれかの末端から5ヌクレオチド超離れている。各事例において、未修飾であるか、または修飾されている場合は、依然として細胞のDNA修復および複製機構によりDNAと認識される保存的修飾(すなわち、ホスホロチオエートまたは5’メチルCを有する、DNAの領域内の編集部位を有することが好ましい場合もある。
A. 細胞株および培養条件
HCT116細胞は、ATCC(American Type Cell Culture,Manassas,VA)から取得した。HCT116-19は、変異eGFP遺伝子を含有するpEGFP-N3ベクター(Clontech,Palo Alto,CA)を組み入れることによって作り出された。変異eGFP遺伝子は、非機能性eGFPタンパク質を生じる167位のナンセンス変異を有する。これらの実験では、10%のウシ胎仔血清、2mMのL-グルタミン、および1%のペニシリン/ストレプトマイシンを補充したマッコイ5A改変培地(Thermo Scientific,Pittsburgh,PA)中で、HCT116-19細胞を培養した。細胞は、37℃および二酸化炭素5%に維持した。
同調細胞を利用した実験では、HCT116-19細胞を100mmの皿に2.5×106細胞で播種し、標的化の前に6mMアフィディコリンで24時間同調させた。細胞を4時間(または指示された時間)にわたって遊離させ、その後、PBS(2/2)で洗浄し、完全増殖培地を添加することによって、トリプシン処理およびトランスフェクションを行った。HCT116-19細胞を同調させたものと同調させていないものとに、4mmギャップのキュベット(BioExpress,Kaysville,UT)内で5×105細胞/100ulの濃度において、トランスフェクションを行った。Bio-Rad Gene Pulser XCell(商標)電気穿孔システム(Bio-Rad Laboratories,Hercules,CA)を使用して、一本鎖オリゴヌクレオチドを電気穿孔した(250V、LV、13msパルス長、2パルス、1秒間隔)。次いで、完全増殖培地を含む6ウェルプレートにおいて、細胞を37℃で指示された時間にわたって回復させ、その後分析した。遺伝子編集された細胞の分析。Guava EasyCyte 5 HT(商標)フローサイトメーター(Millipore,Temecula,CA)によって、蛍光(eGFP)を測定した。細胞をトリプシン処理により採取し、PBSで1回洗浄し、緩衝液(0.5% BSA、2mM EDTA、2mg/mLヨウ化プロピジウム(PI)を含むPBS)中に再懸濁させた。ヨウ化プロピジウムを使用して、細胞生存率をそのように測定し、生存細胞はPI(取り込み)に対して陰性に染色する。補正効率は、各試料中の全生細胞と比べた全eGFP陽性生細胞の割合として計算した。エラーバーは、標準誤差の計算値を使用して3セットのデータ点から生成される。
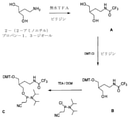
AからIへの変換のための2’-デオキシウリジン-NOC-18接合体を含む編集オリゴヌクレオチドの合成(G模倣体、図3A~C)。
5’-ジメトキシトリチル-(E)-5-(カルボメトキシビニル)-2’-デオキシウリジン-3’-ホスホラミダイトを、国際公開第2013150902号に記載のように調製する。5-カルボキシビニル-2’-デオキシウリジン残基を含有するオリゴヌクレオチド(図3A)を、ヌクレオシドホスホラミダイト構成要素を使用した標準的な自動オリゴヌクレオチド合成により調製する。このオリゴヌクレオチドに、1つ以上の所望の位置で、5’-ジメトキシトリチル-(E)-5-(カルボメトキシビニル)-2’-デオキシウリジン-3’-ホスホラミダイトを組み込む。このオリゴヌクレオチドを、室温で1時間にわたり0.5Mの水性水酸化ナトリウムを用いる処理、続いて50℃で3時間にわたり濃水酸化アンモニウムを用いる処理によって、脱保護する。粗製オリゴヌクレオチドを、アニオン交換と逆相HPLCとの組み合わせによって単離させ、精製する。配列および構造を質量分析によって確認する。
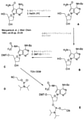
AからIへの変換(G模倣体)およびCからUへの変換のための3,5-ペンタン酸-NOC-18接合体を含むオリゴヌクレオチドの合成
A. 5-(4,4’-ジメトキシトリチル)-ペンタン酸エチルエステル3-ホスホラミダイトの合成(図4)
1. 3,5-ビス-O,O-(tert-ブチルジメチルシリル)ペンタン酸の調製(図4A)
3,5-ジヒドロキシペンタン酸を、室温で12時間にわたり、2.2当量の塩化tert-ブチルジメチルシリル(TBDMS-Cl)を含むピリジンで処理する。この混合物を、減圧下で蒸発させる。この残渣を精製せずに次のステップで使用する。
粗製3,5-ビス-O,O-(tert-ブチルジメチルシリル)ペンタン酸を、無水ピリジンと無水エタノールとの混合物(9:1)中に溶解させる。5モル当量のN,N’-ジシクロヘキシルカルボジイミドを添加し、この混合物を室温で4時間撹拌する。この溶液を濾過し、濾液を蒸発させる。この粗製生成物を次のステップで使用する。
3,5-ビス-O,O-(tert-ブチルジメチルシリル)ペンタン酸エチルエステルを、1Mのフッ化テトラブチルアンモニウム(TBAF)を含むテトラヒドロフラン中に溶解させ、室温で24時間撹拌する。この混合物を蒸発させ、無水ピリジン中に溶解させる。塩化4,4’-ジメトキシイトリチル(4,4’-dimethoxyytrityl chloride)(DMT-Cl、1.2当量)を添加し、この混合物を12時間撹拌する。この生成物をジクロロメタン(DCM)/1M塩化ナトリウムで抽出し、有機層を無水硫酸ナトリウムで乾燥させる。3-ヒドロキシ-5-(4,4’-ジメトキシトリチル)-ペンタン酸エチルエステルを、DCM-メタノール(0.1%ピリジン)でのシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。この化合物の構造を、NMRおよび質量分析によって確認する。
3-ヒドロキシ-5-(4,4’-ジメトキシトリチル)-ペンタン酸エチルエステルをDCM中に溶解させ、1当量のトリエチルアミンおよび1.1当量の2-シアノエチルN,N-ジイソプロピルクロロホスホラミダイトを添加する。2時間後、この混合物を蒸発させ、残渣を酢酸エチル中に溶解させる。粗製の1-(4,4-ジメトキシトリチル)-2-[2-リフルオロアセト(rifluoroacet)-アミド]エチル-3-ホスホラミダイトを、0.1%のピリジンを含有するヘキサン-酢酸エチルでのシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。この化合物の構造を、NMRおよび質量分析によって確認する。
1個以上の内部ペンタン酸残基を含有するオリゴヌクレオチドを、ヌクレオシドホスホラミダイト構成要素を使用した標準的な自動オリゴヌクレオチド合成により調製する。5-(4,4’-ジメトキシトリチル)-ペンタン酸エチルエステル3-ホスホラミダイトを、1つ以上の所望の位置でオリゴヌクレオチドに組み込むために使用する。このオリゴヌクレオチドを、室温で1時間にわたり0.5Mの水性水酸化ナトリウムを用いる処理、続いて50℃で3時間にわたり濃水酸化アンモニウムを用いる処理によって、脱保護する。粗製オリゴヌクレオチドを、アニオン交換と逆相HPLCとの組み合わせによって単離させ、精製する。配列および構造を質量分析によって確認する。
ペンタン酸残基を含有する1μmolのオリゴヌクレオチドを、0.1M炭酸水素ナトリウム緩衝液(pH9.5~10.0)中で、20μmolの1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド(EDAC)および20μmolのNOC-18と共にインキュベートすることによって、オリゴヌクレオチドへのNOC-18の接合を行う。EDACを2μmolに分けて10分毎に添加する。NOC-18-オリゴヌクレオチド接合体を、アニオン交換と逆相HPLCとの組み合わせによって単離させ、精製する。配列および構造を質量分析によって確認する。
CからUへの変換のためのL-システイン酸接合体を含む編集オリゴヌクレオチドの合成
A. N2-イソブチリル-7-デアザ-7-アミノメチル-2’-デオキシグアノシンの合成
1. 9-[3’,5’,N2-トリ(tert-ブチル-ジメチルシリル)-β-D-2’-デオキシリボフラノシル]-7-デアザ-7-カルバミド-6-クロロプリンの調製(図6A)
9-[3’,5’,N2-トリ(tert-ブチル-ジメチルシリル)-β-D-2’-デオキシリボフラノシル]-7-デアザ-7-カルボメトキシ-6-クロロプリン(米国特許公開第2013/0035237号)を、室温で24時間にわたり、7Mアンモニアメタノール溶液で処理する。この溶液を蒸発させ、粗製の固体を精製せずに次のステップで使用する。
9-[3’,5’,N2-トリ(tert-ブチル-ジメチルシリル)-β-D-2’-デオキシリボフラノシル]-7-デアザ-7-カルバミド-6-クロロプリンを、1MのTBAFを含むテトラヒドロフランで24時間処理する。この混合物を蒸発させ、粗製のヌクレオシドを逆相HPLCによって精製する。この化合物の構造を、NMRおよび質量分析によって確認する。
9-β-D-2’-デオキシリボフラノシル-7-デアザ-7-カルバミド-6-クロロプリンを、5モル当量の1,4-ジアザビシクロ[2.2.2]オクタン(DABCO)を含有する水中に溶解させる。この溶液を一晩還流し、粗製のヌクレオシドを逆相HPLCによって精製する。化合物の構造を、NMRおよび質量分析によって確認する。
7-デアザ-7-カルバミド-2’-デオキシグアノシンを無水ピリジンと3回同時蒸発させる。この残渣をピリジンと無水イソ酪酸との混合物(3:1)中に溶解させ、結果として生じる混合物を室温で24時間撹拌する。フラスコを氷水浴中で冷却し、等体積のメタノールをゆっくり添加する。4時間後、この混合物を蒸発させ、残渣をピリジン中に溶解させ、氷水浴中で0℃に冷却し、等体積の1M水酸化ナトリウムを添加する。20分後、過剰量のピリジニウム形態のDowex樹脂を添加する。この混合物を濾過し、Dowex樹脂を50%水性ピリジンで洗浄する。この溶液を蒸発させ、粗製の7-デアザ-7-カルバミド-N2-イソブチリル-2’-デオキシグアノシンを精製せずに次のステップで使用する。
粗製の7-デアザ-7-カルバミド-N2-イソブチリル-2’-デオキシグアノシンをメタノール中に溶解させ、厚肉ガラスバイアルに入れる。10%パラジウム炭素の粉末を添加する。この混合物を、40psiの水素圧力で24時間撹拌する。この溶液を濾過し、7-デアザ-7-アミノメチル-N2-イソブチリル-2’-デオキシグアノシンを逆相HPLCによって精製する。この化合物の構造を、NMRおよび質量分析によって確認する。
1. 5’-ジメトキシトリチル-N2-イソブチリル-7-デアザ-7-(トリフルオロアセトアミド)メチル-2’-デオキシグアノシンの調製(図7A)
7-デアザ-7-アミノメチル-N2-イソブチリル-2’-デオキシグアノシンを無水ピリジン中に溶解させ、10モル当量の無水トリフルオロ酢酸を添加する。混合物を室温で1時間撹拌する。フラスコを氷水浴中で0℃に冷却し、等体積のメタノールを添加し、30分後、この混合物を減圧下で蒸発させる。この混合物を、メタノールとさらに3回、そして無水ピリジンと2回、同時蒸発させる。結果として生じる残渣をピリジン中に溶解させる。
ジメトキシトリチル-N2-イソブチリル-7-デアザ-7-(トリフルオロアセトアミド)メチル-2’-デオキシグアノシンをDCM中に溶解させ、1当量のトリエチルアミンおよび1.1当量の2-シアノエチルN,N-ジイソプロピルクロロホスホラミダイトを添加する。2時間後、この混合物を回転蒸発装置で蒸発させ、残渣を酢酸エチル中に溶解させる。粗製の5’-ジメトキシトリチル-N2-イソブチリル-7-デアザ-7-(トリフルオロアセトアミド)メチル-2’-デオキシグアノシン3’-ホスホラミダイトを、0.1%のピリジンを含有するヘキサン-酢酸エチルでのシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。化合物の構造を、NMRおよび質量分析によって確認する。
1. 2,2,2-トリフルオロ-N-[4-ヒドロキシ-3-(ヒドロキシメチル)ブチル]アセトアミドの調製(図8A)
2-(2-アミノエチル)プロパン-1,3-ジオールを、室温で1時間にわたり、過剰量の無水トリフルオロ酢酸を含むピリジンで処理する。等体積のメタノールを添加し、2時間後、この混合物を減圧下で蒸発させ、無水ピリジンと2回同時蒸発させる。この残渣を精製せずに次のステップで使用する。
粗製の2,2,2-トリフルオロ-N-[4-ヒドロキシ-3-(ヒドロキシメチル)ブチル]アセトアミドをピリジン中に溶解させ、1.1モル当量の塩化4,4-ジメトキシトリチルを溶液に添加する。この混合物を室温で4時間撹拌する。この溶液を蒸発させ、この生成物を、0.1%のピリジンを含有するDCM-メタノールでのシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。化合物の構造を、NMRおよび質量分析によって確認する。
2,2,2-トリフルオロ-N-[4-ジメトキシトリチル-3-(ヒドロキシメチル)ブチル]アセトアミドをDCM中に溶解させ、1当量のトリエチルアミンおよび1.1当量の2-シアノエチルN,N-ジイソプロピルクロロホスホラミダイトを添加する。2時間後、この混合物を蒸発させ、残渣を酢酸エチル中に溶解させる。粗製の1-(4,4-ジメトキシトリチル)-2-[2-リフルオロアセト-アミド]エチル-3-ホスホラミダイトを、0.1%のピリジンを含有するヘキサン-酢酸エチルでのシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。化合物の構造を、NMRおよび質量分析によって確認する。
L-システイン酸(J.Mass Spectrometry,2012,V.47,pp.529-538)を、大過剰の無水トリフルオロ酢酸を含むピリジンで数時間処理する。この混合物を蒸発させ、ピリジンと2回、そしてトルエンと2回、同時蒸発させる。この粗製生成物を精製せずに使用する。
7-デアザ-7-アミノメチル-2’-デオキシグアノシン残基または2-(2-アミノエチル)-1,3-プロピレン残基を含有するオリゴヌクレオチドを、ヌクレオシドホスホラミダイト構成要素を使用した標準的な自動オリゴヌクレオチド合成により調製する。5’-ジメトキシトリチル-N2-イソブチリル-7-デアザ-7-(トリフルオロアセトアミド)メチル-2’-デオキシグアノシン3’-ホスホラミダイトまたは1-(4,4-ジメトキシトリチル)-2-[2-トリフルオロアセトアミド]エチル-3-ホスホラミダイトを、1つ以上の特定の位置でオリゴヌクレオチドに組み込むために使用する。このオリゴヌクレオチドを、50℃で3時間にわたり濃水酸化アンモニウムを用いる処理によって脱保護する。粗製オリゴヌクレオチドを、アニオン交換と逆相HPLCとの組み合わせによって単離させ、精製する。構造および配列を質量分析によって確認する。
一級アミノ基を含有するオリゴヌクレオチドのトリエチルアンモニウム塩を乾燥DMF中に溶解させ、10モル過剰の2,2,2-トリフルオロ-N-(2,2,5-トリオキソオキサチオラン-4-イル)アセトアミドを添加する。この混合物を50℃で一晩撹拌する。この混合物を5体積の100mM TEABで希釈し、アニオン交換と逆相クロマトグラフィとの組み合わせによって精製する。
GからO6-Me-Gへの変換のための2-デオキシシチジン-ニトロソアルキル接合体を含むオリゴヌクレオチド(A模倣体)の合成
1. 5’-ジメトキシトリチル-5-(E)-(3-トリフルオロアセトアミドアリル)-N4-ホルムアミジン-2’-デオキシシチジンの調製(図11A)
5-(E)-(3-トリフルオロアセトアミドアリル)-N4-ホルムアミジン-2’-デオキシシチジン(Tetrahedron Letters,2011,V.52,pp.181-183)を無水ピリジン中に溶解させ、塩化DMT(1.2当量)を添加する。この混合物を室温で6時間撹拌する。この混合物を減圧下で蒸発させ、残渣をDCM中に溶解させる。粗製の5’-ジメトキシトリチル-5-(E)-(3-トリフルオロアセトアミドアリル)-N4-ホルムアミジン-2’-デオキシシチジンを、メタノール/DCMの段階勾配を使用したシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。ヌクレオシドの構造を、NMRおよび質量分析によって確認する。
5’-ジメトキシトリチル-5-(E)-(3-トリフルオロアセトアミドアリル)-N4-ホルムアミジン-2’-デオキシシチジンをDCM中に溶解させ、1当量のトリエチルアミンおよび1.1当量の2-シアノエチルN,N-ジイソプロピルクロロホスホラミダイトを添加する。2時間後、この混合物を回転蒸発装置で蒸発させ、残渣を酢酸エチル中に溶解させる。粗製の5’-ジメトキシトリチル-E-5-(2-カルベトキシビニル)-N4-ベンゾイル-2’-デオキシシチジン3’-ホスホラミダイトを、0.1%のピリジンを含有するヘキサン-酢酸エチルでのシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。ヌクレオシドの構造を、NMRおよび質量分析によって確認する。
ヒドロキシメチルメチルニトロソアミン(Kingston Chemistryカタログ番号KST-14259951)をピリジン中に溶解させ、1.1当量の無水コハク酸を添加する。この混合物を4時間撹拌する。この粗製生成物をヘキサンで沈殿させ、次のステップで使用する。
4-[[メチル(ニトロソ)アミノ]メトキシ]-4-オキソ-ブタン酸をピリジン中に溶解させ、1当量のN-ヒドロキシスクシンイミドを添加する。その混合物に、3当量のN,N’-ジシクロヘキシルカルボジアミドを添加する。この混合物を室温で8時間撹拌する。この混合物を濾過し、粗製生成物をヘキサンで沈殿させ、次のステップで使用する。
5-アミノアリル-2’-デオキシシチジン残基または2-(2-アミノエチル)-1,3-プロピレン残基を含有するオリゴヌクレオチドを、ヌクレオシドホスホラミダイト構成要素を使用した標準的な自動オリゴヌクレオチド合成により調製する。5’-ジメトキシトリチル-5-(E)-(3-トリフルオロアセトアミドアリル)-N4-ホルムアミジン-2’-デオキシシチジン3’-ホスホラミダイトまたは1-(4,4-ジメトキシトリチル)-2-[2-トリフルオロアセトアミド]エチル-3-ホスホラミダイトを、1つ以上の特定の位置でオリゴヌクレオチドに組み込むために使用する。このオリゴヌクレオチドを、50℃で3時間にわたり濃水酸化アンモニウムを用いる処理によって脱保護する。粗製オリゴヌクレオチドを、アニオン交換と逆相HPLCとの組み合わせによって単離させ、精製する。構造および配列を質量分析によって確認する。
(図13)
一級アミノ基を含有する修飾オリゴヌクレオチドをDMF-0.1M炭酸水素ナトリウム(1:3)混合物中に溶解させ、10モル過剰の4-[[メチル(ニトロソ)アミノ]メトキシ]-4-オキソ-ブタン酸のNHSエステルを添加する。混合物を室温で2時間撹拌する。この混合物を5体積の100mM TEABで希釈し、オリゴヌクレオチド-4-[[メチル(ニトロソ)アミノ]メトキシ]-4-オキソ-ブタン酸接合体を、アニオン交換と逆相クロマトグラフィとの組み合わせによって精製する。非ヌクレオシド単位を含むオリゴヌクレオチドは、GからO6-MeGへの変換アデノシン模倣体)のため、またはUからO4-MeUへの変換(シチジン模倣体)のために使用することができる。
UからO4-Me-Uへの変換のための2’-デオキシアデノシン-ニトロソ-N-メチル接合体を含む編集オリゴヌクレオチド(シチジン模倣体)の合成
A. 7-デアザ-7-アミノメチル-N-ベンゾイル-5’-DMT-dA-ホスホラミダイトの合成
1. 7-デアザ-7-カルボキサミド-N6-ベンゾイル-2’-デオキシアデノシンの調製(図14A)
2’-デオキシサンギバマイシン(Maruyama et.al.J.Med.Cmem.1983,vol.26 pp.25-29)を無水ピリジンと3回同時蒸発させる。次いでこの残渣をピリジンと塩化ベンゾイルとの混合物(9:1)中に溶解させ、結果として生じる混合物を室温で24時間撹拌する。フラスコを氷水浴中で冷却し、等体積のメタノールをゆっくり添加する。メタノールを添加したら、この混合物を1時間静置させる。この溶液を蒸発させ、粗製の7-デアザ-7-カルボキサミド-N6-ベンゾイル-2’-デオキシアデノシンを、メタノール/DCMの段階勾配を使用したシリカゲルクロマトグラフィによって、または代替的に、アセトニトリル/100mM炭酸水素トリエチルアンモニウム勾配での逆相HPLCによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。ヌクレオシドの構造を、NMRおよび質量分析によって確認する。
7-デアザ-7-カルボキサミド-N6-ベンゾイル-2’-デオキシアデノシンを、室温で12時間にわたり、水素化ジイソブチルアルミニウム(3モル当量)を含むTHFの1M溶液で処理する。この混合物を、勢いよく撹拌したロッシェル塩溶液(1.2Mの水性酒石酸カリウムナトリウム)中に注ぐ。この溶液を2時間勢いよく撹拌し、混合物をDCMで抽出する。有機層を硫酸ナトリウムで乾燥させ、蒸発させる。粗製の7-デアザ-7-アミノメチル-N6-ベンゾイル-2’-デオキシアデノシンを、アセトニトリル/100mM炭酸水素トリエチルアンモニウム勾配での逆相クロマトグラフィによって精製する。純粋な7-デアザ-7-アミノメチル-N6-ベンゾイル-2’-デオキシアデノシンを含有する留分を合わせ、蒸発させ、メタノールと、そして無水ピリジンと2回、同時蒸発させる。
7-デアザ-7-アミノメチル-N6-ベンゾイル-2’-デオキシアデノシンを無水ピリジン中に溶解させ、10モル当量の無水トリフルオロ酢酸を添加する。混合物を室温で1時間撹拌する。フラスコを氷水浴中で0℃に冷却し、等体積のメタノールを添加し、30分後、この混合物を減圧下で蒸発させる。この混合物を、メタノールと3回、そして無水ピリジンと2回、同時蒸発させる。この残渣をピリジン中に溶解させる。
5’-ジメトキシトリチル-N6-ベンゾイル-7-デアザ-7-(トリフルオロアセトアミド)メチル-2’-デオキシアデノシンをDCM中に溶解させ、1当量のトリエチルアミンおよび1.1当量の2-シアノエチルN,N-ジイソプロピルクロロホスホラミダイトを添加する。2時間後、この混合物を回転蒸発装置で蒸発させ、残渣を酢酸エチル中に溶解させる。粗製の5’-ジメトキシトリチル-N6-ベンゾイル-7-デアザ-7-(トリフルオロアセトアミド)メチル-2’-デオキシアデノシン3’-ホスホラミダイトを、0.1%のピリジンを含有するヘキサン-酢酸エチルでのシリカゲルクロマトグラフィによって精製する。純粋な生成物を含有する留分を合わせ、蒸発させ、高真空で乾燥させる。ヌクレオシドの構造を、NMRおよび質量分析によって確認する。
7-デアザ-7-アミノメチル-2’-デオキシアデノシン残基または2-(2-アミノエチル)-1,3-プロピレン残基を含有するオリゴヌクレオチドを、ヌクレオシドホスホラミダイト構成要素を使用した標準的な自動オリゴヌクレオチド合成により調製する。5’-ジメトキシトリチル-N6-ベンゾイル-7-デアザ-7-(トリフルオロアセトアミド)メチル-2’-デオキシアデノシン3’-ホスホラミダイトまたは1-(4,4-ジメトキシトリチル)-2-[2-トリフルオロアセトアミド]エチル-3-ホスホラミダイトを、1つ以上の特定の位置でオリゴヌクレオチドに組み込むために使用する。このオリゴヌクレオチドを、50℃で3時間にわたり濃水酸化アンモニウムを用いる処理によって脱保護する。粗製オリゴヌクレオチドを、アニオン交換と逆相HPLCとの組み合わせによって単離させ、精製する。構造および配列を質量分析によって確認する。
一級アミノ基を含有する修飾オリゴヌクレオチドをDMF-0.1M炭酸水素ナトリウム(1:3)混合物中に溶解させ、10モル過剰の4-[[メチル(ニトロソ)アミノ]メトキシ]-4-オキソ-ブタン酸のエステルを添加する。この混合物を室温で2時間撹拌する。次いでこの混合物を5体積の100mM炭酸水素トリエチルアンモニウムで希釈し、オリゴヌクレオチド-4-[[メチル(ニトロソ)アミノ]メトキシ]-4-オキソ-ブタン酸接合体を、アニオン交換と逆相クロマトグラフィとの組み合わせによって精製する。
ニトロソアミンメチル化基を含有する編集オリゴヌクレオチドを使用した、mRNAにおけるUからO4-Me-Uへの変換スキーム(図16)
1つの概略的な合成法の一例を図16に示す。
ニトロソアミンメチル化基を含有する編集オリゴヌクレオチドを使用した、mRNAにおけるGからO6-Me-Gへの変換スキーム(図17)
1つの概略的な合成法の一例を図17に示す。
亜硫酸水素塩生成基を含有する編集オリゴヌクレオチドを使用した、mRNAにおけるCからUへの変換スキーム(図18)
1つの概略的な合成法の一例を図18に示す。
編集オリゴヌクレオチドの長さおよび位置決めの最適化のためのプロセス
編集オリゴヌクレオチドが編集部位のおよそ中央(中央の編集部位)に位置するように編集オリゴヌクレオチドを位置付けることは、典型的にいくらかのレベルの編集効率をもたらすが、それは必ずしも最適とは限らない。変異補正、または他の標的配列変化を標的にする(例えば、特定の保護的アレルを作り出す)とき、全体的な標的部位は、所望の配列変化の位置によって決定される。この場合、任意選択の長さの最適化、および標的部位に沿った編集オリゴヌクレオチドの5’-3’位置決めは、いくぶんか拘束され、次のように行うことができる。DNA標的の場合、編集オリゴヌクレオチドは、標的DNAのセンスまたはアンチセンス鎖を標的にするように設計することができる。RNA標的の場合、編集オリゴヌクレオチドは、標的RNAに対して相補的にのみ設計することができる。DNAを標的にする場合とRNAを標的にする場合との両方において、最適化は、標的変異上のおよそ中央に位置する親編集オリゴヌクレオチドから開始することができる。この編集オリゴヌクレオチドは、本明細書に記載される化学修飾パターンのうちの1つを有することができる。好ましくは、部位のスクリーニングのために使用される最初の編集オリゴヌクレオチドは、長さならびに5’および3’の位置決めが単純に変化してもよい、簡素な末端ブロック修飾パターンを有し得る。標的核酸塩基の化学修飾により機能する編集オリゴヌクレオチドの場合、その塩基修飾活性は、標的核酸塩基の付近に位置したままである必要がある。
Claims (7)
- 疾患を引き起こさないアミノ酸を生じる、標的核酸内の変異コドンを修飾するための方法に用いられる医薬組成物であって、該方法は、前記変異コドンを有するかもしくは有する疑いのある個体に、一本鎖の化学修飾オリゴヌクレオチドを投与するステップを含み、前記オリゴヌクレオチドが、標的配列に対する1つ以上のミスマッチを例外として前記ゲノム配列内の標的配列に相補的であり、前記オリゴヌクレオチドの前記修飾が、各末端上に3個のホスホロチオエートを有するオリゴヌクレオチドと比較してヌクレアーゼ安定性を増加させることによって、編集の効率を上昇させ、
前記オリゴヌクレオチドは下記の修飾パターン:
3’8個の2’F高親和性ヌクレオチドアーム及びホスホロチオエート末端ブロック;
5’に非ホスホロチオエート末端ブロック(メチホスホネート)、3’に3個のs末端ブロック;および
5’メチルCにより置換された複数のC、
の1つを含む方法である、
前記化学修飾オリゴヌクレオチドを含む医薬組成物。 - タンパク質をコードする核酸を修飾して、前記タンパク質の活性を調整するための方法に用いられる医薬組成物であって、該方法は、
前記ゲノム配列の編集を補助する追加の外因性タンパク質または核酸を用いずに、個体に、一本鎖の化学修飾オリゴヌクレオチドを投与するステップを含み、前記オリゴヌクレオチドが、標的配列に対する1つ以上のミスマッチを例外として前記ゲノム配列内の標的配列に相補的であり、前記オリゴヌクレオチドの前記修飾が、各末端上に3個のホスホロチオエートを有するオリゴヌクレオチドと比較してヌクレアーゼ安定性を増加させることによって、編集の効率を上昇させ、前記タンパク質の活性が調整され、
前記オリゴヌクレオチドは下記の修飾パターン:
3’8個の2’F高親和性ヌクレオチドアーム及びホスホロチオエート末端ブロック;
5’に非ホスホロチオエート末端ブロック(メチホスホネート)、3’に3個のs末端ブロック;および
5’メチルCにより置換された複数のC、
の1つを含む方法である、
前記化学修飾オリゴヌクレオチドを含む医薬組成物。 - 変異タンパク質をコードする核酸を修飾して、その疾患による影響を抑制するための方法に用いられる医薬組成物であって、該方法は、個体に、一本鎖の化学修飾オリゴヌクレオチドを投与するステップを含み、前記オリゴヌクレオチドが、標的配列に対する1つ以上のミスマッチを例外として前記ゲノム配列内の標的配列に相補的であり、前記オリゴヌクレオチドの前記修飾が、各末端上に3個のホスホロチオエートを有するオリゴヌクレオチドと比較してヌクレアーゼ安定性を増加させることによって、編集の効率を上昇させ、前記変異タンパク質の疾患を引き起こす作用が、減少するか、抑制されるか、または排除され、
前記オリゴヌクレオチドは下記の修飾パターン:
3’8個の2’F高親和性ヌクレオチドアーム及びホスホロチオエート末端ブロック;
5’に非ホスホロチオエート末端ブロック(メチホスホネート)、3’に3個のs末端ブロック;および
5’メチルsCにより置換された複数のC、
の1つを含む方法である、
前記化学修飾オリゴヌクレオチドを含む医薬組成物。 - 前記疾患が、ベータサラセミア、嚢胞性線維症、デュシェンヌ型筋ジストロフィー、またはハーラー症候群である、請求項1~3のいずれかに記載の医薬組成物。
- 前記医学的状態が、アルツハイマー病、乳がん素因変異、嚢胞性線維症デルタ508変異、2型糖尿病(標的遺伝子PTP-1B)、家族性自律神経障害、家族性高コレステロール血症(PCSK9)、卵巣がん素因変異、鎌状赤血球症、および脊髄性筋萎縮症から成る群から選択される、請求項1~3のいずれかに記載の医薬組成物。
- 前記医学的状態が、2型糖尿病であり、前記編集オリゴヌクレオチドが、前記PTP-1B遺伝子を標的にする、請求項1~3のいずれかに記載の医薬組成物。
- 前記医学的状態が、アデノシンデアミナーゼ欠損症、アルファ1アンチトリプシン欠損症、アミロイド病、ベッカー型筋ジストロフィー、カナバン病、シャルコー・マリー・トゥース病、嚢胞性線維症、1型糖尿病、デュシェンヌ型筋ジストロフィー、ファブリー病、家族性大腸腺腫症、家族性アミロイド心筋症、家族性アミロイド多発ニューロパチー、フリートライヒ運動失調症、ゴーシェ病I型、ゴーシェ病II、糖原貯蔵障害II型、GM2ガングリオシドーシス、血色素症、血友病A、血友病B、血友病C、ヘキソサミニダーゼA欠損症、フェニルケトン尿症、多嚢胞性腎疾患、プリオン病、老人性全身性アミロイドーシス、スミス・レムリ・オピッツ症候群、ウィルソン病、および遺伝性盲目から成る群から選択される、請求項1~3のいずれかに記載の医薬組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021159689A JP2022008651A (ja) | 2014-12-12 | 2021-09-29 | オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 |
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462091027P | 2014-12-12 | 2014-12-12 | |
| US62/091,027 | 2014-12-12 | ||
| US201562141077P | 2015-03-31 | 2015-03-31 | |
| US62/141,077 | 2015-03-31 | ||
| US201562180175P | 2015-06-16 | 2015-06-16 | |
| US62/180,175 | 2015-06-16 | ||
| US201562252693P | 2015-11-09 | 2015-11-09 | |
| US62/252,693 | 2015-11-09 | ||
| PCT/US2015/065348 WO2016094845A2 (en) | 2014-12-12 | 2015-12-11 | Compositions and methods for editing nucleic acids in cells utilizing oligonucleotides |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021159689A Division JP2022008651A (ja) | 2014-12-12 | 2021-09-29 | オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018506297A JP2018506297A (ja) | 2018-03-08 |
| JP2018506297A5 JP2018506297A5 (ja) | 2019-01-31 |
| JP6997623B2 true JP6997623B2 (ja) | 2022-02-04 |
Family
ID=56108384
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017550092A Active JP6997623B2 (ja) | 2014-12-12 | 2015-12-11 | オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 |
| JP2021159689A Pending JP2022008651A (ja) | 2014-12-12 | 2021-09-29 | オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021159689A Pending JP2022008651A (ja) | 2014-12-12 | 2021-09-29 | オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 |
Country Status (5)
| Country | Link |
|---|---|
| EP (1) | EP3230445B1 (ja) |
| JP (2) | JP6997623B2 (ja) |
| CN (1) | CN107532162A (ja) |
| CA (1) | CA2969464A1 (ja) |
| WO (1) | WO2016094845A2 (ja) |
Families Citing this family (48)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10323236B2 (en) | 2011-07-22 | 2019-06-18 | President And Fellows Of Harvard College | Evaluation and improvement of nuclease cleavage specificity |
| US9163284B2 (en) | 2013-08-09 | 2015-10-20 | President And Fellows Of Harvard College | Methods for identifying a target site of a Cas9 nuclease |
| US9359599B2 (en) | 2013-08-22 | 2016-06-07 | President And Fellows Of Harvard College | Engineered transcription activator-like effector (TALE) domains and uses thereof |
| US9322037B2 (en) | 2013-09-06 | 2016-04-26 | President And Fellows Of Harvard College | Cas9-FokI fusion proteins and uses thereof |
| US9340800B2 (en) | 2013-09-06 | 2016-05-17 | President And Fellows Of Harvard College | Extended DNA-sensing GRNAS |
| US9526784B2 (en) | 2013-09-06 | 2016-12-27 | President And Fellows Of Harvard College | Delivery system for functional nucleases |
| US9068179B1 (en) | 2013-12-12 | 2015-06-30 | President And Fellows Of Harvard College | Methods for correcting presenilin point mutations |
| AU2015298571B2 (en) | 2014-07-30 | 2020-09-03 | President And Fellows Of Harvard College | Cas9 proteins including ligand-dependent inteins |
| US20210395729A1 (en) * | 2014-12-12 | 2021-12-23 | Tod M. Woolf | Compositions and methods for Editing Nucleic Acids in Cells Utilizing Oligonucleotides |
| CN107532162A (zh) * | 2014-12-12 | 2018-01-02 | 托德·M·伍尔夫 | 用于利用寡核苷酸编辑细胞中核酸的组合物和方法 |
| DK3234134T3 (da) | 2014-12-17 | 2020-07-27 | Proqr Therapeutics Ii Bv | Målrettet rna-redigering |
| IL258821B (en) | 2015-10-23 | 2022-07-01 | Harvard College | Nucleobase editors and their uses |
| US20190300872A1 (en) * | 2016-05-06 | 2019-10-03 | Tod M. Woolf | Improved Methods of Genome Editing with and without Programmable Nucleases |
| WO2017220751A1 (en) | 2016-06-22 | 2017-12-28 | Proqr Therapeutics Ii B.V. | Single-stranded rna-editing oligonucleotides |
| KR102547316B1 (ko) | 2016-08-03 | 2023-06-23 | 프레지던트 앤드 펠로우즈 오브 하바드 칼리지 | 아데노신 핵염기 편집제 및 그의 용도 |
| CN109804066A (zh) | 2016-08-09 | 2019-05-24 | 哈佛大学的校长及成员们 | 可编程cas9-重组酶融合蛋白及其用途 |
| WO2018030536A1 (ja) * | 2016-08-12 | 2018-02-15 | 国立大学法人徳島大学 | ゲノム編集方法 |
| WO2018039438A1 (en) | 2016-08-24 | 2018-03-01 | President And Fellows Of Harvard College | Incorporation of unnatural amino acids into proteins using base editing |
| CN110352244B (zh) | 2016-09-01 | 2023-03-21 | ProQR治疗上市公司Ⅱ | 化学修饰的编辑rna的单链寡核苷酸 |
| KR102622411B1 (ko) | 2016-10-14 | 2024-01-10 | 프레지던트 앤드 펠로우즈 오브 하바드 칼리지 | 핵염기 에디터의 aav 전달 |
| WO2018119359A1 (en) | 2016-12-23 | 2018-06-28 | President And Fellows Of Harvard College | Editing of ccr5 receptor gene to protect against hiv infection |
| KR102569848B1 (ko) * | 2016-12-23 | 2023-08-25 | 프레지던트 앤드 펠로우즈 오브 하바드 칼리지 | Pcsk9의 유전자 편집 |
| US11274300B2 (en) | 2017-01-19 | 2022-03-15 | Proqr Therapeutics Ii B.V. | Oligonucleotide complexes for use in RNA editing |
| WO2018161032A1 (en) | 2017-03-03 | 2018-09-07 | The Regents Of The University Of California | RNA TARGETING OF MUTATIONS VIA SUPPRESSOR tRNAs AND DEAMINASES |
| WO2018165504A1 (en) | 2017-03-09 | 2018-09-13 | President And Fellows Of Harvard College | Suppression of pain by gene editing |
| US11542496B2 (en) | 2017-03-10 | 2023-01-03 | President And Fellows Of Harvard College | Cytosine to guanine base editor |
| GB2575930A (en) | 2017-03-23 | 2020-01-29 | Harvard College | Nucleobase editors comprising nucleic acid programmable DNA binding proteins |
| US11560566B2 (en) | 2017-05-12 | 2023-01-24 | President And Fellows Of Harvard College | Aptazyme-embedded guide RNAs for use with CRISPR-Cas9 in genome editing and transcriptional activation |
| JP2020534795A (ja) | 2017-07-28 | 2020-12-03 | プレジデント アンド フェローズ オブ ハーバード カレッジ | ファージによって支援される連続的進化(pace)を用いて塩基編集因子を進化させるための方法および組成物 |
| CN107267516B (zh) * | 2017-07-28 | 2020-09-29 | 佛山科学技术学院 | 双sgRNA介导的基因精确修饰方法及应用 |
| EP3676376A2 (en) | 2017-08-30 | 2020-07-08 | President and Fellows of Harvard College | High efficiency base editors comprising gam |
| WO2019079347A1 (en) | 2017-10-16 | 2019-04-25 | The Broad Institute, Inc. | USES OF BASIC EDITORS ADENOSINE |
| WO2019104094A2 (en) | 2017-11-21 | 2019-05-31 | The Regents Of The University Of California | Fusion proteins and methods for site-directed genome editing |
| KR20200119242A (ko) | 2018-01-08 | 2020-10-19 | 이오반스 바이오테라퓨틱스, 인크. | 종양 항원-특이적 t-세포에 대해 풍부화된 til 생성물의 생성 방법 |
| WO2019136459A1 (en) | 2018-01-08 | 2019-07-11 | Iovance Biotherapeutics, Inc. | Processes for generating til products enriched for tumor antigen-specific t-cells |
| KR20210076082A (ko) * | 2018-10-12 | 2021-06-23 | 페킹 유니버시티 | Rna를 편집하기 위한 방법 및 조성물 |
| TW202043468A (zh) | 2019-01-22 | 2020-12-01 | 美商科羅生物公司 | Rna編輯之寡核苷酸及其用途 |
| EP3914261A4 (en) | 2019-01-22 | 2023-06-28 | Korro Bio, Inc. | Rna-editing oligonucleotides and uses thereof |
| JP2020124155A (ja) * | 2019-02-05 | 2020-08-20 | 国立大学法人北陸先端科学技術大学院大学 | タンパク質を生合成させる方法および未成熟終止コドンの修飾方法 |
| WO2020191249A1 (en) | 2019-03-19 | 2020-09-24 | The Broad Institute, Inc. | Methods and compositions for editing nucleotide sequences |
| CR20210572A (es) | 2019-04-15 | 2022-04-07 | Univ Beijing | Métodos y composiciones para editar ácido ribonucleicos (arn) |
| AU2020313143B2 (en) | 2019-07-12 | 2024-04-04 | Peking University | Targeted RNA editing by leveraging endogenous adar using engineered RNAs |
| EP4069842A1 (en) * | 2019-12-02 | 2022-10-12 | Shape Therapeutics Inc. | Therapeutic editing |
| BR112022020795A2 (pt) * | 2020-04-15 | 2022-11-29 | Edigene Therapeutics Beijing Inc | Métodos para edição alvejada de um ácido ribonucleico alvo e para prevenir ou tratar síndrome de hurler, ácido ribonucleico de recrutamento da adenosina desaminase engenheirado, construção, e, composição, lipossoma, exossoma, nanopartícula de lipídeo, célula, biblioteca ou kit |
| MX2022014008A (es) | 2020-05-08 | 2023-02-09 | Broad Inst Inc | Métodos y composiciones para la edición simultánea de ambas cadenas de una secuencia de nucleótidos de doble cadena objetivo. |
| EP4349983A1 (en) * | 2021-05-27 | 2024-04-10 | National Institute Of Advanced Industrial Science and Technology | Genome editing method |
| CN113666847A (zh) * | 2021-08-31 | 2021-11-19 | 派普医药(江苏)有限公司 | 一种odmt,n-fmoc-氨基丁基-1,3-丙二醇的合成方法 |
| WO2023190848A1 (ja) * | 2022-03-30 | 2023-10-05 | 国立研究開発法人産業技術総合研究所 | 一本鎖形態のポリヌクレオチド及びゲノム編集におけるその利用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014144951A1 (en) | 2013-03-15 | 2014-09-18 | Cibus Us Llc | Methods and compositions for increasing efficiency of increased efficiency of targeted gene modification using oligonucleotide-mediated gene repair |
| WO2015139008A1 (en) | 2014-03-14 | 2015-09-17 | Cibus Us Llc | Methods and compositions for increasing efficiency of targeted gene modification using oligonucleotide-mediated gene repair |
Family Cites Families (111)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3687808A (en) | 1969-08-14 | 1972-08-29 | Univ Leland Stanford Junior | Synthetic polynucleotides |
| DE3023787A1 (de) | 1980-06-25 | 1982-01-21 | Studiengesellschaft Kohle mbH, 4330 Mülheim | Verfahren zur erhoehung der inkorporation und der expression von genetischem material in die kerne von intakten zellen mit hilfe von liposomen |
| US4469863A (en) | 1980-11-12 | 1984-09-04 | Ts O Paul O P | Nonionic nucleic acid alkyl and aryl phosphonates and processes for manufacture and use thereof |
| US5023243A (en) | 1981-10-23 | 1991-06-11 | Molecular Biosystems, Inc. | Oligonucleotide therapeutic agent and method of making same |
| US4476301A (en) | 1982-04-29 | 1984-10-09 | Centre National De La Recherche Scientifique | Oligonucleotides, a process for preparing the same and their application as mediators of the action of interferon |
| US4522811A (en) | 1982-07-08 | 1985-06-11 | Syntex (U.S.A.) Inc. | Serial injection of muramyldipeptides and liposomes enhances the anti-infective activity of muramyldipeptides |
| US5550111A (en) | 1984-07-11 | 1996-08-27 | Temple University-Of The Commonwealth System Of Higher Education | Dual action 2',5'-oligoadenylate antiviral derivatives and uses thereof |
| US5367066A (en) | 1984-10-16 | 1994-11-22 | Chiron Corporation | Oligonucleotides with selectably cleavable and/or abasic sites |
| FR2575751B1 (fr) | 1985-01-08 | 1987-04-03 | Pasteur Institut | Nouveaux nucleosides de derives de l'adenosine, leur preparation et leurs applications biologiques |
| US5166315A (en) | 1989-12-20 | 1992-11-24 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| US5235033A (en) | 1985-03-15 | 1993-08-10 | Anti-Gene Development Group | Alpha-morpholino ribonucleoside derivatives and polymers thereof |
| US5185444A (en) | 1985-03-15 | 1993-02-09 | Anti-Gene Deveopment Group | Uncharged morpolino-based polymers having phosphorous containing chiral intersubunit linkages |
| US5034506A (en) | 1985-03-15 | 1991-07-23 | Anti-Gene Development Group | Uncharged morpholino-based polymers having achiral intersubunit linkages |
| US5405938A (en) | 1989-12-20 | 1995-04-11 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| US5276019A (en) | 1987-03-25 | 1994-01-04 | The United States Of America As Represented By The Department Of Health And Human Services | Inhibitors for replication of retroviruses and for the expression of oncogene products |
| US5264423A (en) | 1987-03-25 | 1993-11-23 | The United States Of America As Represented By The Department Of Health And Human Services | Inhibitors for replication of retroviruses and for the expression of oncogene products |
| AU598946B2 (en) | 1987-06-24 | 1990-07-05 | Howard Florey Institute Of Experimental Physiology And Medicine | Nucleoside derivatives |
| US4924624A (en) | 1987-10-22 | 1990-05-15 | Temple University-Of The Commonwealth System Of Higher Education | 2,',5'-phosphorothioate oligoadenylates and plant antiviral uses thereof |
| US5188897A (en) | 1987-10-22 | 1993-02-23 | Temple University Of The Commonwealth System Of Higher Education | Encapsulated 2',5'-phosphorothioate oligoadenylates |
| EP0406309A4 (en) | 1988-03-25 | 1992-08-19 | The University Of Virginia Alumni Patents Foundation | Oligonucleotide n-alkylphosphoramidates |
| US5278302A (en) | 1988-05-26 | 1994-01-11 | University Patents, Inc. | Polynucleotide phosphorodithioates |
| US5216141A (en) | 1988-06-06 | 1993-06-01 | Benner Steven A | Oligonucleotide analogs containing sulfur linkages |
| US5175273A (en) | 1988-07-01 | 1992-12-29 | Genentech, Inc. | Nucleic acid intercalating agents |
| US5134066A (en) | 1989-08-29 | 1992-07-28 | Monsanto Company | Improved probes using nucleosides containing 3-dezauracil analogs |
| US5399676A (en) | 1989-10-23 | 1995-03-21 | Gilead Sciences | Oligonucleotides with inverted polarity |
| US5264564A (en) | 1989-10-24 | 1993-11-23 | Gilead Sciences | Oligonucleotide analogs with novel linkages |
| US5264562A (en) | 1989-10-24 | 1993-11-23 | Gilead Sciences, Inc. | Oligonucleotide analogs with novel linkages |
| ATE157012T1 (de) | 1989-11-03 | 1997-09-15 | Univ Vanderbilt | Verfahren zur in vivo-verabreichung von funktionsfähigen fremden genen |
| US5177198A (en) | 1989-11-30 | 1993-01-05 | University Of N.C. At Chapel Hill | Process for preparing oligoribonucleoside and oligodeoxyribonucleoside boranophosphates |
| US5223168A (en) | 1989-12-12 | 1993-06-29 | Gary Holt | Surface cleaner and treatment |
| US5130302A (en) | 1989-12-20 | 1992-07-14 | Boron Bilogicals, Inc. | Boronated nucleoside, nucleotide and oligonucleotide compounds, compositions and methods for using same |
| US5578718A (en) | 1990-01-11 | 1996-11-26 | Isis Pharmaceuticals, Inc. | Thiol-derivatized nucleosides |
| US5587361A (en) | 1991-10-15 | 1996-12-24 | Isis Pharmaceuticals, Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| US5459255A (en) | 1990-01-11 | 1995-10-17 | Isis Pharmaceuticals, Inc. | N-2 substituted purines |
| US5212295A (en) | 1990-01-11 | 1993-05-18 | Isis Pharmaceuticals | Monomers for preparation of oligonucleotides having chiral phosphorus linkages |
| US5681941A (en) | 1990-01-11 | 1997-10-28 | Isis Pharmaceuticals, Inc. | Substituted purines and oligonucleotide cross-linking |
| US5587470A (en) | 1990-01-11 | 1996-12-24 | Isis Pharmaceuticals, Inc. | 3-deazapurines |
| US5457191A (en) | 1990-01-11 | 1995-10-10 | Isis Pharmaceuticals, Inc. | 3-deazapurines |
| US5506351A (en) | 1992-07-23 | 1996-04-09 | Isis Pharmaceuticals | Process for the preparation of 2'-O-alkyl guanosine and related compounds |
| US5321131A (en) | 1990-03-08 | 1994-06-14 | Hybridon, Inc. | Site-specific functionalization of oligodeoxynucleotides for non-radioactive labelling |
| US5470967A (en) | 1990-04-10 | 1995-11-28 | The Dupont Merck Pharmaceutical Company | Oligonucleotide analogs with sulfamate linkages |
| US5602240A (en) | 1990-07-27 | 1997-02-11 | Ciba Geigy Ag. | Backbone modified oligonucleotide analogs |
| WO1992002258A1 (en) | 1990-07-27 | 1992-02-20 | Isis Pharmaceuticals, Inc. | Nuclease resistant, pyrimidine modified oligonucleotides that detect and modulate gene expression |
| US5218105A (en) | 1990-07-27 | 1993-06-08 | Isis Pharmaceuticals | Polyamine conjugated oligonucleotides |
| US5138045A (en) | 1990-07-27 | 1992-08-11 | Isis Pharmaceuticals | Polyamine conjugated oligonucleotides |
| US5378825A (en) | 1990-07-27 | 1995-01-03 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs |
| US5618704A (en) | 1990-07-27 | 1997-04-08 | Isis Pharmacueticals, Inc. | Backbone-modified oligonucleotide analogs and preparation thereof through radical coupling |
| US5608046A (en) | 1990-07-27 | 1997-03-04 | Isis Pharmaceuticals, Inc. | Conjugated 4'-desmethyl nucleoside analog compounds |
| US5541307A (en) | 1990-07-27 | 1996-07-30 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs and solid phase synthesis thereof |
| US5610289A (en) | 1990-07-27 | 1997-03-11 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogues |
| US5623070A (en) | 1990-07-27 | 1997-04-22 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5677437A (en) | 1990-07-27 | 1997-10-14 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5386023A (en) | 1990-07-27 | 1995-01-31 | Isis Pharmaceuticals | Backbone modified oligonucleotide analogs and preparation thereof through reductive coupling |
| US5489677A (en) | 1990-07-27 | 1996-02-06 | Isis Pharmaceuticals, Inc. | Oligonucleoside linkages containing adjacent oxygen and nitrogen atoms |
| DK0541722T3 (da) | 1990-08-03 | 1996-04-22 | Sterling Winthrop Inc | Forbindelser og fremgangsmåder til inhibering af genekspression |
| US6262241B1 (en) | 1990-08-13 | 2001-07-17 | Isis Pharmaceuticals, Inc. | Compound for detecting and modulating RNA activity and gene expression |
| US5177196A (en) | 1990-08-16 | 1993-01-05 | Microprobe Corporation | Oligo (α-arabinofuranosyl nucleotides) and α-arabinofuranosyl precursors thereof |
| US5214134A (en) | 1990-09-12 | 1993-05-25 | Sterling Winthrop Inc. | Process of linking nucleosides with a siloxane bridge |
| US5561225A (en) | 1990-09-19 | 1996-10-01 | Southern Research Institute | Polynucleotide analogs containing sulfonate and sulfonamide internucleoside linkages |
| CA2092002A1 (en) | 1990-09-20 | 1992-03-21 | Mark Matteucci | Modified internucleoside linkages |
| US5432272A (en) | 1990-10-09 | 1995-07-11 | Benner; Steven A. | Method for incorporating into a DNA or RNA oligonucleotide using nucleotides bearing heterocyclic bases |
| US5719262A (en) | 1993-11-22 | 1998-02-17 | Buchardt, Deceased; Ole | Peptide nucleic acids having amino acid side chains |
| US5539082A (en) | 1993-04-26 | 1996-07-23 | Nielsen; Peter E. | Peptide nucleic acids |
| US5714331A (en) | 1991-05-24 | 1998-02-03 | Buchardt, Deceased; Ole | Peptide nucleic acids having enhanced binding affinity, sequence specificity and solubility |
| JPH07502339A (ja) | 1991-07-25 | 1995-03-09 | ザ ホイッタカー コーポレイション | 液位センサ |
| US5571799A (en) | 1991-08-12 | 1996-11-05 | Basco, Ltd. | (2'-5') oligoadenylate analogues useful as inhibitors of host-v5.-graft response |
| US5599797A (en) | 1991-10-15 | 1997-02-04 | Isis Pharmaceuticals, Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| US5594121A (en) | 1991-11-07 | 1997-01-14 | Gilead Sciences, Inc. | Enhanced triple-helix and double-helix formation with oligomers containing modified purines |
| US5484908A (en) | 1991-11-26 | 1996-01-16 | Gilead Sciences, Inc. | Oligonucleotides containing 5-propynyl pyrimidines |
| US5633360A (en) | 1992-04-14 | 1997-05-27 | Gilead Sciences, Inc. | Oligonucleotide analogs capable of passive cell membrane permeation |
| US5434257A (en) | 1992-06-01 | 1995-07-18 | Gilead Sciences, Inc. | Binding compentent oligomers containing unsaturated 3',5' and 2',5' linkages |
| US5476925A (en) | 1993-02-01 | 1995-12-19 | Northwestern University | Oligodeoxyribonucleotides including 3'-aminonucleoside-phosphoramidate linkages and terminal 3'-amino groups |
| GB9304618D0 (en) | 1993-03-06 | 1993-04-21 | Ciba Geigy Ag | Chemical compounds |
| CA2159629A1 (en) | 1993-03-31 | 1994-10-13 | Sanofi | Oligonucleotides with amide linkages replacing phosphodiester linkages |
| US5571902A (en) | 1993-07-29 | 1996-11-05 | Isis Pharmaceuticals, Inc. | Synthesis of oligonucleotides |
| US5502177A (en) | 1993-09-17 | 1996-03-26 | Gilead Sciences, Inc. | Pyrimidine derivatives for labeled binding partners |
| US5457187A (en) | 1993-12-08 | 1995-10-10 | Board Of Regents University Of Nebraska | Oligonucleotides containing 5-fluorouracil |
| US5596091A (en) | 1994-03-18 | 1997-01-21 | The Regents Of The University Of California | Antisense oligonucleotides comprising 5-aminoalkyl pyrimidine nucleotides |
| US5625050A (en) | 1994-03-31 | 1997-04-29 | Amgen Inc. | Modified oligonucleotides and intermediates useful in nucleic acid therapeutics |
| US5554746A (en) | 1994-05-16 | 1996-09-10 | Isis Pharmaceuticals, Inc. | Lactam nucleic acids |
| US5525711A (en) | 1994-05-18 | 1996-06-11 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Pteridine nucleotide analogs as fluorescent DNA probes |
| AU2522095A (en) | 1994-05-19 | 1995-12-18 | Dako A/S | Pna probes for detection of neisseria gonorrhoeae and chlamydia trachomatis |
| US20020055479A1 (en) * | 2000-01-18 | 2002-05-09 | Cowsert Lex M. | Antisense modulation of PTP1B expression |
| US8273866B2 (en) | 2002-02-20 | 2012-09-25 | Merck Sharp & Dohme Corp. | RNA interference mediated inhibition of gene expression using chemically modified short interfering nucleic acid (SINA) |
| US8202979B2 (en) | 2002-02-20 | 2012-06-19 | Sirna Therapeutics, Inc. | RNA interference mediated inhibition of gene expression using chemically modified short interfering nucleic acid |
| ATE335754T1 (de) * | 2001-03-19 | 2006-09-15 | Harvard College | Entwicklung neuer molekularer funktionen |
| US20030045830A1 (en) * | 2001-04-17 | 2003-03-06 | De Bizemont Therese | Gene therapy with chimeric oligonucleotides delivered by a method comprising a step of iontophoresis |
| US20060009409A1 (en) | 2002-02-01 | 2006-01-12 | Woolf Tod M | Double-stranded oligonucleotides |
| US8232383B2 (en) | 2002-02-20 | 2012-07-31 | Sirna Therapeutics, Inc. | RNA interference mediated inhibition of gene expression using chemically modified short interfering nucleic acid (siNA) |
| US9181551B2 (en) | 2002-02-20 | 2015-11-10 | Sirna Therapeutics, Inc. | RNA interference mediated inhibition of gene expression using chemically modified short interfering nucleic acid (siNA) |
| US7566535B2 (en) | 2002-03-07 | 2009-07-28 | University Of Delaware | Enhanced oligonucleotide-mediated nucleic acid sequence alteration |
| BRPI0313202A8 (pt) | 2002-08-05 | 2016-08-16 | Atugen Ag | Formas adicionais para interferir com as moléculas de rna |
| US7923547B2 (en) | 2002-09-05 | 2011-04-12 | Sirna Therapeutics, Inc. | RNA interference mediated inhibition of gene expression using chemically modified short interfering nucleic acid (siNA) |
| GB2415431B (en) | 2003-04-22 | 2008-03-05 | Kyushu Tlo Co Ltd | Thionucleoside S-nitrosyl derivatives |
| WO2007073149A1 (en) * | 2005-12-22 | 2007-06-28 | Keygene N.V. | Alternative nucleotides for improved targeted nucleotide exchange |
| CA2622649C (en) * | 2007-03-09 | 2018-04-24 | Riken | Nucleic acid amplification method using primer exhibiting exciton effect |
| AU2008333811B2 (en) | 2007-12-04 | 2014-05-01 | Alnylam Pharmaceuticals, Inc. | Carbohydrate conjugates as delivery agents for oligonucleotides |
| WO2009102427A2 (en) | 2008-02-11 | 2009-08-20 | Rxi Pharmaceuticals Corp. | Modified rnai polynucleotides and uses thereof |
| CN103588839B (zh) | 2008-06-11 | 2017-04-12 | 激光基因公司 | 核苷酸和核苷以及将其用于dna测序的方法 |
| US20100249214A1 (en) | 2009-02-11 | 2010-09-30 | Dicerna Pharmaceuticals | Multiplex dicer substrate rna interference molecules having joining sequences |
| JP5855463B2 (ja) | 2008-12-18 | 2016-02-09 | ダイセルナ ファーマシューティカルズ, インコーポレイテッドDicerna Pharmaceuticals, Inc. | 遺伝子発現の特異的阻害のための拡張dicer基質薬剤および方法 |
| US9745574B2 (en) | 2009-02-04 | 2017-08-29 | Rxi Pharmaceuticals Corporation | RNA duplexes with single stranded phosphorothioate nucleotide regions for additional functionality |
| US8309356B2 (en) | 2009-04-01 | 2012-11-13 | Yale University | Pseudocomplementary oligonucleotides for targeted gene therapy |
| US9095504B2 (en) | 2010-03-24 | 2015-08-04 | Rxi Pharmaceuticals Corporation | RNA interference in ocular indications |
| IT1400425B1 (it) * | 2010-06-08 | 2013-05-31 | Amsterdam Molecular Therapeutics Bv | Modified snrnas for use in therapy. |
| CA2812046A1 (en) | 2010-09-15 | 2012-03-22 | Alnylam Pharmaceuticals, Inc. | Modified irna agents |
| WO2013150902A1 (ja) | 2012-04-02 | 2013-10-10 | 独立行政法人理化学研究所 | 非天然型塩基を含むオリゴデオキシヌクレオチドの切断による5'末端リン酸化オリゴデオキシヌクレオチドの製造方法 |
| JP2015518710A (ja) * | 2012-05-16 | 2015-07-06 | ラナ セラピューティクス インコーポレイテッド | ヘモグロビン遺伝子ファミリー発現を調節するための組成物及び方法 |
| PL2800811T3 (pl) * | 2012-05-25 | 2017-11-30 | Emmanuelle Charpentier | Sposoby i kompozycje do kierowanej RNA modyfikacji docelowego DNA i do modulacji transkrypcji kierowanej RNA |
| EP2986709A4 (en) * | 2013-04-16 | 2017-03-15 | University Of Washington Through Its Center For Commercialization | Activating an alternative pathway for homology-directed repair to stimulate targeted gene correction and genome engineering |
| CN107532162A (zh) * | 2014-12-12 | 2018-01-02 | 托德·M·伍尔夫 | 用于利用寡核苷酸编辑细胞中核酸的组合物和方法 |
-
2015
- 2015-12-11 CN CN201580075918.5A patent/CN107532162A/zh active Pending
- 2015-12-11 JP JP2017550092A patent/JP6997623B2/ja active Active
- 2015-12-11 CA CA2969464A patent/CA2969464A1/en not_active Abandoned
- 2015-12-11 WO PCT/US2015/065348 patent/WO2016094845A2/en active Application Filing
- 2015-12-11 EP EP15868062.9A patent/EP3230445B1/en active Active
-
2021
- 2021-09-29 JP JP2021159689A patent/JP2022008651A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014144951A1 (en) | 2013-03-15 | 2014-09-18 | Cibus Us Llc | Methods and compositions for increasing efficiency of increased efficiency of targeted gene modification using oligonucleotide-mediated gene repair |
| WO2015139008A1 (en) | 2014-03-14 | 2015-09-17 | Cibus Us Llc | Methods and compositions for increasing efficiency of targeted gene modification using oligonucleotide-mediated gene repair |
Non-Patent Citations (2)
| Title |
|---|
| Nucleic Acid Therapeutics,2012年,vol.22, no.6,p.405-413 |
| Nucleic Acids Research,2011年,vol.39, no.11,p.4783-4794 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN107532162A (zh) | 2018-01-02 |
| WO2016094845A2 (en) | 2016-06-16 |
| JP2018506297A (ja) | 2018-03-08 |
| JP2022008651A (ja) | 2022-01-13 |
| EP3230445B1 (en) | 2024-01-24 |
| EP3230445A2 (en) | 2017-10-18 |
| EP3230445C0 (en) | 2024-01-24 |
| EP3230445A4 (en) | 2018-09-26 |
| CA2969464A1 (en) | 2016-06-16 |
| WO2016094845A3 (en) | 2017-06-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6997623B2 (ja) | オリゴヌクレオチドを利用して細胞内の核酸を編集するための組成物および方法 | |
| JP6872560B2 (ja) | プログラム可能ヌクレアーゼのあるゲノム編集及びプログラム可能ヌクレアーゼのないゲノム編集のための改善された方法 | |
| US20210238597A1 (en) | Chemically modified single-stranded rna-editing oligonucleotides | |
| KR102618864B1 (ko) | 합성 가이드 분자, 그와 관련된 조성물 및 방법 | |
| AU2017281497B2 (en) | Single-stranded RNA-editing oligonucleotides | |
| CA2968336C (en) | Construct for site directed editing of an adenosine nucleotide in target rna | |
| AU2015277924B2 (en) | Antisense nucleic acids | |
| EP3571300A1 (en) | Oligonucleotide complexes for use in rna editing | |
| EP3752611A1 (en) | Antisense oligonucleotides for rna editing | |
| CA3115864A1 (en) | Methods and compositions for editing rnas | |
| CA3100111A1 (en) | Stereospecific linkages in rna editing oligonucleotides | |
| US20220127609A1 (en) | Antisense oligonucleotides for nucleic acid editing | |
| CN113994000A (zh) | 包括胞苷类似物的反义rna编辑寡核苷酸 | |
| TW202237837A (zh) | 經導入化學修飾核酸之穩定型標的編輯引導rna | |
| US20210395729A1 (en) | Compositions and methods for Editing Nucleic Acids in Cells Utilizing Oligonucleotides | |
| US11845934B2 (en) | Specific synthetic chimeric xenonucleic acid guide RNA; s(XNA-gRNA) for enhancing CRISPR mediated genome editing efficiency | |
| WO2024013361A1 (en) | Oligonucleotides for adar-mediated rna editing and use thereof | |
| NZ795956A (en) | Synthetic guide molecules, compositions and methods relating thereto | |
| NZ754735A (en) | Synthetic guide molecules, compositions and methods relating thereto |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181211 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181211 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191031 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200124 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200331 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200430 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200722 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201022 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201222 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210121 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20210602 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210929 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210929 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20210930 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20211101 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20211102 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20211119 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20211217 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6997623 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |