JP6979080B2 - Jak阻害剤を含む医薬組成物 - Google Patents
Jak阻害剤を含む医薬組成物 Download PDFInfo
- Publication number
- JP6979080B2 JP6979080B2 JP2019550213A JP2019550213A JP6979080B2 JP 6979080 B2 JP6979080 B2 JP 6979080B2 JP 2019550213 A JP2019550213 A JP 2019550213A JP 2019550213 A JP2019550213 A JP 2019550213A JP 6979080 B2 JP6979080 B2 JP 6979080B2
- Authority
- JP
- Japan
- Prior art keywords
- pharmaceutical composition
- disease
- composition according
- maleate form
- filgotinib
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
- A61K31/541—Non-condensed thiazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Rheumatology (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pain & Pain Management (AREA)
- Inorganic Chemistry (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Immunology (AREA)
- Physical Education & Sports Medicine (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
ヤヌスキナーゼ(JAK)は、JAK−STAT経路を介してサイトカイン媒介性シグナルを伝達する細胞内非受容体チロシンキナーゼのファミリーである。フィルゴチニブは、JAK1選択的阻害剤である。
本開示は、治療有効量のフィルゴチニブマレイン酸塩形態Iを含む医薬組成物を提供する。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、Cu−Kα線を使用して回折計で決定した場合に、8.2、11.9、16.4および18.9°2θ±0.2°2θにおいてピークを含むXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図1に示されているのと実質的に同じXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図2に示されているのと実質的に同じ示差走査熱量測定(DSC)曲線を特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図2に示されているのと実質的に同じサーモグラムを含む熱重量分析(TGA)を特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図3に示されているのと実質的に同じプロトン核磁気共鳴スペクトル(1H NMR)を特徴とする。
特定の実施形態では、例えば、以下が提供される:
(項目1)
治療有効量のフィルゴチニブマレイン酸塩形態Iを含む、医薬組成物。
(項目2)
フマル酸をさらに含む、項目1に記載の医薬組成物。
(項目3)
ステアリン酸マグネシウムをさらに含む、項目1または2に記載の医薬組成物。
(項目4)
ステアリン酸マグネシウム、微結晶性セルロース、ラクトース一水和物、アルファ化デンプンおよびコロイド状二酸化ケイ素をさらに含む、項目1または2に記載の医薬組成物。
(項目5)
ステアリン酸マグネシウム、微結晶性セルロース、ラクトース一水和物、アルファ化デンプン、コロイド状二酸化ケイ素、PEG 3350、ポリビニルアルコール、タルク、二酸化チタンおよび弁柄をさらに含む、項目1または2に記載の医薬組成物。
(項目6)
約32wt%のフィルゴチニブマレイン酸塩形態I;
約36wt%の微結晶性セルロース;
約20wt%のラクトース一水和物;
約5.0wt%のアルファ化デンプン;
約1.0wt%のコロイド状二酸化ケイ素;
約1.5wt%のステアリン酸マグネシウム;および
約5.0wt%のフマル酸
を含む、医薬組成物。
(項目7)
約29wt%〜約35wt%のフィルゴチニブマレイン酸塩形態I;
約32wt%〜約40wt%の微結晶性セルロース;
約18wt%〜約22wt%のラクトース一水和物;
約4.5wt%〜約5.5wt%のアルファ化デンプン;
約0.9wt%〜約1.1wt%のコロイド状二酸化ケイ素;
約1.3wt%〜約1.8wt%のステアリン酸マグネシウム;および
約4.5wt%〜約5.5wt%のフマル酸
を含む、医薬組成物。
(項目8)
前記組成物が錠剤の形態である、前記項目のいずれか一項に記載の医薬組成物。
(項目9)
前記フィルゴチニブマレイン酸塩形態Iが、Cu−Kα線を使用して回折計で決定した場合に、8.2、11.9、16.4および18.9°2θ±0.2°2θにおいてピークを含むXRPDパターンを特徴とする、前記項目のいずれか一項に記載の医薬組成物。
(項目10)
前記フィルゴチニブマレイン酸塩形態Iが、図1に示されているのと実質的に同じXRPDパターンを特徴とする、前記項目のいずれか一項に記載の医薬組成物。
(項目11)
前記フィルゴチニブマレイン酸塩形態Iが、図2に示されているのと実質的に同じ示差走査熱量測定(DSC)曲線を特徴とする、前記項目のいずれか一項に記載の医薬組成物。
(項目12)
前記フィルゴチニブマレイン酸塩形態Iが、図2に示されているのと実質的に同じサーモグラムを含む熱重量分析(TGA)を特徴とする、前記項目のいずれか一項に記載の医薬組成物。
(項目13)
前記フィルゴチニブマレイン酸塩形態Iが、図3に示されているのと実質的に同じプロトン核磁気共鳴スペクトル( 1 H NMR)を特徴とする、前記項目のいずれか一項に記載の医薬組成物。
(項目14)
JAKにより媒介される疾患または障害を処置する方法であって、前記項目のいずれかに記載の医薬組成物を、それを必要とする患者に投与することを含む、方法。
(項目15)
前記疾患または障害が炎症性疾患または障害である、項目14に記載の方法。
(項目16)
前記炎症性疾患または障害が、関節リウマチ、クローン病、潰瘍性大腸炎、円形脱毛症、ブドウ膜炎、急性移植片対宿主病、皮膚ループス腎炎、膜性ループス腎炎、アトピー性皮膚炎、乾癬、強直性脊椎炎および乾癬性関節炎からなる群より選択される、項目15に記載の方法。
フィルゴチニブは、N−(5−(4−((1,1−ジオキシドチオモルホリノ)メチル)フェニル)−[1,2,4]トリアゾロ[1,5−a]ピリジン−2−イル)シクロプロパンカルボキサミドの化学名および以下の構造:
本開示は、治療有効量のフィルゴチニブマレイン酸塩形態Iを含む医薬組成物を提供する。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、Cu−Kα線を使用して回折計で決定した場合に、8.2、11.9、16.4および18.9°2θ±0.2°2θにおいてピークを含むXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、Cu−Kα線を使用して回折計で決定した場合に、28.9、16.4、8.2、18.9、20.0、11.9、14.9、18.1、20.5および22.6°2θ±0.2°2θからなる群より選択される1つまたはそれより多くのピークを含むXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、Cu−Kα線を使用して回折計で決定した場合に、28.9、16.4、8.2、18.9、20.0、11.9、14.9、18.1、20.5および22.6°2θ±0.2°2θからなる群より選択される1つ、2つ、3つ、4つ、5つ、6つまたはそれより多くのピークを含むXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、Cu−Kα線を使用して回折計で決定した場合に、28.9、16.4、8.2、18.9、20.0、11.9、14.9、18.1、20.5および22.6°2θ±0.2°2θからなる群より選択される少なくとも4つのピークを含むXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、Cu−Kα線を使用して回折計で決定した場合に、28.9、16.4、8.2、18.9、20.0、11.9、14.9、18.1、20.5および22.6°2θ±0.2°2θからなる群より選択される少なくとも5つのピークを含むXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、Cu−Kα線を使用して回折計で決定した場合に、28.9、16.4、8.2、18.9、20.0、11.9、14.9、18.1、20.5および22.6°2θ±0.2°2θにおいてピークを含むXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図1に示されているのと実質的に同じXRPDパターンを特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図2に示されているのと実質的に同じ示差走査熱量測定(DSC)曲線を特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図2に示されているのと実質的に同じサーモグラムを含む熱重量分析(TGA)を特徴とする。いくつかの実施形態では、フィルゴチニブマレイン酸塩形態Iは、図3に示されているのと実質的に同じプロトン核磁気共鳴スペクトル(1H NMR)を特徴とする。
本明細書で使用される場合、以下の単語および句は、一般に、それらが使用されている文脈が別途指示している範囲を除いて、以下に記載されている意味を有することが意図される。
本明細書に記載される医薬組成物は、全般的に、経口投与のためのものである。経口投与を対象とする医薬組成物は、味のよい調製物を提供するために、甘味剤、矯味矯臭剤、着色剤、コーティング剤および/または保存剤をさらに含み得る。一実施形態では、医薬組成物は、錠剤の形態である。錠剤は、圧縮または成形により調製され得る。圧縮錠剤は、適切な機械で自由流動形態(例えば粉末または顆粒など)の活性成分を、結合剤、滑沢剤、不活性希釈剤または保存剤と必要に応じて混合して、圧縮することにより調製され得る。成形錠剤は、不活性液体希釈剤で湿らせた粉末活性成分の混合物を適切な機械で成形することにより作製され得る。錠剤は、必要に応じてコーティングまたはスコアリングされ得る。
本明細書に開示される医薬組成物は、JAKにより媒介される疾患または障害を処置するための治療方法において投与され得る。いくつかの実施形態では、本明細書に開示される医薬組成物は、炎症性疾患または障害を処置するために、それを必要とする患者に投与される。いくつかの実施形態では、本明細書に開示される医薬組成物は、関節リウマチ、クローン病、潰瘍性大腸炎、円形脱毛症、ブドウ膜炎、急性移植片対宿主病、皮膚ループス腎炎、膜性ループス腎炎、アトピー性皮膚炎、乾癬、強直性脊椎炎および乾癬性関節炎からなる群より選択される疾患または障害を処置するために、それを必要とする患者に投与される。
本明細書に開示される医薬組成物は、JAKにより媒介される疾患または障害を処置するために有効な1つまたはそれより多くのさらなる治療剤と組み合わせて、治療方法において投与され得る。いくつかの実施形態では、本明細書に開示される医薬組成物は、炎症性疾患または障害を処置するために有効な1つまたはそれより多くのさらなる治療剤と組み合わせて、それを必要とする患者に投与される。いくつかの実施形態では、本明細書に開示される医薬組成物は、関節リウマチ、クローン病、潰瘍性大腸炎、円形脱毛症、ブドウ膜炎、急性移植片対宿主病、皮膚ループス腎炎、膜性ループス腎炎、アトピー性皮膚炎、乾癬、強直性脊椎炎および乾癬性関節炎からなる群より選択される疾患または障害を処置するために有効な1つまたはそれより多くのさらなる治療剤と組み合わせて、それを必要とする患者に投与される。
N−(5−(4−((1,1−ジオキシドチオモルホリノ)メチル)フェニル)−[1,2,4]トリアゾロ[1,5−a]ピリジン−2−イル)シクロプロパンカルボキサミドを2.1mol当量のマレイン酸と共にアセトン/水(95:5 v/v)中、約50℃で約16時間加熱することにより、フィルゴチニブマレイン酸塩形態Iを調製した。その後、反応内容物を約1.5時間かけて約20℃に冷却し、約20℃で約2時間維持した。次に、反応内容物を濾過した。ウェットケーキをアセトンで洗浄し、撹拌しながら真空下、約50℃で乾燥させた。
制酸剤(ARA)の同時投与の効果を評価するために、ファモチジン前処置イヌにおいて、フィルゴチニブマレイン酸塩形態Iを含む様々な製剤の薬物動態パラメータを試験した。フィルゴチニブマレイン酸塩形態Iを含む医薬組成物へのフマル酸の添加は、フマル酸を含有しない対照製剤と比較して、ファモチジン前処置イヌにおけるフィルゴチニブの曝露の増加をもたらすことが見出された。同様の結果がクエン酸で得られた。さらに、フマル酸およびフィルゴチニブマレイン酸塩形態Iを含む医薬組成物は、国際公開第2015/117980号に記載されている製剤(「参照製剤」)と比べて、ファモチジン前処置イヌにおけるフィルゴチニブの優れた曝露をもたらした。結果を、表2に要約する。100mg用量のフィルゴチニブを各製剤にて投与した。
実施例2に示されているデータを考慮して臨床試験において使用するために、フィルゴチニブマレイン酸塩形態Iおよびフマル酸を含む医薬組成物を開発した。医薬組成物(「試験製剤」)中の成分および成分量は、表3に記載されている。
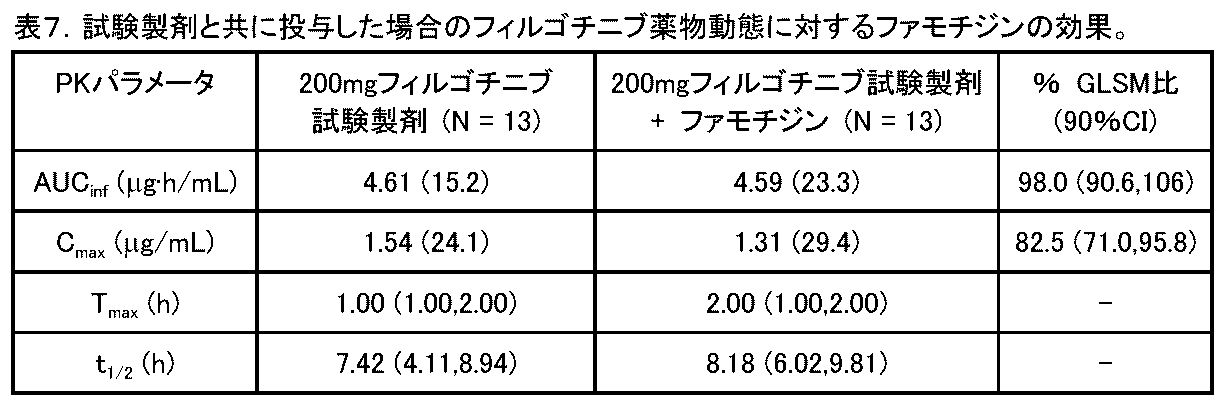
試験製剤を用いて第一相単一施設非盲検複数コホート研究を行って、ヒトにおける参照製剤と比較した試験製剤の相対的バイオアベイラビリティと、ヒトにおけるフィルゴチニブの薬物動態に対する制酸剤(ARA)の同時投与の効果とを評価した。研究設計は、以下に記載されている。
スクリーニングの完了後、適格被験体をコホート内で処置シーケンスに無作為化した。施した処置は、以下のとおりであった:
処置A:絶食でAMに単回200mg用量のフィルゴチニブを含む参照製剤(2×100mgの錠剤)を投与する
処置B:絶食でAMに単回200mg用量のフィルゴチニブを含む試験製剤(1×200mgの錠剤)を投与する
処置C:絶食でAMに単回100mg用量のフィルゴチニブを含む参照製剤(1×100mgの錠剤)を投与する
処置D:絶食でAMに単回100mg用量のフィルゴチニブ試験製剤(1×100mgの錠剤)を投与する
スクリーニングの完了後、以下の処置を適格被験体に投与した:
処置M:絶食でAMに単回200mg用量のフィルゴチニブを含む試験製剤(1×200mgの錠剤)を投与する
処置N:ファモチジン40mg(1×40mgの錠剤)を約12時間あけて1日2回投与する
処置O:絶食状態でAMにファモチジン40mg(1×40mgの錠剤)を投与し、続いて、ファモチジンのAM投与の2時間後に単回用量のフィルゴチニブを含む試験製剤(1×200mgの錠剤)を投与し、フィルゴチニブのAM投与の約12時間後に午後用量のファモチジン40mg(1×40mgの錠剤)を投与する
Claims (10)
- 治療有効量のフィルゴチニブマレイン酸塩形態Iを含む医薬組成物であって、フマル酸をさらに含み、
該フィルゴチニブマレイン酸塩形態Iが、Cu−Kα線を使用して回折計で決定した場合に、28.9、16.4、8.2、18.9、20.0、11.9、14.9、18.1、20.5および22.6°2θ±0.2°2θにおいてピークを含むXRPDパターンを特徴とする、前記医薬組成物。 - ステアリン酸マグネシウムをさらに含む、請求項1に記載の医薬組成物。
- ステアリン酸マグネシウム、微結晶性セルロース、ラクトース一水和物、アルファ化デンプンおよびコロイド状二酸化ケイ素をさらに含む、請求項1に記載の医薬組成物。
- ステアリン酸マグネシウム、微結晶性セルロース、ラクトース一水和物、アルファ化デンプン、コロイド状二酸化ケイ素、PEG 3350、ポリビニルアルコール、タルク、二酸化チタンおよび弁柄をさらに含む、請求項1に記載の医薬組成物。
- 32wt%のフィルゴチニブマレイン酸塩形態I;
36wt%の微結晶性セルロース;
20wt%のラクトース一水和物;
5.0wt%のアルファ化デンプン;
1.0wt%のコロイド状二酸化ケイ素;
1.5wt%のステアリン酸マグネシウム;および
5.0wt%のフマル酸
を含み、
該フィルゴチニブマレイン酸塩形態Iが、Cu−Kα線を使用して回折計で決定した場合に、28.9、16.4、8.2、18.9、20.0、11.9、14.9、18.1、20.5および22.6°2θ±0.2°2θにおいてピークを含むXRPDパターンを特徴とする、医薬組成物。 - 前記組成物が錠剤の形態である、請求項1から5のいずれか一項に記載の医薬組成物。
- JAKにより媒介される疾患または障害を処置するための、請求項1から5のいずれかに記載の医薬組成物。
- 前記疾患または障害が炎症性疾患または障害である、請求項8に記載の組成物。
- 前記炎症性疾患または障害が、関節リウマチ、クローン病、潰瘍性大腸炎、円形脱毛症、ブドウ膜炎、急性移植片対宿主病、皮膚ループス腎炎、膜性ループス腎炎、アトピー性皮膚炎、乾癬、強直性脊椎炎および乾癬性関節炎からなる群より選択される、請求項9に記載の組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021150706A JP2022003053A (ja) | 2017-03-14 | 2021-09-16 | Jak阻害剤を含む医薬組成物 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762471171P | 2017-03-14 | 2017-03-14 | |
| US62/471,171 | 2017-03-14 | ||
| US201762536614P | 2017-07-25 | 2017-07-25 | |
| US62/536,614 | 2017-07-25 | ||
| PCT/US2018/022027 WO2018169875A1 (en) | 2017-03-14 | 2018-03-12 | Pharmaceutical compositions comprising a jak inhibitor |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021150706A Division JP2022003053A (ja) | 2017-03-14 | 2021-09-16 | Jak阻害剤を含む医薬組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020510057A JP2020510057A (ja) | 2020-04-02 |
| JP6979080B2 true JP6979080B2 (ja) | 2021-12-08 |
Family
ID=61768547
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019550213A Active JP6979080B2 (ja) | 2017-03-14 | 2018-03-12 | Jak阻害剤を含む医薬組成物 |
| JP2021150706A Pending JP2022003053A (ja) | 2017-03-14 | 2021-09-16 | Jak阻害剤を含む医薬組成物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021150706A Pending JP2022003053A (ja) | 2017-03-14 | 2021-09-16 | Jak阻害剤を含む医薬組成物 |
Country Status (23)
| Country | Link |
|---|---|
| US (3) | US20180263997A1 (ja) |
| EP (2) | EP4368173A3 (ja) |
| JP (2) | JP6979080B2 (ja) |
| KR (2) | KR102303052B1 (ja) |
| CN (2) | CN116059211A (ja) |
| AU (2) | AU2018236156A1 (ja) |
| BR (1) | BR102018004952A2 (ja) |
| CA (1) | CA3055955C (ja) |
| DK (1) | DK3595667T3 (ja) |
| ES (1) | ES2969519T3 (ja) |
| FI (1) | FI3595667T3 (ja) |
| HR (1) | HRP20240112T1 (ja) |
| HU (1) | HUE065239T2 (ja) |
| JO (1) | JOP20180018A1 (ja) |
| LT (1) | LT3595667T (ja) |
| PL (1) | PL3595667T3 (ja) |
| PT (1) | PT3595667T (ja) |
| RS (1) | RS65118B1 (ja) |
| SI (1) | SI3595667T1 (ja) |
| SM (1) | SMT202400019T1 (ja) |
| TW (1) | TWI670270B (ja) |
| UY (1) | UY37632A (ja) |
| WO (1) | WO2018169875A1 (ja) |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201402071D0 (en) | 2014-02-07 | 2014-03-26 | Galapagos Nv | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| PL3595667T3 (pl) | 2017-03-14 | 2024-03-18 | Galapagos Nv | Kompozycje farmaceutyczne zawierające inhibitor jak |
| GB201808575D0 (en) * | 2018-05-24 | 2018-07-11 | Galapagos Nv | Methods for the treatment of psoriatic arthrits |
| WO2020135401A1 (zh) * | 2018-12-24 | 2020-07-02 | 正大天晴药业集团股份有限公司 | 吡咯并嘧啶化合物的治疗用途及其固体药物组合物 |
| WO2020177705A1 (zh) * | 2019-03-05 | 2020-09-10 | 苏州科睿思制药有限公司 | Filgotinib的马来酸盐晶型CSI及其制备方法和用途 |
| WO2021044327A1 (en) * | 2019-09-03 | 2021-03-11 | Dr. Reddy's Laboratories Limited | Solid forms of filgotinib maleate and processes thereof |
| CN111672456A (zh) * | 2020-06-18 | 2020-09-18 | 贵州大学 | 一种新型球-棒结构的介孔Janus纳米粒子及其制备方法 |
| AU2024265078A1 (en) | 2023-05-04 | 2025-12-11 | Revolution Medicines, Inc. | Combination therapy for a ras related disease or disorder |
| IL326136A (en) | 2023-08-07 | 2026-03-01 | Revolution Medicines Inc | RMC-6291 for use in the treatment of a disease or disorder associated with the RAS protein |
| US20250154171A1 (en) | 2023-10-12 | 2025-05-15 | Revolution Medicines, Inc. | Ras inhibitors |
| WO2025171296A1 (en) | 2024-02-09 | 2025-08-14 | Revolution Medicines, Inc. | Ras inhibitors |
| WO2025240847A1 (en) | 2024-05-17 | 2025-11-20 | Revolution Medicines, Inc. | Ras inhibitors |
| US20250375445A1 (en) | 2024-06-07 | 2025-12-11 | Revolution Medicines, Inc. | Methods of treating a ras protein-related disease or disorder |
| WO2025265060A1 (en) | 2024-06-21 | 2025-12-26 | Revolution Medicines, Inc. | Therapeutic compositions and methods for managing treatment-related effects |
| WO2026006747A1 (en) | 2024-06-28 | 2026-01-02 | Revolution Medicines, Inc. | Ras inhibitors |
| WO2026015825A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Use of ras inhibitor for treating pancreatic cancer |
| WO2026015796A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Methods of treating a ras related disease or disorder |
| WO2026015790A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Methods of treating a ras related disease or disorder |
| WO2026015801A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Methods of treating a ras related disease or disorder |
| WO2026027669A1 (en) | 2024-07-31 | 2026-02-05 | Alfasigma S.P.A. | Biomarkers for determining treatment of ulcerative colitis with filgotinib |
| WO2026027676A1 (en) | 2024-07-31 | 2026-02-05 | Alfasigma S.P.A. | Biomarkers for determining treatment of ulcerative colitis with filgotinib |
| WO2026050446A1 (en) | 2024-08-29 | 2026-03-05 | Revolution Medicines, Inc. | Ras inhibitors |
| WO2026072904A2 (en) | 2024-09-26 | 2026-04-02 | Revolution Medicines, Inc. | Compositions and methods for treating lung cancer |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003032954A1 (en) | 2001-10-17 | 2003-04-24 | Dr. Reddy's Laboratories Ltd. | Stabilized pharmaceutical formulations containing amlodipine maleate |
| JO3041B1 (ar) | 2008-07-25 | 2016-09-05 | Galapagos Nv | مركبات جديدة مفيدة لمعالجة الأمراض التنكسية والالتهابية |
| TWI462920B (zh) | 2009-06-26 | 2014-12-01 | 葛萊伯格有限公司 | 用於治療退化性及發炎疾病之新穎化合物 |
| EP2670398B1 (en) | 2011-02-04 | 2017-06-07 | TARIS Biomedical LLC | Implantable device for controlled release of low solubility drug |
| AU2013279597B2 (en) | 2012-06-22 | 2017-04-20 | Alfasigma S.P.A. | Aminotriazolopyridine for use in the treatment of inflammation, and pharmaceutical compositions thereof |
| GB201402070D0 (en) | 2014-02-07 | 2014-03-26 | Galapagos Nv | Pharmaceutical compositions for the treatment of inflammatory disorders |
| GB201402071D0 (en) | 2014-02-07 | 2014-03-26 | Galapagos Nv | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| RS64677B1 (sr) | 2015-04-13 | 2023-11-30 | Galapagos Nv | Metode lečenja kardiovaskularnih poremećaja |
| WO2017012773A1 (en) | 2015-07-23 | 2017-01-26 | Ratiopharm Gmbh | Solid forms of filgotinib free base |
| WO2017012770A1 (en) | 2015-07-23 | 2017-01-26 | Ratiopharm Gmbh | Acid addition salts of filgotinib |
| EP3434675A4 (en) | 2016-03-21 | 2019-03-06 | Crystal Pharmatech Co., Ltd | HYDROCHLORIDE SALT CREAM OF A MEDICAMENT FOR TREATING OR PREVENTING JAC-ASSOCIATED DISEASES AND METHOD OF PRODUCTION THEREOF |
| CN109476662A (zh) | 2016-08-03 | 2019-03-15 | 苏州科睿思制药有限公司 | 一种jak1选择性抑制剂的新晶型及其制备方法和用途 |
| PL3595667T3 (pl) | 2017-03-14 | 2024-03-18 | Galapagos Nv | Kompozycje farmaceutyczne zawierające inhibitor jak |
-
2018
- 2018-03-12 PL PL18713553.8T patent/PL3595667T3/pl unknown
- 2018-03-12 KR KR1020197029508A patent/KR102303052B1/ko active Active
- 2018-03-12 AU AU2018236156A patent/AU2018236156A1/en not_active Abandoned
- 2018-03-12 HR HRP20240112TT patent/HRP20240112T1/hr unknown
- 2018-03-12 PT PT187135538T patent/PT3595667T/pt unknown
- 2018-03-12 KR KR1020217029180A patent/KR102425226B1/ko active Active
- 2018-03-12 CA CA3055955A patent/CA3055955C/en active Active
- 2018-03-12 DK DK18713553.8T patent/DK3595667T3/da active
- 2018-03-12 CN CN202310082905.7A patent/CN116059211A/zh active Pending
- 2018-03-12 US US15/918,765 patent/US20180263997A1/en not_active Abandoned
- 2018-03-12 SM SM20240019T patent/SMT202400019T1/it unknown
- 2018-03-12 EP EP23208646.2A patent/EP4368173A3/en active Pending
- 2018-03-12 SI SI201831050T patent/SI3595667T1/sl unknown
- 2018-03-12 RS RS20240079A patent/RS65118B1/sr unknown
- 2018-03-12 CN CN201880018328.2A patent/CN110418644A/zh active Pending
- 2018-03-12 EP EP18713553.8A patent/EP3595667B1/en active Active
- 2018-03-12 FI FIEP18713553.8T patent/FI3595667T3/fi active
- 2018-03-12 LT LTEPPCT/US2018/022027T patent/LT3595667T/lt unknown
- 2018-03-12 HU HUE18713553A patent/HUE065239T2/hu unknown
- 2018-03-12 ES ES18713553T patent/ES2969519T3/es active Active
- 2018-03-12 JP JP2019550213A patent/JP6979080B2/ja active Active
- 2018-03-12 WO PCT/US2018/022027 patent/WO2018169875A1/en not_active Ceased
- 2018-03-13 JO JOP/2018/0018A patent/JOP20180018A1/ar unknown
- 2018-03-13 TW TW107108404A patent/TWI670270B/zh active
- 2018-03-13 BR BR102018004952-6A patent/BR102018004952A2/pt not_active Application Discontinuation
- 2018-03-14 UY UY0001037632A patent/UY37632A/es not_active Application Discontinuation
-
2021
- 2021-01-15 AU AU2021200229A patent/AU2021200229B2/en active Active
- 2021-02-26 US US17/186,446 patent/US11975008B2/en active Active
- 2021-09-16 JP JP2021150706A patent/JP2022003053A/ja active Pending
-
2024
- 2024-04-05 US US18/628,560 patent/US12502394B2/en active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6979080B2 (ja) | Jak阻害剤を含む医薬組成物 | |
| JP6508544B2 (ja) | 腫瘍を治療するための薬用組成物 | |
| JP6141958B2 (ja) | 増殖性疾患の治療のための併用療法(ベムラフェニブ及びmdm2阻害剤) | |
| EA003639B1 (ru) | Композиции валдекоксиба | |
| KR102490547B1 (ko) | 퀴놀린 유도체로 갑상선암을 치료하기 위한 방법과 용도 및 갑상선암을 치료하기 위한 약학적 조성물 | |
| JP3841846B2 (ja) | 過血糖症を治療するための薬剤学的製剤 | |
| JP7745086B2 (ja) | ARNiとカルシウムイオンアンタゴニストとの医薬組成物および応用 | |
| CN105832731B (zh) | 一种治疗高血压的药物及其制备方法 | |
| HK40111325A (en) | Pharmaceutical compositions comprising a jak inhibitor | |
| HK40022365A (en) | Pharmaceutical compositions comprising a jak inhibitor | |
| HK40022365B (en) | Pharmaceutical compositions comprising a jak inhibitor | |
| HK40009470A (en) | Pharmaceutical compositions comprising a jak inhibitor | |
| TWI814468B (zh) | 藥用組合物、其製備方法及用途 | |
| BR122024022798A2 (pt) | Composição farmacêutica, e seu no tratamento de uma doença ou distúrbio mediado por jak | |
| CA3217167A1 (en) | Alpelisib formulation | |
| CN119454710A (zh) | 一种治疗幽门螺旋杆菌的复方制剂及其制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191106 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191106 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200929 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201208 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210218 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210329 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20210520 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20210823 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210916 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210916 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20210824 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20211013 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20211019 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20211109 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20211112 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6979080 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |