システイン含有タンパク質は、有糸分裂誘発、増殖、アポトーシス、遺伝子制御、およびタンパク質分解などの多数の細胞機能に関与するタンパク質の大きなレパートリーを包含する。これらのタンパク質は、酵素、輸送体、受容体、チャネルタンパク質、アダプタータンパク質、シャペロン、シグナル伝達タンパク質、血漿タンパク質、転写関連タンパク質、翻訳関連タンパク質、ミトコンドリアタンパク質、あるいは細胞骨格関連タンパク質を含んでいる。システイン含有タンパク質の調節不全の発現は、多くの場合、炎症関連疾患、神経変性疾患、あるいは癌などの疾患に関連付けられるか、あるいはこれらを調節する。そのため、システイン含有タンパク質に対する潜在的なアゴニスト/アンタゴニストの同定は、患者の疾患状態を改善する助けとなる。
いくつかの例では、構造上複雑な化合物のせいで、および、構造上複雑な化合物の一部がタンパク質と相互に作用することができないことから、薬物スクリーニングには潜在的な制約が存在する。そのため、いくつかの例では、小分子断片は、当初の相互作用を高親和性薬物に構造誘導的に同化させるための拠点として役立つように採用される。いくつかの例では、システイン含有タンパク質と相互に作用する小分子断片を同定する1つの方法は、インビトロ環境下でその相互作用をモニタリングすることを介する。しかしながら、場合によっては、インビトロ環境は、システイン含有タンパク質の未変性状態を模倣しない。他の場合では、インビトロ環境は、小分子断片との相互作用を促すための追加のヘルパータンパク質を欠いている。またさらなるいくつかの例では、システイン含有タンパク質の発現および/または精製の段階中に数々の困難が生じる。
システイン含有タンパク質との相互作用のための小分子断片を同定する別の方法が本明細書に記載されている。いくつかの例では、この方法は、未変性状態下でシステイン含有タンパク質との相互作用のための小分子断片をマッピングすることを可能にし、それにより、潜在的な小分子断片との相互作用の正確なマッピングを可能にする。いくつかの例では、この方法は、組み換えの発現と精製の必要をなくすことから、新規なシステイン含有タンパク質標的の同定も可能にする。
いくつかの実施形態において、システイン含有タンパク質との相互作用のための小分子断片を同定する方法に関連する、組成物、細胞、細胞集団、アッセイ、プローブ、およびサービスも本明細書に記載されている。
一般的な方法
いくつかの実施形態において、本明細書に記載された方法は、システイン含有タンパク質との競合的な相互作用のための小分子断片とシステイン反応性プローブを利用する。いくつかの実施形態において、方法は図1のAに記載される通りである。図1のAは、システイン反応性プローブ−タンパク質複合体の第1の群を生成するために、第1のシステイン反応性プローブで第1の細胞溶液をインキュベートする前に、長時間にわたって小分子断片に第1の細胞溶液を接触させる工程を例示する。いくつかの実施形態において、長時間は約5、10、15、20、30、60、90、120分以上である。いくつかの例では、小分子断片は、タンパク質標的との相互作用のために第1のシステイン反応性プローブと競合する。いくつかの例では、小分子断片あるいはシステイン反応性プローブは、システイン含有タンパク質のシステイン残基とのマイケル反応によって共有結合を形成する。図1Aは、システイン反応性プローブ−タンパク質複合体の第2の群を生成するために、第2のシステイン反応性プローブに第2の細胞溶液を接触させる工程をさらに例示する。いくつかの例では、第1のシステイン反応性プローブと第2のシステイン反応性プローブは同じである。
いくつかの実施形態において、第2の細胞溶液からの細胞は富化培地(例えば、同位体富化培地)で育てられる。いくつかの例では、第1の細胞溶液からの細胞は富化培地(例えば同位体富化培地)で育てられる。いくつかの例では、第1の細胞溶液と第2の細胞溶液の両方からの細胞は、第1の細胞溶液で育てられた細胞から得られたタンパク質が、第2の細胞溶液で育てられた細胞から得られたタンパク質から区別できるように、2つの異なる富化培地(例えば、2つの異なる同位体富化培地)で育てられる。他の実施形態では、細胞溶液の1つのみ(例えば、第1の細胞溶液あるいは第2の細胞溶液のいずれか)からの細胞が富化培地(例えば、同位体富化培地)で育てられる。このような場合、富化された細胞(例えば、同位体富化細胞)から得られたタンパク質は、富化(例えば、同位体富化)されていない細胞から得られたタンパク質から区別できる。
図1のAで例示されるように、いくつかの例では、第2の細胞溶液は小分子断片で処理されない。そのような場合、第2の細胞溶液は対照として作用する。
いくつかの例では、第2の細胞溶液からの細胞はさらに緩衝液で処理される。場合によっては、緩衝液はDMSOである。場合によっては、第2の細胞溶液からの細胞は小分子断片で処理されず、第2の細胞溶液は対照として作用する。
いくつかの例では、システイン反応性プローブ−タンパク質複合体の第1の群とシステイン反応性プローブ−タンパク質複合体の第2の群は別々に収集され、組み合わされることでシステイン反応性プローブ−タンパク質複合体のセットを生成し、これはプロテオミクス解析手段によってさらに処理される。場合によっては、システイン反応性プローブ−タンパク質複合体の第1の群あるいはシステイン反応性プローブ−タンパク質複合体の第2の群のいずれかは、富化培地(例えば同位体富化培地)で育てられた細胞から得られた標識されたタンパク質を含む。場合によっては、システイン反応性プローブ−タンパク質複合体の両方の群は、2つの異なる富化培地(例えば2つの異なる同位体富化培地)で育てられた細胞から得られた標識されたタンパク質を含んでいる。他の場合では、システイン反応性プローブ−タンパク質複合体の第1の群、システイン反応性プローブ−タンパク質複合体の第2の群、あるいはシステイン反応性プローブ−タンパク質複合体の両方の群は、細胞から収集した後にタンパク質が標識された標識タンパク質を含んでいる。
いくつかの例では、システイン反応性プローブ−タンパク質複合体の第1の群とシステイン反応性プローブタンパク質複合体の第2の群は別々に収集され、システイン反応性プローブ−タンパク質複合体の2つの群の1つからのタンパク質はその後、(例えばメチル化によって)標識される。場合によっては、その後、システイン反応性プローブ−タンパク質複合体の第1の群とシステイン反応性プローブ−タンパク質複合体の第2の群はその後、組み合わせられ、プロテオミクス解析手段にさらされる。
他の例では、システイン反応性プローブ−タンパク質複合体の第1の群とシステイン反応性プローブタンパク質複合体の第2の群は別々に収集され、両方の群がプロテオミクス解析手段にさらされる。場合によっては、プロテオミクス解析手段から得られたデータをその後、詳しい解析のために組み合わせる。
いくつかの実施形態において、プロテオミクス解析手段は質量分析方法を含む。いくつかの例において、質量分析方法は液体クロマトグラフィー質量分析(LC−MS)方法である。いくつかの例では、プロテオミクス解析手段はタンパク質同定用のアルゴリズムによって質量分析方法からの結果を解析する工程をさらに含む。いくつかの例では、アルゴリズムは、タンパク質同定用のタンパク質配列データベースと、質量分析方法からの結果を組み合わせる。いくつかの例では、アルゴリズムはProLuCIDアルゴリズム、Probity、Scaffold、SEQUEST、あるいは、Mascotを含む。いくつかの例では、質量分析方法はMALDI−TOFベースの方法である。
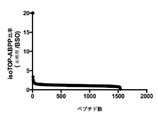
いくつかの実施形態において、プロテオミクス解析の後に、システイン反応性プローブ−タンパク質複合体からのシステイン結合タンパク質の各々に値が割り当てられ、この値はプロテオミクス解析から決定される。いくつかの例では、システイン含有タンパク質の各々に割り当てられた値は、質量分析解析から得られる。いくつかの例では、値は、質量電荷比に応じた信号強度のプロットからの曲線下面積である。いくつかの実施形態において、第1の値が、第1の細胞溶液のシステイン反応性プローブ−タンパク質複合体の第1の群からのシステイン結合タンパク質に割り当てられ、第2の値が第2の細胞溶液のシステイン反応性プローブタンパク質複合体の第2の群からの同じシステイン結合タンパク質に割り当てられる。いくつかの例では、その後、2つの値、すなわち、第1の値と第2の値の間の比率が計算され、同じシステイン結合タンパク質に割り当てられる。いくつかの例では、2を超える比率は、システイン結合タンパク質が小分子断片と相互に作用することに関する候補であることを示す。いくつかの例では、比率は2.5、3、3.5、4、4.5、5、6、7、8、9、あるいは10を超える。場合によっては、比率はせいぜい20である。いくつかの例では、同じ小分子断片はシステイン反応性プローブの存在下で多くのシステイン結合タンパク質と相互に作用する。いくつかの例では、小分子は、そのシステイン結合タンパク質パートナーとのシステイン反応性プローブの相互作用を調節する。いくつかの例では、システイン反応性プローブの存在下でのその相互作用タンパク質パートナーを含む小分子断片に関する比率のスペクトルは、タンパク質への小分子断片の特異性を示す。いくつかの例では、比率のスペクトルは、小分子断片がタンパク質への特異的阻害剤、あるいはパン阻害剤(pan inhibitor)であるかどうかを示す。
いくつかの実施形態において、上記方法によって同定されたシステイン含有タンパク質は、生物学的に活性なシステイン残基を含む。いくつかの例では、生物学的に活性なシステイン部位は、活性部位のリガンドまたは残基に対して約10Å以下に位置するシステイン残基である。いくつかの例では、活性部位のリガンドまたは残基に対して約10Å以下に位置するシステイン残基は、活性部位システインである。いくつかの例では、生物学的に活性なシステイン部位は活性部位システインである。いくつかの実施形態において、生物学的に活性なシステイン部位は、活性部位のリガンドまたは残基から10Åを超えて離れて位置するシステイン残基である。いくつかの例では、活性部位のリガンドまたは残基から10Åを超えて離れて位置するシステイン残基は、非活性部位システインである。いくつかの例では、生物学的に活性なシステイン部位は非活性部位システインである。
いくつかの実施形態において、生物学的に活性なシステインと共有結合的に相互作用する小分子断片は、システイン含有タンパク質の活性を損ない、および/または阻害する。いくつかの例では、システイン含有タンパク質は活性型で存在する。いくつかの実施形態において、小分子断片および/またはシステイン反応性プローブは、システイン含有タンパク質の活性型と相互に作用する。いくつかの例では、システイン含有タンパク質はプロアクティブ型で存在する。いくつかの実施形態において、小分子断片および/またはシステイン反応性プローブは、システイン含有タンパク質のプロアクティブ型と相互に作用する。
いくつかの実施形態において、生物学的に活性なシステイン残基の構造的な環境は、システイン残基の反応性を調節する。いくつかの実施形態において、構造的な環境は疎水性の環境あるいは親水性の環境である。いくつかの実施形態において、構造的な環境は帯電環境である。いくつかの実施形態において、構造的な環境は求核環境である。
いくつかの実施形態において、システイン含有タンパク質は、酵素、輸送体、受容体、チャネルタンパク質、アダプタータンパク質、シャペロン、シグナル伝達タンパク質、血漿タンパク質、転写関連タンパク質、翻訳関連タンパク質、ミトコンドリアタンパク質、あるいは、細胞骨格関連タンパク質である。いくつかの例では、システイン含有タンパク質は、酵素、輸送体、受容体、チャネルタンパク質、アダプタータンパク質、シャペロン、シグナル伝達タンパク質、転写関連タンパク質、あるいは、翻訳関連タンパク質である。いくつかの実施形態において、システイン含有タンパク質は、表1、2、3、8、あるいは9において例示されるタンパク質である。いくつかの例では、表1、2、3、8、あるいは9で例示されたシステイン含有タンパク質のシステイン残基は、表1、2、3、8、あるいは9の(*)によって表示される。
いくつかの例では、システイン反応性プローブのセットが細胞溶液に加えられる。例えば、システイン反応性プローブの第1のセットが第1の細胞溶液に加えられ、システイン反応性プローブの第2のセットが第2の細胞溶液に加えられる。場合によっては、各システイン反応性プローブはセット内で異なる。いくつかの例では、システイン反応性プローブの第1のセットはシステイン反応性プローブの第2のセットと同じである。いくつかの例では、システイン反応性プローブの第1のセットは、システイン反応性プローブ−タンパク質複合体の第3の群を生成し、システイン反応性プローブの第2のセットは、システイン反応性プローブ−タンパク質複合体の第4の群を生成する。いくつかの例では、システイン反応性プローブのセットは、システイン含有タンパク質の同定をさらに促す。
いくつかの実施形態では、サンプルは細胞サンプルである。他の例では、サンプルは組織サンプルである。
いくつかの例では、方法はインサイツ法である。
小分子断片
いくつかの実施形態において、本明細書に記載された小分子断片は非天然分子を含む。いくつかの例では、非天然分子は、天然および/または非天然のペプチド断片、あるいは哺乳動物の身体で自然に生成される小分子を含まない。
いくつかの実施形態において、本明細書に記載される小分子断片は、約100ダルトン以上の分子量を含む。いくつかの実施形態において、小分子断片は、約120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290、300、310、320、330、340、350、360、370、380、390、400、410、420、430、440、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン以上の分子量を含む。いくつかの例では、小分子断片の分子量は、約150〜約500、約150〜約450、約150〜約440、約150〜約430、約150〜約400、約150〜約350、約150〜約300、約150〜約250、約170〜約500、約180〜約450、約190〜約400、約200〜約350、約130〜約300、あるいは約120〜約250ダルトンの間である。
いくつかの実施形態において、本明細書に記載される小分子断片の分子量は、ハロゲン、非金属、遷移金属、あるいはその組み合わせから選択される1つ以上の要素を用いる富化の前の分子量である。いくつかの実施形態において、本明細書に記載される小分子断片の分子量は、ハロゲンを用いる富化の前の分子量である。いくつかの実施形態において、本明細書に記載される小分子断片の分子量は、非金属を用いる富化の前の分子量である。いくつかの実施形態において、本明細書に記載される小分子断片の分子量は、遷移金属を用いる富化の前の分子量である。いくつかの実施形態において、小分子断片の分子量は炭素と水素の原子に基づいて計算され、随意にさらに窒素、酸素、および/または硫黄の原子に基づいて計算される。
いくつかの実施形態において、小分子断片の分子量は、ハロゲン、遷移金属、あるいはその組み合わせの分子量を含まない。場合によっては、小分子断片の分子量はハロゲンの分子量を含まない。小分子断片の分子量は、遷移金属の分子量を含まない。
いくつかの実施形態において、本明細書に記載される小分子断片は、マイクロモルまたはミリモルの結合親和性を含む。いくつかの例では、小分子断片は、約1μM、10μM、100μM、500μM、1mM、10mM、あるいはそれ以上の結合親和性を含む。
いくつかの実施形態において、本明細書に記載される小分子断片は、高リガンド効率(LE)を有する。リガンド効率は、その結合パートナーに対するリガンドの1つの原子当たりの結合エネルギーの測定値である。いくつかの例では、リガンド効率は、化合物(N)の非水素原子の数に対するギブス自由エネルギー(ΔG)の比率として定義される:
LE(ΔG)=/N。
場合によっては、LEは以下のようにも整えられる:LE=1.4(−logIC50)/N。
いくつかの例では、LEスコアは、約0.3kcal mol−1HA−1、約0.35kcal mol−1HA−1、約0.4kcal mol−1HA−1、あるいはそれ以上である。
いくつかの実施形態において、本明細書に記載される小分子断片は、3の法則(the Rule of 3)に基づいて設計されている。いくつかの実施形態において、3の法則は、約3以下の無極性溶媒−極性溶媒(例えば、オクタノール−水)分配係数対数P、約300ダルトン以下の分子量、約3以下の水素結合供与体、約3以下の水素結合受容体、および約3以下の回転可能な結合を含む。
いくつかの実施形態において、本明細書に記載される小分子断片は、3以下の環状環を含む。
いくつかの実施形態において、本明細書に記載される小分子断片は、約20以上のアミノ酸残基長さであるポリペプチドのシステイン残基に結合する。いくつかの例では、本明細書に記載される小分子断片は、約30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600の、700、800、900、1000以上のアミノ酸残基長さであるポリペプチドのシステイン残基に結合する。
いくつかの実施形態において、本明細書に記載される小分子断片は、小分子断片をそれ以上最適化することなく投与される治療薬としては不適切な薬物動態パラメータをさらに含む。いくつかの例では、治療薬として適切な薬物動態パラメータは、米国食品医薬品局(FDA)のガイドラインに沿った、あるいは米国外の同等の食品医薬品局のガイドラインに沿ったパラメータを含む。いくつかの例では、薬物動態パラメータは、ピーク血漿濃度(Cmax)、治療薬(Cmin)の最低濃度、分布容積、Cmax到達時間、排出半減期、クリアランス、および寿命を含む。いくつかの実施形態において、小分子断片の薬物動態パラメータは、FDAのガイドラインによって、あるいは米国外の同等の食品医薬品局のガイドラインによって設定されたパラメータの外にある。いくつかの例では、当業者は、本明細書に記載される小分子断片の薬物動態パラメータを考慮すれば、これらの小分子断片がそれ以上の最適化を伴わない治療薬としては不適切であるということを理解する。
いくつかの実施形態において、本明細書に記載される小分子断片は、システイン含有タンパク質のシステイン残基のチオール基との共有結合的な相互作用を形成する反応性部分と、親和性ハンドル部分とを含む。
いくつかの実施形態において、本明細書に記載される小分子断片は、式(I)の小分子断片であり、
式中、RMは、マイケル受容体部分、脱離基部分、あるいはシステイン残基のチオール基と共有結合を形成することができる部分から選択される反応性部分であり、および、Fは小分子断片部分である。
いくつかの例では、マイケル受容体部分はアルケンあるいはアルキン部分を含む。いくつかの例では、Fは化合物ライブラリーから得られる。いくつかの例では、化合物ライブラリーは、ChemBridge断片ライブラリー、Pyramid Platform Fragmentベースの創薬、Maybridge断片ライブラリー、AnalytiConのFRGx、AnCoreXのTCI−Frag、ASINEXのBio Building Blocks、Charles RiverのBioFocus 3D、Emerald BioのFragments of Life (FOL)、Enamine Fragment Library、IOTA Diverse 1500、BIONET断片ライブラリー、Life Chemicals Fragments Collection、OTAVA断片ライブラリー、Prestwick断片ライブラリー、Selcia断片ライブラリー、TimTec断片ベースのライブラリー、Vitas−M LavoratoryのAllium、あるいはZenobia断片ライブラリーを含む。
いくつかの実施形態において、式(I)の小分子断片は第2の結合部位を含んでいない。いくつかの例では、小分子断片部分はタンパク質に結合しない。場合によっては、小分子断片部分はタンパク質に共有結合しない。いくつかの例では、小分子断片部分は、タンパク質上の第2の結合部位と相互に作用しない。いくつかの例では、第2の結合部位はATP結合部位などの活性部位である。場合によっては、活性部位は、生物学的に活性なシステイン残基から少なくとも約10、15、20、25、35、40Åあるいはそれ以上離れている。いくつかの例では、小分子断片部分はATP結合部位などの活性部位とは相互に作用しない。
いくつかの例では、Fは図3において例示される小分子断片部分である。場合によっては、Fはカルボニル部分にFを結合させるリンカー部分をさらに含む。場合によっては、小分子断片は図3において例示される小分子断片である。
いくつかの例では、Fは、以下から選択される小分子断片部分である:N−(4−ブロモフェニル)−N−フェニルアクリルアミド、N−(1−ベンゾイルピペリジン−4−イル)−2−クロロ−N−フェニルアセトアミド、1−(4−ベンジルピペリジン−1−イル)−2−クロロエタン−1−オン、N−(2−(1H−インドール−3−イル)エチル)−2−クロルアセトアミド、N−(3,5−ビス(トリフルオロメチル)フェニル)アクリルアミド、N−(4−フェノキシ−3−(トリフルオロメチル)フェニル)−N−(ピリジン−3−イルメチル)アクリルアミド、N−(3,5−ビス(トリフルオロメチル)フェニル)アセトアミド、2−クロロ−1−(4−(ヒドロキシジフェニルメチル)ピペリジン−1−イル)エタン−1−オン、(E)−3−(3,5−ビス(トリフルオロメチル)フェニル)−2−シアノアクリルアミド、N−(3,5−ビス(トリフルオロメチル)フェニル)−2−ブロモプロパンアミド、N−(3,5−ビス(トリフルオロメチル)フェニル)−2−クロロプロパンアミド、N−(3,5−ビス(トリフルオロメチル)フェニル)−N−(ピリジン−3−イルメチル)−アクリルアミド、3−(2−クロロアセトアミド)−5−(トリフルオロメチル)安息香酸、1−(4−(5−フルオロベンズイソオキサゾール−3−イル)ピペリジン−1−イル)プロプ−2−エン−1−オン、tert−ブチル4−(4−アクリルアミド−2,6−ジフルオロフェニル)ピペラジン−1−カルボキシラート、N−(4−ブロモ−2,5−ジメチルフェニル)アクリルアミド、2−クロロアセトアミド−2−デオキシ−α/β−D−グルコピラノース、2−クロロ−1−(2−メチル−3,4−ジヒドロキノリン−1(2H)−イル)エタン−1−オン、N−シクロヘキシル−N−フェニルアクリルアミド、1−(5−ブロモインドリン−1−イル)プロプ−2−エン−1−オン、N−(1−ベンジルピペリジン−4−イル)−N−フェニルアクリルアミド、2−クロロ−N−(2−メチル−5−(トリフルオロメチル)フェニル)アセトアミド、1−(5−ブロモインドリン−1−イル)−2−クロロエタン−1−オン、2−クロロ−N−(キノリン−5−イル)アセトアミド、1−(4−ベンジルピペリジン−1−イル)プロプ−2−エン−1−オン、2−クロロ−N−((3−ヒドロキシ−5−(ヒドロキシメチル)−2−メチルピリジン−4−イル)メチル)アセトアミド、あるいは1−(6,7−ジメトキシ−3,4−ジヒドロイソキノリン−2(1H)−イル)プロプ−2−エン−1−オン。
いくつかの実施形態において、式(I)の小分子断片は、約100、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290、300、310、320、330、340、350、360、370、380、390、400、410、420、430、440、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン以上の分子量を含む。いくつかの例では、式(I)の小分子断片の分子量は、約150〜約500、約150〜約450、約150〜約440、約150〜約430、約150〜約400、約150〜約350、約150〜約300、約150〜約250、約170〜約500、約180〜約450、約190〜約400、約200〜約350、約130〜約300、あるいは約120〜約250ダルトンの間である。
いくつかの実施形態において、式(I)の小分子断片の分子量は、ハロゲン、非金属、遷移金属、あるいはその組み合わせから選択される1つ以上の要素を用いる富化の前の分子量である。いくつかの実施形態において、式(I)の小分子断片の分子量は、ハロゲンを用いる富化の前の分子量である。いくつかの実施形態において、式(I)の小分子断片の分子量は、非金属を用いる富化の前の分子量である。いくつかの実施形態において、式(I)の小分子断片の分子量は、遷移金属を用いる富化の前の分子量である。
いくつかの実施形態において、式(I)の小分子断片の分子量は、ハロゲン、遷移金属、あるいはその組み合わせの分子量を含まない。場合によっては、式(I)の小分子断片の分子量はハロゲンの分子量を含まない。場合によっては、式(I)の小分子断片の分子量は遷移金属の分子量を含まない。
いくつかの例では、式(I)の小分子断片はマイクロモルまたはミリモルの結合親和性を含む。いくつかの例では、式(I)の小分子断片は、約1μM、10μM、100μM、500μM、1mM、10mM、あるいはそれ以上の結合親和性を含む。
場合によっては、式(I)の小分子断片は、約0.3kcal mol−1HA−1、約0.35kcal mol−1HA−1、約0.4kcal mol−1HA−1、あるいはそれ以上のLEスコアを有する。
いくつかの実施形態において、式(I)の小分子断片は、3の法則の設計パラメータに続く。いくつかの例では、式(I)の小分子断片は、約3以下の無極性溶媒−極性溶媒(例えば、オクタノール−水)分配係数対数P、約300ダルトン以下の分子量、約3以下の水素結合供与体、約3以下の水素結合受容体、および約3以下の回転可能な結合を有する。
いくつかの実施形態において、本明細書に記載される式(I)の小分子断片は、3以下の環状環を含む。
いくつかの実施形態において、式(I)の小分子断片は、約20以上のアミノ酸残基長さであるポリペプチドのシステイン残基(例えばシステイン含有タンパク質)に結合する。いくつかの例では、本明細書に記載される小分子断片は、約30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000以上のアミノ酸残基長さであるポリペプチドのシステイン残基に結合する。
いくつかの例では、式(I)の小分子断片は、FDAのガイドラインによって、あるいは米国外の同等の食品医薬品局によって設定されたパラメータの外にある薬物動態パラメータを有する。いくつかの例では、当業者は、本明細書に記載される式(I)の小分子断片の薬物動態パラメータを考慮すれば、これらの小分子断片がそれ以上の最適化を伴わない治療薬としては不適切であるということを理解する。
いくつかの実施形態において、小分子断片は特異的阻害剤あるいはpan阻害剤である。
システイン反応性プローブ
いくつかの実施形態において、システイン反応性プローブは、システイン含有タンパク質のシステイン残基のチオール基との共有結合的な相互作用を形成する反応性部分と、親和性ハンドル部分とを含む。
いくつかの実施形態において、システイン反応性プローブは式(II)のシステイン反応性プローブであり、
式中、RMは、マイケル受容体部分、脱離基部分、あるいはシステイン残基のチオール基と共有結合を形成することができる部分から選択される反応性部分であり、および、AHMは親和性ハンドル部分である。
いくつかの例では、マイケル受容体部分はアルケンあるいはアルキン部分を含む。いくつかの例では、親和性ハンドル部分は親和性ハンドルと、システイン含有タンパク質のシステイン残基へのシステイン反応性プローブの共有結合的な相互作用を促す結合部分とを含む。いくつかの例では、結合部分は化合物ライブラリーから得られる小分子断片である。いくつかの例では、化合物ライブラリーは、ChemBridge断片ライブラリー、Pyramid Platform Fragmentベースの創薬、Maybridge断片ライブラリー、AnalytiConのFRGx、AnCoreXのTCI−Frag、ASINEXのBio Building Blocks、Charles RiverのBioFocus 3D、Emerald BioのFragments of Life (FOL)、Enamine Fragment Library、IOTA Diverse 1500、BIONET断片ライブラリー、Life Chemicals Fragments Collection、OTAVA断片ライブラリー、Prestwick断片ライブラリー、Selcia断片ライブラリー、TimTec断片ベースのライブラリー、Vitas−M LavoratoryのAllium、あるいはZenobia断片ライブラリーを含む。
いくつかの実施形態において、親和性ハンドルは生体直交型の親和性ハンドルである。いくつかの実施形態において、親和性ハンドルは生体直交型のケミストリーを利用する。本明細書で使用されるように、生体直交型のケミストリーは、天然の生化学的プロセスに干渉することなく、生物系(例えば、細胞)の内部で生じるあらゆる化学反応を指す。
場合によっては、親和性ハンドルは、カルボジイミド、N−ヒドロキシスクシンイミド(NHS)エステル、イミドエステル、ペンタフルオロフェニルエステル、ヒドロキシメチルホスフィン、マレイミド、ハロアセチル、ピリジルジスルフィド、チオスルフォナート、ビニルスルホン、ヒドラジド、アルコキシアミン、アルキン、アジド、あるいはイソシアネートの基を含む。場合によっては、親和性ハンドルはアルキンあるいはアジド基を含む。
幾つかの事例では、親和性ハンドルはアルキン基である。親和性ハンドルに関連して使用されるような用語「アルキン基」は、H−C≡C−R、HC2R、R1−C≡CR2、またはR1C2R2の化学式を有する基を指す。本化学式に関連して、R、R1、およびR2は、独立して、本明細書に記載されるシステイン反応性プローブ部分、リンカー、またはその組み合わせである。幾つかの場合では、アルキン基は、アジドを含有している分子との化学反応に共有結合的に関連づけられることが可能である。幾つかの事例では、親和性ハンドルはアジド基である。
幾つかの事例では、親和性ハンドル(例えばアルキン基またはアジド基)は、非天然および非変動の(non−perturbed)生体直交型の化学的ハンドルとして機能する。幾つかの事例では、親和性ハンドル(例えばアルキン基またはアジド基)は、クリックケミストリーなどの化学反応によってさらに誘導体化される。幾つかの事例では、クリックケミストリーは、1,2,3−トリアゾールにつながるアルキンおよびアジドの銅(I)触媒性の[3+2]−ヒュスゲン1,3双極性の環化付加である。他の事例では、クリックケミストリーは、上記の反応の銅を含まない変異体(copper free variant)である。
幾つかの事例では、親和性ハンドルは、リンカーをさらに含む。幾つかの事例では、リンカーは、親和性ハンドルを反応性部分に架橋する。
幾つかの事例では、親和性ハンドルは、親和性リガンドにさらに結合される。幾つかの場合では、親和性リガンドは、発色団、標識基、またはそれらの組み合わせを含む。幾つかの実施形態では、発色団は、蛍光色素、非蛍光色素発色団、消光剤、吸収発色団、フルオロフォア、有機染料、無機染料、金属キレート、または蛍光酵素基質を含む。幾つかの場合では、発色団は、非蛍光色素発色団、消光剤、吸収発色団、フルオロフォア、有機染料、無機染料、金属キレート、または蛍光酵素基質を含む。他の場合では、発色団はフルオロフォアを含む。
幾つかの実施形態では、フルオロフォアは、ローダミン、ロドール、フルオレセイン、チオフルオレセイン、アミノフルオレセイン、カルボキシフルオレセイン、クロロフルオレセイン、メチルフルオレセイン、スルホフルオレセイン、アミノロドール、カルボキシロドール、クロロロドール、メチルロドール、スルホロドール、アミノローダミン、カルボキシローダミン、クロロローダミン、メチルローダミン、スルホローダミン、チオローダミン、シアニン、インドカルボシアニン、オキサカルボシアニン、チアカルボシアニン、メロシアニン、シアニン2、シアニン3、シアニン3.5、シアニン5、シアニン5.5、シアニン7、オキサジアゾール誘導体、ピリジルオキサゾール、ニトロベンゾオキサジアゾール、ベンゾオキサジアゾール、ピレン誘導体、カスケードブルー、オキサジン誘導体、ナイルレッド、ナイルブルー、クレシルバイオレット、オキサジン170、アクリジン誘導体、プロフラビン、アクリジンオレンジ、アクリジンイエロー、アリールメチン誘導体、オーラミン、クリスタルバイオレット、マラカイトグリーン、テトラピロール誘導体、ポルフィン、フタロシアニン、ビリルビン1−ジメチアルアミノナフチル−5−スルホン酸塩、1−アニリノ−8−ナフタレンスルホン酸塩、2−p−トウイジニル−6−ナフタレンスルホン酸塩、3−フェニル−7−イソシアナトクマリン、N−(p−(2−ベンゾオキサゾリル)フェニル)マレイミド、スチルベン、ピレン、6−FAM(フルオレセイン)、6−FAM(NHSエステル)、5(6)−FAM、5−FAM、フルオレセインdT、5−TAMRA−カダベリン、2−アミノアクリドン、HEX、JOE(NHSエステル)、MAX、TET、ROX、TAMRA、TARMA(商標)(NHSエステル)、TEX615、ATTO(商標)488、ATTO(商標)532、ATTO(商標)550、ATTO(商標)565、ATTO(商標)RholOl、ATTO(商標)590、ATTO(商標)633、ATTO(商標)647N、TYE(商標)563、TYE(商標)665、またはTYE(商標)705を含む。
幾つかの実施形態では、標識基は、ビオチン部分、ストレプトアビジン部分、ビーズ、樹脂、固体支持体、またはそれらの組み合わせである。本明細書で使用されるように、本明細書に記載されるビオチン部分は、ビオチンおよびビオチン誘導体を含む。典型的なビオチン誘導体は、限定されないが、デスチオビオチン、ビオチンアルキンまたはビオチンアジドを含む。幾つかの事例では、本明細書に記載されるビオチン部分は、デスチオビオチンである。幾つかの場合では、本明細書に記載されるビオチン部分は、d−デスチオビオチンである。
幾つかの事例では、標識基はビオチン部分である。幾つかの事例では、ビオチン部分は、長さが5、6、7、8、9、10、11、12、13、14、15またはそれ以上の残基などのリンカーをさらに含む。幾つかの事例では、リンカーは、プロテアーゼ切断部位などの切断部位をさらに含む。幾つかの場合では、ビオチン部分は、ストレプトアビジン部分と相互作用する。幾つかの事例では、ビオチン部分はさらに、ストレプトアビジン結合ビーズなどのビーズに付けられる。幾つかの事例では、ビオチン部分はさらに、ストレプトアビジン結合樹脂またはストレプトアビジン結合固体支持体などの、樹脂または固体支持体に付けられる。幾つかの事例では、固体支持体は、プレート、プラットフォーム、カバースライド、マイクロ流体チャネルなどである。
幾つかの実施形態では、親和性ハンドル部分はさらに発色団を含む。
幾つかの実施形態では、システイン反応性プローブは、図3に例示されるシステイン反応性プローブである。幾つかの実施形態では、システイン反応性プローブは、次のものから選択されるシステイン反応性プローブである:N−(hex−5−イン−1−イル)−2−ヨードアセトアミド、ヨードアセトアミド−ローダミン、3−アクリルアミド−N−(hex−5−イン−1−イル)−5−(トリフルオロメチル)ベンズアミド、3−アクリルアミド−N−(hex−5−イン−1−イル)−5−(トリフルオロメチル)ベンズアミド、または2−クロロ−N−(1−(3−エチニルベンゾイル)ピペリジン−4−イル)−N−フェニルアセトアミド。
<システイン含有タンパク質>
幾つかの事例では、システイン含有タンパク質は、可溶性タンパク質または膜タンパク質である。幾つかの事例では、システイン含有タンパク質は、タンパク質輸送、脂質代謝、アポトーシス、転写、電子伝達、mRNAプロセシング、または宿主ウイルス相互作用などの生物学的過程の1つ以上に関係している。幾つかの事例では、システイン含有タンパク質は、癌などの疾患の1つ以上、あるいは免疫性、代謝性、発達性、生殖の、神経学的な、精神医学的な、腎臓の、心血管の、または血液学的な障害または疾病などの、1つ以上の障害または疾病に関連付けられている。
幾つかの実施形態では、システイン含有タンパク質は、生物学的に活性なシステイン残基を含む。幾つかの実施形態では、システイン含有タンパク質は、1つ以上のシステインを含み、そこで少なくとも1つのシステインは、生物学的に活性なシステイン残基である。幾つかの場合では、生物学的に活性なシステイン部位は、活性部位のリガンドまたは残基に対して約1OÅ以下に位置するシステイン残基である。幾つかの場合では、活性部位のリガンドまたは残基に対して約1OÅ以下に位置するシステイン残基は、活性部位システインである。他の場合では、生物学的に活性なシステイン部位は、活性部位のリガンドまたは残基から1OÅを超えて位置するシステイン残基である。幾つかの事例では、システイン残基は、活性部位のリガンドまたは残基から12Å、15Å、20Å、25Å、30Å、35Å、40Å、45Åを超える、または50Åを超えて位置する。幾つかの場合では、活性部位のリガンドまたは残基から1OÅを超えて位置するシステイン残基は、非活性部位システインである。さらなる場合では、システイン含有タンパク質は、活性型または活性促進型で存在する。
幾つかの実施形態では、システイン含有タンパク質は、酵素、輸送体、受容体、チャネルタンパク質、アダプタータンパク質、シャペロン、シグナル伝達タンパク質、血漿タンパク質、転写関連のタンパク質、翻訳関連のタンパク質、ミトコンドリアタンパク質、または細胞骨格関連のタンパク質の1つ以上の機能を含む。幾つかの実施形態の、システイン含有タンパク質は、酵素、輸送体、受容体、チャネルタンパク質、アダプタータンパク質、シャペロン、シグナル伝達タンパク質、血漿タンパク質、転写関連のタンパク質、翻訳関連のタンパク質、ミトコンドリアタンパク質、または細胞骨格関連のタンパク質である。幾つかの事例では、システイン含有タンパク質は、分類されていない機能を有している。
幾つかの実施形態では、システイン含有タンパク質は酵素である。酵素は、化学反応を加速させるか又は触媒するタンパク質分子である。幾つかの実施形態では、酵素の限定しない例は、キナーゼ、プロテアーゼ、または脱ユビキチン化酵素を含む。
幾つかの事例では、典型的なキナーゼは、Tec、ブルトン型チロシンキナーゼ(Btk)、インターロイキン−2誘導性のT細胞キナーゼ(Itk)、Bmx(またはEmt/Tsk)、およびTxk/Rlkなどの、キナーゼのTECファミリー;SYKおよびゼータ鎖関連のタンパク質キナーゼ70(ZAP−70)などの、ひ臓チロシンキナーゼ(Syk)ファミリー;Src、Yes、Fyn、Fgr、Lck、Hck、Blk、Lyn、およびFrkなどの、Srcキナーゼ;ヤヌスキナーゼ1(JAK1)、ヤヌスキナーゼ2(JAK2)、ヤヌスキナーゼ3(JAK3)、およびチロシンキナーゼ2(TYK2)などの、JAKキナーゼ;あるいはHerl(EGFR、ErbBl)、Her2(Neu、ErbB2)、Her3(ErbB3)、およびHer4(ErbB4)などの、キナーゼのErbBファミリー、などのチロシンキナーゼを含む。
幾つかの実施形態では、システイン含有タンパク質はプロテアーゼである。幾つかの実施形態では、プロテアーゼはシステインプロテアーゼである。幾つかの場合では、システインプロテアーゼは、カスパーゼである。幾つかの事例では、カスパーゼはイニシエーター(頂端)カスパーゼである。幾つかの事例では、カスパーゼはエフェクター(実行型)カスパーゼである。典型的なカスパーゼは、CASP2、CASP8、CASP9、CASP10、CASP3、CASP6、CASP7、CASP4、およびCASP5を含む。
幾つかの事例では、システインプロテアーゼはカテプシンである。典型的なカテプシンは、カテプシンB、カテプシンC、カテプシンF、カテプシンH、カテプシンK、カテプシンL1、カテプシンL2、カテプシンO、カテプシンS、カテプシンW、またはカテプシンZを含む。
幾つかの実施形態では、システイン含有タンパク質は脱ユビキチン化酵素(DUB)である。幾つかの実施形態では、典型的な脱ユビキチン化酵素は、システインプロテアーゼDUBまたはメタロプロテアーゼを含む。典型的なシステインプロテアーゼDUBは、USP1、USP2、USP3、USP4、USP5、USP6、USP7、USP8、USP9X、USP9Y、USP10、USP11、USP12、USP13、USP14、USP15、USP16、USP17、USP17L2、USP17L3、USP17L4、USP17L5、USP17L7、USP17L8、USP18、USP19、USP20、USP21、USP22、USP23、USP24、USP25、USP26、USP27X、USP28、USP29、USP30、USP31、USP32、USP33、USP34、USP35、USP36、USP37、USP38、USP39、USP40、USP41、USP42、USP43、USP44、USP45、またはUSP46などの、ユビキチンに特異的なプロテアーゼ(USP/UBP);OTUB1およびOTUB2などの卵巣腫瘍(OTU)プロテアーゼ;ATXN3およびATXN3Lなどのマチャド−ジョセフィン(Machado−Josephin)ドメイン(MJD)プロテアーゼ;およびBAP1、UCHL1、UCHL3、およびUCHL5などのユビキチンC末端ヒドロラーゼ(UCH)プロテアーゼを含む。典型的なメタロプロテアーゼは、Jabl/Mov34/Mpr1 Pad1 N末端+(MPN+)(JAMM)ドメインプロテアーゼを含む。
幾つかの実施形態では、酵素としての典型的なシステイン含有タンパク質は、限定されないが、グリセルアルデヒド−3−リン酸デヒドロゲナーゼ(GAPDH)、タンパク質アルギニンN−メチルトランスフェラーゼ1(PRMT1)、ペプチジル−プロリル シス−トランスイソメラーゼNFMA相互作用(PIN1)、アセチル−CoAアセチルトランスフェラーゼ(ミトコンドリア)(ACAT1)、グルタチオンS−トランスフェラーゼP(GSTP1)、伸長因子2(EEF2)、グルタチオンS−トランスフェラーゼオメガ−1(GSTOl)、アセチル−CoAアセチルトランスフェラーゼ(ミトコンドリア)(ACAT1)、タンパク質ジスルフィド−イソメラーゼA4(PDIA4)、プロスタグランジンEシンターゼ3(PTGES3)、アデノシンキナーゼ(ADK)、伸長因子2(EEF2)、酢酸イソアミルを加水分解するエステラーゼ1相同体(IAH1)、ペルオキシレドキシン−5(ミトコンドリア)(PRDX5)、イノシン−5−一リン酸デヒドロゲナーゼ2型(IMPDH2)、3−ヒドロキシアシル−CoAデヒドロゲナーゼ2型(HSD17B10)、オメガ−アミダーゼNIT2(NIT2)、アルドースレダクターゼ(AKRIBI)、単官能性C1−テトラヒドロ葉酸シンターゼ(ミトコンドリア)(MTHFDIL)、タンパク質ジスルフィド−イソメラーゼA6(PDIA6)、ピルビン酸キナーゼアイソザイムM1/M2(PKM)、6−ホスホグルコノラクトナーゼ(PGLS)、アセチル−CoAアセチルトランスフェラーゼ(ミトコンドリア)(ACAT1)、ERO1様タンパク質アルファ(ERO1L)、チオレドキシンドメイン含有タンパク質17(TXNDC17)、タンパク質ジスルフィド−イソメラーゼA4(PDIA4)、タンパク質ジスルフィド−イソメラーゼA3(PDIA3)、3−ケトアシル−CoAチオラーゼ(ミトコンドリア)(ACAA2)、ダイナミン−2(DNM2)、DNA複製ライセンス化因子MCM3(MCM3)、セリン−tRNAリガーゼ(細胞質)(SARS)、脂肪酸シンターゼ(FASN)、アセチル−CoAアセチルトランスフェラーゼ(ミトコンドリア)(ACAT1)、タンパク質ジスルフィド−イソメラーゼ(P4HB)、デオキシシチジン−キナーゼ(DCK)、真核生物翻訳開始因子3サブユニット(EIF3F)、タンパク質ジスルフィド−イソメラーゼA6(PDIA6)、UDP−N−アセチルグルコサミン−ペプチドN−アセチルグルコサミン(OGT)、ケトサミン(Ketosamine)−3−キナーゼ(FN3KRP)、タンパク質DJ−1(PARK7)、ホスホグリコール酸ホスファターゼ (PGP)、DNA複製ライセンス化因子MCM6(MCM6)、フルクトース2,6−ビスホスファターゼTIGAR(TIGAR)、切断・ポリアデニル化特異的因子サブユニット(CPSF3)、ユビキチン結合酵素E2 L3(UBE2L3)、アラニン−−tRNAリガーゼ、細胞質(AARS)、マンノース−1 −リン酸グアニル酸転移酵素アルファ(GMPPA)、C−1−テトラヒドロ葉酸シンターゼ(細胞質)(MTHFD1)、ダイナミン−1様タンパク質(DNM1L)、タンパク質ジスルフィド−イソメラーゼA3(PDIA3)、
アスパルチルアミノペプチダーゼ(DNPEP)、アセチル−CoAアセチルトランスフェラーゼ(細胞質ゾル)(ACAT2)、チオレドキシンドメイン含有タンパク質5(TXNDC5)、チミジンキナーゼ(細胞質ゾル)(TK1)、イノシン−5−一リン酸デヒドロゲナーゼ2(EVIPDH2)、ユビキチンカルボキシル末端ヒドロラーゼアイソザイムL3(UCHL3)、インテグリン結合タンパク質キナーゼ(ILK)、サイクリン依存性キナーゼ2(CDK2)、ヒストンアセチルトランスフェラーゼB型触媒サブユニット(HAT1)、エノイル−CoAデルタイソメラーゼ2(ミトコンドリア)(ECI2)、C−1−テトラヒドロ葉酸シンターゼ(細胞質)(MTHFD1)、デオキシシチジンキナーゼ(DCK)、ユビキチン様修飾酵素活性化酵素6(UBA6)、タンパク質−L−イソアスパラギン酸(D−アスパラギン酸塩)O−メチルトランスフェラーゼ(PCMT1)、単官能性C1−テトラヒドロ葉酸シンターゼ(ミトコンドリア)(MTHFD1L)、チミジル酸キナーゼ(DTYMK)、タンパク質ETHE1(ミトコンドリア)(ETHE1)アルギニン−tRNAリガーゼ(細胞質)(RARS)、NEDD8−活性化酵素E1触媒サブユニット(UBA3)、二重特異性マイトジェン活性化プロテインキナーゼ(MAP2K3)、ユビキチン結合酵素E2S(UBE2S)、アミドホスホリボシルトランスフェラーゼ(PPAT)、コハク酸セミアルデヒドデヒドロゲナーゼ(ミトコンドリア)(ALDH5A1)、CAD、ホスホエノールピルビン酸カルボキシキナーゼ(PCK2)、6−ホスホフルクトキナーゼC型(PFKP)、アシル−CoAシンテターゼファミリーメンバー2(ミトコンドリア)(ACSF2)、多機能タンパク質ADE2(PAICS)、脱SUMO化イソペプチダーゼ1(DESI1)、6−ホスホフルクトキナーゼC型(PFKP)、V型プロトンATPアーゼ触媒サブユニットA(ATP6V1A)、3−ケトアシル−CoAチオラーゼ(ペルオキシソーム)(ACAA1)、ガラクトキナーゼ(GALK1)、チミジンキナーゼ(細胞質ゾル)(TK1)、ATPアーゼWRNIP1(WRNIP1)、ホスホリボシルホルミルグリシンアミジンシンターゼ(PFAS)、V型プロトンATPアーゼ触媒サブユニットA(ATP6V1A)、チオレドキシンドメイン含有タンパク質5(TXNDC5)、4−トリメチルアミノブチルアルデヒドデヒドロゲナーゼ(ALDH9A1)、二重特異性マイトジェン活性化プロテインキナーゼ(MAP2K4)、カルシニューリン様ホスホエステラーゼドメイン含有(CPPED1)、二重特異性プロテインフォスファターゼ12(DUSP12)、ホスホリボシルホルミルグリシンアミジンシンターゼ(PFAS)、ジホスホメバロン酸デカルボキシラーゼ(MVD)、D−3−ホスホグリセリン酸デヒドロゲナーゼ(PHGDH)、細胞周期チェックポイント制御タンパク質RAD9A(RAD9A)、ペルオキシレドキシン−1(PRDX1)、ソルビトールデヒドロゲナーゼ(SORD)、ペルオキシレドキシン−4(PRDX4)、AMPデアミナーゼ2(AMPD2)、イソクエン酸デヒドロゲナーゼ(IDHl)、ピルビン酸カルボキシラーゼ(ミトコンドリア)(PC)、インテグリン結合キナーゼ関連のセリン/トレオニン(ILKAP)、メチルマロン酸セミアルデヒドデヒドロゲナーゼ(ALDH6A1)、26Sプロテアソーム非ATPアーゼ調節サブユニット14(PSMD14)、チミジル酸キナーゼ(DTYMK)、6−ホスホフルクト−2−キナーゼ/フルクトース−2,6−ビスリン酸(bisphosphata)(PFKFB2)、ペルオキシレドキシン−5(ミトコンドリア)(PRDX5)、PDP1、カテプシンB(CTSB)、膜貫通プロテアーゼセリン12(TMPRSS12)、UDP−グルコース6−デヒドロゲナーゼ(UGDH)、ヒスチジントライアドヌクレオチド結合タンパク質1(HINT1)、E3ユビキチン−タンパク質リガーゼUBR5(UBR5)、SAMドメインおよびHDドメイン含有タンパク質1(SAMHD1)、高可能性tRNAトレオニルカルバモイルアデノシン生合成(OSGEP)、メチル化DNA−−タンパク質−システインメチルトランスフェラーゼ(MGMT)、脂肪酸シンターゼ(FASN)、アデノシンデアミナーゼ(ADA)、サイクリン依存性キナーゼ19(CDK19)、セリン/トレオニン−プロテインキナーゼ38(STK38)、マイトジェン活性化プロテインキナーゼ9(MAPK9)、tRNA(アデニン(58)−N(1))−メチルトランスフェラーゼ触媒性(TRMT61A)、グリオキシル酸レダクターゼ/ヒドロキシピルビン酸レダクターゼ(GRHPR)、アルデヒドデヒドロゲナーゼ(ミトコンドリア)(ALDH2)、ミトコンドリアプロセシングペプチダーゼサブユニットベータ(PMPCB)、3−ケトアシル−CoAチオラーゼ、ペルオキシゾーム(ACAA1)リゾフォスファチジン酸ホスファターゼ6型(ACP6)、ユビキチン/ISG15結合酵素E2 L6(UBE2L6)、カスパーゼ−8(CASP8)、2,5−ホスホジエステラーゼ12(PDE12)、チオレドキシンドメイン含有タンパク質12(TXNDC12)、ニトリラーゼ相同体1(NIT1)、ERO1様タンパク質アルファ(ERO1L)、SUMO活性化酵素サブユニット1(SAE1)、ロイシン−−tRNAリガーゼ(細胞質)(LARS)、タンパク質−グルタミンガンマ−グルタミルトランスフェラーゼ2(TGM2)、高可能性DNA dC−dU編集酵素APOBEC−3C(APOBEC3C)、二本鎖RNA特異的アデノシンデアミナーゼ(ADAR)、イソクエン酸デヒドロゲナーゼ(IDH2)、メチルクロトニル−CoAカルボキシラーゼベータ鎖(ミトコンドリア)(MCCC2)、ウリジンホスホリラーゼ1(UPP1)、グリコーゲンホスホリラーゼ(脳型)(PYGB)、E3ユビキチン−タンパク質リガーゼUBR5(UBR5)、プロコラーゲン−リジン,2−オキソグルタラート5−ジオキシゲナーゼ1(PLOD1)、ユビキチンカルボキシル末端ヒドロラーゼ48(USP48)、アコニット酸ヒドラターゼ(ミトコンドリア)(AC02)、GMPレダクターゼ2(GMPR2)、ピロリン−5−カルボン酸塩レダクターゼ1(ミトコンドリア)(PYCR1)、カテプシンZ(CTSZ)、E3ユビキチン−タンパク質リガーゼUBR2(UBR2)、システインプロテアーゼATG4B(ATG4B)、セリン/トレオニン−プロテインキナーゼNek9(NEK9)、リシン特異的デメチラーゼ4B(KDM4B)、インスリン分解酵素(IDE)、ジペプチジルペプチダーゼ9(DPP9)、デカプレニル二リン酸シンターゼサブユニット2(PDSS2)、TFIIH基本転写因子複合体ヘリカーゼ(ERCC3)、メチオニン−R−スルホキシドレダクターゼB2 (ミトコンドリア)(MSRB2)、E3ユビキチン−タンパク質リガーゼBREIB(RNF40)、チミジル酸シンターゼ(TYMS)、サイクリン依存性キナーゼ5(CDK5)、二官能性3−フォスフォアデノシン5−ホスホ硫酸(PAPSS2)、短/分枝鎖特異的アシル−CoAデヒドロゲナーゼ(ACADSB)、カテプシンD(CTSD)、E3ユビキチン−タンパク質リガーゼHUWE1(HUWE1)、カルパイン−2触媒サブユニット(CAPN2)、二重特異性マイトジェン活性化プロテインキナーゼ(MAP2K7)、マイトジェン活性化プロテインキナーゼ・キナーゼ・キナーゼMLT(MLTK)、ブレオマイシンヒドロラーゼ(BLMH)、高可能性ATP依存性RNAヘリカーゼDDX59(DDX59)、シスタチオニンγリアーゼ(CTH)、S−アデノシルメチオニンシンターゼアイソフォーム2型(MAT2A)、6−ホスホフルクトキナーゼC型(PFKP)、シチジンデアミナーゼ(CDA)、DNA指向性RNAポリメラーゼIIサブユニットRPB2(POLR2B)、タンパク質ジスルフィド−イソメラーゼ(P4HB)、プロコラーゲン−リジン,2−オキソグルタラート5−ジオキシゲナーゼ3(PLOD3)、ヌクレオシド二リン酸結合部分Xモチーフ8(ミトコンドリア)(NUDT8)、E3ユビキチン−タンパク質リガーゼHUWE1(HUWE1)、メチル化DNA−−タンパク質−システインメチルトランスフェラーゼ(MGMT)、ニトリラーゼ相同体1(NIT1)、インターフェロン調節因子2結合タンパク質1(IRF2BP1)、ユビキチンカルボキシル末端ヒドロラーゼ16(USP16)、グリシルペプチドN−テトラデカノイルトランスフェラーゼ2(NMT2)、サイクリン依存性キナーゼ阻害剤3(CDKN3)、ヒドロキシステロイドデヒドロゲナーゼ様タンパク質2(HSDL2)、セリン/トレオニン−プロテインキナーゼVRK1(VRK1)、セリン/トレオニン−プロテインキナーゼA−Raf(ARAF)、ATP−クエン酸シンターゼ(ACLY)、高可能性リボヌクレアーゼZC3H12D(ZC3H12D)、末梢原形質膜タンパク質CASK(CASK)、DNAポリメラーゼイプシロンサブユニット3(POLE3)、アルデヒドデヒドロゲナーゼX(ミトコンドリア)(ALDH1B1)、UDP−N−アセチルグルコサミントランスフェラーゼサブユニットALG13(ALG13)、タンパク質ジスルフィド−イソメラーゼA4(PDIA4)、DNAポリメラーゼアルファ触媒サブユニット(POLA1)、エチルマロニル−CoAデカルボキシラーゼ(ECHDC1)、タンパク質−チロシンキナーゼ2−ベータ(PTK2B)、E3 SUMOタンパク質リガーゼRanBP2(RANBP2)、レグマイン(LGMN)、非特異的脂質輸送タンパク質(SCP2)、長鎖脂肪酸−−CoAリガーゼ4(ACSL4)、二重特異性プロテインフォスファターゼ12(DUSP12)、オキシドレダクターゼHTATIP2(HTATIP2)、セリン/トレオニン−プロテインキナーゼMRCKベータ(CDC42BPB)、ヒストン−リシンN−メチルトランスフェラーゼEZH2(EZH2)、非特異的脂質輸送タンパク質(SCP2)、二重特異性マイトジェン活性化プロテインキナーゼ(MAP2K7)、ユビキチンカルボキシル末端ヒドロラーゼ28(USP28)、6−ホスホフルクトキナーゼ(肝臓型)(PFKL)、SWI/SNF関連のマトリックスに会合したアクチン依存性(SMARCAD1)、プロテインフォスファターゼ メチルエストラーゼ1(PPME1)、DNA複製ライセンス化因子MCM5(MCM5)、6−ホスホフルクト−2−キナーゼ/フルクトース−2,6−ビスホスファターゼ(bisphosphata)(PFKFB4)、デヒドロゲナーゼ/レダクターゼSDRファミリーメンバー11(DHRS11)、ピログルタミニル−ペプチダーゼ1(PGPEP1)、高可能性E3ユビキチン−タンパク質リガーゼ(MYCBP2)、DNA断片化因子サブユニットベータ(DFFB)、脱ユビキチン化タンパク質VCIP135(VCPIP1)、推定トランスフェラーゼCAF17(ミトコンドリア)(TOA57)、カルパイン−7(CAPN7)、GDP−L−フコースシンターゼ(TSTA3)、タンパク質ジスルフィド−イソメラーゼA4(PDIA4)、高可能性ATP依存性のRNAヘリカーゼ(DDX59)、RNAエキソヌクレアーゼ4(REX04)、PDK1、E3 SUMO−タンパク質リガーゼ(PIAS4)、DNA(シトシン−5)−メチルトランスフェラーゼ1(DNMT1)、アルファ−アミノアジピン酸セミアルデヒドデヒドロゲナーゼ(ALDH7A1)、ヒドロキシメチルグルタリル−CoAシンターゼ(細胞質)(HMGCS1)、E3ユビキチン−タンパク質リガーゼ(SMURF2)、アルデヒドデヒドロゲナーゼX(ミトコンドリア)(ALDH1B1)、チロシン−タンパク質キナーゼ(BTK)、DNA修復タンパク質RAD50(RAD50)
、ATP結合ドメイン含有タンパク質4(ATPBD4)、ヌクレオシド二リン酸キナーゼ3(NME3)、インターロイキン−1受容体関連のキナーゼ1(IRAK1)、リボヌクレアーゼP/MRPサブユニットタンパク質POP5(POP5)、ペプチド−N(4)−(N−アセチル−ベータ−グルコサミニル)アスパラギン(NGLY1)、カスパーゼ−2(CASP2)、リボソームタンパク質S6キナーゼアルファ−3(RPS6KA3)、E3ユビキチン−タンパク質リガーゼUBR1(UBR1)、セリン/トレオニン−プロテインキナーゼChk2(CHEK2)、ホスファチジルイノシトール3,4,5−トリスホスファート5−ホスファ(INPPL1)、ヒストンアセチルトランスフェラーゼp300(EP300)、クレアチンキナーゼU型(ミトコンドリア)(CKMT1B)、E3ユビキチン−タンパク質リガーゼTREVI33(TRIM33)、癌関連のヌクレオシド−トリフォスファターゼ(NTPCR)、アコニット酸ヒドラターゼ(ミトコンドリア)(AC02)、ユビキチンカルボキシル末端ヒドロラーゼ34(USP34)、高可能性E3ユビキチン−タンパク質リガーゼHERC4(HERC4)、E3ユビキチン−タンパク質リガーゼHECTD1(HECTD1)、ペルオキシゾーム2,4−ジエノイル−CoAレダクターゼ(DECR2)、ヘリカーゼARIP4(RAD54L2)、ユビキチン様修飾酵素活性化酵素7(UBA7)、ER分解促進アルファ−マンノシダーゼ様3(EDEM3)、ユビキチン結合酵素E20(UBE2O)、二重特異性マイトジェン活性化プロテインキナーゼ(MAP2K7)、ミオチューブラリン関連のタンパク質1(MTMR1)、カルシウム依存性ホスホリパーゼA2(PLA2G5)、有系分裂チェックポイントセリン/トレオニン−プロテインキナーゼ(BUB1B)、推定トランスフェラーゼCAF17(ミトコンドリア)(IBA57)、チロシン−タンパク質キナーゼZAP−70(ZAP70)、E3ユビキチン−タンパク質リガーゼペリノ(pellino)相同体1(PELI1)、神経障害標的エステラーゼ(PNPLA6)、リボソームタンパク質S6キナーゼアルファ−3(RPS6KA3)、N6−アデノシン−メチルトランスフェラーゼ70kDaサブユニット(METTL3)、フルクトサミン−3−キナーゼ(FN3K)、ユビキチンカルボキシル末端ヒドロラーゼ22(USP22)、Rab3 GTPアーゼ活性化タンパク質触媒サブユニット(RAB3GAP1)、カスパーゼ−5(CASP5)、L−2−ヒドロキシグルタル酸デヒドロゲナーゼ(ミトコンドリア)(L2HGDH)、サッカロピンデヒドロゲナーゼ様オキシドレダクターゼ(SCCPDH)、FLAD1 FADシンターゼ、リシン特異的デメチラーゼ3A(KDM3A)、またはユビキチンカルボキシル末端ヒドロラーゼ34(USP34)を含む。
幾つかの実施形態では、システイン含有タンパク質は、シグナル伝達タンパク質である。幾つかの事例では、典型的なシグナル伝達タンパク質は、血管内皮増殖因子(VEGF)タンパク質またはレドックスシグナル伝達に関係するタンパク質を含む。典型的なVEGFタンパク質は、VEGF−A、VEGF−B、VEGF−C、VEGF−D、およびPGFを含む。典型的なレドックスシグナル伝達に関係するタンパク質は、酸化還元調節タンパク質FAM213Aを含む。
幾つかの実施形態では、システイン含有タンパク質は、転写因子または制御因子である。転写因子および制御因子としての典型的なシステイン含有タンパク質は、限定されないが、40Sリボソームタンパク質S3(RPS3)、塩基性ロイシンジッパーおよびW2ドメイン含有タンパク質(BZW1)、ポリ(rC)結合タンパク質1(PCBP1)、40Sリボソームタンパク質S11(RPS11)、40Sリボソームタンパク質S4、Xアイソフォーム(RPS4X)、シグナル識別粒子9kDaタンパク質(SRP9)、非POUドメイン含有オクタマー結合タンパク質(NONO)、N−アルファ−アセチルトランスフェラーゼ15、NatA補助サブユニット(NAA15)、切断刺激因子サブユニット2(CSTF2)、ラミナ関連のポリペプチド2、アイソフォームアルファ(TMPO)、ヘテロ核リボヌクレオタンパク質R(HNRNPR)、MMS19ヌクレオチド除去修復タンパク質相同体(MMS19)、SWI/SNF複合体サブユニットSMARCC2(SMARCC2)、mRNAデキャッピングタンパク質3(EDC3)のエンハンサー、H/ACAリボヌクレオタンパク質複合体サブユニット2(NHP2)、コイルドコイルを有するWWドメイン含有アダプタータンパク質(WAC)、N−アルファ−アセチルトランスフェラーゼ15NatA補助サブユニット(NAA15)、40Sリボソームタンパク質S11(RPS11)、シグナル伝達性転写因子1(STAT1)、RNAポリメラーゼII転写サブユニットのメディエーター(MED15)、ラミナ関連のポリペプチド2(アイソフォームアルファ)(TMPO)、MMS19ヌクレオチド除去修復タンパク質相同体(MMS19)、DNAミスマッチ修復タンパク質Msh2(MSH2)、無毛の組換え結合タンパク質抑制因子(RBPJ)、RNAポリメラーゼII転写サブユニットのメディエーター(MED17)、ヘテロ核リボヌクレオタンパク質U(HNRNPU)、転写開始因子IIAサブユニット2(GTF2A2)、クロマチンアクセシビリティ複合タンパク質1(CHRAC1)、CDKN2A相互作用タンパク質(CDKN2AIP)、亜鉛フィンガータンパク質217(ZNF217)、シグナル伝達性転写因子3(STAT3)、WDリピートおよびHMG−ボックスDNA結合タンパク質1(WDHD1)、ラミナ関連のポリペプチド2(アイソフォームアルファ)(TMPO)、ラミナ関連のポリペプチド2(アイソフォームベータ/ガンマ)(TMPO)、インターフェロン調節因子4(IRF4)、タンパク質フライトレス(Protein flightless)−1相同体(FLU)、ヘテロ核リボヌクレオタンパク質F(HNRNPF)、側坐核関連のタンパク質1(NACC1)、転写伸長制御因子1(TCERG1)、タンパク質HEXIM1(HEXFM1)、mRNAデキャッピングタンパク質のエンハンサー(EDC3)、亜鉛フィンガータンパク質Aiolos(IKZF3)、転写伸長因子SPT5(SUPT5H)、フォークヘッドボックスタンパク質K1(FOXK1)、LEVIドメイン含有タンパク質1(LFMD1)、MMS19ヌクレオチド除去修復タンパク質相同体(MMS19)、エロンゲーター(Elongator)複合タンパク質4(ELP4)、アンキリンリピートおよびKHドメイン含有タンパク質1(ANKHDl)、PML、核因子NF−カッパ−B pi 00サブユニット(NFKB2)、ヘテロ核リボヌクレオタンパク質L様(HNRPLL)、CCR4−NOT転写複合体サブユニット3(CNOT3)、PPAR−ガンマ様タンパク質の構成的コアクチベーター(FAM120A)、RNAポリメラーゼII転写サブユニットのメディエーター(MED15)、60Sリボソームタンパク質L7(RPL7)、インターフェロン調節因子8(IRF8)、COUP転写因子2(NR2F2)、RNAポリメラーゼII転写サブユニットのメディエーター(MED1)、tRNA(ウラシル−5−)−メチルトランスフェラーゼA(TRMT2A)、転写因子p65(RELA)、エキソソーム複合成分RRP42 (EXOSC7)、基本転写因子3Cポリペプチド1(GTF3C1)、マザーズ・アゲインスト・デカペンタプレジック相同体(Mothers against decapentaplegic homolog)2(SMAD2)、アンキリンリピートドメイン含有タンパク質17(ANKRD17)、MMS19ヌクレオチド除去修復タンパク質相同体(MMS19)、デスドメイン関連のタンパク質(DAXX)、亜鉛フィンガータンパク質318(ZNF318)6、チオレドキシン相互作用タンパク質(TXNIP)、グルココルチコイド受容体(NR3C1)、鉄応答要素結合タンパク質2(IREB2)、亜鉛フィンガータンパク質295(ZNF295)、ポリコームタンパク質SUZ12(SUZ12)、切断刺激因子サブユニット2タウ変異体(CSTF2T)、C−mycプロモーター結合タンパク質(DENND4A)、ピニン(Pinin)(PNN)、RNAポリメラーゼII転写サブユニットのメディエーター(MED9)、POUドメイン(クラス2)転写因子2(POU2F2)、mRNAデキャッピングタンパク質のエンハンサー3(EDC3)、A−キナーゼアンカータンパク質1(ミトコンドリア)(AKAP1)、転写因子RelB(RELB)RNAポリメラーゼII関連のタンパク質1(RPAP1)、亜鉛フィンガータンパク質346(ZNF346)、染色体関連のキネシンKTF4A(KTF4A)、RNAポリメラーゼII転写サブユニットのメディエーター(MED12)、タンパク質NPAT(NPAT)、ロイシンリッチPPRモチーフ含有タンパク質(ミトコンドリア)(LRPPRC)、ATフックDNA結合モチーフ含有タンパク質1(AHDC1)、RNAポリメラーゼII転写サブユニット(MED12)のメディエーター、ブロモドメイン含有タンパク質8(BRD8)、トリヌクレオチドリピート含有遺伝子6Bタンパク質(TNRC6B)、アリール炭化水素受容体核内輸送体(ARNT)、活性化転写因子7相互作用タンパク質(ATF7IP)、グルココルチコイド受容体(NR3C1)、染色体伝達忠実度関係タンパク質18相同体(CHTF18)、またはC−mycプロモーター結合タンパク質(DENND4A)を含む。
幾つかの実施形態では、システイン含有タンパク質は、チャネル、輸送体または受容体である。チャネル、輸送体または受容体としての典型的なシステイン含有タンパク質は、限定されないが、クロライド細胞内チャネルタンパク質4(CLIC4)、エキスポーチン−1(XPO1)、チオレドキシン(TXN)、タンパク質SEC13相同体(SEC13)、クロライド細胞内チャネルタンパク質1(CLIC1)、グアニンヌクレオチド結合タンパク質サブユニットベータ−2(GNB2L1)、ソーティングネキシン−6
(SNX6)、保存されたオリゴマーゴルジ複合体サブユニット3(COG3)、キャップ結合タンパク質サブユニット1(NCBP1)、細胞質ダイニン1軽中間鎖1(DYNC1LI1)、MOB様タンパク質フォセイン(phocein)(MOB4)、プログラム細胞死6相互作用タンパク質(PDCD6IP)、グルタレドキシン−1(GLRX)、ATPシンターゼサブユニットアルファ(ミトコンドリア)(ATP5A1)、トリークル(treacle)タンパク質(TCOF1)、ダイナクチンサブユニット1(DCTN1)、インポーチン−7(IP07)、エキスポーチン−2(CSE1L)、ATPシンターゼサブユニットガンマ(ミトコンドリアの)(ATP5C1)、輸送タンパク質粒子複合体サブユニット5(TRAPPC5)、チオレドキシンミトコンドリア(TXN2)、THO複合体サブユニット6相同体(THOC6)、エキスポーチン−1(XPO1)、核膜孔複合体タンパク質Nup50(NUP50)、トリークル(treacle)タンパク質(TCOF1)、核膜孔複合体タンパク質Nup93(NUP93)、核膜孔糖タンパク質p62(NUP62)、細胞質ダイニン1重鎖1(DYNC1H1)、チオレドキシン様タンパク質1(TXNL1)、核膜孔複合体タンパク質Nup214(NUP214)、タンパク質lin(Protein lin)−7相同体C(LIN7C)、ADP−リボシル化因子結合タンパク質GGA2(GGA2)、輸送タンパク質粒子複合体サブユニット4(TRAPPC4)、タンパク質クエーキング(Protein quaking)(QKI)、ペリリピン−3(PLIN3)、銅輸送タンパク質ATOX1(ATOX1)、特殊なミオシン−Ic(MYOIC)、ヌクレオポリンNUP53(NUP35)、液胞タンパク質選別関連のタンパク質18相同体(VPS18)、細胞質分裂タンパク質のデディケイター7(DOCK7)、ヌクレオポリンp54(NUP54)、Ras関連のGTP結合タンパク質C(RRAGC)、Rho−GAPドメインを有するArf−GAP(ANKリピートおよびPHドメイン)(ARAP1)、エキスポーチン−5(XPO5)、キネクチン(KTN1)、クロライド細胞内チャネルタンパク質6(CLIC6)、電位開口型カリウムチャネルサブユニットベータ−2(KCNAB2)、エキスポーチン−5(XPO5)、Ras関連のGTP結合タンパク質C(RRAGC)、リボソーム結合タンパク質1(RRBP1)、アシル−CoA結合ドメイン含有タンパク質6(ACBD6)、クロライド細胞内チャネルタンパク質5(CLIC5)、プレクストリン相同ドメイン含有ファミリーAメンバー(PLEKHA2)、ADP−リボシル化因子様タンパク質3(ARL3)、タンパク質輸送タンパク質Sec24C(SEC24C)、電位依存性アニオン選択的チャネルタンパク質(VDAC3)、プログラム細胞死6相互作用タンパク質(PDCD6IP)、クロライド細胞内チャネルタンパク質3(CLIC3)、多胞体サブユニット12A(FAM125A)、真核生物翻訳開始因子4E輸送体(EIF4ENIF1)、NmrA様ファミリードメイン含有タンパク質1(MRAL1)、核膜孔複合体タンパク質Nup98−Nup96(NUP98)、保存されたオリゴマーゴルジ複合体サブユニット1(COG1)、インポーチン−4(IPO4)、プレクストリン相同ドメイン含有ファミリーAメンバー(PLEKHA2)、細胞質ダイニン1重鎖1(DYNC1H1)、DENNドメイン含有タンパク質1C(DENND1C)、細胞質ダイニン1重鎖1(DYNC1H1)、タンパク質ELYS(AHCTF1)、輸送タンパク質粒子複合体サブユニット1(TRAPPC1)、グアニンヌクレオチド結合タンパク質様3(GNL3)、またはインポーチン−13(IP013)を含む。
幾つかの実施形態では、システイン含有タンパク質はシャペロンである。シャペロンとしての典型的なシステイン含有タンパク質は、限定されないが、60kDa熱ショックタンパク質(ミトコンドリア)(HSPD1)、T−複合体タンパク質1サブユニットイータ(CCT7)、T−複合体タンパク質1サブユニットイプシロン(CCT5)、熱ショック70kDaタンパク質4(HSPA4)、GrpEタンパク質相同体1(ミトコンドリア)(GRPELl)、チューブリン特異的シャペロンE(TBCE)、タンパク質unc−45相同体A(UNC45A)、セルピンH1(SERPINH1)、チューブリン特異的シャペロンD(TBCD)、ペルオキシソーム形成因子19(PEX19)、BAGファミリー分子シャペロン制御因子5(BAG5)、T−複合体タンパク質1サブユニットシータ(CCT8)、タンパク質キャノピー相同体3(CNPY3)、DnaJ相同体サブファミリーCメンバー10(DNAJC10)、ATP依存性ClpプロテアーゼATP結合サブユニットclp(CLPX)、またはミダシン(Midasin)(MDN1)を含む。
幾つかの実施形態では、システイン含有タンパク質は、アダプター、足場またはモジュレーターのタンパク質である。アダプター、足場またはモジュレーターのタンパク質としての典型的なシステイン含有タンパク質は、限定されないが、プロテアソーム活性化因子複合体サブユニット1(PSME1)、TIP41様タンパク質(TIPRL)、Crk様タンパク質(CRKL)、コフィリン−1(CFL1)、コンデンシン複合体サブユニット1(NCAPD2)、翻訳活性化因子GCN1(GCN1L1)、セリン/トレオニン−プロテインフォスファターゼ2A 56kDa制御性(PPP2R5D)、UPF0539タンパク質C7orf59(C7orf59)、タンパク質透明相同体(Protein diaphanous homolog)1(DIAPHl)、タンパク質アサンダー相同体(Protein asunder homolog)(Asun)、RasGTPアーゼ活性化様タンパク質IQGAP1(IQGAP1)、姉妹染色分体接着タンパク質PDS5相同体A(PDS5A)、レチクロン(Reticulon)−4(RTN4)、プロテアソーム活性化因子複合体サブユニット4(PSME4)、コンデンシン複合体サブユニット2(NCAPH)、姉妹染色分体接着タンパク質PDS5相同体A(PDS5A)、cAMP依存性タンパク質キナーゼI型−アルファ制御性(PRKAR1A)、宿主細胞因子1(HCFC1)、セリン/トレオニン−プロテインフォスファターゼ4制御性(PPP4R2)、核内のアポトーシスクロマチン凝縮インデューサー(ACIN1)、BRISCおよびBRCA1−A複合体メンバー1(BABAM1)、テトラトリコペプチドを有するインターフェロン誘導タンパク質(IFIT3)、Ras関連ドメイン含有タンパク質2(RASSF2)、Hsp70結合タンパク質1(HSPBP1)、TBC1ドメインファミリーメンバー15(TBC1D15)、ダイナミン結合タンパク質(DNMBP)、コンデンシン複合体サブユニット1(NCAPD2)、ベータ−2−シントロフィン(SNTB2)、Disks large相同体(Disks large homolog)1(DLG1)、TBC1ドメインファミリーメンバー13(TBC1D13)、フォルミン(Formin)結合タンパク質1様(FNBP1L)、翻訳活性化因子GCN1(GCN1L1)、GRB2関連のアダプタータンパク質(GRAP)、G2/有系分裂特異的サイクリン−B1(CCNB1)、ミオチューブラリン関連のタンパク質12(MTMR12)、タンパク質FADD(FADD)、翻訳活性化因子GCN1(GCN1L1)、Wings apart様タンパク質相同体(Wings apart−like protein homolog)(WAPAL)、cAMP依存性タンパク質キナーゼII型ベータ制御性(PRKAR2B)、Malcavernin(CCM2)、MPP1 55kDa赤血球膜タンパク質、アクチンフィラメント関連タンパク質1(AFAP1)、テンシン−3(TNS3)、tRNAメチルトランスフェラーゼ112相同体(TRMT112)、シンプレキン(Symplekin)(SYMPK)、TBC1ドメインファミリーメンバー2A(TBC1D2)、ATR相互作用タンパク質(ATRIP)、アタキシン−10(ATXN10)、コハク酸デヒドロゲナーゼ会合因子2(ミトコンドリア)(SDHAF2)、フォルミン結合タンパク質1(FNBP1)、ミオチューブラリン関連のタンパク質12(MTMR12)、テトラトリコペプチドを有するインターフェロン誘導タンパク質(IFIT3)、タンパク質CBFA2T2(CBFA2T2)、好中球細胞質因子(Neutrophil cytosol factor)1(NCF1)、またはタンパク質syndesmos(Protein syndesmos)(NUDT16L1)を含む。
幾つかの実施形態では、システイン含有タンパク質は、表1−5または表7−9に例示されるタンパク質を含む。幾つかの事例では、システイン含有タンパク質は、表1に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表1に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は、表2に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表2に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は、表3に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表3に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は、表4に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表4に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は、表5に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表5に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は、表7に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表7に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は、表8に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表8に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は、表9に例示されるタンパク質を含む。幾つかの実施形態では、システイン含有タンパク質は、表9に示されるシステイン残基を含む。幾つかの事例では、システイン含有タンパク質は修飾タンパク質であり、ここでタンパク質は、本明細書に記載される小分子断片によって、例えば、本明細書に記載される式(I)の小分子断片、本明細書に記載される式(II)のシステイン反応性プローブ、または図3に例示される小分子断片によって、システイン残基部位で修飾される。
幾つかの実施形態において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載される。幾つかの事例では、システイン含有タンパク質は、表3から選択される。
幾つかの場合では、各それぞれのシステイン含有タンパク質の1つ以上のシステイン残基が、表3に示される。幾つかの場合では、表3から選択されるシステイン含有タンパク質は、表3に示される少なくとも1つのシステイン部位で小分子断片によって修飾され、修飾されたシステイン含有タンパク質が生成される。幾つかの場合では、システイン含有タンパク質は、AIP、PES1、IKBKB、XPO1、KDM4B、R3C1、GSTP1、TNFAIP3、ACAT1、IRAK1、GNB2L1、IRF4、USP34、ZC3HAV1、USP7、PELI1、DCUN1D1、USP28、UBE2O、RRAGC、MLTK、USP22、KDM3A、またはUSP16から選択される。幾つかの場合では、システイン含有タンパク質は、AIP、PES1、IKBKB、XPO1、GSTP1、ACAT1、IRAK1、IRF4、ZC3HAV1、USP7、PELI1、USP28、UBE2O、RRAGC、MLTK、USP22、KDM3A、またはUSP16から選択される。幾つかの場合では、システイン含有タンパク質は、KDM4B、NR3C1、TNFAIP3、USP7、またはUSP22から選択される。幾つかの場合では、システイン含有タンパク質は、GNB2L1またはUSP34から選択される。幾つかの場合では、システイン含有タンパク質はDCUN1D1である。幾つかの場合では、システイン含有タンパク質は、PES1、IKBKB、GSTP1、ACAT1、IRAK1、ZC3HAV1またはRRAGCから選択される。幾つかの場合では、システイン含有タンパク質は、XPO1、GNB2L1、USP34、UBE2O、MLTKまたはUSP22から選択される。幾つかの場合では、システイン含有タンパク質は、KDM4BまたはNR3C1から選択される。幾つかの場合では、システイン含有タンパク質は、TNFAIP3、USP7、USP28、KDM3AまたはUSP16から選択される。幾つかの場合では、システイン含有タンパク質は、IRF4、PELI1、DCUN1D1またはUSP22から選択される。幾つかの場合では、システイン含有タンパク質はAIPである。幾つかの場合では、システイン含有タンパク質は酵素であり、酵素は、IKBKB、KDM4B、GSTP1、TNFAIP3、ACAT1、IRAK1、USP34、USP7、PELI1、USP28、UBE2O、MLTK、USP22、KDM3A、またはUSP16から選択される。幾つかの場合では、システイン含有タンパク質は、転写因子または制御因子であり、転写因子または制御因子は、NR3C1、IRF4またはZC3HAV1から選択される。幾つかの場合では、システイン含有タンパク質は、チャネル、輸送体、または受容体であり、チャネル、輸送体、または受容体は、GNB2L1またはRRAGCから選択される。幾つかの場合では、システイン含有タンパク質は、AIP、PES1、XPO1またはDCUN1D1から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、CYR61、UBE2L6、XPO1、ADA、NR3C1、POU2F2、UCHL3、MGMT、ERCC3、ACAT1、STAT3、UBA7、CASP2、IDH2、LRBA、UBE2L3、RELB、IRF8、CASP8、PDIA6、PCK2、PFKFB4、PDE12、USP34、USP48、SMARCC2またはSAMHD1から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、CYR61、R3C1、UCHL3、ERCC3、ACAT1、STAT3、CASP2、LRBA、UBE2L3、RELB、PDIA6、PCK2、PFKFB4、USP48またはSMARCC2から選択される。幾つかの場合では、システイン含有タンパク質は、UBE2L6、POU2F2、MGMT、ACAT1、UBA7、CASP8、PDE12またはUSP34から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61またはXPO1から選択される。幾つかの場合では、システイン含有タンパク質は、ADA、MGMT、IDH2、IRF8またはSAMHD1から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、CYR61、XPO1、R3C1またはSMARCC2から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、UBE2L6、MGMT、ERCC3、ACAT1またはUSP48から選択される。幾つかの場合では、システイン含有タンパク質は、ADA、RELBまたはUSP34から選択される。幾つかの場合では、システイン含有タンパク質は、UCHL3、CASP2、IDH2、LRBA、CASP8、PCK2またはPDE12から選択される。幾つかの場合では、システイン含有タンパク質は、MGMT、ACAT1、UBA7、UBE2L3またはIRF8から選択される。幾つかの場合では、システイン含有タンパク質は、PFKFB4、ACAT1またはSTAT3から選択される。幾つかの場合では、システイン含有タンパク質は、POU2F2、PDIA6またはSAMHD1から選択される。幾つかの場合では、システイン含有タンパク質は酵素であり、酵素は、UBE2L6、ADA、UCHL3、MGMT、ERCC3、ACAT1、UBA7、CASP2、IDH2、UBE2L3、CASP8、PDIA6、PCK2、PFKFB4、PDE12、USP34、USP48またはSAMHD1から選択される。幾つかの場合では、システイン含有タンパク質は、転写因子または制御因子であり、転写因子または制御因子は、R3C1、POU2F2、STAT3、RELB、IRF8またはSMARCC2から選択される。幾つかの場合では、システイン含有タンパク質は、ZAP70、PRKCQまたはPRMT1から選択される。幾つかの場合では、システイン含有タンパク質は、ZAP70またはPRKCQから選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、ZNF217、NCF1、IREB2、LRBA、CDK5、EP300、EZH2、UBE2S、VCPIP1、RRAGCまたはIRAK4から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、ZNF217、IREB2、EP300、UBE2S、VCPIP1、RRAGCまたはIRAK4から選択される。幾つかの場合では、システイン含有タンパク質は、NCF1、LRBAまたはCDK5から選択される。幾つかの場合では、システイン含有タンパク質はEZH2である。幾つかの場合では、システイン含有タンパク質は、ZNF217、NCF1、CDK5、EP300またはIRAK4から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、IREB2、LRBAまたはUBE2Sから選択される。幾つかの場合では、システイン含有タンパク質は、EZH2、VCPIP1またはRRAGCから選択される。幾つかの場合では、システイン含有タンパク質は酵素であり、酵素は、CDK5、EP300、EZH2、UBE2S、VCPIP1またはIRAK4から選択される。幾つかの場合では、システイン含有タンパク質は、転写因子または制御因子であり、転写因子または制御因子は、ZNF217またはIREB2から選択される。幾つかの場合では、システイン含有タンパク質は、アダプター、足場タンパク質またはモジュレータータンパク質であり、アダプター、足場タンパク質またはモジュレータータンパク質はNCF1から選択される。幾つかの場合では、システイン含有タンパク質は、チャネル、輸送体または受容体であり、チャネル、輸送体または受容体はRRAGCから選択される。幾つかの場合では、システイン含有タンパク質は、CYR61またはLRBAから選択される。幾つかの場合では、システイン含有タンパク質は、長さが約20、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000またはそれ以上のアミノ酸残基である。幾つかの場合では、修飾されたシステイン含有タンパク質のシステイン残基は構造SRを有し、ここでRは、
から選択され、式中、R
1は、H、C1−C3アルキル、またはアリールであり;およびF’は小分子断片部分である。幾つかの場合では、小分子断片は、約175、200、225、250、275、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン、またはそれ以上の分子量を有する。幾つかの場合では、小分子断片の分子量は、ハロゲン、非金属、または遷移金属での富化前のものである。幾つかの実施形態では、小分子断片の分子量は、炭素および水素の原子に基づいて及び随意に窒素、酸素及び/又は硫黄の原子にさらに基づいて計算される。幾つかの実施形態では、小分子断片の分子量は、ハロゲン、遷移金属またはその組み合わせの分子量を含まない。幾つかの場合では、小分子断片は式(I)の小分子断片:
であり、式中、RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;およびFは小分子断片部分である。幾つかの場合では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは、化合物ライブラリーから得られる。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの場合では、小分子断片は、システイン含有タンパク質に不可逆的に結合する。幾つかの場合では、小分子断片は、システイン含有タンパク質に可逆的に結合する。
幾つかの実施形態において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、ここでシステイン含有タンパク質は、表10A(酵素)から選択される。幾つかの場合では、各それぞれのシステイン含有タンパク質の1つ以上のシステイン残基が、表10Aに示される。幾つかの場合では、表10Aから選択されるシステイン含有タンパク質は、表10Aに示される少なくとも1つのシステイン部位で小分子断片によって修飾され、修飾されたシステイン含有タンパク質が生成される。幾つかの場合では、システイン含有タンパク質は、長さが約20、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000またはそれ以上のアミノ酸残基である。幾つかの場合では、修飾されたシステイン含有タンパク質のシステイン残基は、構造SRを有し、ここでRは、
から選択され、式中、R
1は、H、C1−C3アルキル、またはアリールであり;およびF’は小分子断片部分である。幾つかの場合では、小分子断片は、約175、200、225、250、275、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン、またはそれ以上の分子量を有する。幾つかの場合では、小分子断片の分子量は、ハロゲン、非金属、または遷移金属での富化前のものである。幾つかの実施形態では、小分子断片の分子量は、炭素および水素の原子に基づいて及び随意に窒素、酸素及び/又は硫黄の原子にさらに基づいて計算される。幾つかの実施形態では、小分子断片の分子量は、ハロゲン、遷移金属またはその組み合わせの分子量を含まない。幾つかの場合では、小分子断片は式(I)の小分子断片:
であり、式中、RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;およびFは小分子断片部分である。幾つかの場合では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは化合物ライブラリーから得られる。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの場合では、小分子断片は、システイン含有タンパク質に不可逆的に結合する。幾つかの場合では、小分子断片は、システイン含有タンパク質に可逆的に結合する。
幾つかの実施形態において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、ここでシステイン含有タンパク質は、表10B(転写因子および制御因子)から選択される。幾つかの場合では、各それぞれのシステイン含有タンパク質の1つ以上のシステイン残基が、表10Bに示される。幾つかの場合では、表10Bから選択されるシステイン含有タンパク質は、表10Bに示される少なくとも1つのシステイン部位で小分子断片によって修飾され、修飾されたシステイン含有タンパク質が生成される。幾つかの場合では、システイン含有タンパク質は、長さが約20、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000またはそれ以上のアミノ酸残基である。幾つかの場合では、修飾されたシステイン含有タンパク質のシステイン残基は、構造SRを有し、ここでRは、
から選択され、ここでR
1は、H、C1−C3アルキル、またはアリールであり;およびF’は小分子断片部分である。幾つかの場合では、小分子断片は、約175、200、225、250、275、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン、またはそれ以上の分子量を有する。幾つかの場合では、小分子断片の分子量は、ハロゲン、非金属、または遷移金属での富化前のものである。幾つかの実施形態では、小分子断片の分子量は、炭素および水素の原子に基づいて及び随意に窒素、酸素及び/又は硫黄の原子にさらに基づいて計算される。幾つかの実施形態では、小分子断片の分子量は、ハロゲン、遷移金属またはその組み合わせの分子量を含まない。幾つかの場合では、小分子断片は式(I)の小分子断片:
であり、式中、RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;およびFは小分子断片部分である。幾つかの場合では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは化合物ライブラリーから得られる。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの場合では、小分子断片は、システイン含有タンパク質に不可逆的に結合する。幾つかの場合では、小分子断片は、システイン含有タンパク質に可逆的に結合する。
幾つかの実施形態において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、ここでシステイン含有タンパク質は、表10C(チャネル、輸送体または受容体)から選択される。幾つかの場合では、各それぞれのシステイン含有タンパク質の1つ以上のシステイン残基が、表10Cに示される。幾つかの場合では、表10Cから選択されるシステイン含有タンパク質は、表10Cに示される少なくとも1つのシステイン部位で小分子断片によって修飾され、修飾されたシステイン含有タンパク質が生成される。幾つかの場合では、システイン含有タンパク質は、長さが約20、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000またはそれ以上のアミノ酸残基である。幾つかの場合では、修飾されたシステイン含有タンパク質のシステイン残基は、構造SRを有し、ここでRは、
から選択され、式中、R
1は、H、C1−C3アルキル、またはアリールであり;およびF’は小分子断片部分である。幾つかの場合では、小分子断片は、約175、200、225、250、275、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン、またはそれ以上の分子量を有する。幾つかの場合では、小分子断片の分子量は、ハロゲン、非金属、または遷移金属での富化前のものである。幾つかの実施形態では、小分子断片の分子量は、炭素および水素の原子に基づいて及び随意に窒素、酸素及び/又は硫黄の原子にさらに基づいて計算される。幾つかの実施形態では、小分子断片の分子量は、ハロゲン、遷移金属またはその組み合わせの分子量を含まない。幾つかの場合では、小分子断片は式(I)の小分子断片:
であり、式中、RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;およびFは小分子断片部分である。幾つかの場合では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは化合物ライブラリーから得られる。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの場合では、小分子断片は、システイン含有タンパク質に不可逆的に結合する。幾つかの場合では、小分子断片は、システイン含有タンパク質に可逆的に結合する。
幾つかの実施形態において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、ここでシステイン含有タンパク質は、表10D(アダプター、足場またはモジュレーターのタンパク質)から選択される。幾つかの場合では、各それぞれのシステイン含有タンパク質の1つ以上のシステイン残基が、表10Dに示される。幾つかの場合では、表10Dから選択されるシステイン含有タンパク質は、表10Dに示される少なくとも1つのシステイン部位で小分子断片によって修飾され、修飾されたシステイン含有タンパク質が生成される。幾つかの場合では、システイン含有タンパク質は、長さが約20、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000またはそれ以上のアミノ酸残基である。幾つかの場合では、修飾されたシステイン含有タンパク質のシステイン残基は、構造SRを有し、ここでRは、
から選択され、式中、R
1は、H、C1−C3アルキル、またはアリールであり;およびF’は小分子断片部分である。幾つかの場合では、小分子断片は、約175、200、225、250、275、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン、またはそれ以上の分子量を有する。幾つかの場合では、小分子断片の分子量は、ハロゲン、非金属、または遷移金属での富化前のものである。幾つかの実施形態では、小分子断片の分子量は、炭素および水素の原子に基づいて及び随意に窒素、酸素及び/又は硫黄の原子にさらに基づいて計算される。幾つかの実施形態では、小分子断片の分子量は、ハロゲン、遷移金属またはその組み合わせの分子量を含まない。幾つかの場合では、小分子断片は式(I)の小分子断片:
であり、式中、RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;およびFは小分子断片部分である。幾つかの場合では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは化合物ライブラリーから得られる。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの場合では、小分子断片は、システイン含有タンパク質に不可逆的に結合する。幾つかの場合では、小分子断片は、システイン含有タンパク質に可逆的に結合する。
幾つかの実施形態において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、ここでシステイン含有タンパク質は、表10Eから選択される。幾つかの場合では、各それぞれのシステイン含有タンパク質の1つ以上のシステイン残基が、表10Eに示される。幾つかの場合では、表10Eから選択されるシステイン含有タンパク質は、表10Eに示される少なくとも1つのシステイン部位で小分子断片によって修飾され、修飾されたシステイン含有タンパク質が生成される。幾つかの場合では、システイン含有タンパク質は、長さが約20、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000またはそれ以上のアミノ酸残基である。幾つかの場合では、修飾されたシステイン含有タンパク質のシステイン残基は、構造SRを有し、ここでRは、
から選択され、式中、R
1は、H、C 1−C3アルキル、またはアリールであり;およびF’は小分子断片部分である。幾つかの場合では、小分子断片は、約175、200、225、250、275、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン、またはそれ以上の分子量を有する。幾つかの場合では、小分子断片の分子量は、ハロゲン、非金属、または遷移金属での富化前のものである。幾つかの実施形態では、小分子断片の分子量は、炭素および水素の原子に基づいて及び随意に窒素、酸素及び/又は硫黄の原子にさらに基づいて計算される。幾つかの実施形態では、小分子断片の分子量は、ハロゲン、遷移金属またはその組み合わせの分子量を含まない。幾つかの場合では、小分子断片は式(I)の小分子断片:
であり、式中、RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;およびFは小分子断片部分である。幾つかの場合では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは化合物ライブラリーから得られる。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの場合では、小分子断片は、システイン含有タンパク質に不可逆的に結合する。幾つかの場合では、小分子断片は、システイン含有タンパク質に可逆的に結合する。
幾つかの実施形態において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXPC*Zを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、AIP、PES1、IKBKB、XPO1、KDM4B、NR3C1、GSTP1、TNFAIP3、ACAT1、IRAK1、GNB2L1、IRF4、USP34、ZC3HAV1、USP7、PELI1、DCUN1D1、USP28、UBE2O、RRAGC、MLTK、USP22、KDM3A、またはUSP16から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXPC*Xnを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびXnは無極性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、AIP、PES1、IKBKB、XPO1、GSTP1、ACAT1、IRAK1、IRF4、ZC3HAV1、USP7、PELI1、USP28、UBE2O、RRAGC、MLTK、USP22、KDM3A、またはUSP16から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXPC*XPを含み、ここでXPは極性残基であり、C*は修飾の部位を示す。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、KDM4B、NR3C1、TNFAIP3、USP7またはUSP22から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXPC*Xbを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびXは塩基性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、GNB2L1またはUSP34から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXPC*Xaを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびXaは酸性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質はDCUN1D1である。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフSC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、IKBKB、GSTP1、ACAT1、IRAK1、ZC3HAV1またはRRAGCから選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフNC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、XPO1、GNB2L1、USP34、UBE2O、MLTKまたはUSP22から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフYC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、KDM4BまたはR3C1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフTC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、TNFAIP3、USP7、USP28、KDM3AまたはUSP16から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフQC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、IRF4、PELI1、DCUN1D1またはUSP22から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフCC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質はAIPである。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質は酵素であり、酵素はモチーフXPC*Zを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、酵素は、IKBKB、KDM4B、GSTP1、TNFAIP3、ACAT1、IRAK1、USP34、USP7、PELI1、USP28、UBE2O、MLTK、USP22、KDM3A、またはUSP16から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質は転写因子または制御因子であり、転写因子または制御因子はモチーフXPC*Zを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、転写因子または制御因子は、R3C1、IRF4またはZC3HAV1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はチャネル、輸送体または受容体であり、チャネル、輸送体または受容体はモチーフXPC*Zを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、チャネル、輸送体または受容体は、GNB2L1またはRRAGCから選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXPC*Zを含み、ここでXPは極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、AIP、PES1、XPO1またはDCUN1D1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXnC*Zを含み、ここでXnは無極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、CYR61、UBE2L6、XPO1、ADA、R3C1、POU2F2、UCHL3、MGMT、ERCC3、ACAT1、STAT3、UBA7、CASP2、IDH2、LRBA、UBE2L3、RELB、IRF8、CASP8、PDIA6、PCK2、PFKFB4、PDE12、USP34、USP48、SMARCC2またはSAMHD1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXnC*Xnを含み、ここでXnは無極性残基であり、C*は修飾の部位を示す。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、CYR61、R3C1、UCHL3、ERCC3、ACAT1、STAT3、CASP2、LRBA、UBE2L3、RELB、PDIA6、PCK2、PFKFB4、USP48またはSMARCC2から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXnC*XPを含み、ここでXnは無極性残基であり、C*は修飾の部位を示し、およびXPは極性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、UBE2L6、POU2F2、MGMT、ACAT1、UBA7、CASP8、PDE12またはUSP34から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXnC*Xaを含み、ここでXnは無極性残基であり、C*は修飾の部位を示し、およびXaは酸性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61またはXPO1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXnC*Xbを含み、ここでXnは無極性残基であり、C*は修飾の部位を示し、およびXは塩基性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、ADA、MGMT、IDH2、IRF8またはSAMHD1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフLC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、CYR61、XPO1、R3C1またはSMARCC2から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフPC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、UBE2L6、MGMT、ERCC3、ACAT1またはUSP48から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフGC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、ADA、RELBまたはUSP34から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフAC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、UCHL3、CASP2、IDH2、LRBA、CASP8、PCK2またはPDE12から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフVC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、MGMT、ACAT1、UBA7、UBE2L3またはIRF8から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフIC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、PFKFB4、ACAT1またはSTAT3から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXrC*Zを含み、ここでXrは芳香族残基を示し、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、POU2F2、PDIA6またはSAMHD1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質は酵素であり、酵素はモチーフXnC*Zを含み、ここでXnは無極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、酵素は、UBE2L6、ADA、UCHL3、MGMT、ERCC3、ACAT1、UBA7、CASP2、IDH2、UBE2L3、CASP8、PDIA6、PCK2、PFKFB4、PDE12、USP34、USP48またはSAMHD1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質は転写因子または制御因子であり、転写因子または制御因子はモチーフXnC*を含み、ZここでXnは無極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、転写因子または制御因子は、R3C1、POU2F2、STAT3、RELB、IRF8またはSMARCC2から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXnC*Zを含み、ここでXnは無極性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、PES1、CYR61、XPO1またはLRBAから選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXaC*Zを含み、ここでXaは酸性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、ZAP70、PRKCQまたはPRMT1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフEC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、ZAP70またはPRKCQから選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXbC*Zを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、ZNF217、NCF1、IREB2、LRBA、CDK5、EP300、EZH2、UBE2S、VCPIP1、RRAGCまたはIRAK4から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXbC*Xnを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびXnは無極性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、ZNF217、IREB2、EP300、UBE2S、VCPIP1、RRAGCまたはIRAK4から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXbC*XPを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびXPは極性残基である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、NCF1、LRBAまたはCDK5から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXbC*Xを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示す。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質はEZH2である。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフRC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、ZNF217、NCF1、CDK5、EP300またはIRAK4から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフKC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61、IREB2、LRBAまたはUBE2Sから選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフHC*Zを含み、ここでC*は修飾の部位を示し、Zは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、EZH2、VCPIP1またはRRAGCから選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質は酵素であり、酵素はモチーフXbC*Zを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、酵素は、CDK5、EP300、EZH2、UBE2S、VCPIP1またはIRAK4から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質は転写因子または制御因子であり、転写因子または制御因子はモチーフXbC*Zを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、転写因子または制御因子は、ZNF217またはIREB2から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はアダプター、足場タンパク質またはモジュレータータンパク質であり、アダプター、足場タンパク質またはモジュレータータンパク質はモチーフXbC*Zを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、アダプター、足場タンパク質またはモジュレータータンパク質は、NCF1から選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はチャネル、輸送体または受容体であり、チャネル、輸送体または受容体はモチーフXbC*Zを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、チャネル、輸送体または受容体は、RRAGCから選択される。
幾つかの事例において、本明細書には、システイン含有タンパク質のシステイン残基に共有結合している小分子断片を含む修飾されたシステイン含有タンパク質が記載され、システイン含有タンパク質はモチーフXbC*Zを含み、ここでXbは塩基性残基であり、C*は修飾の部位を示し、およびZは任意のアミノ酸である。幾つかの場合では、システイン含有タンパク質は、表3から選択される。幾つかの場合では、システイン含有タンパク質は、CYR61またはLRBAから選択される。
幾つかの場合では、上に記載されるシステイン含有タンパク質は、長さが約20、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、600、700、800、900、1000またはそれ以上のアミノ酸残基を含む。
幾つかの場合では、上に記載される修飾されたシステイン含有タンパク質のシステイン残基は、構造SRを有し、ここでRは、
から選択され、式中、R
1は、H、C1−C3アルキル、またはアリールであり;
およびFは小分子断片部分である。幾つかの場合では、小分子断片は、約175、200、225、250、275、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000ダルトン、またはそれ以上の分子量を有する。幾つかの場合では、小分子断片の分子量は、ハロゲン、非金属、または遷移金属での富化前のものである。幾つかの実施形態では、小分子断片の分子量は、炭素および水素の原子に基づいて及び随意に窒素、酸素及び/又は硫黄の原子にさらに基づいて計算される。幾つかの実施形態では、小分子断片の分子量は、ハロゲン、遷移金属またはその組み合わせの分子量を含まない。幾つかの場合では、小分子断片は式(I)の小分子断片:
であり、ここで、RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;およびFは小分子断片部分である。幾つかの場合では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは化合物ライブラリーから得られる。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの場合では、小分子断片は、上に記載されるシステイン含有タンパク質に不可逆的に結合する。幾つかの場合では、小分子断片は、上に記載されるシステイン含有タンパク質に可逆的に結合する。
<組成物、細胞、および細胞集団>
本明細書にはまた、システイン含有タンパク質に結合された小分子断片の組成物、システイン含有タンパク質に結合されたシステイン反応性プローブ、および処理されたサンプル組成物が開示される。幾つかの実施形態では、本明細書に記載される組成物は、式(I)の小分子断片を含み:
式中:
RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;および
Fは小分子断片部分であり;および
組成物はさらに、小分子断片に対する共有結合であるシステイン含有タンパク質を含む。
幾つかの実施形態において、本明細書にはまた、式(II)のシステイン反応性プローブを含む組成物が記載され:
式中:
RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基に対する共有結合を形成することができる部分から選択される反応性部分であり;および
AHMは親和性ハンドル部分であり;および
組成物はさらに、システイン反応性プローブに対する共有結合であるシステイン含有タンパク質を含む。
幾つかの実施形態において、本明細書にはまた、単離された細胞または組織サンプルである単離されたサンプル;および単離されたサンプル中に発現されたシステイン含有タンパク質と相互作用するその能力に関して分析されるシステイン反応性プローブを含む組成物が記載される。
本明細書にはさらに、単離された処理した細胞および細胞集団が開示される。幾つかの実施形態において、本明細書には、システイン含有タンパク質に共有結合されたシステイン反応性プローブを含む単離された処理した細胞が記載される。幾つかの事例では、単離された処理した細胞は、システイン反応性プローブのセットをさらに含み、ここでシステイン反応性プローブの各々は、システイン含有タンパク質に共有結合される。
幾つかの実施形態において、本明細書には、システイン含有タンパク質に共有結合された小分子断片を含む単離された処理した細胞が記載される。幾つかの事例では、単離された処理した細胞は、小分子断片のセットをさらに含み、ここで小分子断片の各々は、システイン含有タンパク質に共有結合される。幾つかの事例では、単離された処理した細胞はさらに、システイン反応性プローブを含む。幾つかの事例では、単離された処理した細胞はさらに、システイン反応性プローブのセットを含む。
幾つかの実施形態において、本明細書にはまた、システイン含有タンパク質に共有結合されたシステイン反応性プローブのセットを含む細胞の単離された処理した集団が記載される。
幾つかの実施形態において、本明細書にはさらに、システイン含有タンパク質に共有結合された小分子断片のセットを含む細胞の単離された処理した集団が記載される。幾つかの事例では、細胞の単離された処理した集団はさらに、システイン反応性プローブのセットを含む。
本明細書の他のところに開示されるように、小分子断片は式(I)の小分子断片であり:
式中:
RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基との共有結合を形成することができる部分から選択される反応性部分であり;および
Fは小分子断片部分である。
幾つかの事例では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの場合では、Fは化合物ライブラリーから得られる。幾つかの実施形態では、化合物ライブラリーは、ChemBridge断片ライブラリー、Pyramid Platform Fragment −Based Drug Discovery、Maybridge断片ライブラリー、AnalytiConからのFRGx、AnCoreXからのTCI−Flag、ASINEXからのBio Building Blocks、Charles RiverからのBioFocus 3D、Emerald BioからのFragments of Life(FOL)、Enamine Fragmentライブラリー、IOTA Diverse 1500、BIONET断片ライブラリー、ife Chemicals Fragments Collection、OTAVA断片ライブラリー、Prestwick断片ライブラリー、Selcia断片ライブラリー、TimTec断片ベースのライブラリー、Vitas−M LaboratoryからのAllium、またはZenobia断片ライブラリーを含む。幾つかの場合では、Fは、図3に例示される小分子断片部分である。幾つかの場合では、Fは、Fをカルボニル部分に結合させるリンカー部分をさらに含む。幾つかの実施形態では、小分子断片は、図3に例示される小分子断片部分である。
本明細書の他のところに記載されるように、システイン反応性プローブは、式(II)のシステイン反応性プローブであり:
式中:
RMは、マイケル受容体部分、脱離基部分、またはシステイン残基のチオール基に対する共有結合を形成することができる部分から選択される反応性部分であり;および
AHMは親和性ハンドル部分である。
幾つかの実施形態では、マイケル受容体部分は、アルケンまたはアルキンの部分を含む。幾つかの事例では、親和性ハンドル部分は、親和性ハンドル、およびシステイン含有タンパク質のシステイン残基に対するシステイン反応性プローブの共有結合の相互作用を促進する結合部分を含む。幾つかの場合では、結合部分は、化合物ライブラリーから得られた小分子断片である。幾つかの場合では、化合物ライブラリーは、ChemBridge断片ライブラリー、Pyramid Platform Fragment −Based Drug Discovery、Maybridge断片ライブラリー、AnalytiConからのFRGx、 AnCoreXからのTCI−Flag、ASINEXからのBio Building Blocks、Charles RiverからのBioFocus 3D、Emerald BioからのFragments of Life(FOL)、Enamine Fragmentライブラリー、IOTA Diverse 1500、BIONET断片ライブラリー、ife Chemicals Fragments Collection、OTAVA断片ライブラリー、Prestwick断片ライブラリー、Selcia断片ライブラリー、TimTec断片ベースのライブラリー、Vitas−M LaboratoryからのAllium、またはZenobia断片ライブラリーを含む。
幾つかの事例では、親和性ハンドルは、生体直交型の親和性ハンドルである。幾つかの場合では、親和性ハンドルは、カルボジイミド、N−ヒドロキシスクシンイミド(NHS)エステル、イミドエステル、ペンタフルオロフェニルエステル、ヒドロキシメチルホスフィン、マレイミド、ハロアセチル、ピリジルジスルフィド、チオ硫酸塩、ビニルスルホン、ヒドラジド、アルコキシアミン、アルキン、アジド、またはイソシアネートの基を含む。幾つかの場合では、親和性ハンドルは、アルキンまたはアジドの基を含む。幾つかの事例では、親和性ハンドルはさらに、親和性リガンドに結合される。幾つかの事例では、親和性リガンドは、発色団、標識基、またはその組み合わせを含む。幾つかの場合では、発色団は、蛍光色素、非蛍光色素発色団、消光剤、吸収発色団、フルオロフォア、有機染料、無機染料、金属キレート、または蛍光酵素基質を含む。幾つかの場合では、標識基は、ビオチン部分、ストレプトアビジン部分、ビーズ、樹脂、固体支持体、またはそれらの組み合わせである。幾つかの事例では、親和性ハンドル部分はさらに、発色団を含む。幾つかの実施形態では、システイン反応性プローブは、図3に例示されるシステイン反応性プローブである。
本明細書の他のところにさらに記載されるように、細胞または細胞集団は、ヒトまたはヒト以外の霊長類などのあらゆる哺乳動物から得られる。幾つかの実施形態では、細胞または細胞集団は、上皮細胞、結合組織細胞、ホルモン分泌細胞、神経細胞、骨格筋細胞、血液細胞、または免疫系細胞である。追加の実施形態では、細胞または細胞集団は、癌性であるか、または腫瘍部位から得られる。
<システイン相互作用部位を含むポリペプチド>
本明細書にはさらに、本明細書に記載される方法によって特定されたシステイン相互作用部位の1つ以上を含むポリペプチドが開示される。幾つかの実施形態において、本明細書には、表1−3または8−9から選択されるアミノ酸配列の少なくとも7つの連続するアミノ酸に対する少なくとも90%の配列同一性を含む、単離および精製されたポリペプチドが記載される。幾つかの実施形態では、単離および精製されたポリペプチドは、表1−3または8−9から選択されるアミノ酸配列の少なくとも7つの連続するアミノ酸に対する少なくとも91%、92% 93% 94%、95%、96%、97%、98%、または99%の配列同一性を含む。幾つかの実施形態では、単離および精製されたポリペプチドは、表1−3または8−9から選択されるアミノ酸配列の少なくとも7つの連続するアミノ酸に対する100%の配列同一性を含む。幾つかの事例では、単離および精製されたポリペプチドは、表1−3または8−9から選択されるアミノ酸配列の全長に対する100%の配列同一性を含む。幾つかの事例では、単離および精製されたポリペプチドは、長さが最大で50のアミノ酸である。
幾つかの実施形態において、本明細書にはさらに、表1−3または8−9から選択されるアミノ酸配列の少なくとも7つの連続するアミノ酸に対する少なくとも90%の配列同一性を含むポリペプチドをコードする核酸が記載される。幾つかの実施形態では、ポリペプチドをコードする核酸は、表1−3または8−9から選択されるアミノ酸配列の少なくとも7つの連続するアミノ酸に対する少なくとも91%、92%、93%、94%、95%、96%、97%、98%、または99%の配列同一性を含む。幾つかの実施形態では、ポリペプチドをコードする核酸は、表1−3または8−9から選択されるアミノ酸配列の少なくとも7つの連続するアミノ酸に対する100%の配列同一性を含む。幾つかの実施形態では、ポリペプチドをコードする核酸は、表1−3または8−9から選択されるアミノ酸配列の全長に対する100%の配列同一性を含む。
幾つかの実施形態において、本明細書にはさらに、生物学的に活性なシステイン部位をタンパク質上にマッピングする方法が開示され、該方法は、サンプルからシステイン反応性プローブのタンパク質複合体のセットを収集する工程であって、システイン反応性プローブが、システイン含有タンパク質上に位置付けられたシステイン残基との共有結合を形成することができる反応性部分を含む、工程;プロテオミクス解析手段によってシステイン反応性プローブ−タンパク質複合体のセットを解析する工程;および前の工程に基づいて、生物学的に活性なシステイン部位をタンパク質上にマッピングする工程を含む。
幾つかの実施形態では、解析する工程はさらに、タンパク質断片のセットを生成するために、プロテアーゼでシステイン反応性プローブ−タンパク質複合体のセットを処理する工程を含む。プロテアーゼは、セリンプロテアーゼ、トレオニンプロテアーゼ、システインプロテアーゼ、アスパラギン酸プロテアーゼ、グルタミン酸プロテアーゼ、またはメタロプロテアーゼである。幾つかの事例では、プロテアーゼはセリンプロテアーゼである。幾つかの事例では、プロテアーゼはトリプシンである。幾つかの事例では、システイン反応性プローブのタンパク質複合体はさらに、ビオチン部分などの標識基に結合される。幾つかの事例では、ビオチン部分などの標識基はさらに、リンカーを含む。幾つかの事例では、リンカーはペプチドである。幾つかの事例では、ペプチドリンカーは、長さが約7、8、9、10、11、12、13、14、15、16、17、18、19、20またはそれ以上のアミノ酸残基である。幾つかの事例では、ペプチドリンカーは切断部位を含む。切断部位の限定しないリストは、タバコエッチウイルス(TEV)、トロンビン(Thr)、エンテロキナーゼ(EKT)、活性化第X因子(Xa)、またはヒトライノウイルス3Cプロテアーゼ(3C/PreScission)を含む。幾つかの事例では、ペプチドリンカーは、TEVプロテアーゼ切断部位を含む。幾つかの事例では、TEVプロテアーゼ切断部位は、以下の配列:Gly−Gln−Phe−Tyr−Leu−Asn−Glu(SEQ ID NO:860)を含む。幾つかの事例では、ビオチン部分はさらに、ビーズ(例えばストレプトアビジン結合ビーズ)に連結される。
幾つかの事例では、(リンカーを含む及びストレプトアビジン結合ビーズに結合されたビオチン部分を介して)ビーズに結合されたシステイン反応性プローブ−タンパク質複合体からのタンパク質は、トリプシンで温浸され、固定化されたペプチドまたはタンパク質断片はさらに、分離され、収集される。幾つかの事例では、収集されたペプチドまたはタンパク質断片は、その後、プロテアーゼ(例えばTEVプロテアーゼ)によって温浸され、処理されたタンパク質断片は、その後、分離され、解析のために収集される。幾つかの事例では、解析は、上に及び本明細書の他のところに記載されるようなプロテオミクス解析である。幾つかの事例では、タンパク質断片の配列がさらに決定される。幾つかの事例では、タンパク質断片は、システイン含有タンパク質上の小分子断片結合部位に相関する。
幾つかの実施形態では、タンパク質断片の配列は、表1−3または8−9に例示されるような配列に相関する。幾つかの事例では、表1−3または8−9に示されるような配列は、薬物結合部位としての全長タンパク質上の部位に相関する。幾つかの事例では、表1−3または8−9に示されるような配列は、薬物結合部位に相関する。幾つかの事例では、表1−3または8−9に示されるような配列の1つ以上を含むポリペプチドは、小分子断片のスクリーニングのためのプローブとして働く。
幾つかの事例では、ポリペプチドの生成後に、ポリペプチドは、不純物を除去するために精製工程の1以上のラウンドにさらされる。幾つかの事例では、精製工程は、親和性ベース、サイズ排除ベース、イオン交換ベースの方法などの分離方法を利用するクロマトグラフィー工程である。幾つかの場合では、ポリペプチドは、最大で30%、40%、50%、60%、70%、80%、90%、95%、99%、99.9%、または100%純粋であるか、あるいは不純物が存在しない。幾つかの場合では、ポリペプチドは、少なくとも30%、40% 50% 60%、70%、80%、90%、95%、99%、99.9%、または100%純粋でるか、あるいは不純物が存在しない。
上に記載されるように、システイン含有タンパク質に由来するポリペプチドをコードする核酸は、不純物を除去するために精製工程の1以上のラウンドにさらされる。幾つかの事例では、精製工程は、親和性ベース、サイズ排除ベース、イオン交換ベースの方法などの分離方法を利用するクロマトグラフィー工程である。幾つかの場合では、核酸は、最大で30%、40%、50%、60%、70%、80%、90%、95%、99%、99.9%、または100%純粋であるか、あるいは不純物が存在しない。幾つかの場合では、核酸は、少なくとも30%、40%、50%、60%、70%、80%、90%、95%、99%、99.9%、または100%純粋であるか、あるいは不純物が存在しない。
本明細書に使用されるように、ポリペプチドは、天然アミノ酸、非天然アミノ酸、またはその組み合わせを含む。幾つかの事例では、アミノ酸残基は、アミノ基およびカルボキシル基の両方を含有している分子を指す。適切なアミノ酸は、限定することなく、自然発生のアミノ酸のD−異性体およびL−異性体の両方の他に、有機合成または他の代謝経路によって調製された非自然発生のアミノ酸のD−異性体およびL−異性体の両方も含む。用語、アミノ酸は、本明細書で使用されるように、限定することなく、アミノ酸、天然アミノ酸、非天然アミノ酸、およびアミノ酸アナログを含む。
用語「α−アミノ酸」は、α−炭素と指定される炭素に結合されたアミノ基およびカルボキシル基の両方を含有している分子を指す。
用語「β−アミノ酸」は、β構成でアミノ基およびカルボキシル基の両方を含有している分子を指す。
「自然発生のアミノ酸」は、自然で合成されたペプチドにおいて一般に見られる、および1文字の略語A、R、N、C、D、Q、E、G、H、I、L、K、M、F、P、S、T、W、YおよびVによって知られている、20のアミノ酸のいずれか1つを指す。
以下の表は、天然アミノ酸の特性の概要を示す:
「疎水性アミノ酸」は、小さな疎水性アミノ酸および大きな疎水性アミノ酸を含む。「小さな疎水性アミノ酸」は、グリシン、アラニン、プロリン、およびそれらのアナログである。「大きな疎水性アミノ酸」は、バリン、ロイシン、イソロイシン、フェニルアラニン、メチオニン、トリプトファン、およびそれらのアナログである。「極性アミノ酸」は、セリン、トレオニン、アスパラギン、グルタミン、システイン、チロシン、およびそれらのアナログである。「荷電アミノ酸」は、リシン、アルギニン、ヒスチジン、アスパラギン酸塩、グルタミン酸塩、およびそれらのアナログである。幾つかの場合では、アスパラギン酸およびグルタミン酸は、酸性アミノ酸と呼ばれる。他の場合では、リシン、アルギニンおよびヒスチジンは、塩基性アミノ酸と呼ばれる。
用語「アミノ酸アナログ」は、アミノ酸に構造的に類似している及びペプチド模倣大環状分子の形成においてアミノ酸に置換される分子を指す。アミノ酸アナログは、限定することなく、アミノ基またはカルボキシ基が、反応性が類似した基によって置換される(例えば、第一級アミンと第二級または第三級のアミンとの置換、またはカルボキシ基とエステルとの置換)β−アミノ酸およびアミノ酸を含む。
用語「非天然アミノ酸」は、自然で合成されたペプチドにおいて一般に見られる、および1文字の略語A、R、N、C、D、Q、E、G、H、I、L、K、M、F、P、S、T、W、YおよびVによって知られている、20のアミノ酸の1つではないアミノ酸を指す。
幾つかの事例では、アミノ酸アナログは、β−アミノ酸アナログを含む。β−アミノ酸アナログの例は、限定されないが、以下を含む:環状β−アミノ酸アナログ;β−アラニン;(R)−β−フェニルアラニン;(R)−1,2,3,4−テトラヒドロ−イソキノリン−3−酢酸;(R)−3−アミノ−4−(1−ナフチル)−酪酸;(R)−3−アミノ−4−(2,4−ジクロロフェニル)酪酸;(R)−3−アミノ−4−(2−クロロフェニル)−酪酸;(R)−3−アミノ−4−(2−シアノフェニル)−酪酸;(R)−3−アミノ−4−(2−フルオロフェニル)−酪酸;(R)−3−アミノ−4−(2−フラニル)−酪酸;(R)−3−アミノ−4−(2−メチルフェニル)−酪酸;(R)−3−アミノ−4−(2−ナフチル)−酪酸;(R)−3−アミノ−4−(2−チエニル)−酪酸;(R)−3−アミノ−4−(2−トリフルオロメチルフェニル)−酪酸;(R)−3−アミノ−4−(3,4−ジクロロフェニル)酪酸;(R)−3−アミノ−4−(3,4−ジフルオロフェニル)酪酸;(R)−3−アミノ−4−(3−ベンゾチエニル)−酪酸;(R)−3−アミノ−4−(3−クロロフェニル)−酪酸;(R)−3−アミノ−4−(3−シアノフェニル)−酪酸;(R)−3−アミノ−4−(3−フルオロフェニル)−酪酸;(R)−3−アミノ−4−(3−メチルフェニル)−酪酸;(R)−3−アミノ−4−(3−ピリジル)−酪酸;(R)−3−アミノ−4−(3−チエニル)−酪酸;(R)−3−アミノ−4−(3−トリフルオロメチルフェニル)−酪酸;(R)−3−アミノ−4−(4−ブロモフェニル)−酪酸;(R)−3−アミノ−4−(4−クロロフェニル)−酪酸;(R)−3−アミノ−4−(4−シアノフェニル)−酪酸;(R)−3−アミノ−4−(4−フルオロフェニル)−酪酸;(R)−3−アミノ−4−(4−ヨードフェニル−酪酸;(R)−3−アミノ−4−(4−メチルフェニル)−酪酸;(R)−3−アミノ−4−(4−ニトロフェニル)−酪酸;(R)−3−アミノ−4−(4−ピリジル)−酪酸;(R)−3−アミノ−4−(4−トリフルオロメチルフェニル)−酪酸;(R)−3−アミノ−4−ペンタフルオロ−フェニル酪酸;(R)−3−アミノ−5−ヘキセン酸;(R)−3−アミノ−5−ヘキシン酸;(R)−3−アミノ−5−フェニルペンタン酸;(R)−3−アミノ−6−フェニル−5−ヘキセン酸;(S)−1,2,3,4−テトラヒドロ−イソキノリン−3−酢酸;(S)−3−アミノ−4−(1−ナフチル)−酪酸;(S)−3−アミノ−4−(2,4−ジクロロフェニル)酪酸;(S)−3−アミノ−4−(2−クロロフェニル)−酪酸;(S)−3−アミノ−4−(2−シアノフェニル)−酪酸;(S)−3−アミノ−4−(2−フルオロフェニル)−酪酸;(S)−3−アミノ−4−(2−フラニル)−酪酸;(S)−3−アミノ−4−(2−メチルフェニル)−酪酸;(S)−3−アミノ−4−(2−ナフチル)−酪酸;(S)−3−アミノ−4−(2−チエニル)−酪酸;(S)−3−アミノ−4−(2−トリフルオロメチルフェニル)−酪酸;(S)−3−アミノ−4−(3,4−ジクロロフェニル)酪酸;(S)−3−アミノ−4−(3,4−ジフルオロフェニル)酪酸;(S)−3−アミノ−4−(3−ベンゾチエニル)−酪酸;(S)−3−アミノ−4−(3−クロロフェニル)−酪酸;(S)−3−アミノ−4−(3−シアノフェニル)−酪酸;(S)−3−アミノ−4−(3−フルオロフェニル)−酪酸;(S)−3−アミノ−4−(3−メチルフェニル)−酪酸;(S)−3−アミノ−4−(3−ピリジル)−酪酸;(S)−3−アミノ−4−(3−チエニル)−酪酸;(S)−3−アミノ−4−(3−トリフルオロメチルフェニル)−酪酸;(S)−3−アミノ−4−(4−ブロモフェニル)−酪酸;(S)−3−アミノ−4−(4−クロロフェニル)酪酸;(S)−3−アミノ−4−(4−シアノフェニル)−酪酸;(S)−3−アミノ−4−(4−フルオロフェニル)酪酸;(S)−3−アミノ−4−(4−ヨードフェニル)−酪酸;(S)−3−アミノ−4−(4−メチルフェニル)−酪酸;(S)−3−アミノ−4−(4−ニトロフェニル)−酪酸;(S)−3−アミノ−4−(4−ピリジル)−酪酸;(S)−3−アミノ−4−(4−トリフルオロメチルフェニル)−酪酸;(S)−3−アミノ−4−ペンタフルオロ−フェニル酪酸;(S)−3−アミノ−5−ヘキセン酸;(S)−3−アミノ−5−ヘキシン酸;(S)−3−アミノ−5−フェニルペンタン酸;(S)−3−アミノ−6−フェニル−5−ヘキセン酸;1,2,5,6−テトラヒドロピリジン−3−カルボン酸;1,2,5,6−テトラヒドロピリジン−4−カルボン酸;3−アミノ−3−(2−クロロフェニル)−プロピオン酸;3−アミノ−3−(2−チエニル)−プロピオン酸;3−アミノ−3−(3−ブロモフェニル)−プロピオン酸;3−アミノ−3−(4−クロロフェニル)−プロピオン酸;3−アミノ−3−(4−メトキシフェニル)−プロピオン酸;3−アミノ−4,4,4−トリフルオロ−酪酸;3−アミノアジビン酸;D−β−フェニルアラニン;β−ロイシン;L−β−ホモアラニン;L−β−ホモアスパラギン酸γ−ベンジルエステル;L−β−ホモグルタミン酸δ−ベンジルエステル;L−β−ホモイソロイシン;L−β−ホモロイシン;L−β−ホモメチオニン;L−β−ホモフェニルアラニン;L−β−ホモプロリン;L−β−ホモトリプトファン;L−β−ホモバリン;L−Nω−ベンジルオキシカルボニル−β−ホモリシン;Nω−L−β−ホモアルギニン;O−ベンジル−L−β−ホモヒドロキシプロリン;O−ベンジル−L−β−ホモセリン;O−ベンジル−L−β−ホモトレオニン;O−ベンジル−L−β−ホモチロシン;Y−トリチル−L−β−ホモアスパラギン;(R)−β−フェニルアラニン;L−β−ホモアスパラギン酸γ−t−ブチルエステル;L−β−ホモグルタミン酸δ−t−ブチルエステル;L−Νω−β−ホモリシン;Nδ−トリチル−L−β−ホモグルタミン;Nω−2,2,4,6,7−ペンタメチル−ジヒドロベンゾフラン−5−スルホニル−L−β−ホモアルギニン;O−t−ブチル−L−β−ホモヒドロキシ−プロリン;O−t−ブチル−L−β−ホモセリン;O−t−ブチル−L−β−ホモトレオニン;O−t−ブチル−L−β−ホモチロシン;2−アミノシクロペンタンカルボン酸;および2−アミノシクロヘキサンカルボン酸。
幾つかの事例では、アミノ酸アナログは、アラニン、バリン、グリシンまたはロイシンアラニン、バリン、グリシンおよびロイシンのアミノ酸アナログの例は、限定されないが、以下を含む:α−メトキシグリシン;α−アリル−L−アラニン;α−アミノイソ酪酸;α−メチル−ロイシン;β−(1−ナフチル)−D−アラニン;β−(1−ナフチル)−L−アラニン;β−(2−ナフチル)−D−アラニン;β−(2−ナフチル)−L−アラニン;β−(2−ピリジル)−D−アラニン;β−(2−ピリジル)−L−アラニン;β−(2−チエニル)−D−アラニン;β−(2−チエニル)−L−アラニン;β−(3−ベンゾチエニル)−D−アラニン;β−(3−ベンゾチエニル)−L−アラニン;β−(3−ピリジル)−D−アラニン;β−(3−ピリジル)−L−アラニン;β−(4−ピリジル)−D−アラニン;β−(4−ピリジル)−L−アラニン;β−クロロ−L−アラニン;β−シアノ−L−アラニン;β−シクロヘキシル−D−アラニン;β−シクロヘキシル−L−アラニン;β−シクロペンテン−1−イル−アラニン;β−シクロペンチル−アラニン;β−シクロプロピル−L−Ala−OH.ジシクロヘキシルアンモニウム塩;β−t−ブチル−D−アラニン;β−t−ブチル−L−アラニン;γ−アミノ酪酸;L−α,β−ジアミノプロピオン酸;2,4−ジニトロ−フェニルグリシン;2,5−ジヒドロ−D−フェニルグリシン;2−アミノ−4,4,4−トリフルオロ酪酸;2−フルオロ−フェニルグリシン;3−アミノ−4,4,4−トリフルオロ−酪酸;3−フルオロ−バリン;4,4,4−トリフルオロ−バリン;4,5−デヒドロ−L−leu−OH.ジシクロヘキシルアンモニウム塩;4−フルオロ−D−フェニルグリシン;4−フルオロ−L−フェニルグリシン;4−ヒドロキシ−D−フェニルグリシン;5,5,5−トリフルオロ−ロイシン;6−アミノヘキサン酸;シクロペンチル−D−Gly−OH.ジシクロヘキシルアンモニウム塩;シクロペンチル−Gly−OH.ジシクロヘキシルアンモニウム塩;D−α,β−ジアミノプロピオン酸;D−α−アミノ酪酸;D−α−t−ブチルグリシン;D−(2−チエニル)グリシン;D−(3−チエニル)グリシン;D−2−アミノカプロン酸;D−2−インダニルグリシン;D−アリルグリシン−ジシクロヘキシルアンモニウム塩;D−シクロヘキシルグリシン;D−ノルバリン;D−フェニルグリシン;β−アミノ酪酸;β−アミノイソ酪酸;(2−ブロモフェニル)グリシン;(2−メトキシフェニル)グリシン;(2−メチルフェニル)グリシン;(2−チアゾリル)グリシン;(2−チエニル)グリシン;2−アミノ−3−(ジメチルアミノ)−プロピオン酸;L−α,β−ジアミノプロピオン酸;L−α−アミノ酪酸;L−α−t−ブチルグリシン;L−(3−チエニル)グリシン;L−2−アミノ−3−(ジメチルアミノ)−プロピオン酸;L−2−アミノカプロン酸ジシクロヘキシル−アンモニウム塩;L−2−インダニルグリシン;L−アリルグリシン.ジシクロヘキシルアンモニウム塩;L−ジシクロヘキシルグリシン;L−フェニルグリシン;L−プロパルギルグリシン;L−ノルバリン;N−α−アミノメチル−L−アラニン;D−α,γ−ジアミノ酪酸;L−α−ジアミノ酪酸;β−シクロプロピル−L−アラニン;(Ν−β−(2,4−ジニトロフェニル))−L−α,β−ジアミノプロピオン酸;(N−β−1−(4,4−ジメチル−2,6−ジオキソシクロヘキサ−1−イリデン)エチル)−D−α,β−ジアミノプロピオン酸;(N−β−1−(4,4−ジメチル−2,6−ジオキソシクロヘキサ−1−イリデン)エチル)−L−α,β−ジアミノプロピオン酸;(N−β−4−メチルトリチル)−L−α,β−ジアミノプロピオン酸;(N−β−アリルオキシカルボニル)−L−α,β−ジアミノプロピオン酸;(N−γ−1−(4,4−ジメチル−2,6−ジオキソシクロヘキサ−1−イリデン)エチル)−D−α,γ−ジアミノ酪酸;(Ν−γ−1−(4,4−ジメチル−2,6−ジオキソシクロヘキサ−1−イリデン)エチル)−L−α,γ−ジアミノ酪酸;(N−γ−4−メチルトリチル)−D−α,γ−ジアミノ酪酸;(Ν−γ−4−メチルトリチル)−L−α,γ−ジアミノ酪酸;(N−γ−アリルオキシカルボニル)−L−α,γ−ジアミノ酪酸;D−α,γ−ジアミノ酪酸;4,5−デヒドロ−L−ロイシン;シクロペンチル−D−Gly−OH;シクロペンチル−Gly−OH;D−アリルグリシン;D−ホモシクロヘキシルアラニン;L−1−ピレニルアラニン;L−2−アミノカプロン酸;L−アリルグリシン;L−ホモシクロヘキシルアラニン;およびN−(2−ヒドロキシ−4−メトキシ−Bzl)−Gly−OH。
幾つかの事例では、アミノ酸アナログは、アルギニンまたはリシンのアナログを含む。
アルギニンおよびリシンのアミノ酸アナログの例は、限定されないが、以下を含む:シトルリン;L−2−アミノ−3−グアニジノプロピオン酸;L−2−アミノ−3−ウレイドプロピオン酸;L−シトルリン;Lys(Me)2−OH;Lys(N3)―OH;Νδ−ベンジルオキシカルボニル−L−オルニチン;Νω−ニトロ−D−アルギニン;Νω−ニトロ−L−アルギニン;α−メチル−オルニチン;2,6−ジアミノヘプタン二酸;L−オルニチン;(Nδ−1−(4,4−ジメチル−2,6−ジオキソ−シクロヘキサ−1−イリデン)エチル)−D−オルニチン;(Nδ−1−(4,4−ジメチル−2,6−ジオキソ−シクロヘキサ−1−イリデン)エチル)−L−オルニチン;(Nδ−4−メチルトリチル)−D−オルニチン;(Νδ−4−メチルトリチル)−L−オルニチン;D−オルニチン;L−オルニチン;Arg(Me)(Pbf)−OH;Arg(Me)2−OH(非対称的);Arg(Me)2−OH(対称的);Lys(ivDde)−OH;Lys(Me)2−OH.HCl;Lys(Me3)−OHクロリド;Νω−ニトロ−D−アルギニン;およびΝω−ニトロ−L−アルギニン。
幾つかの事例では、アミノ酸アナログは、アスパラギン酸またはグルタミン酸のアナログを含む。アスパラギン酸およびグルタミン酸のアミノ酸アナログの例は、限定されないが、以下を含む:α−メチル−D−アスパラギン酸;α−メチル−グルタミン酸;α−メチル−L−アスパラギン酸;γ−メチレン−グルタミン酸;(N−γ−エチル)−L−グルタミン;[N−α−(4−アミノベンゾイル)]−L−グルタミン酸;2,6−ジアミノピメリン酸;L−α−アミノスベリン酸;D−2−アミノアジピン酸;D−α−アミノスベリン酸;α−アミノピメリン酸;イミノ二酢酸;L−2−アミノアジピン酸;トレオ−β−メチル−アスパラギン酸;γ−カルボキシ−D−グルタミン酸γ,γ−ジ−t−ブチルエステル;γ−カルボキシ−L−グルタミン酸γ,γ−ジ−t−ブチルエステル;Glu(OAll)−OH;L−Asu(OtBu)―OH;およびピログルタミン酸。
幾つかの事例では、アミノ酸アナログは、システインおよびメチオニンのアナログを含む。システインおよびメチオニンのアミノ酸アナログの例は、限定されないが、Cys(ファルネシル)−OH、Cys(ファルネシル)−OMe、α−メチル−メチオニン、Cys(2−ヒドロキシエチル)−OH、Cys(3−アミノプロピル)−OH、2−アミノ−4−(エチルチオ)酪酸、ブチオニン、ブチオニンスルホキシイミン、エチオニン、メチオニンメチルスルホニウムクロリド、セレノメチオニン、システイン酸、[2−(4−ピリジル)エチル]−DL−ペニシラミン、[2−(4−ピリジル)エチル]−L−システイン、4−メトキシベンジル−D−ペニシラミン、4−メトキシベンジル−L−ペニシラミン、4−メチルベンジル−D−ペニシラミン、4−メチルベンジル−L−ペニシラミン、ベンジル−D−システイン、ベンジル−L−システイン、ベンジル−DL−ホモシステイン、カルバモイル−L−システイン、カルボキシエチル−L−システイン、カルボキシメチル−L−システイン、ジフェニルメチル−L−システイン、エチル−L−システイン、メチル−L−システイン、t−ブチル−D−システイン、トリチル−L−ホモシステイン、トリチル−D−ペニシラミン、シスタチオニン、ホモシスチン、L−ホモシスチン、(2−アミノエチル)−L−システイン、セレノ−L−シスチン、シスタチオニン、Cys(StBu)―OH、およびアセトアミドメチル−D−ペニシラミンを含む。
幾つかの事例では、アミノ酸アナログは、フェニルアラニンおよびチロシンのアナログを含む。フェニルアラニンおよびチロシンのアミノ酸アナログの例は、β−メチル−フェニルアラニン、β−ヒドロキシフェニルアラニン、α−メチル−3−メトキシ−DL−フェニルアラニン、α−メチル−D−フェニルアラニン、α−メチル−L−フェニルアラニン、1,2,3,4−テトラヒドロイソキノリン−3−カルボン酸、2,4−ジクロロ−フェニルアラニン、2−(トリフルオロメチル)−D−フェニルアラニン、2−(トリフルオロメチル)−L−フェニルアラニン、2−ブロモ−D−フェニルアラニン、2−ブロモ−L−フェニルアラニン、2−クロロ−D−フェニルアラニン、2−クロロ−L−フェニルアラニン、2−シアノ−D−フェニルアラニン、2−シアノ−L−フェニルアラニン、2−フルオロ−D−フェニルアラニン、2−フルオロ−L−フェニルアラニン、2−メチル−D−フェニルアラニン、2−メチル−L−フェニルアラニン、2−ニトロ−D−フェニルアラニン、2−ニトロ−L−フェニルアラニン、2,4,5−トリヒドロキシ−フェニルアラニン、3,4,5−トリフルオロ−D−フェニルアラニン、3,4,5−トリフルオロ−L−フェニルアラニン、3,4−ジクロロ−D−フェニルアラニン、3,4−ジクロロ−L−フェニルアラニン、3,4−ジフルオロ−D−フェニルアラニン、3,4−ジフルオロ−L−フェニルアラニン、3,4−ジヒドロキシ−L−フェニルアラニン、3,4−ジメトキシ−L−フェニルアラニン、3,5,3’−トリヨード−L−チロニン、3,5−ジヨード−D−チロシン、3,5−ジヨード−L−チロシン、3,5−ジヨード−L−チロニン、3−(トリフルオロメチル)−D−フェニルアラニン、3−(トリフルオロメチル)−L−フェニルアラニン、3−アミノ−L−チロシン、3−ブロモ−D−フェニルアラニン、3−ブロモ−L−フェニルアラニン、3−クロロ−D−フェニルアラニン、3−クロロ−L−フェニルアラニン、3−クロロ−L−チロシン、3−シアノ−D−フェニルアラニン、3−シアノ−L−フェニルアラニン、3−フルオロ−D−フェニルアラニン、3−フルオロ−L−フェニルアラニン、3−フルオロ−チロシン、3−ヨード−D−フェニルアラニン、3−ヨード−L−フェニルアラニン、3−ヨード−L−チロシン、3−メトキシ−L−チロシン、3−メチル−D−フェニルアラニン、3−メチル−L−フェニルアラニン、3−ニトロ−D−フェニルアラニン、3−ニトロ−L−フェニルアラニン、3−ニトロ−L−チロシン、4−(トリフルオロメチル)−D−フェニルアラニン、4−(トリフルオロメチル)−L−フェニルアラニン、4−アミノ−D−フェニルアラニン、4−アミノ−L−フェニルアラニン、4−ベンゾイル−D−フェニルアラニン、4−ベンゾイル−L−フェニルアラニン、4−ビス(2−クロロエチル)アミノ−L−フェニルアラニン、4−ブロモ−D−フェニルアラニン、4−ブロモ−L−フェニルアラニン、4−クロロ−D−フェニルアラニン、4−クロロ−L−フェニルアラニン、4−シアノ−D−フェニルアラニン、4−シアノ−L−フェニルアラニン、4−フルオロ−D−フェニルアラニン、4−フルオロ−L−フェニルアラニン、4−ヨード−D−フェニルアラニン、4−ヨード−L−フェニルアラニン、ホモフェニルアラニン、チロキシン、3,3−ジフェニルアラニン、チロニン、エチル−チロシン、およびメチル−チロシンを含む。
幾つかの事例では、アミノ酸アナログは、プロリンのアナログを含む。プロリンのアミノ酸アナログの例は、限定されないが、3,4−デヒドロ−プロリン、4−フルオロ−プロリン、シス−4−ヒドロキシ−プロリン、チアゾリジン−2−カルボン酸、およびトランス−4−フルオロ−プロリンを含む。
幾つかの事例では、アミノ酸アナログは、セリンおよびトレオニンのアナログを含む。セリンおよびトレオニンのアミノ酸アナログの例は、限定されないが、3−アミノ−2−ヒドロキシ−5−メチルヘキサン酸、2−アミノ−3−ヒドロキシ−4−メチルペンタン酸、2−アミノ−3−エトキシブタン酸、2−アミノ−3−メトキシブタン酸、4−アミノ−3−ヒドロキシ−6−メチルヘプタン酸、2−アミノ−3−ベンジルオキシプロピオン酸、2−アミノ−3−ベンジルオキシプロピオン酸、2−アミノ−3−エトキシプロピオン酸、4−アミノ−3−ヒドロキシブタン酸、およびα−メチルセリンを含む。
幾つかの事例では、アミノ酸アナログは、トリプトファンのアナログを含む。トリプトファンのアミノ酸アナログの例は、限定されないが、以下を含む:α−メチル−トリプトファン;β−(3−ベンゾチエニル)−D−アラニン;β−(3−ベンゾチエニル)−L−アラニン;1−メチル−トリプトファン;4−メチル−トリプトファン;5−ベンジルオキシ−トリプトファン;5−ブロモ−トリプトファン;5−クロロ−トリプトファン;5−フルオロ−トリプトファン;5−ヒドロキシ−トリプトファン;5−ヒドロキシ−L−トリプトファン;5−メトキシ−トリプトファン;5−メトキシ−L−トリプトファン;5−メチル−トリプトファン;6−ブロモ−トリプトファン;6−クロロ−D−トリプトファン;6−クロロ−トリプトファン;6−フルオロ−トリプトファン;6−メチル−トリプトファン;7−ベンジルオキシ−トリプトファン;7−ブロモ−トリプトファン;7−メチル−トリプトファン;D−1,2,3,4−テトラヒドロ−ノルハルマン−3−カルボン酸;6−メトキシ−1,2,3,4−テトラヒドロノルハルマン−1−カルボン酸;7−アザトリプトファンアミド;L−1,2,3,4−テトラヒドロ−ノルハルマン−3−カルボン酸;5−メトキシ−2−メチル−トリプトファン;および6−クロロ−L−トリプトファン。
幾つかの事例では、アミノ酸アナログはラセミ化合物である。幾つかの事例では、アミノ酸アナログのD異性体が使用される。幾つかの場合では、アミノ酸アナログのL異性体が使用される。幾つかの事例では、アミノ酸アナログは、RまたはSの構成であるキラル中心を含む。時に、β−アミノ酸アナログのアミノ基は、保護基、例えば、tert−ブチルオキシカルボニル(BOC基)、9−フルオレニルメチルオキシカルボニル(FMOC)、トシルなどで置換される。時に、β−アミノ酸アナログのカルボン酸官能基は、例えば、そのエステル誘導体として保護される。幾つかの場合では、アミノ酸アナログの塩が使用される。
幾つかの実施形態では、核酸分子は、一緒に共有結合された少なくとも2つのヌクレオチドを指す。幾つかの事例では、本明細書に記載される核酸は、リン酸ジエステル結合を含有するが、幾つかの場合では、下に概説されるように(例えば、標識プローブなどのプライマーおよびプローブの構築において)、交互の骨格を有する核酸アナログが含まれ、これは、例えば、ホスホルアミド(Beaucage et al., Tetrahedron 49(10): 1925 (1993)およびその参考文献; Letsinger, J. Org. Chem. 35:3800 (1970), Sprinzl et al., Eur. J. Biochem. 81 :579 (1977); Letsinger et al., Nucl. Acids Res. 14:3487 (1986); Sawai et al, Chem. Lett. 805 (1984), Letsinger et al., J. Am. Chem. Soc. 110:4470 (1988);およびPauwels et al, Chemica Scripta 26: 141 91986)、ホスホロチオエート(Mag et al, Nucleic Acids Res. 19: 1437 (1991);米国特許出願第5,644,048号)、ジチオリン酸(Briu et al ., J. Am, Chem, Soc. 111 :2321 (1989))、O−メチルホスホロアミダイト連鎖(Eckstein, Oligonucleotides and Analogues: A Practical Approach, Oxford University Pressを参照)、およびペプチド核酸(本明細書で「PNA」とも呼ばれる)骨格および連鎖(Egholm, J. Am. Chem. Soc. 1 14: 1895 (1992); Meier et al, Chem. Int. Ed. Engl . 31 : 1008 (1992); Nielsen, Nature, 365:566 (1993); Carlsson et al., Nature 380:207 (1996)を参照し、それらすべては引用によって組み込まれる)を含む。他のアナログ核酸は、ロックド核酸(本明細書で「LNA」とも呼ばれる)(koshkin et al., J. Am. Chem. Soc. 120.13252 3 (1998));正の骨格(Denpcy et al., Proc. Natl. Acad. Sci. USA 92:6097 (1995));非イオン性の骨格(米国特許出願第5,386,023号、第5,637,684号、第5,602,240号、第5,216,141号および第4,469,863号;Kiedrowshi et al., Angew. Chem. Intl. Ed. English 30:423 (1991); Letsinger et al., J. Am. Chem. Soc. 1 10:4470 (1988); Letsinger et al.. Nucleoside & Nucleotide 13 : 1597 (1994); Chapters 2 and 3, ASC Symposium Series 580, "Carbohydrate Modifications in Antisense Research", Ed. Y. S. Sanghui and P. Dan Cook; Mesmaeker et al ., Bioorganic & Medicinal Chem. Lett. 4:395 (1994); Jeffs et al., J. Biomolecu!ar NMR 34: 17 (1994); Tetrahedron Lett. 37:743 (1996))、および米国特許出願第5,235,033号および第5,034,506号、およびChapters 6 and 7, ASC Symposium Series 580,“Carbohydrate Modifications in Antisense Research”, Ed. Y. S. Sanghui and P. Dan Cookに記載されるものを含む非リボース骨格、を含む二環式構造を有する核酸を含む。1つ以上の炭素環式糖を含有している核酸も、核酸の定義内に含まれる(Jenkins et al., Chem. Soc. Rev. (1995) pp 169 176を参照)。幾つかの核酸アナログは、Rawls, C & E News Jim. 2, 1997 page 35に記載されている。「ロックド核酸」も、核酸アナログの定義内に含まれる。LNAは、リボース環は、2’−O原子を4’−C原子に結合するメチレン架橋によって「ロックされる(locked)」,核酸アナログのクラスである。これらの参考文献はすべて、引用によって本明細書に明確に組み込まれる。幾つかの事例では、リボースリン酸骨格のこれらの修飾は、生理的環境におけるそのような分子の安定性および半減期を増大するために行われる。例えば、PNA:DNAおよびLNA−DNAハイブリッドは、より高い安定性を示し、それ故、幾つかの実施形態において使用される。標的核酸は、指定されるように、一本鎖または二本鎖であるか、あるいは一本鎖または二本鎖両方の配列の部分を含有している。用途によって、核酸は、DNA(例えば、ゲノムDNA、ミトコンドリアDNA、およびcDNAを含む)、RNA(例えば、mRNAおよびrRNAを含む)またはハイブリッドであり、ここで核酸は、デオキシリボヌクレオチドおよびリボヌクレオチドのあらゆる組み合わせ、およびウラシル、アデニン、チミン、シトシン、グアニン、イノシン、キササニン(xathanine、ヒポキササニン(hypoxathanine)、イソシトシン、イソグアニンなどを含む、塩基のあらゆる組み合わせを含有している。
<サンプル、解析技術、および器具使用>
特定の実施形態では、本明細書に開示される方法の1つ以上は、サンプルを含む。幾つかの実施形態では、サンプルは、細胞サンプルまたは組織サンプルである。幾つかの事例では、サンプルは細胞サンプルである。幾つかの実施形態では、本明細書に記載される方法との使用のためのサンプルは、動物の細胞から得られる。幾つかの事例では、動物細胞は、海洋無脊椎動物、魚、昆虫、両生類、爬虫類、または哺乳動物からの細胞を含む。幾つかの事例では、哺乳動物細胞は、霊長類、類人猿、ウマ、ウシ、ブタ、イヌ、ネコ、またはげっ歯類の細胞である。幾つかの事例では、哺乳動物は、霊長類、類人猿、イヌ、ネコ、ウサギ、フェレットなどである。幾つかの場合では、げっ歯類は、マウス、ラット、ハムスター、スナネズミ、ハムスター、チンチラ、またはモルモットである。幾つかの実施形態では、鳥細胞は、カナリア、インコまたはオウム由来である。幾つかの実施形態では、爬虫類細胞は、カメ、トカゲまたはヘビ由来である。幾つかの場合では、魚細胞は熱帯魚由来である。幾つかの場合では、魚細胞はゼブラフィッシュ(例えばDanino rerio)由来である。幾つかの場合では、蠕虫細胞は線虫(例えばC.elegans)由来である。幾つかの場合では、両生類細胞はカエル由来である。幾つかの実施形態では、節足動物細胞は,タランチュラまたはヤドカリ由来である。
幾つかの実施形態では、本明細書に記載される方法との使用のためのサンプルは、哺乳動物細胞から得られる。幾つかの事例では、哺乳動物細胞は、上皮細胞、結合組織細胞、ホルモン分泌細胞、神経細胞、骨格筋細胞、血液細胞、または免疫系細胞である。
典型的な哺乳動物細胞は、限定されないが、293A細胞株、293FT細胞株、293F細胞、293H細胞、HEK293細胞、CHO DG44細胞、CHO−S細胞、CHO−K1細胞、Expi293F(商標)細胞、Flp−In(商標)T−REx(商標)293細胞株、Flp−In(商標)−293細胞株、Flp−In(商標)3T3細胞株、Flp−In(商標)−BHK細胞株、Flp−In(商標)−CHO細胞株、Flp−In(商標)−CV−1細胞株、Flp−In(商標)−Jurkat細胞株、FreeStyle(商標)293−F細胞、FreeStyle(商標)CHO−S細胞、GripTite(商標)293MSR細胞株、GS−CHO細胞株、HepaRG(商標)細胞、T−REx(商標) Jurkat細胞株、Per.C6細胞、T−REx(商標)−293細胞株、T−REx(商標)−CHO細胞株、T−REx(商標)−HeLa細胞株、NC−HEVIT細胞株、およびPC12細胞株を含む。
幾つかの事例では、本明細書に記載される方法との使用のためのサンプルは、腫瘍細胞株の細胞から得られる。幾つかの事例では、サンプルは、固形腫瘍細胞株の細胞から得られる。幾つかの事例では、固形腫瘍細胞株は肉腫細胞株である。幾つかの事例では、固形腫瘍細胞株は癌細胞株である。幾つかの実施形態では、肉腫細胞株は、胞巣状横紋筋肉腫、胞状軟部肉種、エナメル上皮腫、血管肉腫、軟骨肉腫、脊索腫、軟繊維の明細胞肉腫、脱分化型脂肪肉腫、デスモイド、線維形成性小円形細胞腫瘍、胎児性横紋筋肉腫、類上皮線維肉腫、類上皮性血管内皮腫、類上皮肉腫、鼻腔神経芽細胞腫、ユーイング肉腫、腎外ラブドイド腫瘍、骨外性粘液型軟骨肉腫、骨外性骨肉腫、線維肉腫、巨細胞腫の細胞株、血管周囲細胞腫、乳児線維肉腫、炎症性筋線維芽腫瘍、カポジ肉腫、骨の平滑筋肉腫、脂肪肉腫、骨の脂肪肉腫、悪性線維性組織球腫(MFH)、骨の悪性線維性組織球腫(MFH)、悪性間葉腫、悪性末梢神経鞘腫、間葉性軟骨肉腫、粘液線維肉腫、粘液性脂肪肉腫、粘液炎症性線維芽肉腫(myxoinflammatory fibroblastic sarcoma)、血管周囲類上皮細胞分化を有する新生物(複数)、骨肉腫、傍骨性骨肉腫、血管周囲類上皮細胞分化を有する新生物、骨膜性骨肉腫、多形性脂肪肉腫、多形性横紋筋肉腫、PNET/骨外性ユーイング腫瘍、横紋筋肉腫、円形細胞脂肪肉腫、小細胞骨肉腫、単発性線維性腫瘍、滑膜肉腫、血管拡張性骨肉腫から得られる。
幾つかの実施形態では、癌細胞株は、腺癌、扁平上皮癌、腺扁平上皮癌、未分化癌、大細胞癌、小細胞癌、肛門癌、虫垂癌、胆管癌(即ち、肝内胆管癌)、膀胱癌、脳腫瘍、乳癌、子宮頸癌、結腸癌、原発不明癌(CUP)、食道癌、眼癌、ファロピウス管癌の細胞株、消化器癌、腎臓癌、肝臓癌、肺癌、髄芽腫、黒色腫、口腔癌、卵巣癌、膵臓癌、副甲状腺疾患、陰茎癌、下垂体腫瘍、前立腺癌、直腸癌、皮膚癌、胃癌、睾丸癌、喉頭癌、甲状腺癌、子宮癌、膣癌または外陰癌から得られる。
幾つかの事例では、サンプルは、血液悪性細胞株の細胞から得られる。幾つかの事例では、血液悪性細胞株はT細胞細胞株である。幾つかの事例では、血液悪性細胞株はB細胞細胞株である。幾つかの事例では、血液悪性細胞株は、非特定型末梢T細胞リンパ腫(peripheral T−cell lymphoma not otherwise specified)(PTCL−NOS)、未分化大細胞リンパ腫、血液免疫芽細胞リンパ腫、皮膚T細胞リンパ腫、成人T細胞白血病/リンパ腫(ATLL)、芽球性NK細胞リンパ腫、腸症型T細胞リンパ腫、肝脾(hematosplenic)ガンマ−デルタT細胞リンパ腫、リンパ芽球性リンパ腫、鼻NK/T細胞リンパ腫、または治療関連T細胞リンパ腫のT細胞細胞株から得られる。
幾つかの事例では、血液悪性細胞株は、急性リンパ芽球性白血病(ALL)、急性骨髄性白血病(AML)、慢性骨髄性白血病(CML)、急性単球性白血病(AMoL)、慢性リンパ球白血病(CLL)、高リスクの慢性リンパ球白血病(CLL)、小リンパ球性リンパ腫(SLL)、高リスクの小リンパ球性リンパ腫(SLL)、濾胞性リンパ腫(FL)、マントル細胞リンパ腫(MCL)、ヴァルデンストレームマクログロブリン血症、多発性骨髄腫、節外性辺縁帯B細胞リンパ腫、節性辺縁帯B細胞リンパ腫、バーキットリンパ腫、非バーキット高悪性度B細胞リンパ腫、縦隔原発B細胞リンパ腫(PMBL)、免疫芽細胞性大細胞型リンパ腫、前駆Bリンパ芽球性リンパ腫、B細胞性前リンパ球性白血病、リンパ形質細胞性リンパ腫、脾性辺縁帯リンパ腫、形質細胞性骨髄腫、形質細胞腫、縦隔(胸腺)大細胞型B細胞リンパ腫、血管内大細胞型B細胞リンパ腫、原発性体液性リンパ腫、またはリンパ腫様肉芽腫症のB細胞細胞株から得られる。
幾つかの実施形態では、本明細書に記載される方法との使用のためのサンプルは、腫瘍細胞株から得られる。典型的な腫瘍細胞株は、限定されないが、600MPE、AU565、BT−20、BT−474、BT−483、BT−549、Evsa−T、Hs578T、MCF−7、MDA−MB−231、SkBr3、T−47D、HeLa、DU145、PC3、LNCaP、A549、H1299、NCI−H460、A2780、SKOV−3/Luc、Neuro2a、RKO、RKO−AS45−1、HT−29、SW1417、SW948、DLD−1、SW480、Capan−1、MC/9、B72.3、B25.2、B6.2、B38.1、DMS153、SU.86.86、SNU−182、SNU−423、SNU−449、SNU−475、SNU−387、Hs817.T、LMH、LMH/2A、SNU−398、PLHC−1、HepG2/SF、OCI−Ly1、OCI−Ly2、OCI−Ly3、OCI−Ly4、OCI−Ly6、OCI−Ly7、OCI−Ly10、OCI−Ly18、OCI−Ly19、U2932、DB、HBL−1、RIVA、SUDHL2、TMD8、MEC1、MEC2、8E5、CCRF−CEM、MOLT−3、TALL−104、AML−193、THP−1、BDCM、HL−60、Jurkat、RPMI8226、MOLT−4、RS4、K−562、KASUMI−1、Daudi、GA−10、Raji、JeKo−1、K−92、およびMinoを含む。
幾つかの実施形態では、方法に使用されるサンプルは、個体からの組織または流体からのものである。サンプルは、限定されないが、組織(例えば、結合組織、筋組織、神経組織、または上皮組織)、全血、解離した骨髄、骨髄穿刺液、胸膜液、腹腔液、中枢髄液、腹液(abdominal fluid)、膵液、脳脊髄液、脳液、腹水、心膜液、尿、唾液、気管支洗浄液、汗、涙、耳流体(ear flow)、痰、陰嚢水腫液、精液、膣液、ミルク、羊水、および呼吸器、腸管、または尿生殖路の分泌物を含む。幾つかの実施形態では、サンプルは、生検から得られたサンプルまたは腫瘍組織サンプルなどの組織サンプルである。幾つかの実施形態では、サンプルは血清サンプルである。幾つかの実施形態では、サンプルは、1つ以上の末梢血単核細胞(PBMC)を含有している血液細胞サンプルである。幾つかの実施形態では、サンプルは、1つ以上の循環腫瘍細胞(CTC)を含有している。幾つかの実施形態では、サンプルは、1つ以上の播種性腫瘍細胞(例えば、骨髄穿刺液サンプルにおけるDTC)を含有している。
幾つかの実施形態では、サンプルは、周知の及び通例の臨床法を使用してサンプルを得る適切な手段によって個体から得られる。個体から組織サンプルを得るための手順は周知である。例えば、針吸引生検などから組織サンプルを収集および処理するための手順は、周知であり、提供される方法における使用のためのサンプルを得るために利用される。典型的に、そのような組織サンプルの収集のために、細い中空針が、細胞のサンプリングのために腫瘤などの瘤へと挿入され、染色後に、顕微鏡で検査される。
<サンプルの調製および解析>
幾つかの実施形態では、サンプルはサンプル溶液である。幾つかの事例では、サンプル溶液は、緩衝液(例えば、リン酸緩衝食塩水)または培地などの溶液を含む。幾つかの実施形態では、培地は、同位体標識された培地である。幾つかの事例では、サンプル溶液は細胞溶液である。
幾つかの実施形態では、サンプル(例えば細胞または細胞溶液)は、タンパク質のシステイン反応性プローブの相互作用の解析のためにシステイン反応性プローブでインキュベートされる。幾つかの事例では、サンプル(例えば細胞または細胞溶液)は、システイン反応性プローブの追加前に小分子断片が存在下でさらにインキュベートされる。幾つかの事例では、サンプルは対照と比較される。幾つかの事例では、対照は、システイン反応性プローブを含むが、小分子断片を含まない。幾つかの事例では、サンプルと対照との間のシステイン反応性プローブのタンパク質のセットの相互作用間で差が観察される。幾つかの事例では、差は、小分子断片とシステイン含有タンパク質との間の相互作用に相関する。
幾つかの実施形態では、サンプル(例えば細胞または細胞溶液)は、システイン反応性プローブのタンパク質の相互作用の解析のためにさらに標識される。幾つかの事例では、サンプル(例えば細胞または細胞溶液)は、富化培地で標識される。幾つかの場合では、サンプル(例えば細胞または細胞溶液)は、13Cまたは15Nで標識したアミノ酸などの、同位体標識されたアミノ酸で標識される。幾つかの場合では、標識されたサンプルは、2つのサンプル間のシステイン反応性プローブのタンパク質の相互作用の差を検出するために、標識されていないサンプルとさらに比較される。幾つかの事例では、この差は、標識されていないサンプルに対する標識されたサンプルにおけるシステイン含有タンパク質および小分子断片とのその相互作用の差である。幾つかの事例では、差は、2つのサンプルにおけるタンパク質のシステイン反応性プローブの相互作用の増大、低下または欠如である。幾つかの事例では、同位体標識された方法は、SILAC(細胞培養におけるアミノ酸を使用する安定同位体標識化)と名付けられている。
幾つかの事例では、サンプルは、第1の細胞溶液および第2の細胞溶液に分けられる。幾つかの場合では、第1の細胞溶液は、システイン反応性プローブ−タンパク質複合体の第1の群を生成するために、第1のシステイン反応性プローブで第1の細胞溶液をインキュベートする前に、長時間の間小分子断片でインキュベートされる。幾つかの事例では、長時間は、約5、10、15、20、30、60、90、120分またはそれ以上である。幾つかの事例では、第2の細胞溶液は、システイン反応性プローブ−タンパク質複合体の第2の群を生成するために第2のシステイン反応性プローブを含む。幾つかの事例では、第1のシステイン反応性プローブおよび第2のシステイン反応性プローブは、同じである。幾つかの実施形態では、第2の細胞溶液からの細胞は、対照緩衝液などの緩衝液でさらに処理され、ここで緩衝液は小分子断片を含有していない。幾つかの実施形態では、対照緩衝液はジメチルスルホキシド(DMSO)を含む。
幾つかの実施形態では、システイン反応性プローブ−タンパク質複合体はさらに、フルオロフォアなどの発色団に結合される。幾つかの事例では、システイン反応性プローブ−タンパク質複合体は、分離され、ゲル電気泳動法またはキャピラリー電気泳動法などの電気泳動を利用して可視化される。典型的なゲル電気泳動法は、アガロースベースのゲル、ポリアクリルアミドベースのゲル、またはデンプンベースのゲルを含む。幾つかの事例では、システイン反応性プローブ−タンパク質は、未変性電気泳動条件にさらされる。幾つかの事例では、システイン反応性プローブ−タンパク質は、変性電気泳動条件にさらされる。
幾つかの事例では、収集後のシステイン反応性プローブ−タンパク質は、タンパク質断片を生成するために、さらに断片化される。幾つかの事例では、断片化は、機械的ストレス、圧力、または化学的手段によってもたらされる。幾つかの事例では、システイン反応性プローブ−タンパク質複合体からのタンパク質は、化学的手段によって断片化される。幾つかの実施形態では、化学的手段はプロテアーゼである。典型的なプロテアーゼは、限定されないが、キモトリプシンA、ペニシリンGアシラーゼ前駆体、ジペプチターゼE、DmpAアミノペプチダーゼ、サブチリシン、プロリルオリゴペプチダーゼ、D−Ala−D−AlaペプチダーゼC、シグナルペプチターゼI、サイトメガロウイルスアセンブリン、Lon−Aペプチダーゼ、ペプチダーゼClp、大腸菌ファージK1FエンドシアリダーゼCEVICD、自己切断タンパク質、ヌクレオポリン145、ラクトフェリン、ムレインテトラペプチダーゼLD−カルボキシペプチダーゼ、またはロンボイド−1などの、セリンプロテアーゼ;オルニチンアセチルトランスフェラーゼなどのトレオニンプロテアーゼ;TEVプロテアーゼ、アミドホスホリボシルトランスフェラーゼ前駆体、ガンマ−グルタミルヒドロラーゼ(ドブネズミ(Rattus norvegicus))、ヘッジホッグタンパク質、DmpA アミノペプチダーゼ、パパイン、ブロメライン、カテプシンK、カルパイン、カスパーゼ−1、セパラーゼ、アデナイン、ピログルタミル−ペプチダーゼI、ソルターゼA、C型肝炎ウイルスペプチダーゼ2、シンドビスウイルス型nsP2ペプチダーゼ、ジペプチジルペプチダーゼ−VI、またはDeSI−1ペプチダーゼなどの、システインプロテアーゼ;ベータ−セクレターゼ1(BACE1)、ベータ−セクレターゼ2(BACE2)、カテプシンD、カテプシンE、キモシン、ナプシン(napsin)−A、ネペンテシン(nepenthesin)、ペプシン、プラスメプシン、プレセニリン、またはレニンなどの、アスパラギン酸プロテアーゼ;AfuGprAなどのグルタミン酸プロテアーゼ;およびペプチダーゼ_M48などのメタロプロテアーゼを含む。
幾つかの事例では、断片化はランダム断片化である。幾つかの事例では、断片化が明確な長さのタンパク質断片を生成するか、あるいは剪断力がアミノ酸部位の特定の配列で生じる。
幾つかの事例では、タンパク質断片は、液体クロマトグラフィー(LC)(例えば、高速液体クロマトグラフィー)、液体クロマトグラフィー質量分析(LC−MS)、マトリックス支援レーザー脱離/イオン化(MALDI−TOF)、ガスクロマトグラフィー/質量分析(GC−MS)、キャピラリー電気泳動質量分析(CE−MS)、または核磁気共鳴イメージング(MR)などによるプロテオミクス方法によってさらに解析される。
幾つかの実施形態では、LC方法は、サンプルのその個別部分への分離のための、当該技術分野で周知の適切なLC方法である。この分離は、サンプルの移動相および固定相との相互作用に基づいて生じる。混合物を分離するときに利用される多くの固定/移動相の組み合わせが存在するため、それらの相の物理状態に基づいて分類される幾つかの異なるタイプのクロマトグラフィーがある。幾つかの実施形態では、LCは、順相クロマトグラフィー、逆相クロマトグラフィー、サイズ排除クロマトグラフィー、イオン交換クロマトグラフィー、親和性クロマトグラフィー、置換クロマトグラフィー、分配クロマトグラフィー、フラッシュクロマトグラフィー、キラルクロマトグラフィー、および水性順相クロマトグラフィーとしてさらに分類される。
幾つかの実施形態では、LC方法は、高速液体クロマトグラフィー(HPLC)方法である。幾つかの実施形態では、HPLC方法は、順相クロマトグラフィー、逆相クロマトグラフィー、サイズ排除クロマトグラフィー、イオン交換クロマトグラフィー、親和性クロマトグラフィー、置換クロマトグラフィー、分配クロマトグラフィー、キラルクロマトグラフィー、および水性順相クロマトグラフィーとしてさらに分類される。
幾つかの実施形態では、本開示のHPLC方法は、当該技術分野で周知のあらゆる標準技術によって実行される。典型的なHPLC方法は、親水性相互作用液体クロマトグラフィー(HILIC)、静電反発力親水性相互作用液体クロマトグラフィー(ERLIC)および逆相液体クロマトグラフィー(RPLC)を含む。
幾つかの実施形態では、LCは、LC−MS方法として質量分析に結び付けられる。幾つかの実施形態では、LC−MS方法は、超高性能液体クロマトグラフィーエレクトロスプレーイオン化四重極飛行時間型質量分析(UPLC−ESI−QTOF−MS)、超高性能液体クロマトグラフィーエレクトロスプレーイオン化タンデム質量分析(UPLC−ESI−MS/MS)、逆相液体クロマトグラフィー質量分析(RPLC−MS)、親水性相互作用液体クロマトグラフィー質量分析(HILIC−MS)、親水性相互作用液体クロマトグラフィー三連四重極タンデム質量分析(HILIC−QQQ)、静電反発力親水性相互作用液体クロマトグラフィー質量分析(ERLIC−MS)、液体クロマトグラフィー飛行時間型質量分析(LC−QTOF−MS)、液体クロマトグラフィータンデム質量分析(LC−MS/MS)、タンデム質量分析と結び付けられた多次元液体クロマトグラフィー(LC/LC−MS/MS)を含む。幾つかの事例では、LC−MS方法は、LC/LC−MS/MSである。幾つかの実施形態では、本開示のLC−MS方法は、当該技術分野で周知の標準技術によって実行される。
幾つかの実施形態では、GCは、GC−MS方法として質量分析に結び付けられる。幾つかの実施形態では、GC−MS方法は、二次元ガスクロマトグラフィー飛行時間型質量分析(GC*GC−TOFMS)、ガスクロマトグラフィー飛行時間型質量分析(GC−QTOF−MS)およびガスクロマトグラフィータンデム質量分析(GC−MS/MS)を含む。
幾つかの実施形態では、CEは、CE−MS方法として質量分析に結び付けられる。幾つかの実施形態では、CE−MS方法は、キャピラリー電気泳動−負のエレクトロスプレーイオン化質量分析(CE−ESI−MS)、キャピラリー電気泳動−負のエレクトロスプレーイオン化−四重極飛行時間型質量分析(CE−ESI−QTOF−MS)およびキャピラリー電気泳動−四重極飛行時間型質量分析(CE−QTOF−MS)を含む。
幾つかの実施形態では、核磁気共鳴(NMR)方法は、本明細書に開示される1つ以上のシステイン結合タンパク質またはタンパク質断片の検出のための当該技術分野で周知の適切な方法である。幾つかの実施形態では、NMR方法は、一次元(1D)NMR方法、二次元の(2D)NMR方法、固体NMR方法およびNMRクロマトグラフィーを含む。典型的な1D NMR方法は、1水素、13炭素、15窒素、17酸素、19フッ素、31リン、39カリウム、23ナトリウム、33硫黄、87ストロンチウム、27アルミニウム、43カルシウム、35塩素、37塩素、63銅、65銅、57鉄、25マグネシウム、199水銀、または67亜鉛のNMR方法、分極移動による歪みのない増強(DEPT)方法、付属プロトン試験(APT)方法および1D−インクレディブル自然存在比二重量子遷移実験(1D−incredible natural abundance double quantum transition experiment)(INADEQUATE)方法を含む。典型的な2D NMR方法は、相関分光法(COSY)、全相関分光法(TOCSY)、2D−INADEQUATE、2D−アデクエイト二重量子遷移実験(2D−adequate double quantum transfer experiment)(ADEQUATE)、核オーバーハウザー効果分光法(NOSEY)、回転フレームNOE分光法(ROESY)、異種核多量子相関分光法(heteronuclear multiple−quantum correlation spectroscopy)(HMQC)、異種核単一量子コヒーレンス分光法(heteronuclear single quantum coherence spectroscopy)(HSQC)、近距離カップリング(short range coupling)および遠距離カップリング(long range coupling)の方法を含む。典型的な固体NMR方法は、固体13炭素NMR、高解像度のマジック角回転(HR−MAS)および交差分極のマジック角回転(CP−MAS)のNMR方法を含む。典型的なNMR技術は、拡散秩序化分光法(diffusion ordered spectroscopy)(DOSY)、DOSY−TOCSYおよびDOSY−HSQCを含む。
幾つかの実施形態では、タンパク質断片は、Weerapana et al.,“Quantitative reactivity profiling predicts functional cysteines in proteomes,”Nature, 468:790−795 (2010)に記載されるような方法によって解析される。
幾つかの実施形態では、質量分析方法からの結果は、タンパク質同定のためにアルゴリズムによって解析される。幾つかの実施形態では、アルゴリズムは、タンパク質同定のために質量分析方法からの結果をタンパク質の配列データベースと組み合わせる。幾つかの実施形態では、アルゴリズムは、ProLuCIDアルゴリズム、Probity、Scaffold、SEQUEST、またはMascotを含む。
幾つかの実施形態では、システイン反応性プローブ−タンパク質複合体からタンパク質の各々に値が割り当てられる。幾つかの実施形態では、システイン反応性プローブのタンパク質複合体からタンパク質の各々に割り当てられた値は、質量分析の解析から得られる。幾つかの事例では、値は、質量電荷比に応じたシグナル強度のプロットからの曲線下面積である。幾つかの実施形態では、第1の細胞溶液から得られたタンパク質に第1の値が割り当てられ、第2の細胞溶液から得られた同じタンパク質に第2の値が割り当てられる。幾つかの事例では、2つの値間の比率が計算される。幾つかの事例では、2を超える比率は、タンパク質が薬物と相互作用するための候補であるか、またはシステイン結合タンパク質であることを示している。幾つかの事例では、比率は、2.5、3、3.5、4、4.5、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、または20を超える。幾つかの場合では、比率は最大で20である。
幾つかの事例では、比率は、平均された値に基づいて計算される。幾つかの事例では、平均された値は、各細胞溶液からのタンパク質の少なくとも2つ、3つ、または4つの値の平均であるか、あるいはタンパク質が各細胞溶液において少なくとも2、3、または4回観察され、各々の観察された時間に値が割り当てられる。幾つかの事例では、比率はさらに、12、10、または8未満の標準偏差を有する。
幾つかの事例では、値は平均された値ではない。幾つかの事例では、比率は、細胞集団において一度だけ観察されたタンパク質の値に基づいて計算される。幾つかの事例では、比率は、20の値とともに割り当てられる。
幾つかの実施形態では、システイン含有タンパク質を小断片分子結合標的として特定する関連で、2つの細胞溶液から第1の比率が得られ、ここで両方の細胞溶液はシステイン反応性プローブでインキュベートされた、第1の細胞溶液は小分子断片でさらにインキュベートされる。幾つかの事例では、第1の比率は、両方の細胞溶液が小分子断片がない状態でシステイン反応性プローブによって処理された第2の比率とさらに比較される。幾つかの事例では、第1の比率は、0.5、1、1.5、2、2.5、3、3.5、4、4.5、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、または20を超える。幾つかの事例では、第2の比率は、0.5、1、1.5、2、2.5、3、3.5、4、4.5、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、または20を超える。幾つかの事例の、第1の比率が、2、2.5、3、3.5、4、4.5、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、または20を超え、第2の比率が約0.5乃至約2である場合、2つの比率は、タンパク質が薬物結合標的であることを示す。
幾つかの実施形態では、値によってさらに、システイン含有タンパク質に対するシステイン反応性プローブの阻害のパーセンテージを計算することができる。幾つかの実施形態では、50%、60%、70%、80%、90%、または100%を超える阻害のパーセンテージは、システイン含有タンパク質が小分子断片と相互作用するための候補であることを示している。
<キット/製品>
本明細書には、特定の実施形態において、本明細書に記載される1つ以上の方法との使用のためのキットおよび製品が開示される。幾つかの実施形態において、本明細書には、システイン含有タンパク質を小分子断片結合標的として特定するためのキットが記載される。幾つかの事例において、本明細書にはまた、結合部位をシステイン含有タンパク質上にマッピングするためのキットが記載される。幾つかの場合において、本明細書には、システイン結合タンパク質を特定するためのキットが記載される。幾つかの実施形態において、本明細書にはまた、システイン含有タンパク質との相互作用のための小分子断片のハイスループットスクリーニングのためのキットが記載される。
幾つかの実施形態では、そのようなキットは、本明細書に記載されるシステイン反応性プローブなどのシステイン反応性プローブは、小分子断片またはライブラリー及び/又は対照などの試験化合物、および本明細書に記載される方法の1つ以上を実行するのに適した試薬を含む。幾つかの事例では、キットはさらに、細胞サンプルなどのサンプル、および緩衝液または培地などの適切な溶液を含む。幾つかの実施形態では、キットはさらに、本明細書に記載される方法の1つ以上での使用のための組換えタンパク質を含む。幾つかの実施形態では、キットの追加のコンポーネントは、バイアル、チューブなどの1つ以上の容器を受けるように区画されている、担体、パッケージ、または容器を含み、容器の各々は、本明細書に記載される方法で使用される別個の要素の1つを含む。適切な容器としては、例えば、ボトル、バイアル、プレート、シリンジ、および試験管が挙げられる。一実施形態では、容器は、ガラスまたはプラスチックなどの様々な材料から形成される。
本明細書に提供される製品は、パッケージング材を含む。製薬用のパッケージング材の例としては、限定されないが、ボトル、チューブ、バッグ、容器、および選択される製剤および意図した使用の様式に適したパッケージング材が挙げられる。
例えば、容器は、本明細書に開示される方法における使用のためのシステイン反応性プローブ、試験化合物、および1つ以上の試薬を含む。このようなキットは、随意に、識別用の記述またはラベル、あるいは本明細書に記載される方法での使用に関する説明書を含む。
キットはまた、内容物をリストするラベル及び/又は使用のための説明書、および使用のための説明書が伴う添付文書を含む。典型的に説明書のセットも含まれる。一実施形態では、ラベルは、容器上にあるか又はそれに関連付けられている。一実施形態では、ラベルは、それを形成する字、数字または他の文字が、容器自体に付けられているか、成型されているか、またはエッチングされるときに容器上にあり、容器をも保持するレセプタクルまたは担体内に存在するときに、例えば添付文書として、容器と関連付けられている。一実施形態では、ラベルは、内容物が具体的な治療用途に使用されることを示すために使用される。ラベルはまた、本明細書に記載される方法などにおける、内容物の使用のための指示を示す。
<サービス>
幾つかの実施形態では、本明細書に提供される方法は、サービスとしても機能する。幾つかの事例では、サービスプロバイダーは、スクリーニングのためのシステイン反応性プローブの1つ以上とともに解析のための複数の小分子断片の候補を顧客から得る。幾つかの実施形態では、サービスプロバイダーは、本明細書に記載される方法の1つ以上を使用して、小分子断片の候補をスクリーニングし、その後、その結果を顧客に提供する。幾つかの事例では、サービスプロバイダーは、システイン反応性プローブの1つ以上および本明細書に記載される方法の1つ以上を利用する解析のために適切な試薬を顧客に提供する。幾つかの場合では、顧客は、本明細書に記載される方法の1つ以上を実行し、その後、解析のためにその結果をサービスプロバイダーに提供する。幾つかの実施形態では、サービスプロバイダーは、その後、結果を解析し、顧客に提供する。幾つかの場合では、顧客は、(顧客の場所で)ローカルにまたは(例えば、ネットワークを介して到達可能なサーバー上で)遠隔にインストールされたソフトウェアと対話することによって、結果をさらに解析する。典型的な顧客は、製薬会社、臨床検査室、医師、患者などを含む。幾つかの事例では、顧客は、本明細書に記載される方法、システム、組成物、およびキットを使用する必要のある又はそれを望む適切な顧客または関係者である。
<デジタル処理装置>
幾つかの実施形態では、本明細書に記載される方法は、デジタル処理装置、またはその使用を含む。さらなる実施形態では、デジタル処理装置は、装置の機能を実行する1つ以上のハードウェア中央処理装置(CPU)を含む。またさらなる実施形態では、デジタル処理装置は、実行可能命令を実行するように構成されたオペレーティングシステムをさらに含む。幾つかの実施形態では、デジタル処理装置は、コンピュータネットワークに随意に接続される。さらなる実施形態では、デジタル処理装置は、ワールドワイドウェブ(World Wide Web)にアクセスするようにインターネットに随意に接続される。またさらなる実施形態では、デジタル処理装置は、クラウド・コンピューティング・インフラストラクチャーに随意に接続される。他の実施形態では、デジタル処理装置は、イントラネットに随意に接続される。他の実施形態では、デジタル処理装置は、データ記憶装置に随意に接続される。
本明細書の記載に従って、適切なデジタル処理装置は、限定されないが、サーバーコンピュータ、デスクトップコンピュータ、ラップトップコンピュータ、ノート型コンピュータ、サブノート型コンピュータ、ネットブックコンピュータ、ネットパッドコンピュータ、セットトップコンピュータ、メディアストリーミング装置、ハンドヘルドコンピュータ、インターネットアプライアンス、モバイルスマートフォン、タブレットコンピュータ、携帯情報端末、ビデオゲーム機、および媒体を含む。適切なタブレットコンピュータは、ブックレット、スレートまたは変換可能な構成を含む。
幾つかの実施形態では、デジタル処理装置は、実行可能命令を実行するように構成されたオペレーティングシステムを含む。オペレーティングシステムは、例えば、装置のハードウェアを管理し、アプリケーションの実行のためのサービスを提供する、プログラムおよびデータを含むソフトウェアである。適切なサーバーオペレーティングシステムは、限定しない例として、FreeBSD、OpenBSD、NetBSD(登録商標)、Linux(登録商標)、Apple(登録商標)Mac OS X Server(登録商標)、Oracle(登録商標)Solaris(登録商標)、Windows Server(登録商標)、およびNovell(登録商標)NetWare(登録商標)を含む。適切なパーソナルコンピュータのオペレーティングシステムは、限定しない例として、Microsoft(登録商標)Windows(登録商標)、Apple(登録商標)Mac OS X(登録商標)、UNIX(登録商標)、およびGNU/Linux(登録商標)などのUNIX(登録商標)様のオペレーティングシステムを含む。幾つかの実施形態では、オペレーティングシステムは、クラウドコンピューティングによって提供される。適切なモバイルスマートフォンのオペレーティングシステムは、限定しない例として、Nokia(登録商標)Symbian(登録商標)OS、Apple(登録商標)iOS(登録商標)、Research In Motion(登録商標)BlackBerry OS(登録商標)、Google(登録商標)Android(登録商標)、Microsoft(登録商標)Windows Phone(登録商標)OS、Microsoft(登録商標)Windows Mobile(登録商標)OS、Linux(登録商標)、およびPalm(登録商標)WebOS(登録商標)を含む。適切な媒体ストリーミング装置のオペレーティングシステムは、限定しない例として、Apple TV(登録商標)、Roku(登録商標)、Boxee(登録商標)、Google TV(登録商標)、Google Chromecast(登録商標)、Amazon Fire(登録商標)、およびSamsung(登録商標)HomeSync(登録商標)を含む。適切なビデオゲーム機のオペレーティングシステムは、限定しない例として、Sony(登録商標)PS3(登録商標)、Sony(登録商標)PS4(登録商標)、Microsoft(登録商標)Xbox 360(登録商標)、Microsoft Xbox One、Nintendo(登録商標)Wii(登録商標)、Nintendo(登録商標)Wii U(登録商標)、およびOuya(登録商標)を含む。幾つかの実施形態では、装置は、記憶装置及び/又はメモリ装置を含む。記憶装置及び/又はメモリ装置は、一時的又は恒久的にデータまたはプログラムを保存するために使用される1以上の物理的な機器である。幾つかの実施形態では、メモリ装置は、揮発性メモリであり、保存した情報を維持するための動力を必要とする。幾つかの実施形態では、メモリ装置は、不揮発性メモリであり、デジタル処理装置に動力が供給されないときに、保存した情報を保持する。さらなる実施形態では、不揮発性メモリは、フラッシュメモリを含む。幾つかの実施形態では、不揮発性メモリは、ダイナミック・ランダム・アクセス・メモリ(DRAM)を含む。幾つかの実施形態では、不揮発性メモリは、強誘電体ランダムアクセスメモリ(FRAM)を含む。幾つかの実施形態では、不揮発性メモリは、相変化ランダムアクセスメモリ(PRAM)を含む。他の実施形態では、装置は、限定しない例として、CD−ROM、DVD、フラッシュメモリ装置、磁気ディスクドライブ、磁気テープドライブ、光ディスクドライブ、およびクラウドコンピューティングベースのストレージを含む、記憶装置である。さらなる実施形態では、記憶装置及び/又はメモリ装置は、本明細書に開示されるものなどの装置の組み合わせである。
幾つかの実施形態では、デジタル処理装置は、ユーザーに視覚情報を送信するためのディスプレイを備える。幾つかの実施形態では、ディスプレイは、陰極線管(CRT)、液晶ディスプレイ(LCD)、薄膜トランジスター液晶ディスプレイ(TFT−LCD)、有機発光ダイオード(OLED)ディスプレイ、プラズマディスプレイ、ビデオプロジェクター、またはそれらの組み合わせを含む。
幾つかの実施形態では、デジタル処理装置は、ユーザーから情報を受信するための入力装置を備える。幾つかの実施形態では、入力装置は、キーボードである。幾つかの実施形態では、入力装置は、限定しない例として、マウス、トラックボール、トラックパッド、ジョイスティック、ゲームコントローラ、またはスタイラスを含むポインティング装置である。幾つかの実施形態では、入力装置は、タッチスクリーンまたはマルタッチスクリーンである。他の実施形態では、入力装置は、声または他の音入力を捕らえるマイクロフォンである。他の実施形態では、入力装置は、動作または視覚の入力を捕らえるビデオカメラまたは他のセンサーである。さらなる実施形態では、入力装置は、Kinect(商標)、Leap Motion(商標)などである。またさらなる実施形態では、入力装置は、本明細書に開示されるものなどの装置の組み合わせである。
幾つかの実施形態では、本明細書に開示されるシステムおよび方法は、随意にネットワーク化されたデジタル処理装置のオペレーティングシステムによって実行可能な命令を含むプログラムでコードされた、1つ以上の非一時的コンピュータ可読記憶媒体を含む。さらなる実施形態では、コンピュータ可読記憶媒体は、デジタル処理装置の有形成分である。またさらなる実施形態では、コンピュータ可読記憶媒体は、随意に、デジタル処理装置から取り外し可能である。幾つかの実施形態では、コンピュータ可読記憶媒体は、限定しない例として、CD−ROM、DVD、フラッシュメモリ装置、ソリッドステートメモリ、磁気ディスクドライブ、磁気テープドライブ、光ディスクドライブ、クラウドコンピューティングのシステムおよびサービスなどを含む。幾つかの場合では、プログラムおよび命令は、媒体上で恒久的に、略恒久的に、半恒久的に、または非一時的にコードされる。
幾つかの実施形態では、本明細書に開示されるシステムおよび方法は、少なくとも1つのコンピュータプログラム、またはその使用を含む。コンピュータプログラムは、タスクを実行するために書き込まれた、デジタル処理装置のCPUにおいて実行可能である命令のシーケンスを含む。幾つかの実施形態では、コンピュータ可読命令は、特定のタスクを実行する又は特定の抽象データ型を実装する、機能、オブジェクト、アプリケーションプログラムインターフェース(API)、データ構造などのプログラムモジュールとして実施される。
幾つかの実施形態では、コンピュータ可読命令の機能性は、様々な環境に望ましいものとして組み合わせられるか、または分布される。幾つかの実施形態では、コンピュータプログラムは、命令の1つのシーケンスを含む。幾つかの実施形態では、コンピュータプログラムは、命令の複数のシーケンスを含む。幾つかの実施形態では、コンピュータプログラムは、1つの場所から提供される。他の実施形態では、コンピュータプログラムは、複数の場所から提供される。様々な実施形態では、コンピュータプログラムは、1以上のソフトウェアモジュールを含む。様々な実施形態では、コンピュータプログラムは、含む、部分的に又は全体的に、1つ以上のウェブアプリケーション、1つ以上のモバイルアプリケーション、1つ以上、スタンドアロンアプリケーション、1つ以上のウェブブラウザプラグイン、拡張子、アドイン、またはアドオン、あるいはそれらの組み合わせを含む。
幾つかの実施形態では、コンピュータプログラムはウェブアプリケーションを含む。ウェブアプリケーションは、様々な実施形態において、1つ以上のソフトウェアフレームワークおよび1つ以上のデータベースシステムを利用する。幾つかの実施形態では、ウェブアプリケーションは、Microsoft(登録商標).NETまたはRuby on Rails(RoR)などのソフトウェアフレームワーク上で作成される。幾つかの実施形態では、ウェブアプリケーションは、限定しない例として、リレーショナル、非リレーショナル、オブジェクト指向、連想、およびXMLのデータベースシステムを含む、1つ以上のデータベースシステムを利用する。さらなる実施形態では、適切なリレーショナルデータベースシステムは、限定しない例として、Microsoft(登録商標)SQL Server、mySQL(商標)、およびOracle(登録商標)を含む。ウェブアプリケーションは、様々な実施形態において、1つ以上の言語の1つ以上のバージョンで書かれる。幾つかの実施形態では、ウェブアプリケーションは、1つ以上のマークアップ言語、プレゼンテーション定義言語、クライアント側スクリプト言語、サーバー側コーディング言語、データベース問い合わせ言語、またはそれらの組み合わせで書かれる。幾つかの実施形態では、ウェブアプリケーションは、ハイパーテキストマークアップ言語(HTML)、拡張可能ハイパーテキストにおいてマークアップ(XHTML)または拡張可能マークアップ(XML)などのマークアップ言語である程度まで書かれる。幾つかの実施形態では、ウェブアプリケーションは、カスケーディング・スタイル・シート(CSS)などのプレゼンテーション定義言語である程度まで書かれる。幾つかの実施形態では、ウェブアプリケーションは、エイジャックス(Asynchronous Javascript(登録商標) and XML(AJAX)、Flash(登録商標)Actionscript、Javascript(登録商標)、またはSilverlight(登録商標)などの、クライアント側スクリプト言語である程度まで書かれる。幾つかの実施形態では、ウェブアプリケーションは、Active Server Pages(ASP)、ColdFusion(登録商標)、Perl、Java(商標)、JavaServer Pages(JSP)、Hypertext Preprocessor(PHP)、Python(商標)、Ruby、Tcl、Smalltalk、WebDNA(登録商標)、またはGroovyなどの、サーバー側コード言語である程度まで書かれる。幾つかの実施形態では、ウェブアプリケーションは、構造化照会言語(Structured Query Language)(SQL)などのデータベース問い合わせ言語である程度まで書かれる。幾つかの実施形態では、ウェブアプリケーションは、IBM(登録商標)Lotus Domino(登録商標)などの企業サーバー製品を統合する。幾つかの実施形態では、ウェブアプリケーションはメディアプレイヤー要素を含む。様々なさらなる実施形態では、メディアプレイヤー要素は、限定しない例として、Adobe(登録商標)Flash(登録商標)、HTML5、Apple(登録商標)QuickTime(登録商標)、Microsoft(登録商標)Silverlight(登録商標)、Java(商標)、およびUnity(登録商標)を含む、多くの適切なマルチメディア技術の1つ以上を利用する。
幾つかの実施形態では、コンピュータプログラムは、モバイルデジタル処理装置に提供されるモバイルアプリケーションを含む。幾つかの実施形態では、モバイルアプリケーションは、モバイルデジタル処理装置にそれが製造される時に提供される。他の実施形態では、モバイルアプリケーションは、本明細書に記載されるコンピュータネットワークを介してモバイルデジタル処理装置に提供される。
本明細書に提供される開示に照らすと、モバイルアプリケーションは、ハードウェア、言語、および開発環境を使用する技術によって作成される。適切なプログラミング言語は、限定しない例として、CSSを有する又は有さない、C、C++、C#、オブジェクティブC(Objective−C)、Java(商標)、Javascript(登録商標)、Pascal、Object Pascal、Python(商標)、Ruby、VB.NET、WML、およびXHTML/HTML、またはそれらの組み合わせを含む。
適切なモバイルアプリケーションの開発環境は、幾つかのソースから利用可能である。
市販の開発環境は、限定しない例として、AirplaySDK、alcheMo、Appcelerator(登録商標)、Celsius、Bedrock、Flash Lite、.NET Compact Framework、Rhomobile、およびWorkLight Mobile Platformを含む。他の開発環境は、コストをかけることなく利用可能であり、その限定しない例として、Lazarus、MobiFlex、MoSync、およびPhonegapを含む。また、モバイルデバイスの製造業者は、限定しない例として、iPhone(登録商標)およびiPad(登録商標)(iOS)SDK、アンドロイド(商標)SDK、BlackBerry(登録商標)SDK、BREW SDK、Palm(登録商標)OS SDK、Symbian SDK、webOS SDK、およびWindows(登録商標)Mobile SDKを含む、ソフトウェアディベロッパキットを流通させている。
幾つかの実施形態では、モバイルアプリケーションの流通ための商用フォーラムは、限定しない例として、Apple(登録商標)App Store、アンドロイドの(商標)Market、BlackBerry(登録商標)App World、App Store for Palm device、App Catalog for webOS、Windows(登録商標)Marketplace for Mobile、Ovi Store for Nokia(登録商標)装置、Samsung(登録商標)Apps、およびNintendo(登録商標)DSi Shopを含む。
幾つかの実施形態では、コンピュータプログラムは、既存プロセスに対するアドオンでない、例えば、プラグインでない、独立したコンピュータプロセスとして実行されるプログラムである、スタンドアロンアプリケーションを含む。幾つかの事例では、スタンドアロンアプリケーションはコンパイルされる。コンパイラーは、プログラミング言語で書き込まれたソースコードをアセンブリ言語または機械コードなどのバイナリーオブジェクトコードに変換するコンピュータプログラムである。適切なコンパイルされたプログラミング言語は、限定しない例として、C、C++、オブジェクティブC、COBOL、Delphi、Eiffel、Java(商標)、Lisp、Python(商標)、Visual Basic(登録商標)、およびVB.NET、またはそれらの組み合わせを含む。コンパイルは、少なくとも部分的に実行可能プログラムを作成するためにしばしば実行される。幾つかの実施形態では、コンピュータプログラムは、1つ以上のソフトウェアモジュールを含む。
幾つかの実施形態では、コンピュータプログラムは、ウェブブラウザプラグインを含む。コンピューティングでは、プラグインは、より大きなソフトウェアアプリケーションに具体的な機能性を加える1つ以上のソフトウェアコンポーネントである。第三者の開発者がアプリケーションを拡張する能力を作成する、容易に新しい特徴を加えるサポートを行う、およびアプリケーションのサイズを縮小することができるように、ソフトウェアアプリケーションのメーカーは、プラグインをサポートする。サポートされるときに、プラグインは、ソフトウェアアプリケーションの機能性のカスタマイズを可能にする。例えば、プラグインは、一般に、ビデオを再生する、対話機能を作成する、ウイルスをスキャンする、および特定のファイルタイプを表示するために、ウェブブラウザで使用される。幾つかの事例では、ウェブブラウザプラグインは、Adobe(登録商標)Flash(登録商標)Player、Microsoft(登録商標)Silverlight(登録商標)、およびApple(登録商標)QuickTime(登録商標)を含む。幾つかの実施形態では、ツールバーは、1つ以上のウェブブラウザ拡張機能、アドイン、またはアドオンを含む。幾つかの実施形態では、ツールバーは、1つ以上のエクスプローラーバー、ツールバンド、またはデスクバンドを含む。
本明細書に提供される開示に照らすと、限定しない例として、C++、Delphi、Java(商標)、PHP、Python(商標)、およびVB.NET、またはそれらの組み合わせを含む、様々なプログラミング言語でのプラグインの開発を可能にする、プラグインのフレームワークが利用可能である。
ウェブブラウザ(インターネットブラウザとも呼ばれる)は、ワールドワイドウェブ上の情報資源を検索する、表示する、およびスキャンする(traversing)ための、ネットワーク接続したデジタル処理装置との使用のために設計された、ソフトウェアアプリケーションである。適切なウェブブラウザは、限定しない例として、Microsoft(登録商標)Internet Explorer(登録商標)、Mozilla(登録商標)Firefox(登録商標)、Google(登録商標)Chrome、Apple(登録商標)Safari(登録商標)、Opera Software(登録商標)Opera(登録商標)、およびKDE Konquerorを含む。幾つかの実施形態では、ウェブブラウザは、モバイルのウェブブラウザである。モバイルのウェブブラウザ(マイクロブラウザ、ミニブラウザ、およびワイヤレスブラウザ)は、限定しない例として、ハンドヘルドコンピュータ、タブレットコンピュータ、ネットブックコンピュータ、サブノートブックコンピュータ、スマートフォン、ニュージックプレーヤー、携帯情報端末(PDA)およびハンドヘルドビデオゲームシステムを含む、モバイルのデジタル処理装置上の使用のために設計されている。適切なモバイルのウェブブラウザは、限定しない例として、Google(登録商標)Android(登録商標)ブラウザ、RFM BlackBerry(登録商標)Browser、Apple(登録商標)Safari(登録商標)、Palm(登録商標)Blazer、Palm(登録商標)WebOS(登録商標)Browser、携帯用のMozilla(登録商標)Firefox(登録商標)、Microsoft(登録商標)Internet Explorer(登録商標)Mobile、Amazon(登録商標)Kindle(登録商標)Basic Web、Nokia(登録商標)Browser、Opera Software(登録商標)Opera(登録商標)Mobil、およびSony(登録商標)PSP(商標)ブラウザを含む。
幾つかの実施形態では、本明細書に開示されるシステムおよび方法は、ソフトウェア、サーバー、及び/又はデータベースモジュール、またはそれらの使用を含む。本明細書に提供される開示に照らすと、ソフトウェアモジュールは、多数の方法で作成され、実施される。様々な実施形態では、ソフトウェアモジュールは、ファイル、コードのセクション、プログラミングオブジェクト、プログラミング構造、またはそれらの組み合わせを含む。さらなる様々な実施形態では、ソフトウェアモジュールは、複数のファイル、複数のコードのセクション、複数のプログラミングオブジェクト、複数のプログラミング構造、またそれらの組み合わせを含む。様々な実施形態では、1つ以上のソフトウェアモジュールは、限定しない例として、ウェブアプリケーション、モバイルアプリケーション、およびスタンドアロンアプリケーションを含む。幾つかの実施形態では、ソフトウェアモジュールは、1つのコンピュータプログラムまたはアプリケーション中にある。他の実施形態では、ソフトウェアモジュールは、1つを超えるコンピュータプログラムまたはアプリケーション中にある。幾つかの実施形態では、ソフトウェアモジュールは、1つのマシン上でホストされる。他の実施形態では、ソフトウェアモジュールは、1つを超えるマシン上でホストされる。さらなる実施形態では、ソフトウェアモジュールは、クラウドコンピューティングプラットフォーム上でホストされる。幾つかの実施形態では、ソフトウェアモジュールは、1つの場所において1つ以上のマシン上でホストされる。他の実施形態では、ソフトウェアモジュールは、1つを超える位置において1つ以上のマシン上でホストされる。
幾つかの実施形態において、本明細書に開示される方法及びシステムは、1以上のデータベース又はその使用を含む。本明細書で提供される開示に照らして、データベースは、本明細書に別記される分析情報の記憶及び検索に適している。様々な実施形態において、適切なデータベースは、限定されないが、リレーショナルデータベース、非リレーショナルデータベース、オブジェクト指向型データベース、オブジェクトデータベース、実体関連モデルデータベース、連想データベース、及びXMLデータベースを含む。他の実施形態において、データベースはインターネットベースである。更なる実施形態において、データベースはウェブベースである。また更なる実施形態において、データベースは、クラウドコンピューティングベースである。他の実施形態において、データベースは、1以上のローカルコンピュータ記憶デバイスベースである。
サーバー
幾つかの実施形態において、本明細書に提供される方法は、サーバー又はコンピュータサーバー上で処理される(図2)。幾つかの実施形態において、サーバー(401)は、シングルコアプロセッサ、マルチコアプロセッサ、又は、並行処理のための複数のプロセッサである、中央処理装置(CPU、「プロセッサ」とも称す)(405)を含む。幾つかの実施形態において、制御組立体の一部として使用されるプロセッサは、マイクロプロセッサである。幾つかの実施形態において、サーバー(401)はまた、メモリ(410)(例えば、ランダムアクセスメモリー、読み出し専用メモリ、フラッシュメモリ);電子記憶装置(415)(例えばハードディスク);1以上の他のシステムと通信するための通信用インターフェース(420)(例えばネットワークアダプタ);及び、キャッシュ、他のメモリ、データストレージ、及び/又は電子ディスプレイアダプタを含む周辺機器(425)を含む。メモリ(410)、記憶装置(415)、インターフェース(420)、及び周辺機器(425)は、マザーボードなどの通信バス(実線)を介したプロセッサ(405)との通信状態にある。幾つかの実施形態において、記憶装置(415)は、データを保存するためのデータ記憶装置である。サーバー(401)は、通信用インターフェース(420)の補助によりコンピュータネットワーク(「ネットワーク」)(430)に動作自在につながれる。幾つかの実施形態において、追加のハードウェアの補助によりプロセッサも、ネットワークに動作自在につながれる。幾つかの実施形態において、ネットワーク(430)は、インターネット、イントラネット及び/又はエクストラネット、インターネットと通信状態にあるイントラネット及び/又はエクストラネット、テレコミュニケーション、又はデータネットワークである。幾つかの実施形態において、サーバー(401)の補助によりネットワーク(430)は、サーバー(401)につながれたデバイスがクライアント又はサーバーとして作用するのを可能にする、ピアツーピアのネットワークを実施する。幾つかの実施形態において、サーバーは、ネットワーク(430)を通って運ばれた電子信号を介して、コンピュータ可読命令(例えば、デバイス/システム動作プロトコル又はパラメータ)、又はデータ(例えば、センサー測定値、代謝物質の検出から得た生データ、代謝物質の検出から得た生データの解析、代謝物質の検出から得た生データの解釈など)を送受信することができる。更に、幾つかの実施形態において、ネットワークは例えば、国境線にわたってデータを送受信するために使用される。
幾つかの実施形態において、サーバー(401)は、ディスプレイ又はプリンターなどの1以上の出力装置(435)と通信状態に、及び/又は、例えばキーボード、マウス、又はジョイスティックなどの1以上の入力装置(440)と通信状態にある。幾つかの実施形態において、ディスプレイはタッチスクリーンディスプレイであり、その場合、ディスプレイ装置と入力装置の両方として機能する。幾つかの実施形態において、異なる及び/又は追加の入力装置は、アナンシエイタ(enunciator)、スピーカー、又はマイクロフォンなどとして提供される。幾つかの実施形態において、サーバーは、例えば、Windows(登録商標)、MacOS(登録商標)、又はUnix(登録商標)、或いはLinux(登録商標)の様々なバージョンの何れか1つなどの、様々な動作システムの何れか1つを使用する。
幾つかの実施形態において、記憶装置(415)は、本明細書に記載される装置、システム、又は方法の動作に関連したファイル又はデータを保存する。
幾つかの実施形態において、サーバーは、ネットワーク(430)を介して1以上のリモートコンピュータシステムと通信する。幾つかの実施形態において、1以上のリモートコンピュータシステムは、例えば、パーソナルコンピュータ、ラップトップ、タブレット、電話、スマートフォン、又は携帯情報端末を含む。
幾つかの実施形態において、制御組立体は単一のサーバー(401)を含む。他の状況において、システムは、イントラネット、エクストラネット、及び/又はインターネットを通じて互いに通信する複数のサーバーを含む。
幾つかの実施形態において、サーバー(401)は、装置動作パラメータ、プロトコル、本明細書に記載される方法、及び潜在的な関連の他の情報を保存するのに適している。幾つかの実施形態において、そのような情報は、記憶装置(415)又はサーバー(401)に保存され、そのようなデータはネットワークを通じて送信される。
特定の用語
他に定義されない限り、本明細書で用いる全ての技術用語及び科学用語は、請求される主題が属する技術分野における当業者によって、一般に理解されるものと同じ意味を有する。前述の一般的な記載及び次の詳細な記載は、典型的且つ例示的なものにすぎず、請求された任意の内容を限定するものではないことが理解される。本出願において、単数形の使用は、特に別記しない限り複数を含む。明細書と添付の特許請求の範囲に使用されるように、単数形「a」、「an」、及び「the」は、他にその内容が明確に指示しない限り、複数の指示対象を含むということに留意しなければならない。本出願において、「又は」の使用は、特に明記しない限り、「及び/又は」を意味する。更に、用語「含むこと(including)」の使用は、「含む(include)」、「含む(includes)」、及び「含まれる(included)」といった他の形態と同じく、制限はない。
本明細書で使用されるように、範囲及び量は、特定の値又は範囲の「約(about)」として表わすことができる。「約」は正確な量も含む。従って、「約5μL」は、「約5μL」及び「5μL」も意味する。通常、用語「約」は、実験誤差内にあると予想される量を含む。
本明細書で使用されるセクションの見出しは、構成上の目的のみのためのものであり、記載される主題を限定すると解釈されるものではない。
本明細書で使用されるように、用語「タンパク質」は、完全長のシステインを含有するタンパク質、完全長の機能的システインを含有するタンパク質、システイン含有タンパク質の断片、又は機能的に活性なシステイン含有タンパク質の断片を包含している。幾つかの例において、本明細書に記載されるタンパク質はまた、「単離されたタンパク質」、或いは、誘導の起源又は源が理由で、その未変性の状態で付随する自然に結合する成分とは結合せず;同じ種から他のタンパク質を実質的に含まず;異なる種の細胞により発現され;又は、自然に生じない、タンパク質としても称される。
本明細書で使用されるように、用語「ポリペプチド」は、アミノ酸の任意の重合鎖を指す。用語「ポリペプチド」は、未変性又は修飾されたシステイン含有タンパク質、システイン含有タンパク質の断片、或いは、非天然のアミノ酸残基を含むポリペプチドアナログを包含する。幾つかの例において、ポリペプチドは単量体である。幾つかの例において、ポリペプチドは重合体である。幾つかの例において、本明細書に記載されるポリペプチドはまた、「単離されたポリペプチド」、或いは、誘導の起源又は源が理由で、その未変性の状態で付随する自然に結合する成分とは結合せず;同じ種から他のタンパク質を実質的に含まず;異なる種の細胞により発現され;又は、自然に生じない、ポリペプチドとしても称される。
本明細書で使用されるように、用語「個体」、「被験体」、及び「患者」は、任意の哺乳動物を意味する。幾つかの実施形態において、哺乳動物は、ヒトである。幾つかの実施形態では、哺乳動物はヒトではない。どの用語も、保健従事者(例えば、医師、正看護士、ナース・プラクティショナー、医師助手、用務係、又はホスピス職員)の監督(例えば、持続的又は断続的)によって特徴付けられた状況を要求せず、又はそれに限定されない。
本明細書で使用されるように、用語「アルキル」は、メチル、エチル、n−プロピル、イソプロピル、n−ブチル、イソブチル、s−ブチル、t−ブチル、n−ペンチル、イソペンチル、s−ペンチル、ネオペンチル、ヘキシル、ヘプチル、オクチル、ノニル、デシル、ドデシル、テトラデシル、ヘキサデシル、アイコシル、テトラコシルなどの、1〜24の炭素原子の分枝した又は分枝していない飽和炭化水素基である。アルキル基は非環式であることが理解される。幾つかの例において、アルキル基は分子している、又は分枝していない。幾つかの例において、アルキル基はまた置換されている、又は置換されていない。例えば、アルキル基は、アルキル、シクロアルキル、アルコキシ、アミノ、エーテル、ハロゲン化物、ヒドロキシ、ニトロ、シリル、スルホ−オキソ、又はチオールを含むがこれらに限定されない、1以上の基で置換される。「低級アルキル」基は、1〜6(例えば1〜4)の炭素原子を含有するアルキル基である。幾つかの例において、アルキル基という用語はまた、C1アルキル、C1−C2アルキル、C1−C3アルキル、C1−C4アルキル、C1−05アルキル、C1−C6アルキル、C1−C7アルキル、C1−C8アルキル、C1−C9アルキル、C1−C10アルキルなど、最大でC1−C24アルキルまでである。
本明細書で使用されるように、用語「アリール」は、ベンゼン、ナフタレン、フェニル、ビフェニル、アントラセンなどを含むがこれらに限定されない、任意の炭素ベースの芳香族基を含有する基である。アリール基は置換される場合もあれば、置換されない場合もある。幾つかの例において、アリール基は、アルキル、シクロアルキル、アルコキシ、アルケニル、シクロアルケニル、アルキニル、シクロアルキニル、アリール、ヘテロアリール、アルデヒド、−NH2、カルボン酸、エステル、エーテル、ハロゲン化物、ヒドロキシ、ケトン、アジド、ニトロ、シリル、スルホ−オキソ、又はチオールを含むがこれらに限定されない、1以上の基で置換される。用語「ビアリール」は、アリール基の特定型式であり、「アリール」の定義に含まれている。加えて、アリール基は随意に単環構造であり、或いは、融合環構造であるか又は炭素炭素結合などの1以上の架橋基を介して結合される多環構造を含んでいる。例えば、ビアリールは、ナフタレンにおけるような融合環構造を介して共に結合される、又は、ビフェニルにおけるような1以上の炭素炭素結合を介して結合される、2つのアリール基を指す。
これら実施例は、例示目的のためのみに提供され、本明細書で提供される請求項の範囲を制限するものではない。
実施例1
生物学的方法
ヒト癌細胞株のプロテオームの調製
細胞株を全てATCCから得て、少ない継代数と共に使用して、5%のCO2で37℃で成長させた。MDA−MB−231細胞及びHEK−293T細胞を、10%のウシ胎仔血清、ペニシリン、ストレプトマイシン、及びグルタミンで補足されたDMEMの中で成長させた。Jurkat、Ramos、及びMUM2Cの細胞を、10%のウシ胎仔血清、ペニシリン、及びストレプトマイシンで補足されたRPMI−1640培地の中で成長させた。インビトロでの標識化のために、細胞を、MDA−MB−231細胞に対しては100%のコンフルエンスまで成長させ、或いは、Ramos又はJurkatの細胞に対しては細胞密度が150万個の細胞/mLに到達するまで成長させた。細胞を冷たいPBSで洗浄し、冷たいPBSでこすり、細胞ペレットを遠心分離(1,400g、3分、4℃)により単離して、使用するまで−80℃で保存した。細胞ペレットを超音波処理により溶解し、分画して(100,000g、45分)、可溶性及び膜画分をもたらして、その後、これらを、プロテオミクス実験のために1.5mg/mLの最終タンパク濃度、及びゲルベースのABPP実験のために1mg/mLに調整した。可溶性の溶解物を、各実験の前に凍結させたペレットから直接、新たに調製した。タンパク濃度を、Bio−Rad DC(商標)タンパク質アッセイキットを使用して判定した。
IA−ローダミン及びAc−Rho−DEVD−AMK(SEQ ID NO:857として開示される「DEVD」)でのゲルベースのABPPによる断片求電子ライブラリーのスクリーニング
25μLの可溶性のプロテオーム(1mg/mL)を、1時間周囲温度で、断片求電子(DMSO中で1μLの25倍の保存溶液)で処理した。その後、IA−ローダミン(25μΜの1μL、最終濃度=1μΜ)を加え、更に1時間反応させた。反応物を、8μLの4倍のSDS−PAGEローディングバッファーでクエンチし、クエンチしたサンプルをSDS−PAGE(10%のポリアクリルアミド;1つのレーンにつき15μLのサンプル)により分析し、平台の蛍光スキャナー(BioRad ChemiDoc(商標)MP又はHitachi FMBio He)を使用してゲル内蛍光により視覚化した。大腸菌の中で発現された組換え型タンパク質の標識化を測定するために、精製されたタンパク質を可溶性のプロテオームに加えて、1μΜ(CASP8、PRMT1、EVIPDH2)、2μΜ(TIGAR、IDH1)、又は4μΜ(IDH1 R132H)の最終濃度とし、プロテオームを上述のように処理した。Ramos及びJurkatの可溶性プロテオームと比較すると、IA−ローダミンによるIDH1の標識化の方が、MDA−MB−231の可溶性プロテオームにおいて比較的優れている。可溶性プロテオーム中の組換え型の活性CASP8を、Rho−DEVD−AOMK(SEQ ID NO:857として開示された「DEVD」)(50μΜの1μL、最終濃度=2μΜ)で標識し、クエンチし、14%のポリアクリルアミドゲル上でのSDS−PAGEにより分析した。
アルキン含有のクリックプローブでのゲルベースのABPP
25μLの可溶性プロテオーム(1mg/mL)を、周囲温度で1時間、18又は19の示された濃度(DMSO中で1μLの25倍の保存溶液)で標識し、その後、ローダミン−アジドへの銅触媒のアジド−アルキン環化付加(CuAAC)の結合にさらした。CuAACを、20μMのローダミン−アジド(DMSO中で50倍の保存溶液(stock))、1mMのトリス(2−カルボキシエチル)ホスフィン塩酸塩(TCEP;水中で新鮮な50倍の保存溶液、最終濃度=1mM)、リガンド(DMSO中で17倍の保存溶液:t−ブタノール1:4、最終濃度=100μM)、及び1mMのCuSO4(水中で50倍の保存溶液、最終濃度=1mM)で実行した。サンプルを、8μLの4倍のSDS−PAGEローディングバッファーでクエンチする前に、周囲温度で1時間反応させた。クエンチした反応物をSDS−PAGEにより分析し、ゲル内蛍光により視覚化した。CASP8とIMPDH2のために、IMPDH2又はPro−CASP8(それぞれ1μM)を含む25μLの可溶性プロテオームを、示された断片により処理し、その後、IMPDH2については18(625μMの1μl、最終濃度=25μM)、又はCASP8については61(625μMの1μl、最終濃度=25μM)で1時間、インキュベーションを行った。MLTKのために、MTLK2を安定して過剰発現するHEK 293T細胞を1時間、示された断片求電子で処理し、その後、1時間にわたり59(125μMの1μl、最終濃度=5μM)での標識化を行った。これらは、ローダミンーアジドへのCuAAC結合、及び上述のようなSDS−PAGEによる評価の後に行われた。
インビトロのIC50値の判定
示されたタンパク質を含有する25μLのプロテオームを、1時間周囲温度で断片求電子により処理し、1時間にわたり上述のプローブで標識し、クエンチし、SDS−PAGE及びゲル内蛍光視覚化(n=3)により分析した。IA−ローダミンを、C161S−TIGAR、C409S−CASP8、及びPRMT1のためのプローブとして使用した。59を、MLTKのためのプローブとして使用した。IMPDH2を含有する可溶性プロテオームを15分間ATPで処理し、その後、1時間にわたり18(625μMの1μl、最終濃度=25μM)でのインキュベーションを行った。MLTKとIMPDH2を、上述のようなローダミン−アジドへのCuAAC結合にさらした。標識化のパーセンテージを、ImageJソフトウェアを使用して帯(bands)の統合された光学強度を定量化することにより判定した。非線形回帰分析を用いて、GraphPadプリズム6を使用して生成された用量−反応曲線からIC50値を判定した。
isoTOP−ABPPサンプルの調製
インサイツの標識化のために、MDA−MB−231細胞を95%のコンフルエンスに成長させ、Ramos細胞を100万個の細胞/mLに成長させた。全てのサンプルにおける培地を、200μMの示された断片を含む新鮮な培地と交換し、細胞を37℃で2時間インキュベートし、冷たいPBSで洗浄し、冷たいPBSでこすり、遠心分離により収集した(以前の「ヒト癌細胞株のプロテオームの調製」のセクションを参照)。
断片2、3、8、9、10、12、13、14、21、27、28、29、31、33、38、45、51、及び56を、インサイツで200μMでスクリーニングした。断片4及び11を、インサイツで100μMでスクリーニングした。断片2、3、8、及び20を、インサイツで50μMで試験した。
インビトロ又はインサイツでの断片の処理後、サンプルを、100μMのヨードアセトアミドアルキン(IAアルキン、DMSO中で10mMの保存溶液の5μL)により、周囲温度で1時間、標識した。61での直接的な標識化のために、61(DMSO中で1又は10mMの保存溶液の5μL、最終濃度=10又は100μM)を、IA−アルキンの代わりに用いた。サンプルを、CuAACにより、上述のような軽(断片処理)又は重(DMSO処理)TEVタグ(DMSO中で5mMの保存溶液の10μL、最終濃度=100μM)、TCEP、TBTAリガンド、及びCuSO4に結合させた。サンプルを1時間反応させ、その時点でサンプルを遠心分離させた(16,000g、5分、4℃)。結果として生じるペレットを、氷冷のメタノール(500μL)の中で超音波処理し、次に、再懸濁させた軽及び重の標識されたサンプルを組み合わせ、遠心分離した(16,000g、5分、4℃)。ペレットを、超音波処理及び加熱(5分、95℃)で1.2%のSDSを含むPBS(1mL)の中で可溶化し、任意の不溶性物質を、周囲温度での追加の遠心分離工程(14,000g、1分)により取り除いた。
各サンプルについて、100μLのストレプトアビジン−アガロースビーズスラリー(Pierce)を、10mLのPBSの中で洗浄し、次に5mLのPBSの中で再懸濁した。SDSで可溶化されたタンパク質を、ストレプトアビジンアガロースビーズの懸濁液に加え、ビーズ混合物を周囲温度で3時間回転させた。インキュベーション後、ビーズを遠心分離(1,400g、3分)によりペレット状にし、洗浄した(2×10mLのPBS及び2×10mLの水)。
ビーズを、1mLのPBSを含むeppendorfチューブに移し、遠心分離し(1,400g、3分)、6Mの尿素を含むPBS(500μL)の中で再懸濁した。これに、10mMのDTT(水中で200mMの保存溶液の25μL)を加え、ビーズを65℃で15分間インキュベートした。その後、20mMのヨードアセトアミド(水中で400mMの保存溶液の25μL)を加え、振盪により37℃で30分間反応させた。ビーズ混合物を900μLのPBSで希釈し、遠心分離(1,400g、3分)によりペレット状にし、200μLのPBSの中で再懸濁した。これに、1mMのCaCl2(水中で200mMの保存溶液の2μL)、及びトリプシン(2μg、Promega、sequencing grade)を加え、振盪により37℃で一晩、消化を進めた。ビーズを、遠心分離(1,000g、1分)によるMicro Bio−Spin(Bio−Rad)で消化物から分離し、洗浄し(2×1mLのPBS及び2×1mLの水)、次いで1mLの水を含む新鮮なeppendorfに移した。洗浄したビーズを、140μLのTEV緩衝液(50mMのトリス、pH8、0.5mMのEDTA、1mMのDTT)の中でもう1回洗浄し、次に140μLのTEV緩衝液の中で再懸濁した。5μLのTEVプロテアーゼ(80μM)を加え、反応物を29℃で一晩回転させた。TEV消化物を、遠心分離(1,400g、3分)によるMicro Bio−Spinカラムでビーズから分離し、ビーズを水(100μL)で1回洗浄した。その後、サンプルを、5%(v/v)のギ酸の最終濃度へと酸性化し、分析前に−80℃で保存した。
isoTOP−ABPPサンプルの液体クロマトグラフィー質量分析(LC−MS)
TEV消化物を、C18樹脂(Aqua 5μm、Phenomenex)を詰めた250μm(内径)の石英ガラスキャピラリーカラムの上に載せ、圧力を加えた。サンプルを、Agilent 1200シリーズのクォータナリーポンプ(quaternary pump)につないだLTQ−Velos Orbitrap質量分析計(Thermo Scientific)を使用して、多次元の液体クロマトグラフィータンデム型質量分析(MudPIT)により分析した。Weerapana et al. Nat Protoc 2:1414−1425 (2007)に記載されるように、ペプチドを、500mMの水性酢酸アンモニウムの0%、30%、60%、90%、及び100%の塩隆起(salt bumps)を使用して、又は緩衝液Aにおける5−100%の緩衝液Bの勾配(緩衝液A:95%の水、5%のアセトニトリル、0.1%のギ酸;緩衝液B:5%の水、95%のアセトニトリル、0.1%のギ酸))を使用して、5つの工程のMudPIT実験において、5μmのチップ(100μmの石英ガラス、C18(10cm)、及びかさ高い強固なカチオン交換樹脂(3cm、SCX、Phenomenex))を含む二相のカラムの上に溶出させた。データ依存の獲得モードでデータを収集し、ダイナミックエクスクルージョン(dynamic exclusion)が可能になった(20s、2回の繰り返し)。1つの完全なMS(MS1)スキャン(400−1800m/z)、その後、n番目の最も豊富なイオンの30 MS2スキャン(ITMS)を行った。
ペプチド及びタンパク質の同定
MS2スペクトルデータを、RAW Xtractor(バージョン1.9.9.2;http://fields.scripps.edu/downloads.phpで利用可能)を使用して未加工のファイルから抽出した。MS2スペクトルデータを、ヒトのUniProtデータベース(release−2012_11)の逆連鎖状の(reverse concatenated)非冗長性の変異体を用いた、ProLuCIDアルゴリズム(http://fields.scripps.edu/downloads.phpで公に利用可能)を使用して探索した。システイン残基を、カルボキサミドメチル化のための静的な修飾により(+57.02146)、及び、軽又は重のTEVタグ(それぞれ+464.28595又は+470.29976)の何れかのための最大1つの特異な修飾により探索した。ペプチドは、少なくとも1つのトリプシン末端を有し、且つTEV修飾を含むことを要求される。ProLuCIDデータをDTASelect(バージョン2.0)に通して濾過し、1%未満のペプチド無病誤診率を達成した。
R値の算出及び処理
各固有のペプチド(DMSO/化合物処理;isoTOP−ABPPの比率、R値)の重/軽の比率を、デフォルトパラメータ(1つのピークにつき3ms1s及び信号対雑音の閾値2.5)を使用してインハウスの(in−house)CIMAGEソフトウェアで定量化した。求電子の断片の部位特異的な結合(engagement)を、IA−アルキンプローブの標識化の遮断により評価した。DMSOで処置したプロテオーム(重TEVタグ)と比べて、断片で処理したプロテオーム(軽TEVタグ)からのMS1ピーク面積において≧95%の減少を示したペプチドについて、20の最大の比率を割り当てた。固有のペプチドの侵入のための比率を、各実験のために計算し;同じ修飾されたシステイン(例えば、異なる荷電状態、MudPITクロマトグラフィーの工程、又はトリプシンの末端)でのペプチドの重複を1つにまとめ、中央の比率を最終的な比率(R)として報告した。CIMAGEにより報告されたペプチドの比率を更にフィルタ処理して、個々のデータセットにおける低品質比率の除去又は補正を確実にした。適用される品質フィルタは以下のとおりであった:トリプシンペプチドの半分の除去;中央(中央の90%以上)からの高い標準偏差との比率のために、最低の比率を中央の代わりに取り入れた;R=20を備えたペプチドの除去、及び親イオンの溶出中に引き起こされる単一のms2事象のみ;20の比率を持つ全てのペプチドのマニュアルアノテーション、以前のキュレーション工程の後に残った低品質溶出プロファイルを持つ任意のペプチドの除去。個々の断片に対するプロテオームの反応値を、各複製実験試験のためのR値≧4(リガンド結合したシステイン(liganded cysteines)として定義される)を含む合計の定量化されたシステイン含有ペプチドのパーセンテージとして計算し、最終のプロテオーム反応値を、MDA−MB−231及びRamosの細胞プロテオームの両方からの各断片の全ての複製実験のための平均として計算する。
クロスデータ処理
標準偏差が平均の60%未満であった場合、同じ化合物及び細胞株の生物学的な複製を平均化し;そうでなければ、比率のセットの最低値を得た。複数の修飾されたシステインを含むペプチドについて、最多数の定量化事象でのシステインを維持し、残りの冗長なペプチドを捨てた。総計のデータセット(更なる生物情報科学及び統計分析のために使用されたもの)に含まれるペプチドは、3つの実験において定量化されていることが求められた。システインに少なくとも2つの比率R≧4(ヒット断片)、及び0.5と2の間の1つの比率(対照断片)がある場合、システインはリガンドと分類される。大多数(断片の>75%)は少なくとも2つの生物学的な複製において特性を明らかにされるが、単一の複製のMS実験からのデータの一部が含まれていた。全ての断片についての平均化されたフィルタ処理したデータ、及び代表的な個々のフィルタ処理したデータセットは、表1−3に見出される。
インサイツのデータ処理
R値を計算し、個々のデータセットを上述(R値の算出及び処理)のようにフィルタ処理した。インサイツでのヒットの2つの分類を定めた:1)インビトロでヒットとしても観察された、インサイツでリガンド結合されるシステイン、及び、2)インビトロで検出されるがインサイツでのみリガンド結合されるシステイン。第1の分類について、インビトロ及びインサイツでの実験からの同じシステイン含有ペプチドのR値を比較し、両方に比率R≧4がある場合、システインはインサイツでリガンド結合可能であると考慮される。第2の分類について適格化するために、2つの異なる断片の複製のための2つの比率R≧4はインサイツで検出されることを求められ、これらの断片の少なくとも1つは、インビトロでR≦2を持つ非ヒット(non−hit)として定量化されねばならない。加えて、同じタンパク質からの別のシステインは、断片の競合からではなく断片の処置後のタンパク質発現の変化からR値において変わる可能性を制御するために、同じ断片によりインサイツでリガンド結合されない(R≦2)であることを求められた。
リガンド結合されたシステインの機能アノテーション
カスタムのpython scriptを使用して、UniProtKB/Swiss−Prot Protein Knowledgeのデータベース(release−2012_11)において利用可能な機能アノテーションをコンパイルした。関連するUniprotのエントリーを、残りの残基での利用可能な機能アノテーション、特に酵素触媒残基(活性部位)、ジスルフィド(レドックス活性及び構造的)、及び金属結合部位のために引き出した(mined)。リガンド結合されたタンパク質を、Drugbankのデータベース(バージョン4.2)に対して問い合わせ、DrugBank及び非Drugbankのタンパク質へと分画した。タンパク質レベルで割り当てられる機能的なキーワードを、Uniprotのデータベース殻収集し、Drugbank及び非Drugbankの分類をタンパク質の機能別の区分へと更に分類した。システイン反応データを、上述(ペプチド及びタンパク質の同定)のようにProLuCIDを使用して再処理した。反応及びリガンド結合可能性のデータセット両方に見出されるシステインを、それらの反応値(より低い比率はより高い反応を示す)に基づいて選別した。各反応ビン(刻み幅50)内の合計のリガンド結合されたシステインのパーセンテージの移動平均を得た。カスタムのpython scriptを開発して、RCSB Protein Data Bank(PDB)から関連するNMR及びX線の構造を収集した。利用可能なPDB構造のないタンパク質について、PDBにおいて堆積されるタンパク質に対してBLASTで実行される配列アラインメントを使用して、構造的な相同体を同定した。活性部位及び非活性システインのアノテーションについて、PDBにおける構造を含む酵素を手で検査して、システインの位置を評価した。システインは、10Åの活性部位のリガンド又は残基内にある場合、酵素活性部位に存在すると考慮された。10Åの範囲の外側のシステインを、非活性部位の残基であると考えた。高い被覆率、リガンド結合可能なシステイン、活性部位及び非活性部位のシステインにわたる断片のヒット率のヒストグラムを、10以上の別個の実験において定量化されたリガンド結合可能なシステインの亜群から計算した。断片のヒット率を、R≧4での合計の定量化事象のパーセンテージとして報告する。ヒストグラム及びヒートマップを含む全体のデータ内の傾向の分析のために、細胞株混合データセットを使用し、ここで、MDA−MB−231実験からのデータを得て、特定の断片及びシステインについてのMDA−MB−231実験からのデータが無い場合、第1及びRamosのデータを使用した。ヒートマップを、ヒートマップ2アルゴリズムを使用してR(バージョン3.1.3)において生成した。タンパク質構造を、Pymolを使用して再現した。
GSH反応
グルタチオン(GSH)を、アッセイ緩衝液(100mMのトリス、pH8.8、共溶媒として10%のエタノール)において125μMの最終濃度に希釈した。三通りで、透明な96ウェルプレート(Costar(登録商標)Corning(登録商標))中の100μLのGSH混合物に、示された求電子(DMSO中で50mM保存溶液の2μL、最終濃度=500μM)を加え、反応混合物を室温で1時間インキュベートした。5μLのEllman試薬(1M NaOH中で100mMの保存溶液、最終濃度=5mM)を加え、吸収度をプレートリーダー(Tecan Infinite F500)上で440nmで測定した。残りのGSHの濃度を標準曲線から計算した。
反応的なシステインドッキング(cysteine docking)
図3からのクロルアセトアミド及びアクリルアミドの断片を全て含む、インシリコの断片ライブラリーを、カスタムのPython scriptを備えたOpen Babelライブラリーを使用して調製した。断片を、それらの反応型(即ち、明確なクロルアセトアミド及びアクリルアミドの頭部(warheads)を備える)でモデル化した。3D座標をSMILESのストリングから生成し、pH7.4でそれらのプロトン化状態を計算し、次いでMMF94sの力場(50Kの反復の最も急勾配の降下;90Kの結合勾配)を使用してそれらを最小限にし;不確定の構成を持つキラル分子について、全てのエナンチオマーを精製し、合計53の断片を結果としてもたらした。
各タンパク質について、UniProtKB IDを使用し、PDBをフィルタ処理した。X線結晶学により判定される構造を選択し、より高い配列被覆率及び構造分解能をもたらす(privileging)(選択されたPDB IDについて表5を参照)。ヒトの構造が利用可能ではない時、利用可能な最も同族に近い生物を選択した(例えば、PRMT1:R.norvegicus)。タンパク質構造を、標準のAutoDockプロトコルに従い調製した。水、塩、及び結晶学的な添加剤を取り除き;AutoDockToolを使用し、水素を加えて、Gasteiger−Marsili電荷を計算し、PDBQTファイルを生成した。
MSMSを減らした表面の方法(MSMS reduced surface method)を使用して、アクセス可能なシステインを同定した。タンパク質量を、1.5Åのプローブ範囲を使用してスキャンし;残基は、外部表面又は内部空洞の何れかと接する少なくとも1つの原子がある場合、アクセス可能であると考慮された。
断片のライブラリーを、AutoDock 4.2を使用して個々のアクセス可能なシステイン上で独立してドッキングさせた。24.4×24.4×24.4Åのグリッドボックスを、残基の幾何学的中心に収集し;チオール水素を側鎖から取り除き、これをドッキング中に可撓性のものとしてモデル化し;構造の残りを固く保った。カスタムの13−7相互作用電位を、リガンドにおいて求核性の硫黄と反応的な炭素との間で定めた。平衡距離(req)を、C−S共有結合の長さ(1.8Å)に設定し;潜在的なウェルの深さ(εeq)は1.0と0.175の間で変動し、異なるリガンドの反応へとモデル化した。各断片のために、潜在的なウェルの深さを、そのプロテオミクス反応のパーセンテージを20で割ることにより判定し、ヨードアセトアミドの値を参考のために最大(2.5)として近似させた。潜在性を、AutoDockの力場の表の修正により実施した。断片を制約無しでドッキングし、デフォルトGA設定を使用して100のポーズを生成した。各断片について、最良のドッキングのスコアのポーズを分析し:求核性の硫黄と反応的な炭素との間の距離が≦2.0Åであった場合、システインは共有結合的に修飾されると考慮された。残基は、少なくとも1つのリガンドによりアルキル化された場合、標識されたと考慮された。ドッキングのスコア(即ち、負の結合エネルギー)を、そのドッキングしたポーズにおける各断片の推定された相互作用エネルギーに基づいて計算した。最良のアルキル化断片のドッキングのスコアを、標識化スコアとして定めた。最良の標識化スコアを持つ残基は、最も標識される可能性が高いものとして考慮された。
構造のモデリング
Batemanドメインを含むIMPDH2構造を、I−TASSERを使用してモデル化した。
サブクローン化及び突然変異生成
IDH1(Open Biosystems, Clone ID: 3880331)及びIMPDH2(Open Biosystems, Clone ID: 3447994)をコードする完全長のcDNAを、C末端His6−アフィニティータグ(SEQ ID NO:861)によりpET22b(+)(Novagen)へとサブクローン化した。TIGAR(Origene,Sc320794)をコードする完全長のcDNAを、N末端His6−アフィニティータグ(SEQ ID NO:861)によりpET28a(+)(Novagen)へとサブクローン化した。pET45b(+)(Novagen)へとサブクローン化された完全長のPRMT1は、Cravatt labにより以前に制された。完全長のヒトCASP3(残基1−277)及びCARDドメインの無い切断型CASP8(残基217−479)を、C末端His6−アフィニティータグ(SEQ ID NO:861)によりpET23b(Novagen)へとサブクローン化した。システイン突然変異体を、所望の突然変異及びそれぞれの補体(compliments)を含むプライマーを使用する、QuikChangeの部位特異的突然変異誘発を使用して生成した。
TIGAR、IDH1、PRMT1、及びIMPDH2の組換え型の過剰発現
TIGAR、IDH1、PRMT1、及びIMPDH2を、0.8のOD600へと、所望の抗生物質(50μg/mLのカナマイシン又は50μg/mLのカルベニシリン)で補足されたTerrific Broth上で成長させたBL21(DE3)化学的なコンピテント細胞(NEB)の中で発現させ、18℃で16時間、0.5mMのIPTGで誘導した。細胞を直ちに収集し、リゾチーム(Sigma)、デオキシリボヌクレアーゼ(NEB)、及びcOmpleteプロテアーゼ阻害剤の錠剤(Roche)で補足した30mLの冷たい緩衝液A(25mMのトリス、pH7.4、200mMのNaCl、10%のグリセロール、1mMのBME)中で再懸濁させ、超音波で処理し、遠心分離機した(45,000g、30分、4℃)。可溶性画分を収集し、4℃で1mLのNi−NTAスラリー(Qiagen)により1時間回転させた。その後、スラリーを50mLの量の溶融カラムに移し、重力流により収集した。その後、樹脂を、20mMのイミダゾールを含む100mLの緩衝液Aで洗浄し、200mMのイミダゾールを含む10mL緩衝液Aで溶出した。溶出剤を、2.5mL(Amicon−Ultra−15、10kDaのMWカットオフ)に濃縮し、PD10カラム(GE Amersham)を使用して緩衝液を貯蔵緩衝液(50mMのHEPES、pH7.4、150mMのNaCl、10%のグリセロール、1mMのBME)と交換し、更に濃縮して(Amicon−Ultra−4、10kDaのMWカットオフ)、およそ100μMのタンパク質の最終濃度とした。タンパク濃度を、Bio−Rad DC(商標)タンパク質アッセイキットを使用して判定した。タンパク質純度を、還元条件下でSDS−PAGEにより分析し、>95%の純度であった。
組換え型のCASP3、CASP8、及びTEVプロテアーゼの発現
CASP3、CASP8、プロCASP8(D374A、D384A)、及びN末端MBP融合−His6−TEV−Arg6プロテアーゼの構築物pRK793(SEQ ID NO:861として開示された「His6」、及びSEQ ID NO:862として開示された「Arg6」)を、大腸菌BL21(DE3)pLysS細胞(Stratagene)の中で発現させた。細胞を、0.8−1.0のOD600に対して、37℃で200μg/mlのアンピシリン及び50μg/mlのクロラムフェニコールで補足された2xYT培地の中で成長させた。カスパーゼの過剰発現を、30℃で4時間0.2mMのIPTGで(CASP3)、12℃で一晩(CASP8)、又は30℃で4時間0.5mMのIPTGで(TEVプロテアーゼ)、誘導した。細胞を直ちに収集し、氷冷の緩衝液A(カスパーゼ:100mMのトリス、pH8.0、100mMのNaCl;TEVプロテアーゼ:PBS)の中で再懸濁し、微少溶液操作(Microfluidics)により溶解の3つのサイクルにさらした。細胞溶解物を遠心分離(45,000g、30分、4℃)により明確にし、可溶性画分を、緩衝液Aで予め平衡に保ち且つ200mMのイミダゾールを含む緩衝液Aで溶出される1mLのHisTrap HP Ni−NTAアフィニティカラム(GE Amersham)に充填した。溶出されたタンパク質を、緩衝液B(20mMのトリス、pH8.0)で直ちに2倍に希釈し、1MのNaClを含む緩衝液Bの50%まで、30カラムの量の勾配での陰イオン交換クロマトグラフィー(HiTrap Q HP、GE Amersham)により精製した。緩衝液の交換及び任意の残りの汚染物質の除去のために、緩衝液C(カスパーゼ:20mMのトリス、pH8.0、50mMのNaCl;TEVプロテアーゼ:PBS、10mMのDTT)において、カスパーゼをSuperdex 200 16/60ゲル濾過カラム(GE Amersham)上で、及びTEVプロテアーゼをSuperdex 75ゲル濾過カラム(GE Amersham)上で注入した。所望のタンパク質を含む画分をプールし、およそ1mg/mL(Millipore Ultrafree−15, 10kDaのMWカットオフ)に濃縮した。精製されたタンパク質を直ちに凍結し、−80℃で保存した。タンパク質濃度を、変性条件においてBio−Rad比色測定法及びA280の吸収度の両方を使用して測定した。タンパク質純度を、還元条件下でSDS−PAGEにより分析し、>98%の純度であった。
フラグタグを付けられたIDH1タンパク質のレトロウイルスの過剰発現
望まれない制限部位及びGFPを除去するために、付加的なK345Kサイレント突然変異を含むR132H−IDH1を、修飾したpCLNCXレトロウイルスベクターへとサブクローン化した。レトロウイルスを、HEK−293RTV細胞をトランスフェクトするために、1.5μgの各pCLNCXベクター、1.5μgのpCMV−VSVG、及び20μLのRoche X−tremeGeneHP DNAトランスフェクション試薬を得ることにより調製した。培地をトランスフェクションの1日後に交換し、翌日、培養物の上清を収集し、0.5μMのフィルタに通して濾過した。所望のウイルスを含む10mLの濾液を使用して、48時間にわたりポリブレン(8μg/mL)の存在下でMUM2C細胞を感染させ、その時点で、感染細胞を、7−10日間100μg/mLのヒグロマイシンを含む培地において選択した。生存細胞を拡張し、ヒグロマイシンを含む完全なRPMI−1640培地の中で培養した。
IDH1 NADPアッセイ
組換え型のIDH1及びC269S−IDH1(貯蔵緩衝液において100μM)を、MDA−MB−231の細胞プロテオーム(1mg/mL)において1:200に希釈した。25μLのこの混合物に、1μLの示された化合物(DMSO中で25倍の保存溶液)を加え、溶解物を透明な96ウェルプレート(Corning(登録商標)Costar(登録商標))において室温で1時間、インキュベートした。IDH1緩衝液(40mMのトリス、pH7.4、2mMのMgCl2、0.01%のプルロニック)中の、NADP(13.3mM)とイソシトラート(13.3mM)との1つのウェルにつき75μLの保存溶液を、96ウェルのUV吸光度プレートリーダー(TECAN)上で、340nmでUV吸光度を測定する直前に加えた。吸収度は45分間測定し、相対活性を、曲線の直線部分に関する吸収度の変化から計算した。
IDH1 2−ヒドロキシグルタラート(2−HG)形成アッセイ
IDH1 R132Hを安定して過剰発現するMUM2C細胞を、1.5×106細胞/150mmの皿に播種した。翌日、示された化合物(DMSO中で50mMの保存溶液)又はDMSOを細胞に加え、示された最終濃度とし、2時間インキュベートした。GFPを過剰発現する対照細胞を平行して処理した。細胞を氷冷PBSの中で洗浄し、氷冷PBS及び遠心分離(1,400g、3分、4℃)においてこすることにより収集した。その後、細胞ペレットを100μLの氷冷PBSにおいて再懸濁し、その後、10分間16,000gで超音波処理と遠心分離を行った。その後、溶解物を、0.5mLのZEBAスピン脱塩カラム(Thermo Fisher, 89882)により、IDH1緩衝液(40mMのトリス、pH7.4、2mMのMgCl2)へと緩衝液交換した。タンパク質濃度を3.5mg/mLに調整し、25μLの溶解物を25μLの反応混合物(IDH1緩衝液中で2.5mMのNADPH及び2.5mMのα−ケトグルタル酸塩)と混合し、反応を4時間にわたり進めて、その時点で反応混合物を50μLの冷たいメタノールでクエンチし、その後遠心分離(16,000g、10分、4℃)を行った。2−HGの形成の後、標的とされたLC/MS分析を行った。反応混合物を、移動相A及びB(移動相A:100%のCH3CN、0.1%のギ酸;移動相B:95:5(v/v)H2O:CH3CN、50mMのNH4OAc、0.2%のNH4OH)の勾配を使用して、前置カラム(NH2、4×3.0mm)を持つLuna−NH2カラム(5μm、100Å、50×4.6mm、Phenomenex)で分離した。流量は0.1mL/分で開始し、勾配は5分の0%のB、0.4mL/分の流量で20分にわたり100%のBへの直線の増大、その後の、0.4mL/分(合計30分)で0%のBで3分間にわたり平衡化する前の、0.5mL/分で2分間にわたり100%のBの均一濃度の勾配から成る。各実行について、注入量は25μLであった。MS分析を、ESIのソースを持つAgilent G6410Bタンデム質量分析計上で行った。2−HGのための滞留時間を100msに設定した。また、2−HGのための衝突エネルギーを5に設定した。キャピラリーを4kVに設定し、フラグメンターを100Vに設定した。乾燥ガス温度は350℃であり、乾燥ガスの流量は11L/分であり、ネブライザー圧力は35psiであった。質量分析計をMRMモードで実行し、2−HG(負のイオン化モード)について146.7〜129のm/zの変化をモニタリングした。処理を3回繰り返して行った。発現細胞上の「模擬の」GFPから計算されたバックグラウンドの2−HG産生を、合計の2−HGの産生から控除した。
TIGAR活性のアッセイ
Gerin et al. The Biochemical Journal 458:439−448 (2014)に記載されるように、TIGAR活性のアッセイを行った。23BPG(2,3−ビスホスホグリセラート)からの3PG(3−ホスホグリセラート)の産生の形成を、TECANプレートリーダー上で分光測光法により測定し、透明で平底の96ウェルのマイクロプレート(Corning(登録商標)Costar(登録商標))において340nmでの吸収度の減少を測定した。2μLの組換え型のTIGAR(10mg/mL)を、1mLの希釈緩衝液(25mMのHEPES、pH7.1、25mMのKCl、1mMのMgCl2)に希釈した。25μLの希釈したタンパク質を、示された濃度の化合物(1μL、DMSO中で25倍の保存溶液)で1時間インキュベートした。その後、25mMのHEPES(pH7.1)、25mMのKCl、1mMのMgCl2、0.5mMのNADH、1mMのDTT、1mMの23BPG、1mMのATP−Mg、1μLの各ウサギの筋肉GAPDHの相当物(4000の単位/mL、Sigma、G5537)、及び酵母PGキナーゼ(6300の単位/mL、Sigma、P7634)で構成される、75μLのアッセイ混合物を、タンパク質に加え、吸収度の減少を340nmでモニタリングした。TIGARを欠くサンプルから計算したバックグラウンドを、TIGARを含むサンプルから控除した。実験を4回繰り返して実行した。
PRMT1のインビトロでのメチル化のアッセイ
Weerapana et al. Nature 468:790−795 (2010)に記載されるように、PRMT1アッセイを行った。25μLのメチル化緩衝液(20mMのトリス、pH8.0、200mMのNaCl、0.4mMのEDTA)における組換え型のヒトPRMT1(0.85μM、野生型又はC101S突然変異体)を、1時間にわたり示された断片で予めインキュベートし、メチル化活性を、1mgの組換え型のヒストン4(NEB、M2504S)及び3H−SAM(2μCi)の追加後にモニタリングした。反応物を、周囲温度で60分間にわたり更にインキュベートし、4×SDSサンプル緩衝液で止めた。SDS−PAGEゲルを、10%の酢酸/10%のメタノール(v/v)で固定し、洗浄し、増幅試薬(Amersham)でインキュベートした後、−80℃で3日間、薄膜に曝した。
MLTKのインビトロでのキナーゼ活性のアッセイ
Wang et al. ACS Chemical biology 9:2194−2198 (2014)に記載されるように、キナーゼ活性のアッセイプロトコルを行った。キナーゼアッセイ緩衝液、ミエリン塩基性タンパク質(MBP)基質、及びATP保存溶液を、SignalChemから購入した。放射標識した[γ−33P]ATPをPerkinElmerから購入した。WT、C22A、又はK45M MLTKを安定して過剰発現する、250μLのHEK−293Tの可溶性の溶解物(8mg/mL)を、100μMの断片又はDMSOで1時間標識した。その後、サンプルを、1つのサンプル当たり20μLのフラグ樹脂のスラリーで個々に免疫沈殿させ、次に15μLの3×Flag−ペプチドで溶出した。各サンプルに、5μLのMBPを加え、次に、5μLの[γ−33P]ATPアッセイカクテル(250μM、167μCi/mL)を加え、キナーゼ反応を開始した。各反応混合物を周囲温度で30分間インキュベートし、反応を、個々の予め切られたホスホセルロースP81紙上に25μLの反応混合物の点を付けることにより終わらせた。点を付けたP81紙片を、10mLの1%のリン酸(3×10分)で洗浄した。MLTK活性を、シンチレーション計数器中にシンチレーション流体がある状態でP81紙上の放射活性を数えることにより測定した。バックグラウンドを、K45M−不活性突然変異体MLTK活性レベルから判定し、これをWTとC22Aのサンプルから控除した。WTとC22Aのための相対活性を、それぞれのDMSOで処理したサンプルへ標準化した。実験を3回繰り返して実行した。
CASP3とCASP8のインビトロの活性のアッセイ
カスパーゼ3と8のアッセイを、製造業者の指示に従い、CASP8活性のアッセイキット(BioVision,K112−100)及びカスパーゼ3活性のアッセイキット(Invitrogen, EnzChekR Caspase−3 Assay Kit)により行った。簡単に、組換え型のカスパーゼ3(10μM)を可溶性のRamos溶解物(1mg/mL)に加え、100nMの最終濃度のプロテアーゼを得た。カスパーゼ8(30μM)を可溶性のRamos溶解物に加え、1μMの最終濃度のプロテアーゼを得た。三通りで、50μLの溶解物を、1時間、DMSO、DEVD−CHO(SEQ ID NO:857として開示された「DEVD」)(20μM)、又は示された化合物(100μM)で処理し、その後、10mMのDTT及び5μLの基質を含む50μLの2倍の反応緩衝液(CASP8についてはIETD−AFC(SEQ ID NO:858として開示された「IETD」)のDMSO中の4mMの保存溶液;CASP3についてはDEVD−AMC(SEQ ID NO:857として開示された「DEVD」)のDMSO中の10mMの保存溶液)を、各ウェルに加えて、サンプルを周囲温度で2時間インキュベートした。カスパーゼ活性を、蛍光の増大(励起380nm、発光460nm)から測定した。実験を3回繰り返して実行した。バックグラウンドを、組換え型のカスパーゼを欠くサンプルから計算した。
カスパーゼ8阻害剤でのアポトーシスアッセイ
RPMI中の4mLJurkat細胞(150万個の細胞/mL)を、30μMで30分間、示された化合物で処理した(DMSO中の50mMの保存溶液)。Z−VAD−FMK(EMD Millipore Biosciences, 627610)を、100μMの最終濃度で使用した。プレインキュベーションの後、FASL(水中のSuperFasLigand(商標)の100μg/μLの保存溶液の4μL、最終濃度=100ng/mL、Enzo life Sciences)又はスタウロスポリン(DMSO中で1mMの保存溶液の8μL、最終濃度=2μM、Fisher Scientific, 50664333)。6時間後、細胞を遠心分離により収集し、洗浄し、細胞溶解緩衝液(BioVision,1067−100)の中で溶解して、40μgの各サンプルを14%のポリアクリルアミドゲル上でのSDS−Pageにより分離した。ゲルをニトロセルロース膜に移し、示された抗体で一晩免疫ブロットした。細胞の生存率の測定のために、各条件について4通りで、150,000の細胞(150万の細胞/mLの100μL)を、Nunc(商標)MicroWell(商標)96−Well Optical−Bottom Plates with Polymer Base(Fisher Scientific)に蒔いた。化合物としてFASL及びSTSを同じ濃度で使用し、化合物での30分のプレインキュベーション、その後STS、FASL、又はDMSOの何れかで6時間のプレインキュベーションを行った。細胞の生存率を、CellTiter−Glo(登録商標)Luminescent Cell Viability Assay (Promega)で測定し、Biotech Synergy 4のプレートリーダー上で読み出した。
ウエスタンブロット法
CASP8、CASP3、及びPARPについて、細胞ペレットを、1×cOmpleteプロテアーゼ阻害剤(Roche)を含む(BioVision,1067−100)からの細胞溶解緩衝液の中で再懸濁し、遠心分離(10分、16,000g)前に30分間、氷の上でインキュベートした。他の全てのタンパク質について、細胞ペレットをPBS中で再懸濁され、遠心分離(10分、16,000g)前に超音波処理で溶解した。その後、タンパク質をSDS−PAGEにより分解し、ニトロセルロース膜に移し、TBST中の5%のBSAで遮断して、示された抗体で探索した。使用される一次抗体及び希釈物は以下のとおりである:抗parp(Cell Signaling, 9532, 1:1000)、抗casp3(Cell Signaling, 9662, 1:500)、抗casp8(Cell Signaling, 9746, 1:500)、抗IDH1(Cell Signaling, 1:500, 3997s)、抗アクチン(Cell Signaling, 3700, 1:3000)、抗gapdh(Santa Cruz, sc−32233, 1:2000)、抗flag(Sigma Aldrich, F1804, 1:3000)。ブロットを、振動により4℃で一晩、一次抗体でインキュベートし、その後、洗浄し(3×5分、TBST)、周囲温度で1時間、二次抗体(LICOR、IRDye(登録商標)800CW又はIRDye(登録商標)800LT、1:10,000)でインキュベートした。ブロットを更に洗浄し(3×5分、TBST)、LICOR Odyssey Scanner上で視覚化した。
統計分析
データを平均±SEMとして示す。独立両側スチューデントt検定を使用してP値を計算した。<0.05のP値を、有意であると考慮した。
反応的なドッキングにおける予測の失敗
予想の失敗は、非常に可撓性の/溶解力のある曝露されたループ領域(STAT1:C255、PDB ID:1YVL;HAT1:C101、PDB ID:2P0W;ZAP70:C117、PDB ID:4K2R)、又は部分的に埋められた残基(SARS:C438、PDB ID:4l87;PAICS:C374、PDB ID:2H31)と共に使用される、剛性モデルの近似によるものであった。幾つかの実施形態において、(可撓性の側鎖など)可撓性のある程度のシミュレーションが、成功率を改善する。幾つかの実施形態において、配列が利用可能なモデル(XPO1:C34、C1070、PDB ID: 3GB8、FNBP1、C555、C609、PDB ID:C511:2EFL;IMPDH2:C140、PDB ID:1NF7)において完全に分解されない時、又はオルソログ配列のみが利用可能(PRMT1:R.Norvegicus、PDB ID:1ORI)である時に、方法は結晶構造の利用可能性及び品質により限定されなかった。
一般的な合成法
化学物質と試薬を、Sigma Aldrich、Acros、Fisher、Fluka、Santa Cruz、CombiBlocks、BioBlocks、及びMatrix Scientificを含む様々な供給業者から購入し、特に定めの無い限り、更に精製することなくこれらを使用した。無水溶媒を、市販で入手可能な予め乾燥させた無酸素の製剤として得た。フラッシュクロマトグラフィーを、230−400のメッシュのシリカゲルを使用し実行した。分取薄層クロマトグラフィー(PTLC)を、500−2000μmの厚みを持つガラスで裏打ちした(glass backed)PTLCプレート(Analtech)を使用して実行した。全ての反応を、0.25mmのE.Merckのシリカゲルプレート(60F−254)上で実行された薄層クロマトグラフィーによりモニタリングし、UV光で、又は、ニンヒドリン、エタノール性のリンモリブデン酸、ヨウ素、p−アニスアルデヒド、又は過マンガン酸カリウムの染色により、視覚化した。NMRスペクトルを、示された溶媒において、Varian INOVA−400、Bruker DRX−600、又はBruker DRX−500の分光計上で記録した。多様性を以下の略語で報告する:s 一重項;d 二重項;t 三重項;q 四重項;p 五重項(pentet);m 多重項;br 広範囲。化学シフトをTMSに対するppmで報告し、J値をHzで報告した。質量分析のデータを、HP1100の単一の四極子の器具(ESI;低解像度)又はAgilent ESI−TOFの器具(HRMS)の上に収集した。
幾つかの実施形態において、基本手順Aを、本明細書に記載される小分子断片及び/又はシステイン反応性プローブの1つ以上の合成のために使用した。アミンを無水CH2Cl2(0.2M)の中で溶解し、0℃に冷却した。これに、無水ピリジン(1.5当量)を一度に加え、次にクロロアセチルクロリド(1.5当量)を滴下で加え、出発物質の完全消失及び生成物への変換が検出されるまで(典型的に1時間)、反応をTLCによりモニタリングした。反応が完了まで進まなかった場合、ピリジン(0.5当量)およびクロロアセチルクロリド(0.5当量)の追加のアリコートを加えた。反応物をH2O(1mL)でクエンチし、CH2Cl2(20mL)で希釈し、飽和NaHCO3(100mL)で2回洗浄した。有機質層を真空内で濃縮し、分取薄層又はフラッシュカラムクロマトグラフィーにより精製して、所望の生成物を得た。幾つかの実施形態において、基本手順A1は、トリエチルアミン(3当量)がピリジンの代わりに使用されること以外は、基本手順Aと同様である。幾つかの実施形態において、基本手順A2は、N−メチルモルホリン(3当量)がピリジンの代わりに使用されること以外は、基本手順Aと同様である。
幾つかの実施形態において、基本手順Bを、本明細書に記載される小分子断片及び/又はシステイン反応性プローブの1つ以上の合成のために使用した。アミンを無水CH2Cl2(0.2M)の中で溶解し、0℃に冷却した。これに、トリエチルアミン(TEA、1.5当量)を一度に加え、次にアクリロイルクロリド(1.5当量)を滴下で加え、出発物質の完全消失及び生成物への変換が検出されるまで(典型的に1時間)、反応をTLCによりモニタリングした。反応が完了まで進まなかった場合、TEA(0.5当量)及びアクリロイルクロリド(0.5当量)の追加のアリコートを加えた。反応物をH2O(1mL)でクエンチし、CH2Cl2(20mL)で希釈し、飽和NaHCO3(100mL)で2回洗浄した。有機質層をシリカのプラグに通して、その後、溶離液を真空内で濃縮し、分取薄層又はフラッシュカラムクロマトグラフィーにより精製して、所望の生成物を得た。
幾つかの実施形態において、基本手順Cを、本明細書に記載される小分子断片及び/又はシステイン反応性プローブの1つ以上の合成のために使用した。アクリロイルクロリド(80.4μL、1.0mmol、2当量)を、無水CH2Cl2(4mL)に溶解し、0℃に冷却した。その後、CH2Cl2(2mL)中のアミン(0.5mmol、1当量)及びN−メチルモルホリン(0.16mL、1.5mmol、3当量)の溶液を、滴下で加えた。反応物を0℃で1時間撹拌し、その後室温にまでゆっくりと暖めた。TLC分析により出発物質の消失を示した後、又は6時間後、どちらが早く生じたとしても、反応物を飽和水性NaHCO3(5mL)でクエンチし、CH2Cl2(3×10mL)で抽出した。組み合わせた有機質層を無水Na2SO4で乾燥し、真空内で濃縮し、得られた残留物を分取薄層クロマトグラフィーにより精製して、所望の生成物を得た。
プローブ及びフラグメントの合成
購入された断片
以下の求電子の断片は示された供給業者から購入された。2(Santa Cruz Biotechnology sc−345083)、3(Key Organics JS−092C)、4(Sigma Aldrich T142433−10mg)、6(Toronto Research Chemicals M320600)、8(Alfa Aesar H33763)、10(Santa Cruz Biotechnology sc−345060)、11(Santa Cruz Biotechnology sc−354895)、12(Santa Cruz Biotechnology sc−354966)、21(Santa Cruz Biotechnology, sc−279681)、22(Sigma Aldrich 699357−5G)、26(Sigma Aldrich T109959)、27(Santa Cruz Biotechnology sc−342184)、28(Santa Cruz Biotechnology sc−335173)、29(Santa Cruz Biotechnology sc−348978)、30(Santa Cruz Biotechnology sc−355362)、32(Santa Cruz Biotechnology sc−354613)、33(Sigma Aldrich R996505)、34(Santa Cruz Biotechnology sc−355477)、35(Santa Cruz Biotechnology sc−328985)、41(Sigma Aldrich L469769)、42(Sigma Aldrich R901946)、43(Santa Cruz Biotechnology sc−307626)、52(Enamine, EN300−08075)、55(Santa Cruz Biotechnology sc−354880)、57(VWR 100268−442)、58(Enzo Life Sciences ALX−430−142−M005)、62(WuXi Apptec)。
同位体的に標識されたTEVタグの合成:
同位体的に標識された重及び軽タグを、Weerapana et al. Nat Protoc 2:1414−1425 (2007)及びWeerapana et al. Nature 468:790−795 (2010)にて報告される手順に対して細かな修正を加えて、合成した。Fmoc−Rink−アミド−MBHA樹脂(EMD Biosciences;0.5M、830mg、0.6mmol/gの充填)を、DMF(50% v/v、2×5mL、1分)において4−メチルピペリジンで脱保護した。Fmoc−Lys(N3)−OH(Anaspec)(500mg、1.26mmol、1.26当量)を、DIEA(113μl)及び2−(6−クロロ−1H−ベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルアミニウムヘキサフルオロホスファート(HCTU;DMF中の0.5Mの保存溶液の1.3mL)により室温で一晩、樹脂に結合させ、その後、Fmoc−Lys(N3)−OH(500mg、1.26mmol、1.26当量)、DIEA(113μl)、O−(7−アザベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムヘキサフルオロホスファート(HATU;DMF中の0.5Mの保存溶液の1.3mL)により一晩、2回目の結合を行った。その後、修飾していない樹脂を、DMF中でAc2O(400μL)及びDIEA(700μL)により覆い(2×30分)、その後、樹脂をDMF(2×1分)で洗浄した。その後、DMF(50% v/v、2×5mL、1分)における4−メチルピペリジンでの脱保護、及びHCTU(2mL、DMF中で0.5M)とDIEA(347.7μL)での結合サイクル(DMF中で4当量のFmocで保護されたアミノ酸(EMD biosciences))を、残りのアミノ酸のために繰り返した。重TEVタグについて、Fmoc−バリン−OH(13C5C15H21 15NO4、13C5、97−99%、15N、97−99%、Cambridge Isotope Laboratories, Inc.)を使用した。反応をニンヒドリン染色によりモニタリングし、二重の結合を、完了まで進まなかった全ての工程に使用した。ビオチン(0.24g、2当量)を、室温で2日間、NHS(0.1g、2当量)、DIC(0.16g、2当量)、及びDIEA(0.175g、2当量)と結合させた。その後、樹脂をDMF(5mL、2×1分))で洗浄し、その後、1:1のCH2Cl2:MeOH(5mL、2×1分)で洗浄し、窒素の流れの下で乾燥させ、丸底フラスコに移した。95:2.5:2.5のトリフルオロ酢酸:水:トリイソプロピルシランでの処理により、90分かけてペプチドを樹脂から切断した。樹脂を濾過により取り除き、残りの溶液を冷たいエーテルで粉砕して、白色固形物として軽又は重のTEVタグの何れかを得た。HPLC−MSにより僅かな不純物のみが明らかとなり、化合物を更に精製することなく使用した。HRMS−ESI (m/z):calculated for C83H128N23O23S [M+H]:(Light−TEV−Tag) 1846.9268;found:1846.9187;calculated for C78 13C5H128N22 15NO23S [M+H]:(Heavy−TEV−Tag):1852.9237;found:1852.9309。
プローブ及び断片の合成
1の合成
N−(ヘキサ−5−イン−1−イル)−2−クロロアセトアミド(SI−1)
0℃でCH2Cl2(3.2mL、0.2M)中の5−ヘキシニルアミン(63mg、0.65mmol、1.0当量)の溶液に、N−メチルモルホリン(215μL、3当量)、その後、少量ずつクロロ酢酸無水物(222mg、2当量)を加えた。反応物を室温にし、次いで一晩撹拌した。その後、反応物をエーテル(50mL)で希釈し、1MのHCl、1MのNaOH、次いでブライン(各々20mL)で洗浄した。組み合わせた有機質層を硫酸マグネシウムで乾燥し、濃縮して、クロロアセトアミドSI−1(74mg、66%)を得た。1H NMR (400 MHz, クロロホルム−d) δ 6.79 (s, 1H), 4.09 (d, J = 1.1 Hz, 2H), 3.34 (q, J = 6.8 Hz, 2H), 2.23 (td, J = 6.9, 2.7 Hz, 2H), 1.98 (t, J = 2.7 Hz, 1H), 1.75−1.62 (m, 4H), 1.62−1.51 (m, 2H)。
N−(hex−5−イン−1−イル)−2−ヨードアセトアミド(1)
アセトン(1mL、0.2M)中のクロロアセトアミドSI−1(36.1mg、0.2mmol)の溶液にヨウ化ナトリウム(47mg、1.5当量)を加え、反応物を一晩撹拌した。翌日、反応物を、ヘキサン中で20%の酢酸エチルで溶出するシリカのプラグに通して濾過し、濾液を濃縮して、所望のヨードアセトアミド1及び出発物質の10:1の混合物を得た。この混合物を更に1日にわたり反応条件に再びさらし、その時点で完全な変換を観察した。生成物を、ヘキサン中で5〜10%から15〜20%の酢酸エチルの勾配を利用するシリカゲルクロマトグラフィーにより精製して、所望の生成物(24mg、44%)を得た。幾つか実施形態において、反応物を2.5当量のヨウ化ナトリウムにより実行し、その場合、再度の曝露は必要とされず、PTLCによる精製を、溶離剤として30%のEtOAc/ヘキサンの中で遂行する。1H NMR (500 MHz, クロロホルム−d) δ 6.16 (s, 1H), 3.69 (s, 2H), 3.30 (q, J = 6.8 Hz, 2H), 2.23 (td, J = 6.8, 2.6 Hz, 2H), 1.97 (t, J = 2.6 Hz, 1H), 1.75−1.61 (m, 2H), 1.61−1.52 (m, 2H)。
N−(4−ブロモフェニル)−N−フェニルアクリルアミド(5)
4−ブロモフェニルアニリン(18.9mg、0.0762mmol、1当量)から、表題化合物を基本手順Cに従い合成した。分取TLC(30%のEtOAc/ヘキサン)による粗製生成物の精製によって、白色固形物(12.5mg、54%)として表題化合物を得た。1H NMR (500 MHz, クロロホルム−d) δ 7.47 (d, J = 8.2 Hz, 2H), 7.39 (t, J = 7.6 Hz, 2H), 7.32 (d, J = 7.4 Hz, 1H), 7.21 (d, J = 7.7 Hz, 2H), 7.12 (d, J = 8.2 Hz, 2H), 6.48 (d, J = 16.7 Hz, 1H), 6.17 (dd, J = 16.8, 10.3 Hz, 1H), 5.65 (d, J = 10.3 Hz, 1H);HRMS−ESI (m/z) calculated for C15H13BrNO [M+H]:302.0175;found:302.0176。
7の合成
tert−ブチル4−(フェニルアミノ)ピペリジン−1−カルボン酸塩(SI−2)
Thoma et al, J. Med. Chem. 47:1939−1955 (2004)に従い、SI−2を調製した。1H NMR (400 MHz, クロロホルム−d) δ 7.24−7.12 (m, 2H), 6.75−6.68 (m, 1H), 6.66−6.58 (m, 2H), 3.88−3.81 (m, 1H), 3.44 (tt, J = 10.4, 3.9 Hz, 2H), 3.00−2.88 (m, 2H), 2.10−1.99 (m, 2H), 1.48 (bs 9H), 1.41−1.27 (m, 2H)。
tert−ブチル4−(2−クロロ−N−フェニルアセトアミド)ピペリジン−1−カルボン酸塩(SI−3)
CH2Cl2(0.6mL)中の0℃でのアニリンSI−2(65mg、0.24mmol)の溶液に、ピリジン(38μL、2当量)、その後、CH2Cl2(0.6mL)中のクロロアセチルクロリド(37.4μL、2.0当量)を加えた。結果として生じる溶液を室温に暖め、一晩撹拌した。その後、溶液を、飽和水性重炭酸ナトリウムでクエンチし、Et2O(3×10mL)で抽出した。組み合わせた有機質層を硫酸マグネシウムで乾燥し、濾過し、濃縮して、オフホワイトの固形物を得て、それを更に生成することなく使用した(47mg、57%)。1H NMR (400 MHz, クロロホルム−d) δ 7.47−7.38 (m, 3H), 7.18−7.03 (m, 2H), 4.75−4.63 (m, 1H), 4.07 (s, 2H), 3.68 (s, 2H), 2.76 (s, 2H), 1.84−1.69 (m, 2H), 1.35 (s, 9H), 1.27−1.12 (m, 2H)。
N−(1−ベンゾイルピペリジン−4−イル)−2−クロロ−N−フェニルアセトアミド(7)
きれいな(neat)SI−3(47mg、0.128mmol)に、トリフルオロ酢酸(0.7mL、最終0.2M)を加えた。これ以上蒸発が観察されなくなるまで結果として生じる溶液を窒素の流れの下で濃縮し、そのトリフルオロ酢酸塩として脱保護されたアミンを得た。その後、この粘着性ガムを、酢酸エチル中のトリエチルアミン(10% v/v、2mL;追加後に溶液は煙を出す)で処理した。結果として生じる溶液を濃縮し、遊離塩基を得て、これは、プロトンNMRによりトリエチルアンモニウムトリフルオロアセテート及び遊離アミンしか含んでいなかった。保存溶液を、CH2Cl2(1.2mL、〜0.1Mの最終)の中で結果として生じるガムを溶解することにより調製した。
脱保護したアミン(0.3mLの保存溶液、0.0319mmol)を、ヒューニッヒ塩基(17.5μL、3当量)及び塩化ベンゾイル(7.6μL、2.0当量)で処理した。この溶液を一晩撹拌し、飽和水性重炭酸ナトリウムでクエンチし、Et2O(3×10mL)で抽出した。結果として生じる溶液を硫酸マグネシウムで乾燥し、濾過し、濃縮した。結果として生じる油をシリカゲルクロマトグラフィー(20%のEtOAc/ヘキサン)により精製し、白色固形物(8.6mg、75%)としてクロロアセトアミド7を得た。1H NMR (500 MHz, クロロホルム−d) δ 7.55 (dd, J = 5.5, 3.0 Hz, 3H), 7.50−7.32 (m, 5H), 7.21 (s, 2H), 4.92 (tt, J = 12.3, 4.0 Hz, 1H), 4.87 (s, 1H), 3.87 (s, 1H), 3.78 (s, 2H), 3.21 (s, 1H),2.97−2.90 (m, 1H), 2.01 (s, 1H), 1.90 (s, 1H), 1.45 (s, 1H), 1.36−1.26 (m, 1H);HRMS−ESI (m/z) calculated for C20H22ClN2O2 [M+H]:357.1364;found:357.1362。
1−(4−ベンジルピペリジン−1−イル)−2−クロロエタン−1−オン(9)
基本手順Aに従い、4−ベンジルピペリジン(840mg、5.2mmol、1当量)から出発して、所望の化合物を黄色の油(1g、81%)としてカラムクロマトグラフィーの後に得た。分光分析データは、Papadopoulou et al. J. Med. Chem. 55:5554−5565 (2012)において以前に報告されたものと一致する。1H NMR (500 MHz, クロロホルム−d) δ 7.42−7.14 (m, 5H), 4.61 (d, J = 13.4 Hz, 1H), 4.14 (q, J = 21.9, 11.5 Hz, 2H), 3.89 (d, J = 13.5, 1H), 3.11 (td, J = 13.1, 2.7 Hz, 1H), 2.69−2.57 (m, 3H), 1.92−1.75 (m, 3H), 1.40−1.21 (m, 2H);HRMS−ESI (m/z) calculated for C14H19ClNO [M+H]:252.115;found:252.115。
N−(2−(1H−インドール−3−イル)エチル)−2−クロロアセトアミド(13)
基本手順Aに従い、トリプトアミン(400mg、2.5mmol、1当量)から出発して、所望の化合物を茶色がかった固形物(460mg、77%)としてカラムクロマトグラフィーの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 8.55 (s, 1H), 7.70 (d, J = 7.9 Hz, 1H), 7.45 (d, J = 8.1 Hz, 1H), 7.30 (t, J = 7.5 Hz, 1H), 7.23 (t, J = 7.4 Hz, 1H), 7.10 (s, 1H), 6.84 (s, 1H), 4.08 (s, 2H), 3.72 (q, J = 6.4 Hz, 2H), 3.10 (t, J = 6.8 Hz, 2H);HRMS−ESI (m/z) calculated for C12H14ClN2O2 [M+H]:237.0789;found:237.0791。
N−(3,5−ビス(トリフルオロメチル)フェニル)アクリルアミド(14)
基本手順Bに従い、3,5−ビス(トリフルオロメチル)アニリン(1.16g、5mmol、1当量)から出発して、所望の化合物を白色固形物(1.05g、74%)としてカラムクロマトグラフィーの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 8.33 (s, 1H), 8.18 (s, 2H), 7.68 (s, 1H), 6.57 (d, J = 17.5 Hz, 1H), 6.38 (dd, J = 16.9, 10.3 Hz, 1H), 5.93 (d, J = 12.5 Hz, 1H);HRMS−ESI (m/z) calculated for C11H8F6NO2 [M+H]:284.0505;found:284.0504。
N−(4−フェノキシ−3−(トリフルオロメチル)フェニル)−N−(ピリジン−3−イルメチル)アクリルアミド(15)
4−フェノキシ−3−(トリフルオロメチル)アニリン(260mg、1mmol、1当量)(Combi−Blocks)をTFA(5mL)中に溶解した。Boros et al. J. Org. Chem 74:3587−3590 (2009)により報告されたBorosらにより報告された還元的アミノ化のプロトコルに従い、反応混合物を0℃に冷却し、これにナトリウムトリアセトキシボロヒドリド(STAB)(270mg、1.3mmol、1.3当量)を加えた。3−ピリジンカルボキサルデヒド(200mg、2mmol、2当量)をCH2Cl2(5mL)中で溶解し、反応混合物へとゆっくり加えた。生成物への完全な変換後、反応物をCH2Cl2(20mL)で希釈し、飽和重炭酸ナトリウム溶液(3×20mL)で洗浄し、次いで有機質層を乾燥し、減圧下で濃縮した。更なる精製を必要とせず、粗製物を無水CH2Cl2中で溶解し、基本手順Bにさらした。結果として生じる粗製物を、分取TLCにより精製して、白色固形物(31mg、10%)を得た。1H NMR (500 MHz, クロロホルム−d) δ 8.52 (d, J = 3.5 Hz, 1H), 8.39 (s, 1H), 7.68 (d, J = 7.8 Hz, 1H), 7.40 (t, J = 7.7 Hz, 2H), 7.34 (s, 1H), 7.28−7.18 (m, 2H), 7.07 (d, J = 8.2 Hz, 2H),6.98 (d, J = 7.5 Hz, 1H), 6.82 (d, J = 8.8 Hz, 1H), 6.46 (d, J = 16.8 Hz, 1H), 6.01 (dd, J = 16.2, 10.7 Hz, 1H), 5.64 (d, J = 10.3 Hz, 1H), 4.96 (s, 2H)。HRMS−ESI (m/z) calculated for C22H18F3N2O2 [M+H]:399.1315;found:399.1315。
ヨードアセトアミド−ローダミン(16)
5−(及び−6)−((N−(5−アミノペンチル)アミノ)カルボニル)テトラメチルローダミン(テトラメチルローダミンカダベリン)を混合した異性体(60mg、0.12mmol、1当量)を、超音波処理により無水DMF(500μL)中で溶解した。これにDIPEA(60μL、0.34mmol、3当量)及びクロロアセチルクロリド(10μL、0.13mmol、1当量、DMF中で1:10に希釈)を加え、生成物への完全な変換をTLCにより検出するまで、反応物を室温で20分間撹拌した。DMFを窒素の流れの下で取り除き、反応混合物をMeOH:CH2Cl2:TEA(15:85:0.001)におけるPTLCにより分離した。その後、クロロアセトアミドローダミンをMeOH:CH2Cl2(15:85)の中で溶出し、減圧下で濃縮し、アセトン(500μL)の中で再溶解した。これにNaI(150mg、1mmol、10当量)を加え、生成物への完全な変換を検出するまで反応物を50℃で20分間撹拌し、粗製の反応混合物をC18カラム上での逆相HPLCにより精製し、濃縮して、5及び6のカルボキサミドテトラメチルローダミン異性体(比率〜6:1)(10mg、12%)の混合物である紫色の固形物として表題化合物を得た。1H NMR (600 MHz, メタノール−d4) δ 8.87 (t, J = 4.8 Hz, 0.14 H), 8.80−8.71 (m, 1H), 8.41 (dd, J = 8.2, 1.1 Hz, 0.86H), 8.35 (br s, 1H), 8.27 (dt, J = 7.9, 1.5 Hz, 0.164 H), 8.20 (dt, J = 8.2, 1.5 Hz, 0.86H),7.81 (s, 0.86H), 7.53 (d, J = 7.8 Hz, 0.14 H), 7.18−7.11 (m, 2H), 7.07 (d, J = 9.5 Hz, 2H), 7.00 (s, 2H), 3.68−3.62 (m, 2H), 3.46−3.37 (m, 2H), 3.31 (s, 12H, 溶媒により不明瞭にされる) 3.21−3.12 (m, 2H), 1.81−1.21 (m, 6H);HRMS−ESI (m/z) calculated for C32H36IN4O5 [M+H]:683.1725;found:683.1716。
N−(3,5−ビス(トリフルオロメチル)フェニル)アセトアミド(17)
基本手順Aに従い、3,5−ビス(トリフルオロメチル)アニリン(327mg、1.42mmol、1当量)及び無水酢酸(200μL、3mmol、2当量)から出発して、表題化合物を白色固形物(302mg、78%)としてPTLCの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 8.10 (s, 2H), 7.72 (s, 1H), 7.68 (s, 1H), 2.32 (d, J = 0.9 Hz, 3H)。HRMS−ESI (m/z) calculated for C11H8F6NO2 [M+H]:284.0505;found:284.0504。
18及び19の合成
3−アミノ−N−(hex−5−イン−1−イル)−(トリフルオロメチル)ベンズアミド(SI−5)
アセトニトリル(3.6mL、0.1Mの最終)中の3−アミノ−5−(トリフルオロメチル)安息香酸(74mg、0.36mmol)の溶液に、EDCI(83mg、1.2当量)、その後1−ヒドロキシベンゾトリアゾール水和物(HOBt、66.3mg、1.2当量)を加え、結果として生じる溶液を一晩撹拌した。反応物を酢酸エチルで希釈し、1MのHClで2回、次いでブラインで洗浄した。有機質層を硫酸マグネシウムで乾燥し、濃縮して、白色固形物としてアニリンSI−5(97.4mg、95%)を得た。1H NMR (400 MHz, クロロホルム−d) δ 7.29−7.22 (m, 2H), 6.98 (t, J = 1.8 Hz, 1H), 6.38 (t, J = 5.5 Hz, 1H), 4.08 (s, 2H), 3.46 (td, J = 7.1, 5.7 Hz, 2H), 2.25 (td, J = 6.9, 2.6 Hz, 2H), 1.99 (t, J = 2.7 Hz, 1H), 1.81−1.55 (m, 4H)。
3−アクリルアミド−N−(hex−5−イン−1−イル)−(トリフルオロメチル)ベンズアミド(18)
基本手順Bに従い、SI−5(42mg、0.15mmol、1当量)で出発して、表題化合物を白色固形物(34mg、70%)としてカラムクロマトグラフィーの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 8.94 (s, 1H), 8.24 (d, J = 11.9 Hz, 2H), 7.71 (s, 1H), 6.87 (t, J = 5.7 Hz, 1H), 6.55 (dd, J = 17.4, 0.7 Hz, 1H), 6.43 (dd, J = 16.9, 10.1 Hz, 1H), 5.88 (dd, J = 10.1,1.3 Hz, 1H), 3.56 (q, J = 6.7 Hz, 2H), 2.33 (td, J = 6.9, 2.7 Hz, 2H), 2.06 (t, J = 2.7 Hz, 1H), 1.87 (p, J = 7.3 Hz, 2H), 1.69 (p, J = 7.8 Hz, 2H);HRMS−ESI (m/z) calculated for C17H18F3N2O2 [M+H]:339.1314;found 339.1313。
3−アクリルアミド−N−(hex−5−イン−1−イル)−(トリフルオロメチル)ベンズアミド(19)
SI−5から出発して、基本手順A2に従い合成した。1H NMR (600 MHz, クロロホルム−d) δ 8.57 (s, 1H), 8.16 (t, J = 1.8 Hz, 1H), 8.05 (t, J = 1.8 Hz, 1H), 7.79 (d, J = 2.0 Hz, 1H), 6.38 (d, J = 6.1 Hz, 1H), 4.23 (s, 2H), 3.51 (td, J = 7.1, 5.7 Hz,2H), 2.27 (td, J = 6.9, 2.7 Hz, 2H), 2.00 (t, J = 2.6 Hz, 1H), 1.82−1.74 (m, 2H), 1.71−1.59 (m, 2H);HRMS−ESI (m/z) calculated for C16H17ClF3N2O2 [M+H]:361.0925;found:361.0925。
2−クロロ−1−(4−(ヒドロキシジフェニルメチル)ピペリジン−1−イル)エタン−1−オン(20)
基本手順Aに従い、α,α−ジフェニル−4−ピペリジノメタノール(800mg、3mmol、1当量)で出発して、表題化合物を白色固形物(637mg、61%)としてカラムクロマトグラフィーの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 7.56 (d, J = 7.6 Hz, 4H), 7.39 (q, J = 7.1 Hz, 4H), 7.28 (q, J = 6.8 Hz, 2H), 4.66 (d, J = 13.3 Hz, 1H), 4.07 (dd, J = 12.2, 4.2 Hz, 2H), 3.91 (d, J = 13.4 Hz,1H), 3.18 (t, J = 12.9 Hz, 1H), 2.77−2.62 (m, 3H), 1.67 (t, J = 12.5 Hz, 2H), 1.56 (q, J = 11.8 Hz, 1H), 1.44 (q, J = 12.4, 11.8 Hz, 1H);HRMS−ESI (m/z) calculated for C20H23ClNO2 [M+H]:344.1412;found:344.1412。
(E)−3−(3,5−ビス(トリフルオロメチル)フェニル)−2−シアノアクリルアミド(23)
3,5−ビス(トリフルオロメチル)ベンズアルデヒド(880mg、3.6mmol、1当量)及び2−シアノアセトアミド(460mg、5.5mmol、1.5当量)をMeOH(10mL)中で溶解した。これにピペリジン(214mg、0.7当量)を加え、反応物を室温で30分間撹拌し、その時点で出発物質を消耗させた。当量の水(10mL)の追加後、沈澱物を濾過により集め、水/メタノール(1:1)で洗浄し、白色固形物(534mg、47%)として表題化合物を得た。1H NMR (400 MHz, アセトン−d6) δ 8.78 (s, 2H), 8.61 (s, 1H), 8.41 (s, 1H), 7.57 (s, 1H), 7.42 (s, 1H);HRMS−ESI (m/z) calculated for C12H7F6N2O2 [M+H]:309.0457;found:309.0459。
N−(3,5−ビス(トリフルオロメチル)フェニル)−2−ブロモプロパンアミド(24)
基本手順A1に従い、3,5−ビス(トリフルオロメチル)アニリン(250mg、1.1mmol、1当量)及び2−ブロモプロピオニルクロリド(200μL、2mmol、1.8当量)から出発して、表題化合物を白色固形物(130mg、35%)としてPTLCの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 8.34 (s, 1H), 8.06 (s, 2H), 7.66 (s, 1H), 4.58 (q, J = 7.0 Hz, 1H), 1.98 (d, J = 7.0 Hz, 3H);HRMS−ESI (m/z) calculated for C11H7BrF6NO [M−H]:361.9621;found:361.9623。
N−(3,5−ビス(トリフルオロメチル)フェニル)−2−クロロプロパンアミド(25)
基本手順A1に従い、3,5−ビス(トリフルオロメチル)アニリン(327mg、1.42mmol、1当量)及び2−クロロプロピオニルクロリド(200μL、2mmol、1.8当量)から出発して、表題化合物を白色固形物(250mg、55%)としてPTLCの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 8.61 (s, 1H), 8.16 (s, 2H), 7.75 (s, 1H), 4.67 (q, J = 7.1 Hz, 1H), 1.93 (d, J = 7.1 Hz, 3H)。HRMS−ESI (m/z) calculated for C11H7ClF6NO [M−H]:318.0126;found:318.0126。
N−(3,5−ビス(トリフルオロメチル)フェニル)−N−(ピリジン−3−イルメチル)アクリルアミド(31)
3,5−ビス(トリフルオロメチル)アニリン(350mg、1.6mmol、1当量)をTFA(5mL)中で溶解した。反応混合物を0℃に冷却し、これにナトリウムトリアセトキシボロヒドリド(STAB)(400mg、2mmol、1.3当量)を加えた。3−ピリジンカルボキサルデヒド(244mg、2mmol、1当量)をCH2Cl2(5mL)中で溶解し、10分にわたり滴下で反応混合物へとゆっくり加えた。生成物への完全な変換後、反応混合物をCH2Cl2(20mL)で希釈し、飽和重炭酸ナトリウム溶液(3×20mL)で洗浄し、次いで有機質層を乾燥し、減圧下で濃縮した。更なる精製を必要とせず、粗製物を無水CH2Cl2中で溶解し、基本手順Bにさらした。結果として生じる粗製物をPTLCにより精製して、白色固形物(10mg、2%)を得た。1H NMR (500 MHz, クロロホルム−d) δ 8.63 (d, J = 3.8 Hz, 1H), 8.49 (s, 1H), 7.93 (s, 1H), 7.70 (d, J = 7.7 Hz, 1H), 7.55 (s, 2H), 7.35 (dd, J = 7.6, 5.3 Hz, 1H), 6.60 (dd, J = 16.6, 1.6 Hz, 1H), 6.02 (dd, J = 16.9, 10.2 Hz, 1H), 5.79 (dd, J = 10.3, 1.6 Hz, 1H), 5.11 (s, 2H)。HRMS−ESI (m/z) calculated for C17H13F6N2O [M+H]:375.0927;found:375.0928。
3−(2−クロロアセトアミド)−5−(トリフルオロメチル)安息香酸(36)
0℃で1.5mLのジメチルアセトアミド(1.6M)中のる3−アミノ−5−(トリフルオロメチル)安息香酸(500mg、2.44mmol)の溶液に、クロロアセチルクロリド(214μL、2.69mmol、1.1当量)を加えた。結果として生じる溶液を周囲温度に暖め、20分間撹拌し、その時点で酢酸エチル(40mL)及び水(30mL)を加えた。水層のpHを、1NのNaOHの追加によりpH10に調整し、相を分離した。水層を40mLの酢酸エチルで洗浄し、次いで1NのHClを加えることにより酸性化した。生成物を酢酸エチル(40mL)で抽出し、有機質層を1MのHCl(2×40mL)、ブライン(40mL)で洗浄し、硫酸マグネシウムで乾燥し、濃縮して所望の生成物(456mg、66%)を得た。1H NMR (500 MHz, クロロホルム−d) δ 8.31 (s, 1H), 8.27 (s, 1H), 8.14 (s, 1H), 4.13 (s, 2H);HRMS−ESI (m/z) calculated for C10H8ClF3NO3 [M+H]:282.0139;found:282.0141。
1−(4−(5−フルオロベンズイソキサゾール−3−イル)ピペリジン−1−イル)prop−2−エン−1−オン(37)
基本手順Cに従い、6−フルオロ−3(4−ピペリジニル)−1,2−ベンズイソキサゾール塩酸塩(53mg、0.2mmol、1当量)から出発して、表題化合物を無色の油(49.1mg、87%)として得た。1H NMR (400 MHz, クロロホルム−d) δ 7.64 (dd, J = 8.7, 5.1 Hz, 1H), 7.27 (dd, J = 8.4, 2.3 Hz, 1H), 7.08 (td, J = 8.9, 2.1 Hz, 1H), 6.64 (dd, J = 16.8, 10.6 Hz, 1H), 6.32 (dd, J = 16.9, 1.9 Hz, 1H), 5.73 (dd,J = 10.6, 1.9 Hz, 1H), 4.70 (d, J = 13.4 Hz, 1H), 4.15 (d, J = 12.4 Hz, 1H), 3.53−3.13 (m, 2H), 2.99 (t, J = 13.1 Hz, 1H), 2.25−2.07 (m, 2H), 2.00 (ddd, J = 23.1, 14.2, 7.8 Hz, 2H);HRMS−ESI (m/z) calculated for C15H16FN2O [M+H]:275.119;found:275.119。
tert−ブチル4−(4−アクリルアミド−2,6−ジフルオロフェニル)ピペラジン−1−カルボン酸塩(38)
基本手順Bに従い、tert−ブチル4−(4−アミノ−2,6−ジフルオロフェニル)ピペラジン−1−カルボン酸塩から出発して、表題化合物を得た。1H NMR (400 MHz, クロロホルム−d) δ 8.12 (s, 1H), 7.13 (d, J = 10.4 Hz, 2H), 6.36 (d, J = 16.9 Hz, 1H), 6.19 (dd, J = 16.8, 10.2 Hz, 1H),5.70 (d, J = 10.2 Hz, 1H), 3.45 (t, J = 4.7 Hz, 4H), 3.00 (t, J = 3.7 Hz, 4H), 1.41 (s, 9H);HRMS−ESI (m/z) calculated for C18H24F2N3O3 [M+H]:368.178;found:368.178。
N−(4−ブロモ−2,5−ジメチルフェニル)アクリルアミド(40)
基本手順Bに従い、4−ブロモ−2,5−ジメチルアニリン(900mg、4.5mmol、1当量)から出発して、表題化合物を白色固形物(611mg、40%)として、カラムクロマトグラフィー及び冷たいCH2Cl2からの再結晶化の後に得た。1H NMR (500 MHz, クロロホルム−d) δ 7.87 (s, 1H), 7.43 (s, 1H), 7.16 (s, 1H), 6.50 (d, J = 16.7 Hz, 1H), 6.35 (dd, J = 16.4, 10.3 Hz, 1H), 5.86 (d, J = 10.3 Hz, 1H), 2.42 (s, 3H), 2.28 (s, 3H);HRMS−ESI (m/z) calculated for C11H13BrNO [M+H]:254.0175;found:254.0175。
2−クロロアセトアミド−2−デオキシ−α/β−D−グルコピラノース(44)
室温で無水MeOH(200mL)中のヘキソサミン塩酸塩(590mg、3.39mmol、1当量)の撹拌溶液に、ナトリウム金属(60mg、2.6mmol、0.78当量)、TEA(400μL、5.7mmol、1.8当量)を加えた。その後、クロロ酢酸無水物(1g、5.9mmol、1当量)を加え、混合物を6時間撹拌し、TLCにより完全性についてモニタリングした。その後、反応混合物を真空内で濃縮した。その後、粗製生成物を2回のカラムクロマトグラフィーにより精製して、白色固形物(610mg、72%)として純粋な表題生成物を得た。1H NMR (500 MHz, メタノール−d4) δ 5.20 (d, J = 3.7 Hz, 1Hα), 4.75 (d, J = 8.3 Hz, 1Hβ), 4.19 (dd, J = 20.2, 13.9 Hz, 2H), 4.19 (d, J = 12.6 Hz, 1H), 3.95 (dd, J = 10.6, 3.5 Hz, 1Hα), 3.83 (m, 3Hα, 3Hβ),3.74 (d, J = 5.1 Hz, 1Hβ), 3.70 (dd, J = 11.4, 8.9 Hz, 1Hβ), 3.60 (dd, J = 10.7, 9.5 Hz, 1Hβ), 3.46 (t, J = 9.3 Hz, 1H), 3.42 (t, J = 10.0 Hz, 1Hβ);HRMS−ESI (m/z) calculated for C8H15ClNO6 [M+H]:256.0582;found:256.0582。
2−クロロ−1−(2−メチル−3,4−ジヒドロキノリン−1(2H)−イル)エタン−1−オン(45)
クロロアセチルクロリド(80.4μL、0.9mmol、1.7当量)を、無水CH2Cl2(3mL)中で溶解し、0℃に冷却した。その後、CH2Cl2(2mL)中の2−メチル−1,2,3,4−テトラヒドロキノリン(80.1mg、0.544mmol、1当量)及びN−メチルモルホリン(0.11mL、1.0mmol、1.8当量)の溶液を、滴下で加えた。6時間後、反応物を飽和水性NaHCO3(5mL)でクエンチし、CH2Cl2(3×10mL)で抽出した。組み合わせた有機質層を無水Na2SO4で乾燥し、減圧下で濃縮した。結果として生じる残留物を分取TLC(30%のEtOAc/ヘキサン)により生成して、オフホワイトの固形物(108.8mg、89%)として表題化合物を得た。1H NMR (400 MHz, クロロホルム−d) δ 7.30−7.13 (m, 4H), 4.86−4.75 (m, 1H), 4.20 (d, J = 12.5 Hz, 1H), 4.09 (d, J = 12.5 Hz, 1H), 2.69−2.58 (m, 1H), 2.59−2.46 (m, 1H), 2.46−2.31 (m, 1H), 1.36−1.29 (m, 1H), 1.15 (d, J = 6.5 Hz, 3H);HRMS−ESI (m/z) calculated for C12H15ClNO [M+H]:224.0837;found:224.0836。
N−シクロヘキシル−N−フェニルアクリルアミド(46)
N−シクロへキシルアニリン(89.5mg、0.511mmol、1当量)から、基本手順Cに従い表題化合物を合成した。フラッシュカラムクロマトグラフィー(10−20%のEtOAc/ヘキサン)、その後分取TLC(30%のEtOAc/ヘキサン)による粗製生成物の精製により、オフホワイトの固形物(53.1mg、45%)として表題化合物を得た。1H NMR (400 MHz, クロロホルム−d) δ 7.42−7.33 (m, 3H), 7.10−7.06 (m, 2H), 6.31 (dd, J = 16.7, 2.1 Hz, 1H), 5.77 (dd, J = 16.7, 10.3 Hz, 1H), 5.41 (dd, J = 10.4, 2.1 Hz, 1H), 4.65 (tt, J = 12.2, 3.7 Hz,1H), 1.85 (dt, J = 11.2, 1.8 Hz, 2H), 1.75−1.68 (m, 2H), 1.61−1.53 (m, 1H), 1.40 (qt, J = 13.3, 3.6 Hz, 2H), 1.07 (qd, J = 12.4, 3.6 Hz, 2H), 0.91 (qt, J = 13.1, 3.8 Hz, 1H);HRMS−ESI (m/z) calculated for C15H20NO [M+H]:230.1539;found:230.1539。
1−(5−ブロモインドリン−1−イル)prop−2−エン−1−オン(47)
5−ブロモインドリン(41.7mg、0.211mmol、1当量)、アクリロイルクロリド(32μL、0.40mmol、1.9当量)から、基本手順Cに従い、且つ塩基をピリジン(32μL、0.40mmol、1.9当量)に変更して、表題化合物を合成した。EtOAcからの再沈殿による粗製生成物の精製によって、白色固形物(67.8mg、64%)として表題化合物を得た。1H NMR (400 MHz, クロロホルム−d) δ 8.16 (d, J = 8.6 Hz, 1H), 7.33−7.25 (m, 2H), 6.60−6.42 (m, 2H), 5.84−5.76 (m, 1H), 4.15 (t, J = 8.6 Hz, 2H), 3.17 (t, J = 8.6 Hz, 2H);HRMS−ESI (m/z) calculated for C11H11BrNO [M+H]:252.0018;found:252.0017。
N−(1−ベンジルピペリジン−4−イル)−N−フェニルアクリルアミド(48)
1−ベンジル−N−フェニルピペリジン−4−アミン(30.0mg、0.113mmol、1当量)、アクリロイルクロリド(17μL、0.21mmol、1.9当量)から、基本手順Cに従い、且つ塩基をピリジン(17μL、0.21mmol、1.9当量)に変更して、表題化合物を合成した。分取TLCによる粗製生成物の精製によって、白色固形物(22.5mg、64%)として表題化合物を得た。1H NMR (400 MHz, クロロホルム−d) δ 7.62−7.56 (m, 2H), 7.43−7.36 (m, 6H), 7.05 (d, J = 6.2 Hz, 2H), 6.29 (dd, J = 16.8, 2.1 Hz, 1H), 5.79 (dd, J = 16.8, 10.3 Hz, 1H), 5.46 (dd, J = 10.3, 2.1 Hz, 1H),4.81−4.70 (m, 1H), 4.09 (s, 2H), 3.41 (d, J = 12.0 Hz, 2H), 2.82 (q, J = 11.5 Hz, 2H), 2.21 (q, J = 11.9 Hz, 2H), 1.94 (d, J = 14.2 Hz, 2H);HRMS−ESI (m/z) calculated for C21H25N2O [M+H]:321.1961;found:321.1962。
2−クロロ−N−(2−メチル−5−(トリフルオロメチル)フェニル)アセトアミド(49)
2−メチル−5−(トリフルオロメチル)アニリン(35.0mg、0.2mmol、1当量)から、基本手順A1に従い表題化合物を合成した。分取TLC(20%のEtOAc/ヘキサン)による粗製生成物の精製によって、白色固形物(48.2mg、95%)として表題化合物を得た。1H NMR (600 MHz, クロロホルム−d) δ 8.31 (s, 1H), 8.25 (d, J = 1.9 Hz, 1H), 7.37 (dd, J = 7.9, 1.8 Hz, 1H), 7.32 (d, J = 7.9 Hz, 1H), 4.25 (s, 2H), 2.36 (s, 3H);HRMS−ESI calculated for C10H10ClF3NO [M+H]:252.0397;found:252.0397。
1−(5−ブロモインドリン−1−イル)−2−クロロエタン−1−オン(50)
5−ブロモインドリン(39.6mg、0.2mmol、1当量)から、表題化合物を基本手順A1に従い合成した。分取TLC(25%のEtOAc/ヘキサン)による粗製生成物の精製によって、オフホワイトの固形物(48.6mg、89%)として表題化合物を得た。1H NMR (600 MHz, CDCl3) δ 8.07 (d, J = 8.4 Hz, 1H), 7.32 (d, J = 8.8 Hz, 2H), 4.17 (t, J = 8.6 Hz, 2H), 4.14 (s, 2H), 3.22 (t, J = 8.4 Hz, 2H);HRMS−ESI (m/z) calculated for C10H10BrClNO [M+H]:273.9629;found:273.9629。
2−クロロ−N−(キノリン−5−イル)アセトアミド(51)
0℃で無水CH2Cl2(3mL)中の、5−アミノキノリン(28.8mg、0.2mmol、1当量)及び炭酸カリウム(82.9mg、0.6mmol、3当量)の撹拌懸濁液に、クロロアセチルクロリド(24μL、1.5の当量)を加えた。反応物を室温にまでゆっくりと暖めた。3時間後、混合物を濾過し、EtOAc(10mL)及びCH2Cl2(10mL)で洗浄した。その後、固形のケーキをMeOH(20mL)で溶出し、濾液を真空内で濃縮した。残留物を10%のMeOH/CH2Cl2の中で取り上げ、シリカのパッドに通して、オフホワイトの固形物(42.6mg、82%)として表題化合物を得た。1H NMR (500 MHz, CDCl3) δ 8.96 (d, J = 2.5 Hz, 1H), 8.71 (s, 1H), 8.20 (d, J = 8.6 Hz, 1H), 8.04 (d, J = 8.5 Hz, 1H), 7.94 (d, J = 7.5 Hz, 1H), 7.74 (t, J = 8.0 Hz, 1H), 7.48 (dd, J = 8.5, 4.2 Hz, 1H), 4.35 (s, 2H);HRMS−ESI (m/z) calculated for C11H9ClN2O [M+H]:221.0476;found:221.0477。
1−(4−ベンジルピペリジン−1−イル)prop−2−エン−1−オン(53)
基本手順Bに従い、4−ベンジルピペリジン(1g、5.7mmol、1当量)から出発して、表題化合物を黄色の油(748mg、57%)としてカラムクロマトグラフィーの後に得た。1H NMR (500 MHz, クロロホルム−d) δ 7.36 (t, J = 7.4 Hz, 2H), 7.28 (t, J = 7.4 Hz, 1H), 7.20 (d, J = 7.1 Hz, 2H), 6.64 (dd, J = 16.8, 10.6 Hz, 1H), 6.32 (dd, J = 16.8, 1.9 Hz, 1H), 5.72 (dd, J = 10.6,1.9 Hz, 1H), 4.72 (d, J = 12.7 Hz, 1H), 4.03 (d, J = 13.0 Hz, 1H), 3.05 (t, J = 12.7 Hz, 1H), 2.70−2.59 (m, 3H), 1.86 (ddp, J = 14.6, 7.2, 3.5 Hz, 1H), 1.77 (m, 2H), 1.37−1.18 (m, 2H);HRMS−ESI (m/z) calculated for C15H20ClNO [M+H]:230.1539;found:230.1539。
2−クロロ−N−((3−ヒドロキシ−5−(ヒドロキシメチル)−2−メチルピリジン−4−イル)メチル)アセトアミド(54)
室温で無水MeOH(20mL)中のピリドキサミン塩酸塩(150mg、0.64mmol、1当量)の撹拌溶液に、ナトリウム金属(30mg、1.5mmol、2.3当量)、TEA(100μL、1mmol、1.6当量)を加えた。クロロ酢酸無水物(390mg、2.29mmol、3.5当量)を加え、混合物を6時間撹拌し、TLCにより完全性についてモニタリングした。その後、反応混合物を真空内で濃縮した。その後、粗製生成物を分取TLCにより精製して、白色固形物(46mg、30%)として表題化合物を得た。1H NMR (500 MHz, メタノール−d4) δ 7.97 (s, 1H), 4.81 (s, 2H), 4.61 (s, 2H), 4.17 (s, 3H), 4.06 (s, 1H), 3.35 (s, 1H), 2.52 (s, 3H);HRMS−ESI (m/z) calculated for C10H14ClN2O3 [M+H]:245.0687;found:245.0688。
1−(6,7−ジメトキシ−3,4−ジヒドロイソキノリン−2(1H)−イル)prop−2−エン−1−オン(56)
0℃で無水THF(10mL)中の6,7−ジメトキシ−3,4−ジヒドロイソキノリン(1g、5.2mmol、1当量)及びTEA(1800μL、12.6mmol、2.5当量)の撹拌懸濁液に、アクリロイルクロリド(1320μL、13.2mmol、2.6当量)を加え、反応物を室温にまでゆっくり暖めた。2時間後、混合物をCH2Cl2(2×50mL)で希釈し、飽和ブライン(2×50mL)で洗浄し、組み合わせた有機物を真空内で濃縮した。残留物を10%のMeOH/CH2Cl2の中で取り上げ、カラムクロマトグラフィーにより精製して、白色固形物(700mg、54%、E/Z異性体の混合物)として表題化合物を得た。1H NMR (500 MHz, クロロホルム−d) δ 6.63 (m, 3H), 6.29 (d, J = 16.8 Hz, 1H), 5.69 (dd, J = 10.6, 1.8 Hz, 1H), 4.69 (s, 1H [major]), 4.63 (s, 0.8H [minor]), 3.82 (s, 7H), 3.73 (t, J = 5.6 Hz, 1H), 2.84−2.77 (m, 2H);HRMS−ESI (m/z) calculated for C14H18NO3 [M+H]:248.128;found:248.1281。
2−クロロ−N−(1−(3−エチニルベンゾイル)ピペリジン−4−イル)−N−フェニルアセトアミド(61)
過剰量のきれいなSI−3に、0.7mLのトリフルオロ酢酸(0.2M)を加えた。これ以上蒸発が観察されなくなるまで結果として生じる溶液を窒素の流れの下で濃縮し、そのトリフルオロ酢酸塩として脱保護されたアミンを得た。トリフルオロアセテートアミン塩(90.6mg、0.25mmol)をDMF(0.5mL、0.5M)の中で取り上げ、結果として生じる溶液を0℃に冷却した。3−エチニル安息香酸(44mg、1.2当量)、HATU(113mg、1.2当量)、及びヒューニッヒ塩基(86μL、2当量)を連続で加えた。反応物を0℃で2時間撹拌し、Et2Oで希釈し、次いで1MのHClで洗浄した。有機質層を硫酸マグネシウムで乾燥し、濃縮し、フラッシュクロマトグラフィー(ヘキサン中で40から70%の酢酸エチルの勾配)により精製して、表題化合物(87mg、92%)を得た。1H NMR (400 MHz, クロロホルム−d) δ 7.51 (dd, J = 9.5, 5.4 Hz, 4H), 7.43 (d, J = 1.9 Hz, 1H), 7.39−7.25 (m, 2H), 7.14 (d, J = 10.4 Hz, 2H), 4.86 (tt, J = 15.1, 5.3 Hz, 2H), 3.72 (s, 3H), 3.19 (d,J = 14.0 Hz, 1H), 3.11 (s, 1H), 2.86 (s, 1H), 1.90 (d, J = 36.6 Hz, 2H), 1.38 (s, 1H), 1.24 (d, J = 19.9 Hz, 1H);HRMS−ESI (m/z) calculated for C22H22ClN2O2 [M+H]:381.1364;found:381.1363。
未変性の集団におけるシステインに反応的な断片の全体的なプロファイリング
システインは、その高い求核性、及び酸化的修飾に対する感度に起因して、タンパク質をコードするアミノ酸の中で固有なものである。システイン残基は、多様な酵素の分類において触媒機能を実行し、ジスルフィド結合、鉄−硫黄のクラスター形成、スルフィン酸及びスルホン酸への変換、ニトロシル化、S−グルタチオン化、及び脂質修飾を通じたタンパク質の翻訳後の調節のための部位を表わす。isoTOP−ABPP(isotopic Tandem Orthogonal Proteolysis−Activity−Based Protein Profiling)と称される、定量的で化学的なプロテオミクス方法を使用して、システイン残基の固有の反応の全体的な測定を行い、脂質由来の求電子による修飾に対するそれらの感度を評価した。isoTOP−ABPPが、未変性の生物系における共有結合性のFBLDを実行するように適合されるかどうかを判定するために、細胞調製物(溶解物又は無傷細胞)を、DMSO、又は求電子性の小分子断片のライブラリーの一員で予め処理し、次に、広域スペクトルのシステイン反応性プローブヨードアセトアミド(IA)−アルキン1にさらした(図1A)。DMSO及び断片で処理したサンプルからのIA−アルキンで標識されたシステイン残基を持つタンパク質を、同位体的に分化されたアジド−ビオチンのタグ(それぞれ重及び軽)へと、銅触媒のアジド−アルキンの環化付加(CuAAC又はクリック)の化学により結合させ、組み合わせ、ストレプトアビジンにより富化し、ビーズ上でタンパク分解性に消化して、LC−MSにより分析された同位体のペプチド対を得た。ペプチド対のためのMS1クロマトグラフィーのピーク比の定量化は、DMSO/断片の比較において、断片競合化(fragment−competed)システイン残基を、高い競合比率又はR値を表示するものであると確認した。
50+のメンバーの断片ライブラリーを、クロルアセトアミド又はアクリルアミドの求電子(図1B及び図3)の何れかを含む大半の化合物で構築され、これらは、多くの化学プローブ及び一部の臨床的に承認された薬物に見出される、十分に特徴づけられたシステインに反応的な群である。これらの求電子を、ヒトのプロテオームの異なる亜群との相互作用を促進する認識要素として機能するように意図される、構造上多様な小分子断片(<300da)に付加した。ライブラリーはまた、シアノアクリルアミド及びビニルスルホンアミドなどの幾つか追加の求電子、並びに、既知の生物活性の求電子性化合物(例えば、抗癌剤であるピペルロングミン(piperlongumine)及び抗遊走性薬剤(anti−migratory agent)であるロコスタチン(locostatin))を含んでいた(図1B及び図3)。求電子ライブラリーを、典型的なFBLD実験に使用されるリガンド濃度に匹敵する高濃度(500μM)でスクリーンした。断片ライブラリーの亜群を、IA−ローダミンプローブ16を使用して、ヒトMDA−MB−231乳癌細胞株プロテオームにおける競合的なプロファイリングにより最初に分析して、システイン反応事象の容易なSDS−PAGE検出を可能にした。この実験は、1つ以上の断片の存在下でのIA−ローダミンの標識化の減少を示した、様々なタンパク質を同定した(図1C、アスタリスク)。興味深いことに、タンパク質は、試験断片のセットにわたって別個のSARを示し、このことは、ライブラリーの認識要素が特異的な断片−タンパク質反応性事象に対し強い影響を及ぼすことを示している。
競合的なisoTOP−ABPPを使用して、断片求電子により標的とされるこれらタンパク質内でヒトタンパク質及びシステイン残基を大域的にマッピングした。各断片を、通常、2つの別個のヒト癌細胞プロテオーム(MDA−MB−231及びRamos細胞)に対して試験し、大半の断片を、これらプロテオームの少なくとも1つに対して2通りにスクリーンした。平均で、927のシステインを1つのデータセットごとに定量化し、個々のシステインを説明のために少なくとも3つのデータセットにおいて定量化することを要求した。これらの標準に基づいて、2885のタンパク質から6157を超えるシステインを、1つのシステイン当たり22のデータセットの平均定量化周波数を持つ全てのデータセットにわたり集合体の中で定量化した(図4A)。断片競合的なシステイン残基、又は「リガンド結合された」システインを、IA−アルキン標識化において≧75%の減少を示すものとして定めた(DMSO/断片についてR値≧4)。偽陽性の可能性を最小限にするために、2つ以上のデータセットにおいてR値≧4を示し、且つデータ品質管理の追加の基準を満たしたシステインのみを、断片求電子の標的と見なした。その後、個々の断片のプロテオミクス反応値、又はリガンド結合したシステインの割合を、その断片上で実行されるisoTOP−ABPP実験におけるリガンド結合した/合計の定量化したシステインのパーセンテージとして計算した。
大半の断片求電子は、ライブラリーについて3.8%の中央のリガンド結合したシステインの割合で、ヒトプロテオームにわたり調節された反応を示した(図4B)。しかし、反応における実質的な差異を観察し、個々の求電子は<0.1%のリガンド結合したシステインの割合を示し、その他は>15%の割合を表示した(図4B)。ピペルロングミン及びロコスタチンが後者の分類へと分けられることは、断片求電子の固有のプロテオミクス反応が通常、前述の求電子性プローブのものを超過しなかったことを示した。断片の亜群をまた、より低い濃度(25−50μM)でスクリーンし、これにより、それらのプロテオミクス反応が濃度依存性であることを確認した(図4C)。断片求電子の相対反応性は、MDA−MB−231及びRamos細胞のプロテオームにおいて同様であり(図4D)、このことは、このパラメータが化合物の固有特性であることを示している。生物学的な複製の実験で分析した時、断片は一貫した反応特性も示した(図4E)。興味深いことに、断片求電子のプロテオミクス反応は、タンパク質性のシステイン反応の測定のための、共通して使用される代用アッセイである、それらのグルタチオンの内転(adduction)の可能性と僅かにしか関連していないことが分かった(図4F)。このような差は、断片求電子の認識要素の、それらの相互作用、及び最終的にタンパク質との反応性に対する影響に起因する。
断片3、14、17、及び23−26の比較は、共通の認識要素(3,5−ジ(トリフルオロメチル)フェニル基)に結合される異なる求電子性の基の相対的なプロテオミクス反応への見識をもたらした。クロロアセトアミド3は、アクリルアミド14よりも大きな反応を示し(それぞれ、15%対3.4%のリガンド結合したシステイン;図1D)、シアノアクリルアミド23は、アクリルアミド14及びその他に対する同様の反応を示し、より立体的に充満した求電子(24−26)はプロテオミクス反応の減少を示している(図4G)。重要なことに、非求電子性のアセトアミド対照の断片17は、競合的なisoTOP−ABPP実験においてごくわずかな活性を示し(リガンド結合したシステインの割合<0.2%)、このことは、検出された断片−システイン相互作用の大部分が共有結合反応対非共有結合事象を反映したことを示している(図1D)。また、この結論の支持において、3及び14(それぞれ化合物19及び18)の「クリック可能な」アルキンアナログは、競合的なisoTOP−ABPP実験において3及び14により表示されるそれぞれのリガンド結合したシステインの割合を映す(3>14;図1D)、異なる濃度依存性のプロテオーム標識化特性(19>18;図1E)を示した。アクリルアミド14及びシアノアクリルアミド23に対するクロロアセトアミド3のより大きな全体的なプロテオミクス反応にもかかわらず、システインの明確な例は、後者の断片により優先的にリガンド結合されたことが分かった(図1F)。
幾つかの例において、これらの発見により、isoTOP−ABPPのプラットフォームは、未変性のプロテオームにおける数千のシステイン残基に対して断片求電子の特性を競合的に明らかにするための使用のための1つの方法であることが、実証された。
未変性のプロテオームにおける断片求電子により標的とされるシステイン
組み合わせた全てのisoTOP−ABPPのデータセットにわたり、758のリガンド結合したシステインを、それぞれ合計の定量化されたシステイン及びタンパク質の〜12及び22%に相当する637の別個のタンパク質上で同定した(図5A及び表1−3)。リガンド結合したシステインを持つタンパク質の適度の断片のみがDrugBankのデータベースにおいて見出され(15%;図5B)、このことは、断片求電子が小分子プローブを欠く多くのタンパク質を標的としたことを示している。既知の共有結合のリガンドを持つタンパク質標的の中で、断片求電子は頻繁に、このような既知のリガンドと同じシステイン残基を標的とし(表4);例として、求電子性断片が制癌剤であるイブルチニブとも反応する活性部位システインを標的としたタンパク質キナーゼBTK、及び、求電子性断片が生物活性の天然の生成物及び候補の抗癌剤により修飾される保存されたシステインを標的としたXPO1とERCC3が、挙げられる。BTKの場合、このキナーゼとのイブルチニブの相互作用が、Ramos細胞溶解物において既知のイブルチニブオフターゲット−MAP2K7−も同定した、isoTOP−ABPPにより検出されたことを確認した(図7A)。
リガンド結合したシステインを含むDrugBankのタンパク質の大半は、酵素、チャネル、及び輸送体を含む、「ドラッガブル」と見なされる分類から生じた(図5C)。他方、リガンド結合したシステインを含む非DrugBankのタンパク質は、小分子リガンドで標的を負荷すると考慮される、転写因子及びアダプター/スキャフォールディングタンパク質などのタンパク質を含んでいた、より広範囲の分類の分布を示した(図5C)。断片求電子により標的とされた酵素の中でさえ、リガンド結合したシステインが非活性部位の残基であった多くの例が、注目された(図7B)。これらのデータは、断片求電子により修飾されるシステインがタンパク質上の古典的なリガンド結合ポケットに制限されないことを示した。また、この前提と一貫して、リガンド結合したシステインの全てのうち〜6%のみを、活性部位残基として機能的に注釈した(図5D)。しかし、活性部位システインに加え、レドックス活性システインも、isoTOP−ABPPにより定量化されるリガンド結合されていないシステインと比較して、リガンド結合したシステイン基の中で実質的に豊富であった(図5D)。活性部位及びレドックス活性のシステインが通常、他のシステインと比較してより大きな固有の反応性(IA−アルキンプローブで測定されるような)も示すことが、以前に分かっている。断片求電子の標的として検出された過反応性システインの高い比率で反映されるように(図5E)、この増大した反応性はシステインのリガンド結合可能性に寄与する可能性の高い要因である一方、リガンド結合したシステインはまた、広範囲の固有の反応性にわたり十分に表示される(図5E)。最終的に、大半のタンパク質は、平均でisoTOP−ABPPにより1つのタンパク質ごとに定量化された様々なシステインの中で単一のリガンド結合したシステインを持つことが分かった。核外輸送因子XPO1及び代謝性酵素PHGDHは、タンパク質内の個々のシステインのための断片求電子により表示された選択性の説得力のある例を提供する(図5G及び図7C)。isoTOP−ABPPにより定量化される6つの異なるXPO1システイン残基の中で、単一のシステインとしてC528は頻繁に断片求電子により標的とされ(図5G)、この残基はまた、癌40のための臨床開発における求電子性の薬物により修飾される。同様に、PHGDHにおける8つの定量化されたシステインの中で、C369、非活性部位残基のみが、求電子性断片により標的とされた(図7C)。
リガンド結合したシステインは、断片求電子ライブラリーで著しく異なるSARを表示した(図6A及び表1−3)。少数のシステインは多数の断片(>50%)により標的とされたが、大半のシステインは更に制限された反応性を示した(図6A、B、及び表1−3)。断片求電子の、それらの相対的なプロテオミクス反応値(群A、>10%;群B、<10%)に基づいた操作上のグループ化は、システイン−求電子の相互作用の認識及び反応性の成分の両方を強調したSARの特徴を明らかにした。例えば、特定のシステインは、あまり反応性でない(群B)断片(例えば、GLRX5;MSTO1;SRP9;UCHL3;図6A)と優先的に相互作用し、一方でその他は、最も反応的な(群A)断片(例えば、ATXN7L3B;CRKL;C2ORF49;図6A)により主にリガンド結合されるが、このような場合でさえ、相互作用は群Aの断片にわたり実質的に異なっていた。タンパク質の活性部位にあるリガンド結合したシステインは、他のシステインと比較して断片求電子とのより広範囲の反応を示す傾向があり(図6C)、このことは恐らく、それらのより大きなリガンド結合可能性を反映しているが、明らかなSARが多くの非活性部位システインについて観察され、これら残基が群Aの断片により不釣り合いに標的とされなかった(図6D)。異なるタンパク質の分類にわたり適用されるこのような原理は、キナーゼにおいて十分に例証され、そのため、活性及び非活性部位の残基間でほぼ均一に分布した、>20のリガンド結合したシステインが同定された(図7D−F)。転写因子/制御因子などの、薬物に対する負荷と考慮されるタンパク質中に見出されるシステインでさえ、結合性及び反応性の両方に関与する明瞭な相互作用を示す、異なるSARを示した(図6D及び図9G)。加えて、リガンド結合したシステインの60%より多くについて、求電子(IA−アルキン又は断片)反応性をプロテオームの熱変性により遮断し、その一方で、リガンド結合されていないシステインの画分(約20%)について、熱変性後にIA−アルキン標識化の減少を示した(図15及び16)。幾つかの例において、これらの結果により、リガンド−システインの相互作用は、タンパク質中のリガンド及び構造化された部位の群の両方に依存するという点で特異的であることが、示された。
リガンド結合したシステインを持つタンパク質の亜群の三次元構造の利用可能性は、ドッキングが断片求電子反応性の部位を予測するかどうかを試験する機会をもたらした。共有結合性のドッキングプログラムが近年、タンパク質中で予め特定されたシステインを標的とするリガンドを発見するように導入され;しかし、ここでの目的は、タンパク質内の全てのシステインの相対的なリガンド結合可能性を計算的に評価し、isoTOP−ABPP実験で獲得したデータにこれらの出力を一致させることであった。先ず、29の典型的なタンパク質標的を走査し、99の溶媒露出のシステインを同定した。その後、断片求電子ライブラリーを、アルキル化事象に先行する非共有結合性の相互作用をシミュレートするために修飾された電位(potential)を独立して使用して、各残基上でドッキングした。断片求電子が好ましくはシステインの付近で結合され、且つ反応基がシステインの共有結合距離内にあった場合、システインは断片により修飾されると考慮された。その後、ドッキングスコアを、そのドッキングされたポーズにおける各断片の推定された相互作用エネルギーに基づいて計算し、これら予測の順位付けは、29のシステムのうち19のシステムにおける実験データと一致した(即ち、上位の予測されたリガンド結合可能なシステインが、isoTOP−ABPPにより判定されるリガンド結合したシステインに一致する場合)(図6E、F、及び表5)。残りの10のシステムのうち6つにおいて、リガンド結合したシステインを、反応的なドッキングにより2番目に順位を付けた。残りの4つのシステムにおいて、反応的なドッキングは、使用されるモデルにおけるドッキングのスコア付けの機能又は構造的な問題における制限が原因で、リガンド結合したシステインを予測することはできなかった。著しいことに、反応的なドッキングにより評価される29のタンパク質全体にわたり、リガンド結合可能であると予測されるシステインは、リガンド結合可能でないと予測されるシステインと比べて、isoTOP−ABPPにより検出される可能性が非常に高いことが分かった(図6E及び図7H)。また、リガンド結合可能であると予測されるシステインは、isoTOP−ABPPにより検出された可能性が高く、感熱性のIA−アルキン反応性を示したことも、分かった(図17A及び図17B)。これらの結果により、反応的なドッキングは、タンパク質性のシステインのリガンド結合可能性の優れた全体的な予測をもたらスことが示され、且つ、IA−アルキン反応性自体がタンパク質中で潜在的にリガンド結合可能なシステインを指定するのに有用な独立した実験パラメータを提供することが示唆された。
リガンド−システインの相互作用の機能分析
次の工程は、組換え型タンパク質を使用するisoTOP−ABPPによりマッピングされたリガンド−システインの相互作用の機能的な影響を確認且つ判定することであった。リガンド結合したシステインの機能的な有意性が以前に実証された、2つのタンパク質を選択した。タンパク質メチルトランスフェラーゼPRMT1は、4−ヒドロキシノネナール(HNE)のような求電子性の小分子により修飾された時、PRMT1活性27の阻害を結果としてもたらす、非触媒性の活性部位システイン(C109)を持つ。競合的なisoTOP−ABPPは、PRMT1のC109のリガンド結合のための非常に選択的なSARを明らかにし、3つの断片(2、11、及び51)だけが、この残基のIA−アルキン標識化を遮断した(図6A及び図8A及び表1−3)。PRMT1における様々な追加のシステインをisoTOP−ABPP実験において定量化したとしても(いずれも試験された断片求電子に対する感度を示さなかった;図8A及び表1−3)、組換え型PRMT1のIA−ローダミン標識化はセリンへのC109の突然変異により遮断されたことが分かった(図8B)。これらのデータは、C109がPRMT1において最も反応性のシステインであり、且つ低濃度の求電子性プローブにより選択的に標識されることを示す、過去の研究と一貫している。都合のよいSDS−PAGEの読み出しを使用して、断片11が、36μMのIC50値を持つPRMT1のIA−ローダミン標識化を遮断した一方で、11に対する同様の全体的なプロテオーム反応性を示すにも関わらず(図4B)、対照の断片3は不活性であった(図8B、C)ことを確認した。3ではなく11での前処理はまた、C109に依存した方式でヒストン4のPRMT1で触媒されるメチル化を阻害した(図8D)。これらのデータは、C109を標的とするその求電子性リガンドがPRMT1阻害剤として作用することを示す。
その後、酸化ストレスの条件下でJNK経路をフィードバック阻害するためにHNEにより修飾される活性部位の近位のシステイン残基C22を持つMAP3キナーゼである、MLTK又はZAKを調べた。MLTKは近年、胃癌における発癌性のドライバーとしても関与され、且つ、MLTKのC22と反応するイブルチニブのためのオフターゲットである。競合的なisoTOP−ABPP実験により、MLTKにおけるC22のIA−アルキン標識化を遮断した断片求電子の亜群を同定した(図9A及び表1−3)。isoTOP−ABPPにより提供されるSARを検証し、イブルチニブ由来の活性プローブを使用して組換え型MLTKの標識化の遮断のために断片を試験することにより拡張して(図8E及び図9B)、MLTKの阻害のための優れた潜在能を持つものとしてベンゾフランの断片60(2.6μMのIC50値)、及び、不活性の対照プローブとして断片3(図8E、F、及び図9A、B)を同定した。断片3ではなく、断片60はまた、基質リン酸化アッセイを使用してMLTKの触媒活性を遮断し、この阻害効果は、C22A−MLTK突然変異体では観察されなかった(図8G及び図18)。
次に、以前に特徴化されていないリガンド結合したシステインを有していたタンパク質を評価した。グアニンヌクレオチドの新規合成における律速酵素であり、且つ免疫細胞増殖及び癌を調節する、IMPDH2は、競合的なisoTOP−ABPP実験において重複しているが異なるSARを示した2つのリガンド結合したシステイン−C140及びC331−を含んでいた(図9C、D;図19及び表1−3)。C331は、触媒性の求核分子として機能し、IMPDH2の活性部位特異的な阻害剤を記載した。他方、C140をIMPDH2の別個のBatemanドメインにおいて見出し、これは、ヌクレオチドの感知によりアロステリック調節のためのモジュールとして機能し(図9D)、求電子性小分子と反応することは示されていない。それ故、C140の特徴づけに重点を置いた。最初に、断片14は、MS方法により組換え型IMPDH2のC140を直接標識したことを確認した(表6)。その後、14のアルキンアナログ(18;図8H)を合成し、これにより、ローダミン−アジドのタグへのクリックケミストリー結合(click chemistry conjugation)及びSDS−PAGE分析によってC140でのリガンドの相互作用を直接モニタリングする手段をもたらした。クリックプローブ18はWT−IMPDH2及びC331S−IMPDH2突然変異体を標識したが、C140S又はこの酵素のC140S/C331S突然変異体は標識しなかった(図8H)。このアッセイを使用して、対照の断片8ではなく14が、18によるIMPDH2の標識化を阻害したことを確認した(図9E)。18によるIMPDH2標識化はまた、ヌクレオチドATP、AMP、及びGTPにより阻害されたが、UTP又はIMPでは阻害されなかった(図8I及び図9F)。ATPは、45μMのIC50値でIMPDH2の18の標識化を遮断した(図8J)。故に、IMPDH2のBatemanドメインを標的とする共有結合性のリガンドは、阻害剤としてだけでなく、この酵素へのヌクレオチド結合のプローブとしても機能する。
2つのリガンド結合したシステインであるC114及びC161はまた、p53で誘導されたホスファターゼTIGARにおいて同定された(図9G、H)。幾つかの例において、TIGARは、癌細胞の代謝状態を形成し且つそれらをROSで誘導された細胞死から保護するために、フルクトース−2,6−ビスホスファターゼ及び2,3−ビスホスホグリセラートホスファターゼの両方として作用する。TIGARの阻害剤は記載しない。C114は、リン酸塩基質結合部位から〜15Åの、TIGAR活性部位の蓋(lid)の上で見出される(図9H)。C161はタンパク質の対向面上に存在する。TIGAR活性部位への近接性を与えられたC114の断片標識化の特徴づけに重点を置いた。組換え型TIGARのC114及びC161の両方をIA−ローダミンにより標識し、この標識化はC114S及びC161Sの単一の突然変異体において部分的に縮小し、TIGARのC114S/C116Sの二重突然変異体において完全に遮断されたことを、最初に確認した(図9I)。また、LC−MS分析(表6)により、及び、16μMのIC50値でC161S−TIGAR突然変異体のIA−ローダミン標識化を断片が遮断したことを示すことにより、TIGARのC114を持つヒット断片5の相互作用を検証し(図8K、L);対照的に、対照断片3は、はるかに低い潜在能を示した(図8K、L)。5はまた、基質アッセイを使用して、WT−TIGAR及びC161S−TIGARの触媒活性を遮断したが、C114S−TIGAR又はC114S/C161S−TIGARは遮断しなかった(図8M)。対照断片3は、TIGAR触媒活性に影響を及ぼさなかった(図8L)。5によるTIGAR基質の代謝回転(turnover)の阻害は、70%で定常に達し(図9J)、これは、共有結合性のリガンドがアロステリック機構により作用し、又は完全な阻害をもたらすためにTIGARの活性部位へと完全に伸長しないことを示している。
癌細胞におけるIDH1活性を阻害する求電子性リガンド
イソクエン酸デヒドロゲナーゼ1(IDH1)及び2(IDH2)は、多くのヒトの癌において突然変異し、イソシトラートを2−ヒドロキシグルタラート(2−HG)に変換する新形質の触媒活性を持つ変異型酵素を生成する。2−HGの増大は、特にDNA及びタンパク質をメチル化することにより、腫瘍抑制因子として機能するα−ケトグルタラート依存性のジオキシゲナーゼを阻害する。競合的なisoTOP−ABPP実験により、IDH1及びIDH2において保存されたシステインを標的としたリガンドの異なる亜群を同定した(それぞれ、C269及びC308;表1−3)。このシステインは、IDH1の結晶構造においてNADP+分子から13Åである、活性部位に近接した残基であり(図10A);C308のグルタチオン化は以前に、IDH2活性を遮断することを示したが、我々の知る限りでは、IDH酵素の不可逆阻害剤は特徴付けられなかった。
IDH1の野生型(WT)及びC269S突然変異体を組み換えで発現することによるIDH酵素とのリガンド相互作用の機能的な有意性を、調べた。C269S−IDH1ではなくWT−IDH1が、SDS−PAGEにより検出されるようなIA−ローダミンプローブと反応し、断片求電子は、競合的なisoTOP−ABPP実験における内因的なIDH1について観察されるものを映したSARとの、この反応を遮断した(図11A及び表1−3)。断片20は、2.9μMのIC50値でWT−IDH1のIA−ローダミン標識化を阻害し(図11B及び図10B)、IDH1のR132H発癌性突然変異体と同様の活性を示した(図10C及び図20)。isoTOP−ABPPにより、20(25μM)がMDA−MD−231プロテオームにおける内因的なIDH1のIA−アルキン標識化を完全に遮断し(R値=20;図10D)、及びMS分析により、20がIDH1のC269を修飾する(表6)ことも、確認した。断片2は、IDH1のC269に対して非常により少ない活気を示し(IC50>50μM;図11B及び図10B)、故に対照のプローブとして選択された。20は、(イソシトラートの存在下でNADPHへのNADP+の減少により測定されるように)濃度依存性の方式でWT−IDH1の触媒作用を遮断したが、C269S−IDH1突然変異体の活性を阻害しなかったことが分かった(図11C)。20のインサイツでの活性も、R132H−IDH1を安定して過剰発現したヒト癌細胞株の生成により試験した(図10E)。R132H−IDH1細胞を2時間、断片20及び2で処理し、溶解し、2−HG産生のために実験施設内で(ex situ)アッセイした。20(50μM)は、R132H細胞溶解物により2−HGの産生を略完全に遮断し、一方で2(50μM)は、この活性のわずかな減少を引き起こしただけであった(図11D)。平行の競合的なisoTOP−ABPP実験により、断片2ではなく断片20が、インサイツでのIDH1のC269のIA−アルキン標識化を阻害したことを確認した(図10F)。
細胞におけるシステインに反応的な断片の全体的なプロファイリング
IDH1リガンド20の細胞活性により促されて、インサイツでタンパク質性のシステインを修飾する断片求電子の能力を、更に広く評価した。MDA−MB−231及びRamos細胞を、断片ライブラリーの典型的なメンバーで処理し(合計23の化合物を試験;各化合物を、インサイツの処理で2時間、200μMで試験した)、その後細胞を収集し、溶解し、isoTOP−ABPPにより分析した。少量の断片は細胞に対し細胞傷害性であり、更に低い(50又は100μM)濃度で再試験した。試験した断片は、インビトロでのそれぞれの反応性に通常一致する広範囲のインサイツの反応性を示した(図11E及び表1−3)。しかし、一部の断片は細胞において幾らか大きな反応性を示したが、断片11はインサイツでの活性を著しく欠いていた(図11E)。これらの差は、断片求電子の細胞内濃度に対する輸送及び/又は代謝経路の影響を反映している。細胞溶解物において同定される、リガンド結合したシステインの実質的な断片(64%)も、細胞における同じ求電子性断片に敏感であった(図11F)。少量の断片−システインの相互作用も、p53(TP53)のC182、DNA結合ドメイン50の二量体化インターフェースでレドックス調節された残基を含む溶解物ではなく、インサイツで選択的に観察される(図11G)。幾つかの例において、これらのリガンド結合したシステインは、断片求電子との相互作用を保つための無傷の細胞環境に必要とする。総合すれば、これらの発見は、システイン残基のリガンド結合可能性が通常、溶解物と細胞において同様であるが、例外的な場合は、インサイツでリガンド発見実験を行う能力を持つ重要性を強調することを、示している。
プロ−カスパーゼ−8を標的とし且つ外因性の細胞死を遮断する、求電子性リガンド
様々な断片は、インビトロ及びインサイツで行われるisoTOP−ABPP実験において、プロテアーゼカスパーゼ−8(CASP8)の、触媒性のシステイン求核分子C360を標的とした(図12A及び表1−3)。CASP8は、アポトーシス、免疫細胞増殖、及び胚発生において重要な役割を果たすが、このプロテアーゼのための選択的で非ペプチド性の細胞活性の阻害剤が不足している。組換え型の活性なCASP8に対する典型的な断片のヒットを、基質、及び、活性に基づくプローブ(Rho−DEVD−AOMKプローブ(SEQ ID NO:857として開示された「DEVD」))アッセイを使用してスクリーンし、大半の断片でわずかなものから阻害が無いものまでを確認した(図12B)。最初はこの結果に当惑したが、isoTOP−ABPP実験におけるCASP8の断片標識化が、このプロテアーゼの活性型ではなく不活性な酵素前駆体(プロ−)との反応を反映するかもしれないことを、仮定した。ウエスタンブロットにより、MDA−MB−231細胞溶解物におけるCASP8の全てではないにしても大半がプロ型で存在したことを確認した(図12C)。次に、プロ−CASP8の組換え型を、突然変異した切断部位(D374A及びD384A)で発現し、処理及び活性化を防いだ。プロ−CASP8の非触媒性システインC409Sも突然変異し、これにより、SDS−PAGE分析によるIA−ローダミンでのC360の標識化の検出を可能にした(図13A)。isoTOP−ABPP実験において検出された様々なヒット断片は、プロ−CASP8のIA−ローダミン標識化を遮断した(図12D)。断片7は、〜5μMのIC50値での最も高い潜在能を表示し(図13A、B)、これは、この断片の低い全体的なプロテオーム反応性(3%)と組み合わさると、更なる研究のための適切なツール化合物として指定される。
断片7(50μM)は、Ramos及びJurkat細胞溶解物の両方で実行されたisoTOP−ABPP実験において、CASP8のC360のIA−アルキン標識化を完全に遮断した(図13C)。次に、7(61)のクリック可能なアナログを合成し、このプローブ(25μM)は、C360S−プロ−CASP8突然変異体ではなくプロ−CASP8突然変異体を強く標識したことが分かった(図13D及び図12E)。7(50μM)は、61によるプロ−CASP8の標識化を遮断したが、活性型カスパーゼを標的とするために開発されたRho−DEVD−AOMKプローブ(SEQ ID NO:857として開示された「DEVD」)による活性CASP8の標識化を阻害しなかった(図13D及び図12F)。反対に、一般的なカスパーゼ阻害剤であるAc−DEVD−CHO(SEQ ID NO:857として開示された「DEVD」)(20μM)は、活性CASP8のRho−DEVD−AOMK(SEQ ID NO:857として開示された「DEVD」)の標識化を遮断したが、プロ−CASP8の61の標識化は阻害しなかった(図13D、図12F、図21A)。同様の結果を基質アッセイにおいて得て、そこでは、7ではなくDEVD−CHO(SEQ ID NO:857として開示された「DEVD」)がCASP8活性を遮断した(図13E)。基質でアッセイされた組換え型の活性なCASP3(図13E)、又はRho−DEVD−AOMKプローブ(SEQ ID NO:857として開示される「DEVD」)(図12F)、或いはisoTOP−ABPPにより測定される細胞溶解物におけるCASP2とCASP7(図12G)を含む、他のカスパーゼとの7の交差反応性は観察されなかった。最終的に、7が複雑な生物系において活性なCASP8の上でプロ−CASP8と優先的に反応することを更に検証するために、これらのタンパク質の組換え型をMDA−MB−231細胞溶解物にドープし、その後、7(30μM、1時間)又はDMSOでの処理、及びisoTOP−ABPPによる分析を行った。7は、プロ−CASP8(R=10)のためのC360のIA−アルキン標識化のほぼ完全な遮断をもたらしたが、活性CASP8(R=1.9)のC360とのIA−アルキン反応には効果がほとんどなかった(図13F)。
10又は100μMの61でのJurkat細胞溶解物の処理、その後のisoTOP−ABPPによる組み合わせたサンプルの分析により、61によるCASP8のC360の直接的な標識化を確認した(図12H)。この分析においてC360について観察された低いR値(R=2)は、CASP8のC360のIA−ローダミン標識化を阻害するために親断片7により表示される低いμMのIC50値と一貫している、細胞溶解物において10μMでの61によるこのシステインのほぼ完全な標識化を示した(図13B)。細胞のアポトーシスアッセイにおけるプロ−CASP8阻害の効果を次に評価した。C360はCASP8の触媒性の求核分子であるため、この残基の突然変異は、細胞における7の薬理学的効果を評価するために制御タンパク質を作り出すことができなかった。代わりに、構造上関連する不活性のプローブを、この目的のために開発した。7のアニリン環上に置かれるかさ高い置換基が、IA−ローダミンによるプロ−CASP8標識化を阻害しなかった62などの化合物を与えたことが分かった(図13B、G)。62はまた、基質(図13E)及び活性プローブ(図12F)のアッセイを使用して活性CASP3又はCASP8を阻害せず、且つ、isoTOP−ABPPにより判定されるようにJurkat溶解物において内因性のCASP8、CASP2、又はCASP7に対して不活性であったことを、確認した(図12G)。これらのデータに基づいて、62を、7によるプロ−CASP8の阻害を研究するために適切な不活性の対照プローブとして設計した。Jurkat細胞を、FASL又はスタウロスポリン(STS)の追加前に7又は62(30μM、30分)で処理し、外因性且つ内因性のアポトーシスをそれぞれ誘導した。62ではなく7が、FASLで誘導されたアポトーシスを完全に遮断し(図13Hおよび図21B−C)、同様に、CASP3、CASP8、及びアポトーシスマーカーPARPのタンパク質分解性の処理を遮断した(図13I)。対照的に、7は、STSで誘導された固有のアポトーシス(図13H)又はPARP及びCASP3の切断を遮断しなかったが、化合物はこれら細胞におけるCASP8の切断を実質的に阻害した(図13I)。選択的でないカスパーゼ阻害剤VAD−FMKは、FASL及びSTSで誘導されたアポトーシス、並びに関連するタンパク質分解性の処理事象の両方を妨げた(図13H、I)。化学的なプロテオミクス実験により、7が、CASP8に加えて、Jurkat細胞の関連するイニシエーターであるカスパーゼCASP10(CASP2、3、6、及び9を含む他のカスパーゼではない)を完全に阻害したことを明らかにした(図14A及び図22A)。Rho−DEVD−AOMKプローブ(SEQ ID NO:857として開示された「DEVD」)(図21A)又は基質アッセイ(図22E)での標識化により測定されるように、7は、4.5μMの明白なIC50値で61によるプロ−CASP10の標識化を遮断したが(図22B−D)、活性CASP10を阻害しなかったことを確認した。そのため、幾つかの例において、FASL及びSTSの両方で処理した細胞におけるCASP8処理を遮断する7は、CASP8活性化が外因性又は内因性のアポトーシスにおける自己処理を介して主に生じるモデルを支持しているが、プログラム細胞死の以前のタイプのみを必要としている。
幾つかの例において、外因性のアポトーシス及び他の細胞プロセスにおけるCASP8及びCASP10のそれぞれの機能は、これらの酵素のための選択的で非ペプチド性の、細胞活性の阻害剤の欠如、及び、CASP10(げっ歯類において発現されない)のための動物モデルの欠如が原因で、大部分で理解が乏しいままである。場合によっては、7の潜在能及び選択性を、この問題を扱うために改善した。4−ピペリジノ部分の3−ピペリジノ基への変換、及び7のベンゾイル環へのp−モルホリノ置換基の追加は、キラルクロマトグラフィーにより2つの精製されたエナンチオマー、63−R(図4C)及び63−Sへと分離された、化合物63をもたらし、その前者は、CASP8に対して実質的に改善された活性(0.7μMの明白なIC50値(95%のCI、0.5−0.8);図22F−H)、及びCASP10とのごくわずかな交差反応性(IC50値>100μM;図22C、D、F)を示した。63−Sは、CASP8(15μMの明白なIC50値;図22G、H)に対する活性が非常により少なく、また、CASP10に対して不活性であった(図14A)。二重のCASP8/10(7)及びCASP8に選択的(63−R)なリガンドを手に取り、次にこれらプロテアーゼの生物学的機能を調べ始めた。
ヒトT細胞のカスパーゼリガンドの効果は評価し、そこでは、CASP8とCASP10の両方が、共通して研究された不死のヒトT細胞株であるJurkat細胞の中で高度に発現される(図22I)。63−Rは、Jurkat細胞においてFasLで誘導されたアポトーシスを完全に遮断し、7(図14B及び図22J)又は63−S(図22K)よりも大きな潜在能で遮断を行ったことが分かった。同様の結果を、CASP1026ではなく、CASP8を発現するHeLa細胞において得た(図22L)。これらの細胞株の結果とは対照的に、初代ヒトT細胞のFasLで誘導されたアポトーシスは、全ての試験された濃度で63−Rに対する実質的な抵抗を示し、その代りに、二重のCASP8/10リガンド7により完全に阻害された(図14B)。プローブ61での化学プロテオミクスにより、初代ヒトT細胞及びJurkat細胞において、7はCASP8とCASP10の両方を遮断し、一方で63−RはCASP8を阻害したが、CASP10は阻害しなかったことを確認した(図14A)。これら細胞死の結果と一貫して、63−Rではなく7は、初代ヒトT細胞のCASP3及びCASP10のタンパク質分解性の処理を妨げた(図22M)。幾つかの例において、CASP8及びイニシエーターカスパーゼ基質RIPキナーゼの両方の処理も、7対63−Rにより有線的に阻害され(図22M)、このことは、生化学試験により示唆されるように、CASP10がT細胞におけるこれらタンパク質分解性の事象にも寄与することを示している。
実施例2
フマル酸ジメチル(DMF)は、多発性硬化症と乾癬を含む自己免疫性疾病を処置するために使用される薬物である。幾つかの例において、DMFの作用機序は不明瞭であるが、タンパク質の共有結合性修飾に関与し、及び/又はフマル酸モノメチル(MMF)に変換されるプロドラッグとして機能すると提唱されている。isoTOP−ABPP手法を使用して、DMFの作用機序を調べる。
化学試薬
アッセイを以下の試薬で行った:フマル酸ジメチル(DMF; 242926; Sigma Aldrich)、フマル酸モノメチル(MMF; 651419; Sigma Aldrich)、コハク酸ジメチル(DMS; W239607; Sigma Aldrich)、及びブチオニンスルホキシミン(BSO; 14484; Cayman Chemical)。
初代ヒトT細胞の単離
ヒトボランティアのサンプルを使用する全ての研究は、TSRI治験審査委員会により承認されたプロトコルに従う。健康なドナー(30−49歳の女性)から血液を、インフォームドコンセントの後で得た。末梢血単核細胞(PBMC)を、製造業者の指示に従ってHistopaque−1077の勾配(10771;Sigma)上で精製した。簡単に、血液(20×25mLの血液アリコート)をHistopaque−1077(12.5mL)の上に重ね、その後、サンプルを遠心分離(2000rpm、20分、20℃、ブレーキ無し)により分画した。PBMCをHistopaque−プラズマ界面から収集し、PBSで2回洗浄した。その後、T細胞を、製造業者の指示に従いEasySep(商標)のヒトT細胞単離キット(17951;STEMCELL)を使用して単離した。
マウス
C57BL/6J及びNrf2−/−マウス(Stock No:017009;Nfe2l2tm1Ywk;Jackson Labs)を繁殖させ、The Scripps Research Instituteの閉鎖した繁殖用施設の中で維持し、実験での使用時には6−8週齢であった。全てのマウスを、The Scripps Research InstituteのInstitutional Animal Care and Use Committeeのガイドラインに従って使用した。
PKCθ研究のために、C57BL/6マウス及びPrkcq−/−マウスを、特定の病原体の無い条件下で収容し、Allergy and Immunology Animal Care CommitteeのLa Jolla Instituteにより承認されたプロトコルに従って使用した。
初代マウスT細胞の単離
雌のマウスから脾臓を採取し、コラゲナーゼを潅流させ、30分間、5%のCO2により37℃でインキュベートした。この後、脾臓を均質化した。100μmのセルストレーナーに通して細胞を収集し、RPMIで洗浄した。製造業者の指示に従い、EasySep(商標)のマウスT細胞単離キット(19851;STEMCELL)を使用して、T細胞を脾細胞から単離した。
PKCθ研究のために、CD4+T細胞を、抗マウスCD4磁気微粒子(L3T4;BD IMag)により単離し、10%(vol/vol)の熱失活したFBS、2mMのグルタミン、1mMのピルビン酸ナトリウム、1mMのMEM非必須アミノ酸、各々100U/mLのペニシリンG及びストレプトマイシン(Life Technologies)及び組換え型IL−2(100U/mL、Biolegend)で補足されたRPMI−1640培地(Gibco)において培養した。
T細胞の刺激
96−ウェルのプレートを、4℃で一晩、PBS(100μL/ウェル)において抗CD3(1:200;BioXcell)及び抗CD28(1:500;302933;BioLegend)で覆った。その後、プレートをPBSで2回洗浄し、各ウェルに、10%のFBS、グルタミン、及びPen−Strepで補足された100μLのRPMIにおいて500,000の初代T細胞を加えた。その後、示された濃度(200μLの最終のウェルの量)で化合物を含有する100μLの培地で細胞を処理した。細胞を、示された時間にわたり5%のCO2インキュベーター中で37℃で放置し、遠心分離(500g、8分、4℃)により収集して、PBSで洗浄した。
フローサイトメトリーによる細胞の分析及び選別
細胞を丸底の96−ウェルのプレート(0720095;Fisher Scientific)に移し、遠心分離(500g、3分、4℃)により収集し、PBSで洗浄して、製造業者の指示に従いLIVE/DEADの固定可能な細胞染色(L23105;ThermoFisher)で染色した。簡単に、LIVE/DEAD染色の1つのバイアルを50μLのDMSOの中で再懸濁され、20mLのPBSを加えた。96−ウェルのプレートの各ウェルに200μLの染色物を加え、細胞を暗所で30分間、氷の上でインキュベートした。この後、細胞をペレット状にし、PBSで1回洗浄し、その後、細胞表面抗原のために染色した。
細胞表面抗原のフローサイトメトリー分析を、以下の抗体で行った:Pacific Blueで結合した抗CD8(1:25の希釈;クローンRPA−T8;BD Biosciences)、APCで結合した抗CD4(1:25の希釈;クローンRPA−T4;eBioscience)、フィコエリスリンで結合した抗CD25(1:25の希釈;クローンBC96;eBioscience又はPC61;BioLegend(PKCθ studies))、FITCで結合した抗CD69(1:25の希釈;クローンFN50;eBioscience)。全ての抗体をPBS中の1%のFBSにおいて希釈し、50μLの染色液を各ウェルに加えた。細胞を暗所の中、氷の上で15分間染色し、その後、細胞を遠心分離(500g、3分、4℃)により収集し、PBS中の1%のFBSで洗浄し、PBS中の200μL/ウェルの4%のPFAにおいて再懸濁した。フローサイトメトリーでの獲得を、BD FACSDiva(商標)により駆動するBD(商標)LSR IIフローサイトメーター(Becton, Dickinson and Company)で行った。その後、データをFlowJoソフトウェア(Treestar Inc.)で分析した。データは、1つの群につき4−5の実験のための平均±SEを表わす。
酵素結合免疫吸着測定法(ELISA)による分泌されたサイトカインの定量化
上述のようにT細胞を収集して刺激した。示された時点で、細胞培養の上清を収集し、IL−2レベルを、製造業者の指示(ヒトIL−2 DuoSet ELISA;DY202;R&D Systems)に従い透明のマイクロプレート(991427;R&D Systems)において測定した。プレートを、450nmに設定されたGemini SpectraMax 250マイクロプレートリーダにおいて読み出した。データは、1つの群につき4つの実験のための平均±SEを表わす。
PKCθ研究のために、形質導入されたPrkcq−/−CD4+T細胞(1×106)のアリコートを、抗CD3のみ、又は抗CD28と抗CD3で48時間刺激し、培養液の上清におけるIL−2の濃度を、製造業者の指示(BioLegend)に従い酵素結合免疫吸着測定法により測定する。簡単に、96−ウェルのプレート(Corning Costar)を4℃で一晩、IL−2に対しmAbで覆った。その後、培養細胞からのIL−2基準及び上清を三通り、プレートに加えて、その後に室温で2時間インキュベーションを行った。IL−2に対するビオチン化されたポリクローナル抗体をプレートに加え、その後、室温で1時間のインキュベーションを行い、次いでAvidin−HRPを加え、そして室温で30分間のインキュベーションを行った。その後、結合されたアビジンの量を、2NのH2SO4により酸性化されたTMBペルオキシダーゼで評価した。その後、450nmでの各ウェルの吸収度を、分光測光法プレートリーダー(BioTek)により測定した。
細胞グルタチオン(GSH)レベルの定量化
初代ヒトT細胞(250万個の細胞/mL、1つの条件につき20mL)を、示されるように処理し、遠心分離(500g、8分、4℃)により収集し、PBSで2回洗浄した。細胞ペレットに、75μLの溶解緩衝液を加えた。ボルテックス後、サンプルを氷の上で15分間インキュベートし、次いで遠心分離(16,000g、10分、4℃)により収集した。タンパク質濃度を少なくとも5mg/mLに調整し、製造業者の指示(Sigma−Aldrich, CS1020)に従いアッセイを行った。データは、2つの生物学的な複製のための平均±SEを表わす。
タンパク質標識化及びクリックケミストリー
細胞を超音波処理により溶解し、2mgのタンパク質/mLの濃度に希釈した。タンパク質濃度を、Bio−Rad DC(商標)タンパク質アッセイ試薬A及びB(5000113、5000114;Bio−Rad)で測定した。500μLのプロテオームサンプルを、10mMのDMSO保存溶液の10μLを使用して100μMのIA−アルキンのプローブにより処理した。標識化反応物を室温で1時間インキュベートし、その後、サンプルを、銅で触媒されたアジド−アルキンの環化付加(CuACC又は「クリックケミストリー」)により、同位体的に標識されたTEVで開裂可能なタグ(TEVタグ)に結合させた。60μLの重クリックケミストリー反応混合物を、DMSOで処置し対照サンプルに加え、60μLの軽反応混合物を化合物で処置したサンプルに加えた。クリック反応混合物は、TEVタグ(5mMの保存溶液の10μL、軽(断片で処置)又は重(DMSOで処置))、CuSO4(水中の50mMの保存溶液の10μL)、及びTBTA(4:1のtBuOH:DMSOにおける1.7mMの保存溶液の30μL)を含んでいた。これに、TCEP(50mMの保存溶液の10μL)を加えた。反応を室温で1時間行った。
その後、軽及び重標識されたサンプルを遠心分離し(16,000g、5分、4℃)、沈殿したタンパク質を収集した。結果として生じるペレットを、超音波処理により500μLの冷たいメタノール中で再懸濁し、重及び軽サンプルを対で組み合わせた。その後、組み合わせたペレットを、冷たいMeOHで洗浄し、その後、超音波処理により1.2%のSDSを含有するPBSノ中でペレットを可溶化した。サンプルを90℃で5分間加熱し、公表されたisoTOP−ABPPプロトコルに従って、プローブで標識されたタンパク質のストレプトアビジン富化、連続するオンビーズ・トリプシン及びTEVの消化、並びに液体クロマトグラフィータンデム質量分析(LC−MS/MS)にさらした。
ペプチド及びタンパク質の同定
RAW Xtractor(バージョン1.9.9.2)を使用して、未加工のファイルからMS2スペクトルデータを抽出した。ProLuCIDアルゴリズムを使用して、MS2データを、Human UniProtのデータベース(release−2012_11)の逆連鎖の非冗長的な変異体に対して探索した。システイン残基を、カルボキサミドメチル化のための静的な修飾により(+57.02146)、及び、軽又は重のTEVタグ(それぞれ+464.28595又は+470.29976)の何れかのための最大1つの特異な修飾により探索した。ペプチドは、少なくとも1つのトリプシン末端を有し、且つTEV修飾を含むことを要求される。ProLuCIDデータをDTASelect(バージョン2.0)に通して濾過し、1%未満のペプチド無病誤診率を達成した。
R値の算出及び処理
重/軽の比率の定量化(isoTOP−ABPPの比率、R値)の定量化を、デフォルトパラメータ(1つのピークにつき3MS1’s及び信号対ノイズの閾値2.5)を使用して、インハウスのCIMAGEソフトウェアにより行った。求電子化合物の部位特異的な結合を、IA−アルキンプローブの標識化の遮断により評価した。DMSOで処理したプロテオーム(重TEVタグ)と比べて、化合物で処理したプロテオーム(軽TEVタグ)からのMS1ピーク面積において≧95%の減少を示したペプチドについて、20の最大の比率を割り当てた。同じ標識されたシステインと重複するペプチド(例えば、標識されたシステインの周囲の同じ局所的配列であるが、異なる荷電状態、MudPITセグメントの数、又はトリプシンの末端)を1つにまとめ、各群からの中央の比率を、その実行のためにペプチドのR値として記録した。
システイン保存の分析
DMF感受性のシステインを含有するヒトタンパク質それぞれについて、マウスの相同体を同定し、ヒト及びマウスの配列をUniProtの上でAlignツールを使用して整列させた。
NF−kB転位の免疫蛍光分析
上述のように初代ヒトT細胞を収集して刺激し(500,000個の細胞/ウェル)、それに付随して60分間のDMSOでの処理を行った。細胞をペレット状にし(500g、3分、4℃)、次に各ウェルを50μLのPBSにおいて再懸濁し、ポリ−D−リジンでコーティングしたカバーガラス(12mm;354087;Corning(登録商標)BioCoat(商標))に加えた。細胞を4℃で30−60分間、カバーガラスに付けた。カバーガラスを6ウェルのプレートに移し、室温で10分間、4%のPFA(157−4−100;Electron Microscopy Sciences)で固定した。PBSで3回洗浄後、細胞を室温で10分間、PBS中で0.1%のTriton X−100で透過処理した。細胞をPBSで3回洗浄し、次いでParafilm上で細胞を上向きに置いた。各カバーグラスに、150μLの遮断緩衝液(PBS中で2%のBSA)を加え、スライドを室温で30分間遮断した。
遮断緩衝液を吸引し、カバーガラスを下向きにして40μLの抗体緩衝液(抗ヒトp65;p65Ab;FivePhoton Biochemicals;遮断緩衝液において1:500の希釈物)の中に置き、湿ったチャンバの中で4℃で一晩かけて染色した。カバーガラスをPBSで3回洗浄し、次に室温で2時間、150μLの二次抗体(抗ウサギのAlexa Fluor 488;A21441;Life Technologies;PBSにおいて1:200の希釈物)でインキュベートした。PBSで3回の洗浄後、150μLのHoechst対比染色を加え(PBSにおいて5μg/mL)、カバーガラスを室温で30−60分間放置した。細胞を再びPBSで3回洗浄し、その後、Alexa Fluor 555 Phalloidin red(8953S;Cell Signaling;PBSにおいて1:20の希釈物)で染色する。カバーガラスをPBSで最後に3回洗浄し、その後、10μLのProlong(登録商標)Gold Antifade Mountant(P36934、ThermoFisher)で染みをつけたSuperFrost Plusのスライド(12−550−15、Fisherbrand)に移した。各カバーガラスの周囲を、透明なマニキュア液(72180;Electron Microscopy Sciences)で密閉した。
63倍の対物レンズ(Objective)(0.3μmの画像の刻み幅)と自動ステッチングモジュール(automated stitching module)を統合したZeiss780レーザー走査共焦点顕微鏡を使用して画像を獲得し(10%の重複)、3次元のマルチパネルの大規模な画像の複合体を作成する。複合画像を、zenソフトウェアを使用して自動に統合された、少なくとも9の個別画像パネルのz−シリーズとして収集した。大規模な画像の複合体を、zenソフトウェアにおいて最大の画像投影へと投影し、その後、Zen(Zeiss Inc)及びImage Pro Premier(Media Cybernetics)を使用して分析した。Manderの相関係数(MCC)、具体的に、蛍光標識の様々な組み合わせの間のM1及びM2(Rhodamine Phalloidin vs NFkB−P65及びHoechst vs NFkB−p65)を、1つの細胞当たりZEN(Zeiss inc)において計算し、パーセントとして表示する。対象のモジュールの領域を使用して各細胞の概略を示し、その後ソフトウェアにより、2つのフルオロフォア間のM1及びM2の相関係数を計算し、結果を表にした。蛍光シグナルのダイナミックレンジ、及び実信号の閾値カットオフを、複数のバックグラウンド及び二次制御により定めた。Image Pro Premier(IPP)(Media Cybernetics)を使用して相関係数を比較し、そこでは画像を未加工の較正されたcziファイルとして取り込み、IPPにおいて同様のモジュールを使用して分析した。同様の結果を、両方のプラットフォームにより得た(図示せず)。データは、2−3の生物学的な複製のための平均±SEを表わす。
サブクローン化及び突然変異生成
QuikChange部位特異的突然変異誘発を、完全長のヒトPKCθ(残基1−707)を含有するpEF4 His Aプラスミド上で行った。BamHI及びXhoIを使用してPKCθ挿入物を切除し、次にpMIGベクターへとライゲートした。
PKCθのレトロウイルスの導入及び刺激
白金Eパッケージング細胞を、10%のFBSを加えた2mLのRPMI−1640培地において、6ウェルのプレートに蒔いた。24時間後、細胞を、TransIT−LT1トランスフェクション試薬(Mirus Bio)により、空のpMIGベクター又は適切なPKCθ発現ベクターDNA(3μg)をトランスフェクトした。一晩のインキュベーション後、培地を交換し、培養を更に24時間維持した。その後、レトロウイルスの上清を収集して濾過し、8μg/mLのポリブレンで補足し、これを使用して、CD3(8μg/mL)及びCD28(8μg/mL)へとプレート結合されたモノクローナル抗体で24時間、予め活性化されたCD4+T細胞を感染させた。2,000r.p.m.で1.5時間のプレートの遠心分離後、細胞の上清を、10%のFBS及び組換え型IL−2(100U/mL)で補足された新鮮なRPMI−1640と取り替えた。細胞を37℃で更に24時間インキュベートした。3日目に、細胞を洗浄し、新しいプレートに移して、mAbによるCD3のみへの再刺激、加えてmAbによるCD28への再刺激の前に更に2日間の刺激を行うことなく、10%のFBS及び組換え型IL−2(10のU/mL)を含有するRPMI−1640培地において培養した。
PKCθの免疫沈降及びイムノブロット解析
プロテアーゼ阻害剤(10μg/mLのアプロチニン、10μg/mLのロイペプチン、及び1mMのPMSF)、並びにホスファターゼ阻害剤(5mMのピロリン酸ナトリウム及び1mMのNa3VO4)で補足された、1%(wt/vol)のジギトニン(D141、Sigma)の溶解緩衝液(20mMのTris−HCl、pH7.5、150mMのNaCl、5mMのEDTA)において、細胞を溶解した。上清を1μgの抗CD28 mAbで2時間インキュベートし、タンパク質を、Gタンパク質セファロースビーズ(GE Healthcare)により4℃で一晩、免疫沈降させた。免疫沈降させたタンパク質をSDS−PAGEにより分解し、PVDF膜上に移し、一次抗体により4℃で一晩探索し、その後、ワサビペルオキシダーゼ(HRP)で結合した二次抗体により室温で1時間のインキュベーションを行った。化学発光(ECL;GE Healthcare)によりシグナルを視覚化し、X線フィルムに晒した。デンシトメトリー分析をImageJソフトウェアにより行った。CD28(C−20)及びPKCθ(C−19)に対するイムノブロッティング抗体を、Santa Cruz Biotechnologyから得た。
MMFではなくDMFがT細胞活性化を阻害する。
多発性硬化症は、顕著なT細胞成分を伴う自己免疫疾患である;そのため、DMFが場合によっては初代T細胞活性化に影響を及ぼすことが論じられた。これに一貫して、以前の報告は、DMFがマウス脾細胞からのサイトカイン放出を阻害し、且つIL−10を産生するII型樹状細胞の誘導を介してTh2表現型を促進することを示している。DMF及びMMF(図23A)の効果を、抗CD3及び抗CD28の抗体により活性化された初代ヒトT細胞からのサイトカイン放出に対して試験した。IL−2の分泌は、MMFではなくDMFにより強く阻害された(図23B)。MMFではなくDMF、又は非求電子性のアナログであるコハク酸ジメチル(DMS、図23A)も、抗CD3、抗CD28で刺激されたT細胞において、早期活性化マーカーCD25(図23C、D)及びCD69(図23E)の発現を遮断した。DMFによるT細胞活性化の遮断は濃度依存性であり、10、25、及び50μMの薬物がそれぞれ、周縁の/ごくわずかな、部分的な、及びほぼ完全な阻害をもたらした(図23B、D、E)。幾つかの例において、サイトカイン放出及び活性化マーカーに対するDMFの効果は、T細胞の生存度を損なわなかった薬物の濃度で生じた(図24)。同様の結果をC57BL/6マウスの初代脾臓T細胞から得て、その活性化はまた、MMFまたはDMSではなくDMFにより抑えられた(図25)。注目すべきことに、薬物が抗CD3、抗CD28での刺激の2時間後に加えられた場合、DMFの阻害効果は低減し、及び、薬物が刺激の6時間後に加えられた場合、DMFの阻害効果は完全に取り除かれ(図23F)、このことは、T細胞活性化に対するDMFの効果がNrf2及びGSHとは独立しているT細胞活性化経路における初期の事象を阻害することを示唆している。
DMFは、Nrf2−Keap1経路の活性化を介して神経保護効果をもたらすと考えられるが、この経路がDMFの免疫修飾物質の効果に寄与するかどうかは不明瞭である。近年の研究は、DMFが初代マウス脾細胞からの炎症促進性サイトカインの放出を阻害し、活この効果が、野生型及びNrf2(−/−)の脾細胞において比較可能であったことを示した(Gillard, et al., “DMF, but not other fumarates, inhibits NF−kappaB activity in vitro in an Nrf2−independent manner,” J. Neuroimmunol. 283, 74−85 (2015))。これに一貫して、Nrf2(+/+)及び(−/−)のT細胞の活性化は同様に、DMFによる阻害に敏感であったことが分かった(図26A)。幾つかの例において、DMFはまた、グルタチオン(GSH)を枯渇させることによりT細胞活性化を損ない、実際に、DMFで処理した初代ヒトT細胞は、細胞のGSH含有量の著しい減少を示した(図26B)。しかし、GSHの著しい減少はまた、T細胞活性化に対する効果を持たないGSH合成阻害剤であるブチオニンスルホキシミン(BSO)により観察された(図26C、D)。場合によっては、これらのデータは、DMFによるT細胞活性化の遮断がNrf2活性化又はGSH枯渇以外のプロセスに関与することを示している。
T細胞におけるDMF感受性Cys残基の化学的なプロテオミクスの発見
非求電子性のアナログであるMMF及びDMSではなく、DMFによるT細胞活性化の阻害は、T細胞の機能に重要な1以上のタンパク質とので共有結合性の反応に関与する機構を指し示した。そのため、初代ヒト及びマウスT細胞におけるDMF感受性Cys残基の全体的な一覧(inventory)を、定量的で化学的なプロテオミクスのプラットフォーム、isoTOP−ABPPを使用して調べた。この方法において、DMFを、通常の求電子性プローブであるヨードアセトアミド−アルキン(IA−アルキン)とのタンパク質性Cys残基の反応を遮断する能力について評価する。同位体的に分化されたアジド−ビオチンのタグ(TEVプロテアーゼ開裂可能なリンカーを含む)を使用して、Cys残基を同定して、DMF対DMSO対照で処理された細胞におけるIA−反応性のために比較的定量化する。isoTOP−ABPPプラットフォームの主な利点は、以下の通りである:1)競合する求電子は標的の同定のために自身を化学的に改質する必要は無く、DMFのような非常に小さな化合物を研究する時に特に有益となる;及び2)同位体的標識化はサンプル処理において遅く生じ、代謝標識化に容易に従わない初代細胞及び組織の定量分析を容易にする。
isoTOP−ABPP方法を、DMSO又はDMF(50μM、4時間)で処理された初代ヒトT細胞上で実行した。独立した5つの複製を実行し、固有の定量化されたペプチド及びタンパク質の総数は、第4及び第5の複製により定常に達し始め(図28)、このことは、利用される条件下でヒトT細胞におけるIAに反応的なCys残基の最大のプロテオミクスの適用範囲に近づいたことを示している。2400を超える定量化されたCys残基のうち、ごく一部(〜40)が、DMFで処理したT細胞におけるIA−アルキン標識化において実質的な減少(>4倍;isoTOP−ABPP比率(R値)>4)を示した(図27A及び表7−9)。同様のisoTOP−ABPP分析は、〜40のDMF感受性Cys残基は何れもMMF(50μM、4時間)又はBSO(2.5mM、4時間)の処理により改質されず、このことは通常、T細胞プロテオームにわたるごくわずかなCys残基の反応に影響を及ぼしたことを明らかにした(それぞれ図27A、B、及び図29)。より低濃度のDMF(10及び25μM、4時間)での、又はより短期間(50μMのDMF、1又は2時間)にわたり処理されたヒトT細胞で実行されるisoTOP−ABPP実験により明らかとなるように、DMFにより標的とされたCys残基は、DMFの感度における濃度(図27C及び表8−9)及び時間(図27D)に依存した増大を示した。注目すべきことに、ごくわずかなDMF感受性Cys残基が、10μMのDMFで処理したT細胞において検出され、薬物の濃度はまた、T細胞活性化への影響を制限した(図23B、D、E)。これらの濃度及び時間に依存する研究は、本来の50μM/4時間のisoTOP−ABPP実験において検出されなかった別の〜10のDMF感受性Cys残基を明らかにし、このことは恐らく、データ依存性のMS実験におけるペプチド発見の確率的性質を反映している。
DMFでの処理後のシステイン反応における変化の一部がタンパク質発現の変化を反映し得る可能性を考慮し;しかし、多数のCys残基は、DMF感受性Cys残基を持つ大多数のタンパク質のためのisoTOP−ABPPにより定量化され、このような事例の大半において、更に定量化されたCys残基はDMF処理による影響を明らかに受けなかった(図27E)。DNAで活性化されたタンパク質キナーゼPRKDCを1つの典型的な例として示し、そのため、IA−アルキン反応は様々なCys残基のために定量化され、その1つのみ(C4045)がDMFにより遮断された(図27F)。これらの結果は、DMFがヒトT細胞におけるタンパク質発現に間接的に影響を及ぼすのではなく、特定のCys残基のIA−アルキン反応を直接損なったことを示している。
ヒト及びマウスT細胞におけるDMF感受性Cys残基の保存
ヒト及びマウス両方のT細胞の活性化をDMFが損なったことを考慮して、DMF作用の媒介に潜在的に重要な少なくとも1つのCys残基の亜群はヒト及びマウスに保存されたことが推測された。これに一貫して、ヒトT細胞において発見されたDMF感受性Cys残基のおよそ3分の2は、マウスに保存されている(図30A及び表7)。isoTOP−ABPP実験をDMF(50μM、4時間)で処理したマウスT細胞上で行い、ヒトT細胞におけるDMFに敏感な保存された定量化Cys残基のうち大部分(>80%)はまた、マウスT細胞においてこの薬物により遮断された(R値>4)ことが分かった(図30B及び表8−9)。これらの結果は、DMFがヒト及びマウスT細胞におけるCys残基の同様のアレイを標的とすることを示しており、このことは、この求電子性の薬物のための作用の候補部位としてタンパク質の特定のセットを指し示している。
DMF感受性Cys残基を含有するタンパク質は、全体として、酵素、チャネル、輸送体、足場タンパク質、及び転写制御因子を含む様々な機能別の区分から生じた(図30C)。これらタンパク質の中には、重要な免疫機能を持つものが幾つか存在していた(表7)。DMF感受性Cys残基は、例えば、IκBキナーゼβ(IKKβ又はIKBKB)、タンパク質キナーゼC−θ(PKCθ又はPRKCQ)、及びTNFAIP3を含む、NF−κBシグナル経路の成分又は制御因子の何れかである、複数のタンパク質において見出された(表7)。NF−κB経路内のDMFの作用及び潜在的にその他のこのような部位に一貫して、他の細胞型において示されるように、DMF処理がp65の核転位を遮断したことが分かった(図31)。DMF感受性Cys残基は、以下においても見出された:1)アデノシンデアミナーゼ酵素ADA、ヒトにおいて重症複合免疫不全症を引き起こす有害突然変異、2)転写因子であるインターフェロン調節因子−4(IRF4)及び−8(IRF8)、並びに3)免疫修飾物質のサイトカインIL−16(表7)。
DMFは、PKCθ−CD28の相互作用及びT細胞活性化に重要なCXXCモチーフを変動させる。
PKCθは、T細胞受容体及びCD28コレセプターの結合によりNF−κBを含む多数の下流経路の活性化が生じる免疫学的シナプスでのT細胞シグナル伝達に関与する、重大なキナーゼである。PKCθ(−/−)マウスのT細胞は早期活性化を欠いている。isoTOP−ABPP分析は、ヒト(図32A)及びマウス(図33A)T細胞における2つのDMF感受性Cys残基であるC14とC17を同定し、これらのシステイン残基は、DMF感受性における時間及び濃度に依存した増加を示したが(図33B、C)、MMF処理による影響を受けなかった(図33D)。C14及びC17が同じトリプシンペプチド上で見出されるため、1つ又は両方の残基がDMF処理に敏感であったかどうかを区別するのは困難であったが、特定のisoTOP−ABPP実験において、このトリプシンペプチドは、共にDMF感度を示した2つの隣接するピークとして遊走すると思われ(図32A)、このことは、C14とC17両方のIA−アルキン反応がDMF処理により遮断されることを示唆している。isoTOP−ABPP実験はまた、DMF処理により影響を受けなかったPKCθにおいて第3のCysを同定し(図32A)、このことは、PKCθ発現の変化ではなくC14/17反応の減少をDMFが引き起こしたことを示している。C14とC17は、他のPKCアイソフォームではなくPKCθのC2ドメインにおいて見出されるCXXCモチーフを形成する(図32B、C)。PKCθのC2ドメインは近年、ホスホチロシン含有ペプチドに結合すると示され、且つ、免疫学的シナプスにてPKCθの原形質膜の会合を安定させると仮定された。TCR/CD28での刺激後、PKCθは免疫学的シナプスに動員され、そこでは、PKCθは、CD28の細胞質尾部と結合させることによりCD28コレセプターと相互に作用する。MMFではなくDMFが、マウスT細胞におけるPKCθとCD28との相互作用を遮断したことが分かった(図32D)。レトロウイルスの導入を使用して、WT−又はC14S/C17S−PKCθ突然変異体の何れかを持つPKCθ(−/−)T細胞を再構成し、突然変異タンパク質はCD28と結合しないことが分かった(図32E)。C14S/C17SPKCθ突然変異体で再構成されたPKCθ(−/−)T細胞はまた、WT PKCθで再構成され、その後抗CD3、抗CD28での処置を受けた細胞と比較して、CD25(図32F)及びIL−2(図32G)の発現が損なわれたことを示した。総合すれば、これらのデータは、PKCθのC2ドメイン内のC14/C17モチーフがこのキナーゼの免疫学的シナプスへの局在化を調節し、DMF又は遺伝子突然変異によるこのモチーフの破壊がT細胞活性化を損なうことを示している。
プローブADAの方へのDMFにおける感受性システイン残基部位
DMF感受性Cys残基C75は、ヒトにおいて突然変異した時に免疫抑制性の表現型に寄与する2つのアミノ酸、G74とR76の間に位置している。ADAのアミノ酸74−76の領域は、酵素の活性部位から25オングストローム以上であり(図34)、このことは、前記領域が恐らくDMF反応により混乱される非触媒性の機能を実行することを示唆している。IKBKBにおけるDMF感受性Cysは、ロイシンジッパードメインに位置し、且つ、このキナーゼの活性部位に見出される別の求電子感受性Cys残基C179とは異なっている。
表1はリガンド結合されたシステイン、及び、(インビトロで)細胞溶解物において実行されたisoTOP−ABPP実験からの断片求電子ライブラリーとの反応特性のリストを例示する。表1は更に、タンパク質の受入番号(又はタンパク質の同定子)を示す。
表2は、インサイツで実施されたisoTOP−ABPP実験からのリガンド結合されたシステインおよび断片求電子ライブラリーを伴うそれらの反応性プロフィールのリストを示す。表2はさらにタンパク質の受入番号(またはタンパク質識別子)を示す。
表3はシステイン含有タンパク質および潜在的な結合のシステイン部位のリストを示す。
表4は、isoTOP−ABPP実験において断片求電子によって標的化された既知の共有結合性リガンドを有する代表的なシステインを示す。
表5はリガンド結合されたシステインの反応性ドッキングの結果を示す。
表6は 組換え型タンパク質の断片標識化の部位を示す。下線部分は、断片が修飾されたシステインを示す。
表7は、DMSO処理細胞対DMF処理細胞を比較するisoTOP−ABPP実験において、R値(DMSO/DMF)>4を示したCys残基として定義される、ヒトT細胞におけるDMF感受性Cys残基のリストを示す。
表8はヒトT細胞標的におけるDMF感受性システイン含有タンパク質の例示的なリストを示す。表8はさらに、タンパク質の受入番号(またはタンパク質識別子)を示す。
表9は本明細書中に記載された例示的なシステイン含有タンパク質の全タンパク質配列を示す。対象のシステイン残基には*が付されている。
表10A−10Eはシステイン含有タンパク質、およびタンパク質の種類によって分けられた、潜在的な結合のシステイン部位のリストを示す。表10Aはシステイン含有酵素および潜在的なシステイン結合部位を示す。表10Bはシステイン含有転写因子および制御因子のリストを示す。表10Cはシステイン含有のチャネル、輸送体、および受容体の例示的なリストを示す。表10Dは例示的なシステイン含有のアダプター、足場、および修飾因子のタンパク質を示す。表10Eは未分類のシステイン含有タンパク質の例示的なリストを示す。
本明細書に記載されている実施例および実施例は、例示のみを目的とするものであり、当業者に示唆された様々な修正または変更が本願の精神および範囲内に含まれるべきである。