JP6831496B2 - ベンゾオキサゾール誘導体の結晶 - Google Patents
ベンゾオキサゾール誘導体の結晶 Download PDFInfo
- Publication number
- JP6831496B2 JP6831496B2 JP2020527613A JP2020527613A JP6831496B2 JP 6831496 B2 JP6831496 B2 JP 6831496B2 JP 2020527613 A JP2020527613 A JP 2020527613A JP 2020527613 A JP2020527613 A JP 2020527613A JP 6831496 B2 JP6831496 B2 JP 6831496B2
- Authority
- JP
- Japan
- Prior art keywords
- crystal
- added
- crystals
- formula
- solvent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000013078 crystal Substances 0.000 title claims description 67
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical class C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 title 1
- 238000000634 powder X-ray diffraction Methods 0.000 claims description 23
- 238000000113 differential scanning calorimetry Methods 0.000 claims description 11
- -1 2- (3,6-diazabicyclo [3.1.1] heptane-3-yl) -7- (thiazole-2-yl) benzo [d] oxazole-4-yl Chemical group 0.000 claims description 9
- 239000008194 pharmaceutical composition Substances 0.000 claims description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 69
- 150000001875 compounds Chemical class 0.000 description 57
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 48
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 33
- 239000002904 solvent Substances 0.000 description 26
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical group OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- 239000000243 solution Substances 0.000 description 20
- 239000000203 mixture Substances 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 16
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 15
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 14
- 239000012046 mixed solvent Substances 0.000 description 14
- 101100296720 Dictyostelium discoideum Pde4 gene Proteins 0.000 description 12
- 101100082610 Plasmodium falciparum (isolate 3D7) PDEdelta gene Proteins 0.000 description 12
- 239000000706 filtrate Substances 0.000 description 11
- 238000000034 method Methods 0.000 description 10
- 239000012044 organic layer Substances 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical group ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 9
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 8
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 8
- 238000010898 silica gel chromatography Methods 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 238000001914 filtration Methods 0.000 description 7
- 230000002401 inhibitory effect Effects 0.000 description 7
- 230000005764 inhibitory process Effects 0.000 description 7
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 6
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 6
- 201000010099 disease Diseases 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- 238000013112 stability test Methods 0.000 description 6
- 238000001816 cooling Methods 0.000 description 5
- 239000000825 pharmaceutical preparation Substances 0.000 description 5
- 229940127557 pharmaceutical product Drugs 0.000 description 5
- 239000000523 sample Substances 0.000 description 5
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 229940088679 drug related substance Drugs 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 229910052736 halogen Inorganic materials 0.000 description 4
- 150000002367 halogens Chemical class 0.000 description 4
- 239000011535 reaction buffer Substances 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- QGJOPFRUJISHPQ-UHFFFAOYSA-N Carbon disulfide Chemical compound S=C=S QGJOPFRUJISHPQ-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000008186 active pharmaceutical agent Substances 0.000 description 3
- 238000002425 crystallisation Methods 0.000 description 3
- 230000008025 crystallization Effects 0.000 description 3
- 239000012153 distilled water Substances 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 230000007704 transition Effects 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical group CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- 102000004861 Phosphoric Diester Hydrolases Human genes 0.000 description 2
- 108090001050 Phosphoric Diester Hydrolases Proteins 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 2
- 201000004681 Psoriasis Diseases 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 235000019270 ammonium chloride Nutrition 0.000 description 2
- 239000012300 argon atmosphere Substances 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- TZIHFWKZFHZASV-UHFFFAOYSA-N methyl formate Chemical group COC=O TZIHFWKZFHZASV-UHFFFAOYSA-N 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 238000002076 thermal analysis method Methods 0.000 description 2
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 1
- FJBDQIRRDKSQTK-UHFFFAOYSA-N 1-[[2-(3,6-diazabicyclo[3.1.1]heptan-3-yl)-7-(1,3-thiazol-2-yl)-1,3-benzoxazol-4-yl]oxy]-1,1-difluoro-2-methylpropan-2-ol Chemical compound C12CN(CC(N1)C2)C=1OC2=C(N=1)C(=CC=C2C=1SC=CN=1)OC(C(C)(O)C)(F)F FJBDQIRRDKSQTK-UHFFFAOYSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- YJKYCRSONHRGJN-UHFFFAOYSA-N 2-nitro-3-phenylmethoxyphenol Chemical compound OC1=CC=CC(OCC=2C=CC=CC=2)=C1[N+]([O-])=O YJKYCRSONHRGJN-UHFFFAOYSA-N 0.000 description 1
- WRTCOFURCZSROR-UHFFFAOYSA-N 7-bromo-4-phenylmethoxy-3H-1,3-benzoxazole-2-thione Chemical compound C(C1=CC=CC=C1)OC1=CC=C(C2=C1N=C(O2)S)Br WRTCOFURCZSROR-UHFFFAOYSA-N 0.000 description 1
- 208000002874 Acne Vulgaris Diseases 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- SRPHFINORTZEJV-UHFFFAOYSA-N C(C)#N.C(C1=CC=CC=C1)OC=1C(=C(C(=CC1)Br)O)[N+](=O)[O-] Chemical compound C(C)#N.C(C1=CC=CC=C1)OC=1C(=C(C(=CC1)Br)O)[N+](=O)[O-] SRPHFINORTZEJV-UHFFFAOYSA-N 0.000 description 1
- AQWZROYGDMVAAM-UHFFFAOYSA-N CC1=CC=CC=C1.C(C1=CC=CC=C1)OC1=CC=C(C2=C1N=C(O2)N2CC1N(C(C2)C1)C(=O)OC(C)(C)C)C=1SC=CN1 Chemical compound CC1=CC=CC=C1.C(C1=CC=CC=C1)OC1=CC=C(C2=C1N=C(O2)N2CC1N(C(C2)C1)C(=O)OC(C)(C)C)C=1SC=CN1 AQWZROYGDMVAAM-UHFFFAOYSA-N 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- 208000028698 Cognitive impairment Diseases 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- 208000003556 Dry Eye Syndromes Diseases 0.000 description 1
- 206010013774 Dry eye Diseases 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 201000009794 Idiopathic Pulmonary Fibrosis Diseases 0.000 description 1
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 1
- 208000029523 Interstitial Lung disease Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 230000004570 RNA-binding Effects 0.000 description 1
- NQVAHSDJQUCQGC-UHFFFAOYSA-L S(=O)([O-])S(=O)[O-].[Na+].NC1=C(C(=CC=C1OCC1=CC=CC=C1)Br)O.[Na+] Chemical compound S(=O)([O-])S(=O)[O-].[Na+].NC1=C(C(=CC=C1OCC1=CC=CC=C1)Br)O.[Na+] NQVAHSDJQUCQGC-UHFFFAOYSA-L 0.000 description 1
- 201000002661 Spondylitis Diseases 0.000 description 1
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 206010000496 acne Diseases 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 208000002205 allergic conjunctivitis Diseases 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 208000024998 atopic conjunctivitis Diseases 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 125000005605 benzo group Chemical group 0.000 description 1
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 208000010877 cognitive disease Diseases 0.000 description 1
- SNRCKKQHDUIRIY-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloromethane;dichloropalladium;iron(2+) Chemical compound [Fe+2].ClCCl.Cl[Pd]Cl.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 SNRCKKQHDUIRIY-UHFFFAOYSA-L 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- OJCSPXHYDFONPU-UHFFFAOYSA-N etoac etoac Chemical compound CCOC(C)=O.CCOC(C)=O OJCSPXHYDFONPU-UHFFFAOYSA-N 0.000 description 1
- 230000003176 fibrotic effect Effects 0.000 description 1
- WBJINCZRORDGAQ-UHFFFAOYSA-N formic acid ethyl ester Natural products CCOC=O WBJINCZRORDGAQ-UHFFFAOYSA-N 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 201000005787 hematologic cancer Diseases 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- JQOAQUXIUNVRQW-UHFFFAOYSA-N hexane Chemical compound CCCCCC.CCCCCC JQOAQUXIUNVRQW-UHFFFAOYSA-N 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 208000036971 interstitial lung disease 2 Diseases 0.000 description 1
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 1
- 229940011051 isopropyl acetate Drugs 0.000 description 1
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical compound CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 1
- 208000002741 leukoplakia Diseases 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 201000003265 lymphadenitis Diseases 0.000 description 1
- IVSZLXZYQVIEFR-UHFFFAOYSA-N m-xylene Chemical group CC1=CC=CC(C)=C1 IVSZLXZYQVIEFR-UHFFFAOYSA-N 0.000 description 1
- NXPHGHWWQRMDIA-UHFFFAOYSA-M magnesium;carbanide;bromide Chemical compound [CH3-].[Mg+2].[Br-] NXPHGHWWQRMDIA-UHFFFAOYSA-M 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 208000030159 metabolic disease Diseases 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 201000006938 muscular dystrophy Diseases 0.000 description 1
- UBLQIESZTDNNAO-UHFFFAOYSA-N n,n-diethylethanamine;phosphoric acid Chemical compound [O-]P([O-])([O-])=O.CC[NH+](CC)CC.CC[NH+](CC)CC.CC[NH+](CC)CC UBLQIESZTDNNAO-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- NXJCBFBQEVOTOW-UHFFFAOYSA-L palladium(2+);dihydroxide Chemical compound O[Pd]O NXJCBFBQEVOTOW-UHFFFAOYSA-L 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 201000003086 pulmonary systemic sclerosis Diseases 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 206010039083 rhinitis Diseases 0.000 description 1
- 239000012488 sample solution Substances 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 201000000306 sarcoidosis Diseases 0.000 description 1
- 201000000980 schizophrenia Diseases 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 238000004441 surface measurement Methods 0.000 description 1
- 210000004243 sweat Anatomy 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- HNINFCBLGHCFOJ-UHFFFAOYSA-N tert-butyl 3,8-diazabicyclo[3.2.1]octane-8-carboxylate Chemical compound C1NCC2CCC1N2C(=O)OC(C)(C)C HNINFCBLGHCFOJ-UHFFFAOYSA-N 0.000 description 1
- ZKJYHDZCRMDJPA-UHFFFAOYSA-N tert-butyl 3-(7-bromo-4-phenylmethoxy-1,3-benzoxazol-2-yl)-3,6-diazabicyclo[3.1.1]heptane-6-carboxylate Chemical compound C(C1=CC=CC=C1)OC1=CC=C(C2=C1N=C(O2)N1CC2N(C(C1)C2)C(=O)OC(C)(C)C)Br ZKJYHDZCRMDJPA-UHFFFAOYSA-N 0.000 description 1
- FPLFDOOUHGQQHM-UHFFFAOYSA-N tert-butyl 3-[4-(1,1-difluoro-2-hydroxy-2-methylpropoxy)-7-(1,3-thiazol-2-yl)-1,3-benzoxazol-2-yl]-3,6-diazabicyclo[3.1.1]heptane-6-carboxylate Chemical compound FC(C(C)(C)O)(OC1=CC=C(C2=C1N=C(O2)N1CC2N(C(C1)C2)C(=O)OC(C)(C)C)C=1SC=CN=1)F FPLFDOOUHGQQHM-UHFFFAOYSA-N 0.000 description 1
- YQCNEUZMFPDKNZ-UHFFFAOYSA-N tert-butyl 3-[4-(2-ethoxy-1,1-difluoro-2-oxoethoxy)-7-(1,3-thiazol-2-yl)-1,3-benzoxazol-2-yl]-3,6-diazabicyclo[3.1.1]heptane-6-carboxylate Chemical compound C(C)OC(C(OC1=CC=C(C2=C1N=C(O2)N1CC2N(C(C1)C2)C(=O)OC(C)(C)C)C=1SC=CN=1)(F)F)=O YQCNEUZMFPDKNZ-UHFFFAOYSA-N 0.000 description 1
- KKUNANNSTFXBEN-UHFFFAOYSA-N tert-butyl 3-[4-hydroxy-7-(1,3-thiazol-2-yl)-1,3-benzoxazol-2-yl]-3,6-diazabicyclo[3.1.1]heptane-6-carboxylate Chemical compound OC1=CC=C(C2=C1N=C(O2)N1CC2N(C(C1)C2)C(=O)OC(C)(C)C)C=1SC=CN=1 KKUNANNSTFXBEN-UHFFFAOYSA-N 0.000 description 1
- 230000001256 tonic effect Effects 0.000 description 1
- FAQYAMRNWDIXMY-UHFFFAOYSA-N trichloroborane Chemical compound ClB(Cl)Cl FAQYAMRNWDIXMY-UHFFFAOYSA-N 0.000 description 1
- JABYJIQOLGWMQW-UHFFFAOYSA-N undec-4-ene Chemical compound CCCCCCC=CCCC JABYJIQOLGWMQW-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4995—Pyrazines or piperazines forming part of bridged ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/10—Anti-acne agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Diabetes (AREA)
- Pulmonology (AREA)
- Immunology (AREA)
- Psychiatry (AREA)
- Dermatology (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Pain & Pain Management (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
- Hospice & Palliative Care (AREA)
- Ophthalmology & Optometry (AREA)
- Child & Adolescent Psychology (AREA)
- Psychology (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Description
式(1)で示される化合物の合成
(工程1)(((2−ニトロ−1,3−フェニレン)ビス(オキシ))ビス(メチレン))ジベンゼン
2−ニトロレゾルシノール(5g)をN,N−ジメチルホルムアミド(88mL)に溶解し、ベンジルブロミド(8.4mL,2.2当量)及び炭酸セシウム(25g,2.4当量)を加え、室温で12時間攪拌した。反応液に酢酸エチルを加え1%塩酸水溶液で有機層を洗浄後、蒸留水で有機層を再度洗浄した。有機層を無水硫酸マグネシウムで乾燥後これを濾過し、濾液を減圧濃縮して得られた残渣にヘキサンを加え析出した固体を濾取して、表題の化合物を10g得た。
工程1で得られた化合物(10g)をジクロロメタン(270mL)に溶解し、−78℃で三塩化ホウ素の1.0Mヘプタン溶液(45mL,1.5当量)を加え、−78℃で1時間攪拌した。反応液にメタノールを10分間かけて加え室温に昇温し、蒸留水を加えた。この混合物をジクロロメタンで2回抽出し、有機層を無水硫酸マグネシウムで乾燥した。これを濾過し、濾液を減圧濃縮して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=9.5:0.5)で精製して、表題の化合物を4.7g得た。
工程2で得られた化合物(3.0g)にアセトニトリル(41mL)、クロロトリメチルシラン(0.16mL,0.1当量)及びN−ブロモスクシンイミド(2.2g,1.0当量)を加え室温で1時間攪拌した。0℃で反応液に水を加え、酢酸エチルで抽出した後、有機層を無水硫酸マグネシウムで乾燥した。濾過後、濾液を減圧濃縮して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=7:3)で精製して、表題の化合物を3.1g得た。
亜ジチオン酸ナトリウム(3.1g,8当量)の水溶液(63mL)に、工程3で得られた化合物(3.1g)のエタノール溶液(37mL)を0℃で滴下した。室温とした後、水(30mL)及びエタノール(18mL)を加え、1時間20分間攪拌した。反応液を濾過し、エタノールで洗浄した。濾液を減圧濃縮して得られた残渣に0℃で、水(67mL)を加え撹拌した。固体を濾取し、蒸留水、酢酸エチルで洗浄後、減圧乾燥して表題の化合物を3.3g得た。
工程4で得られた化合物(3.3g)をエタノール(15mL)に溶解し、0.5M水酸化カリウムのエタノール溶液(35mL)と二硫化炭素(2.9mL,5当量)を加え、50℃で1時間20分間加熱した。室温とした後、水(68mL)と5M塩酸(6mL)を加えた。固体を濾取し、表題の化合物を2.3g得た。
工程5で得られた化合物(2.3g)及びtert−ブチル 3,8−ジアザビシクロ[3.2.1]オクタン−8−カルボキシレート(1.5g,1.1当量)にm−キシレン(17mL)を加え、120℃で一晩攪拌した。1N水酸化ナトリウム水溶液(20mL)を加え、酢酸エチルで抽出した。有機層を無水硫酸マグネシウムで乾燥後、濾過し、濾液を減圧濃縮して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=50:1〜ヘキサン:酢酸エチル7:3)で精製して、表題の化合物を2.9g得た。
工程6で得られた化合物(2.9g)にトルエン(19mL)を加え、2−チアゾリルジンクブロミドの0.5Mテトラヒドロフラン溶液(29mL,2.5当量)及び1,1’−ビス(ジフェニルホスフィノ)フェロセンパラジウム(II)ジクロリド・ジクロロメタン錯体(480mg,0.1当量)を加え、アルゴン雰囲気下90℃で6時間攪拌した。反応液に飽和重曹水を加えセライト濾過した。濾液を酢酸エチルで抽出した後、有機層を無水硫酸マグネシウムで乾燥した。濾過後、濾液を減圧濃縮して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル9:1〜ヘキサン:酢酸エチル=1:1)で精製して、表題の化合物を2.5g得た。
工程7で得られた化合物(1.5g)をテトラヒドロフラン(60mL)に溶解し、アルゴン雰囲気下で20%水酸化パラジウム/炭素(水分含量50%)(2.5g)を加え、水素を充填し50℃で4.5時間攪拌した。反応液をセライト濾過し、濾液を減圧濃縮して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム〜クロロホルム:メタノール=94:6)で精製して、表題の化合物を1.0g得た。
工程8で得られた化合物(1.0g)をアセトニトリル(24mL)に溶解し、1,8−ジアザビシクロ[5.4.0]ウンデク−7−エン(3.6mL,10当量)とエチル 2−ブロモ−2,2−ジフルオロアセテート(3.1mL,10当量)を加え室温で2時間撹拌した。反応液に飽和塩化アンモニウム水溶液を加え、酢酸エチルで3回抽出した。有機層を無水硫酸マグネシウムで乾燥後、これを濾過し、濾液を減圧濃縮して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン〜ヘキサン:酢酸エチル=5:5)で精製して、表題の化合物を1.0g得た。
工程9で得られた化合物(92mg)をテトラヒドロフラン(1.7mL)に溶解し、0℃でメチルマグネシウムブロミドの0.95Mテトラヒドロフラン溶液(0.85mL,5当量)を加えた。室温に昇温後1時間撹拌し、飽和塩化アンモニウム水溶液を加え、酢酸エチルで3回抽出した。有機層を無水硫酸マグネシウムで乾燥後、これを濾過し、濾液を減圧濃縮して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン〜ヘキサン:酢酸エチル〜酢酸エチル)で精製して、表題の化合物を82mg得た。
工程10で得られた化合物(307mg)にクロロホルム(5.9mL)を加え、0℃でトリフルオロ酢酸(1.4mL)を加え、0℃で3.5時間攪拌した。反応液に飽和重曹水を加えクロロホルムで抽出した。有機層を無水硫酸マグネシウムで乾燥後、濾過し、濾液を減圧濃縮して得られた残渣をアミノシリカゲルカラムクロマトグラフィー(クロロホルム〜クロロホルム:メタノール=9:1)で精製して、式(1)で示される化合物を白色個体として223mg得た。
ESI−MS(m/z) 423(M+H)+
1H−NMR(クロロホルム‐d、TMS)δ(ppm):1.53(s,6H),1.65(d,J=9.3 Hz,1H),2.82−2.87(m,1H),3.90−4.01(m,7H),7.23−7.25(m,1H),7.44(d,J=3.3 Hz,1H),7.84(d,J=8.8 Hz,1H),7.94(d,J=3.3 Hz,1H).
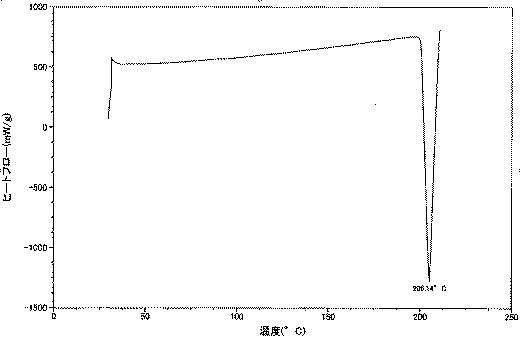
参考合成例1で得られた式(1)で示される化合物の固体(219mg)に酢酸エチルと2−プロパノールの混合溶媒(1:1,v/v)を21.9mL加え、60℃に加熱し溶解させた。本溶液を濃縮乾固し得られた残渣に、酢酸エチルと2−プロパノールの混合溶媒(1:1,v/v)4.38mLを加え、45℃で1時間撹拌した。室温とした後、ヘキサン21.9mLを加え1時間撹拌した。濾過後、ヘキサンで洗浄し乾燥させることで、I型結晶を194mg得た。得られたI型結晶は、粉末X線回折による回折角(2θ±0.2°)として、7.7°、9.4°、13.2°、13.7°、14.5°、15.7°、17.0°、18.9°、19.4°、22.9°、23.3°、25.7°、28.7°、35.7°に特徴的なピークを示した。I型結晶の粉末X線回折パターンを図1に示す。得られた結晶の示差走査熱量測定(DSC)分析の結果、205℃に吸熱ピークを認めた。I型結晶の示差走査熱量測定(DSC)熱分析データを図3に示す。
実施例1で得られたI型結晶584mgにメタノール50mLを加え溶解させた。減圧濃縮して約1/6の重量とし得られる均一な溶液を、0℃に冷却し10分間撹拌することで、固体を析出させた。濃縮乾固後、残渣にヘキサンと酢酸エチルの混合溶媒(2:1,v/v)を35mL加え、室温で30分間撹拌した。濾過後、ヘキサンと酢酸エチルの混合溶媒(2:1,v/v)で洗浄し乾燥させることで、II型結晶566mgを得た。得られたII型結晶は、粉末X線回折による回折角(2θ±0.2°)として、7.4°、7.8°、8.2°、12.7°、13.6°、14.3°、14.7°、15.7°、16.5°、19.3°、22.1°、25.0°、25.6°に特徴的なピークを示した。II型結晶の粉末X線回折パターンを図2に示す。
PDE4阻害活性はシンチレーション近接アッセイ(Scintillation Proximity Assay(SPA))を用いて、以下のようにして測定した。ジメチルスルホキシドに溶解した検体化合物を50mM Tris−HCl,pH7.4,8.3mM MgCl2,1.7mM EGTA,3mg/mL ウシ血清アルブミン(BSA)を含む反応用緩衝溶液で10倍希釈したものを、96ウェルのアッセイプレートに10μL加えた。さらに、反応用緩衝溶液で375倍希釈したPDE4を50μL加えた後、反応用緩衝溶液で1000倍希釈した[2,8−3H]−Adenosine−3’,5’−cyclic phosphate triethylammonium saltを40μL加え、室温で120分間静置した。その後、200mMのZnSO4を含むRNA binding YSi−SPA Beads懸濁液を50μL加え、室温で15分間静置して、酵素反応生成物をBeadsに吸着させた。その後、96ウェルプレート用液体シンチレーションカウンターにて放射活性を計測した。酵素標品を加えずに反応用緩衝溶液のみを加えたものをブランク、酵素標品を加えるが検体溶液の代わりにジメチルスルホキシドのみを加えたものをコントロールとし、式(1)で示される化合物のコントロールに対する阻害率を以下の計算式により計算した。
阻害率(%)={1−(検体添加時の数値−ブランク値)/(コントロール値−ブランク値)}×100
また被験化合物のPDE4阻害活性(50%阻害率における濃度)は各濃度における阻害率に基づく阻害曲線から算出した。
上記の方法により、式(1)で示される化合物のPDE4阻害活性(50%阻害率における濃度)は、100nM未満であった。
式(1)で示される化合物のI型結晶及びII型結晶(各々約300mg)をガラス瓶に入れ、各条件下で保存した。保存期間後、取り出した試料をHPLCにより化学純度を測定した。各試験の条件は以下の通りである。
熱安定性試験:60℃、気密、期間3週間
光安定性試験:25℃、120万ルクス時間(2000ルクス、25日間)
加速安定性試験(気密):40℃、75%RH*、期間1か月
加速安定性試験(開放):40℃、75%RH*、期間1か月
*RH:相対湿度
各安定性の評価結果は、結晶中に含まれる式(1)で示される化合物の量を、残存率(初期値に対するHPLCの面積百分率の比をパーセント表示)として表1に示した。
式(1)で示される化合物のI型結晶及びII型結晶について、水蒸気吸着測定装置(Surface Measurement Systems社製、DVS Advantage 1)を用いて等温吸着測定を行った(試料約10mg、25℃、0〜95%RH)。
吸湿性の評価結果は、95%RHにおける重量増加率(初期値からの重量増加/初期値×100、※初期値:0%RHにおける重量平衡値)として表2に示した。
<1>式(1)
<2>粉末X線回折による回折角(2θ±0.2°)として、7.7°、14.5°、17.0°、18.9°、19.4°、23.3°、25.7°に特徴的なピークを有する、前記<1>に記載の結晶である。
<3>粉末X線回折による回折角(2θ±0.2°)として、7.7°、9.4°、13.2°、13.7°、14.5°、15.7°、17.0°、18.9°、19.4°、22.9°、23.3°、25.7°、28.7°、35.7°に特徴的なピークを有する、前記<1>に記載の結晶である。
<4>示差走査熱量測定(DSC)による吸熱ピーク温度が205±3℃であることを特徴とする、前記<2>または<3>に記載の結晶である。
<5>粉末X線回折による回折角(2θ±0.2°)として、7.8°、14.7°、15.7°、19.3°、25.0°に特徴的なピークを有する、前記<1>に記載の結晶である。
<6>粉末X線回折による回折角(2θ±0.2°)として、7.4°、7.8°、8.2°、12.7°、13.6°、14.3°、14.7°、15.7°、16.5°、19.3°、22.1°、25.0°、25.6°に特徴的なピークを有する、前記<1>に記載の結晶である。
<7>前記<1>〜<6>のいずれかに記載の結晶を含む、医薬組成物である。
Claims (7)
- 粉末X線回折による回折角(2θ±0.2°)として、7.7°、14.5°、17.0°、18.9°、19.4°、23.3°、25.7°に特徴的なピークを有する、請求項1に記載の結晶。
- 粉末X線回折による回折角(2θ±0.2°)として、7.7°、9.4°、13.2°、13.7°、14.5°、15.7°、17.0°、18.9°、19.4°、22.9°、23.3°、25.7°、28.7°、35.7°に特徴的なピークを有する、請求項1に記載の結晶。
- 示差走査熱量測定(DSC)による吸熱ピーク温度が205±3℃であることを特徴とする、請求項2または請求項3に記載の結晶。
- 粉末X線回折による回折角(2θ±0.2°)として、7.8°、14.7°、15.7°、19.3°、25.0°に特徴的なピークを有する、請求項1に記載の結晶。
- 粉末X線回折による回折角(2θ±0.2°)として、7.4°、7.8°、8.2°、12.7°、13.6°、14.3°、14.7°、15.7°、16.5°、19.3°、22.1°、25.0°、25.6°に特徴的なピークを有する、請求項1に記載の結晶。
- 請求項1〜6のいずれか一項に記載の結晶を含む、医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018121413 | 2018-06-27 | ||
| JP2018121413 | 2018-06-27 | ||
| PCT/JP2019/025512 WO2020004517A1 (ja) | 2018-06-27 | 2019-06-27 | ベンゾオキサゾール誘導体の結晶 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP6831496B2 true JP6831496B2 (ja) | 2021-02-17 |
| JPWO2020004517A1 JPWO2020004517A1 (ja) | 2021-02-25 |
Family
ID=68986306
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020527613A Active JP6831496B2 (ja) | 2018-06-27 | 2019-06-27 | ベンゾオキサゾール誘導体の結晶 |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US11512091B2 (ja) |
| EP (1) | EP3816167B1 (ja) |
| JP (1) | JP6831496B2 (ja) |
| KR (1) | KR20210024551A (ja) |
| CN (1) | CN112351986B (ja) |
| AR (1) | AR114977A1 (ja) |
| AU (1) | AU2019293572B2 (ja) |
| BR (1) | BR112020026202A2 (ja) |
| CA (1) | CA3104829A1 (ja) |
| ES (1) | ES2926469T3 (ja) |
| IL (1) | IL279763B2 (ja) |
| MX (1) | MX2020014317A (ja) |
| NZ (1) | NZ772151A (ja) |
| TW (1) | TWI788580B (ja) |
| WO (1) | WO2020004517A1 (ja) |
| ZA (1) | ZA202100484B (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3815687A4 (en) * | 2018-06-27 | 2022-03-16 | Meiji Seika Pharma Co., Ltd. | THERAPEUTIC AGENT AGAINST INFLAMMATORY DISEASES, AUTOIMMUNE DISEASES, FIBROTIC DISEASES AND CANCER DISEASES |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2570769T3 (es) | 2008-12-19 | 2016-05-20 | Leo Pharma As | Triazolopiridinas como inhibidores fosfodiesterasa para el tratamiento de enfermedades dérmicas |
| ES2714705T3 (es) * | 2013-07-10 | 2019-05-29 | Meiji Seika Pharma Co Ltd | Inhibidor de PDE4 novedoso |
| WO2018104060A1 (en) * | 2016-12-05 | 2018-06-14 | Telefonaktiebolaget Lm Ericsson (Publ) | Service continuity after an application server fallback |
| US10669283B2 (en) | 2016-12-26 | 2020-06-02 | Meiji Seika Pharma Co., Ltd. | Compound and pharmacologically acceptable salt thereof |
| EP3815687A4 (en) | 2018-06-27 | 2022-03-16 | Meiji Seika Pharma Co., Ltd. | THERAPEUTIC AGENT AGAINST INFLAMMATORY DISEASES, AUTOIMMUNE DISEASES, FIBROTIC DISEASES AND CANCER DISEASES |
-
2019
- 2019-06-24 AR ARP190101746A patent/AR114977A1/es unknown
- 2019-06-27 BR BR112020026202-1A patent/BR112020026202A2/pt unknown
- 2019-06-27 US US17/255,584 patent/US11512091B2/en active Active
- 2019-06-27 TW TW108122583A patent/TWI788580B/zh active
- 2019-06-27 CN CN201980042488.5A patent/CN112351986B/zh active Active
- 2019-06-27 CA CA3104829A patent/CA3104829A1/en active Pending
- 2019-06-27 ES ES19826594T patent/ES2926469T3/es active Active
- 2019-06-27 KR KR1020217001557A patent/KR20210024551A/ko not_active Application Discontinuation
- 2019-06-27 WO PCT/JP2019/025512 patent/WO2020004517A1/ja unknown
- 2019-06-27 EP EP19826594.4A patent/EP3816167B1/en active Active
- 2019-06-27 IL IL279763A patent/IL279763B2/en unknown
- 2019-06-27 NZ NZ772151A patent/NZ772151A/en unknown
- 2019-06-27 MX MX2020014317A patent/MX2020014317A/es unknown
- 2019-06-27 AU AU2019293572A patent/AU2019293572B2/en active Active
- 2019-06-27 JP JP2020527613A patent/JP6831496B2/ja active Active
-
2021
- 2021-01-22 ZA ZA2021/00484A patent/ZA202100484B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| ZA202100484B (en) | 2022-08-31 |
| JPWO2020004517A1 (ja) | 2021-02-25 |
| CA3104829A1 (en) | 2020-01-02 |
| IL279763B2 (en) | 2024-02-01 |
| TW202000664A (zh) | 2020-01-01 |
| KR20210024551A (ko) | 2021-03-05 |
| US11512091B2 (en) | 2022-11-29 |
| AU2019293572B2 (en) | 2024-01-04 |
| BR112020026202A2 (pt) | 2021-03-23 |
| MX2020014317A (es) | 2021-03-09 |
| WO2020004517A1 (ja) | 2020-01-02 |
| AU2019293572A1 (en) | 2021-02-11 |
| EP3816167B1 (en) | 2022-08-03 |
| AR114977A1 (es) | 2020-11-11 |
| US20210155630A1 (en) | 2021-05-27 |
| ES2926469T3 (es) | 2022-10-26 |
| EP3816167A4 (en) | 2021-12-15 |
| CN112351986A (zh) | 2021-02-09 |
| CN112351986B (zh) | 2023-04-18 |
| TWI788580B (zh) | 2023-01-01 |
| EP3816167A1 (en) | 2021-05-05 |
| IL279763A (en) | 2021-03-01 |
| IL279763B1 (en) | 2023-10-01 |
| NZ772151A (en) | 2024-03-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2018086547A1 (zh) | 2-取代芳环-嘧啶类衍生物及制备和应用 | |
| EP3337485B1 (en) | Crystalline forms of ibrutinib | |
| JP2011515370A (ja) | 4−アミノ−5−フルオロ−3−[5−(4−メチルピペラジン−1−イル)−1h−ベンズイミダゾール−2−イル]キノリン−2(1h)−オン乳酸塩の結晶形態及び2つの溶媒和物形態 | |
| AU2015414743B2 (en) | Process for the preparation of kinase inhibitors and intermediates thereof | |
| JP2019509320A (ja) | 1−(5−(2,4−ジフルオロフェニル)−1−((3−フルオロフェニル)スルホニル)−4−メトキシ−1h−ピロール−3−イル)−n−メチルメタンアミンの新規な酸付加塩 | |
| WO2018181345A1 (ja) | 複素環化合物 | |
| JP6632127B2 (ja) | トロンボポエチン受容体アゴニスト作用を有する光学活性な化合物およびその中間体の製造方法 | |
| JPWO2009004792A1 (ja) | スルホンアミド化合物及びその結晶 | |
| JP6831496B2 (ja) | ベンゾオキサゾール誘導体の結晶 | |
| JPWO2018117267A1 (ja) | 置換ピペリジン化合物の塩 | |
| TW201840557A (zh) | (s)-[2-氯-4-氟-5-(7-嗎啉-4-基喹唑啉-4-基)苯基]-(6-甲氧基-嗒𠯤-3-基)-甲醇之結晶型 | |
| WO2021075494A1 (ja) | センタナファジンの製造方法 | |
| JP2020535193A (ja) | 結晶のリナグリプチン中間体およびリナグリプチンの調製のためのプロセス | |
| TWI714702B (zh) | 一種吡啶衍生物類化合物的製備方法及其中間體和晶型 | |
| TWI706949B (zh) | (3-胺基-環氧丙-3-基甲基)-[2-(5,5-二氧-5,6,7,9-四氫-5入*6*-硫-8-氮雜-苯并環庚烯-8-基)-6-甲基-喹唑啉-4-基]-胺之新穎晶形 | |
| KR20120098745A (ko) | 치환된 피라졸로피리미딘의 결정질 형태 | |
| JP6974618B2 (ja) | Fgfr及びvegfr阻害剤としての化合物の塩形態、結晶形およびその製造方法 | |
| JP5065020B2 (ja) | レボフロキサシンまたはその水和物の製造方法 | |
| RU2787767C2 (ru) | Кристалл производного бензоксазола | |
| WO2023060362A1 (en) | Ras inhibitors, compositions and methods of use thereof | |
| JP2022520629A (ja) | 固体形態のfgfr阻害剤化合物およびその製造方法 | |
| JP5622565B2 (ja) | 安定なヴィナミジニウム塩およびそれを用いた含窒素複素環合成 | |
| JP7333420B2 (ja) | トリアゾロピリミジン化合物及びその塩、組成物と使用 | |
| TW201922733A (zh) | 作為fgfr4抑制劑化合物的鹽型、晶型及其製備方法 | |
| RU2809821C2 (ru) | Соединения на основе триазолопиримидина и их соли, композиции на их основе и пути их применения |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20201014 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20201014 |
|
| AA64 | Notification of invalidation of claim of internal priority (with term) |
Free format text: JAPANESE INTERMEDIATE CODE: A241764 Effective date: 20201027 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20201104 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20201210 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210112 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210128 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6831496 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |