JP6749685B2 - 被験物質の皮膚感作性の検定方法 - Google Patents
被験物質の皮膚感作性の検定方法 Download PDFInfo
- Publication number
- JP6749685B2 JP6749685B2 JP2016092093A JP2016092093A JP6749685B2 JP 6749685 B2 JP6749685 B2 JP 6749685B2 JP 2016092093 A JP2016092093 A JP 2016092093A JP 2016092093 A JP2016092093 A JP 2016092093A JP 6749685 B2 JP6749685 B2 JP 6749685B2
- Authority
- JP
- Japan
- Prior art keywords
- peptide
- resin
- test substance
- immobilized
- linker
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000000126 substance Substances 0.000 title claims description 111
- 238000012360 testing method Methods 0.000 title claims description 102
- 238000003556 assay Methods 0.000 title claims description 36
- 206010070835 Skin sensitisation Diseases 0.000 title claims description 27
- 231100000370 skin sensitisation Toxicity 0.000 title claims description 27
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 193
- 238000000034 method Methods 0.000 claims description 50
- 229920005989 resin Polymers 0.000 claims description 41
- 239000011347 resin Substances 0.000 claims description 41
- 238000003776 cleavage reaction Methods 0.000 claims description 16
- 150000001875 compounds Chemical class 0.000 claims description 16
- 230000007017 scission Effects 0.000 claims description 16
- 231100000121 skin sensitizing Toxicity 0.000 claims description 14
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 claims description 11
- 150000001413 amino acids Chemical class 0.000 claims description 9
- 238000004587 chromatography analysis Methods 0.000 claims description 9
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 claims description 7
- 235000001014 amino acid Nutrition 0.000 claims description 6
- 229920005862 polyol Polymers 0.000 claims description 3
- 150000003077 polyols Chemical class 0.000 claims description 3
- 238000006116 polymerization reaction Methods 0.000 claims description 2
- 239000002904 solvent Substances 0.000 description 22
- 231100000051 skin sensitiser Toxicity 0.000 description 19
- 238000000926 separation method Methods 0.000 description 15
- -1 olive oil Chemical compound 0.000 description 14
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 11
- 238000004128 high performance liquid chromatography Methods 0.000 description 11
- 239000000203 mixture Substances 0.000 description 11
- 102000004196 processed proteins & peptides Human genes 0.000 description 11
- 125000006239 protecting group Chemical group 0.000 description 11
- 239000003795 chemical substances by application Substances 0.000 description 9
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 8
- 210000004899 c-terminal region Anatomy 0.000 description 8
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 8
- QWXZOFZKSQXPDC-NSHDSACASA-N (2s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)propanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H](C)C(O)=O)C3=CC=CC=C3C2=C1 QWXZOFZKSQXPDC-NSHDSACASA-N 0.000 description 7
- 239000003513 alkali Substances 0.000 description 7
- 125000003277 amino group Chemical group 0.000 description 7
- 239000003153 chemical reaction reagent Substances 0.000 description 7
- 150000002430 hydrocarbons Chemical group 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 6
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 239000000654 additive Substances 0.000 description 6
- 239000011324 bead Substances 0.000 description 6
- 238000005119 centrifugation Methods 0.000 description 6
- 238000001914 filtration Methods 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 238000002156 mixing Methods 0.000 description 6
- 229920001223 polyethylene glycol Polymers 0.000 description 6
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 5
- 229910052753 mercury Inorganic materials 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 125000001433 C-terminal amino-acid group Chemical group 0.000 description 4
- 0 CCC(C=C)C(CC(CC=CC(C)C(CCCCCC(C)C1*=CC1)C1C(C)C1)c1ccccc1C(C)CCCCC1CCC1)=C Chemical compound CCC(C=C)C(CC(CC=CC(C)C(CCCCCC(C)C1*=CC1)C1C(C)C1)c1ccccc1C(C)CCCCC1CCC1)=C 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 4
- 125000001429 N-terminal alpha-amino-acid group Chemical group 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 125000000524 functional group Chemical group 0.000 description 4
- SJVFAHZPLIXNDH-QFIPXVFZSA-N (2s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-3-phenylpropanoic acid Chemical compound C([C@@H](C(=O)O)NC(=O)OCC1C2=CC=CC=C2C2=CC=CC=C21)C1=CC=CC=C1 SJVFAHZPLIXNDH-QFIPXVFZSA-N 0.000 description 3
- VZXQYACYLGRQJU-IBGZPJMESA-N (3s)-3-(9h-fluoren-9-ylmethoxycarbonylamino)-4-[(2-methylpropan-2-yl)oxy]-4-oxobutanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H](CC(O)=O)C(=O)OC(C)(C)C)C3=CC=CC=C3C2=C1 VZXQYACYLGRQJU-IBGZPJMESA-N 0.000 description 3
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 3
- LINBWYYLPWJQHE-UHFFFAOYSA-N 3-(9h-fluoren-9-ylmethoxycarbonylamino)propanoic acid Chemical compound C1=CC=C2C(COC(=O)NCCC(=O)O)C3=CC=CC=C3C2=C1 LINBWYYLPWJQHE-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 229940019836 cyclamen aldehyde Drugs 0.000 description 3
- 238000010828 elution Methods 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- LQNUZADURLCDLV-UHFFFAOYSA-N nitrobenzene Chemical group [O-][N+](=O)C1=CC=CC=C1 LQNUZADURLCDLV-UHFFFAOYSA-N 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- ZFNVDHOSLNRHNN-UHFFFAOYSA-N xi-3-(4-Isopropylphenyl)-2-methylpropanal Chemical compound O=CC(C)CC1=CC=C(C(C)C)C=C1 ZFNVDHOSLNRHNN-UHFFFAOYSA-N 0.000 description 3
- KLBPUVPNPAJWHZ-UMSFTDKQSA-N (2r)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-3-tritylsulfanylpropanoic acid Chemical compound C([C@@H](C(=O)O)NC(=O)OCC1C2=CC=CC=C2C2=CC=CC=C21)SC(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 KLBPUVPNPAJWHZ-UMSFTDKQSA-N 0.000 description 2
- UMRUUWFGLGNQLI-QFIPXVFZSA-N (2s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-6-[(2-methylpropan-2-yl)oxycarbonylamino]hexanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H](CCCCNC(=O)OC(C)(C)C)C(O)=O)C3=CC=CC=C3C2=C1 UMRUUWFGLGNQLI-QFIPXVFZSA-N 0.000 description 2
- RTZZCYNQPHTPPL-UHFFFAOYSA-N 3-nitrophenol Chemical group OC1=CC=CC([N+]([O-])=O)=C1 RTZZCYNQPHTPPL-UHFFFAOYSA-N 0.000 description 2
- DRESTDPDCGPKNI-OAQYLSRUSA-N 517905-93-0 Chemical compound C1([C@H](NC(=O)OCC2C3=CC=CC=C3C3=CC=CC=C32)CC(=O)O)=CC=CC=C1[N+]([O-])=O DRESTDPDCGPKNI-OAQYLSRUSA-N 0.000 description 2
- RWQUWTMOHXGTNN-UHFFFAOYSA-N 9-n,10-n-bis(4-butylphenyl)-9-n,10-n-bis(4-methylphenyl)phenanthrene-9,10-diamine Chemical compound C1=CC(CCCC)=CC=C1N(C=1C2=CC=CC=C2C2=CC=CC=C2C=1N(C=1C=CC(C)=CC=1)C=1C=CC(CCCC)=CC=1)C1=CC=C(C)C=C1 RWQUWTMOHXGTNN-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- BKNNPGVXULBULJ-UHFFFAOYSA-N CC(CCCNC(N)=N)NC(C)=O Chemical compound CC(CCCNC(N)=N)NC(C)=O BKNNPGVXULBULJ-UHFFFAOYSA-N 0.000 description 2
- JNWJQOCPCZKSQI-UHFFFAOYSA-N CC(Cc1ccccc1)N=O Chemical compound CC(Cc1ccccc1)N=O JNWJQOCPCZKSQI-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 101000881943 Homo sapiens Protein EURL homolog Proteins 0.000 description 2
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 2
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 2
- 239000004472 Lysine Substances 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 102100037083 Protein EURL homolog Human genes 0.000 description 2
- 229920002125 Sokalan® Polymers 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 239000003905 agrochemical Substances 0.000 description 2
- 229920003180 amino resin Polymers 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 235000003704 aspartic acid Nutrition 0.000 description 2
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- 239000003599 detergent Substances 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 238000000132 electrospray ionisation Methods 0.000 description 2
- 150000002148 esters Chemical group 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 230000001678 irradiating effect Effects 0.000 description 2
- ZXEKIIBDNHEJCQ-UHFFFAOYSA-N isobutanol Chemical compound CC(C)CO ZXEKIIBDNHEJCQ-UHFFFAOYSA-N 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 125000006178 methyl benzyl group Chemical group 0.000 description 2
- 239000012046 mixed solvent Substances 0.000 description 2
- 239000003002 pH adjusting agent Substances 0.000 description 2
- 239000004584 polyacrylic acid Substances 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 239000002002 slurry Substances 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 238000010998 test method Methods 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- 125000002088 tosyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])S(*)(=O)=O 0.000 description 2
- ZGYICYBLPGRURT-UHFFFAOYSA-N tri(propan-2-yl)silicon Chemical compound CC(C)[Si](C(C)C)C(C)C ZGYICYBLPGRURT-UHFFFAOYSA-N 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- HNICLNKVURBTKV-NDEPHWFRSA-N (2s)-5-[[amino-[(2,2,4,6,7-pentamethyl-3h-1-benzofuran-5-yl)sulfonylamino]methylidene]amino]-2-(9h-fluoren-9-ylmethoxycarbonylamino)pentanoic acid Chemical compound C12=CC=CC=C2C2=CC=CC=C2C1COC(=O)N[C@H](C(O)=O)CCCN=C(N)NS(=O)(=O)C1=C(C)C(C)=C2OC(C)(C)CC2=C1C HNICLNKVURBTKV-NDEPHWFRSA-N 0.000 description 1
- HCGYMSSYSAKGPK-UHFFFAOYSA-N 2-nitro-1h-indole Chemical group C1=CC=C2NC([N+](=O)[O-])=CC2=C1 HCGYMSSYSAKGPK-UHFFFAOYSA-N 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- UPGNSNJMTGKMRN-UHFFFAOYSA-N CC(CCCCN)NC(C(C)N=O)=O Chemical compound CC(CCCCN)NC(C(C)N=O)=O UPGNSNJMTGKMRN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 231100000493 OECD 406 (Buehler) Skin Sensitisation Toxicity 0.000 description 1
- 231100000220 OECD 429 (LLNA) Skin Sensitisation Toxicity 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000002723 alicyclic group Chemical group 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 239000012670 alkaline solution Substances 0.000 description 1
- 208000030961 allergic reaction Diseases 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 238000004873 anchoring Methods 0.000 description 1
- 239000012062 aqueous buffer Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 1
- 238000000065 atmospheric pressure chemical ionisation Methods 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 125000000332 coumarinyl group Chemical group O1C(=O)C(=CC2=CC=CC=C12)* 0.000 description 1
- GCFAUZGWPDYAJN-UHFFFAOYSA-N cyclohexyl 3-phenylprop-2-enoate Chemical group C=1C=CC=CC=1C=CC(=O)OC1CCCCC1 GCFAUZGWPDYAJN-UHFFFAOYSA-N 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 238000001641 gel filtration chromatography Methods 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000000816 matrix-assisted laser desorption--ionisation Methods 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 229910001507 metal halide Inorganic materials 0.000 description 1
- 150000005309 metal halides Chemical class 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 229920003207 poly(ethylene-2,6-naphthalate) Polymers 0.000 description 1
- 229920001707 polybutylene terephthalate Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 239000011112 polyethylene naphthalate Substances 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000012279 sodium borohydride Substances 0.000 description 1
- 229910000033 sodium borohydride Inorganic materials 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 238000010532 solid phase synthesis reaction Methods 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
Description
(式中、Pはリジン残基を1個以上含むペプチド又はシステイン残基を1個以上含むペプチドを示す。L’は2価の炭化水素基、エーテル結合、チオエーテル結合、エステル結合、アミド結合、カルボニル基、又はこれらの2以上が結合した2価の基を示す。Rは樹脂を示す。)
本発明の検定方法は、特定の樹脂固定ペプチドに被験物質を接触させた後、ペプチドと被験物質との結合の有無を測定することを特徴とする。被験物質に皮膚感作性物質が含まれる場合は、樹脂固定ペプチドと被験物質とを接触させることで、被験物質に含まれる皮膚感作性物質が樹脂固定ペプチドのペプチド部位と反応・結合し、結合物が生じる。一方、被験物質に皮膚感作性物質が含まれない場合は、前記の結合物は生じない。本発明は、この様な結合の有無(結合物の有無)を測定することで、被験物質に皮膚感作性物質が含まれるか否かを判断するものである。
工程A:樹脂固定ペプチドと被験物質とを接触させる工程
工程B:工程Aにより得られた混合物から、樹脂固定ペプチド(被験物質と結合したものを含む)を分離する工程
工程C:工程Bで分離した樹脂固定ペプチド(被験物質と結合したものを含む)のリンカー部を切断する工程
工程D:工程Cにて生じたペプチド部位を含む化合物(被験物質と結合したものを含む)を分離する工程
工程E:工程Dにて分離されたペプチド部位を含む化合物(被験物質と結合したものを含む)について、ペプチドと被験物質との結合の有無を測定する工程
本発明の検定方法における工程Aは、樹脂固定ペプチドと被験物質とを接触させる工程である。本工程において、被験物質に皮膚感作性物質が含まれる場合は、樹脂固定ペプチドと被験物質とを接触させることにより、樹脂固定ペプチドのペプチド部位と皮膚感作性物質とが結合することとなる。接触させる方法としては、例えば、樹脂固定ペプチドと被験物質とを溶媒中で混合させる方法が挙げられる。また、混合した後に静置する工程を有していても良い。
本発明の検定方法における工程Bは、工程Aにて得られた混合物から、樹脂固定ペプチド(被験物質と結合したものを含む)を分離する工程である。工程Bにおける分離方法としては、例えば、遠心分離、フィルターろ過による分離、磁性ビーズを利用した分離等が挙げられる。なお、工程Bにて用いられる溶媒は特に限定されず、例えば、工程Aにて例示したものを用いることができる。
本発明の検定方法における工程Cは、工程Bで分離した樹脂固定ペプチド(被験物質と結合したものを含む)のリンカー部を切断する工程である。これにより、切断リンカーの一部を含むペプチド(被験物質と結合したものを含む)と、切断リンカーの一部を含む樹脂が得られる。なお、切断リンカーの一部を含むペプチドを、「ペプチド部位を含む化合物」と称する場合がある。なお、工程Cにて用いられる溶媒は特に限定されず、例えば、工程Aにて例示したものを用いることができる。
本発明の検定方法における工程Dは、工程Cにて生じたペプチド部位を含む化合物(被験物質と結合したものを含む)を分離する工程である。より具体的には、工程Bにおける分離方法として例示した、遠心分離、フィルターろ過による分離、磁性ビーズを利用した分離等により、工程Cにて生じるペプチド部位を含む化合物(被験物質と結合したものを含む)を分離し、切断リンカーの一部を含む樹脂を除去する工程である。なお、工程Dにて用いられる溶媒は特に限定されず、例えば、工程Aにて例示したものを用いることができる。
本発明の検定方法における工程Eは、工程Dにて分離されたペプチド部位を含む化合物(被験物質と結合したものを含む)について、ペプチドと被験物質との結合の有無を測定する工程である。具体的な測定方法としては特に限定されないが、例えば、イオン交換クロマトグラフィー、ゲルろ過クロマトグラフィー、順相クロマトグラフィー、逆相クロマトグラフィー、薄層クロマトグラフィー法(TLC)等のクロマトグラフィー法を用いた方法が挙げられる。具体的には、例えば、樹脂固定ペプチドと被験物質とを接触させて得られるサンプル(溶液)と、樹脂固定ペプチドのみを含むリファレンス(溶液)とを用意し、必要に応じて上記の工程B〜Dを行った後にそれぞれをクロマトグラフィー法にて測定し、得られる量比(例えばHPLCにて得られるピークの面積)の差から、ペプチドと被験物質との結合物が生じているか否かを判断する方法が挙げられる。
本発明の樹脂固定ペプチドは、皮膚感作性物質との結合能を有するペプチド(以下、「ペプチド」と称する場合がある)と樹脂とが切断リンカーを介して結合した樹脂固定ペプチドである。なお、本発明の樹脂固定ペプチドは下記式(1)で表すことができ、式中のPは皮膚感作性物質との結合能を有するペプチド(ペプチド部位)、Lは切断リンカー(リンカー部位)、Rは樹脂(樹脂部位)を示す。
P−L−R (1)
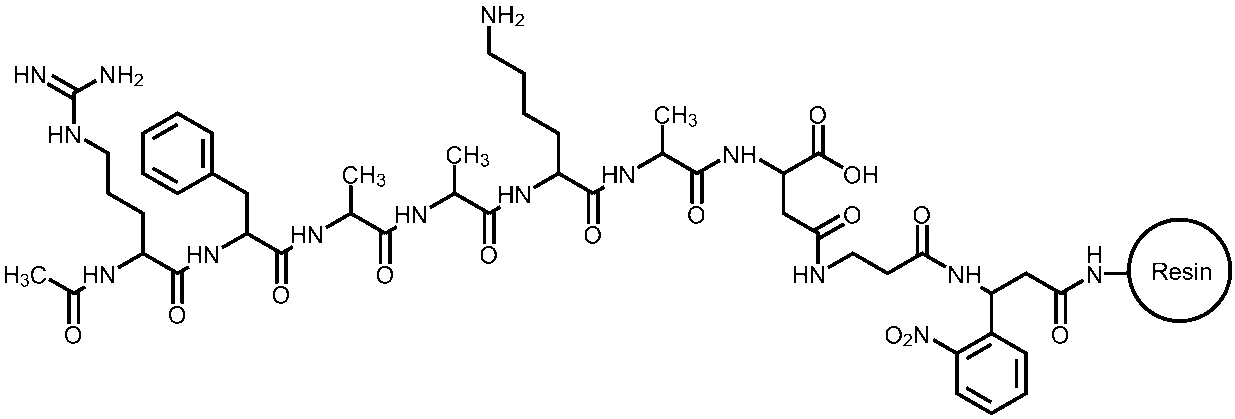
NH2−PEG樹脂(官能基導入率0.2mmol/g)上のアミノ基とFmoc−Phg(2−NO2)−(C#CH2)OHをカップリングさせた。次に、得られた反応生成物のFmoc基をピペリジンで脱保護し、脱保護されたアミノ基とFmoc−βAla−OHとをカップリングさせた。以下、同様の手法を用いて、Fmoc−Asp−Otbu、Fmoc−Ala−OH、Fmoc−Lys(Boc)−OH、Fmoc−Ala−OH、Fmoc−Ala−OH、Fmoc−Phe−OH、Fmoc−Arg(Pbf)−OHの順にカップリングを行い、無水酢酸を反応させた後、脱保護溶液(水:トリイソプロピルシラン:TFA(体積比)=0.02:0.02:1)で2時間反応させ、洗浄及び乾燥を行うことで、以下のモデル構造を有する樹脂固定ペプチド(1)を作製した。
NH2−PEG樹脂(官能基導入率0.2mmol/g)上のアミノ基とFmoc−Phg(2−NO2)−(C#CH2)OHをカップリングさせた。次に、得られた反応生成物のFmoc基をピペリジンで脱保護し、脱保護されたアミノ基とFmoc−βAla−OHとをカップリングさせた。以下、同様の手法を用いて、Fmoc−Asp−Otbu、Fmoc−Ala−OH、Fmoc−Cys(Trt)−OH、Fmoc−Ala−OH、Fmoc−Ala−OH、Fmoc−Phe−OH、Fmoc−Arg(Pbf)−OHの順にカップリングを行い、無水酢酸を反応させた後、脱保護溶液(水:トリイソプロピルシラン:TFA(体積比)=0.02:0.02:1)で2時間反応させ、洗浄及び乾燥を行うことで、以下のモデル構造を有する樹脂固定ペプチド(2)を作製した。
以下の操作手順でエチルアクリレートの皮膚感作性を検定した。
1mgの樹脂固定ペプチド(1)を、5mlのチューブ(株式会社ハイペップ研究所製)に入れ、500μlのDMFで5回洗浄した後、500μlのA溶媒(水:TFA(体積比)=100:0.1)で5回洗浄した。次に、1mlの0.1重量%トリエチルアミンを含むDMFにエチルアクリレートの濃度が100mMになるように添加して調製したものに樹脂固定ペプチド(1)を添加し、24時間反応させた。次に、500μlのDMFで5回洗浄した後、500μlのA溶媒で5回洗浄した。次に、A溶媒を500μl加えて撹拌した後、ピペットを使用してエッペンドルフチューブに回収した。次に、15000rpm×1minの条件で遠心し、上清を廃棄した後、再度A溶媒を500μl加えて撹拌する操作を4回繰り返した。次に、400μlのA溶媒を投入し、紫外−可視ファイバ光源(浜松ホトニクス、LED光源用コントローラ(C11924))を用い、光量80%、照射距離:5cmの条件で、20分間、光(波長:約365nm)を照射した。次に、光照射後の試料を遠心(15000rpm×1min)し、その上清をフィルター(ミリポア 0.45μm 100/pk:メルク社製)へ移すと共に、遠心(15000rpm×1min)し、100μlとなった所でHPLC測定(カラム;zorbax社製SB−C18(2.1×100mm)、A溶媒;水:TFA(体積比)=100:0.1、B溶媒;アセトニトリル:TFA=100:0.08、グラジエント;0分/B溶媒10%、11分/B溶媒90%;流速:0.35ml/分)を行った。以下に、樹脂固定ペプチド(1)に光を照射して得られる切断物のモデルを示す。
エチルアクリレートの代わりにシクラメンアルデヒドを用いたこと以外は実施例1と同様にして、HPLC測定を行った。
皮膚感作性物質(エチルアクリレート)を用いないこと以外は実施例1と同様にして、HPLC測定を行った。
樹脂固定ペプチド(1)の代わりに樹脂固定ペプチド(2)を用いたこと以外は実施例1と同様にして、HPLC測定を行った。
樹脂固定ペプチド(1)の代わりに樹脂固定ペプチド(2)を用いたこと以外は実施例2と同様にして、HPLC測定を行った。
皮膚感作性物質を用いないこと以外は実施例3と同様にして、HPLC測定を行った。
実施例1にて得られたHPLCのチャートと、そのリファレンスにて得られたHPLCのチャートとを比較することで、樹脂固定ペプチドのペプチド部位に由来する溶出ピーク面積が減少することを確認した。このことから、実施例1において、樹脂固定ペプチドのペプチド部位にエチルアクリレートが結合したことが示唆された。さらに、樹脂固定ペプチド(1)から切断されたペプチド部分とエチルアクリレートとの結合物に由来すると考えられる溶出ピークが見られた。また、実施例2〜4においても同様の結果が得られた。
Claims (4)
- 前記の樹脂固定ペプチドに被験物質を接触させた後、前記の樹脂固定ペプチドのリンカー部を切断し、生成したペプチド部位を含む化合物について、ペプチドと被験物質との結合の有無を測定することを特徴とする請求項1又は2に記載の被験物質の皮膚感作性の検定方法。
- ペプチドと被験物質との結合の有無を、クロマトグラフィー法を用いて測定する請求項1〜3の何れか1項に記載の被験物質の皮膚感作性の検定方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016092093A JP6749685B2 (ja) | 2016-04-28 | 2016-04-28 | 被験物質の皮膚感作性の検定方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016092093A JP6749685B2 (ja) | 2016-04-28 | 2016-04-28 | 被験物質の皮膚感作性の検定方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017198637A JP2017198637A (ja) | 2017-11-02 |
| JP6749685B2 true JP6749685B2 (ja) | 2020-09-02 |
Family
ID=60239263
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016092093A Expired - Fee Related JP6749685B2 (ja) | 2016-04-28 | 2016-04-28 | 被験物質の皮膚感作性の検定方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6749685B2 (ja) |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5241012A (en) * | 1987-05-19 | 1993-08-31 | Applied Immune Sciences, Inc. | Activated and conjugated polystyrene substrate |
| DE19654764A1 (de) * | 1996-12-30 | 1998-07-02 | Boehringer Mannheim Gmbh | Verfahren zur Herstellung eines Peptidgemisches |
| JP4750035B2 (ja) * | 2004-07-30 | 2011-08-17 | 株式会社リバース・プロテオミクス研究所 | 光切断型リンカーを利用したリガンド固定化固相担体 |
| FR2945042B1 (fr) * | 2009-04-30 | 2016-05-13 | Immunosearch | Nouveaux polypeptides pour l'evaluation in vitro du potentiel sensibilisant d'un compose test |
| KR101617407B1 (ko) * | 2010-01-08 | 2016-05-02 | (주)아모레퍼시픽 | 피부 감작성 평가 방법 |
-
2016
- 2016-04-28 JP JP2016092093A patent/JP6749685B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017198637A (ja) | 2017-11-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8853133B2 (en) | Analyte determination utilizing mass tagging reagents comprising a non-encoded detectable label | |
| CN103217523B (zh) | 糖链捕获物及其用途 | |
| US9688663B2 (en) | Crosslinking reagents, methods, and compositions for studying protein-protein interactions | |
| US11396527B2 (en) | Dual mass spectrometry-cleavable crosslinking reagents for protein-protein interactions | |
| JP2016510413A (ja) | 分子の検出のための光又は化学解離性コンジュゲート | |
| KR20180136436A (ko) | 폴리플루오레노[4,5-cde]옥세핀 접합체 및 피분석물 검출 방법에서의 이의 용도 | |
| WO2022085762A1 (ja) | 皮膚感作性測定試薬、化合物、及び皮膚感作性の測定方法 | |
| US20210395606A1 (en) | Chromophoric structures for macrocyclic lanthanide chelates | |
| Chiba et al. | Specific fluorescence labeling of target proteins by using a ligand–4-azidophthalimide conjugate | |
| Yoshimatsu et al. | Peptide-imprinted polymer microspheres prepared by precipitation polymerization using a single bi-functional monomer | |
| JP6889432B2 (ja) | 樹脂固定ペプチド | |
| JP6749685B2 (ja) | 被験物質の皮膚感作性の検定方法 | |
| WO2013144656A1 (en) | Active site probes | |
| JP6793290B2 (ja) | 被験物質の皮膚感作性の評価方法、及び樹脂固定ペプチド | |
| EP3469370A1 (en) | Background blockers for binding assays | |
| JP2012518613A (ja) | スイッチング可能な親和性結合剤 | |
| Yan et al. | Nonprotein based enrichment method to analyze peptide cross-linking in protein complexes | |
| JP2002131232A (ja) | ヒドロキシプロリンの検出方法および検出用キット | |
| CN115280147A (zh) | 可紫外激发的基于聚芴的缀合物及其在分析物检测方法中的用途 | |
| JP2010143883A (ja) | ビスアクリジンペプチド誘導体及びそれを主成分するpHセンサ試薬 | |
| JP2005291836A (ja) | 標的物質濃縮用機能性タグ、及び該機能性タグの使用方法 | |
| PL240086B1 (pl) | Sole estrów arylowych N-podstawionych kwasów akrydynylo- 9-karboksylowych, sposób ich otrzymywania oraz odczynnik immunochemiczny do oznaczeń chemiluminescencyjnych |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190215 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20191226 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200114 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200313 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200804 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200806 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6749685 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |