JP6552487B2 - 癌幹細胞を培養する方法 - Google Patents
癌幹細胞を培養する方法 Download PDFInfo
- Publication number
- JP6552487B2 JP6552487B2 JP2016521251A JP2016521251A JP6552487B2 JP 6552487 B2 JP6552487 B2 JP 6552487B2 JP 2016521251 A JP2016521251 A JP 2016521251A JP 2016521251 A JP2016521251 A JP 2016521251A JP 6552487 B2 JP6552487 B2 JP 6552487B2
- Authority
- JP
- Japan
- Prior art keywords
- glycosaminoglycan
- cancer stem
- cells
- kpa
- gel
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0693—Tumour cells; Cancer cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0693—Tumour cells; Cancer cells
- C12N5/0695—Stem cells; Progenitor cells; Precursor cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5011—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing antineoplastic activity
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2503/00—Use of cells in diagnostics
- C12N2503/02—Drug screening
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/70—Polysaccharides
- C12N2533/80—Hyaluronan
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- General Engineering & Computer Science (AREA)
- Oncology (AREA)
- Toxicology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Developmental Biology & Embryology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
癌幹細胞(CSC)は、特定の癌において見出される全ての細胞タイプを生じることができるという意味において通常の幹細胞と類似している癌細胞の亜集団(腫瘍または血液の癌において見出される)である。癌幹細胞は、自己再生、癌の増殖、または様々なタイプの癌細胞への分化などの特徴を含む。そのような細胞は、腫瘍において別個の集団として存続することができ、新しい腫瘍の形成による癌の再発および転移を引き起こすと考えられる。
第一の局面により、細胞培養基質上でまたは細胞培養基質中に癌幹細胞を導入する段階を含む、癌幹細胞集団を培養するための方法であって、細胞培養基質がグリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状である、方法が提供される。
[本発明1001]
細胞培養基質上または細胞培養基質中に癌幹細胞を導入する段階を含む、癌幹細胞集団を培養するための方法であって、該細胞培養基質が、グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状である、方法。
[本発明1002]
前記細胞培養基質上で前記癌幹細胞をインキュベートする段階を含む、本発明1001の方法。
[本発明1003]
前記細胞培養基質に付着していない癌細胞を除去する段階を含む、本発明1002の方法。
[本発明1004]
前記ゲルの貯蔵弾性率を30から100,000 Paの範囲の値から選択する段階を含む、前記本発明のいずれかの方法。
[本発明1005]
前記ゲルの剛性を0.1から100 Paの範囲の値から選択する段階を含む、前記本発明のいずれかの方法。
[本発明1006]
前記グリコサミノグリカンを非硫酸化グリコサミノグリカンとして選択する段階を含む、前記本発明のいずれかの方法。
[本発明1007]
前記非硫酸化グリコサミノグリカンをヒアルロン酸として選択する段階を含む、本発明1006の方法。
[本発明1008]
置換フェンアルキルアミンを、フェンメチルアミン、フェンエチルアミン、フェンプロピルアミン、フェンブチルアミン、およびフェンペンチルアミンからなる群より選択する段階を含む、前記本発明のいずれかの方法。
[本発明1009]
前記置換フェンエチルアミンをチラミンとして選択する段階を含む、本発明1008の方法。
[本発明1010]
前記チラミンをメタチラミンまたはパラチラミンとして選択する段階を含む、本発明1009の方法。
[本発明1011]
前記複合体の置換度を1から20の範囲の値から選択する段階を含む、前記本発明のいずれかの方法。
[本発明1012]
前記癌幹細胞が、前記グリコサミノグリカンと相互作用するマーカーを含む、前記本発明のいずれかの方法。
[本発明1013]
前記マーカーが前記グリコサミノグリカンの受容体である、本発明1012の方法。
[本発明1014]
前記マーカーが、CD44、HAを介する運動性受容体(RHAMM)、および細胞内接着分子-1(ICAM-1)からなる群より選択される、本発明1012または1013の方法。
[本発明1015]
前記細胞培養基質の剛性が100 kPa未満であるかまたはそれに等しい場合に、前記癌幹細胞が、抗癌剤に対して抵抗性となる、本発明1005から1014のいずれかの方法。
[本発明1016]
前記癌幹細胞が、前記抗癌剤の存在下で少なくとも70%の生存率を有する、本発明1015の方法。
[本発明1017]
前記抗癌剤をシスプラチンまたはドキソルビシンから選択する段階を含む、本発明1015または1016の方法。
[本発明1018]
a.グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状である細胞培養基質に、複数の癌細胞を供する段階;および
b.癌幹細胞を前記細胞培養基質と相互作用させて、それによって前記複数の癌細胞から前記癌幹細胞を分離する段階
を含む、複数の癌細胞から癌幹細胞集団を選択的に分離するための方法。
[本発明1019]
段階(b)が、受容体-リガンド結合を介して前記細胞培養基質の前記グリコサミノグリカンに前記癌幹細胞を結合させる段階を含む、本発明1018の方法。
[本発明1020]
前記癌幹細胞が、前記グリコサミノグリカンの受容体であるマーカーを含む、本発明1019の方法。
[本発明1021]
細胞培養基質上または細胞培養基質中で癌幹細胞を培養する段階を含む、癌幹細胞集団に対する薬物をスクリーニングする方法であって、該細胞培養基質が、グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状であり、前記ゲルが100 kPaに等しいまたはそれ未満である剛性を有する、方法。
[本発明1022]
グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの、細胞培養基質としての使用。
[本発明1023]
前記細胞培養基質が、癌幹細胞集団に対して選択的である、本発明1022の使用。
[本発明1024]
前記癌幹細胞が、受容体-リガンド結合を介して前記グリコサミノグリカンと相互作用するマーカーを発現する、本発明1022または1023の使用。
[本発明1025]
細胞培養基質上または細胞培養基質中で癌幹細胞を培養する、グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状である細胞培養基質の、抗癌剤をスクリーニングするための使用。
本明細書において用いられる以下の単語および用語は、表記された意味を有する。
癌幹細胞集団を培養するための方法の例示的で非制限的な態様を以下に開示する。
a.複数の癌細胞を、グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状である細胞培養基質に供する段階;および
b.癌幹細胞を細胞培養基質と相互作用させて、それによって複数の癌細胞から癌幹細胞を分離する段階。
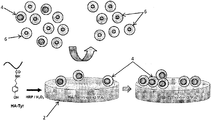
図1を参照すると、癌幹細胞マーカー4を含む癌細胞集団の選択および培養を支持するためのゲル2を示す概略図が提供される。
HA-チラミンゲルの合成
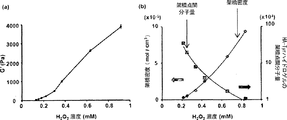
HA-チラミン複合体で構成される酵素的に架橋されたHAゲルは、H2O2およびHRPによって触媒されるチラミン部分の酸化的カップリングを用いて形成された。本明細書において、HRPおよび異なる濃度のH2O2(0.22 mM〜1.15 mMの範囲のH2O2)の溶液をHA-Tyr複合体(PBS中で3%w/v、175μl)に添加した。混合物の全量が300μlとなるように、適当量のPBSを混合物に加えた。HA-Tyr複合体およびHRPの最終濃度はそれぞれ、1.75%(w/v)および0.125単位/mlであった。混合物を直ちにボルテックスミキサーで撹拌した。
癌細胞の接着
MDA-MB-231、MCF-7、HCC1937、およびBT-474などの4つのタイプの乳癌細胞株を調べた。これらの癌細胞株におけるCD44陽性細胞集団を試験するために、CD44の表面発現のフローサイトメトリー分析(FACS)を行った。
癌細胞の増殖
付着したMDA-MB-231細胞の細胞形態学を決定するために、IX71倒立顕微鏡を備えたOlympus顕微鏡カメラ(Tokyo, Japan)を用いて位相差顕微鏡画像を得た。図6(a)を参照して、付着したMDA-MB-231細胞は全て、ゲルの剛性によらず丸いが、ポリスチレン培養フラスコ上では、他の細胞の多くが伸展していることが観察された。
HA-Tyrハイドロゲルによる癌幹細胞マーカーの発現レベルの増強
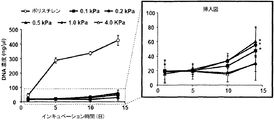
HA-Tyrゲル(剛性0.2、0.5、1.0、および4.0 kPa)上での培養13日後のMDA-MB-231細胞におけるNanog、Sox-2、およびEpCAMのmRNA発現レベルを調べた。さらに、HA-Tyrハイドロゲル(剛性0.1、0.2、0.5、1.0、および4.0 kPa)上でのMDA-MB-231細胞におけるCD44(CD44標準)、CD44v3-10(CD44変種イソ型)、CD44v8-10(CD44変種イソ型)、Sox-2、EpCAM、およびALDHD1A1遺伝子の転写レベルもまた調べた。
抗CD44抗体を用いてHA-Tyrハイドロゲル上でのMDA-MB-231細胞接着の阻害を評価した。MDA-MB-231細胞をPBSによって洗浄して、トリプシン-EDTAを用いて細胞培養フラスコから収集した。剥離した細胞を、FBSを含まないRPMI-1640培地によって洗浄して、30 μg/ml抗CD44抗体と共に氷中で1時間インキュベートした。抗CD44抗体を有しない細胞浮遊液を比較として用いた。FBSを含まないRPMI-1640培地によって洗浄後、培養培地中で細胞密度1.0×105個/mlのMDA-MB-231細胞250μlを、上記と同様の方法で24ウェルプレートで調製した0.1 kPa HA-Tyrハイドロゲル上に播種した。細胞を、5%CO2を含む37℃の湿潤大気中で1時間インキュベートした。その後、非付着細胞を有する培地を吸引して、ウェルをPBSによって3回洗浄した。HA-Tyrハイドロゲル上の付着細胞数を評価するために、上記のCyQUANT(登録商標)細胞増殖アッセイキットを用いて、蛍光測定を行った。
癌細胞の選択および維持
癌細胞の選択を評価するために、HA-Tyr(0.1、0.2、0.5、1.0、および4.0 kPa)上に付着したMDA-MB-231細胞におけるCD44s、CD44v3-10、CD44v8-10、EpCAM、およびALHD1A1遺伝子の転写レベルを分析した。培養培地中で細胞密度1.0×105個/mlの乳癌細胞250μlをハイドロゲル上に播種した。細胞を、5%CO2を含む37℃の湿潤大気中で1時間インキュベートした後、PBS 500μlによって3回洗浄して、非付着細胞を除去した。本実施例では、実施例4と比較して、ここで追加の洗浄段階を用いた。HA-Tyrハイドロゲルおよびポリスチレン上の細胞をそれぞれ、ヒアルロニダーゼ(1,000単位/ml)およびトリプシン-EDTAと共にインキュベートすることによって収集した。細胞沈降物をPBSによって2回洗浄して、mRNA発現レベルの測定のために用いた。
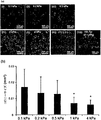
癌細胞の化学療法抵抗性
化学療法抵抗性を評価するために、HA-Tyrゲル上のMDA-MB-231の細胞生存率を、シスプラチンおよびドキソルビシンなどの従来の抗癌剤の存在下または非存在下で測定した。本明細書において、培養培地中で5.2×103個/mlの細胞密度のMDA-MB-231細胞250μlを、ゲル(0.2、0.5、1.0、2.5、および4.0 kPa)に播種した。培養培地を3日毎に交換した。細胞播種の10日後、10〜100μMシスプラチンまたはドキソルビシンを、ゲル上の培養細胞に添加して、48時間インキュベートした。次に、細胞をPBSによって洗浄して、上記のようにAlamarBlue細胞生存率アッセイを用いて蛍光強度を測定した。抗癌剤の存在下での細胞生存率を無処置対照(0μM)に対して標準化した。
開示の方法は、所望の癌幹細胞または癌幹細胞を含む癌細胞株を培養するために細胞培養用途において用いることができる。
Claims (15)
- 細胞培養基質上または細胞培養基質中に癌幹細胞を導入する段階を含む、癌幹細胞集団を培養するための方法であって、該細胞培養基質が、グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状であり、該ゲルが0.1 kPa〜4 kPaの範囲にある剛性を有し、該癌幹細胞が、該グリコサミノグリカンと相互作用し、かつ該グリコサミノグリカンの受容体であるマーカーを含み、該グリコサミノグリカンが非硫酸化グリコサミノグリカンであり、該非硫酸化グリコサミノグリカンがヒアルロン酸であり、かつ該マーカーがCD44である、方法。
- 前記細胞培養基質上で前記癌幹細胞をインキュベートする段階を含む、請求項1記載の方法。
- 前記細胞培養基質に付着していない癌細胞を除去する段階を含む、請求項2記載の方法。
- 前記ゲルの貯蔵弾性率が30から100,000 Paの範囲にある、請求項1から3のいずれか一項記載の方法。
- 置換フェンアルキルアミンが、フェンメチルアミン、フェンエチルアミン、フェンプロピルアミン、フェンブチルアミン、およびフェンペンチルアミンからなる群より選択される、請求項1から4のいずれか一項記載の方法。
- 前記置換フェンエチルアミンがチラミンである、請求項5記載の方法。
- 前記チラミンがメタチラミンまたはパラチラミンである、請求項6記載の方法。
- 前記複合体の置換度が1から20の範囲にある、請求項1から7のいずれか一項記載の方法。
- 前記細胞培養基質の剛性が4.0 kPa未満であるかまたはそれに等しい場合に、前記癌幹細胞が、抗癌剤に対して抵抗性となる、請求項1から8のいずれか一項記載の方法。
- 前記癌幹細胞が、前記抗癌剤の存在下で少なくとも70%の生存率を有する、請求項9記載の方法。
- 前記抗癌剤がシスプラチンまたはドキソルビシンである、請求項9または10記載の方法。
- a.グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状である細胞培養基質に、複数の癌細胞を供する段階であって、該ゲルが、0.1 kPa〜4 kPaの範囲にある剛性を有する、段階;および
b.癌幹細胞を前記細胞培養基質と相互作用させて、それによって前記複数の癌細胞から前記癌幹細胞を分離する段階
を含む、複数の癌細胞から癌幹細胞集団を選択的に分離するための方法であって、段階bが、受容体-リガンド結合を介して該細胞培養基質の該グリコサミノグリカンに該癌幹細胞を結合させる段階を含み、該グリコサミノグリカンがヒアルロン酸である、方法。 - 前記癌幹細胞が、前記グリコサミノグリカンの受容体であるマーカーを含む、請求項12記載の方法。
- 細胞培養基質上または細胞培養基質中で癌幹細胞を培養する段階を含む、癌幹細胞集団に対する薬物をスクリーニングする方法であって、該細胞培養基質が、グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの形状であり、前記ゲルが4.0 kPaに等しいまたはそれ未満である剛性を有し、該癌幹細胞が、該グリコサミノグリカンと相互作用し、かつ該グリコサミノグリカンの受容体であるマーカーを含み、該グリコサミノグリカンが非硫酸化グリコサミノグリカンであり、該非硫酸化グリコサミノグリカンがヒアルロン酸であり、かつ該マーカーがCD44である、方法。
- グリコサミノグリカンと置換フェンアルキルアミンとの複合体を含むゲルの、癌幹細胞集団に対して選択的である細胞培養基質としての使用であって、該癌幹細胞が、受容体-リガンド結合を介して前記グリコサミノグリカンと相互作用するマーカーを発現し、該ゲルが4.0 kPaに等しいまたはそれ未満である剛性を有し、該グリコサミノグリカンが非硫酸化グリコサミノグリカンであり、該非硫酸化グリコサミノグリカンがヒアルロン酸であり、かつ該マーカーがCD44である、使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SG201304704-8 | 2013-06-18 | ||
| SG2013047048 | 2013-06-18 | ||
| PCT/SG2014/000290 WO2014204406A1 (en) | 2013-06-18 | 2014-06-18 | Method of culturing cancer stem cells |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2016523079A JP2016523079A (ja) | 2016-08-08 |
| JP2016523079A5 JP2016523079A5 (ja) | 2017-06-15 |
| JP6552487B2 true JP6552487B2 (ja) | 2019-07-31 |
Family
ID=52104999
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016521251A Expired - Fee Related JP6552487B2 (ja) | 2013-06-18 | 2014-06-18 | 癌幹細胞を培養する方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20160145580A1 (ja) |
| EP (1) | EP3011016B1 (ja) |
| JP (1) | JP6552487B2 (ja) |
| CN (1) | CN105452450B (ja) |
| SG (1) | SG11201510462QA (ja) |
| WO (1) | WO2014204406A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018151309A1 (ja) * | 2017-02-20 | 2018-08-23 | 国立大学法人北海道大学 | 癌幹細胞の製造方法 |
| WO2018168955A1 (ja) * | 2017-03-15 | 2018-09-20 | メカノジェニック株式会社 | 細胞のin vivoでの特性を反映した細胞の反応の評価 |
| WO2019226120A1 (en) * | 2018-05-23 | 2019-11-28 | Agency For Science, Technology And Research | A tumour cell culture system and a method of preparing a tumour cell culture system |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008505716A (ja) * | 2004-07-09 | 2008-02-28 | ザ クリーヴランド クリニック ファウンデーション | ヒドロキシフェニル架橋高分子ネットワーク及びその用途 |
| JP2007297360A (ja) * | 2006-05-08 | 2007-11-15 | Ihara Suisan Kk | ハイドロゲル、その製造方法およびその用途 |
| ES2580161T3 (es) * | 2007-06-29 | 2016-08-19 | Makoto Funaki | Sistemas de geles blandos en la modulación del desarrollo de células madre |
| WO2009116951A2 (en) * | 2008-03-17 | 2009-09-24 | Agency For Science, Technology And Research | Microcarriers for stem cell culture |
| US8691206B2 (en) * | 2008-05-06 | 2014-04-08 | Agency For Science, Technology And Research | Formation of hydrogel in the presence of peroxidase and low concentration of hydrogen peroxide |
| JP5563563B2 (ja) * | 2008-06-05 | 2014-07-30 | エージェンシー フォー サイエンス, テクノロジー アンド リサーチ | ペルオキシダーゼおよび低濃度の過酸化水素の存在下でのヒドロゲルの形成方法 |
| GB201111244D0 (en) * | 2011-06-30 | 2011-08-17 | Konink Nl Akademie Van Wetenschappen Knaw | Culture media for stem cells |
| SG168430A1 (en) * | 2009-07-22 | 2011-02-28 | Agency Science Tech & Res | Molecular signature of human lung cancer initiating cells |
| WO2010138082A1 (en) * | 2009-05-29 | 2010-12-02 | Agency For Science, Technology And Research | Flavonoid hydrogel |
| US20120301441A1 (en) * | 2009-11-11 | 2012-11-29 | Hermanus Bernardus Johannes Karperien | Dextran-hyaluronic acid based hydrogels |
| US9132201B2 (en) * | 2009-11-11 | 2015-09-15 | University Of Twente, Institute For Biomedical And Technical Medicine (Mira) | Hydrogels based on polymers of dextran tyramine and tyramine conjugates of natural polymers |
| US8853162B2 (en) * | 2011-05-11 | 2014-10-07 | Agency For Science, Technology And Research | Interpenetrating polymer network comprising fibrin |
-
2014
- 2014-06-18 EP EP14814177.3A patent/EP3011016B1/en active Active
- 2014-06-18 US US14/900,080 patent/US20160145580A1/en not_active Abandoned
- 2014-06-18 JP JP2016521251A patent/JP6552487B2/ja not_active Expired - Fee Related
- 2014-06-18 SG SG11201510462QA patent/SG11201510462QA/en unknown
- 2014-06-18 WO PCT/SG2014/000290 patent/WO2014204406A1/en not_active Ceased
- 2014-06-18 CN CN201480045085.3A patent/CN105452450B/zh not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| EP3011016B1 (en) | 2019-08-07 |
| US20160145580A1 (en) | 2016-05-26 |
| CN105452450B (zh) | 2020-07-07 |
| SG11201510462QA (en) | 2016-01-28 |
| EP3011016A1 (en) | 2016-04-27 |
| WO2014204406A1 (en) | 2014-12-24 |
| CN105452450A (zh) | 2016-03-30 |
| EP3011016A4 (en) | 2016-11-30 |
| JP2016523079A (ja) | 2016-08-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| LeSavage et al. | Engineered matrices reveal stiffness-mediated chemoresistance in patient-derived pancreatic cancer organoids | |
| Wang et al. | Acquisition of epithelial–mesenchymal transition phenotype and cancer stem cell-like properties in cisplatin-resistant lung cancer cells through AKT/β-catenin/Snail signaling pathway | |
| Huang et al. | MiR‐223/PAX6 axis regulates glioblastoma stem cell proliferation and the chemo resistance to TMZ via regulating PI3K/Akt pathway | |
| O’Brien et al. | Exosomes from triple-negative breast cancer cells can transfer phenotypic traits representing their cells of origin to secondary cells | |
| Du et al. | CD44 is of functional importance for colorectal cancer stem cells | |
| Yoshida et al. | Clinical and functional significance of intracellular and extracellular microRNA-25-3p in osteosarcoma | |
| Battula et al. | Ganglioside GD2 identifies breast cancer stem cells and promotes tumorigenesis | |
| Zhu et al. | Reduced miR-128 in breast tumor–initiating cells induces chemotherapeutic resistance via Bmi-1 and ABCC5 | |
| Shen et al. | Exosome-mediated transfer of CD44 from high-metastatic ovarian cancer cells promotes migration and invasion of low-metastatic ovarian cancer cells | |
| Hazawa et al. | Radiation increases the cellular uptake of exosomes through CD29/CD81 complex formation | |
| Mina et al. | The role of shear stress and altered tissue properties on endothelial to mesenchymal transformation and tumor-endothelial cell interaction | |
| Fan et al. | MicroRNA-101-3p reverses gemcitabine resistance by inhibition of ribonucleotide reductase M1 in pancreatic cancer | |
| Jiang et al. | miR‐365 regulates liver cancer stem cells via RAC1 pathway | |
| Gong et al. | Retracted: Knockdown of long non‐coding RNA MEG3 protects H9c2 cells from hypoxia‐induced injury by targeting microRNA‐183 | |
| Ritter et al. | Cancer-educated mammary adipose tissue-derived stromal/stem cells in obesity and breast cancer: spatial regulation and function | |
| Peng et al. | Let‐7c restores radiosensitivity and chemosensitivity and impairs stemness in oral cancer cells through inhibiting interleukin‐8 | |
| US20190085298A1 (en) | Three Dimensional Matrix for Cancer Stem Cells | |
| Song et al. | Annexin A7 and its binding protein galectin-3 influence mouse hepatocellular carcinoma cell line in vitro | |
| Zhang et al. | Sphingosine kinase 2 promotes colorectal cancer cell proliferation and invasion by enhancing MYC expression | |
| Wang et al. | OV6+ cancer stem cells drive esophageal squamous cell carcinoma progression through ATG7-dependent β-catenin stabilization | |
| JP6552487B2 (ja) | 癌幹細胞を培養する方法 | |
| WO2011149013A1 (ja) | 癌組織由来細胞塊または癌細胞凝集塊の薬剤または放射線感受性評価方法 | |
| Nikpour et al. | MTDH/AEG-1 contributes to central features of the neoplastic phenotype in bladder cancer | |
| Qu et al. | MiR-449 overexpression inhibits osteogenic differentiation of bone marrow mesenchymal stem cells via suppressing Sirt1/Fra-1 pathway in high glucose and free fatty acids microenvironment | |
| Han et al. | Estrogen receptor β (ERβ) is a novel prognostic marker of recurrence survival in non-muscle-invasive bladder cancer potentially by inhibiting cadherin switch |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160125 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170426 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170426 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20180221 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180301 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180531 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20181029 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190117 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190612 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190702 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6552487 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |