JP6548052B2 - 抗体 - Google Patents
抗体 Download PDFInfo
- Publication number
- JP6548052B2 JP6548052B2 JP2017534378A JP2017534378A JP6548052B2 JP 6548052 B2 JP6548052 B2 JP 6548052B2 JP 2017534378 A JP2017534378 A JP 2017534378A JP 2017534378 A JP2017534378 A JP 2017534378A JP 6548052 B2 JP6548052 B2 JP 6548052B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- cells
- amino acid
- cell
- human
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 210000004027 cell Anatomy 0.000 claims description 318
- 102000006495 integrins Human genes 0.000 claims description 181
- 108010044426 integrins Proteins 0.000 claims description 181
- 206010035226 Plasma cell myeloma Diseases 0.000 claims description 99
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 53
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 claims description 52
- 239000008194 pharmaceutical composition Substances 0.000 claims description 48
- 102000036639 antigens Human genes 0.000 claims description 47
- 108091007433 antigens Proteins 0.000 claims description 47
- 239000000427 antigen Substances 0.000 claims description 45
- 108091033319 polynucleotide Proteins 0.000 claims description 44
- 102000040430 polynucleotide Human genes 0.000 claims description 44
- 239000002157 polynucleotide Substances 0.000 claims description 40
- 208000034578 Multiple myelomas Diseases 0.000 claims description 27
- 108091007741 Chimeric antigen receptor T cells Proteins 0.000 claims description 25
- 238000011282 treatment Methods 0.000 claims description 17
- 239000013598 vector Substances 0.000 claims description 15
- 210000000822 natural killer cell Anatomy 0.000 claims description 10
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 4
- 125000003275 alpha amino acid group Chemical group 0.000 claims 8
- 125000000539 amino acid group Chemical group 0.000 description 111
- 150000001413 amino acids Chemical group 0.000 description 84
- 238000000034 method Methods 0.000 description 81
- 201000000050 myeloid neoplasm Diseases 0.000 description 72
- 206010028980 Neoplasm Diseases 0.000 description 53
- 230000027455 binding Effects 0.000 description 53
- 201000010099 disease Diseases 0.000 description 43
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 43
- 108090000623 proteins and genes Proteins 0.000 description 40
- 210000004180 plasmocyte Anatomy 0.000 description 39
- 102000004169 proteins and genes Human genes 0.000 description 36
- 235000018102 proteins Nutrition 0.000 description 34
- 230000000694 effects Effects 0.000 description 33
- 241000699666 Mus <mouse, genus> Species 0.000 description 31
- 201000011510 cancer Diseases 0.000 description 28
- 230000001472 cytotoxic effect Effects 0.000 description 25
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 24
- 230000014509 gene expression Effects 0.000 description 20
- 239000000126 substance Substances 0.000 description 20
- 230000035772 mutation Effects 0.000 description 19
- 201000005787 hematologic cancer Diseases 0.000 description 18
- 238000012216 screening Methods 0.000 description 18
- 210000001185 bone marrow Anatomy 0.000 description 15
- 239000013604 expression vector Substances 0.000 description 15
- 101001015037 Homo sapiens Integrin beta-7 Proteins 0.000 description 14
- 241000699670 Mus sp. Species 0.000 description 14
- 238000002405 diagnostic procedure Methods 0.000 description 14
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 13
- 241001465754 Metazoa Species 0.000 description 13
- 239000004480 active ingredient Substances 0.000 description 13
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 13
- 239000002299 complementary DNA Substances 0.000 description 13
- 210000004408 hybridoma Anatomy 0.000 description 13
- 102100031585 ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Human genes 0.000 description 12
- 101000777636 Homo sapiens ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Proteins 0.000 description 12
- 102100033016 Integrin beta-7 Human genes 0.000 description 12
- 238000006467 substitution reaction Methods 0.000 description 11
- 210000000601 blood cell Anatomy 0.000 description 10
- 210000002798 bone marrow cell Anatomy 0.000 description 10
- 239000011886 peripheral blood Substances 0.000 description 10
- 239000002243 precursor Substances 0.000 description 10
- 238000010186 staining Methods 0.000 description 10
- 101001053395 Arabidopsis thaliana Acid beta-fructofuranosidase 4, vacuolar Proteins 0.000 description 9
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 9
- 210000003719 b-lymphocyte Anatomy 0.000 description 9
- 239000002773 nucleotide Substances 0.000 description 9
- 125000003729 nucleotide group Chemical group 0.000 description 9
- 210000005259 peripheral blood Anatomy 0.000 description 9
- 101000994375 Homo sapiens Integrin alpha-4 Proteins 0.000 description 8
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 8
- 102100032818 Integrin alpha-4 Human genes 0.000 description 8
- 239000004698 Polyethylene Substances 0.000 description 8
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 8
- 239000012634 fragment Substances 0.000 description 8
- 230000003834 intracellular effect Effects 0.000 description 8
- 230000001225 therapeutic effect Effects 0.000 description 8
- 108060003951 Immunoglobulin Proteins 0.000 description 7
- 230000003213 activating effect Effects 0.000 description 7
- 231100000599 cytotoxic agent Toxicity 0.000 description 7
- 239000002619 cytotoxin Substances 0.000 description 7
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 7
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 7
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 7
- 102000018358 immunoglobulin Human genes 0.000 description 7
- 238000001727 in vivo Methods 0.000 description 7
- 239000006228 supernatant Substances 0.000 description 7
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 6
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 description 6
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 description 6
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 6
- -1 PMA Chemical class 0.000 description 6
- 239000012980 RPMI-1640 medium Substances 0.000 description 6
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 6
- 230000002159 abnormal effect Effects 0.000 description 6
- 230000004913 activation Effects 0.000 description 6
- 230000000139 costimulatory effect Effects 0.000 description 6
- 230000006378 damage Effects 0.000 description 6
- 230000002950 deficient Effects 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 230000009878 intermolecular interaction Effects 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 6
- 230000002269 spontaneous effect Effects 0.000 description 6
- 238000005406 washing Methods 0.000 description 6
- 108020004705 Codon Proteins 0.000 description 5
- 101710112752 Cytotoxin Proteins 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 5
- 102100037850 Interferon gamma Human genes 0.000 description 5
- 108010074328 Interferon-gamma Proteins 0.000 description 5
- 108091028043 Nucleic acid sequence Proteins 0.000 description 5
- 108010076504 Protein Sorting Signals Proteins 0.000 description 5
- 108091008874 T cell receptors Proteins 0.000 description 5
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 239000008280 blood Substances 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- 210000003527 eukaryotic cell Anatomy 0.000 description 5
- 239000012091 fetal bovine serum Substances 0.000 description 5
- 230000016784 immunoglobulin production Effects 0.000 description 5
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 125000006850 spacer group Chemical group 0.000 description 5
- 125000003396 thiol group Chemical group [H]S* 0.000 description 5
- 238000012546 transfer Methods 0.000 description 5
- 101100132433 Arabidopsis thaliana VIII-1 gene Proteins 0.000 description 4
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 4
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 4
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 4
- 101710085938 Matrix protein Proteins 0.000 description 4
- 101710127721 Membrane protein Proteins 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 230000037396 body weight Effects 0.000 description 4
- 210000000170 cell membrane Anatomy 0.000 description 4
- 238000010367 cloning Methods 0.000 description 4
- 238000007796 conventional method Methods 0.000 description 4
- 238000012258 culturing Methods 0.000 description 4
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 4
- 238000012217 deletion Methods 0.000 description 4
- 230000037430 deletion Effects 0.000 description 4
- 230000001900 immune effect Effects 0.000 description 4
- GOTYRUGSSMKFNF-UHFFFAOYSA-N lenalidomide Chemical compound C1C=2C(N)=CC=CC=2C(=O)N1C1CCC(=O)NC1=O GOTYRUGSSMKFNF-UHFFFAOYSA-N 0.000 description 4
- 229960004942 lenalidomide Drugs 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 230000002265 prevention Effects 0.000 description 4
- 238000012163 sequencing technique Methods 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- 210000004881 tumor cell Anatomy 0.000 description 4
- 241001430294 unidentified retrovirus Species 0.000 description 4
- 241000186361 Actinobacteria <class> Species 0.000 description 3
- 241000588724 Escherichia coli Species 0.000 description 3
- 241000238631 Hexapoda Species 0.000 description 3
- 101001046687 Homo sapiens Integrin alpha-E Proteins 0.000 description 3
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 3
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 3
- 102100022341 Integrin alpha-E Human genes 0.000 description 3
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 101100113998 Mus musculus Cnbd2 gene Proteins 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 108010033276 Peptide Fragments Proteins 0.000 description 3
- 102000007079 Peptide Fragments Human genes 0.000 description 3
- 239000004365 Protease Substances 0.000 description 3
- 241000700159 Rattus Species 0.000 description 3
- 229920004890 Triton X-100 Polymers 0.000 description 3
- 239000013504 Triton X-100 Substances 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 235000001014 amino acid Nutrition 0.000 description 3
- 229940024606 amino acid Drugs 0.000 description 3
- 210000000628 antibody-producing cell Anatomy 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 229930195731 calicheamicin Natural products 0.000 description 3
- HXCHCVDVKSCDHU-LULTVBGHSA-N calicheamicin Chemical compound C1[C@H](OC)[C@@H](NCC)CO[C@H]1O[C@H]1[C@H](O[C@@H]2C\3=C(NC(=O)OC)C(=O)C[C@](C/3=C/CSSSC)(O)C#C\C=C/C#C2)O[C@H](C)[C@@H](NO[C@@H]2O[C@H](C)[C@@H](SC(=O)C=3C(=C(OC)C(O[C@H]4[C@@H]([C@H](OC)[C@@H](O)[C@H](C)O4)O)=C(I)C=3C)OC)[C@@H](O)C2)[C@@H]1O HXCHCVDVKSCDHU-LULTVBGHSA-N 0.000 description 3
- 230000000295 complement effect Effects 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 238000012790 confirmation Methods 0.000 description 3
- 231100000433 cytotoxic Toxicity 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 210000003743 erythrocyte Anatomy 0.000 description 3
- 238000000684 flow cytometry Methods 0.000 description 3
- 238000010353 genetic engineering Methods 0.000 description 3
- 238000003384 imaging method Methods 0.000 description 3
- 238000010324 immunological assay Methods 0.000 description 3
- 238000000126 in silico method Methods 0.000 description 3
- 238000003780 insertion Methods 0.000 description 3
- 230000037431 insertion Effects 0.000 description 3
- 210000000265 leukocyte Anatomy 0.000 description 3
- 238000001638 lipofection Methods 0.000 description 3
- 210000004962 mammalian cell Anatomy 0.000 description 3
- 239000011572 manganese Substances 0.000 description 3
- 150000002696 manganese Chemical class 0.000 description 3
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 3
- 229960001924 melphalan Drugs 0.000 description 3
- 210000005087 mononuclear cell Anatomy 0.000 description 3
- 238000002703 mutagenesis Methods 0.000 description 3
- 231100000350 mutagenesis Toxicity 0.000 description 3
- 210000004976 peripheral blood cell Anatomy 0.000 description 3
- 150000004633 phorbol derivatives Chemical class 0.000 description 3
- 239000002644 phorbol ester Substances 0.000 description 3
- 230000003449 preventive effect Effects 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 210000001236 prokaryotic cell Anatomy 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- 230000009870 specific binding Effects 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 235000002374 tyrosine Nutrition 0.000 description 3
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 3
- 210000005253 yeast cell Anatomy 0.000 description 3
- UEJJHQNACJXSKW-UHFFFAOYSA-N 2-(2,6-dioxopiperidin-3-yl)-1H-isoindole-1,3(2H)-dione Chemical compound O=C1C2=CC=CC=C2C(=O)N1C1CCC(=O)NC1=O UEJJHQNACJXSKW-UHFFFAOYSA-N 0.000 description 2
- 101001053401 Arabidopsis thaliana Acid beta-fructofuranosidase 3, vacuolar Proteins 0.000 description 2
- 101100459319 Arabidopsis thaliana VIII-2 gene Proteins 0.000 description 2
- 108091033409 CRISPR Proteins 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 208000002250 Hematologic Neoplasms Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000946889 Homo sapiens Monocyte differentiation antigen CD14 Proteins 0.000 description 2
- 101000851370 Homo sapiens Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 2
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 2
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 2
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 2
- 102000018697 Membrane Proteins Human genes 0.000 description 2
- 108010052285 Membrane Proteins Proteins 0.000 description 2
- 102100035877 Monocyte differentiation antigen CD14 Human genes 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 2
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 2
- 239000004473 Threonine Substances 0.000 description 2
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 2
- 102100036856 Tumor necrosis factor receptor superfamily member 9 Human genes 0.000 description 2
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 2
- 210000001772 blood platelet Anatomy 0.000 description 2
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 description 2
- 229960001467 bortezomib Drugs 0.000 description 2
- 230000005779 cell damage Effects 0.000 description 2
- 230000007910 cell fusion Effects 0.000 description 2
- 208000037887 cell injury Diseases 0.000 description 2
- 230000004663 cell proliferation Effects 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 238000003501 co-culture Methods 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 2
- 230000003013 cytotoxicity Effects 0.000 description 2
- 231100000135 cytotoxicity Toxicity 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 239000012636 effector Substances 0.000 description 2
- 238000001400 expression cloning Methods 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 238000003018 immunoassay Methods 0.000 description 2
- 238000001114 immunoprecipitation Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 2
- 229960000310 isoleucine Drugs 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 239000003607 modifier Substances 0.000 description 2
- 230000001613 neoplastic effect Effects 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- XJMOSONTPMZWPB-UHFFFAOYSA-M propidium iodide Chemical compound [I-].[I-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CCC[N+](C)(CC)CC)=C1C1=CC=CC=C1 XJMOSONTPMZWPB-UHFFFAOYSA-M 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 108010056030 retronectin Proteins 0.000 description 2
- 102220014598 rs397517195 Human genes 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 229960003433 thalidomide Drugs 0.000 description 2
- 235000008521 threonine Nutrition 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- 239000004474 valine Substances 0.000 description 2
- 235000014393 valine Nutrition 0.000 description 2
- AQTQHPDCURKLKT-JKDPCDLQSA-N vincristine sulfate Chemical compound OS(O)(=O)=O.C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C=O)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 AQTQHPDCURKLKT-JKDPCDLQSA-N 0.000 description 2
- 229960002110 vincristine sulfate Drugs 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 1
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- CLPFFLWZZBQMAO-UHFFFAOYSA-N 4-(5,6,7,8-tetrahydroimidazo[1,5-a]pyridin-5-yl)benzonitrile Chemical compound C1=CC(C#N)=CC=C1C1N2C=NC=C2CCC1 CLPFFLWZZBQMAO-UHFFFAOYSA-N 0.000 description 1
- KABRXLINDSPGDF-UHFFFAOYSA-N 7-bromoisoquinoline Chemical compound C1=CN=CC2=CC(Br)=CC=C21 KABRXLINDSPGDF-UHFFFAOYSA-N 0.000 description 1
- 108010083359 Antigen Receptors Proteins 0.000 description 1
- 102000006306 Antigen Receptors Human genes 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- BFYIZQONLCFLEV-DAELLWKTSA-N Aromasine Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC(=C)C2=C1 BFYIZQONLCFLEV-DAELLWKTSA-N 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 208000008720 Bone Marrow Neoplasms Diseases 0.000 description 1
- 206010006002 Bone pain Diseases 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- 102100036008 CD48 antigen Human genes 0.000 description 1
- 210000001239 CD8-positive, alpha-beta cytotoxic T lymphocyte Anatomy 0.000 description 1
- 101100180402 Caenorhabditis elegans jun-1 gene Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 description 1
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- PTOAARAWEBMLNO-KVQBGUIXSA-N Cladribine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)O1 PTOAARAWEBMLNO-KVQBGUIXSA-N 0.000 description 1
- 108020004635 Complementary DNA Proteins 0.000 description 1
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- MWWSFMDVAYGXBV-RUELKSSGSA-N Doxorubicin hydrochloride Chemical compound Cl.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 MWWSFMDVAYGXBV-RUELKSSGSA-N 0.000 description 1
- 102220508029 Endogenous retrovirus group K member 6 Rec protein_N36D_mutation Human genes 0.000 description 1
- YQYJSBFKSSDGFO-UHFFFAOYSA-N Epihygromycin Natural products OC1C(O)C(C(=O)C)OC1OC(C(=C1)O)=CC=C1C=C(C)C(=O)NC1C(O)C(O)C2OCOC2C1O YQYJSBFKSSDGFO-UHFFFAOYSA-N 0.000 description 1
- 108010087819 Fc receptors Proteins 0.000 description 1
- 102000009109 Fc receptors Human genes 0.000 description 1
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 101000716130 Homo sapiens CD48 antigen Proteins 0.000 description 1
- 101001033280 Homo sapiens Cytokine receptor common subunit beta Proteins 0.000 description 1
- 101001078143 Homo sapiens Integrin alpha-IIb Proteins 0.000 description 1
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 1
- 101000917839 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-B Proteins 0.000 description 1
- 208000037147 Hypercalcaemia Diseases 0.000 description 1
- 102100025306 Integrin alpha-IIb Human genes 0.000 description 1
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 239000012097 Lipofectamine 2000 Substances 0.000 description 1
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 101000746372 Mus musculus Granulocyte-macrophage colony-stimulating factor Proteins 0.000 description 1
- 102220500387 Neutral and basic amino acid transport protein rBAT_M41Y_mutation Human genes 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 241000282577 Pan troglodytes Species 0.000 description 1
- 108090000526 Papain Proteins 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 208000033014 Plasma cell tumor Diseases 0.000 description 1
- 208000007452 Plasmacytoma Diseases 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 229940079156 Proteasome inhibitor Drugs 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 208000001647 Renal Insufficiency Diseases 0.000 description 1
- 206010061481 Renal injury Diseases 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- 238000011579 SCID mouse model Methods 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 108091081024 Start codon Proteins 0.000 description 1
- 102220499972 Target of EGR1 protein 1_R35E_mutation Human genes 0.000 description 1
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 1
- FOCVUCIESVLUNU-UHFFFAOYSA-N Thiotepa Chemical compound C1CN1P(N1CC1)(=S)N1CC1 FOCVUCIESVLUNU-UHFFFAOYSA-N 0.000 description 1
- 102100022153 Tumor necrosis factor receptor superfamily member 4 Human genes 0.000 description 1
- 101710165473 Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 description 1
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 108010058061 alpha E integrins Proteins 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000012197 amplification kit Methods 0.000 description 1
- 229960002550 amrubicin Drugs 0.000 description 1
- VJZITPJGSQKZMX-XDPRQOKASA-N amrubicin Chemical compound O([C@H]1C[C@](CC2=C(O)C=3C(=O)C4=CC=CC=C4C(=O)C=3C(O)=C21)(N)C(=O)C)[C@H]1C[C@H](O)[C@H](O)CO1 VJZITPJGSQKZMX-XDPRQOKASA-N 0.000 description 1
- 206010002022 amyloidosis Diseases 0.000 description 1
- 229960002932 anastrozole Drugs 0.000 description 1
- YBBLVLTVTVSKRW-UHFFFAOYSA-N anastrozole Chemical compound N#CC(C)(C)C1=CC(C(C)(C#N)C)=CC(CN2N=CN=C2)=C1 YBBLVLTVTVSKRW-UHFFFAOYSA-N 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000001446 anti-myeloma Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 239000003886 aromatase inhibitor Substances 0.000 description 1
- 229940046844 aromatase inhibitors Drugs 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- KLNFSAOEKUDMFA-UHFFFAOYSA-N azanide;2-hydroxyacetic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OCC(O)=O KLNFSAOEKUDMFA-UHFFFAOYSA-N 0.000 description 1
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 201000006491 bone marrow cancer Diseases 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- 102220395310 c.125T>A Human genes 0.000 description 1
- 238000010804 cDNA synthesis Methods 0.000 description 1
- 238000010805 cDNA synthesis kit Methods 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229960004117 capecitabine Drugs 0.000 description 1
- 229960004562 carboplatin Drugs 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 101150038500 cas9 gene Proteins 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960002436 cladribine Drugs 0.000 description 1
- 239000013599 cloning vector Substances 0.000 description 1
- 230000004540 complement-dependent cytotoxicity Effects 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 239000012050 conventional carrier Substances 0.000 description 1
- 239000012228 culture supernatant Substances 0.000 description 1
- 229960004397 cyclophosphamide Drugs 0.000 description 1
- PWOQRKCAHTVFLB-UHFFFAOYSA-N cyclophosphamide hydrate Chemical compound O.ClCCN(CCCl)P1(=O)NCCCO1 PWOQRKCAHTVFLB-UHFFFAOYSA-N 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 229960000684 cytarabine Drugs 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 229960000640 dactinomycin Drugs 0.000 description 1
- 230000000254 damaging effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 230000006334 disulfide bridging Effects 0.000 description 1
- 229950005454 doxifluridine Drugs 0.000 description 1
- ZWAOHEXOSAUJHY-ZIYNGMLESA-N doxifluridine Chemical compound O[C@@H]1[C@H](O)[C@@H](C)O[C@H]1N1C(=O)NC(=O)C(F)=C1 ZWAOHEXOSAUJHY-ZIYNGMLESA-N 0.000 description 1
- 229960002918 doxorubicin hydrochloride Drugs 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 229960000255 exemestane Drugs 0.000 description 1
- 229950011548 fadrozole Drugs 0.000 description 1
- 229960005304 fludarabine phosphate Drugs 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 229960005144 gemcitabine hydrochloride Drugs 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 235000004554 glutamine Nutrition 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 238000011134 hematopoietic stem cell transplantation Methods 0.000 description 1
- 102000055647 human CSF2RB Human genes 0.000 description 1
- 102000053391 human F Human genes 0.000 description 1
- 108700031895 human F Proteins 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000000148 hypercalcaemia Effects 0.000 description 1
- 208000030915 hypercalcemia disease Diseases 0.000 description 1
- 229960001101 ifosfamide Drugs 0.000 description 1
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 description 1
- 210000003692 ilium Anatomy 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 239000012133 immunoprecipitate Substances 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 229960000779 irinotecan hydrochloride Drugs 0.000 description 1
- GURKHSYORGJETM-WAQYZQTGSA-N irinotecan hydrochloride (anhydrous) Chemical compound Cl.C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 GURKHSYORGJETM-WAQYZQTGSA-N 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 201000006370 kidney failure Diseases 0.000 description 1
- 208000037806 kidney injury Diseases 0.000 description 1
- 210000003127 knee Anatomy 0.000 description 1
- 229960003881 letrozole Drugs 0.000 description 1
- HPJKCIUCZWXJDR-UHFFFAOYSA-N letrozole Chemical compound C1=CC(C#N)=CC=C1C(N1N=CN=C1)C1=CC=C(C#N)C=C1 HPJKCIUCZWXJDR-UHFFFAOYSA-N 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 231100000782 microtubule inhibitor Toxicity 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- ZAHQPTJLOCWVPG-UHFFFAOYSA-N mitoxantrone dihydrochloride Chemical compound Cl.Cl.O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO ZAHQPTJLOCWVPG-UHFFFAOYSA-N 0.000 description 1
- 229960004169 mitoxantrone hydrochloride Drugs 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 229950007221 nedaplatin Drugs 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- IXOXBSCIXZEQEQ-UHTZMRCNSA-N nelarabine Chemical compound C1=NC=2C(OC)=NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@@H]1O IXOXBSCIXZEQEQ-UHTZMRCNSA-N 0.000 description 1
- 229960000801 nelarabine Drugs 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 229960001420 nimustine Drugs 0.000 description 1
- VFEDRRNHLBGPNN-UHFFFAOYSA-N nimustine Chemical compound CC1=NC=C(CNC(=O)N(CCCl)N=O)C(N)=N1 VFEDRRNHLBGPNN-UHFFFAOYSA-N 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 229940127075 other antimetabolite Drugs 0.000 description 1
- 229960001756 oxaliplatin Drugs 0.000 description 1
- DWAFYCQODLXJNR-BNTLRKBRSA-L oxaliplatin Chemical compound O1C(=O)C(=O)O[Pt]11N[C@@H]2CCCC[C@H]2N1 DWAFYCQODLXJNR-BNTLRKBRSA-L 0.000 description 1
- VYNDHICBIRRPFP-UHFFFAOYSA-N pacific blue Chemical compound FC1=C(O)C(F)=C2OC(=O)C(C(=O)O)=CC2=C1 VYNDHICBIRRPFP-UHFFFAOYSA-N 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- 229940055729 papain Drugs 0.000 description 1
- 235000019834 papain Nutrition 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 229960005079 pemetrexed Drugs 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 208000031223 plasma cell leukemia Diseases 0.000 description 1
- 208000010626 plasma cell neoplasm Diseases 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 239000003207 proteasome inhibitor Substances 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 239000002336 ribonucleotide Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 235000004400 serine Nutrition 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000007447 staining method Methods 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- 229960004964 temozolomide Drugs 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- ZCTCZKWJFTYNMZ-WKUCUCPSSA-J tetrasodium;(2s)-2-[[4-[2-(2-amino-4-oxo-1,7-dihydropyrrolo[2,3-d]pyrimidin-5-yl)ethyl]benzoyl]amino]pentanedioate;pentahydrate Chemical compound O.O.O.O.O.[Na+].[Na+].[Na+].[Na+].C=1NC=2NC(N)=NC(=O)C=2C=1CCC1=CC=C(C(=O)N[C@@H](CCC([O-])=O)C([O-])=O)C=C1.C=1NC=2NC(N)=NC(=O)C=2C=1CCC1=CC=C(C(=O)N[C@@H](CCC([O-])=O)C([O-])=O)C=C1 ZCTCZKWJFTYNMZ-WKUCUCPSSA-J 0.000 description 1
- 229960001196 thiotepa Drugs 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 102000035160 transmembrane proteins Human genes 0.000 description 1
- 108091005703 transmembrane proteins Proteins 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
- 241000701161 unidentified adenovirus Species 0.000 description 1
- KDQAABAKXDWYSZ-PNYVAJAMSA-N vinblastine sulfate Chemical compound OS(O)(=O)=O.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 KDQAABAKXDWYSZ-PNYVAJAMSA-N 0.000 description 1
- 229960004982 vinblastine sulfate Drugs 0.000 description 1
- 229960005212 vindesine sulfate Drugs 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 108010065816 zeta chain antigen T cell receptor Proteins 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2839—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the integrin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4611—T-cells, e.g. tumor infiltrating lymphocytes [TIL], lymphokine-activated killer cells [LAK] or regulatory T cells [Treg]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/463—Cellular immunotherapy characterised by recombinant expression
- A61K39/4631—Chimeric Antigen Receptors [CAR]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/4644—Cancer antigens
- A61K39/464402—Receptors, cell surface antigens or cell surface determinants
- A61K39/464411—Immunoglobulin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K19/00—Hybrid peptides, i.e. peptides covalently bound to nucleic acids, or non-covalently bound protein-protein complexes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/577—Immunoassay; Biospecific binding assay; Materials therefor involving monoclonal antibodies binding reaction mechanisms characterised by the use of monoclonal antibodies; monoclonal antibodies per se are classified with their corresponding antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5156—Animal cells expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5158—Antigen-pulsed cells, e.g. T-cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/31—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterized by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the dose, timing or administration schedule
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/03—Fusion polypeptide containing a localisation/targetting motif containing a transmembrane segment
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/33—Fusion polypeptide fusions for targeting to specific cell types, e.g. tissue specific targeting, targeting of a bacterial subspecies
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Molecular Biology (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- General Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Hematology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Oncology (AREA)
- Physics & Mathematics (AREA)
- Urology & Nephrology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Plant Pathology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Food Science & Technology (AREA)
- Analytical Chemistry (AREA)
- Gastroenterology & Hepatology (AREA)
Description
抗体(I)は、以下の(I-1)〜(I-25)に示す抗体を包含する。
抗ヒトインテグリンβ7抗体であって、ヒトインテグリンβ7の20〜109番目のアミノ酸残基からなる領域にエピトープを有する抗体。
(1-1A)
ヒトインテグリンβ7の33〜109番目のアミノ酸残基からなる領域にエピトープを有する、(I-1)に記載の抗体。
(1-1B)
ヒトインテグリンβ7の20〜90番目のアミノ酸残基からなる領域にエピトープを有する、(I-1)に記載の抗体。
(1-1C)
ヒトインテグリンβ7の33〜90番目のアミノ酸残基からなる領域にエピトープを有する、(I-1)に記載の抗体。
(I-2)
ヒトインテグリンβ7の379〜721番目のアミノ酸残基からなる領域の少なくとも一部の存在下で、前記エピトープへの親和性が上昇する、(I-1)に記載の抗体。
(I-3)
ヒトインテグリンβ7の417〜721番目のアミノ酸残基からなる領域の少なくとも一部の存在下で、前記エピトープへの親和性が上昇する、(I-2)に記載の抗体。
(I-4)
ヒトインテグリンβ7の564〜721番目のアミノ酸残基からなる領域の少なくとも一部の存在下で、前記エピトープへの親和性が上昇する、(I-2)に記載の抗体。
(I-5)
ヒトインテグリンβ7の379〜563番目のアミノ酸残基からなる領域の少なくとも一部の存在下で、前記エピトープへの親和性が上昇する、(I-2)に記載の抗体。
(I-6)
ヒトインテグリンβ7の417〜563番目のアミノ酸残基からなる領域の少なくとも一部の存在下で、前記エピトープへの親和性が上昇する、(I-2)に記載の抗体。
(I-7)
ヒトインテグリンβ7の379〜416番目のアミノ酸残基からなる領域の少なくとも一部の存在下で、前記エピトープへの親和性が上昇する、(I-2)に記載の抗体。
(I-8)
ヒトインテグリンβ7を活性化することにより、前記エピトープへの親和性が上昇する、(I-1)〜(I-7)のいずれか1項に記載の抗体。
(I-9)
抗ヒトインテグリンβ7抗体であって、正常細胞上にて発現するヒトインテグリンβ7よりも、骨髄腫細胞上で発現するヒトインテグリンβ7に対して親和性が高い抗体。
(I-10)
MMG49抗体と同一のエピトープを有する、(I-1)〜(I-9)のいずれか1項に記載の抗体。
(I-11)
配列番号1に示すアミノ酸配列を有する重鎖CDR1、
配列番号2に示すアミノ酸配列を有する重鎖CDR2、および/または
配列番号3に示すアミノ酸配列を有する重鎖CDR3
を含む重鎖可変領域、ならびに/あるいは
配列番号6に示すアミノ酸配列を有する軽鎖CDR1、
配列番号7に示すアミノ酸配列を有する軽鎖CDR2、および/または
配列番号8に示すアミノ酸配列を有する軽鎖CDR3
を含む軽鎖可変領域
を含む、(I-1)〜(I-10)のいずれか1項に記載の抗体。
(I-12)
配列番号4に示すアミノ酸配列を有する重鎖可変領域および/または
配列番号9に示すアミノ酸配列を有する軽鎖可変領域
を含む、(I-1)〜(I-10)のいずれか1項に記載の抗体。
(I-13)
Fv、scFv、ディアボディ(diabody)、トリアボディ(triabody)、テトラボディ(tetrabody)、またはこれらの組み合わせである、(I-1)〜(I-12)のいずれか1項に記載の抗体。
(I-14)
定常領域を含む、(I-1)〜(I-11)のいずれか1項に記載の抗体。
(I-15)
キメラ抗体である、(I-1)〜(I-12)および(I-14)のいずれか1項に記載の抗体。
(I-16)
ヒト化抗体である、(I-1)〜(I-12)および(I-14)のいずれか1項に記載の抗体。
(I-17)
ヒト抗体である、(I-1)〜(I-12)および(I-14)のいずれか1項に記載の抗体。
(I-18)
イムノグロブリン、Fab、F(ab')2、ミニボディ(minibody)、scFv-Fc、またはこれらの組みあわせである、(I-1)〜(I-12)および(I-14)〜(I-17)のいずれか1項に記載の抗体。
(I-19)
IgA、IgD、IgE、IgG、またはIgMである、(I-1)〜(I-12)および(I-14)〜(I-18)のいずれか1項に記載の抗体。
(I-20)
配列番号5に示すアミノ酸配列を有する重鎖および/または配列番号10に示すアミノ酸配列を有する軽鎖を含む、(I-1)〜(I-12)および(I-14)〜(I-19)のいずれか1項に記載の抗体。
(I-21)
細胞障害活性を有する、(I-1)〜(I-20)のいずれか1項に記載の抗体。
(I-22)
細胞障害活性が、ADCC活性および/またはCDC活性である、(I-21)に記載の抗体。
(I-23)
多重特異性抗体である、(I-1)〜(I-22)のいずれか1項に記載の抗体。
(I-24)
サイトトキシンが結合してなる、(I-1)〜(I-23)のいずれか1項に記載の抗体。
(I-25)
モノクローナル抗体である、(I-1)〜(I-24)のいずれか1項に記載の抗体。
ポリヌクレオチド(II)は、以下の(II-1)に示すポリヌクレオチドを包含する。
(II-1)
上記抗体(I)のアミノ酸配列をコードする塩基配列を有するポリヌクレオチド。
宿主細胞(III)は、以下の(III-1)または(III-2)に示す宿主細胞を包含する。
(III-1)
ポリヌクレオチド(II)を保持する宿主細胞。
(III-2)
真核細胞である、(III-1)に記載の宿主細胞。
キメラ抗原受容体(IV)は、以下の(IV-1)〜(IV-5)に示すキメラ抗原受容体を包含する。
(IV-1)
上記抗体(I)と同一のエピトープを有するキメラ抗原受容体。
(IV-2)
上記抗体(I)の抗原認識部位を含む、(IV-1)に記載のキメラ抗原受容体。
(IV-3)
抗原認識部位が、
配列番号1に示すアミノ酸配列を有する重鎖CDR1、
配列番号2に示すアミノ酸配列を有する重鎖CDR2、および/または
配列番号3に示すアミノ酸配列を有する重鎖CDR3
を含む重鎖可変領域、ならびに/あるいは
配列番号6に示すアミノ酸配列を有する軽鎖CDR1、
配列番号7に示すアミノ酸配列を有する軽鎖CDR2、および/または
配列番号8に示すアミノ酸配列を有する軽鎖CDR3
を含む軽鎖可変領域
を含む、(IV-1)または(IV-2)に記載のキメラ抗原受容体。
(IV-4)
抗原認識部位が、
配列番号4に示すアミノ酸配列を有する重鎖可変領域および/または
配列番号9に示すアミノ酸配列を有する軽鎖可変領域
を含む、(IV-1)〜(IV-3)のいずれかに記載のキメラ抗原受容体。
(IV-5)
配列番号21に示すアミノ酸配列を有する(IV-1)〜(IV-4)のいずれか1項に記載のキメラ抗原受容体。
ポリヌクレオチド(V)は、上記ポリヌクレオチド(II)とは異なり、以下の(V-1)または(V-2)に示すポリヌクレオチドを包含する。
(V-1)
上記キメラ抗原受容体(IV)のアミノ酸配列をコードするポリヌクレオチド。
(V-2)
配列番号22に示す塩基配列を有する、(V-1)に記載のポリヌクレオチド。
細胞(VI)は、上記宿主細胞(III)とは異なり、以下の(VI-1)〜(VI-4)のいずれかに示す細胞を包含する。
(VI-1)
上記ポリヌクレオチド(V)を保持する細胞。
(VI-2)
真核細胞である、(VI-1)に記載の細胞。
(VI-3)
T細胞またはNK細胞である、(VI-1)または(VI-2)に記載の細胞。
(VI-4)
キメラ抗原受容体T細胞またはキメラ抗原受容体NK細胞である、(VI-1)〜(VI-3)のいずれか1項に記載の細胞。
医薬組成物(VII)は、以下の(VII-1)〜(VII-5)に示す医薬組成物を包含する。
(VII-1)
上記抗体(I)または上記細胞(VI)を含む医薬組成物。
(VII-2)
上記細胞がキメラ抗原受容体T細胞(VI-4)である、上記(VII-1)に記載の医薬組成物。
(VII-3)
癌の治療用である、(VII-1)または(VII-2)に記載の医薬組成物。
(VII-4)
癌が血液癌である、(VII-3)に記載の医薬組成物。
(VII-5)
血液癌が、形質細胞の腫瘍性増殖をきたす疾患である、(VII-4)に記載の医薬組成物。
疾患の治療または予防方法(VIII)は、以下の(VIII-1)〜(VIII-6)に示す疾患の治療または予防方法を包含する。
(VIII-1)
上記抗体(I)または上記細胞(VI)の治療有効量を被験体に投与する工程を含む、疾患の治療または予防方法。
(VIII-2)
上記細胞がキメラ抗原受容体T細胞(VI-4)である、上記(VIII-1)に記載の治療または予防方法。
(VIII-3)
疾患が癌であり、かつ被験体が癌に罹患する患者または癌に罹患する可能性のある動物である、(VIII-1)または(VIII-2)に記載の治療または予防方法。
(VIII-4)
癌が血液癌である、(VIII-3)に記載の治療または予防方法。
(VIII-5)
血液癌が、形質細胞の腫瘍性増殖をきたす疾患である、(VIII-4)に記載の治療または予防方法。
(VIII-6)
活性型ヒトインテグリンβ7を標的とした多発性骨髄腫の治療または予防方法。
使用(IX)は、以下の(IX-1)〜(IX-5)に示す使用を包含する。
(IX-1)
医薬組成物を製造するための、上記抗体(I)または上記細胞(VI)の使用。
(IX-2)
上記細胞がキメラ抗原受容体T細胞(VI-4)である、上記(IX-1)に記載の治療または予防方法。
(IX-3)
癌の治療用である、(IX-1)または(IX-2)に記載の使用。
(IX-4)
癌が血液癌である、(IX-3)に記載の使用。
(IX-5)
血液癌が、形質細胞の腫瘍性増殖をきたす疾患である、(IX-4)に記載の使用。
スクリーニング方法(X)は、以下の(X-1)〜(X-5)に示すスクリーニング方法を包含する。
(X-1)
化合物ライブラリーからヒトインテグリンβ7に特異的に結合し、且つ、ヒトインテグリンβ7の20〜109番目のアミノ酸残基からなる領域に結合する候補物質を選別する工程を含む、癌の治療用または予防用の医薬組成物の有効成分のスクリーニング方法。
(X-2)
さらに、細胞障害活性を有する物質を選別する工程を含む、(X-1)に記載のスクリーニング方法。
(X-3)
選別される物質がモノクローナル抗体である、(X-1)または(X-2)に記載のスクリーニング方法。
(X-4)
癌が血液癌である、(X-1)〜(X-3)のいずれか1項に記載のスクリーニング方法。
(X-5)
血液癌が、形質細胞の腫瘍性増殖をきたす疾患である、(X-4)に記載のスクリーニング方法。
診断方法(XI)は、以下の(XI-1)〜(XI-5)に示す診断方法を包含する。
(XI-1)
被験体から採取したサンプルと、上記抗体(I)とを接触させる工程を含む、癌の診断方法。
(XI-2)
被験体から採取したサンプルが、血液または骨髄液である、(XI-1)に記載の診断方法。
(XI-3)
上記抗体(I)と結合する細胞が検出された場合に癌に罹患した、または罹患する可能性があると判断する(XI-1)または(XI-2)に記載の診断方法。
(XI-4)
癌が血液癌である、(XI-3)に記載の診断方法。
(XI-5)
該細胞が形質細胞であり、かつ該癌が形質細胞の腫瘍性増殖をきたす疾患である、(XI-4)に記載の診断方法。
キット(XII)は、以下の(XII-1)〜(XII-3)に示すキットを包含する。
(XII-1)
上記抗体(I)を含む、癌の診断用キット。
(XII-2)
癌が血液癌である、(XII-1)に記載の診断方法。
(XII-3)
癌が、形質細胞の腫瘍性増殖をきたす疾患である、(XII-2)に記載のキット。
抗体(I)とは、好ましくは抗ヒトインテグリンβ7抗体であって、ヒトインテグリンβ7の20〜109番目のアミノ酸残基からなる領域にエピトープを有する抗体である。
配列番号1に示すアミノ酸配列を有する重鎖CDR1、
配列番号2に示すアミノ酸配列を有する重鎖CDR2、
配列番号3に示すアミノ酸配列を有する重鎖CDR3、
配列番号6に示すアミノ酸配列を有する軽鎖CDR1、
配列番号7に示すアミノ酸配列を有する軽鎖CDR2、
配列番号8に示すアミノ酸配列を有する軽鎖CDR3、
などが挙げられる。
細胞傷害活性を有する抗体は、例えば上記方法を用いて細胞傷害活性の有無を評価し、当該活性を有する抗体を選抜することによって得ることが出来る。
(1)ヒトインテグリンβ7の20〜109番目のアミノ酸残基からなる領域をエピトープとする、上記F(ab')2の構造の抗体を作製する:
(2)一方で、他の抗原に特異的に結合するF(ab')2の構造の抗体も同様に作製する:
(3)(1)および(2)で得られたそれぞれのF(ab')2の構造の抗体をDTTなどの還元剤を用いて処理した後に、どちらか片方の処理物にはさらにエルマン試薬で処理する:
(4)(3)で得られたこれらの処理後のF(ab')2構造の抗体を混合して反応させる:
といった(1)〜(4)に示す手順によっても二重特異性抗体を作製することができる。
(B)一方で、他の抗原に特異的に結合する抗体も同様に作製する。
(C)(A)および(B)で得られたそれぞれの可変領域のアミノ酸配列およびこれをコードするポリヌクレオチドの塩基配列を同定する。
(D)(C)にて同定したそれぞれの塩基配列を有するポリヌクレオチドを、要すれば定常部位の塩基配列配列、リンカー配列を有するポリヌクレオチドと共に組みこんだ発現ベクターを作製したのち、これをCHO細胞など抗体産生に適した宿主細胞に導入する。
といった(A)〜(D)に示す手順によっても二重特異性抗体を産生させることができる。
ポリヌクレオチド(II)とは、上記抗体(I)のアミノ酸配列をコードする塩基配列を有するポリヌクレオチドである。用語「ポリヌクレオチド」とは、たとえばリボヌクレオチド、デオキシリボヌクレオチド、またはこれらのいずれかのヌクレオチドなどが適宜公知の方法によって修飾されてなる一本鎖または二本鎖の形態を含む。
宿主細胞(III)とは、上記ポリヌクレオチド(II)を保持する細胞である。用語「保持」とは、細胞内に上記ポリヌクレオチド(II)が存在する状態を維持することをいい、当該細胞が自発的に上記ポリヌクレオチドを積極的かどうかに関わらず細胞外に排出しない状態であることを意味する。
キメラ抗原受容体とは、人工のT細胞受容体(TCR)様のタンパク質であり、T細胞の細胞膜上にて発現する(細胞外ドメインに相当する)抗原認識部位を所望の抗原認識部位に置換し、且つT細胞そのものが有する細胞障害活性などの機能を、より効果的に発揮できるように構築されたタンパク質である。
ポリヌクレオチド(V)とは、上記ポリヌクレオチド(II)とは異なり上記キメラ抗原受容体(IV)のアミノ酸配列をコードするポリヌクレオチドである。
細胞(VI)とは、上記宿主細胞(III)とは異なり、上記ポリヌクレオチド(V)を保持する細胞である。用語「保持」とは、上記宿主細胞(III)と同様にすることができる。具体的な細胞の種類も、上記宿主細胞(III)と同様にすることができるが、細胞障害活性を有するが好ましい。例えば、T細胞、NK細胞、K細胞などを挙げることができ、なかでもT細胞の一種であるキラーT細胞(細胞障害性T細胞〔CTL〕ともいう)が最も好ましい。
医薬組成物(VII)とは、上記抗体(I)または上記細胞(VI)を含む。上記細胞(VI)として、キメラ抗原受容体T細胞(VI-4)であることが好ましい。
疾患の治療または予防方法(VIII)とは、上記抗体(I)または上記細胞(VI)の治療有効量を被験体に投与する工程を含む、疾患の治療または予防方法である。細胞(VI)として、は好ましくはキメラ抗原受容体T細胞(VI-4)である。
使用(IX)とは、医薬組成物を製造するための、上記抗体(I)または上記細胞(IV)の使用である。
スクリーニング方法(X)とは形質細胞の腫瘍性増殖をきたす疾患の治療用または予防用の医薬組成物の有効成分のスクリーニング方法であって、化合物ライブラリーからヒトインテグリンβ7に特異的に結合し、且つ、ヒトインテグリンβ7の20〜109番目のアミノ酸残基からなる領域に結合する候補物質を選別する工程を含む。
診断方法(XI)とは癌の診断方法であり、被験体から採取したサンプルと、上記抗体(I)とを接触させる工程を含む。
キット(XII)とは、上記抗体(I)を含む、癌の診断用キットである。
以下の実施例において、細胞の選別のために用いたフローサイトメトリー(FACS)は下記の要領で行った。
・APC-conjugated anti-human CD34 antibody(BD Pharmingen社製)
・PE-Cy7-conjugated anti-human CD34 antibody(BD Pharmingen社製)
・APC/Cy7 -conjugated anti-human CD19 antibody(Biolegend社製)
・FITC-conjugated anti-human CD38 antibody(eBioscoience社製)
・APC-conjugated anti-human CD138 antibody(Biolegend社製)
・PE/Cy7-conjugated anti-human CD3 antibody(Biolegend社製)
・FITC-conjugated anti-human CD14 antibody(BD Pharmingen社製)
・PE/Cy7-conjugated anti-human CD45 antibody(Biolegend社製)。
骨髄腫細胞株に結合し健常人末梢血に結合しないモノクローナル抗体ライブラリーの作製 多発性骨髄腫に対する抗体治療においては、骨髄腫細胞には結合するが正常血液細胞には結合しない抗体を用いることが重要である。そこで、このような抗体を以下の方法により同定した。まず、以下の手法を用いて、様々な骨髄腫細胞株に結合するモノクローナル抗体を1万クローン以上作製した。
ヒト多発性骨髄腫患者骨髄において骨髄腫細胞特異的に結合する抗体の同定
上記の実施例1にて得られた約200クローンの候補抗体を用いて、骨髄腫患者由来の骨髄細胞を染色し、FACSを用いて解析した。
MMG49抗体が結合する抗原タンパクの同定
MMG49抗体が結合する抗原タンパクの同定を発現クローニング法によって行った。
ITGB7欠損骨髄腫細胞の作製によるMMG49抗体の結合抗原がITGB7発現タンパク質であることの確認
Crisp-Cas9システムを用いてITGB7欠損U266骨髄腫細胞株を作製した。
健常人末梢血および骨髄腫患者骨髄の各細胞分画におけるMMG49抗体の結合パターンの測定
市販されている抗インテグリンβ7抗体(FIB27抗体;Biolegend社)およびMMG49抗体を用いて、健常人末梢血および骨髄細胞における様々な細胞分画への結合を測定した。
MMG49の各種細胞株への結合の解析
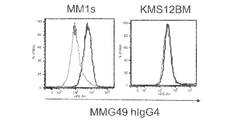
各種細胞株(MM1s細胞、U266細胞、RPMI8226細胞、およびJJN3細胞)におけるMMG49抗体およびFIB27抗体の結合をFACSを用いて解析した。染色の方法は上記実施例5に示す末梢血などの場合と同じである。
インテグリンの活性化とMMG49抗体の結合の関連の解析
上記のMMG49抗体の特異な結合様式から考えて、MMG49抗体は活性化して構造の変化したインテグリンβ7を認識しているのではないかと推測された。
MMG49抗体の認識に必須のエピトープの同定
MMG49抗体が認識しているエピトープを同定するために、オーバーラッピングPCR法を用いて、図11に示すような8種類のヒト/マウスキメラインテグリンβ7タンパク質発現用ベクターを作製した。
MMG49抗体の抗体分子可変部領域の塩基配列の決定
MMG49抗体サブクラスの確認はIsotyping kit(Roche社)を用いて行ったところ、IgG2aサブクラスであることを確認した。さらに、MMG49抗体の可変部領域の塩基配列およびアミノ酸配列を決定した。
MMG49抗体の抗体分子可変部領域を用いたキメラ抗原受容体T細胞の作製
MMG49抗体分子可変部配列を用いたchimeric antigen receptor T cell(以下、MMG49抗体由来キメラ抗原受容体T細胞と呼ぶ。)の作製は、非特許文献2〜4などを参照しながら以下の手順で行った。
Jurkat細胞からTrizol(Invitrogen社)を用いてRNAを採取し、さらにSuperscript III cDNA synthesis kit(Invitrogen社)を用いてcDNAを作製した。そして、それを鋳型としてPCRによりCD28およびCD3zのcDNAを増幅し、それぞれ、TA cloning kit(Invitrogen社)を用いてクローニングし、シークエンシングによりこれらの塩基配列を確認した。
オーバーラッピングPCR法を用いて、MMG49抗体由来のVL領域およびVH領域、ならびに上記クローニングしたCD28およびCD3zの各遺伝子断片を結合し、キメラcDNAを作製した。その手順と用いたプライマーを図15に示す。用いたプライマーの塩基配列を以下の表5に示す。
次いで、(2)で結合されたキメラcDNAをEcoRI/SalIの二つの制限酵素で切り出し、MSCV-ires-GFPベクターに挿入した。
次いで、ヒトT細胞へMMG49抗体由来キメラ抗原受容体のcDNAの導入は以下のように行った。
MMG49抗体由来キメラ抗原受容体T細胞によるITGB7発現腫瘍細胞の認識と細胞傷害活性の解析
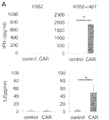
上述の方法により作製したMMG49抗体由来キメラ抗原受容体T細胞あるいはGFPだけを導入されたコントロールT細胞とインテグリンβ7を発現していないK562細胞あるいはインテグリンα4β7を強制発現させたK562細胞を共培養し、産生されるサイトカインの量を定量した。具体的にはT細胞およびターゲット細胞のそれぞれ1x105個を96ウェルプレートに加えた。24時間後に上清を回収し、ELISAにてIFN-γの産生量を測定した。測定はQuantikine kit(R&D社)を用いて行った。その結果、インテグリンα4β7を強制発現させたK562細胞とMMG49抗体由来キメラ抗原受容体T細胞との共培養においてのみ、control(GFP発現ベクターを導入した刺激後の末梢血単核球を同様に培養して得られるT細胞)よりも高いIFN-γおよびIL2の産生が見られた(図17)。
次に、MMG49抗体由来キメラ抗原受容体T細胞あるいはGFPだけを導入されたコントロールT細胞とMMG49抗体が結合する骨髄腫細胞株(MM.1s細胞、RPMI8226細胞、およびJJN3細胞)あるいはMMG49抗体が結合しない細胞(KMS12BM, Molt4, およびRaji細胞)とを共培養し、同様に産生されるサイトカインの量を定量した。その結果、MMG49抗体が結合する細胞であるMM.1s、RPMI8226細胞、およびJJN3細胞とMMG49抗体由来キメラ抗原受容体T細胞とを共培養したときにのみ、control(GFP発現ベクターを導入した刺激後の末梢血単核球を同様に培養して得られるT細胞)よりも高いIFN-γおよびIL2の産生が見られた(図18および19)。これらの結果は、MMG49抗体由来キメラ抗原受容体T細胞はMMG49抗体が認識する抗原(これをMMG49抗原と呼ぶことがある。)を認識することにより活性化していることを示している。
A: 実験に用いた細胞からの51Crの放出量
B: 抗体の存在しない状態での自発的な51Crの放出量
C: 1%のTriton X-100の添加による最大51Cr放出量
D: 抗体の存在しない状態での自発的51Crの放出量。
MMG49抗体由来キメラ抗原受容体T細胞によるin vivoにおける骨髄腫瘍細胞排除能の解析 MMG49抗体由来キメラ抗原受容体T細胞を用いて、in vivoでの多発性骨髄腫に対する治療効果を調べた。
MMG49抗体のエピトープについて、実施例8にて検討した結果を更に詳細に検討する実験を行った。図25に示すような3種類のヒト/マウスキメラインテグリンβ7タンパク質発現用ベクターを作製し、それぞれの発現ベクターをリポフェクション法により293T細胞に導入し、48時間後にMMG49抗体の結合の有無をFACSにて解析した。
ヒトインテグリンβ7、マウスインテグリンβ7、およびヒトインテグリンβ7の1あるいは2アミノ酸のみをマウス由来のアミノ酸配列に変異させた各種変異体(R35E/N36D、H38D、M41L/L42Q、およびA48V)を発現するベクターをリポフェクション法により293T細胞に導入し、その後は実施例8と同様に実験を行った。その結果、図26に示すように、A48V変異体のみがMMG49抗体に対する結合力がヒトインテグリンβ7と比べて顕著に減少し、マウマウスインテグリンβ7の数値に近くなることが明らかとなった。この結果より、ヒトインテグリンβ7の48番目のアミノ酸残基が、MMG49抗体のエピトープに強く関連するか、またはMMG49抗体のエピトープに含まれることが明らかとなった。
Claims (12)
- 配列番号1に示すアミノ酸配列を有する重鎖CDR1、
配列番号2に示すアミノ酸配列を有する重鎖CDR2、および
配列番号3に示すアミノ酸配列を有する重鎖CDR3
を含む重鎖可変領域、ならびに
配列番号6に示すアミノ酸配列を有する軽鎖CDR1、
配列番号7に示すアミノ酸配列を有する軽鎖CDR2、および
配列番号8に示すアミノ酸配列を有する軽鎖CDR3
を含む軽鎖可変領域
を含む、抗ヒトインテグリンβ 7 抗体。 - 前記抗体が、配列番号4に示すアミノ酸配列を有する重鎖可変領域および配列番号9に示すアミノ酸配列を有する軽鎖可変領域
を含む、請求項1に記載の抗体。 - 多重特異性抗体である、請求項1又は2に記載の抗体。
- 請求項1〜3のいずれか1項に記載の抗体の抗原認識部位を含む、キメラ抗原受容体。
- 請求項4に記載のキメラ抗原受容体を発現する細胞。
- 請求項4に記載のキメラ抗原受容体をコードするポリヌクレオチド。
- 請求項6に記載するポリヌクレオチドを含むベクター。
- 請求項6に記載のポリヌクレオチドまたは請求項7の記載のベクターを保持する細胞。
- キメラ抗原受容体T細胞又はNK細胞である、請求項5または8に記載の細胞。
- 請求項1〜3のいずれか1項に記載の抗体を含む、多発性骨髄腫の治療のための医薬組成物。
- 請求項9に記載のキメラ抗原受容体T細胞又はNK細胞を含む、多発性骨髄腫の治療のための医薬組成物。
- 前記キメラ抗原受容体T細胞またはNK細胞を、1日あたり、104細胞/kg〜109細胞/kgで投与されること特徴とする、請求項11に記載の医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015159240 | 2015-08-11 | ||
| JP2015159240 | 2015-08-11 | ||
| PCT/JP2016/072688 WO2017026331A1 (ja) | 2015-08-11 | 2016-08-02 | 抗体 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019101116A Division JP2019201641A (ja) | 2015-08-11 | 2019-05-30 | 抗体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2017026331A1 JPWO2017026331A1 (ja) | 2018-05-31 |
| JP6548052B2 true JP6548052B2 (ja) | 2019-07-24 |
Family
ID=57983824
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017534378A Active JP6548052B2 (ja) | 2015-08-11 | 2016-08-02 | 抗体 |
| JP2019101116A Withdrawn JP2019201641A (ja) | 2015-08-11 | 2019-05-30 | 抗体 |
| JP2021085852A Pending JP2021130676A (ja) | 2015-08-11 | 2021-05-21 | 抗体 |
| JP2023070426A Pending JP2023093656A (ja) | 2015-08-11 | 2023-04-21 | 抗体 |
Family Applications After (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019101116A Withdrawn JP2019201641A (ja) | 2015-08-11 | 2019-05-30 | 抗体 |
| JP2021085852A Pending JP2021130676A (ja) | 2015-08-11 | 2021-05-21 | 抗体 |
| JP2023070426A Pending JP2023093656A (ja) | 2015-08-11 | 2023-04-21 | 抗体 |
Country Status (13)
| Country | Link |
|---|---|
| US (4) | US10654931B2 (ja) |
| EP (1) | EP3336184A4 (ja) |
| JP (4) | JP6548052B2 (ja) |
| KR (1) | KR20180030922A (ja) |
| CN (2) | CN113893341A (ja) |
| AU (2) | AU2016306320B2 (ja) |
| CA (1) | CA2995046A1 (ja) |
| HK (1) | HK1249549A1 (ja) |
| IL (2) | IL301753A (ja) |
| MX (2) | MX2018001668A (ja) |
| PH (1) | PH12018500258A1 (ja) |
| SG (2) | SG11201800864XA (ja) |
| WO (1) | WO2017026331A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017026331A1 (ja) * | 2015-08-11 | 2017-02-16 | 国立大学法人大阪大学 | 抗体 |
| JP2020511498A (ja) * | 2017-03-20 | 2020-04-16 | シティ・オブ・ホープCity of Hope | Alアミロイドーシスの治療のためのcs1標的化キメラ抗原レセプター改変t細胞 |
| CN110577605A (zh) * | 2018-06-11 | 2019-12-17 | 浙江启新生物技术有限公司 | 一种靶向多发性骨髓瘤多种抗原的嵌合抗原受体t(car-t)细胞的构建方法及其应用 |
| WO2023013765A1 (ja) * | 2021-08-06 | 2023-02-09 | 大塚製薬株式会社 | キメラ抗原受容体を検出するためのプライマーセット |
| TW202322822A (zh) | 2021-08-20 | 2023-06-16 | 日商大塚製藥股份有限公司 | 組合醫藥 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3180125B2 (ja) | 1992-03-07 | 2001-06-25 | 道生 河野 | ヒト成熟骨髄腫細胞に対するモノクローナル抗体 |
| JPH06303990A (ja) * | 1993-04-24 | 1994-11-01 | Kanebo Ltd | モノクローナル抗体、それを産生するハイブリドーマおよび該抗体の製造方法 |
| SK170497A3 (en) | 1996-04-15 | 1998-09-09 | Icos Corp | Cytoplasmic modulators of integrin regulation/signaling |
| US7147851B1 (en) | 1996-08-15 | 2006-12-12 | Millennium Pharmaceuticals, Inc. | Humanized immunoglobulin reactive with α4β7 integrin |
| US6376654B1 (en) | 1999-08-13 | 2002-04-23 | Molecular Discoveries, Llc | Myeloma cell and ovarian cancer cell surface glycoproteins, antibodies thereto, and uses thereof |
| CA2532547C (en) * | 2003-07-24 | 2020-02-25 | Innate Pharma | Methods and compositions for increasing the efficiency of therapeutic antibodies using nk cell potentiating compounds |
| AU2007240507B2 (en) | 2006-04-21 | 2013-07-18 | Novartis Ag | Antagonist anti-CD40 antibody pharmaceutical compositions |
| EP2315779A2 (en) | 2008-07-09 | 2011-05-04 | Biogen Idec MA Inc. | Compositions comprising antibodies to lingo or fragments thereof |
| CN102388068B (zh) | 2009-03-20 | 2015-05-20 | 安姆根有限公司 | α-4-β-7异二聚体特异性拮抗剂抗体 |
| WO2010117059A1 (ja) | 2009-04-10 | 2010-10-14 | 国立大学法人大阪大学 | 形質細胞の腫瘍性増殖をきたす疾患の治療薬 |
| WO2012022634A1 (en) * | 2010-08-16 | 2012-02-23 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | Classification, diagnosis and prognosis of multiple myeloma |
| UA116189C2 (uk) * | 2011-05-02 | 2018-02-26 | Мілленніум Фармасьютікалз, Інк. | КОМПОЗИЦІЯ АНТИ-α4β7 АНТИТІЛА |
| AU2013221672B2 (en) | 2012-02-13 | 2017-11-09 | Seattle Children's Hospital D/B/A Seattle Children's Research Institute | Bispecific chimeric antigen receptors and therapeutic uses thereof |
| CN103374073A (zh) * | 2012-04-26 | 2013-10-30 | 中国科学院上海生命科学研究院 | 识别活化形式整合素α4β7的人源化单克隆抗体 |
| CN105143876B (zh) | 2013-03-27 | 2018-04-20 | 豪夫迈·罗氏有限公司 | 生物标志物用于评估用β7整联蛋白拮抗剂治疗胃肠炎性病症的用途 |
| CN105722859B (zh) * | 2013-07-25 | 2021-05-07 | 西托姆克斯治疗公司 | 多特异性抗体、多特异性可活化抗体及其使用方法 |
| WO2017026331A1 (ja) * | 2015-08-11 | 2017-02-16 | 国立大学法人大阪大学 | 抗体 |
-
2016
- 2016-08-02 WO PCT/JP2016/072688 patent/WO2017026331A1/ja active Application Filing
- 2016-08-02 AU AU2016306320A patent/AU2016306320B2/en active Active
- 2016-08-02 SG SG11201800864XA patent/SG11201800864XA/en unknown
- 2016-08-02 IL IL301753A patent/IL301753A/en unknown
- 2016-08-02 CN CN202111106559.9A patent/CN113893341A/zh active Pending
- 2016-08-02 US US15/751,574 patent/US10654931B2/en active Active
- 2016-08-02 IL IL257368A patent/IL257368B2/en unknown
- 2016-08-02 MX MX2018001668A patent/MX2018001668A/es unknown
- 2016-08-02 EP EP16835028.8A patent/EP3336184A4/en active Pending
- 2016-08-02 CA CA2995046A patent/CA2995046A1/en active Pending
- 2016-08-02 KR KR1020187006417A patent/KR20180030922A/ko not_active Application Discontinuation
- 2016-08-02 JP JP2017534378A patent/JP6548052B2/ja active Active
- 2016-08-02 SG SG10201913748QA patent/SG10201913748QA/en unknown
- 2016-08-02 CN CN201680046842.8A patent/CN107922938B/zh active Active
-
2018
- 2018-02-02 PH PH12018500258A patent/PH12018500258A1/en unknown
- 2018-02-08 MX MX2022013566A patent/MX2022013566A/es unknown
- 2018-07-16 HK HK18109155.2A patent/HK1249549A1/zh unknown
-
2019
- 2019-05-30 JP JP2019101116A patent/JP2019201641A/ja not_active Withdrawn
-
2020
- 2020-03-04 US US16/808,451 patent/US20200283533A1/en not_active Abandoned
- 2020-06-18 US US16/905,211 patent/US10988540B2/en active Active
-
2021
- 2021-03-22 US US17/208,014 patent/US20220041735A1/en active Pending
- 2021-05-21 JP JP2021085852A patent/JP2021130676A/ja active Pending
-
2022
- 2022-07-04 AU AU2022204792A patent/AU2022204792A1/en active Pending
-
2023
- 2023-04-21 JP JP2023070426A patent/JP2023093656A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CN107922938B (zh) | 2021-09-17 |
| US10654931B2 (en) | 2020-05-19 |
| IL257368B2 (en) | 2023-09-01 |
| JPWO2017026331A1 (ja) | 2018-05-31 |
| AU2016306320B2 (en) | 2022-04-14 |
| IL257368B1 (en) | 2023-05-01 |
| CA2995046A1 (en) | 2017-02-16 |
| JP2019201641A (ja) | 2019-11-28 |
| KR20180030922A (ko) | 2018-03-26 |
| US20220041735A1 (en) | 2022-02-10 |
| US20180230216A1 (en) | 2018-08-16 |
| HK1249549A1 (zh) | 2018-11-02 |
| SG11201800864XA (en) | 2018-03-28 |
| MX2022013566A (es) | 2022-11-30 |
| EP3336184A4 (en) | 2019-01-23 |
| EP3336184A1 (en) | 2018-06-20 |
| CN113893341A (zh) | 2022-01-07 |
| IL301753A (en) | 2023-05-01 |
| AU2016306320A1 (en) | 2018-03-08 |
| US20200283533A1 (en) | 2020-09-10 |
| MX2018001668A (es) | 2018-05-07 |
| IL257368A (en) | 2018-04-30 |
| CN107922938A (zh) | 2018-04-17 |
| SG10201913748QA (en) | 2020-03-30 |
| AU2022204792A1 (en) | 2022-09-15 |
| WO2017026331A1 (ja) | 2017-02-16 |
| US20200385474A1 (en) | 2020-12-10 |
| PH12018500258A1 (en) | 2018-08-13 |
| JP2021130676A (ja) | 2021-09-09 |
| JP2023093656A (ja) | 2023-07-04 |
| AU2016306320A2 (en) | 2018-03-22 |
| US10988540B2 (en) | 2021-04-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2976361B1 (en) | Humanized anti-cd134 (ox40) antibodies and uses thereof | |
| ES2792183T3 (es) | Anticuerpos anti-PD1 y su uso como productos terapéuticos y de diagnóstico | |
| JP6548052B2 (ja) | 抗体 | |
| JP2020514363A (ja) | 腫瘍特異的細胞枯渇のためのFc最適化抗CD25 | |
| JP6534074B2 (ja) | 抗体 | |
| KR20210111792A (ko) | 암 및 다른 질환을 치료하기 위한 클라우딘 18.2에 특이적인 결합 분자, 이의 조성물 및 방법 | |
| KR20210075090A (ko) | Gm-csf 길항제를 이용한 면역요법-관련 독성의 치료 방법 | |
| JP2022515258A (ja) | Cd19及びcd3と結合可能な多重特異性抗原結合タンパク質、ならびにその使用 | |
| KR20240073008A (ko) | Cd137 및 종양 연관 항원에 결합하는 이중특이적 결합 단백질 | |
| WO2022082005A1 (en) | Multispecific binding compounds that bind to pd-l1 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180206 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181122 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181122 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20181122 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20181212 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190313 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190514 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190612 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6548052 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |