JP6476181B2 - ペプチド - Google Patents
ペプチド Download PDFInfo
- Publication number
- JP6476181B2 JP6476181B2 JP2016532780A JP2016532780A JP6476181B2 JP 6476181 B2 JP6476181 B2 JP 6476181B2 JP 2016532780 A JP2016532780 A JP 2016532780A JP 2016532780 A JP2016532780 A JP 2016532780A JP 6476181 B2 JP6476181 B2 JP 6476181B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- rnb
- peptide
- tshr
- peptides
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims description 212
- 102000003911 Thyrotropin Receptors Human genes 0.000 claims description 108
- 108090000253 Thyrotropin Receptors Proteins 0.000 claims description 108
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 92
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 59
- 239000000427 antigen Substances 0.000 claims description 48
- 108091007433 antigens Proteins 0.000 claims description 48
- 102000036639 antigens Human genes 0.000 claims description 48
- 239000000203 mixture Substances 0.000 claims description 37
- 208000015023 Graves' disease Diseases 0.000 claims description 34
- 238000011282 treatment Methods 0.000 claims description 29
- 238000001727 in vivo Methods 0.000 claims description 15
- 238000004519 manufacturing process Methods 0.000 claims description 13
- 108010064885 HLA-DR3 Antigen Proteins 0.000 claims description 12
- 238000000338 in vitro Methods 0.000 claims description 12
- 108010046732 HLA-DR4 Antigen Proteins 0.000 claims description 11
- 208000023328 Basedow disease Diseases 0.000 claims description 7
- 230000030741 antigen processing and presentation Effects 0.000 claims description 5
- 230000002401 inhibitory effect Effects 0.000 claims description 5
- 230000000903 blocking effect Effects 0.000 claims description 4
- 239000003814 drug Substances 0.000 claims description 4
- 230000002265 prevention Effects 0.000 claims description 4
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 2
- 241000699670 Mus sp. Species 0.000 description 94
- 210000004027 cell Anatomy 0.000 description 57
- 150000001413 amino acids Chemical class 0.000 description 43
- 235000001014 amino acid Nutrition 0.000 description 41
- 210000004408 hybridoma Anatomy 0.000 description 33
- 210000000612 antigen-presenting cell Anatomy 0.000 description 30
- 208000003807 Graves Disease Diseases 0.000 description 27
- 230000003053 immunization Effects 0.000 description 21
- 210000001165 lymph node Anatomy 0.000 description 20
- 238000000034 method Methods 0.000 description 20
- 238000002649 immunization Methods 0.000 description 18
- 206010020850 Hyperthyroidism Diseases 0.000 description 16
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 16
- 239000002953 phosphate buffered saline Substances 0.000 description 16
- 230000020382 suppression by virus of host antigen processing and presentation of peptide antigen via MHC class I Effects 0.000 description 16
- 210000001685 thyroid gland Anatomy 0.000 description 16
- 108091005601 modified peptides Proteins 0.000 description 14
- 230000004044 response Effects 0.000 description 14
- 230000004073 interleukin-2 production Effects 0.000 description 13
- 108010047214 HLA-DRB1*03:01 antigen Proteins 0.000 description 12
- 102000004169 proteins and genes Human genes 0.000 description 12
- 108090000623 proteins and genes Proteins 0.000 description 12
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 11
- 230000028993 immune response Effects 0.000 description 11
- 235000018102 proteins Nutrition 0.000 description 11
- 230000000638 stimulation Effects 0.000 description 11
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 10
- 241000699666 Mus <mouse, genus> Species 0.000 description 10
- 238000005259 measurement Methods 0.000 description 10
- 102000043131 MHC class II family Human genes 0.000 description 9
- 108091054438 MHC class II family Proteins 0.000 description 9
- 230000006052 T cell proliferation Effects 0.000 description 9
- 238000002347 injection Methods 0.000 description 9
- 239000007924 injection Substances 0.000 description 9
- 210000004988 splenocyte Anatomy 0.000 description 9
- 102000043129 MHC class I family Human genes 0.000 description 8
- 108091054437 MHC class I family Proteins 0.000 description 8
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 8
- 238000002474 experimental method Methods 0.000 description 8
- 230000001965 increasing effect Effects 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 208000024891 symptom Diseases 0.000 description 8
- 238000002965 ELISA Methods 0.000 description 7
- 108010029657 HLA-DRB1*04:01 antigen Proteins 0.000 description 7
- 108010002350 Interleukin-2 Proteins 0.000 description 7
- 102000000588 Interleukin-2 Human genes 0.000 description 7
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 7
- 201000010099 disease Diseases 0.000 description 7
- 230000000694 effects Effects 0.000 description 7
- 239000002609 medium Substances 0.000 description 7
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 6
- XUIIKFGFIJCVMT-GFCCVEGCSA-N D-thyroxine Chemical compound IC1=CC(C[C@@H](N)C(O)=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-GFCCVEGCSA-N 0.000 description 6
- 239000012894 fetal calf serum Substances 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 230000024664 tolerance induction Effects 0.000 description 6
- 206010011968 Decreased immune responsiveness Diseases 0.000 description 5
- 239000004471 Glycine Substances 0.000 description 5
- AUYYCJSJGJYCDS-LBPRGKRZSA-N Thyrolar Chemical class IC1=CC(C[C@H](N)C(O)=O)=CC(I)=C1OC1=CC=C(O)C(I)=C1 AUYYCJSJGJYCDS-LBPRGKRZSA-N 0.000 description 5
- 102000011923 Thyrotropin Human genes 0.000 description 5
- 108010061174 Thyrotropin Proteins 0.000 description 5
- 239000003200 antithyroid agent Substances 0.000 description 5
- 229940043671 antithyroid preparations Drugs 0.000 description 5
- 210000003719 b-lymphocyte Anatomy 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 230000004663 cell proliferation Effects 0.000 description 5
- 239000003086 colorant Substances 0.000 description 5
- 229910052740 iodine Inorganic materials 0.000 description 5
- 239000008194 pharmaceutical composition Substances 0.000 description 5
- 102000005962 receptors Human genes 0.000 description 5
- 108020003175 receptors Proteins 0.000 description 5
- 239000006228 supernatant Substances 0.000 description 5
- 230000003614 tolerogenic effect Effects 0.000 description 5
- 238000010152 Bonferroni least significant difference Methods 0.000 description 4
- 239000002671 adjuvant Substances 0.000 description 4
- 238000000540 analysis of variance Methods 0.000 description 4
- 238000010171 animal model Methods 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 239000012634 fragment Substances 0.000 description 4
- 102000054766 genetic haplotypes Human genes 0.000 description 4
- 230000002163 immunogen Effects 0.000 description 4
- 230000006698 induction Effects 0.000 description 4
- KDXKERNSBIXSRK-UHFFFAOYSA-N lysine Chemical compound NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 4
- 230000003287 optical effect Effects 0.000 description 4
- 239000002245 particle Substances 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- 230000035755 proliferation Effects 0.000 description 4
- 230000004043 responsiveness Effects 0.000 description 4
- 230000004936 stimulating effect Effects 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- 239000005495 thyroid hormone Substances 0.000 description 4
- 229940036555 thyroid hormone Drugs 0.000 description 4
- 229940034208 thyroxine Drugs 0.000 description 4
- XUIIKFGFIJCVMT-UHFFFAOYSA-N thyroxine-binding globulin Natural products IC1=CC(CC([NH3+])C([O-])=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-UHFFFAOYSA-N 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 3
- 208000023275 Autoimmune disease Diseases 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 108010027412 Histocompatibility Antigens Class II Proteins 0.000 description 3
- 102000018713 Histocompatibility Antigens Class II Human genes 0.000 description 3
- 206010020751 Hypersensitivity Diseases 0.000 description 3
- 239000004472 Lysine Substances 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 108091008874 T cell receptors Proteins 0.000 description 3
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 3
- 208000026935 allergic disease Diseases 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 238000003776 cleavage reaction Methods 0.000 description 3
- 239000012228 culture supernatant Substances 0.000 description 3
- 238000004108 freeze drying Methods 0.000 description 3
- 230000004927 fusion Effects 0.000 description 3
- 210000005260 human cell Anatomy 0.000 description 3
- 230000005847 immunogenicity Effects 0.000 description 3
- 239000011630 iodine Substances 0.000 description 3
- 239000003446 ligand Substances 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 230000002093 peripheral effect Effects 0.000 description 3
- 230000037452 priming Effects 0.000 description 3
- 230000007017 scission Effects 0.000 description 3
- 239000012679 serum free medium Substances 0.000 description 3
- 210000000952 spleen Anatomy 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 238000011830 transgenic mouse model Methods 0.000 description 3
- 241000701161 unidentified adenovirus Species 0.000 description 3
- 210000002845 virion Anatomy 0.000 description 3
- 230000000007 visual effect Effects 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- 108091006027 G proteins Proteins 0.000 description 2
- 102000030782 GTP binding Human genes 0.000 description 2
- 108091000058 GTP-Binding Proteins 0.000 description 2
- 206010018498 Goitre Diseases 0.000 description 2
- 108010067802 HLA-DR alpha-Chains Proteins 0.000 description 2
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 206010020880 Hypertrophy Diseases 0.000 description 2
- 102100037850 Interferon gamma Human genes 0.000 description 2
- 108010074328 Interferon-gamma Proteins 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- 206010028665 Myxoedema Diseases 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 230000033289 adaptive immune response Effects 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 230000007815 allergy Effects 0.000 description 2
- 210000004899 c-terminal region Anatomy 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 238000001516 cell proliferation assay Methods 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 210000004443 dendritic cell Anatomy 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 210000002257 embryonic structure Anatomy 0.000 description 2
- 210000002919 epithelial cell Anatomy 0.000 description 2
- 208000030533 eye disease Diseases 0.000 description 2
- 210000000744 eyelid Anatomy 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 201000003872 goiter Diseases 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 230000016784 immunoglobulin production Effects 0.000 description 2
- 230000017307 interleukin-4 production Effects 0.000 description 2
- 108020001756 ligand binding domains Proteins 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- 208000003786 myxedema Diseases 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 239000008188 pellet Substances 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000012552 review Methods 0.000 description 2
- 230000003248 secreting effect Effects 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 229940104230 thymidine Drugs 0.000 description 2
- 210000001541 thymus gland Anatomy 0.000 description 2
- 102000015486 thyroid-stimulating hormone receptor activity proteins Human genes 0.000 description 2
- 108040006218 thyroid-stimulating hormone receptor activity proteins Proteins 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- IQFYYKKMVGJFEH-OFKYTIFKSA-N 1-[(2r,4s,5r)-4-hydroxy-5-(tritiooxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound C1[C@H](O)[C@@H](CO[3H])O[C@H]1N1C(=O)NC(=O)C(C)=C1 IQFYYKKMVGJFEH-OFKYTIFKSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- UAIUNKRWKOVEES-UHFFFAOYSA-N 3,3',5,5'-tetramethylbenzidine Chemical compound CC1=C(N)C(C)=CC(C=2C=C(C)C(N)=C(C)C=2)=C1 UAIUNKRWKOVEES-UHFFFAOYSA-N 0.000 description 1
- HYCKBFLTZGORKA-HNPMAXIBSA-N 3,7-dihydropurin-6-one;1-[(2r,4s,5r)-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound O=C1NC=NC2=C1NC=N2.O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 HYCKBFLTZGORKA-HNPMAXIBSA-N 0.000 description 1
- -1 8-25 amino acids Chemical class 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 206010054196 Affect lability Diseases 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 208000019901 Anxiety disease Diseases 0.000 description 1
- 208000032116 Autoimmune Experimental Encephalomyelitis Diseases 0.000 description 1
- 101150076489 B gene Proteins 0.000 description 1
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 1
- 201000004569 Blindness Diseases 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 102100040505 HLA class II histocompatibility antigen, DR alpha chain Human genes 0.000 description 1
- 102100040485 HLA class II histocompatibility antigen, DRB1 beta chain Human genes 0.000 description 1
- 108010058597 HLA-DR Antigens Proteins 0.000 description 1
- 102000006354 HLA-DR Antigens Human genes 0.000 description 1
- 108010039343 HLA-DRB1 Chains Proteins 0.000 description 1
- 101000599940 Homo sapiens Interferon gamma Proteins 0.000 description 1
- 101001002657 Homo sapiens Interleukin-2 Proteins 0.000 description 1
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 1
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 1
- 101000772267 Homo sapiens Thyrotropin receptor Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 208000008454 Hyperhidrosis Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 108010036012 Iodide peroxidase Proteins 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- 150000008575 L-amino acids Chemical class 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 206010023644 Lacrimation increased Diseases 0.000 description 1
- 102100037611 Lysophospholipase Human genes 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 101100394237 Mus musculus Hand1 gene Proteins 0.000 description 1
- 241000187479 Mycobacterium tuberculosis Species 0.000 description 1
- 206010061323 Optic neuropathy Diseases 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 102000007079 Peptide Fragments Human genes 0.000 description 1
- 108010033276 Peptide Fragments Proteins 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 206010034719 Personality change Diseases 0.000 description 1
- 108010058864 Phospholipases A2 Proteins 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 208000001431 Psychomotor Agitation Diseases 0.000 description 1
- 208000028017 Psychotic disease Diseases 0.000 description 1
- 239000012979 RPMI medium Substances 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 206010038743 Restlessness Diseases 0.000 description 1
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 1
- 208000032023 Signs and Symptoms Diseases 0.000 description 1
- 208000013738 Sleep Initiation and Maintenance disease Diseases 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 230000006044 T cell activation Effects 0.000 description 1
- 230000017274 T cell anergy Effects 0.000 description 1
- 230000005867 T cell response Effects 0.000 description 1
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 1
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 1
- 206010057040 Temperature intolerance Diseases 0.000 description 1
- 102000009843 Thyroglobulin Human genes 0.000 description 1
- 108010034949 Thyroglobulin Proteins 0.000 description 1
- 102000014267 Thyroid peroxidases Human genes 0.000 description 1
- 206010052779 Transplant rejections Diseases 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- 206010044565 Tremor Diseases 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 238000011481 absorbance measurement Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 210000005006 adaptive immune system Anatomy 0.000 description 1
- 102000030621 adenylate cyclase Human genes 0.000 description 1
- 108060000200 adenylate cyclase Proteins 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- WYTGDNHDOZPMIW-RCBQFDQVSA-N alstonine Natural products C1=CC2=C3C=CC=CC3=NC2=C2N1C[C@H]1[C@H](C)OC=C(C(=O)OC)[C@H]1C2 WYTGDNHDOZPMIW-RCBQFDQVSA-N 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 230000036506 anxiety Effects 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000006470 autoimmune attack Effects 0.000 description 1
- 239000003659 bee venom Substances 0.000 description 1
- 230000003542 behavioural effect Effects 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 102000005936 beta-Galactosidase Human genes 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000000337 buffer salt Substances 0.000 description 1
- 230000011496 cAMP-mediated signaling Effects 0.000 description 1
- 238000012754 cardiac puncture Methods 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 210000004087 cornea Anatomy 0.000 description 1
- 230000004940 costimulation Effects 0.000 description 1
- 230000000139 costimulatory effect Effects 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000012202 endocytosis Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 1
- 208000012997 experimental autoimmune encephalomyelitis Diseases 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 239000012595 freezing medium Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 125000000291 glutamic acid group Chemical group N[C@@H](CCC(O)=O)C(=O)* 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 229960002743 glutamine Drugs 0.000 description 1
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 description 1
- 208000024963 hair loss Diseases 0.000 description 1
- 230000003676 hair loss Effects 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 102000051345 human TSHR Human genes 0.000 description 1
- 208000013403 hyperactivity Diseases 0.000 description 1
- 206010020718 hyperplasia Diseases 0.000 description 1
- 230000009610 hypersensitivity Effects 0.000 description 1
- 230000001969 hypertrophic effect Effects 0.000 description 1
- 208000003532 hypothyroidism Diseases 0.000 description 1
- 230000002989 hypothyroidism Effects 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000003832 immune regulation Effects 0.000 description 1
- 230000006058 immune tolerance Effects 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000002998 immunogenetic effect Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000000126 in silico method Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 206010021654 increased appetite Diseases 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 239000012678 infectious agent Substances 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000011221 initial treatment Methods 0.000 description 1
- 206010022437 insomnia Diseases 0.000 description 1
- 230000031261 interleukin-10 production Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 230000026045 iodination Effects 0.000 description 1
- 238000006192 iodination reaction Methods 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 1
- 238000011813 knockout mouse model Methods 0.000 description 1
- 230000004317 lacrimation Effects 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 230000013011 mating Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 230000003557 neuropsychological effect Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 210000001328 optic nerve Anatomy 0.000 description 1
- 208000020911 optic nerve disease Diseases 0.000 description 1
- 238000010979 pH adjustment Methods 0.000 description 1
- 239000006179 pH buffering agent Substances 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 231100000915 pathological change Toxicity 0.000 description 1
- 230000036285 pathological change Effects 0.000 description 1
- 108010009699 peptide 5F Proteins 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 231100000572 poisoning Toxicity 0.000 description 1
- 230000000607 poisoning effect Effects 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000002953 preparative HPLC Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 230000017854 proteolysis Effects 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 238000012163 sequencing technique Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 230000035900 sweating Effects 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 229960002175 thyroglobulin Drugs 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000009966 trimming Methods 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 208000034280 venom allergy Diseases 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/72—Receptors; Cell surface antigens; Cell surface determinants for hormones
- C07K14/723—G protein coupled receptor, e.g. TSHR-thyrotropin-receptor, LH/hCG receptor, FSH receptor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/14—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/14—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4
- A61P5/16—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4 for decreasing, blocking or antagonising the activity of the thyroid hormones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Toxicology (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Endocrinology (AREA)
- Epidemiology (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Diabetes (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
[ここで、
aa1は、アミノ酸無し、I、K又はTであり、
RNB-5Dペプチドは、YVSIDVTLQQLE、又は1つ以上のアミノ酸がKによって置換されているその変異体であり、
aa2は、アミノ酸無し、S又はKであり、
aa3は、アミノ酸無し、H又はKである]
を含み、in vitroでMHC分子に結合し、抗原処理無しにT細胞に提示されることが可能な、ペプチドを提供する。
第1の態様では、本発明は、ペプチドに関する。
適応免疫応答では、Tリンパ球は、タンパク質抗原の内部エピトープを認識することができる。抗原提示細胞(APC)は、タンパク質抗原を取り込み、それらを短いペプチド断片に分解する。ペプチドは、細胞内部の主要組織適合遺伝子複合体(MHC)クラスI又はII分子に結合し、細胞表面に運ばれ得る。MHC分子と共に細胞表面に提示された場合、ペプチドは、T細胞によって(T細胞受容体(TCR)を介して)認識され得、その場合、ペプチドは、T細胞エピトープである。
本発明のペプチドは、配列番号1〜3として示されるTSHR由来ペプチドのすべて又は部分を含み得る。
GDは、一次自己抗原、甲状腺刺激ホルモン受容体(TSHR)を標的とする自己反応性T及びBリンパ球によって引き起こされる自己免疫疾患である。
[ここで、
aa1は、アミノ酸無し、I、K又はTであり、
RNB-5Dペプチドは、YVSIDVTLQQLE、又は1つ以上のアミノ酸がKによって置換されているその変異体であり、
aa2は、アミノ酸無し、S又はKであり、
aa3は、アミノ酸無し、H又はKである]
を含み、in vitroでMHC分子に結合し、抗原処理無しにT細胞に提示されることが可能な、ペプチドを提供する。
T細胞エピトープは、自己であれ又は外来であれ、任意の抗原に対する適応免疫応答において中心的役割を果たす。過敏性疾患(アレルギー、自己免疫疾患及び移植拒絶を含む)におけるT細胞エピトープによって果たされる中心的役割は、実験モデルの使用によって実証されている。アジュバントと組み合わせた合成ペプチド(T細胞エピトープの構造に基づく)の注射によって、炎症又はアレルギー疾患を誘発することが可能である。
(i)TSHR自己抗体、
(ii)TSHRに特異的なCD4+ T細胞、及び/又は
(iii)TSHR自己抗体を分泌することが可能なB細胞。
(a)CD4+ T細胞におけるアネルギーの誘導(in vitroでの続く抗原投与によって検出され得る)、
(b)以下を含む、CD4+ T細胞集団の変化
(i)増殖の低下、
(ii)IL-2、IFN-γ及びIL-4の産生の下方調節、並びに
(iii)IL-10の産生の増加。
本発明また、本発明の第一又は第二の態様に従う1つ以上のペプチドを含む医薬組成物などの組成物に関する。
(i)TSHR自己抗体
(ii)TSHRに特異的なCD4+ T細胞
(iii)TSHR自己抗体を分泌するB細胞。
組成物は、液体溶液又は懸濁液のいずれかとして、注射剤として調製され得る; 注射前の液体における溶液又は懸濁液に好適な固体形態も調製され得る。調製物はまた、乳化されてよく、又はペプチドは、リポソームに封入されてもよい。活性成分は、薬学的に許容され、かつ活性成分と相溶性のある添加剤と混合されてよい。好適な添加剤は、例えば、水、生理食塩水(例えば、リン酸緩衝生理食塩水)、デキストロース、グリセロール、エタノールなど、及びそれらの組合せである。
好都合に、組成物が複数のペプチドを含む場合、それらは、混合組成物又はカクテルの形態で、一緒に投与されてよい。しかし、同時、別々、連続又は併用投与のために、ペプチドをキットの形態で別個に提供することが好ましい状況があり得る。
HLA-DR3 TSHRペプチドの選択
TSHRにおける重要なエピトープ領域を同定するために、TSHRのECD(AA20-418)を、以下に示すように、15アミノ酸によって重複する、28〜30アミノ酸(28〜30マー)の28個の重複ペプチドに分けた。
RNB-5内のアピトープの同定
RNB-5内の正確なエピトープ位置を決定するために、RNB-5にわたる、一連の15マーの重複ペプチドを、標準的なF-moc化学を用いて合成した。各ペプチドを、以下に示すように、1アミノ酸によって表示する:
Ex vivo寛容アッセイ
RNB-5アピトープの、寛容を誘導する能力を評価するために、これらのアピトープの、免疫応答を阻害する能力を、最初に、ex vivoで健康なHLA-DRB1*0301又はHLA-DRB1*0401マウスにおいて調べた。方法の項に記載するように、マウスを、高用量又は用量漸増スケジュールに従って、異なるRNB-5アピトープで前処理した。研究は、RNB-5アピトープでの前処理が、DR3及びDR4マウスの両方において、TSHR誘導性T細胞増殖を有意に低減することを示した(図6A〜D)。RNB-5DEFネステッドペプチドを、C末端及びN末端の両方にアミノ酸「GKK」を付加することによって改変した。これらの改変アピトープによる前処理も、TSHR誘導性T細胞増殖を有意に低減した(図6E〜F)。
GDについての動物モデル
RNB-5アピトープの、マウスにおいてGD様症状を低減する能力を調べるために、GDについての2つの異なる動物モデルを開発した。
RNB12領域におけるアピトープの同定
RNB12及びネステッドペプチドは、マウスにおいて免疫原性ではない。したがって、領域を、グレーブス病患者から生成されたT細胞株の応答性により同定した。図17は、このようなT細胞株から得られた結果を示す。
マウス
HLA-DRB1*0301トランスジェニックマウス(DR3マウス)を、メイヨークリニック(Mayo Clinic)の免疫遺伝学マウスコロニー(Immunogenetics mouse colony)で飼育し、維持した。HLA DR3-tgの創始マウス(founder mice)を、Gunter Hammerling(German Cancer Research Center, Heidelberg, Germany)から入手した。簡単に述べると、pUCにおけるHLA DRAゲノムクローンの6-kb NdeI断片及びB遺伝子を含有するcos 4.1の24-kb ClaIxSalI断片を、C57BL/6の雄と交配させた(C57BL/6xDBA/2)-F1ドナーに由来する受精卵に同時注入した。トランスジェニックマウスを、I-Abノックアウトマウスに交配させた。DR3マウスを、10世代にわたってC57BL/10背景に交配させた。これらのDR3マウスは、HLA-DRB1*0301分子を発現するが、マウスMHC-II分子を発現しない。
ペプチドを、GL Biochem Ltd(Shangai, China)によって合成し、-80℃にてジメチルスルホキシド(DMSO; Sigma-Aldrich, Bornem, Belgium)中で保存した。
NetMHCII 2.2サーバ
NetMHCII 2.2サーバは、人工ニューロンネットワークを使用して、ペプチドの、HLA-DRB1*0301への結合を予測する。予測値は、nM IC50値で与えられる。強い及び弱い結合ペプチドは、出力に示される。高い親和性結合ペプチドは、50 nM未満のIC50値を有し、弱い結合ペプチドは、500 nM未満のIC50値を有する。結果は、以下のように計算される予測スコアとして提示される: 1-log50000(aff)。ウェブサイトのアドレス: http://www.cbs.dtu.dk/services/NetMHCII。
各ペプチドについて、ペプチドのスコアを、SWISSPROTデータベースから選択された500万のランダムな15マーのスコアに対して比較することによって、4つの方法(ARB、コンビナトリアルライブラリー、SMM_align及びSturniolo)のそれぞれについて、パーセンタイルランクを生成した。小さな番号を付けたパーセンタイルランクは、高い親和性を示す。次いで、4つの方法の中央値パーセンタイルランクを、コンセンサス法についてのランクを生成するために使用した。ウェブサイトのアドレス: http://tools.immuneepitope.org/analyze/html/mhc_II_binding.html。
プライミング
DR3マウスに、完全フロイントアジュバント((CFA; BD Benelux, Erembodegem, Belgium)4mg/mlの結核菌(Mycobacterium tuberculosis)(MTb, BD Benelux)を含有する)と共に乳化した、PBS(Lonza, Verviers, Belgium)中の100μgの抗原を、尾の基部に皮下注射した(100μl/注射)。実験に応じて、RNBペプチド又は完全長TSHR-289タンパク質を抗原として用いた。対照動物には、PBS/CFAのみを同じ時に注射した。
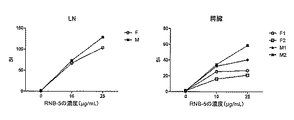
免疫化10日後に、排出リンパ節(draining lymph node)(LN)及び脾臓を回収した。LN細胞及び脾細胞を単離し、96ウェル平底プレート中のX-vivo 15培地(グルタミン、ペニシリン及びストレプトマイシンを補充した; Lonza)中で培養した。抗原誘導性細胞増殖を調べるため、0.5×106細胞/ウェルを、異なる抗原濃度(0〜25μg/ml)又は12.5μg/mlの精製タンパク質誘導体(PPD; プライミング対照; Statens serum institut, Copenhagen, Denmark)と共に72時間培養した(200μL/ウェル)。
72時間後、60μLの細胞上清を回収し、凍結させた。次いで、20μL/ウェルのトリチウム化チミジン(PerkinElmer, Zaventem, Belgium)を、1μCi/ウェルの最終濃度を得るために細胞に添加した。細胞を37℃でインキュベートし、16時間後に、プレートを凍結させた。解凍したプレートを回収し、細胞増殖を評価するために、βカウンター(Wallac 1450 Microbeta Trilux液体シンチレーションカウンター)を用いて読み取った。解凍した上清を、抗原誘導性サイトカイン産生を測定するために、マウスTh1/Th2 10plex FlowCytomix Multiplex(Bender MedSystems, Vienna, Austria)を用いて分析した。
プライミング及びT細胞株の確立
0日目に、マウスに、100μgの抗原/CFAを尾の基部に皮下注射した(DR3マウスについてRNB-5; DR4マウスについてTSHR)。対照マウスは、PBS/CFAで免疫化した。10日目に、排出LN及び脾臓を取り出し、単一細胞懸濁液を作製した。細胞のいくつかを、上述のように、抗原誘導性細胞増殖を測定するために使用した。残りの脾細胞及びLN細胞を混合し、CD4+ T細胞を陰性精製キット(アンタッチド(untouched)CD4+ T細胞; Miltenyi, Leiden, The Netherlands)を用いて単離した。次いで、CD4+ T細胞を、抗原(25μg/mlのRNB-5若しくは0.5μg/mlのTSHR-289タンパク質)及びDR3マウス由来の照射された脾細胞(3000 rad)と一緒に培養した(APC:CD4+ T細胞比1:1; 5×106細胞/ml)。ウシ胎児血清(FCS)誘導性細胞活性化を避けるために、細胞を、X-vivo 15培地中で培養した。4日目に、20 U/mlの組換えヒトIL-2(R&D, Abingdon, United Kingdom)を細胞に添加した。7日目に、生細胞を、Ficoll密度勾配分離(Histopaque 1083, Sigma-Aldrich)を用いて死細胞を除去することにより回収した。次いで、細胞を上記のように再刺激し、APC:CD4+ T細胞比を2:1に変えた。9日目に、生細胞を回収し、それらのいくつかを、融合のために使用した。残りのCD4+T細胞を培養中に残し、IL-2を10日目に添加した。14日目に、生細胞を回収し、APCの存在下で抗原で再刺激し(3:1でのAPC:CD4+ T細胞の比)、16日目に第二の融合に使用した。
1×107個のBW5147細胞(Health Protection Agency Culture Collections, Salisbury, UK)及び5×106個のCD4+ T細胞を、50mlチューブ中で混合し、37℃の無血清培地で洗浄した。遠心分離後、細胞ペレットを穏やかに再懸濁した。1mlの37℃ポリエチレングリコール(PEG; 40〜50%溶液、Sigma-Aldrich)を45秒かけて添加し、細胞を小さな37℃の水浴中に維持した。細胞を、45秒間37℃でインキュベートした。次いで、旋回させながら、1mlの37℃無血清培地を30秒かけて添加し、連続して2、3、4、10及び30mlが続いた。チューブを非常にゆっくりと反転させ、4分間37℃でインキュベートした。細胞を、ブレーキなしで室温(RT)で1300rpmで5分間遠心分離した。上清を除去し、50mlのRT無血清培地を、細胞ペレットを取り除くことを避けるためにゆっくりと添加した。洗浄工程を、完全培地を用いて繰り返した。最後に、細胞を、10%-FCSを有するRT完全培地に再懸濁し、96ウェル平底プレートに、異なる細胞濃度で播種した(100μl/ウェル)。48時間後、細胞を1×ヒポキサンチン-アミノプテリン-チミジン(HAT、Sigma-Aldrich)培地中で培養し、ハイブリドーマ細胞増殖を、約6日後に検出した。クローンをそれらが安定になるまでHAT培地中で維持し、次いでヒポキサンチン-チミジン(HT、Sigma-Aldrich)培地を介して完全RPMI培地へと断ち切らせた。定期的なベースで、クローンを、凍結培地(90%FCS+10%DMSO)中で凍結させた。
ハイブリドーマ細胞を、5×104個のVAVY若しくはBM14細胞(それぞれHLA-DRB1*0301又はHLA-DRB1*0401を発現するヒト細胞株; International Histocompatibility Working group, Seattle, USA)及び抗原(10〜25μg/ml)と共に培養した。48時間後、抗原誘導性IL-2産生を、酵素結合免疫吸着アッセイ(ELISA)によって測定した。
96ウェルプレート(Immunosorb 96ウェル, Fisher Scientific, Erembodegem, Belgium)を、炭酸バッファー中に1:250希釈した、50μl/ウェルの精製ラット抗マウスIL-2捕捉Ab(BD Biosciences, Oxford, UK)を用いて4℃で一晩コーティングした。PBS-0.05%Tweenで2回洗浄した後、ウェルを、10%FCS/PBSで室温にて1時間ブロッキングした。次いで、ウェルを、50μlの細胞培養上清又はIL-2標準(BD Biosciences, Belgium, Erembodegem)と共に室温で2時間インキュベートした。ウェルを、10%FCS/PBS中に1:1000希釈した、50μl/ウェルのビオチンラット抗マウスIL-2(BD Biosciences)と共に室温で1時間インキュベートし、その後、PBS中に1:1000希釈した50μl/ウェルのエクストラアビジンペルオキシダーゼ(Sigma-Aldrich)との室温にて30分間のインキュベーションが続いた。抗体結合を検出するために、50μl/ウェルのTMB基質溶液(Perbio Science, Erembodegem, Belgium)を添加した。11分後、発色反応を、50μl/ウェルの2M H2SO4を用いて停止した。光学密度(OD)を450nm(630nm ref)で測定した(Tecan Benelux, Mechelen, Belgium)。
抗原特異的クローンを、固定された又は固定されていないVAVY又はBM14細胞(=APC)によって提示される、15マーのペプチド(RNB-5A〜5O)に対するそれらの応答性について試験した。個々のクローンからの5×104個の細胞を、25μg/mlのペプチド及び5×104個の固定された又は新鮮なAPCと共に培養した。APCを固定するために、細胞を、0.5%パラホルムアルデヒド(Merck, Darmstadt, Germany)(pH7)と共に室温で5分間インキュベートした。固定反応を、0.4Mグリシン(Sigma-Aldrich)を添加し、RPMI-10%FCS中で細胞を洗浄することにより停止させた。さらに、ヒトTSHR-289タンパク質(Chesapeake-PERL, Savage, Maryland, USA)に対する応答性を、潜在性エピトープを同定するために測定した。48時間後、抗原誘導性IL-2産生を、ELISAによって測定した。
ペプチドの溶解性を、Anabiotec(Zwijnaarde, Belgium)によって分析した。要するに、ペプチドサンプルを、PBS pH7.0±0.1を添加することによって、2つの異なる標的濃度(1mg/ml及び4mg/ml)で溶解した。ペプチド溶液を、少なくとも16時間室温でインキュベートした。濁度を、遠心分離の前及び後に、320及び360nmで測定した。ペプチド濃度を、280及び205nmの吸光度を用いて、かつHPLC-UVによって決定した。
DR3マウスに、-8、-6、-4日目に、RNB-5 15マーペプチド(100μg/注射)又はPBSを首の後ろに皮下注射した(高用量スケジュール)(図5)。あるいは、マウスに、-15、-13及び-11日目に、それぞれ0.1μg、1μg及び10μgペプチドを注射し、その後、-8、-6及び-4日目に100μgのペプチドの3回の注射が続いた(用量漸増スケジュール)。0日目に、マウスに、100μgの抗原/CFA(RNB-5ペプチド又はTSHR-289タンパク質)を尾の基部に皮下注射した。免疫化の10日後、排出LN及び脾臓を回収した。増殖アッセイ及びサイトカイン測定を、上記のように行った。
TSHR Aサブユニットアデノウイルスによるマウスの免疫化
ヒトTSHR Aサブユニット(アミノ酸残基1〜289、AサブユニットAd)を発現するアデノウイルス及びβガラクトシダーゼを発現する対照アデノウイルス(LacZ-Ad)を、Viraquest(North Liberty, IA, USA)から購入した。6週齢の雌Balb/cJOlaHsdマウス(Harlan Laboratories, Venray, The Netherlands)に、TSHR-Ad(1010又は1011個の粒子)又はLacZ-Ad(1010個の粒子)を大腿筋に筋肉内注射した。すべてのマウスを、アデノウイルスの同じバッチを使用して同時に免疫化した。マウスに、3週間間隔(0、21及び42日目)で3回注射し、血液を、初回免疫の前、及び二次免疫の1週後に採取した。すべてのマウスを、血液及び甲状腺を得るために、3回目の注射(10週)の4週後に安楽死させた。
雌の6週齢C57/Bl6JOlaHsdマウス(Harlan Laboratories)(1群あたり8匹のマウス)に、4 mg/mlのMTb(50μl)と共にCFA中で乳化させた50μgのTSHR-289タンパク質を尾の基部で皮下に投与した。マウスは、0(免疫前)、7、21、35、49、63日目(群A)、0、14、28、42、56日目(群B)又は0、21、28、42、56日目(群C)に尾から採血した。群Cのマウスは、不完全フロイントアジュバント(IFA)中に乳化させた50μgのTSHR-289タンパク質で4週に追加免疫を受けた。初回免疫の10週後、すべてのマウスを安楽死させ、血液を心臓穿刺によって採取した。
精製したTSHR-289タンパク質(Chesapeake-Perl)に対する抗TSHR抗体(IgGクラス)を、ELISAを用いて測定した。96ウェルプレート(ハーフエリア(half area)96ウェル, Fisher Scientific)を、PBS中の50μL/ウェルのTSHR-289タンパク質(0.5μg/ml)で室温で一晩コーティングした。PBS-0.05%Tweenで洗浄した後、ウェルを、PBS中の1%BSA(w/v)で室温にて1時間ブロッキングし、試験血清(二重のアリコート、1:50希釈)と共にインキュベートした。マウス抗TSHR抗体(A9, Abcam, Cambridge, UK)を陽性対照として使用した。次いで、抗体結合を、西洋ワサビペルオキシダーゼ結合ヤギ抗マウスIgG(Abcam)で検出し、シグナルをTMBで発色させた。光学密度(OD)を、450nmにてプレートリーダーで測定した(Tecan Benelux)。
総チロキシン(T4)を、CBIマウス/ラットチロキシンELISAキット(Calbiotech, Spring Valley, CA, USA)を使用して、製造者の説明書に従って、未希釈マウス血清(10μl)において測定した。T4値をキットにおける標準から計算し、μg/dlで表した。甲状腺を、10%中性緩衝ホルマリン液(pH7.5)中で固定し、切片に加工し、ヘマトキシリン及びエオシンで染色した。切片を、病理学的変化(肥大、上皮細胞の過形成及びリンパ球の浸潤)について観察し、スコア付けした(KWS Biotest, Bristol, UK)。
健康なドナー又はグレーブス病患者からの末梢血単球(PBMC)を、単離し(Histopaque-1077, Sigma-Aldrich)、アリコートで凍結した。0日目に、細胞を解凍し、106のPBMC/mlを、6ウェルプレート(Greiner Bio-one)中に添加した5%AB血清(Sigma Aldrich)を有する、補充された(10mM HEPES、50U/ml ペニシリン/ストレプトマイシン及び4mM L-グルタミン(Lonza))RPMI 1640(Lonza)中の20μg/mlのペプチドと共に培養し、37℃及び5%CO2中でインキュベートした。7日後、rhIL-2(R&D Systems)を、20U/mlの最終濃度まで添加する。12日目に、細胞を回収し、洗浄し、5〜10μg/mlのペプチド及び20U/mlのrhIL-2で刺激された、6ウェルプレート中、1mlあたり106+2×106個の新たに解凍した照射自己PBMCの濃度で培養物に戻す。15、18及び21日目に、追加のrhIL-2を、20u/mlの最終濃度まで添加した。
TCL培養物からの上清を、ヒトIFN-γDuosetキット、R&D Systemsを用いて、製造者の説明書に従って、IFNガンマ含有量について評価した。光学密度を、450nmで測定した(Tecan Benelux)。
Claims (16)
- in vitroでMHC分子に結合し、抗原処理無しにT細胞に提示されることが可能なペプチドであって、以下の甲状腺刺激ホルモン受容体(TSHR)ペプチドのうちの1つを含む、ペプチド。
RNB_5: ISRIYVSIDVTLQQLESHSFYNLSKVTHI (配列番号1)
RNB_4: LRTIPSHAFSNLPNISRIYVSIDVTLQQL (配列番号2)
RNB_9: TGLKMFPDLTKVYSTDIFFILEITDNPYM (配列番号3)
RNB_12: LTLKLYNNGFTSVQGYAFNGTKLDAVYL (配列番号64) - 以下から選択される、in vitroでMHC分子に結合し、抗原処理無しにT細胞に提示されることが可能なペプチド。
RNB_5D-GKK: KKGIYVSIDVTLQQLESHGKK (配列番号12)
RNB_5D-KKK: KKKIYVSIDVTLQQLESHKKK (配列番号21)
RNB_5E-GKK: KKGYVSIDVTLQQLESHSGKK (配列番号13)
RNB_5A: ISRIYVSIDVTLQQL (配列番号6)
RNB_5B: SRIYVSIDVTLQQLE (配列番号7)
RNB_5C: RIYVSIDVTLQQLES (配列番号8)
RNB_5D: IYVSIDVTLQQLESH (配列番号9)
RNB_5E: YVSIDVTLQQLESHS (配列番号10)
RNB_5F: VSIDVTLQQLESHSF (配列番号11)
RNB_5F-GKK: KKGVSIDVTLQQLESHSFGKK (配列番号14)
RNB_4J-GKK: KKGSNLPNISRIYVSIDVGKK (配列番号16)
RNB_4J: SNLPNISRIYVSIDV (配列番号15)
RNB_4K: NLPNISRIYVSIDVT (配列番号62)
RNB_4K-GKK: KKGNLPNISRIYVSIDVTGKK (配列番号63)
RNB_9B: GLKMFPDLTKVYSTD (配列番号18)
RNB_9A: TGLKMFPDLTKVYST (配列番号17)
RNB_9C: LKMFPDLTKVYSTDI (配列番号19)
RNB_9D: KMFPDLTKVYSTDIF (配列番号20)
RNB_12A: LTLKLYNNGFTSVQG (配列番号65)
RNB_12B: TLKLYNNGFTSVQGY (配列番号66)
RNB_12B-KKK: KKKTLKLYNNGFTSVQGYKKK (配列番号67) - 以下の群から選択される、in vitroでMHC分子に結合し、抗原処理無しにT細胞に提示されることが可能なペプチド:
KKGIYVSIDVTLQQLESHGKK(配列番号12)、
KKGKYVSIDVTLQQLESHGKK(配列番号22)、
KKGIKVSIDVTLQQLESHGKK(配列番号23)、
KKGIYKSIDVTLQQLESHGKK(配列番号24)、
KKGIYVSIDVKLQQLESHGKK(配列番号25)、
KKGIYVSIDVTLQKLESHGKK(配列番号26)、
KKGIYVSIDVTLQQKESHGKK(配列番号27)、
KKGIYVSIDVTLQQLKSHGKK(配列番号28)、
KKGIYVSIDVTLQQLEKHGKK(配列番号29)、
KKGIYVSIDVTLQQLESKGKK(配列番号30)、
KKGYVSIDVTLQQLEGKK(配列番号31)、
KKGYVSIDVKLQQLEGKK(配列番号32)、
KKGYVSIDVTLQKLEGKK(配列番号33)、
KKGYVSIDVTLQQKEGKK(配列番号34)、
KKGYVSIDVKLQKKEGKK(配列番号35)、
KKGIYVSIDVTLQQLEGKK(配列番号36)、
KKGIYVSIDVKLQQLEGKK(配列番号37)、
KKGIYVSIDVTLQKLEGKK(配列番号38)、
KKGIYVSIDVTLQQKEGKK(配列番号39)、
KKGIYVSIDVKLQKKEGKK(配列番号40)、
KKGTYVSIDVTLQQLEGKK(配列番号41)、
KKGTYVSIDVKLQQLEGKK(配列番号42)、
KKGTYVSIDVTLQKLEGKK(配列番号43)、
KKGTYVSIDVTLQQKEGKK(配列番号44)、
KKGTYVSIDVKLQKKEGKK(配列番号45)、
KKKIYVSIDVTLQQLESHKKK(配列番号21)、
KKKKYVSIDVTLQQLESHKKK(配列番号46)、
KKKIKVSIDVTLQQLESHKKK(配列番号47)、
KKKIYKSIDVTLQQLESHKKK(配列番号48)、
KKKIYVKIDVTLQQLESHKKK(配列番号49)、
KKKIYVSIDVKLQQLESHKKK(配列番号50)、
KKKIYVSIDVTLKQLESHKKK(配列番号51)、
KKKIYVSIDVTLQKLESHKKK(配列番号52)、
KKKIYVSIDVTLQQKESHKKK(配列番号53)、
KKKIYVSIDVTLQQLKSHKKK(配列番号54)、
KKKIYVSIDVTLQQLEKHKKK(配列番号55)、
KKKIYVSIDVTLQQLESKKKK(配列番号56)、
KKKYVSIDVTLQQLEKKK(配列番号57)、
KKKYVSIDVKLQQLEKKK(配列番号58)、
KKKYVSIDVTLQKLEKKK(配列番号59)、
KKKYVSIDVTLQQKEKKK(配列番号60)、
KKKYVSIDVKLQKKEKKK(配列番号61)。 - 以下からなる群から選択される、請求項3に記載のペプチド:
KKGKYVSIDVTLQQLESHGKK(配列番号22)、
KKGIYKSIDVTLQQLESHGKK(配列番号24)、
KKGYVSIDVTLQQLEGKK(配列番号31)、
KKGYVSIDVKLQQLEGKK(配列番号32)、
KKGYVSIDVTLQKLEGKK(配列番号33)、
KKGYVSIDVTLQQKEGKK(配列番号34)、
KKGYVSIDVKLQKKEGKK(配列番号35)、
KKGIYVSIDVKLQKKEGKK(配列番号40)、
KKGTYVSIDVKLQQLEGKK(配列番号42)、
KKGTYVSIDVKLQKKEGKK(配列番号45)、
KKKKYVSIDVTLQQLESHKKK(配列番号46)、
KKKIYKSIDVTLQQLESHKKK(配列番号48)、
KKKIYVKIDVTLQQLESHKKK(配列番号49)、
KKKYVSIDVTLQQLEKKK(配列番号57)、
KKKYVSIDVKLQQLEKKK(配列番号58)、
KKKYVSIDVTLQQKEKKK(配列番号60)、
KKKYVSIDVKLQKKEKKK(配列番号61)。 - 以下からなる群から選択される、請求項4に記載のペプチド:
KKGIYKSIDVTLQQLESHGKK(配列番号24)、
KKGYVSIDVKLQQLEGKK(配列番号32)、
KKGYVSIDVTLQKLEGKK(配列番号33)、
KKGYVSIDVTLQQKEGKK(配列番号34)、
KKGYVSIDVKLQKKEGKK(配列番号35)、
KKGTYVSIDVKLQQLEGKK(配列番号42)、
KKGTYVSIDVKLQKKEGKK(配列番号45)、
KKKKYVSIDVTLQQLESHKKK(配列番号46)、
KKKIYKSIDVTLQQLESHKKK(配列番号48)、
KKKYVSIDVTLQQLEKKK(配列番号57)、
KKKYVSIDVTLQQKEKKK(配列番号60)。 - 以下からなる群から選択される、請求項5に記載のペプチド:
KKGYVSIDVTLQKLEGKK(配列番号32)、
KKGYVSIDVKLQKKEGKK(配列番号34)、
KKKKYVSIDVTLQQLESHKKK(配列番号46)、
KKKIYKSIDVTLQQLESHKKK(配列番号48)、
KKKYVSIDVTLQQLEKKK(配列番号57)、
KKKYVSIDVTLQQKEKKK(配列番号60)。 - 請求項1〜6のいずれか一項に記載の1つ以上のペプチドを含む、組成物。
- 複数のペプチドを含む、請求項7に記載の組成物。
- 被験体におけるin vivoでのTSHR自己抗体の産生の抑制又は阻止に使用するための、請求項7又は8に記載の組成物。
- 被験体におけるグレーブス病の治療及び/又は予防に使用するための、請求項7又は8に記載の組成物。
- 被験体におけるin vivoでのTSHR自己抗体の産生を抑制又は阻止するための医薬の製造における、請求項1〜6のいずれか一項に記載のペプチド又は請求項7又は8に記載の組成物の使用。
- 被験体におけるグレーブス病を治療及び/又は予防するための医薬の製造における、請求項1〜6のいずれか一項に記載のペプチド又は請求項7又は8に記載の組成物の使用。
- 被験体が、HLA-DR3である、請求項9又は10に記載の組成物。
- 被験体が、HLA-DR4である、請求項9又は10に記載の組成物。
- 被験体が、HLA-DR3である、請求項11又は12に記載の使用。
- 被験体が、HLA-DR4である、請求項11又は12に記載の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB201314052A GB201314052D0 (en) | 2013-08-06 | 2013-08-06 | Peptides |
| GB1314052.0 | 2013-08-06 | ||
| PCT/IB2014/063739 WO2015019302A2 (en) | 2013-08-06 | 2014-08-06 | Peptides |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016527304A JP2016527304A (ja) | 2016-09-08 |
| JP6476181B2 true JP6476181B2 (ja) | 2019-02-27 |
Family
ID=49224229
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016532780A Active JP6476181B2 (ja) | 2013-08-06 | 2014-08-06 | ペプチド |
Country Status (32)
| Country | Link |
|---|---|
| US (2) | US9938329B2 (ja) |
| EP (1) | EP3030259B1 (ja) |
| JP (1) | JP6476181B2 (ja) |
| KR (1) | KR102431507B1 (ja) |
| CN (1) | CN105636980B (ja) |
| AU (1) | AU2014304108B2 (ja) |
| BR (1) | BR112016002572A2 (ja) |
| CA (1) | CA2920321C (ja) |
| CY (1) | CY1120212T1 (ja) |
| DK (1) | DK3030259T3 (ja) |
| ES (1) | ES2664045T3 (ja) |
| GB (1) | GB201314052D0 (ja) |
| HK (1) | HK1219058A1 (ja) |
| HR (1) | HRP20180452T1 (ja) |
| HU (1) | HUE038569T2 (ja) |
| IL (1) | IL243892B (ja) |
| LT (1) | LT3030259T (ja) |
| MX (1) | MX369412B (ja) |
| MY (1) | MY177371A (ja) |
| NO (1) | NO3030259T3 (ja) |
| NZ (1) | NZ717350A (ja) |
| PE (1) | PE20160778A1 (ja) |
| PH (1) | PH12016500218A1 (ja) |
| PL (1) | PL3030259T3 (ja) |
| PT (1) | PT3030259T (ja) |
| RS (1) | RS57196B1 (ja) |
| RU (1) | RU2676149C2 (ja) |
| SG (1) | SG11201600895SA (ja) |
| SI (1) | SI3030259T1 (ja) |
| UA (1) | UA120746C2 (ja) |
| WO (1) | WO2015019302A2 (ja) |
| ZA (1) | ZA201600729B (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018502093A (ja) * | 2014-12-24 | 2018-01-25 | アピトープ インターナショナル エヌブイ | 組成物 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201314052D0 (en) * | 2013-08-06 | 2013-09-18 | Apitope Int Nv | Peptides |
| AU2018206356A1 (en) * | 2017-01-04 | 2019-07-18 | Worg Pharmaceuticals (Zhejiang) Co., Ltd. | Therapeutic method using tolerogenic peptides |
| EP3369743A1 (en) * | 2017-03-01 | 2018-09-05 | advanceCOR GmbH | Cyclic peptides for the treatment of graves' disease |
| EP3622962A1 (en) * | 2018-09-14 | 2020-03-18 | advanceCOR GmbH | Short cyclic peptides for the treatment of graves' disease |
| GB201909774D0 (en) | 2019-07-08 | 2019-08-21 | Apitope Tech Bristol Limited | Method |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0433509B1 (en) | 1989-12-14 | 1996-11-13 | B.R.A.H.M.S Diagnostica GmbH | Polypeptides having thyrotropin receptor activity, nucleic acid sequences coding for such receptors and polypeptides, and applications of these polypeptides |
| HU230233B1 (hu) | 2000-08-21 | 2015-10-28 | Apitope Technology (Bristol) Limited | Peptid szelekciós módszer |
| GB0202399D0 (en) * | 2002-02-01 | 2002-03-20 | Univ Bristol | Peptide |
| FR2842812A1 (fr) * | 2002-07-26 | 2004-01-30 | Pf Medicament | Procede de solubilisation de peptides hydrophobes et leur utilisation pour generer une reponse de type ctl antitumorale ou anti-infectueuse |
| JP2006188507A (ja) * | 2004-12-10 | 2006-07-20 | Tokyo Univ Of Agriculture & Technology | 蛋白質の溶解度向上方法 |
| EP2080772A3 (en) * | 2005-11-21 | 2009-10-07 | Dr. Fenning Biomed GmbH | Recombinant polypeptides and methods for detecting and/or quantifying autoantibodies against TSH receptor |
| EP2084188A2 (en) | 2006-10-12 | 2009-08-05 | Genentech, Inc. | Antibodies to lymphotoxin-alpha |
| GB0723712D0 (en) | 2007-12-04 | 2008-01-16 | Apitope Technology Bristol Ltd | Peptides |
| GB0908515D0 (en) * | 2009-05-18 | 2009-06-24 | Apitope Technology Bristol Ltd | Peptide |
| GB201314052D0 (en) * | 2013-08-06 | 2013-09-18 | Apitope Int Nv | Peptides |
-
2013
- 2013-08-06 GB GB201314052A patent/GB201314052D0/en not_active Ceased
-
2014
- 2014-08-06 UA UAA201602098A patent/UA120746C2/uk unknown
- 2014-08-06 NZ NZ717350A patent/NZ717350A/en unknown
- 2014-08-06 WO PCT/IB2014/063739 patent/WO2015019302A2/en active Application Filing
- 2014-08-06 PT PT147724447T patent/PT3030259T/pt unknown
- 2014-08-06 KR KR1020167005185A patent/KR102431507B1/ko active IP Right Grant
- 2014-08-06 NO NO14772444A patent/NO3030259T3/no unknown
- 2014-08-06 US US14/910,372 patent/US9938329B2/en active Active
- 2014-08-06 JP JP2016532780A patent/JP6476181B2/ja active Active
- 2014-08-06 PL PL14772444T patent/PL3030259T3/pl unknown
- 2014-08-06 MY MYPI2016000224A patent/MY177371A/en unknown
- 2014-08-06 PE PE2016000223A patent/PE20160778A1/es unknown
- 2014-08-06 BR BR112016002572A patent/BR112016002572A2/pt not_active IP Right Cessation
- 2014-08-06 SI SI201430666T patent/SI3030259T1/en unknown
- 2014-08-06 EP EP14772444.7A patent/EP3030259B1/en active Active
- 2014-08-06 DK DK14772444.7T patent/DK3030259T3/en active
- 2014-08-06 HU HUE14772444A patent/HUE038569T2/hu unknown
- 2014-08-06 ES ES14772444.7T patent/ES2664045T3/es active Active
- 2014-08-06 RS RS20180316A patent/RS57196B1/sr unknown
- 2014-08-06 CN CN201480053788.0A patent/CN105636980B/zh active Active
- 2014-08-06 CA CA2920321A patent/CA2920321C/en active Active
- 2014-08-06 MX MX2016001744A patent/MX369412B/es active IP Right Grant
- 2014-08-06 LT LTEP14772444.7T patent/LT3030259T/lt unknown
- 2014-08-06 AU AU2014304108A patent/AU2014304108B2/en active Active
- 2014-08-06 RU RU2016107873A patent/RU2676149C2/ru active
- 2014-08-06 SG SG11201600895SA patent/SG11201600895SA/en unknown
-
2016
- 2016-02-01 PH PH12016500218A patent/PH12016500218A1/en unknown
- 2016-02-01 IL IL24389216A patent/IL243892B/en active IP Right Grant
- 2016-02-02 ZA ZA2016/00729A patent/ZA201600729B/en unknown
- 2016-06-21 HK HK16107175.4A patent/HK1219058A1/zh unknown
-
2018
- 2018-02-23 US US15/903,379 patent/US10730919B2/en active Active
- 2018-03-16 HR HRP20180452TT patent/HRP20180452T1/hr unknown
- 2018-03-26 CY CY20181100337T patent/CY1120212T1/el unknown
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018502093A (ja) * | 2014-12-24 | 2018-01-25 | アピトープ インターナショナル エヌブイ | 組成物 |
| JP7117847B2 (ja) | 2014-12-24 | 2022-08-15 | アピトープ インターナショナル エヌブイ | 組成物 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6476181B2 (ja) | ペプチド | |
| JP2021020927A (ja) | 組成物 | |
| JP6347065B2 (ja) | ペプチド | |
| JP7174492B2 (ja) | S-アレスチンペプチドおよびその治療的使用 | |
| JP5784009B2 (ja) | Fviii由来ペプチド | |
| RU2773344C2 (ru) | Композиция | |
| JP2023508141A (ja) | S-アレスチンペプチドを含む組成物 | |
| NZ732987B2 (en) | Thyroid stimulating hormone receptor peptides and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD01 | Notification of change of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7426 Effective date: 20160725 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20160725 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170517 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180529 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180829 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190108 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190204 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6476181 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |