JP5732603B2 - 骨標的アルカリホスファターゼ、キット及びその使用方法 - Google Patents
骨標的アルカリホスファターゼ、キット及びその使用方法 Download PDFInfo
- Publication number
- JP5732603B2 JP5732603B2 JP2010507770A JP2010507770A JP5732603B2 JP 5732603 B2 JP5732603 B2 JP 5732603B2 JP 2010507770 A JP2010507770 A JP 2010507770A JP 2010507770 A JP2010507770 A JP 2010507770A JP 5732603 B2 JP5732603 B2 JP 5732603B2
- Authority
- JP
- Japan
- Prior art keywords
- alkaline phosphatase
- amino acid
- sequence
- seq
- residue
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/16—Hydrolases (3) acting on ester bonds (3.1)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y301/00—Hydrolases acting on ester bonds (3.1)
- C12Y301/03—Phosphoric monoester hydrolases (3.1.3)
- C12Y301/03001—Alkaline phosphatase (3.1.3.1)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/33—Fusion polypeptide fusions for targeting to specific cell types, e.g. tissue specific targeting, targeting of a bacterial subspecies
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/021—Uses of viruses as vector for the expression of a heterologous nucleic acid
- C12N2799/025—Uses of viruses as vector for the expression of a heterologous nucleic acid where the vector is derived from a parvovirus
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Physical Education & Sports Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Microbiology (AREA)
- Rheumatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Materials For Medical Uses (AREA)
- Enzymes And Modification Thereof (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Adornments (AREA)
- Cereal-Derived Products (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Immobilizing And Processing Of Enzymes And Microorganisms (AREA)
Description
該当なし。
本発明の骨標的組成物は、アミノ側からカルボキシル側へ順に、sALP、スペーサー、及び骨標的負に帯電したペプチドを含む融合タンパク質を含む。
ALPの4種類の既知イソ酵素があり、即ち、下で更に説明される組織非特異的アルカリホスファターゼ、胎盤アルカリホスファターゼ(PALP)(例えば、[NP−112603]、[NP−001623])、生殖細胞アルカリホスファターゼ(GCALP)(例えば、[P10696])及び腸アルカリホスファターゼ(例えば、[NP−001622])である。これらの酵素は、きわめて類似の三次元構造を有する。その触媒部位のそれぞれには、2つのZnと1つのMgを含む酵素活性に必要な金属イオンのための4つの金属結合ドメインを含有する。これらの酵素は、リン酸のモノエステルの加水分解を触媒し、高濃度のリン酸受容体の存在下でリン酸転移反応も触媒する。PALPは、ホスホエタノールアミン(PEA)、無機ピロリン酸(PPi)及びピロドキサール5’−リン酸(PLP)に向かって生理学的に活性であり、3つ全てがTNALPに対する既知の天然基質であることが特に明らかにされている(Whyte、1995)。これらのイソ酵素間のアラインメントは図30に示されている。
前述の通り、TNALPは、糖脂質を通じてそのC末端に固定された膜結合型タンパク質である(Swiss−Prot、P05186)。この糖脂質アンカー(GPI)は、一時的膜アンカーとしても前記GPIの付加のためのシグナルとしても働く疎水性C末端の除去後、翻訳後的に付加される。したがって、下の全ての実施例で使用される可溶性ヒトTNALPは、疎水性C末端配列の最初のアミノ酸、即ちアラニンが終止コドンにより置き換えられているTNALPを含む。そのようにして形成された可溶性TNALP(本明細書ではsTNALPと呼ばれる)は、触媒部位の形成に必要な天然固定化型のTNALPの全アミノ酸を含有しているが、GPI膜アンカーを欠いている。既知のTNALPには、ヒトTNALP[NP−000469、AAI10910、AAH90861、AAH66116、AAH21289、AAI26166];アカゲザルTNALP[XP−001109717];ラットTNALP[NP−037191];イヌTNALP[AAF64516];ブタTNALP[AAN64273]、マウス[NP−031457]、ウシ[NP−789828、AAI18209、AAC33858]、及びネコ[NP−001036028]が挙げられる。
ナルペプチドのない配列では452位)のアミノ酸残基はスレオニン残基ではなく;479位(シグナルペプチドのない配列では457位)のアミノ酸残基はセリン残基ではなく;482位(シグナルペプチドのない配列では460位)のアミノ酸残基はリシン又はグリシン残基ではなく;484位(シグナルペプチドのない配列では462位)のアミノ酸残基はロイシン残基ではなく;495位(シグナルペプチドのない配列では473位)のアミノ酸残基はセリン残基ではなく;496位(シグナルペプチドのない配列では474位)のアミノ酸残基はフェニルアラニン残基ではなく;及び497位(シグナルペプチドのない配列では475位)のアミノ酸残基はアルギニン残基ではない。
ドのない配列では456位)のアミノ酸残基はセリン残基ではなく;476位(シグナルペプチドのない配列では459位)のアミノ酸残基はリシン又はグリシン残基ではなく;478位(シグナルペプチドのない配列では461位)のアミノ酸残基はロイシン残基ではなく;489位(シグナルペプチドのない配列では472位)のアミノ酸残基はセリン残基ではなく;490位(シグナルペプチドのない配列では473位)のアミノ酸残基はフェニルアラニン残基ではなく;及び491位(シグナルペプチドのない配列では474位)のアミノ酸残基はアルギニン残基ではない。他の特定の実施形態では、1つ又は複数のXは、アラインメントの配列中のその位置に見出されるアミノ酸のいずれか、又はこれらのアミノ酸のいずれかの保存若しくは半保存された置換を構成する残基であると定義される。他の特定の実施形態では、Xはアラインメントの配列中のその位置に見出されるアミノ酸のいずれかであると定義される。例えば、51位(シグナルペプチドのない配列では34位)のアミノ酸残基はアラニン又はバリン残基であり;177位(シグナルペプチドのない配列では160位)のアミノ酸残基はアラニン又はセリン残基であり;212位(シグナルペプチドのない配列では195位)のアミノ酸残基はイソロイシン又はバリン残基であり;291位(シグナルペプチドのない配列では274位)のアミノ酸残基はグルタミン酸又はアスパラギン酸残基であり;及び374位(シグナルペプチドのない配列では357位)のアミノ酸残基はバリン又はイソロイシン残基である。
この理論に限定されることなく、下の実施例に示される骨標的sALP融合タンパク質中で使用されるFcフラグメントは、sTNALP−Fc−D10の発現がsTNALP−D10の発現より高度であった(下の実施例2参照)ので、前記タンパク質をより効率よく折り畳ませるスペーサーとして働くと考えられる。1つの可能な説明は、Fcフラグメントの導入により、試験されたsALP配列のC末端に付加された高度に負に帯電したD10配列の存在により引き起こされる反発力が軽減されるというものである。
本発明に有用なFcフラグメントには、ヒンジ並びにCH2及びCH3ドメインを含むIgGのFCフラグメントが挙げられる。例えば、IgG−1、IgG−2、IgG−3、IgG−3及びIgG−4を使うことができる。
本発明による負に帯電したペプチドは、D10〜D16又はE10〜E16からなる群から選択されるポリアスパラギン酸又はポリグルタミン酸でもよい。
本発明の骨標的sALPは、経口的に、経鼻的に、静脈内に、筋肉内に、皮下に、舌下に、髄腔内に、又は皮内になどの経路により投与することができる。投与経路は、環境及び治療目的などの種々の要因に依拠することがある。本明細書で使用するように、対象は、HPP若しくはHPPに付随する他の表現型を特徴づける骨ミネラル化欠損の予防若しくは改善、又は欠損セメント質の予防若しくは改善が望ましいヒトなどの動物に言及している。
いかなる量の医薬組成物も対象に投与することができる。その投与量は、投与方法及び対象の年齢を含む多くの要因に依拠することになる。典型的には、単回投与内に含有される本発明の骨標的ALPの量は、著しい毒性を誘導することなくHPPにおける骨ミネラル化欠損を効果的に予防する、遅延させる又は改善する量になる。本明細書で使用するように、用語「治療的な有効量」は、目的の治療効果を達成し、有害な副作用は回避するのに有効な量に言及するように意図されている。典型的には、本発明による骨標的sALPは、0.001〜500mg/kg/日、更に特定の実施形態では、約0.1〜約100mg/kg/日、更に特定の実施形態では、約0.2〜約20mg/kg/日の範囲の用量で対象に投与することができる。Mahmoodらの相対成長率法(Mahmoodら、2003)を使用して、マウスからヒトへ用量を外挿することができる。投与量は、疾患の程度及び患者の異なるパラメータなどの従来の要因に従って臨床医が適合させることになる。
骨標的sALPを含有する調製物は、薬学的に許容可能な無菌水性若しくは非水溶媒、懸濁液又は乳濁液と組み合わせて患者に与えてもよい。非水溶媒の例は、プロピレングリコール、ポリエチレングリコール、植物油、魚油、及び注射用有機エステルである。水性担体には、水、水アルコール溶液、生理食塩水を含む乳濁液又は懸濁液、及び塩化ナトリウム溶液、リンゲルブドウ糖溶液、ブドウ糖プラス塩化ナトリウム溶液、乳糖を含有するリンゲル溶液又は固定油を含む緩衝医療用非経口溶媒が挙げられる。静脈内溶媒は、液体と栄養補填剤、リンゲルブドウ糖を主成分とする補填剤などの電解質補填剤などを含んでいてよい。
本発明は、本発明による核酸、タンパク質又はリガンドを含む、HPP表現型又はセメント質欠損を改善又は予防するためのキットにも関する。例えば、前記キットは、本発明の骨標的組成物又は同一物をコードするベクター、及びHPP表現型を改善又は予防するために対象に前記組成物又はベクターを投与するための使用説明書を含んでいてもよい。そのようなキットは、HPP表現型を予防又は改善することができる少なくとも1つの他の活性薬剤を更に含んでいてもよい。前記キットを使用してHPP対象のHPP表現型を予防又は改善する場合、前記キットは、HPPの他のどんな有害な症状も予防又は改善することができる少なくとも1つの他の活性薬剤を更に含んでいてもよい。更に、本発明による区画化されたキットには、試薬が別々の容器に含有されるどんなキットも挙げられる。そのような容器には、小ガラス容器、プラスチック容器、又はプラスチック若しくは紙の条片が挙げられる。そのような容器は、試料及び試薬が相互汚染しないように、並びに各容器の薬剤又は溶液が定量的な形で区画から区画へと添加することができるように、区画から区画への試薬の効率的な移動を可能にする。
組換えsTNALP−FcD10の発現及び精製
組換えTNALPの発現及び精製を容易にするために、TNALPにおけるGPIアンカー付加を指定する疎水性C末端配列を除去して可溶性の分泌酵素とした(Di Mauroら、2002)。また、ヒトIgG(γ1型(IgG1)、Swiss−Prot P01857)のFc領域でTNALPエクトドメインのコード配列を拡大させた。これにより、Protein Aクロマトグラフィーにおける組換え酵素の精製を迅速に行うことが可能になり、驚くべきことにその発現を増大させることも可能になった。更に、組換えTNALPを骨組織にターゲティングするために、Fc領域のC末端にデカアスパルテート(D10)配列を付加した。このキメラ型のTNALP(sTNALP−FcD10と呼ぶ)は、生理学的基質として、人工基質p−ニトロフェニルリン酸を用いてpH9.8でアッセイした場合と、無機ピロリン酸(PPi)を用いてpH7.4でアッセイした場合との両方において、完全な酵素活性を保持する。天然型のTNALPのように、N末端シグナルペプチドは、粗面小胞体を横断するタンパク質の共翻訳的トランスロケーションの間に切断される。その設計及び構造を、図1に概略的に例示する。図2に、融合タンパク質(シグナルペプチドを含む)のアミノ酸配列を示す。図3に、分泌される融合タンパク質(即ちシグナルペプチドを有さない)のアミノ酸配列を示す。
sTNALP−D10及びsTNALP−FcD10の発現の比較
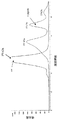
sTNALP−FcD10又はsTNALP−D10のいずれかをコードするプラスミドベクターを、Lipofectamine(商標)を使用してCHO−DG44細胞においてトランスフェクションし、上記の例1に記載したようにDHFR遺伝子を発現する細胞の生存を促進するように設計された選択培地(即ちヌクレオチドを含まない)中で増殖させた。安定したトランスフェクタントをプラーククローニングによって単離し、上記の例1にも記載したアルカリホスファターゼ酵素アッセイを使用してタンパク質発現のそれらのレベルの順に分類した。スクリーニングにより、sTNALP−D10についてのみ1個のクローン(0.120pg/細胞/日)、sTNALP−FcD10については5個のクローン(0.377、0.258、0.203、0.099及び0.088pg/細胞/日)を同定することができた。メトトレキサート(MTX)遺伝子の増幅を、上記の例1に記載したように行い(0〜100mMの範囲のMTX)、それによりsTNALP−FcD10については発現を8倍増大させることができたが、一方でsTNALP−D10の培養物では増幅は認められなかった(図4参照)。細胞系の発達のための同様の方法を使用して、予想外にも、sTNALP−FcD10タンパク質は、sTNALP−D10よりも容易に発現することが分かった(図4参照)。
sTNALP−FcD10の特性評価
sTNALP−FcD10を、まずProtein−A Sepharose(商標)で精製し、還元条件及び非還元条件の下でSDS−PAGEで解析した。
ヒドロキシアパタイトに対するsTNALP−FcD10タンパク質及びウシ腎臓sALPの親和性の比較
また、以下の手順を用いて、ヒドロキシアパタイトに対する精製sTNALP−FcD10タンパク質の親和性を、ウシ腎臓(組織非特異性)可溶アルカリホスファターゼ(Calzyme)と比較した。ウシ腎臓TNALPが市販されていたので、それをヒト骨TNALPの代わりに使用した。まず、1M HClでヒドロキシアパタイトセラミックビーズ(Biorad)を可溶化し、その溶液を10N NaOHでpH7.4にすることによりミネラルを沈殿させた。100μLの150mM NaCl(80mMリン酸ナトリウム、pH7.4)緩衝液において5μgのタンパク質で750μgのミネラルを含有するミネラル懸濁液のアリコートをインキュベーションすることによって、この再組成ミネラルへの結合を行った。試料を、回転輪上に30分間21±2℃で維持した。低速遠心分離によってミネラルを遠沈し、ミネラルペレット及び上清の両方において得られた総酵素活性を測定した。図9は、sTNALP−FcD10が、ウシ腎臓TNALPよりも、再組成ヒドロキシアパタイトミネラルに効率的に結合することを明確に示している。更に、アッセイにおいて導入されたほとんどの組換えsTNALP−FcD10タンパク質量を、結合画分及び非結合画分の両方において得られた酵素活性を合計することによって得た。このことは、再組成ミネラル相への組換えタンパク質の結合によってその酵素活性が著しく変化しないことを示す。
マウスモデル
相同組換え(Narisawaら、1997;Feddeら、1999)によりNeoカセットをマウスTNALP遺伝子(Akp2)のエクソンVIに挿入することによって、Akp2−/−マウスを作製した。この突然変異によってAkp2遺伝子の機能的不活性化が引き起こされ、これらのノックアウトマウスにおいてmRNAもTNALPタンパク質も検出され得なかった(Narisawaら、1997)。表現型的に、Akp2−/−マウスは、重症小児性HPPを模倣する。これらのマウスは、出生時には明らかな低ホスファターゼ血症の表現型を有さず、通常6日目又はその頃に骨格の欠損が発現し、その後悪化する。それらのマウスは、くる病により発育が阻害され、てんかん発作及び無呼吸を発現し、出生後12〜16日目の間に死亡することが報告された。HPP患者と同様に、Akp2−/−マウスは、TNALP活性の全身的不足、ALP基質(PPi、PLP及びPEA)の内因的蓄積、による低リン血症を特徴とし、くる病又は骨軟化症につながる骨格基質ミネラル化の欠損を患う(Feddeら、1999)。
WTマウスに注射されたsTNALP−FcD10の薬物動態及び組織分布
血液試料の採取
血液試料をヘパリンリチウムチューブ(VWR、番号CBD365958)内に採取し、最高で20分間氷上に置き、その後室温で10分間、2500gで遠心分離した。少なくとも、15μLの血漿を0.5mLチューブ(Sarstedt、番号72.699)内に移し、液体窒素中で凍結し、アッセイするまで−80℃で保持した。可能な場合、別の50μL以下の血漿を0.5mLチューブ内に移し、65℃で10分間不活化し、液体窒素中で凍結し、アッセイするまで−80℃で保持した。いずれの残留血漿も15μLのアリコートにプールし、液体窒素中で凍結し、アッセイするまで−80℃で保持した。
血漿試料中のsTNALP−FcD10の存在について、比色酵素アッセイを用いて投与完了時に評価した。吸光度の増加が産物への基質転化率に比例する色素原基質を用いて、酵素活性を決定した。10μLの希釈血漿試料を添加した0.5mM MgCl2及び50μM ZnCl2を含有する100μLの50mM NaCl緩衝液(20mMビス−トリスプロパン(HCl)pH9緩衝液)において反応を行った。反応を開始するために、ALP基質のp−ニトロフェニルを、1mMの終濃度で最後に添加した。Spectramax(商標)190(Molecular devices)プレートリーダを用いて、20分間に亘って45秒毎に405nmで吸光度を記録した。隣接する8つの読取値に最も急な勾配を適用することにより、初期反応速度として表したsTNALP−FcD10酵素活性を評価した。治験薬の濃度を変化させて標準液を調製し、例1において先に記載したように酵素活性を決定した。標準液の量の対数の関数としての初期速度の対数をプロットすることによって標準曲線を作成した。異なる血漿試料のsTNALP−FcD10濃度を、それぞれの酵素活性を用いて標準曲線から直接読み取った。
既に記載したように、6−ホスホ[6−3H]グルコネートの反応生成物からのUDP−D−[6−3H]グルコース(Amersham Pharmacia)の活性炭上の示差吸着を用いて、心臓穿刺から得た血清中のPPiの循環値を測定した(Johnsonら、1999)。
成体WTマウスにおいて、マウスに注射したsTNALP−FcD10の半減期及び組織分布を決定した。図10は、成体WTマウスへの5mg/kgの単回ボーラス静脈内注射の後の、その薬物動態及び組織分布をまとめたものである。
表2:新生児WTマウスにおけるsTNALP−FcD10の薬物動態パラメータ
ボーラス静脈内投与の後の成体WTマウスの骨におけるsTNALP−FcD10の濃度
129J成体WTマウスに、投与量5mg/kgでsTNALP−FcD10を静脈内投与した。T=25時間での骨におけるsTNALP−FcD10濃度は、以下の通りだった。頭頂骨:0.64μg/g;脛骨:1.33μg/g;及び大腿骨:1.37μg/g、平均濃度:1.11μg/g。ラットにおいて、骨組織は総質量の16.3%である。この割合もまたマウスにおいて明らかにされることが期待される。この実験に使用するマウスの体重は18.4gだった。したがって、これらのマウスの算出骨組織重量は、約18.4g×0.163=3.00gだった。骨組織のsTNALP−FcD10の算出量は3.33μgだった。したがって、骨組織における注射投与量の割合は、(3.33μg/(5μg/g*18.4g))*100=4%だった。
ボーラス皮下注射の15日後の新生児WTマウスの骨におけるsTNALP−FcD10の濃度
129J新生児のWTマウスに、投与量4.3mg/kgでsTNALP−FcD10を、総投与量65mg/kgで15日間毎日皮下投与した。T=24時間での骨のsTNALP−FcD10濃度は、以下の通りだった。頭頂骨:6.45μg/g;脛骨:3.05μg/g;及び大腿骨:3.71μg/g、平均濃度:4.40μg/g。この実験に使用するマウスの体重は9.83gだった。したがって、これらのマウスの算出骨組織重量は、約9.83g×0.163=1.60gだった。したがって、その際のマウス骨組織のsTNALP−FcD10の量は約7.04μgだった。したがって、骨組織における注射投与量の割合は、(7.04μg/(65μg/g*9.83g))*100=1%だった。
表3:sTNALP−FcD10の平均濃度及び骨における注射投与量の割合
(1)示された時間は、最後の注射からのものである。
Akp2−/−マウスにおけるHPPについての低用量(1mg/kg)のsTNALP−FcD10の短期(15日間)の有効性
sTNALP−FcD10の皮下注射を、1mg/kgを用いてAkp2−/−マウスにおいて15日間毎日行った。投与群は、19匹の同腹仔から構成された。Akp2−/−マウスには、媒体(N=13)又はsTNALP−FcD10(N=12)を投与した。対照は、15匹のWTマウス(1匹の同腹仔につき1匹)からなった。対照に対して注射を行わなかった。例6に記載したように、最後の注射の24時間後に血液を採取した。
Akp2−/−マウスのHPPについての高用量(8.2mg/kg)のsTNALP−FcD10の短期(15日間)の有効性
成長及び骨ミネラル化に対する、有意により高い用量のsTNALP−FcD10(8.2mg/kg)を用いた毎日15日間の皮下注射を評価するために、20匹の同腹仔からのマウス(合計で141匹のマウス)を用いた。それらを以下の2群に分けた。1)媒体が投与されたAkp2−/−マウス(N=19);2)sTNALP−FcD10が投与されたAkp2−/−マウス(N=20);更に1匹の同腹仔につき1匹のWTマウス(投与なし)(N=18)がいた。
Akp2−/−マウスの成長は、WTマウスよりも遅かった。1日目において、媒体動物、sTNALP−FcD10動物及びWT動物の間に体重の統計学的な差は認められなかった。しかしながら、1日平均体重は、6日目で相違した(図18)。WT(4.2±0.6g)及び媒体(3.7±0.7g)の間の差は、6日目に統計学的有意性に達した(p=0.0217)が、媒体(5.9±1.0g)及びsTNALP−FcD10を投与した場合の値(6.7±1.0g)の間の差は、11日目に統計学的有意性に達し(p=0.04)、逆に投与群のほうがWTよりも重かった。16日目において、投与動物(8.2±1.1g)及びWT(8.4±0.8g)の平均体重に統計学的な差はなかった。sTNALP−FcD10が投与された動物の体重は、媒体が投与された動物(6.6±1.4g)よりも統計学的に大きかった(p=0.026)。体重について、ERT群とWT群との間に有意差はいずれの時点においても認められなかった。
この実験の終了時(16日目)、脛骨の長さは、Akp2−/−マウスにとっての骨格の有益性を示す更なる測定値を提供した。ERTの脛骨長は、12.6±0.7mmであり、媒体が投与された動物(11.7±1.1mm)より長かった(p=0.0135)(図19)。また、sTNALP−FcD10(9.2±0.4mm)群と媒体(8.6±0.8mm)群との間で大腿骨長を比較した際においても、統計学的な差が得られた(p=0.0267)。WTマウスと比較してERTの脛骨長又は大腿骨長に統計学的な差は示されなかった。脛骨及び大腿骨の成長の部分的維持(即ち、約2週齢で明らかに認められる骨成長の減少の部分的防止)は、剖検時に長さを測定することにより観察された(図19)。
足及び胸郭のFaxitron(商標)画像のブラインド評価において、Akp2−/−マウスのミネラル化の欠損の重症度を2つの程度に区別した(図21)。重症に罹患したマウス(重症)には、指の骨(指骨)及び二次骨化中心の欠如が認められた。中等度に罹患した(中程度)マウスには、異常な二次骨化中心があったが、指の骨は全て存在した。WTマウス(健康)は、通常の構築物と共に存在する全ての骨構造を有した。後肢のX線画像も同様に、急性骨折又は慢性骨折のエビデンスが存在する場合には異常と、いずれの異常所見もない場合には健康と類別した(図21)。ERTは、重症の欠損を有するAkp2−/−マウスの数で記録された足のミネラル化の欠損をできる限り小さく抑え、それは、未投与群では5例だったが、ERT群では0例だった(図21の表)。カイ二乗は有意であったが(p≦0.05)、それは、ERTが後天性骨欠損の重症度を低下させたことを示している。重症に罹患した小児性HPP患者は、多くの場合、呼吸の支持を不可能にする肋骨のミネラル低下及び骨折により死亡するため、胸部も綿密に検討した。また、ERTは、重症の異形胸郭の発現率を減少させた(図21の表)。カイ二乗解析は、p≦0.025で有意だった。同様に、後肢は、全投与動物で健康であると思われた(図21の表)。カイ二乗解析は、p≦0.025で有意だった。
16日齢マウスからの下顎骨を、カコジル酸ナトリウム緩衝アルデヒド溶液中に終夜浸漬固定し、第一大臼歯、根元の切歯及び周囲の歯槽骨を含むセグメントに切断した。試料を、等級分けされたエタノール系で脱水し、アクリル(LR White)樹脂又はエポキシ(Epon812)樹脂のいずれかで浸潤し、その後55℃で2日間組織含有樹脂ブロックの重合を行った。薄切片(1μm)は、ダイヤモンドナイフを用いたウルトラミクロトームで切断し、ガラススライドに載置した切片を、1%の硝酸銀を用いてミネラルについて染色し(フォンコッサ染色、黒)、1%トルイジンブルーで対比染色した。比較組織学的解析のために、下顎骨までの(第一大臼歯の最も近心の根と同じレベルでの)前額面切片により、縦に切断された大臼歯と断面化された切歯とを得た。
Akp2−/−マウスのHPPについての高用量(8.2mg/kg)のsTNALP−FcD10の長期(52日間)の有効性
最終的に、Akp2−/−マウスの長期の生存及び骨ミネラル化を評価するために、sTNALP−FcD10(8.2mg/kg)又は媒体のいずれかを52日間毎日投与した(皮下注射)。
未投与のマウスは、生存期間の中央値が18.5日間だった(図23)のに対して、ERTでは生存期間が非常に増加し、この投与によってもまた、投与を受けたマウスの正常な活動性及び健康な外観は維持された(図24)。
16日齢のAkp2−/−マウスの足のX線写真は、前記疾患の特質である二次的な骨形成の欠損を示した(図25参照)。これらの欠損は、46日間又は53日間のsTNALP−FcD10の1日用量によって、全投与マウスにおいて予防された(図25)。
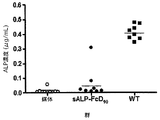
53日後に投与を受けたAkp2−/−マウスにおいて血漿中ALP活性レベルを測定した。図26は、ほとんどの値が1〜4μg/mLのALP活性だったことを示している。しかしながら、3匹の動物のALP濃度は検出することができなかった。
Akp2−/−マウスにおけるsTNALP−FcD10の異なる投与間隔の長期間の有効性
新生児Akp2−/−マウスに、毎日4.3mg/kg(Tx−1)、3日毎に15.2mg/kg(Tx−3)又は7日毎に15.2mg/kg(Tx−7)のsTNALP−FcD10を注射した。投与を43日間行い、44日目、即ち最後の注射の24時間後にマウスを屠殺した。それらのマウスの生存期間及び骨格のミネラル化のあらゆる向上を評価するために、それらのマウスのモニタリングを行った。
投与を受けたマウスの生存期間は、媒体が注射されたマウスと比較して増加した(図27)。この増加は、統計学的に有意だった(p<0.0001)。投与群の生存曲線をそれら自身の間で比較した際、統計学的な有意差はなかった。
A)各投与について、足のX線写真を解析し、正常と異常とに区分した。下記の表4に、数及び割合(括弧内)を示す。23日目及び試験終了時(23〜45日目)に骨ミネラル化の欠損について評価した。
表4:足のX線写真の区分
B)
15日齢のAkp2−/−マウスの高用量(8.2mg/kg)のsTNALP−FcD10の長期間の有効性
15日齢のマウスにおいて、例11に記載された通りの有効性の試験を行ったが、それは、足のX線写真で観察した場合の骨格の欠損を明示するために開始したものであった(例11、図25参照)。試験終了時までsTNALP−FcD10を投与した。生存期間、体重及び骨格のミネラル化についてのあらゆる改善を評価するために、動物のモニタリングを行った。
15日目で開始した8.2mg/kgのsTNALP−FcD10のAkp2−/−マウスへの毎日の注射により、媒体が注射されたマウスと比較して、生存期間は増加した(図28)。この増加は、統計学的に有意だった(p<0.05)。
試験開始時、体重の有意差は群間に認められなかった(図29)。投与の初めは(15日目)、Akp2−/−マウスの体重は野生型動物よりも小さかった。媒体が注射された動物の体重は減少し続けたが、一方で、sTNALP−FcD10が投与されたAkp2−/−マウスは、投与開始の4〜5日後に体重の増加が始まり、試験終了時まで体重の増加が続いたが、野生型動物の値には達しなかった。この体重増加は、sTNALP−FcD10が投与された動物の健康の改善を示唆している。
各投与について、足のX線写真を解析し、正常と異常とに区別した。表5に、数及び割合(括弧内)を示す。剖検時にX線写真を撮影した。
表5:足のX線写真の分布
Akp2−/−マウスの救出に対するsTNALP−FcD10の異なる投与間隔の長期の有効性
マウスに、12日目において投与を開始し、8.2mg/Kgの媒体(RV)を毎日46/47日目まで皮下注入(RTx−1)した後、又は、8.2.mg/Kgを毎日7日間注入した後、3日毎に24.6mg/Kg(RTx−3)又は7日毎に57.4mg/Kg(RTx−7)を注射した。生存期間の中央値は、RVマウスについては19.5日間、RTx−7マウスについては21.0日間、RTx−3マウスについては30.5日間、及びRTx−1マウスについては37.5日間であった。全例において、媒体投与群と比較した場合、生存期間は統計学的に増加した。既知の低ホスファターゼ血症のAkp2−/−マウスにおいて、ERTの明確な有益性が認められる。毎日よりも少ない投与によっても、生存期間を統計学的に増加させると思われる。
幼若Sprague−Dawleyラットにおける最大耐量の静脈内注射の毒性試験
本試験の目的は、治験薬(sTNALP−FcD10)の最大耐量(MTD)及び毒性を決定した後、静脈内注射によって幼若Sprague−Dawleyラットに反復投与を行うことであった。例15〜18において、使用するsALP−FcD10は、図3に具体的に記載されているものである。
幼若カニクイザルにおける静脈内注射及び注入の最大耐量の毒性試験
この試験の目的は、幼若カニクイザルへの静脈内注射又は注入により1回投与する際のsTNALP−FcD10の最大耐量を決定することだった。下記の表7に示すように、治験薬の投与製剤を、漸増的に1回投与した。
表7:試験デザイン
*主要試験の動物にのみ46日目に投与を行った。
28日間の回復期間を伴う、幼若アルビノラットにおけるsTNALP−FcD10の4週間(1週間に1回)の静脈内注射の毒性試験
この試験の目的は、28日間の回復を伴う、少なくとも4週間連続で幼若ラットに静脈内注射することによって1週間に1回投与(合計4回の投与)されたsTNALP−FcD10の潜在的毒性を調査することだった。動物には、試験1、8、15及び22日目に投与を行い、回復期間は試験29日目から開始した。下記の表8に試験デザインを詳述する。
表8:試験デザイン
28日間の回復期間を伴う、幼若カニクイザルにおける4週間の静脈内注射の毒性試験
この試験の目的は、4週間の緩やかなボーラス静脈内注射によって1週間に1回投与した際の幼若カニクイザルにおけるsTNALP−FcD10の毒性及び毒物動態を決定すること、及び28日間の回復期間後のあらゆる変化の回復能を評価することだった。
表9:試験デザイン
*群1の動物に、媒体/対照薬(25mMリン酸ナトリウムpH7.4(150mM NaCl))を投与した。
ヒトについての最大推奨初回用量の決定
無毒性量(NOAEL、Guidance for Industry and Reviewers、2002年12月を参照すること)を確立することによって、ヒトについての最大推奨初回用量(MRSD)を算出する。皮下に毎日1mg/kg、5mg/kg及び8.2mg/kg;3mg/kg、5mg/kg、10mg/kg、30mg/kg、45mg/kg、90mg/kg及び180mg/kgを含む上記の製剤の各種濃度を、マウス、ラット及びサルで試験した。最も感受性が高い種(即ちラット)のNOAELは、30mg/kgだった。
Claims (52)
- 構造:
Z−sALP−Y−スペーサー−X−Wn−V
を有するポリペプチドを含む骨標的アルカリホスファターゼ
[配列中、sALPはアルカリホスファターゼの細胞外ドメインであり、
Vは不在である又は少なくとも1つのアミノ酸のアミノ酸配列であり、
Xは不在である又は少なくとも1つのアミノ酸のアミノ酸配列であり、
Yは不在である又は少なくとも1つのアミノ酸のアミノ酸配列であり、
Zは不在である又は少なくとも1つのアミノ酸のアミノ酸配列であり、
Wnはn=10〜16のポリアスパラギン酸又はポリグルタミン酸であり、及び、
スペーサーはフラグメント結晶化可能領域(Fc)を含む]であって、sALPは生理学的に活性である、上記アルカリホスファターゼ。 - 前記sALPは組織非特異的アルカリホスファターゼ(TNALP)の細胞外ドメインである、請求項1に記載のアルカリホスファターゼ。
- a)前記TNALPは配列番号21、22、23、24、25、又は26に記載の配列を有するヒトTNALPであるか;
b)前記TNALPは配列番号27に記載の配列を有するアカゲザルTNALPであるか;
c)前記TNALPは配列番号28に記載の配列を有するラットTNALPであるか;
d)前記TNALPは配列番号29に記載の配列を有するイヌTNALPであるか;
e)前記TNALPは配列番号30に記載の配列を有するブタTNALPであるか;
f)前記TNALPは配列番号31に記載の配列を有するマウスTNALPであるか;
g)前記TNALPは配列番号32、33又は34に記載の配列を有するウシTNALPであるか;又は、
h)前記TNALPは配列番号35に記載の配列を有するネコTNALPである;
請求項2に記載のアルカリホスファターゼ。 - a)sALPが配列番号15のアミノ酸残基23〜508を含むか、若しくは、
sALPが配列番号15のアミノ酸残基23〜512からなるか、又は、
b)sALPが配列番号18のアミノ酸残基23〜508を含むか、若しくは、
sALPが配列番号18のアミノ酸残基23〜512からなるか、又は、
c)sALPが配列番号16のアミノ酸残基18〜498を含むか、若しくは、sALPが配列番号16のアミノ酸残基18〜502からなるか、又は、
d)sALPが配列番号19のアミノ酸残基18〜498を含むか、若しくは、sALPが配列番号19のアミノ酸残基18〜502からなるか、又は、
e)sALPが配列番号8のアミノ酸残基18〜498を含むか、若しくは、
sALPが配列番号8のアミノ酸残基18〜502からなる、請求項1に記載のアルカリホスファターゼ。 - 前記sALPは配列番号8のアミノ酸残基18〜502からなる、請求項4に記載のアルカリホスファターゼ。
- a)前記アルカリホスファターゼは胎盤アルカリホスファターゼ(PAL)由来のものであるか、若しくは、配列番号36又は37に記載の配列を有する胎盤アルカリホスファターゼ由来のものであるか;
b)前記アルカリホスファターゼは生殖細胞アルカリホスファターゼ(GCAL)由来のものであるか、若しくは、配列番号38に記載の配列を有する生殖細胞アルカリホスファターゼ由来のものであるか;又は、
c)前記アルカリホスファターゼは腸アルカリホスファターゼ(IALP)由来のものであるか、若しくは、配列番号39に記載の配列を有する腸アルカリホスファターゼ由来のものである;
請求項1に記載のアルカリホスファターゼ。 - Wnがポリアスパラギン酸であるか、又は、ここで、n=10である、請求項1から6までのいずれか一項に記載のアルカリホスファターゼ。
- Zが不在である、及び/又は、Vが不在である、請求項1から7までのいずれか一項に記載のアルカリホスファターゼ。
- Yが2つのアミノ酸残基である、請求項1から8までのいずれか一項に記載のアルカリホスファターゼ。
- Yがロイシン−リシンである、請求項9に記載のアルカリホスファターゼ。
- Xが2つのアミノ酸残基である、請求項1から10までのいずれか一項に記載のアルカリホスファターゼ。
- Xがアスパラギン酸−イソロイシンである、請求項11に記載のアルカリホスファターゼ。
- a)sALPが配列番号8のアミノ酸残基18〜502からなり、
b)Wnがポリアスパラギン酸であって、n=10であり、
c)Z及びVが不在であり、
d)Yがロイシン−リシンであり、及び、
e)Xがアスパラギン酸−イソロイシンである、請求項1に記載のアルカリホスファターゼ。 - FcがCH2ドメイン、CH3ドメイン及びヒンジ領域を含むか、又は、Fcが、IgG−1、IgG−2、IgG−3及びIgG−4からなる群から選択される免疫グロブリンの定常ドメインである、請求項1から13までのいずれか一項に記載のアルカリホスファターゼ。
- Fcが免疫グロブリンIgG−1の定常ドメインである、請求項14に記載のアルカリホスファターゼ。
- Fcが配列番号3に記載の通りである、請求項15に記載のアルカリホスファターゼ。
- 前記ポリペプチドが配列番号4に記載の通りである、請求項1に記載のアルカリホスファターゼ。
- 前記ポリペプチドを二量体又は四量体を含む形で含む、請求項1から17までのいずれか一項に記載のアルカリホスファターゼであって、ここで、該二量体は2つのジスルフィド架橋により結合しているか結合していないものである、上記アルカリホスファターゼ。
- 前記アルカリホスファターゼが前記ポリペプチドからなり、Z及びVが不在である、請求項1から18までのいずれか一項に記載のアルカリホスファターゼ。
- 前記アルカリホスファターゼがグリコシル化されたものである、請求項1から19までのいずれか一項に記載のアルカリホスファターゼ。
- 前記sALPがホスホエタノールアミン(PEA)、無機ピロリン酸(PPi)及びピリドキサール5’−リン酸(PLP)に対して生理学的に活性である、請求項1から20までのいずれか一項に記載のアルカリホスファターゼ。
- 請求項1から21までのいずれか一項に記載のアルカリホスファターゼと薬学的に許容可能な担体を含む、医薬組成物。
- 薬学的に許容可能な担体が生理食塩水である、請求項22に記載の医薬組成物。
- 前記薬学的に許容可能な担体が塩化ナトリウム及び/又はリン酸ナトリウムを含むか、又は、組成物が150mM塩化ナトリウム及び25mMリン酸ナトリウム、pH7.4を含む、請求項23に記載の医薬組成物。
- 前記アルカリホスファターゼが凍結乾燥された形の、請求項22から24までのいずれか一項に記載の医薬組成物。
- 医薬として使用するための、請求項1から22までのいずれか一項に記載のアルカリホスファターゼ。
- 0.2〜20mg/kgの1日投与量であるか、又は、1.4〜140mg/kgの1週投与量である、請求項26に記載のアルカリホスファターゼ。
- 請求項1から21までのいずれか一項に定義のポリペプチドをコードする配列を含むか、又は、からなる、単離された核酸分子。
- 請求項28に記載の核酸分子を含む、組換え発現ベクター。
- 請求項28に記載の核酸分子を含む、組換えアデノ随伴ウイルスベクター。
- 請求項29又は30に記載のベクターで形質転換された又はトランスフェクトされた、単離された組換え宿主細胞。
- 請求項1から21までのいずれか一項に記載のアルカリホスファターゼを作製する方法であって、アルカリホスファターゼの発現をもたらすのに適した条件下で、請求項31に記載の宿主細胞を培養すること、及び培地からアルカリホスファターゼを回収することを含む、上記方法。
- 宿主細胞が、L細胞、C127細胞、3T3細胞、BHK細胞、COS−7細胞又はチャイニーズハムスター卵巣(CHO)細胞である、請求項32に記載の方法。
- 宿主細胞がチャイニーズハムスター卵巣(CHO)細胞である、請求項33に記載の方法。
- 宿主細胞がCHO−DG44細胞である、請求項34に記載の方法。
- 請求項1から21までのいずれか一項に定義のアルカリホスファターゼ又は請求項22から25までのいずれか一項に記載の医薬組成物、及び低ホスファターゼ血症(HPP)表現型を改善又は予防する方法における該アルカリホスファターゼ又は該組成物の使用のための使用説明書を含む、キット。
- それを必要とする対象における少なくとも1つの低ホスファターゼ血症(HPP)表現型を改善又は予防するための方法の使用のための、請求項1から21までのいずれか一項に記載のアルカリホスファターゼ。
- 対象が少なくとも1つのHPP表現型を有する、請求項37に記載の使用のためのアルカリホスファターゼ。
- 前記少なくとも1つのHPP表現型が、
i)HPP関連発作、
ii)乳歯の早期喪失、
iii)不完全な骨ミネラル化、
iv)無機ピロリン酸(PPi)の血液及び/又は尿レベルの上昇、
v)ホスホエタノールアミン(PEA)の血液及び/又は尿レベルの上昇、
vi)ピリドキサール5’−リン酸(PLP)の血液及び/又は尿レベルの上昇、
vii)不十分な体重増加、
viii)くる病、
ix)骨痛、
x)ピロリン酸カルシウム二水和物結晶沈着、又は、
xi)歯セメント質の形成不全、発育不全若しくは異形成、又は
xii)骨軟化症
を含む、請求項37又は38に記載の使用のためのアルカリホスファターゼ。 - 前記不完全な骨ミネラル化が不完全な大腿骨ミネラル化、不完全な脛骨ミネラル化、不完全な中足骨ミネラル化、又は、不完全な肋骨ミネラル化である、請求項39に記載の使用のためのアルカリホスファターゼ。
- それを必要とする対象が、
a)幼児期HPP、又は
b)小児期HPP、又は
c)出生時HPP、又は
d)成人期HPP、又は
e)歯限局型低ホスファターゼ血症HPP
を有する、請求項37から40までのいずれか一項に記載の使用のためのアルカリホスファターゼ。 - 対象がヒトである、請求項37から41までのいずれか一項に記載の使用のためのアルカリホスファターゼ。
- 前記アルカリホスファターゼが下記の組成物中:
a)0.2〜20mg/kgの1日投与量であるか、又は、1.4〜140mg/kgの1週投与量であるように処方された組成物;
b)1日に投与されるか1週間に投与されるか若しくはその画分で投与されるように処方された組成物であるか、又は、毎日、1日おき、3日毎、若しくは7日毎に投与されるように処方された組成物;
c)皮下に、静脈内に、経口的に、経鼻的に、筋肉内に、舌下に、髄腔内に、又は皮内に投与されるように処方された組成物;
d)液体、溶液、懸濁液、丸薬、カプセル、錠剤、ジェルキャップ、粉末、ゲル、軟膏剤、クリーム、ネビュラ、ミスト、微粒化蒸気、エアロゾル、又はフィトソームの形状の組成物;
e)5mg/kg以下の1日投与量であるように処方された組成物であるか、又は、1又は2mg/kgの1日投与量であるように処方された組成物;
f)前記ポリペプチドが65mg/L以上、396mg/L以下の間の最大循環レベル(Cmax)を満たすように処方された組成物;又は、
g)前記ポリペプチドが1230mg/L以上、7720mg/L以下の間の最大循環レベル(Cmax)を満たすように処方された組成物;
に存在するものである、請求項37から42までのいずれか一項に記載の使用のためのアルカリホスファターゼ。 - 前記ポリペプチドが骨に蓄積するが、筋肉中には蓄積しないものである、請求項37から43までのいずれか一項に記載の使用のためのアルカリホスファターゼ。
- 前記アルカリホスファターゼが薬学的に許容可能な担体と混合されるものである、請求項37から44までのいずれか一項に記載の使用のためのアルカリホスファターゼ。
- 前記薬学的に許容可能な担体が塩化ナトリウム及び/又はリン酸ナトリウムを含むか、又は、組成物が150mM塩化ナトリウム及び25mMリン酸ナトリウム、pH7.4を含む、請求項45に記載の使用のためのアルカリホスファターゼ。
- 前記アルカリホスファターゼが凍結乾燥された形の、請求項37から45までのいずれか一項に記載の使用のためのアルカリホスファターゼ。
- 前記使用が、アルカリホスファターゼをコードする核酸分子で対象の細胞をトランスフェクトすることを含む、請求項37から42までのいずれか一項に記載の使用のためのアルカリホスファターゼ。
- 細胞をトランスフェクトすることが、アルカリホスファターゼが発現され、及び活性型で分泌されるようにインビトロで行われ、及び該細胞によって対象に投与される、請求項48に記載の使用のためのアルカリホスファターゼ。
- アルカリホスファターゼが皮下投与、又は静脈内投与のために処方された、請求項37から47までのいずれか一項に記載の使用のためのアルカリホスファターゼ。
- 前記アルカリホスファターゼが皮下投与のために処方された、請求項50に記載の使用のためのアルカリホスファターゼ。
- それを必要とする対象又はヒトにおける、少なくとも1つの低アルカリホスファターゼ症(HPP)表現型を改善又は予防する方法の使用のための、請求項22から25までのいずれか一項に記載の医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US91758907P | 2007-05-11 | 2007-05-11 | |
| US60/917,589 | 2007-05-11 | ||
| PCT/CA2008/000923 WO2008138131A1 (en) | 2007-05-11 | 2008-05-12 | Bone targeted alkaline phosphatase, kits and methods of use thereof |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2010526543A JP2010526543A (ja) | 2010-08-05 |
| JP2010526543A5 JP2010526543A5 (ja) | 2011-06-30 |
| JP5732603B2 true JP5732603B2 (ja) | 2015-06-10 |
Family
ID=40001639
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010507770A Active JP5732603B2 (ja) | 2007-05-11 | 2008-05-12 | 骨標的アルカリホスファターゼ、キット及びその使用方法 |
Country Status (25)
| Country | Link |
|---|---|
| US (1) | US20100297119A1 (ja) |
| EP (3) | EP2158319B1 (ja) |
| JP (1) | JP5732603B2 (ja) |
| AT (1) | ATE536413T1 (ja) |
| AU (1) | AU2008250945B2 (ja) |
| BR (2) | BRPI0811198B8 (ja) |
| CA (1) | CA2687001C (ja) |
| CY (1) | CY2016005I2 (ja) |
| DE (1) | DE202008018131U1 (ja) |
| DK (3) | DK2158319T3 (ja) |
| ES (3) | ES2471915T3 (ja) |
| FR (1) | FR16C0007I2 (ja) |
| HR (1) | HRP20140416T1 (ja) |
| HU (2) | HUE031655T2 (ja) |
| IL (1) | IL202057A0 (ja) |
| LT (1) | LTC2368999I2 (ja) |
| LU (1) | LU92976I2 (ja) |
| ME (1) | ME01828B (ja) |
| NL (1) | NL300798I1 (ja) |
| NO (1) | NO2016002I1 (ja) |
| PL (3) | PL2158319T4 (ja) |
| PT (3) | PT2662448T (ja) |
| RS (1) | RS53302B (ja) |
| SI (2) | SI2662448T1 (ja) |
| WO (1) | WO2008138131A1 (ja) |
Families Citing this family (48)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HUE055861T2 (hu) | 2004-04-21 | 2021-12-28 | Alexion Pharma Inc | Csontbejuttató konjugátumok és azok alkalmazási módszere fehérjék csonthoz kötéséhez |
| US20070081984A1 (en) | 2005-10-11 | 2007-04-12 | Shunji Tomatsu | Compositions and methods for treating hypophosphatasia |
| US8784833B2 (en) * | 2006-06-27 | 2014-07-22 | Saint Louis University | Prenatal enzyme replacement therapy for hypophosphatasia |
| MX367012B (es) | 2007-06-01 | 2019-08-02 | Univ Maryland | Agentes de union al receptor de la region constante fc de inmunoglobulina. |
| WO2011113027A2 (en) | 2010-03-12 | 2011-09-15 | Synageva Biopharma Corp | Npp1 fusion proteins |
| BR112012027765A2 (pt) * | 2010-04-30 | 2019-09-24 | Enobia Pharma Inc | métodos, composições e kits para tratamento de distúrbios de mineralização da matriz. |
| AU2011282579B2 (en) | 2010-07-28 | 2014-10-23 | Gliknik Inc. | Fusion proteins of natural human protein fragments to create orderly multimerized immunoglobulin Fc compositions |
| US9266939B2 (en) | 2010-12-27 | 2016-02-23 | Alexion Pharmaceuticals, Inc. | Compositions comprising natriuretic peptides and methods of use thereof |
| SG11201401605QA (en) * | 2011-10-19 | 2014-09-26 | Alexion Pharma Holding | Compositions comprising alkaline phosphatase and/or natriuretic peptide and methods of use thereof |
| US10052366B2 (en) | 2012-05-21 | 2018-08-21 | Alexion Pharmaceuticsl, Inc. | Compositions comprising alkaline phosphatase and/or natriuretic peptide and methods of use thereof |
| EP2885320A4 (en) | 2012-08-20 | 2016-04-06 | Gliknik Inc | MOLECULES WITH ANTIGEN-BINDING AND POLYVALENT FC GAMMA RECEPTOR BINDING ACTIVITY |
| PE20161442A1 (es) * | 2014-01-24 | 2017-01-12 | Am-Pharma B V | Proteinas quimericas tipo fosfatasa alcalina |
| WO2016007873A1 (en) | 2014-07-11 | 2016-01-14 | The Regents Of The University Of Michigan | Compositions and methods for treating craniosynostosis |
| CA2967851C (en) | 2014-12-05 | 2024-02-27 | Alexion Pharmaceuticals, Inc. | Treating seizure with recombinant alkaline phosphatase |
| AU2016211447B2 (en) | 2015-01-28 | 2021-09-23 | Alexion Pharmaceuticals, Inc. | Methods of treating a subject with an alkaline phosphatase deficiency |
| FI3325011T6 (fi) | 2015-07-24 | 2023-05-11 | Ihmisen proteiinifragmenttien fuusioproteiineja järjestyksenmukaisesti multimerisoitujen, paremmin komplementtia sitovien immunoglobuliini-fc-koostumusten muodostamiseksi | |
| EP3337894A1 (en) * | 2015-08-17 | 2018-06-27 | Alexion Pharmaceuticals, Inc. | Manufacturing of alkaline phosphatases |
| JP6868617B2 (ja) * | 2015-09-28 | 2021-05-12 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | 低ホスファターゼ血症の組織非特異的アルカリホスファターゼ(tnsalp)酵素補充療法に有効な投薬計画の特定 |
| US11400140B2 (en) | 2015-10-30 | 2022-08-02 | Alexion Pharmaceuticals, Inc. | Methods for treating craniosynostosis in a patient |
| US11065306B2 (en) | 2016-03-08 | 2021-07-20 | Alexion Pharmaceuticals, Inc. | Methods for treating hypophosphatasia in children |
| WO2017171871A1 (en) * | 2016-04-01 | 2017-10-05 | Alexion Pharmaceuticals, Inc. | Methods for treating hypophosphatasia in adolescents and adults |
| KR20220162816A (ko) * | 2016-04-01 | 2022-12-08 | 알렉시온 파마슈티칼스, 인코포레이티드 | 알칼리성 포스파타아제로 근육 약화의 치료 |
| WO2017173395A1 (en) * | 2016-04-01 | 2017-10-05 | Alexion Pharmaceuticals, Inc. | Methods for treating hypophosphatasia in adolescents and adults |
| US10988744B2 (en) | 2016-06-06 | 2021-04-27 | Alexion Pharmaceuticals, Inc. | Method of producing alkaline phosphatase |
| US11034775B2 (en) | 2016-06-07 | 2021-06-15 | Gliknik Inc. | Cysteine-optimized stradomers |
| EP3474886B1 (en) | 2016-06-27 | 2021-08-04 | Alexion Pharmaceuticals, Inc. | Methods for treating hypophosphatasia in children and adolescents |
| WO2018035420A1 (en) | 2016-08-18 | 2018-02-22 | Alexion Pharmaceuticals, Inc. | Methods for treating tracheobronchomalacia |
| WO2018102616A1 (en) * | 2016-11-30 | 2018-06-07 | Purdue Research Foundation | Fracture targeted bone regeneration through parathyroid hormone receptor stimulation |
| JP7519774B2 (ja) | 2016-12-09 | 2024-07-22 | グリックニック インコーポレイテッド | 多価fc化合物を用いる炎症性疾患の治療方法 |
| KR102729723B1 (ko) | 2016-12-09 | 2024-11-15 | 글리크닉 인코포레이티드 | 다합체화 스트라도머인 gl-2045의 제조 최적화 |
| US20220348977A1 (en) * | 2017-03-09 | 2022-11-03 | Alexion Pharmaceuticals, Inc. | Glycoprotein manufacturing process |
| JP2020512363A (ja) * | 2017-03-31 | 2020-04-23 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | 成人及び青年における低ホスファターゼ症(hpp)を治療する方法 |
| WO2019067502A1 (en) | 2017-09-27 | 2019-04-04 | Alexion Pharmaceuticals, Inc. | METHODS FOR IMPROVING CARDIOVASCULAR FUNCTION AND TREATING CARDIOVASCULAR DISEASE USING RECOMBINANT ECTO-NUCLEOTIDE PYROPHOSPHATASE / PHOSPHODIESTERASE |
| EP3737750B1 (en) | 2018-01-09 | 2024-06-05 | Theriva Biologics, Inc. | Alkaline phosphatase agents for treatment of neurodevelopmental disorders |
| JP7214962B2 (ja) * | 2018-01-17 | 2023-01-31 | 東ソー株式会社 | アルカリホスファターゼ高発現動物細胞 |
| ES3032290T3 (en) | 2018-03-20 | 2025-07-16 | Theriva Biologics Inc | Intestinal alkaline phosphatase formulations |
| WO2019183209A1 (en) | 2018-03-20 | 2019-09-26 | Synthetic Biologics, Inc. | Alkaline phosphatase agents for treatment of radiation disorders |
| JP2021519590A (ja) * | 2018-03-30 | 2021-08-12 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | 糖タンパク質の製造 |
| CN110499284A (zh) * | 2018-05-17 | 2019-11-26 | 西安组织工程与再生医学研究所 | Wnt信号通路激活剂在制备治疗基因ALPL敲除小鼠牙硬组织矿化异常产品中的应用 |
| US20210214408A1 (en) | 2018-05-30 | 2021-07-15 | Purdue Research Foundation | Targeting anabolic drugs for accelerated fracture repair |
| WO2020033867A2 (en) | 2018-08-10 | 2020-02-13 | Alexion Pharmaceuticals, Inc. | Methods of treating neurofibromatosis type 1 and related conditions with alkaline phosphatase |
| AU2020270046B2 (en) | 2019-05-06 | 2026-02-05 | Theriva Biologics, Inc. | Alkaline phosphate-based oncology treatments |
| JP7796645B2 (ja) * | 2019-12-09 | 2026-01-09 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | アルカリホスファターゼポリペプチド及びその使用方法 |
| EP4084819A1 (en) | 2020-01-03 | 2022-11-09 | The United States of America, as represented by the Secretary, Department of Health and Human Services | Tnap locally administered for promoting periodontal health |
| KR20230117327A (ko) * | 2020-09-03 | 2023-08-08 | 어빈 에스.와이. 첸 | 가용성 알칼리성 포스파타제 작제물 및 가용성 알칼리성 포스파타제 작제물을 인코딩하는 폴리뉴클레오티드를 포함하는 발현 벡터 |
| KR102571967B1 (ko) * | 2021-01-21 | 2023-08-30 | 주식회사 마라나노텍코리아 | Alp 측정용 바이오 센서 |
| CA3173631A1 (en) | 2021-02-12 | 2022-08-18 | Walter C. Voegtli | Alkaline phosphatase polypeptides and methods of use thereof |
| US20260027233A1 (en) * | 2022-08-31 | 2026-01-29 | University Of Utah Research Foundation | Gja1-20k compositions and methods for mitigating ischemia-reperfusion injury |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7008A (en) * | 1850-01-08 | Improvement in alloys for points of lightning-rods | ||
| ES2249761T3 (es) | 1993-06-24 | 2006-04-01 | Advec Inc. | Vectores de adenovirus para terapia genica. |
| SK283703B6 (sk) | 1993-10-25 | 2003-12-02 | Canji, Inc. | Rekombinantný adenovírusový vektor a jeho použitie |
| US7252989B1 (en) | 1994-04-04 | 2007-08-07 | Board Of Regents, The University Of Texas System | Adenovirus supervector system |
| ATE360082T1 (de) | 1999-11-16 | 2007-05-15 | Genzyme Corp | Vektoren und transgene mit regulatorischen elementen zur genverabreichung in leber |
| US6808905B2 (en) | 2001-05-14 | 2004-10-26 | Cell Genesys, Inc. | Lentiviral vectors encoding clotting factors for gene therapy |
| CA2433479A1 (en) | 2002-07-22 | 2004-01-22 | F. Hoffmann-La Roche Ag | Conjugate of a tissue non-specific alkaline phosphatase and dextran, process for its production and use thereof |
| HUE055861T2 (hu) | 2004-04-21 | 2021-12-28 | Alexion Pharma Inc | Csontbejuttató konjugátumok és azok alkalmazási módszere fehérjék csonthoz kötéséhez |
| US20070081984A1 (en) * | 2005-10-11 | 2007-04-12 | Shunji Tomatsu | Compositions and methods for treating hypophosphatasia |
| WO2006002203A2 (en) | 2004-06-23 | 2006-01-05 | Genzyme Corporation | Methods and compositions for the treatment of polycystic diseases |
| WO2006039480A2 (en) * | 2004-09-29 | 2006-04-13 | The Burnham Institute For Medical Research | Tissue non-specific alkaline phosphate (tnap): a therapeutic target for arterial calcification |
| MX2007006524A (es) | 2004-12-01 | 2007-06-22 | Genzyme Corp | Metodos para el suministro dirigido de material genetico al higado. |
-
2008
- 2008-05-12 PL PL08757088T patent/PL2158319T4/pl unknown
- 2008-05-12 CA CA2687001A patent/CA2687001C/en active Active
- 2008-05-12 DK DK08757088.3T patent/DK2158319T3/da active
- 2008-05-12 US US12/599,679 patent/US20100297119A1/en not_active Abandoned
- 2008-05-12 WO PCT/CA2008/000923 patent/WO2008138131A1/en not_active Ceased
- 2008-05-12 BR BRPI0811198A patent/BRPI0811198B8/pt active IP Right Grant
- 2008-05-12 SI SI200831780A patent/SI2662448T1/sl unknown
- 2008-05-12 JP JP2010507770A patent/JP5732603B2/ja active Active
- 2008-05-12 ES ES11004496.3T patent/ES2471915T3/es active Active
- 2008-05-12 ES ES08757088T patent/ES2380546T3/es active Active
- 2008-05-12 EP EP08757088A patent/EP2158319B1/en active Active
- 2008-05-12 EP EP13002327.8A patent/EP2662448B1/en active Active
- 2008-05-12 ME MEP-2014-48A patent/ME01828B/me unknown
- 2008-05-12 RS RS20140237A patent/RS53302B/sr unknown
- 2008-05-12 AT AT08757088T patent/ATE536413T1/de active
- 2008-05-12 DE DE202008018131U patent/DE202008018131U1/de not_active Expired - Lifetime
- 2008-05-12 DK DK11004496.3T patent/DK2368999T3/da active
- 2008-05-12 PL PL13002327T patent/PL2662448T3/pl unknown
- 2008-05-12 BR BR122019000505-2A patent/BR122019000505B1/pt active Search and Examination
- 2008-05-12 HU HUE13002327A patent/HUE031655T2/hu unknown
- 2008-05-12 PL PL11004496T patent/PL2368999T3/pl unknown
- 2008-05-12 DK DK13002327.8T patent/DK2662448T3/en active
- 2008-05-12 AU AU2008250945A patent/AU2008250945B2/en active Active
- 2008-05-12 PT PT130023278T patent/PT2662448T/pt unknown
- 2008-05-12 SI SI200831200T patent/SI2368999T1/sl unknown
- 2008-05-12 PT PT110044963T patent/PT2368999E/pt unknown
- 2008-05-12 EP EP11004496.3A patent/EP2368999B1/en active Active
- 2008-05-12 PT PT08757088T patent/PT2158319E/pt unknown
- 2008-05-12 ES ES13002327T patent/ES2619332T3/es active Active
-
2009
- 2009-11-11 IL IL202057A patent/IL202057A0/en unknown
-
2014
- 2014-05-08 HR HRP20140416AT patent/HRP20140416T1/hr unknown
-
2016
- 2016-01-15 HU HUS1600005C patent/HUS1600005I1/hu unknown
- 2016-01-28 LT LTPA2016004C patent/LTC2368999I2/lt unknown
- 2016-02-02 NO NO2016002C patent/NO2016002I1/no not_active IP Right Cessation
- 2016-02-10 LU LU92976C patent/LU92976I2/xx unknown
- 2016-02-19 FR FR16C0007C patent/FR16C0007I2/fr active Active
- 2016-02-23 CY CY2016005C patent/CY2016005I2/el unknown
- 2016-02-26 NL NL300798C patent/NL300798I1/nl unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5732603B2 (ja) | 骨標的アルカリホスファターゼ、キット及びその使用方法 | |
| Millán et al. | Enzyme replacement therapy for murine hypophosphatasia | |
| KR101672156B1 (ko) | 액티빈-ActRⅡA 길항제 및 암 환자에서 골 생장을 촉진시키기 위한 이의 용도 | |
| JP5986986B2 (ja) | 基質石灰化障害を治療する方法、組成物、およびキット | |
| RU2678117C2 (ru) | Антагонисты активина-actrii и их применение для лечения нарушений костной ткани и других нарушений | |
| KR102249454B1 (ko) | 골격 성장 지연 질환의 예방 또는 치료에 사용하기 위한 용해성 섬유아세포 성장 인자 수용체 3(fgr3) 폴리펩티드 | |
| CN114786712A (zh) | 用于治疗高胱氨酸尿症的酶疗法的PEG化胱硫醚β合成酶 | |
| HK1162589B (en) | Bone targeted alkaline phosphatase, kits and methods of use thereof | |
| HK1141047B (en) | Bone targeted alkaline phosphatase, kits and methods of use thereof | |
| HK1191372B (en) | Bone targeted alkaline phosphatase, kits and methods of use thereof | |
| AU2013203875A1 (en) | Bone Targeted Alkaline Phosphatase, Kits and Methods of Use Thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20100119 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A525 Effective date: 20100112 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110512 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110512 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20120323 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20120323 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20130422 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20130423 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130628 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130926 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20131003 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131025 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20131025 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140627 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140929 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20141001 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20141120 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20141222 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20150306 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20150313 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5732603 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |