JP5080452B2 - 改良された発現エレメント - Google Patents
改良された発現エレメント Download PDFInfo
- Publication number
- JP5080452B2 JP5080452B2 JP2008511772A JP2008511772A JP5080452B2 JP 5080452 B2 JP5080452 B2 JP 5080452B2 JP 2008511772 A JP2008511772 A JP 2008511772A JP 2008511772 A JP2008511772 A JP 2008511772A JP 5080452 B2 JP5080452 B2 JP 5080452B2
- Authority
- JP
- Japan
- Prior art keywords
- promoter
- polynucleotide
- gene
- vector
- expression
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000014509 gene expression Effects 0.000 title claims abstract description 49
- 210000004027 cell Anatomy 0.000 claims abstract description 57
- 239000013598 vector Substances 0.000 claims abstract description 34
- 108091029523 CpG island Proteins 0.000 claims abstract description 31
- 238000000034 method Methods 0.000 claims abstract description 10
- 108090000623 proteins and genes Proteins 0.000 claims description 49
- 102000040430 polynucleotide Human genes 0.000 claims description 29
- 108091033319 polynucleotide Proteins 0.000 claims description 29
- 239000002157 polynucleotide Substances 0.000 claims description 29
- 150000007523 nucleic acids Chemical group 0.000 claims description 19
- 102000039446 nucleic acids Human genes 0.000 claims description 15
- 108020004707 nucleic acids Proteins 0.000 claims description 15
- 239000012634 fragment Substances 0.000 claims description 14
- 239000002773 nucleotide Substances 0.000 claims description 14
- 125000003729 nucleotide group Chemical group 0.000 claims description 14
- 229920001184 polypeptide Polymers 0.000 claims description 13
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 13
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 13
- 101150013092 rps3 gene Proteins 0.000 claims description 13
- 239000013604 expression vector Substances 0.000 claims description 12
- 210000001519 tissue Anatomy 0.000 claims description 12
- 108700039691 Genetic Promoter Regions Proteins 0.000 claims description 11
- 230000001965 increasing effect Effects 0.000 claims description 11
- 238000010367 cloning Methods 0.000 claims description 7
- 241000701022 Cytomegalovirus Species 0.000 claims description 5
- 108010022366 Carcinoembryonic Antigen Proteins 0.000 claims description 4
- 102100025475 Carcinoembryonic antigen-related cell adhesion molecule 5 Human genes 0.000 claims description 4
- 108010037462 Cyclooxygenase 2 Proteins 0.000 claims description 4
- 206010028980 Neoplasm Diseases 0.000 claims description 4
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 4
- 102000007066 Prostate-Specific Antigen Human genes 0.000 claims description 4
- 108010072866 Prostate-Specific Antigen Proteins 0.000 claims description 4
- 241000714474 Rous sarcoma virus Species 0.000 claims description 4
- 108020003175 receptors Proteins 0.000 claims description 4
- 102000005962 receptors Human genes 0.000 claims description 4
- 241000894007 species Species 0.000 claims description 4
- 241000283984 Rodentia Species 0.000 claims description 3
- 102000003425 Tyrosinase Human genes 0.000 claims description 3
- 108060008724 Tyrosinase Proteins 0.000 claims description 3
- 230000002103 transcriptional effect Effects 0.000 claims description 3
- 102100023635 Alpha-fetoprotein Human genes 0.000 claims description 2
- 108090000695 Cytokines Proteins 0.000 claims description 2
- 102000004127 Cytokines Human genes 0.000 claims description 2
- 108700024394 Exon Proteins 0.000 claims description 2
- 241000713340 Human immunodeficiency virus 2 Species 0.000 claims description 2
- 102000010292 Peptide Elongation Factor 1 Human genes 0.000 claims description 2
- 108010077524 Peptide Elongation Factor 1 Proteins 0.000 claims description 2
- 102000001253 Protein Kinase Human genes 0.000 claims description 2
- 102000000479 TCF Transcription Factors Human genes 0.000 claims description 2
- 108010016283 TCF Transcription Factors Proteins 0.000 claims description 2
- 102000013529 alpha-Fetoproteins Human genes 0.000 claims description 2
- 108010026331 alpha-Fetoproteins Proteins 0.000 claims description 2
- 239000003114 blood coagulation factor Substances 0.000 claims description 2
- 238000012258 culturing Methods 0.000 claims description 2
- 239000003937 drug carrier Substances 0.000 claims description 2
- 239000003102 growth factor Substances 0.000 claims description 2
- 239000012528 membrane Substances 0.000 claims description 2
- 108060006633 protein kinase Proteins 0.000 claims description 2
- 102000010907 Cyclooxygenase 2 Human genes 0.000 claims 2
- 241001467055 Caviid betaherpesvirus 2 Species 0.000 claims 1
- 101100147232 Homo sapiens RPS3 gene Proteins 0.000 claims 1
- 239000003814 drug Substances 0.000 claims 1
- 239000000203 mixture Substances 0.000 claims 1
- 239000008194 pharmaceutical composition Substances 0.000 claims 1
- 108010000605 Ribosomal Proteins Proteins 0.000 abstract description 23
- 230000035897 transcription Effects 0.000 abstract description 19
- 238000013518 transcription Methods 0.000 abstract description 19
- 230000002068 genetic effect Effects 0.000 abstract description 4
- 108091026898 Leader sequence (mRNA) Proteins 0.000 abstract description 2
- 108020004414 DNA Proteins 0.000 description 17
- 108010077544 Chromatin Proteins 0.000 description 16
- 210000003483 chromatin Anatomy 0.000 description 16
- 238000011144 upstream manufacturing Methods 0.000 description 13
- CTMZLDSMFCVUNX-VMIOUTBZSA-N cytidylyl-(3'->5')-guanosine Chemical class O=C1N=C(N)C=CN1[C@H]1[C@H](O)[C@H](OP(O)(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C3=C(C(N=C(N)N3)=O)N=C2)O)[C@@H](CO)O1 CTMZLDSMFCVUNX-VMIOUTBZSA-N 0.000 description 11
- 102000002278 Ribosomal Proteins Human genes 0.000 description 9
- 108010048367 enhanced green fluorescent protein Proteins 0.000 description 9
- 239000013612 plasmid Substances 0.000 description 9
- 230000001105 regulatory effect Effects 0.000 description 9
- 238000001890 transfection Methods 0.000 description 9
- 108700019146 Transgenes Proteins 0.000 description 8
- 230000006870 function Effects 0.000 description 8
- 101150042484 rps11 gene Proteins 0.000 description 8
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 7
- 102100033409 40S ribosomal protein S3 Human genes 0.000 description 7
- 101000656561 Homo sapiens 40S ribosomal protein S3 Proteins 0.000 description 7
- 241000699666 Mus <mouse, genus> Species 0.000 description 7
- 108090000848 Ubiquitin Proteins 0.000 description 7
- 102000044159 Ubiquitin Human genes 0.000 description 7
- 108700009124 Transcription Initiation Site Proteins 0.000 description 6
- 239000003623 enhancer Substances 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 108700008625 Reporter Genes Proteins 0.000 description 5
- 102000006467 TATA-Box Binding Protein Human genes 0.000 description 5
- 108010044281 TATA-Box Binding Protein Proteins 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 230000000977 initiatory effect Effects 0.000 description 5
- 230000001225 therapeutic effect Effects 0.000 description 5
- 102100026726 40S ribosomal protein S11 Human genes 0.000 description 4
- 101001119215 Homo sapiens 40S ribosomal protein S11 Proteins 0.000 description 4
- 238000012408 PCR amplification Methods 0.000 description 4
- 101100362214 Schizosaccharomyces pombe (strain 972 / ATCC 24843) rps1101 gene Proteins 0.000 description 4
- 108700026226 TATA Box Proteins 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 238000010208 microarray analysis Methods 0.000 description 4
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 4
- 101150039612 rpsK gene Proteins 0.000 description 4
- 108091026890 Coding region Proteins 0.000 description 3
- 108090000626 DNA-directed RNA polymerases Proteins 0.000 description 3
- 102000004163 DNA-directed RNA polymerases Human genes 0.000 description 3
- 108010034791 Heterochromatin Proteins 0.000 description 3
- 108091034117 Oligonucleotide Proteins 0.000 description 3
- 108020004511 Recombinant DNA Proteins 0.000 description 3
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 3
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 3
- 101000849522 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 40S ribosomal protein S13 Proteins 0.000 description 3
- 102000040945 Transcription factor Human genes 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- 230000006978 adaptation Effects 0.000 description 3
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 3
- 230000010354 integration Effects 0.000 description 3
- 210000004962 mammalian cell Anatomy 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 238000002493 microarray Methods 0.000 description 3
- 210000003705 ribosome Anatomy 0.000 description 3
- 101150018028 rpsC gene Proteins 0.000 description 3
- 230000005026 transcription initiation Effects 0.000 description 3
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- 102100037563 40S ribosomal protein S2 Human genes 0.000 description 2
- LRSASMSXMSNRBT-UHFFFAOYSA-N 5-methylcytosine Chemical compound CC1=CNC(=O)N=C1N LRSASMSXMSNRBT-UHFFFAOYSA-N 0.000 description 2
- FVFVNNKYKYZTJU-UHFFFAOYSA-N 6-chloro-1,3,5-triazine-2,4-diamine Chemical compound NC1=NC(N)=NC(Cl)=N1 FVFVNNKYKYZTJU-UHFFFAOYSA-N 0.000 description 2
- 108091029430 CpG site Proteins 0.000 description 2
- 241000699800 Cricetinae Species 0.000 description 2
- 102000007260 Deoxyribonuclease I Human genes 0.000 description 2
- 108010008532 Deoxyribonuclease I Proteins 0.000 description 2
- 108700039887 Essential Genes Proteins 0.000 description 2
- 206010020751 Hypersensitivity Diseases 0.000 description 2
- 108020004684 Internal Ribosome Entry Sites Proteins 0.000 description 2
- 102000007530 Neurofibromin 1 Human genes 0.000 description 2
- 108010085793 Neurofibromin 1 Proteins 0.000 description 2
- 102100038280 Prostaglandin G/H synthase 2 Human genes 0.000 description 2
- 108091081021 Sense strand Proteins 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 2
- 230000000692 anti-sense effect Effects 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 210000004458 heterochromatin Anatomy 0.000 description 2
- 230000009610 hypersensitivity Effects 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 230000011987 methylation Effects 0.000 description 2
- 238000007069 methylation reaction Methods 0.000 description 2
- 229950010131 puromycin Drugs 0.000 description 2
- 238000007634 remodeling Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 230000014616 translation Effects 0.000 description 2
- 102100026744 40S ribosomal protein S10 Human genes 0.000 description 1
- 102100023912 40S ribosomal protein S12 Human genes 0.000 description 1
- 102100026357 40S ribosomal protein S13 Human genes 0.000 description 1
- 102100023216 40S ribosomal protein S15 Human genes 0.000 description 1
- 102100024113 40S ribosomal protein S15a Human genes 0.000 description 1
- 102100031571 40S ribosomal protein S16 Human genes 0.000 description 1
- 102100039882 40S ribosomal protein S17 Human genes 0.000 description 1
- 102100039980 40S ribosomal protein S18 Human genes 0.000 description 1
- 102100033051 40S ribosomal protein S19 Human genes 0.000 description 1
- 102100023415 40S ribosomal protein S20 Human genes 0.000 description 1
- 102100037710 40S ribosomal protein S21 Human genes 0.000 description 1
- 102100037513 40S ribosomal protein S23 Human genes 0.000 description 1
- 102100033449 40S ribosomal protein S24 Human genes 0.000 description 1
- 102100022721 40S ribosomal protein S25 Human genes 0.000 description 1
- 102100027337 40S ribosomal protein S26 Human genes 0.000 description 1
- 102100022681 40S ribosomal protein S27 Human genes 0.000 description 1
- 102100023679 40S ribosomal protein S28 Human genes 0.000 description 1
- 102100031928 40S ribosomal protein S29 Human genes 0.000 description 1
- 102100022600 40S ribosomal protein S3a Human genes 0.000 description 1
- 102100023779 40S ribosomal protein S5 Human genes 0.000 description 1
- 102100033714 40S ribosomal protein S6 Human genes 0.000 description 1
- 102100024088 40S ribosomal protein S7 Human genes 0.000 description 1
- 102100037663 40S ribosomal protein S8 Human genes 0.000 description 1
- 102100033731 40S ribosomal protein S9 Human genes 0.000 description 1
- 102100027271 40S ribosomal protein SA Human genes 0.000 description 1
- 102100040881 60S acidic ribosomal protein P0 Human genes 0.000 description 1
- 102100033416 60S acidic ribosomal protein P1 Human genes 0.000 description 1
- 102100026112 60S acidic ribosomal protein P2 Human genes 0.000 description 1
- 102100021546 60S ribosomal protein L10 Human genes 0.000 description 1
- 102100022406 60S ribosomal protein L10a Human genes 0.000 description 1
- 102100035916 60S ribosomal protein L11 Human genes 0.000 description 1
- 102100025643 60S ribosomal protein L12 Human genes 0.000 description 1
- 102100023990 60S ribosomal protein L17 Human genes 0.000 description 1
- 102100032411 60S ribosomal protein L18 Human genes 0.000 description 1
- 102100021690 60S ribosomal protein L18a Human genes 0.000 description 1
- 102100021206 60S ribosomal protein L19 Human genes 0.000 description 1
- 102100037965 60S ribosomal protein L21 Human genes 0.000 description 1
- 102100037685 60S ribosomal protein L22 Human genes 0.000 description 1
- 102100021308 60S ribosomal protein L23 Human genes 0.000 description 1
- 102100035322 60S ribosomal protein L24 Human genes 0.000 description 1
- 102100028348 60S ribosomal protein L26 Human genes 0.000 description 1
- 102100025601 60S ribosomal protein L27 Human genes 0.000 description 1
- 102100021660 60S ribosomal protein L28 Human genes 0.000 description 1
- 102100021671 60S ribosomal protein L29 Human genes 0.000 description 1
- 102100040540 60S ribosomal protein L3 Human genes 0.000 description 1
- 102100038237 60S ribosomal protein L30 Human genes 0.000 description 1
- 102100023777 60S ribosomal protein L31 Human genes 0.000 description 1
- 102100040768 60S ribosomal protein L32 Human genes 0.000 description 1
- 102100040637 60S ribosomal protein L34 Human genes 0.000 description 1
- 102100036116 60S ribosomal protein L35 Human genes 0.000 description 1
- 102100022276 60S ribosomal protein L35a Human genes 0.000 description 1
- 102100022048 60S ribosomal protein L36 Human genes 0.000 description 1
- 102100031002 60S ribosomal protein L36a Human genes 0.000 description 1
- 102100040131 60S ribosomal protein L37 Human genes 0.000 description 1
- 102100036126 60S ribosomal protein L37a Human genes 0.000 description 1
- 102100030982 60S ribosomal protein L38 Human genes 0.000 description 1
- 102100035988 60S ribosomal protein L39 Human genes 0.000 description 1
- 102100026926 60S ribosomal protein L4 Human genes 0.000 description 1
- 102100040623 60S ribosomal protein L41 Human genes 0.000 description 1
- 102100026750 60S ribosomal protein L5 Human genes 0.000 description 1
- 102100040924 60S ribosomal protein L6 Human genes 0.000 description 1
- 102100035841 60S ribosomal protein L7 Human genes 0.000 description 1
- 102100036630 60S ribosomal protein L7a Human genes 0.000 description 1
- 102100035931 60S ribosomal protein L8 Human genes 0.000 description 1
- 102100041029 60S ribosomal protein L9 Human genes 0.000 description 1
- 240000006108 Allium ampeloprasum Species 0.000 description 1
- 108020005544 Antisense RNA Proteins 0.000 description 1
- 101100472041 Arabidopsis thaliana RPL8A gene Proteins 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 241000700199 Cavia porcellus Species 0.000 description 1
- 102100032902 Chromobox protein homolog 3 Human genes 0.000 description 1
- 206010010099 Combined immunodeficiency Diseases 0.000 description 1
- 206010053138 Congenital aplastic anaemia Diseases 0.000 description 1
- 108091035707 Consensus sequence Proteins 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- 230000004544 DNA amplification Effects 0.000 description 1
- 230000006429 DNA hypomethylation Effects 0.000 description 1
- 241000450599 DNA viruses Species 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 102100036912 Desmin Human genes 0.000 description 1
- 108010044052 Desmin Proteins 0.000 description 1
- 102100024746 Dihydrofolate reductase Human genes 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- 102100034003 FAU ubiquitin-like and ribosomal protein S30 Human genes 0.000 description 1
- 201000004939 Fanconi anemia Diseases 0.000 description 1
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 1
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 1
- 102100021519 Hemoglobin subunit beta Human genes 0.000 description 1
- 108091005904 Hemoglobin subunit beta Proteins 0.000 description 1
- 208000031220 Hemophilia Diseases 0.000 description 1
- 208000009292 Hemophilia A Diseases 0.000 description 1
- 102100035616 Heterogeneous nuclear ribonucleoproteins A2/B1 Human genes 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 108010033040 Histones Proteins 0.000 description 1
- 108010025076 Holoenzymes Proteins 0.000 description 1
- 101000639726 Homo sapiens 28S ribosomal protein S12, mitochondrial Proteins 0.000 description 1
- 101001119189 Homo sapiens 40S ribosomal protein S10 Proteins 0.000 description 1
- 101000682687 Homo sapiens 40S ribosomal protein S12 Proteins 0.000 description 1
- 101000718313 Homo sapiens 40S ribosomal protein S13 Proteins 0.000 description 1
- 101000623543 Homo sapiens 40S ribosomal protein S15 Proteins 0.000 description 1
- 101001118566 Homo sapiens 40S ribosomal protein S15a Proteins 0.000 description 1
- 101000706746 Homo sapiens 40S ribosomal protein S16 Proteins 0.000 description 1
- 101000812077 Homo sapiens 40S ribosomal protein S17 Proteins 0.000 description 1
- 101000811259 Homo sapiens 40S ribosomal protein S18 Proteins 0.000 description 1
- 101000733040 Homo sapiens 40S ribosomal protein S19 Proteins 0.000 description 1
- 101001098029 Homo sapiens 40S ribosomal protein S2 Proteins 0.000 description 1
- 101001114932 Homo sapiens 40S ribosomal protein S20 Proteins 0.000 description 1
- 101001097814 Homo sapiens 40S ribosomal protein S21 Proteins 0.000 description 1
- 101001097953 Homo sapiens 40S ribosomal protein S23 Proteins 0.000 description 1
- 101000656669 Homo sapiens 40S ribosomal protein S24 Proteins 0.000 description 1
- 101000678929 Homo sapiens 40S ribosomal protein S25 Proteins 0.000 description 1
- 101000862491 Homo sapiens 40S ribosomal protein S26 Proteins 0.000 description 1
- 101000678466 Homo sapiens 40S ribosomal protein S27 Proteins 0.000 description 1
- 101000623076 Homo sapiens 40S ribosomal protein S28 Proteins 0.000 description 1
- 101000704060 Homo sapiens 40S ribosomal protein S29 Proteins 0.000 description 1
- 101000679249 Homo sapiens 40S ribosomal protein S3a Proteins 0.000 description 1
- 101000732165 Homo sapiens 40S ribosomal protein S4, X isoform Proteins 0.000 description 1
- 101000622644 Homo sapiens 40S ribosomal protein S5 Proteins 0.000 description 1
- 101000656896 Homo sapiens 40S ribosomal protein S6 Proteins 0.000 description 1
- 101000690200 Homo sapiens 40S ribosomal protein S7 Proteins 0.000 description 1
- 101001097439 Homo sapiens 40S ribosomal protein S8 Proteins 0.000 description 1
- 101000657066 Homo sapiens 40S ribosomal protein S9 Proteins 0.000 description 1
- 101000694288 Homo sapiens 40S ribosomal protein SA Proteins 0.000 description 1
- 101000673456 Homo sapiens 60S acidic ribosomal protein P0 Proteins 0.000 description 1
- 101000712357 Homo sapiens 60S acidic ribosomal protein P1 Proteins 0.000 description 1
- 101000691878 Homo sapiens 60S acidic ribosomal protein P2 Proteins 0.000 description 1
- 101001108634 Homo sapiens 60S ribosomal protein L10 Proteins 0.000 description 1
- 101000755323 Homo sapiens 60S ribosomal protein L10a Proteins 0.000 description 1
- 101001073740 Homo sapiens 60S ribosomal protein L11 Proteins 0.000 description 1
- 101000575173 Homo sapiens 60S ribosomal protein L12 Proteins 0.000 description 1
- 101001117935 Homo sapiens 60S ribosomal protein L15 Proteins 0.000 description 1
- 101000682512 Homo sapiens 60S ribosomal protein L17 Proteins 0.000 description 1
- 101001087985 Homo sapiens 60S ribosomal protein L18 Proteins 0.000 description 1
- 101000752293 Homo sapiens 60S ribosomal protein L18a Proteins 0.000 description 1
- 101001105789 Homo sapiens 60S ribosomal protein L19 Proteins 0.000 description 1
- 101000661708 Homo sapiens 60S ribosomal protein L21 Proteins 0.000 description 1
- 101001097555 Homo sapiens 60S ribosomal protein L22 Proteins 0.000 description 1
- 101000675833 Homo sapiens 60S ribosomal protein L23 Proteins 0.000 description 1
- 101000660926 Homo sapiens 60S ribosomal protein L24 Proteins 0.000 description 1
- 101001080179 Homo sapiens 60S ribosomal protein L26 Proteins 0.000 description 1
- 101000719728 Homo sapiens 60S ribosomal protein L27 Proteins 0.000 description 1
- 101000676271 Homo sapiens 60S ribosomal protein L28 Proteins 0.000 description 1
- 101000676246 Homo sapiens 60S ribosomal protein L29 Proteins 0.000 description 1
- 101000673985 Homo sapiens 60S ribosomal protein L3 Proteins 0.000 description 1
- 101001101319 Homo sapiens 60S ribosomal protein L30 Proteins 0.000 description 1
- 101001113162 Homo sapiens 60S ribosomal protein L31 Proteins 0.000 description 1
- 101000672453 Homo sapiens 60S ribosomal protein L32 Proteins 0.000 description 1
- 101000672659 Homo sapiens 60S ribosomal protein L34 Proteins 0.000 description 1
- 101000715818 Homo sapiens 60S ribosomal protein L35 Proteins 0.000 description 1
- 101001110988 Homo sapiens 60S ribosomal protein L35a Proteins 0.000 description 1
- 101001110263 Homo sapiens 60S ribosomal protein L36 Proteins 0.000 description 1
- 101001127203 Homo sapiens 60S ribosomal protein L36a Proteins 0.000 description 1
- 101001127258 Homo sapiens 60S ribosomal protein L36a-like Proteins 0.000 description 1
- 101000671735 Homo sapiens 60S ribosomal protein L37 Proteins 0.000 description 1
- 101001092424 Homo sapiens 60S ribosomal protein L37a Proteins 0.000 description 1
- 101001127039 Homo sapiens 60S ribosomal protein L38 Proteins 0.000 description 1
- 101000716179 Homo sapiens 60S ribosomal protein L39 Proteins 0.000 description 1
- 101000691203 Homo sapiens 60S ribosomal protein L4 Proteins 0.000 description 1
- 101000674326 Homo sapiens 60S ribosomal protein L41 Proteins 0.000 description 1
- 101000691083 Homo sapiens 60S ribosomal protein L5 Proteins 0.000 description 1
- 101000673524 Homo sapiens 60S ribosomal protein L6 Proteins 0.000 description 1
- 101000853617 Homo sapiens 60S ribosomal protein L7 Proteins 0.000 description 1
- 101000853243 Homo sapiens 60S ribosomal protein L7a Proteins 0.000 description 1
- 101000853659 Homo sapiens 60S ribosomal protein L8 Proteins 0.000 description 1
- 101000672886 Homo sapiens 60S ribosomal protein L9 Proteins 0.000 description 1
- 101000797578 Homo sapiens Chromobox protein homolog 3 Proteins 0.000 description 1
- 101000732045 Homo sapiens FAU ubiquitin-like and ribosomal protein S30 Proteins 0.000 description 1
- 101000854026 Homo sapiens Heterogeneous nuclear ribonucleoproteins A2/B1 Proteins 0.000 description 1
- 101000973510 Homo sapiens Melanoma-derived growth regulatory protein Proteins 0.000 description 1
- 101000986595 Homo sapiens Ornithine transcarbamylase, mitochondrial Proteins 0.000 description 1
- 101000711369 Homo sapiens Probable ribosome biogenesis protein RLP24 Proteins 0.000 description 1
- 101000934346 Homo sapiens T-cell surface antigen CD2 Proteins 0.000 description 1
- 101001115218 Homo sapiens Ubiquitin-40S ribosomal protein S27a Proteins 0.000 description 1
- 241000701024 Human betaherpesvirus 5 Species 0.000 description 1
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 1
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 1
- 108010090227 Immunoglobulin kappa-Chains Proteins 0.000 description 1
- 108010004020 Immunoglobulin lambda-Chains Proteins 0.000 description 1
- 108010002386 Interleukin-3 Proteins 0.000 description 1
- 102000000646 Interleukin-3 Human genes 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- 102000011782 Keratins Human genes 0.000 description 1
- 108010076876 Keratins Proteins 0.000 description 1
- 241000713666 Lentivirus Species 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 108060004795 Methyltransferase Proteins 0.000 description 1
- 102000016397 Methyltransferase Human genes 0.000 description 1
- 108010085220 Multiprotein Complexes Proteins 0.000 description 1
- 102000007474 Multiprotein Complexes Human genes 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- 102000016349 Myosin Light Chains Human genes 0.000 description 1
- 108010067385 Myosin Light Chains Proteins 0.000 description 1
- 241000244206 Nematoda Species 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 208000000599 Ornithine Carbamoyltransferase Deficiency Disease Diseases 0.000 description 1
- 206010052450 Ornithine transcarbamoylase deficiency Diseases 0.000 description 1
- 208000035903 Ornithine transcarbamylase deficiency Diseases 0.000 description 1
- 102100028200 Ornithine transcarbamylase, mitochondrial Human genes 0.000 description 1
- 206010031243 Osteogenesis imperfecta Diseases 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 201000011252 Phenylketonuria Diseases 0.000 description 1
- 108010068086 Polyubiquitin Proteins 0.000 description 1
- 108020004412 RNA 3' Polyadenylation Signals Proteins 0.000 description 1
- 238000010802 RNA extraction kit Methods 0.000 description 1
- -1 RPL13APL Proteins 0.000 description 1
- 102000006382 Ribonucleases Human genes 0.000 description 1
- 108010083644 Ribonucleases Proteins 0.000 description 1
- 102000004389 Ribonucleoproteins Human genes 0.000 description 1
- 108010081734 Ribonucleoproteins Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 101100527654 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) RPL4A gene Proteins 0.000 description 1
- 101100527652 Schizosaccharomyces pombe (strain 972 / ATCC 24843) rpl402 gene Proteins 0.000 description 1
- 108091081024 Start codon Proteins 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 102100025237 T-cell surface antigen CD2 Human genes 0.000 description 1
- 108010006785 Taq Polymerase Proteins 0.000 description 1
- 208000002903 Thalassemia Diseases 0.000 description 1
- 102000006290 Transcription Factor TFIID Human genes 0.000 description 1
- 108010083268 Transcription Factor TFIID Proteins 0.000 description 1
- 102100030246 Transcription factor Sp1 Human genes 0.000 description 1
- 101710085924 Transcription factor Sp1 Proteins 0.000 description 1
- 108700029229 Transcriptional Regulatory Elements Proteins 0.000 description 1
- 101710195626 Transcriptional activator protein Proteins 0.000 description 1
- 102100023341 Ubiquitin-40S ribosomal protein S27a Human genes 0.000 description 1
- 241000700618 Vaccinia virus Species 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 208000006682 alpha 1-Antitrypsin Deficiency Diseases 0.000 description 1
- 150000001413 amino acids Chemical group 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000002457 bidirectional effect Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000007960 cellular response to stress Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 239000003184 complementary RNA Substances 0.000 description 1
- 239000000306 component Substances 0.000 description 1
- 150000001875 compounds Chemical group 0.000 description 1
- 108091036078 conserved sequence Proteins 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 239000002254 cytotoxic agent Substances 0.000 description 1
- 231100000599 cytotoxic agent Toxicity 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 210000005045 desmin Anatomy 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 108020001096 dihydrofolate reductase Proteins 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- 108091006047 fluorescent proteins Proteins 0.000 description 1
- 102000034287 fluorescent proteins Human genes 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 238000001476 gene delivery Methods 0.000 description 1
- 230000030279 gene silencing Effects 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 102000005396 glutamine synthetase Human genes 0.000 description 1
- 108020002326 glutamine synthetase Proteins 0.000 description 1
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 102000048342 human MIA Human genes 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 101150112128 mrpl2 gene Proteins 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 108091027963 non-coding RNA Proteins 0.000 description 1
- 102000042567 non-coding RNA Human genes 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 201000011278 ornithine carbamoyltransferase deficiency Diseases 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 235000020030 perry Nutrition 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 238000001243 protein synthesis Methods 0.000 description 1
- 230000017854 proteolysis Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000022983 regulation of cell cycle Effects 0.000 description 1
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 description 1
- 230000003362 replicative effect Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 108020004418 ribosomal RNA Proteins 0.000 description 1
- 108090000850 ribosomal protein S14 Proteins 0.000 description 1
- 102000004314 ribosomal protein S14 Human genes 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 101150003660 rpl2 gene Proteins 0.000 description 1
- 101150027142 rpl8 gene Proteins 0.000 description 1
- 101150015255 rplB gene Proteins 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000000126 substance Chemical group 0.000 description 1
- 230000001502 supplementing effect Effects 0.000 description 1
- 101150056532 terf2ip gene Proteins 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 230000005030 transcription termination Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- 230000014621 translational initiation Effects 0.000 description 1
- 241000701161 unidentified adenovirus Species 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/46—Vector systems having a special element relevant for transcription elements influencing chromatin structure, e.g. scaffold/matrix attachment region, methylation free island
Landscapes
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Medicinal Chemistry (AREA)
- Toxicology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
Description
本発明は、作動可能に連結された転写ユニットに対して改良された発現を与えるエレメントを含むポリヌクレオチドに関する。これらのエレメントは、リボソームタンパク質遺伝子のプロモーター領域と自然に連結され、そして組み換えDNA構築物において、高く、かつ再現性あるレベルの遺伝子発現を与える。本発明はまた、細胞培養およびその他の生物工学適用における組み換えタンパク質の産生のための、このようなポリヌクレオチド配列を含むベクター、このようなベクターを含む宿主細胞、およびこのようなポリヌクレオチド、ベクターまたは宿主細胞の治療における使用に関する。
本明細書の説明および請求項全体で、用語「包含する(comprise)」および「含む(contain)」およびこれら用語の改変例、例えば、「包含している(comprising)」および「包含する(comprises)」は、「制限されずに含むこと」を意味し、そしてその他の成分、添加物、構成要素、完全体または工程を排除することは意図されない(そしてされない)。
本明細書で用いられるとき、プロモーター領域は、プロモーター、および転写開始部位の5’配列の上流の5kbおよび最初のエキソンの遠位端の下流の500bp3’配列と一緒の転写開始部位であるとして規定される。
a)リボソームタンパク質遺伝子のプロモーター領域からの少なくとも500の連続するヌクレオチドを含むエレメント、
b)異質プロモーター、
c)この異質プロモーターに隣接する転写可能な核酸配列を含む、単離されたポリヌクレオチドを提供し、
ここで、上記転写可能な核酸配列は、上記異質プロモーターから転写され、そしてこの転写のレベルが上記エレメントによって増大される。好ましくは、上記エレメントは、1kbを超え、そして最も好ましくは3kbを超えるリボソームタンパク質遺伝子の5’非翻訳配列を含む。
a)リボソームタンパク質遺伝子のプロモーター領域からの少なくとも500の連続するヌクレオチドを含むエレメント、
b)異質プロモーター、
c)複数クローニング部位、を含み、
ここで、上記複数クローニング部位中に挿入された転写可能な核酸が、上記異質プロモーターから転写され得、そしてこの転写のレベルは上記エレメントによって増大される。
(材料および方法)
(マイクロアレイ分析)
総RNAを、RNeasyRNA抽出キット(Qiagen、Crawley、UK)を用い、製造業者のプロトコールに従って、約80%集密のCHO−K1細胞から抽出した。総RNA(2μg/μl)を、13,443の公知の転写物を提示するマウス70マーオリゴヌクレオチドライブラリー(オペロンV.1)を用いるマイクロアレイ発現分析に供した。Cincinnati大学、Genomics and Microarray Laboratoryが、参照プロトコール(http://microarray.uc.edu)に従って、マイクロアレイ分析を請け負った。
PCRオリゴヌクレオチドは、完全なCpGアイランドが包埋されたプロモーター領域を包含し、その一方、公知または推定されるコード配列構造に従って約500bpのコード配列を含む約3kbのフラグメントを増幅するように設計された(表2を参照のこと)。
プレミックスA−F(Cambio、UK)、1ユニットのTaq DNAポリメラーゼ(Promega、UK)および200ngのテンプレートDNAを用いた達成された。初期変性は96℃で2分間であり、その一方PCR増幅は、35サイクル(94℃1分間、55〜60℃1分間、72℃5分間実施された。)最終伸長ステップ(72℃10分間)が含められた。
コントロール発現ベクター(CET1005EGFP、配列番号20と指定される)を、pEGFP−N1からのhCMV/EGFP/sv40pA(NheI/AgeI欠失複数クローニング部位)のCET900中への挿入により、次いで、このベクターからのAscIカセットのCET1005のAscI部位中への挿入により構築した。
CHO−K1細胞を、HAMS F12(Invitrogen、UK)プラス4500mg/l L−アナニル−L−グルタミン、10μg/mlの各々ペニシリンおよびストレプトマイシン、および10%(v/v)熱不活性化ウシ胎児血清(FCS;Invitrogen、Paisley、UK)中で増殖した。トランスフェクションは、80%の集密培養からの約107細胞、および250Vで975μFの単一パルスを送達するためのBioRad Gene PulserIITMセットを用いるエレクトロポーレーションによって実施した。トランスフェクションは、2μgの線状化CET1005EGFPプラスミド、および異なるサイズの発現ベクターに対して当モル量を用いた。安定にトランスフェクションされた細胞を選択し、そして12.5μ/mlの硫酸ピューロマイシン(Sigma、UK)を含む増殖培地中に維持した。
EGFPレポーター構築物でトランスフェクトされた細胞の分析は、Becton−Dickinson FACScanで、親CHO−K1細胞株をバックグラウンドの自動蛍光コントロールとして用いた。
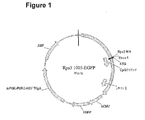
配列番号1は、RPS3クローン化配列(ヌクレオチド38〜3154)を示し;配列番号17は、pRPS3−1005−EGFPの完全プラスミド配列を示し;配列番号18は、pCET1015−EGFPの完全プラスミド配列を示す。
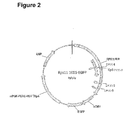
配列番号2は、RPS11のクローン化された配列(ヌクレオチド12〜3032)を示し;配列番号19は、pRPS11−1005−EGFPの完全配列を示す。
Claims (23)
- 単離されたポリヌクレオチドであって、
a)哺乳動物rps3遺伝子のプロモーター領域からの3000より多い連続するヌクレオチドを含む拡大されたメチル化のないCpGアイランド、
b)異種プロモーター、
c)該異種プロモーターに隣接する転写可能な核酸配列を含み、
ここで、該転写可能な核酸配列の該異種プロモーターからの転写が、該拡大されたメチル化のないCpGアイランドの存在下で、該拡大されたメチル化のないCpGアイランドの不存在下に比べて増大される、ポリヌクレオチド。 - 前記拡大されたメチル化のないCpGアイランドが、前記哺乳動物rps3遺伝子の1つ以上のエキソンをさらに含む、請求項1に記載のポリヌクレオチド。
- 前記哺乳動物rps3遺伝子はヒトrps3遺伝子である、請求項1に記載のポリヌクレオチド。
- 前記哺乳動物rps3遺伝子はげっ歯類rps3遺伝子である、請求項1に記載のポリヌクレオチド。
- 前記げっ歯類rps3遺伝子はマウスのrps遺伝子である、請求項4に記載のポリヌクレオチド。
- 配列番号1のヌクレオチド配列を含む、請求項5に記載のポリヌクレオチド。
- 前記異種プロモーターが構成的プロモーターである、請求項1に記載のポリヌクレオチド。
- 前記構成的プロモーターが、サイトメガロウイルス初期/即時プロモーター、SV40、EF−1α、ラウスザルコーマウイルス(RSV)LTRおよびHIV2 LTRからなるリストから選択される、請求項7に記載のポリヌクレオチド。
- 前記構成的プロモーターが、サイトメガロウイルス初期/即時プロモーターである、請求項8に記載のポリヌクレオチド。
- 前記構成的プロモーターが、モルモットサイトメガロウイルス初期/即時プロモーターである、請求項9に記載のポリヌクレオチド。
- 前記構成的プロモーターが、マウスサイトメガロウイルス初期/即時プロモーターである、請求項9に記載のポリヌクレオチド。
- 前記異種プロモーターが、組織特異的プロモーターである、請求項1に記載のポリヌクレオチド。
- 前記異種プロモーターが、腫瘍特異的プロモーターである、請求項12に記載のポリヌクレオチド。
- 前記プロモーターが、癌胎児抗原(CEA)、前立腺特異的抗原(PSA)、シクロオキシゲナーゼ−2(COX−2)、α−フェトプロテイン(AFP)、チロシナーゼ、およびT細胞因子1−4(TCF)を基礎にしたプロモーターからなるリストから選択される、請求項13に記載のポリヌクレオチド。
- 前記転写可能な核酸が、抗体、抗体の機能的エピトープ結合性フラグメント、成長因子、サイトカイン、プロテインキナーゼ、可溶性レセプター、膜結合レセプター、血液凝固因子などから選択されるポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 請求項1〜15のいずれか1項に記載のポリヌクレオチドを含むベクター。
- 請求項16に記載の真核生物発現ベクター。
- 真核生物発現ベクターであって、
a)哺乳動物rps3遺伝子のプロモーター領域からの3000より多い連続するヌクレオチドを含む拡大されたメチル化のないCpGアイランド、
b)異種プロモーター、
c)複数クローニング部位、を含み、
ここで、該複数クローニング部位中に挿入された転写可能な核酸が、該異種プロモーターから転写され得、そして該転写のレベルが該拡大されたメチル化のないCpGアイランドによって増大される、ベクター。 - 請求項1〜15のいずれか1項に記載の単離されたポリヌクレオチド、または請求項16、17または18に記載のベクターを含む、宿主細胞。
- 前記細胞が、CHO、NSO、BHK、HeLa、HepG2からなるリストから選択される、請求項19に記載の宿主細胞。
- 転写可能な核酸によってコードされるポリペプチドを発現する方法であって、該方法は、請求項16〜18のいずれかに記載の発現ベクターを適切な宿主細胞に挿入する工程、および該宿主細胞を該ポリペプチドの発現を可能にするに適切な条件で培養する工程、を包含する、方法。
- 請求項1〜15のいずれか1項に記載のポリヌクレオチド、請求項16〜18のいずれか1項に記載のベクター、または請求項19もしくは請求項20のいずれか1項に記載の宿主細胞、および薬学的に受容可能なキャリアを含む、薬学的組成物。
- 請求項1〜15のいずれか1項に記載のポリヌクレオチド、請求項16〜18のいずれか1項に記載のベクター、または請求項19もしくは請求項20のいずれか1項に記載の宿主細胞を含む、医薬として使用するための組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0509965.0A GB0509965D0 (en) | 2005-05-17 | 2005-05-17 | Improved expression elements |
| GB0509965.0 | 2005-05-17 | ||
| US68227705P | 2005-05-18 | 2005-05-18 | |
| US60/682,277 | 2005-05-18 | ||
| PCT/GB2006/001656 WO2006123097A2 (en) | 2005-05-17 | 2006-05-09 | Improved expression elements |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008539781A JP2008539781A (ja) | 2008-11-20 |
| JP5080452B2 true JP5080452B2 (ja) | 2012-11-21 |
Family
ID=34708242
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008511772A Active JP5080452B2 (ja) | 2005-05-17 | 2006-05-09 | 改良された発現エレメント |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US7632661B2 (ja) |
| EP (2) | EP2295589A1 (ja) |
| JP (1) | JP5080452B2 (ja) |
| CN (1) | CN101208435B (ja) |
| AT (1) | ATE494381T1 (ja) |
| DE (1) | DE602006019422D1 (ja) |
| ES (1) | ES2358680T3 (ja) |
| GB (1) | GB0509965D0 (ja) |
| WO (1) | WO2006123097A2 (ja) |
Families Citing this family (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HUE036449T2 (hu) | 2003-06-24 | 2018-07-30 | Genzyme Corp | Új béta-aktin és RPS21 promóterek és alkalmazásaik |
| WO2008044869A1 (en) * | 2006-10-10 | 2008-04-17 | Viromed Co., Ltd. | Expression vectors with improved safety |
| US20090142805A1 (en) * | 2007-01-08 | 2009-06-04 | Millipore Corporation | High expression cell line that eliminates gene amplification |
| WO2009155950A1 (en) | 2008-06-27 | 2009-12-30 | King Faisal Specialist Hospital And Research Centre | Cloning-free method of generating transcriptionally and post-transcriptionally controllable expression active linear reporter constructs |
| US20110190156A1 (en) * | 2008-07-15 | 2011-08-04 | Trustees Of Dartmouth College | Molecular signatures for diagnosing scleroderma |
| WO2010111653A2 (en) * | 2009-03-27 | 2010-09-30 | The Uab Research Foundation | Modulating ires-mediated translation |
| WO2010147464A1 (en) | 2009-06-15 | 2010-12-23 | Cellagenics B.V. | Use of a cysteine synthesizing enzyme as selectable marker |
| WO2012019630A1 (en) | 2010-08-13 | 2012-02-16 | Curevac Gmbh | Nucleic acid comprising or coding for a histone stem-loop and a poly(a) sequence or a polyadenylation signal for increasing the expression of an encoded protein |
| CN103180443B (zh) * | 2010-09-01 | 2016-01-13 | 萨拉基尼克有限公司 | 用于增强基因表达的来自核糖体蛋白启动子的核酸片段 |
| JP6025745B2 (ja) | 2011-11-28 | 2016-11-16 | 第一三共株式会社 | ヒト遺伝子由来プロモーター |
| WO2013120499A1 (en) | 2012-02-15 | 2013-08-22 | Curevac Gmbh | Nucleic acid comprising or coding for a histone stem-loop and a poly (a) sequence or a polyadenylation signal for increasing the expression of an encoded pathogenic antigen |
| DK3578659T3 (da) | 2012-03-27 | 2024-02-05 | CureVac SE | Kunstige nukelinsyremolekyler til forbedret protein- eller peptidekspression |
| US20150105433A1 (en) * | 2012-04-27 | 2015-04-16 | The Uab Research Foundation | TREATING VIRAL INFECTIONS HAVING VIRAL RNAs TRANSLATED BY A NON-IRES MEDIATED MECHANISM |
| MX372790B (es) * | 2013-12-30 | 2020-07-03 | CureVac SE | Moleculas artificiales de acido nucleico. |
| US11254951B2 (en) | 2014-12-30 | 2022-02-22 | Curevac Ag | Artificial nucleic acid molecules |
| EP3842537A1 (en) * | 2013-12-30 | 2021-06-30 | CureVac AG | Artificial nucleic acid molecules |
| ES2962385T3 (es) * | 2014-10-15 | 2024-03-18 | Amgen Inc | Elementos promotores y reguladores para mejorar la expresión de genes heterólogos en células hospederas |
| WO2017040738A1 (en) * | 2015-09-02 | 2017-03-09 | Regeneron Pharmaceuticals, Inc. | Rodent model of prostate cancer |
| WO2018206168A1 (en) * | 2017-05-11 | 2018-11-15 | Zentrum Für Forschungsförderung In Der Pädiatrie Gmbh | Concept for the treatment of monogenetic disorders |
| US20210317498A1 (en) | 2018-08-09 | 2021-10-14 | Daiichi Sankyo Company, Limited | PROMOTER of Hspa8 GENE |
| CN111249457A (zh) * | 2020-04-13 | 2020-06-09 | 吉林大学 | 核糖体蛋白sa抗体在免疫调节中的医用用途 |
| KR20250007570A (ko) | 2022-04-26 | 2025-01-14 | 다이이찌 산쿄 가부시키가이샤 | Eno1 유전자의 프로모터 |
| CN116064624A (zh) * | 2022-09-15 | 2023-05-05 | 思鹏生物科技(苏州)有限公司 | 利用rpl基因促进载体稳定表达的方法及其功能基因 |
| CN116064663A (zh) * | 2022-09-15 | 2023-05-05 | 思鹏生物科技(苏州)有限公司 | 利用rps基因促进载体稳定表达的方法及其功能基因 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5583009A (en) | 1992-12-08 | 1996-12-10 | University Of Washington | Method of preparing recombinant proteins in transgenic animals containing metallothionein gene elements that bestow tissue-independent copy number-dependent, position-indepedent gene expression |
| US5610053A (en) * | 1993-04-07 | 1997-03-11 | The United States Of America As Represented By The Department Of Health And Human Services | DNA sequence which acts as a chromatin insulator element to protect expressed genes from cis-acting regulatory sequences in mammalian cells |
| US6110666A (en) | 1994-06-09 | 2000-08-29 | Medical Research Council | Locus control subregions conferring integration-site independent transgene expression abstract of the disclosure |
| DE19539493A1 (de) * | 1995-10-24 | 1997-04-30 | Thomae Gmbh Dr K | Starker homologer Promotor aus Hamster |
| AU725474B2 (en) | 1996-08-16 | 2000-10-12 | Medical Research Council | Self-replicating episomal expression vectors conferring tissue-specific gene expression |
| ES2375266T3 (es) * | 1998-07-21 | 2012-02-28 | Millipore Corporation | Un polinucleótido que comprende un elemento de apertura de cromatina ubicuo (ucoe). |
| KR100795626B1 (ko) * | 1998-07-21 | 2008-01-17 | 코브라 바이오매뉴팩쳐링 피엘씨. | 도처에 있는 염색질 개방 요소(유씨오이)를 포함하는폴리뉴클레오티드 |
| GB0022995D0 (en) * | 2000-09-20 | 2000-11-01 | Cobra Therapeutics Ltd | Polynucleotide |
| CN1461343B (zh) | 2000-09-20 | 2012-10-31 | Emd密理博公司 | 多核苷酸 |
| EP2224010B1 (en) * | 2001-04-05 | 2012-06-20 | EMD Millipore Corporation | Improved gene expression |
| US7812148B2 (en) | 2001-04-05 | 2010-10-12 | Millipore Corporation | Vectors comprising CpG islands without position effect varigation and having increased expression |
| WO2002099089A1 (en) * | 2001-06-04 | 2002-12-12 | Corixa Corporation | Compositions and methods for high-level, large-scale production of recombinant proteins |
| EP1414948B1 (en) | 2001-07-10 | 2009-09-16 | Biogen Idec Inc. | Inhibition of apoptosis process and improvement of cell performance |
| US7384744B2 (en) * | 2002-11-29 | 2008-06-10 | Boehringer Ingelheim Pharma Gmbh & Co., Kg | Expression vector, methods for the production of heterologous gene products and for the selection of recombinant cells producing high levels of such products |
-
2005
- 2005-05-17 GB GBGB0509965.0A patent/GB0509965D0/en not_active Ceased
-
2006
- 2006-05-09 EP EP10177866A patent/EP2295589A1/en not_active Withdrawn
- 2006-05-09 ES ES06727026T patent/ES2358680T3/es active Active
- 2006-05-09 EP EP06727026A patent/EP1891223B1/en active Active
- 2006-05-09 AT AT06727026T patent/ATE494381T1/de not_active IP Right Cessation
- 2006-05-09 DE DE602006019422T patent/DE602006019422D1/de active Active
- 2006-05-09 JP JP2008511772A patent/JP5080452B2/ja active Active
- 2006-05-09 CN CN2006800173095A patent/CN101208435B/zh active Active
- 2006-05-09 WO PCT/GB2006/001656 patent/WO2006123097A2/en not_active Ceased
- 2006-05-17 US US11/435,930 patent/US7632661B2/en active Active
-
2009
- 2009-09-09 US US12/584,634 patent/US20100015107A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| DE602006019422D1 (de) | 2011-02-17 |
| CN101208435A (zh) | 2008-06-25 |
| GB0509965D0 (en) | 2005-06-22 |
| EP1891223B1 (en) | 2011-01-05 |
| JP2008539781A (ja) | 2008-11-20 |
| US20100015107A1 (en) | 2010-01-21 |
| EP1891223A2 (en) | 2008-02-27 |
| ATE494381T1 (de) | 2011-01-15 |
| US7632661B2 (en) | 2009-12-15 |
| EP2295589A1 (en) | 2011-03-16 |
| CN101208435B (zh) | 2012-05-23 |
| WO2006123097A3 (en) | 2007-01-11 |
| US20080097088A1 (en) | 2008-04-24 |
| ES2358680T3 (es) | 2011-05-12 |
| WO2006123097A2 (en) | 2006-11-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5080452B2 (ja) | 改良された発現エレメント | |
| JP5051738B2 (ja) | 人工遍在的クロマチン開放エレメント(ucoe) | |
| CA2859452C (en) | Artificial nucleic acid molecules for improved protein or peptide expression | |
| JP2009017886A (ja) | 改良された遺伝子発現 | |
| Hovemann et al. | Heat-shock locus 93D of Drosophila melanogaster: an RNA with limited coding capacity accumulates precursor transcripts after heat shock | |
| US7812148B2 (en) | Vectors comprising CpG islands without position effect varigation and having increased expression | |
| Kwong et al. | The recruitment of blood coagulation factor X into snake venom gland as a toxin | |
| CN1748034B (zh) | 改进的表达元件 | |
| JP4642865B2 (ja) | 新規制御エレメントを含むベクター | |
| US9057079B2 (en) | Expression elements | |
| US6881834B1 (en) | Myeloid cell promoter and constructs containing same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090424 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100405 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111005 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120302 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120529 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120605 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120629 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120706 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120821 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120830 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150907 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5080452 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |