JP4939397B2 - アレルギー性反応に関与する細胞を標的化するための二重特異性抗体、ならびにその組成物および使用 - Google Patents
アレルギー性反応に関与する細胞を標的化するための二重特異性抗体、ならびにその組成物および使用 Download PDFInfo
- Publication number
- JP4939397B2 JP4939397B2 JP2007505735A JP2007505735A JP4939397B2 JP 4939397 B2 JP4939397 B2 JP 4939397B2 JP 2007505735 A JP2007505735 A JP 2007505735A JP 2007505735 A JP2007505735 A JP 2007505735A JP 4939397 B2 JP4939397 B2 JP 4939397B2
- Authority
- JP
- Japan
- Prior art keywords
- irp60
- cells
- allergic
- bispecific
- antibodies
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/42—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against immunoglobulins
- C07K16/4283—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against immunoglobulins against an allotypic or isotypic determinant on Ig
- C07K16/4291—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against immunoglobulins against an allotypic or isotypic determinant on Ig against IgE
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6873—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting an immunoglobulin; the antibody being an anti-idiotypic antibody
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/06—Antigout agents, e.g. antihyperuricemic or uricosuric agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pulmonology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
- Oncology (AREA)
- Cell Biology (AREA)
- Physical Education & Sports Medicine (AREA)
- Pain & Pain Management (AREA)
- Ophthalmology & Optometry (AREA)
- Urology & Nephrology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Otolaryngology (AREA)
- Biomedical Technology (AREA)
- Vascular Medicine (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Hematology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Dermatology (AREA)
Description
アレルギー性炎症は、様々な細胞タイプ(例えば、炎症性細胞および構造的細胞など)を伴う複雑な現象である。マスト細胞はアレルギー性炎症の十分に確立された開始因子であり、炎症性細胞(主として、好酸球)を引き寄せ、活性化し、最終的にはその炎症性細胞と相互に作用する。アレルギー性炎症は様々な病状(例えば、喘息、アレルギー性鼻炎、アレルギー性結膜炎、アトピー性湿疹など)を構成する。これらの疾患の中で、また、一例として、喘息は幼児期の最も一般的な病気であり、西欧諸国では20%にまで達すると考えられ、現在増加している[Busse WW、Lemanske RF Jr.(2001)、N Engl J Med.、344:3501]。
マスト細胞は、顕著な細胞質顆粒を含有する、組織に存在するFcεRI保有細胞である。アレルギー性反応における非常に重要な役割を有することのほかに、マスト細胞はまた、線維症、腫瘍、自己免疫疾患および生来的免疫にも関与している。マスト細胞は、身体中至るところ、結合組織および粘膜表面に広く分布し、通常、血管および末梢神経の非常に近いところに存在する。従って、マスト細胞は、マスト細胞が数分以内および/または数時間の期間の両方で反応し得る環境刺激(例えば、微生物およびアレルゲンなど)にさらされ、事前に形成された媒介因子および新たに合成された媒介因子の調節された分泌を受ける。
マスト細胞および好酸球がともに、Ig受容体スーパーファミリー(これは細胞外部分における1つだけのVタイプIg様ドメインによって特徴づけられる;例えば、KIR、LIR/ILT、LAIR、gp49B1など)またはc型(カルシウム依存性)レクチンスーパーファミリー(例えば、MAFA、CD94/NKG2Aなど)のいずれかに属するいくつかの阻害性受容体を発現することがますます明らかになってきている。この大きなファミリーの免疫阻害性受容体は、コンセンサスなアミノ酸配列、すなわち、免疫受容体のチロシン型阻害性モチーフ(ITIM)によって特定することができる。ITIMはこれらの分子の細胞質ドメインに存在する。原型となるITIM配列は6個のアミノ酸から構成される:(Ile/Val/Leu/Ser)−X−Tyr−X−X−(Leu/Val)、式中、Xは任意のアミノ酸を表す。活性化されたとき、これらの阻害性受容体は、多くの場合にはSrcファミリーのキナーゼによるチロシンのリン酸化を受け、これにより、Src相同性2(SH2)ドメインを有する細胞質ホスファターゼ(例えば、SHP−1、SHP−2、SHIP−1およびSHIP−2など)を動員するための結合部位を提供する[Ravetch JV、Lanier LL(2000)、Science、290:848]。
近年では、抗体治療が非常に様々な疾患(例えば、ガン、マラリアおよび喘息など)のための新しい治療様式になってきている。それにもかかわらず、抗体の効力はさらなる改善を必要とすることが広く認められている。
図面の簡略説明
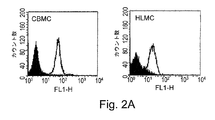
図1は阻害性NK受容体についてのヒトマスト細胞のスクリーニングを示す。NK細胞に対する阻害性機能が知られている受容体の大きな集団のFACS分析により、ヒトマスト細胞がIRp60を高レベルで発現することが明らかにされた。この発現は、他の阻害性受容体が発現していなかった[n=4]ので特異である。
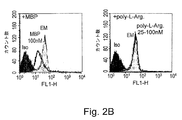
図2はIRp60がマスト細胞および好酸球において発現することを示す。
図2A:ヒトマスト細胞はIRp60を発現する。CBMCおよびHLMCにおけるIRp60発現のFACS分析。IRp60が、モノクローナル抗IRp60抗体を使用し、その後、抗マウスFITCを使用して、CBMC[左側]およびHLMC[右側]において検出された。黒色ピークは陰性のイソ型コントロールを表す。白色ピークは抗IRp60染色を表す。n=10[CBMC]およびn=3[HLMC]を表す。
図2B:IRp60の発現が好酸球の主要塩基性タンパク質(MBP)によって調節される。CBMCを好酸球由来MBP[左側]またはポリ−L−アルギニン[右側]と24時間インキュベーションし、IRp60の発現をFACSによって分析した。黒色ピーク[iso]は、IgGを使用する陰性のイソ型コントロールを表す。灰色ピーク[EM]は、富化培地単独により処理されたCBMCの抗IRp60染色を表す。白色ピークはMBP処理CBMC[左側]またはポリ−L−アルギニン処理CBMC[右側]の抗IRp60染色を表す。
図3はIRp60の架橋はIgE媒介による放出を阻害することを示す。
図3A:抗IRp60による刺激の後におけるIgE活性化CBMCからのβ−ヘキソサミニダーゼおよびトリプターゼのパーセント放出。
図3B:抗IRp60による刺激の後におけるIgE活性化CBMCからのIL−4のパーセント放出。
CBMCを抗IRp60被覆プレートでインキュベーションし、抗IgE抗体により30分間活性化した。β−ヘキソサミニダーゼおよびトリプターゼの放出レベルを、記載されるような酵素発色法アッセイによって評価し、%放出として表した。IL−4の放出レベルをELISAによって評価し、pg/mLで表した。β−ヘキソサミニダーゼの放出を記載されるように評価した。EM、富化培地単独;X、架橋剤[ヒツジ抗マウス、ヤギ抗マウスIgE];抗IRp60、抗IRp60により被覆されたプレート;IgG、イソ型により被覆されたプレート。
図4はIRp60の架橋はSCF誘導によるCBMCの生存を阻害することを示す。CBMCを、SCF[100ng/mL]とともに、または、SCFを伴うことなく、抗IRp60被覆プレートで24時間および48時間インキュベーションし、ヨウ化プロピジウム[PI]について染色し、PIについて陽性の細胞をFACSによって分析した。データは全細胞のPI陽性細胞の%として示される。EM、富化培地単独;X、架橋剤[ヒツジ抗マウス、ヤギ抗マウスIgE];IRp60、抗IRp60により被覆されたウェル;Iso、イソ型により被覆されたウェル。
図5はIRp60の架橋はIgE誘導による[Ca2+]流入を阻害することを示す。CBMC上のIRp60を抗IRp60抗体およびヒツジ抗マウス抗体とのインキュベーションによって架橋し、細胞にカルシウムGreen−1AMを負荷した。[Ca2+]がFL−1の幾何平均によって表される。EM、富化培地単独;X、架橋剤[ヒツジ抗マウス、ヤギ抗マウスIgE];IRp60、抗IRp60;Iso、イソ型。
図6はIRp60チロシンリン酸化およびホスファターゼ動員を示す。
図6A:CBMCをオルトバナジン酸ナトリウムで処理した。IRp60を、抗IRp60またはIgG1[陰性コントロール]を使用して沈殿させ、ホスホチロシン[pY99]、SHP−1、SHP−2およびSHIP−1に対してブロットした。
図6B:IRp60チロシンリン酸化は受容体架橋に依存的である。CBMCを、抗IRp60/IgG1被覆プレートにおいて0秒間、15秒間、30秒間、60秒間および120秒間、または、IgG被覆ウェルにおいて30秒間および60秒間インキュベーションし、その後、沈殿させ、ウェスタンブロットをホスホチロシン[pY99]に対して、または、タンパク質量のためのコントロールとしてのIRp60に対して行った。
図7はマウスマスト細胞はLMIR1を発現することを示す。BALB/マウス由来の骨髄マスト細胞および新しく単離された腹膜マスト細胞をモノクローナル抗体により染色し、FACSによって分析した。BMMC、骨髄マスト細胞;MPMC、腹膜マスト細胞。
図8はLMIR1の中和はアレルギー性腹膜炎のマウスモデルにおける強化されたマスト細胞活性化およびその後の好酸球浸潤をもたらすことを示す。OVA誘導によるアレルギー性腹膜炎を記載されたように誘導し、OVAによる抗原攻撃後45分または48時間で屠殺し、腹膜腔を媒介因子分析および細胞計数ならびにフローサイトメトリーのためにそれぞれ洗浄した。トリプターゼおよびβ−ヘキソサミニダーゼのレベルを、記載されるような酵素発色アッセイを使用して評価した。抗原攻撃後48時間で集められた洗浄液からの細胞をCCR3について染色し、FACSにより分析した。
図8A:LMIR1の中和は抗原攻撃後45分において腹膜トリプターゼレベルにおける劇的な増大をもたらした。
図8B:LMIR1の中和は抗原攻撃後45分において腹膜β−ヘキソサミニダーゼレベルにおける劇的な増大をもたらした。
図8C:増大した数の好酸球が、LMIR1中和後(抗原攻撃後24時間)、腹膜腔に浸潤した。
図8D:LMIR1の中和は抗原攻撃後24時間において腹膜エオタキシン−2レベルにおける劇的な増大をもたらした。
図9はIRp60がヒト好酸球において発現することを示す。
図9A:ヒトマスト細胞上における阻害性受容体の発現パターン。IRp60、p140、LIR3/ILT5、FcγRIIB、LIR1/ILT2、LIR3/ILT5、p58.1、p58.2、p70およびNKG2A/CD94の、CBMCにおける発現を示すFACS分析(n=10)。
図9B:鼻ポリープの好酸球は著しいレベルのIRp60を発現する。左側のピークは、イソ型コントロールと一致した抗体に対応し、一方、右側のピークはIRp60についての染色を示す。
図10はIRp60はヒト好酸球のgM−CSF媒介による生存を阻害することを示す。グラフは、抗IRp60またはイソ型一致コントロールおよびヒツジ抗マウスによる架橋、ならびに、様々な時点での示された濃度のGM−CSFによる処置の後におけるアポトーシス好酸球の割合を示す。
図10A:GM−CSFとの18時間のインキュベーションの後。
図10B:GM−CSFとの36時間のインキュベーションの後。
図11はIRp60はヒト好酸球のGM−CSF媒介による活性化を阻害することを示す。
図11A:IRp60を架橋したときに著しく阻害された、IL−1β、IL−4およびIFN−γのGM−CSF媒介による放出を示すヒストグラム。
図11B:IRp60を架橋したときに完全に阻止された、IL−8のGM−CSF媒介による放出を示すヒストグラム。
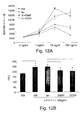
図12はIRp60はヒト好酸球のエオタキシン依存的走化性を阻害することを示す。
図12A:グラフは、エオタキシンの異なる濃度に向かって移動した、抗IRp60、抗CCR3、イソ型(Iso)または富化培地単独(EM)による処理の後における好酸球の数を示す。
図12B:ヒストグラムは、抗IRp60、抗CCR3、イソ型(Iso)または富化培地単独(EM)とのインキュベーションの後、FACSによって測定された、好酸球におけるエオタキシン誘導による形状変化を示す。
図13は二重特異性F(ab’)2フラグメントの作製および特徴づけを示す。
図13A:起こり得る物質損失をモニターするために、二重特異性F(ab’)の合成における各段階から得られたサンプルを非変性SDS−PAGEで泳動した[Fab’作製:kDa、サイズマーカー;IgG、出発抗体;int、3回のゲルろ過からのサンプル;Fab’、カップリングのための準備ができた得られたFab’フラグメント]。カップリング後、還元性SDS−PAGEを行って、BsAb複合化を確認した[BsAb:kDa、サイズマーカー;BsAb、二重特異性抗体;IgG、完全な抗体のコントロール]。BsAbの重鎖は約37kDaにおいて明らかに三量体化している。
図13B:FACSによるBsAb二重特異性の評価。抗ヒトIgE、抗ヒトIRp60またはIE1を使用して、新しい非感作ヒトマスト細胞[CBMC]、および、ヒトIgEにより感作されたRBL細胞[IgE−RBL]の両方を染色し、その後、抗マウスFITCにより染色した。染色がFL−1チャネルでの平均蛍光強度[MFI]として表された。
図14はIE1はインビトロでIgE誘導によるマスト細胞脱顆粒化を阻害することを示す。IgE感作のヒトマスト細胞を、抗IgE媒介による活性化の前に、5μg/mLのIE1またはイソ型コントロールと30分間インキュベーションした。β−ヘキソサミニダーゼの放出を、発色酵素アッセイを使用して測定した[EM、富化培地により処理された細胞;X、抗IgE処理;iso、一致するイソ型コントロール]。
図15はLE1はアレルギー性腹膜炎のマウスモデルにおいてトリプターゼ放出を阻害することを示す。
図15A:オバルブミン感作マウスに3μgのLE1またはイソ型コントロールを注射し、続いて、30分後にオバルブミンにより抗原攻撃した。45分後、マウスを屠殺し、トリプターゼを、発色酵素アッセイを使用して腹膜洗浄液において測定した[Sal.、生理的食塩水攻撃のマウス;OVA、オバルブミン攻撃のマウス;LE1、LE1による前処理、その後、オバルブミン攻撃;Iso、イソ型による前処理、その後、オバルブミン攻撃]。
図15B:LE1はアレルギー性腹膜炎のマウスモデルにおいてエオタキシン−2放出を阻害する。オバルブミン感作マウスに3μgのLE1またはイソ型コントロールを注射し、続いて、30分後にオバルブミンにより抗原攻撃した。24時間後、マウスを屠殺し、エオタキシン−2をELISAによって腹膜洗浄液において測定した[Sal.、生理的食塩水抗原のマウス;OVA、オバルブミン攻撃のマウス;LE1、LE1による前処理、その後、オバルブミン攻撃;Iso、イソ型による前処理、その後、オバルブミン攻撃]。
図16はLE1はアレルギー性腹膜炎のマウスモデルにおいて好酸球の動員を阻害することを示す。オバルブミン感作マウスに3μgのLE1またはイソ型コントロールを注射し、続いて、30分後にオバルブミンにより抗原攻撃した。48時間後、マウスを屠殺し、腹膜洗浄液中の細胞を2x105個の細胞に正規化し、好酸球集団をより良好に明らかにするためにCCR3−FITCおよびCD48−PEについて染色した。
図16A:FACS分析を、腹膜腔における好酸球の割合を定量するために行った。
図16B:FACS分析で得られた結果を表すヒストグラム[Saline、生理的食塩水攻撃のマウス;OVA、オバルブミン攻撃のマウス;LE1、LE1による前処理、その後、オバルブミン攻撃;Iso、イソ型による前処理、その後、オバルブミン攻撃]。
図17はLE1は受動的皮膚アナフィラキシーのマウスモデルにおいてマスト細胞の脱顆粒化を阻害することを示す。マウスを、LE1またはイソ型コントロールによる前処理と同時にIgE抗DNPにより感作した。2時間後、マウスをエバンスブルー溶液と一緒に静脈内DNPボーラスによって抗原攻撃した。皮膚のアナフィラキシーを青色色素のスポットサイズによって目視評価した[Saline+DNA、IgEなし;IgE+DNP、IgEのみ;IgE+LE1+DNP、LE1前処理部位;IgE+isotype+DNP、イソ型前処理部位]。
図17A:青色色素スポットアッセイを示す皮膚の区域。
図17B:異なる試料を用いた図17Aと同じ図。
・BsAb:二重特異性抗体
・CBMC:ヒト臍帯血マスト細胞
・ECP:好酸球カチオン性タンパク質
・FCS:ウシ胎児血清
・HLMC:ヒト肺マスト細胞
・IE1:IRp60およびIgEを認識する二重特異性抗体
・ITAM:免疫受容体のチロシン型活性化モチーフ
・ITIM:免疫受容体のチロシン型阻害性モチーフ
・LE1:LMIR−1およびIgEを認識する二重特異性抗体
・mAb:モノクローナル抗体
・MAPK:マイトジェン活性化プロテインキナーゼ
・MBP:好酸球由来主の要塩基性タンパク質
・NGF:神経増殖因子
・SCF:幹細胞因子
・SH2:Src相同性2
・Siglec:シアル酸結合性Ig様レクチン
・抗体および試薬
すべての細胞培養培地、試薬および緩衝液をBilogical Industries(Beit Haemek、イスラエル)から購入した。SCFはAmgen,Inc.[Thousand Oaks、カリフォルニア州、米国]からの譲渡である。様々な阻害性受容体を認識する下記のmAbを、文献に記載される標準的な手順によって調製し、使用した:P192およびE59[抗IRp60]、XA−185[抗CD94]、11PB6[抗p58.1]、GL183[抗p58.2]、Z27[抗p70]、Q66[抗p140]、AZ158[抗p70/p140]、F278[抗LIR1/ILT2]。LIR3/ILT5を認識する抗体[15F3]はColonna M.(Washington University、St Louis、米国)によって譲渡された。抗LMIR1をR&D Systems[Minneapolis、ミネソタ州、米国]から購入した。ヒト肺マスト細胞の精製のための抗ヒトCD117抗体をBD−Pharmingen[San Diego、カリフォルニア州、米国]から購入した。抗ヒトトリプターゼ抗体[クローンAA1]およびイソ型コントロール抗体[IgG1およびIgG2A]をDako[Glostrup、デンマーク]から購入した。ヒツジ抗マウスF[ab’]2抗体をICN Biomedicals[Aurora、オハイオ州、米国]から購入した。キメラマウス/ヒトIgE抗NP抗体をSerotec[Raleigh、ノースカロライナ州、米国]から購入した。ヤギ抗マウスλ鎖特異的抗体をSouthern Biotech[Birmingham、アラバマ州、米国]から購入した。ポリクローナル抗ヒトホスホチロシン[pY99]抗体、SHP−1/2抗体およびSHIP−1抗体をSanta Cruz[Santa Cruz、カリフォルニア州、米国]から購入した。西洋ワサビペルオキシダーゼコンジュゲート化された抗ウサギ抗体および抗マウス抗体、フルオレセインイソチオシアナート[FITC]コンジュゲート化抗マウス抗体、Cy5コンジュゲート化抗マウス抗体およびフィコエリトリンコンジュゲート化抗マウス抗体をすべてJackson Laboratories[West Grove、ペンシルバニア州、米国]から購入した。発色性基質をSigma[St.Louis、ミズーリ州、米国]から購入した。カルシウムグリーン−1AMをMolecular Probes[Eugene、オレゴン州、米国]から購入した。Ficoll−paqueをAmersham Biosciences[Uppsala、スウェーデン]から購入した。すべての他の試薬は、別途言及されない限り、Sigmaから購入され、入手可能な最高の化学規格であった。
別個のエピトープを認識する完全なマウスIgG抗体またはラットIgG抗体に由来する二重特異性のF(ab’)2フラグメントを、わずかな改変とともに、基本的にはBrennanおよびGrazianoによって記載されるように作製した。マウスの抗ヒトIgEおよび抗ヒトIRp60を、固定化ペプシンビーズを製造者のプロトコルに従って使用して、記載されるように、37℃で4時間、振とう浴において消化した。F(ab’)2フラグメントを、vivaspinカラムでの遠心分離ゲルろ過を使用して精製し、還元性緩衝液[1mMのEDTA、1mMの2−メルカプトエチルアミン、10mMの亜ヒ酸ナトリウム、0.1Mのリン酸ナトリウム、pH6.8]において25℃で一晩インキュベーションすることによってFab’フラグメントに還元した。抗IRp60のみには、5’,5−ジチオビス[2−ニトロ安息香酸][Ellman試薬]を10mMの最終濃度に加え、インキュベーションを25℃で4時間続けた。その後、両方の抗体をゲルろ過によって清浄化し、カップリング緩衝液[1mMのEDTA、0.1Mのリン酸ナトリウム、pH6.8]に移し、混合し、25℃で一晩インキュベーションした。得られたF(ab’)2をゲルろ過によって精製し、PBSにおいて回収し、分光光度法を使用して定量した。特異性をFACSによって評価した。マウスのIgEおよびLMIR1について、ラットIgGは、固定化ペプシンとの5時間のインキュベーションを除いて同じプロセスを受けた。下記の標的組を認識するBsAbを作製した:IE1[hIgE−IRp60]、hIgE−イソ型[コントロール]、LE1[mIgE−LMIR1]、mIgE−イソ型[コントロール]。
a.マスト細胞の精製および培養
今日までのマスト細胞に関する知識のほとんどが、齧歯類のマスト細胞およびヒトのマスト細胞株に対して行われた研究に依ることは注目に値する。本発明者らの研究室では、ヒト治療に集中しており、臍帯血、肺、皮膚および腸からヒトマスト細胞を精製し、ヒトマスト細胞を特異的に培養するための技術が開発されている。
フローサイトメトリーを、Becton−Dickinson FACScaliburおよびCellQuestソフトウエアを使用して行った。すべての段階を100μLの体積で丸底96ウェル培養プレート[Nunc、Roskilde、デンマーク]において行った。大部分の細胞[約105個/サンプル]を氷冷のHBA緩衝液[BSA[0.1%(w/v)]およびNaN3「0.01%(w/v)」を含有するハンクス溶液]により洗浄し、その後、抗IRp60または適切なイソ型コントロールのいずれかとインキュベーションし[4℃、30分間]、その後、冷HBAにより2回洗浄した。その後、細胞を二次抗体とインキュベーションし[推奨される希釈度でのFITCコンジュゲート化抗マウスまたはCy5コンジュゲート化抗マウス、4℃、30分間]、その後、さらに2回洗浄し、FACSによって直ちに分析した。細胞内FACSを、一次抗体を加える前の2つの段階を除いて本質的には同じに行った。この場合、細胞を、最初に2%ホルムアルデヒドにおいて固定処理し[4℃、10分間]、BSA[10%(w/v)]、ヤギ血清[0.1%(w/v)]、サポニン[0.1%(w/v)]およびHEPES[10mM]を含有するHBAによりブロッキング処理した[4℃、10分間]。サポニン[0.1%(w/v)]およびHEPES[10mM]を含有するHBAもまた、インキュベーションおよび洗浄のために用いた。
活性化の5日前に、CBMCをキメラマウス/ヒトIgE抗NP抗体[5μg/mL]とインキュベーションした。活性化のために、Immunolon−2HB 96ウェルプレート[ThermoLabsystems、Franklin、マサチューセッツ州、米国]をヒツジ抗マウスF[ab’]2[PBSにおいて25μg/mL]の存在下または非存在下でインキュベーションし[37℃、4時間]、その後、PBSにより2回洗浄した。次いで、プレートを、抗IRp60[20μg/mL]、イソ型コントロールまたはPBSとインキュベーションし[37℃、4時間]、PBSにより2回洗浄した。活性化の当日において、細胞[2x105細胞/サンプル]を、SCF[100ng/mL]が補充された温いTyrodeゼラチン−カルシウム緩衝液[137mMのNaCl、12mMのNaHCO3、5.5mMのL−グルコース、2mMのKCl、0.3mMのNa2HPO4、0.1%(w/v)のゼラチン、1.8mMのCaCl2、0.9mMのMgCl2]で2回洗浄した。その後、細胞を被覆プレートに移し、抗マウスIgEのλ鎖特異的抗体[5μg/mL]または化合物48/80[10μg/mL]のいずれかを加え、細胞を37℃で30分間インキュベーションした。最後に、細胞を直ちに遠心分離し[1500xg、1分間]、上清から分離し、3回の凍結/融解サイクルによって溶解し、溶解物を回収して、放出された媒介因子の量について評価されるまで−80℃で保存した。
β−ヘキソサミニダーゼおよびトリプターゼを、わずかな改変とともに、記載されるように発色性アッセイによって測定した[Woolhiser,M.R.他(2004)、Clin.Immunol.、110(2):172〜80;Greenfeder S.他(2003)、Biotechniques、34(5):910〜2、914]。β−ヘキソサミニダーゼについては、18μLのサンプル[上清または細胞溶解物]を42μLの基質溶液[48mMのクエン酸および56mMのNa2HPO4(pH4.5)における8mMのp−ニトロフェニル−N−アセチル−β−D−グルコサミニド]と混合し、37℃で2時間インキュベーションした。反応を120μLの氷冷グリシン[0.2M](pH10.7)の添加によって停止させ、O.D.を410nmの吸光度において標準的な分光光度計で直ちに読み取った。トリプターゼについては、48μLのサンプルを2μLの基質溶液[100%DMSOにおける25mMのN−p−トシル−gly−pro−lys−p−ニトロアニリド]と十分に混合し、発色するまで37℃でインキュベーションし、上記のように直ちに読み取った。パーセント放出を、O.D.曲線の直線範囲内で、下記の式を使用して計算した:%R=100x上清/[溶解物+上清]。IL−4の放出を市販のELISAキット[Diaclone、Besancon、フランス]によって測定した。
CBMC[2x105細胞/サンプル]を、増殖因子を含まないMEM−Alphaにより洗浄し、上記で記載されたように被覆された培養プレートにおいて、SCF[100ng/mL]を含むMEM−AlphaまたはSCFを含まないMEM−Alphaの200μLにおいてインキュベーションした。24時間および48時間で、サンプルをPBSにおけるヨウ化プロピジウム溶液[10%(v/v)]の5μLの添加によって染色し、直ちにFACSによって分析した。
CBMC[3x105細胞/サンプル]を、TNF−α[20ng/mL]、IL−3[20ng/mL]、IL−4[20ng/mL]、NGF[50ng/mL][すべてをPeprotech(Rocky Hill、ニュージャージー州、米国)から購入した]、キメラIgE[5μg/mL][Serotec]、好酸球MBP[0.01μM〜0.1μM](これは記載されたように精製された;Piliponsky(2003)、同上同頁)またはポリ−L−アルギニン[25μM〜100μM]のいずれかの存在下、37℃で、0時間、4時間、12時間および24時間培養した。これらの時点でIRp60の発現をFACSによって評価した。
カルシウムセンサーを負荷する前に、CBMC[3x105細胞/サンプル]上のIRp60を抗IRp60またはイソ型とのインキュベーション[10μg/mL、氷上で30分間]によって架橋し、その後、洗浄し、MEM−Alphaにおけるヒツジ抗マウスF[ab’]2とインキュベーションした[25μg/mL、氷上で30分]。細胞にMEM−Alpha[FCS、2%(v/v)]におけるカルシウムグリーン−1AMを負荷し[5μM、45分間、37℃]、洗浄し、37℃に暖められた400μLのTyrodeゼラチン−カルシウム緩衝液に懸濁した。細胞を、100秒間、サイトメーター内を自由に流れさせ、そのとき、抗IgE[5μg/mL]を加えた。FL−1の幾何平均の変化を合計で5分間にわたって記録した。
CBMCを、市販の溶解緩衝液[Pierce、Rockford、IL、米国]を使用して溶解し、10%SDS−PAGEで泳動し、PVDFメンブレン[Pierce]に転写し、IRp60[抗IRp60、1μg/mL]に対してブロットした。IRp60沈殿のために、CBMC[8x106細胞/サンプル]をオルトバナジン酸ナトリウム[4mM、10分間、37℃]で処理し、または、被覆プレートにおいて様々な時間インキュベーションした。IRp60を、市販のキット[SeizeTM Classic Mammalianキット、Pierce]を製造者の説明書に従って使用してCBMCから沈殿させた。サンプルを記載されるように泳動し、ホスホチロシン[pY99]、SHP−1/2およびSHIP−1に対してブロットした。検出のために、西洋ワサビペルオキシダーゼコンジュゲート化された抗マウス抗体または抗ウサギ抗体を、製造者によって推奨されるように使用した。
a.好酸球の精製
好酸球を軽度のアトピー性者(血中好酸球レベル、5%〜10%)の末梢血から精製した。書面によるインフォームドコンセントを、Hadassah−Hebrew Universityのヒト実験ヘルシンキ委員会により制定されたガイドラインに従ってすべての志願者から得た。簡単に記載すると、静脈血(50ml〜100ml)をヘパリン添加シリンジに集め、6%デキストラン(Amersham Bioscineces)において沈降させた。白血球をFicoll−Hypaqueでの遠心分離(密度、1.077;25分間、700g、22℃;Amersham Bioscineces)に供した。好中球および混入しているリンパ球を、抗CD16Abおよび抗CD3Abに結合させた微小磁石ビーズ(Miltenyi Biotec)を用いて顆粒球濃縮ペレットに捕捉した。好酸球を、細胞懸濁物を磁石カラム(MACS)に通すことによって精製した。細胞を、Kimura染色によって少なくとも98%の純度で回収し、生存性はトリパンブルー染色により少なくとも98%であった。CD56+細胞またはCD3+細胞はいずれも、FACS分析によって、混入画分において観測されなかった(データは示されず)。
フローサイトメトリー(FACS)分析のために、細胞(1X105個)を、0.1%のBSAおよび0.02%のアジ化ナトリウムが補充されたHBSS(HBA)の100μlの最終体積において氷上で30分間、(FcRをブロッキングするために)15%のヒト血清とインキュベーションした。好酸球を、様々な阻害性受容体を認識する種々のAbと一緒に培養し、その後、ヤギ抗マウスFITCAb(1/200)と一緒に培養した。生存実験のために、アネキシン−PI染色を、R&Dアネキシン−PIキットを製造者の説明書に従って使用して行った。
96ウェルプレート(Nunc)をPBSにおけるヒツジ抗マウスF(ab’)2によりプレコーティングした(25μg/ml、2時間、37℃、5%CO2)。その後、プレートをPBSにより3回洗浄し、P192(抗IRp60)Abまたは関連性のないイソ型一致のコントロールAbとインキュベーションし(1μg/ml〜5μg/ml、2時間、37℃、5%CO2)、再び3回洗浄した。新しく分離された好酸球を、RPMI1640、200U/mlのペニシリン、200μg/mlのストレプトマイシンおよび5%(v/v)の熱不活化FCSを含有する培地(富化培地(EM))においてこれらのプレコーティングされたウェルに播種し(2X105個/200μl)、IL−5またはGM−CSFを種々の濃度で加えた(1ng/ml〜100ng/ml)。細胞を18時間〜24時間インキュベーションした(37℃、5%CO2)。インキュベーションが終了したとき、細胞を遠心分離し(250g、5分間、4℃)、上清を集め、小分けし、サイトカインまたは繊維芽細胞増殖アッセイについて評価されるまで−80℃で保存した。
IL−8を、DuoSet(R&D Systems)を使用して好酸球培養上清において定量した。アッセイ感度についての下限はIL−8について7pg/mlであった。IL−1b、IFN−γおよびIL−4を、10個の異なるサイトカインを検出するFlowCytomixキットを製造者の説明書に従って使用して検出した。
好酸球の遊走を、マイクロウェル二重チャンバーシステム(ChemoTxチャンバー:フィルター細孔サイズ 5μm、直径60mmのウェル;Neuro Probe Inc.、Gaithersburg、MD)を使用して測定した。組換えヒトエオタキシン(1ng/ml〜100ng/ml)を三連で底部チャンバー内のウェルに加え、枠取られたフィルターで覆った。次いで、抗IRp60またはイソ型一致コントロールによって活性化された好酸球の懸濁物(30000細胞/30μl)を、各ウェルを覆っているフィルターの上に置き、チャンバーシステムを90分間インキュベーションした(37℃、5%CO2)。インキュベーション後、フィルターの上における非遊走の好酸球の懸濁物を、ティッシュペーパーを使用して除き、下部チャンバーにおける細胞をフローサイトメトリーによって計数した(FACScalibur、Beckton Dickinson)。簡単に記載すると、相対的な細胞カウント数を、事象を60秒間にわたって取得することによって得た。
エオタキシン誘導による好酸球の形状変化を、フローサイトメトリー分析を使用することによって評価した。抗IRp60またはイソ型一致コントロールによって活性化された好酸球の懸濁物を組換えヒトエオタキシン(1ng/ml〜100ng/ml)と5分間〜10分間インキュベーションした(37℃、5%CO2)。その後、細胞を洗浄し、フローサイトメトリー(FACScalibur、Beckton Dickinson)によって分析し、10000細胞のFSCを取得した。
サブコンフルエントの繊維芽細胞単層物の増殖を[3H]−チミジン取り込みによって評価した。繊維芽細胞を、200mlの補充されたDMEM/10%FCSにおいて、一晩、96ウェルプレートに播種し(5X103細胞/ウェル)、補充されたDMEM/0.5%FCSにより2回洗浄し、IRp60またはイソ型一致コントロールによって24時間活性化された好酸球の上清を用いて刺激した。[3H]−チミジン(NENTM Life Science Products,Inc.、Boston、MA)を最後の24時間のパルス(1μCi/ウェル)として加え、サンプルを以前に記載されたように処理した。
アレルギー性腹膜炎を、オバルブミン[OVA]を記載[Zuany−Amorim他(1994)、Ann NY Acad Sci、725:34〜43]のように使用して8週齢〜10週齢のメスのBALB/cマウスにおいて誘導した。簡単に記載すると、0日目および7日目に、マウスを、300μLの生理的食塩水における1.6mgのミョウバン水酸化物に吸着させた100μgのOVAにより皮内に感作した。マウスを、11日目に、300μLの生理的食塩水における30μgのOVにより腹腔内に抗原攻撃し、その後、マウスを媒介因子分析および好酸球定量のために45分後または48時間後のいずれかでそれぞれ屠殺した。腹膜腔を、カルシウムを含まないTyrodeゼラチン緩衝液の5mLにより洗浄した。腹腔洗浄液を遠心分離し[150xg、5分間]、細胞ペレットを媒介因子分析および好酸球定量のために2mLのTyrodeゼラチン緩衝液に再懸濁した。すべての実験において、抗LMIR1をアレルゲン攻撃の30分前に投与した[1μg/マウス〜20μg/マウス、腹腔内]。すべての実験プロトコルがHebrew University(Jerusalem)の動物実験委員会により承認された。
活性化アッセイ、生存アッセイおよび媒介因子放出アッセイを、三連または四連で、かつ、常に少なくとも3つの異なるドナーから行った。データは平均±S.Dとして表される。データをANOVAによって分析し、その後、ペアードスチューデントt検定[分散が等しいと仮定して]およびTukey−Kramerポストホクによって分析した。
CBMCはIRp60を発現する
ヒトマスト細胞における阻害性受容体の発現パターンを調べるために、様々な阻害性受容体を認識するmAbの大きなパネルを使用するスクリーニング法を用いた。図1Aに示されるように、FACS分析は、CBMCが高レベルのIRp60を発現し、LIR1/ILT2、LIR3/ILT5、p58.1、p58.2、p70、p140またはNKG2A/CD94を発現していないことを明らかにした[n=10]。10個のドナーのうちの1つがCD94を発現し、NKG2Aを発現していなかった。加えて、CBMCはFcγRIIB(知られている阻害性受容体)について陽性に染色された[データは示されず]。
好酸球由来MBPはCBMC上におけるIRp60の発現をダウンレギュレーションする
本発明者らは次に、CBMC上におけるIRp60の発現を調節する、アレルギー性の炎症環境において見出される様々な媒介因子の能力を調べた。このために、CBMCを、TNF−α、IL−3、IL−4、単量体IgE、NGFおよび好酸球由来MBPの存在下で様々な時点について培養した。MBPを除いて、これらの媒介因子はどれも、IRp60の発現に著しい影響を及ぼさなかった。図2に示されるように、MBPは、12時間から始まり、24時間後に著しい影響に達したIRp60の発現レベルにおける低下を誘導した[n=3、p<0.01]。等モル濃度範囲[25nM〜100nM]でのポリ−L−アルギニンはIRp60の発現に影響しなかったので、MBPの影響は電荷依存的であった。
IRp60の架橋はCBMCからのIgE依存的な媒介因子放出を阻害する
CBMCの表面におけるIRp60の発現は、それらの応答がこの受容体によって調節され得ることを示唆する。CBMCの脱顆粒化を阻害するIRp60の能力を評価するために、CBMCをIgEにより感作し、抗IRp60被覆プレートにおいて抗IgE抗体または化合物48/80を使用して脱顆粒させるために誘発した。図3Aおよび図3Bに示されるように、IRp60の架橋は、β−ヘキソサミニダーゼ、トリプターゼおよびIL−4のIgE媒介による放出を強く、かつ、著しく阻害した:β−ヘキソサミニダーゼ[47.61±2.00%対11.71±1.12%(抗IRp60に関して)、p<0.001];トリプターゼ[60.90±7.35%対14.11±1.45%(抗IRp60に関して)、p<0.001]およびIL−4[8.41±1.19%対0.32±0.09%(抗IRp60に関して)、p<0.001]。興味深いことに、図3Cに示されるように、IRp60の架橋は、β−ヘキソサミニダーゼ、トリプターゼおよびIL−4の化合物48/80媒介による放出を阻害しなかった[データは示されず]。
IRp60の架橋はIgE誘導による[Ca2+]流入を阻害する
CBMCのFcεRI依存的活性化における初期工程の1つは細胞内カルシウム流入である。従って、カルシウム流入に対するIRp60架橋の影響を、カルシウムセンサーのカルシウムグリーン−1AMを使用して調べた。図4に示されるように、抗IgE添加の10秒〜20秒のうちに、顕著な[Ca2+]の増大が観測された。この増大は、IRp60の架橋に応答して完全になくなった[n=3]。
IRp60の架橋はSCF媒介によるCBMC生存を阻害する
SCFはこれまで、ヒトマスト細胞のための最も重要な生存因子である。SCFのシグナル伝達は、c−kitに結合し、Srcキナーゼおよびホスファチジルイノシトール−3−キナーゼのリン酸化を伴うシグナル伝達カスケードを開始したときにその作用を発揮する。c−kitのシグナル伝達を妨害するIRp60の能力を調べるために、CBMCを、架橋された抗IRp60被覆プレートにおいてSCF[100ng/ml]の存在下または非存在で培養し、その後、ヨウ化プロピジウム[PI]陽性細胞のFACS分析を行った。図5に示されるように、IRp60の架橋は両方の時点でマスト細胞の生存を著しく阻害した[24時間および48時間でそれぞれ、10.02±0.79%および37.68±0.69%のPI+細胞、これに対して、1.83±0.38%および3.65±0.33%のPI+細胞、p<0.001][n=3]。
IRp60はチロシンのリン酸化を受け、SHP−1およびSHIP−1を動員する
上記で述べられたように、NK細胞上におけるIRp60の阻害性作用はSHP−1およびSHP−2の動員を介して媒介される。ヒトマスト細胞上におけるIRp60の阻害性活性の機構を明らかにするために、CBMCをオルトバナジン酸ナトリウムで処理し、あるいは、架橋し、沈殿させ、ホスホチロシン、SHP−1、SHP−2およびSHIP−1についてブロットした。図6Aに示されるように、オルトバナジン酸塩の前処理およびIRp60の架橋を行ったとき、IRp60はチロシンのリン酸化を受けた。加えて、図6Bにおいて明らかにされるように、IRp60はSHP−1およびSHIP−1と共沈殿し、SHP−2とは共沈殿しなかった[n=3]。
IRp60はアレルギー性腹膜炎マウスモデルにおいてマスト細胞の活性化およびその後の炎症性応答を調節する
IRp60が、マスト細胞の活性化をインビボで調節する際において役割を有するかどうかを理解するために、アレルギー性炎症のマウスモデルを使用した。マスト細胞の役割が不明確である実験的な喘息プロトコルとは異なり、マウスのアレルギー性腹膜炎モデルにおけるマスト細胞の役割は十分に明らかにされている[Zuany−Amorim(1994)、同上同頁]。バイオインフォマティク分析により、LMIR1がIRp60のマウス相同体であることが明らかにされた[データは示されず]。従って、本発明者らは、マウスのマスト細胞がLMIR1を発現するかどうかを調べた。図7に示されるように、BMMCおよび腹膜マスト細胞はともに著しいレベルのLMIR1を発現する。続いて、LMIR1の調節作用を、この受容体を認識する中和抗体を加えることによって調べた。図8Aに示されるように、マイクロモル濃度での抗LMIR1モノクローナル抗体で前処理されたマウスは、アレルゲンの抗原攻撃に対する応答において高まったマスト細胞活性化を示し、また、増大したトリプターゼレベルおよびβヘキソサミニダーゼレベルが腹膜洗浄液において測定された。加えて、図8Bに示されるように、腹膜洗浄における生じた好酸球性炎症が強くなり、全体的な好酸球性炎症が、オバルブミン処理マウス群およびオバルブミン/イソ型コントロール群に対する比較では増大していた。
IRp60がヒト好酸球において発現する
ヒトマスト細胞上における阻害性受容体の発現パターンを調べるために、様々な阻害性受容体を認識するmAbの大きなパネルを使用するスクリーニング法を用いた。図9Aに示されるように、FACS分析により、好酸球が、高レベルのIRp60、p140、LIR3/ILT5およびFcγRIIBを発現し、LIM1/ILT2、LIR3/ILT5、p58.1、p58.2、p70またはNKG2A/CD94を発現していないことが明らかにされた(n=10)。興味深いことに、分析された好酸球の30%のみがp140を発現していた。
IRp60はヒト好酸球のIL−5媒介およびGM−CSF媒介の生存を阻害する
IL−5、GM−CSFおよびIL−3は、好酸球の生物学における重要なサイトカインであり、「好酸球生存因子」と呼ばれることが多い。ヒトにおいて、低親和性のα鎖に結合したとき、3つのサイトカインのすべてが、それらのシグナル伝達経路を働かせる共通のβ鎖を動員する。このシグナル伝達経路はチロシンのリン酸化およびSrcファミリーのキナーゼ(例えば、LynおよびSykなど)の動員に依存する。従って、本発明者らは、IRp60が、これらのサイトカインが伝達する抗アポトーシス作用を調節し得るかどうかを評価することを目指した。このために、新しく単離された好酸球を抗IRp60またはイソ型一致コントロールおよびヒツジ抗マウスにより架橋した。その後、IL−5またはGM−CSFを異なる濃度で様々な時点について加えた。図10Aおよび図10Bに示されるように、IRp60はGM−CSFおよびIL−5の抗アポトーシス作用を阻害した(データは示されず)。例えば、18時間のインキュベーションおよび50ng/mlのGM−CSFで、非処理群におけるアポトーシス細胞の割合は23.16±0.65%であり、これに対して、GM−CSFで処理された細胞は1.25±0.23%でしかなかった。抗IRp60の架橋およびGM−CSFにより処理された細胞は15.62±3.9%がアポトーシス性であった。この作用はまた、36時間でも認められ、この場合、GM−CSFで処理された細胞は13.85±0.6%がアポトーシス性であり、IRp60で処理された細胞は36.7±0.45%がアポトーシス性であった。興味深いことに、IL−5およびGM−CSFの抗アポトーシス作用を阻害するIRp60の能力は、両方の時点で、濃度が5ng/mlから50ng/mlに増大するに従って高まった(6.7±1.7%、9.45±1.95%、15.6±3.9%、それぞれ、5ng/ml、20ng/ml、50ng/mlのGM−CSF、18時間、19.6±0.21%、27.5±0.63%、36.7±0.45%、それぞれ、5ng/ml、20ng/ml、50ng/mlのGM−CSF、36時間)。
IRp60はヒト好酸球のIL−5媒介およびGM−CSF媒介の活性化を阻害する
IL−5、GM−CSFおよびIL−3はまた、好酸球を活性化することができる。従って、本発明者らは、IRp60の架橋が活性化因子様作用を同様に阻害するかどうかを調べた。図11Aおよび図11Bに示されるように、IRp60の架橋は、IL−8、IL−1b、IL−4およびIFN−γのGM−CSF媒介による放出を完全に阻止した。
IRp60はヒト好酸球のエオタキシン依存的走化性を阻害する
好酸球が炎症組織に移動することを調節する非常に重要な因子の1つがエオタキシンである。多くのことがエオタキシンのシグナル伝達に関して知られていないが、いくつかの報告では、エオタキシンがチロシンのリン酸化およびSrcファミリーのキナーゼ(例えば、HckおよびFgrなど)の動員を誘導することが明らかにされている。従って、本発明者らは、IRp60が好酸球のエオタキシン依存的活性化を阻止し得るかどうかを評価した。2つのパラメーターを調べた(走化性および形状変化)。
IgE−IRp60BsAbの作製
BsAb作製プロセスの各工程をモニターするために、サンプルを、起こり得る物質喪失を評価するために、それぞれのゲルろ過の後で採取した。サンプルを、カップリング前の反応物Fab’フラグメントおよびカップリング後のF(ab’)2生成物を評価するためにSDS−PAGEで泳動した。図13Aに示されるように、非変性SDS−PAGEはFab’反応物の1つを約50kDaにおいてカップリング前に示す。カップリング後、還元性SDS−PAGEは、2つのIgGサイズコントロールに隣接して、2つの約37kDaの重鎖フラグメントおよび2つの約25kDaの軽鎖に分離したBsAbを示す。IE1の二重特異性認識をFACSによって評価した。図13Bに示されるように、IE1は、IgE感作のRBL細胞を、抗ヒトIRp60とではなく、抗ヒトIgEと同様に認識し、これに対して、新鮮なヒトマスト細胞を、抗ヒトIgEとではなく、抗ヒトIRp60と同様に認識した。作製プロセスの平均見かけ収率は約40%であった。
インビトロでのマスト細胞脱顆粒化の阻害
マスト細胞の活性化を阻害するIE1の潜在的能力を評価するために、IgE感作のヒトマスト細胞をIE1または一致するイソ型コントロールとインキュベーションし、その後、抗IgE抗体を使用して活性化した。図14に示されるように、IE1はマスト細胞からのβ−ヘキソサミニダーゼの放出をほぼ完全に阻害した。
インビボでのアレルギー性応答の阻害
単離されたヒトマスト細胞においてインビトロで認められた作用がまたインビボでも認められるかどうかを明らかにするために、マウスのIgEおよびLMIR1(マウスのIRp60相同体)を認識するBsAbを作製した(これはLE1と称される)。LE1またはその一致するイソ型コントロールを、2つのアレルギー性応答モデルにおいて動物にさらに投与した。アレルギー性腹膜炎では、図15に示されるように、LE1は、アレルゲン攻撃の後、脱顆粒化途中の腹膜マスト細胞からのトリプターゼの放出を完全に阻害した。そのうえ、図16Aおよび図16Bに示されるように、好酸球カウント数が、アレルゲン攻撃の前にLE1により処理された群では劇的に低下した。このことは、より少ない好酸球がマスト細胞によって腹膜に動員されたことを意味する。受動的皮膚アナフィラキシーでは、LE1は、ヒスタミンに由来する色素漏出、および、皮膚マスト細胞からのロイコトリエン放出を完全に阻害した(図17A〜図17B)。
Claims (14)
- 以下のものを含む、二重特異性抗体:
(i)阻害性受容体IRp60に特異的に結合する第1の標的認識成分;および
(ii)IgEに特異的に結合する第2の標的認識成分。 - 以下のものを含む、二重特異性抗体:
(i)阻害性受容体IRp60に特異的に結合する第1の標的認識成分;および
(ii)cKITに特異的に結合する第2の標的認識成分。 - 以下のものを含む、二重特異性抗体:
(i)阻害性受容体IRp60に特異的に結合する第1の標的認識成分;および
(ii)FcεRIに特異的に結合する第2の標的認識成分。 - 以下のものを含む、二重特異性抗体:
(i)阻害性受容体IRp60に特異的に結合する第1の標的認識成分;および
(ii)CCR3に特異的に結合する第2の標的認識成分。 - 以下のものを含む、二重特異性抗体:
(i)阻害性受容体IRp60に特異的に結合する第1の標的認識成分;および
(ii)IL−5Rに特異的に結合する第2の標的認識成分。 - 前記抗体が前記細胞に結合することにより、アレルギー性反応が阻害される請求項1〜5のいずれか一項に記載の二重特異性抗体。
- 前記第1および第2の標的認識成分は、架橋剤、リンカー化合物、キャリア、合成スペーサー、固定化基質、および、(Gly4Ser)3モチーフに基づく柔軟な領域のいずれか1つを介して連結される請求項1〜5のいずれか一項に記載の二重特異性抗体。
- 前記第1および第2の標的認識成分は架橋される請求項1〜5のいずれか一項に記載の二重特異性抗体。
- 前記認識成分は、天然に存在する抗体、組換え抗体、単鎖Fv(scFv)、二機能性scFv、ジアボディー、F(ab)ユニット、F(ab’)ユニット、二重特異性F(ab’)コンジュゲート、化学的に架橋された二機能性抗体、線状抗体、あるいは抗体のF(ab’)2抗原結合性フラグメントのいずれか1つから選択される請求項1〜5のいずれか一項に記載の二重特異性抗体。
- 前記認識成分はF(ab’)ユニットである請求項1〜5のいずれか一項に記載の二重特異性抗体。
- 請求項1〜10のいずれか一項に記載の二重特異性抗体の少なくとも1つを活性な薬剤として含む医薬組成物。
- 緩衝剤、添加剤、安定化剤、希釈剤および/または賦形剤をさらに含む請求項11に記載の医薬組成物。
- アレルギー性喘息、アレルギー性鼻炎、アレルギー性結膜炎、アトピー性皮膚炎およびアトピー性湿疹、様々なアレルゲンに対するアレルギー性の障害および応答、全身性アナフィラキシー、全身性肥満細胞過剰増殖、限局性強皮症/色素性じんま疹、マスト細胞白血病、アテローム性動脈硬化、移植片拒絶、多発性硬化症、線維形成性肺疾患、神経線維腫症、ケロイド、強皮症、リウマチ様関節炎、変形性関節炎、急性痛風、眼の瘢痕性類天疱瘡、クローン病、腹膜癒着、慢性移植片対宿主病(GVHD)、好酸球増多筋痛症候群、気管支喘息、鼻ポリープ症、ヴェーゲナー肉芽腫症、間質性肺疾患、慢性好酸球性肺炎、過敏性肺臓炎、アレルギー性気管支肺アスペルギルス症、および特発性肺線維症からなる群から選択される疾患または状態を治療するための医薬組成物の製造における、請求項1〜10のいずれか一項に記載の二重特異性抗体の少なくとも1つの使用。
- 前記疾患または状態は、外因性気管支喘息、アレルギー性鼻炎、オンコセルカ皮膚炎、アトピー性皮膚炎、鼻ポリープ症、小結節、好酸球増加症、リウマチ、皮膚炎および腫れ(NERDS)、脈管炎性肉芽腫性疾患、一時的脈管炎、チャーグ・ストラウス症候群、多関節炎、ヴェーゲナー肉芽腫症、多発性硬化症、移植片拒絶、気管支喘息、間質性肺疾患、好酸球性胸膜滲出、一過性肺好酸球浸潤物(Loeffler)、組織球症、慢性好酸球性肺炎、過敏性肺臓炎、アレルギー性気管支肺アスペルギルス症、特発性肺線維症、局所的好酸球増加症、幼児期におけるクラミジア肺炎、好酸球増加症候群、クローン病、春季角結膜炎母斑、若年性炎症結膜炎母斑、および木村病からなる群から選択される請求項13に記載の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US55737704P | 2004-03-30 | 2004-03-30 | |
| US60/557,377 | 2004-03-30 | ||
| PCT/IL2005/000358 WO2005095460A2 (en) | 2004-03-30 | 2005-03-30 | Bi-specific antibodies for targeting cells involved in allergic-type reactions, compositions and uses thereof |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2007537157A JP2007537157A (ja) | 2007-12-20 |
| JP2007537157A5 JP2007537157A5 (ja) | 2008-03-27 |
| JP4939397B2 true JP4939397B2 (ja) | 2012-05-23 |
Family
ID=35064449
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007505735A Expired - Fee Related JP4939397B2 (ja) | 2004-03-30 | 2005-03-30 | アレルギー性反応に関与する細胞を標的化するための二重特異性抗体、ならびにその組成物および使用 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US8133485B2 (ja) |
| EP (1) | EP1730194B1 (ja) |
| JP (1) | JP4939397B2 (ja) |
| AT (1) | ATE531732T1 (ja) |
| ES (1) | ES2375481T3 (ja) |
| WO (1) | WO2005095460A2 (ja) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7754208B2 (en) | 2001-01-17 | 2010-07-13 | Trubion Pharmaceuticals, Inc. | Binding domain-immunoglobulin fusion proteins |
| ITRM20050297A1 (it) * | 2005-06-08 | 2006-12-09 | Univ Siena | Anticorpi diretti contro la proteina basica della mielina che riconoscono un epitopo del cd64 e uso di essi come immunodepressivi. |
| SG155912A1 (en) | 2005-07-25 | 2009-10-29 | Trubion Pharmaceuticals Inc | B-cell reduction using cd37-specific and cd20-specific binding molecules |
| AU2007257692B2 (en) | 2006-06-12 | 2013-11-14 | Aptevo Research And Development Llc | Single-chain multivalent binding proteins with effector function |
| PT2132228E (pt) | 2008-04-11 | 2011-10-11 | Emergent Product Dev Seattle | Imunoterapia de cd37 e sua combinação com um quimioterápico bifuncional |
| JP6149226B2 (ja) | 2010-10-01 | 2017-06-21 | ホーバ セラピューティクス アンパルトセルスカブ | アロディニア、痛覚過敏、自発痛及び幻肢痛の処置 |
| AR085091A1 (es) | 2011-01-26 | 2013-09-11 | Kolltan Pharmaceuticals Inc | Anticuerpos anti-kit y sus usos |
| JP2013079210A (ja) * | 2011-10-04 | 2013-05-02 | Nagoya City Univ | 治療剤、遺伝子治療剤及び好酸球の浸潤抑制方法 |
| DK2808028T3 (da) | 2011-11-21 | 2019-10-07 | Univ Tsukuba | Aktivitetsmodulator, medicinsk middel omfattende samme, anvendelse af mus med cd300a-gen-mangel og anti-cd300a antistof |
| EP3381943B1 (en) | 2012-07-25 | 2022-03-16 | Celldex Therapeutics, Inc. | Anti-kit antibodies and uses thereof |
| EP2918289A4 (en) | 2012-11-07 | 2016-06-15 | Univ Tsukuba | MEDICAMENT WITH MODULATOR OF THE ACTIVITY OF A CD300A EXPRESSIVE CELL RELATED TO ALLERGIC DISEASES, CD300A GENE KNOCKOUT MOUSE, AND USE OF A MODULATOR OF THE ACTIVITY OF A CD300A EXPRESSIVE CELL |
| WO2014188423A1 (en) | 2013-05-21 | 2014-11-27 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Treatment of mast cell related pathologies |
| WO2015058861A1 (en) * | 2013-10-25 | 2015-04-30 | Numab Ag | Bispecific constructs and their use in the treatment of various diseases |
| CN113975386A (zh) | 2014-05-23 | 2022-01-28 | 塞尔德克斯医疗公司 | 嗜酸性粒细胞或肥大细胞相关病症的治疗 |
| CA2959775A1 (en) | 2014-09-08 | 2016-03-17 | Yeda Research And Development Co. Ltd. | Compositions and methods for treating cancer resistant to a tyrosine kinase inhibitor (tki) |
| EP3352760B1 (en) | 2015-09-21 | 2026-03-11 | Aptevo Research and Development LLC | Cd3 binding polypeptides |
| EP3176183A1 (en) | 2015-12-02 | 2017-06-07 | Yeda Research and Development Co. Ltd | Compositions and methods for treating cancer not resistant to a tyrosine kinase inhibitor (tki) |
| EP3841201A1 (en) | 2018-08-24 | 2021-06-30 | Yeda Research and Development Co. Ltd | Methods of modulating m2 macrophage polarization and use of same in therapy |
| US11730762B2 (en) | 2018-08-30 | 2023-08-22 | HCW Biologics, Inc. | Methods for stimulating proliferation or differentiation of an immune cell with a multi-chain chimeric polypeptide |
| CN120535649A (zh) | 2018-08-30 | 2025-08-26 | 免疫生物公司 | 单链嵌合多肽和其用途 |
| US11518792B2 (en) | 2018-08-30 | 2022-12-06 | HCW Biologics, Inc. | Multi-chain chimeric polypeptides and uses thereof |
| JPWO2020166714A1 (ja) * | 2019-02-15 | 2021-12-16 | 国立大学法人愛媛大学 | 複合体化タンパク質、抗体複合体、医薬組成物、および核酸 |
| CN114269903B (zh) | 2019-06-21 | 2025-11-25 | 免疫生物公司 | 多链嵌合多肽和其用途 |
| AU2021220196A1 (en) | 2020-02-11 | 2022-08-04 | HCW Biologics, Inc. | Methods of activating regulatory T cells |
| AU2021219720B2 (en) | 2020-02-11 | 2025-10-02 | Immunitybio, Inc. | Chromatography resin and uses thereof |
| JP2023513573A (ja) | 2020-02-11 | 2023-03-31 | エイチシーダブリュー バイオロジックス インコーポレイテッド | 加齢性および炎症性疾患を治療する方法 |
| JP7734693B2 (ja) | 2020-04-29 | 2025-09-05 | イミュニティーバイオ インコーポレイテッド | 抗cd26タンパク質及びそれらの使用法 |
| IL298608A (en) | 2020-06-01 | 2023-01-01 | Hcw Biologics Inc | Methods for treating disorders related to aging |
| WO2021247003A1 (en) | 2020-06-01 | 2021-12-09 | HCW Biologics, Inc. | Methods of treating aging-related disorders |
| US12024545B2 (en) | 2020-06-01 | 2024-07-02 | HCW Biologics, Inc. | Methods of treating aging-related disorders |
| EP4130028A1 (en) | 2021-08-03 | 2023-02-08 | Rhazes Therapeutics Ltd | Engineered tcr complex and methods of using same |
| JP2024536647A (ja) | 2021-08-03 | 2024-10-07 | ジェニシティー リミテッド | 操作されたtcr複合体及びそれを使用する方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003064662A1 (en) * | 2001-03-16 | 2003-08-07 | Tanox, Inc. | Bispecific molecules cross-linking itim and itam for therapy of allergies |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2321701T3 (es) * | 2001-10-12 | 2009-06-10 | Schering Corporation | Uso de anticuerpos biespecificos que se unen al receptor de activacion fcepsilonri y al receptor de inhibicion ox2ra (cd200ra) para regular respuestas inmunes. |
-
2005
- 2005-03-30 AT AT05718931T patent/ATE531732T1/de active
- 2005-03-30 JP JP2007505735A patent/JP4939397B2/ja not_active Expired - Fee Related
- 2005-03-30 US US10/594,926 patent/US8133485B2/en not_active Expired - Fee Related
- 2005-03-30 EP EP05718931A patent/EP1730194B1/en not_active Expired - Lifetime
- 2005-03-30 ES ES05718931T patent/ES2375481T3/es not_active Expired - Lifetime
- 2005-03-30 WO PCT/IL2005/000358 patent/WO2005095460A2/en not_active Ceased
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003064662A1 (en) * | 2001-03-16 | 2003-08-07 | Tanox, Inc. | Bispecific molecules cross-linking itim and itam for therapy of allergies |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2005095460A3 (en) | 2006-03-30 |
| JP2007537157A (ja) | 2007-12-20 |
| US8133485B2 (en) | 2012-03-13 |
| EP1730194B1 (en) | 2011-11-02 |
| WO2005095460A2 (en) | 2005-10-13 |
| EP1730194A2 (en) | 2006-12-13 |
| US20080219980A1 (en) | 2008-09-11 |
| ES2375481T3 (es) | 2012-03-01 |
| ATE531732T1 (de) | 2011-11-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4939397B2 (ja) | アレルギー性反応に関与する細胞を標的化するための二重特異性抗体、ならびにその組成物および使用 | |
| KR102382804B1 (ko) | 다양한 질환 및 장애의 치료를 위해 masp-3을 억제하는 조성물 및 방법 | |
| CA3176792C (en) | Anti-cd3 and anti-bcma bispecific antibodies wth modified heavy chain constant regions | |
| AU2010217100B2 (en) | Anti-CepsilonmX antibodies capable of binding to human mIgE on B lymphocytes | |
| Hu et al. | Anti-IgE therapy for IgE-mediated allergic diseases: from neutralizing IgE antibodies to eliminating IgE+ B cells | |
| JP6397938B2 (ja) | Bリンパ球のCD23と架橋するが肥満細胞を感作しないヒト化抗IgE抗体 | |
| HK1199405A1 (en) | Humanized antibodies to inkt | |
| Zhang et al. | A recombinant human IgG1 Fc multimer designed to mimic the active fraction of IVIG in autoimmunity | |
| JP2014502962A (ja) | 治療におけるcd89活性化 | |
| US10279034B2 (en) | Anti-PD-L1-anti-TIM-3 bispecific antibodies | |
| WO2005012494A2 (en) | Treatment of organ transplant rejection | |
| TW202332691A (zh) | Ige調節的疾病的治療 | |
| US20210324076A1 (en) | Cd33×cd3 binding proteins for treating inflammatory conditions and diseases | |
| CN101466735A (zh) | 多发性硬化和/或类风湿性关节炎的治疗 | |
| AU2004235595A1 (en) | Human antihuman interleukin-18 antibody, fragment thereof and method of using the same | |
| EP1972640A1 (en) | Apoptosis inducing antibodies | |
| US20260070999A1 (en) | Methods of treating autoimmune disorders using multimeric anti-cd38/anti-cd3 antibodies | |
| KR20230142834A (ko) | 항-cd38 항체 및 이의 용도 | |
| KR102096509B1 (ko) | 항-Tspan12 항체 또는 그의 항원-결합 단편, 및 그의 용도 | |
| Amber et al. | Role of intravenous immunoglobulin in dermatologic disorders | |
| Huang et al. | A novel trivalent non-Fc anti-CD3 Collabody preferentially induces Th1 cell apoptosis in vitro and long-lasting remission in recent-onset diabetic NOD mice | |
| JP7576847B2 (ja) | 免疫応答抑制剤 | |
| RU2797348C2 (ru) | Антитела, содержащие только тяжелые цепи, которые связываются с cd22 | |
| CN118662628A (zh) | 抗ox40抗体在治疗炎症或免疫性疾病中的应用 | |
| Kormelink et al. | Co-crosslinking of immunoglobulin free light chains can enhance IgE-mediated human basophil activation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080207 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080207 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20080310 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20080310 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20080310 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101029 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110126 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111025 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120113 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120203 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120224 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150302 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |