JP4748923B2 - 低温微粉砕による脂質マイクロ粒子 - Google Patents
低温微粉砕による脂質マイクロ粒子 Download PDFInfo
- Publication number
- JP4748923B2 JP4748923B2 JP2002552532A JP2002552532A JP4748923B2 JP 4748923 B2 JP4748923 B2 JP 4748923B2 JP 2002552532 A JP2002552532 A JP 2002552532A JP 2002552532 A JP2002552532 A JP 2002552532A JP 4748923 B2 JP4748923 B2 JP 4748923B2
- Authority
- JP
- Japan
- Prior art keywords
- lipid
- drug
- microparticles
- matrix
- microparticle
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/08—Peptides having 5 to 11 amino acids
- A61K38/09—Luteinising hormone-releasing hormone [LHRH], i.e. Gonadotropin-releasing hormone [GnRH]; Related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/21—Interferons [IFN]
- A61K38/215—IFN-beta
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/145—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/18—Feminine contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/24—Drugs for disorders of the endocrine system of the sex hormones
- A61P5/30—Oestrogens
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Endocrinology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Reproductive Health (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Diabetes (AREA)
- Gynecology & Obstetrics (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Manufacturing Of Micro-Capsules (AREA)
- Peptides Or Proteins (AREA)
Description
本発明は、ペプチドおよび/またはタンパク質の取込みを促進する、両親媒性成分に富む脂質から成る脂質マイクロ粒子、それらを得るための方法、ならびにそれらの使用に関する。低温微粉砕(cryogenic micronization)による製造方法も開示する。
マイクロスフェアは、幾つかの療法分野で高く評価されている薬物送達システムの一例である。それらは本質的に直径1〜500μmの固体粒子であり、血管内に物理的にトラップすることによりそれらの積載薬物をターゲティングさせ(化学的塞栓形成)、かつ制御放出により治療薬の作用を持続させることができる。マイクロスフェアは、タンパク質、多糖、ポリエステルおよび脂質を含めた広範な材料から多様な方法(乳化、熱安定化、コアセルベーションおよび転相などの技術)で製造できる。マイクロスフェアはモノリシック構造をもち、全体が固体であって、リポソームのようなより流体状で軟質の小胞系とは区別できる。マイクロスフェアは普通は直径1〜500μmであり、顆粒(>100μm)と微粒子(<1μm)の間にある。それらは、その内部構造が小胞状ではなく均質なマトリックスであるため、マイクロカプセルと区別される。マイクロスフェアは多数の異なる生体適合性、生物分解性の材料から製造できる;たとえばタンパク質(アルブミンおよびゼラチン)(Biopharm. Drug Dispos. (1985) 6, pp.91-104およびIntern. J. Pharm. (1987) 35, pp.177-179)、ポリエステル(グリコシドおよびラクチド)(J. Microencap. (1986) 3, pp.181-193およびDrug Dev. Ind. Pharm. (1990) 16, pp.2353-2367)、多糖(デンプン、エチルセルロース、アルギナートおよびキトサン)(Drug Dev. Ind. Pharm. (1996) 22, pp.457-463およびJ. Contrl. Rel. (1997) 43, pp.65-74)、イオン交換樹脂(J. Contrl. Rel. (1989) 8, pp.251-257)および脂質(Adv. Drug Deliv. Rev. (1996) 20, pp.209-219)。
−化学的安定化(Biopharm. Drug Dispos. (1985) 6, pp.91-104);
−熱安定化(Experientia (1983) 39, pp.913-916);
−多重エマルジョン溶媒蒸発(J. Contr. Rel. (1994) 28, pp.121-129);
−多重エマルジョン溶媒抽出(J. Contr. Rel. (1997) 43, pp.261-272);
−コアセルベーション(Cancer Res. (1993) 53, pp.5841-5844);
−転相ナノカプセル封入(PIN)(Nature (1997) 386, pp.410-414);
−噴霧乾燥(Pharm. Sci. (1997) 86, pp.603-607)。
この選択は幾つかの要因に依存する:
−必要なマイクロスフェアのサイズ;
−薬物固有の特性、たとえば水溶性および安定性;
−粒子の表面特性、たとえば透過性および電荷;
−生物分解度および生体適合度;
−目的とする薬物放出プロフィル。
薬物がマイクロスフェアから放出される速度は、3つの主な要因に依存する:
−封入される薬物の溶解度および拡散プロセス;
−粒子の浸食および生物分解の速度;
−薬物と粒子マトリックスの、固定化を生じる相互作用。
ポリマーマイクロ粒子は、通常は単一/二重エマルジョン溶媒蒸発、コアセルベーションおよび噴霧乾燥などの方法で製造される。
発明の説明:
特に本発明の主な目的は、薬物および脂質マトリックスを含む新規タイプの脂質マイクロ粒子であって、薬物がペプチドまたはタンパク質であり、脂質マトリックスが脂質マトリックスの重量に対して少なくとも70%w/wのモノグリセリド含量を有することを特徴とする脂質マイクロ粒子を提供することである。
一般に治療上有効であるいかなるペプチドまたはタンパク質も本発明の脂質マイクロ粒子に取り込ませることができる。治療に有用な大部分のタンパク質は3クラスに分類できる:
−調節因子:ホルモン、サイトカイン、リンホカイン、ケモカイン、それらの受容体、ならびに細胞の増殖および代謝を調節する他の因子(酵素を含む)が含まれる;
−血液産物:血清由来の血液因子および酵素性フィブリノーゲン活性化因子が含まれる;
−モノクローナル抗体。
本発明の特に好ましい態様において、限定ではないがペプチドのリストには下記の化合物が含まれる:
−アバレリックス(Abarelix)(WO96/40757号に開示):LHRHアンタゴニストとして作用し、次式により定められる:
D−アラニンアミド,N−アセチル−3−(2−ナフタレニル)−D−Ala−4−Cl−D−Phe−3−(3−ピリジニル)−D−Ala−L−Ser−N−メチル−L−Tyr−D−Asn−L−Leu−N6−(1−メチルエチル)−L−Lys−L−Pro。
D−アラニンアミド,N−アセチル−3−(2−ナフタレニル)−D−Ala−4−Cl−D−Phe−3−(3−ピリジニル)−D−Ala−L−Ser−L−Tyr−N6−(アミノカルボニル)−D−Lys−L−Leu−N6−(1−メチルエチル)−L−Lys−L−Pro。
D−アラニンアミド,N−アセチル−3−(2−ナフタレニル)−D−Ala−4−Cl−D−Phe−3−(3−ピリジニル)−D−Ala−L−Ser−4−[(5−アミノ−1H−1,2,4−トリアゾール−3−イル)アミノ]−L−Phe−4−[(5−アミノ−1H−1,2,4−トリアゾール−3−イル)アミノ]−D−Phe−L−Leu−N6−(1−メチルエチル)−L−Lys−L−Pro。
D−アラニンアミド,N−アセチル−3−(2−ナフタレニル)−D−Ala−4−Cl−D−Phe−3−(3−ピリジニル)−D−Ala−L−Ser−L−Tyr−N6−[ビス(エチルアミノ)メチレン]−D−Lys−L−Leu−N6−[ビス(エチルアミノ)メチレン]−L−Lys−L−Pro。
経口投与に適した液体剤形は、好適な水性または非水性ビヒクル、ならびに緩衝剤、沈殿防止剤および分散剤、着色剤、着香剤などを含有できる。
本発明の他の目的は、前記のペプチドまたはタンパク質を充填した脂質マイクロ粒子を製造する方法である。本発明のペプチドまたはタンパク質を充填した脂質マイクロ粒子は、好ましい製造方法によれば、生物活性物質、好ましくはペプチドを含む脂質マイクロ粒子を製造するための新規な低温微粉砕法により製造でき、医薬組成物として使用できる。
−溶媒に溶解して薬物を脂質に充填し;
−溶媒を除去し;
−薬物充填した脂質マトリックスを冷却し;
−こうして得た材料のサイズを摩砕(grinding)により予備縮小し;
−冷却後に低温微粉砕を実施し、粉砕およびふるい分けする。
−ペプチドを融解脂質に充填し;
−薬物充填した脂質マトリックスを冷却し;
−こうして得た材料のサイズを摩砕により予備縮小し;
−冷却後に低温微粉砕を実施し、粉砕およびふるい分けする。
最終工程の前に述べた摩砕プロセスに関して、この摩砕は医薬固体剤形の製造に際して粉末の粒度を低下させるための基本的方法である(Lachman L. and Lieberman H., Lea & Febiger (1986) pp.21-46)。しかし最近の装置改良により(高速ミル、ミクロナイザー、インライン分級機)、現在では制御された寸法および粒度分布をもつミクロンおよびミクロン以下の範囲の粒子を粉砕により得ることができる。
したがって微粉砕は、脂質材料のマイクロ粒子を得るための製造方法において、特にペプチド/タンパク質を取り込ませなければならない場合、顕著な利点をもたらす別法とみることができる。
−有機溶媒に共溶解して脂質にペプチドを充填し;
−溶媒を除去し;
−薬物充填した脂質マトリックスを冷却し;
−こうして得たマトリックスのサイズを摩砕により予備縮小し;
−低温微粉砕を実施し;
−こうして得たマイクロ粒子を粉砕およびふるい分けする。
本発明の好ましい製造方法によれば、ペプチド充填した脂質マイクロ粒子は下記の工程を含む共融法により製造される:
−ペプチドを融解脂質に充填し;
−薬物充填した脂質マトリックスを冷却し;
−こうして得たマトリックスのサイズを摩砕により予備縮小し;
−低温微粉砕を実施し;
−こうして得たマイクロ粒子を粉砕およびふるい分けする。
低温微粉砕工程においては、薬物充填した脂質マトリックスを微粉砕する前に、液体窒素注入により−196〜0℃、好ましくは−80〜−20℃、より好ましくは−50〜−30℃の温度に冷却する。こうして得たマイクロ粒子のサイズは1〜500μm、好ましくは1〜300μm、より好ましくは1〜100μm、特に5〜50μmである。
「AAT」は、α−1−アンチトリプシンを表わす。
「アンタイド」(提示されたINNはIturelix)は、下記のデカペプチドを表わす;
N−Ac−D−2−Nal,D−pClPhe,D−3−Pal,Ser,NicLys,D−NicLys,Leu,Ilys,Pro,D−Ala,NH2。
「2−Nal」は、3−(2−ナフチル)アラニンを表わす。
「Ilys」は、N−イソプロピルリジンを表わす。
「3−Pal」は、3−(3−ピリジル)アラニンを表わす。
「DMPC」は、ジミリストイルホスファチジルコリンを表わす。
「第VIII因子」は、2331個のアミノ酸を含有する糖タンパク質を表わす。
「FSH」は、卵胞刺激ホルモンを表わす。
「グリセリド」は、C4〜C30の飽和または不飽和脂肪酸のグリセロールエステルを意味するものとする。
「GnRH」は、ゴナドトロピン放出ホルモンを表わす。
「HPH」は、高圧均質化を表わす。
「LHRH」は、黄体形成ホルモン放出ホルモンを表わす。
「脂質」は、本発明によれば、水には難溶性であるが有機溶媒には可溶性である物質を表わす。本発明によれば、脂質には脂肪酸、モノ−、ジ−およびトリ−グリセリド、リン脂質、PEG−グリセリド、糖−グリセリドまたはろう、並びにそのいずれかの混合物が含まれる。本発明によれば、脂質マトリックスは常に医薬的に許容できるものとする。
「マイクロ粒子」は、その平均直径が3〜500μmにある粒子を表わす。
「モノグリセリド」は、下記に示すようにグリセロールアルコール官能基の1つを脂肪酸でエステル化することにより:
CH2OH−CHOH−CH2OH → CH2OCOR1−CHOH−CH2OH
グリセロール モノグリセリド
(式中のR1はC4〜C30の飽和または不飽和炭化水素鎖である)、またはトリグリセリドの加水分解により得られる化合物を表わす。
「PCS」は、光子相関分光分析を表わす。
「PEG」は、ポリエチレングリコールを表わす。
「タンパク質」は、ポリペプチドアミノ酸配列を含む分子を表わす。ペプチドとタンパク質の主な相異はサイズの相異である。本発明によれば、ペプチドは100個以下のアミノ酸を含有し、一方タンパク質は100個を超えるアミノ酸を含有する。
「糖(糖質)」は、少なくとも2個のヒドロキシル基をもつアルデヒド基またはケトン基を表わす。糖は幾つかの形態をとる:モノマー形(単糖)、ダイマー形(二糖)、トリマー形(三糖)、オリゴマー(オリゴ糖)およびポリマー(多糖)。
「溶媒ストリッピング法」は、溶媒に溶解した薬物(すなわちペプチド)を、融解または溶媒中で溶解した担体材料(すなわち脂質)に充填する方法を表わす。
「tPA」は、組織プラスミノーゲン活性化因子を表わす。
「UK」は、ウロキナーゼを表わす。
本発明を幾つかの実施例により説明する。これらは、種々の脂質に各種方法を採用して種々の薬物を充填し、異なる放出速度を得るのが可能であることを証明する。ただしこれらは本発明の範囲を限定するためのものではない。実施例では添付の図面を参照する。
以下に報告する実施例で用いたペプチドはアンタイドである。このペプチドは、下記のデータが証明するように両親媒性をもつ。
数種類の脂質中におけるアンタイド準定量的溶解度評価の結果を、脂質モノグリセリド含量と共に表1に示す。
アンタイドバルク、Bachem。
Imwitor 900(グリセリルモノステアレート)、Condea Chemie−DE。
Compritol 888 ATO(グリセリルベヘネート)、Gattefosse−FR。
Imwitor 312(ラウリン酸モノグリセリド)、Condea Chemie−DE。
Geleol(グリセリル モノ−パルミテート/ステアレート)、Gattefosse−FR。
Compritol HD 5 ATO(グリセリル/ポリエチレングリコール ベヘネート)、Gattefosse−FR。
Precirol ATO 5(グリセリルモノ−/ジ−/トリ−パルミテート/ステアレート)、Gattefosse−FR。
Softisan 142(水素化ヤシグリセリド)、Condea Chemie−DE。
Gelot 64(グリセリル/ポリエチレングリコールパルミテート/ステアレート)、Gattefosse−FR。
Gelucire 44/14(特定ブレンド:グリセロールおよびポリエチレングリコールのラウリン酸モノ−/ジ−/トリ−エステル)、Gattefosse−FR。
セチルアルコール、Sigma。
ベンジルアルコール、Sigma−USA。
IFN−β液体製剤(REBIF(登録商標)−Serono)。
自動ふるいシステム、Retsch AS 200。
Waters HPLCシステム:2690分離モジュール;RPカラム、Jupiter 5μm C18(250×4.6mm、5μm);2487二重λ吸光度検出器
低温ミル−Apex、Mod.MPX3:下記のように特注:
これらの試験に用いた低温ミルは、冷却ガス(すなわち液体窒素)をチャンバーへ導入するのに適したノズルを備えた一般的なハンマーミルである。予備摩砕試験後、本発明者らの要求にさらに適切なものにするためにミルを特注した。下記の改変を行った:
−粉砕チャンバーの温度測定のために検温プローブを導入した;
−粉砕チャンバーからの粉末損失を避けるために底スクリーンを盲ブレードでシールした;
−粉砕チャンバーへの粉末導入のためにピストンを取り付けた;
−断熱パイプで液体窒素タンクに接続した。
重量比2:98のペプチド(アンタイド)および脂質(Compritol E ATO)を85℃で有機溶媒(ベンジルアルコールとエタノールの混合物、1:5)に撹拌下で溶解した。溶媒を真空下に80℃で蒸発させた。次いで脂質マトリックスを室温に冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
重量比2:98のペプチド(アンタイド)および脂質(Imwitor 900)を80℃で有機溶媒(ベンジルアルコールとエタノールの混合物、1:2)に撹拌下で溶解した。溶媒を真空下に60℃で蒸発させた。次いで脂質マトリックスを室温に冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
ペプチド(アンタイド)を融解脂質(Compritol E ATO)に撹拌下で取り込ませた(薬物−脂質重量比は2:98)。次いで脂質マトリックスを氷浴中で冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
脂質(Imwitor 900)をその融点より15℃高い温度で融解させた。次いでペプチド(アンタイド)を融解脂質に撹拌下で取り込ませた(薬物−脂質重量比は2:98)。次いで脂質マトリックスを氷浴中で冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
粉末状のImwitor 900とImwitor 312を固体状態で混合し、次いで58℃±2℃に温度調節した水浴中で共融させた。IFN−β液体製剤(245μg/mL)を、58℃±2℃に保持した融解脂質に添加し、穏やかに撹拌しながら20分以内に溶解させた。次いでこの素材を室温で放冷し、手動で粗い粒子に砕き、−80℃に保存した。粉砕前にIFN−β脂質製剤を少なくとも12時間、−80℃に保持した。操作条件としてローター速度18000rpmおよびスクリーンサイズ0.5mmを用いて摩砕を実施した。摩砕した材料を4℃に保持した。レーザー回折計を用いて脂質マイクロ粒子特性をその粒度分布により解明した。粒度分析結果を表6に報告する。
重量比1:9のペプチド(アンタイド)および脂質(Compritol E ATO)を85℃で有機溶媒(ベンジルアルコール)に撹拌下で溶解した。溶媒を真空下に85℃で蒸発させた。次いで脂質マトリックスを室温に冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
重量比1:4のペプチド(アンタイド)および脂質(Compritol E ATO)を85℃で有機溶媒(ベンジルアルコール)に撹拌下で溶解した。溶媒を真空下に85℃で蒸発させた。次いで脂質マトリックスを室温に冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
ペプチド(アンタイド)を融解脂質(Compritol 888 ATO)に撹拌下で取り込ませた(薬物−脂質重量比は2:98)。次いで脂質マトリックスを氷浴中で冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
重量比2:98のペプチド(アンタイド)および脂質(Compritol 888 ATO)を85℃で有機溶媒(ベンジルアルコール)に撹拌下で溶解した。溶媒を真空下に85℃で蒸発させた。次いで脂質マトリックスを室温に冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。
重量比1:9のペプチド(アンタイド)および脂質(Compritol 888 ATO)を85℃で有機溶媒(ベンジルアルコール)に撹拌下で溶解した。溶媒を真空下に85℃で蒸発させた。次いで脂質マトリックスを室温に冷却し、予備摩砕し、そして低温条件下で微粉砕した。最後にマイクロスフェアを125μmでふるい分けし、採集した。実施例1〜10の記載に従って製造した脂質マイクロ粒子の特性解明を以下に報告する。
脂質マイクロ粒子のアンタイド含量をRP−HPLCにより測定した:アンタイド充填した脂質マイクロ粒子50mgをまず5mLのアセトンに溶解し、振とうし、2分間超音波処理した。5mLの蒸留水をアセトン溶液に添加した。得られた混合物を2分間超音波処理し、次いで8000rpmで15分間遠心した。
実施例12: 脂質マトリックス内におけるペプチド安定性の測定
2種類のアンタイド充填Imwitor 900配合物について、前の節の記載に従ってt=0およびt=3カ月目に脂質マイクロ粒子の薬物含量をRP−HPLCにより測定した。結果を表3に示す。
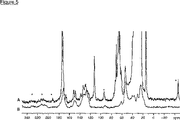
脂質マイクロ粒子の完全な物理化学的特性解明を、それらの粒度分布(レーザー回折計分析)、脂質マトリックスの表面分析、およびNMR検査を評価することにより行った。125μm未満の粒子は皮下投与に適するので、その画分の重量収率も測定した。
− D(v,0.1)=10%(体積)の粒子がこの数値未満のサイズをもつ;
− D(v,0.5)=50%(体積)の粒子がこの数値未満のサイズをもつ;
− D(v,0.9)=90%(体積)の粒子がこの数値未満のサイズをもつ;
の例を、図3および表4に示す。これらから分かるように、両方の製造方法で同様なマイクロ粒子粒度分布が得られ、主に1〜125μmからなっていた。
脂質マイクロ粒子からのアンタイド放出を、放出媒体として水(保存剤として+NaN3 0.05%)またはPBS(リン酸塩緩衝塩類溶液)を用いて評価した。約40mgの脂質マイクロ粒子を20mLの放出媒体に懸濁して実験を行った。これらの懸濁液を37℃に温度調節した水浴中で撹拌し続けた。テフロン(登録商標)注射器および0.2μmAcrodiscフィルターを用いて、1mLの試料を種々の時点で取り出した。濾過した脂質マイクロ粒子を容器に戻し、等量の放出媒体を再導入した。
実施例15: in vitroアッセイ
図2に示す結果から、脂質マイクロ粒子製造方法が薬物活性を大きく変化させないことが確認される。これは、下記に従って実施したラット下垂体細胞アッセイにおいて証明された。
ラット下垂体細胞において脂質マイクロ粒子によるin vitroLH分泌阻害を評価することにより、本発明のマイクロ粒子製造方法はペプチドの生物学的統合性を低下させないことが証明された。図1の結果は、試験した製剤においてアンタイドの生物活性が保持されていることを示す。
成体(63〜70日齢および約300g)Sprague Dawley雄ラットをこの試験に用いた。飼料をすべての動物に「自由」摂取させた。飲料水も動物に「自由」摂取させた。
下記の実験計画に従った。
配合物2:アンタイド(2%w/w)−Imwitor 900(ストリッピング)
配合物3:アンタイド(2%w/w)−Compritol E ATO(共融)
配合物4:アンタイド(2%w/w)−Imwitor 900(共融)。
第1〜5群の動物から約0.5〜1mlの血液を、8時間までの各サンプリング時間に舌下または尾静脈より採取した。24時間目(第1群については72時間)に動物をエーテルで麻酔し、腹部大動脈からの放血により殺した。
ヘパリン添加試験管内に血液を採集し、4℃での遠心(2500×g)により血漿を分離した。殺した時点で得た血漿を少なくとも1mlずつ3つのアリコートに分割した。
殺した時点で得たすべての血漿試料について、薬理マーカーであるテストステロンを測定した。
アンタイドおよびテストステロン血漿レベルを、投与後の異なる時点で測定した。それらの結果を図8および図9に示す。in vitro溶解速度試験でみられた「バースト低下」が、最初の24時間以内に血漿プロフィルから確認される。1カ月間の観察中、薬物のPKプロフィルおよびテストステロン抑制に及ぼすPD作用の両方とも、送達システムの持続放出性能と一致した。
Claims (15)
- 薬物および脂質マトリックスを含む脂質マイクロ粒子であって、該薬物がLHRHアンタゴニストとして作用するデカペプチド及びIFN−βから成る群より選択され、該脂質マトリックスが該脂質マトリックスの重量に対して少なくとも70%w/wのモノグリセリド含量を有し、該マイクロ粒子が、該脂質及び該薬物を含有する混合物の−196〜0℃の温度における低温微粉砕によって製造されることを特徴とする脂質マイクロ粒子。
- 該モノグリセリド含量が脂質マトリックスの重量に対して75〜99%w/wであることを特徴とする、請求項1に記載の脂質マイクロ粒子。
- 該デカペプチドが、N−Ac−D−2−Nal,D−pClPhe,D−3−Pal,Ser,NicLys,D−NicLys,Leu,Ilys,Pro,D−Ala,NH2であることを特徴とする、請求項1または2に記載の脂質マイクロ粒子。
- 該デカペプチドがセトロレリックスであることを特徴とする、請求項1または2に記載の脂質マイクロ粒子。
- 該マイクロ粒子が他の医薬的に許容できる賦形剤をも含むことを特徴とする、請求項1〜4のいずれか1項に記載の脂質マイクロ粒子。
- 該賦形剤が、アクリルポリマー、中鎖脂肪酸およびポリエチレングリコールよりなる群から選択される、生体接着性または吸収増強性を有するポリマーであることを特徴とする、請求項5に記載の脂質マイクロ粒子。
- 該マイクロ粒子が3〜500μmの平均直径を有することを特徴とする、請求項1〜6のいずれか1項に記載の脂質マイクロ粒子。
- 医薬として使用するための、請求項1〜7のいずれか1項に記載の脂質マイクロ粒子。
- 請求項1〜8のいずれか1項に記載の脂質マイクロ粒子、および医薬的に許容できる担体、希釈剤または賦形剤を含有する、医薬組成物。
- 請求項1〜8のいずれか1項に記載の脂質マイクロ粒子の製造方法であって、脂質及び薬物を含有する混合物を−196〜0℃の温度で粉砕することによって低温微粉砕を実施する工程を含む方法。
- 低温微粉砕の温度が−80〜−20℃である、請求項10に記載の方法。
- 低温微粉砕の温度が−50〜−30℃である、請求項10または11に記載の方法。
- 低温微粉砕後にふるい分け工程を含む、請求項10〜12のいずれか1項に記載の方法。
- 低温微粉砕の前に、摩砕によるサイズ予備縮小工程を含む、請求項10〜13のいずれか1項に記載の方法。
- 脂質及び薬物を含有する混合物の冷却を液体窒素注入により実施することを特徴とする、請求項10〜14のいずれか1項に記載の方法。
========================================
本件に関するお問合せは、下記までお願いします。
ユアサハラ法律特許事務所 特許国内事務担当
TEL (03) 3270-6641 内線405 / FAX (03) 3246-0233
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP00128556.8 | 2000-12-27 | ||
| EP00128556 | 2000-12-27 | ||
| EP01125741.7 | 2001-10-26 | ||
| EP01125741 | 2001-10-26 | ||
| PCT/EP2001/014890 WO2002051386A2 (en) | 2000-12-27 | 2001-12-17 | Lipid microparticles by cryogenic micronization |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004529864A JP2004529864A (ja) | 2004-09-30 |
| JP4748923B2 true JP4748923B2 (ja) | 2011-08-17 |
Family
ID=26071690
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002552532A Expired - Fee Related JP4748923B2 (ja) | 2000-12-27 | 2001-12-17 | 低温微粉砕による脂質マイクロ粒子 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US7704525B2 (ja) |
| JP (1) | JP4748923B2 (ja) |
| AR (1) | AR032074A1 (ja) |
| AT (1) | ATE373471T1 (ja) |
| AU (1) | AU2002219198B2 (ja) |
| CA (1) | CA2431890C (ja) |
| DE (1) | DE60130580T2 (ja) |
| DK (1) | DK1345593T3 (ja) |
| ES (1) | ES2290095T3 (ja) |
| IL (2) | IL156532A0 (ja) |
| PT (1) | PT1345593E (ja) |
| WO (1) | WO2002051386A2 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8067032B2 (en) | 2000-12-22 | 2011-11-29 | Baxter International Inc. | Method for preparing submicron particles of antineoplastic agents |
| US9700866B2 (en) | 2000-12-22 | 2017-07-11 | Baxter International Inc. | Surfactant systems for delivery of organic compounds |
| IL160570A0 (en) | 2001-09-26 | 2004-07-25 | Baxter Int | Preparation of submicron sized nanoparticles via dispersion and solvent or liquid phase removal |
| US20060003012A9 (en) | 2001-09-26 | 2006-01-05 | Sean Brynjelsen | Preparation of submicron solid particle suspensions by sonication of multiphase systems |
| US7879320B2 (en) | 2004-05-17 | 2011-02-01 | Ares Trading S.A. | Hydrogel interferon formulations |
| EA010979B1 (ru) | 2004-06-01 | 2008-12-30 | Арес Трейдинг С.А. | Стабилизированные жидкие препаративные формы интерферона |
| WO2009080699A2 (en) | 2007-12-20 | 2009-07-02 | Merck Serono S.A. | Peg-interferon-beta formulations |
| WO2012059936A1 (en) | 2010-11-03 | 2012-05-10 | Padma Venkitachalam Devarajan | Pharmaceutical compositions for colloidal drug delivery |
| US9505771B2 (en) * | 2011-05-18 | 2016-11-29 | Laboratories Lesvi S.L. | Stable micronised monoclin form of asenapine maleate and its synthesis |
| DE102013224627A1 (de) | 2013-11-29 | 2015-06-03 | Andreas Lauterbach | Pharmazeutische Formulierung mit Lipidmikropartikeln und Herstellungsverfahren |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3024416C2 (de) | 1980-06-28 | 1982-04-15 | Gödecke AG, 1000 Berlin | Verfahren zur Herstellung von Arzneimitteln mit retardierter Wirkstoff-Freisetzung |
| US4610868A (en) | 1984-03-20 | 1986-09-09 | The Liposome Company, Inc. | Lipid matrix carriers for use in drug delivery systems |
| US4837381A (en) | 1986-08-11 | 1989-06-06 | American Cyanamid Company | Compositions for parenteral administration and their use |
| ATE74009T1 (de) * | 1986-08-11 | 1992-04-15 | American Cyanamid Co | Zusammensetzungen zur parenteralen verabreichung und deren verwendung. |
| US4935491A (en) * | 1987-08-24 | 1990-06-19 | Board Of Regents, The University Of Texas System | Effective antagonists of the luteinizing hormone releasing hormone which release negligible histamine |
| GB2209937B (en) | 1987-09-21 | 1991-07-03 | Depiopharm S A | Water insoluble polypeptides |
| IE904098A1 (en) * | 1989-11-13 | 1991-05-22 | Nova Pharm Corp | Lipospheres for controlled delivery of substances |
| AU658608B2 (en) * | 1991-03-25 | 1995-04-27 | Astellas Pharma Europe B.V. | Topical preparation containing a suspension of solid lipid particles |
| AU692506B2 (en) * | 1993-11-17 | 1998-06-11 | Ibah, Inc. | Transparent liquid for encapsulated drug delivery |
| US5430021A (en) * | 1994-03-18 | 1995-07-04 | Pharmavene, Inc. | Hydrophobic drug delivery systems |
| DE19819273A1 (de) * | 1998-04-30 | 1999-11-11 | Pharmatec International S Giul | Pharmazeutische Ciclosporin-Formulierung mit verbesserten biopharmazeutischen Eigenschaften, erhöhter physikalischer Qualität und Stabilität sowie Verfahren zur Herstellung |
-
2001
- 2001-12-17 DE DE60130580T patent/DE60130580T2/de not_active Expired - Lifetime
- 2001-12-17 CA CA2431890A patent/CA2431890C/en not_active Expired - Fee Related
- 2001-12-17 US US10/451,676 patent/US7704525B2/en not_active Expired - Fee Related
- 2001-12-17 AT AT01272020T patent/ATE373471T1/de active
- 2001-12-17 AU AU2002219198A patent/AU2002219198B2/en not_active Ceased
- 2001-12-17 JP JP2002552532A patent/JP4748923B2/ja not_active Expired - Fee Related
- 2001-12-17 IL IL15653201A patent/IL156532A0/xx unknown
- 2001-12-17 WO PCT/EP2001/014890 patent/WO2002051386A2/en active IP Right Grant
- 2001-12-17 PT PT01272020T patent/PT1345593E/pt unknown
- 2001-12-17 DK DK01272020T patent/DK1345593T3/da active
- 2001-12-17 ES ES01272020T patent/ES2290095T3/es not_active Expired - Lifetime
- 2001-12-27 AR ARP010106067A patent/AR032074A1/es active IP Right Grant
-
2003
- 2003-06-19 IL IL156532A patent/IL156532A/en not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| US7704525B2 (en) | 2010-04-27 |
| AR032074A1 (es) | 2003-10-22 |
| PT1345593E (pt) | 2007-10-10 |
| ATE373471T1 (de) | 2007-10-15 |
| CA2431890C (en) | 2011-05-10 |
| JP2004529864A (ja) | 2004-09-30 |
| AU2002219198B2 (en) | 2006-06-29 |
| DE60130580D1 (de) | 2007-10-31 |
| IL156532A0 (en) | 2004-01-04 |
| DK1345593T3 (da) | 2007-12-10 |
| IL156532A (en) | 2011-04-28 |
| WO2002051386A3 (en) | 2002-10-10 |
| US20040091522A1 (en) | 2004-05-13 |
| WO2002051386A2 (en) | 2002-07-04 |
| ES2290095T3 (es) | 2008-02-16 |
| DE60130580T2 (de) | 2008-06-12 |
| CA2431890A1 (en) | 2002-07-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4072057B2 (ja) | ペプチド及び/またはタンパク質取り込み用の両親媒性脂質ナノ粒子 | |
| AU2002226374A1 (en) | Amphiphilic lipid nanoparticles for peptide and/or protein incorporation | |
| CA2412885C (en) | Porous celecoxib matrices and methods of manufacture thereof | |
| JP4819173B2 (ja) | 徐放性組成物およびその製造法 | |
| JP6078660B2 (ja) | GnRH誘導体の徐放性脂質初期製剤およびこれを含む薬剤学的組成物 | |
| JP4748923B2 (ja) | 低温微粉砕による脂質マイクロ粒子 | |
| JP4927729B2 (ja) | 性腺刺激ホルモン放出ホルモンアンタゴニスト | |
| SK15612003A3 (sk) | Prípravok s trvalým uvoľňovaním a spôsob jeho výroby | |
| CN101903014A (zh) | 固体内核中包含生长激素的固体脂质微囊 | |
| EP0256726B1 (en) | Encapsulation of trh or its analog | |
| AU2002219198A1 (en) | Lipid microparticles by cryogenic micronization | |
| JPH10273447A (ja) | 徐放性マイクロスフィア、その製造法および用途 | |
| EP1345593B1 (en) | Lipid microparticles by cryogenic micronization | |
| CN109419771B (zh) | 十一酸睾酮缓释药物组合物、其制备方法及用途 | |
| Traub-Hoffmann et al. | Spray congealed solid lipid microparticles as a sustained release delivery system for Gonadorelin [6-D-Phe]: Production, optimization and in vitro release behavior | |
| JPH11503466A (ja) | 排卵開始薬 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040818 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20071012 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080115 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080122 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080212 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20080307 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20080821 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20081121 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110125 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110131 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110517 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140527 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |