JP4536986B2 - 腫瘍からの同時多数マーカー放射(casmmen)に基づいた細胞解析を行う装置 - Google Patents
腫瘍からの同時多数マーカー放射(casmmen)に基づいた細胞解析を行う装置 Download PDFInfo
- Publication number
- JP4536986B2 JP4536986B2 JP2001536559A JP2001536559A JP4536986B2 JP 4536986 B2 JP4536986 B2 JP 4536986B2 JP 2001536559 A JP2001536559 A JP 2001536559A JP 2001536559 A JP2001536559 A JP 2001536559A JP 4536986 B2 JP4536986 B2 JP 4536986B2
- Authority
- JP
- Japan
- Prior art keywords
- sample
- block
- control processor
- wavelength
- imaging system
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6456—Spatial resolved fluorescence measurements; Imaging
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6408—Fluorescence; Phosphorescence with measurement of decay time, time resolved fluorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/58—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving labelled substances
- G01N33/582—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving labelled substances with fluorescent label
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
- G01N2021/6439—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks
- G01N2021/6441—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks with two or more labels
Description
【発明の属する技術分野】
本発明は光学システムおよび方法、特に腫瘍(ネオプラシア)からの同時的な多数のマーカー放射をベースとした癌の解析を実行するイメージングシステムに関する。
【0002】
【従来の技術】
異なるタイプの腫瘍細胞が対応するタイプのプロテインを発生することが知られている。特定のタイプのプロテインがサンプルに含まれるか否かを決定するため組織サンプルを試験し、それによってサンプルが癌性の細胞に関連するタイプを含んでいるか否かの決定をさらに行うことも知られている。例えば、このタイプの試験を行う通常の技術はサンプルに特別なタイプの抗体および関連する蛍光材料(“マーカー”とも呼ぶ)を配備することを含んでいる。通常、癌性細胞および対応するタイプのプロテインがサンプルに含まれていることを想定すると、配備された抗体およびマーカーは1以上のプロテインに結合される。その後、通常のイメージングシステムを使用して、マーカーを“励起”することが知られている特別な波長を使用してサンプルは照射され、マーカーを蛍光発光させ、特定の波長の蛍光放射を放射させる。例えばイメージングシステムの放射検出器アレイコンポーネントを使用して放射された放射の波長を検出することにより、サンプルが実際にプロテインおよび関連する癌性細胞を含んでいことかの決定が行われる。そうでなければ、癌性細胞および関連するプロテインがサンプルに含まれていないならば、抗体およびマーカーは通常、イメージングシステム内の“励起”波長を使用して検出されることができない。
【0003】
残念ながら、前述したような技術を実行する通常のイメージングシステムは、単一のタイプのプロテインが存在する場合についてしかサンプルを一度に試験することができない欠点を有し、多数の励起波長ではなく、ただ1つの単一の“励起”波長だけが典型的に一度に使用される。この理由の1つは、通常のイメージングシステムは多数のマーカーが多数の励起波長を使用して励起される場合に生じる光の散乱のような不所望な光現象の影響を最少にするコンポーネントを典型的に含まないことである。結果として、マーカー放射波長検出がサンプル中のプロテインの存在を示すか否かについての正確な決定が行われることができない。通常のイメージングシステムの別の欠点は、放射された波長が類似であり同時に放射される場合に、これらのシステムが異なるタイプのマーカーにより放射された波長を弁別できないことである。例えば、ルシフェルイエローCHおよびカルシウムグリーンのようなマーカーが通常のイメージングシステムを用いて試験されるサンプルで使用され、マーカーに533nmの類似の波長値を有する蛍光放射を同時に放射させるような波長でこれらのマーカーが照射されると仮定すると、通常のイメージングシステムはこれらのマーカーの一方または両者が照射に応答して実際に蛍光発光したか否かを決定することはできない。結果として、プロテインがサンプルに含まれるか否かについての正確な決定は行われることができない。
【0004】
通常のイメージングシステムは、複数のタイプのプロテインがサンプルに存在するか否かを決定することが所望である場合に、複数の単タイプのプロテインが存在するかについて一度に組織サンプルを試験できないので、試験を受ける各タイプのプロテインを個別に試験するため他の個々のタイプのマーカーをサンプルへ付加することが必要である。代わりに、他の組織サンプルは各タイプのプロテインについて前述の解析を行う目的で、採取される必要がある。認識されるように、これらの代りのもののいずれも特に多数の異なるタイプの癌に関連するプロテインの存在についてサンプルを試験することが必要である場合、サンプルを解析する人に対して過剰な重荷を与える。
【0005】
前述の説明を考慮して、従来技術のイメージングシステムに関する問題および欠点を克服するような方法で組織サンプルの癌解析を実行するためのイメージングシステムの提供が有効であることが認識される。
【0006】
【発明が解決しようとする課題】
本発明の目的は、組織サンプルの癌解析を行うための改良されたイメージングシステムを提供することである。
【0007】
本発明の別の目的は、組織サンプルが癌に関連するプロテインを含んでいるか否かを決定するために組織サンプルを解析し、狭帯域または広帯域のいずれかの励起波長を使用して多数のタイプのプロテインの存在について同時にサンプルが解析されるような方法でこの解析を実行するイメージングシステムを提供することである。
【0008】
本発明の別の目的は、癌に関連するプロテインが、1以上の励起波長による照射に応答して蛍光材料により放射された蛍光放射波長の評価に基づいて、蛍光材料を含む組織サンプルに含まれるか否かを識別できるイメージングシステムを提供することであり、それにおいて、識別は蛍光材料が類似または異なる蛍光放射波長を放射するか否かについて行われることができる。
【0009】
本発明の更に別の目的および利点は、図面および以下の説明を考慮することによって明白になるであろう。
【0010】
【課題を解決するための手段】
前述および他の問題は克服され、本発明の目的は、1以上の癌に関連するプロテインが組織サンプル中に存在するか否かについて決定するため本発明にしたがった方法および装置により実現される。本発明の方法は、組織サンプル中に多数のタイプの蛍光材料を配備するステップを含んでいる。多数のタイプの蛍光材料は対応するタイプのプロテインに結合し、これらのプロテインはサンプルに含まれると仮定される。次のステップは組織サンプルを少なくとも1つの励起波長で照射して、少なくとも幾らかの蛍光材料にそれぞれの特徴的な放射波長で放射させるステップを含んでいる。次のステップは、これらの蛍光材料により放射されるそれぞれの特徴的な放射波長を同時に検出し、その後、それぞれの特徴的な放射波長をそれぞれの信号に変換するステップを含んでいる。信号は蛍光材料により放射されるそれぞれの特徴的な放射波長に対応する。次に、信号の振幅を検出し、対応する振幅プロフィールを発生するステップが実行される。さらに、ステップは少なくとも1つの検出された振幅が予め定められたしきい値レベルを超えることを決定し、少なくとも1つの検出された振幅が予め定められたしきい値レベルを超えるという決定に応答して、少なくとも1つの癌に関連するプロテインが組織サンプル内に存在することを示すステップを含んでいる。
【0011】
本発明の別の特徴にしたがって、サンプルに含まれる特別なタイプのプロテインは本発明のスペクトルおよび時間解析を使用して識別される。その解析は同時的な識別がサンプルに含まれる多数のタイプのプロテインについて行われることを可能にする。時間解析はマーカー蛍光放射応答“ライフタイム”が記録されることを可能にし、任意のスペクトル的にオーバーラップする検出された蛍光応答が評価され区別されることを可能にする。
【0012】
【発明の実施の形態】
本発明の前述および他の特徴は添付図面を伴って以下の本発明の詳細な説明を読むことによりさらに明白になるであろう。
異なる図面で見られる同一のラベルを付けられた素子は同一素子を表すが、全ての図面の説明で参照されるものではない。
【0013】
基体4の例示的な表示が図6のaで示されている。このように、基体は以後
“スライド4”と呼ばれる。スライド4は、ネオプラシス(即ち腫瘍)細胞であり得る組織細胞40' (例えば人間の組織細胞)からなるサンプル4aを含むことを想定される。本発明の目的に対して、任意の細胞40' が癌性であるか否かを確実にし、また存在するならばサンプル4aに存在する癌細胞の特定のタイプを識別することが所望であることが想定される。本発明にしたがって、サンプル4aが種々のタイプの癌細胞および癌に関連するプロテインの存在について同時に検査されることを可能にし、またプロテインが識別されることを可能にする方法および装置が提供される。試験は最初にサンプル4aに特定のタイプの蛍光材料
(即ちいわゆる“マーカー”)40および関連する抗体41を位置させることにより行われる。特に、例えば種々の既知のタイプの胸部癌に関する細胞等の1以上の特定のタイプの癌細胞をの存在についてサンプル4aを試験することが所望されると仮定すると、その後、これらの細胞に関連するプロテイン42に結びつくことが知られている特定のタイプのマーカー40および関連する抗体41がサンプル4aに位置される。サンプル4a中で使用されてもよい種々のタイプのマーカー40の例は図7および8の表の最初の列に示されているが、サンプル4aが試験される癌細胞のタイプに応じて他のタイプの蛍光材料が使用されてもよいことが注意すべきである。
【0014】
マーカー40および関連する抗体41をサンプル4aに位置させるとき、1以上の細胞40' が確かに癌性であることが想定されると、マーカー40および抗体41は細胞40' に関連されるプロテイン42に結び付く。そうでなければ、サンプル4aに含まれる細胞40' が癌性の細胞ではないことが想定され、結果として関連するプロテイン42を生成しないと、サンプル中4aに位置されたマーカー40および抗体41は細胞に結合されず、マーカー40はサンプル4aから流れ出て、検出不可能な状態になる。典型的に十分な量のマーカーがサンプル4aに配備され、それによって、サンプル4aに含まれる1以上の癌細胞40' および関連するプロテイン42が存在することが想定されると、配備されたマーカーはイメージングシステム1に可視である癌細胞40' の領域を“カバーする”ことが注意すべきである。
【0015】
マーカー40がサンプル4aに付加された後、サンプル4aは本発明にしたがって構成され動作されるイメージングシステムを使用して多数のタイプの癌に関連するプロテインの存在に対して試験される。以後“イメージングシステム”と呼ぶシステムは本発明の優れた技術にしたがって検査を実行し、サンプル4aが1以上の単タイプの癌に関連するプロテインの存在について一度に試験されることを可能にし、サンプル4aが癌細胞を含んでいることを想定すると、以下さらに説明するように癌に関連するプロテインが識別されることを可能にする。イメージングシステムは共焦システムである。
【0016】
図1および2は本発明の1実施形態にしたがって構成されたイメージングシステム(符号1で示されている)のブロック図を示している。システム1はパルスレーザまたはランプ等のパルス源投光器3を具備しており、これはパルスビームを照準レンズ5 へ与えるためにCPU30' の制御プロセッサ30により制御可能である。本発明の1実施形態にしたがって、パルス源投光器3は好ましくは335nm乃至700nmの範囲内の広帯域の波長を与えることができる。パルス源投光器3のパルスレートは制御プロセッサ30の制御下で変化されてもよい。CPU30' のオペレータは、適切な情報をキーパッド33を介して制御プロセッサ30へ入力することによってCPU30' からパルス源投光器3のパルスレートを変化してもよい。(“励起パルスビーム”とも呼ばれる)パルスビームは好ましくは以下さらに説明するように少なくとも1nsのパルス幅を有する。
【0017】
パルス源投光器3からのパルスビームの受けると、照準レンズ5はビームを照準し、その結果照準されたパルスビーム5aを格子7へ与える。格子7は制御プロセッサ30の制御下で軸Ax を中心に回転し、図1で認識されることができるように、ビーム5aが延在する平面と、格子7の上面が延在する平面との間に角度(θ1)が存在するように傾斜される。角度(θ1)の値に応じて、格子7は受信されたビーム5aを回折して、波長の特定の狭帯域を含んでいる結果的なビーム部分8を結像光学装置9へ与える。結像光学装置9は受信されたビームを照準するための形状を有することが好ましい。ビーム部分8の受信に応答して、結像光学装置9はビーム部分8を波長の対応する照準された狭帯域の波長へ照準し、これらの波長を単色計スリット11へ反射する。角度(θ1)の値と格子7の特定の回転角度に基づいて、単色計スリット11は特定の1つの波長(即ち“励起イメージ”とも呼ばれる所望の波長)を円筒形レンズ12へ透過する。
【0018】
図1と前述の説明で認識されることができるように、コンポーネント5、7、9および11の組合わせは所望の波長がスリット11から円筒形レンズ12へ透過されることを可能にするように機能する。好ましくは、この波長はサンプル4aで使用される1以上のタイプのマーカー40を“励起”し、マーカーに対応する蛍光放射を放射させることが知られている。
【0019】
本発明はスリット11を通して所望の波長を与えるためにこの構造に限定されることを意図せず、本発明の他の実施形態では、他の適切なコンポーネントが所望の波長を与えるために使用されてもよいことに留意すべきである。所望の波長が円筒形レンズ12へ与えられることを可能にするために、例えばコンポーネント5、7、9ではなく、単一のレーザが所望の波長の単色ビームを直接スリット11へ与えるために使用されてもよい。また例示すると、本発明の別の実施形態にしたがって構成されたイメージングシステム1' 部分にしたがって構成された図3を参照することにによって、格子7はミラー7aに置換されることができ、それによってパルス源投光器3により出力された単一の1つの広帯域波長がスリット11によって円筒形レンズ12へ透過される。イメージングシステムのこの実施形態は、格子7がミラー7aで置換されることを除いて図1および2のイメージングシステム1と類似のコンポーネントを含んでいる。本発明のイメージングシステムのいずれの実施形態(即ちイメージングシステム1または1' )は以下説明するように、サンプル4aが種々のタイプの癌細胞の存在について同時に検査されることを可能にするために使用されてもよい。
【0020】
スリット11からの1以上の波長の受信に応答して、円筒形レンズ12はストライプビーム12aをシステム1の瞳孔に位置される円筒形レンズレットアレイ13へ提供する。ストライプビーム12aはアレイ13の個々のレンズレット13a−13cの全体を均一に照射する。
【0021】
レンズレットアレイ13の断面が図15に示されている。本発明の好ましい実施形態ではレンズレットアレイ13は3つの個々のレンズレット13a−13cを含んでいる。アレイ13の各個々のレンズレット13a−13cは深さ(d)(例えばdは好ましくは6mmに等しい)と、幅(w)(例えばwは好ましくは1.26mmに等しい)を有し、好ましくは焼成シリカで構成されている。またはレンズレット13aの正面13eの中心の軸Y1は好ましくは例えば1.26mmの距離だけレンズレット13fの正面13fの中心の軸Y2から離れている。同様に軸Y2は好ましくは例えば1.26mmの距離だけレンズレット13cの正面13gの中心の軸Y3から離れている。各個々のレンズレット13a−13cは好ましくは積2×fに実質上等しい曲率半径を有し、ここでfはレンズレットの焦点距離を表している。例えば各個々のレンズレット13a−13cは約9.5mmの曲率半径を有する。レンズレット13aは以下説明するように、空間的分離がサンプル4aの照射に使用されるイメージの行間に設けられることを可能にし、したがって、不所望の光背景“雑音”が抑制されることを可能にする。
【0022】
ストライプビーム12aによる照射に応答して、各レンズレット13a−13cはビーム12aのそれぞれの受信された部分をマスク14のそれぞれの部分へ焦点を結び、それによってマスク14のスリットのそれぞれの行を均一に照射させる。レンズレット13a−13cによりマスク14へ焦点を結ばれたビーム部分はまた“中断されたストライプビーム”と集合的に呼ばれ、多数の励起イメージをマスク14へ与える。
【0023】
図16はマスク14を見下ろした斜視図から観察したときのマスク14をさらに詳細に示している。本発明の好ましい実施形態にしたがって、マスク14はスリットの3つの行、即ち行14a、14b、14cを含んでいる。各行14a、14b、14cは好ましくは85の個々のスリット(集合的に“14d”で示す)を含んでおり、これらは以下説明するように行14a−14cの隣接する1つの行のスリットに関して互いにずらされて配列されている。各個々のスリットは長さ(L)と幅(W1)を有する。各個々の行14a−14c内のスリット14dは好ましくは2(L)に等しい距離だけ隔てられ、隣接する行14a−14cの対応するスリット14dの中心線は図16で理解されるように好ましくは長さ(L)に等しい距離だけ相互から水平にオフセット(即ち互い違いに配列)されている。さらに、行14a−14cは相互に隔てられ、それによって行14a−14cの隣接する行のスリットの対応するエッジは距離(d1)だけ分離されている。距離(d1)は積幅(W1)×85に等しい。さらにマスク14は幅(W2)を有する。
【0024】
本発明にしたがって、各行14a−14c内の個々のスリット14dは2(L)に等しい距離だけ相互から隔てられ、ここで(L)はマスク14の個々のスリットの長さを表し、イメージングシステム1の総合的な性能における(マーカーの自動蛍光発光から生じる)光散乱のような不所望の光現象の効果は実質上最少にされる。
【0025】
図1を再度参照すると、レンズレットアレイ13から受けられたそれぞれのビームにより照射されるとき、マスク14の各行14a−14cのスリット14dはこれらのビームを対物レンズ16へ通過させ、対物レンズ16はこれらのビームを段18の上部表面18' へ焦点を結ばせ、またはサンプルスライド4が段18の上部表面18' に配置されたと仮定すると、サンプルスライド4の上部表面へ焦点を結ばせる。
【0026】
対物レンズ16により段18の表面18' またはサンプルスライド4の上部表面へ焦点を結ばれたビームを以後“スリットイメージビーム”と呼び、スリットイメージビームの結果としてこれらのコンポーネントに現れるイメージを以後“スリットイメージ”と呼ぶ。各スリットイメージおよび関連するスリットイメージビームは行14a−14cのそれぞれの各スリットに対応している。それぞれの個々のスリット行14a、14b、14cのスリット14dにより発生されたスリットイメージビームをそれぞれスリットイメージビームグループ14a' 、14b' 、14c' と集合的に呼び、これらのスリットイメージビームグループ14a' 、14b' 、14c' に対応する(スライド4または段18の上部表面上に現れ照射する)スリットイメージを以後それぞれスリットイメージグループ14a''、14b''、14c''と呼ぶ。本発明の1実施形態によれば、対物レンズ16は1:1の拡大レベルを与える。例により説明すると、対物レンズ16により与えられた拡大レベルに基づいて、各個々のスリットイメージは、0.5μm、2μm、5μm、20μmまたは50μmの幅(W' )を有し、各グループ14a''−14c''の第1のスリットイメージの外部エッジと、グループ14a''−14c''の最後のスリットイメージの外部エッジとの間の距離(W'')は0.13mm、0.64mm、5.12mm、12.8mmである(例えば図21参照)。
【0027】
段18は(x,y,z)座標系の1以上の軸に沿って、サンプルスライド4等のようなオブジェクトを変位するために制御可能である技術で知られている適切なタイプの段装置である。段18は所望の軸(x,y,z)に沿ってスライド4を変位するため制御プロセッサ30の制御下で動作する。好ましくは、段18は少なくともマスク14の個々のスリット14の幅(W1)程度に小さい距離だけこれらの軸 (x,y,z)のうち所望の軸に沿ってサンプルスライド4を変位することができる。例により、本発明の1実施形態にしたがって説明すると、段18は少なくとも6/10ミクロン程度に小さい距離だけ軸(x,y,z)のうち所望の軸に沿ってサンプルスライド4を変位する能力を有する。
【0028】
本発明のイメージングシステム1のさらに別の部分を説明する、イメージングシステム1のこの部分を説明する目的で、パルスビームがパルス源投光器3から発射された後、少なくともサンプル4aの幾らかの部分が1以上のイメージグループ14a''−14c''により照射される位置に段18の上部表面18' 上にサンプルスライド4が配置されることが想定される。サンプル4aの1以上の細胞40' が癌性であり、サンプル4aは複数のマーカー40を含んでおり、少なくとも幾らかのこれらのマーカーが少なくとも1つのスリットイメージグループ14a''−14c''からの1以上のスリットイメージにより照射されることも想定される。パルス源投光器3により発射されるパルスビームの波長と、照射されたマーカー40の蛍光特性に応じて、これらのマーカー40の少なくとも幾らかは照射に応答して“励起され”(即ち蛍光発光)、(便宜上“放射波長”と呼ばれる)結果的に特徴的な蛍光放射波長を放射する。図7および8の第2の列で示されている種々のパルス源投光器の“励起”波長による“励起”に応答して図7および8の第1の列で示されている種々のマーカーによりもたらされた種々の放射波長の例が図7および8の第3の列に示されている。図7および8の表の第3の列で認識されることができるように、幾つかのマーカーは実質上類似した波長を放射してもよい(例えばマーカールシフェルイエローCH、カルシウムグリーン、Toto−1は列2で示されているそれぞれの励起波長による照射に応答して533nmの放射波長を有する)。図7および8の第4の列は図7および8のそれぞれのマーカーに対応する励起波長と放射波長との差を示している。
【0029】
1以上のスリットイメージグループ14a''−14c''からの1以上のスリットイメージにより放射された結果として、サンプル4aからマーカー40により生じた放射波長は対物レンズ16を介して放射ビームとしてビームスプリッタ15へ誘導される。ビームスプリッタ15はこれらのビームを分割し、これらのビームの一部はビームスプリッタ15により単色計スリット光学装置19(便宜上“スリット光学装置19”と呼ばれる)の部分へ焦点を結ばれる放射ビーム部分44になる。スリット光学装置19は前述し図16で示されているマスク14と類似の構造を有し、したがってさらに詳細には説明しないが、マスク14の1以上のスリット14dから出力されたビームによる照射に応答して1以上のマーカー40により放射される波長がビームスプリッタ15によりスリット光学装置19の対応するスリットへ焦点を結ばれるようにビームスプリッタ15とスリット光学装置19は位置されることが好ましい。
【0030】
スリット光学装置19で、ビームスプリッタ15から放射ビーム部分44を受けるスリット光学装置19の各個々のスリットは受信した放射ビーム部分44を照準レンズ19' へ透過する。スリット光学装置19の種々のスリットを通過したビーム部分を以後ビーム19''と集合的に呼ぶ。照準レンズ19' はスリット光学装置19から受信したビーム19''を照準し、結果的な照準されたビーム20' を格子20へ与える。
【0031】
格子20は照準されたビーム20' の波長を予め定められた波長帯域へ分離するように照準されたビーム20' を回折する。格子20は固定された角度の台20aに取付け、その角度(θ2)は選択された波長が格子20から回折され、結像光学装置22へ誘導されるように選択されており、結像光学装置22はこれらの各波長を2次元検出器アレイ25(即ち光検出器アレイ)の放射感知性表面25aのそれぞれの行へ誘導する。適用可能な性能基準に基づいて、格子20と角度(θ2)は波長の狭波長帯域または広波長帯域への必要な分離(即ちセグレゲーション)を与えるように選択されてもよい。
【0032】
本発明の好ましい実施形態にしたがって、検出器アレイ25の表面25aは放射検出器素子の複数の行(I)と複数の列(J)を含んでいる。好ましくは、表面25aは放射検出器素子の256以上の行(I)と256以上の列(J)を含んでいる。図17で見られるように、行(I)は検出器素子の行の第1のグループ(G1)と、検出器素子の行の第2のグループ(G2)と、検出器素子の行の第3のグループ(G3)とを含んでいる。行の各個々のこれらのグループ(G1)、(G2)、(G3)は好ましくは放射検出器素子の85の行を含んでいる。
【0033】
本発明の好ましい実施形態では、コンポーネント20、22は、1)第1のグループ(G1)からの検出器素子の行は、マーカーがスリットイメージグループ14a''からのスリットイメージにより照射される結果としてサンプル4aの1以上の マーカー40から放射される波長を検出し、2)第2のグループ(G2)からの検出器素子の行は、マーカーがスリットイメージグループ14b''からのスリットイメージにより照射される結果としてサンプル4aからの1以上のマーカー40により放射される波長を検出し、3)第3のグループ(G3)からの検出器素子の行は、マーカーがスリットイメージグループ14c''からのスリットイメージにより照射される結果としてサンプル4aからの1以上のマーカー40により放射される波長を検出するように構成されている。各グループ(G1)、(G2)、(G3)内では、グループ内の放射検出器素子の各行はそれぞれの波長範囲に対応するそれを受信する。例により、格子20と結像光学装置22を再度参照して説明すると、格子は好ましくは結像光学装置22と組合わせて動作し、それによってほぼ405nm乃至661nmのおおよその範囲内のマーカー放射波長を、検出器アレイ表面25aの行の各グループ(G1)、(G2)、(G3)へ誘導し、ここでグループ(G1)、(G2)、(G3)に導かれる波長はそれぞれスリットイメージグループ14a''、14b''、14c''に対応する。特に、本発明の好ましい実施形態にしたがって、格子20は好ましくはスリットイメージグループ14a''がサンプルスライド4を照射した結果として放射されたKnm乃至(K+2)nmの範囲の任意の波長を対応するグループ(G1)の行のN番目の行に誘導するため結像光学装置22と組み合わせて動作し、ここでN=1、2、3…256の対応する値では、K=405、408、411…658である。同様に、格子20は結像光学装置22と組合わせて、スリットイメージグループ14b''がサンプルスライド4を照射した結果として放射されたKnm乃至(K+2)nmの範囲の任意の波長を対応するグループ(G2)の行のN番目の行に誘導し、ここでN=1、2、3…256の対応する値では、K=405、408、411…658である。さらに、格子20は結像光学装置22と組合わせて、スリットイメージグループ14c''がサンプルスライド4を照射した結果として放射されたKnm乃至(K+2)nmの範囲の任意の波長を対応するグループ(G3)の行のN番目の行に誘導し、ここでN=1、2、3…256の対応する値では、K=405、408、411…658である。
【0034】
これは図17でさらに理解されるであろう。図17は格子20、検出器アレイ25の表面25a、サンプル4aからの種々のマーカー40(種々のマーカーはラベル “40a”、“40b”、“40c”によりさらに参照される)、それぞれのスリットイメージビーム14a' 、14b' 、14c' のグループのからの1以上のビームによる放射に応答してマーカー40a、40b、40cにより生成された例示的な放射波長(例えばλ1=406nm、λ2=412nm、λ3=415nm)の斜視図を示している。図17で認識されることができるように、それぞれのスリットイメージビームグループ14a' 、14b' 、14c' からのビームによる照射に応答してそれぞれのマーカー40a、40b、40cにより放射される波長(λ1、λ2、λ3)は格子20により回折され、その後、結像光学装置22を経てそれぞれの行のグループ(G3)、(G2)、(G1)の対応する行(I1)、(I3)、(I4)の対応する放射検出器素子へ導かれる。また、それぞれの行のグループ(G1)、(G2)、(G3)内では、行の放射検出器により受信される波長は、マーカーに波長を放射させる対応するスリットイメージグループ14a''、14b''、14c''のそれぞれ個々のスリットイメージに対応する。
【0035】
検出器アレイ25をさらに詳細に説明する。検出器アレイ25は電荷結合装置(CCD)技術にしたがって構成されてもよいが、本発明の考察はCCD映像アレイでのみ使用することに限定されない。検出器アレイ25の1つの適切な実施形態はKentech Instruments 有限会社により製造されたシングルフレームゲート光学イメ−ジャを含んでいる。
【0036】
検出器アレイ25の表面25aに入射するマーカー放射波長は検出器アレイ25のポテンシャル井戸中に対応する電荷イメージを発生する。即ち、波長の受信は検出器アレイ25のポテンシャル井戸内に対応する電荷パケットまたは電荷イメージを発生する。検出器アレイ25はまた内部ゲートアレイ25cを含んでいる読出し部25bを含んでいる。ゲートアレイ25cは(サンプリング時間中に)“エネーブル”または(他のサンプリングではない時間に)“ディスエーブル”されるように制御プロセッサ30により制御される。ゲートアレイ25cがエネーブルされる期間に、検出器アレイ25の読出し25bは行×行ベースで、それぞれの行(I)の放射検出器素子により検出される波長に対応する出力信号を与える。イメージ情報を表すこれらの出力信号は、以下説明する方法で信号を処理する制御プロセッサ30(図3)へ転送される。
【0037】
本発明の方法を説明する前に、最初にメモリ31、フレーム記憶装置F1−F4、本発明のイメージングシステム1の表T1およびT2を説明する。メモリ31はイメージングシステム1の動作中に制御プロセッサ30によって使用される種々の定数および変数を記憶している。例により説明すると、メモリ31は変数Tp 値を記憶している。変数Tp 値は第1の予め定められた時間期間値を特定し、以下説明する方法で制御プロセッサ30により使用される。また例により説明すれば、メモリ31は変数“STEP”の値を記憶している。変数STEPは制御プロセッサ30のカウンタ30aにより維持されている“ステップ”数を表しており、ここで“ステップ”は予め定められた距離だけ(段18上の)軸(x)に沿ったサンプルスライド4の完全な移動またはインクレメントを含んでいる。変数STEPの値は以下説明するようにサンプルスライド4の各“ステップ”でカウンタ30aにより更新される。メモリ31は、以下説明するように、パルス源投光器3がパルスビームを発射する回数を識別するために本発明の“高解像度動作モード”中に使用される変数PFをさらに記憶している。制御プロセッサ30の動作を制御するための動作プログラムもメモリ31に記憶されている。
【0038】
フレーム記憶装置F1−F4が使用され、システム1は複数のそれぞれのサンプリング時間の期間中に検出器アレイ25から出力され予め定められたしきい値レベルを超えると決定された信号を記憶するために“高解像度動作モード”で動作する。図30を参照すると、各フレームは記憶装置F1−F4は記憶ビン70のそれぞれのアレイを含んでいる。これらの各記憶ビン70は検出器アレイ25の表面25aの特定の1つの放射検出器素子に対応する。したがって、第1の1つのサンプリング時間中に、検出器アレイ25により出力され予め定められたしきい値レベルを超える振幅を有することが決定された各それぞれの信号では、信号に対応する波長を検出した(表面25aの特定の行(I)および列(J)からの)特定の放射検出器素子に対応するフレーム記憶装置F1内の特定の記憶ビン70に信号は記憶される。同様に、第2、第3、第4のサンプリング時間中に、検出器アレイ25により出力され予め定められたしきい値レベルを超える振幅を有すると決定された各信号では、信号はそれぞれフレーム記憶装置F2、フレーム記憶装置F3、フレーム記憶装置F4内の特定の記憶ビン79にそれぞれ記憶され、ここで記憶ビン70は信号に対応する波長を検出した(表面25aの特定の行(I)および列(J)からの)特定の放射検出器素子に対応する。サンプリング時間期間を以下説明する。図30はこれらのサンプリング期間に放射波長71a' を受信する検出器アレイ25の表面25aの特定の検出器素子72に応答して、それぞれのサンプリング期間中に検出器アレイ25によりそれぞれのフレーム記憶装置F1−F4の記憶ビン70a−70dへ出力された信号71の例示的な表示を示している。
【0039】
図31のaでさらに詳細に示されている(検索表であることが好ましい)表T1を参照する。表T1はマーカーおよび/またはプロテインが存在するならば、そのその中でサンプル4aに含まれるタイプを決定するために本発明にしたがった技術を行いながら、制御プロセッサ30により使用される種々のタイプの情報を記憶している。例により説明すると、本発明の1実施形態にしたがって、表T1はサンプル4aの試験中に使用される特定のタイプのマーカーを識別する情報を記憶している。また例により説明すると、本発明の別の実施形態にしたがって、表T1はまたサンプル4aが試験される特定のタイプのプロテインを識別する情報を記憶している。表T1はまた(パルス源投光器3からの)特定の励起波長による“励起”に応答してこれらのマーカーにより放射される特徴的な波長の基準値を規定する情報を記憶している。表T1はこれらの放射波長に関連する基準蛍光減衰時定数値を限定する情報をさらに記憶している。種々のタイプのマーカーとそれらの関連する放射波長および、放射波長(蛍光)減衰時定数の例は図7および8の各列1、3、5に示されている。即ち表T1は少なくとも図7および8で示されている情報を記憶することを想定される。
【0040】
サンプル4aで使用されるマーカーと、これらのマーカーの特徴的な放射波長を識別する情報はフレーム記憶装置F1−F4内の記憶ビン70の各行71a−71nに対応している。例えば(それぞれの記憶ビン70a−70dを含んでいる)各フレーム記憶装置F1−F4の行71aは405nm乃至407nmなどの特定の波長帯域にそれぞれ対応している。表T1に記憶された情報が、335nmの励起波長で照射されるとき405nmの特徴的な放射波長を有するマーカーINDO 1(図7の列1参照)を特定する情報を含んでいることを想定すると、マーカーINDO 1および405nmの対応する放射波長を特定する情報はそれぞれのフレーム記憶装置F1−F4の記憶ビン70の行71aに対応する。これは制御プロセッサ30により知られていると想定される。
【0041】
表T2を参照する。表T2は計算された減衰時定数情報を記憶するためにイメージングシステム1の動作中に制御プロセッサ30により使用される。図31bを参照すると、表T2(即ち検索表)は好ましくは記憶ビン74のアレイを含み、そんぼそれぞれはフレーム記憶装置F1−F4の特定の1つの記憶ビン70にそれぞれ対応する。制御プロセッサ30がフレーム記憶装置F1−F4内の対応する記憶ビン70に記憶されている信号の減衰時定数を計算した後、時定数情報は以下説明するように表T2内の対応する記憶ビン74に記憶される。
【0042】
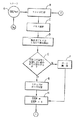
本発明にしたがった方法のフロー図を示している図9乃至14を参照して説明する。その方法は種々の動作モード、即ち“初期スクリーニングモード”、“高解像度動作モード”を含んでおり、これは“スペクトル解析モード”と“時間解析モード”を含んでいるサブモードからなる。これらの各動作モードを以下説明する。
【0043】
図9および10は“初期スクリーニングモード”と呼ばれる方法の一部を表している、このモードでは、サンプル4aは最初に“スクリーン”され、すなわちサンプル4aが試験される特定のタイプの癌に関連することが知られているプロテインの存在について試験される。単なる例示として、技術で知られているように、組織サンプル中の任意の1つのRASプロテイン、P53プロテイン、BRCA1プロテインの存在はサンプル中に癌細胞(例えば胸部癌)が含まれていることを約70%の正確性で示す。したがって、この説明のために、初期スクリーニングモードがこれらのプロテインのいずれかの存在についてサンプル4aを試験するために実行され、サンプル4aには3つの対応するタイプの蛍光マーカー40a、40b、40cが与えられと仮定し、これはサンプル4aが癌細胞を含み、特定の波長による照射に応答して特徴的な放射波長を放射することを仮定する。単なる例示として、サンプル4aは、それぞれ典型的にRASプロテインの存在の検出に使用される蛍光体またはFluo−3と、典型的にP53プロテインの存在の検出に使用されるローダミン123と、それぞれ典型的にプロテインBRCA1の存在の検出に使用されるCY3またはCY5のようなマーカーが設けられることが想定される。またこの説明では、同時に3つの任意のプロテインの存在についてサンプル4aを試験することが所望されると仮定している。さらに、一度にただ1つの選択された励起波長を使用してサンプル4aを試験することが所望される他のケースでは、図1および3のイメージングシステム1が使用されてもよいことに注意すべきであるが、図3および2で示されているイメージングシステム1' の実施形態が本発明の方法を実行するために使用されると仮定する。他の適切なケースでは、サンプル4aが試験されるプロテインのタイプに基づいて、1以上の他の選択されたタイプのマーカーがサンプルに含まれてもよいことをさらに注意すべきである。
【0044】
便宜上、以下の説明では、サンプルスライド4(図6のa)は256×(W1)の積にほぼ等しい長さ(L1)を有するものと仮定し、ここでは前述したように、(W1)はマスク14のスリット行14a−14cの個々の幅を表している。また、サンプルスライド4の幅(W2)は256×(L)の積にほぼ等しく、ここでは前述したように、(L)はマスク14のスリット行14a−14cのスリットの個々の長さを表していると仮定する。このように、サンプルスライド4は、それぞれ幅 (W1)を有する256の“行”と、それぞれ長さ(L)を有する256の“列”を含んでいると仮定する。図6のbはサンプルスライド4を示しており、その上には仮想行R1−R256が便宜上重畳されている。
【0045】
図9を再度参照すると、ブロックAで、この方法が開始され、メモリ31からの変数“STEP”は値“1”に初期化される。前述したように、変数STEPは制御プロセッサ30のカウンタ30aにより維持されている“ステップ”数を表しており、ここで“ステップ”は予め定められた距離による軸(x)に沿ったサンプルスライド4の完全な前進または変位を含んでいる。この説明のために、予め定められた距離は幅(W1)に等しいと仮定する。特に、この説明では、各“ステップ”はサンプルスライド4の個々の“行”の幅(W1)に等しい距離によるサンプルスライド4の完全な変位を含んでいると仮定する。各“ステップ”が(図18および図19で示されている)軸y' に関して段18上の対応する位置または場所にサンプルスライド4のフロントエッジ4a' を位置させると仮定する。例えば図18のaと図21は段18に配置されたサンプルスライド4を示しており、ここでスライド4のエッジ4a' は軸y' に平行に位置されている。また例により、サンプルスライド4が全部で426の個々の“ステップ”により結果的に前進されると仮定すると、これら各ステップはサンプルスライド4のエッジ4a' を軸y' に関して426の異なる位置のうちの対応する1つに位置付ける。これらの位置を以後位置または場所P1−P426とそれぞれ呼ぶ。
【0046】
また、ブロックAでは、サンプルスライド4が段18の上部表面18' 上に配置され、それによって図18のaと図21で示されているようにスライド4のエッジ4a' は軸y' に平行であると仮定する。図18のaと図21で認識されることができるように、サンプルスライド4の位置は、パルスビームがパルス源投光器3から発射されると仮定すると、それぞれのスリットイメージビームグループ14a' −14c' からのビームはスライド4を照射しないで、代わりに段18の上部表面18' を照射する。
【0047】
ブロックBでは、サンプルスライド4の前進における第1のステップとして、制御プロセッサ30はサンプルスライド4を軸(x)に沿って、幅(W1)に実質上等しい距離だけ(即ちサンプルスライド4の“行”の幅(W1)に実質上等しい距離だけ)前進するように段18を制御する。サンプルスライド4の前進によって、サンプルスライド4のエッジ4a' が軸y' に関して段18上の位置P1に到達する。その後、ブロックCで、制御プロセッサ30はパルス源投光器3に選択された広帯域波長の単一パルスビームを発射させるようにパルス源投光器3を制御する。好ましくは、パルスビームの波長はサンプル4aで使用されるマーカー40a−40cのそれぞれを“励起”し、マーカーに対応する蛍光放射を放射させることが知られている波長を含んでいる。また、コンポーネント5、7a、9、11はサンプルスライド4を照射するためにこれらの波長がスリット11を通って与えられることを可能にするように構成されていると仮定する。
【0048】
ブロックCにおけるパルスビームの発射の結果として、図18のbと図22を見て理解されるように、サンプルスライド4の“行”R1が(スリットイメージビームグループ14a' に対応する)スリットイメージグループ14a''からのスリットイメージにより照射される。また図18のbと図22で認識されるように、ブロックCにおけるパルスビームの発射の結果として、段18の上部表面18' はスリットイメージグループ14b''と14c''に対応するスリットイメージビームグループ14b' と14c' により照射される。これはまたマスク14部分と、段18の上部表面18' 上に配置されたスライド4の斜視図を示している図20のaで見られることができる。
【0049】
ブロックDにおいて、検出器アレイ25の表面25aの放射検出素子は、前述の方法で、サンプルスライド4を照射するスリットイメージ14a''(および段18の表面18' を照射するスリットイメージ14b''−14c'')から生じる放射を検出する。ゲートアレイ25cが制御プロセッサ30により“エネーブル”されることを想定すると、検出器アレイ25の読出し部25bは行毎のベースで、出力信号を制御プロセッサ30へ提供し、前述したように、各行からの信号は検出器アレイ25により受信された波長のそれぞれの帯域に対応する。
【0050】
制御プロセッサ30内では、検出器アレイ25から各出力信号が受信されたとき、信号の振幅は本発明の好ましい実施形態にしたがって、A/D変換器ブロック30cを使用して検出される。その後、各信号の検出された振幅は、それが存在するならば、少なくとも1つの検出された振幅が予め定められたしきい値レベルを超えることが決定される(ブロックE)まで予め定められたしきい値レベルと比較される。ブロックEで振幅が予め定められたしきい値レベルを超える信号がないことが決定されたならば(ブロックEで“ノー”N)、ブロックFで全ての信号は制御プロセッサ30により無視され、以下説明するように、制御はコネクタ1を経てブロックHへ通過する。
【0051】
予め定められたしきい値レベルはキーパッド33を使用して、CPU30' のユーザにより特定されてもよいことに注目すべきである。好ましくは、予め定められたしきい値レベルは検出器アレイ25により検出されることのできる周囲波長の振幅レベルよりも大きく、周囲波長は例示によりサンプルスライド4ではなく段18の上部表面18' を照射するスリットビームグループ14b' と14c' の結果として発生された任意の波長を含んでいる。この方法では、サンプルスライドを照射しない任意のスリットイメージビームグループ14b' と14c' の結果として検出器アレイ24により検出されることのできる任意の波長はCPU30により無視される。
【0052】
検出器アレイ25から受信された1以上の信号がブロックEで予め定められたしきい値レベルを超えたことを制御プロセッサ30が決定したとき、制御プロセッサ30は変数STEPの値(例えば値“1”)をメモリ31に記憶する。また、予め定められたしきい値レベルを超えた振幅を有することが決定されている信号は制御プロセッサ30によりフレーム記憶装置F1内の対応する記憶ビン70に記憶される。制御はその後、ブロックHへ進み、ここでは制御プロセッサ30は変数STEP値を“1”だけ増加する。その後、制御はコネクタ1を経てブロックI' へ通過し、ここでは制御プロセッサ30は変数STEPの値が、ステップ数(即ち426)を特定する予め定められた基準値よりも大きいか否かを決定し、ここでは図19のdで示されているように、サンプルスライド4は段18上の位置に前進されず、スライド4の後部エッジ4b' は軸y1' と平行であり、スライド4は任意のビーム部分14a' −14c' により照射されない。ブロックI' で“ノー”であるならば、制御はコネクタ2を経てブロックB(図9)へ戻り、ここではスライド4を前進する第2の“スエップ”が実行される。即ち、ブロックBでは、制御プロセッサ30は幅(W1)に等しい距離だけサンプルスライド4を前進するように(即ちエッジ4a' が軸y' に関して位置P2に到達するようにスライド4を前進することによって)再度段18を制御する。その後、ブロックC−I' で識別される手順が前述した方法と類似の方法で実行され、ステップ数2乃至85で(即ち2と85間の各STEP値で)スライド4をそれぞれ結果的に前進するために継続して反復される。検出器アレイ25から制御プロセッサ30へ出力される1以上の信号がブロックEで予め定められたしきい値レベルを超えたことが決定されるこれらの任意の“ステップ”では、“ステップ”数を示す変数STEP値がメモリ31に記憶され、信号はフレーム記憶装置F1のそれぞれの記憶ビン70に記憶される。例示により説明すると、サンプルスライド4のエッジ4a' がそれぞれのステップ2、16、20、85期間にそれぞれの位置P2、P16、P20、P85に位置付けられながら、検出器アレイ25により出力された少なくとも1つの信号がブロックEで予め定められたしきい値レベルを超えたことが決定されたと仮定すると、変数STEPの対応する値“2”、“16”、“20”、“85”はそれぞれブロックGでメモリ31に記憶される。
【0053】
ステップ番号86から170 を参照する。最初に図9および10のブロックB−I' により示されている処理の実行期間に、変数STEP値がブロックHで値86に 到達しており、ステップ86として、エッジ4a' が位置P86に到達されるようにサンプルスライド4がブロックBで再度距離(W1)だけ前進される。別のパルスビームがブロックCでパルス源投光器3から発射されると仮定する。この場合、図18のcおよび図23を見て理解されるように、両スリットイメージグループ14a''、14b''からのスリットイメージはサンプル4aを照射し、図23ではスリットイメージグループ14a''、14b''により照射されている行R1とR86をそれぞれ示している。これはマスク14の一部分とサンプルスライド4の斜視図を示している図20bでも認められ、ここではマスク14のスリット行14bと14aからのイメージはスライド4のそれぞれの行R86とR1を照射する。図18のcと図23で示されている位置から、STEPの値が170に等しい場合(即ちスライド4のフロントエッジ4a' が位置P170 に到達する場合)に対応する位置へのスライド4のそれぞれの前進では、ブロックBのパルスビームの発射により、サンプルスライド4はスリットイメージグループ14c''ではなく両スリットイメージグループ14a''、14b''からのスリットイメージにより照射される。マーカー40a−40cがこれらのスリットイメージグループ14a''、14b''により照射される結果として生じた任意の蛍光放射はブロックDで検出され、ブロックE−I' で示されている処理はその後、前述の方法と類似の方法で実行される。各ステップ番号86から170 では、検出器アレイ25により制御プロセッサ30へ出力された少なくとも1つの信号の振幅が、ブロックEで予め定められたしきい値レベルよりも大きいことが決定されたと仮定すると、前述した方法と類似の方法で、ステップ数を識別する変数STEPの値はブロックGでメモリ31中に記憶される。
【0054】
サンプルスライド4がステップ170 を経て前進された後、ステップ171 としてスライド4はブロックBで距離(W1)だけ再度前進され(それによってエッジ4a' は位置P171 へ到達し)別のパルスビームがブロックCでパルス源投光器3から発射されると仮定すると、図19のdと図20のcと図24で認められるように、サンプルスライド4は全ての3つのスリットイメージグループ14a''、14b''、14c''により照射され、ここで図20cはサンプルスライド4とマスク14の部分の斜視図を示している。特に、ステップ171 に対しては、行R1、R86、R171 は、パルスビームがブロックCで発射された結果として、それぞれスリットイメージグループ14c''、14b''、14a''からのスリットイメージにより照射される(図24参照)。マーカー40a−40cがこれらのスリットイメージグループ14a''、14b''、14c''により照射された結果として生じる任意の蛍光放射はブロックDで検出され、ブロックE−I' により示されたステップがその後、前述の方法と類似の方法で実行される。
【0055】
172 から256 の各ステップ番号では、ブロックCのパルスビーム発射によってサンプルスライド4はスリットイメージグループ14a''、14b''、14c''により照射される。マーカー40a−40cがこれらのスリットイメージグループ14a''−14c''により照射された結果として生じる任意のマーカー蛍光放射はブロックDで検出され、ブロックE−I' により示されたステップは前述の方法と類似の方法で実行される。これらの個々のステップ中に検出器アレイ25により出力された少なくとも1つの信号の振幅がブロックEで予め定められたしきい値レベルよりも大きいと決定されたと仮定すると、ステップ数を識別する変数STEP値はブロックGでメモリ31に記憶される。
【0056】
サンプルスライド4がステップ256 を経て前進された後、ステップ257 としてサンプルスライド4がブロックBで距離(W1)だけ再度進行され、別のパルスビームがブロックCでパルス源投光器3から発射されたとすると、パルスビームによりサンプルスライド4はスリットによってスリットイメージグループ14b''と14c''のみから照射される。これは図19のbと図25で認識されることができる。ステップ257 乃至241 を経るスライド4のそれぞれの前進では、マーカー40a−40cがこれらのスリットイメージグループ14b''および14c''により照射された結果として生じる任意のマーカー放射はブロックDで検出され、検出器アレイ25により出力された少なくとも1つの信号の振幅が予め定められたしきい値レベルを超えたとすると、ステップ数を識別するSTEP値は前述した方法と類似の方法でメモリ31に記憶される。他のスリットイメージグループ14a''が段18の表面18' を照射して行われる任意の検出は前述したように制御プロセッサ30により無視される。
【0057】
ステップ数342 から426 までのスライド4の前進に対しては、(パルス源投光器3がブロックCで各ステップ数でパルスビームを発射したと仮定すると、)サンプルスライド4がスリットイメージビームグループ14c' (および対応するスリットイメージグループ14c'')のみにより照射される。これは図19のcと図20のdと図26で認められることができ、ステップ数342 に対応する位置のサンプルスライド4を示している。ステップ数342 −426 では、マーカー40a−40cがこれらのスリットイメージグループ14c''により照射された結果として生じる任意のマーカー蛍光放射はブロックDで検出され、検出器アレイ25により出力された少なくとも1つの信号の振幅が予め定められたしきい値レベルを超えたとすると、ステップ数を示すSTEP値は前述した方法と類似の方法でメモリ31に記憶される。他のスリットイメージグループ14a''と14b''が段18の表面18' を照射して行われる任意の検出は前述した方法で制御プロセッサ30により無視される。
【0058】
ブロックI' で、変数STEPが426を超えたことが決定された場合を参照する。制御プロセッサ30が変数STEP値がブロックI' で426よりも大きいことを決定したとき、制御はブロックJへ移り、このブロックJで制御プロセッサ30はそれぞれの任意のステップ1乃至426に対してブロックGで任意の情報が前もって記憶されているか否かを決定するためにメモリ31を検査する。制御プロセッサ30が、情報(即ち変数STEPの値)が任意のステップ数1乃至426でメモリ31に記憶されたことを決定したならば(ブロックKで“Y”によって示されている)、制御はブロックK1へ移行し、このブロックK1では制御プロセッサ30はサンプルスライド4を図18のaと図21に示されている位置へ再度位置させるように段18を制御する(ここではスライド4のフロントエッジ4a' は軸y' に平行である)。制御はコネクタ3によりブロックM(図11)へ移り、ここではさらに処理が以下説明する方法で実行される。
【0059】
ブロックKで制御プロセッサ30が、任意のステップ数1乃至426で前もってメモリ31に記憶されている情報がないと判定したならば(試験されているプロテインがサンプル4a内に存在しないことを示す)、制御はブロックL' に移り、ブロックL' では、他のタイプのプロテインの存在についてサンプル4をさらに試験することが所望であるならば、付加的なタイプの蛍光マーカーがサンプル4aに付加されてもよい。
【0060】
他のタイプのプロテインの存在についてサンプル4aを試験し、付加的マーカーがサンプル4aに付加されることが所望ではないならば(ブロックL' で“N”)、処理手順はブロックL2で終了される。
【0061】
他のタイプのプロテインの存在についてサンプル4aを試験することが所望であるならば(ブロックL' で“Y”)、付加的な蛍光マーカーがブロックL1' でサンプル4aに付加される。技術で知られているように、全部で25のマーカーが1つのサンプルに含まれるから1以上のマーカーにより発生される蛍光放射は他のマーカーを励起するので、ブロックL1' でサンプル4aに付加されるマーカーの数およびタイプは任意の選択された数およびタイプのマーカーであるが、好ましくは全部で22までの付加的なマーカーが付加される。この説明の目的で、種々のタイプのプロテインの存在に対してサンプル4を試験することが所望され、図7および8で示されているリストから22のマーカーがブロックL' でサンプル4 に付加され、これらのマーカーが前もってサンプル4に含まれているマーカー40a−40cとは異なると仮定する。
【0062】
付加的なマーカーばブロックL1' でサンプル4aに付加された後、制御はコネクタ3aを経てブロックAに戻り、ブロックAでは図9および10の初期スクリーニングモード処理手順が、試験されているプロテインがサンプル4aに存在するか否かを決定するために再度行われる。これらの処理手順は前述した方法と類似の方法で実行され、したがってさらに詳細に説明しないが、サンプル4aはブロックL1' でサンプル4に付加される付加的なマーカーを含んでいるので、サンプル4aの照射に使用される波長はこれらの付加的なマーカーを“励起”することが知られている波長を含んでいることに注意すべきである(即ち、ブロックCで光源投光器3から発射されたパルスビームは付加的なマーカーを“励起”するための波長を含んでいる)。
【0063】
前述の説明を考慮して、“初期スクリーニングモード”処理手順はプロテイン(および癌細胞)がサンプル4aに含まれているか否かについての決定を行うことを可能にすることが認識されることができる。サンプル4aにプロテインが含まれていることの決定が行われた後(ブロックKでイエス“Y”により示されている)、“高解像度動作モード”処理が、サンプル4aに含まれるプロテインの特別なタイプを識別することを可能にするために実行される。“高解像度動作モード”処理手順について以下説明する。
【0064】
前述したように、制御プロセッサ30がブロックKで、情報が任意のステップ数1乃至426でメモリ31に記憶されたことを決定したならば(1以上のプロテインがサンプル4aに存在することを示している)、制御はブロックK1へ移り、このブロックK1では段18はサンプルスライド4を図18のaと図21により示されている位置へ再度位置させるように再度制御される。その後、制御はコネクタ3によりブロックM(図11)へ移る。ブロックMでは、所望ならば、対物レンズ16が、初期スクリーニングモード中に使用されたものよりも大きな拡大レベル(例えば1:15の拡大比)を与える別の対物レンズで置換されてもよく、それによってより大きな解像度が検出器25により検出されるイメージのために与えられる。この説明のために、対物レンズ16はブロックMで拡大レベルが増加した別の対物レンズと置換されると仮定する。
【0065】
ブロックM後、制御はブロックNへ移り、ブロックNでは制御プロセッサ30はブロックGで前もってメモリ31に記憶された変数STEP値を検索する。その後、ブロックOで、制御プロセッサ30はステップ値のリストを与えるため、ブロックNで検索された値を増加する順序で分類するアルゴリズムを実行する。制御プロセッサ30により使用される分類アルゴリズムは増加する順序で値を分類する技術で知られた任意の適切なタイプのアルゴリズムであってもよい。
【0066】
ブロックPで、制御プロセッサ30はブロックOで分類された値リストから最小の値を検索し、ブロックQで制御プロセッサ30はブロックPで検索された値により示されているステップ数だけ(即ち幅(W1)×ブロックPで検索された値の積に等しい距離だけ)サンプルスライド4を前進するように段18を制御し、それによってブロックPで検索された値に対応する段18上の位置にスライド4を位置させる。このようにして、初期スクリーニングモード中に1以上のプロテインを含むことが前もって決定されているサンプル4aの第1の部分はサンプル4aのこの部分に含まれるプロテインの特定のタイプを識別するために試験されてもよい。
【0067】
ブロックQ後、制御はブロックRへ移り、ブロックRでは、制御プロセッサ30はパルス源投光器3に選択された波長の単一のパルスビームを発射させるようにパルス源投光器3を制御する。例により説明すると、3つだけのマーカーがサンプルに含まれると仮定すると、ブロックRで発射されたパルスビームはそれぞれのマーカーを蛍光発光させることが知られている3つの対応する波長を含んでいる。また例により、22のマーカーがブロックL1' で前もってサンプル4aに付加されていると仮定すると、ブロックRで発射されたパルスビームはそれぞれのマーカーを蛍光発光させ特徴的な放射波長を放射させることが知られている22の対応する波長を含んでいる。
【0068】
ブロックSで、制御プロセッサ30はブロックRでパルス源投光器3により発射されたパルスビームが終了したときに開始するように(制御プロセッサ30の)タイマー30bを設定し、変数PFは“1”に等しく設定される。その後、制御プロセッサ30が、タイマー30bがメモリ31に記憶されている変数Tp により特定された第1の予め定められた時間期間値に到達したことを決定したとき、制御はブロックUへ移る。ブロックUで、制御プロセッサ30は、第1の予め定められた時間期間が終了したときに開始する第2の予め定められた時間期間(“サンプリング期間”とも呼ぶ)に検出器アレイ25のゲートアレイ25cをエネーブルするようにゲート検出器25に通報する。結果として、検出器アレイ25はゲートアレイ25cがエネーブルされながら検出器アレイ25により検出される任意の波長に対応する信号を制御プロセッサ30に出力する。前述したように、検出器アレイ25により出力される信号は検出器アレイ25により検出されるイメージ情報を表している。
【0069】
好ましくは、変数Tp により特定された第1の予め定められた時間の期間の値とサンプリング期間は、ブロックRで発射されたパルスビームに応答してサンプル4aから放射された波長のピーク振幅が検出器アレイ25により検出されることができ(マーカー放射の特徴的な“ライフタイム”または減衰時間を考慮する)、対応する信号はサンプリング期間中に検出器アレイ25から出力されることができるようにされている。例により説明すると、本発明の好ましい実施形態にしたがって、第1の予め定められた時間の値は約100psに等しく、マーカー放射の最小の破壊減衰が約1nsであるとを仮定すると、“サンプリング期間”の長さも100psである。また実施例では、マーカー放射の最小の減衰時間が約4nsであることを想定すると、“サンプリング期間”の継続は好ましくは500psである。ブロックUでサンプリング期間中に検出されたマーカー放射波長に対応する信号部分を表す例示的な曲線は図28aで示されている。
【0070】
検出器アレイ25がブロックUで行単位で情報信号を制御プロセッサ30に出力した後、信号はA/D変換され、信号の振幅は前述した方法で予め定められたしきい値レベルと比較される。予め定められたしきい値レベルを超えないと判定された振幅を有する信号は制御プロセッサ30により無視され、予め定められたしきい値レベルを超えると判定された振幅を有する信号はフレーム記憶装置F1のそれぞれの記憶ビン70に記憶される(ブロックV)。即ち、予め定められたしきい値レベルを超えると判定された振幅を有するそれぞれの各信号に対しては、信号は信号に対応する波長を検出した放射検出器素子に対応するフレーム記憶装置F1内の特定の記憶ビン70に記憶される。その後、変数PFの値が“1”に等しく、ただ1つの単一パルスビームが高解像度モード中にパルス源投光器3から発射されていることを示しているので(ブロックWでノ−“N”)、制御はブロックXXに移り、ここでは変数Tp として記憶される値は検索され、第1の更新された値を提供するために予め定められた量だけ増加される。第1の更新された値はその後変数Tp として記憶される。実施例では、本発明の好ましい実施形態にしたがって、変数Tp の値は第1の予め定められた時間の期間(即ち約100ps)の値に等しい量だけブロックXXで増加され、第1の更新された値は200に等しい。
【0071】
制御はブロックYYへ移り、ブロックYYでは、制御プロセッサ30はパルス源投光器3を再度制御してサンプル4aを照射するための別のパルスビームをパルス源投光器3を発射させる。その後、タイマー30bがパルスビームの発射が終了したときに開始するようにリセットされ(ブロックY1'')、変数PF値は“1”だけ増加される。その後、ブロックT−Wにより示されるステップは前述した方法と類似の方法で再度実行されるが、ただしブロックUで、タイマー30bがブロックXXで前もって得られた第1の更新された値に(ブロックTで)到達したことに応答して“サンプリング期間”(例えば少なくとも100ps)の期間中に検出器アレイ25のゲートアレイ25cがエネーブルされる点を除いてである。また、ブロックUで検出器アレイ25により出力され、予め定められたしきい値レベルを超えた振幅を有すると決定されている各それぞれの信号では、信号は信号に対応する波長を検出した放射検出器素子に対応するフレーム記憶装置F2内の特定の記憶ビン70に記憶される(ブロックV)。これらの信号の1つを表す曲線の例示的な部分が図28のbに示されている。
【0072】
先にパルスビームを発射した結果として信号がブロックVにおいて記憶された後、変数PF値は“2”に等しいので(2つのパルスビームだけが高解像度の動作モード中に発射されることを示しており、即ちブロックWで“N)、制御はブロックWを経てブロックXXへ移る。ブロックXXで、変数Tp として最も最近記憶された値(即ち第1の更新された値)が検索され、第2の更新された値(例えば300ps)を与えるために予め定められた時間値(例えば100ps)に等しい量だけ増加される。第2の更新された値はその後、変数Tp として記憶される。その後、タイマー30bはパルスビームの発射が終了したときに開始するように再度リセットされ(ブロックY1''),ブロックY2''−Wにより示された処理手順は前述した方法と類似の方法で実行されるが、ただし、ブロックUで、タイマー30bがブロックXXで特定された第2の更新された値(例えば300ps)に(ブロックTで)到達したことに応答して検出器アレイ25のゲートアレイ25cがエネーブルされる点を除く。またブロックUで検出器アレイ25により出力され、予め定められたしきい値レベルを超えた振幅を有すると判定されている各信号では、信号は信号に対応する波長を検出した放射検出器素子に対応するフレーム記憶装置F3内の特定の記憶ビン70に記憶される(ブロックV)。これらの信号の1つを表す曲線の例示的な部分が図28のcに示されている。
【0073】
信号がブロックVに記憶された後、PFの値が“3”に等しい(3つのパルスビームが高解像度の動作モード中に発射されることを示しており、即ちブロックWで“N)とを仮定すると、制御はブロックWを経てブロックXXへ再度移行する。ブロックXXで、変数Tp の最も最近記憶された値(即ち第2の更新された値)が検索され、第3の更新された値(例えば400ps)を与えるために第1の予め定められた長さの時間値(例えば100ps)に等しい量だけ増加される。第3の更新された値はその後、変数Tp として記憶される。ブロックYYで、パルス源投光器3に別の(即ち第4の)パルスビームを発射されるようにパルス源投光器3を再度制御する。ブロックY1''で、タイマー30bはパルスビームの発射がブロックYYで終了したときに開始するように再度リセットされ,ブロックY2''で、PF値は“1”だけ値“4”へ増加される。制御プロセッサ30が、タイマー30bが第3の更新された値(例えば400ps)に到達したことを決定したとき、制御プロセッサ30は検出器アレイ25のゲートアレイ25cを再度エネーブルする。またブロックUで検出器アレイ25により出力され、予め定められたしきい値レベルを超えた振幅を有すると決定されている各それぞれの信号では、信号は信号に対応する波長を検出した放射検出器素子に対応するフレーム記憶装置F4内の特定の記憶ビン70に記憶される(ブロックV)。これらの信号の1つの部分を表す例示的な曲線が図28のdに示されている。
【0074】
別の例として、図32はサンプリング期間にわたって検出器アレイ25により検出されたときの種々のタイプのマーカーの例示的な放射応答プロフィールを合成的に示している。
【0075】
制御プロセッサ30が変数PFの値が“4”に等しいことを決定し、第4のパルスビームが高解像度動作モード中に発射されていることを示した後(ブロックWで“Y”)、制御はブロックZへ移る。ブロックZで、制御プロセッサ30はぞれぞれのフレーム記憶装置F1−F4の記憶ビン70の対応するものから信号を検索し、検索された信号を使用して予め定められたアルゴリズムを行い、それぞれの減衰時定数を計算する。実施例では図28のa−dと図31のbを参照すると、1)フレーム記憶装置F1の第1の記憶ビン70aが図28のaに示されている曲線と類似の曲線を有する信号を記憶し、2)フレーム記憶装置F2の記憶ビン70bが図28のbに示されている曲線と類似の曲線を有する信号を記憶し、3)フレーム記憶装置F3の記憶ビン70cが図28のcに示されている曲線と類似の曲線を有する信号を記憶し、4)フレーム記憶装置下4 の記憶ビン70d が図28のdに示されている曲線と類似の曲線を有する信号を記憶していると仮定すると、制御プロセッサ30はこれらの信号を検索し、予め定められアルゴリズムでこれらを使用して、これらの信号に基づいて減衰時定数を計算する。それぞれのフレーム記憶装置F1−F4の他の対応する記憶ビン70に記憶された信号の減衰時定数を決定するために類似の処理が制御プロセッサ30により実行される。それぞれのフレーム記憶装置F1−F4の対応する記憶ビン70からの信号について計算された減衰時定数は表T2のそれぞれの記憶ビン74に記憶されている。実施例では、それぞれのフレーム記憶装置F1−F4の記憶ビン70a−70dから検索された情報に基づいて計算された減衰時定数(TC)値は表T2の記憶ビン74dに記憶されている。
【0076】
予め規定されたアルゴリズムは、信号情報に基づいて減衰時定数を計算するための任意の適切な既知のタイプのアルゴリズムであることに留意すべきである。
【0077】
減衰時定数がブロックZで計算された後、制御はコネクタ5を経て図13のブロックAAに移行し、ここで本発明のスペクトル解析モードにしたがった処理手順が実行される。スペクトル解析モードにしたがって、ブロックAAで、制御プロセッサ30は、記憶ビン70の行71a−71nのうちそこに信号を記憶している行を決定するため(即ちこれらの信号はブロックVで前もって記憶された)フレーム記憶装置F1の記憶ビン70を検査する。前述したように(および制御プロセッサにより知られているように)、記憶ビン70の各行71a−71nは特定の帯域に対応する。それにおいて、検出器アレイ25の放射検出器素子のそれぞれの行により検出される波長の特定の帯域内の波長を有する信号を記憶しており(便宜上、各行71a−71nはサンプル4aに含まれるマーカー40により放射された特定の波長に対応するとを単に仮定する。)記憶ビン70の各行71a−71nも(行が対応する波長帯域内にある)1以上の基準マーカー放射波長値に対応し、これらの基準放射波長値として表T1の同一行(図7および8参照)内に位置する対応するマーカーにも対応する。このように、信号を含んでいることが決定された記憶ビン70のこれらの行71a−71nに対しては、制御プロセッサ30は記憶ビン70のこれらの行71a−71n(およびしたがって記憶ビンと、これらの記憶ビンに記憶されている信号波長)を、表T1からの対応する1以上の基準マーカー放射波長値に相関する(ブロックBB)。実施例では、制御プロセッサ30は、行71aが波長405nmに対応することを知っていると仮定すると、相関ステップは制御プロセッサ30により実行され、値405nmを表T1からの基準放射波長値と比較し、それによってこの表中の一致した基準放射波長値を発見する。この例では、マーカーINDO1が405nmの一致した基準放射波長値を有することが図7で認められる。
【0078】
制御プロセッサ30が、記憶ビン70のそれぞれのこれらの行71a−71n(およびこれらのビンに記憶されているそれぞれの信号波長)を、表T1の単一タイプのみのマーカーの基準放射波長に相関することを決定した場合(ブロックCCで “N”)、制御はコネクタ6を経てブロックHHへ移行し、ブロックHHでは、制御プロセッサ30は表T1からの波長値に関連するマーカーの名称を識別する情報を検索し、ディスプレイ32にマーカーの名称を表示する。前述の例では、行71aが表T1からの405nmの基準放射波長値(図7の列3を参照)に対応することを決定した後、制御プロセッサ30は表T1から“INDO1”を特定する関連した情報を検索し、この情報をディスプレイ32上に示す。オペレータは与えられたマーカーの名称を関連するプロテインに関連付けて、サンプル4aに存在するプロテインのタイプと、対応する癌細胞のタイプを決定する。
【0079】
本発明の他の実施形態にしたがって、他の情報もディスプレイ32で与えられることに注意すべきである。実施例で、前述したように、マーカー名称を特定する情報に加えて、表T1はまたマーカーの名称に対応するプロテイン識別子名称を特定する情報を記憶していることが好ましい。本発明の別の実施形態にしたがって、表T1はまたこれらのプロテインのそれぞれ1つを発生する特定のタイプの癌細胞の識別子名称を特定する情報も記憶している。このように1実施形態では、制御プロセッサ30が、記憶ビン70のそれぞれのこれらの行71a−71nが表T1の単一タイプのみのマーカーの基準放射波長に相関することを決定した場合(ブロックCCで“N”)、ブロックHHで制御プロセッサ30は基準放射波長値に関連するプロテインおよび/または癌細胞の名称を特定する情報を検索し、この情報をディスプレイ32に示すためにディスプレイ32を制御する。
【0080】
記憶ビン70のそれぞれの行71a−71nに対してが表T1からの1以上の単一タイプのマ−カが基準放射波長に対応することが決定された場合(ブロックCCで“Y”)、記憶ビン70の行71a−71nが対応するマーカーを決定するための時間解析が実行される。実施例で、記憶ビン70の行71a−71nの1つがブロックCCで、表T1からの値533nmに対応すると決定されてもよい。図7および8で分かるように、値533nmは図7、8では複数回現れ、したがってカルシウムグリーンおよびTOTOー1のような単一のマーカーよりも多くのピーク放射波長値である。この場合、ブロックCCの実行により制御はブロックDDへ通過し、ブロックDDではスリットイメージによる照射に応答して蛍光放射を放射したマーカーを解像するための時間解析が開始される。ブロックCCのステップは任意の適切な表処理技術を使用して実行されてもよいことに注意すべきである。
【0081】
時間解析にしたがって、制御プロセッサ30は表T1からの基準蛍光減衰時定数値を、表T1からの複数のマーカーに対応することがブロックCCで決定されたこれらの行71a−71nの記憶ビン70に対応する計算された蛍光減衰時定数値と比較する。前述したように、基準減衰時定数値は、サンプル4aで使用される種々のタイプのマーカーの既知の減衰時定数値を規定する。種々のタイプのマーカーに関連した(表T1に記憶されている)基準時定数値の数の例が図7および8の列5で示されている。計算された減衰時定数値を、記憶ビン70に対応する基準減衰時定数値と比較することにより、これらの記憶ビン70に対応するマーカーと、スリットイメージによる照射に応答して蛍光放射を放射するマーカーが決定されることができる。したがって、1以上の特定のタイプのプロテインがサンプル4aに存在することも決定され、対応する癌細胞のタイプもサンプル4aに含まれることを示す。
【0082】
図13を再度参照して、時間解析をさらに詳細に説明する。ブロックDDで、制御プロセッサ30は(表T1からの)複数の単一タイプのマーカーの基準放射波長値に対応することがブロックCCで決定されたこれらの行71a−71nの記憶ビン70に対応する各減衰時定数値を検索する。各減衰時定数値はこれらの行71a−71nのそれぞれの記憶ビン70に対応する(表T2の)記憶ビン74から検索される。例により説明すると、ブロックCCで行71aが表T1からの複数の単一タイプのマーカーの基準放射波長値に対応することが決定されたと仮定すると、ブロックDDで、行71aに対応する(表T2の)記憶ビン74の行74bから減衰時定数値が検索される。
【0083】
ブロックDDの実行後、制御はブロックEEへ移る。ブロックEEで、制御プロセッサ30は複数の単一タイプのマーカーに対応することがブロックCCで決定されている行71a−71nに対応する基準放射波長に対応した基準減衰時定数値を検索する。例として、前述の例では、制御プロセッサ30は表T1から行71aが対応する基準放射波長に対応した基準減衰時定数値を検索する。前述したように、表T1に記憶されている少なくとも幾つかの基準減衰時定数が図7、8の列5で示されており、これらの基準減衰時定数に対応する基準放射波長値の例は図7、8の列1に示されている。
【0084】
その後、制御はコネクタ7を経て図14のブロックFFへ移行する。ブロックFFで、制御プロセッサ30はブロックDDで検索された各値をブロックEEで検索された各値と比較し、ブロックDDで検索された値がブロックEEで検索されたそれぞれの値の予め定められた範囲内であるか否かを決定する。本発明の1実施形態にしたがって、ブロックFFのステップは、ブロックDDで検索されたそれぞれの値がブロックEEで検索されたそれぞれの値の±10%内であるか否かを決定するために実行される。
【0085】
ブロックFFで“ノー”であるならば、情報はディスプレイ32で示されず、制御はブロックGGへ移行し、ブロックGGで方法が終了される。実施例では、ブロックDDで検索された値が1nsおよび1.7nsであり、ブロックEEで基準減衰時定数2.4nsと3.4nsが検索されたと仮定すると、ブロックFFのステップの動作により制御はブロックGGへ移行する。
【0086】
ブロックFFにおいて、ブロックDDで前もって検索されたそれぞれの減衰時定数値がブロックEEで前に検索された1つの基準減衰時定数値の予め定められた範囲内であるならば(ブロックFFで“Y”)、制御はブロックHHへ移行する、ブロックHHでは制御プロセッサ30はこの基準減衰時定数値に関連するマーカーの名称を特定する情報を検索し、ディスプレイ32上にマーカーの名称を示すようにディスプレイ32を制御する。その後、オペレータは示されたマーカー名称を関連するプロテインに関連付け、サンプル4a中に存在するプロテインのタイプと、対応する癌細胞のタイプを決定する。例として、ブロックDDで前もって検索された減衰時定数値が1nsと1.7nsであり、ブロックEEで1nsと1.7nsの基準減衰時定数値が検索されると仮定すると、ブロックFFのステップの実行により制御はブロックHHへ移り、ブロックHHでは、これらのそれぞれの減衰時定数値に関連するマーカーの名称がディスプレイ32で示される。また例として、ブロックDDで前もって検索された減衰時定数値が1nsと1.7nsであり、ブロックEEで2.7nsと1.7nsの基準減衰時定数値が検索されるとすると、ブロックFFのステップの実行により制御はブロックHHへ移行し、ブロックHHでは、値1.7nsに対応するマーカーの名称(例えばTOTO−1)だけがディスプレイ32で示される。
【0087】
ブロックHHにより示されているステップは他の適切な実施形態にしたがって実行されてもよいことに注意すべきである。例により、前述したように、基準減衰時定数値とマーカー名称識別子を特定する情報に加えて、表T1はまたマーカー名称に対応するプロテイン識別子名称を特定する情報を記憶することが好ましい。別の実施形態によれば、表T1はまたそれぞれのこれらのプロテインを発生する特別なタイプの癌細胞の識別子名称を特定する情報も記憶してもよい。このように、ブロックFFで、ブロックDDで検索された1つの減衰時定数値がブロックEEで検索された基準減衰時定数値の予め定められた範囲内であることを決定した後、ブロックHHで制御プロセッサ30は、1以上のこれらの識別子名称をディスプレイ32上に示すため、基準減衰時定数値に関連する1以上のこれらの識別子名称を特定する情報を検索してもよい。
【0088】
ブロックHHにより識別されるステップが実行された後、ブロックIIで、制御プロセッサ30は、ブロックOで前もって得られた分類リストから検索された付加的なステップ数値(即ち変数STEPの値)が存在するか否かを決定する。ブロックIIで“イエス”であるならば、制御プロセッサ30はブロックKKでリストからこれらの値のうち次に小さい値を検索する。その後、ブロックLLで、制御プロセッサ30はサンプルスライド4を前進するように段18を制御し、それによってスライドのエッジ4a' は検索されたステップ数値に対応する位置に到達する。制御はコネクタ8を経て図11のブロックRへ移行し、ブロックRでは前述したように方法が継続する。
【0089】
ブロックIIで“ノー”ならば(ブロックOで前もって分類されたリストから検索された値が存在しないことを示す)、制御はブロックJJへ移行し、ブロックJJで方法が終了される。
【0090】
本発明の別の観点について説明する。前述したように、初期スクリーニングモード中において、サンプル4aが完全に“スクリーン”された後、変数STEP値が予め記憶され、マーカー放射波長が検出器アレイ25により検出されたこと、すなわち1以上のプロテインおよび対応する癌細胞がサンプル4aに含まれることを示すか否かを決定するためにメモリ31はブロックJで検査される(ブロックK)。また前述したように、サンプル4aに含まれるマーカー40は典型的に対応する癌細胞の領域(即ちイメージングシステムに可視の領域)を実質上カバーする。このように、これらのマーカーの放射波長(即ちイメージ)を検出することにより、癌細胞の形態および大きさは決定されることができる。本発明のこの特徴にしたがって、サンプルスライド4が全ての426“ステップ”を前進し、1以上のプロテインがサンプル4aに含まれていることを決定された後(ブロックK1の前に)、制御プロセッサ30は癌細胞のおおよその寸法(例えば面積)と形状を決定する処理を実行する。例として、制御プロセッサ30は(初期スクリーニングモード処理の実行結果として)信号を記憶しているフレーム記憶装置F1の記憶ビンの数を決定するためにフレーム記憶装置F1を検査する。制御プロセッサ30が検出器アレイ25の各放射検出器素子の表面領域(例えば5乃至10ミクロン)を知っていると仮定すると、制御プロセッサは癌細胞のおおよその領域を決定するアルゴリズムを実行する。例示として、制御プロセッサ30は個々の放射検出器素子の表面面積の既知の値を、記憶された信号であると決定された記憶ビン70の数により乗算することによりアルゴリズムを実行して、癌細胞のおおよその面積を表す値を計算する。
【0091】
その後、制御プロセッサ30は、ディスプレイ32を制御し、イメージングシステム11のオペレータに対して計算された値を与える、制御プロセッサ30はまた記憶ビンから信号を検索してもよく(即ち記憶され検出したイメージを検索する)、ディスプレイ32上にイメージを示し、それによってサンプル4aに含まれている癌細胞の形状はオペレータにより観察されることができる。このステップはイメージが適切にスケールされるように適切なスケーリング係数を使用して実行されてもよい。
【0092】
また、本発明にしたがって、既知のタイプの癌細胞のイメージを表す情報が対応するプロテインとマーカー情報に関連して表T1に記憶されてもよい。本発明のこの特徴にしたがって、検出器アレイ25により検出されたイメージは表T1に記憶された情報と比較され、比較されたイメージが実質上相互に類似しているか否かを決定する。このステップは任意の適切な光学的相関技術を使用して行われてもよい。比較されたイメージが実質上相互に類似していると決定されたならば、制御プロセッサ30は表T1から(検出されたイメージと実質上類似であると決定された)イメージを検索し、ディスプレイ32上に検索されたイメージを示すようにディスプレイ32を制御する。このステップは検出されたイメージと、イメージに対応する癌細胞の名称と、これらのイメージに対応する癌細胞、プロテインおよび/またはマーカーの名称等、他の適切な情報をディスプレイ32上に表示する行われてもよいことに注意すべきである。適切なスケール係数もこれらの処理中に使用されてもよい。
【0093】
癌細胞の形状および/または寸法を決定するためのこれらの処理手順は好ましくはブロックMの前に実行され、ブロックMではシステムの解像度と拡大レベルが増加され、それによって対物レンズ16は1:1の拡大レベルを与えるが、他の実施形態では他の拡大レベルが使用されてもよい。これらの実施形態では、他の拡大レベルが癌細胞の領域と形状を決定する場合に考慮される(即ち適切なスケーリング係数が使用される)。
【0094】
図29を参照すると、例示的なブロック図60が示されており、サンプル4aと、分子バイオロジ−ブロック52と、診断ブロック54と、CPU30' および本発明のイメージングシステムの種々の光コンポーネント3−25cを表すCPU30' およびブロック50を含む本発明のイメージングシステム(“56”のラベルを付されている)とを含んでいる。本発明の前述の説明を考慮すると、イメージングシステムによりサンプル4aで多数のマーカーを使用して癌に関連するプロテインの存在についてサンプル4aを検査することができることが認識されることができる。これは前述の初期スクリーニングモード処理を使用して実現される。1以上の癌に関連するプロテインがサンプル4aに含まれることが決定された後、本発明のスペクトルおよび時間解析にしたがった処理はCPU30' 内で実行され、それによってサンプル4aに含まれるプロテインの特別なタイプが識別される。図29のシステムはサンプル4aに関するこれらおよびその他の決定が行われることを可能にするための人工的なインテリジェンス技術を使用する訓練可能な神経網ベースのシステムとして実施されてもよいことに注意すべきである。例として、本発明の時間/スペクトル解析中に識別されたプロテインのタイプに基づいて、(ブロック52で)前述の方法でプロテインを発生する癌細胞のタイプを決定することができ、また適切な分子バイオロジ−技術を使用して、プロテインを生成する(サンプル4aからの)細胞組織のDNA内の特別な遺伝子に欠陥または異常があるか否かを決定することもできる。診断/勧告がその後、ブロック54で医療関係者により行われる。例えば、1以上の遺伝子に欠陥があることが決定されたとを仮定すると、これらの遺伝子を適切な化学的置換物で置換することが適切である。特定のタイプの癌細胞がサンプル4aに含まれるプロテインの識別に基づいて識別されることができるので、本発明のイメージングシステムはガンが発達の早期の段階で検出されることを可能にする。例として、サンプル4a中のプロテインの識別は人間の染色体のブレークポイントを示すことができ、人間の22の染色体の全てを同時にマッピングするためにさらに処理が実行されることを可能にし、人間のゲノムプログラムが加速されることを可能にする。
【0095】
本発明を好ましい実施形態に関して特別に示し説明したが、形態および詳細の変化が本発明の技術的範囲を逸脱せずに行われてもよいことが当業者により理解されよう。例として、本発明の別の実施形態では、プリズム23は格子20の代わりに本発明のイメージングシステム中で使用されてもよい。また、本発明の方法はサンプル4aを検査するため(図2および3の)イメージングシステム1' を使用するコンテキストで説明したが、適切なケースでは図1および2のイメージングシステム1が使用されてもよいことに注意すべきである。この場合、システム1は一度に(すなわち各“ステップ”で)サンプル4aを単一波長でのみ照射するために使用され、それによってサンプル4aがプロテインの存在について試験されることを可能にする。イメージングシステム1が使用される場合、本発明の方法は前述した方法と類似の方法で実行されるが、サンプル4aが各“ステップ”で単一波長でのみ照射される点で異なっている。また、前述の種々の長さの時間(例えば第1および第2の予め定められた時間期間)と、本発明のイメージングシステムの種々のコンポーネントで前述した寸法(例えば幅(W)、(W1)、(W2)、長さ(L)等)は単なる例示であり、本発明を限定するものではない。また、サンプルスライド4を前進するステップはCPU30またはCPU30のオペレータにより制御されるように任意の適切な周波数で実行されてもよい。
【0096】
さらに、前述したように、光源の投光器3から発射されたパルスの好ましい継続期間(パルス幅)は約1nsであるが、応用可能な性能標準に基づいて他のパルス幅が使用されてもよい。例として、選択されたパルス幅は、1)サンプルスライド4が前進される選択された速度と、2)励起波長が変化される選択された速度と、および/または3)予測されたマーカー放射励起応答時間に依存している。パルス源投光器3のパルスレートもこれらを考慮して選択されてもよい。
【0097】
さらに、サンプルスライド4がマスク14の各個々のスリットの幅(W1)に実質上等しい距離だけ各ステップで前進されるコンテキストについて本発明を説明したが、段18はスライド4を他の適切な距離だけ変位するように制御されてもよいことに注意すべきである。例として、スリットイメージグループ14a''−14c''からの個々のスリットイメージによってサンプル4aのさらに大きな領域を照 射させるため、対物レンズ16の拡大レベルがブロックMにおいて増加されると仮定し、ここで各個々のスリットイメージが前述したよりも大きな幅を有すると、スライド4の前進ステップはこのさらに大きな幅に等しい距離だけスライド4を変位することにより実行されてもよい。さらに、スペクトルおよび時間解析を4つのパルスが各ステップでパルス源投光器3から発射されるコンテキストで説明したが、例えばサンプル4aで使用されるマーカーの蛍光応答減衰時間期間に応じてて、このパルス発射数よりも多い或いは少ないパルスが発射されることも本発明の技術的範囲内であることに注意すべきである。
【0098】
本発明のイメージングシステム1および1' は好ましくは走査方向では毎秒約1000画素(検出器アレイ素子)の速度および断面走査方向では毎秒約256,000画素の速度で検出器アレイ25により検出される波長を同時に評価する能力を有することにさらに注意すべきである。さらに、本発明のイメージングシステム1および1' は癌に関連するプロテインだけを検出し識別することに限定されない。これらのシステム1および1' はまた他の所望のタイプの物質および/または細胞の検出に使用されてもよい。
【0099】
さらに、本発明は、スライド4でのみ使用することに限定されないことに注意すべきである。例として、不透明基体がスライド4の代わりに使用されてもよい。また、透明の基体が使用されるとを仮定すると、この透明基体を透過して蛍光材料を励起することも本発明の技術的範囲内である。例により、励起波長は蛍光マーカーを励起するために透明なスライドの下方の位置から与えられてもよい。
【図面の簡単な説明】
【図1】 本発明の1実施形態にしたがって構成されたイメージングシステムの図。
【図2】 本発明の1実施形態にしたがって構成されたイメージングシステムの図。
【図3】 図1および2で示されているコンポーネントを含んでいる本発明の別の実施形態にしたがって構成されたイメージングシステムの一部を示す図。
【図4】 図1および2が相互に関連している方法を示した説明図。
【図5】 図2および3が相互に関連している方法を示した説明図。
【図6】 サンプル4aが配置されている例示的なサンプルスライド4と、仮想の行がサンプルスライド4上に重畳されているサンプルスライド4を示した図。
【図7】 図6のサンプル4aで使用されてもよい種々の例示的なタイプの蛍光材料を識別し、これらの蛍光材料のさらに対応する“励起”波長、放射波長、減衰時定数を示している表の図。
【図8】 図6のサンプル4aで使用されてもよい種々の例示的なタイプの蛍光材料を識別し、これらの蛍光材料のさらに対応する“励起”波長、放射波長、減衰時定数を示している表の図。
【図9】 本発明の方法の一部を示しているフロー図。
【図10】 本発明の方法の一部を示しているフロー図。
【図11】 本発明の方法の別の部分を示しているフロー図。
【図12】 本発明の方法の別の部分を示しているフロー図。
【図13】 本発明の方法の別の部分を示しているフロー図。
【図14】 本発明の方法の別の部分を示しているフロー図。
【図15】 図1および2のイメージングシステムのレンズレットアレイ13を示した図。
【図16】 マスク14を見下ろした斜視図から観察したときの図1および3のイメージングシステム部分のマスク14を示した図。
【図17】 全て図1および図3のイメージングシステムのコンポーネントであり、図2および図3のイメージングシステムのコンポーネントである格子20、検出器アレイ25の表面25a、結像光学系22の斜視図と、種々の蛍光材料40a−40cとこれらの蛍光材料の例示的な放射波長を示している図。
【図18】 図1および図3の段18に配置された図6のサンプルスライド4の側面と、図面全体を通じて段18の種々の位置に位置付けられているサンプルスライド4を照射するためイメージングシステム内で発生されたスリットイメージビーム14a' −14c' とを示した図。
【図19】 図1および図3の段18に配置された図6のサンプルスライド4の側面と、図面全体を通じて段18の種々の位置に位置付けられているサンプルスライド4を照射するためイメージングシステム内で発生されたスリットイメージビーム14a' −14c' とを示した図。
【図20】 図16のマスク14の斜視図と、それぞれ図18、図19で示されているスライド4の位置に対応した位置のサンプルスライド4とを示した図。
【図21】 サンプルスライド4と段18上を見下ろした斜視図から観察したときの図18乃至図19のサンプルスライド4および段18と、図18乃至図19のスリットイメージビーム14a' −14c' がサンプルスライド4を照射した結果としてサンプルスライド4に現れたスリットイメージグループ14a”−14c”とを示した図。
【図22】 サンプルスライド4と段18上を見下ろした斜視図から観察したときの図18乃至図19のサンプルスライド4および段18と、図18乃至図19のスリットイメージビーム14a' −14c' がサンプルスライド4を照射した結果としてサンプルスライド4に現れたスリットイメージグループ14a”−14c”とを示した図。
【図23】 サンプルスライド4と段18上を見下ろした斜視図から観察したときの図18乃至図19のサンプルスライド4および段18と、図18乃至図19のスリットイメージビーム14a' −14c' がサンプルスライド4を照射した結果としてサンプルスライド4に現れたスリットイメージグループ14a”−14c”とを示した図。
【図24】 サンプルスライド4と段18上を見下ろした斜視図から観察したときの図18乃至図19のサンプルスライド4および段18と、図18乃至図19のスリットイメージビーム14a' −14c' がサンプルスライド4を照射した結果としてサンプルスライド4に現れたスリットイメージグループ14a”−14c”とを示した図。
【図25】 サンプルスライド4と段18上を見下ろした斜視図から観察したときの図18乃至図19のサンプルスライド4および段18と、図18乃至図19のスリットイメージビーム14a' −14c' がサンプルスライド4を照射した結果としてサンプルスライド4に現れたスリットイメージグループ14a”−14c”とを示した図。
【図26】 サンプルスライド4と段18上を見下ろした斜視図から観察したときの図18乃至図19のサンプルスライド4および段18と、図18乃至図19のスリットイメージビーム14a' −14c' がサンプルスライド4を照射した結果としてサンプルスライド4に現れたスリットイメージグループ14a”−14c”とを示した図。
【図27】 サンプルスライド4と段18上を見下ろした斜視図から観察したときの図18乃至図19のサンプルスライド4および段18と、図18乃至図19のスリットイメージビーム14a' −14c' がサンプルスライド4を照射した結果としてサンプルスライド4に現れたスリットイメージグループ14a”−14c”とを示した図。
【図28】 種々のサンプリング期間中に図17の検出器アレイにより検出された放射波長に対応する信号の例示的な曲線を示した特性図。
【図29】 (“56”のラベルを付された)本発明のイメージングシステムが図6のサンプル4aに関する種々のタイプの医療データが得られることを可能にしている例示的なシステム60を示したブロック図。
【図30】 図17の検出器アレイ25の表面25aの斜視図と、図1および図2のイメージングシステムおよび図2および図3のイメージングシステムのフレーム記憶装置F1−F4の斜視図。
【図31】 本発明の方法にしたがって使用される情報を記憶している図2のイメージングシステム部分の表T1と、図30のフレーム記憶装置F1−F4の斜視図と、本発明にしたがって計算されたマーカー放射減衰時定数値を記憶している図1および図2のイメージングシステムおよび図2および図3のイメージングシステムの表T2の斜視図。
【図32】 例示的なマーカー放射応答プロフィール特性図。
Claims (5)
- サンプル中の有機物質の存在を検出し、少なくともあるタイプの有機物質は特定のタイプの蛍光材料と結合されるイメージングシステムにおいて、
複数のスリットイメージビームを使用して、少なくともサンプルの一部分を少なくとも1つの励起波長で照射し、1以上の蛍光材料にそれぞれの特徴的な波長を放射させる同調可能な励起光源と、
放射された特徴的な波長を検出するように配置され、検出された1つの放射された特徴的な波長に対応する信号を出力するために前記放射された特徴的な波長の検出に応答する光検出器アレイと、
出力ユーザインターフェイスと、
前記光検出器アレイの出力と、前記出力ユーザインターフェイスに結合され、前記検出器アレイにより出力された少なくとも1つの前記信号を受信するように応答し、それによって少なくとも1つの前記有機物質がサンプル内に存在するものとして識別するメッセージをユーザに与えるために前記出力ユーザインターフェイスを制御する制御プロセッサとを具備しているイメージングシステム。 - さらに、前記制御プロセッサと両方向で結合され、複数の基準波長値と、有機物質を識別する情報とを記憶し、各基準波長値は少なくともそれぞれの有機物質に対応しているデータテーブルと、
前記制御プロセッサと両方向で結合され、記憶ビンの複数のグループを含み、記憶ビンの各前記グループは前記データテーブルに記憶されている少なくとも1つの基準波長値に対応している記憶装置とをさらに具備しており、
前記制御プロセッサはまた、対応するそれぞれの記憶ビンに個々のこれらの信号を記憶するために、前記光検出器アレイにより出力された前記信号の受信にも応答し、前記制御プロセッサは、前記対応する1つの前記記憶ビンを含んでいる個々のグループを対応する1つの基準波長値およびデータテーブルに記憶された情報により識別される対応する1つの有機物質と相関させ、前記制御プロセッサはまた、対応する1つの有機物質がサンプル中に存在するものとして識別するメッセージをユーザへ与える出力ユーザインターフェースを制御する請求項1記載のイメージングシステム。 - さらに、前記制御プロセッサと両方向で結合され、複数の基準波長値と、有機物質を識別する情報とを記憶し、各基準波長値は少なくとも1つの有機物質に関連され、さらに基準減衰時定数値を記憶し、各基準減衰時定数値はそれぞれ1つの基準波長値とそれぞれ1つの有機物質に対応しているデータテーブルと、
前記制御プロセッサと両方向で結合され、記憶ビンの複数のグループを含み、記憶ビンの前記各グループは前記データテーブルに記憶されている少なくとも1つの基準波長値に対応している記憶装置とをさらに具備しており、
前記制御プロセッサはまた、対応する1つの記憶ビンに個々のこれらの信号を記憶するために、前記光検出器アレイにより出力された前記信号の受信に応答し、前記制御プロセッサはまた、記憶ビンに記憶されている各信号に基づいてそれぞれの放射減衰時定数値を計算し、前記制御プロセッサはまた、信号を記憶している前記記憶ビンの個々のグループが複数の有機物質に関連されるそれぞれ1つの前記基準波長値に対応するか否かを決定し、前記制御プロセッサはまた、計算された放射減衰時定数値を、対応する1つの基準減衰時定数値および対応する1つの有機物質と相関させるために、記憶ビンの個々のこれらのグループがそれぞれ1つのこれらの基準波長値に対応することの決定に応答し、前記制御プロセッサはまた、対応する1つの有機物質がサンプル中に存在するものとして識別するメッセージをユーザへ与える出力ユーザインターフェースを制御する請求項1記載のイメージングシステム。 - 前記光検出器アレイは放射検出素子の複数の行を有する放射感知性表面を含んでおり、前記イメージングシステムはさらに、予め定められた波長帯域内である前記放射された特徴的な波長の1つを、これらの予め定められた波長帯域に対応する放射検出器素子の特定の1つの前記行に導くための光誘導装置をさらに具備している請求項1乃至3のいずれか1項記載のイメージングシステム。
- 有機物質は対応する癌細胞のタイプに関連する種々のタイプのプロテインを含んでいる請求項1乃至3のいずれか1項記載のイメージングシステム。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/US1999/026542 WO2001035078A1 (en) | 1999-11-09 | 1999-11-09 | Method and apparatus for performing cell analysis based on simultaneous multiple marker emissions from neoplasia (casmmen) |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2003514222A JP2003514222A (ja) | 2003-04-15 |
| JP2003514222A5 JP2003514222A5 (ja) | 2006-10-19 |
| JP4536986B2 true JP4536986B2 (ja) | 2010-09-01 |
Family
ID=22274028
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2001536559A Expired - Lifetime JP4536986B2 (ja) | 1999-11-09 | 1999-11-09 | 腫瘍からの同時多数マーカー放射(casmmen)に基づいた細胞解析を行う装置 |
Country Status (4)
| Country | Link |
|---|---|
| EP (1) | EP1147400B1 (ja) |
| JP (1) | JP4536986B2 (ja) |
| DE (1) | DE69940524D1 (ja) |
| WO (1) | WO2001035078A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5563405B2 (ja) * | 2010-08-24 | 2014-07-30 | 荏原実業株式会社 | 分光画像取得装置及び方法 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8623494D0 (en) * | 1986-09-30 | 1986-11-05 | Mackay C D | Assay technique |
| JPH0694526A (ja) * | 1990-12-28 | 1994-04-05 | Nec Corp | 光パルス発生方法および装置ならびに時間分解分光装置 |
| US5784162A (en) * | 1993-08-18 | 1998-07-21 | Applied Spectral Imaging Ltd. | Spectral bio-imaging methods for biological research, medical diagnostics and therapy |
| US5817462A (en) * | 1995-02-21 | 1998-10-06 | Applied Spectral Imaging | Method for simultaneous detection of multiple fluorophores for in situ hybridization and multicolor chromosome painting and banding |
| DE4136769A1 (de) * | 1991-11-05 | 1993-05-06 | Humboldt-Universitaet Zu Berlin, O-1086 Berlin, De | Verfahren zum diagnostizieren von mit fluoreszierenden substanzen angereicherten, insbesondere tumoroesen gewebebereichen |
| FR2694193B1 (fr) * | 1992-07-28 | 1994-10-28 | Abraxas Bio Labs Sa | Méthode de cytodiagnostic utilisant l'alstonine comme marqueur sélectif et kit de diagnostic contenant ce marqueur. |
| WO1994003470A1 (en) * | 1992-08-10 | 1994-02-17 | Davies Richard J | Method and apparatus for screening and diagnosing for cancers |
| FI93781C (fi) * | 1993-03-18 | 1995-05-26 | Wallac Oy | Biospesifinen multiparametrinen määritysmenetelmä |
| DE19634873A1 (de) * | 1996-08-29 | 1998-03-12 | Boehringer Mannheim Gmbh | System zur Unterscheidung fluoreszierender Molekülgruppen durch zeitaufgelöste Fluoreszenzmessung |
| GB9704054D0 (en) * | 1997-02-27 | 1997-04-16 | Univ Cambridge Tech | Assay |
| US5986271A (en) * | 1997-07-03 | 1999-11-16 | Lazarev; Victor | Fluorescence imaging system |
| ATE272224T1 (de) * | 1997-11-17 | 2004-08-15 | Max Planck Gesellschaft | Konfokales spektroskopiesystem und -verfahren |
-
1999
- 1999-11-09 JP JP2001536559A patent/JP4536986B2/ja not_active Expired - Lifetime
- 1999-11-09 EP EP99958870A patent/EP1147400B1/en not_active Expired - Lifetime
- 1999-11-09 DE DE69940524T patent/DE69940524D1/de not_active Expired - Lifetime
- 1999-11-09 WO PCT/US1999/026542 patent/WO2001035078A1/en active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| WO2001035078A1 (en) | 2001-05-17 |
| EP1147400A1 (en) | 2001-10-24 |
| EP1147400B1 (en) | 2009-03-04 |
| DE69940524D1 (de) | 2009-04-16 |
| JP2003514222A (ja) | 2003-04-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7330268B2 (en) | Spectral imaging apparatus and methodology | |
| US7420674B2 (en) | Method and arrangement for analyzing samples | |
| US6005256A (en) | Method and apparatus for performing cell analysis based on simultaneous multiple marker emissions from neoplasia (CASMMEN) | |
| US6958811B2 (en) | Method for the detection of dyes in fluorescence microscopy | |
| US5784152A (en) | Tunable excitation and/or tunable detection microplate reader | |
| US20030151741A1 (en) | Method for investigating a sample | |
| US5885531A (en) | Fluorescence imaging instrument utilizing fish | |
| WO1986002730A1 (en) | A fluorescence imaging system | |
| JP2006098419A (ja) | 照射サンプルの特性寸法の光学的取得方法 | |
| CN108139578A (zh) | 分辨至少两个光谱范围的高分辨率扫描显微术 | |
| US7257289B2 (en) | Spectral microscope and method for data acquisition using a spectral microscope | |
| US20050064427A1 (en) | Method and/or system for identifying fluorescent, luminescent and/or absorbing substances on and/or in sample carriers | |
| US6552794B2 (en) | Optical detection method for improved sensitivity | |
| JP6484234B2 (ja) | 試料の共焦点観察のための装置 | |
| US7119898B2 (en) | Method for the detection of fluorescent light | |
| JP4536986B2 (ja) | 腫瘍からの同時多数マーカー放射(casmmen)に基づいた細胞解析を行う装置 | |
| US7446867B2 (en) | Method and apparatus for detection and analysis of biological materials through laser induced fluorescence | |
| US7596454B2 (en) | Method for separating detection channels of a microscope system | |
| US20220228968A1 (en) | Hyperspectral quantitative imaging cytometry system | |
| CN108801987A (zh) | 共焦分立荧光光谱及荧光寿命探测方法与装置 | |
| CN116478802A (zh) | 一种基因测序仪及基因测序仪的使用方法 | |
| JP2005069827A (ja) | レーザ走査型蛍光顕微鏡 | |
| JP3222270B2 (ja) | 分光ファイバースコープ | |
| JP2008180637A (ja) | 光信号解析方法および光信号解析装置 | |
| CA2497775A1 (en) | Spectral imaging apparatus and methodology |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060829 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060829 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090804 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091029 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100518 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100617 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130625 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4536986 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |