JP4365531B2 - 腫瘍の動的監視のための方法及びシステムとそれに関連する移植可能デバイス - Google Patents
腫瘍の動的監視のための方法及びシステムとそれに関連する移植可能デバイス Download PDFInfo
- Publication number
- JP4365531B2 JP4365531B2 JP2000571817A JP2000571817A JP4365531B2 JP 4365531 B2 JP4365531 B2 JP 4365531B2 JP 2000571817 A JP2000571817 A JP 2000571817A JP 2000571817 A JP2000571817 A JP 2000571817A JP 4365531 B2 JP4365531 B2 JP 4365531B2
- Authority
- JP
- Japan
- Prior art keywords
- tumor
- treatment
- sensor
- sensor unit
- radiation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/1468—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using chemical or electrochemical methods, e.g. by polarographic means
- A61B5/1473—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using chemical or electrochemical methods, e.g. by polarographic means invasive, e.g. introduced into the body by a catheter
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/0002—Remote monitoring of patients using telemetry, e.g. transmission of vital signals via a communication network
- A61B5/0031—Implanted circuitry
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/14539—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue for measuring pH
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/1486—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using enzyme electrodes, e.g. with immobilised oxidase
- A61B5/14865—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using enzyme electrodes, e.g. with immobilised oxidase invasive, e.g. introduced into the body by a catheter or needle or using implanted sensors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/1495—Calibrating or testing of in-vivo probes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/41—Detecting, measuring or recording for evaluating the immune or lymphatic systems
- A61B5/414—Evaluating particular organs or parts of the immune or lymphatic systems
- A61B5/417—Evaluating particular organs or parts of the immune or lymphatic systems the bone marrow
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H20/00—ICT specially adapted for therapies or health-improving plans, e.g. for handling prescriptions, for steering therapy or for monitoring patient compliance
- G16H20/10—ICT specially adapted for therapies or health-improving plans, e.g. for handling prescriptions, for steering therapy or for monitoring patient compliance relating to drugs or medications, e.g. for ensuring correct administration to patients
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H40/00—ICT specially adapted for the management or administration of healthcare resources or facilities; ICT specially adapted for the management or operation of medical equipment or devices
- G16H40/60—ICT specially adapted for the management or administration of healthcare resources or facilities; ICT specially adapted for the management or operation of medical equipment or devices for the operation of medical equipment or devices
- G16H40/63—ICT specially adapted for the management or administration of healthcare resources or facilities; ICT specially adapted for the management or operation of medical equipment or devices for the operation of medical equipment or devices for local operation
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H40/00—ICT specially adapted for the management or administration of healthcare resources or facilities; ICT specially adapted for the management or operation of medical equipment or devices
- G16H40/60—ICT specially adapted for the management or administration of healthcare resources or facilities; ICT specially adapted for the management or operation of medical equipment or devices for the operation of medical equipment or devices
- G16H40/67—ICT specially adapted for the management or administration of healthcare resources or facilities; ICT specially adapted for the management or operation of medical equipment or devices for the operation of medical equipment or devices for remote operation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B2562/00—Details of sensors; Constructional details of sensor housings or probes; Accessories for sensors
- A61B2562/02—Details of sensors specially adapted for in-vivo measurements
- A61B2562/028—Microscale sensors, e.g. electromechanical sensors [MEMS]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B2562/00—Details of sensors; Constructional details of sensor housings or probes; Accessories for sensors
- A61B2562/08—Sensors provided with means for identification, e.g. barcodes or memory chips
- A61B2562/085—Sensors provided with means for identification, e.g. barcodes or memory chips combined with means for recording calibration data
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/10—X-ray therapy; Gamma-ray therapy; Particle-irradiation therapy
- A61N5/1048—Monitoring, verifying, controlling systems and methods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/10—X-ray therapy; Gamma-ray therapy; Particle-irradiation therapy
- A61N5/1048—Monitoring, verifying, controlling systems and methods
- A61N5/1071—Monitoring, verifying, controlling systems and methods for verifying the dose delivered by the treatment plan
Description
<関連出願>
本願は1998年9月30日に提出された仮特許出願第60/102,447号に基づいて優先権を主張する。この出願の内容は本明細書に組み込まれるものとする。
【0002】
<発明の分野>
本発明は診断用医療器具と処置(procedures)、特に、生理的パラメータをモニタするための移植可能デバイス及び方法に関する。
【0003】
<発明の背景>
興味のあるどんな細胞集団の変化もモニタすることができるシステム及びデバイスの利用可能性は、がん治療器具への重要な追加機能であり、腫瘍細胞集団を治療するための最も微妙な時間のより正確な知識を利用可能にすることによって必要性を満足するであろう。このような重要な情報は、今日の経験的かつ幾分一般化された治療計画よりも、相当程度特定的な個別の治療法(treatment regime)を提供することにおいて助けになりうる。
【0004】
悪性細胞集団の生体外研究は、それによって臨床治療の標準的手続(プロトコル)が開発される重要な一般的な原則を確立した。これらの原則は悪性及び正常な細胞集団の間の相違を確定し、悪性疾患の治療において使用されてきた。前臨床的及び臨床的研究の両方において、完全なる腫瘍の抹殺と改善された治癒率を獲得するために、これらの相違を利用する多くの試みがなされてきた。この目標を達成することにおいての主要な障害の1つは、腫瘍細胞の抹殺(治療指数)を増大させながら、正常組織への毒性を最小にすることの困難であった。従って、現在、ほとんどの治療法(治療戦略)が悪性疾患の治療において経験的アプローチを使用している。すなわち、細胞毒素薬の送出と投与のタイミングは、悪性の細胞集団への効果によってというよりも、正常な組織に対する反応と毒性によって導かれる。この経験的アプローチの主要な欠陥は、悪性細胞集団内で生じる治療(長期間にわたり延長可能)の間の動的変化に関する正確な情報を与えるための効率的な方法または技術が欠如しているということである。この貴重な情報を主治医にとって利用可能にすることによって、臨床家は悪性及び正常な細胞の間の明らかになった相違を利用して、そしてそれによって治療処置を改善して、もっと良い結果を達成することが可能になる。
【0005】
腫瘍生物学の研究の多くは、治療の指数を改善するために腫瘤と正常細胞の間の細胞的、生化学的、そして分子的な相違を探究することにあった。早期の細胞運動学的研究は、がん細胞は正常細胞よりも速く分裂しないが、しかしそれよりもむしろ細胞集団のより大きな部分が分裂していることを明らかにした(ヤング(Young)ら、1970年)。その当時、より多くの腫瘍を直す障害は成長特性の変化によるものであった。1980年代、これらの障害は不安定なゲノムの突然変異による腫瘍細胞の耐性の発達のためであったことが提案された(ゴディ(Goldie)ら、1984年)。後の研究は、腫瘍細胞生存のメカニズムは、細胞からの細胞毒素薬を追放あるいは押し出す特定のタンパク質をコードする遺伝子の表現に基づいていることを示唆した(チャドハリ(Chaudhary)ら、1992年)。より最近では、耐性は細胞成長率を変える細胞サイクルの異常(dysregulation)と関係があることが提案されている(ローウェ(Lowe)ら、1994年)。除去の障害に関係する追加因子または効果が改善された治療率には低酸素症細胞集団(hypoxic cell populations)、細胞増殖変化(cell proliferation variants)、細胞分染薬(cell differentiation agents)、及び細胞サイクル感知段階(cell cycle sensitive stages)が含まれる。どんな治療の間の、そしてそれに引き続くこれらの変化をモニタする能力は、どんな細胞集団の最も微妙な部分の正確な知識と、より個別化され、より経験的あるいは一般化されていない治療プログラムを送出(delivery)する際の助けを提供することができる。
【0006】
細胞集団の中で起こっているある特定の動的変化を研究する多くの試みがなされてきたが、しかしこれらの試みは一般にリアルタイムでの変化をモニタする能力を欠いていた。実際、これらの方法は一般に一時点における情報を提供し、ほとんどは一つの特定の機能またはパラメータに関する情報を提供するよう設計されている。さらに、従来の方法の大部分は、時間を消費すると共に高価な場合がある。放射線または薬または化学療法の延長治療期間を経験している患者にとって、特に、治療期間を通して積極活動治療(active treatment)の間と、その積極活動治療の後の両方の動的変化をフォローすることが望ましい場合には、これは問題となり得る。
【0007】
最も信頼できる最新の監視する技術は生検(biopsy)である。生検はいつでも採用でき、十分な情報量を提供することができる。しかしながら、毎日生体組織検査を行うことは出来るとしても実際的でなく、そしてサンプルの様々な検査を実行する際に生じる時間遅延は、医者によって受け取られる情報が患者の現時点の状態の正確な表現ではないことを意味している。生検資料のほかに、NMR及びPET走査の放射線技術はそれぞれ、特定の生物学的(細胞サイクル段階)及び生理学的(リン(phosphorus))情報を得ることができるが、しかし共に反復的または毎日の情報がほとんど利用できないほど十分に高価である。特定の免疫抗体(antibodies)あるいは配位子(ligands)への放射線ラベル付けは別の利用可能な技術であるが、しかしこの方法にはその他の試みと同様に多くの問題がある。
【0008】
さらに、長い間には、腫瘍は、それらが強靱さが低下して、従って放射線あるいは薬餌療法による治療に対してより影響されやすい期間を経過する。継続的あるいは半継続的に監視して、影響されやすい状態をもしかすると識別することができる監視システムを提供することによって、腫瘍破壊率の歓迎すべき増大が実現可能である。さらに、特に局部的に目標を定められた腫瘍治療については、望ましいドーズ(dose)が腫瘍部位において受入れられたかどうか確かめることは難しいことがあり、そしてもし受け入れられば、比較的執刀を要さない方法でその有効性を評価することは難しいことがあり得る。従って、目標薬の局所的あるいは局部的な存在を数量化及び/または評価することができる監視システムの必要性がある。
【0009】
最も攻撃されやすい腫瘍段階と、従って好ましい積極的治療時機を識別できるであろう、特定の腫瘍特有かつ/または内部的な全身情報の多くは(従って究極的な治療戦略あるいは治療の標準的手順は)まだ未解決であるけれども、種々な研究者は、腫瘍の脆弱性(vulnerability)あるいは感受性(susceptibility)に関係し、従ってある特定の治療法に影響を与えるかもしれない、酸素化(oxygenation)、pH、細胞増殖率といった潜在的に重要な生理学的かつ/または生物学的なパラメータを提案してきた。
【0010】
例えば、アダム(Adam)等によるInt J. Radiation Oncology Biol Phys., Vol. 45, 1998, pp.l71-180に掲載された「マウスで成長している腫瘍の酸素伸張測定(Oxygen tension measurements of tumors growing in mice)」と題された論文には、治療の間の腫瘍における低酸素症を評価することが助けになるかもしれないことが提案されている。さらに、腫瘍低酸素症は放射線療法の有効性に影響を与えるために提案された。放射線腫瘍学(Radiation Oncology),Vol.8, 1998, pp141-142のセミナーを参照されたい。同様に、「前立腺癌腫上に目標を定めた温熱療法の発展と、臨床治療における温熱療法の役割(Development of targeting hyperthermia on prostatic carcinoma and the role of hyperthermia in clinical treatment)」の著者は、治療の間に腫瘍場所の温度を評価する方法が必要であることを指摘している。ウエダ(Ueda)等によるJpn J. Hyperthermic Oncol., Vol.15(supplement), 1999, pp18-19を参照。さらに、ロビンソン(Robinson)等は、腫瘍酸素化レベルと血流を知ることが重要であると意見を述べている。放射線腫瘍学(Radiation Oncology)Vol.8, 1998, pp197-207のセミナーに掲載されたロビンソン(Robinson)等による「血流における腫瘍酸素化の変化を監視するためのMRI技術(MRI techniques for monitoring changes in tumor oxygenation in blood flow)」を参照。不幸にも、腫瘍酸素化は変化することがあり、そして腫瘍酸素化がフラックスの連続状態にあることを提案する証拠がある。放射線腫瘍学(Radiation Oncology),Vol.8, 1998, pp.143-150のセミナーに掲載されたドゥハースト(Dewhirst)による「微小循環レベルにおける酸素輸送の概念(Concepts of oxygen transport at the microcirculatory level)」を参照。このフラックスによって、動的監視方法は、腫瘍酸素化レベルがより積極的な治療法が望まれるようなものであるときを識別するために重要とされる。さらに、腫瘍pHは、腫瘍治療の薬設計にとって利用可能なパラメータとして提案されている。8 Seminars in Radiation Oncology No.5, pp176-182 (July 1998)におけるレオ・E・ガベック(Leo E. Gerweck)による「腫瘍pH:治療と新規な薬デザインにとっての意味(Tumor pH: Implications for Treatment and Novel Drug Design)」を参照。
【0011】
過去、種々な生体遠隔測定デバイスと移植可能センサが、心臓の状態またはブドウ糖もしくは温度に関連する生理学的パラメータをモニタするために提案されてきた。例えば、シュールマン(Schulman)等に付与された「患者監視システム(Patient Monitoring System)」と題された米国特許第5,791,344号は、一つの酵素センサがブドウ糖を監視するために患者に挿入されており被験者の血液中物質の濃度を監視して、そして次にそれに応じてインシュリンを送出するシステムを提案している。同様に、シュールマン(Schulman)等の「身体パラメータを監視またはそれに影響を与えるための移植可能デバイス・システム(System of Implantable Devices for Monitoring or Affecting Body Parameters)」と題されたPCT US98 05965は、ブドウ糖レベル、O2含有量、温度などを感知するためにマイクロセンサまたはマイクロスティミュレータを使用することを提案している。遠隔測定によって心臓に関連する生理学的データを監視する多数の移植可能な医療用デバイス及びシステムもある。このタイプのデバイスの一例が、スネル(Snell)による「移植可能な医療用デバイスからの生理学的データを監視するための方法及び装置(Method and Apparatus for Monitoring Physiological Data From an Implantable Medical Device)」と題された米国特許第5,720,771号に記述されている。詳しくはこれらの出願の内容を参照されたい。
【0012】
さらに、従来の移植センサと異なり、腫瘍の監視に使用される腫瘍監視システム及び/またはセンサは、何週間あるいは何ヶ月にも及ぶことがある治療の標準的手続または法の間に比較的厳しい環境(加えられた熱、化学物質、及び/または放射線など)にさらされることがある。さらに、このような長い治療期間と相まった厳しい環境は、デバイスの機能に影響を与え、従って潜在的にそれが生成する測定データを改悪させることがあり得る。
【0013】
以上の説明から、特に、治療サイクルの間に腫瘍の生理学的かつ/または生物学的状態を監視して、そうした治療に関連する生体内治療の効果を増大させることができる強化されたあるいは好ましい治療の時間帯(window)を識別することができる、腫瘍監視システム及びデバイスの必要性が残されている。
【0014】
<発明の目的と概要>
これらの目的及び他の目的は、被験者の腫瘍の状況を表す複数の選択されたパラメータを監視するよう配置された生体内センサを備えた生体遠隔測定ベースの腫瘍監視システムによって達成される。
【0015】
特に、本発明の第1の側面は、治療を経験している腫瘍の状態を監視及び評価する方法である。この方法は、その場で働く(in situ)センサで治療を経験している被験者内の腫瘍に関連する少なくとも一つの生理学的パラメータを生体内で監視する監視段階を含む。少なくとも一つの監視された生理学的パラメータに関連するデータが被験者の外側に置かれた受信器に送信される。送信されたデータは、どのように腫瘍が治療に感応しているかを決定するために解析される。追加的データが、一連の複数の時点において周期的に送信及び解析され、腫瘍治療法がその解析段階に基づいて評価される。
【0016】
前記送信及び解析段階は、前記少なくとも一つの監視された生理学的パラメータの変化を追跡して、それによって長時間にわたる腫瘍の振る舞いを評価するために十分に頻繁に(少なくとも治療の特定時間区分の間に、少なくとも24時間毎、好ましくは1時間に一回)繰り返されることが好ましい。少なくとも一つのパラメータは複数のパラメータであり、前記解析段階では、監視されたパラメータに関連する複数の所定の検査条件を定義して、腫瘍の状態に対応する治療(治療の効果、あるいは治療の好ましい指標の存在もしくは不存在)を評価数することも好ましい。もし前記送信されたデータが監視された生理学的パラメータに関係する少なくとも一つの検査条件を満足するなら、腫瘍に対する次の積極的治療を施すための好ましいあるいは好ましくない治療の時間帯(window)の少なくとも一つの存在として医者に警告されることが可能である。好ましくは、好ましい治療の時間帯(window)は治療の感受性段階または脆弱性段階の識別に対応する。
【0017】
前記送信段階は、患者のホームサイトから遠隔臨床サイトへデータを送信して前記生理学的パラメータをリアルタイムに遠隔的動的に監視ことが可能であることも好ましい。さらに、前記送信段階は、次の積極的治療送出時間の直前に一時的に繰り返され、計画された治療のタイミングの望ましさ、あるいは繰り出された治療の効果に関するリアルタイム情報が提供される。
【0018】
本発明のもう一つの側面は、放射線治療または薬物療法の効果を評価し、かつ/または強化した、あるいは好ましい積極的治療の時間帯(window)を識別するための腫瘍の監視システムである。このシステムは、治療を経験している患者においてがん性腫瘍と生体内で接触するように構成された複数のセンサ要素及び関連するセンサ・エレクトロニクスを含む、少なくとも一つのセンサユニットを備える。センサ要素は腫瘍に関連する異なる複数の生理学的パラメータを感知して、感知したデータを送信するように構成される。センサユニットは少なくとも約6−10週間、好ましくは約8−12週間の移植されたサービス寿命を持つ。このシステムは、前記少なくとも一つのセンサと無線通信して前記送信されたデータを受信するように構成され、遠隔受信器も備える。この受信器は被験者外部に配置される。
【0019】
このシステムは、送信されたデータを受信するように構成されており、被験者内の環境にさらされたことによる信号データの変化を補正するために前記受信された送信データを再検討及び調整するためのコンピュータ読み取り可能なプログラムコード手段を備えた、データ・プロセッサも備える。
【0020】
本発明の追加的な側面は、治療を経験している腫瘍の状態を監視及び解析するためのコンピュータ・プログラム製品である。このコンピュータ・プログラム製品は、その中にコンピュータ読取り可能なプログラムコード手段が具現化されるコンピュータ読取り可能な記憶媒体を備える。このコンピュータ読取り可能なプログラムコード手段は、腫瘍の少なくとも一つの生理学的または生物学的パラメータを監視するために治療を経験している腫瘍直前に被験者内に配置された少なくとも一つのセンサ要素を有する生体内センサからの、前記少なくとも一つのセンサ要素の出力に対応するデータを含む第1の無線データ送信を、開始するためのコンピュータ読取り可能なプログラムコード手段を含む。この製品は、前記第1の無線データ送信から時間的に分離した、前記生体内センサからの第2の無線データ送信を、開始するためのコンピュータ読取り可能なプログラムコード手段と、前記第1及び第2の無線データ送信の合間の変化を追跡して当該治療に応答した腫瘍の動的挙動モデルを提供するためのコンピュータ読取り可能なプログラムコード手段も含む。
【0021】
好ましくは、前記コンピュータ・プログラム製品は、長時間にわたって監視された少なくとも一つの生理学的パラメータの所定の絶対値あるいは相対的変化のいずれかに対応する治療の効果を評価するためのコンピュータ読取り可能なプログラムコード手段をさらに含む。前記コンピュータ・プログラム製品は、所定の期間にわたって進行中の周期的なデータ送信を開始するためのコンピュータ読取り可能なプログラムコード手段と、前記データ送信を解析して好ましい積極的治療の機会を見出すためのコンピュータ読取り可能なプログラムコード手段とをさらに含むことが好ましい。
【0022】
有利には、そして積極的治療(化学療法または放射線治療)を計画するために過去に使用された試験的治療法とは対照的に、本発明はいまや、腫瘍直前の正常細胞の反応並びに腫瘍それ自体の悪性細胞の反応または振る舞いをによって指示される目標腫瘍治療を可能にする。さらに、本発明は、非積極的期間を動的に追跡するのみならず積極的治療セッションの間のリアルタイム情報を可能にする。実際、患者は定期的に監視されたパラメータを、移植可能な遠隔測定ベースのセンシングデバイス及びホームベースの受信器を使って(例えば24時間毎に複数回)、比較的コスト効果のある方法で臨床サイトと送信または通信することができる。この進行中通信では、腫瘍の状況を臨床監視局までリアルタイム情報をダウンロードする。次いでこの情報はコンピュータプログラムによって解析され、特定の腫瘍タイプに関連する腫瘍学的治療法を確認または評価することが可能である。例えば、前記動的追跡では、腫瘍の相対的変化と/または治療に対する正または負の反応に関連する絶対値を確認することができる。この反応追跡は治療に対する腫瘍の反応に基づいてより先行型の療法判定を可能にする。動的追跡は、徴候を識別、または腫瘍の潜在的な脆弱性段階を予測して、腫瘍の実際の振る舞いに対応する治療投薬計画のより効果的なタイミングを可能にする。好ましくは、センサは、治療に対する腫瘍全体の反応を数量化することができるように、腫瘍の複数の場所(表面及び所定の深さ)、より好ましくは腫瘍に関連する複数の領域に配置される。
【0023】
有利には、本発明のシステム、方法、及びデバイスは、リアルタイムかつ/または動的に、それらを治療判定において即座利用することを可能にするための、腫瘍の生理学に関連する特定の指標を監視することができる。従って、本発明は、より明確な患者特定治療標準手続に導き、腫瘍反応を増大させ、治療疾病率を減少させ、かつ/または腫瘍反応、耐性、及び感度の予測を評価することができる。本発明は研究及び療法の新たな分野を切り開く可能性がある、商用臨床応用に以前は利用できなかった情報を提供することができる。本デバイスは特に腫瘍学的応用に適する。
【0024】
<詳細な説明>
以下、添付図面を参照しながら、本発明の好ましい実施の態様を詳細に説明する。本発明は、しかしながら、多くの異なった形式で実施でき、ここに述べられる実施の態様に限定されるものではない。むしろ、これらの実施の態様は、本開示が徹底的かつ完全となるように与えられ、当業者に本発明の範囲を明示するものである。類似の符号が全体を通して類似の要素に付与される。図面では、特定の層、領域、あるいは成分が説明の便宜のためにやや誇張して描かれている場合もある。
【0025】
一般的に、本発明のシステム、デバイス及び方法は、生命システムの生理学的及び動力学的変化を監視することを目指している。特に、本発明の目的は、十分な間隔で(好ましくは半継続的、より好ましくは実質的に継続的に)、どんな器官または腫瘍システムの酸素、pH、及び細胞増殖の変化を、こうしたシステムの摂動(放射線療法、化学療法、あるいは細胞毒素刺激、温熱療法など)の前、間、あるいは後、並びに、本来の「正常な」な生理学的状態にあるときも、監視することにある。従って、本発明の監視システム及び方法は、例えば肺、胃腸、神経科学と前臨床研究のような多くの応用において有用である。それにもかかわらず、本発明は、腫瘍システムに特有の重要性と適合性を有する。従って、好ましい実施態様の以下の説明では、主にガン応用に対する本発明の利用性が議論される。
【0026】
上記の発明の背景で述べられたように、最も従来的なガン治療法では経験的アプローチが使用される。すなわち、細胞毒素薬のタイミングと送出は、悪性細胞母集団に対する効果によってというよりも、正常組織に対する反応及び毒性によってより導かれる。従って、この経験的アプローチの主要な欠陥は、悪性細胞母集団内で生じる治療の間の動的変化についての正確な情報を提供するための有効な方法または技術を欠いていることである。主治医にとってこの貴重な情報が利用可能になることによって、主治医は悪性または正常な細胞の間の明らかになった相違を利用して、従って、より良い結果を実現するために治療手続を改善することが可能になるであろう。従来的に、腫瘍を取り巻く正常細胞は放射線の照射線量を支配し、化学療法のスケジューリング及び投薬量は患者の骨髄の許容性に最も依存する。治療の個別化の欠如の主要な理由は、腫瘍の動力学と生理学についての基本的な情報がそれによって治療の間及び後に得られる商業的に利用可能な手段が現在のところ存在しないということである。腫瘍の生検は、一時点における情報を与え、それ故にその時点にだけ有効である。細胞動力学、特に何らかの細胞毒素薬による摂動の直後の細胞動力学を予測することにとって、この静的な「スナップ写真」情報は有効ではないかもしれない。
【0027】
細胞母集団の中で生じている動的変化を研究する多くの試みが存在している。しかしながら、これらはリアルタイムでの変化を監視する能力に欠ける。その代わり、従来の方法は、ある一時点における情報を提供し、ほとんどの方法は一つの機能についての情報を提供するよう設計され、それに特に、治療の前、間、後にパラメータを監視することが重要だと考えられるときには、高価で時間消費的である。
【0028】
ガン治療の主要な目標はすべての腫瘍細胞を抹殺することである。腫瘍の中で実質的にどんなときにも生じている特定変化の知識は、最大の腫瘍細胞殺傷及び最小の正常組織へのダメージを実現するために望ましい場合がある。細胞毒素薬は特定の時と腫瘍成長の状態において最も効果的である。もし腫瘍細胞の最も攻撃されやすい時、つまり、細胞サイクルの段階に関連する最大酸素化あるいは細胞増殖の増加の確認の時が決定できるなら、この情報は細胞毒素薬の送出と選択の時を指図するために使用できる。
【0029】
前臨床医学及び臨床医学は、腫瘍反応を増大させるための環境をより明らかに定義するために、細胞毒素(積極的)療法セッションの前、間、及び後に悪性腫瘍内で生じる動的変化の情報を必要とする。このような情報を利用することによって、例えば放射線あるいは化学療法治療といった最も適切な作用薬を割り出すことと共に、細胞毒素薬送出のより正確なタイミングを考慮することができる。NMR及びPET走査は若干の機能的変化を識別することができるけども、従来の放射線学的調査は動的変化を観測する能力によって制限される。現在利用可能な抗がん剤は、限定数の腫瘍に効果的であるけれども、大部分のガンに対しては比較的効果的でない。本発明では、結果の改善のこの欠如の理由は一般に多重原因的であり、最も感受性のあるパラメータの時間分布をその場で測定することが不能であることに一部関係していることが認識される。これらの腫瘍パラメータは、限定はされないが、酸素化、pH、細胞サイクル段階、細胞増殖の度合い、及び細胞毒素薬に対する感受性(影響の受けやすさ(sensitivity))または耐性の分子的細胞的決定子の少なくとも一つを含む。本発明では、このような情報の有効性とこのような情報に作用する能力はガン治療における結果の改善に対する主な障壁を克服する手段を提供することが認識される。さらに、この新たに与えられた情報は、「経験的(empirical)」ベース治療から、個別の患者腫瘍の分子的細胞的特徴に(少なくとも部分的に)頼ることができる「個別的(individual)」ベース治療への治療のパラダイムシフトを生み出すことができること信じられている。
【0030】
有利には、本発明はいまや、治療を指図しかつ/またはその治療の効果を監視するために利用できる、治療の間または後で生じている変化についての情報を提供することができる。治療のこの個別化は結果を改善するだけではなく、治療の毒性と罹病率を減少させることができる。すなわち、それぞれの患者の腫瘍に関して得られた情報は根本的に治療のスケジューリングを変え、そして改善された結果をもたらすことができる。例えば、患者はいまや、家から電話回線または他の遠隔的インターフェースを介して、治療の好ましいあるいは最も適切な時を決定することができる。
【0031】
従って、上記のとおり本発明は、積極的治療の前、間、後、好ましくは全治療投薬計画または期間にわたっての腫瘍の生体内評価及び監視に向けられている。すなわち、本発明は特に、特定の非緩解治療期間(non-remission treatment period)にわたってサルコーマとカルチノーマのようなガン性腫瘍の振る舞いを監視することに適する。従って、本発明の内部的なその場で働くセンサは好ましくは、生物学的に適合するように、かつ、腫瘍に向けられた放射線、化学療法、温熱療法、あるいはイオン電界(サーモトロン(Thermotron)(登録商標))にさらされても、少なくとも約4−6週間、好ましくは約6−10週間、さらに好ましくは少なくとも約10−12週間、の断続的な治療評価に適するサービス寿命を実現するように構成される。センサと好ましい腫瘍監視パラメータは以下さらに詳細に論じられる。
【0032】
次に図1Aを参照すると、リアルタイム腫瘍監視システム10が示されている。示されているように、腫瘍監視システム10は、腫瘍25直前に被験者20内に配置されたその場で働くセンサユニット50を含む。好ましくは、同様に示されているように、センサユニット50は腫瘍25の上及び/または中の異なる場所に配置された複数のセンサ要素51を含む。センサ要素51は、以下詳細に説明されるように、腫瘍の中、上、あるいは付近の2つ以上の場所に関連する2つ以上の生理学的パラメータもしくは選択された生理学的パラメータを監視することが好ましい。センサユニット50は外部に位置する受信器75と無線通信する遠隔測定リンク60と共に構成される。受信器75はコンピュータインターフェース76を備え、中央演算処理ユニットに付随するディスプレイモニタ、コンピュータ、または医者が監視されたデータにアクセスすることを可能にする他のコンピュータ手段といった、医者インターフェースモジュール80に動作上付随する。示されているように、医者インターフェース80は、医者が実質的にリアルタイムの監視された腫瘍パラメータに即座にアクセスすることを可能にするラップトップまたはモバイル/携帯可能コンピュータ手段である。
【0033】
図2Aと図2Bは本発明によるリアルタイム評価の模範的な応用を示した図である。図2Aは、温熱療法治療セッション(例えばサーモトロン(登録商標)を使用)の間に腫瘍の監視されたパラメータを使用して治療の長さ、パワー、電界強度、または極性を制御する様子を示している。少なくとも一つのパラメータに関連するリアルタイムで監視されたパラメータは腫瘍それ自体における実際の治療浸入度に対して(温度あるいは他のパラメータを介して)フィードバックを提供することができるから、この制御は実現可能である。代わりに、腫瘍の状態あるいは振る舞いに関係する情報は、別の治療がより有益であること、あるいは更なる治療は(その時点で)有益でないことを提案するかもしれない。実際、どの積極的治療の開始の前にも、腫瘍データが、提案された治療法にとって、状態が好ましいあるいは本当は好ましくないかどうかを決めるために、監視されることが好ましい。すなわち、もし薬餌療法がある決められた値以上のpHを示す腫瘍に対して推奨されるならば、そしてデータが腫瘍のpHがこの値以下にあることを示唆するならば、医者はその特定の療法をより好ましい時に延期することを選択できる。もちろん、高まった酸素化レベルと増大した細胞増殖の段階といった他のパラメータは、他の治療がより有利であり、あるいは薬餌療法をそれにもかかわらず進めるべきであることを示唆するかもしれない。以下、腫瘍パラメータと治療との関係に関する追加の論議が提供される。
【0034】
図2Bは、温熱療法と放射線治療セッションのパワー、ドーズ、または期間の一つ以上を制御するために制御フィードバックループにおいて腫瘍データを使用する様子を示している。示されているように、監視された送信されたデータは、そのデータをアクチュエータ92と治療源(treatment source)91を指図する(治療を患者に向ける)制御装置を有するコンピュータに入力する受信器75に送られる。患者20はこの図では被制御「プラント(plant)」で示されている。
【0035】
図1Bは、別の実施態様における腫瘍監視システム10’を示している。この実施態様では、腫瘍監視システム10’は、ホーム受信器ユニット75’と、医者用インターフェース80(この実施態様で示された医者用インターフェースは中央演算処理ユニットである)と通信する遠隔インターフェース78を含む。患者20(点線は家の中の受信器75’の直前にいる患者を表している)は、家にいても監視を継続し、データを遠隔サイトへ送信することができる。遠隔インターフェース78は監視されたローカル・データと遠隔にある臨床監督局の間の通信リンクを提供することができる。従って、遠隔インターフェース78は、コンピュータモデム、無線通信システム、インターネット接続あるいは電話接続を含むどんな数のインターフェースまたはデータロード手段によっても提供できる。この実施態様では、治療の好ましい条件の存在または徴候が確認されると、中央演算処理サイトは、好都合または好ましい治療の時間帯(window)を利用するために、自動的に評価アポイントメントを予定し、あるいは治療装置に対して治療セッションを予定することができる。
【0036】
図3は、本発明による好ましい腫瘍監視及び治療評価方法を示している。治療を経験している患者における腫瘍に関連する少なくとも一つの(好ましくは複数の)生理学的パラメータが監視される(ブロック100)。前記少なくとも一つの生理学的パラメータはその場に配置されたセンサユニット50から被験者外部に位置する受信器50に送信される(ブロック110)。データ送信は非臨床サイト(患者の家)から臨床サイトへモデム、電話、無線通信などを介して遠隔的に送信される(ブロック115)。送信されたデータは次いで腫瘍の状態を決定するために解析される(ブロック120)。監視、送信、解析段階は複数の一連の時点において繰り返される(ブロック125)。すなわち、「静的な」単一時点のデータポイントとは反対に、本発明は(複数の一連の時点での)動的監視を可能にする。腫瘍の変化の動的追跡は貴重な治療的及び診断的情報をもたらすことができる。データは特定の治療期間にわたって周期的(4−24時間毎といったように)に送信される。データは、一般に1−3ヶ月に及ぶ全治療サイクルの間に、少なくとも断続的に送信される(データは多かれ少なかれ頻繁なデータ送信において送信されてよいが)。好ましくは、データは実質的に継続的または半継続的に(1−60分毎、好ましくは1−30分毎に)監視され、少なくとも局所的に送信される。この進行中の(断続的半継続的あるいは実質的に継続的な)監視によって生理学的パラメータの動的追跡または監視が可能になる。
【0037】
もちろん、継続的または半継続的な監視/送信は受信器/コンピュータインターフェース75’に付随するメモリ内に電子的に記憶させるために局所的に実行でき、その後続いて(一時間毎、一日毎といったようにそれほど頻繁的でなく中央監視サイトへ)送信できる。医者の入力(例えば、10−15分毎または一時間毎といった頻繁的でない監視と共に、細胞毒性薬または摂動(perturbation)の導入から時間的により接近した1−5分毎のより頻繁な監視)に対応する受信器75’と通信するタイマを介してデータ送信/取得時間を予めセットすることは有益かも知れない。代わりに、データ監視/送信または取得時間は、送信されたデータを周期的に比較・再検討して、それについてより頻繁な評価を開始するための変化の割合を決定して、値の変化がより小さい時間の間により低度に頻繁に送信するといったことによって自己調整的となり、かつ相対的に設定できる。とにかく、静的な受信器ユニット75,75’については、患者は適切なデータ伝送を容易にするために受信器75’の直前の場所にいる必要がある。受信器75’への次の伝送のために患者が適切なポジションを取ることを容易にするため、受信器75’は好ましくは、望ましい監視伝送時間が近づいているときに警告または警報を発するよう構成される。これによって被験者に適切な伝送のために受信器に接近するよう思い出させることができる。もちろん、受信器75’は、より現在の伝送がまだ進行中であっても、より最近に送信されたデータの値に基づいて(あるいは一連のより最近の伝送の変化に基づいて)次の送信時間を聞こえるように知らせるようプログラムできる。
【0038】
図1Bに示されたホーム・ベースの腫瘍監視システム10’の代わりの実施態様では、受信器75’は、継続的または半継続的な動的データ追跡をより容易に実現するために望ましく埋め込まれたセンサユニット50の直前に配置されるよう、携帯可能かつ、ユーザがそれを着用できるよう(衣服、または他の支持ベルトもしくはサスペンダなどに取り付けらるよう)に十分に軽量に構成できる。好ましくは、携帯可能な受信器ユニット(図示されていない)は細流充電器(自動車の付属電源または家のコンセントに差し込むことができる)によって自己電力供給され、ユーザが移動していないときにそのユニットを再充電することが可能である。携帯可能ユニットは、遠隔インターフェースに、または臨床サイトにあるコンピュータインターフェースに直接的にアップロードする前に、ある一期間にわたって1ブロックのデータを記憶するのに十分なメモリを備えて構成されることも好ましい。
【0039】
いずれにせよ、再び図3を参照すると、腫瘍治療法は監視されたパラメータによって提供される動的情報に基づいて評価できる(ブロック130)。この評価は、例えば、腫瘍が治療に反応しているあるいは抵抗しているかどうかを決定するために、治療の効果の証明を結果としてもたらすことができる(ブロック132)。さらに、この評価によって、所定の積極的ドーズが腫瘍で受け取られたこと、そしてどの程度の量が受け取られたかを確かめることができる。一つの例は、腫瘍が受けた放射線量を数量化することである(これは、もし腫瘍が密な組織によってブロックされ、あるいは体内に不規則に構成もしくは配置され領域に到達することが困難な場合に役立つことがある)。この確認は、体内の特定の治療ゾーンを目標とするよう設計されたより新しい目標薬を使用するユーザにとって特に適することもある。この証明によって従って薬が意図された領域に送出されることを確認することができる。
【0040】
さらに、その評価は、好ましいあるいは好ましくない治療時機の存在のいずれかもしくは両方を識別するために有利に使用できる(ブロック134)。例えば、もし状態が、腫瘍が計画された治療に対する感受性が強くないことを示しているなら、計画された治療の変更が即座に開始でき、あるいはその反面、耐性が計画された治療のより好ましい時間への再スケジューリングを結果としてもたらすことができ、それによって好ましくない時間において不必要な治療セッションに被験者をさらすことが最小化される。さらに、治療の評価は、治療が予測モデルに従って進行しているかどうかを決定するために、相対的または絶対的なパラメータ値(あるいは実際は、一塊りの不規則な正、または負のパラメータ値)のいずれかあるいは両方に基づくことができる。予測モデルは、特定の時点における送出された治療に対する測定された腫瘍の反応の、集団標準に対する、あるいは以前に送出された治療の患者自身の反応の履歴に対する、ずれに基づくことができる。これによって、医者は腫瘍それ自身の反応性に基づいて被験者のために治療を選択(または修正)することが可能となる。従って、前記情報は計画された治療形態の修正をもたらす(ブロック136)ことができる。例えば、論議目的のために、化学療法タイプとドーズから3日目に、腫瘍酸素化が低い、そして毒物に対する正常細胞の感受性が高いと仮定する。それとは対照的に、3日目に、腫瘍酸素化が高い、そして毒物への正常細胞の感受性が低いと仮定する。後者では、この振る舞いは予測された結果あるいは不測の結果による。つまりもし不測ならば、人は治療にとって好ましい状態を利用するよう即座に追加の治療セッション(つまり好ましい積極的治療時機)を計画するよう進めて良いだろう。もし予測されたなら、計画された治療をスケジュールされたように進めることができる。
【0041】
(腫瘍の生理学的パラメータを決定すること)
腫瘍酸素化と血流はたいていのタイプのガン治療の効力に重要であることは一般に十分に受け入れられている。低酸素症(hypoxia)(低酸素)と従って放射線耐性は腫瘍の潅流性が悪い領域(poorly perfused regions)で起こる(グレイ(Gray)等、1953年)。さらに、すべての種類の抗ガン剤は血管を通して腫瘍細胞にアクセスするが、潅流性が悪い領域も薬の到達を妨げる(ジェイン(Jain)等、1988年)。これらの理由のために、主に放射線感受性を増大させる方法を見つけるために、腫瘍血流及び酸素化を修正及び監視するための方法を開発することに大きな関心があった。しかしながら、腫瘍酸素レベルの知識は代わりのアプローチ、例えば低酸素症において強化される温熱療法効果、に導くことができる(ストラットフォード(Stratford)等、1994年)。遺伝子と細胞質分裂における低酸素症の影響についてのより最近の情報はこの領域の興味を刺激し続けている(サザランド(Sutherland)等、1994年)。さらに、転移(ヤング(Young)等、1997年)、脈管形成(シュベキ(Schweiki)等、l992年)と薬物耐性(サカタ(Sakata)、1991年)のパタンに影響を与えることにこれらの効果がある可能性がある。
【0042】
現在、腫瘍低酸素症を評価する商業的に実行可能な臨床的に応用可能な非観血的方法はない(マッコイ(McCoy)、1996年)。磁気共鳴イメージングと陽電子放出(ロビンソン(Robinson)、1998年)は腫瘍の潅流と血液酸素化の変化を監視する可能な手段と考えられてきた。しかしながら、これらの方法は、腫瘍の摂動の間に起こる毎日のダイナミックな変化を監視するには扱いにくい。種々な挑戦の間に腫瘍内の腫瘍酸素化と変化を監視する能力はガン治療を改善するために重要である。得られる情報は、細胞毒素効果を増大させるために、適切な治療のタイプとそのタイミングを指示することができる。
【0043】
電極評価された(electrode-evaluated)人間腫瘍のpHは平均的に正常組織のそれ未満であることを示す内容のある一連の証拠が過去50年にわたって蓄積されてきた。しかしながら、この差を調べるための法は2つの理由によって妨げられてきた。一つは、特にデータが集積されたときの、電極測定された腫瘍と正常組織のpHのオーバラップである。第2に、31P磁気共鳴分光学(MRS(magnetic resonance spectroscopy))を使用するより最近のデモンストレーションは、組織のpHは細胞内及び細胞外の2つの区画に分割可能であることを示している。つまり、(a)電極によって決定されるpHは主に間質性または細胞外のpHを測定し、(b)MRSによって測定されるpHは主に細胞内のpH(「pHi」)を反映する。さらに、正常組織及び腫瘍組織のpHiは類似するが、その一方、細胞外pHは、正常な組織及び腫瘍と異なる患者の同じ起源の腫瘍との間を著しく変動する。例えば、乳房腫瘍のpHの範囲は6.85−7.5にあることが明らかにされ、正常な志願者の皮下組織では7.3−7.9にあった。
【0044】
腫瘍の電極測定されたpHは平均で0.4単位だけ正常な皮下組織または筋肉組織よりも低い。正常組織と腫瘍組織の間の重複が存在するかもしれないけれども、それらは技術的な要因及び患者に関係する要因によって説明がつくかもしれない。しかしながら、本発明では、正常組織と腫瘍組織のpHの両方を同時に、そして継続的に測定することによってこの変化を消し去ることができることが認識されている。これを達成する能力によって医者が差異を利用すること可能にすることができる。酸度は供給容器からの距離が増大するにつれて増加し、pHiは各組織において類似するので、細胞内外のpHの勾配は血管の最も末端にあるそれらの細胞において増大することが期待できる。全体的な効果は、通常は最低の薬濃度にさらされて特に放射線療法と関係がある細胞の薬の取り入れと死滅を向上させることである。この放射線療法では、低酸素濃度とそれ故に放射線耐性は距離の増加と共に増大する。
【0045】
したがって、本発明の一実施態様において、センサユニット50は腫瘍内に挿入でき、すでに論じられたように好ましくは数週間の間、情報を収集するために、腫瘍内または腫瘍に固定され得る。図19Bに示されるように、センサ要素51は、それらが異なるレベルと腫瘍の異なる場所に配置されるように構成される。同様に、図19Bに示されているように、少なくとも一つのセンサ要素が正常細胞に対する治療の有毒性及び/または腫瘍直前の正常細胞組織のpHレベルを監視するように構成されることが好ましい。
【0046】
酸素レベルの違い(約32mmHg)が腫瘍にフィードする細動脈の間に存在することが示されている。これは回復組織または正常組織における約50mmHgレベルと対立する。そして上記のとおり、低酸素レベルは腫瘍細胞の治療耐性に導く。デバイスの助けを借りて、大多数の腫瘍が低酸素症(すなわち、50mmHg未満、好ましくは40mmHg未満、より好ましくは32mmHg未満)であることが決定されれば、腫瘍の酸素化が改善されるまで治療されるべきではない。これはいくつかの方法で生じ得る。腫瘍は加熱可能で(温熱療法)、これは低酸素状態で最も良く作用し、残りの母集団をより低度に低酸素症にするために十分な細胞を抹殺することができ、あるいは腫瘍は酸素濃度を改善するために特定の薬にさらすことができる。重要な点は、より多くの細胞が酸素化されるまで、それ故に放射線療法または化学療法といった従来の積極的治療に対してより影響を受けやすく、あるいは脆弱になるまで、腫瘍は治療されないということである。同様に、悪性細胞の感受性とそれ故に細胞抹殺はpHと細胞増殖によって影響されることが可能で、腫瘍組織のpH測定は、pHが薬の取り入れや送出に影響するだけではなく、腫瘍の酸素化にも影響することができるので重要である。そのために、特定の腫瘤のpHが7.2で、選択した薬の取り入れが6.9よりも大きなpHによって望ましくない影響を受けることが決定されれば、その薬は差し控えられ、pHは変更されるべきである。細胞増殖は、何らかの放射性タグを付けられた物質の取り入れあるいは配位子を監視して、そして細胞動力学と増殖に関する情報を提供することが可能なベータ線センサの助けによって測定することができる。もし細胞繁殖に関して測定する特定の配位子の取り入れが高い(積極的細胞増殖とそれ故に増大した感受性を示している)ならば、薬または放射線が送出されるべきである。
【0047】
当業者であれば、この時点で、特定の動的変化及び/または治療の間及び後の細胞増殖のpHまたは酸素化に生じているそれらの変化の値は明確に数量化(しかし今や本発明によって提供される動的監視によって確立できる)されていないことを理解するであろう。さらに、pH、細胞増殖率とスケジュール、そして酸素化は、同じタイプの腫瘍を持つ患者グループ内でさえ、患者毎に著しく変化する。実際、同じ薬で処置されるとき、この可変性は患者毎の反応の違いを説明することできることが信じられている。では、なぜ10、20、あるいは30%たらずの患者だけが、試験管内データに従って50%を越える腫瘍反応を生み出すはずの薬に効き目があるのか?有利なことに、本発明はいまや、細胞毒素治療の間及び後の(好ましくはpH、酸素分圧、及び細胞増殖を含む)各監視されたパラメータまたは変数に関するデータが収集されることを可能にする。収集されたデータは研究可能で、特定の変数のセットが特定の反応に影響を与えるものとして識別される。この情報のおかげで、患者はより効果的に治療がなされ得る。従って、本発明はいまや、評価のための特定の変数情報の確立を可能にするだけではなく、治療の効果を指示及び監視するためにも使用できる。
【0048】
従って、本発明の好ましい実施態様では、腫瘍監視システムは腫瘍pH、酸素化レベル、温度、及び細胞増殖の一つ以上を監視するように設計されたセンサ要素を備えるよう構成される。細胞増殖は現在では放射線センサ(放射線療法の間に腫瘍において受け取られた放射線のドーズを確かめるためにも使用できる)を使用して測定できる。他の生化学的あるいは生体分子は治療に対する腫瘍の脆弱性の感度インジィケータと成ること、従って、本発明によれば有用であることが決められることが期待される。本発明は、リアルタイムで情報を収集して、その情報を処理して患者が治療されるべきかどうか、いかに治療されるべきかを決めるためのアルゴリズムを含むコンピュータに送信する全てのこれらのセンサを腫瘍内に提供することができる。
【0049】
次に図4を参照すると、監視されたパラメータに関連するデータを評価及び分析する模範的なデータ解析方法が示されている。示されているように、選択された生理学的パラメータ(少なくとも3つのパラメータA、BとCで示された)の望ましい値は、それらが積極的療法の直前に望ましい状態に関係するときに、割り出され、または定められる(ブロック200)。各パラメータの望ましい値は最小または最大として入力されてよく、特定の治療タイプに相互に関係する。すなわち、論議のために、パラメータ「C」(pHのような)として識別された1つのパラメータは、(特定の化学療法あるいは薬物療法のような)ある特定の治療タイプに特有の最大効力を実現するために最大値または最小値を必要または切望するかもしれない。それとは対照的に、議論のために、(酸素化レベルのような)パラメータ「A」として識別された別のパラメータは、すべての治療形態にわたって同じ好ましい値を有してよい(一般に標準的値としての最小値あるいは高まった酸素化レベルが望ましい)。従って、もしそこでは治療が進むべきではない最小値または最大値が存在すれば、それは、治療を被験者に送出する直前のデータ解析のための検査基準として識別される。
【0050】
同様に、生理学的パラメータに特有なその生理学的パラメータの値の範囲は検査基準の基礎として使用できる。例えば、「高まった(elevated)」「減少した(decreased)」「ノーマルな(normal)」に関連するレベルの定義が入力できる(ブロック210)。この基準は(相対的レベル、集団平均、または腫瘍の振る舞いの指標及び治療効果と共に)、腫瘍治療の評価に対応する検査条件(test conditions)を定めるために使用できる(ブロック220)。すなわち、検査条件は腫瘍と治療の評価を表すどんな数の検査でも可能である。示されているように、検査条件は監視されたパラメータの異常な値も検査する(ブロック231)。これによって、医療評価に即座に必要なものを確認すると共に、監視システムのセンサ、センサ要素あるいは他の部品の故障が確認できる。他の検査条件は高まったまたは減少したパラメータ値をそれぞれ検査することを含む(ブロック232、233)。同様に、増加または高まったパラメータ値を有するパラメータと減少したパラメータ値を持つ別のパラメータの中の2つによって表された一塊りの「好ましい条件」の存在はより好ましい治療時機の存在を表しているかもしれない。例えば、増大した細胞繁殖の期間と減少したpHレベルと共に高まった酸素化レベルは好ましい治療の時間帯(window)を引き起こすこともある。もちろん、ちょうど2つの増大したパラメータの一塊りも検査条件に成り得る。さらに、1つの検査条件が、治療の間及び後の一時点に基づいて予測モデルに基づく期待値からのずれ(相対的反応または集団平均からの統計学的に関連のあるずれ)を決定するためにパラメータ値を再検討することができる(ブロック234)。パラメータが、定められた望ましい値を満たすかどうかを確認する検査条件も役に立つ(ブロック236)。期待されたデータの監視(局所的及び/または遠隔的)が受け取られ、または見落とされてるかどうかを決定するための検査を行うことも有益かも知れない(ブロック237)。これは、データ変造(data corruption)、ファイル変造(file corruption)を示し、あるいは自動的に被験者を(例えばプログラムされた、または記憶された電話メッセージを使って)呼び出すために使用できる。
【0051】
いずれにしても、生理学的データは周期的に監視され(ブロック240)、データは検査条件/定められた値と比較される(ブロック250)。好ましくない積極的治療時機及び好ましい積極的治療時機が次いでそれぞれ確認できる(ブロック260,261)。もちろん、他の評価と治療判定も行うことができる。好ましい検査時は、正の指標(好ましい状態または良い経過)を示す検査条件/パラメータ値によって識別可能である。もちろん、データは正常な指標(中立の条件)、及び負の指標(好ましくない状態または治療に対する耐性)を反映することが出来る。適切な値を識別するグローバルネットワークのデータベースまたは各病院または臨床サイトに付随する地域的データベースは特定の患者に必要とされる入力データを最小化するために予め確定できると想定される。
【0052】
ブロック図の各ブロック(または手順流れ図のブロック)、及び手順流れ図のブロックまたはブロック図のブロックの組合せはコンピュータ・プログラム命令によって実行できることは理解されるであろう。これらのコンピュータ・プログラム命令はマシーンを作り出すためにコンピュータまたは他のプログラマブルデータ処理装置にロードすることができ、その結果、コンピュータまたは他のプログラマブルデータ処理装置上で実行する命令は手順流れ図またはブロックで特定される機能を実現するための手段を生成する。これらのコンピュータ・プログラム命令は、特定の方法で機能するようコンピュータまたは他のプログラマブルデータ処理手段に指示することができ、コンピュータ読み取り可能メモリに記憶でき、コンピュータ読み取り可能メモリに記憶された命令は、手順流れ図またはブロック図で特定される機能を実現する命令手段を含む製造品を作り出すことができる。コンピュータ・プログラム命令は、一連の作業ステップがコンピュータまたは他のプログラマブルデータ処理装置で実行され、コンピュータ実行されるプロセスを生み出すために、コンピュータまたは他のプログラマブルデータ処理装置にロードすることもでき、その結果コンピュータまたは他のプログラマブルデータ処理装置で実行される命令は手順流れ図またはブロック図で特定される機能を実現するステップを提供する。
【0053】
したがって、ブロック図または手順流れ図のブロックは、特定の機能を実行するための手段及び特定の機能を実行するためのプログラム命令手段の組合せをサポートする。ブロック図または手順流れ図の各ブロックと、ブロック図または手順流れ図のブロックの組合せは、特定機能またはステップ、または特定目的のハードウェア及びコンピュータ命令の組合せを実行する特定目的のハードウェアベースのコンピュータシステムによって実現できることも理解されるであろう。
【0054】
本発明は、監視された腫瘍生理学的パラメータのより明確な数の値を確定するための付加的基礎を提供することができるけれども、以下のパラメータ及びレベル及び指標(インジケータ)は、治療または腫瘍状態に関連する検査基準に適するものとして提供される。従来の治療は、温度及び放射線といった組合せ療法を使用する(腫瘍に毎日放射線を照射しながら、一週間に2回加熱する)。
【0055】
(温度)
大きな切除不可能な腫瘍に対するアプローチは放射線及び温熱療法の使用である。一般に、このような場合、腫瘍は毎日放射線照射され、そしてその毎日の放射線治療に続いて1週間当たり2回加熱される。細胞死(cell kill)を増大かつ望ましく最大化するのに好ましい温度範囲は約42−43.5℃である。その際この温度は好ましくは約20分間維持される。温度は周囲の正常組織に対する効果を最小にして、そして同じ温度が腫瘍全体にわたって十分に均等になることを確実にするために注意深く監視される。この治療技術が利用され、そして、以下に限定はされないが、肺、前立腺、胸、黒色腫、膵臓と骨盤を含む、多数の腫瘍サイトからの主な腫瘍に対して効果的であることが見出される。従って、本発明は、温度を監視することができる簡単で効果的な温度監視手段を提供することができ、温度監視は特に、従来の手段では容易に監視されなかった外部からアクセスできない腫瘍あるいは体内深くに位置する腫瘍にとって適切であることを証明できる。
【0056】
(酸素化レベル)
酸素化レベルは放射線療法及び/または化学療法に打ち勝つ必要があり、上記のように耐性は動的システム上で明確に確立されていない。治療の間に生じる正確な変化が数量化されてなく、それ故にどんな最終値が究極的に放射線耐性を克服するために必要なものとして確立されるかを予測することが難しいから、今や動的監視標準的手続(dynamic monitoring protocols)は有効である。この情報は、提案された発明の臨床応用の際に、治療及び反応との特定の相互関係と一緒に得られるだろう。究極的には、より低い酸素分圧(oxygen tension)は治療にとって効果的であること、そしてノーマルなまたは高まった酸素化は成功した治療には必要とされないことが見出されるかも知れない。それにもかかわらず、現在の好ましい治療アプローチは少なくともできるだけノーマルなレベルを達成すること(酸素化が減少した期間の間に送出することではなく)である。したがって、参考のために、用語「高まった(elevated)」は52mmHg以上のレベルとして記述できる。用語「ノーマル(normal)」は約50−52mmHgからのレベルを記述できる。用語「減少した(decreased)」は49mmHg以下のレベル、好ましくは40mmHg以下のレベルとして記述できる。酸素は、もしすべての腫瘍タイプでないとしても、大部分にとって重要であって、(特定のレベルが一つのタイプの腫瘍により適することがあっても)一つのタイプの腫瘍に特有ではない。さらに、本発明によるその場で働くセンサは酸素の分布を監視するために腫瘍の異なった位置に配置可能である。もし著しい違い(あるいはデルタ)が検出されれば、酸素レベルを腫瘍にわたって十分なレベルまで増大させる試みをなすことができる。
【0057】
したがって、放射線療法または化学療法治療は、酸素化レベルが約50mmHgの最小値に近づく、あるいは当該患者に(相対的反応及び/または絶対的反応データに基づいて)適切となるように決定された範囲内にあるときにだけ、差し控えておくことができる。
【0058】
(細胞増殖(Cell Proliferation))
上記のとおり、細胞増殖は結果をもたらすことができる悪性腫瘍の重要な性質である。腫瘍細胞が増殖する間の時間の知識は、より大きな細胞死を達成し、治療に対するより大きな反応と改善された結果をもたらすために重要である。細胞繁殖の度合いは循環する細胞数と関係がある。従って、もし細胞繁殖に関連する配位子(ligand)がタグ付けされたなら、それは循環している細胞に取り入れられて、増大した放射能として腫瘍内でそれ自体を示すであろう。正常または鎮静状態の下で、約2−5%の細胞だけが一般には循環している。この量は、中または高程度の増殖状態において約20−25%の大きさだけ一般的には増加する。放射性物質の取り入れにおける違いは顕著で、増大した細胞繁殖の期間に関連づけられることが可能である。この増大した増殖が容易に知られない間の時間は容易に識別可能ではなかった。細胞繁殖が起こる間の時間は、増殖それ自体の割合(集団が2倍になるのに要する時間)のみならず特定の腫瘍タイプと共に変化することがある。
【0059】
(腫瘍pH)
腫瘍のpHは正常組織に関連するpHよりも低い(より酸性である)ことが見出されている。最大効果に必要とされる正確なpHまたはpHの範囲は知られておらず、また上記のとおり治療の間に遭遇する変動も数量化されていなかった。pHは酸素レベル、薬の取り入れ、及び細胞増殖に変化をもたらすことがあるので、pHに関する情報の影響は酸素よりも複雑な場合がある。さらに、周囲の正常組織も腫瘍pHをもたらすことがあり得る。現在のところ、より酸性の環境(約6.8−7.0にあるpH)が悪性を治療するのに好ましそうである。このことは、アドリアマイシン(adriamycin)といった少なくとも一つ薬が低いpHにおいてより効果的であることを示す試験管内データ(in vitro data)に基づいている。同様に上記のように、正常細胞と悪性細胞の間のpHの違いは狭い(約0.4単位)場合があり、それ故に薬と放射線がより効果的である狭い治療範囲が存在することを示しているかもしれない。上記のとおり、本発明は今や、リアルタイムに、細胞毒素療法の間及び後に生じる変化を決定することができる。
【0060】
(放射線)
放射線(一般にベータ線)監視は細胞増殖を識別するため使用することができる。放射線センサも光子照射治療の間に送出される放射線量(一般的には約3000−6000cGの間)を確かめるために使用することができる。従って、リアルタイム送出の間の放射線監視を使用することは腫瘍サイトへのガンマ放射線のより正確な送出ドーズ(特に高いドーズのコフォーマル治療による、光子放射の後の腫瘍内でのドーズ分布、または計算されたドーズの確認)を制御することを助けることができる。β放射線モニタも放射能的にレベル付けされた化合物を監視して、薬の取り入れと利用、腫瘍の血流、特定の薬に対する感受性、様々な器官における薬の分布を(上で議論された細胞増殖と共に)監視することができる。
【0061】
まとめると、多数の腫瘍(と直前の正常細胞)のパラメータが監視でき、それらのパラメータはそれぞれ被験者内の腫瘍の治療及び状態とって重要な情報を提供することができる。その個別のパラメータの組合せや、識別されるべき生体分子パラメータも本発明によれば監視されてよい。
【0062】
(生体遠隔測定と移植可能センサ)
外来の物体が体内に移植されると、一連の宿主反応(host responses)、すなわち、1)血漿タンパク質の析出、2)フィブリン形成、3)免疫細胞とタンパク質による侵攻、4)炎症細胞による攻撃、及び5)物体の周りでの細胞カプセルの形成(レイヒャート(Reichert)等、1992年)、が生じることは当業者によって認められるであろう。それ故に、移植されるデバイスに使用される材料がこの宿主反応を何とかすることは重要である。多くのことがセンサシステムの移植について知られている。カプトン(KaptonR)(登録商標)重合体は、それがセンサ基板として使用されるときには、比較的良性であることが示されている(リンドラ(Lindner)等、1993年)。ペースメーカ会社は、外部の鉛結線を密閉包装するための医療用エポキシ(medical grade epoxies)とシリコーンゴム(silicone rubber)を有するチタニウム製ケースをしばしば使用する(ウェブスタ(Webster)、1995年)。移植可能なブドウ糖センサは、様々な生体保護膜で被覆されたセンサ表面を有すし、ダクロンベロアでカバーされたポリエチレン製ケースを使用して構成されてきた(ギリガン(Gilligan)等、1994年)。(これらのユニットは、移植され、最大3ヶ月間生体内で検査される前に、24時間だけ0.05%のチメロサール(thimerosal)で湿式消毒された。)移植デバイスを殺菌するより一般的な方法は、20分間115℃から120℃の温度のガス殺菌である。
【0063】
早期の研究者は移植可能センサの単純な発振器回路を実現するために個別の部品を使用した(マッケイ(Mackay)、1995年)。近年、焦点は小型化にあり、システムの電子部分にハイブリッドの集積回路を使用している。過去において「ハイテク」の生体遠隔測定システムに対する需要が小さかったので、最新式システム及びデバイスの開発に資金を投資する業者はほとんどいなかった。この開発の大部分は、機能性が増大したより小さなより効率的な遠隔測定用及び遠隔測定ライクなデバイスに重点が置かれ、世界中の学術的研究機関で行われてきた。
【0064】
集積回路(IC)技術は過去20年にわたって生体遠隔測定デバイスエレクトロニクスのために大いに使用されてきた。1970年代中ごろ、IC使用はハイブリッド技術を使用することによって実行可能になった。この技術によって、技術者は、商業的に入手可能なIC、単純な注文製IC、及び他の個別の部品をセラミック基板上で相互接続して生体遠隔測定デバイスを厚膜または薄膜技術を使用して構築することが可能になった(フライヤ(Fryer)等、1973年、ドウツユ(Deutsch)、1979年、ゲシュベント(Gschwend)等、1979年、ドナルド(Donald)等、1981年)。多分この技術の最良の例は、NASAエームズ研究所で完成したユニットである(ヒンズ(Hines)等、1995年)。NASAは455kHzのキャリアと、デジタル式PCMを使用する。移植されるユニットはハイブリッド技術を使用して制作され、pH、心拍、温度、及びバッテリ電圧を監視する。その現在の消費は0,75A−hrリチウム電池から引き出される120マイクロアンペア未満である。バッテリ寿命は6−9カ月である。このユニットは注文生産された、20ccの容積を占める直径が約3.0cmの円盤状のセラミックパッケージに包装される。遠隔測定リンクは12から24インチの取得範囲(acquisition range)を有する。
【0065】
マイクロ製造(microfabrication)プロセスが改善されたので、遠隔測定ユニットはミリメータの長さ及び幅のみを有する個別のシリコン基板上で製造可能となった。最近、生体遠隔測定システムが主要な部品として注文製集積回路を備えて登場してきた(オーシマ(Oshima)等、1987年;ウィリアム(Williams)等、1994年;ウーターズ(Wouters)等、l994年;アキンス(Akin)、1995年)。典型的な例(プアズ(Puers)等、1993年)では、インテリジェントな4チャンネル・ユニットが設計され、家畜学研究のために製造された。このデバイスに使用されるエレクトロニクスは4.7×7.1mm2のシリコン基板上に生成され、入ってくる信号を処理して、それらを適宜に送信し、必要なときには電力を適切な部分回路に差し向けるためのアナログ及びデジタル両方の調整エレクトロニクスを含む。ほとんどのICベースの送信器と同じように、IC発振器を駆動するためのコンデンサと水晶、加速度計と温度センサ、そしてゲイン及び識別子コードを設定するための抵抗器とスイッチなどを含む、少数の外部デバイスが稼働に必要とされる。こうした追加的部品はエレクトロニクスの物理的サイズを増大させ製造に含まれる間接費を増加させるので、そうした追加的部品は望ましくないことがある。そらは、しかしながら、ユーザ/設計者に回路動作における一層の柔軟さを提供する。
【0066】
新規の移植可能遠隔測定システムは、最近、ノースカロライナ州立大学で開発中であった(フェルナンド(Fernald)等、1991年と1992年)。そのシステムは迅速な試作品作りへの応用のために意図されたものであって、非技術研究者が最小努力でカスタマイズされた移植デバイスを組み立てることができるように設計された。システムは2つのコアとなるインテリジェントな集積回路、すなわち、お互いの上に積み重ねられ10本未満のバスワイアで相互接続された、マイクロプロセッサ/遠隔測定チップとデータ取得チップ、から構成された。データ取得チップには8つの入力チャネルが提供されたけれども、追加のチャネルはこのようなチップを追加的に積み重ねて、それらをデージーチェーンでバスラインに取り付けることによって入手できる。マイクロプロセッサは(移植の前後両方で)完全にプログラマブルで、生物学的信号を処理するのに適した命令セットを所有する。このシステムは、バンド幅を変えることで、いろいろなトランスデューサのために意図された。直列バスアーキテクチャの結果として、システムのスループットはたいていのアプリケーションに適した20kHzの総合バンド幅に制限された。
【0067】
研究者は長きにわたって移植デバイスからバッテリを取り除くための方法を探し求めてきた(ハンセン(Hansen)等、1982年)。誘導型パワーカプリングが近年注目を集めている。一つの研究グループ(ベネデッチ(Benedetti)、1995年)は、圧力とEMGを測定するための4つのチャネルを有する誘導的に電力供給されるインプラントを開発した。サンプリング速度は200Hz/チャネルであった。そのサイズは、15×19×86mm3、重さは55g(40gは筐体)。そのインプラントは金めっきの黄銅筐体に組み込まれた。表面取り付け部品が、積重可能なプリント回路基板に取り付けられた。内部電源は、27.1MHzの電力搬送周波数から得られる+3Vと−3Vであった。電流消費は6mAであった。伝送/カプリング範囲は30−70mmであった。遠隔測定リンクは36kHz−120kMzの周波数範囲を有するサンプルFM(sampled FM)であった。
【0068】
誘導的電力供給を含む第2例のシステムが整形外科的測定のために設計された(グライチェン(Graichen)等、1991年と1995年)。このユニットは8つの遠隔測定チャネル(歪みセンシングに6チャネル、温度に1チャネル、電力供給電圧に1チャネル)を実現した。エレクトロニクスモジュールは、注文製ICと別々のコンポーネントを備えた厚膜ハイブリッド基板であった。基板は、直径が8mm、高さが27mmのチタン円筒で密封包装された。遠隔測定リンク、150MHzの搬送周波数によるパルス−インターバル変調を使って動作する。動作範囲は20cmである。インプラントは4kHzのカプリングチャンネルを通じて誘導的に電力供給される。
【0069】
誘導的電力供給は、心臓血管及び神経の研究への応用も見出されている。新規な3Dパワーステアリング・スキームは高いデータ速度の心臓のマッピング研究のために提案された(ミューラー(Mueller)等、1995年)。研究者は一部の遠隔測定制御の神経刺激装置における誘導的電力供給も実現した。それらのサイズは大いに減少し、皮下注射針を使って組織に注射可能となった。2つのこうしたデバイスがミシガン大学(アトキンス(Akin)等、1990年)とイリノイ工科大学(ローブ(Loeb)等、l991年)の研究者によって報告された。両方のシステムは、デバイスに電力を与えるためのマイクロコイルと磁気誘導に依存し、従ってバッテリに係るサイズと重さを無くした。誘導リンクはインプラントにコマンド情報を送るために変調もされる。CMOS集積回路技術を使ってさらにサイズが減少した。両方の研究グループは、移植デバイスが遠隔測定監視機能も実行することができるように、逆通信能力を組み込むことを提案した(ナーディン(Nardin)等、1995年)。
【0070】
商業的な製造業者は、いろいろなモデルを作って市場に出すことに成功してきた。これらのシステムはただ2,3のチャネルを持つだけであって、動物研究に合わせて仕立てられた。例えば、データサイエンスインターナショナル社(Data Sciences International)(米国ミネソタ州セントポール(St. Paul, Minnesota))は多くのモデルを提供している。それらのシステムはパルス間隔変調(pulse-interval modulation)、低電力消費技術を使用している。しかしながら、それらのシステムは一般に、チャネル毎に単一搬送周波数を使用し、実現できるチャネル数が制限されていた。それらのエレクトロニクスの低い入力インピーダンスもpHセンサと他のイオン選択センサ(ion-selective sensors)を含む可能性を制限している。データサイエンスインターナショナル社のシステムのもう1つの制限因子は、ユニークな専用の信号符号化、送信、及び受信器ユニットである。そのために、4つのチャネル(上限)を越えて拡張する可能性は全くありそうにない。これらのユニットが必要とされるより大きく、そしてそれらの温度センサの上限が35℃であるという事実との関連で、データサイエンス社のユニットは応用には適切ではない。
【0071】
ミニミター(Mini Mitter)社(米国オレゴン州サンリバー)の遠隔測定ユニットはサイズが非常に小さい(XM−FHシリーズでは9.0mm(直径)×15mm;VM−FHシリーズでは12mm(直径)×19mm)。それらはパルス間隔変調送信を使用して非常に低い電力動作を実現する。しかしながら、それらは単一チャネルだけを監視する。そのために、多重チャンネルのデバイスを作るためにいくつかの単一チャンネル送信器を積み重ねることは、全てを含めたサイズを受入不可能なものとする。小さいボタンタイプのバッテリが使用され、かつ置き換えが容易である。これらのユニットは単一チャネル応用にとって魅力的である。
【0072】
バイオメトリクス(Biotelemetrics)社(米国フロリダ州ボカラトン)は、多重チャネルユニットを作るために一連の単一チャネル送信器を積み重ねることを可能にする、その搬送周波数が調整可能な送信器を作っている。典型的なユニットの大きさは約2.5mm×7.5mm×10mmである。その送信器は電力消費を減らすために周期的にターンオン・オフができる。エレクトロニクスは、ユニットがどんな種類のセンサ(例えば、送信器、pHセンサ、及び他のイオン選択センサ)にも接続されることを可能にする高い入力インピーダンスを示す。
【0073】
ケーニヒスベルク・インスツルメント(onigsberg Instruments)社(米国カリフォルニア州パサディナ((Pasadena, California)))は、温度及び生体電位信号を測定するための最大1kHzのバンド幅を有する(EEG、ECG、EMGといった)4及び8チャンネルのインプラントを提供している。そのユニットのサイズは最小で1.0cm×1.5cm×3.3cmから最大で5.1cm×2.3cm×1.5cmまでの範囲に及ぶ。そのユニットはバッテリで電力供給され、そのバッテリの寿命は5−20ヶ月に及ぶ。RFスイッチがバッテリをターンオン・オフするために含まれる。伝達範囲は一般に3−5mである。多重チャネル増幅器ユニットもインプラントからの送信を受信してそれらを遠隔の基地局に中継するために利用可能である。いくつかの他の小さな会社が生体遠隔測定デバイスを作っている(Bio-Sentry,CME Telemetrix, Coulbourn, MIE Medical, Micro Probe, Telefactor, and Transkinetics)が、しかしそれらは移植可能でなく、あるいは単一チャネルユニットである(Biotelemetry Page, 1997年)。
【0074】
ボタンバッテリ電池はほぼ30年の間利用可能であったし、補聴器デバイスで広範囲に使用された。このタイプの最も一般に使用される電池は、2つの化学物質、すなわち亜鉛水銀酸化物(zinc-mercury oxide)と亜鉛銀酸化物(zinc-silver oxide)、で利用可能である。これら2つの間の主要な機能的な相違は次の通りである。(1)亜鉛水銀酸化物は長い時間にわたってより平坦な放電電圧特性を示す、(2)亜鉛水銀酸化物はもっと良く瞬間の高電力需要に答える(低内部抵抗)、(3)亜鉛銀酸化物は、亜鉛水銀酸化物の1.35Vに対して1.5Vから1.6Vまでの、より高い出力電圧を有する、そして(4)亜鉛銀(一価)の容積エネルギー密度はより大きく400−550Wh/cm3に及ぶ。これらの電池の供給能力は一般にほぼ100mA/時(mA-hours)である。
【0075】
これらの電池タイプの代わりは最近のリチウム陽極ベースの電池である。これらの電池は、その出力電圧(ICに必要なほぼ3V)が一般に亜鉛陽極電池のそれの2倍であるので、望ましい。もう1つの顕著な違いは、リチウム電池は一般にフラットパッケージで利用可能で、「コイン電池」と呼ばれるにふさわしいということである。容積率の見地から、たいていのリチウム・ベースの電池のエネルギ密度は亜鉛ベースの電池と好ましく匹敵する。例えば、リチウムヨード電池は約1,000Wh/cm*3の高いエネルギー密度を持ち2.8V出力を示す。ペースメーカは1970年代からリチウム電池を使用している。
【0076】
(好ましい腫瘍監視デバイス)
本発明のいくつかの好ましいセンサの実施態様が図5,6A、8,9、そして22に示されている。一般的に説明すると、本発明のその場で働く(in situ)センサ50は被験者内に移植可能(implantable)または注入可能(injectable)となるように構成される。図5,6、21、そして22は、好ましい移植可能な実施態様を示しているが、図8は注入可能な実施態様を示している。図9は移植可能なサテライトセンサ本体50Sと関連する注入可能な従属センサ本体50Dの両方を有するハイブリッドセンサユニット50”を示している。本発明のセンサユニットはそれぞれ、バッテリによって電力供給(図5)、あるいはより好ましくは誘導的に電力供給(図6A、8、と9)される。(移植可能または注入可能な)センサユニット本体はそれぞれ生物学的に適合する材料で密封され、当業者に周知の方法で殺菌される。
【0077】
図5に示されているように、センサユニット50’は少なくとも一つのセンサ要素51を備えて構成される。図5に示されたセンサ要素51はサーミスタ(thermistor)である。より好ましくは、図6Aに示されているように、センサユニット50は、温度、放射線、酸素及びpHの一つ以上を監視するように好ましくは構成された複数のセンサ要素51a−51eを備える。適切な個別のpH、放射線、そして温度の要素51a−51eは当業者に知られている。好ましい温度センサのタイプはサーミスタである。好ましい放射線センサはMOSFET(金属酸化物半導体電界効果形トランジスタ)ベースのデザインといったものはよく知られている。好ましい自己較正型の酸素センサ及び組合さった酸素/pHセンサの態様は以下詳細に説明される。
【0078】
本発明のための温度センサ要素は約0.1℃の精度で約35℃から45℃の温度範囲において動作するよう構成される。この移植可能なデバイス全体は最小限に侵入すべきであるので、サイズは主要な関心事項である。好ましくは、移植可能なセンサユニット全体は約1.0cm*3未満のサイズを有する。さらに、腫瘍監視システム10のセンサユニット50,50’、50”は放射線にさられたときでさえ動作するよう構成される。る。すなわち、センサユニット50,50’、50”は、放射線が腫瘍に与えられている間は必ずしも機能する必要はないが、その後には即座に好ましく機能しなければならない。センサユニット50,50’、50”は従って放射線照射後に即座に(数秒内に)反応するように構成される。好ましい実施態様では、図8に示されたように、センサユニット50”は、それが挿入プローブの先端上に配置され、そして例えばポジションへの画像誘導配置を使って大きなボア・カニューレ(bore canula)によって挿入できるようなサイズと構成を有する。
【0079】
次に図6Aと図6Bを参照すると、そこにはセンサユニット50の好ましい実施態様が示されている。センサユニット50は、主要本体部分50Bとそこから外向きに伸びる複数のアーム部分50Aを備えて構成される。図6Bに示されているように、アーム50Aは薄い平らな輪郭を有する。好ましくは、アーム50Aはポリイミド(カプトン(KaptonR)(登録商標)、ポリイミド(polyimide)材料のような)といった柔軟な生物学的に適合する基板材料で形成される。少なくとも一つのセンサ要素51が、各アーム50A上に、好ましくは(主要本体50Bから離れた)末端部分に、配置される。個別のチャンネル151は、センサ要素51を、主要本体50B上に配置された電気動作回路125に電気的に接続する。もちろん、複数のセンサ要素51が各アーム上に配置可能で、各アームは個別の電気通信チャネル151を備える。好ましくは、それぞれのチャネルは、柔軟な基板の最上面に金属真空蒸着によって形成される一対のリードによって確定される(センサO2は3つ以上のリードを有してよい)。
【0080】
同様に図6Aと図6Bに示されているように、送信コイル58ははエレクトロニクス125を取り囲むように実質的に円周状に重ねられる。電気回路125は、以下詳細に説明されるような信号データ参照のために、少なくとも一つ、好ましくは複数の固定抵抗125Rを含む。
【0081】
図6Bに示されているように、生物学的に適合するコーティング160がセンサユニット50の外面に(好ましくは封入、より好ましく密閉されるように)与えられる。表面取り付け電気部品も主要本体50Bの最下面上に、バイアスに通じてメッキされている相互接続を備えて(柔軟なプリント回路ボード技術において使用される一般的な方法)配置できる。有利には、この多重アーム構成は、腫瘍のより略式な分析を考慮するために増加した地域データを提供することができる。上に論じられたように、多重センサ要素51は内部で異なった場所と接触し(異なる深さに侵入し)、そして/または包みこんで腫瘍に沿った異なる外面の周囲の場所に接触することが可能である。代わりに、一つ以上のアームが、正常組織の状態に関する情報を提供するためにその正常組織に取り付けられることが可能である。いずれにせよ、センサアーム50Aは好ましくは、被験者におけるそれらのポジションを確保するための取り付け手段150を備えて構成される。例えば、センサ要素51Aは、それを決まった場所に縫合することを可能にするための、基板の末端部分に形成された開口部を示している。代わりに、センサ要素51bはとげのある外面150’を示している。
【0082】
図7、図8Aと図8Bは、シリンダ形状で注入用サイズにあるセンサユニット50”、例えば注入可能なセンサユニット50I、を示している。この実施態様において、PCBまたはICチップ125pはセンサ本体の長さに沿って少しの距離だけ延びるよう方向付けられている。コイル58もPCBまたはIC125の一部分を囲むようシリンダ状に拡がる。示された実施態様では、PCBはコイル58の外側をある距離だけ拡がる基板(好ましくは柔軟な基板)である(全体的距離は約1.27cm(0.5インチ)未満)。もちろん、IC構成を使用すれば、このサイズは更に減少させることができる。さらに、ICあるいはPCBはコイル58と同じ距離だけ実質的に拡がるような構成とサイズを有することが可能である。センサ本体は単一チャネル(すなわち、約3mmの幅を有するPCBバージョンに対する1センサ要素)、または多重チャネル(各チャネルが並行に引かれた複数の要素で、一般に単一チャネルバージョンよりも幅広い)を保持するように構成できる。センサユニット50Iの先端125Tは、腫瘍組織への侵入を容易にするための丸いあるいは鋭いエッジを備えて構成できる。再び、センサ本体全体は生物学的に適合する材料で封入され、医療応用のために殺菌される。
【0083】
好ましくは、本発明のセンサユニットの注入可能バーションと移植可能なバージョン50I、50の両方はそれぞれ、図6と図7で示されたもののように、誘導的に電力供給される。すなわち、監視システムは、内部に配置されたセンサと結合して電力供給するための変圧器(患者の体の表面に一つのコイル、モニタ内部に第2のコイルを備える)として作用するよう構成されるが、当業者には周知で上でも短く議論された。従って、その場で働くセンサユニット50、50’、50”、50’’’は自己包含的で、断続的または長期にわたる治療判定のために臨床的に有用な長期にわたる情報を提供するために身体内で十分に長いサービス寿命を持ち、そしてカテーテル、または外部と接続されたワイヤがセンサ内と身体外に導かれることを必要とせずに、最小化が可能である。
【0084】
コイル58を形成するために従来的に使用される個別の銅線ラップコイルの代わりに、コイル58はフェライト基板(磁束集線装置(flux concentrator))による回路ボードそれ自身の中に統合化される。さらに、回路ボード125pとそれに関連する電気部品は最小化されたチップとして構成可能で、それよってコイル58は同様に最小化されることが可能である。しかしながら、信号は一般にコイル面積に比例し、デバイス面積が減少するにつれ、コイル58に付随する、あるいはデバイスの周囲の、その信号強度は減少する可能性がある。
【0085】
さらにデバイスを小型化するために、温度センサ共鳴要素(temperature sensor resonant element)が正温度係数(PTC(positive temperature coefficient))(一般にセラミック)として構成できることは認められるであろう。たいていの従来デバイスはNTC(負温度係数(negative temperature coefficient))バージョンを使するが、本願については、PTCが有利かもしれない。
図9は、上で説明されたような誘導的に電力供給される移植可能及び注入可能センサ50、50Iのハイブリッド型センサユニット50”’を示しており、これは最小化されたセンサ要素本体と送信において有用な信号強度を可能にする。示されているように、このセンサユニット50”’の態様は、その上にICまたは外部と通信するエレクトロニクス125を備えたサテライトセンサ50Sと、複数の従属センサユニット50Dとを含む。従属センサユニット50Dは、サテライトセンサユニット50Sと誘導結合され、そのサテライトセンサユニット50も誘導的に電力供給され、かつ外部のシステムと結合する。さらに、従属センサユニット50Dはサテライトセンサユニット50Iに遠隔測定用に接続され(60I)、サテライトセンサは外部の受信器75に遠隔測定用に接続される(60)。従属センサユニット50Dはサテライトセンサユニット50Sに関して局所的に配置されるので、信号強度の要求は減少され、それにより、注入可能なサイズの従属センサユニット50Dはさらにサイズが減少することが可能になる。好ましくは、各従属センサユニット50Diは、電子的に符号化され、あるいは識別され、あるいは、監視システム10の送信されたセンサデータの整合性のある解析のために(もし絶対的でなければ)相対的な位置的情報を維持するためにサテライトセンサユニット50S内の特定のチャネルまたはポートに場所的に関係することが可能である。
【0086】
図19Aは、本発明の別の実施態様を示しており、そこでは腫瘍監視システム10”’は複数のセンサユニット50を使用している。すなわち、少なくとも一つのセンサユニット50は図示されているように異なる(別々の)腫瘍サイト(部位)に配置されている。この多重センサユニット腫瘍システム10”’は関心のある各腫瘍サイトにおいて有効あがるために必要に応じて治療を調整するためのより地域特定的な情報を結果としてもたらすことができる。好ましくはこの多重センサ監視システム10”’は、各個別のセンサユニット50、50”、50”’がデータの完全性と腫瘍サイト/特定場所との関連性を保全するように電子的に識別可能であるよう構成される。これは受信器75と個別のセンサユニット50(50Iと50S/50D)を体内の特定のセンサユニット50の場所または位置に送信するための相対的順序を識別かつ/維持するためのポート通信プロトコルを使って構成することにより提供できる(つまり、「センサ1」に対してチャネル1、「センサ2」に対してチャネル2といった具合に、各英数字識別子は手作業あるいはプログラマブルに、関係軸に沿って左から右または上から下への順序で腫瘍上に挿入部またはポジションにおいて設定されている)。受信器75は適切なデータ送信のためにセンサユニットコイル58の直前(一般に約30cm)に配置されるべきであるので、受信器75は送信の間に適切なセンサユニットに重なるよう移動するよう構成されることが好ましく(図19Aでは矢印または点線によって受信機器の移動が示されている)、またデータの完全性を保証するためにセンサユニット送信の順序を認識するようプログラムされることも好ましい。もちろん、各センサユニットの場所に一つずつ、2つの受信器が使用可能である。これは特に、患者対話型システムが使用されてよい患者の家といったところで、非臨床使用にとって適切である。従って、複式受信器構成は、それによればユーザは各監視された腫瘍サイト上で携帯型受信器のポジションを維持することができ、有利な場合がある。
【0087】
もちろん、適切な配列を可能にするための配列の外部のマークあるいは指標も役に立つかも知れない(単一の腫瘍/領域センサユニット態様と多重センサユニット/間隔を置いたポジション態様の両方において)。これは、肌の上になされる半永久的な身体マーク175及び/または受信器75と協働できる赤外線的もしくは写真測量的ポジション読み取り可能なまたは表示手段(受信器ループ)であることが可能で、受信器75は選択された場所における送信の前/間にポジション確認光線を送出して適切な配列の位置確認を容易にすることができる。
【0088】
遠隔送信のため、本発明の腫瘍監視システムは好ましくは低いあるいは非常に低いバンド幅で情報を送信するよう好ましくは構成される。すなわち、搬送バンド幅は好ましくはMHAzレンジにあるが、その一方、変調周波数は好ましくは約1kHz以下にある。この低いバンド幅動作によれば、モデムと声電話接続のような遅い通信リンクを介してセンサから受信した信号データを送信することが可能である。好ましくは、測定された信号情報はいくつかの時間ベースの変調スキームの一つに符号化される。時間ベースの符号化によれば、振幅情報を不正確に、そして周波数情報を正確に運ぶかもしれない、音声電話ネットワークといった通信リンクを介して正確なデータ送信が可能になる。さらに、ホームサイトにおける非臨床使用の腫瘍監視システム10’に関して、腫瘍監視装置は、遠隔地においてセットアップ及び操作されるよう好ましくは小さく、かつ比較的高価でなくもしくは費用効果が高いことが好ましい。
【0089】
もちろん、時、日、週の期間あるいはもっと長い期間をカバーするデータセットまたはデータセグメント/レコードが、一つ以上の個別の比較的短いデータ送信セッションにわって、収集され、かつ中央の演算処理サイトへ送信されるよう、上記のように、遠隔の場所におけるPCを使って十分に継続的あるいは半継続的に監視して、同じ時間/日付スタンプに関連するデータを記憶することといった、遠隔作業に適する基本的に任意数の適切な符号化または送信スキームに、センサユニット50、50I、50Sからのデータが変換されることが可能なときには、低いバンド幅動作は必要ではない。
【0090】
すべての主要タイプの温度センサの中では、一般にサーミスタがはるかに最も感度が良い。それはインターフェース接続にとって速い応答時間と高い出力を有し、小さなデバイスが商業的に利用可能である。非線形応答はセンサが機能する小さな温度範囲(一般に約10℃未満)では重大ではない。インターフェース接続回路は電流源を必要とするけれども、シリコンの塔頂留出物は少数の付加的なトランジスタだけである。デバイスは産業目的にとって壊れやすいと思われるが、しかし本願では十分に頑丈であるべきである。デバイスが限定された温度範囲で動作し、かつ電流は小さくあることができ、そして継続的に与えられ必要がないので、センサの自己加熱は減少する。もしバッテリ源が使用されるならば、そのバッテリが原因となった加熱にさらされることを防ぐために、センサ要素は好ましくは絶縁されあるいは空間的に離してに配置される。
【0091】
腫瘍センサ設計の妥当性を検査するため、サーミスタが外部に取り付けられた、単一チャネルの個別部品の商用遠隔測定ユニット(ミニ・ミッタ社製(MiniMitter,Inc.)、モデルVM−FH)が購入された。実験はTriangle Radiation Oncology Services(TROS)において、サーミスタと送信器を寒天ジェル模型(agar-gel phantom)ターゲット内に配置して、そして温熱療法治療デバイス(サーモトロンRF−8(Thermotron RF-8))内のターゲットを37℃から45℃の治療範囲にわって加熱することによって、行われた。図2Aは、サーモトロン(登録商標)デバイスによる温熱療法治療の動作原理を示している。8MHzのRF信号がマシーンのプレートの間に印加され、イオンはそれらのプレートの間で振動させられる。これらの振動は摩擦によって熱を発生させて、身体組織の一様な自己加熱を生じさせる。寒天ジェル模型はほぼ人間の胴の大きさであって、身体組織の加熱特性をまねている。患者との治療セッションの間では、皮膚の表面温度は常に監視される。さらに、カテーテルは通常、皮膚の表面を通して治療を経験している腫瘍部とその近傍に挿入される。治療の間、RFエネルギが印加される際に熱電対プローブが腫瘍温度を記録するためにこれらのカテーテルを通して挿入される。これらのカテーテルは治療セッションにわたって患者内の決まった場所に残され、そのためしばしば不快と汚染の源となる。
【0092】
この実験は2つの目的のために設計された。第1に、絶縁されたサーミスタの性能がサーモトロン(Thermotron)の熱電対のそれと比較された、第2に、サーモトロンデバイスのRFエネルギの加熱効果を観察するため、むき出しのボタンサイズのバッテリが寒天ジェル内に配置された。実験的なセットアップが図11に示されている。2本のカテーテル99が寒天ジェル模型101内に挿入された。ただし、一つ99Rはサーミスタの近くに、第2のもの99Bはバッテリの近くに置かれた。サーモトロン(登録商標)(ThermotronR)デバイスの熱電対プローブがカテーテルに挿入され、そしてRFエネルギが次第に治療範囲上の温度を掃引するよう寒天ジェル模型に印加された。実験は寒天ジェルが一様に加熱されたことを保証するために75分間にわたって行われるよう設計された。
【0093】
実験の結果が表1に示されている。表1の最初の2つの縦列(図11参照)は、実験の時間進行と、熱電対1によって採取されたサーモトロンデバイスの計器盤パネルからの温度読み取り値である。この測定値は正しいと仮定され、参照値または「金」の標準値として用いられた。第3の縦列は第1の横列にある初期値からの熱電対1の温度の相対的変化を示している。第4の横列(縦列?)は同じ測定時におけるサーミスタの読み取り値の相対的変化を示している。サーモトロンデバイスの熱電対の読み取り値との密接な相関関係に注意されたい。
【0094】
ボタンバッテリ加熱実験の結果は表1の第5の縦列に報告されている。これらのデータは寒天ジェル模型に置かれたボタンサイズの電池の近くに位置している熱電対2から記録された。サーモトロンデバイスのRFエネルギが寒天ジェルを治療範囲にわたって加熱するにつれ、バッテリ近くの温度はより大きな程度まで増加したことに注意されたい。サーミスタの近くの熱電対1の温度は8.8℃だけ増加したが、一方、バッテリ近くの熱電対2の温度は11.1℃だけ増加した。これは、バッテリによって電力供給されるどんなインプラントも、腫瘍細胞集団の環境を監視している温度センサに対する影響を最小化させるため適切に熱的に絶縁されるべきであることを示している。
【0095】
【表1】
【0096】
次の仕事は、ブレッドボーディング(breadboarding)技術を使用して4チャンネルの、個別部品の試作品回路を設計及び制作することにある。この回路は温度監視するのために4つのサーミスタを利用した。回路のブロック図が図12に示されている。温度の増加が、4つのサーミスタ51a−51dによって、対応する抵抗の減少に応じて感知された。サーミスタ51a−51dを駆動する一定の電流源が抵抗を測定するために使用された。増幅器53の電圧出力は抵抗の変化に比例した。増幅器53に繋げられた電圧電流変換器(voltage to current converter)54がタイミングコンデンサ56を充電するために使用された。タイミングコンデンサにかかる電圧がある一つの閾値に到達するまでに要する期間はサーミスタ51eの抵抗の変化に比例し、従ってサーミスタの表面における温度変化に比例した。図13と図14A−14Cはセンサ回路の適切な動作設計を示している。コンデンサ電圧が予めセットされた閾値に達すると、送信器157はコイル58に1.0MHzにおける信号バーストを送る。同時に、閾値検出回路158はコンデンサ56を放電させる。信号バーストの終わりにコンデンサ56は再び閾値に向かって充電を開始することが許される。もし増幅器53の電圧が高ければ、大きな電流がコンデンサ56に流れ込み、それによって充電時間間隔が短くなる。もし増幅器出力の電圧がゼロであるなら、電流はタイミングコンデンサ56に一切流れ込まない。このケースでは、小さい電流源がデバイスが適切に稼働していることを保証するために含まれた。この小さな電流源は、送信器157に対して、検査目的のためにより大きな時間間隔で信号バーストを送出させた。より長い時間間隔はより低い温度測定(値)を示すが、他方より短い時間間隔はより高い温度を示す。
【0097】
クロック&カウンタ155、及び制御論理回路(control logic)156は総当たり的に生体遠隔測定チャネル上で4つのサーミスタを多重送信する役割を果たす。LabVIEW(登録商標)ソフト(米国テキサス州オースティンに所在するナショナルインスツルメンツ社(National Instruments, Inc.,Austin.TX))を走らせるラップトップPCに繋げられた修正されたAMラジオ受信器が送信器バーストを検出するために使用された。水槽実験がインプラント設計の動作を確かめるために使用された。遠隔測定リンクの範囲は約30cmであった。
【0098】
個別部品の機能試験品(discrete-component breadboard)の設計と構成に続いて、表面取り付け(SMT(surface-mount))ユニットがサイズを減少させるよう設計された。図12の回路は精密化(refined)され、そして両面の5.6×8.9cm(2.5×3.5インチ)のプリント回路(PCB(printed-circuit))が制作された。低い輪郭のSMT部品が使用された。消費電力は3.0Vバッテリからの4.5Wであった。送信コイル58(直径13.5mm)には巻数25の#38AWG銅線が使用され、30cmのレンジが作り出された。4つのサーミスタ51a−dがデバイスに繋げられ、水槽実験が繰り返された。結果はシステムの機能性を確かめるより以前の実験に類似していた。
【0099】
成功したSMT実験の後に、第1世代の集積回路(IC)試験チップが設計された。その目的は、SMTユニットに適用された動作コンセプトが集積回路技術に適用可能であることを明らかにすることであった。図15と図16は、ICデザインとそのチップレイアウトの機能ブロック図である。回路デザインは最初に精密化され、SPIECEを使用してシュミレートされた。次いでICレイアウトが標準的セル技術を使用して実行された。回路は特にラッチアップ(latch-up)に対する感受性を最小にするよう意図された。試験チップはMOSIS製造サービス(MOSIS fabrication service)(2.0ミクロン、CMOS、n型ウェル、低ノイズ、オービットアナログプロセス、微小チップフレーム(tiny-chip frame))を使用して実現された。いくつかの内部テストポイントがIC部分回路の完全試験を可能にするために挿入された。ヂュアルインライン(DIP(dual-in-line))パッケージで配送された4つのICが小さなPCB(1.5x4.0cm)を使って構築されたIC試作品ユニット内に取り付けられた。すべての4つのICはベンチトップ機能試験を受けさせられ、そして期待されたように機能した。
【0100】
機能試験を通過した後、試験チップは一連の放射線及び冷熱試験にさらされた。最初にユニットは、図17Aと図17Bに示されているように、温度制御された水槽を使用して熱的に検査された。IC試作品ユニットはセンサデータのための7つのチャネルを使用した。それらのチャネル中の4つがサーミスタに接続され、残りの3つは固定抵抗器に接続された。図17Aは、サーミスタがチャネルのパルス幅を0.1℃当たり約0.03msだけ変化させたことを示しており、それに対し、図17Bに示されているように、固定抵抗器チャネルは0.1℃当たり約0.003msだけ変化した。これらの結果は本発明による腫瘍センサの精度仕様の十分範囲内である。
【0101】
次にユニットは、米国ノースカロライナ州に所在するレックス病院(Rex Hospital in Raleigh, NC)に位置するTriangle Radiation Oncology Services (TROS)のガン治療施設を使用して放射線にさらされた。一連の400cGy放射線ドーズが、線源にVarian Clinac 4/80を使って表面距離80cmにドーズ率1.2Gy/minで送出された。IC試作品は、インプラントが利用可能な臨床環境を刺激する照射の間は電力供給されなかった。放射線被曝試験の結果は図18Aと図18Bに示されている。サーミスタと固定抵抗器チャンネルのパルス幅は1Gy当たり約0.0015msだけ変化するが、これは1Gy当たり約0.005℃に翻訳されることに注意する。患者は一般に8000cGy以上にさらされないとすれば、放射線の影響は0.4℃未満で、これは以下説明されるように信号処理によって補正できる。
【0102】
図18Aと図18Bのサーミスタ及び固定抵抗器データは、放射線照射にさらされる間のパルス幅の増大はICのアクティブトランジスタパラメータの変化によるものであることを示唆している。これらのパラメータの変化は超小形電子回路(NPS、1997年)に対する放射線の効果に関する多くの研究者の実験に基づいて予測される。それ故に、ICデバイスは放射線照射に対するセンサと考えることが可能である。
【0103】
したがって、固定抵抗器チャネルは全照射線量を測定するために使用することができる。製造の間のそれぞれのインプラントについての較正から、固定抵抗器チャネルに対する初期のパルス幅は知られるであろう。放射線照射下にあるICの振る舞いについて得られる統計データ(図17Aと図17Bに類似するデータ)から、カーブの傾きが知られるであろう。それ故に、固定抵抗器チャネルからのリアルタイム測定は、参照固定抵抗器と既知の較正データに基づいて変化を考慮してインプラントに対する放射線照射線量履歴の正確な表示を与えるよう補正することが可能である。この全体的な照射線量計算を使って、サーミスタのチャネルからの温度読み取り値はどんな放射線照射線量レベルにおいても正確な温度読み取り値を与えるために数学的に補正されることが可能である。すなわち、放射線損傷あるいは被曝によってICドリフトと温度ドリフトが引き起こされる可能性がある。これは3つのパラメータ、つまり、一定にある既知の固定抵抗器値と、温度に応じてのみ変化する温度センサ値と、両者(熱気泡(サーマル)と放射線)によって影響を受けるIC、と比較される。セットアップ(または工場で)で確定された較正データを使用すれば、信号データの放射線に基づくドリフトと調整を決定するための既知パラメータの数に基づいて信号データを較正することが可能である。放射線のドーズが、図17と図18に示されるように、ドリフト調整の十分範囲内であるときには、このドリフトは補正可能である。稼働中、コンピュータ手段は一つ以上の固定抵抗器から受け取るデータに基づいて計算上補正を実行することができる。
【0104】
したがって、少なくとも一つの固定抵抗器125R、好ましくは複数の固定抵抗器が、センサの動作回路に使用されることが好ましい。図14Bは、一つの固定抵抗器チャネル(一つの参照)と4つの積極的監視チャネルを示している。一実施態様において、センサユニット50は3つの抵抗器を含むが、一つは実質的に温度または照射線に対して不変で(固定抵抗器125R)、一つは温度と共に変化し(サーミスタ)、一つは温度と放射線の両方と共に変化する(一般にチップにおけるMOSFETは両方と共に変化する抵抗を持つ)。サーミスタは関連する測定された温度に依存するカーブを有する。固定抵抗器はMOSFET上のバイアスを修正する(放射線被曝/損傷によるそれらのドリフトを調整または補正する)ために使用することができる。コンピュータは温度分布のような修正された読み取り値を与えることができる。
【0105】
正常な動作状態の間は、放射線(高照射率ガンマ線、熱RFとマイクロ波、または超音波)が患者に当てられているときは移植デバイスはパワーダウンされて(電力消費量を下げて)よい。一連の試験が、Triangle Radiation Oncology Services(TROS)における典型的な治療源からの被曝/エネルギー誘発事象(exposure/energy challenge events)の効果を決定するために行われた。最初に、患者を治療するのに使用されるレベル以上のレベルにある8MHzのエネルギー(サーモトロンRF−8(Thermotron RF-8))がパワーダウンした状態とアップした状態の両方のデバイスに当てられた。次に、Varian Clinac4/80を使用してガンマ放射線に対して繰り返された。最後に、クリニサーム社(Clini Therm)の表面腫瘍加熱器機(Clini Them surface tumor heating instrument)からのマイクロ波(915MHz)エネルギーを使用して再び試験が繰り返された。全ての場合に、デバイスはエネルギー誘発試験によって損傷を与えられることはなく、試験の結論が出た後も正確な温度測定を継続した。全ての試験が、誘発試験の累積的な効果が否定的であるように同一の移植デバイスに対して行われた。
【0106】
生物学的生存性(biosurvivability)と生物学的適合性(biocompatibility)を評価するために、いくつかの見せかけの移植デバイスが上に記述されたセンサユニットの好ましい実施態様に類似する材料を使って製造された。見せかけのインプラントを製造するための全体的なスキームは図5に強調表示されている。基板120は25ミクロンの銅層によって覆われた5ミルの柔軟なカプトン(登録商標)(KaptonR)ポリイミド材料を使って製造することができる。金属層122はフォトリソグラフィを使って単純な発振器回路のための配線のまとめ取付け(wiring harness)にパタン化される。次にポリイミドの絶縁層が、金属トレースへの伝導バイアスをオープンにするよう堆積及びパタン化できる。次いで表面取り付け電気部品125が基板上に配置され、その基板に半田付けされる。次に、サーミスタ51が図5に示されているように移植基板の端のブランチに接続される。次いでアンテナワイヤのコイル58が図のようにIC及び/またはSMT部品125と一緒に取り付けられる。最後に、リチウムのコイン形バッテリ52が基板120に取り付けられる。バッテリ52は図5に示されたポジションに最初に基板に貼り付けられる。エンドフラップ(end flap)129(第2のバッテリ接続を含むサークル)がバッテリ上に折り重ねられ、導電性銀エポキシを使用して貼り付けられる。デバイス全体がその後、インプラントの間にそれを生物学的環境から守るために、サイラスティック(silastic)及び/または医療グレードのシリコーン(medical-grade silicone)の薄い層といった生物学的適合材料で密封される。
【0107】
ユーザインターフェースの規格に基づくセンサ50,50’,50”,50”’は追加的特徴も含むことができる。例えば、バッテリを外部から印加されるRF信号によってON・OFFにする能力をIC(チップ)デザインに含めることができる。もう1つの特徴としてpHセンサインターフェースエレクトロニクスを含めることが可能である。pHセンサは好ましくは図10Aに示されたカプトン(登録商標)基板といった生物学的に適合する柔軟な基板上に実現される(コソフレット(Cosofret)、1995年)。このデザインは図5に示されたカプトン(登録商標)基板と両立する。
【0108】
好ましい実施態様において、本発明は自己較正する、酸素、pH、または組合せ型酸素/pHセンサを利用する。その場で働く生体内の自己較正する長期間移植されるセンサユニット200、201、300の動作原理は、図20と図22に示されたような貴金属電極における水の電気分解に基づいている。酸素または水素は、発生電極(generating electrode)(”GE”)227とカウンタ発生電極(counter-generating electrode)(”GE”’)227’に電流を印加することによる水の電気分解により生み出すことができる。GE227におけるこれらの分解されたガス分子の蓄積により、素早くマイクロセンサの直前に酸素飽和または水素飽和の微環境が確立される。次いで、高ポイント較正が酸素飽和相(oxygen-saturated phase)で確立され、低ポイント較正が水素で微環境を飽和させることにより作り出される酸素空乏相(oxygen-depleted phase)で確立される、酸素センサユニット200の2点較正手続(two-point calibration procedure)が実行できる。微環境のこれらの短期的摂動は素早く周囲の媒質(組織)と平衡状態になることが期待される。この生体内のその場に置かれる自己較正するセンサユニット200、201、300の周期的センサ較正は長期間移植されるデバイスの動作性及び生物学的生存性をチェックするために実行される。
【0109】
自己較正するセンサユニット200、201、300は、以下の動作上及び物理的仕様、すなわち、
1)動的範囲:
(a)少なくとも10mmHgの分解能で0−760mmHg(酸素分圧に対して)、
(b)約0.1のpH分解能でpH5.0−8.0、
(2)温熱療法治療セッションの間に同時稼働:
(3)最小4−6週間(好ましくは6週間あるいは1.5ヶ月)の稼働期間と、より好ましくは少なくとも3ヶ月の稼働期間、
に従って構成される。
【0110】
水電気分解法は、移植されるpHセンサユニット201(図10B)の1点の生体内のその場において(in situ)較正を実行するよう拡張することもできる。発生電極によって囲まれるマイクロpHセンサユニット201は水の電気分解の間に滴定pH微環境(titrating pH microenvironment)を経験するであろう。もし人が電気分解電流を発生電極を通して繰り返し前後に動かすならば、pHセンサの時間応答における最高の傾斜が中性のpH(pH7.0)の瞬間に生じるだろう。従って、中性のpHにおける1点較正は、水の電気分解の間に、滴定の間のセンサ応答の最初の派生物をチェックすることにより実行することができる。類似のpH滴定微環境の機能性はpHスタティックな酵素センサまたは緩衝能センサ(buffer capacity sensor)(オルスイス(Olthuis)、1992年)に対して実証された。この以前の仕事は腫瘍監視アプリケーションにおける選択肢として1点pH較正の実現可能性を強くサポートする。
【0111】
以前、ポーラログラフィー・マイクロ酸素センサが柔軟なカプトン(登録商標)材料上に製造された。図21に示された基本的な電気化学的3電極式セル構成が、電流を回避して、マイクロ参照電極における表面材料消費を最小化するために採用された。すべての電極はすべての半径方向で電気化学的化学種の分散的質量輸送を保証するために幾何学的に対称であるよう設計された。
【0112】
2つの異なるデザインが考慮された。一つは長方形帯(バンド)を備え、もう一つは同心円を備える。同心円を有するデザインはより良い性能を与えたが、このことは理論的に説明可能である。電極・電解液境界面におけるノイズは、ホワイトノイズと1/fノイズの2つのソースによって生成される(ランブレヒツ(Lambrechts)、1992年)。電極のより低い形状係数(円周対表面積比(circumference to surface area ratio))がより低いホワイトノイズレベルを結果としてもたらすが、このことは円形電極によって生成されるノイズが同じ幾何学的面積を有する帯状電極のノイズよりも低いことを意味している。1/fノイズは逆に電極面積に反比例する。同じく、電流出力の大きさは電極面積に比例する。このことは、電流出力レベルと1/fノイズが組織酸素測定に対して極限の小さなサイズへの電流測定センサのスケーリングを制限することを意味する。
【0113】
両方の構成のレイアウトは20、10、及び5ミクロンの線幅を使用して実行された。図21は製造された試作品酸素センサ200(同心円構成)の構成図である。すべての貴金属電極は金、酸素触媒として使用されるときには最大の安定性を持つことが示されている物質(ホアレ(Hoare)、1984年)から作られる。
【0114】
次に図21に示された各同心円の機能に目を向けると、溶存酸素分子(dissolved oxygen molecules)が電気化学的に減少する中央の電極は作用電極(working electrode)(「WS」)225としての役割を果たす。GE227は作用電極の周りにくるみこまれる。この構成は、自己較正サイクルの間に酸素飽和または水素飽和した微環境を確立する。内側から外部へ進むと、次の同心円が参照電極(「RE」)229として使用される。図21の最も外側の電極はこの3電極セルのカウンタ電極(counter electrode)(「CE」)231である。それはCE231において生成される副産物のWEでの電気化学的干渉を排除するためにWS225からできるだけ遠くに配置される。GE’227’(図示されていない)も同じ理由からWE225から遠隔に位置する。
【0115】
過去において、pHセンサも柔軟な基板上に製造されてきた(コスフレット(Cosfret)、1995年)。図10Aは、Ag/AgCl電極上にp−HEMA(POLY-HEMA)中央ドームを含むpHセンサ構造物を示している。最終製造ステップはpHイオノファ(ionophore)を含む外側の重合体膜の堆積である。これらのセンサは、最大2ヶ月間、血液中の生体内の予備テストで正確に能力を発揮した。これらのポテンシオメトリック・センサのサイズは空間勾配を解決する能力を改善するために好ましくは最小化される。図10Aに示されたpHセンサの更なるサイズ減少は、膜の接触領域が減少するにつれ、重合体膜溶剤の手動堆積、基板への弱い接着性と高インピーダンスによって制限される。重合体膜の使用によって課されるもう一つの欠点は、長期稼働の間に膜の可塑剤とイオノファが漏出及び劣化する可能性があるということである。さらに最近は、重合体膜を固体状態の類似物によって置き換えることによってpHセンサを小型化する仕事がなされている。今日までに確認された最良の選択肢は、優れたpHセンシング能力を示しており単純な電気メッキ法を使用してセンサ表面上に堆積可能な、インジウム酸化物である(マルゾーク(Marzonk)、1998年)。この新しい構造は図10Bに示されている。
【0116】
図21に示されているような自己較正するO2センサは米国ノースカロライナ州立大学のBMMSL(Biomedical Microsensors laboratory)施設によって製造されている。表2と表3はそれぞれ酸素センサ200とpHセンサ201の好ましい製造プロセスをまとめたものである。
【0117】
【表2】
【0118】
【表3】
【0119】
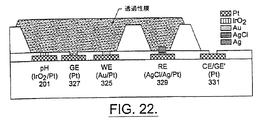
その場で働くセンサユニットのもう一つの好ましい実施態様が組合せ式pH/O2センサユニット300として図22に示されている。組合せ式センサユニット300はより小さな特徴サイズを想定しているので、発生電極の面積と、従って、その電流容量は減少する。より小さな構造によって、この新たなセンサが勾配測定(gradient measurements)のために線形アレー(線形配列)で使用されることも可能になる。より小さいセンサの微環境は飽和するのにそれほど酸素を必要としない。GE327が飽和した微環境をいったん確立すると、構造的手段が酸素及びpH平衡を遅らせるために採られる場合を除いては、これらの状態は急速に消滅するであろう。それ故、自己較正する設計は、制限されたセンサ較正期間の間だけ飽和した微環境を維持するために凹所を設けた構造(recessed structure)(マイクロプール(micropool))を使用することができる。従って、3次元マイクロプールは、作用電極及び発生電極325,327を閉じ込めるための壁を作るために感光性重合体の層を使用することによって構成することができる。マイクロプールの容積はセンサユニット300の全性能と較正に必要な期間を決定することもできる。ほとんど最適な設計は、様々な製造ラン(fabrication runs)におけるいくつかの設計パラメータを逐次代入することによって決定することができる。電極エッジにおけるポリイミド/金属界面での若干の表面劣化と接着性問題が(10mA/cm2を越える電流密度における)試作品実験の間に観察されたことは指摘しておく。
【0120】
従来のクラーク酸素センサ(Clark oxygen sensor)は、疎水性の非導電性膜によって密封された同じ隔室内に位置する参照電極(陽極)と作用電極(陰極)を含む。それとは対照的に、図21と図22に示されているように本設計は、GE227(RE329とWE325の間に配置されWE225の微環境を制御するために置かれた)のためのスペースを許すためにRE329とWE325を分離する。この新しい構成は、膜破裂の危険と後に来るセンサの内部充填溶液の劣化のために長期の移植に適切ではないかもしれない従来のクラークセンサとは対照的である。この設計では、分離したREとWEは親水性の透過性膜と組織液を介して電気的に結合する。REとWEに対するこの分離した構成は、陽極が陰極から非常に離れているときに、増大した溶液抵抗による問題を引き起こす可能性がある。しかしながら、当該3電極システムはこの効果を減らす。もう1つの困難が、透過性膜に浸透する組織液の成分との直接接触によるWE表面汚染によって導入される可能性がある。従って、使用される電極材料はこの振る舞いを減少させるよう選択されることが好ましい。例えば、酸素監視のために最長4年間移植されたむき出しの金電極は鏡のような炭素電極より少ない血液タンパク質を吸収したことが実証された(ホルムストロム(Holmstrom)、l998年)。
【0121】
3電極セルと発生電流源との間のどんな静電結合も最小にするために、センサ300の動作は好ましくは別々の較正モードと測定モードとに分割される。デバイス構造を単純化するために、カウンタ電極(CE(counter electrode))は好ましくは発生源(generating source)のカウンタ・発生電極(GE’)として二重の役割を果たすであろう。従って、2つの動作モードの間で切り替え可能な単一電極は2つの機能を果たすことができる。
【0122】
好ましくは、特徴サイズ(eature size)を減少させて製造の間に確かにそれを形成するために、シリコンウエハースによって支持される柔軟基板のプロセスが熱膨張と表面あらさ歪曲(surface roughness distortions)を減らすために使用される。この製造プロセスにおいて、ポリイミド(デュポンP2723(DuPont P12723))は熱酸化物(thermal oxide)で覆われたシリコンウエハース上に約25ミクロン(μm)の厚さまでスピンキャストされる。すべてのセンサ処理ステップが完了した後、ウエハースは希釈したH.F.溶液に浸される。熱酸化物はエッチングで除かれて、それによって柔軟なポリイミド基板とそのセンサ構造がリリースされる。
【0123】
凹所を設けたセンサ構造は感光性重合体材料を使って実現することがもできる。最高30μmの層厚は2ステップのスピン被覆手続によって得ることができる。他の材料もこの目的のために利用可能である。例えば、ドライフィルム(25から100μm層厚を有するデュポンピラルックスまたはバクレル(DuPont Pyralux or Vacrel))が熱真空処理(thermal vacuum process)を使用してデバイス上にラミネートされる。これらのラミネートされたフィルムを使用して製造可能なマイクロプールの最も高い面比率(深さ:幅)は一般に1:1である。この比率は10から100μmまで深さに対して維持できる。
【0124】
白金は水の電気分解にとってベストな貴金属電極として知られており、マイクロ製造技術を使用して容易に堆積及びパタン化される。豊富な塩化物イオンを含む生理溶液による以前の実験では、金発生電極の表面の塩素化は水の電気分解の正電位領域に観察された。この問題は金発生電極とカウンタ電極を白金で置き換えることによって軽減されるはずである。単純には、写真処理ステップにおいて、チタン白金層が電極と配線リードの両方の役割を果たすであろう。他の電極表面を生成するために、白金層上に、金が(作用電極のために)電気メッキされ、銀が(参照電極のために)電気メッキされることが可能である。pHセンサに対して、イリジウム酸化物もメッキされるであろう。電気メッキステップが自己整列的であり、かつ付加的なフォトパタニングが全く必要とされないようにデバイスが設計される。これらの手続はすでに確立されている(マルゾーク(Marzonk)、1998年)。現在、好ましい透過性膜材料は、ポリスチレン(polystyrene)またはコロジオン(collodion)で覆われたp−HEMAである(クロイツァ(Kreuzer)、1980年)。
【0125】
全体的なプロセスシーケンスは図23A−23Cに示されている。白金はスパッタリングによって堆積され、次いでフォトリソグラフィによりパタン化される。次に、ポリイミドの薄い層が、様々な電極領域を確定し、配線伝導体を絶縁するためにスピン被覆及びパタン化される。次いで、厚い重合体マイクロプールがラミネーションプロセスによって作用電極領域と参照電極領域の周りに確定される。次に、金(酸素触媒として)またはイリジウム酸化物(pH感知層として)が電気メッキされ、銀(REとして)のメッキと塩素化がそれに続く。最後に、透過性膜が顕微操作によってキャストされ、硬化される。作動中は、酸素センサ作動の間に継続的な二分化電圧(polarizing voltage)を使用すると、一つの不利な点は、老朽化効果に加えて酸素消費と電力消費が比較的大きいということであることを指摘しておく。この電力消費は好ましくは電極安定性を実現するよう減じられる。従って、断続的または周期的な測定が潜在ステップによって好ましくは始められる。電流密度と持続時間のような必要な較正パラメータは周期的な測定の適切な較正のために決定することができる。
【0126】
本発明は以下の実施例においてさらに説明される。これらの実施例は説明目的のみのためであって、それに限定されるものとして考えてはならない。
【0127】
(実施例)
患者に切除不可能な肺がん(腺癌あるいは扁平上皮細胞)が存在する。従来受け入れられる治療は放射線治療と化学療法の組合せである。放射線は月曜日から金曜日まで毎日与えられ、化学療法(タクソル(taxol)とシスプラチン(cisplatin))は1週間に1度低いドーズで、あるいは3週ごとにより高いドーズで行われる。全ての患者が実質的に同じ方法で治療され、そして期待される効き目率は50−75%の間にある。酸素レベル、pHと、特に細胞倍増時間が、患者によって広く変化するかもしれないことは知られているにもかかわらず、治療は個別化されていない。
【0128】
pH、酸素、そして放射線を監視するように構成された本発明の方法、システム、移植可能センサは今や治療に対するよりカスタマイズされたアプローチを提供する。センサは、地域特有情報を提供するために、腫瘍内に異なる侵入深度にあるいは腫瘍の異なる領域にわたってその場に(in situ)配置される。特定の値あるいは酸素、pHと細胞増殖は、治療の開始に先だって既成のデータベースの予測統計基準(predictive statistical norm)によって、あるいは、相対値を確定するための初期治療の間に、定めることができ、その特定の値は、治療がいつ開始されるべきか、開始されるべきかどうかを判定するために、治療に対する「ゴー(go)(適切)」あるいは治療に対する「ノーゴー(no go)(不適切)」のいずれかとして識別できる。監視アルゴリズムは変数の重要な値を数量化するために使用でき、治療における望ましい特定レベルに近づくよう各変数を補正するための積極的な試みが実行可能である。例えば、約6.8というより低い腫瘍pHを示すことはいうに及ばず、腫瘍の実質的なボリューム上で約50−52mHgの酸素化を達成するよう腫瘍を操作すること、及び増大した細胞増殖の期間の間に刺激または識別そして送出すること。
【0129】
放射線あるいは化学療法の初回投与に引き続いて、各変数は放射線治療及び/または化学療法の次の投与を送出するための適切な時間(好ましい治療期間に関連)を決定するために監視される。好ましくは、それぞれの患者は個別の患者の特定の反応パタンを確定するための治療に続いて少なくとも毎日4回監視される。この進行中の周期的な監視アプローチを利用することによって、より正確な好ましい方法でどれかの細胞毒素薬の送出と/または腫瘍の治療耐性期間(tumor treatment resistant periods)の間は治療を差し控えることが可能になる。高い酸素化レベル、低いpH、及び増大した細胞増殖の表示が存在するときといった、全ての変数が腫瘍が脆弱であることを示すときに治療することが好ましい。変数は同時に好ましい指標を表示するよう同期することはなく、そのときは統計的回帰分析が適切な治療時を確定するために判断できる。放射と化学療法のほかに、温熱療法及び/または他の治療が、特に高い低酸素症部分を示している腫瘍において、治療標準手続に組み込まれることが可能であることが理解されよう。これによって増大した腫瘍死を見込むことができ、しかる後、腫瘍の動力学が変化して、放射線及び/または化学療法のより正確な送出時を考慮することができる。こうして、個別化された治療によって増大した腫瘍細胞死を達せいするための好ましい治療時において細胞毒素剤を送出して、それにより治療に対する腫瘍の効き目を増大させることが可能になる。この実施例では、満足な反応が得られているときには、腫瘍は除去され得る。
【0130】
まとめると、治療の個別化は今や各個別の患者の腫瘍内の動的変化についての情報を得ることに基づいて実施することができる。この情報は腫瘍細胞死の増大、生存率の増大及び罹病率の減少を導くはずである。このことは、例えば、増加したドーズの送出を許すことにより細胞毒素剤の効果を増大させ、あるいは細胞毒素の送出のより効果的なタイミングを通してドーズを減少させることによって、罹病率が減少してそのために入院の機会がより少なくなることによって、患者の治療に要するコストが減少することを意味する。本発明は、腫瘍内で起きている動的変化についての情報を監視及び提供することができる。
【0131】
以上の説明は本発明を例証するためのもので、それに限定されるものとして与えられていない。本発明の2,3の模範的な実施態様が記述されたけれども、当業者であれば容易にここに与えられた実施態様の多くの修正や変更が本発明の新規技術と利点から逸脱することなく可能であることは理解されよう。従って、全てのこのような修正及び変更は以下の請求の範囲内に含まれることが意図されている。請求項において、ミーンズ・プラス・ファンクション表現(means-plus-function clause)は、列挙された機能とその構造的均等物のみならずその均等構造を実現するものとしてここに記述された構造をカバーすることが意図されている。そのために、以上の説明は本発明を例証するためのものであって、開示された特定の実施態様に限定されるとして構成されたものではなく、そして他の実施態様のみならず開示された実施態様の修正及び変更は発明の範囲に含まれるものとして意図されていることは理解されるはずである。本発明は、以下の請求項によってその均等物を含めて定義される。
【0132】
<引用文献>
【表4】
【表4(つづき)】
【表4(つづき)】
【表4(つづき)】
【図面の簡単な説明】
【図1A】 本発明による腫瘍監視システムの略図である。これはリアルタイム監視可能を説明するための図である。
【図1B】 本発明による代わりの腫瘍監視システムの略図である。この図は、進行中の動的遠隔監視能力を説明するためのものである。
【図2A】 積極的治療セッション(この図では電界治療法)の間にリアルタイムの腫瘍情報を伝えるよう構成された、本発明の一実施態様による腫瘍監視システムの略図である。
【図2B】 温熱療法と放射線治療セッションの間に情報(リアルタイム)を伝えるように構成された腫瘍監視システムのブロック図である。
【図3】 本発明による治療を経験している腫瘍の監視方法のブロック図である。
【図4】 腫瘍の複数の生理学的パラメータを周期的(動的)に監視して好ましい治療期間及び好ましくない治療期間を割り出すための本発明による方法の手順流れ図である。
【図5】 本発明による移植可能な生物学的に適合するセンサの平面図である。
【図6A】 本発明による代わりの移植可能な生物学的に適合するセンサの平面図である。
【図6B】 図6Aに示されたセンサの側面図である。
【図7】 本発明による注入可能なマイクロプロセッサの側断面図である。
【図8A】 図7に示されたセンサの線8A−8Aに沿った断面図である。
【図8B】 図7に示された実施態様に類似する、注入可能なマイクロプロセッサの代わりの実施態様の正面斜視図である。
【図9】 本発明の別の実施態様による移植センサの略図である。
【図10A】 本発明によるpH(イオノファ)膜を有するpHセンサの見せかけのインプラントの大いに拡大された切欠正面図である。
【図10B】 (イリジウム酸化膜を有する)pHセンサの代わりの実施態様の側面図である。
【図11】 本発明による移植腫瘍センサを評価するために使われる試験的なセットアップの略図である。
【図12】 本発明による移植可能センサ用回路のブロック図である。
【図13】 本発明による模範的な送信器の動作のグラフである。
【図14A】 本発明の一実施態様による、送信器の操作パラメータを示したグラフであり、長時間にわたってコンデンサ電圧を示した図である。
【図14B】 本発明の一実施態様による、送信器の操作パラメータを示したグラフであり、長時間にわたって制御電圧を示した図である。
【図14C】 本発明の一実施態様による、送信器の操作パラメータを示したグラフであり、出力電圧波形を示した図である。
【図15】 本発明の一実施態様によるICブロック図を示した図である。
【図16】 図15に対応するICレイアウトの写真的表現である。
【図17A】 IC試作品温度実験の結果のグラフであり、サーミスタに対応するデータの、温度に対するパルス幅(チップはさまざまな温度の水槽内にある)を示している。
【図17B】 IC試作品温度実験の結果のグラフであり、固定抵抗器に対応するデータの、温度に対するパルス幅(同様にチップはさまざまな温度の水槽内にある)を示している。
【図18A】 IC試作品放射線実験の結果のグラフであり、チップがさまざまな温度の水槽内にあり、約0−8000cGray(患者は一般に約3000−6000cGrayの範囲の放射で処置される)の放射線で照射されているときの、サーミスタに対応するデータの、放射線量に対するパルス幅を示している。
【図18B】 IC試作品放射線実験の結果のグラフであり、チップが水槽内にあり、約0−8000cGrayの放射線で照射されているときの、固定抵抗器データに対応するデータを示している。
【図19A】 本発明の一実施態様において、2つの異なった腫瘍上に配置された2つの別個の空間的に離れた移植センサを備えた監視システムを有する被験者の略図である。監視システム受信器は、両方の位置を監視して、遠隔地にデータを送信するために方向を変えることができる。
【図19B】 本発明の一実施態様による、(体内の)所定の場所にある4つのセンサ要素を有する移植センサを示している。示されているように、センサ要素の2つは腫瘍上の異なる表面位置に配置されているが、センサ要素の一つは腫瘍のある深さまで入り込んだ位置にある。センサ要素の残りの一つは、悪性の組織または腫瘍の直前にある正常組織の直前に配置されている。
【図20】 自己較正するその場で働く生体内マイクロセンサの略図である。
【図21】 自己較正する酸素センサの写真である。
【図22】 自己較正するpHセンサ及びO2センサの組合せの断面図である。
【図23A】 図22のセンサの製造工程の説明するための側面図である。
【図23B】 図22のセンサの製造工程の説明するための側面図である。
【図23C】 図22のセンサの製造工程の説明するための側面図である。
Claims (37)
- 治療を経験している腫瘍の状態を監視及び評価するシステムであって、
(a)その場で働く(in situ)センサユニットを使用して治療を経験している被験者における腫瘍に関連する少なくとも一つの生体内パラメータを監視する監視手段と、ここで、選択された生体内のパラメータが、放射線照射量、pH、細胞増殖率、及び細胞の酸素化の少なくとも一つを含む、監視手段と、
(b)前記その場で働くセンサユニットからの前記監視手段で監視された少なくとも一つの生理学的パラメータに関連するデータを前記被験者の外側に位置する受信器に送信する送信手段と、
(c)前記送信手段で送信されたデータを解析する解析手段と、
(d)複数の一連の時点において周期的に前記監視手段、前記送信手段、そして前記解析手段を繰り返す繰り返し手段と、
(e)前記解析データに基づいて腫瘍治療法を評価する評価手段と
を備えることを特徴とするシステム。 - 前記送信手段と前記解析手段は、前記少なくとも一つの監視された生理学的パラメータの変化を追跡して、それによって長時間にわたる前記腫瘍の振る舞いを評価するために十分に繰り返されることを特徴とする請求項1に記載のシステム。
- 前記監視手段では、複数の腫瘍パラメータを監視し、前記解析手段では、その中の少なくとも一つが好ましい治療時機の識別に関連しており、かつその中の少なくとも一つが好ましくない治療時機の識別に関連する、複数の所定の検査条件(テストコンディション)を定義すると共に、当該システムは、送信されたデータが、前記腫瘍に対する次の積極的治療を施すための好ましいあるいは好ましくない治療の時間帯(window)を識別する前記検査条件の一つを満足するときに関して医者に警告する警告手段をさらに有することを特徴とする請求項1に記載のシステム。
- 前記監視手段と前記送信手段は、当該腫瘍と、当該積極的治療をその時点で進めることの適切さに関するリアルタイム情報または腫瘍部位もしくは当該腫瘍部位近辺に積極的治療の受取られたドーズ(dose)を提供するために、当該積極的治療の送出の直前に繰り返されることを特徴とする請求項1に記載のシステム。
- 治療の標準的手続は、前記被験者に特有な腫瘍の前記監視された生体内生理学的パラメータによって与えられる腫瘍情報に基づいて調整されることを特徴とする請求項1に記載のシステム。
- 長時間にわたって前記監視されたパラメータの変化を動的に監視するために時間的に関係する一連のデータ測定値を電子的に記憶することをさらに含むことを特徴とする請求項1に記載のシステム。
- その場で働くセンサユニットは、複数それぞれ離間され、目標腫瘍部位において複数のパラメータを監視するように構成されており、前記センサユニットは少なくとも約6〜10週間のサービス寿命を有することを特徴とする請求項1に記載のシステム。
- 前記評価手段は、腫瘍部位に放射線量の決定と、当該治療の効果の決定と、積極的な好ましい治療の時間帯の識別との少なくとも一つを実行することを有することを特徴とする請求項1に記載のシステム。
- 前記センサユニットは、複数それぞれ離間され、前記センサユニットの少なくとも一つは、前記腫瘍の直前にある正常な細胞組織に対する治療の毒作用を監視するように構成されていることを特徴とする請求項1に記載のシステム。
- 前記監視手段は、放射線照射量、細胞外pH、温度、細胞の酸素化、及び細胞周期の少なくとも二つを含む、腫瘍の複数の異なる生理学的パラメータを監視することを特徴とする請求項1に記載のシステム。
- 前記監視手段は、腫瘍において受け取られた治療ドーズの量を監視し、前記解析手段は、前記受け取られたドーズを事前に計画されたドーズと比較して、ずれを識別してそれによって目標とされた治療ドーズの効果を確認することを特徴とする請求項1に記載のシステム。
- 前記センサユニットはセンサ・エレクトロニクスを備え、当該システムは、前記センサユニットが放射線及び温度の少なくとも一つにさらされることによるデータのずれを補償するために前記送信データを調整することを特徴とする請求項1に記載のシステム。
- 前記監視手段は、少なくとも約6−10週間のサービス寿命を持つ少なくとも一つのセンサユニットにより実行され、当該システムは、腫瘍に関連する生理学的状態を表す少なくとも一つの監視された生理学的パラメータに関連するデータを局所的に送信し、それによって該腫瘍の状態に関する実質的にリアルタイムな情報を提供する手段をさらに有することを特徴とする請求項1に記載のシステム。
- 放射線治療または薬物療法の効果を評価し、かつ/または、強化された積極的治療の時間帯を識別するための腫瘍の監視システムであって、
少なくとも一つの埋め込み可能なセンサユニット及び関連するセンサ・エレクトロニクスであって、前記センサユニットが、治療を経験している被験者におけるガン性腫瘍部位の直前に埋め込まれるように構成され、複数の異なったパラメータを検出し、検出されたパラメータに関連するデータを無線的に送信するように構成され、前記複数の異なったパラメータは、腫瘍部位への放射線照射量と、腫瘍の細胞外pHと、正常組織のpHと、腫瘍細胞の酸素化と、腫瘍細胞増殖率と、温度とのうちの少なくとも二つを含む、センサユニット及び関連するセンタ・エレクトロニクスと、
少なくとも一つのセンサユニットと無線通信する遠隔受信機であって、前記遠隔受信機が前記送信されたデータを受信するように構成され、前記少なくとも一つのセンサユニットとは空間的に隔たっており、前記被験者の外部に配置され、前記少なくとも一つのセンサユニットは、少なくとも約6−10週間の移植されたサービス寿命を持つ、遠隔受信機と
を備えることを特徴とする腫瘍監視システム。 - 前記少なくとも一つセンサユニットは、前記遠隔受信器によって誘導的に結合され、前記システムが、前記送信されたデータを受信するように構成されており、前記被験者内の前記センサユニットの環境にさらされたことによる信号データの変化を補正するために前記受信された送信データを再検討及び調整するためのコンピュータ読み取り可能なプログラムコード手段を備えた、データ・プロセッサを更に備えたことを特徴とする請求項14に記載の腫瘍監視システム。
- 前記センサユニットは対向する第1及び第2の端を有するシリンダ形状体として構成されており、前記センサユニットは電源に誘導的に結合され、前記センサは、約0.5インチ(1.27cm)未満であり、前記第1及び第2の端の少なくとも一つが哺乳類の体内の腫瘍に接触するようにトロカールを使って注入可能なサイズと構成を有することを特徴とする請求項14に記載の腫瘍監視システム。
- 前記センサユニットは腫瘍の望まれる部分に位置決めされて取り付けられるアンカー部分を含むことを特徴とする請求項16に記載の腫瘍監視システム。
- 前記センサユニットは少なくとも一つのpHセンサ要素、少なくとも一つの酸素センサ要素、少なくとも一つの温度センサ要素、そして少なくとも一つの放射線センサ要素を含むことを特徴とする請求項14に記載の腫瘍監視システム。
- 前記少なくとも一つのセンサユニットはセンサユニットに受動的に働く複数の無線であり、各センサユニットは送信データが適切なその場に置くセンサユニットのポジションと関連することを可能にするためのユニークな識別子を含むことを特徴とする請求項42に記載の腫瘍監視システム。
- 治療を経験している腫瘍の状態を監視及び解析するためのコンピュータ・プログラム製品であって、
その中にコンピュータ読取り可能なプログラムコード手段が具現化されるコンピュータ読取り可能な記憶媒体を備え、前記コンピュータ読取り可能なプログラムコード手段は、
治療を経験している腫瘍直前に被験者内に配置された少なくとも一つのセンサ要素を有するその場で働くセンサからの、前記少なくとも一つのセンサ要素の出力に対応するデータを含む第1の無線データ送信を、開始するためのコンピュータ読取り可能なプログラムコード手段と、
前記第1の無線データ送信から時間的に分離した、前記その場で働くセンサからの第2の無線データ送信を、開始するためのコンピュータ読取り可能なプログラムコード手段と、
(a)腫瘍照射処理セッションから腫瘍部位への放射照射量と、(b)腫瘍に関連する細胞増殖率と、(c)腫瘍処理に対する腫瘍部位近傍の正常細胞の反応と、(d)細胞毒性、ターゲット・ドラッグ、または化学処理の効果を評価するため、もしくは腫瘍部位への細胞毒性、ターゲット・ドラッグ、または化学処理の投射を確認するための腫瘍の生理的または生物学的パラメータの少なくとも一つの値と、(e)予想モデルからの腫瘍の生理的または生物学的パラメータの値の変位と、(f)好ましいまたは好ましくない腫瘍治療期間の存在と、(g)特定の腫瘍治療型の受容を確認するため、腫瘍の生理的または生物学的パラメータの少なくとも一つの値と、の少なくとも一つ評価するコンピュータ読取り可能なプログラムコード手段と
を含む、コンピュータ・プログラム製品。 - 評価するための前記コンピュータ読取り可能なプログラムコード手段は、事前に計画された放射線ドーズ、および生理学的または生物学的パラメータの少なくとも一つの値と、対応する少なくとも一つの生理学的または生物学的パラメータのそれぞれに確立された事前に決定される値とを比較することによって、腫瘍治療の効果を評価するコンピュータプログラムコード手段を含む請求項20に記載のコンピュータ・プログラム製品。
- 治療セッションの間に、前記一つ以上の監視された生理学的パラメータの変化に対応する治療行為それ自体を制御するためのコンピュータ読取り可能なプログラムコード手段をさらに備えたことを特徴とする請求項20に記載のコンピュータ・プログラム製品。
- 前記コンピュータプログラムコード手段は、前記項目(a)〜(e)を評価する請求項20に記載のコンピュータ・プログラム製品。
- 前記コンピュータプログラムコード手段は、前記項目(a)〜(e)の少なくとも3つを評価する請求項23に記載のコンピュータ・プログラム製品。
- 細胞毒性ドラッグや化学処理の効果を評価する、または腫瘍部位への細胞毒性ドラッグや化学処理の伝達を確認するため、前記少なくとも一つの腫瘍の生理学的または生物学的パラメータの値を評価する前記コンピュータ読取り可能なプログラムコード手段は、被験者の正常組織のpHを腫瘍組織の細胞外pHと比較することを含む請求項23に記載のコンピュータ・プログラム製品。
- 腫瘍放射線治療セッション中に腫瘍部位への放射線照射量を評価する前記コンピュータ読取り可能なプログラムコード手段は、腫瘍部位への放射線レベルを確かめる、または腫瘍部位への放射線レベルの不一致を識別することを特徴とする請求項20に記載のコンピュータ・プログラム製品。
- 少なくとも一つの腫瘍の生理学的または生物学的パラメータの値を評価する前記コンピュータ読取り可能なプログラムコード手段は、腫瘍が低酸素状態であったときに関連する好ましくない腫瘍処理時間を識別することを特徴とする請求項20に記載のコンピュータ・プログラム製品。
- 被験者のガン性腫瘍部位、かつ/または腫瘍部位の直ぐ近くにある正常な組織に移植するため、細胞外での腫瘍のpH、腫瘍の酸素化、正常組織のpH、腫瘍の細胞周期活性、および腫瘍部位への放射線照射の少なくとも1つを含んでいる少なくとも2つの異なった検出された状態に関するデータを出力するために構成されるその場で働く無線センサと、
前記センサに結合して動作し、空間的に離れた受信機に前記センサ出力データの無線伝送を構成する、送信コイルと、それに関連する電器部品と
を備える、前記センサは約0.5インチ(1.27cm)以下で、被験者に化膿止め(canula)を介して移植されるように構成される、移植可能な生物学的に適合するセンサユニット。 - 前記センサユニットは多数チャンネルユニットである請求項28に記載の移植可能な生物学的に適合するセンサユニット。
- 前記センサユニットは、腫瘍部位の放射線照射及び局部的な温度の少なくとも1つを検出するように構成される請求項28に記載の移植可能な生物学的に適合するセンサユニット。
- 前記センサ体は、腫瘍に近い部分において、前記センサが望ましい位置に保持されるようする取り付け手段を有するように構成される請求項28に記載の移植可能な生物学的に適合するセンサユニット。
- 前記センサユニットは、被験者に送られたイオン化した放射線を検出するように構成されるMOSFETベース放射線センサ要素を含み、前記MOSFETベース放射線センサ要素が、照射中にイオン化した放射線に受動的であり、移植され続けている間、内部に目標部位に送られた放射線のドーズに対応したデータを無線で伝送するために放射線が照射した後に誘導的に電力が与えられる構成されることを特徴とする請求項28に記載の移植可能な生物学的に適合するセンサユニット。
- 前記センサユニットは4週間以上被験者に移植されるように構成される、ここで、MOSFETベース放射線センサ要素は、腫瘍の放射線治療セッションで空間的に離された、腫瘍部位の近傍にある放射線を検出するように構成されている、請求項28に記載の移植可能な生物学的に適合するセンサユニット。
- (a)その場で働く(in situ)センサユニットを使用して治療を経験している被験者における腫瘍に関連する少なくとも一つのパラメータを生体内で監視する手段と、
(b)前記その場で働くセンサユニットからの前記監視段階で監視された少なくとも一つのパラメータに関連するデータを前記被験者の外側に位置する受信器に無線で送信する手段と、
(c)前記腫瘍に関連したパラメータを決定するため、前記送信段階で送信されたデータを解析する手段と、
(d)複数の一連の時点において周期的に前記監視段階、前記送信段階、そして前記解析段階を繰り返す手段と、
(e)腫瘍処理を評価する手段であって、
放射線、薬、及び化学療法の少なくとも少なくとも一つの適用に好ましいまたは好ましくない腫瘍処理の時間を識別する段階と、
腫瘍に対する治療放射線、薬、及び化学療法の少なくとも一つの効果を評価する段階と、
生体内の腫瘍部位に照射される放射線量を決定する段階と、
腫瘍部位に取り込まれた放射線ラベルされた薬を監視する段階と、
伝送されたデータに基づいて温度と、化学と、放射線治療との少なくとも一つの影響を監視するために伝送データを分析するステップとの少なくとも一つを有する、腫瘍処理を評価する手段と
を含む、治療を受けていている腫瘍の状態を評価する監視システム。 - 前記評価する手段は、内部に投与された放射性能のあるまたは放射線ラベルの物質、または放射性のあるまたは放射線ラベルの薬に被験者の局所的な反応を求め、被験者の特異的な腫瘍処理の統計を取るために被験者の特定の反応データを提供し、および/または被験者において腫瘍処理の伝達的または治療的な効果を評価するように構成される請求項34に記載のシステム。
- 前記評価する手段は、目標位置に放射された放射線のドーズ量を決定する、および/または検証するため、センサユニットから得られる放射線データに基づいて被験者が腫瘍部位に受取る外部ソースから放射線ドーズを計算するように構成される請求項34に記載のシステム。
- センサ位置を内部腫瘍位置に関連付けるための手段をさらに有する請求項34に記載のシステム。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10244798P | 1998-09-30 | 1998-09-30 | |
| US60/102,447 | 1998-09-30 | ||
| PCT/US1999/022638 WO2000018294A1 (en) | 1998-09-30 | 1999-09-29 | Methods, systems, and associated implantable devices for dynamic monitoring of tumors |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2002525153A JP2002525153A (ja) | 2002-08-13 |
| JP2002525153A5 JP2002525153A5 (ja) | 2006-12-21 |
| JP4365531B2 true JP4365531B2 (ja) | 2009-11-18 |
Family
ID=22289894
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000571817A Expired - Lifetime JP4365531B2 (ja) | 1998-09-30 | 1999-09-29 | 腫瘍の動的監視のための方法及びシステムとそれに関連する移植可能デバイス |
Country Status (10)
| Country | Link |
|---|---|
| EP (2) | EP1117328B1 (ja) |
| JP (1) | JP4365531B2 (ja) |
| AT (2) | ATE490725T1 (ja) |
| AU (1) | AU763446B2 (ja) |
| CA (1) | CA2341724C (ja) |
| DE (2) | DE69939592D1 (ja) |
| DK (2) | DK1117328T3 (ja) |
| ES (1) | ES2316193T3 (ja) |
| PT (1) | PT1117328E (ja) |
| WO (1) | WO2000018294A1 (ja) |
Families Citing this family (66)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8346337B2 (en) | 1998-04-30 | 2013-01-01 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US9066695B2 (en) | 1998-04-30 | 2015-06-30 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US8688188B2 (en) | 1998-04-30 | 2014-04-01 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US8974386B2 (en) | 1998-04-30 | 2015-03-10 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US8465425B2 (en) | 1998-04-30 | 2013-06-18 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US6175752B1 (en) | 1998-04-30 | 2001-01-16 | Therasense, Inc. | Analyte monitoring device and methods of use |
| US8480580B2 (en) | 1998-04-30 | 2013-07-09 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US20050103624A1 (en) | 1999-10-04 | 2005-05-19 | Bhullar Raghbir S. | Biosensor and method of making |
| US20010027384A1 (en) * | 2000-03-01 | 2001-10-04 | Schulze Arthur E. | Wireless internet bio-telemetry monitoring system and method |
| US8909325B2 (en) | 2000-08-21 | 2014-12-09 | Biosensors International Group, Ltd. | Radioactive emission detector equipped with a position tracking system and utilization thereof with medical systems and in medical procedures |
| US6560471B1 (en) | 2001-01-02 | 2003-05-06 | Therasense, Inc. | Analyte monitoring device and methods of use |
| US7011814B2 (en) * | 2001-04-23 | 2006-03-14 | Sicel Technologies, Inc. | Systems, methods and devices for in vivo monitoring of a localized response via a radiolabeled analyte in a subject |
| CA2474359A1 (en) | 2002-01-29 | 2003-08-07 | Sicel Technologies, Inc. | Implantable sensor housing and fabrication methods |
| US7736309B2 (en) * | 2002-09-27 | 2010-06-15 | Medtronic Minimed, Inc. | Implantable sensor method and system |
| US7244264B2 (en) | 2002-12-03 | 2007-07-17 | Roche Diagnostics Operations, Inc. | Dual blade lancing test strip |
| AU2003303597A1 (en) | 2002-12-31 | 2004-07-29 | Therasense, Inc. | Continuous glucose monitoring system and methods of use |
| AU2004214420A1 (en) | 2003-02-19 | 2004-09-02 | Sicel Technologies Inc. | In vivo fluorescence sensors, systems, and related methods operating in conjunction with fluorescent analytes |
| EP1620714B1 (en) * | 2003-04-15 | 2014-03-12 | Senseonics, Incorporated | System and method for attenuating the effect of ambient light on an optical sensor |
| US8066639B2 (en) | 2003-06-10 | 2011-11-29 | Abbott Diabetes Care Inc. | Glucose measuring device for use in personal area network |
| US9470801B2 (en) | 2004-01-13 | 2016-10-18 | Spectrum Dynamics Llc | Gating with anatomically varying durations |
| US7968851B2 (en) | 2004-01-13 | 2011-06-28 | Spectrum Dynamics Llc | Dynamic spect camera |
| US9040016B2 (en) | 2004-01-13 | 2015-05-26 | Biosensors International Group, Ltd. | Diagnostic kit and methods for radioimaging myocardial perfusion |
| CA2556331A1 (en) | 2004-02-17 | 2005-09-29 | Therasense, Inc. | Method and system for providing data communication in continuous glucose monitoring and management system |
| WO2005112895A2 (en) | 2004-05-20 | 2005-12-01 | Spectrum Dynamics Llc | Ingestible device platform for the colon |
| EP1778957A4 (en) | 2004-06-01 | 2015-12-23 | Biosensors Int Group Ltd | OPTIMIZING THE MEASUREMENT OF RADIOACTIVE EMISSIONS IN SPECIFIC BODY STRUCTURES |
| JP3950977B2 (ja) * | 2004-06-25 | 2007-08-01 | 国立大学法人東北大学 | 体内埋め込み型リアルタイム式マイクロ線量計装置ならびに測定方法 |
| US9316743B2 (en) | 2004-11-09 | 2016-04-19 | Biosensors International Group, Ltd. | System and method for radioactive emission measurement |
| US9943274B2 (en) | 2004-11-09 | 2018-04-17 | Spectrum Dynamics Medical Limited | Radioimaging using low dose isotope |
| KR101274641B1 (ko) * | 2005-03-29 | 2013-06-17 | 마틴 로슈 | 생체 변수를 검출하는 생체 센서 |
| EP3095379A1 (en) | 2005-04-15 | 2016-11-23 | Surgisense Corporation | Surgical instruments with sensors for detecting tissue properties, and systems using such instruments |
| US8837793B2 (en) | 2005-07-19 | 2014-09-16 | Biosensors International Group, Ltd. | Reconstruction stabilizer and active vision |
| US7766829B2 (en) | 2005-11-04 | 2010-08-03 | Abbott Diabetes Care Inc. | Method and system for providing basal profile modification in analyte monitoring and management systems |
| US8226891B2 (en) | 2006-03-31 | 2012-07-24 | Abbott Diabetes Care Inc. | Analyte monitoring devices and methods therefor |
| US7620438B2 (en) | 2006-03-31 | 2009-11-17 | Abbott Diabetes Care Inc. | Method and system for powering an electronic device |
| US8894974B2 (en) | 2006-05-11 | 2014-11-25 | Spectrum Dynamics Llc | Radiopharmaceuticals for diagnosis and therapy |
| WO2008075362A2 (en) | 2006-12-20 | 2008-06-26 | Spectrum Dynamics Llc | A method, a system, and an apparatus for using and processing multidimensional data |
| US8930203B2 (en) | 2007-02-18 | 2015-01-06 | Abbott Diabetes Care Inc. | Multi-function analyte test device and methods therefor |
| US8123686B2 (en) | 2007-03-01 | 2012-02-28 | Abbott Diabetes Care Inc. | Method and apparatus for providing rolling data in communication systems |
| PL1972275T3 (pl) * | 2007-03-20 | 2016-04-29 | Hoffmann La Roche | Układ do pomiaru in vivo stężenia analitu |
| US8456301B2 (en) | 2007-05-08 | 2013-06-04 | Abbott Diabetes Care Inc. | Analyte monitoring system and methods |
| US7928850B2 (en) | 2007-05-08 | 2011-04-19 | Abbott Diabetes Care Inc. | Analyte monitoring system and methods |
| US8665091B2 (en) | 2007-05-08 | 2014-03-04 | Abbott Diabetes Care Inc. | Method and device for determining elapsed sensor life |
| US8461985B2 (en) | 2007-05-08 | 2013-06-11 | Abbott Diabetes Care Inc. | Analyte monitoring system and methods |
| EP2355692A1 (en) * | 2008-11-11 | 2011-08-17 | Koninklijke Philips Electronics N.V. | Medical device comprising a probe for measuring temperature data in a patient's tissue |
| US8103456B2 (en) | 2009-01-29 | 2012-01-24 | Abbott Diabetes Care Inc. | Method and device for early signal attenuation detection using blood glucose measurements |
| US9226701B2 (en) | 2009-04-28 | 2016-01-05 | Abbott Diabetes Care Inc. | Error detection in critical repeating data in a wireless sensor system |
| WO2010138856A1 (en) | 2009-05-29 | 2010-12-02 | Abbott Diabetes Care Inc. | Medical device antenna systems having external antenna configurations |
| ES2843628T3 (es) * | 2009-06-26 | 2021-07-19 | Cianna Medical Inc | Sistema para localizar marcadores o estructuras de tejido dentro un cuerpo |
| US9314195B2 (en) | 2009-08-31 | 2016-04-19 | Abbott Diabetes Care Inc. | Analyte signal processing device and methods |
| EP2473099A4 (en) | 2009-08-31 | 2015-01-14 | Abbott Diabetes Care Inc | ANALYTICAL SUBSTANCE MONITORING SYSTEM AND METHODS OF MANAGING ENERGY AND NOISE |
| EP2482720A4 (en) | 2009-09-29 | 2014-04-23 | Abbott Diabetes Care Inc | METHOD AND APPARATUS FOR PROVIDING NOTIFICATION FUNCTION IN SUBSTANCE MONITORING SYSTEMS |
| JP6443802B2 (ja) | 2011-11-07 | 2018-12-26 | アボット ダイアベティス ケア インコーポレイテッドAbbott Diabetes Care Inc. | 分析物モニタリング装置および方法 |
| US8790400B2 (en) | 2012-06-13 | 2014-07-29 | Elwha Llc | Breast implant with covering and analyte sensors responsive to external power source |
| US9144489B2 (en) | 2012-06-13 | 2015-09-29 | Elwha Llc | Breast implant with covering, analyte sensors and internal power source |
| US9144488B2 (en) | 2012-06-13 | 2015-09-29 | Elwha Llc | Breast implant with analyte sensors responsive to external power source |
| US9211185B2 (en) | 2012-06-13 | 2015-12-15 | Elwha Llc | Breast implant with analyte sensors and internal power source |
| US8795359B2 (en) | 2012-06-13 | 2014-08-05 | Elwha Llc | Breast implant with regionalized analyte sensors and internal power source |
| US8808373B2 (en) | 2012-06-13 | 2014-08-19 | Elwha Llc | Breast implant with regionalized analyte sensors responsive to external power source |
| US9968306B2 (en) | 2012-09-17 | 2018-05-15 | Abbott Diabetes Care Inc. | Methods and apparatuses for providing adverse condition notification with enhanced wireless communication range in analyte monitoring systems |
| JP6554089B2 (ja) | 2013-03-19 | 2019-07-31 | サージセンス コーポレイション | 組織酸素化の測定用の器具、システムおよびメソッド |
| JP6512623B2 (ja) * | 2014-02-07 | 2019-05-15 | 国立大学法人北海道大学 | 吸収線量測定システムおよび測定装置および方法 |
| JP6385740B2 (ja) | 2014-07-04 | 2018-09-05 | ルネサスエレクトロニクス株式会社 | 電子装置およびその製造方法 |
| CN104970806B (zh) * | 2015-07-12 | 2017-08-04 | 北京泱深生物信息技术有限公司 | 一种用于癌症复发实时动态监测的智能设备 |
| GB2566463A (en) * | 2017-09-13 | 2019-03-20 | Univ Southampton | pH Sensor and Calibration method |
| CA3072646A1 (en) | 2017-09-13 | 2019-03-21 | Hologic, Inc. | Wireless active monitoring implant system |
| SI25656A (sl) | 2018-06-01 | 2019-12-31 | Jože Abram | Mešalno brizgalna glava za tridimenzionalni tiskalnik za tiskanje sten zgradb in metoda tiskanja |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3219558C2 (de) * | 1982-05-25 | 1986-10-23 | Norbert H.L. Dr.-Ing. 5173 Aldenhoven Koster | Vorrichtung zur Bestimmung der lokalen Temperatur in lebendem Gewebe |
| JPS61146230A (ja) * | 1984-12-19 | 1986-07-03 | 東洋通信機株式会社 | 係止具を設けた生体内埋込みセンサ |
| JPS62102733A (ja) * | 1985-10-31 | 1987-05-13 | 東洋通信機株式会社 | 生体内温度検出表示装置 |
| IL86470A (en) * | 1988-05-23 | 1994-11-28 | E M T Electro Magnetic Technol | Means and method for temperature control from a distance |
| JP2762283B2 (ja) * | 1988-10-31 | 1998-06-04 | 東洋通信機株式会社 | 生体内埋め込みセンサ |
| DE3932428A1 (de) | 1989-09-28 | 1991-04-11 | Argumens Gmbh | Vorrichtung zur drahtlosen messung einer lokalen physikalischen groesse |
| US5791344A (en) | 1993-11-19 | 1998-08-11 | Alfred E. Mann Foundation For Scientific Research | Patient monitoring system |
| DE4341903A1 (de) * | 1993-12-09 | 1995-06-14 | Josef Prof Dr Rer Nat Binder | Implantierbares telemetrisches Endosystem |
| US5544661A (en) * | 1994-01-13 | 1996-08-13 | Charles L. Davis | Real time ambulatory patient monitor |
| US5593430A (en) * | 1995-01-27 | 1997-01-14 | Pacesetter, Inc. | Bus system for interconnecting an implantable medical device with a plurality of sensors |
| US5720771A (en) | 1995-08-02 | 1998-02-24 | Pacesetter, Inc. | Method and apparatus for monitoring physiological data from an implantable medical device |
| US5833603A (en) * | 1996-03-13 | 1998-11-10 | Lipomatrix, Inc. | Implantable biosensing transponder |
| WO1997036192A1 (de) * | 1996-03-27 | 1997-10-02 | Paul Scherrer Institut | Vorrichtung und verfahren zur positionsbestimmung |
| US5814089A (en) * | 1996-12-18 | 1998-09-29 | Medtronic, Inc. | Leadless multisite implantable stimulus and diagnostic system |
| JP4157168B2 (ja) * | 1997-03-27 | 2008-09-24 | アルフレッド イー マン ファウンデーション フォア サイエンティフィック リサーチ | 身体のパラメータを監視及び又はそれに作用するための植込型装置のシステム |
| WO1998058250A2 (en) * | 1997-06-16 | 1998-12-23 | Elan Corporation, Plc | Methods of calibrating and testing a sensor for in vivo measurement of an analyte and devices for use in such methods |
| JP2000005136A (ja) * | 1998-06-26 | 2000-01-11 | Nippon Telegr & Teleph Corp <Ntt> | 温度測定装置およびインプラント |
| US9472410B2 (en) | 2014-03-05 | 2016-10-18 | Applied Materials, Inc. | Pixelated capacitance controlled ESC |
-
1999
- 1999-09-29 AT AT07016983T patent/ATE490725T1/de not_active IP Right Cessation
- 1999-09-29 AU AU62764/99A patent/AU763446B2/en not_active Ceased
- 1999-09-29 WO PCT/US1999/022638 patent/WO2000018294A1/en active IP Right Grant
- 1999-09-29 CA CA2341724A patent/CA2341724C/en not_active Expired - Fee Related
- 1999-09-29 PT PT99950017T patent/PT1117328E/pt unknown
- 1999-09-29 ES ES99950017T patent/ES2316193T3/es not_active Expired - Lifetime
- 1999-09-29 AT AT99950017T patent/ATE408369T1/de active
- 1999-09-29 DE DE69939592T patent/DE69939592D1/de not_active Expired - Lifetime
- 1999-09-29 DK DK99950017T patent/DK1117328T3/da active
- 1999-09-29 JP JP2000571817A patent/JP4365531B2/ja not_active Expired - Lifetime
- 1999-09-29 DK DK07016983.4T patent/DK1867275T3/da active
- 1999-09-29 EP EP99950017A patent/EP1117328B1/en not_active Expired - Lifetime
- 1999-09-29 DE DE69943029T patent/DE69943029D1/de not_active Expired - Lifetime
- 1999-09-29 EP EP07016983A patent/EP1867275B1/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| EP1867275A2 (en) | 2007-12-19 |
| PT1117328E (pt) | 2008-12-02 |
| EP1867275B1 (en) | 2010-12-08 |
| DK1867275T3 (da) | 2011-04-04 |
| DE69943029D1 (de) | 2011-01-20 |
| EP1117328B1 (en) | 2008-09-17 |
| WO2000018294A1 (en) | 2000-04-06 |
| ATE408369T1 (de) | 2008-10-15 |
| DE69939592D1 (de) | 2008-10-30 |
| EP1867275A3 (en) | 2008-04-09 |
| DK1117328T3 (da) | 2009-01-19 |
| ES2316193T3 (es) | 2009-04-01 |
| EP1117328A1 (en) | 2001-07-25 |
| JP2002525153A (ja) | 2002-08-13 |
| CA2341724A1 (en) | 2000-04-06 |
| CA2341724C (en) | 2010-12-21 |
| AU763446B2 (en) | 2003-07-24 |
| AU6276499A (en) | 2000-04-17 |
| ATE490725T1 (de) | 2010-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4365531B2 (ja) | 腫瘍の動的監視のための方法及びシステムとそれに関連する移植可能デバイス | |
| US6402689B1 (en) | Methods, systems, and associated implantable devices for dynamic monitoring of physiological and biological properties of tumors | |
| CN102469965B (zh) | 分析物监测装置和使用方法 | |
| CN102469964B (zh) | 分析物监测装置和使用方法 | |
| CN102472719B (zh) | 分析物监测装置和使用方法 | |
| US20140163338A1 (en) | Analyte Sensor with Slot Antenna | |
| US20060064142A1 (en) | Systems and methods for deriving relative physiologic measurements using an implanted sensor device | |
| US20230109023A1 (en) | System and method for intra-body communication of sensed physiologic data | |
| CN102917636A (zh) | 具有缝隙天线的分析物传感器 | |
| CN110831500A (zh) | 医疗系统 | |
| US11357425B2 (en) | Intraosseous implanted biological sensor | |
| WO2022245804A1 (en) | Detection of changes in patient health based on glucose data |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20041022 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20041022 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060929 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060929 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20061101 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20090731 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20090821 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120828 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 4365531 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130828 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |